Группа изобретений относится к области косметологии/дерматологии, а именно, к способам повышения трансдермальной проницаемости косметических или лечебных средств для наружного применения посредством введения в кожу инертного газа ксенона.
Принцип повышения эффективности лекарственных средств, предназначенных для наружного применения (кремы, мази, пластыри), хорошо известен. В настоящее время для этой цели все более широко используют транспортные системы трансдермальной доставки активных субстанций, входящих в композиции данных средств (Mbah C.J., Uzor P.F., Omeje E.O.. Perspectives on transdermal drug delivery / J Chem. Pharm. Res. - 2011, - V.3 (3), - P.680-700; Milind M.T., Pancholi S.S. Review of penetration enhancement techniques in transdermal delivery system / American J of PharmTech Research. - 2012, - V.2(1). - P.256-273). В 2009 г в США из 129 различных транспортных систем для лекарств, находящихся на стадии клинических исследований, 51% являлись системами трансдермальной и дермальной доставки. В настоящее время в США одобрены 20 оригинальных транспортных систем для ряда лекарственных средств для лечения кожных заболеваний, сахарного диабета, патологии сердца и сосудов, никотиновой зависимости, проведения заместительной гормонотерапии у женщин, а также анальгетиков и анестетиков.
Существует несколько основных технологических трендов разработки систем трансдермальной транспортировки активных субстанций:
1. Использование носителей (липосомы, трансферсомы, этосомы, ниосомы, аспасомы, наносомы, дендримеры, эутектические системы и т.д.).
2. Физические методы повышения проницаемости кожи - ионофорез, ультразвук, электропорация, термопорация, магнитофорез, микроиглы, безигольные инъекции и т.д.
3. Химические соединения - энхансеры - сульфоксиды, спирты, полиолы, алканы, эфиры, терпены и т.д.
Преимущества энхансеров по сравнению с другими методами заключаются в том, что они просто вводятся в композицию средства, при этом исключается необходимость дополнительного производства носителей (липосомы и т.д.), а также не требуется дополнительная аппаратура для ионофореза, ултразвукового воздействия и т.д. Основной механизм действия энхансеров (от англ. "enhance" - повышать, усиливать) - модификация физико-химических параметров рогового слоя, разрыхление его, нарушение целостности и упорядоченности структуры межклеточного липидного слоя эпидермиса, что способствует улучшению текучести этого слоя и растворимости активных субстанций в роговом слое.
Недостатком химических энхансеров является риск развития побочных воспалительных явлений, связанных с раздражением, покраснением, шелушением и т.п. Проникновение этих химических соединений либо их метаболитов вглубь кожи и попадание в кровь может оказать нежелательное системное действие на весь организм. Кроме того, такие энхансеры повышают риск передозировки или изменения биологической активности субстанций, содержащихся в косметических либо лечебных средствах (Patel H.J., Trivedi D.G., Bhandari A.K., Shah D.A. Penetration enhancers for transdermal drug delivery system: A review / IJPI's Journal of Pharmaceutics and Cosmetology. - 2011. - V.1(2). - P.67-80).
Поиск способов повышения эффективности косметических и лечебных средств для наружного применения путем введения в состав их транспортных систем энхансеров остается актуальным.
Известны способы лечения различных заболеваний с применением фитохитодезов и хитозансодержащих мазей, например, в хирургической практике для воздействия на раневой процесс с целью ускорения заживления различных ран и предупреждения их нагноения [RU 2151601 С1, 2000], при лечении хронического гастрита, язвенной болезни желудка и двенадцатиперстной кишки [RU 2150271 С1, 2000], острых гнойных периоститов [RU 2153318 С1, 2000].
Известен способ повышения эффективности лечения атопического дерматита [RU 2170092 С1, 2001]. Способ заключается в местном использовании на очагах поражения глюкокортикостероидной мази, дополнительно содержащей гепарин, при этом дозу стероидов уменьшают в 13-40 раз. Способ приводит к повышению эффекта лечения и уменьшению осложнений стероидной терапии.
Из уровня технике известны устройства для трансдермальной доставки лекарственных препаратов, содержащие O-Десметилвенлафаксин (ODV) или его соли [RU 2008106935 А, 2009], по сути представляющие трансдермальный пластырь для введения топической композиции, содержащей терапевтически эффективную дозу ODV или его фармацевтически допустимой соли и по меньшей мере один физиологически допустимый носитель или наполнитель.
Известна фармацевтическая композиция для повышения проницаемости кожи для улучшенной локальной доставки лекарств [RU 94019942 A1, 1995], включающая безопасное и эффективное количество фармацевтически активного вещества, 0,05%-5% неионного полиакриламида с молекулярной массой 1000000-30000000.
Из уровня техники также известна фармацевтическая композиция для местного применения [RU 2005132004 А, 2006], в которой агентом для повышения проницаемости через кожу, является вещество, выбранное из группы мочевины, пирролидона, N-метилпирролидина, децилметилсульфоксида, лаурилсульфата натрия и диметилсульфоксида.
Известно биологически активное вещество косметических средств, стимулирующее процессы обмена веществ в покровных тканях [RU 2033789 C1, 1995], в котором в качестве биологически активного компонента применяется блок-сополимер оксида этилена и оксида пропилена (сополимера полиокси-этилен-полиоксипропилена) общей структурной формулы 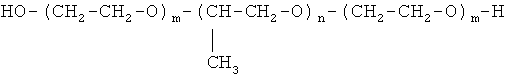
имеющего молекулярную массу 3-25 Kg и соотношение оксипропиленовой и оксиэтиленовой частей (20-2):(80-2).
Известно тетрациклическое соединение, используемое для повышения проницаемости кожи для фармацевтически активного соединения и предложен способ повышения проницаемости кожи для фармацевтически активного соединения [RU 2007105687 А, 2008], включающий обработку кожи тетрациклическим соединением и введение фармацевтически активного соединения.
Среди газообразных энхансеров известен кислород [RU 2191566 C1, 2002; RU 2119790 C1, 1998; RU 2304959 C2, 2007]. Данная технология применяется российской компанией Фаберлик, использующей в своих продуктах Аквафтэм - соединение нано-размеров (200 нм) на основе перфторуглеродов (перфтордекалина), активно сорбирующее молекулярный кислород. Авторы утверждают, что основным эффектом подобной «кислородной косметики» является стимуляция метаболизма клеток кожи в результате повышения уровня образования энергетических субстратов в митохондриях и, как следствие, стимуляция регенерации и процессов «омоложения» за счет увеличения содержания белков коллагенов и эластина в дерме и восстановления упругости кожи, а также эффекты при лечении ожогов. Действительно, оксидазный путь (когда молекулярный кислород не встраивается в молекулу окисляемого субстрата) имеет место в цитохромоксидазах дыхательной пути митохондрий. Тем не менее, в результате еще двух путей - моно- и диоксигеназного в молекулы субстратов встраивается либо один либо вся молекула кислорода, в результате чего образуются активные формы кислорода (АФК) - инициаторов процессов свободнорадикального окисления (СРО) и перекисного окисления липидов (ПОЛ), белков, молекул ДНК с нарушением их функции и необратимым разрушением [Кузьменко Д.И., Серебров В.Ю., Удинцев С.Н. Свободнорадикальное окисление липидов, активные формы кислорода и антиоксиданты: роль в физиологии и патологии клетки / Томск, 2007. - 214 с.]. Аналогичные процессы протекают в коже, в частности, на фоне избыточного ультрафиолетового облучения (фотостарение кожи). Кислород, по их данным, среди указанных выше эффектов, также усиливает проникновение в глубокие слои и усвоение клетками кожи биологически активных веществ, например, популярной в косметологии в последнее время RALA (R-альфалипоевой кислоты), и усиливает активность других косметических препаратов, в частности, солнцезащитных средств. Таким образом, Аквафтэм рассматривается также и в качестве энхансера.
Недостатком данного изобретения является образование избытка активных форм кислорода - развитие окислительного стресса, и эффект Аквафтэма как энхансера следует рассматривать не только как следствие повышение утилизации активных соединений клетками кожи в результате активации метаболизма, но в больше степени в результате воздействия агрессивных активных форм кислорода, инициирующих процессы свободнорадикального окисления и перекисного окисления липидов, белков, молекул ДНК с нарушением их функции и необратимым разрушением. Подобные процессы, протекающие в клетках кожи, приводят к ее разрыхлению и нарушению целостности липидных межклеточных структур, в результате чего повышается ее проницаемость для активных субстанций. Риск развития окислительного стресса на фоне избытка кислорода требует дополнительного введения в состав композиции актиоксидантов, что и было сделано компанией Фаберлик - после создания Aquaftem появился Aquaftem Protect, в который был добавлено соединение пропилфенол, антиоксидантные свойства которого на порядок выше, чем у витамина Е. Этот продукт также используется компанией в качестве энхансера для компонентов эфирных масел, с которыми он комбинируется.
Своим действием интерес представляют липофильные инертные газы, такие как криптон, аргон, ксенон. Особенно среди них хотелось бы выделить ксенон, который известен как ингаляционный анестетик, поскольку этот инертный газ обладает анестезирующим и болеутоляющим действием.
Известен патент США [US 2005255169, 2005], в котором авторы предлагают использовать анестезию (ингаляции) ксеноном либо газовой смесью, содержащей ксенон, в качестве средства для усиления эффекта (энхансера) фармакологических препаратов, предназначенных для проведения антивирусной, антибактериальной, антигрибковой терапии, а также нейропротекторов, противоопухолевых препаратов, парасимпатомиметиков, спазмолитиков, симпатомиметиков, трнквилизаторов, витаминов, гормонов.
Недостатком данного изобретения является то, что анестезия ксеноном требует специального оборудования, может проводиться только в лечебных учреждениях специалистами-анестезиологами и, соответственно, недоступна для массового применения и, тем более, в качестве средства для повышения эффективности косметических средств.
Известен препарат для адаптогенной терапии и способ его изготовления [RU 2228739 С1, 2004]. Препарат снабжен герметичной упаковкой и содержит наполнитель - жировую эмульсию или твердый сорбент, в котором растворен или адсорбирован газообразный действующий компонент, представляющий собой, по меньшей мере, один газ из группы, включающей: ксенон, криптон, закись азота. Предпочтительно наполнитель представляет собой жировую эмульсию, имеющую рН не ниже 6,0, жировая эмульсия содержит жир, а именно: молоко крупного или мелкого рогатого скота или иную эмульсию на основе животного масла, или в качестве наполнителя содержит растительное масло или активированный уголь или термоксид. Изобретение обеспечивает получение нетоксичного препарата с повышенной способностью к регуляции сопротивляемости организма при экстремальных воздействиях за счет гуморальной регуляции, регуляции обмена веществ и психоэмоциональной регуляции пациента.
Способ получения препарата для адаптогенной терапии выбран наиболее близким способом того же назначения к заявляемому способу в группе изобретений.
Технической задачей изобретения является создание нового способа повышения эффективности лекарственных или косметических препаратов посредством введения (доставки) в кожу инертного газа ксенона за счет проявления ксеноном эффекта энхансера.
Другой технической задачей, стоящей перед разработчиками, была разработка нового способа введения в кожу газообразного ксенона.
Задача при осуществлении заявляемой группы изобретений достигается тем, что заявляемый способ повышения трансдермальной проницаемости лечебных или косметических препаратов для наружного применения включает введение в кожу от 1,0 до 300,0 об.% газообразного ксенона в составе приемлемого нейтрального носителя или лечебного, или косметического препарата.
Кроме того, в качестве приемлемого нейтрального носителя газообразного ксенона выбирают, по меньшей мере, одно вещество.
Эффективное количество газообразного ксенона растворяют в приемлемом нейтральном носителе, или лечебном или косметическом препарате.
При этом приемлемый нейтральный носитель ксенона, лечебный или косметический препарат используют в газообразной или жидкой, или полутвердой, или твердой форме.
Для ухода за кожей, ногтями, волосами, слизистыми оболочками эффективным количеством газообразного ксенона является количество ксенона, достаточное для достижения улучшенного состояния кожи, ногтей, волос, слизистых оболочек.
Для лечения заболеваний кожи, ногтей, волос, слизистых оболочек, подкожно-жировой клетчатки, соединительной ткани, опорно-двигательного аппарата, мышечной ткани эффективным количеством газообразного ксенона является количество ксенона, достаточное для повышения эффективности проводимой терапии.
Задача достигается также тем, что заявляемый способ введения в кожу газообразного ксенона заключается в том, что для повышения трансдермальной проницаемости лечебных или косметических препаратов для наружного применения введение в кожу от 1,0 до 300,0 об.% газообразного ксенона в составе приемлемого нейтрального носителя или лечебного, или косметического препарата, осуществляют топически по любому из пп.1-6.
Введение в кожу газообразного ксенона для повышения трансдермальной проницаемости лечебных или косметических препаратов осуществляют с разнесением во времени и очередности или одновременно.
Ксенон - инертный благородный газ, абсолютно не токсичен, не вступает в реакции с биологическими молекулами, не проявляет мутагенных, тератогенных, цито- и иммунотоксических свойств. В медицине используется с 1951 г. для ингаляционного наркоза. При введении в организм газ полностью выводится в течение 4-х часов (Sanders R.D., Franks N.P., Maze M. Xenon: no stranger to anaesthesia / Brit J Anaesthesia, 2003. - V.91 (5). - P.709-717). Показан лечебный эффект газа при нейротоксичности различного генеза, болезни Паркинсона, шизофрении, ишемии головного мозга [Буров Н.Е., Потапов В.Н., Макеев Г.Н. Ксенон в анестезиологии - M., Пульс., 2000. - 356 с.; Abraini J.H., David H.N., Lemaire M. Potentially Neuroprotective and Therapeutic Properties of Nitrous Oxide and Xenon - Ann. N.Y. Acad. Sci. 2005, 1053: P.289-300]. Все более широко газ применяется в субнаркотических (малых) дозах для лечебного наркоза при нейротоксичности различного генеза (Abraini J.H., David H.N., Lemaire M. Potentially Neuroprotective and Therapeutic Properties of Nitrous Oxide and Xenon - Ann. N.Y. Acad. Sci. 2005, 1053: P.289-300). Ксенон эффективен и при введении в сосуды головного мозга липосом с этим газом, это способствует значительному ускорению восстановления репарации ткани головного мозга и снижению нейротоксичности после инсульта (Britton G.L., Kim Н., Кее Р.Н. et al. In Vivo Therapeutic Gas Delivery for Neuroprotection with Echogenic Liposomes / Circulation. 2010, 122(16): 1578-1587).
В качестве основного механизма действия ксенона рассматривается его влияние на системы медиаторов, обеспечивающих проведение нервного импульса, в первую очередь, блокаду N-methyl-D-aspartate (NMDA)-рецепторов. Эта сигнальная система первоначально описана для центральной нервной системы, но в дальнейшем была также обнаружена в костной и кроветворной тканях, поджелудочной железе, в глубоких тканях (мышцах, сухожилиях, суставах), нервных окончаниях в сердечной мышце, миокардиоцитах (Skerry Т.М., Genever P.G. Glutamate signalling in non-neuronal tissues / Trends Pharmacol Sci, 2001. V.22. - P.174-181; Alfredson Н., Lorentzon R.J. Chronic tendon pain: no signs of chemical inflammation but high concentrations of the neurotransmitter glutamate. Implications for treatment/Curr Drug Targets, 2002. - V. 3. - P.43-54). Идентифицированы NMDA-рецепторы и в базальном шиповатом и гранулярном слоях кожи человека - (Kinkelin I, Brocker Е-В, Koltzenburg М. et al. Localization ionotropic glutamate receptors in peripheral axons of human skin/Neurosci Lett, 2000. - V. 283. - P.149-152; Nahm W.K., Philpot B.D., Adams M.M. et al. Significance of N-methyl-D-aspartate (NMDA) receptor-mediated signaling in human keratinocytes/J Cell Physiol, 2004. - V. 200 (2). - P.309-317; Fischer M., Glanz D., William T. et al. N-methyl-D-aspartate-receptors influence the intracellular calcium concentration of keratinocytes/Experimental Dermatology, 2004. - V.13 (8). - P.512-519). В настоящее время NMDA-рецепторы рассматривают как мишени для лечения кожных заболеваний человека (Nahm W.K., Philpot B.D., Adams M.M. et al. Significance of N-methyl-D-aspartate (NMDA) receptor-mediated signaling in human keratinocytes/J Cell Physiol, 2004. - V. 200 (2). - P.309-317). С воздействием на них связана эффективность топического применения антагонистов кальциевых каналов, ускоряющих процессы репарации эпителиального барьера (Fuziwara S., Inoue К., Denda М. NMDA-type glutamate receptor is associated with cutaneous barrier homeostasis/J. Invest. Dermatol, 2003, - V..120. - P. 1023-1029). Показано снижение выраженности гиперальгезии, воспалительной гиперемии и мышечной боли у людей при местном поверхностном интрадермальном введении антагониста NMDA кетамина и опиоида фентамина (Koppert W., Zeck S., Blunt J.A., Schmelz M. The Effects of Intradermal Fentanyl and Ketamine on Capsaicin-Induced Secondary Hyperalgesia and Flare Reaction / Anesth Analg, 1999. - V. 89 (6). - p.1521-1527; Cairns B.E., Svensson P., Wang K. et al. Activation of Peripheral NMDA Receptors Contributes to Human Pain and Rat Afferent Discharges Evoked by Injection of Glutamate into the Masseter Muscle J Neurophysiol, 2003. - # 90. - P.2098-2105).
Гиперактивация NMDA-рецепторов является важнейшим фактором в механизмах повреждения тканей при окислительном стрессе (Said S.I., Pakbaz Н., Berisha H.I., Raza S. NMDA receptor activation: critical role in oxidant tissue injury /Free Radical Biology and Medicine, 2000. - V. 28 (8). - P. 1300-1302). В этом отношении вышеописанный механизм действия ксенона непосредственно связан с еще одним его механизмом - способностью регулировать антиоксидантный статус организма. Данный феномен был выявлен российскими ученными в экспериментах на животных, у которых при введении газа отмечено снижение активности процессов перекисного окисления липидов (Буров Н.Е., Потапов В.И., Макеев Г.Н. Ксенон в анестезиологии/М., Пульс, 2000. - 356 с; Применение ксенона в медицине. Под ред. Н.И.Суслова, М.Н.Шписмана, В.Н.Потапова/Томск, 2008. - 300 с). Поскольку ксенон является инертным газом, он не способен непосредственно инактивировать токсичные продукты перекисного окисления липидов, а его эффект определяется свойствами структурного (неспецифического) антиоксиданта. Такие соединения изменяют конфигурацию структурных элементов мембранного липидного бислоя, повышая его резистентность к токсическому действию перекисных радикалов (Кузьменко Д.И., Серебров В.Ю., Удинцев С.Н. Свободнорадикальное окисление липидов, активные формы кислорода и антиоксиданты: роль в физиологии и патологии клетки/Томск, 2007. - 214 с). Ксенон также обладает высоким сродством к основному липидному компоненту биомембран - фосфатидилхолину, растворимость в котором у газа в 6 раз выше, чем в других липидах. Включаясь в него, ксенон изменяет показатели площади поверхности и толщины мембран, а также конфигурации жирнокислотных цепей, экранируя участки липидов, предрасположенные к образованию активных радикалов (Stimson L.M., Vattulainen L, Rog Т. Et al. Exploring the effect of xenon on biomembranes. Cellular & Molecular biology letters, v. 10, 2005, p.563-569; Yuan H.; Jameson C.J.; Murad S. Exploring gas permeability of lipid membranes using coarse-grained molecular dynamics. Molecular Simulation, Volume 35, Issue 10 & 11 September 2009, pages 953-961). Изменяя физико-химические характеристики мембран, в том числе и их вязкость, ксенон влияет и на их проницаемость, тем самым проявляя свойства энхансера, эффект которого является двухэтапным. На первом этапе ксенон снижает вязкость липидов, изменяет конформацию мембран, с одной стороны, повышая их пропускную способность для молекул активных субстанций, с другой стороны - проявляя защитный эффект в качестве антиоксиданта. Второй этап - воздействие газа на NMDA-рецепторы коже, в результате чего меняется ее гомеостаз (Fuziwara S., Inoue К., Denda М. NMDA-type glutamate receptor is associated with cutaneous barrier homeostasis/J. Invest. Dermatol, 2003, - V.. 120. - P. 1023-1029). Наконец, ксенон проявляет специфическое описанное выше анальгетическое воздействие, что создает условия для усиления (потенцирования) эффекта активных субстанций, обладающих аналогичным эффектом.
Обнаружено, что введение ксенона или газообразной смеси, содержащей ксенон, в приемлемый носитель, повышает эффективность лекарственных или косметических средств, нанесенных на кожу или слизистую, вследствие повышения трансэпидермального транспорта биоактивных соединений, входящих в композицию данных средств.
Термин «приемлемый нейтральный носитель» подразумевает газообразные, жидкие, твердые, полутвердые носители. Носители могут также содержать различные активные и целевые добавки, а также носители могут включать стандартные компоненты.
Термин «стандартные компоненты», входящие в приемлемый носитель, используемый в данном тексте описания, подразумевает необходимые ингредиенты, составляющие любую композицию, т.е. смесь натуральных и синтетических продуктов, а именно: растительные и животные масла, стабилизаторы, структурообразователи, загустители, гелеобразователи, эмульгаторы и соэмульгаторы, силиконы и их производные, консерванты, отдушки, реологические добавки, активные субстанции и их смеси, и любые другие, известные и используемые в производстве косметической продукции.
Количество ксенона в конечной композиции в предлагаемых вариантах выполнения композиции составляет 1-300 об.%. При этом, количество введенного ксенона определяют, главным образом, исходя из содержания жировой (масляной) фазы в приемлемом нейтральном носителе, либо лекарственном и/или косметическом препарате.
Верхний предел концентрации ксенона (300 об.%) обоснован возможно максимальной растворимостью газа в чистом масле. Нижний предел концентрации ксенона в приемлемом нейтральном носителе, либо лекарственном и/или косметическом препарате (1 об.%) обоснован тем, что с этого значения содержания ксенона становится заметным проявление свойств этого газа.
Предлагаемые приемлемый нейтральный носитель, либо лекарственный и/или косметический препарат могут находиться в жидкой форме, например, в виде раствора, аэрозоля, пены, капель, суспензии, эмульсии, геля, жидкой мази или других форм, подходящих для нанесения на кожные покровы или слизистые оболочки. Также могут находиться в твердой или полутвердой форме, например, в виде порошка, гранул, пессария, суппозитория, крема, геля, твердой мази или других форм, подходящих для нанесения на кожные покровы или слизистые оболочки.
Термин «эффективное количество газообразного ксенона» в косметических средствах для ухода за кожей, ногтями, волосами, слизистыми оболочками предполагает количество, достаточное для достижения улучшенного состояния кожи, ногтей, волос, слизистых оболочек. А средствах для лечения заболеваний кожи, ногтей, волос, слизистых оболочек, подкожно-жировой клетчатки, соединительной ткани, опорно-двигательного аппарата, мышечной ткани эффективным количеством газообразного ксенона является количество ксенона, достаточное для повышения эффективности проводимой терапии.
Изобретение поясняется примерами и иллюстрациями, отображенными на фигурах 1-4.
На фиг.1 - изображена граница нормальной кожи и полнослойной раны.
На фиг.2 - изображено наползание эпителия через 7 суток эксперимента.
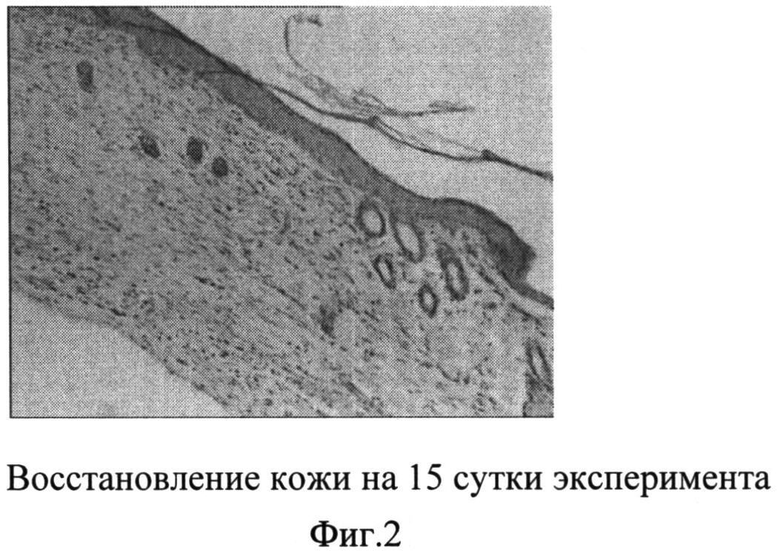
На фиг.3 - изображено восстановление кожи на 15 сутки эксперимента.
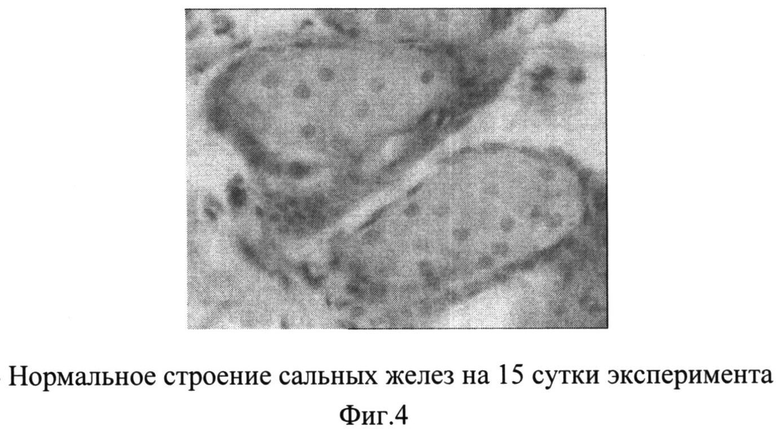
На фиг.4 - изображено нормальное строение сальных желез на 15 сутки эксперимента.
Пример 1
Для демонстрации заявленных эффектов ксенона по повышению проницаемости кожи для компонентов наружных средств, проводили испытания, применяя стандартное оборудование (диффузионные камеры Франца), на коже беспородных кроликов. В качестве образца наружного средства использовали базовую эмульсию следующего состава:
вода деионизированная - 85,0%,
эмульгатор DC 5329 (ПЕГ-12 диметикон) - 3,0%,
циклометикон - 4,0%,
каприк/каприловый триглицерид - 6,0%,
эмульгатор/загуститель SEPIGEL EG - 2,0%
В эту базовую эмульсию во время приготовления добавляли аскорбиновую кислоту в количестве 2,0% в качестве активного компонента. Кожу для испытаний готовили стандартным способом. Площадь диффузии кожи составляла 2,55 см, объем нижней, приемной, камеры составлял 15 мл. В нижней камере находился фосфатный буфер (рН 7,4). Температура в камере составляла 37°С. В начале испытания сверху на кожу наносили 1 мл эмульсии с аскорбиновой кислотой. Испытание проводили в течение 24 часов. Эффективность проницаемости кожи определяли путем измерения количества аскорбиновой кислоты спектрофотометрическим методом. Для этого брали образцы, объемом 1 мл, из нижней камеры. Путем стандартных вычислений и суммирования результатов в течение 24 часов получали количество аскорбиновой кислоты, прошедшей через кожу в нижнюю камеру. Результаты выражали в % от количества аскорбиновой кислоты, содержавшейся в эмульсии, нанесенной в верхней части сверху на кожу.
Описанный выше способ испытания использовали для изучения влияния ксенона в различных способах введения в кожу.
Первый способ: введение ксенона в составе эмульсии, содержащей аскорбиновую кислоту. При данном способе при приготовлении эмульсии, предварительно, в масляную фазу вводили ксенон в различных количествах следующим способом: в шприц объемом 150 мл набирали определенное количество масляной фазы, затем через трубку из баллона туда же набирали необходимое количество ксенона, затем интенсивно перемешивали, растворяя ксенон и компенсируя уменьшение объема перемещением поршня. Масляная фаза в эмульсии составляет 10%. Соответственно, в объемных процентах, содержание ксенона в опытных образцах эмульсии составляло 2 об.%, 5 об.%, 10 об.%, 20 об.% и 30 об.% на 100 г эмульсии. На контрольные образцы кожи наносили эмульсию без ксенона.
Получили следующие результаты, отраженные в таблице 1.
Результаты показали, что максимальный эффект на проницаемость кожи оказывает введение ксенона в концентрации 20 об.% и 30 об.%. Небольшой эффект наблюдается при содержании ксенона в эмульсии в количестве 2 об.% и 5 об.%.
Второй способ: предварительная обработка кожи носителем ксенона. В качестве носителей ксенона использовали деионизированную воду или полиизобутен. В воду ксенон вводили в следующих дозировках: 1 об.%, 5 об.%, 10 об.%. В полиизобутен - 5 об.%, 10 об.%, 50 об.%, 100 об.%, 200 об.%, 300 об.%. Введение ксенона в воду и полиизобутен проводили с помощью шприца, как описано выше.
Контрольные образцы кожи предварительно обрабатывали отдельно водой и полиизобутеном без ксенона путем 3-х кратного смачивания поверхности образцов кожи. Опытные образцы обрабатывали так же, но с содержанием ксенона, как описано выше. Сразу после обработки наносили эмульсию с аскорбиновой кислотой.
Результаты испытания, отраженные в таблицах 2, 3.
Результаты показали, что предварительная обработка поверхности кожи водой с ксеноном увеличивают ее проницаемость для аскорбиновой кислоты. Наибольший эффект наблюдается при содержании ксенона 10 об.%.
В результате испытания получили результаты, показывающие, что предварительная обработка поверхности кожи носителем (полиизобутен) с ксеноном увеличивает проницаемость кожи для аскорбиновой кислоты. Эффект возрастает при увеличении содержания ксенона в носителе.
Аналогичные эффекты были получены при нанесении на кожу носителя с ксеноном перед эмульсией с аскорбиновой кислотой, либо при одновременном нанесении обеих композиций.
Пример 2
Для исследования влияния насыщенной ксеноном воды на гидратантность кожи лица провели испытание на добровольцах (15 женщин) в возрасте от 24 до 39 лет, не имеющих каких-то выраженных изменений кожи лица. Все испытуемые были разбиты на 3 группы, по 5 человек в каждой.
Для исследования готовили деионизированную воду с различным содержанием ксенона: 1%; 5%; 10%. В качестве контроля использовали деионизированную воду.
Схема испытания: в течение 8 дней, испытуемые в группах покрывали левую сторону лица марлевой салфеткой, обильно смоченной водой с ксеноном, в течение 10 минут, в соответствующей концентрации, ежедневно днем и вечером. Правая сторона лица (контроль) у всех испытуемых также обрабатывалась водой без ксенона.
Гидратантность кожи определяли при помощи портативного прибора для определения влажности кожи "Moisture Monitor", (SK, Китай) в % через каждые 2 дня утром. Результаты в группах оценивали в %, суммировали, и выражали в средних показателях.
Результаты испытания отражены в таблице 4.
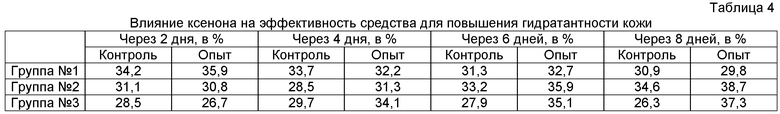
На основе полученных данных видно, что наибольший увлажняющий эффект наблюдался при использовании воды с содержанием ксенона 10 об.% уже через 4 дня наблюдений. Менее выраженный эффект наблюдался при использовании воды с содержанием ксенона 5 об.%. При содержании ксенона в воде в количестве 1 об.% эффекта не наблюдали. Полученные результаты показывают, что поверхностная обработка кожи водой с ксеноном увеличивают проницаемость кожи для воды, таким образом увлажняя ее.
Пример 3
В представленных ниже экспериментах мы исследовали влияние ксенона на процесс заживления раневого повреждения кожи в эксперименте. Эта работа была выполнена на 30 беспородных белых крысах-самцах весом 150-180 г. Всем животным под легким эфирным наркозом, в центральной области верхней трети спины производилось полнослойное иссечение участка кожи. Предварительно на этой поверхности удалялся волосяной покров. Рана имела округлую форму диаметром 6 мм.
Заживление раневой области у всех крыс происходило путем первичного натяжения с формированием характерного струпа темно-коричневого цвета. Материал для исследования забирали на 7 и 15 сутки после операции. Гистологические препараты окрашивали общепринятыми обзорными методами (гематоксилин-эозин, нейтральный красный, азур II-эозин). Все экспериментальные животные были разбиты на 3 группы. Первая группа (10 крыс) - контрольная, т.е. эти животные после иссечения кожи не подвергались никаким воздействиям. Вторая группа (10 крыс) - опытная. Этим животным после иссечения кожи на раневую поверхность наносили крем без ксенона ежедневно утром и вечером. Третья группа (10 крыс) - опытная. Данная группа животных после иссечения кожи подвергалась воздействию крема с ксеноном ежедневно также утром и вечером, результаты отражены на фиг.1-4.
Крем готовили в соответствии с одной из простых рецептур, в состав которой входит: масло оливковое, водный экстракт зверобоя, ксенон, загуститель/эмульгатор DC RM 2051, консервант (смесь парабенов). Использование DC RM 2051 позволяет вводить в состав данного крема большое количество масла (40%). Перед смешиванием и гомогенизацией компонентов, в оливковое масло вводили ксенон из расчета 200 мл ксенона на 100 мл масла. Конечная концентрация ксенона в креме составляла 80 об.%.
В результате морфологических исследований у животных первой группы макроскопически наблюдали незначительное уменьшение размеров раны на протяжении первых 7 суток. Морфологически отмечается начало наползания эпителия на раневую поверхность. На 15 сутки у животных этой группы макроскопически отмечается заживление раны с отторжением струпа. На гистологических препаратах видно восстановление эпителия, однако, элементы дермы и придатков кожи развиты слабо.
Во второй группе крыс картина регенерации (макро- и микроскопически) незначительно отличалась и соответствовала описанной выше. Струп практически исчезал на 9-10 сутки.
В третьей группе на 7 сутки наблюдалось более выраженное заживление раны. Размер раны уменьшался примерно на 2/3, струп почти исчезал. Наблюдалось ускоренное восстановление волосяного покрова в области раны. На 15 сутки строение эпидермиса приближалось к норме, наблюдалась активная регенерация дермы и придатков кожи за счет пролиферации клеточных дермальных элементов, новообразования сосудов.
В результате выполненной экспериментальной работы нами была показана эффективность введения ксенона в состав крема, наносимого на раневую поверхность, для активизации процессов регенерации кожи. Кроме того, было замечено ускоренное восстановление волосяного покрова.
Пример 4
Для исследований и подтверждения заявляемого эффекта использовали две композиции. Первая композиция - носитель с ксеноном. В качестве носителя использовали диизопропил адипат (DIA), в котором растворяли ксенон в диапазоне от 1 до 300 об.% (1%; 3%; 5%; 10%; 50%; 100%; 200%; 300%;). Вторая композиция - крем-гель, включающий следующие стандартные ингредиенты: деионизированная вода, карбопол 974, гиалуроновая кислота, полоксамер 188, диизопропил адипат, витамин А, турмерон (экстракт куркумы), этаноламин, консервант, взятые в известных соотношениях. Используемая косметическая композиция крема для кожи лица имеет увлажняющее, антиоксидантное, разглаживающее действие.
Проведено клиническое исследование, в котором приняли участие добровольцы - 45 женщин в возрасте 35-56 лет с признаками возрастных изменений кожи. В эксперименте участвовали женщины, не принимающие гормональные препараты, не страдающие дерматитами и аллергическими заболеваниями.
Обе композиции предварительно был исследованы в соответствии с требованиями СанПиН 1.2.681-97 «Гигиенические требования к производству и безопасности парфюмерно-косметической продукции», утвержденным Постановлением Главного Государственного санитарного врача РФ от 20/11/97 г. N 26».
Результаты проведенных микробиологических, химико-аналитических, токсикологических исследований показали, что изучаемые композиции безопасны для здоровья человека, не оказывает раздражающего действия, не вызывают аллергию.
Женщины были распределены на 9 групп по 5 человек в каждой. Участницы каждой из групп дважды в день (утром и вечером) в течение 30 дней наносили на кожу лица обе композиции по схеме: после легкой очистки кожи лица сначала наносилась первая композиция, затем, после равномерного распределения и впитывания (через 5 минут), на эту же область наносилась вторая композиция. Оценка эффективности оценивалась методом анкетирования. Предварительное проведение кожных тестов контрольных и опытных образцов кремов у всех участников дало отрицательный результат: у 100% испытуемых отсутствовали признаки раздражения и/или аллергии. Общая удовлетворенность результатами у всех женщин была положительная.
Субъективную оценку эффективности применения композиций проводили по следующим показателям:
- органолептические показатели продукта: текстура, комфортность при применении, отсутствие липкости и жирного блеска.
- показатели состояния кожи: уровень кератинизации, увлажненности, эластичности, микрорельеф кожи, лифтинговый эффект.
- психо-эмоциональное состояние пациентов: самочувствие, активность, уровень невротизации (отсутствие беспокойства, раздражительности), работоспособность.
Показатели оценивали через каждые 3 дня испытания по 5-балльной шкале, суммируя оценки каждой группы. Положительным результатом считали суммарную оценку группы не ниже 20 баллов.
Результаты испытания отражены в таблице 5.
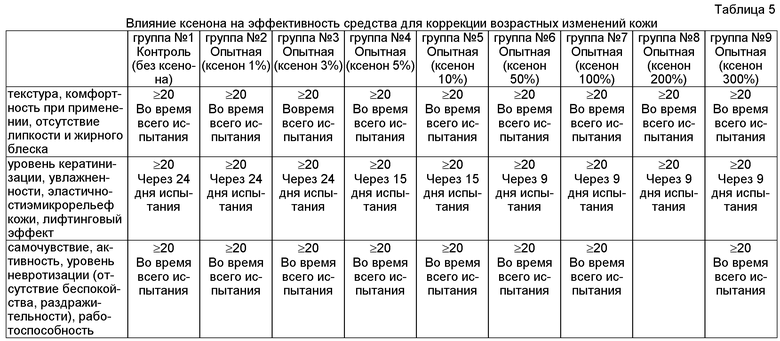
Положительные результаты, полученные в ходе данного исследования, показали, что результат повышения эффективности крема для кожи лица достигается при применении первой композиции с содержанием ксенона уже при 3-5 об.%. Наиболее быстрый эффект в данном испытании достигается при использовании концентрации ксенона в первой композиции начиная с 50 об.%.
Аналогичные эффекты были получены при нанесении на кожу носителя с ксеноном перед нанесением крема-геля либо при одновременном нанесении обеих композиций.
Пример 5
Проведено клиническое исследование, в котором приняли участие добровольцы - 26 женщин в возрасте 42-56 лет с жалобами на боли в поясничном отделе позвоночника. На основании клинического обследования был установлен диагноз: Поясничный остеохондроз, синдром люмбалгии в стадии умеренного обострения.
В эксперименте не участвовали женщины, перенесшие в течение последних 6 месяцев оперативные вмешательства, принимающие какие-либо лекарственные средства либо биологически активные добавки к пище, гормональные препараты, страдающие дерматитами и аллергическими заболеваниями.
Для лечения был использован препарат ДИКЛАК-гель (активное вещество - диклофенак, вспомогательные вещества - изопропиловый спирт, макроголь-7-глицеролкокоат, гипромеллоза, ароматное масло, вода) для локального воздействия на поясничную область.
Содержание ксенона в препарате составляло 1,0 об.%, 5,0 об.%, 10,0 об%, 30,0 об.%.
Женщины были распределены на 5 групп по 3-5 человек в каждой. Участницы каждой из групп дважды в день (утром и вечером) втирали в течение 1-2 минут в кожу поясничной области лекарственное средство без ксенона (контроль), либо данное средство с содержанием ксенона в соответствии с указанными выше концентрациями (опытные группы).
Оценка эффективности оценивалась на основании анализа сроков исчезновения болевого синдрома.
Получены следующие результаты:
Группа 1 (контроль): исчезновение болей через 9-10 дней. (5 пациентов). Группа 2 (содержание ксенона в креме 1,0 об.%): исчезновение болей через 7-11 дней (3 пациента).
Группа 3 (содержание ксенона в креме 5,0 об.%): исчезновение болей через 4-5 дней (5 пациентов).
Группа 4 (содержание ксенона в креме 10,0 об.%): исчезновение болей через 4-5 дней (5 пациентов).
Группа 5 (содержание ксенона в креме 30,0 об.%): исчезновение болей через 2-3 дня (4 пациента).
Результаты показали, что видимый эффект проявляется при содержании ксенона 5,0 об.% в препарате ДИКЛАК-гель. Наибольший эффект - при содержании ксенона 30,0 об.%.
Пример 6
Проведено клиническое исследование, в котором приняли участие добровольцы - 24 женщины в возрасте 42-56 лет с жалобами на боли в поясничном отделе позвоночника. На основании клинического обследования был установлен диагноз: поясничный остеохондроз, синдром люмбалгии в стадии умеренного обострения.
Для лечения был использован препарат ДИКЛАК-гель (активное вещество - диклофенак, вспомогательные вещества - изопропиловый спирт, макроголь-7-глицеролкокоат, гипромеллоза, ароматное масло, вода) для локального воздействия на поясничную область.
В качестве второго средства использовали композицию в виде эмульсии следующего состава: вода, масло оливковое (20%), загуститель/эмульгатор RM 2051 (натрия полиакрилат и диметикон и циклопентасилоксан и тридецет-6 и ПЕГ/ППГ-18/18 диметикон). В эту композицию вводили ксенон в концентрациях: 1%; 5%; 10%; 50%; 100%; 200%; 300% в перерасчете на содержание масла. Конечное содержание ксенона в опытных образцах композиции составляло: 0,2%; 1%; 2%; 10%; 20%; 40%; 60%. Контрольный образец данной композиции не содержал ксенон.
Женщины были распределены на 8 групп по 3 человека в каждой. Участницы каждой из групп дважды в день (утром и вечером) втирали в течение 1-2 минут в кожу поясничной области лекарственное средство с последующим нанесением второго средства/композиции. Интервал между нанесением лекарственного средства и приготовленной композиции/крема составлял 5 минут.
Оценка эффективности композиций оценивалась на основании анализа сроков исчезновения болевого синдрома.
Получены следующие результаты:
Группа 1 (контроль): исчезновение болей через 9-11 дней.
Группа 2 (содержание ксенона в средстве 0,2 об.%): исчезновение болей через 8-11
дней.
Группа 3 (содержание ксенона в средстве 1 об.%): исчезновение болей через 6-8 дней Группа 4 (содержание ксенона в средстве 2 об.%): исчезновение болей через 5-8
дней.
Группа 5 (содержание ксенона в средстве 10 об.%): исчезновение болей через 3-4
дня.
Группа 6 (содержание ксенона в средстве 20 об.%): исчезновение болей через 4-6
дней.
Группа 7 (содержание ксенона в средстве 40 об.%): исчезновение болей через 2-3
дня.
Группа 8 (содержание ксенона в средстве 60 об.%): исчезновение болей через 2-Здня.
В результате испытания можно сказать, - что небольшой эффект наблюдался уже при содержании во втором средстве ксенона 1 об.%. Максимальный эффект наблюдался при содержании ксенона 10-60 об.%.
Аналогичные эффекты были получены при нанесении на кожу носителя с ксеноном перед нанесением препарата ДИКЛАК-гель либо при одновременном нанесении обеих композиций.
Пример 7
Проведено клиническое исследование, в котором приняли участие добровольцы - 18 мужчин в возрасте 30-48 лет с инфицированными бытовыми ранами мягких тканей различной этиологии (порезы, ожоги).
В комплексе лечения был использован препарат ЛЕВОСИН-мазь для наружного применения (активные вещества - левомицетин, сульфадиметоксин, метилурацил, тримекаин).
В препарат вводили ксенон. Содержание газа в препарате составляло 1,0 об.%, 5,0 об.%, 10,0 об.%, 50,0 об.%, 100,0 об.%.
Участники были распределены на 6 групп по 3 человека в каждой. Участники каждой из групп однократно в утренние часы накладывали на раневую поверхность стерильную марлевую салфетку, пропитанную лекарственным средством без ксенона (контроль), либо препарата с содержанием ксенона в соответствии с указанными выше концентрациями (опытные группы).
Оценка эффективности препарата оценивалась на основании анализа сроков эпителизации раневой поверхности.
Получены следующие результаты:
Группа 1 (контроль): эпителизация через 6-7 дней.
Группа 2 (содержание ксенона в креме 1,0 об.%): эпителизация через 6-7 дней.
Группа 3 (содержание ксенона в креме 5,0 об.%): эпителизация через 6-7 дней.
Группа 4 (содержание ксенона в креме 10,0 об.%): эпителизация через 4-6 дней.
Группа 5 (содержание ксенона в креме 50,0 об.%): эпителизация через 4 дня.
Группа 6 (содержание ксенона в креме 100,0 об.%): эпителизация через 3 дня. Результаты: максимальный эффект наблюдали при содержании ксенона в препарате 100,0 об.%. Заметный эффект наступал при содержании ксенона 10,0 об.%.
Пример 8
Проведено клиническое исследование, в котором приняли участие добровольцы - 17 мужчин в возрасте 28-54 лет с открытыми бытовыми ранами мягких тканей рук различной этиологии (порезы, ожоги) небольшой площади (4-7 см2).
В комплексном лечении был использован препарат ЛЕВОСИН-мазь для наружного применения (активные вещества - левомицетин, сульфадиметоксин, метилурацил, тримекаин).
В качестве второго средства использовали композицию в виде эмульсии следующего состава: вода, масло оливковое (20%), загуститель/эмульгатор RM 2051 (натрия полиакрилат и диметикон и циклопентасилоксан и тридецет-6 и ПЭГ/ППГ-18/18 диметикон). В эту композицию вводили ксенон в концентрациях: 1%; 5%; 10%; 50%; 100%; 200%; 300% в перерасчете на содержание масла. Конечное содержание ксенона в опытных образцах композиции составляло: 0,2%; 1%; 2%; 10%; 20%; 40%; 60%. Контрольный образец данной композиции не содержал ксенон.
Участники были распределены на 7 опытных групп по 2 человека в каждой, в контрольной группе было 3 человека. Участники каждой из групп однократно в утренние часы накладывали на раневую поверхность стерильную марлевую салфетку, пропитанную лекарственным средством, поверх которой накладывали такую же салфетку, пропитанную вторым средством без ксенона (контроль), либо средства с содержанием ксенона в соответствии с указанными выше концентрациями (опытные группы).
Оценка эффективности композиций оценивалась на основании анализа сроков эпителизации раневой поверхности.
Получены следующие результаты:
Группа 1 (контроль): эпителизация через 6-8 дней.
Группа 2 (содержание ксенона в средстве 0,2 об.%): эпителизация через 6-7 дней.
Группа 3 (содержание ксенона в средстве 1об.%): эпителизация через 5дней.
Группа 4 (содержание ксенона в средстве 2 об.%): эпителизация через 5-6 дней.
Группа 5 (содержание ксенона в средстве 10 об.%): эпителизация через 4-5 дней.
Группа 6 (содержание ксенона в средстве 20 об.%): эпителизация через 3-5 дней.
Группа 7 (содержание ксенона в средстве 40 об.%): эпителизация через 3 дня.
Группа 8 (содержание ксенона в средстве 60 об.%): эпителизация через 3 дня.
В результате можно сделать вывод что эффект наступает уже при концентрации ксенона во втором средстве 1 об.%, а максимальный эффект - при содержании ксенона 20-60 об.%.
Аналогичные эффекты были получены при нанесении на кожу носителя с ксеноном перед нанесением мази - ЛЕВОСИН либо при одновременном нанесении обеих композиций.
Пример 9
В исследовании использовали оливковое масло, в котором растворяли липофильный краситель - судан черный в концентрации 1%. В опытном образце растворяли ксенон в концентрации 100 об.%. Оба образца, контрольный (без ксенона) и опытный, наносили на переднюю поверхность кожи в области предплечья, площадь нанесения составляла 1 см2, на расстоянии 5 см друг от друга. Наблюдение вели непрерывно в течение 20 минут, визуально определяя площади растекаемости и впитываемости на коже. Всего проводили пять наблюдений, используя различные участки передней поверхности предплечий обеих рук. Результаты наблюдений выражали в процентах. В результате наблюдений было отмечено, что опытный образец имел способность к растеканию на коже в среднем на 38% больше, чем контрольный. Кроме того, после удаления образцов с кожи путем аккуратного промакивания фильтровальной бумагой, было отмечено более интенсивное окрашивание на местах опытных образцов. Таким образом, образцы масла с ксеноном демонстрировали более высокую проницаемость в эпидермис кожи.
Пример 10
Были использованы два средства: молочко для автозагара GARNIER (средство №1) и лосьон для тела также с эффектом автозагара DOVE (средство №2). В средство №1 вводили ксенон в концентрации 30 об.%. В средство №2 вводили ксенон в концентрации 25 об.%. В испытании использовали оба средства с ксеноном (опытные образцы) и без ксенона (контрольные образцы). Контрольные и опытные образцы наносили на кожу передней поверхности предплечья. Площадь нанесения составляла 3 см. Появление пигментации наблюдали в течение 24 часов. Испытание повторяли 5 раз с каждым средством.
Результаты представлены в таблице 6.
В результате наблюдений показано, что введение ксенона в состав коммерческих продуктов Gamier и Dove в концентрации 25-30 об.% ускоряло появление пигментации кожи.
Пример 11
Мы проводили исследование влияния ксенона на эффективность лечения угревой болезни. Для лечения использовалась серная мазь (10%) без ксенона и с ксеноном в концентрации 100 мл ксенона на 100 мл мази. Контрольные и опытные образцы мази наносились на пораженные области кожи лица 3 раза в день, утром, днем, вечером. По итогам работы был получен очень хороший результат у всех 9 пациентов при использовании серной мази с ксеноном. Лечебный эффект отмечался уже через 1 сутки после применения. Причем пациенты наблюдали ускорение впитываемости мази. Через 4-5 дней наблюдались устойчивые признаки выздоровления. При применении серной мази без ксенона признаки выздоровления появлялись только через 7-8 дней.
Вывод: ксенон заметно повышает эффективность серной мази в лечении угревой болезни.
Пример 12
Нами было проведено дерматологическое исследование действия ксенона у больных с микозом стоп, осложненным аллергическим контактным дерматитом, и у больных с себоррейным дерматитом. Для испытания были выбраны пациенты с ярко выраженными симптомами кожных заболеваний. Для испытания готовили оливковое масло с ксеноном (200 мл ксенона на 100 мл масла).
У двух больных (женщины, 52 года и 48 лет) был поставлен диагноз: микоз стоп, осложненный аллергическим контактным дерматитом. Для лечения был использован крем «Тербизил», 1%. Схема лечения: локальное воздействие на правую конечность крема «Тербизил» в режиме чередования - утро-вечер; на левую конечность - крем «Тербизил» в смеси с ксеноновым маслом (1/2) в том же режиме. Результаты оценивали через 7 и 14 дней. Оценка результатов: на левой конечности через дней эритематозная окраска очагов и шелушение уменьшилсь значительно больше, чем на правой. Отчетливо наблюдается регрессия элементов сыпи. Через 14 дней левая конечность имела кожу обычной окраски, элементы сыпи регрессировали, трещины на коже пятки не определяются; на коже правой конечности шелушение сохранялось, трещины на пятке наблюдались. На обоих конечностях микроскопически грибок не выявлялся. Таким образом было отмечено очевидное сокращение сроков лечениия при воздействии на кожу традиционного лекарственного средства (крем «Тербизил», 1%) в сочетании с ксеноновым маслом.
Пример 13
Нами было проведено исследование, в котором участвовали 2 больных (женщины, 18 и 22 лет), с установленным диагнозом - себоррейный дерматит в области волосистой части головы, лба и переносицы. В лечении пациенток в течение 14 дней использовали лосьон «Элокон» по схеме: правая часть головы - лосьон «Элокон» 2 раза в день; левая часть головы - лосьон «Элокон» в смеси с ксеноновым маслом (1/2) тоже 2 раза в день. В результате лечения было отмечено, что через 7 дней на левой части кожи головы эритема и шелушение не наблюдалось, на правой стороне - количество бляшек и краснота уменьшилось, но еще ссохраняется. Через 14 дней левая сторона была полностью здорова, на правой стороне были заметны небольшие очаги шелушения, эритемотозности. На основании полученных результатов мы делаем вывод об ускоренном клиническом выздоровлении при воздействии традиционного лекарственного средства (лосьон «Элокон») в сочетании с ксеноновым маслом. *


Изобретение относится косметической и фармацевтической отраслям промышленности и представляет собой способ повышения трансдермальной проницаемости лечебных или косметических препаратов для наружного применения. Способ включает введение в кожу от 1,0 до 300,0 об.% газообразного ксенона в составе приемлемого нейтрального носителя или лечебного, или косметического препарата. Изобретение обеспечивает повышение эффективности лекарственных или косметических средств за счет повышения трансэпидермального транспорта биоактивных соединений. 2 н. и 6 з.п. ф-лы, 13 пр., 4 илг., 6 табл.
1. Способ повышения трансдермальной проницаемости лечебных или косметических препаратов для наружного применения, включающий введение в кожу от 1,0 до 300,0 об.% газообразного ксенона в составе приемлемого нейтрального носителя или лечебного или косметического препарата.
2. Способ по п.1, в котором в качестве приемлемого нейтрального носителя газообразного ксенона выбирают, по меньшей мере, одно вещество.
3. Способ по п.1, в котором эффективное количество газообразного ксенона растворяют в приемлемом нейтральном носителе, или лечебном или косметическом препарате.
4. Способ по п.1, в котором приемлемый нейтральный носитель ксенона, лечебный или косметический препарат используют в газообразной, или жидкой, или полутвердой, или твердой форме.
5. Способ по п.1, в котором для ухода за кожей, ногтями, волосами, слизистыми оболочками эффективным количеством газообразного ксенона является количество ксенона, достаточное для достижения улучшенного состояния кожи, ногтей, волос, слизистых оболочек.
6. Способ по п.1, в котором для лечения заболеваний кожи, ногтей, волос, слизистых оболочек, подкожно-жировой клетчатки, соединительной ткани, опорно-двигательного аппарата, мышечной ткани эффективным количеством газообразного ксенона является количество ксенона, достаточное для повышения эффективности проводимой терапии.
7. Способ введения в кожу газообразного ксенона, заключающийся в том, что для повышения трансдермальной проницаемости лечебных или косметических препаратов для наружного применения введение в кожу от 1,0 до 300,0 об.% газообразного ксенона в составе приемлемого нейтрального носителя или лечебного или косметического препарата осуществляют топически по любому из пп.1-6.
8. Способ по п.7, в котором введение в кожу эффективного количества газообразного ксенона для повышения трансдермальной проницаемости лечебных или косметических препаратов осуществляют с разнесением во времени и очередности или одновременно.
| US 2005255169 A1, 17.11.2005 | |||
| ПРИМЕНЕНИЕ КСЕНОНА ДЛЯ КОРРЕКЦИИ ПАТОЛОГИЧЕСКИХ ИЗМЕНЕНИЙ В ОРГАНИЗМЕ, СВЯЗАННЫХ С НАРУШЕНИЕМ АНТИОКСИДАНТНОГО СТАТУСА | 2006 |
|
RU2346695C2 |
| ПРИМЕНЕНИЕ КСЕНОНА ДЛЯ СОХРАНЕНИЯ АНТИОКСИДАНТНЫХ СВОЙСТВ ОБЛЕПИХОВОГО МАСЛА | 2006 |
|
RU2325188C1 |
| ПРЕПАРАТ ДЛЯ АДАПТОГЕННОЙ ТЕРАПИИ (ВАРИАНТЫ) И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2003 |
|
RU2228739C1 |
| ШТАМП ДЛЯ ОБЪЕМНОЙ ШТАМПОВКИ КОЛЕЦ | 0 |
|
SU222141A1 |
Авторы
Даты
2014-02-20—Публикация
2012-09-24—Подача