Изобретение относится к способам приготовления нанокристаллического композиционного материала и способам изготовления катода для электролитического получения водорода из водных щелочных и кислотных растворов.
В промышленных электролизерах для электролитического получения водорода из водных щелочных и кислотных растворов используют в качестве материала для катодов железо и/или никель. Известно использование железоникелевых сплавов разного состава. Однако данные металлические электроды обладают высоким перенапряжением реакции выделения водорода. Данные по активности железа, никеля и их сплавов в качестве катодных материалов обобщены в литературе [1]. В случае платиновых металлов перенапряжение низкое, но эти металлы не используются, поскольку являются дорогими и имеют склонность к отравлению каталитическими ядами [1].
В качестве альтернативы металлическим материалам катодов были исследованы карбиды ряда металлов. Одним из наиболее перспективных оказался карбид вольфрама, в частности, в виде спеченных композитов. Однако дефицитность данного материала и вольфрама [2] не позволили использовать карбид вольфрама в качестве материала катода.
Известен способ электролитического получения водорода из растворов электролитов с использованием растворимых анодов по патенту RU №2089670 [3]. Электролиз ведут постоянным током с использованием в качестве растворимых анодов магния или его сплавов. Недостатком данного способа является использование дорогих и дефицитных анодов из магния или его сплавов, а также потери части электроэнергии, связанные с преобразованием переменного тока в постоянный.
Известен способ изготовления наноструктурированного катодного материала на основе никеля для электрохимического водного выделения по полезной модели UA 65397 [4], который включает размещение на горизонтальной поверхности никеля с одной стороны наноструктурированных элементов в виде конусов. На вершины конусов дозированно осаждают платину с насеченного K2[PtC16]. Подают импульсами постоянное напряжение. Недостатком данного способа является необходимость использования дорогостоящей платины.
Была поставлена задача подбора недорогого материала, обладающего пониженным перенапряжением реакции электрохимического выделения водорода, и приготовления на его основе нанокристаллического композиционного материала катода для электролитического получения водорода из водных щелочных и кислотных растворов. Данный материал был получен в результате лабораторных исследований с использованием дешевых исходных компонентов (железа и графита), которые были подвергнуты механохимической обработке для получения метастабильной карбидной фазы (цементита) Fe3C. Известно, что механохимический синтез является традиционным методом получения метастабильных фаз и нанокристаллических композиционных материалов [5].
Кроме того, известно, что получить индивидуальную фазу цементита путем высокотемпературного сплавления железа с углеродом невозможно. Известен метод изготовления электродов из белого чугуна путем обогащения его поверхности цементитом [6]. Сложность получения такого материала не позволяет использовать его в качестве катодного материала.
Поставленная задача решалась тем, что проводят механоактивацию смеси порошков железа и графита в атомном отношении 75:25 в среде аргона в течение 15÷20 ч с получением порошка из наноразмерных зерен цементита и α-Fe при их соотношении (90÷95):(10÷5) мас.% в шаровой планетарной мельнице [7].
Далее материал для изготовления катода предварительно выдерживают в вакууме (остаточное давление 5-10 Па) в течение 1÷2 ч при температуре не более 450÷550°C, а затем ведут его магнитно-импульсное прессование при амплитуде 1÷2 ГПа и длительности импульсов давления 300÷400 мкс [8].
Полученный нанокристаллический композиционный материал сохраняет наноразмерность объемных элементов и обладает электрокаталитической активностью, что дает возможность изготовить из него катод для электролитического получения водорода из водных щелочных и кислотных растворов при перенапряжении электрохимической водородной реакции, например, всего 200 мВ. При этом скорость выделения водорода находится на том же уровне, что и при электролизе кислых сред с помощью платинового катода.
Пример конкретного осуществления предлагаемого изобретения. Механоактивацию проводили в шаровой планетарной мельнице “Fritsch P-7” с ускорением 25 g. В мельницу загружали 10 г смеси порошков железа и графита в атомном соотношении 75:25. Время синтеза составляло 16 ч. Сосуды мельницы (объем 45 см3) и размольные шары диаметром 10 мм (20 шт.) были изготовлены из стали ШХ15 (1% C и 1,5% Cr), отличающейся высокой твердостью, чтобы свести к минимуму загрязнения порошков посторонними примесями. Полученную порошковую смесь цементита Fe3C и α-Fe, находящихся в нанокристаллическом состоянии, подвергали магнитно-импульсному прессованию, которое позволило получить объемный материал катода с сохранением нанокристаллического состояния [5]. Прессование проводили в вакууме (остаточное давление 5-10 Па) при температуре 500°C, амплитуда импульса ~1.5 ГПа и длительность импульса 300 мкс. Предварительно осуществляли дегазацию порошковой смеси в вакууме в течение 1 ч при температуре 500°C.
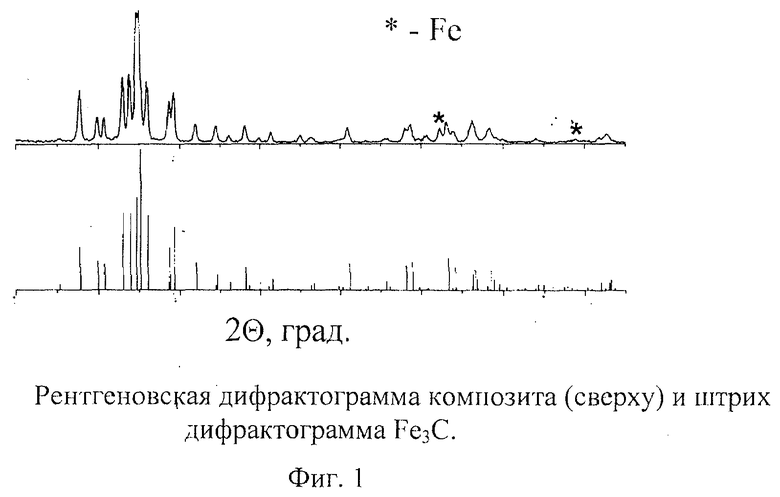
Полученный в результате магнитно-импульсного прессования композит имел форму диска с диаметром 15 мм и толщиной от 1 до 2 мм. Рентгеновская дифрактометрия показала наличие в нем нанокристаллической структуры со средним размером зерна 40 нм (фиг.1) и содержанием не более 5 мас.% железа.
Поляризационные измерения были выполнены в потенциодинамическом режиме на потенциостате IPC-Pro в стандартной электрохимиической ячейке ЯСЭ-2 при комнатной температуре в условиях естественной аэрации. Для сравнения использовали хлорид-серебряный электрод. Измерения проводили для следующих электродов: из заявляемого материала и платины. Измеренные потенциалы приводились относительно стандартного водородного электрода, токи пересчитывались на видимую площадь поверхности образцов. Подготовка поверхности образцов перед электрохимическими исследованиями заключалась в зачистке их поверхности на шлифовальной бумаге и дополнительной шлифовке поверхности порошком Al2O3, смоченным дистиллированной водой. Рабочий Pt-электрод не зачищали, а для удаления примесей его выдерживали в кипящей смеси концентрированной серной кислоты и перекиси водорода (1:1).
Модельными электролитами служили кислые и щелочные сульфатные растворы: 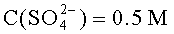
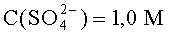
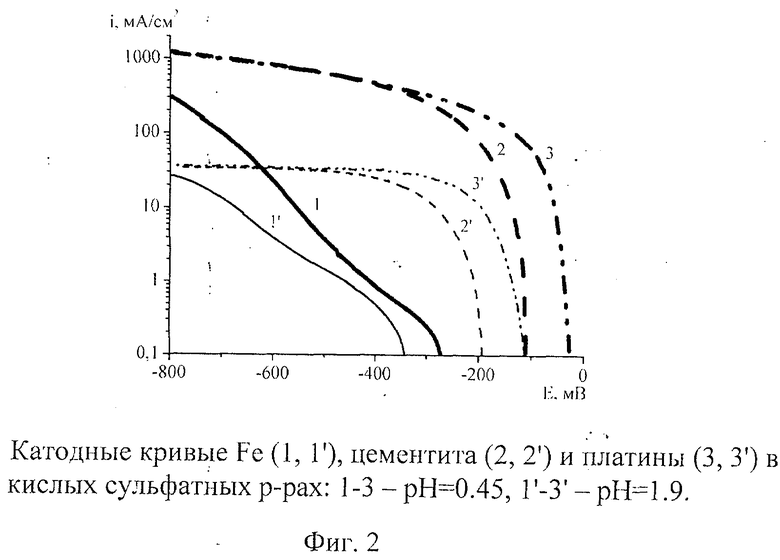
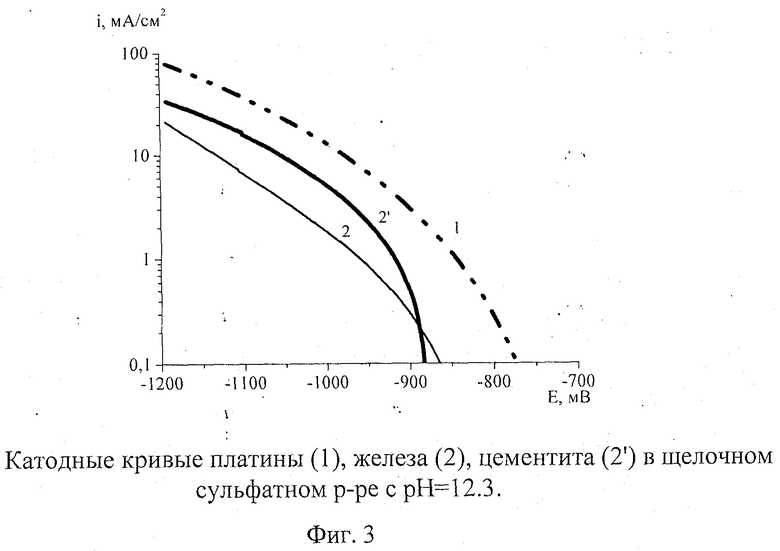
Электрохимическая активность заявленного материала катода измерялась с помощью поляризационных кривых в кислых и щелочных сульфатных растворах. На фиг.2, 3 представлены кривые катодной поляризации ряда материалов - заявленного материала катода, материала катода из железа и гладкой платины в кислых (фиг.2) и щелочных сульфатных (фиг.3) электролитах. В кислых средах при перенапряжении водородной реакции |η|=300 мВ скорость выделения водорода на катоде из заявляемого материала на 3 порядка выше, чем на железе. В щелочных средах скорость выделения водорода на катоде из заявляемого материала в 3 раза выше скорости выделения водорода на электроде из железа. В кислых электролитах в широком диапазоне катодных потенциалов (при перенапряжении реакции выделения водорода |η|>200 мВ) скорости выделения водорода на катоде из заявляемого материала и гладкой платине практически совпадают.
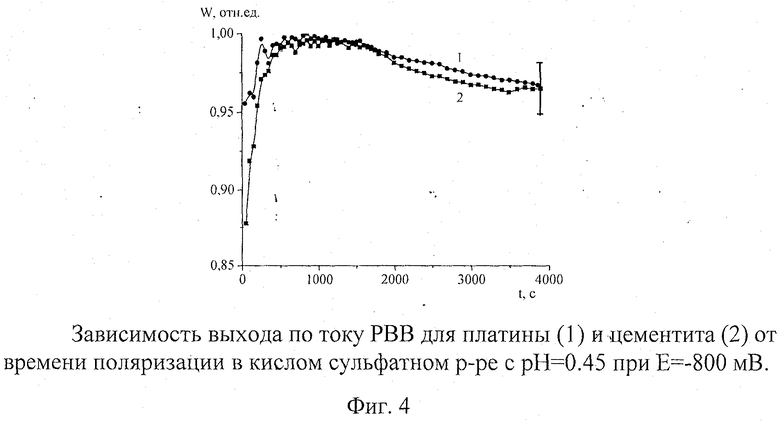
Отдельными экспериментами показано, что катодное выделение водорода в кислом сульфатном растворе (pH=0.45) при потенциале 800 мВ идет с выходом по току, близким к 100% (фиг.4), и разрушения катода из заявляемого материала не происходит. Заявляемый материал катода значительно более активен в кислых средах, чем в щелочных средах.
Одновременно он более коррозионно стоек в кислых средах по сравнению с железом, что делает возможным его использование для электролиза кислых сред.
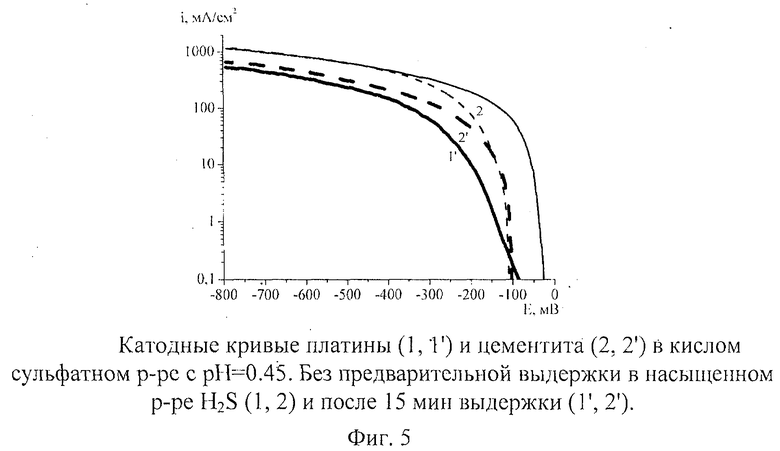
Дополнительными экспериментами показано, что предлагаемый катод не проявляет склонности к отравлению серосодержащими соединениями по сравнению с катодом из платины (фиг.5).
Таким образом, использование признаков заявляемого изобретения дало возможность приготовить недорогой нанокристаллический композиционный материал катода для электролитического получения водорода из водных щелочных и кислотных растворов, обладающий пониженным перенапряжением реакции электрохимического выделения водорода.
Источники информации, принятые во внимание
1. Якименко Л.М. Электрохимическое процессы в химической промышленности: Производство водорода, кислорода, хлора и щелочей. М.: Химия, 1981. 52-60 с. (прототип).
2. Цирлина Г.А., Петрий О.А. // В сб. Итоги науки и техники. Серия Электрохимия. М.: ВИНИТИ, 1987. Т.24. С.154.
3. Патент RU №2089670. Алиев З.М., Гусейнов М.А. Способ получения водорода. C25B 1/02, 1/12. - 3 с.
4. Патент на полезную модель UA №65397. Шевченко А.П., Аксиментьева Е.И., Лут Е.А., Белый А.В. Способ изготовления наноструктурированного катодного материала на основе никеля для электрохимического водного выделения. C25B 1/02, 12.12.2011. - 6 с.
5. Suryanarayana С. Mechanical alloying and milling // Proc. Mater. Sci. - 2001. - V.46. - №1-2. Р.1-184.
6. Коростылева Т.К., Подобаев Н.И., Девяткина Т.С. и др. // Защита металлов. 1982. Т.18. №4. С.551.
7. Елсуков Е.П., Дорофеев Г.А., Фомин В.М., Коныгин Г.Н., Загайнов А.В., Маратканова А.Н. Механически сплавленные порошки Fe(100-x)C(x); x=5-25 ат.%. I. Структура, фазовый состав и температурная стабильность // ФММ. - 2002. - Т.94. - №4. - С.43-54.
8. Иванов В.В., Паранин А.С., Вихрев А.Н. // Патент России №2083328, МПК B22F 3/087, приоритет от 25.10.94. Бюл. №25. 1996. С.4.
| название | год | авторы | номер документа |
|---|---|---|---|
| МАТЕРИАЛ ЭЛЕКТРОДА НА ОСНОВЕ ЖЕЛЕЗА ДЛЯ ЭЛЕКТРОХИМИЧЕСКОГО ПОЛУЧЕНИЯ ВОДОРОДА И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2013 |
|
RU2518466C1 |
| КАТОД ДЛЯ ЭЛЕКТРОХИМИЧЕСКОГО ПОЛУЧЕНИЯ ВОДОРОДА И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2013 |
|
RU2553737C2 |
| СПОСОБ ПОЛУЧЕНИЯ НАНОВИСКЕРНЫХ СТРУКТУР ОКСИДНЫХ ВОЛЬФРАМОВЫХ БРОНЗ НА УГОЛЬНОМ МАТЕРИАЛЕ | 2013 |
|
RU2525543C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СПОСОБ ПОЛУЧЕНИЯ СЛОЖНЫХ ГИБРИДНЫХ КАТАЛИТИЧЕСКИХ СИСТЕМ НА ОСНОВЕ МОДИФИЦИРОВАННОГО УГЛЕРОДА, СОДЕРЖАЩИХ НА ПОВЕРХНОСТИ ОКСИДНЫЕ ВОЛЬФРАМОВЫЕ БРОНЗЫ | 2015 |
|
RU2579119C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЭЛЕКТРОДОВ С ПОРИСТЫМ НИКЕЛЕВЫМ ПОКРЫТИЕМ ДЛЯ ЩЕЛОЧНЫХ ЭЛЕКТРОЛИЗЕРОВ ВОДЫ | 2013 |
|
RU2534014C1 |
| Способ приготовления электрода-катализатора для электрохимического получения водорода | 2022 |
|
RU2813184C1 |
| ЭЛЕКТРОАКТИВИРОВАННЫЙ МАТЕРИАЛ ДЛЯ КАТОДНЫХ ЭЛЕМЕНТОВ И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 1995 |
|
RU2146308C1 |
| Способ изготовления катода | 1981 |
|
SU990876A1 |
| Способ плазмоэлектрохимической переработки графита из использованных литий-ионных аккумуляторов | 2023 |
|
RU2825576C1 |
| АКТИВАЦИЯ КАТОДА | 2010 |
|
RU2518899C2 |
Группа изобретений относится к изготовлению электродов для электролитического получения водорода из водных щелочных и кислотных растворов. Способ получения нанокристаллического композиционного материала катода включает проведение механоактивации смеси порошков железа и графита в атомном отношении 75:25 в среде аргона в течение 15÷20 ч с получением порошковой смеси из наноразмерных зерен цементита Fe3C и α-Fe при их соотношении в мас.%: (90÷95):(10÷5). Способ изготовления катода включает предварительную выдержку упомянутого нанокристаллического композиционного материала в вакууме 5÷10 Па в течение 1÷2 ч при температуре 450÷550°С, после чего проводят его магнитно-импульсное прессование при амплитуде 1÷2 ГПа и длительности импульсов давления 300÷400 мкс. Обеспечивается изготовление катода с пониженным перенапряжением реакции электрохимического выделения водорода. 4 н. и 1 з.п. ф-лы, 1 пр., 5 ил.
1. Способ получения нанокристаллического композиционного материала катода для электролитического получения водорода из водных щелочных и кислотных растворов, отличающийся тем, что проводят механоактивацию смеси порошков железа и графита в атомном отношении 75:25 в среде аргона в течение 15÷20 ч с получением порошковой смеси из наноразмерных зерен цементита Fe3C и α-Fe при их соотношении в мас.%: (90÷95):(10÷5).
2. Способ по п.1, отличающийся тем, что механоактивацию смеси порошков железа и графита проводят в шаровой планетарной мельнице.
3. Нанокристаллический композиционный материал катода для электролитического получения водорода из водных щелочных и кислотных растворов, характеризующийся тем, что он получен способом по любому из пп.1, 2.
4. Способ изготовления катода для электролитического получения водорода из водных щелочных и кислотных растворов, характеризующийся тем, что нанокристаллический композиционный материал по п.3 предварительно выдерживают в вакууме 5÷10 Па в течение 1÷2 ч при температуре 450÷550°С и затем проводят его магнитно-импульсное прессование при амплитуде 1÷2 ГПа и длительности импульсов давления 300÷400 мкс.
5. Катод для электролитического получения водорода из водных щелочных и кислотных растворов, характеризующийся тем, что он изготовлен способом по п.4.
| Способ количественного определения ортодинитробензола в техническом динитробензоле | 1944 |
|
SU65397A1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРОДА | 1995 |
|
RU2089670C1 |
| WO 1986006108 A1, 23.10.1986 | |||
| ЛОМАЕВА С.Ф | |||
| и др., Структура и свойства нанокомпозитов, полученных механоактивацией железа в кремнийорганической среде, Химическая физика и мезоскопия, Том 10, N2, 2008, стр.186-199 | |||
Авторы
Даты
2014-04-10—Публикация
2011-12-13—Подача