Изобретение относится к химической технологии, связано с извлечением редкоземельных элементов из фосфорной кислоты при переработке хибинских апатитовых концентратов на удобрения.
Следует отметить, что мировой рынок редких и, особенно, редкоземельных элементов в последние годы несколько лихорадит. Окончательно истощились накопления, образованные некоторыми оффшорными компаниями при ликвидации госзапасов Советского Союза. Китайская Народная Республика в течение десяти-пятнадцати лет практически завоевала место основного поставщика редкоземельных элементов (далее РЗЭ) и их производных на мировой рынок, имея большие запасы редкоземельного сырья (Баатоу) и мощные предприятия по его переработке. В 2010 г., после ухода с рынка РЗЭ многих компаний, КНР подняла цены на редкометальную продукцию (оксиды РЗЭ, РЗЭ в металлическом виде) на порядок! В связи с этим обстоятельством решение проблем попутного извлечения РЗМ за счет повышения коэффициента комплексного использования такого сырья как хибинские апатитовые концентраты (далее ХАК) становится весьма актуальным.
Содержание РЗМ в фосфорной кислоте при переработке ХАК составляет в среднем 1+-0,3 г/л, казалось бы не много, однако, ежегодно перерабатывается не менее 10 миллионов тонн ХАК, т.е. речь идет примерно о 2-3 тысячах попутных тонн РЗЭ только в составе экстракционной фосфорной кислоты. Локшин и сотр. [1] отмечают, что при переработке ХАК по методу двойного гидрата в экстракционную фосфорную кислоту (далее ЭФК) переходит в среднем от 30 до 75% иттрия, содержащегося в ХАК, 18-30% европия, 20-26% самария, 6,3-8,5% лантана, 11,3-14,5% церия, до 20% неодима.
При проведении патентно-лицензионного исследования за последние 15 лет по вопросам извлечения РЗМ из ЭФК в России было обнаружено всего три технических решения на уровне выданных патентов на изобретения:
- RU - 2040472, Чиркст Д.Э., Чалиян К.Н., Мелихов И.В., Дибров И.А. и др. "Способ выделения фосфата редкоземельных металлов из экстракционной фосфорной кислоты" 1995.07.25 [2],
- RU - 2132303, Завизион П.Я., Классен П.В., Казак В.Г., Олифсон А.Л. "Способ осаждения редкоземельных элементов из экстракционной фосфорной кислоты," 1999.06.27 [3],
- RU - 2381178, Локшин Э.П., Тареева О.А. "Способ извлечения лантаноидов из экстракционной фосфорной кислоты," 2010.02.10 [4].
Авторы работы [2] предлагают пропускать ЭФК снизу вверх через затравку из гранул гексагонального фосфата суммы РЗЭ в течение 5-15 мин при 60-80°C и массовом соотношении ЭФК и затравки 5-15:1, причем РЗМ осаждаются из ЭФК на затравке в виде фосфатов. Предложение вряд ли осуществимо в производственных условиях, ибо подразумевает смену затравки каждые 5-15 мин, а требование выдержки массового соотношения ЭФК и затравки на уровне 5-15:1 свидетельствует о том, что затравка очень быстро пассивируется (теряет способность осаждать на поверхности гранул новые порции фосфатов РЗМ). Эта потеря активности в той или иной степени свойственна всем методам извлечения РЗМ из ЭФК путем образования труднорастворимых соединений: будь то фосфаты, фториды или двойные сульфаты РЗЭ и щелочных металлов. К тому же даже в лабораторных условиях извлечение РЗМ в концентраты часто не превышает 50-70%, а отделение концентратов и их переработка связаны с большой продолжительностью этих операций.
В работе [3] предлагается нейтрализовать ЭФК до pH 3-3,5 циркуляционной пульпой, предварительно нейтрализованной до pH 4-4,5, причем нейтрализацию циркулярной пульпы до pH 4-4,5 ведут аммиаком, кальцинированной содой, карбонатом кальция, известью или другими нейтрализующими реагентами, а отделение осадка фосфатов РЗЭ (концентрата РЗЭ) ведут либо фильтрацией, либо центрифугированием.
Следует отметить, что авторы уделили должное внимание деликатному выполнению операции осаждения с тем, чтобы pH 3-3,5 было достигнуто постепенно и во всем объеме ЭФК, что влияет на качество концентрата, минимизируя соосаждение примесей. Приводится средний состав фосфатного концентрата в мас.%: Сумма РЗЭ - 1,73-2,3; диоксид титана - 2,1-2,2; оксид железа 3+ - 3,2-3,5; оксид кальция - 10,3-10,5; фтор - 4,3-4,6; фосфорный ангидрид - 46,4-46,7; сульфат-ион - 3,0-3,5. Специалисты считают, что переработка столь бедного по содержанию суммы РЗЭ фосфатного концентрата затруднена и нецелесообразна [1].
Локшин Э.П. и Тареева О.А. [4] рекомендуют предварительно добавлять при 65-80°C в ЭФК натриевую соль (карбонат, сульфат или хлорид) до содержания 10 г/л по Na2O. Осадок гексафторсиликата натрия отделяют от ЭФК и прибавляют к ней серную кислоту до обеспечения ее концентрации 10-15%. При этом в течение 5 часов формируется осадок двойных сульфатов РЗМ и натрия, который является концентратом РЗМ. Способ совместим с дигидратной технологией переработки ХАК. Степень извлечения лантаноидов в концентрат достигает 87,7%, а максимальное содержание суммы РЗЭ в концентрате составило 21,9 мас.%.
Метод Локшина Э.П. и Тареевой О.А. следует признать высшим достижением методик концентрирования РЗМ из ЭФК в виде труднорастворимых соединений, этот способ является прототипом предлагаемого технического решения, однако при всем совершенстве и глубочайшем понимании авторами как технологии РЗМ, так и технологии переработки ХАК прототип отнюдь не свободен от недостатков. Часть этих недостатков сформулировали сами авторы [1, 5], отметив то обстоятельство, что РЗЭ иттриевой группы далеко не полно осаждаются в виде двойных сульфатов. Весьма продолжительные процессы созревания и отделения двух осадков требуют установки громоздкого и дорогостоящего оборудования и увеличивают такой показатель как объем незавершенного производства.
Настоящее изобретение направлено на достижение технического результата, заключающегося в увеличении извлечения суммы РЗЭ (до близкого к 100%) из ЭФК (30-38,5% масс.) с температурой от 15 до 80°C и позволяющего преодолеть недостатки аналогов в существенной мере или полностью, с получением концентратов, содержащих от 38,4 до 72,9 суммы РЗЭ при уменьшенном содержании примесей других элементов.
Технический результат достигается за счет того, что в известный способ извлечения редкоземельных элементов из экстракционной фосфорной кислоты при переработке хибинских апатитовых концентратов, включающий сорбцию, осуществляемую в заданном диапазоне температур, отделение очищенной фосфорной кислоты от насыщенного сорбента, промывку сорбента водой, десорбцию с получением товарного десорбата, внесены изменения, а именно:
- в качестве сорбента применяют сильнокислотные макропористые катиониты, преимущественно Purolite С-150;
- десорбцию проводят раствором нитрата аммония, имеющего концентрацию в пределах заданного диапазона;
- полученный товарный десорбат подвергают дополнительной экстракционной очистке 100%-ным трибутилфосфатом.
Кроме того, процесс сорбции осуществляют в противотоке "ЭФК - смола" при объемном соотношении Ж:Т, равном (8÷10):1, при температуре 40-80°C, а десорбцию проводят в противотоке "десорбирующий раствор-смола" при объемном соотношении Ж:Т=(0,5÷1):1, причем десорбирующий раствор нитрата аммония имеет концентрацию в диапазоне 200-600 г/л, предпочтительно - 450-550 г/л.
Оптимальные параметры процессов сорбции и десорбции установлены на основании многочисленных испытаний и анализа полученных результатов.
Нами было открыто и изучено явление сорбции суммы РЗЭ и примесей из ЭФК на макропористых сильнокислотных катионитах. Катиониты такого типа отличаются высокой термостойкостью, не теряют емкость при нагреве до 120-150°C, превышают по своей емкости в среде ЭФК гелевые сильнокислотные катиониты, в среднем, в полтора-два раза, позволяют организовать процесс “сорбции-десорбции” в режиме противотока в аппаратах со стационарным или движущимся слоем, в пачуках или в режиме пульсационного перемешивания с обеспечением практически 95-100% извлечения катионов РЗЭ, содержащихся в ЭФК.
То обстоятельство, что ионообменные методы ранее не были обнаружены при патентно-лицензионном поиске технических решений для извлечения ионов РЗЭ из ЭФК может быть связано с глубоким априорным убеждением специалистов даже очень высокой квалификации в невозможности сколько-нибудь существенной сорбции катионов РЗЭ на ионообменных смолах при таких высоких концентрациях фосфорной кислоты как 300-400 г/дм3. О справедливости заключения, сделанного выше, свидетельствует то обстоятельство, что такие опытные специалисты как Локшин и его сотрудники, приводя в своей работе [1] обзор всех существующих способов извлечения суммы РЗЭ из ЭФК, ни словом не упоминают об ионном обмене.
Сорбция суммы катионов РЗЭ из ЭФК на различных катионитах была изучена нами как в статических, так и в динамических условиях на стационарных слоях ионообменников и при комнатной и при повышенных температурах вплоть до 80°C на заводском образце ЭФК, содержащем в г/дм3 следующие компоненты:
P2O5 - 350,0; F - 19,52; Fe2O3 - 2,91; Al2O3 - 5,90; TiO2 - 1,62; ΣРЗЭ - 1,1; плотность ρ - 1,276 г/см3. При этом доля индивидуальных РЗЭ в сумме составляла в мас.%: La2O3 - 14,1; CeO2 - 26,7; Рг6О11 - 3,9; Nd2O3 - 24,8; Sm2O3 - 4,0; Dy2O3 - 2,3; Y2O3 - 18,2; Eu2O3 - 1,0; Gd2O3 - 4,3; Ho2O3 - 0,7. Десорбцию РЗЭ с катеонита проводили растворами нитрата аммония, начальная концентрация десорбирующего раствора указывается конкретно в каждом примере.
Пример 1. Сорбция в статических условиях изучалась в стаканах из полипропилена объемом 0,5 литра при использовании 10 различных образцов смол
Объем загруженного сорбента в набухшем состоянии в среде дистиллированной воды после промывки щелочью, дистиллированной водой, кислотой, дистиллированной водой - 5 см3. Объем ЭФК - 400 см3.
Продолжительность контакта при постоянном перемешивании - 8 час, причем скорость вращения пропеллерной мешалки подбиралась такой, чтобы вся смола зависала в растворе ЭФК. Контроль состояния контакта “катеонит - ЭФК” проводили визуально, благодаря прозрачности полипропиленовых стаканов. Температура процесса - 20°C.
Содержание поглощенных из ЭФК веществ в образцах смол определяли после мокрого озоления каждого образца обработкой при нагреве в концентрированной серной кислоте при периодических добавках перекиси водорода и азотной кислоты для полного перевода минеральных компонентов в раствор. При анализе использовались современные приборы для эмиссионного спектрального анализа с индукционно стабилизированной плазмой и для атомно-абсорбционного анализа. Результаты приведены в табл.1.
Лучшим по сорбции РЗЭ из ЭФК оказался английский сорбент сильнокислотный макропористый Purolite С-150 (далее Пьюролайт С-150), образец №3 в табл.1, его емкость - 17 кг/тонну при 20°C. Заслуживают дальнейшего изучения также образцы №4 и №5.
Следует особо отметить, что образцы 3-5 очень слабо поглощают (по-видимому, по механизму доннановского поглощения) железо, титан, фосфор и фтор. Образец №9 довольно хорошо поглощает РЗЭ, однако имеет высокую емкость по примесям.
С целью окончательного выбора сорбента были проведены динамические испытания образцов сорбента.
Пример 2. Сорбция в динамических условиях изучалась на колонках из органического стекла со стационарным слоем
Испытывались три образца смол №№1, 2 и 3 из табл.1. Объем каждого образца смолы, набухшего в дистиллированной воде, был равен 1100 мл, внутренний диаметр колонок из оргстекла равнялся 45 мм, их высота - 800 мм. Начальная высота слоя сорбентов равнялась 700 мм. ЭФК подавалась перистальтическими насосами сверху вниз в каждую колонку с линейной скоростью 0,63 м/час, что соответствует для колонок такого диаметра объемной скорости, равной 1 литр/час. Всего через каждую колонку было пропущено по 20 литров ЭФК. Из каждого литра раствора ЭФК, прошедшего через колонку, отбиралась аликвота для анализа на сумму РЗЭ, а также на содержание железа, алюминия и титана. По результатам анализа строились выходные кривые и по ним определялась полная обменная емкость в динамических условиях по сумме РЗЭ, железу, алюминию и титану. Оказалось, что при относительно большой скорости подачи ЭФК на всех трех образцах проскок наступал уже на первом литре раствора ЭФК, однако проскок по примесям железа, алюминия и титана выражен гораздо ярче и насыщение по ним происходит раньше, чем насыщение по сумме РЗМ. Форма и сильная растянутость выходных кривых позволяют предположить, что процесс “сорбции-десорбции” РЗЭ из ЭФК целесообразно выполнять в аппаратах с воздушным перемешиванием - пачуках, при этом сорбцию проводят в противотоке “ЭФК-смола” при объемном соотношении Ж:Т, равном (8÷10):1, а полную десорбцию суммы РЗЭ из катеонитов проводят при объемном соотношении Ж:Т, равном (0,5÷1):1. Установлено, что полная динамическая обменная емкость для КУ-2-8, КУ-23 и Пьюролайт С - 150 составляет соответственно (% мас.), 10; 0,69 и 1,60, что для сорбентов №№1 и 3 в табл.1 хорошо согласуется с их емкостью в статических условиях.
Пример 3. Влияние температуры на извлечение суммы РЗЭ на макропористых сильнокислотных катионитах
Взаимосвязь между емкостью катионита и температурой процесса ионообмена была изучена на образцах катионитов КУ - 2-8 и Пьюролайт С-150 в статических условиях. При этом 10 мл образца смолы в набухшем в дистиллированной воде состоянии приводили в контакт с одним литром ЭФК при перемешивании в полипропиленовых стаканах в течение 4 часов в термостате, поддерживавшем температуру процесса с отклонением не более 0,5°C. Для каждой марки катионита проводилось два параллельных идентичных опыта при одной температуре. По окончании контакта образец катионита отделяли от раствора ЭФК и определяли содержание в нем суммы РЗЭ. Данные о емкости катионитов в зависимости от температуры процесса приведены в табл.2.
Данные табл.2 свидетельствуют об умеренном росте емкости катионитов по сумме РЗЭ с увеличением температуры процесса. С повышением температуры также снижается в несколько раз продолжительность достижения равновесия при сорбции на катионите суммы РЗЭ из ЭФК, т.е. улучшается кинетика процесса. В связи с этими обстоятельствами предпочтительно проводить извлечение РЗЭ из ЭФК в интервале температур от 40 до 80°C, что согласуется с производственными условиями, где температура кислоты находится в пределах от 60 до 80°C.
На основании вышеприведенных исследований был выбран наиболее оптимальный сорбент и установлены предварительные параметры процессов сорбции, десорбции и промывки сорбента.
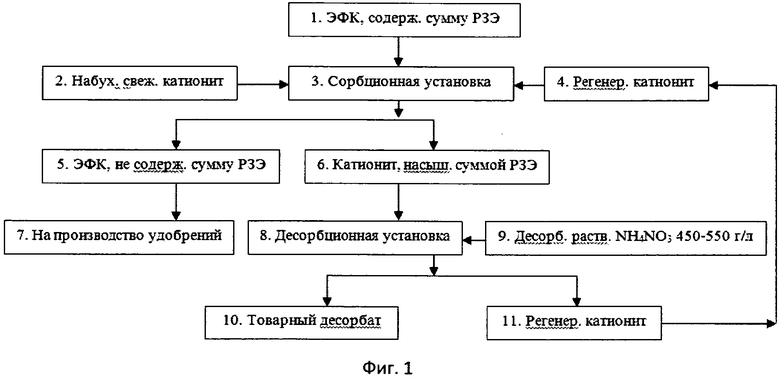
Для выбора оптимальных параметров были проведены испытания предлагаемого способа извлечения РЗЭ из ЭФК на полупромышленной установке. Химико-технологическая блок-схема (ХТС) приведена на фиг.1. Она включает основные средства для осуществления отдельных операций процесса извлечения РЗЭ из ЭФК.
На схеме (фиг.1) приведены следующие блоки: 1 - подачи ЭФК, содержащей РЗЭ, на сорбцию; 2 - подачи катеонита на сорбционную установку 3; 3 - сорбционная установка; 4 - подачи регенерированного катеонита на сорбционную установку; 5 - емкость для ЭФК, не содержащей РЗЭ; 6 - емкость для катионита, насыщенного РЗЭ; 7 - средства для транспортировки ЭФК, не содержащей РЗЭ на производство удобрений; 8 - десорбционная установка; 9 - средства подачи нитрата аммония на десорбцию; 10 - хранилище товарного десорбата; 11 - емкость для регенерированного катионита.
Пример 4. Экстракционная фосфорная кислота с температурой 40°C (блок 1) поступала на четыре сорбционные колонки высотой по 2 метра (блок 3), в которых находился сильнокислотный макропористый катеонит (смола Пьюролайт С-150) из блока 2. Смола насыщалась по сумме РЗЭ путем пропускания через колонки ЭФК при соотношении Ж:Т=(8÷9):1 до окончания процесса сорбции.
Затем смола промывалась от ЭФК водой при соотношении 2 объема воды на 1 объем смолы, причем ЭФК, не содержащая сумму РЗЭ, из блока 5 поступала на производство удобрений (блок 7), а катеонит (смола), насыщенная суммой РЗЭ, из емкости 6 поступала на десорбционную установку 8, где проводилась десорбция суммы РЗЭ раствором, содержащим 550 г/дм3 нитрата аммония. Одновременно с РЗЭ при десорбции вымывались примеси железа, алюминия, титана, фосфора, фтора и др. элементов с получением раствора, называемого товарный десорбат, а регенерированный катеонит возвращался в процесс на стадию сорбции (блок 4).
Большую часть товарного десорбата обработали раствором аммиачной воды с получением 282 г осадка - концентрат РЗЭ №1. Остаток товарного десорбата обработали 100% трибутилфосфатом (ТБФ) с целью извлечения РЗЭ в органическую фазу для очистки от примесей железа, алюминия, фосфора и фтора. Рафинат может идти на приготовление десорбирующего раствора после фильтрации через уголь МАУ для отделения микропримесей ТБФ. Экстракт подвергался реэкстракции водой, подкисленной азотной кислотой, с получением реэкстракта РЗЭ, практически не содержащего примесей железа и др. элементов и оборотного 100% ТБФ. Реэкстракт также обработали раствором аммиачной воды с получением 64 г концентрата №2. Данные о содержании суммы РЗЭ и примесей во влажных и сухих концентратах №1 и №2 приведены в табл.3.
Как видно из данных табл.3, в концентрате №2 резко снижено содержание примесей железа, алюминия, фосфорного ангидрида и фтора.
Для сравнения приведем состав одного из лучших концентратов, полученного по способу-прототипу (% мас., на сухое вещество): Сумма РЗЭ - 21,9; Оксид натрия - 4,2; Сульфат-ион - 30,0; Фосфорный ангидрид - 0,46; Оксид кальция - 10,0; Оксид стронция - 0,49; Оксид алюминия - 0,2; Оксид железа - 3,14; Диоксид кремния - 0,23; Диоксид титана - 0,4. Большое содержание кальция и стронция, а также диоксидов титана и кремния в этом концентрате могут вызвать дополнительные трудности при получении чистых лантаноидов.
В табл.4 приведен состав суммы РЗЭ в концентратах №1 и №2 по индивидуальным элементам.
Данные табл.4 фактически впервые подтверждают предположения о переходе в состав ЭФК в небольших, но реальных количествах (просто больше в ЭФК не содержится!) таких индивидуальных РЗЭ, как празеодим, самарий, европий, диспрозий, гадолиний и гольмий. Необходимо особо отметить, что этот факт свидетельствует о получении новых знаний в технологии РЗЭ из ЭФК. Доказано, что тяжелые РЗЭ не только переходят в состав ЭФК при переработке ХАК, но и могут быть извлечены из нее путем сорбции на сильнокислотных макропористых катионитах. Это обстоятельство является также косвенным свидетельством возможности практически 100% извлечения суммы РЗЭ из ЭФК методом ионообмена на сильнокислотных макропористых катионитах.
По методу прототипа как раз тяжелые индивидуальные РЗЭ иттриевой группы не полностью осаждаются в виде двойных сульфатов.
ХТС, приведенная на фиг.1, отличается гибкостью, позволяя проводить выпуск двух разных по качеству концентратов. На ней были отработаны все операции и возможные пределы параметров для рекомендации их в условиях крупномасштабного химического производства.
Испытания по влиянию соотношения Ж:Т на процесс сорбции проводились при одинаковых условиях - температуре и времени контакта (см. табл.5)
Из таблицы 5 видно, что при соотношении Ж:Т=7:1 емкость сорбента развивается недостаточно и составляет около 70% от максимально возможной при одинаковых условиях эксперимента.
При увеличении соотношения Ж:Т емкость сорбента практически достигает максимальной величины уже при Ж:Т=8:1 и сохраняется при дальнейшем увеличении соотношения. Однако оптимальным является выбор соотношения Ж:Т в пределах (8÷10):1, при этом остаточная концентрация РЗЭ в ЭФК не превышает 0,04 г/л, а также достигается наилучшее перемешивание пульпы и емкость сорбента по РЗЭ.
При дальнейшем увеличении соотношения Ж:Т концентрация РЗЭ в катионите немного падает; для достижения максимальной емкости сорбента необходимо увеличивать время контакта смолы с ЭФК.
Результаты опытов по влиянию концентрации десорбирующего раствора нитрата аммония на процесс десорбции приведены в таблице 6.
Из таблицы 6 видно, что при низких концентрациях нитрата аммония (100, 200 г/л) остаточное содержание ΣРЗО в сорбенте составляет 1,12 и 0,63% (75 и 58% от исходного) соответственно, при общем объеме пропущенного раствора 4,0 л. Для практически полной десорбции РЗЭ при таких концентрациях нитрата аммония (до концентрации в сорбенте менее 0,1%) необходимо увеличивать объемы десорбирующего раствора в 1,5 раза. При дальнейшем повышении концентрации нитрата аммония видно, что остаточная концентрация РЗЭ в сорбенте не превышает 0,07% в диапазоне концентраций нитрата аммония 450-550 г/л, причем объем десорбирующего раствора не увеличивается, что является оптимальным для проведения процесса. Также из таблицы 6 видно, что увеличение концентрации нитрата аммония выше 600 г/л нецелесообразно, так как равновесная остаточная концентрация РЗЭ в сорбенте - 0,04% достигается уже при максимальной концентрации 600 г/л по нитрату аммония.
Результаты испытаний на влияние отношения Ж:Т на процесс десорбции приведены в таблице 7.
Из таблицы 7 видно, что при соотношении Ж:Т=0,3:1 остаточная концентрация РЗЭ в сорбенте равна 0,6%, что свидетельствует о недостаточном объеме десорбирующего раствора. Полный съем РЗЭ со смолы достигается при Ж:Т, равным не менее 0,5:1. При увеличении Ж:Т выше значения 1:1 происходит разбавление десорбата. В данном случае оптимальным можно считать значение Ж:Т=0,8:1.
Преимущество предлагаемого способа перед известными техническими решениями является более полное извлечение суммы РЗЭ и получение более качественного концентрата при обработке полученного товарного десорбата, позволяющего извлечь такие индивидуальные РЗЭ, как празеодим, самарий, европий, диспрозий, гадолиний и гольмий. В настоящее время способ извлечения РЗЭ из ЭФК, полученной из хибинского апатитового концентрата, проходит заводские испытания на ОАО «ФосАгро-Череповец» и после их окончания, а также анализа полученных результатов, планируется внедрение на других предприятиях ЗАО «ФосАгро АГ».
Список литературы
[1] Локшин Э.П., Иваненко В.И., Тареева О.А., Корнейков Р.И. // Извлечение лантаноидов из фосфорнокислых растворов с использованием сорбционных методов. - ЖПХ. - 2009. - т.82. - вып.4. - С.544-551.
[2] RU - 2040472. - “Способ выделения фосфата редкоземельных металлов из экстракционной фосфорной кислоты”. - 1995.07.25.
[3] RU - 2132303. - “Способ осаждения редкоземельных элементов из экстракционной фосфорной кислоты”. - 1999.06.27.
[4] RU - 23811178. - “Способ извлечения лантаноидов из экстракционной фосфорной кислоты”. - 2010.02.10
[5] Локшин Э.П., Тареева О.А. // Выделение лантаноидов из экстракционной фосфорной кислоты дигидратного процесса. - 2010. - ЖПХ. - т.83. - вып.6. - С.899-905.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ИЗВЛЕЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ ИЗ НИТРОФОСФАТНОГО РАСТВОРА ПРИ АЗОТНОКИСЛОТНОЙ ПЕРЕРАБОТКЕ АПАТИТОВОГО КОНЦЕНТРАТА | 2014 |
|
RU2559476C1 |
| СПОСОБ ПЕРЕРАБОТКИ КОНЦЕНТРАТА РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ | 2015 |
|
RU2595672C1 |
| СПОСОБ ПЕРЕРАБОТКИ ФОСФОГИПСА ДЛЯ ПРОИЗВОДСТВА КОНЦЕНТРАТА РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ И ГИПСА | 2013 |
|
RU2520877C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ ИЗ ЭКСТРАКЦИОННОЙ ФОСФОРНОЙ КИСЛОТЫ | 2013 |
|
RU2525947C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ МЕТАЛЛОВ ИЗ ФОСФОГИПСА | 2012 |
|
RU2491362C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ ИЗ ЭКСТРАКЦИОННОЙ ФОСФОРНОЙ КИСЛОТЫ | 2013 |
|
RU2545337C2 |
| СПОСОБ ИЗВЛЕЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ ИЗ ЭКСТРАКЦИОННОЙ ФОСФОРНОЙ КИСЛОТЫ | 2013 |
|
RU2544731C2 |
| Способ извлечения редкоземельных элементов из фосфогипса | 2017 |
|
RU2663512C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ ИЗ ЭКСТРАКЦИОННОЙ ФОСФОРНОЙ КИСЛОТЫ | 2011 |
|
RU2465207C1 |
| Способ переработки фосфогипса | 2017 |
|
RU2665512C1 |
Изобретение относится к способу извлечения редкоземельных элементов из фосфорной кислоты при переработке хибинских апатитовых концентратов на удобрения. Способ включает сорбцию с помощью сильно-кислотного макропористого катионита Purolite С-150, осуществляемую в диапазоне температур 40-80°C, промывку насыщенного суммой редкоземельных элементов сорбента водой, десорбцию раствором нитрата аммония с получением товарного десорбата и дополнительную экстракционную очистку полученного десорбата 100% трибутилфосфатом. Изобретение обеспечивает увеличение извлечения суммы редкоземельных элементов при уменьшенном содержании примесей других элементов. 2 з.п. ф-лы, 1 ил., 7 табл., 4 пр.
1. Способ извлечения редкоземельных элементов из экстракционной фосфорной кислоты (ЭФК) при переработке хибинских апатитовых концентратов, включающий сорбцию, осуществляемую в диапазоне температур 40-80°C, промывку насыщенного суммой редкоземельных элементов сорбента водой, десорбцию с получением товарного десорбата, отличающийся тем, что в качестве сорбента применяют сильно-кислотные макропористые катиониты, преимущественно Purolite С-150, десорбцию проводят раствором нитрата аммония, а полученный товарный десорбат подвергают дополнительной экстракционной очистке 100% трибутилфосфатом.
2. Способ по п.1, отличающийся тем, что операции сорбции осуществляют в противотоке "ЭФК-смола" при объемном соотношении Ж:Т, равном (8÷10):1, а десорбцию проводят в противотоке "десорбирующий раствор-смола" при объемном соотношении Ж:Т=(0,5÷1):1.
3. Способ по пп.1 и 2, отличающийся тем, что десорбирующий раствор нитрата аммония имеет концентрацию в диапазоне 200-600 г/л, предпочтительно - 450-550 г/л.
| СПОСОБ ИЗВЛЕЧЕНИЯ РЕДКОЗЕМЕЛЬНЫХ ЭЛЕМЕНТОВ ИЗ ЭКСТРАКЦИОННОЙ ФОСФОРНОЙ КИСЛОТЫ | 2011 |
|
RU2465207C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ И КОНЦЕНТРИРОВАНИЯ ТОРИЯ ИЗ ТЕХНОЛОГИЧЕСКИХ РАСТВОРОВ | 2001 |
|
RU2207393C1 |
| СПОСОБ ПЕРЕРАБОТКИ ЛОПАРИТОВОГО КОНЦЕНТРАТА | 2001 |
|
RU2211871C1 |
| СПОСОБ ПЕРЕРАБОТКИ СКАНДИЙСОДЕРЖАЩИХ РАСТВОРОВ | 2001 |
|
RU2196184C2 |
| СПОСОБ ИЗБИРАТЕЛЬНОГО ИЗВЛЕЧЕНИЯ СКАНДИЯ ИЗ СОЛЯНОКИСЛЫХ РАСТВОРОВ | 1993 |
|
RU2062810C1 |
| CN 101186284 A, 28.05.2008 | |||
Авторы
Даты
2014-09-20—Публикация
2011-11-24—Подача