1. Область техники, к которой относится изобретение
Изобретение относится к области биологически активных соединений и касается 5-метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинида l-аргининия моногидрата, обладающего противовирусным действием, предназначенного для лечения и профилактики вирусных заболеваний человека и животных. Изобретение может быть использовано в научно-исследовательских лабораториях, химико-фармацевтической промышленности, лечебных учреждениях, а также в ветеринарии.
2. Уровень техники
Актуальность проблемы противовирусной терапии, в особенности в условиях быстрой мутации вирусов, выявления новых возбудителей опасных и медленных вирусных инфекций, вызывает постоянную потребность в новых средствах, которые бы обладали высокой эффективностью и устойчивым эффектом при мутациях вирусов, продолжительным действием, низкой токсичностью и отсутствием побочных эффектов. Важным фактором является доступность синтетической реализации и возможность создания доступной технологии получения лекарственного средства.
В широком кругу синтетических гетероциклических соединений, обладающих противовирусным действием, значимое место занимают азолоазины, содержащие в структуре молекулы мостиковый атом азота. Известны тиадиазолотриазины, проявляющие активность в отношении вируса гепатита B, вируса Коксаки (A.M. Демченко, В.В. Кислый, З.Б. Квачева, М.О. Лозинський. Синтез и противовирусная активность производных [1,3,4]тиади-азоло[2,5-c][1,2,4]триазина. Журнал органичной та фармацевтичной химии, 2003, т.1, вып.1-2, стр.55-58; М.А. El-Badawi, А.А. El-Barbary, Y.M. Lokshaa, Mai El-Daly. Synthesis and biological evaluation of some novel N,N'-bis-(1,2,4-Triazin-4-yl) dicarboxylic acid amides and some fused rings with 1,2,4-triazine ring. Phosph., Sulfur, Silicon and Related Elements, 2002, V.177, pp.587-596).
Противовирусной активностью в отношении герпеса обладают пиразоло[5,7-c][1,2,4]триазины (G. Bravi, A. Goretti Cheasty, J.A.Corfield, R.M.Grimes. 4-Carboxy pyra-zole derivates as antiviral agents. WO 2007039146; F.A. Attaby, A.H. Elghandour, M.A. AH, Y.M. Ibrahem. Synthesis, reactions, and antiviral activity of 1-(1h-pyrazolo[3,4-b]pyridin-5-yl)ethanone and pyrido[2',3':3,4]pyrazolo[5,1-c][1,2,4]triazine derivatives. Phosph., Sulfur, Silicon and Related Elements, 2006, v. 181, №5, pp.1087-1102).
Противовирусным действием в отношении гриппа и герпеса обладают триазоло[5,1-c]-1,2,4-триазины (V.A. Plastunov, М.М. Kozlovs'kii, L.V. Benzel, G.V. Bilets'ka, I.M. Lozins'kii,; E.G. Rogochii, Sholomei, M.D. L'viv. NDI Epidemiol, ta Gigieni. Mikrobiologichnii Zhurnal. 2001, 63, №2, 14-19; В.Л. Русинов, E.H. Уломский, O.H. Чупахин, М.М. Зубаиров, А.Б. Капустин, Н.И. Митин и др. Синтез и противовирусная активность 6-нитро-7-оксо-4,7-дигидроазоло[5,1-c][1,2,4]триазинов. Химико-фармацевтический журнал. 1990, №9, с.41-44).
Анализ известных в мире технических решений показал, что аналоги 1,2,4-триазоло[7,5-α]триазинов - 1,2,4-триазоло[1,5-a]пиримидины, являются перспективным направлением поиска новых противовирусных соединений.
Наиболее близким по структуре к заявляемому соединению (прототипом) является препарат «Триазавирин» - натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло[5,1-c]-1,2,4-триазин-7-(4H)-она, дигидрат (О.Н. Чупахин, В.Л. Русинов, Е.Н. Уломский, В.Н. Чарушин, А.Ю. Петров, О.И. Киселев. Патент РФ №2294936. 10.03.2007).
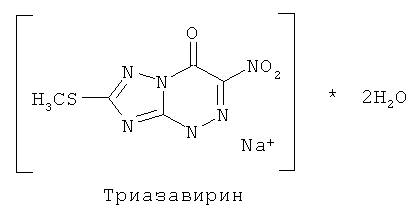
Препарат успешно прошел две фазы клинических исследований, в настоящее время проводятся многоцентровые клинические исследования в отношении вирусов гриппа в клиниках РФ.
3. Сущность изобретения
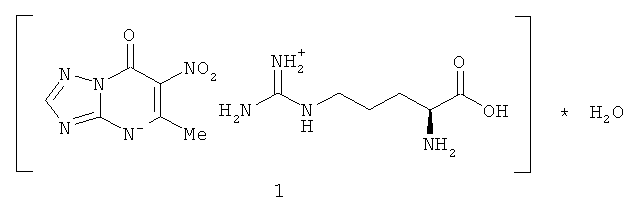
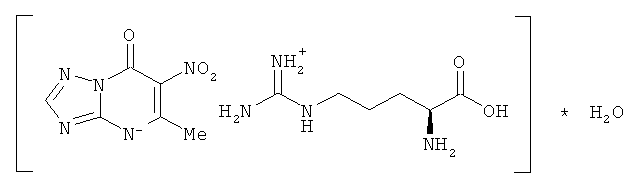
Сущность изобретения составляет 5-метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинид l-аргининия моногидрат, формулы 1, обладающий противовирусным действием
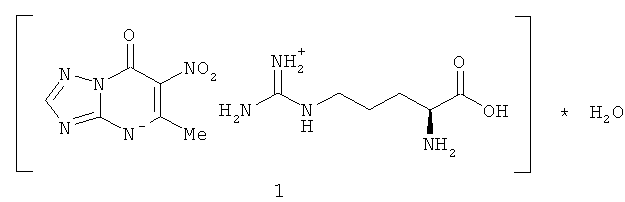
Задачей данного исследования являлось получение нового вещества азолоазинового ряда, обладающего противовирусной активностью в отношении обширной группы РНК-содержащих вирусов, и снижение зависимости активного соединения от клеточного метаболизма. Поставленная задача решена путем модификации гетероциклического основания молекулы «Триазавирина» - удаления одного гетероциклического атома азота и функционализации структуры фрагментами заместителей.
В литературе соединение 1, способ его получения и физико-химические характеристики не описаны.
Исследование противовирусного действия заявляемого соединения 1 было проведено в сравнении с соединением-прототипом («Триазавирином»).
4. Сведения, подтверждающие сущность изобретения
4.1. Синтез 5-метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинида l-аргининия моногидрата
Процесс получения 5-метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинида l-аргининия, моногидрата (1), включает одну химическую стадию: реакцию взаимодействия 5-метил-6-нитро-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидин-7-она (2) с l-аргинином.
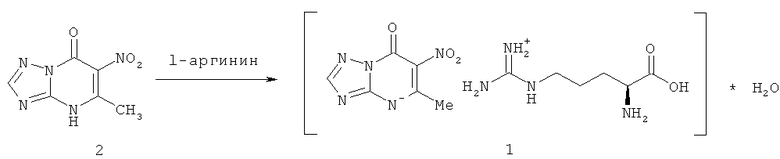
Исходное соединение - 5-метил-6-нитро-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидин-7-он (2) получают по ранее описанной методике (Kofman, Т.Р.; Uvarova, Т.А.; Kartseva, G.Yu.; Uspenskaya, T.L. Russian Journal of Organic Chemistry, 1997, v.33, №12, p.1784-1793).
5-Метил-6-нитро-7-оксо-47-дигидро-1,2,4-триазоло[1,5-α]пиримидинид l-аргининия моногидрат (1) имеет следующие физико-химические характеристики: желтое аморфное вещество, Т ПЛ 132-140°C; растворимо в воде, диметилформамиде, диметилсульфоксиде; не растворимо в хлороформе, этаноле, бензоле. Найдено, %: C 37,19; H 5,45; N 35,51. Брутто-формула C12H21N9O6. Вычислено, %: C 37,21; H 5,46; N 35,24. Спектр 1H ЯМР (400 МГц, D2O), δ (м.д.): 1,69 (м, 2H, CH2), 1,92 (м, 2H, CH2), 2,58 (с, 3H, CH3), 3,23 (м, 2H, CH2), 3,79 (м, 1H, CH), 8,21 (с, 1H, CH).
Способ получения 5-метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинида l-аргининия, моногидрата (1) иллюстрируется следующим примером.
Пример 1. Получение 5-метил-6-нитро-7-оксо-1,2,4-триазоло[1,5-α]пиримидинида l-аргининия моногидрата (1).
В круглодонную двугорлую колбу объемом 1000 мл, снабженную мешалкой и обратным холодильником с водяным охлаждением, при перемешивании загружают 13,7 г (0,078 моль) l-аргинина и приливают 92 мл воды, доводят смесь до полного растворения. К полученному раствору прибавляют 15,4 г (0,079 моль) 5-метил-6-нитро-1,2,4-триазоло[1,5-α]пиримидин-7-она 2, перемешивают 1 час, затем нагревают при 70°C 1 час. В колбу приливают 368 мл изо-пропанола, смесь перемешивают 6 часов. Выпавший осадок отфильтровывают и перекристаллизовывают из смеси вода - изо-пропанол (1:4). Выход 5-метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинида l-аргининия, моногидрата 22 г (72%).
4.2. Противовирусные свойства 5-метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинида l-аргининия моногидрата (1)
Оценку противовирусной активности проводили в соответствии с Методическими рекомендациями по исследованию противовирусной активности (Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ, под редакцией Р.У. Хабриева, изд. 2. 2005.). Результаты опытов регистрировали следующим образом:
- визуально, оценивая целостность монослоя по сравнению с контролем клеток и степень цитопатического действия вируса на культуру клеток (ЦПД);
- осуществляя количественный учет реакции гемагглютинации (РГА);
- с помощью метода иммуноферментного анализа (ИФА);
- с помощью метода МТТ для количественной оценки жизнеспособности клеток с использованием планшетного ридера «Termofisher VarioScan». Метод основан на способности дигидрогеназ живых клеток восстанавливать желтую соль метилтетразолия (МТТ реагент) в формазан, имеющий фиолетовую окраску, интенсивность которой фиксируется спектрофотометрически.
Пример 2. Определение противовирусной активности соединения 1 в отношении вирусов гриппа в системе in vitro
При оценке противовирусной эффективности соединения 1 в отношении вирусов гриппа A и B in vitro использованы эталонные штаммы вирусов гриппа A и B, циркулировавшие в человеческой популяции, а также эпидемически и пандемически актуальные штаммы. Исследования проводили на клеточной линии МДСК.
Противовирусную активность соединения 1 изучали по лечебно-профилактической схеме: предынкубация клеток с препаратом 60 мин, заражение вирусом, инкубация 1 сутки (для ИФА) или 3 суток (для определения титра вируса в РГА или МТТ). Исследовали концентрации соединения 1 от 5 до 100 мкг/мл.
Оценка токсичности соединения 1 in vitro методом МТТ показала, что соединение малотоксично в отношении клеток в культуре: максимальная нетоксическая концентрация - 500 мкг/мл, среднетоксическая концентрация - 750 мкг/мл.
Соединение 1 в опытах in vitro показало:
- высокую противовирусную активность в отношении штамма вируса гриппа A/Сидней/5/97 (H3N2) - % ингибирования >83%, индекс селективности - 150 (табл.1);
- умеренную противовирусную активность в отношении штамма вируса гриппа A/Новая Каледония/20/99 (H1N1) - % ингибирования - 50%, индекс селективности - 7,5 (табл.2);
- умеренную противовирусную активность в отношении штамма вируса гриппа A/Hong Kong/1073/99 (H9N2) - % ингибирования - 50%, индекс селективности - 7,5 (табл.3).
Таким образом, соединение 1 является низкотоксичным (наивысшая нетоксическая концентрация в культуре клеток - 500 мкг/мл, среднетоксическая концентрация - 750 мкг/мл) и в системе in vitro обладает высокой противовирусной активностью в отношении штамма вируса гриппа A(H3N2) и умеренной - в отношении штаммов A(H1N1), A(H9N2).
Пример 3. Определение противовирусной активности соединения 1 в отношении вирусов гриппа в системе in vivo
При изучении специфической активности соединения 1 на модели летальной гриппозной инфекции у мышей использовали штаммы вирусов гриппа, адаптированные к мышам - A/Aichi/2/68 (H3N2), A/California/07/09 (H1N1)pdm2009 и B/Lee/40.
Соединение 1 вводили животным в диапазоне доз от 25 мг/кг до 100 мг/кг перорально и внутрибрюшинно. Соединение 1 вводили животным по трем схемам: лечебно-профилактической - за 24 часа и 1 час до заражения и через 24, 48 и 72 часа после заражения, лечебной - 1 раз в сутки в течение 5 дней после заражения и профилактической - за 24 часа и 1 час до заражения.
В ходе исследования противовирусной активности соединения 1 на животных не было отмечено неспецифической смертности в контрольных группах интактных животных. Клинические признаки заболевания были типичными для гриппозной инфекции и включали затрудненное дыхание, атаксию, тремор, а также снижение потребления корма и воды, и как следствие, веса животных.
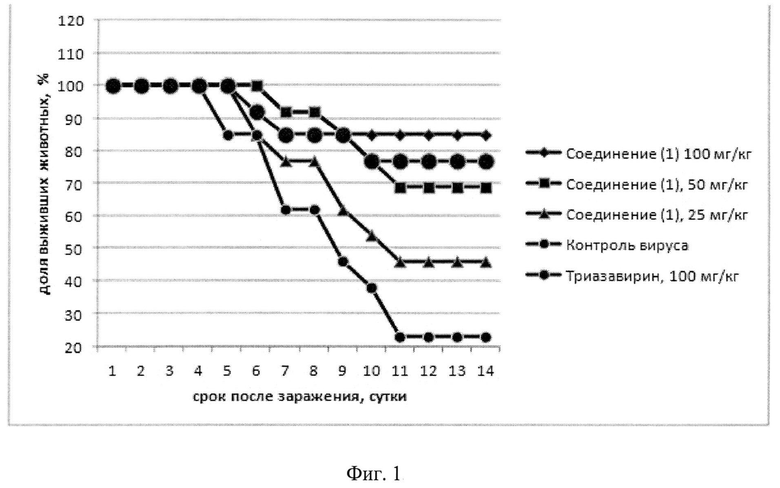
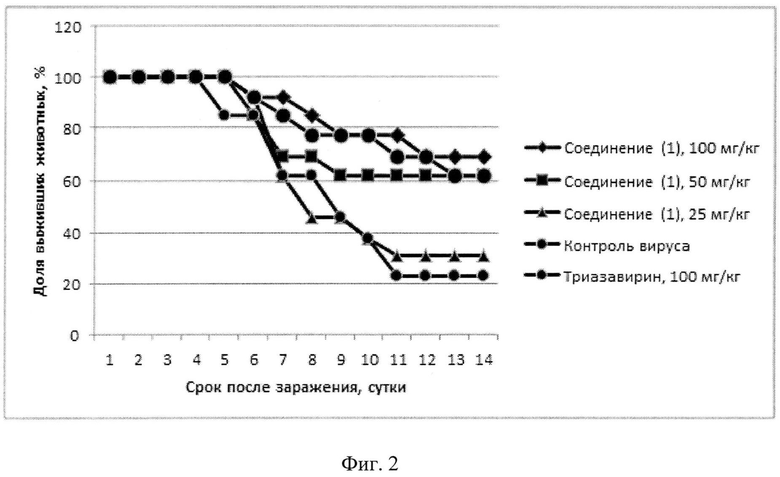
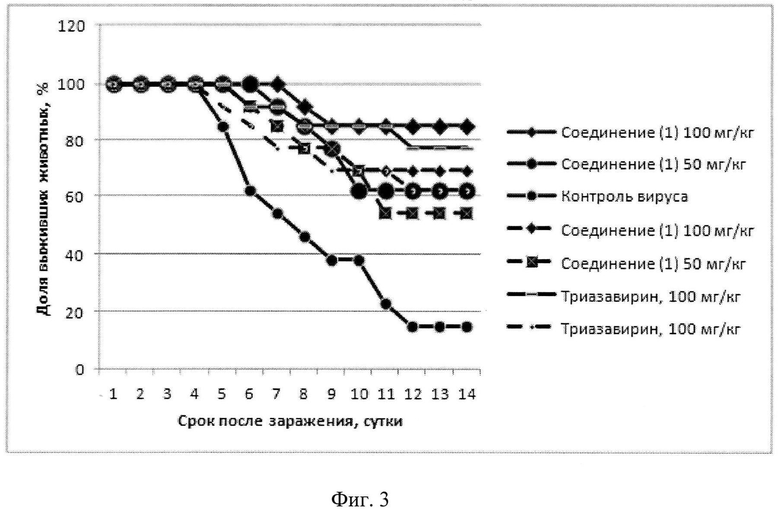
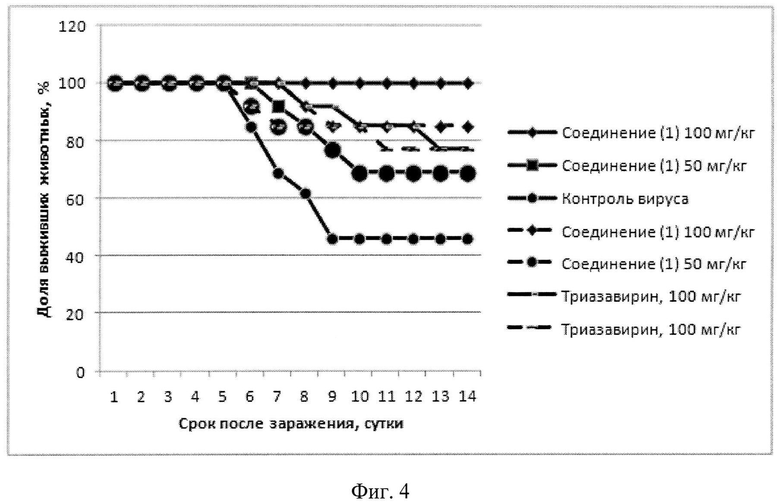
Соединение 1 показало высокий уровень противовирусной активности на модели летальной гриппозной инфекции у мышей, вызванной вирусами A/Aichi/2/68 (H3N2) (фиг.1, 2), A/California/05/09 pdm2009 (фиг.3) и B/Lee/40 (фиг.4).
Наиболее эффективным способом введения соединения 1 является пероральный. При пероральном введении соединение 1 обладает высокой противовирусной активностью (коэффициент защиты >70%), при внутрибрюшинном - умеренной противовирусной защитой (коэффициент защиты >50%).
Эффективные дозы - 100 мг/кг (высокая противовирусная активность, коэффициент защиты 80÷100%) и 50 мг/кг (умеренная противовирусная активность, коэффициент защиты 50÷70%). Соединение 1 эффективно при лечебно-профилактической, лечебной и профилактической схемах введения.
Эффективность соединения 1 в дозе 100 мг/кг незначительно превышает эффективности Триазавирина, что более выражено при пероральном введении.
Таким образом, соединение 1 обладает выраженной противовирусной активностью в отношении штаммов вируса гриппа типов A и B, причем противовирусная активность соединения 1 является дозозависимой, эффективные дозы в системе in vivo составляют 100 мг/кг и 50 мг/кг.
Пример 4. Определение LD50 при изучении острой токсичности на лабораторных животных.
При исследовании острой токсичности соединения 1 на аутбредных крысах и мышах, а также беспородных собаках значения LD50 установить не удалось в связи с отсутствием гибели экспериментальных животных. Максимальная доза субстанции для грызунов при внутрижелудочном введении составила 40000 мг/кг. Максимальная доза соединения 1 при пероральном введении собакам составила 20000 мг/кг.
Учитывая, что максимальная доза при внутрижелудочном введении крысам составила 40000 мг/кг, исследуемое соединение 1 можно отнести к VI классу относительно безвредных веществ по классификации Hodge и Sterner.
Препарат сравнения - Триазавирин, отнесен к малотоксичным лекарственным веществам (IV-V класс по классификации Hodge и Sterner), LD50 при внутрижелудочном введении Триазавирина аутбредным крысам и мышам разного пола - 8000-9500 мг/кг. Максимальная доза Триазавирина при пероральном введении собакам - 400 мг/кг.
Заявляемое соединение 1-5-метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинид l-аргининия моногидрат проявляет высокую и умеренную противовирусную активность in vitro и in vivo. В сравнении с прототипом - «Триазавирином» - заявляемое соединение показывает либо более высокую, либо соизмеримую активность. В то же время острая токсичность заявляемого соединения 1 оказалась в несколько раз ниже по сравнению с «Триазавирином».
Таким образом, при совместной оценке противовирусного действия и токсичности заявляемое соединение 1 является более эффективным в сравнении с соединением-прототипом.
Краткое описание чертежей
Фиг.1.
Активность соединения 1 перорально, при лечебно-профилактической схеме введения (вирус гриппа A/Aichi/2/68). Заражающая доза вируса 10 LD50.
Фиг.2.
Активность соединения 1 внутрибрюшинно, при лечебно-профилактической схеме введения (вирус гриппа A/Aichi/2/68). Заражающая доза вируса 10 LD50.
Фиг.3.
Активность соединения 1 перорально (вирус гриппа A/California/05/09 (H1N1)pdm). Заражающая доза вируса 10 LD50.
Данные по лечебной схеме введения обозначены сплошной линией, данные по профилактической схеме введения обозначены пунктирной линией.
Фиг.4.
Активность соединения 1 перорально (вирус гриппа B/Lee/40).
Заражающая доза вируса 10 LD50.
Данные по лечебной схеме введения обозначены сплошной линией, данные по профилактической схеме введения обозначены пунктирной линией.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНЪЕКЦИОННЫЙ ИЛИ ИНФУЗИОННЫЙ РАСТВОР L-АРГИНИНИЕВОЙ СОЛИ 5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-а]ПИРИМИДИН-7-ОНА МОНОГИДРАТА ДЛЯ ТЕРАПИИ ГРИППА И ДРУГИХ ВИРУСНЫХ ИНФЕКЦИЙ | 2014 |
|
RU2586283C1 |
| АЗОЛОАЗИНИЕВЫЕ СОЛИ ФТОРХИНОЛОНОВ, ОБЛАДАЮЩИЕ АНТИБАКТЕРИАЛЬНЫМ И ПРОТИВОВИРУСНЫМ ДЕЙСТВИЕМ | 2014 |
|
RU2547835C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ТРИАЗИДА МЕТОДОМ ВОЛЬТАМПЕРОМЕТРИИ | 2019 |
|
RU2733397C2 |
| НАТРИЕВАЯ СОЛЬ 2-МЕТИЛТИО-6-ЦИАНО-1,2,4-ТРИАЗОЛО[5,1-с]-1,2,4-ТРИАЗИН-7(4Н)-ОНА, ТРИГИДРАТ | 2015 |
|
RU2607628C1 |
| НАТРИЕВАЯ СОЛЬ 5-МЕТИЛ-6-НИТРО-1,2,4,-ТРИАЗОЛО[1,5-a]ПИРИМИДИН-7-ОНА ДИГИДРАТ | 2006 |
|
RU2330036C1 |
| ИНЪЕКЦИОННЫЙ РАСТВОР ДЛЯ ЛЕЧЕНИЯ ВИРУСНЫХ ЗАБОЛЕВАНИЙ, ВЫБРАННЫХ ИЗ ГРИППА H1N1, H3N2, H5N1, КЛЕЩЕВОГО ЭНЦЕФАЛИТА И ЛИХОРАДКИ ЗАПАДНОГО НИЛА | 2013 |
|
RU2574007C2 |
| НАТРИЕВАЯ СОЛЬ 2-МЕТИЛ-6-ФТОР-1,2,4-ТРИАЗОЛО[5,1-с]-1,2,4-ТРИАЗИН-7(4Н)-ОНА ДИГИДРАТ, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНЫМ ДЕЙСТВИЕМ | 2009 |
|
RU2493158C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВИРУСНЫМ ДЕЙСТВИЕМ И СОДЕРЖАЩЕЕ 2-МЕТИЛТИО-5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИН-7(3Н)-ОН | 2007 |
|
RU2365591C2 |
| Этиловый эфир 2-(адамантан-1-ил)-3-бром-7-оксо-4,7-дигидропиразоло[1,5-a]пиримидин-6-карбоновой кислоты, обладающий противовирусным действием в отношении коронавируса SARS-CoV-2 | 2024 |
|
RU2839407C1 |
| КОНЪЮГАТЫ 2-МЕТИЛТИО-6-НИТРО-1,2,4-ТРИАЗОЛО[5,1-c]-1,2,4-ТРИАЗИН-7(4I')-ОНА С ГЛУТАТИОНОМ И ДРУГИМИ ПЕПТИДАМИ, ОБЛАДАЮЩИЕ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2012 |
|
RU2516936C2 |
Изобретение относится к новому 5-метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинид l-аргининия моногидрату формулы (1)
Соединение обладает противовирусной активностью в отношении вирусов штаммов гриппа А и В в системах in vitro и in vivo. Соединение является низкотоксичным. 4 ил., 3 табл., 4 пр.
5-Метил-6-нитро-7-оксо-4,7-дигидро-1,2,4-триазоло[1,5-α]пиримидинид l-аргининия моногидрат (1)
| НАТРИЕВАЯ СОЛЬ 5-МЕТИЛ-6-НИТРО-1,2,4,-ТРИАЗОЛО[1,5-a]ПИРИМИДИН-7-ОНА ДИГИДРАТ | 2006 |
|
RU2330036C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВИРУСНЫМ ДЕЙСТВИЕМ И СОДЕРЖАЩЕЕ 2-МЕТИЛТИО-5-МЕТИЛ-6-НИТРО-1,2,4-ТРИАЗОЛО[1,5-a]ПИРИМИДИН-7(3Н)-ОН | 2007 |
|
RU2365591C2 |
| VINOGRAD I.A | |||
| et al., Antiarboviral properties of different substances of chemical and plant origin, Microbiologichnii i Virusologii Zhurnal,2001,63(2),pp.14-19, CAS REGISTRY Number: 372487-44-0 | |||
Авторы
Даты
2014-09-27—Публикация
2013-04-15—Подача