Область техники, к которой относится изобретение
Настоящее изобретение относится к производному N-ацилантраниловой кислоты или его соли, обладающим ингибирующим действием на продукцию коллагена.
Уровень техники
Фиброгенез, в процессе которого продуцируется внеклеточный матрикс, включающий коллаген в качестве типичного примера, представляет собой механизм заживления ран. Однако если повреждение является длительным, то его процесс отклоняется от обычного, и происходит широкое отложение избыточного внеклеточного матрикса, что приводит к возникновению фиброза. Фиброз наблюдается в различных органах, но источники происхождения продуцирующих внеклеточный матрикс клеток считаются одними и теми же. Считается, что такими источниками происхождения являются эндогенные фибробласты, эпителиальные клетки, претерпевшие переход из эпителия в мезенхиму, и фиброциты (Непатентный Документ 1). Фиброз представляет собой заболевание, при котором функциональное нарушение происходит в результате повреждения самой ткани вследствие причинного заболевания и последующего образования волокон, приводящего к органной недостаточности. Это заболевание характеризуется неблагоприятным прогнозом.
К настоящему времени для лечения фиброза предпринимались попытки подавления воспалительной реакции, но значимые эффекты от такого лечения не могли быть получены. Были проведены исследования с целью разработки антифиброзного средства, направленно воздействующего на регуляторные факторы фиброза, такие как TGF (трансформирующий фактор роста)-β1, VEGF (фактор роста эндотелия сосудов), PDGF (фактор роста тромбоцитов) и ангиотензин II (Непатентный Документ 2).
Пирфенидон применялся в качестве единственного такого антифиброзного средства для идиопатического легочного фиброза. Эффективность пирфенидона, обнаруженная в клинических испытаниях, представляла собой лишь супрессию снижения жизненной емкости легких. Кроме того, пирфенидон обладал побочными эффектами, такими как фотосенсибилизация у 87,9% пациентов (Непатентный Документ 3). Следовательно, использование пирфенидона не является адекватным способом терапии в плане эффективности и безопасности.
Основной составляющей внеклеточного матрикса, которая избыточно откладывается при фиброзе, является коллаген. Среди прочих, наиболее распространенным коллагеном является коллаген типа I. Соответственно, вещество, ингибирующее продукцию коллагена, применимо для профилактики или лечения заболеваний, сопровождаемых фиброзным поражением.
К настоящему времени были представлены данные, что производное антраниловой кислоты обладает ингибирующим действием на продукцию матриксной металлопротеиназы-13 (Патентный Документ 1). Однако было совершенно неизвестно, что производное антраниловой кислоты обладает ингибирующим действием на продукцию коллагена.
Список цитируемых источников
Патентные Документы
Патентный Документ 1: Международная публикация WO2006/062093, брошюра
Непатентные Документы
Непатентный Документ 1: Experimental Biology and Medicine, Vol. 233, pp. 109-122, 2008
Непатентный Документ 2: Journal of Pathology, Vol. 214, pp. 199-210, 2008
Непатентный Документ 3: Pirespa 200 мг, вкладыш в упаковке, Vol. 1, Shionogi & Co., Ltd., приготовлен в октябре 2008 г.
Краткое описание сущности изобретения
Техническая задача
Имелось намерение разработать средство, обладающее ингибирующим действием на продукцию коллагена и используемое для профилактики, лечения и тому подобное, заболеваний, ассоциированных с избыточной продукцией коллагена.
Решение задачи
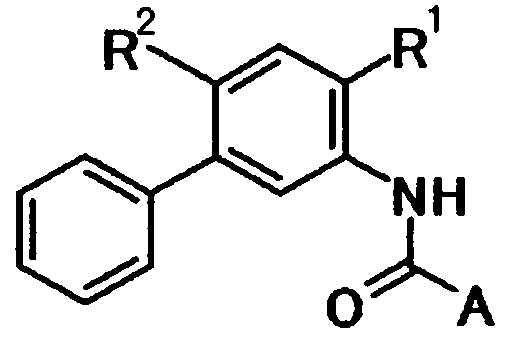
В связи с вышеуказанными обстоятельствами, авторы настоящего изобретения провели тщательное изучение. В результате авторы изобретения обнаружили, что производное N-ацилантраниловой кислоты, представленное следующей общей формулой [1] или его соль:
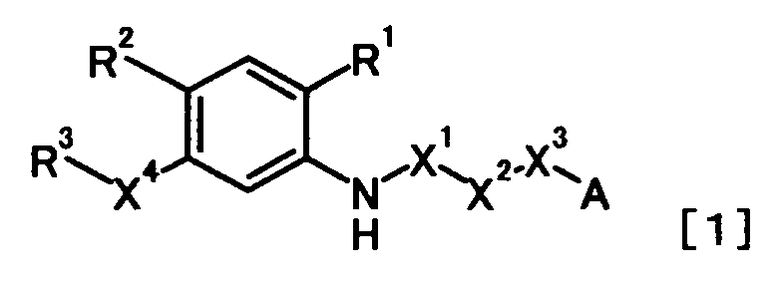
в которой
R1 представляет собой необязательно защищенную карбоксильную группу или необязательно защищенную 1H-тетразол-5-ильную группу;
R2 представляет собой атом водорода, атом галогена, цианогруппу, нитрогруппу, необязательно защищенную гидроксильную группу, необязательно защищенную аминогруппу, необязательно защищенную или замещенную алкиламиногруппу, необязательно замещенную диалкиламиногруппу, необязательно замещенную алкильную группу или необязательно замещенную алкоксигруппу;
R3 представляет собой необязательно замещенную циклоалкильную группу, необязательно замещенную циклоалкенильную группу, необязательно замещенную арильную группу или необязательно замещенную гетероциклическую группу;
X1 представляет собой карбонильную группу;
X2 представляет собой необязательно замещенную алкиленовую группу, необязательно замещенную алкениленовую группу, необязательно замещенную алкиниленовую группу или связь;
X3 представляет собой атом кислорода, атом серы или связь;
X4 представляет собой группу, представленную общей формулой -X5-X6- или -X6-X5- (при условии, что связь с левой части каждой общей формулы связана с R3), в которой
X5 представляет собой атом кислорода, атом серы, необязательно защищенную иминогруппу, сульфинильную группу, сульфонильную группу или связь; и
X6 представляет собой необязательно замещенную алкиленовую группу, необязательно замещенную алкениленовую группу, необязательно замещенную алкиниленовую группу или связь; и
А представляет собой необязательно замещенную фенильную группу, необязательно замещенную циклоалкильную группу или необязательно замещенную гетероциклическую группу,
обладает ингибирующим действием на продукцию коллагена и применимо для профилактики, лечения и тому подобное, заболеваний, ассоциированных с избыточной продукцией коллагена.
Более того, авторы настоящего изобретения также обнаружили, что новое производное N-ацилантраниловой кислоты, представленное следующей общей формулой [1], или его соль:
[Формула 2]
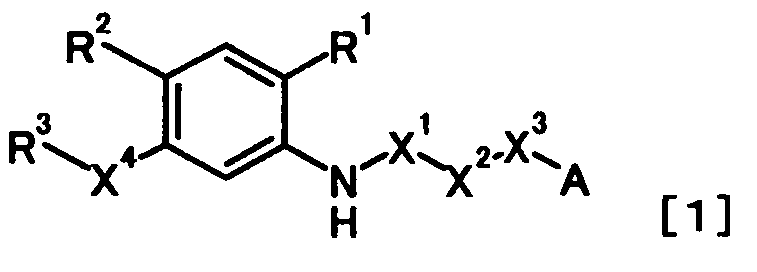
в которой
R1 представляет собой необязательно защищенную карбоксильную группу или необязательно защищенную 1H-тетразол-5-ильную группу;
R2 представляет собой атом водорода, атом галогена, цианогруппу, нитрогруппу, необязательно защищенную гидроксильную группу, необязательно защищенную аминогруппу, необязательно защищенную или замещенную алкиламиногруппу, необязательно замещенную диалкиламиногруппу, необязательно замещенную алкильную группу или необязательно замещенную алкоксигруппу;
R3 представляет собой необязательно замещенную арильную группу или необязательно замещенную гетероциклическую группу;
X1 представляет собой карбонильную группу;
X2 представляет собой связь;
X3 представляет собой связь;
X4 представляет собой атом кислорода, необязательно защищенную иминогруппу, необязательно замещенную алкиленовую группу или связь; и
А представляет собой группу, представленную следующей общей формулой:
[Формула 3]
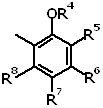
в которой
R4 представляет собой атом водорода или защитную группу фенольного гидроксила;
один из R5, R6, R7 и R8 представляет собой группу, представленную общей формулой -Y-R9,
в которой
R9 представляет собой атом галогена, цианогруппу, нитрогруппу, необязательно защищенную гидроксильную группу, необязательно защищенную аминогруппу, необязательно защищенную или замещенную алкиламиногруппу, необязательно замещенную диалкиламиногруппу, необязательно замещенную алкильную группу, необязательно замещенную алкоксигруппу, необязательно замещенную арильную группу, необязательно замещенную арилоксигруппу, необязательно замещенную гетероциклическую группу, необязательно замещенную гетероциклическую оксигруппу, необязательно замещенную ацильную группу или необязательно замещенную ацилоксигруппу;
Y представляет собой необязательно замещенную алкиленовую группу, необязательно замещенную алкениленовую группу, необязательно замещенную алкиниленовую группу, связь, группу, представленную общей формулой -(CH2)m-O-(CH2)n-,
в которой m представляет собой целое число от 0 до 4; и n представляет собой целое число от 1 до 4, или общей формулой -(CH2)m-NR10-(CH2)n-,
в которой R10 представляет собой атом водорода, необязательно замещенную низшую алкильную группу или иминозащитную группу; и m и n имеют те же определенные выше значения, и
каждый из оставшихся, являющихся одинаковыми или разными, представляет собой атом водорода, атом галогена, необязательно защищенную гидроксильную группу, необязательно защищенную аминогруппу, необязательно защищенную или замещенную алкиламиногруппу или необязательно замещенную диалкиламиногруппу; или
каждый из R5 и R8, являющихся одинаковыми или разными, представляет собой атом водорода, атом галогена, необязательно защищенную гидроксильную группу, необязательно защищенную аминогруппу, и
каждый R6 и R7 вместе с атомами углерода, с которыми они связаны, представляют собой необязательно замещенную 5-7-членную гетероциклическую группу, или
группу, представленную следующей общей формулой:
[Формула 4]
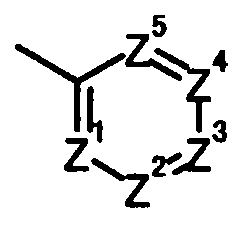
в которой
один из Z1, Z2, Z3, Z4 и Z5 представляет собой атом азота,
один из оставшихся четырех представляет собой группу, представленную общей формулой C-R11,
в которой R11 представляет собой необязательно замещенную арильную группу, необязательно замещенную азотсодержащую 6-членную ароматическую гетероциклическую группу, необязательно замещенную кислородсодержащую 5-членную ароматическую гетероциклическую группу, необязательно замещенную азотсодержащую кислородсодержащую 5-членную ароматическую гетероциклическую группу или необязательно замещенную азотсодержащую серосодержащую 5-членную ароматическую гетероциклическую группу,
каждый из оставшихся трех, являющихся одинаковыми или разными, представляет собой группу, представленную общей формулой C-R12,
в которой R12 представляет собой атом водорода или атом галогена,
обладает ингибирующим действием на продукцию коллагена и применимо для профилактики, лечения и тому подобное, заболеваний, ассоциированных с избыточной продукцией коллагена, и является превосходным с точки зрения безопасности и кинетики, оформив тем самым настоящее изобретение.
Полезные эффекты изобретения
Поскольку производное N-ацилантраниловой кислоты по настоящему изобретению или его соль обладает ингибирующим действием на продукцию коллагена и является превосходным с точки зрения безопасности и кинетики, оно применимо для профилактики, лечения и тому подобное, заболеваний, ассоциированных с избыточной продукцией коллагена, таких как легочный фиброз, склеродермия, нефросклероз и цирроз печени.
Описание вариантов осуществления
Соединение по настоящему изобретению подробно описано ниже.
В настоящем описании каждый термин имеет следующие значения, если иное не указано особо.
Атом галогена означает атом фтора, атом хлора, атом брома или атом йода.
Алкильная группа означает неразветвленную или разветвленную C1-12алкильную группу, такую как метил, этил, пропил, изопропил, бутил, втор-бутил, изобутил, трет-бутил, пентил, изопентил, гексил, гептил и октил.
Низшая алкильная группа означает неразветвленную или разветвленную C1-6алкильную группу, такую как метил, этил, пропил, изопропил, бутил, втор-бутил, изобутил, трет-бутил, пентил и изопентил.
Алкенильная группа означает неразветвленную или разветвленную C2-12алкенильную группу, такую как винил, аллил, пропенил, изопропенил, бутенил, изобутенил, пентенил, гексенил, гептенил и октенил.
Алкинильная группа означает неразветвленную или разветвленную C2-12алкинильную группу, такую как этинил, 2-пропинил и 2-бутинил.
Циклоалкильная группа означает С3-8циклоалкильную группу, такую как циклопропил, циклобутил, циклопентил и циклогексил.
Арильная группа означает группу, такую как фенил или нафтил.
Аралкильная группа означает ар-C1-6алкильную группу, такую как бензил, дифенилметил, тритил, фенэтил и нафтилметил.
Алкиленовая группа означает неразветвленную или разветвленную C1-6алкиленовую группу, такую как метилен, этилен, пропилен, бутилены и гексилен.
Алкениленовая группа означает неразветвленную или разветвленную C2-6алкениленовую группу, такую как винилен, пропенилен, 1-бутенилен и 2-бутенилен.
Алкиниленовая группа означает неразветвленную или разветвленную C2-6алкиниленовую группу, такую как этинилен, пропинилен, 1-бутинилен и 2-бутинилен.
Алкоксигруппа означает неразветвленную или разветвленную C1-6алкоксигруппу, такую как метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентилокси и изопентилокси.
Арилоксигруппа означает группу, такую как фенокси или нафтокси.
Алкоксиалкильная группа означает C1-6алкоксиC1-6алкильную группу, такую как метоксиметил и 1-этоксиэтил.
Аралкилоксиалкильная группа означает ар-C1-6алкоксиC1-6алкильную группу, такую как бензилоксиметил и фенэтилоксиметил.
Ацильная группа означает, например, формильную группу, неразветвленную или разветвленную C2-12алканоильную группу, такую как ацетил, пропионил и изовалерил, ар-C1-6алкилкарбонильную группу, такую как бензилкарбонил, циклическую углеводородную карбонильную группу, такую как бензоил и нафтоил, гетероциклическую карбонильную группу, такую как никотиноил, теноил, пирролидинокарбонил и фуроил, сукцинильную группу, глутарильную группу, малеоильную группу, фталоильную группу или неразветвленную или разветвленную α-аминоалканоильную группу, содержащую необязательно защищенный N-конец, полученный из аминокислоты (где примеры аминокислот включают глицин, аланин, валин, лейцин, изолейцин, серин, треонин, цистеин, метионин, аспарагиновую кислоту, глутаминовую кислоту, аспарагин, глутамин, аргинин, лизин, гистидин, гидроксилизин, фенилаланин, тирозин, триптофан, пролин и гидроксипролин).
Ацилалкильная группа означает группу, такую как ацетилметил, бензоилметил, пара-нитробензоилметил, пара-бромбензоилметил, пара-метоксибензоилметил или 1-бензоилэтил.
Ацилоксигруппа означает неразветвленную или разветвленную C2-6алканоилоксигруппу, такую как ацетилокси и пропионилокси, или ароилоксигруппу, такую как бензоилокси.
Ацилоксиалкильная группа означает группу, такую как ацетоксиметил, пропионилоксиметил или пивалоилоксиметил.
Алкилоксикарбонильная группа означает неразветвленную или разветвленную C1-12алкилоксикарбонильную группу, такую как метоксикарбонил, этоксикарбонил, 1,1-диметилпропоксикарбонил, изопропоксикарбонил, 2-этилгексилоксикарбонил, трет-бутоксикарбонил и трет-пентилоксикарбонил.
Аралкилоксикарбонильная группа означает ар-C1-6алкилоксикарбонильную группу, такую как бензилоксикарбонил и фенэтилоксикарбонил.
Арилоксикарбонильная группа означает группу, такую как фенилоксикарбонил.
Алкиламиногруппа означает моно(C1-6алкил)аминогруппу, такую как метиламино, этиламино, пропиламино, изопропиламино, бутиламино, трет-бутиламино и пентиламино.
Диалкиламиногруппа означает ди(C1-6алкил)аминогруппу, такую как диметиламино, диэтиламино, дипропиламино, дибутиламино, (этил)(метил)амино, (метил)(пропил)амино, (бутил)(метил)амино и (метил)(пентил)амино.
Алкилтиоалкильная группа означает C1-6алкилтиоC1-6алкильную группу, такую как метилтиометил, этилтиометил и пропилтиометил.
Арилтиогруппа означает группу, такую как фенилтио.
Арилтиоалкильная группа означает группу, такую как фенилсульфенилметил или 2-(пара-нитрофенилсульфенил)этил.
Алкилсульфонильная группа означает C1-6алкилсульфонильную группу, такую как метилсульфонил, этилсульфонил и пропилсульфонил.
Арилсульфонильная группа означает группу, такую как бензолсульфонил, пара-толуолсульфонил или нафталинсульфонил.
Арилсульфонилалкильная группа означает группу, такую как пара-толуолсульфонилэтил.
Алкилсульфонилоксигруппа означает C1-6алкилсульфонилоксигруппу, такую как метилсульфонилокси и этилсульфонилокси.
Арилсульфонилоксигруппа означает группу, такую как бензолсульфонилокси или пара-толуолсульфонилокси.
Алкилсульфониламиногруппа означает C1-6алкилсульфониламиногруппу, такую как метилсульфониламино и этилсульфониламино.
Замещенная силильная группа означает группу, такую как триметилсилил, триэтилсилил или трибутилсилил.
Алкилсилилалкильная группа означает группу, такую как 2-(триметилсилил)этил.
Азотсодержащая 6-членная ароматическая гетероциклическая группа означает пиридильную, пиразинильную, пиримидинильную или пиридазинильную группу и тому подобное.
Кислородсодержащая 5-членная ароматическая гетероциклическая группа означает фуранильную группу и тому подобное.
Азотсодержащая кислородсодержащая 5-членная ароматическая гетероциклическая группа означает оксазолильную, оксадиазолильную или изоксазолильную группу и тому подобное.
Азотсодержащая серосодержащая 5-членная ароматическая гетероциклическая группа означает тиазолильную, тиадиазолильную или изотиазолильную группу и тому подобное.
Кислородсодержащая гетероциклическая группа означает группу, такую как 2-тетрагидропиранил или 2-тетрагидрофуранил.
Серосодержащая гетероциклическая группа означает группу, такую как тетрагидротиопиранил.
Гетероциклическая оксикарбонильная группа означает группу, такую как 2-фурфурилоксикарбонил или 8-хинолилоксикарбонил.
Азотсодержащая гетероциклическая алкильная группа означает группу, такую как фталимидметил или сукцинимидметил.
Моноциклическая гетероциклическая группа означает: моноциклическую азотсодержащую гетероциклическую группу, которая в качестве гетероатома для образования кольца содержит только атом азота, такую как азетинидильная, пирролильная, пирролинильная, пирролидинильная, пиперидильная, пиперазинильная, гомопиперазинильная, азепанильная, диазепанильная, октагидроазоценильная, имидазолильная, пиразолильная, пиридильная, тетрагидропиридильная, пиридазинильная, пиразинильная, пиримидинильная, тетразолильная, имидазолинильная, имидазолидинильная, пиразолинильная и пиразолидинильная группы; моноциклическую кислородсодержащую гетероциклическую группу, которая в качестве гетероатома для образования кольца содержит только атом кислорода, такую как тетрагидрофуранильная, фуранильная и пиранильная группы; моноциклическую серосодержащую гетероциклическую группу, которая в качестве гетероатома для образования кольца содержит только атом серы, такую как тиенильная группа; моноциклическую азот- и кислородсодержащую гетероциклическую группу, которая в качестве гетероатомов для образования кольца содержит только атом азота и атом кислорода, такую как оксазолильная, оксадиазолильная, изоксазолильная и морфолинильная группы; моноциклическую азот- и серосодержащую гетероциклическую группу, которая в качестве гетероатомов для образования кольца содержит только атом азота и атом серы, такую как тиазолильная, изотиазолильная, тиадиазолильная, тиаморфолинильная, 1-оксидотиоморфолинильная и 1,1-диоксидотиоморфолинильная группы; моноциклическую кислород- и серосодержащую гетероциклическую группу, которая в качестве гетероатомов для образования кольца содержит только атом кислорода и атом серы, такую как тиоксанильная группы; или тому подобное.
Бициклическая гетероциклическая группа означает: бициклическую азотсодержащую гетероциклическую группу, представленную с конденсированным кольцом или сшитым кольцом, которая в качестве гетероатома для образования кольца содержит только атом азота, такую как индолильная, индолинильная, 2-оксоиндолилнильная, изоиндолильная, индолидинильная, бензимидазолильная, бензотриазолильная, индазолильная, хинолильная, тетрагидрохинолинильная, тетрагидроизохинолинильная, хинолидинильная, изохинолильная, фталадинильная, нафтилидинильная, хиноксалинильная, дигидрохиноксалинильная, хиназолинильная, циннолинильная, хинуклидинильная и 2,3-дигидробензопирролильная группы; бициклическую кислородсодержащую гетероциклическую группу, представленную с конденсированным кольцом или сшитым кольцом, которая в качестве гетероатома для образования кольца содержит только атом кислорода, такую как бензофуранильная, изобензофуранильная, хроменильная, хроманильная, изохроманильная, бензо-1,3-диоксолильная, бензо-1,4-диоксанильная и 2,3-дигидробензофуранильная группы; бициклическую серосодержащую гетероциклическую группу, представленную с конденсированным кольцом или сшитым кольцом, которая в качестве гетероатома для образования кольца содержит только атом серы, такую как бензотиенильная и 2,3-дигидробензотиенильная группы; бициклическую азот- и кислородсодержащую гетероциклическую группу, представленную с конденсированным кольцом или сшитым кольцом, которая образует кольцо с 10 или более атомами и которая в качестве гетероатомов для образования кольца содержит атом азота и атом кислорода, такую как бензоморфолинильная и бензоморфолонильная группы; бициклическую азот- и серосодержащую гетероциклическую группу, представленную с конденсированным кольцом или сшитым кольцом, которая в качестве гетероатомов для образования кольца содержит атом азота и атом серы, такую как бензотиазолильная и бензотиадиазолильная группы.
Гетероциклическая группа означает: моноциклическую гетероциклическую группу; бициклическую гетероциклическую группу; или трициклическую гетероциклическую группу, такую как тиантоленил, ксантенил, феноксатиинил, карбазолил, β-карболинил, фенантридинил, акридинил, пиримидинил, фенантролинил, феназинил, фенотиазинил и феноксазинил.
5-7-членная гетероциклическая группа означает группу, такую как имидазолил, триазолил, пирролил, фуранил, диоксолил, диоксанил, тиенил, морфолинил, морфолонил или тиазолил.
Гетероциклическая оксигруппа означает группу, такую как пирролидинилокси, пиперидинилокси, пиперазинилокси, морфолинилокси, тиоморфолинилокси, тетрагидрофуранилокси, тетрагидропиранилокси, тетрагидротиопиранилокси, пиридилокси или пиримидинилокси.
Циклическая аминогруппа может быть как насыщенной, так и ненасыщенной циклической аминогруппой. Кроме того, она может дополнительно содержать в своем кольце один или несколько гетероатомов, таких как атом азота, атом кислорода или атом серы, и карбонильный атом углерода. Более того, она может быть моноциклической, бициклической или трициклической группой. Более конкретно, циклическая аминогруппа означает насыщенную или ненасыщенную моноциклическую 3-7-членную циклическую аминогруппу, содержащую один атом азота, такую как азиридин-1-ил, азетидин-1-ил, пирролидин-1-ил, пирролин-1-ил, пиррол-1-ил, дигидропиридин-1-ил, тетрагидропиридин-1-ил, пиперидин-1-ил, дигидроазепин-1-ил и пергидроазепин-1-ил; насыщенную или ненасыщенную моноциклическую 3-7-членную циклическую аминогруппу, содержащую два атома азота, такую как имидазол-1-ил, имидазолидин-1-ил, имидазолин-1-ил, пиразолидин-1-ил, пиперазин-1-ил, 1,4-дигидропиразин-1-ил, 1,2-дигидропиримидин-1-ил, пергидропиразин-1-ил и гомопиперазин-1-ил; насыщенную или ненасыщенную моноциклическую 3-7-членную циклическую аминогруппу, содержащую три или более атомов азота, такую как 1,2,4-триазол-1-ил, 1,2,3-триазол-1-ил, 1,2-дигидро-1,2,4-триазин-1-ил и пергидро-S-триазин-1-ил; насыщенную или ненасыщенную моноциклическую 3-7-членную циклическую аминогруппу, содержащую от 1 до 4 гетероатомов, выбранных из атома кислорода и атома серы, а также атома азота, такую как оксазолидин-3-ил, изоксазолидин-2-ил, морфолин-4-ил, тиазолидин-3-ил, изотиазолидин-2-ил, тиоморфолин-4-ил, гомотиоморфолин-4-ил и 1,2,4-тиадиазолин-2-ил; насыщенную или ненасыщенную бициклическую или трициклическую циклическую аминогруппу, такую как изоиндолин-2-ил, индолин-1-ил, 1H-индазол-1-ил, 1H-индол-1-ил, 1H-бензимидазол-1-ил, пурин-7-ил, тетрагидрохинолин-1-ил и тетрагидроизохинолин-2-ил; или спиральную или сшитую насыщенную или ненасыщенную 5-12-членную циклическую аминогруппу, такую как 5-азаспиро[2.4]гептан-5-ил, 2,8-диазабицикло[4.3.0]нонан-8-ил, 3-азабицикло[3.1.0]гексан-3-ил, 2-окса-5,8-диазабицикло[4.3.0]нонан-8-ил, 2,8-диазаспиро[4.4]нонан-2-ил и 7-азабицикло[2.2.1]гептан-7-ил.
Аминозащитная группа включает все группы, которые могут быть использованы в качестве общих аминозащитных групп. Примеры таких аминозащитных групп включают группы, описанные в W. Greene et al., Protective Groups in Organic Synthesis, 4th edition, pp. 696-868, 2007, John Wiley & Sons, INC. Конкретные примеры включают ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, арилоксикарбонильную группу, аралкильную группу, алкоксиалкильную группу, аралкилоксиалкильную группу, арилтиогруппу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу.
Иминозащитная группа включает все группы, которые могут быть использованы в качестве общих иминозащитных групп. Примеры таких иминозащитных групп включают описанные в W. Greene et al., Protective Groups in Organic Synthesis, 4th edition, pp. 696-868, 2007, John Wiley & Sons, INC. Конкретные примеры включают ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, арилоксикарбонильную группу, аралкильную группу, алкоксиалкильную группу, арилтиогруппу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу.
Гидроксилзащитная группа включает все группы, которые могут быть использованы в качестве общих гидроксилзащитных групп. Примеры таких гидроксилзащитных групп включают описанные в W. Greene et al., Protective Groups in Organic Synthesis, 4th edition, pp.16-299, 2007, John Wiley & Sons, INC. Конкретные примеры включают ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, гетероциклическую оксикарбонильную группу, алкильную группу, алкенильную группу, аралкильную группу, кислородсодержащую гетероциклическую группу, серосодержащую гетероциклическую группу, алкоксиалкильную группу, аралкилоксиалкильную группу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу.
Карбоксилзащитная группа включает все группы, которые могут быть использованы в качестве общих карбоксилзащитных групп. Примеры таких карбоксилзащитных групп включают описанные в W. Greene et al., Protective Groups in Organic Synthesis, 4th edition, pp.533-643, 2007, John Wiley & Sons, INC. Конкретные примеры включают алкильную группу, арильную группу, аралкильную группу, ацилалкильную группу, арилтиоалкильную группу, арилсульфонилалкильную группу, кислородсодержащую гетероциклическую группу, алкилсилилалкильную группу, ацилоксиалкильную группу, азотсодержащую гетероциклическую алкильную группу, циклоалкильную группу, алкоксиалкильную группу, алкилоксиалкильную группу, аралкилоксиалкильную группу, алкилтиоалкильную группу, алкенильную группу и замещенную силильную группу.
Защитная группа фенольного гидроксила включает все группы, которые могут быть использованы в качестве общих защитных групп фенольного гидроксила. Примеры таких защитных групп фенольного гидроксила включают описанные в W. Greene et al., Protective Groups in Organic Synthesis, 4th edition, pp.370-424, 2007, John Wiley & Sons, INC. Конкретные примеры включают ацильную группу, алкильную группу, алкенильную группу, аралкильную группу, кислородсодержащую гетероциклическую группу, серосодержащую гетероциклическую группу, алкоксиалкильную группу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу.
Тетразолзащитная группа включает все группы, которые могут быть использованы в качестве общих тетразолзащитных групп. Примеры таких тетразолзащитных групп включают описанные в W. Greene et al., Protective Groups in Organic Synthesis, 4th edition, pp. 872-894, 2007, John Wiley & Sons, INC. Конкретные примеры включают ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, арилоксикарбонильную группу, аралкильную группу, ацилалкильную группу, алкоксиалкильную группу, арилсульфонильную группу и замещенную силильную группу.
Примеры уходящей группы включают атом галогена, алкилсульфонилоксигруппу и арилсульфонилоксигруппу.
Примеры алифатического углеводорода включают пентан, гексан, циклогексан.
Примеры галогенированного углеводорода включают хлористый метилен, хлороформ и дихлорэтан.
Примеры спирта включают метанол, этанол, пропанол, 2-пропанол, бутанол и 2-метил-2-пропанол.
Примеры простого эфира включают диэтиловый эфир, диизопропиловый эфир, диоксан, тетрагидрофуран, анизол, диметиловый эфир этиленгликоля, диметиловый эфир диэтиленгликоля и диэтиловый эфир диэтиленгликоля.
Примеры кетона включают ацетон, 2-бутанон и 4-метил-2-пентанон.
Примеры сложного эфира включают метилацетат, этилацетат, пропилацетат и бутилацетат.
Примеры амида включают N,N-диметилформамид, N,N-диметилацетамид и 1-метил-2-пирролидон.
Примеры ароматического углеводорода включают бензол, толуол и ксилол.
Примеры соли соединения общей формулы [1] включают: соли основных групп, таких как общеизвестная аминогруппа; или соли кислых групп, таких как гидроксильная группа фенола или карбоксильная группа.
Примеры солей основных групп включают: соли с минеральными кислотами, такими как соляная кислота, бромистоводородная и серная кислота; соли с органическими карбоксильными кислотами, такими как винная кислота, муравьиная кислота, уксусная кислота, лимонная кислота, трихлоруксусная кислота и трифторуксусная кислота; соли с сульфоновыми кислотами, такими как метансульфоновая кислота, бензолсульфоновая кислота, пара-толуолсульфоновая кислота, мезитиленсульфоновая кислота и нафталинсульфоновая кислота.
Примеры солей кислых групп включают: соли с щелочными металлами, такими как натрий и калий; соли с щелочноземельными металлами, такими как кальций и магний; соли аммония; соли с азотсодержащими органическими основаниями, такими как триметиламин, триэтиламин, трибутиламин, пиридин, N,N-диметиланилин, N-метилпиперидин, N-метилморфолин, диэтиламин, дициклогексиламин, прокаин, дибензиламин, N-бензил-β-фенэтиламин и N,N'-дибензилэтилендиамин.
Более того, среди вышеупомянутых солей предпочтительные соли соединения, представленного общей формулой [1], включают фармакологически приемлемые соли.
Алкиламиногруппа в качестве R2 и диалкиламиногруппа в качестве R2 могут быть необязательно замещены одной или несколькими группами, выбранными из аминогруппы, гидроксильной группы, карбоксильной группы и алкоксигруппы.
Алкильная группа в качестве R2 и алкоксигруппа в качестве R2 могут быть необязательно замещены одной или несколькими группами, выбранными из атома галогена, цианогруппы, гидроксильной группы, карбоксильной группы и алкоксигруппы.
Циклоалкильная группа в качестве R3, циклоалкенильная группа в качестве R3, арильная группа в качестве R3, моноциклическая гетероциклическая группа в качестве R3, бициклическая гетероциклическая группа в качестве R3 и гетероциклическая группа в качестве R3 могут быть необязательно замещены одной или несколькими группами, выбранными из атома галогена, цианогруппы, нитрогруппы, ацильной группы, ацилоксигруппы, сульфогруппы, фосфорильной группы, алкилсульфонильной группы, алкилсульфониламидной группы, ацетамидной группы, карбамоильной группы, оксогруппы, необязательно защищенной карбоксильной, амино, алкиламино и гидроксильной групп, и необязательно замещенной алкильной, алкенильной, алкинильной, алкокси, арильной, алкиламино, диалкиламино, циклической амино, аралкильной и гетероциклической групп.
Алкиламиногруппы в качестве R5, R6, R7 и R8 и диалкиламиногруппы в качестве R5, R6, R7 и R8 могут быть необязательно замещены одной или несколькими группами, выбранными из аминогруппы, гидроксильной группы и алкоксигруппы.
5-, 6- и 7-членная гетероциклическая группа образованная R6 и R7 вместе с атомами углерода, с которыми они связаны, может быть необязательно замещена одной или несколькими группами, выбранными из атома галогена, цианогруппы, нитрогруппы, ацильной группы, ацилоксигруппы, сульфогруппы, фосфорильной группы, алкилсульфонильной группы, алкилсульфониламиногруппы, ацетамидной группы, карбамоильной группы, оксогруппы, необязательно защищенной карбоксильной, амино, алкиламино и гидроксильной групп, и необязательно замещенной алкильной, алкенильной, алкинильной, алкокси, арильной, алкиламино, диалкиламино, циклической амино, аралкильной и гетероциклической групп.
Алкиламиногруппы в качестве R9 и R9a и диалкиламиногруппы в качестве R9 и R9a могут быть необязательно замещены одной или несколькими группами, выбранными из гидроксильной группы, необязательно защищенных карбоксильной, амино и алкиламино групп, и необязательно замещенных алкильной, алкенильной, алкинильной, алкокси, арильной, алкиламино, диалкиламино, циклической амино, аралкильной и гетероциклической групп.
Алкильные группы в качестве R9 и R9a и алкоксигруппы в качестве R9 и R9a могут быть необязательно замещены одной или несколькими группами, выбранными из атома галогена, цианогруппы, гидроксильной группы и алкоксигруппы.
Арильные группы в качестве R9 и R9a, арилоксигруппы в качестве R9 и R9a, гетероциклические группы в качестве R9, R9a и R9b, и гетероциклические оксигруппы в качестве R9 и R9a могут быть необязательно замещены одной или несколькими группами, выбранными из атома галогена, цианогруппы, нитрогруппы, ацильной группы, ацилоксигруппы, сульфогруппы, фосфорильной группы, алкилсульфонильной группы, алкилсульфониламиногруппы, ацетамидной группы, карбамоильной группы, оксогруппы, необязательно защищенной карбоксильной, амино, алкиламино и гидроксильной групп, и необязательно замещенной алкильной, алкенильной, алкинильной, алкокси, арильной, алкиламино, диалкиламино, циклической амино, аралкильной и гетероциклической групп.
Ацильные группы в качестве R9 и R9a и ацилоксигруппы в качестве R9 и R9a могут быть необязательно замещены одной или несколькими группами, выбранными из атома галогена, цианогруппы, гидроксильной группы и алкоксигруппы.
Низшая алкильная группа в качестве R10 может быть необязательно замещена одной или несколькими группами, выбранными из гидроксильной группы, необязательно защищенной карбоксильной, амино и алкиламино групп, и необязательно замещенной алкильной, алкенильной, алкинильной, алкокси, арильной, алкиламино, диалкиламино, циклической амино, аралкильной и гетероциклической групп.
Арильные группы в качестве R11 и R11a, азотсодержащие 6-членные ароматические гетероциклические группы в качестве R11 и R11a, кислородсодержащие 5-членные ароматические гетероциклические группы в качестве R11 и R11a, азотсодержащие кислородсодержащие 5-членные ароматические гетероциклические группы в качестве R11 и азотсодержащие серосодержащие 5-членные ароматические гетероциклические группы в качестве R11, могут быть необязательно замещены одной или несколькими группами, выбранными из атома галогена, цианогруппы, нитрогруппы, ацильной группы, ацилоксигруппы, сульфогруппы, фосфорильной группы, алкилсульфонильной группы, алкилсульфониламиногруппы, ацетамидной группы, карбамоильной группы, оксогруппы, необязательно защищенной карбоксильной, амино, алкиламино и гидроксильной групп, и необязательно замещенной алкильной, алкенильной, алкинильной, алкокси, арильной, алкиламино, диалкиламино, циклической амино, аралкильной и гетероциклической групп.
Алкиленовые группы в качестве X2 и X6, алкениленовые группы в качестве X2 и X6 и алкиниленовые группы в качестве X2 и X6, могут быть необязательно замещены одной или несколькими группами, выбранными из атома галогена и необязательно замещенной алкильной, фенильной, циклической амино и гетероциклической групп.
Алкиленовая группа в качестве X4 может быть необязательно замещена одной или несколькими группами, выбранными из атома галогена, цианогруппы, гидроксильной группы и алкоксигруппы.
Алкиленовая группа в качестве Y и Ya, алкениленовая группа в качестве Y, и алкиниленовая группа в качестве Y могут быть необязательно замещены одной или несколькими группами, выбранными из гидроксильной группы и алкоксигруппы.
Фенильная группа в качестве А, циклоалкильная группа в качестве А, и гетероциклическая группа в качестве А могут быть необязательно замещены одной или несколькими группами, выбранными из атома галогена, цианогруппы, нитрогруппы, ацетамидной группы, карбамоильной группы, необязательно защищенной карбоксильной, амино и гидроксильной групп и необязательно замещенной алкильной, алкокси, фенильной, циклической амино и гетероциклической групп.
Примеры заместителя для вышеописанных необязательно замещенных алкильной, алкенильной, алкинильной, алкокси, арильной, алкиламино, диалкиламино, циклической амино, аралкильной и гетероциклической групп включают атом галогена, цианогруппу, нитрогруппу, ацильную группу, сульфогруппу, фосфорильную группу, циклическую аминогруппу, алкилсульфонильную группу, алкилсульфониламиногруппу, ацетамидную группу, аралкильную группу, карбамоильную группу, алкильную группу, алкенильную группу, алкинильную группу, алкоксигруппу, арильную группу, гетероциклическую группу и необязательно защищенную карбоксильную, амино и гидроксильную группы.
Соединение, представленное общей формулой [1] по настоящему изобретению, предпочтительно включает следующие соединения.
Соединение, в котором R1 представляет собой необязательно защищенную карбоксильную группу, является предпочтительным.
Соединение, в котором R2 представляет собой атом водорода или атом галогена, является предпочтительным, и соединение, в котором R2 представляет собой атом водорода, является наиболее предпочтительным.
Соединение, в котором R3 представляет собой необязательно замещенную фенильную группу, необязательно замещенную фуранильную группу или необязательно замещенную тиенильную группу, является предпочтительным, и соединение, в котором R3 представляет собой необязательно замещенную фенильную группу или необязательно замещенную фуранильную группу, является наиболее предпочтительным.
Соединение, в котором R3 представляет собой необязательно замещенную циклоалкильную группу, необязательно замещенную циклоалкенильную группу, необязательно замещенную фенильную группу, необязательно замещенную моноциклическую гетероциклическую группу или необязательно замещенную бициклическую гетероциклическую группу, является предпочтительным; соединение, в котором R3 представляет собой необязательно замещенную фенильную группу или необязательно замещенную бициклическую гетероциклическую группу, является более предпочтительным; и соединение, в котором R3 представляет собой необязательно замещенную фенильную группу, является еще более предпочтительным.
Соединение, в котором R4 представляет собой атом водорода, является предпочтительным.
Соединение, в котором один из R5, R6, R7 и R8 представляет собой группу, представленную общей формулой -Y-R9a [в которой R9a представляет собой атом галогена, нитрогруппу, необязательно защищенную гидроксильную группу, необязательно защищенную аминогруппу, необязательно защищенную или замещенную алкиламиногруппу, необязательно замещенную диалкиламиногруппу, необязательно замещенную алкильную группу, необязательно замещенную алкоксигруппу, необязательно замещенную арильную группу, необязательно замещенную арилоксигруппу, необязательно замещенную гетероциклическую группу, необязательно замещенную гетероциклическую оксигруппу, необязательно замещенную ацильную группу или необязательно замещенную ацилоксигруппу;
Ya представляет собой необязательно замещенную алкиленовую группу, связь, группу, представленную общей формулой -O-(CH2)n- [в которой n представляет собой целое число от 1 до 4], или группу, представленную общей формулой NR10a-(CH2)n- [в которой R10a представляет собой низшую алкильную группу; и n имеет те же значения, что и указанные выше]], а каждый из других оставшихся представляет собой атом водорода, является предпочтительным. Соединение, в котором каждый R5, R6 и R8 представляет собой атом водорода, и R7 представляет собой группу, представленную общей формулой -Yb-R9b [в которой R9b представляет собой необязательно замещенную гетероциклическую группу; и Yb представляет собой алкиленовую группу, связь или группу, представленную общей формулой -O-(CH2)n- [в которой n представляет собой целое число от 1 до 4]], является более предпочтительным. Соединение, в котором каждый R5, R6 и R8 представляет собой атом водорода, и R7 представляет собой группу, представленную общей формулой-Yc-R9c [в которой R9c представляет собой гетероциклическую группу, которая может быть необязательно замещена низшей алкильной группой; и Yc представляет собой метиленовую группу, связь или группу, представленную общей формулой -O-(CH2)2-], является еще более предпочтительным.
Соединение, в котором X2 представляет собой необязательно замещенную алкиленовую группу, необязательно замещенную алкениленовую группу или связь, является предпочтительным, и соединение, в котором X2 представляет собой связь, является более предпочтительным.
Соединение, в котором X3 представляет собой связь, является предпочтительным.
Соединение, в котором X4 представляет собой атом кислорода, необязательно защищенную иминогруппу или связь, является предпочтительным, и соединение, в котором X4 представляет собой связь, является более предпочтительным.
Соединение, в котором X4 представляет собой атом кислорода, алкиленовую группу, алкениленовую группу или связь, является предпочтительным, и соединение, в котором X4 представляет собой связь, является более предпочтительным.
Соединение, в котором Z1 представляет собой CH, Z2 представляет собой атом азота, Z3 представляет собой CH, Z4 представляет собой группу, представленную общей формулой C-R11a [в которой R11a представляет собой необязательно замещенную арильную группу, необязательно замещенную азотсодержащую 6-членную ароматическую гетероциклическую группу или необязательно замещенную кислородсодержащую 5-членную ароматическую гетероциклическую группу], и Z5 представляет собой CH, является предпочтительным. Соединение, в котором Z1 представляет собой CH, Z2 представляет собой атом азота, Z3 представляет собой CH, Z4 представляет собой C-C6H5, и Z5 представляет собой CH, является более предпочтительным.
Соединение, в котором А представляет собой необязательно замещенную фенильную группу или необязательно замещенную гетероциклическую группу, является предпочтительным, и соединение, в котором А представляет собой необязательно замещенную фенильную группу или необязательно замещенную пиридильную группу, является более предпочтительным.
Примеры заболеваний, ассоциированных с избыточной продукцией коллагена, включают легочный фиброз, склеродермию, нефросклероз и цирроз печени. Из них предпочтительным заболеванием является легочный фиброз.
Предпочтительные примеры соединения, представленного общей формулой [1] по настоящему изобретению, включают следующие соединения:
2-(2-гидрокси-5-(пиридин-4-ил)бензамидо)-4-фенилбензойную кислоту,
2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)-4-фенилбензойную кислоту,
2-(2-гидрокси-5-(пиримидин-2-ил)бензамидо)-4-фенилбензойную кислоту,
2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-фенилбензойную кислоту,
2-(2-гидрокси-5-(1-метилпиперидин-4-ил)бензамидо)-4-фенилбензойную кислоту,
2-(5-(1-этилпиперидин-4-ил)-2-гидроксибензамидо)-4-фенилбензойную кислоту,
2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(3-метилфенил)бензойную кислоту,
2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)-4-фенилбензойную кислоту,
4-(3-фторфенил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойную кислоту,
2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)-4-(3-метоксифенил)бензойную кислоту,
2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)-4-(3-метилфенил)бензойную кислоту,
2-(2-гидрокси-5-(метил(2-(пирролидин-1-ил)этил)амино)бензамидо)-4-фенилбензойную кислоту,
2-(2-гидрокси-5-(2-(4-метилпиперазин-1-ил)этил)бензамидо)-4-фенилбензойную кислоту,
2-(2-гидрокси-5-((4-метилпиперазин-1-ил)метил)бензамидо)-4-фенилбензойную кислоту,
2-(5-(2-(4-этилпиперазин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензойную кислоту,
2-(2-гидрокси-5-(2-(1-метилпиперидин-4-ил)этокси)бензамидо)-4-фенилбензойную кислоту,
4-(2-(метиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойную кислоту,
4-(2-(этиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойную кислоту и
4-(фуран-2-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензойную кислоту.
Типичные примеры соединения по настоящему изобретению включают соединения, представленные в Таблицах 1a, 1b, 1c, 2a и 2b. Указанные соединения являются новыми соединениями. Указанные соединения обладают ингибирующим действием на продукцию коллагена и применимы для профилактики, лечения и тому подобное, заболеваний, ассоциированных с избыточной продукцией коллагена.
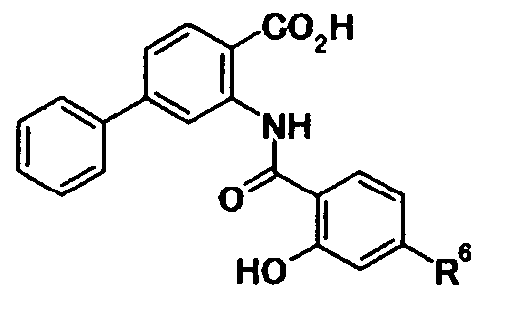
метил
метокси
диметиламино
фенил
пиридин-2-ил
пиридин-3-ил
пиридин-4-ил
пиримидин-2-ил
фуран-3-ил
1H-пиразол-1-ил
1H-имидазол-1-ил
пиперидин-1-ил
1-метилпиперидин-4-ил
морфилин-4-ил
(2-(диметиламино)этил)(метил)амино
2-(морфолин-4-ил)этокси
2-(4-метилпиперазин-1-ил)этокси
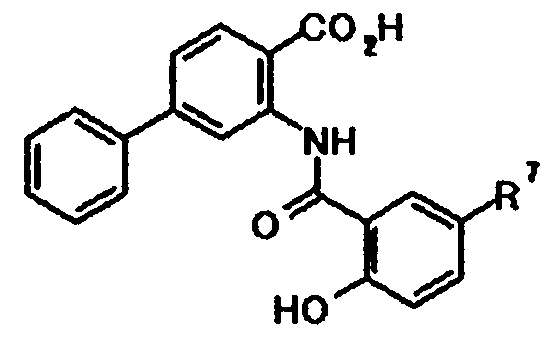
Br
ацетил
метил
метокси
этокси
пропокси
изопропокси
диметиламино
диэтиламино
фенил
фенокси
пиперидин-1-ил
пиперидин-2-ил
пиперидин-3-ил
1-метилпиперидин-2-ил
1-метилпиперидин-4-ил
2-метилпиперидин-1-ил
3-метилпиперидин-1-ил
4-метилпиперидин-1-ил
1-этилпиперидин-4-ил
4-метил-3-оксопиперазин-1-ил
4-этил-3-оксопиперазин-1-ил
метил(2-(пирролидин-1-ил)этил)амино
метил(2-(пиперидин-1-ил)этил)амино
метил(2-(морфолин-4-ил)этил)амино
(2-(диметиламино)этил)(метил)амино
(2-(диэтиламино)этил)(метил)амино
(3-(диметиламино)пропил)(метил)амино
(2-(диметиламино)этил)(этил)амино
(4-метилпиперазин-1-ил)метил
(4-этилпиперазин-1-ил)метил
(4-пропилпиперазин-1-ил)метил
(4-изопропилпиперазин-1-ил)метил
(пиперидин-1-ил)метил
(пиперазин-1-ил)метил
(морфолин-4-ил)метил
(4-метилгомопиперазин-1-ил)метил
(4-аминопиперидин-1-ил)метил
(4-(метиламино)пиперидин-1-ил)метил
(4-(диметиламино)пиперидин-1-ил)метил
1-(2-гидроксиэтил)пиперидин-4-ил
3-гидроксипиперидин-1-ил
4-(гидроксиметил)пиперидин-1-ил
4-(диэтиламино)пиперидин-1-ил
азетидин-1-ил
тиоморфолин-4-ил
морфолин-4-ил
4-метилпиперазин-1-ил
4-этилпиперазин-1-ил
пиридин-2-ил
пиридин-3-ил
пиридин-4-ил
пиримидин-2-ил
пиримидин-5-ил
6-аминопиридин-2-ил
фуран-2-ил
фуран-3-ил
тетрагидрофуран-3-ил
1H-пиразол-1-ил
1H-имидазол-1-ил
оксазол-5-ил
2-(пиперазин-1-ил)этил
2-(4-метилпиперазин-1-ил)этил
2-(4-этилпиперазин-1-ил)этил
1-метилпиперидин-4-илокси
2-(диметиламино)этокси
2-(диэтиламино)этокси
2-(морфолин-4-ил)этокси
2-(пирролидин-1-ил)этокси
2-(пиперазин-1-ил)этокси
2-(тиоморфолин-4-ил)этокси
2-(азетидин-1-ил)этокси
2-(4-гидроксипиперидин-1-ил)этокси
2-(4-(гидроксиметил)пиперидин-1-ил)этокси
2-(4-(2-гидроксиэтил)пиперидин-1-ил)этокси
2-(4-метилпиперазин-1-ил)этокси
2-(4-этилпиперазин-1-ил)этокси
3-(4-метилпиперазин-1-ил)пропокси
2-(4-(2-гидроксиэтил)пиперазин-1-ил)этокси
2-(4-(3-гидроксипропил)пиперазин-1-ил)этокси
(1-метилпиперидин-4-ил)метокси
2-(1-метилпиперидин-4-ил)этокси
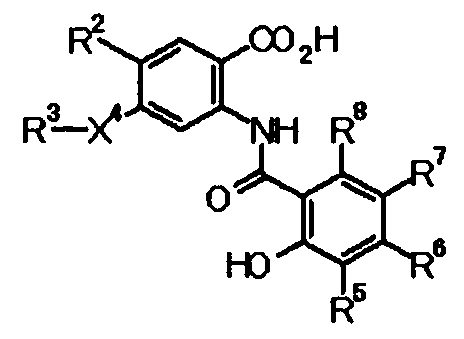
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
F
метокси
H
H
фенил
фенил
фенил
фенил
фенил
2-метоксифенил
2-метоксифенил
2-метоксифенил
2-метоксифенил
2-метоксифенил
3-метоксифенил
4-метоксифенил
2-метилфенил
3-метилфенил
4-метилфенил
2-фторфенил
3-фторфенил
4-фторфенил
фенил
фенил
фенокси
фенэтил
метокси
метил
H
пиридин-3-ил
пиридин-4-ил
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
метокси
пиридин-2-ил
пиридин-3-ил
пиридин-4-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
пиперидин-1-ил
H
H
метокси
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
фуран-2-ил
фуран-2-ил
фуран-3-ил
тиофен-2-ил
1H-пиррол-2-ил
2-(метиламино)фенил
2-(метиламино)фенил
2-(этиламино)фенил
2-фторфенил
3-фторфенил
4-фторфенил
2-метилфенил
3-метилфенил
4-метилфенил
2-метоксифенил
3-метоксифенил
4-метоксифенил
3,4-диметоксифенил
3,5-диметоксифенил
фуран-2-ил
тиофен-2-ил
тиофен-3-ил
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
пиридин-3-ил
пиперидин-1-ил
пиридин-3-ил
пиперидин-1-ил
пиперидин-1-ил
метокси
пиридин-3-ил
пиридин-3-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
морфолин-4-ил
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
H
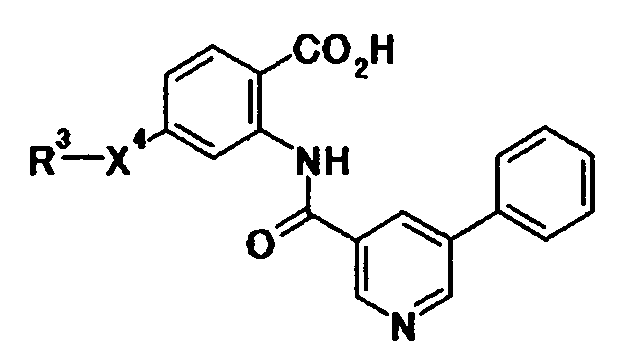
анилино
пиперидин-1-ил
морфолин-4-ил
фуран-2-ил
фуран-3-ил
тетрагидрофуран-2-ил
тиофен-2-ил
тиофен-3-ил
пиридин-2-ил
1H-пиррол-1-ил
1-метил-1H-пиррол-2-ил
1H-пиразол-1-ил
2-аминофенил
2-фторфенил
2-(трифторметил)фенил
3-(трифторметил)фенил
2-нитрофенил
2-гидроксифенил
3-метоксифенил
4-метоксифенил
2,3-диметоксифенил
2-этоксифенил
3-этоксифенил
2-метилфенил
2-(дифторметокси)фенил
3-(дифторметокси)фенил
4-(дифторметокси)фенил
2-(трифторметокси)фенил
3-(трифторметокси)фенил
2-(метиламино)фенил
3-(метиламино)фенил
4-(метиламино)фенил
2-(этиламино)фенил
3-(этиламино)фенил
3-(диметиламино)фенил
3-(диэтиламино)фенил
CO2H
CO2H
CO2H
CO2H
CO2H
CO2H
CO2H
CO2H
CO2H
CO2H
CO2H
CO2H
CO2H
метокси
H
H
H
H
H
H
H
H
H
H
H
H
5-фенилпиридин-3-ил
2-фенилпиридин-4-ил
6-фенилпиридин-3-ил
6-фенилпиридин-2-ил
5-фенилпиридин-2-ил
4-фенилпиридин-2-ил
5-(2-фторфенил)пиридин-3-ил
5-(фуран-2-ил)пиридин-3-ил
5-(фуран-3-ил)пиридин-3-ил
5-(пиридин-3-ил)пиридин-3-ил
5-(пиридин-4-ил)пиридин-3-ил
6-(пиридин-4-ил)пиридин-3-ил
5-(пиримидин-2-ил)пиридин-3-ил
Типичные примеры соединения по настоящему изобретению дополнительно включают соединения, представленные в Таблице 3a. Указанные соединения представляют собой соединения, описанные в Патентном документе 1. Тем не менее, было совершенно неизвестно, что указанные соединения обладают ингибирующим действием на продукцию коллагена. Указанные соединения применимы для профилактики, лечения и тому подобное, заболеваний, ассоциированных с избыточной продукцией коллагена.
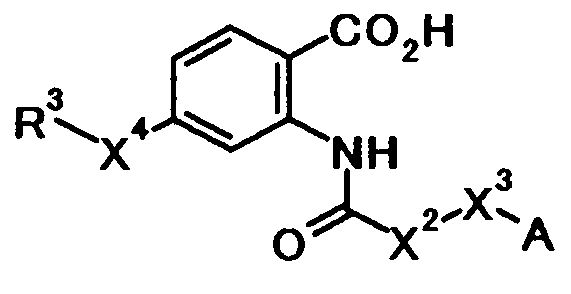
Если для соединения общей формулы [1] или его соли существуют изомеры (например, оптический изомер, геометрический изомер, таутомер), то настоящее изобретение включает эти изомеры. Кроме того, настоящее изобретение также включает сольват, гидрат и различные формы кристаллического вещества.
Далее будет описан способ получения соединения по настоящему изобретению.
Соединение по настоящему изобретению получают посредством сочетания известных способов. Например, оно может быть получено следующими способами получения.
Способ получения 1
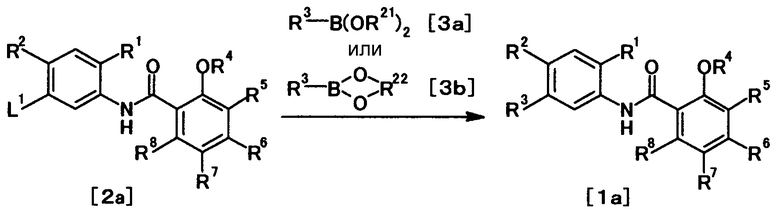
где R21 представляет собой атом водорода или низшую алкильную группу; R22 представляет собой необязательно замещенную алкиленовую группу; L1 представляет собой уходящую группу; и R1, R2, R3, R4, R5, R6, R7 и R8 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [3a] известны, например, пиридин-3-бороновая кислота, 3-(метансульфонамидо)фенилбороновая кислота, тиофен-2-бороновая кислота, бензофуран-2-бороновая кислота и 3-метоксифенилбороновая кислота.
В качестве соединения общей формулы [3b] известен, например, 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фуран.
Соединения общей формулы [3a] и [3b] могут быть получены, например, из соответствующих галоидных соединений, в соответствии со способом, описанным в JP 2003-206290A или в The Journal of Organic Chemistry, 1995, vol. 60, pp. 7508-7510.
Соединение общей формулы [1a] может быть получено путем осуществления взаимодействия соединения общей формулы [2a] с соединением общей формулы [3a] или [3b] в присутствии или в отсутствие основания, в присутствии палладиевого катализатора и в присутствии или в отсутствие лиганда.
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, спирты, ароматические углеводороды, амиды, галоидзамещенные углеводороды, простые эфиры, кетоны, ацетонитрил, сложные эфиры и диметилсульфоксид. Указанные вещества могут быть использованы в виде смеси.
Примеры основания, используемого в случае необходимости в этой реакции, включают неорганические основания, такие как бикарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия и трикалийфосфат и органические основания, такие как триэтиламин и N,N-диизопропилэтиламин. Количество в молях используемого основания может быть 1-50-кратным, предпочтительно 2-5-кратным, по отношению к количеству в молях соединения общей формулы [2a].
Примеры палладиевого катализатора, используемого в этой реакции, включают металлические палладиевые катализаторы, такие как палладированный уголь и палладиевая чернь; неорганические палладиевые соли, такие как хлорид палладия; органические палладиевые соли, такие как ацетат палладия; и органические палладиевые комплексы, такие как тетракис(трифенилфосфин)палладий(0), дихлорид бис(трифенилфосфин)палладия(II), дихлорид 1,1'-бис(дифенилфосфино)ферроценпалладия(II), трис(дибензилиденацетон)дипалладий(0) и дихлорид бис(ди-трет-бутил(4-диметиламинофенил)фосфин)палладия(II). Указанные вещества могут быть использованы в сочетании. Количество в молях используемого палладиевого катализатора может быть 0,00001-1-кратным, предпочтительно 0,001-0,1-кратным, по отношению к количеству в молях соединения общей формулы [2a].
Примеры лиганда, используемого в случае необходимости в этой реакции, включают триалкилфосфины, такие как триметилфосфин и три-трет-бутилфосфин; трициклоалкилфосфины, такие как трициклогексилфосфин; триарилфосфины, такие как трифенилфосфин и тритолилфосфин; триалкилфосфиты, такие как триметилфосфит, триэтилфосфит и трибутилфосфит; трициклоалкилфосфиты, такие трициклогексилфосфит; триарилфосфиты, такие как трифенилфосфит; соли имидазолия, такие как хлорид 1,3-бис(2,4,6-триметилфенил)имидазолия; дикетоны, такие как ацетилацетон и октафторацетилацетон; амины, такие как триметиламин, триэтиламин, трипропиламин и триизопропиламин; 1,1'-бис(дифенилфосфино)ферроцен, 2,2'-бис(дифенилфосфино)-1,1'-бинафтил, 2-дициклогексилфосфино-2',6'-диметоксибифенил, 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил и 2-(ди-трет-бутилфосфино)-2',4',6'-триизопропилбифенил; и 2-(ди-трет-бутилфосфино)бифенил. Указанные вещества могут быть использованы в сочетании. Количество в молях используемого лиганда может быть 0,00001-1-кратным, предпочтительно 0,001-0,1-кратным, по отношению к количеству в молях соединения общей формулы [2a].
Количество в молях используемого соединения общей формулы [3a] или [3b] может быть 1-50-кратным, предпочтительно 1-2-кратным, по отношению к количеству в молях соединения общей формулы [2a].
Эта реакция может предпочтительно проводиться в атмосфере инертного газа (например, азота или аргона) при температуре от 40 до 170°C в течение от 1 минуты до 96 часов.
Способ получения 2
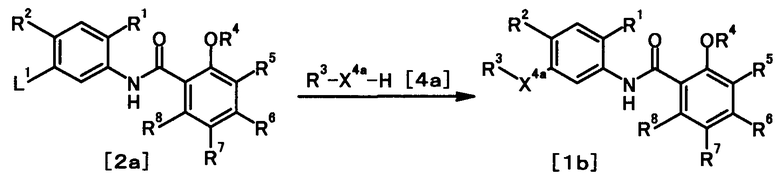
где X4a представляет собой атом кислорода или необязательно защищенную иминогруппу; и R1, R2, R3, R4, R5, R6, R7, R8 и L1 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [4a] известны, например, анилин, бензиламин и фенол. Соединение общей формулы [4a] может быть получено, например, из соответствующего галоидного соединения обычным способом.
Соединение общей формулы [1b] может быть получено в соответствии со Способом получении 1 путем осуществления взаимодействия соединения общей формулы [2a] с соединением общей формулы [4a].
Способ получения 3
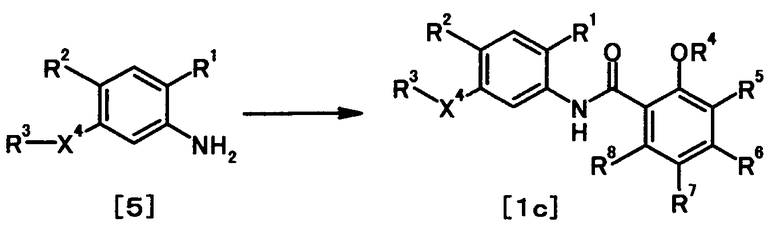
где R1, R2, R3, R4, R5, R6, R7, R8 и X4 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [5] известны, например, метил-2-амино-4-фенилбензоат (Патентный Документ 1); трет-бутил-2-амино-4-фенилбензоат, трет-бутил-2-амино-4-феноксибензоат и трет-бутил-2-амино-4-фенэтилбензоат (WO2006/098308).
Соединение общей формулы [1c] может быть получено путем ацилирования соединения общей формулы [5]. Конкретные примеры способа включают способ с использованием галоидангидрида в присутствии или в отсутствие основания.
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают амиды, галоидзамещенные углеводороды, ароматические углеводороды, простые эфиры, ацетонитрил, кетоны, сложные эфиры, сульфолан и диметилсульфоксид. Указанные вещества могут быть использованы в виде смеси.
Галоидангидрид, используемый в этой реакции, может быть получен путем осуществления взаимодействия соединения представленного общей формулой [6]:
[Формула 5]
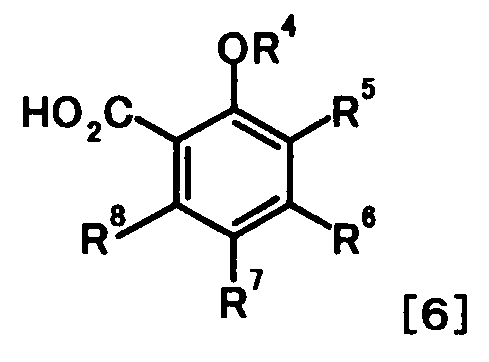
(в которой R4, R5, R6, R7 и R8 имеют те же значения, что и представленные выше), например, с тионилхлоридом или оксалилхлоридом.
Количество в молях используемого галоидангидрида может быть 1-50-кратным, предпочтительно 1-5-кратным, по отношению к количеству в молях соединения общей формулы [5].
В качестве соединений общей формулы [6] известны, например, 2-ацетокси-3-хлорбензойная кислота, 2-ацетокси-5-бромбензойная кислота, 2-ацетокси-5-йодбензойная кислота, 2-ацетокси-5-метилбензойная кислота, 2-ацетокси-5-нитробензойная кислота, 2-(бензилокси)-5-бромбензойная кислота, 2-(бензилокси)-5-нитробензойная кислота, 2-(бензилокси)-5-(пиридин-2-ил)бензойная кислота и 2-(бензилокси)-5-(пиридин-3-ил)бензойная кислота.
Примеры основания, используемого в случае необходимости в этой реакции, включают неорганические основания, такие как гидроксид натрия, гидроксид калия и гидроксид лития; органические основания, такие как метоксид натрия, этоксид натрия, трет-бутоксид калия, триэтиламин, N,N-диизопропилэтиламин и пиридин; и карбонаты, такие как бикарбонат натрия, карбонат натрия, карбонат калия и карбонат цезия. Количество в молях используемого основания может быть 1-50-кратным, предпочтительно 1-5-кратным, по отношению к количеству в молях соединения общей формулы [5].
Эта реакция обычно может проводиться при температуре от -78 до 100°C, предпочтительно от 0 до 80°C, в течение от 10 минут до 24 часов.
Способ получения 4
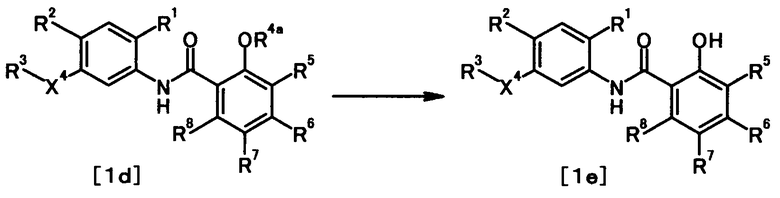
где R4a представляет собой защитную группу фенольного гидроксила; и R1, R2, R3, R5, R6, R7, R8 и X4 имеют те же значения, что и представленные выше.
Соединение общей формулы [1e] может быть получено путем снятия защитных групп с соединения общей формулы [1d].
Примеры этого способа включают способы, описанные в W. Greene, et al., Protective Groups in Organic Synthesis, 4th Edition, pp. 370-424, 2007 (John Wiley & Sons, Inc.).
Конкретные примеры способов включают реакцию гидролиза с использованием кислоты или основания, реакцию деалкилирования с использованием соли и реакцию восстановительного деалкилирования, включая реакцию каталитического гидрирования с использованием металлического катализатора.
(4-1)
Примеры кислоты, используемой в реакции гидролиза с использованием кислоты, включают муравьиную кислоту, соляную кислоту, серную кислоту, бромистоводородную кислоту, трифторуксусную кислоту, метансульфоновую кислоту, хлорид алюминия и йодид триметилсилана. Количество в молях используемой кислоты может быть 1-100000-кратным, предпочтительно 1-1000-кратным, по отношению к количеству в молях соединения общей формулы [1d].
Примеры основания, используемого в реакции гидролиза с использованием основания, включают неорганические основания, такие как гидроксид натрия, гидроксид калия и гидроксид лития; органические основания, такие как метоксид натрия, этоксид натрия и трет-бутоксид калия; карбонаты, такие как карбонат калия и карбонат натрия; и фторид тетрабутиламмония. Количество в молях используемого основания может быть 1-1000-кратным, предпочтительно 1-50-кратным, по отношению к количеству в молях соединения общей формулы [1d].
Примеры соли, используемой в реакции деалкилирования с использованием соли, включают йодид лития и хлорид натрия. Количество в молях используемой соли может быть 1-100-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [1d].
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, спирты, амиды, галоидзамещенные углеводороды, ароматические углеводороды, простые эфиры, ацетонитрил, кетоны и сложные эфиры. Указанные вещества могут быть использованы в виде смеси.
(4-2)
Растворитель, используемый в реакции каталитического гидрирования с использованием металлического катализатора, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, спирты, амиды, галоидзамещенные углеводороды, ароматические углеводороды, простые эфиры, ацетонитрил, кетоны, сложные эфиры, уксусную кислоту и пиридин. Указанные вещества могут быть использованы в виде смеси.
Примеры металлического катализатора, используемого в этой реакции, включают палладиевые металлические катализаторы, такие как палладированный уголь и палладиевая чернь; соли палладия, такие как оксид палладия и гидроксид палладия; никелевые металлические катализаторы, такие как никель Ренея; соли платины, такие как оксид платины. Количество используемого металлического катализатора может быть 0,001-5-кратным (по массе), предпочтительно 0,01-1-кратным (по массе), по отношению к количеству соединения общей формулы [1d].
Примеры источника водорода включают водород; муравьиную кислоту; формиаты, такие как формиат натрия, формиат аммония и формиат триэтиламмония; циклогексен; и циклогексадиен. Количество в молях используемого источника водорода может быть 2-100-кратным, предпочтительно 2-10-кратным, по отношению к количеству в молях соединения общей формулы [1d].
Эта реакция может проводиться при температуре от 0 до 200°C, предпочтительно от 0 до 100°C, в течение от 1 минуты до 24 часов.
Способ получения 5
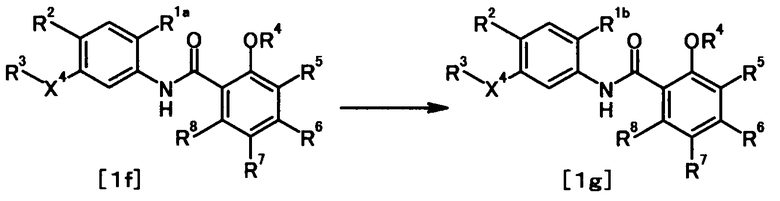
где R1a представляет собой защищенную карбоксильную группу или защищенную 1H-тетразол-5-ильную группу; R1b представляет собой карбоксильную группу или 1H-тетразол-5-ильную группу; и R2, R3, R4, R5, R6, R7, R8 и X4 имеют те же значения, что и представленные выше.
Соединение общей формулы [1g] может быть получено путем снятия защитных групп с соединения общей формулы [1f].
Снятие карбоксилзащитной группы может быть осуществлено, например, способом, описанным в W. Greene, et al., Protective Groups in Organic Synthesis, 4th Edition, pp. 533-643, 2007 (John Wiley & Sons, Inc.).
Снятие тетразолзащитной группы может быть осуществлено, например, способом, описанным в W. Greene, et al., Protective Groups in Organic Synthesis, 4th Edition, pp. 872-894, 2007 (John Wiley & Sons, Inc.).
Конкретно, соединение общей формулы [1g] может быть получено в соответствии со Способом получения 4.
Способ получения 6
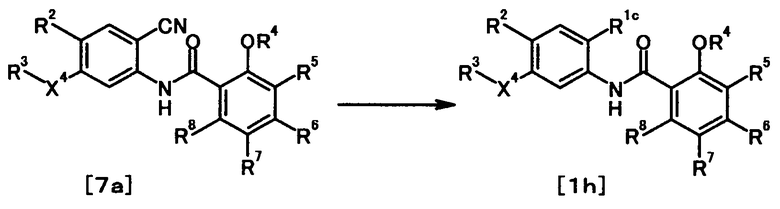
где R1c представляет собой необязательно защищенную 1H-тетразол-5-ильную группу; и R2, R3, R4, R5, R6, R7, R8 и X4 имеют те же значения, что и представленные выше.
Соединение общей формулы [1h] может быть получено, например, способом, описанным в Shinpen Heterokan Kagobutsu, Oyo-hen (New Heterocyclic Compounds, Advanced), pp. 98-100, 2004, Kodansha, или способом, находящимся в соответствии с ним. Конкретно, соединение общей формулы [1h] может быть получено путем проведения реакции циклоприсоединения соединения общей формулы [7а] с азидом в присутствии или в отсутствие соли.
Растворители, используемые в этих реакциях, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и их примеры включают простые эфиры, галоидзамещенные углеводороды, алифатические углеводороды, ароматические углеводороды, диметилсульфоксид и амиды. Указанные вещества могут быть использованы в виде смеси.
Примеры используемого азида включают азид натрия и азид триметилсилила. Количество в молях используемого азида может быть 1-100-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [7а].
Примеры используемой соли включают хлорид аммония. Количество в молях используемой соли может быть 1-100-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [7а].
Эта реакция обычно может проводиться при температуре от -78 до 150°C, предпочтительно от 0 до 120°C, в течение от 10 минут до 24 часов.
Способ получения 7
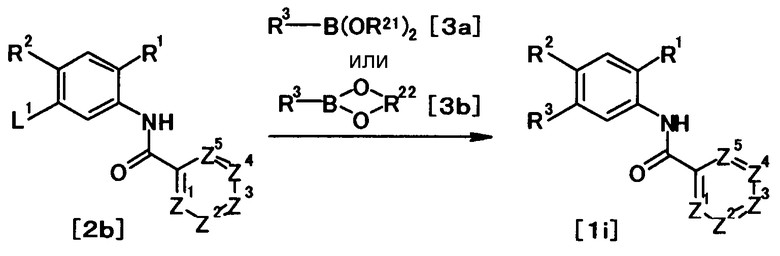
где R1, R2, R3, R21, R22, L1, Z1, Z2, Z3, Z4 и Z5 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [3a] известны, например, пиридин-3-бороновая кислота, 3-(метансульфонамидо)фенилбороновая кислота, тиофен-2-бороновая кислота, бензофуран-2-бороновая кислота и 3-метоксифенилбороновая кислота. В качестве соединения общей формулы [3b] известен, например, 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фуран. Кроме того, соединения общей формулы [3a] и [3b] могут быть получены, например, из соответствующих галоидных соединений в соответствии со способом, описанным в JP 2003-206290A или в The Journal of Organic Chemistry, 1995, vol. 60, pp. 7508-7510.
Соединение общей формулы [1i] может быть получено путем осуществления взаимодействия соединения общей формулы [2b] с соединением общей формулы [3а] или [3b] в присутствии или в отсутствие основания, в присутствии палладиевого катализатора и в присутствии или в отсутствие лиганда.
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, спирты, ароматические углеводороды, амиды, галоидзамещенные углеводороды, простые эфиры, кетоны, ацетонитрил, сложные эфиры и диметилсульфоксид. Указанные вещества могут быть использованы в виде смеси.
Примеры основания, используемого в случае необходимости в этой реакции, включают неорганические основания, такие как бикарбонат натрия, карбонат натрия, карбонат калия, карбонат цезия и трикалийфосфат; и органические основания, такие как триэтиламин и N,N-диизопропилэтиламин. Количество в молях используемого основания может быть 1-50-кратным, предпочтительно 2-5-кратным, по отношению к количеству в молях соединения общей формулы [2b].
Примеры палладиевого катализатора, используемого в этой реакции, включают палладиевые металлические катализаторы, такие как палладированный уголь и палладиевая чернь; неорганические палладиевые соли, такие как хлорид палладия; органические палладиевые соли, такие как ацетат палладия; и органические палладиевые комплексы, такие как тетракис(трифенилфосфин)палладий(0), дихлорид бис(трифенилфосфин)палладия(II), дихлорид 1,1'-бис(дифенилфосфино)ферроценпалладия(II), трис(дибензилиденацетон)дипалладий(0) и дихлорид бис(ди-трет-бутил(4-диметиламинофенил)фосфин)палладия(II). Указанные вещества могут быть использованы в сочетании. Количество в молях используемого палладиевого катализатора может быть 0,00001-1-кратным, предпочтительно 0,001-0,1-кратным, по отношению к количеству в молях соединения общей формулы [2b].
Примеры лиганда, используемого в случае необходимости в этой реакции, включают триалкилфосфины, такие как триметилфосфин и три-трет-бутилфосфин; трициклоалкилфосфины, такие как трициклогексилфосфин; триарилфосфины, такие как трифенилфосфин и тритолилфосфин; триалкилфосфиты, такие как триметилфосфит, триэтилфосфит и трибутилфосфит; трициклоалкилфосфиты, такие как трициклогексилфосфит; триарилфосфиты, такие как трифенилфосфит; соли имидазолия, такие как хлорид 1,3-бис(2,4,6-триметилфенил)имидазолия; дикетоны, такие как ацетилацетон и октафторацетилацетон; амины, такие как триметиламин, триэтиламин, трипропиламин и триизопропиламин; 1,1'-бис(дифенилфосфино)ферроцен, 2,2'-бис(дифенилфосфино)-1,1'-бинафтил, 2-дициклогексилфосфино-2',6'-диметоксибифенил, 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил и 2-(ди-трет-бутилфосфино)-2',4',6'-триизопропилбифенил; и 2-(ди-трет-бутилфосфино)бифенил. Указанные вещества могут быть использованы в сочетании. Количество в молях используемого лиганда может быть 0,00001-1-кратным, предпочтительно 0,001-0,1-кратным, по отношению к количеству в молях соединения общей формулы [2b].
Количество в молях используемого соединения общей формулы [3a] или [3b] может быть 1-50-кратным, предпочтительно 1-2-кратным, по отношению к количеству в молях соединения общей формулы [2b].
Эта реакция может предпочтительно проводиться в атмосфере инертного газа (например, азота или аргона) при температуре от 40 до 170°C в течение от 1 минуты до 96 часов.
Способ получения 8
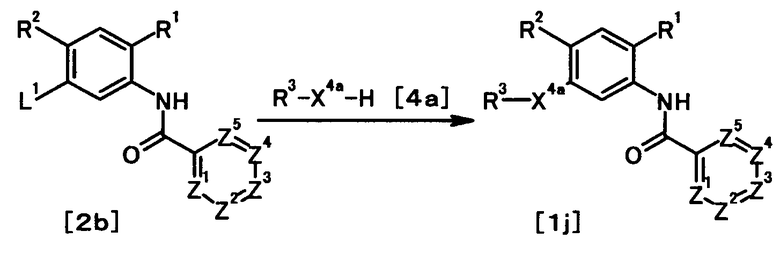
где R1, R2, R3, Z1, Z2, Z3, Z4, Z5, L1 и X4a имеют те же значения, что и представленные выше.
В качестве соединения общей формулы [4a] известны, например, анилин, бензиламин и фенол. Кроме того, соединение общей формулы [4a] может быть получено, например, из соответствующего галоидного соединения обычным способом.
Соединение общей формулы [1j] может быть получено в соответствии со Способом получения 7 путем осуществления взаимодействия соединения общей формулы [2b] с соединением общей формулы [4а].
Способ получения 9
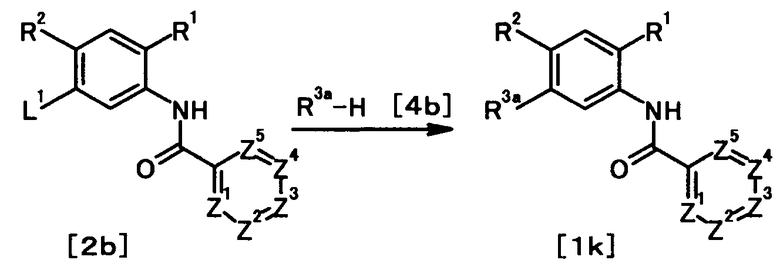
где R3a представляет собой моноциклическое гетероциклическое кольцо или бициклическое гетероциклическое кольцо, которое связано через атом азота с образованием кольца; и R1, R2, Z1, Z2, Z3, Z4, Z5 и L1 имеют те же значения, что и представленные выше.
В качестве соединения общей формулы [4b] известны, например, пиперидин, морфолин, тиоморфолин и 1H-пиразол.
Соединение общей формулы [1k] может быть получено путем осуществления взаимодействия соединения общей формулы [2b] с соединением общей формулы [4b]. Конкретные примеры этой реакции включают реакцию с использованием палладиевого катализатора и реакцию с использованием медного катализатора.
В реакции с использованием палладиевого катализатора соединение общей формулы [1k] может быть получено в соответствии со Способом получения 7 путем осуществления взаимодействия соединения общей формулы [2b] с соединением общей формулы [4b].
В реакции с использованием медного катализатора соединение общей формулы [1k] может быть получено путем осуществления взаимодействия соединения общей формулы [2b] с соединением общей формулы [4b] в присутствии или в отсутствие основания, в присутствии или в отсутствие лиганда и в присутствии медного катализатора.
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, спирты, ароматические углеводороды, амиды, галоидзамещенные углеводороды, простые эфиры, кетоны, ацетонитрил, сложные эфиры и диметилсульфоксид. Указанные вещества могут быть использованы в виде смеси.
Примеры основания, используемого в случае необходимости в этой реакции, включают неорганические основания, такие как бикарбонат натрия, карбонат натрия, карбонат калия и карбонат цезия; и органические основания, такие как триэтиламин, N,N-диизопропилэтиламин и N-метилморфолин. Количество в молях используемого основания может быть 1-50-кратным, предпочтительно 2-5-кратным, по отношению к количеству в молях соединения общей формулы [2b].
Примеры лиганда, используемого в случае необходимости в этой реакции, включают аминокислоты, такие как пролин, N,N-диметилглицин и аланин. Количество в молях используемого лиганда может быть 1-50-кратным, предпочтительно 2-5-кратным, по отношению к количеству в молях соединения общей формулы [2b].
Примеры медного катализатора, используемого в этой реакции, включают медь, бромид меди и йодид меди. Указанные вещества могут быть использованы в сочетании. Количество в молях используемого медного катализатора может быть 0,01-50-кратным, предпочтительно 0,1-5-кратным, по отношению к количеству в молях соединения общей формулы [2b].
Количество в молях используемого соединения общей формулы [4b] может быть 1-50-кратным, предпочтительно 1-2-кратным, по отношению к количеству в молях соединения общей формулы [2b].
Эта реакция может предпочтительно проводиться в атмосфере инертного газа (например, азота или аргона) при температуре от 10 до 180°C в течение от 1 минуты до 24 часов.
Способ получения 10
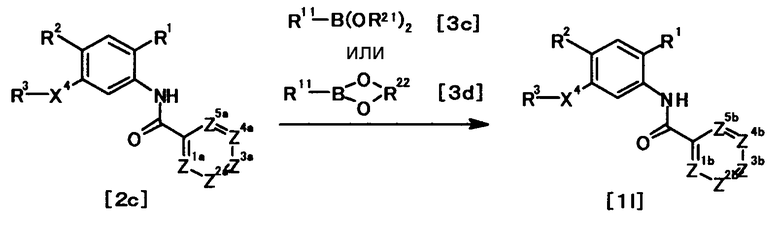
где один из Z1a, Z2a, Z3a, Z4a и Z5a представляет собой атом азота, один из оставшихся четырех представляет собой группу, представленную общей формулой C-L2 (в которой L2 представляет собой уходящую группу), и каждый из оставшихся трех представляет собой CH; один из Z1b, Z2b, Z3b, Z4b и Z5b представляет собой атом азота, один из оставшихся четырех представляет собой группу, представленную общей формулой C-R11 (в которой R11 имеет то же значение, что и представленное выше), и каждый из оставшихся трех представляет собой CH; и R1, R2, R3, R11, R21, R22 и X4 имеют те же значения, что и представленные выше.
Соединение общей формулы [1l] может быть получено в соответствии со Способом получения 7 путем осуществления взаимодействия соединения общей формулы [2c] с соединением общей формулы [3c] или [3d].
Способ получения 11
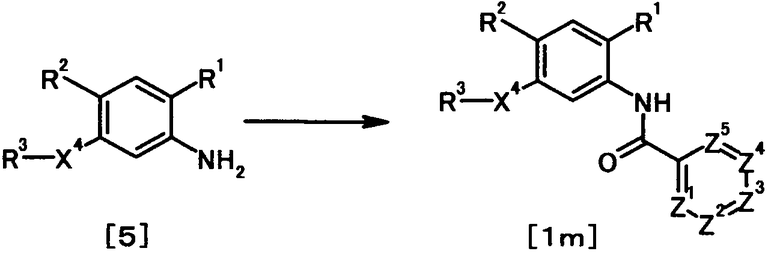
где R1, R2, R3, Z1, Z2, Z3, Z4, Z5 и X4 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [5] известны, например, метил-2-амино-4-фенилбензоат (Патентный Документ 1) и трет-бутил-2-амино-4-фенилбензоат (WO2006/098308).
Соединение общей формулы [1m] может быть получено путем ацилирования соединения общей формулы [5]. Конкретные примеры способа включают способ с использованием галоидангидрида в присутствии или в отсутствие основания.
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают амиды, галоидзамещенные углеводороды, ароматические углеводороды, простые эфиры, ацетонитрил, кетоны, сложные эфиры, сульфолан и диметилсульфоксид. Указанные вещества могут быть использованы в виде смеси.
Галоидангидрид, используемый в этой реакции, может быть получен путем осуществления взаимодействия соединения, представленного общей формулой [8]:
[Формула 6]
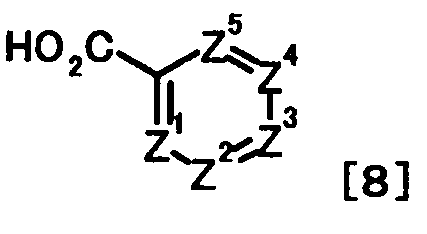
(в которой Z1, Z2, Z3, Z4 и Z5 имеют те же значения, что и представленные выше), например, с тионилхлоридом или оксалилхлоридом.
Количество в молях используемого галоидангидрида может быть 1-50-кратным, предпочтительно 1-5-кратным, по отношению к количеству в молях соединения общей формулы [5].
Примеры основания, используемого в случае необходимости в этой реакции, включают неорганические основания, такие как бикарбонат натрия, карбонат натрия, карбонат калия и карбонат цезия; и органические основания, такие как триэтиламин, пиридин и N,N-диизопропилэтиламин.
Количество в молях используемого основания может быть 1-50-кратным, предпочтительно 1-5-кратным, по отношению к количеству в молях соединения общей формулы [5].
Эта реакция обычно может проводиться при температуре от -78 до 100°C, предпочтительно от 0 до 80°C, в течение от 10 минут до 24 часов.
Способ получения 12
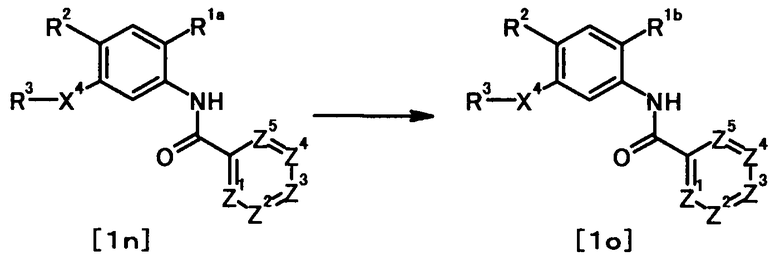
где R1a, R1b, R2, R3, Z1, Z2, Z3, Z4, Z5 и X4 имеют те же значения, что и представленные выше.
Соединение общей формулы [1o] может быть получено путем снятия защитных групп с соединения общей формулы [1n].
Снятие карбоксилзащитной группы может быть осуществлено, например, способом, описанным в W. Greene, et al., Protective Groups in Organic Synthesis, 4th Edition, pp. 533-643, 2007 (John Wiley & Sons, Inc.).
Снятие тетразолзащитной группы может быть осуществлено, например, способом, описанным в W. Greene, et al., Protective Groups in Organic Synthesis, 4th Edition, pp. 872-894, 2007 (John Wiley & Sons, Inc.).
Конкретные примеры способов включают реакцию гидролиза с использованием кислоты или основания, реакцию деалкилирования с использованием соли и реакцию восстановительного деалкилирования, включая реакцию каталитического гидрирования с использованием металлического катализатора.
(12-1)
Примеры кислоты, используемой в реакции гидролиза с использованием кислоты, включают муравьиную кислоту, соляную кислоту, серную кислоту, бромистоводородную кислоту, трифторуксусную кислоту, метансульфоновую кислоту, хлорид алюминия и йодид триметилсилана. Количество в молях используемой кислоты может быть 1-100000-кратным, предпочтительно 1-1000-кратным, по отношению к количеству в молях соединения общей формулы [1n].
Примеры основания, используемого в реакции гидролиза с использованием основания, включают неорганические основания, такие как гидроксид натрия, гидроксид калия и гидроксид лития; органические основания, такие как метоксид натрия, этоксид натрия и трет-бутоксид калия; карбонаты, такие как карбонат калия и карбонат натрия; и фторид тетрабутиламмония.
Количество в молях используемого основания может быть 1-1000-кратным, предпочтительно 1-50-кратным, по отношению к количеству в молях соединения общей формулы [1n].
Примеры соли, используемой в реакции деалкилирования с использованием соли, включают йодид лития и хлорид натрия. Количество в молях используемой соли может быть 1-100-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [1n].
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, спирты, амиды, галоидзамещенные углеводороды, ароматические углеводороды, простые эфиры, ацетонитрил, кетоны и сложные эфиры. Указанные вещества могут быть использованы в виде смеси.
(12-2)
Растворитель, используемый в реакции каталитического гидрирования с использованием металлического катализатора, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, спирты, амиды, галоидзамещенные углеводороды, ароматические углеводороды, простые эфиры, ацетонитрил, кетоны, сложные эфиры, уксусную кислоту и пиридин. Указанные вещества могут быть использованы в виде смеси.
Примеры металлического катализатора, используемого в этой реакции, включают палладиевые металлические катализаторы, такие как палладированный уголь и палладиевая чернь; соли палладия, такие как оксид палладия и гидроксид палладия; никелевые металлические катализаторы, такие как никель Ренея; и соли платины, такие как оксид платины. Количество используемого металлического катализатора может быть 0,001-5-кратным (по массе), предпочтительно 0,01-1-кратным (по массе), по отношению к количеству соединения общей формулы [1n].
Примеры источника водорода включают водород; муравьиную кислоту; формиаты, такие как формиат натрия, формиат аммония и формиат триэтиламмония; циклогексен; и циклогексадиен. Количество в молях используемого источника водорода может быть 2-100-кратным, предпочтительно 2-10-кратным, по отношению к количеству в молях соединения общей формулы [1n].
Эта реакция обычно может проводиться при температуре от 0 до 200°C, предпочтительно от 0 до 100°C, в течение от 1 минуты до 24 часов.
Способ получения 13
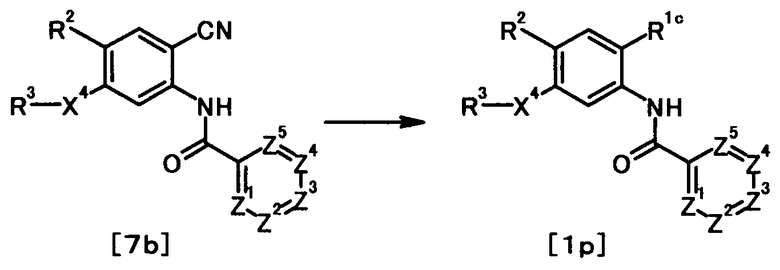
где R1c, R2, R3, Z1, Z2, Z3, Z4, Z5 и X4 имеют те же значения, что и представленные выше.
Соединение общей формулы [1p] может быть получено, например, способом, описанным в Shinpen Heterokan Kagobutsu, Oyo-hen (New Heterocyclic Compounds, Advanced), pp. 98-100, 2004, Kodansha, или способом, находящимся в соответствии с ним. Конкретно, соединение общей формулы [1p] может быть получено путем проведения реакции циклоприсоединения соединения общей формулы [7b] с азидом в присутствии или в отсутствие соли.
Растворители, используемые в этих реакциях, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и их примеры включают простые эфиры, галоидзамещенные углеводороды, алифатические углеводороды, ароматические углеводороды, диметилсульфоксид и амиды. Указанные вещества могут быть использованы в виде смеси.
Примеры используемого азида включают азид натрия и азид триметилсилила.
Количество в молях используемого азида может быть 1-100-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [7b].
Примеры используемой соли включают хлорид аммония. Количество в молях используемой соли может быть 1-100-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [7b].
Эта реакция обычно может проводиться при температуре от -78 до 150°C, предпочтительно от 0 до 120°C, в течение от 10 минут до 24 часов.
Полученные таким образом соединения общей формулы [1] или их соли могут быть преобразованы до других соединений общей формулы [1] или их солей известными реакциями, такими как конденсация, присоединение, окисление, восстановление, перегруппировка, замещение, галогенирование, дегидратация или гидролиз или посредством подходящего сочетания таких реакций.
Далее будут описаны способы получения веществ для получения соединений по настоящему изобретению.
Способ получения А
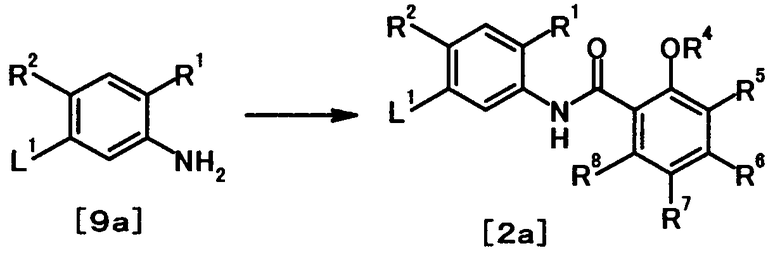
где R1, R2, R4, R5, R6, R7, R8 и L1 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [9a] известны, например, метил-2-амино-4-бромбензоат и трет-бутил-2-амино-4-бромбензоат (Патентный Документ 1).
Соединение общей формулы [2a] может быть получено в соответствии со Способом получения 3 путем ацилирования соединения общей формулы [9a].
Способ получения B
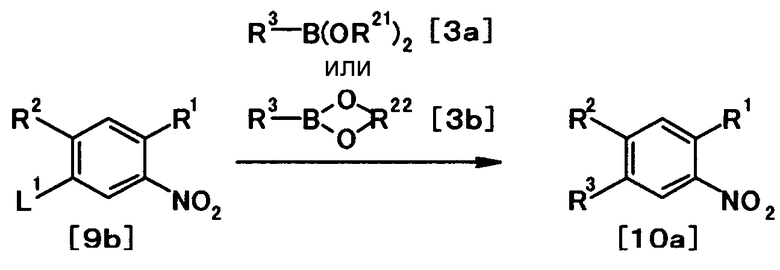
где R1, R2, R3, R21, R22 и L1 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [9b] известны, например, метил-4-бром-2-нитробензоат, трет-бутил-4-хлор-2-нитробензоат и трет-бутил-4-бром-2-нитробензоат (Патентный Документ 1).
Соединение общей формулы [10a] может быть получено в соответствии со Способом получения 1 путем осуществления взаимодействия соединения общей формулы [9b] с соединением общей формулы [3a] или [3b].
Способ получения C
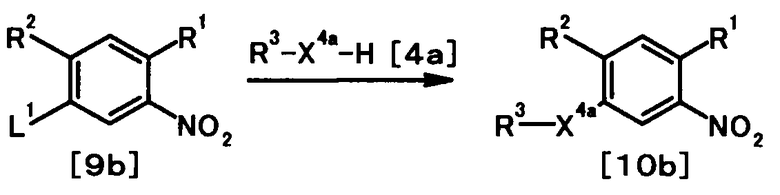
где R1, R2, R3, X4a и L1 имеют те же значения, что и представленные выше.
Соединение общей формулы [10b] может быть получено в соответствии со Способом получения 2 путем осуществления взаимодействия соединения общей формулы [9b] с соединением общей формулы [4a].
Способ получения D
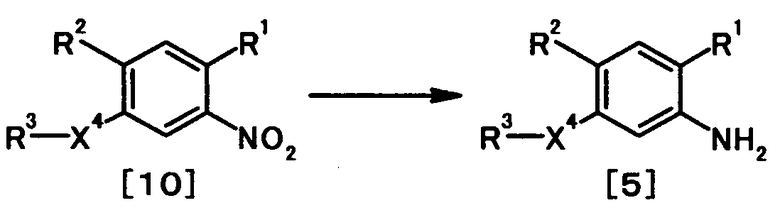
где R1, R2, R3 и X4 имеют те же значения, что и представленные выше.
Соединение общей формулы [5] может быть получено путем восстановления соединения общей формулы [10]. Эта реакция может проводиться способом, описанным в Richard C. Larock, et al., Comprehensive Organic Transformations, 2nd Edition, pp. 823-827, 1999 (John Wiley & Sons, Inc.), или способом, находящимся в соответствии с ним. Конкретные примеры способов включают реакцию каталитического гидрирования с использованием металлического катализатора и реакцию восстановления с использованием металла, такого как железо или цинк.
Реакция каталитического гидрирования соединения общей формулы [10] может проводиться в соответствии со Способом получения (4-2).
В случае, когда соединение общей формулы [10] подвергают реакции восстановления с использованием металла, используемый растворитель конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, спирты, амиды, галоидзамещенные углеводороды, ароматические углеводороды, простые эфиры, ацетонитрил, кетоны и сложные эфиры. Указанные вещества могут быть использованы в виде смеси.
Примеры металла, используемого в этой реакции, включают железо, цинк, олово и хлорид олова(II). Количество в молях используемого металла может быть 1-50-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [10].
Примеры кислоты, используемой в случае необходимости в этой реакции, включают соляную кислоту, бромистоводородную кислоту и уксусную кислоту. Количество используемой кислоты может быть 0,001-100-кратным (об./масс.), предпочтительно 0,01-20-кратным (об./масс.), по отношению к количеству соединения общей формулы [10].
Эта реакция может проводиться при температуре от 0 до 200°C, предпочтительно от 0 до 100°C, в течение от 1 минуты до 24 часов.
Способ получения E
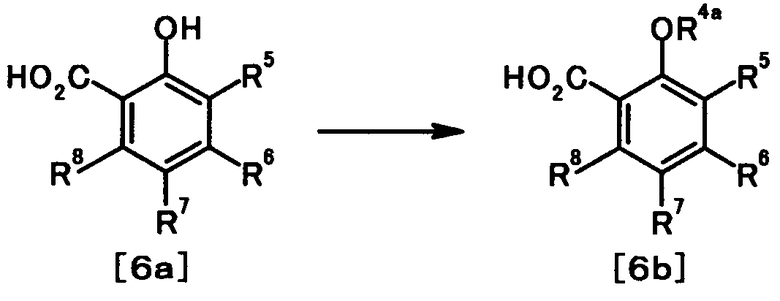
где R4a, R5, R6, R7 и R8 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [6a] известны, например, 5-этоксисалициловая кислота и 5-изопропоксисалициловая кислота.
Соединение общей формулы [6b] может быть получено, например, путем защиты фенольной гидроксильной группы соединения общей формулы [6a] способом, описанным в W. Greene, et al., Protective Groups in Organic Synthesis, 4th Edition, pp. 370-424, 2007 (John Wiley & Sons, Inc.).
Способ получения F
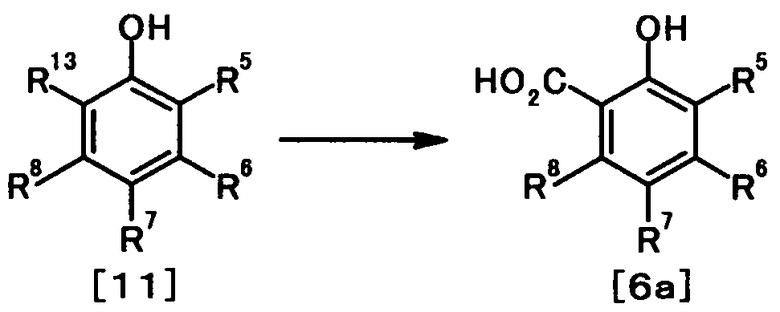
где R13 представляет собой защищенную карбоксильную группу; и R5, R6, R7 и R8 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [11] известны, например, метил-2-гидрокси-4-йодбензоат и метил-2-гидрокси-5-изопропоксибензоат.
Соединение общей формулы [6a] может быть получено в соответствии со Способом получения 4 путем снятия карбоксилзащитной группы с соединения общей формулы [11].
Способ получения G
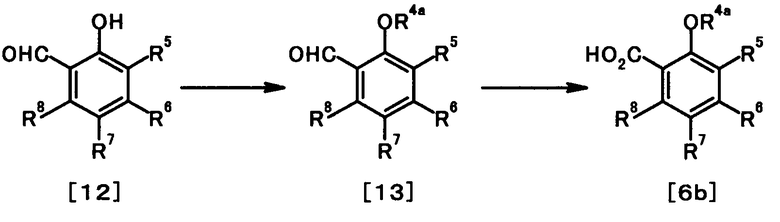
где R4a, R5, R6, R7 и R8 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [12] известны, например, 7-гидрокси-2,3-дигидробензо[1,4]диоксин-6-карбальдегид и 3-формил-4-гидроксифенэтилацетат.
(G-1)
Соединение общей формулы [13] может быть получено в соответствии со Способом получения Е путем защиты фенольной гидроксильной группы соединения общей формулы [12].
(G-2)
Соединение общей формулы [6b] может быть получено путем осуществления взаимодействия соединения общей формулы [13] с окислителем в присутствии или в отсутствие кислоты и в присутствии или в отсутствие соли.
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, галоидзамещенные углеводороды, ароматические углеводороды, ацетонитрил и пиридин. Указанные вещества могут быть использованы в виде смеси.
Примеры кислоты, используемой в случае необходимости в этой реакции, включают неорганические кислоты, такие как соляная кислота и серная кислота; и органические кислоты, такие как уксусная кислота. Количество в молях используемой кислоты может быть 1-1000-кратным по отношению к количеству в молях соединения общей формулы [13].
Примеры соли, используемой в случае необходимости в этой реакции, включают дигидрофосфат натрия, сульфат магния, сульфат аммония и хлорид магния. Количество в молях используемой соли может быть 1-50-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [13].
Примеры окислителя, используемого в этой реакции, включают хроматы, такие как дихромат натрия и оксид хрома(VI); перманганаты, такие как перманганат калия, перманганат бария, перманганат кальция и перманганат магния; раствор перекиси водорода; и хлорит натрия. Указанные вещества могут быть использованы в виде смеси. Количество в молях используемого окислителя может быть 1-50-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [13].
Эта реакция обычно может проводиться при температуре от 0 до 150°C, предпочтительно от 40 до 130°C, в течение от 30 минут до 48 часов.
Способ получения H
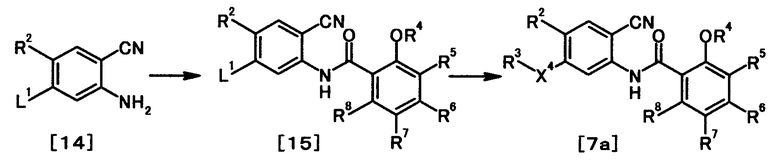
где R2, R3, R4, R5, R6, R7, R8, X4 и L1 имеют те же значения, что и представленные выше.
В качестве соединения общей формулы [14] известен, например, 2-амино-4-хлорбензонитрил.
(H-1)
Соединение общей формулы [15] может быть получено в соответствии со Способом получения 3 путем ацилирования соединения общей формулы [14].
(H-2)
Если X4 представляет собой связующий элемент, то соединение общей формулы [7a] может быть получено в соответствии со Способом получения 1 путем осуществления взаимодействия соединения общей формулы [15] с соединением общей формулы [3a] или [3b].
(H-3)
Если X4 представляет собой атом кислорода или необязательно защищенную иминогруппу, то соединение общей формулы [7a] может быть получено в соответствии со Способом получения 2 путем осуществления взаимодействия соединения общей формулы [15] с соединением общей формулы [4a].
Способ получения I
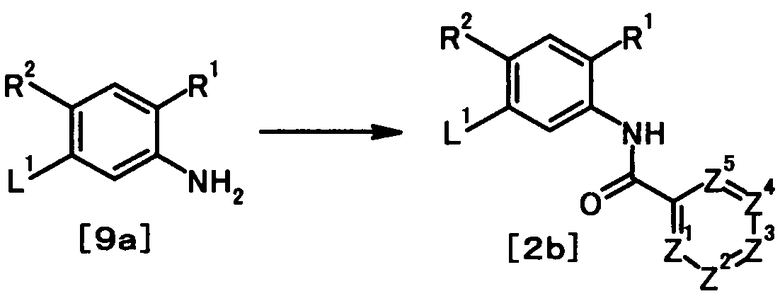
где R1, R2, Z1, Z2, Z3, Z4, Z5 и L1 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [9а] известны, например, метил-2-амино-4-бромбензоат и трет-бутил-2-амино-4-бромбензоат (Патентный Документ 1).
Соединение общей формулы [2b] может быть получено в соответствии со Способом получения 11 путем ацилирования соединения общей формулы [9a].
Способ получения J
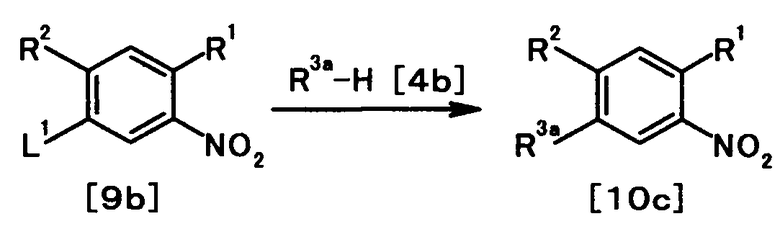
где R1, R2, R3a и L1 имеют те же значения, что и представленные выше.
Соединение общей формулы [10c] может быть получено в соответствии со Способом получения 9 путем осуществления взаимодействия соединения общей формулы [9b] с соединением общей формулы [4b].
Способ получения K
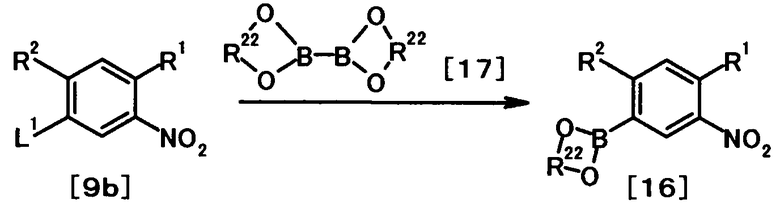
где R1, R2, R22 и L1 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [17] известны, например, бис(пинаколато)дибор, бис(неопентилглилято)дибор и бис(гексиленгликолято)дибор.
Соединение общей формулы [16] может быть получено в соответствии со Способом получения 7 путем осуществления взаимодействия соединения общей формулы [9b] с соединением общей формулы [17].
Способ получения L
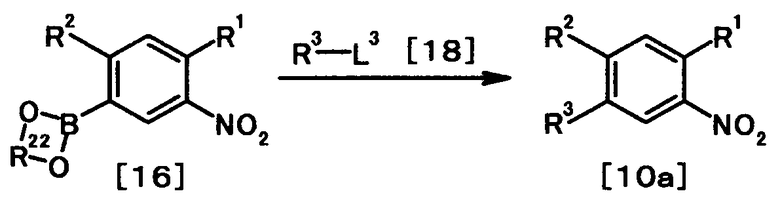
где L3 представляет собой уходящую группу; и R1, R2, R3 и R22 имеют те же значения, что и представленные выше.
В качестве соединений общей формулы [18] известны, например, 2-бромпиридин и 1-бром-2-(дифторметокси)бензол.
Соединение общей формулы [10a] может быть получено в соответствии со Способом получения 7 путем осуществления взаимодействия соединения общей формулы [16] с соединением общей формулы [18].
Способ получения M
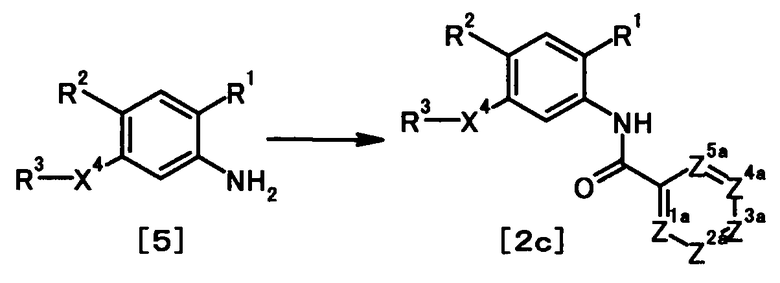
где R1, R2, R3, X4, Z1a, Z2a, Z3a, Z4a и Z5a имеют те же значения, что и представленные выше.
Соединение общей формулы [2c] может быть получено путем ацилирования соединения общей формулы [5]. Конкретные примеры способа включают способ с использованием галоидангидрида в присутствии или в отсутствие основания.
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают амиды, галоидзамещенные углеводороды, ароматические углеводороды, простые эфиры, ацетонитрил, кетоны, сложные эфиры, сульфолан и диметилсульфоксид. Указанные вещества могут быть использованы в виде смеси.
Галоидангидрид, используемый в этой реакции, может быть получен путем осуществления взаимодействия соединения, представленного общей формулой [8a]:
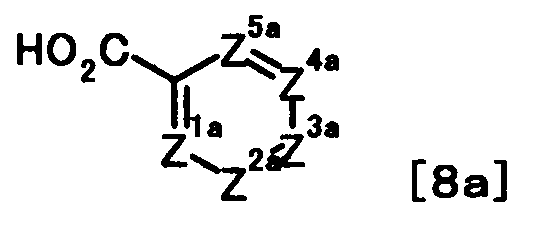
(в которой Z1a, Z2a, Z3a, Z4a и Z5a имеют те же значения, что и представленные выше), например, с тионилхлоридом или оксалилхлоридом.
Количество в молях используемого галоидангидрида может быть 1-50-кратным, предпочтительно 1-5-кратным, по отношению к количеству в молях соединения общей формулы [5].
Примеры основания, используемого в случае необходимости в этой реакции, включают неорганические основания, такие как бикарбонат натрия, карбонат натрия, карбонат калия и карбонат цезия; и органические основания, такие как триэтиламин, пиридин и N,N-диизопропилэтиламин.
Количество в молях используемого основания может быть 1-50-кратным, предпочтительно 1-5-кратным, по отношению к количеству в молях соединения общей формулы [5].
Эта реакция обычно может проводиться при температуре от -78 до 100°C, предпочтительно от 0 до 80°C, в течение от 10 минут до 24 часов.
Способ получения N
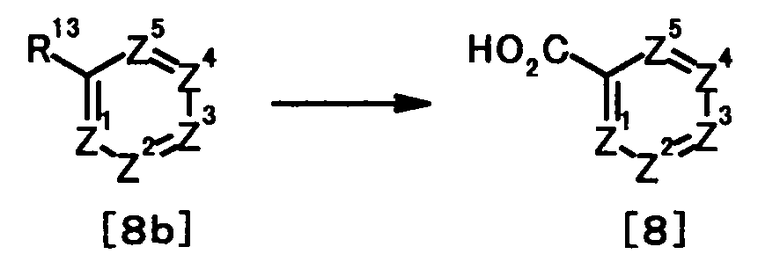
где R13, Z1, Z2, Z3, Z4 и Z5 имеют те же значения, что и представленные выше.
В качестве соединения общей формулы [8b] известен, например, метил-5-(фуран-3-ил)пиридин-3-карбоксилат.
Соединение общей формулы [8] может быть получено в соответствии со Способом получения 12 путем снятия карбоксилзащитной группы с соединения общей формулы [8b].
Способ получения O
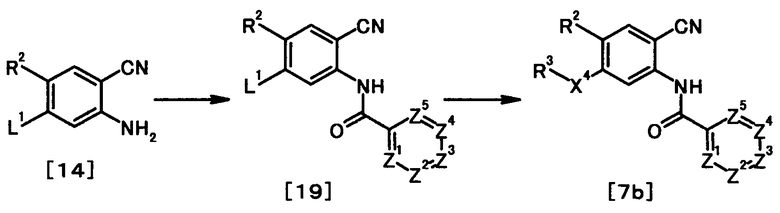
где R2, R3, Z1, Z2, Z3, Z4, Z5, X4 и L1 имеют те же значения, что и представленные выше.
В качестве соединения общей формулы [14] известен, например, 2-амино-4-хлорбензонитрил.
(O-1)
Соединение общей формулы [19] может быть получено в соответствии со Способом получения 11 путем ацилирования соединения общей формулы [14].
(O-2)
Если X4 представляет собой связующий элемент, то соединение общей формулы [7b] может быть получено в соответствии со Способом получения 7 путем осуществления взаимодействия соединения общей формулы [19] с соединением общей формулы [3a] или [3b].
(O-3)
Если X4 представляет собой атом кислорода или необязательно защищенную иминогруппу, то соединение общей формулы [7b] может быть получено в соответствии со Способом получения 8 путем осуществления взаимодействия соединения общей формулы [19] с соединением общей формулы [4a].
Способ получения P
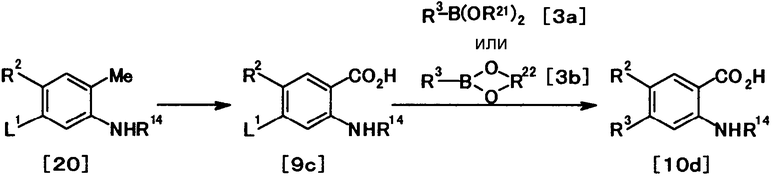
где R14 представляет собой аминозащитную группу; и R2, R3, R21, R22 и L1 имеют те же значения, что и представленные выше.
В качестве соединения общей формулы [20] известен, например, N-(5-бром-4-метокси-2-метилфенил)ацетамид.
(P-1)
Соединение общей формулы [9с] может быть получено путем осуществления взаимодействия соединения общей формулы [20] с окислителем в присутствии или в отсутствие кислоты или основания и в присутствии или в отсутствие соли.
Растворитель, используемый в этой реакции, конкретно не ограничивают при условии, что он не оказывает отрицательного влияния на реакцию, и его примеры включают воду, галоидзамещенные углеводороды, алифатические углеводороды и пиридин. Указанные вещества могут быть использованы в виде смеси.
Примеры кислоты, используемой в случае необходимости в этой реакции, включают неорганические кислоты, такие как, соляная кислота и серная кислота; и органические кислоты, такие как уксусная кислота.
Количество в молях используемой кислоты может быть 1-1000-кратным по отношению к количеству в молях соединения общей формулы [20].
Примеры основания, используемого в случае необходимости в этой реакции, включают неорганические основания, такие как гидроксид натрия и гидроксид калия; и органические основания, такие как пиридин.
Количество в молях используемого основания может быть 1-1000-кратным по отношению к количеству в молях соединения общей формулы [20].
Примеры соли, используемой в случае необходимости в этой реакции, включают сульфат магния, сульфат аммония и хлорид магния.
Количество в молях используемой соли может быть 1-50-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [20].
Примеры окислителя, используемого в этой реакции, включают хроматы, такие как оксид хрома(VI) и дихромат натрия; и перманганаты, такие как перманганат калия, перманганат бария, перманганат кальция и перманганат магния.
Количество в молях используемого окислителя может быть 1-50-кратным, предпочтительно 1-10-кратным, по отношению к количеству в молях соединения общей формулы [20].
Эта реакция обычно может проводиться при температуре от 0 до 150°C, предпочтительно от 40 до 130°C, в течение от 30 минут до 48 часов.
(P-2)
Соединение общей формулы [10d] может быть получено в соответствии со Способом получения 7 путем осуществления взаимодействия соединения общей формулы [9c] с соединением общей формулы [3a] или [3b].
Способ получения Q
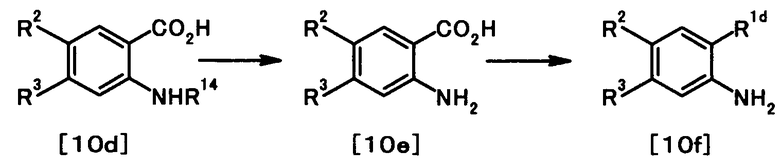
где R1d представляет собой защищенную карбоксильную группу; и R2, R3 и R14 имеют те же значения, что и представленные выше.
(Q-1)
Соединение общей формулы [10e] может быть получено путем снятия аминозащитной группы с соединения общей формулы [10d].
Снятие аминозащитной группы может быть осуществлено, например, способом, описанным в W. Greene, et al., Protective Groups in Organic Synthesis, 4th Edition, pp. 696-868, 2007 (John Wiley & Sons, Inc.).
(Q-2)
Соединение общей формулы [10f] может быть получено путем защиты карбоксильной группы соединения общей формулы [10e].
Защита карбоксильной группы может быть осуществлена, например, способом, описанным в W. Greene, et al., Protective Groups in Organic Synthesis, 4th Edition, pp. 533-643, 2007 (John Wiley & Sons, Inc.).
В соединениях, используемых в вышеописанных способах получения, соединение, способное образовывать соль, также может использоваться в виде соли. Примеры такой соли включают те же соли, что и соли соединения общей формулы [1].
Если для соединений, используемых в вышеописанных способах получения, существуют изомеры (например, оптический изомер, геометрический изомер и таутомер), то эти изомеры также могут быть использованы. Кроме того, если существуют сольваты, гидраты и различные формы кристаллического вещества, то эти сольваты, гидраты и различные формы кристаллического вещества также могут быть использованы. Кроме того, если соединения, используемые в вышеописанных способах получения, содержат заместители, которые могут быть защищены, например, в соединении, содержащем аминогруппу, гидроксильную группу или карбоксильную группу, то такую группу предварительно защищают обычной защитной группой, и после проведения реакции защитная группа может быть снята известным способом.
Соединения, полученные вышеописанными способами получения, или их соли могут быть преобразованы до других соединений или их солей посредством известных реакций, таких как конденсация, присоединение, окисление, восстановление, перегруппировка, замещение, галогенирование, дегидратация или гидролиз, или посредством подходящего сочетания таких реакций.
Если соединение по настоящему изобретению используют в качестве фармацевтического лекарства, то вспомогательные фармацевтические средства, обычно используемые для приготовления фармацевтического состава, такие как наполнитель, носитель и разбавитель, могут быть подходящим образом смешаны. Соединение может вводиться перорально или парентерально в виде таблетки, капсулы, порошка, сиропа, гранулы, пилюли, суспензии, эмульсии, раствора, порошкообразного препарата, суппозитория, глазных капель, капель в нос, ушных капель, пластыря, мази или инъецируемого раствора, в соответствии с общим способом. Способ введения, доза и частота введения могут быть подходящим образом подобраны в зависимости от возраста, веса и состояния пациента. Обычно, взрослому человеку может вводиться от 0,01 до 1000 мг/кг в сутки перорально или парентерально (например, путем инъекции, внутривенного капельного введения или введения в ректальный отдел) единовременно или несколькими кратными введениями.
Далее, применимость типичных соединений по настоящему изобретению будет описана в следующих Тестовых примерах.
Тестовый пример 1: Тест на ингибирование экспрессии мРНК, кодирующей α1 цепь коллагена типа I
Клетки линии WI-38 эмбриональных фибробластов легкого человека суспендировали в модифицированной по Дульбекко среде Игла, содержащей 10% эмбриональной бычьей сыворотки, и 7,5×104 клеток высевали в 12-луночный планшет и выращивали в течение 3 суток, или 1,5×105 клеток высевали и выращивали в течение 2 суток. После роста клеток до субконфлюэнтного состояния питательную среду заменяли модифицированной по Дульбекко средой Игла, содержащей 0,4% эмбриональной бычьей сыворотки и 50 мкг/мл аскорбиновой кислоты, и далее выращивали клетки в течение 24 часов. Затем к ним добавляли тестируемое соединение и, спустя один час, добавляли TGF-β1 в конечной концентрации 1 нг/мл. Через двадцать четыре часа после добавления тотальную РНК экстрагировали из клеток с использованием набора для выделения РНК (SV Total RNA Isolation System, Promega), и синтезировали кДНК с использованием обратной транскриптазы (ReverTra Ace, TOYOBO). Уровень экспрессии мРНК, кодирующей α1 цепь коллагена типа I, анализировали с помощью прибора для проведения ПЦР в масштабе реального времени (ABI PRISM 7700 Sequence Detection System, Applied Biosystems) по методу проведения ПЦР в реальном времени с использованием премикс-реагента для ПЦР в масштабе реального времени (SYBR Premix Ex Taq или SYBR Premix Ex Taq II (Perfect Real Time), TaKaRa). ПЦР проводили с разведенной кДНК в качестве матрицы, с использованием праймеров, специфичных к гену мРНК, кодирующей α1 цепь коллагена типа I, или гену GAPDH в качестве внутреннего стандарта, и измеряли продукт реакции. ПЦР проводили путем инкубации при 95°C в течение 10 секунд, 45 циклов денатурации при 95°C в течение 5 секунд и гибридизации/удлинения при 60°C в течение 30 секунд. Уровень экспрессии мРНК, кодирующей α1 цепь коллагена типа I, корректировали по GAPDH, и выражали в виде относительного значения, принимая уровень экспрессии, полученный в отсутствие тестируемого соединения, за 100%.
Результаты представлены в Таблицах 4a, 4b, и 4c.
Соединения, использованные в настоящем изобретении, показали превосходное ингибирующее действие на продукцию коллагена.
Тестовый пример 2: Легочный фиброз мышей, индуцированный блеомицином
Тест проводили с использованием самцов мышей C57BL/6N (Charles River Laboratories Japan, Inc.) в возрасте от 8 до 10,5 недель. Блеомицин (Nippon Kayaku Co., Ltd.) растворяли в физиологическом растворе в концентрации 1,0 или 1,5 мг/мл, и 2 мкл/г раствора интраназально вводили каждой мыши для индукции легочного фиброза. Тестируемое соединение растворяли или суспендировали в 10% водном растворе полиоксиэтиленового касторового масла (торговое название Cremophor EL) или в воде и перорально вводили в количестве 10 мг/кг дважды в сутки, от 14-х до 28-х суток со дня индукции. В контрольной группе тем же способом вводили 10% водный раствор полиоксиэтиленового касторового масла или воду. На 28-е сутки со дня индукции у каждой мыши извлекали легкое, и количественно измеряли содержание коллагена. Извлеченное легкое гомогенизировали в 0,5 моль/л водном растворе уксусной кислоты, содержащем смесь ингибиторов протеаз (Complete, EDTA-free, Roche Diagnostics) в количестве 1 таблетка/50 мл, и экстрагировали водорастворимый коллаген в присутствии 10 мг/мл пепсина (Sigma) в течение ночи. Содержание коллагена измеряли с помощью набора (Sircol Soluble Collagen assay kit, Biocolor).
Степень ингибирования определяли по следующей формуле:
Степень ингибирования (%) = [1 - (количество коллагена в легком в группе с введением тестируемого соединения)/(количество коллагена в легком в контрольной группе)]×100
Содержание коллагена в легком в группах с введением соединения Примеров 23a, 80a, 83a, 108a, 122a, 143a, 1b, 16b, 19b, 57b или 7c, было ниже на 30% или более по сравнению с таковым в контрольной группе.
Следует отметить, что соединения Примеров 23a, 1b и 7c использовали в виде их натриевых солей.
Кроме того, соединения Примеров 122a и 143a использовали в виде солей добавления соляной кислоты.
Тестовый пример 3: Тест на токсичность с повторным введением на крысах (пероральное введение, две недели)
В качестве тестируемых соединений использовали соединения Примеров 80a, 122a, 139a, 1b, 16b и 19b. Следует отметить, что соединения Примеров 80a и 1b использовали в виде натриевых солей.
Каждое из тестируемых соединений суспендировали в 0,5% растворе метилцеллюлозы или в дистиллированной воде для приготовления 100 мг/мл суспензии. Суспензию тестируемого соединения вводили перорально (10 мл/кг, тестируемое соединение: 1000 мг/кг) самцам крыс линии SD (в возрасте 6 недель, 5 крыс в каждой группе). В результате, на 14-е сутки после введения все крысы выжили.
Тестовый пример 4: Ингибирующее действие на метаболизирующий лекарства фермент печени человека (CYP2C9)
В качестве тестируемых соединений использовали соединения Примеров 80a, 83a, 108a, 117a, 123a, 128a, 139a, 142a и 143a. Следует отметить, что соединение Примера 80а использовали в виде свободного основания.
Использовали объединенные микросомы печени человека и толбутамид в качестве субстрата. Реакцию проводили в фосфатном буфере (100 ммоль/л, pH 7,4), и конечные концентрации в реакционной системе корректировали до 0,5 мг/мл белка микросом печени человека, 200 мкмоль/л субстрата, 1,55 ммоль/л окисленного никотинамидадениндинуклеотидфосфата (NADP+), 3,3 ммоль/л глюкоза-6-фосфата, 3,3 ммоль/л хлорида магния и 0,4 ед./мл глюкоза-6-фосфатдегидрогеназы (G6PDH). Конечную концентрацию каждого соединения в реакционном растворе корректировали до 0,08-50 мкг/мл. Указанные реакционные растворы подвергали реакции при 37°C в течение 30 минут. Реакцию останавливали добавлением равного количества ацетонитрила. После центрифугирования концентрацию метаболита толбутамида в надосадочной жидкости количественно измеряли с помощью ЖХ/МС/МС. Ингибирующую активность определяли как IC50. В качестве положительного контроля использовали сульфафеназол.
Соединения примеров 80a, 83a, 108a, 117a, 123a, 128a, 139a, 142a и 143a имели значение IC50 более 50 мкг/мл.
Соединения по настоящему изобретению обладали слабым ингибирующим действием на метаболизирующий лекарства фермент печени, а поэтому превосходны в плане безопасности.
Далее, настоящее изобретение будет описано со ссылкой на Справочные примеры и Примеры, но оно ими не ограничивается.
Соотношения при смешивании элюентов являются объемными соотношениями. Если иное не указано особо, то носитель при проведении колоночной хроматографии на силикагеле представляет собой Purif-Pack SI (60 мкм) производства Fuji Silysia Chemical Ltd.
Каждое из обозначений в каждом Примере имеет следующее значение: Ac: ацетил, Bn: бензил, Boc: трет-бутоксикарбонил, tBu: трет-бутил, Bz: бензоил, Et: этил, iPr: изопропил, Me: метил, Pr: пропил, и DMSO-d6: дейтерированный диметилсульфоксид.
Справочный пример 1a
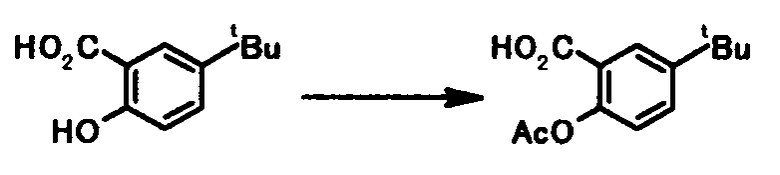
К раствору 5-трет-бутилсалициловой кислоты (0,054 г) в хлористом метилене (0,54 мл) последовательно добавляли пиридин (0,034 мл) и уксусный ангидрид (0,034 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 1 моль/л соляную кислоту и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,049 г 2-ацетокси-5-трет-бутилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,35 (9H, с), 2,35 (3H, с), 7,06 (1H, д, J=8,3 Гц), 7,63 (1H, дд, J=8,3, 2,4 Гц), 8,12 (1H, д, J=2,4 Гц).
Справочные примеры 2a-4a
Соединения, представленные в Таблице 5a, получали, как описано в Справочном примере 1a.
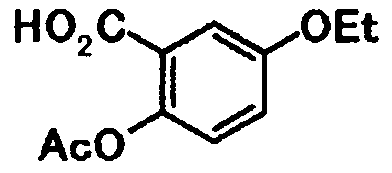
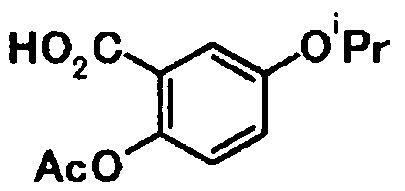
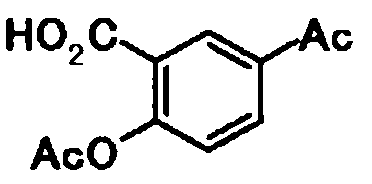
2-Ацетокси-5-этоксибензойная кислота
1H-ЯМР(DMSO-d6) δ: 1,33 (3H, т, J=7,0 Гц), 2,21 (3H, с), 4,06 (2H, кв, J=7,0 Гц), 7,09 (1H, д, J=8,8 Гц), 7,17 (1H, дд, J=8,8, 3,2 Гц), 7,37 (1H, д, J=3,2 Гц), 13,06-13,16 (1H, уширенный).
2-Ацетокси-5-изопропоксибензойная кислота
1H-ЯМР(DMSO-d6) δ: 1,27 (6H, д, J=6,1 Гц), 2,21 (3H, с), 4,56-4,68 (1H, м), 7,08 (1H, д, J=8,8 Гц), 7,16 (1H, дд, J=8,8, 2,9 Гц), 7,35 (1H, д, J=2,8 Гц).
2-Ацетокси-5-ацетилбензойная кислота
(1H-ЯМР(CDCl3) δ: 2,38 (3H, с), 2,66 (3H, с), 7,26 (1H, д, J=8,6 Гц), 8,23 (1H, дд, J=8,6, 2,2 Гц), 8,69 (1H, д, J=2,2 Гц).
Справочный пример 5a

Следующее соединение получали, как описано в Справочном примере 1a.
5-Ацетокси-2-(бензилокси)бензойная кислота
1H-ЯМР(CDCl3) δ: 2,30 (3H, с), 5,29 (2H, с), 7,13 (1H, д, J=8,9 Гц), 7,30 (1H, дд, J=8,9, 3,0 Гц), 7,38-7,48 (5H, м), 7,91 (1H, д, J=3,0 Гц), 10,60-10,95 (1H, м).
Справочный пример 6a

Следующее соединение получали, как описано в Справочном примере 1a.
4-Ацетокси-2-(бензилокси)бензойная кислота
1H-ЯМР(DMSO-d6) δ: 2,28 (3H, с), 5,17 (2H, с), 6,77-6,84 (1H, м), 7,04 (1H, д, J=1,7 Гц), 7,29-7,35 (1H, м), 7,36-7,43 (2H, м), 7,46-7,53 (2H, м), 7,72 (1H, д, J=8,5 Гц), 12,68 (1H, с).
Справочный пример 7a

К раствору метил-2-гидрокси-4-йодбензоата (2,5 г) в N,N-диметилацетамиде (20 мл) последовательно добавляли карбонат калия (1,9 г) и бензилбромид (1,2 мл), а затем перемешивали при 80°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 1 моль/л соляную кислоту и этилацетат. Органический слой разделяли, последовательно промывали 1 моль/л соляной кислотой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-80% гексан/этилацетат] с получением 3,3 г метил-2-(бензилокси)-4-йодбензоата в виде желтого маслянистого вещества.
1H-ЯМР(CDCl3) δ: 3,88 (3H, с), 5,15 (2H, с), 7,30-7,43 (5H, м), 7,47-7,51 (2H, м), 7,53 (1H, д, J=8,1 Гц).
Справочный пример 8a
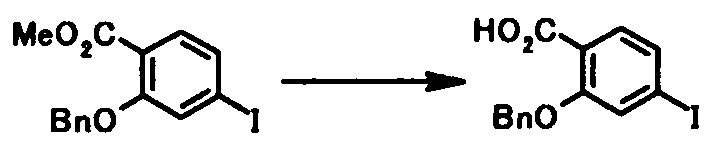
К раствору метил-2-(бензилокси)-4-йодбензоата (1,0 г) в смеси диоксана (5,0 мл) и метанола (5,0 мл) добавляли 2 моль/л водный раствор гидроксида натрия (4,1 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду. После корректировки значения pH до 2,5 добавлением 6,0 моль/л соляной кислоты при охлаждении на льду добавляли этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли гексан и диизопропиловый эфир, и собирали полученное твердое вещество путем фильтрования с получением 0,93 г 2-(бензилокси)-4-йодбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 5,27 (2H, с), 7,40-7,55 (7H, м), 7,88 (1H, д, J=8,3 Гц), 10,35-10,55 (1H, уширенный).
Справочный пример 9a
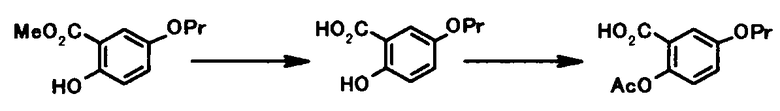
К раствору метил-2-гидрокси-5-пропоксибензоата (0,19 г) в диоксане (3,0 мл) добавляли 4 моль/л водный раствор гидроксида натрия (0,67 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут, а затем при 55-60°C в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты (15 мл). Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли гексан, и собирали твердое вещество путем фильтрования с получением 0,13 г 2-гидрокси-5-пропоксибензойной кислоты в виде светло-желтого твердого вещества.
К раствору полученной 2-гидрокси-5-пропоксибензойной кислоты (0,12 г) в смеси хлористого метилена (3,0 мл) и пиридина (0,12 мл) при охлаждении на льду добавляли уксусный ангидрид (0,069 мл), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. К реакционной смеси добавляли пиридин (0,050 мл) и уксусный ангидрид (0,058 мл), а затем перемешивали при комнатной температуре в течение 50 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку 1 моль/л соляную кислоту и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 65-55% гексан/этилацетат] с получением 0,091 г 2-ацетокси-5-пропоксибензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 0,98 (3H, т, J=7,4 Гц), 1,67-1,79 (2H, м), 2,21 (3H, с), 3,96 (2H, т, J=6,5 Гц), 7,09 (1H, д, J=8,8 Гц), 7,17 (1H, дд, J=8,8, 3,2 Гц), 7,37 (1H, д, J=3,2 Гц), 13,00-13,24 (1H, уширенный).
Справочный пример 10a
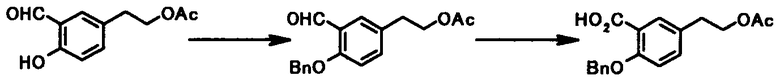
К раствору 3-формил-4-гидроксифенэтилацетата (0,40 г) в 2-бутаноне (4,0 мл) последовательно добавляли карбонат калия (0,40 г) и бензилбромид (0,25 мл), а затем нагревали с обратным холодильником в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-85% гексан/этилацетат] с получением 0,36 г 4-(бензилокси)-3-формилфенэтилацетата в виде бесцветного маслянистого вещества.
К раствору ацетонитрила (3,6 мл), содержащего полученный 4-(бензилокси)-3-формилфенэтилацетат (0,36 г), и воды (1,5 мл), содержащей двухводный дигидрофосфат натрия (0,51 г), при охлаждении на льду последовательно добавляли 30% раствор перекиси водорода (0,21 мл) и раствор хлорита натрия (0,18 г) в воде (0,5 мл), затем перемешивали при той же температуре в течение 10 минут, а затем при комнатной температуре в течение 1 часа. К реакционной смеси добавляли воду и хлористый метилен. После корректировки значения pH до 3,5 добавлением 6,0 моль/л соляной кислоты органический слой разделяли, последовательно промывали водой и насыщенным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления с получением 0,38 г 5-(2-ацетоксиэтил)-2-(бензилокси)бензойной кислоты в виде бесцветного маслянистого вещества.
1H-ЯМР(CDCl3) δ: 2,03 (3H, с), 2,94 (2H, т, J=6,8 Гц), 4,27 (2H, т, J=6,8 Гц), 5,29 (2H, с), 7,08 (1H, д, J=8,6 Гц), 7,38-7,46 (6H, м), 8,08 (1H, д, J=2,2 Гц), 10,75-10,90 (1H, уширенный).
Справочный пример 11a
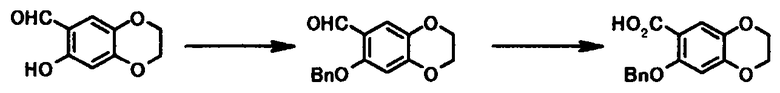
К раствору 7-гидрокси-2,3-дигидробензо[1,4]диоксин-6-карбальдегида (0,23 г) в N,N-диметилформамиде (2 мл) последовательно добавляли карбонат калия (0,27 г) и бензилбромид (0,17 мл), а затем перемешивали при 65°C в течение 2 часов. К реакционной смеси добавляли бензилбромид (0,077 мл), а затем перемешивали при 65°C в течение 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 75-60% гексан/этилацетат] с получением 0,32 г 7-(бензилокси)-2,3-дигидробензо[1,4]диоксин-6-карбальдегида в виде светло-желтого твердого вещества.
К суспензии полученного 7-(бензилокси)-2,3-дигидробензо[1,4]диоксин-6-карбальдегида (0,32 г) в ацетонитриле (1,6 мл) добавляли раствор двухводного дигидрофосфата натрия (0,50 г) в воде (0,60 мл), при охлаждении на льду последовательно добавляли 30% раствор перекиси водорода (0,20 мл) и раствор хлорита натрия (0,17 г) в воде (0,30 мл), затем перемешивали при той же температуре в течение 15 минут, а затем при комнатной температуре в течение 1 часа 30 минут. Значение pH реакционной смеси корректировали до 1,4 добавлением 1 моль/л соляной кислоты, и добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления с получением 0,34 г 7-(бензилокси)-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 4,17-4,24 (2H, м), 4,25-4,32 (2H, м), 5,11 (2H, с), 6,70 (1H, с), 7,23 (1H, с), 7,27-7,34 (1H, м), 7,34-7,42 (2H, м), 7,45-7,53 (2H, м), 12,34 (1H, с).
Справочный пример 12a
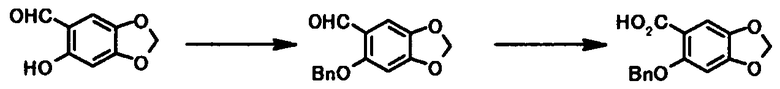
Следующее соединение получали, как описано в Справочном примере 11a.
6-(Бензилокси)бензо[1,3]диоксол-5-карбоновая кислота
1H-ЯМР(CDCl3) δ: 5,23 (2H, с), 6,04 (2H, с), 6,67 (1H, с), 7,38-7,46 (5H, м), 7,59 (1H, с), 10,64-10,96 (1H, уширенный).
Справочный пример 13a
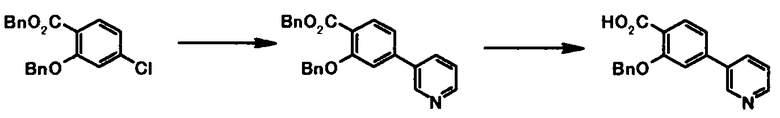
К раствору бензил-2-(бензилокси)-4-хлорбензоата (0,35 г) в толуоле (5,3 мл) добавляли 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (0,24 г), трикалийфосфат (0,46 г), ацетат палладия(II) (4,5 мг) и 2-дициклогексилфосфино-2',6'-диметоксибифенил (4,1 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (0,16 г), трикалийфосфат (0,25 г), ацетат палладия(II) (4,5 мг) и 2-дициклогексилфосфино-2',6'-диметоксибифенил (4,1 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов 30 минут. После охлаждения реакционной смеси до комнатной температуры к ней добавляли 10% водный раствор лимонной кислоты и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-50% гексан/этилацетат] с получением 0,35 г бензил-2-(бензилокси)-4-(пиридин-3-ил)бензоата.
К раствору полученного бензил-2-(бензилокси)-4-(пиридин-3-ил)бензоата (0,35 г) в смеси диоксана (1,8 мл) и метанола (1,8 мл) добавляли 2 моль/л водный раствор гидроксида натрия (1,3 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли воду. После корректировки значения pH до 4,5 добавлением 6 моль/л соляной кислоты к смеси добавляли этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,20 г 2-(бензилокси)-4-(пиридин-3-ил)бензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 5,35 (2H, с), 7,29-7,44 (4H, м), 7,50-7,57 (4H, м), 7,78 (1H, д, J=8,0 Гц), 8,12-8,18 (1H, м), 8,62 (1H, дд, J=4,6, 1,5 Гц), 8,96 (1H, д, J=2,2 Гц).
Справочные примеры 14a-16a
Соединения, представленные в Таблице 6a, получали, как описано в Справочном примере 13a.
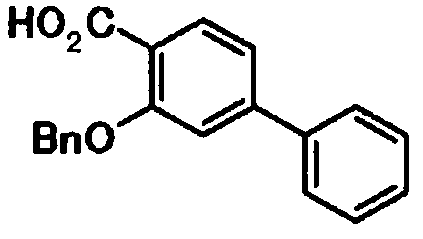
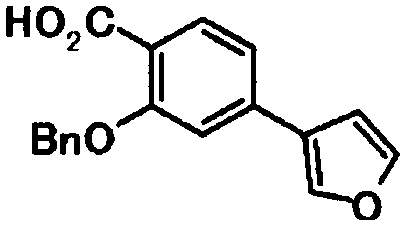
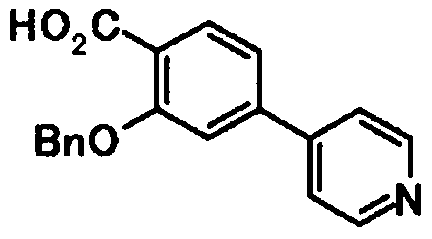
2-(Бензилокси)-4-фенилбензойная кислота
1H-ЯМР(CDCl3) δ: 5,37 (2H, с), 7,32 (1H, д, J=1,5 Гц), 7,34-7,52 (9H, м), 7,55-7,61 (2H, м), 8,26 (1H, д, J=8,0 Гц), 10,62-10,96 (1H, уширенный).
2-(Бензилокси)-4-(фуран-3-ил)бензойная кислота
1H-ЯМР(DMSO-d6) δ: 5,29 (2H, с), 7,04-7,07 (1H, м), 7,27 (1H, дд, J=8,1, 1,0 Гц), 7,28-7,36 (1H, м), 7,37-7,46 (3H, м), 7,52-7,58 (2H, м), 7,70 (1H, д, J=8,1 Гц), 7,76-7,81 (1H, м), 8,31-8,35 (1H, м), 12,56 (1H, с).
2-(Бензилокси)-4-(пиридин-4-ил)бензойная кислота
1H-ЯМР(DMSO-d6) δ: 5,36 (2H, с), 7,30-7,36 (1H, м), 7,38-7,47 (3H, м), 7,51-7,57 (2H, м), 7,59 (1H, д, J=1,5 Гц), 7,75-7,81 (3H, м), 8,66-8,71 (2H, м).
Справочный пример 17a
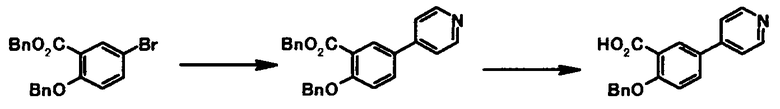
К раствору бензил-2-(бензилокси)-5-бромбензоата (0,40 г) в диметиловом эфире этиленгликоля (4 мл) добавляли воду (1,2 мл), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (0,25 г), бикарбонат натрия (0,21 г) и бис(трифенилфосфин)палладия(II) дихлорид (14 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (0,12 г), бикарбонат натрия (0,10 г), и бис(трифенилфосфин)палладия(II) дихлорид (14 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры к ней добавляли воду и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-45% гексан/этилацетат] с получением 0,29 г бензил-2-(бензилокси)-5-(пиридин-4-ил)бензоата в виде белого твердого вещества.
К раствору полученного бензил-2-(бензилокси)-5-(пиридин-4-ил)бензоата (0,29 г) в смеси диоксана (2,9 мл) и метанола (2,9 мл) добавляли 2 моль/л водный раствор гидроксида натрия (1,1 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду. После корректировки значения pH до 4 добавлением 6 моль/л соляной кислоты добавляли этилацетат. Реакционную смесь фильтровали для сбора твердого вещества с получением 0,19 г 2-(бензилокси)-5-(пиридин-4-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 5,30 (2H, с), 7,30-7,44 (4H, м), 7,49-7,55 (2H, м), 7,69-7,74 (2H, м), 7,96 (1H, дд, J=8,7, 2,6 Гц), 8,06 (1H, д, J=2,7 Гц), 8,58-8,64 (2H, м), 12,85-13,00 (1H, уширенный).
Справочный пример 18a
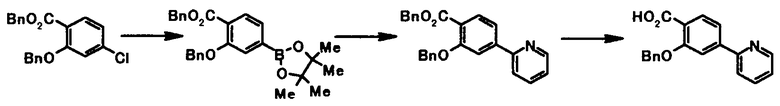
К раствору бензил-2-(бензилокси)-4-хлорбензоат (0,35 г) в диоксане (3,5 мл) добавляли бис(пинаколато)дибор (0,41 г), ацетат калия (0,25 г), трис(дибензилиденацетон)дипалладий(0) (46 мг) и 15% раствор трициклогексилфосфина в толуоле (0,25 мл), а затем перемешивали в атмосфере азота при комнатной температуре в течение 30 минут, а затем при 80°C в течение 5 часов 30 минут. После охлаждения реакционной смеси до комнатной температуры к ней добавляли трис(дибензилиденацетон)дипалладий(0) (46 мг) и 15% раствор трициклогексилфосфина в толуоле (0,25 мл), а затем перемешивали в атмосфере азота при 90°C в течение 8 часов. После охлаждения реакционной смеси до комнатной температуры к ней добавляли насыщенный водный раствор бикарбоната натрия и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 100-75% гексан/этилацетат] с получением бензил-2-(бензилокси)-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензоата.
К раствору полученного бензил-2-(бензилокси)-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензоата в диметиловом эфире этиленгликоля (3,5 мл) добавляли воду (1,1 мл), 2-бромпиридин (0,11 мл), карбонат натрия (0,21 г) и дихлорид бис(трифенилфосфин)палладия(II) (14 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. После охлаждения реакционной смеси до комнатной температуры к ней добавляли 2-бромпиридин (0,11 мл), карбонат натрия (0,21 г), и дихлорид бис(трифенилфосфин)палладия(II) (14 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. После охлаждения реакционной смеси до комнатной температуры к ней добавляли воду и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 100-80% гексан/этилацетат] с получением 0,18 г бензил-2-(бензилокси)-4-(пиридин-2-ил)бензоата.
К раствору полученного бензил-2-(бензилокси)-4-(пиридин-2-ил)бензоата (0,18 г) в смеси диоксана (0,9 мл) и метанола (0,9 мл) добавляли 2 моль/л водный раствор гидроксида натрия (0,69 мл), а затем перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду. После корректировки значения pH до 4 добавлением 6 моль/л соляной кислоты к смеси добавляли этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир гексан, и собирали твердое вещество путем фильтрования с получением 0,12 г 2-(бензилокси)-4-(пиридин-2-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 5,43 (2H, с), 7,31-7,36 (1H, м), 7,40-7,53 (5H, м), 7,69 (1H, дд, J=8,2, 1,5 Гц), 7,78-7,86 (2H, м), 8,02 (1H, д, J=1,5 Гц), 8,30 (1H, д, J=8,2 Гц), 8,71-8,77 (1H, м), 10,70-10,95 (1H, уширенный).
Справочные примеры 19a и 20a
Соединения, представленные в Таблице 7a, получали, как описано в Справочном примере 18a.
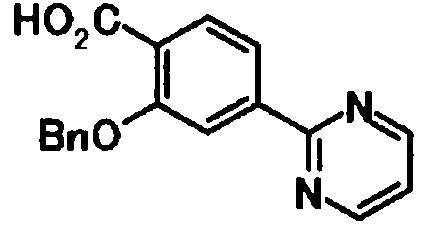
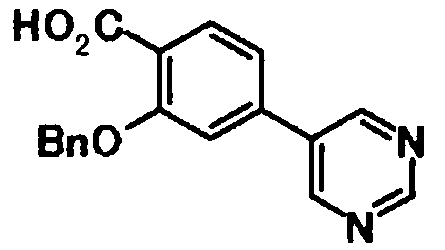
2-(Бензилокси)-4-(пиримидин-2-ил)бензойная кислота
1H-ЯМР(CDCl3) δ: 5,44 (2H, с), 7,30 (1H, т, J=4,9 Гц), 7,40-7,53 (5H, м), 8,27 (1H, дд, J=8,3, 1,2 Гц), 8,31-8,36 (2H, м), 8,87 (2H, д, J=4,9 Гц), 10,75-10,95 (1H, уширенный).
2-(Бензилокси)-4-(пиримидин-5-ил)бензойная кислота
1H-ЯМР(CDCl3) δ: 5,41 (2H, с), 7,28 (1H, д, J=1,7 Гц), 7,37 (1H, дд, J=8,1, 1,7 Гц), 7,42-7,50 (5H, м), 8,36 (1H, д, J=8,1 Гц), 8,94 (2H, с), 9,28 (1H, с), 10,55-10,70 (1H, уширенный).
Справочный пример 21a
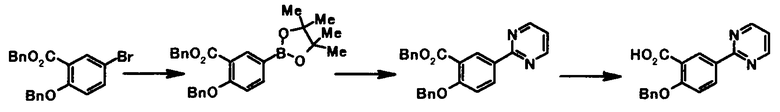
К бензил-2-(бензилокси)-5-бромбензоату (5,3 г) добавляли диоксан (53 мл), бис(пинаколато)дибор (4,0 г), ацетат калия (2,6 г) и комплекс (1,1'-бис(дифенилфосфино)ферроцен)палладия(II) дихлорида и хлористого метилена (0,54 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. После охлаждения реакционной смеси до комнатной температуры нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 98-82% гексан/этилацетат] с получением 5,3 г бензил-2-(бензилокси)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензоата.
К раствору полученного бензил-2-(бензилокси)-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензоата (1,8 г) в диметиловом эфире этиленгликоля (18 мл) добавляли воду (5,3 мл), 2-бромпиримидин (0,95 г), карбонат натрия (1,3 г) и дихлорид бис(трифенилфосфин)палладия(II) (0,14 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней дихлорид бис(трифенилфосфин)палладия(II) (0,14 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 5 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 80-50% гексан/этилацетат] с получением 1,4 г бензил-2-(бензилокси)-5-(пиримидин-2-ил)бензоата.
К раствору полученного бензил-2-(бензилокси)-5-(пиримидин-2-ил)бензоата (1,4 г) в смеси диоксана (10 мл) и метанола (5 мл) добавляли 2 моль/л водный раствор гидроксида натрия (8,6 мл), а затем перемешивали при комнатной температуре в течение 4 часов. К реакционной смеси добавляли толуол, и разделяли водный слой. После корректировки значения pH до 1 добавлением 6 моль/л соляной кислоты, твердое вещество собирали путем фильтрования с получением 0,65 г 2-(бензилокси)-5-(пиримидин-2-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 5,31 (2H, с), 7,30-7,45 (5H, м), 7,50-7,57 (2H, м), 8,50 (1H, дд, J=8,8, 2,4 Гц), 8,74 (1H, д, J=2,4 Гц), 8,88 (2H, д, J=4,9 Гц), 12,82-12,88 (1H, уширенный).
Справочный пример 22a
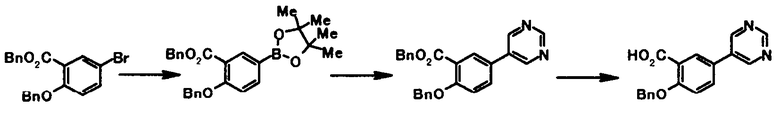
Следующее соединение получали, как описано в Справочном примере 21a.
2-(Бензилокси)-5-(пиримидин-5-ил)бензойная кислота
1H-ЯМР(DMSO-d6) δ: 5,30 (2H, с), 7,29-7,45 (4H, м), 7,49-7,55 (2H, м), 7,94 (1H, дд, J=8,8, 2,4 Гц), 8,04 (1H, д, J=2,4 Гц), 9,13 (2H, с), 9,15 (1H, с), 12,93 (1H, с).
Справочный пример 23a
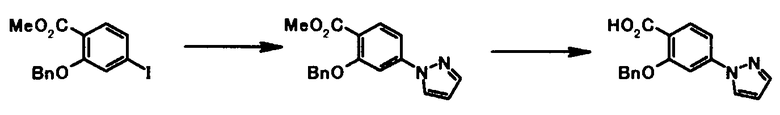
К раствору метил-2-(бензилокси)-4-йодбензоата (0,20 г) в диметилсульфоксиде (1,5 мл) добавляли 1H-пиразол (0,044 г), D-пролин (0,013 г), карбонат калия (0,15 г) и йодид меди(I) (0,010 г), а затем перемешивали в атмосфере азота при 90°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней D-пролин (0,013 г) и йодид меди(I) (0,010 г), а затем перемешивали в атмосфере азота при 100°C в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры к ней добавляли воду и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, последовательно промывали водой и насыщенным раствором хлорида натрия, и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 100-60% гексан/этилацетат] с получением 0,12 г метил-2-(бензилокси)-4-(1H-пиразол-1-ил)бензоата в виде белого твердого вещества.
К раствору полученного метил-2-(бензилокси)-4-(1H-пиразол-1-ил)бензоата (0,11 г) в смеси диоксана (1,1 мл) и метанола (1,1 мл) добавляли 2 моль/л водный раствор гидроксида натрия (0,56 мл), а затем перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду. После корректировки значения pH до 3 добавлением 6 моль/л соляной кислоты добавляли этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир гексан, и собирали твердое вещество путем фильтрования с получением 0,10 г 2-(бензилокси)-4-(1H-пиразол-1-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 5,39 (2H, с), 6,50-6,57 (1H, м), 7,34 (1H, дд, J=8,6, 2,2 Гц), 7,40-7,51 (5H, м), 7,74-7,80 (2H, м), 8,01 (1H, д, J=2,2 Гц), 8,28 (1H, д, J=8,6 Гц), 10,50-10,70 (1H, уширенный).
Справочный пример 24a
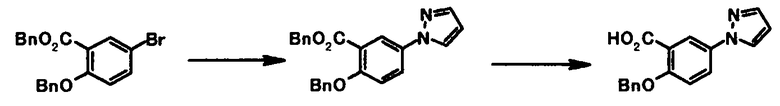
Следующее соединение получали, как описано в Справочном примере 23a.
2-(Бензилокси)-5-(1H-пиразол-1-ил)бензойная кислота
1H-ЯМР(CDCl3) δ: 5,35 (2H, с), 6,49 (1H, дд, J=2,4, 1,9 Гц), 7,23-7,28 (1H, м), 7,41-7,48 (5H, м), 7,72 (1H, д, J=1,4 Гц), 7,95-7,99 (1H, м), 8,07 (1H, дд, J=9,0, 2,9 Гц), 8,39 (1H, д, J=2,9 Гц), 10,75-10,90 (1H, уширенный).
Справочный пример 25a
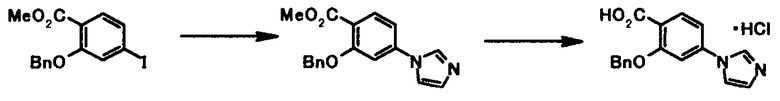
К раствору метил-2-(бензилокси)-4-йодбензоата (0,20 г) в диметилсульфоксиде (1 мл) добавляли 1H-имидазол (0,044 г), D-пролин (0,013 г), карбонат калия (0,15 г) и йодид меди(I) (0,010 г), а затем перемешивали в атмосфере азота при 90°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней диметилсульфоксид (0,5 мл), D-пролин (0,013 г) и йодид меди(I) (0,010 г), а затем перемешивали в атмосфере азота при 90°C в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры к ней добавляли воду и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, последовательно промывали водой и насыщенным раствором хлорида натрия, и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-20% гексан/этилацетат] с получением 0,13 г метил-2-(бензилокси)-4-(1H-имидазол-1-ил)бензоата в виде белого твердого вещества.
К раствору полученного метил-2-(бензилокси)-4-(1H-имидазол-1-ил)бензоата (0,13 г) в смеси диоксана (0,65 мл) и метанола (0,65 мл) добавляли 2 моль/л водный раствор гидроксида натрия (0,63 мл), а затем перемешивали при комнатной температуре в течение 3 часов. При охлаждении на льду к реакционной смеси добавляли 6 моль/л соляную кислоту (0,21 мл), и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли воду, и собирали твердое вещество путем фильтрования. К полученному твердому веществу добавляли диоксан (1 мл) и 4 моль/л раствор хлорводорода в диоксане (0,5 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,097 г гидрохлорида 2-(бензилокси)-4-(1H-имидазол-1-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 5,33 (2H, с), 7,32-7,38 (1H, м), 7,39-7,45 (2H, м), 7,47 (1H, дд, J=8,3, 2,0 Гц), 7,50-7,55 (2H, м), 7,71 (1H, д, J=2,0 Гц), 7,86-7,91 (2H, м), 8,35 (1H, с), 9,68 (1H, с).
Справочный пример 26a
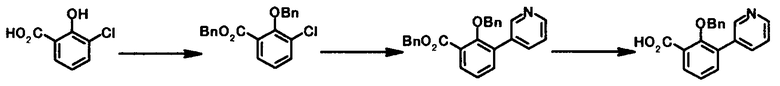
К 3-хлорсалициловой кислоте (0,92 г) последовательно добавляли N,N-диметилацетамид (9,2 мл), карбонат калия (2,2 г) и бензилбромид (1,4 мл), а затем перемешивали при 80°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем последовательно добавляли к ней карбонат калия (0,37 г) и бензилбромид (0,19 мл), а затем перемешивали при 80°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 100-95% гексан/этилацетат] с получением 1,8 г бензил-2-(бензилокси)-3-хлорбензоата в виде бесцветного маслянистого вещества.
К раствору полученного бензил-2-(бензилокси)-3-хлорбензоата (0,35 г) в толуоле (5,3 мл) добавляли 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (0,25 г), трикалийфосфат (0,47 г), ацетат палладия(II) (4,5 мг) и 2-дициклогексилфосфино-2',6'-диметоксибифенил (4,1 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 40 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (0,12 г), трикалийфосфат (0,23 г), ацетат палладия(II) (4,5 мг) и 2-дициклогексилфосфино-2',6'-диметоксибифенил (4,1 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов. После охлаждения реакционной смеси до комнатной температуры к ней добавляли 10% водный раствор лимонной кислоты и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-65% гексан/этилацетат] с получением 0,35 г бензил-2-(бензилокси)-3-(пиридин-3-ил)бензоата.
К раствору полученного бензил-2-(бензилокси)-3-(пиридин-3-ил)бензоата (0,35 г) в смеси диоксана (3,5 мл) и метанола (3,5 мл) добавляли 2 моль/л водный раствор гидроксида натрия (1,3 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 2 моль/л водный раствор гидроксида натрия (1,3 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду. После корректировки значения pH до 4,5 добавлением 6 моль/л соляной кислоты добавляли этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,18 г 2-(бензилокси)-3-(пиридин-3-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 4,61 (2H, с), 7,02-7,08 (2H, м), 7,22-7,39 (3H, м), 7,39-7,47 (2H, м), 7,62 (1H, дд, J=7,6, 2,0 Гц), 7,95 (1H, ддд, J=7,8, 2,0, 2,0 Гц), 8,21 (1H, дд, J=7,9, 1,8 Гц), 8,72 (1H, дд, J=4,9, 1,4 Гц), 8,85-8,90 (1H, м).
Справочный пример 27a
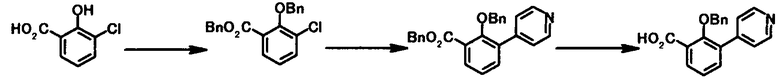
Следующее соединение получали, как описано в Справочном примере 26a.
2-(Бензилокси)-3-(пиридин-4-ил)бензойная кислота
1H-ЯМР(CDCl3) δ: 4,62 (2H, с), 7,03-7,08 (2H, м), 7,23-7,38 (3H, м), 7,43 (1H, дд, J=7,8, 7,8 Гц), 7,54-7,58 (2H, м), 7,62 (1H, дд, J=7,7, 1,8 Гц), 8,23 (1H, дд, J=7,9, 1,8 Гц), 8,74-8,78 (2H, м).
Справочный пример 28a
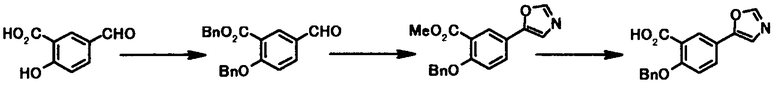
К раствору 5-формил-2-гидроксибензойной кислоты (0,50 г) в N,N-диметилформамиде (5 мл) последовательно добавляли карбонат калия (1,2 г) и бензилбромид (0,79 мл), затем перемешивали при комнатной температуре в течение 10 минут, а затем при 100°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, твердое вещество собирали путем фильтрования с получением 0,93 г бензил-2-(бензилокси)-5-формилбензоата в виде белого твердого вещества.
К суспензии полученного бензил-2-(бензилокси)-5-формилбензоата (0,93 г) в метаноле (9 мл) добавляли пара-толуолсульфонилметилизоцианид (0,55 г) и карбонат калия (0,39 г), а затем нагревали с обратным холодильником в течение 1 часа 40 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней пара-толуолсульфонилметилизоцианид (0,079 г) и карбонат калия (0,058 г), а затем нагревали с обратным холодильником в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 70-50% гексан/этилацетат] с получением 0,56 г метил-2-(бензилокси)-5-(оксазол-5-ил)бензоата в виде светло-желтого твердого вещества.
К раствору полученного метил-2-(бензилокси)-5-(оксазол-5-ил)бензоата (0,55 г) в диоксане (5 мл) добавляли 2 моль/л водный раствор гидроксида натрия (4,5 мл), а затем перемешивали при комнатной температуре в течение 2 часов 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду. После корректировки значения pH до 4,0 добавлением 6 моль/л соляной кислоты, твердое вещество собирали путем фильтрования с получением 0,46 г 2-(бензилокси)-5-(оксазол-5-ил)бензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 5,27 (2H, с), 7,28-7,45 (4H, м), 7,47-7,55 (2H, м), 7,65 (1H, с), 7,84 (1H, дд, J=8,7, 2,1 Гц), 7,99 (1H, д, J=2,1 Гц), 8,41 (1H, с), 12,95 (1H, с).
Справочный пример 29a
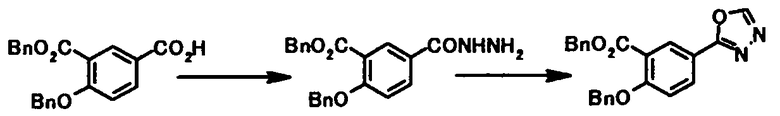
К суспензии 4-(бензилокси)-3-(бензилоксикарбонил)бензойной кислоты (0,50 г) в хлористом метилене (5 мл) добавляли N,N-диметилформамид (0,011 мл) и оксалилхлорид (0,18 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку диоксан (5 мл). Полученную смесь добавляли к раствору гидразина моногидрата (0,67 мл) в воде (6,7 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Твердое вещество собирали из реакционной смеси путем фильтрования, и промывали полученное твердое вещество этанолом с получением 0,38 г бензил-2-(бензилокси)-5-(гидразинокарбонил)бензоата в виде светло-желтого твердого вещества.
Суспензию полученного бензил-2-(бензилокси)-5-(гидразинокарбонил)бензоата (0,20 г) в триметил-ортоформиате (2 мл) нагревали с обратным холодильником в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли этилацетат и диизопропиловый эфир, и собирали 0,16 г твердого вещества путем фильтрования. Полученное твердое вещество (0,11 г) перемешивали при 200°C в течение 15 минут. Реакционную смесь охлаждали до комнатной температуры а затем очищали по методу колоночной хроматографии [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 90-50% гексан/этилацетат] с получением 0,079 г бензил-2-(бензилокси)-5-(1,3,4-оксадиазол-2-ил)бензоата в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 5,26 (2H, с), 5,38 (2H, с), 7,16 (1H, д, J=8,8 Гц), 7,30-7,47 (10H, м), 8,18 (1H, дд, J=8,8, 2,3 Гц), 8,43 (1H, с), 8,53 (1H, д, J=2,3 Гц).
Справочный пример 30a

Следующее соединение получали, как описано в Справочном примере 8a.
2-(Бензилокси)-5-(1,3,4-оксадиазол-2-ил)бензойная кислота
1H-ЯМР(DMSO-d6) δ: 5,33 (2H, с), 7,30-7,37 (1H, м), 7,38-7,47 (3H, м), 7,49-7,55 (2H, м), 8,13 (1H, дд, J=8,8, 2,3 Гц), 8,28 (1H, д, J=2,3 Гц), 9,31 (1H, с).
Справочный пример 31a
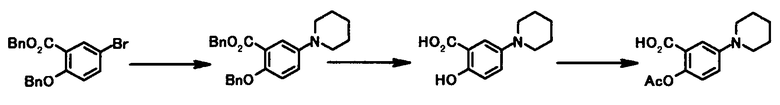
К раствору бензил-2-(бензилокси)-5-бромбензоата (3,0 г) в толуоле (30 мл) добавляли пиперидин (1,1 мл), карбонат цезия (4,9 г), трис(дибензилиденацетон)дипалладий(0) (0,069 г), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (0,18 г) и ацетат палладия(II) (0,034 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней пиперидин (0,37 мл), карбонат цезия (1,2 г), трис(дибензилиденацетон)дипалладий(0) (0,069 г), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (0,18 г) и ацетат палладия(II) (0,034 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 5 часов 30 минут. После охлаждения реакционной смеси до комнатной температуры к ней добавляли воду и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-80% гексан/этилацетат] с получением 2,4 г бензил-2-(бензилокси)-5-(пиперидин-1-ил)бензоата в виде светло-желтого твердого вещества.
К раствору полученного бензил-2-(бензилокси)-5-(пиперидин-1-ил)бензоата (2,2 г) в смеси диоксана (11 мл), этилацетата (17 мл) и метанола (5,5 мл), добавляли 10% палладированый уголь (1,1 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли тетрагидрофуран, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 1,1 г 2-гидрокси-5-(пиперидин-1-ил)бензойной кислоты в виде светло-желтого твердого вещества.
К полученной 2-гидрокси-5-(пиперидин-1-ил)бензойной кислоте (0,90 г) последовательно добавляли хлористый метилен (9,0 мл), пиридин (0,82 мл) и уксусный ангидрид (0,46 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, и экстрагировали водный слой этилацетатом. Органический слой и экстракт объединяли, полученную смесь последовательно промывали водой и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,55 г 2-ацетокси-5-(пиперидин-1-ил)бензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,55-1,63 (2H, м), 1,67-1,77 (4H, м), 2,31 (3H, с), 3,15-3,22 (4H, м), 6,99 (1H, д, J=8,8 Гц), 7,11-7,20 (1H, м), 7,60 (1H, д, J=2,9 Гц).
Справочный пример 32a

К раствору метил 2,4-дигидроксибензоата (0,25 г) в N,N-диметилацетамиде (5 мл) добавляли карбонат калия (0,31 г) и 1-(метилсульфонил)пиперидин-4-ила метансульфонат (0,46 г), а затем перемешивали при 90°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней йодид натрия (0,045 г), а затем перемешивали при 90°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней карбонат калия (0,10 г) и 1-(метилсульфонил)пиперидин-4-ила метансульфонат (0,12 г), а затем перемешивали при 90°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-60% гексан/этилацетат] с получением 0,19 г метил-2-гидрокси-4-((1-(метилсульфонил)пиперидин-4-ил)окси)бензоата в виде белого твердого вещества.
К раствору полученного метил-2-гидрокси-4-((1-(метилсульфонил)пиперидин-4-ил)окси)бензоата (0,19 г) в смеси диоксана (0,95 мл) и метанола (0,95 мл) добавляли 2 моль/л водный раствор гидроксида натрия (0,87 мл), а затем перемешивали при комнатной температуре в течение 3 часов. К реакционной смеси добавляли 2 моль/л водный раствор гидроксида натрия (0,58 мл), а затем нагревали с обратным холодильником в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду. После корректировки значения pH до 3 добавлением 6 моль/л соляной кислоты добавляли этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления с получением 0,18 г 2-гидрокси-4-((1-(метилсульфонил)пиперидин-4-ил)окси)бензойной кислоты в виде белого твердого вещества.
При охлаждении на льду к суспензии полученной 2-гидрокси-4-((1-(метилсульфонил)пиперидин-4-ил)окси)бензойной кислоты (0,18 г) в хлористом метилене (1,8 мл) последовательно добавляли пиридин (0,12 мл) и уксусный ангидрид (0,065 мл), а затем перемешивали при комнатной температуре в течение 1 часа. При охлаждении на льду к реакционной смеси последовательно добавляли пиридин (0,023 мл) и уксусный ангидрид (0,016 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 1 моль/л соляную кислоту и этилацетат. Органический слой разделяли, последовательно промывали 1 моль/л соляной кислотой, водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,18 г 2-ацетокси-4-((1-(метилсульфонил)пиперидин-4-ил)окси)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,97-2,13 (4H, м), 2,34 (3H, с), 2,82 (3H, с), 3,27-3,47 (4H, м), 4,59-4,67 (1H, м), 6,63 (1H, д, J=2,5 Гц), 6,84 (1H, дд, J=8,8, 2,5 Гц), 8,07 (1H, д, J=8,8 Гц).
Справочный пример 33a
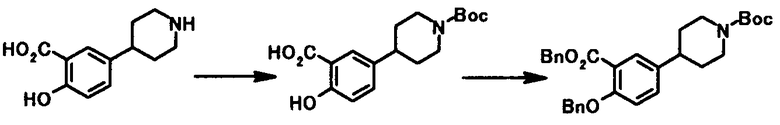
К 2-гидрокси-5-(пиперидин-4-ил)бензойной кислоте (1,6 г) добавляли 2 моль/л водный раствор гидроксида натрия (25 мл) и (ди-трет-бутил)дикарбонат (2,1 г), а затем перемешивали при комнатной температуре в течение 19 часов. Значение pH реакционной смеси корректировали до 3,0 добавлением 10% водного раствора лимонной кислоты, а затем собирали твердое вещество путем фильтрования. К раствору полученного твердого вещества в N,N-диметилацетамиде (20 мл) последовательно добавляли карбонат калия (2,6 г) и бензилбромид (1,6 мл), а затем перемешивали при 55°C в течение 1 часа 45 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле (AB., KP-Sil, элюент: 97-80% хлороформ/метанол), а затем очищали по методу колоночной хроматографии [Biotage AB, KP-Sil, элюент: 95-80% гексан/этилацетат], с получением 0,42 г трет-бутил-4-(4-(бензилокси)-3-(бензилоксикарбонил)фенилпиперидин-1-карбоксилата в виде бесцветного маслянистого вещества.
1H-ЯМР(CDCl3) δ: 1,48 (9H, с), 1,50-1,65 (2H, м), 1,72-1,83 (2H, м), 2,54-2,66 (1H, м), 2,68-2,86 (2H, м), 4,14-4,32 (2H, м), 5,14 (2H, с), 5,35 (2H, с), 6,96 (1H, д, J=8,6 Гц), 7,21-7,45 (11H, м), 7,67 (1H, д, J=2,4 Гц).
Справочный пример 34a
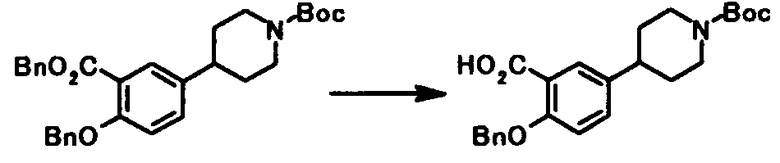
Следующее соединение получали, как описано в Справочном примере 8a.
2-(Бензилокси)-5-(1-(трет-бутоксикарбонил)пиперидин-4-ил)бензойная кислота
1H-ЯМР(DMSO-d6) δ: 1,34-1,50 (2H, м), 1,41 (9H, с), 1,67-1,79 (2H, м), 2,60-2,90 (3H, м), 3,97-4,13 (2H, м), 5,17 (2H, с), 7,11 (1H, д, J=8,6 Гц), 7,27-7,42 (4H, м), 7,44-7,52 (3H, м), 12,62 (1H, с).
Справочный пример 35a

К раствору трет-бутил-4-бром-2-нитробензоата (3,0 г) в диметиловом эфире этиленгликоля (30 мл) добавляли воду (9,0 мл), карбонат натрия (2,6 г), 2-метоксифенилбороновую кислоту (1,8 г) и дихлорид бис(трифенилфосфин)палладия(II) (0,14 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 99-91% гексан/этилацетат] с получением 3,3 г трет-бутил-4-(2-метоксифенил)-2-нитробензоата в виде светло-желтого маслянистого вещества.
1H-ЯМР(CDCl3) δ: 1,58 (9H, с), 3,83 (3H, с), 6,99-7,04 (1H, м), 7,04-7,10 (1H, м), 7,32 (1H, дд, J=7,6, 1,7 Гц), 7,40 (1H, ддд, J=8,3, 7,6, 1,7 Гц), 7,73-7,77 (1H, м), 7,78 (1H, дд, J=7,9, 1,6 Гц), 8,01 (1H, д, J=1,0 Гц).
Справочный пример 36a
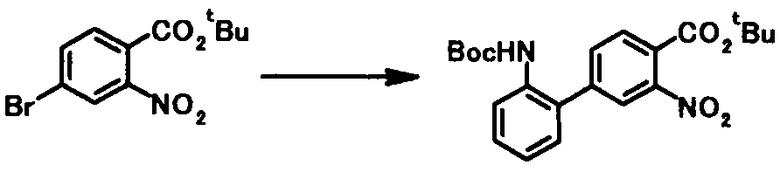
К раствору трет-бутил-4-бром-2-нитробензоата (0,15 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,6 мл), карбонат натрия (0,16 г), трет-бутил-2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенилкарбамат (0,19 г) и тетракис(трифенилфосфин)палладий(0) (29 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 91-80% гексан/этилацетат] с получением 0,21 г трет-бутил-4-(2-(трет-бутоксикарбониламино)фенил)-2-нитробензоата в виде желтого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,46 (9H, с), 1,60 (9H, с), 6,14-6,22 (1H, уширенный), 7,16-7,23 (2H, м), 7,38-7,45 (1H, м), 7,67 (1H, дд, J=8,1, 1,7 Гц), 7,84 (1H, д, J=8,1 Гц), 7,85 (1H, д, J=1,7 Гц), 7,96 (1H, д, J=8,5 Гц).
Справочный пример 37a

Следующее соединение получали, как описано в Справочном примере 36a.
Метил-4-(фуран-2-ил)-2-нитробензоат
1H-ЯМР(CDCl3) δ: 3,92 (3H, с), 6,55 (1H, дд, J=3,4, 1,7 Гц), 6,87 (1H, д, J=3,4 Гц), 7,57 (1H, д, J=1,7 Гц), 7,80 (1H, д, J=8,1 Гц), 7,88 (1H, дд, J=8,1, 1,7 Гц), 8,08 (1H, д, J=1,7 Гц).
Справочный пример 38a
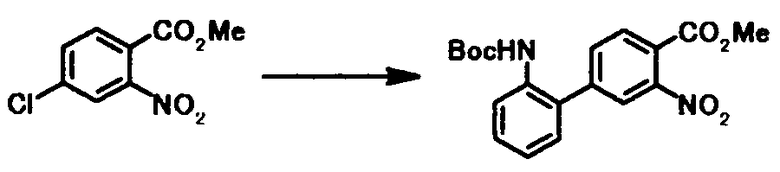
К раствору метил-4-хлор-2-нитробензоата (0,90 г) в диметиловом эфире этиленгликоля (10 мл) добавляли воду (3,0 мл), карбонат натрия (1,1 г), трет-бутил-2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенилкарбамат (1,5 г) и дихлорид бис(ди-трет-бутил(4-диметиламинофенил)фосфин)палладия(II) (30 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 1,5 г метил-4-(2-(трет-бутоксикарбониламино)фенил)-2-нитробензоата в виде светло-желтого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,45 (9H, с), 3,97 (3H, с), 6,13-6,21 (1H, уширенный), 7,17-7,25 (2H, м), 7,40-7,46 (1H, м), 7,71 (1H, дд, J=8,1, 1,7 Гц), 7,86 (1H, д, J=8,1 Гц), 7,91-7,97 (2H, м).
Справочный пример 39a

Следующее соединение получали, как описано в Справочном примере 38a.
Метил-4-(фуран-3-ил)-2-нитробензоат
1H-ЯМР(DMSO-d6) δ: 3,85 (3H, с), 7,15-7,22 (1H, м), 7,84 (1H, дд, J=1,7, 1,7 Гц), 7,92 (1H, д, J=8,1 Гц), 8,07 (1H, дд, J=8,1, 1,7 Гц), 8,30 (1H, д, J=1,7 Гц), 8,49-8,55 (1H, м).
Справочный пример 40a
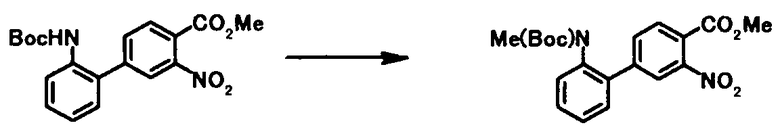
При охлаждении на льду к раствору метил-4-(2-(трет-бутоксикарбониламино)фенил)-2-нитробензоата (1,3 г) в N,N-диметилформамиде (15 мл) добавляли 60% гидрид натрия (0,21 г), а затем перемешивали при комнатной температуре в течение 10 минут. Затем, при охлаждении на льду к смеси добавляли метилйодид (0,32 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли воду, 10% водный раствор лимонной кислоты и диэтиловый эфир. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 1,1 г метил-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)-2-нитробензоата в виде светло-желтого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,17-1,43 (9H, м), 2,94-3,08 (3H, м), 3,94 (3H, с), 7,24-7,31 (1H, м), 7,33-7,41 (2H, м), 7,42-7,49 (1H, м), 7,60-7,72 (1H, м), 7,80 (1H, д, J=7,8 Гц), 7,89 (1H, д, J=1,5 Гц).
Справочный пример 41a
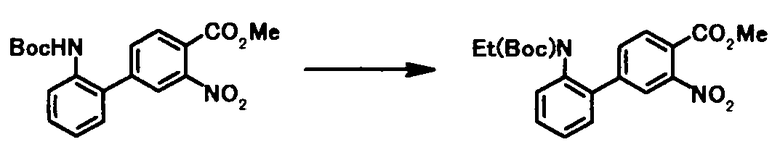
Следующее соединение получали, как описано в Справочном примере 40a.
Метил-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)-2-нитробензоат
1H-ЯМР(CD3OD) δ: 1,06 (3H, т, J=7,1 Гц), 1,22-1,45 (9H, м), 2,85-3,05 (1H, м), 3,50-3,70 (1H, м), 3,91 (3H, с), 7,26-7,39 (1H, м), 7,42-7,54 (3H, м), 7,72-7,80 (1H, м), 7,88 (1H, д, J=7,8 Гц), 7,90-7,98 (1H, м).
Справочный пример 42a
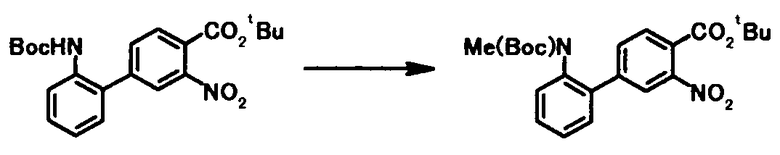
К раствору трет-бутил-4-(2-(трет-бутоксикарбониламино)фенил)-2-нитробензоата (0,27 г) в ацетоне (4,0 мл) добавляли карбонат калия (0,16 г) и диметилсульфат (0,094 мл), а затем нагревали с обратным холодильником в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат], а затем очищали по методу колоночной хроматографии [элюент: 91-85% гексан/этилацетат] с получением 0,061 г трет-бутил-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)-2-нитробензоата в виде бесцветного маслянистого вещества.
1H-ЯМР(DMSO-d6) δ: 0,99-1,28 (9H, м), 1,51 (9H, м), 3,00-3,11 (3H, м), 7,39-7,54 (4H, м), 7,74 (1H, д, J=8,3 Гц), 7,83-7,94 (2H, м).
Справочный пример 43a
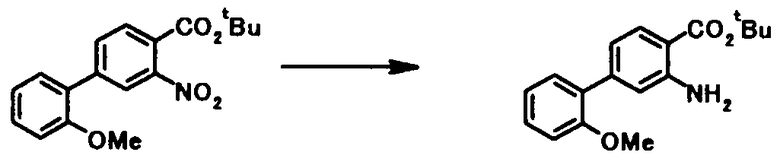
К раствору трет-бутил-4-(2-метоксифенил)-2-нитробензоата (3,3 г) в смеси 2-пропанола (40 мл), воды (10 мл) и уксусной кислоты (2,6 мл) последовательно добавляли формиат натрия (2,7 г) и 10% палладированый уголь (0,65 г), а затем нагревали с обратным холодильником в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 99-91% гексан/этилацетат] с получением 3,0 г трет-бутил-2-амино-4-(2-метоксифенил)бензоата в виде белого маслянистого вещества.
1H-ЯМР(CDCl3) δ: 1,59 (9H, с), 3,80 (3H, с), 5,65-5,78 (2H, уширенный), 6,77-6,83 (2H, м), 6,97 (1H, д, J=8,0 Гц), 7,01 (1H, дд, J=7,4, 7,4 Гц), 7,27-7,36 (2H, м), 7,81-7,87 (1H, м).
Справочный пример 44a
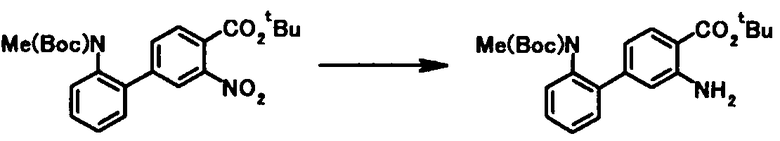
К раствору трет-бутил-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)-2-нитробензоата (0,057 г) в смеси этилацетата (2,5 мл) и метанола (2,5 мл) добавляли 10% палладированый уголь (0,011 г). Смесь перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 0,048 г трет-бутил-2-амино-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)бензоата в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 1,02-1,38 (9H, м), 1,54 (9H, с), 2,83-3,05 (3H, м), 6,44 (1H, дд, J=8,2, 1,3 Гц), 6,56-6,74 (3H, м), 7,26-7,43 (4H, м), 7,61-7,70 (1H, м).
Справочные примеры 45a и 46a
Соединения, представленные в таблице 8a, получали, как описано в Справочном примере 44a.
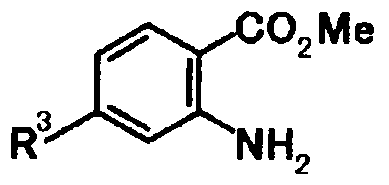
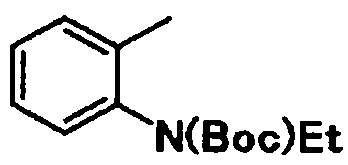
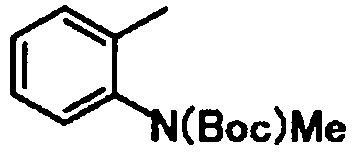
Метил-2-амино-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)бензоат
1H-ЯМР(CD3OD) δ: 0,96-1,11 (3H, м), 1,24-1,50 (9H, м), 2,77-2,95 (1H, м), 3,45-3,75 (1H, м), 3,86 (3H, с), 6,56 (1H, дд, J=8,3, 1,7 Гц), 6,73 (1H, д, J=1,7 Гц), 7,17-7,27 (1H, м), 7,33-7,42 (3H, м), 7,75-7,83 (1H, м).
Метил-2-амино-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)бензоат
1H-ЯМР(CDCl3) δ: 1,21-1,49 (9H, м), 2,80-3,04 (3H, м), 3,89 (3H, с), 6,60-6,72 (2H, м), 7,17-7,23 (1H, м), 7,24-7,40 (3H, м), 7,83-7,91 (1H, м).
Справочный пример 47a

К суспензии метил-4-(фуран-2-ил)-2-нитробензоата (0,14 г) в этаноле (2,1 мл) добавляли воду (0,56 мл), хлорид аммония (18 мг) и порошковое железо (94 мг), а затем нагревали с обратным холодильником в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней хлорид аммония (18 мг), порошковое железо (31 мг) и воду (0,28 мл), а затем нагревали с обратным холодильником в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли насыщенный водный раствор бикарбоната натрия и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 99-95% гексан/этилацетат] с получением 78 мг метил-2-амино-4-(фуран-2-ил)бензоата в виде светло-желтого твердого вещества.
1H-ЯМР(CDCl3) δ: 3,88 (3H, с), 5,72-5,86 (2H, уширенный), 6,49 (1H, дд, J=3,3, 1,8 Гц), 6,72 (1H, д, J=3,3 Гц), 6,94 (1H, дд, J=8,5, 1,7 Гц), 6,99 (1H, д, J=1,7 Гц), 7,47-7,51 (1H, м), 7,86 (1H, д, J=8,5 Гц).
Справочный пример 48a

Следующее соединение получали, как описано в Справочном примере 47a.
Метил-2-амино-4-(фуран-3-ил)бензоат
1H-ЯМР(DMSO-d6) δ: 3,78 (3H, с), 6,61-6,70 (2H, уширенный), 6,80 (1H, дд, J=8,6, 1,7 Гц), 6,84 (1H, дд, J=1,8,0,7 Гц), 6,97 (1H, д, J=1,7 Гц), 7,70 (1H, д, J=8,6 Гц), 7,76 (1H, дд, J=1,8, 1,7 Гц), 8,15-8,19 (1H, м).
Справочный пример 49a
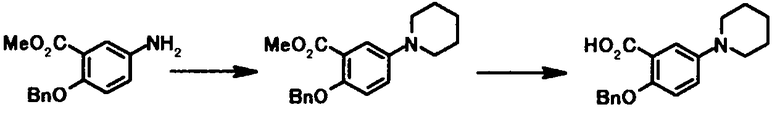
К раствору метил-5-амино-2-(бензилокси)бензоата (4,6 г) в N,N-диметилформамиде (23 мл) последовательно добавляли карбонат калия (5,1 г) и 1,5-дибромпентан (2,5 мл), а затем перемешивали при 50-55°C в течение 1 часа, при 55-60°C в течение 1 часа, при 70°C в течение 1 часа 30 минут, а затем при 75-80°C в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-65% гексан/этилацетат] с получением 4,3 г метил-2-(бензилокси)-5-(пиперидин-1-ил)бензоата в виде светло-желтого маслянистого вещества.
К раствору полученного метил-2-(бензилокси)-5-(пиперидин-1-ил)бензоата (4,3 г) в диоксане (45 мл) добавляли 4 моль/л водный раствор гидроксида натрия (9,8 мл), а затем перемешивали при комнатной температуре в течение 1 часа, а затем при 50-55°C в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры значение pH реакционной смеси корректировали до 6,3 добавлением уксусной кислоты, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли воду, и собирали твердое вещество путем фильтрования с получением 3,7 г 2-(бензилокси)-5-(пиперидин-1-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,52-1,62 (2H, м), 1,65-1,76 (4H, м), 3,08-3,16 (4H, м), 5,23 (2H, с), 7,03 (1H, д, J=9,0 Гц), 7,08-7,16 (1H, м), 7,36-7,45 (5H, м), 7,75 (1H, д, J=3,2 Гц).
Справочный пример 50a
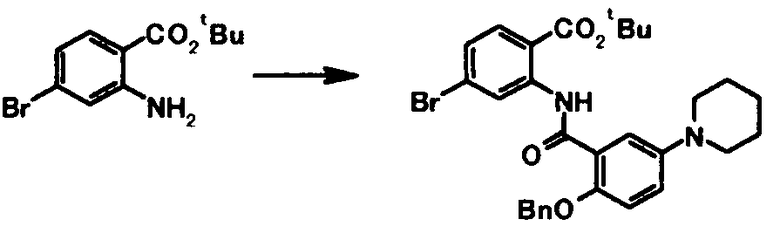
При охлаждении на льду к раствору 2-(бензилокси)-5-(пиперидин-1-ил)бензойной кислоты (2,5 г) в смеси хлористого метилена (25 мл) и N,N-диметилформамида (0,050 мл) добавляли оксалилхлорид (0,96 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (25 мл). Затем, при охлаждении на льду полученную смесь добавляли к раствору трет-бутил-2-амино-4-бромбензоата (2,0 г) в смеси пиридина (0,89 мл) и хлористого метилена (20 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 80-70% гексан/этилацетат] с получением 3,8 г трет-бутил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-бромбензоата в виде желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 1,44-1,54 (2H, м), 1,46 (9H, с), 1,57-1,66 (4H, м), 2,99-3,08 (4H, м), 5,39 (2H, с), 7,04-7,14 (2H, м), 7,21-7,34 (3H, м), 7,38-7,50 (4H, м), 7,86-7,92 (1H, м), 9,00-9,05 (1H, м), 12,17 (1H, с).
Справочный пример 51a
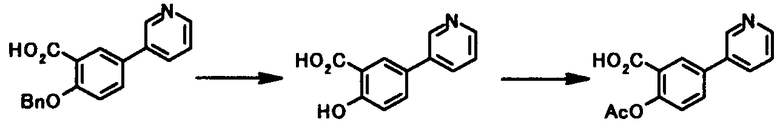
К 2-(бензилокси)-5-(пиридин-3-ил)бензойной кислоте (0,31 г) добавляли трифторуксусную кислоту (6,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этилацетат. Твердое вещество собирали путем фильтрования с получением 2-гидрокси-5-(пиридин-3-ил)бензойной кислоты в виде белого твердого вещества.
К полученной 2-гидрокси-5-(пиридин-3-ил)бензойной кислоте последовательно добавляли хлористый метилен (5,0 мл), пиридин (0,25 мл) и уксусный ангидрид (0,19 мл), а затем нагревали с обратным холодильником в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней пиридин (0,082 мл) и уксусный ангидрид (0,095 мл), а затем нагревали с обратным холодильником в течение 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 99-93% хлороформ/метанол] с получением 0,035 г 2-ацетокси-5-(пиридин-3-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 2,28 (3H, с), 7,35 (1H, д, J=8,4 Гц), 7,52 (1H, дд, J=8,0, 4,8 Гц), 8,00 (1H, дд, J=8,4, 2,4 Гц), 8,13 (1H, ддд, J=8,0, 2,2, 1,8 Гц), 8,19 (1H, д, J=2,4 Гц), 8,62 (1H, дд, J=4,8, 1,8 Гц), 8,92 (1H, д, J=2,2 Гц), 13,10-13,60 (1H, уширенный).
Справочный пример 52a
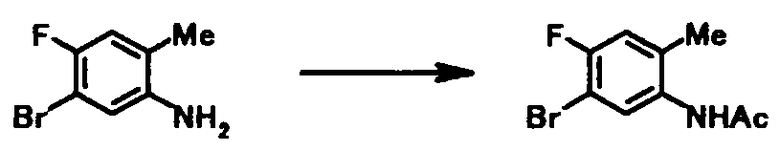
К раствору 5-бром-4-фтор-2-метиланилина (1,74 г) в хлористом метилене (17 мл) последовательно добавляли пиридин (1,0 мл) и ацетилхлорид (0,67 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли воду, 1 моль/л соляную кислоту и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Гексан добавляли к полученному остатку, и собирали твердое вещество путем фильтрования с получением 1,83 г N-(5-бром-4-фтор-2-метилфенил)ацетамида в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 2,06 (3H, с), 2,18 (3H, с), 7,27 (1H, д, J=9,5 Гц), 7,74 (1H, д, J=6,8 Гц), 9,38 (1H, с).
Справочный пример 53a

При нагревании с обратным холодильником к раствору N-(5-бром-4-метокси-2-метилфенил)ацетамида (1,0 г) в смеси воды (10 мл), трет-бутилового спирта (10 мл) и сульфата магния (0,79 г) добавляли перманганат калия (0,98 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 6 часов 20 минут. После охлаждения реакционной смеси до комнатной температуры нерастворимые вещества удаляли путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и этилацетат. Водный слой разделяли, и добавляли к нему 1 моль/л соляную кислоту (4 мл) и хлороформ. Органический слой разделяли, и экстрагировали водный слой хлороформом. Органический слой и экстракт объединяли, полученную смесь промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,36 г 2-(ацетамидо)-4-бром-5-метоксибензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 2,11 (3H, с), 3,86 (3H, с), 7,53 (1H, с), 8,68 (1H, с), 10,78 (1H, с).
Справочный пример 54a

Следующее соединение получали, как описано в Справочном примере 53a.
2-(Ацетамидо)-4-бром-5-фторбензойная кислота
1H-ЯМР(DMSO-d6) δ: 2,14 (3H, с), 7,81 (1H, д, J=9,3 Гц), 8,77 (1H, д, J=6,8 Гц), 10,92 (1H, с), 13,70-14,44 (1H, уширенный).
Справочный пример 55a
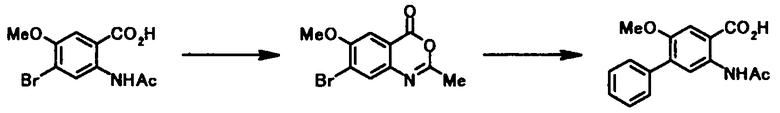
К раствору ди-трет-бутил-дикарбоната (0,75 г) в тетрагидрофуране (1,5 мл) при комнатной температуре добавляли 4-(диметиламино)пиридин (63 мг) и 2-(ацетамидо)-4-бром-5-метоксибензойную кислоту (0,49 г), а затем перемешивали при той же температуре в течение 4 часов и 15 минут. К реакционной смеси при комнатной температуре добавляли тетрагидрофуран (2 мл), а затем перемешивали при той же температуре в течение 3 суток. К реакционной смеси при комнатной температуре добавляли (ди-трет-бутил)дикарбонат (0,37 г), а затем перемешивали при той же температуре в течение 1 суток. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли гексан и диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,40 г 7-бром-6-метокси-2-метил-4H-3,1-бензоксазин-4-она в виде коричневого твердого вещества.
К суспензии полученного 7-бром-6-метокси-2-метил-4H-3,1-бензоксазин-4-она (0,40 г) в диметиловом эфире этиленгликоля (4 мл) добавляли воду (1,2 мл), фенилбороновую кислоту (0,22 г), карбонат натрия (0,38 г) и дихлорид бис(трифенилфосфин)палладия(II) (21 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Водный слой разделяли, и органический слой экстрагировали 2 моль/л водным раствором гидроксида натрия. Водный слой и экстракт объединяли. Значение pH полученной смеси корректировали до 1 добавлением 6 моль/л соляной кислоты, и добавляли этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,27 г 2-(ацетамидо)-5-метокси-4-фенилбензойной кислоты в виде желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 2,11 (3H, с), 3,78 (3H, с), 7,35-7,52 (5H, м), 7,57 (1H, с), 8,39 (1H, с), 10,79 (1H, с).
Справочный пример 56a
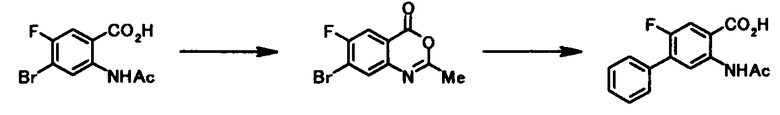
Следующее соединение получали, как описано в Справочном примере 55a.
2-(Ацетамидо)-5-фтор-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 2,15 (3H, с), 7,45-7,59 (5H, м), 7,79 (1H, д, J=11,2 Гц), 8,60 (1H, д, J=7,3 Гц), 10,93 (1H, с), 13,60-14,28 (1H, уширенный).
Справочный пример 57a
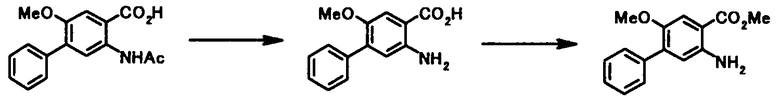
Раствор 2-(ацетамидо)-5-метокси-4-фенилбензойной кислоты (0,41 г) в смеси диоксана (1,2 мл) и концентрированной соляной кислоты (1,2 мл) нагревали с обратным холодильником в течение 3 часов 40 минут. После охлаждения реакционной смеси до комнатной температуры выпаривали растворитель в условиях пониженного давления, и добавляли к остатку воду. После корректировки значения pH до 7 добавлением 1 моль/л водного раствора гидроксида натрия к смеси добавляли хлороформ. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления с получением 2-амино-5-метокси-4-фенилбензойной кислоты в виде коричневого твердого вещества.
При охлаждении на льду к суспензии полученной 2-амино-5-метокси-4-фенилбензойной кислоты в метаноле (10 мл) добавляли концентрированную серную кислоту (1 мл), а затем нагревали с обратным холодильником в течение 6 часов. Реакционную смесь охлаждали до комнатной температуры и корректировали значение pH до 8,0 добавлением насыщенного водного раствора бикарбоната натрия, а затем добавляли к ней хлороформ. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли гексан, и собирали твердое вещество путем фильтрования с получением 0,24 г метил-2-амино-5-метокси-4-фенилбензоата в виде коричневого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 3,65 (3H, с), 3,82 (3H, с), 6,35 (2H, с), 6,78 (1H, с), 7,30 (1H, с), 7,32-7,49 (5H, м).
Справочный пример 58a
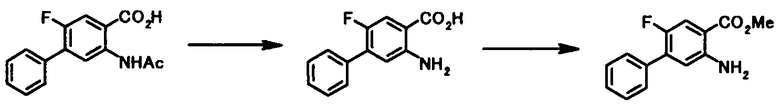
Следующее соединение получали, как описано в Справочном примере 57a.
Метил-2-амино-5-фтор-4-фенилбензоат
1H-ЯМР(CDCl3) δ: 3,90 (3H, с), 5,42-5,81 (2H, уширенный), 6,71 (1H, д, J=6,3 Гц), 7,36-7,47 (3H, м), 7,51-7,56 (2H, м), 7,63 (1H, д, J=11,5 Гц).
Справочный пример 59a
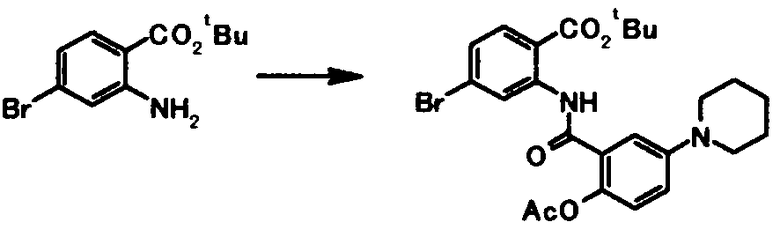
Следующее соединение получали, как описано в Справочном примере 50a.
трет-Бутил-2-(2-ацетокси-5-(пиперидин-1-ил)бензамидо)-4-бромбензоат
1H-ЯМР(DMSO-d6) δ: 1,52-1,67 (6H, м), 1,54 (9H, с), 2,19 (3H, с), 3,18-3,26 (4H, м), 7,09 (1H, д, J=9,0 Гц), 7,17 (1H, дд, J=8,5, 2,9 Гц), 7,32 (1H, д, J=2,9 Гц), 7,41-7,48 (1H, м), 7,89 (1H, д, J=8,5 Гц), 8,78 (1H, д, J=1,7 Гц), 11,47 (1H, с).
Справочный пример 60a
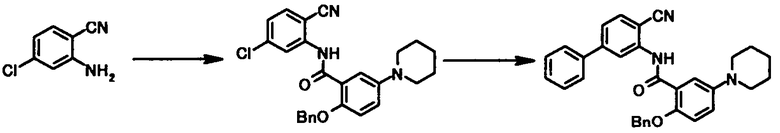
К суспензии 2-(бензилокси)-5-(пиперидин-1-ил)бензойной кислоты (0,56 г) в хлористом метилене (3,0 мл) последовательно добавляли N,N-диметилформамид (0,010 мл) и оксалилхлорид (0,21 мл), а затем перемешивали при комнатной температуре в течение 1 часа 20 минут. При охлаждении на льду реакционную смесь добавляли к раствору 2-амино-4-хлорбензонитрила (0,23 г) в смеси хлористого метилена (3,0 мл) и пиридина (0,30 мл), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 10% водный раствор лимонной кислоты и хлороформ Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 2-(бензилокси)-N-(5-хлор-2-цианофенил)-5-(пиперидин-1-ил)бензамида в виде желтого твердого вещества.
К суспензии полученного 2-(бензилокси)-N-(5-хлор-2-цианофенил)-5-(пиперидин-1-ил)бензамида в диметиловом эфире этиленгликоля (3,0 мл) добавляли воду (0,74 мл), фенилбороновую кислоту (0,12 г), карбонат натрия (0,21 г) и дихлорид бис(ди-трет-бутил(4-диметиламинофенил)фосфин)палладия(II) (3,0 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа. После охлаждения реакционной смеси до комнатной температуры к ней добавляли фенилбороновую кислоту (0,12 г), карбонат натрия (0,21 г), и дихлорид бис(ди-трет-бутил(4-диметиламинофенил)фосфин)палладия(II) (3,0 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 40 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней хлороформ и 10% водный раствор лимонной кислоты. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 90-50% гексан/этилацетат] с получением 0,32 г 2-(бензилокси)-N-(4-цианобифенил-3-ил)-5-(пиперидин-1-ил)бензамида в виде желтого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,50-1,59 (2H, м), 1,65-1,73 (4H, м), 3,07-3,12 (4H, м), 5,54 (2H, с), 6,92 (1H, д, J=9,0 Гц), 7,01 (1H, дд, J=9,0, 3,2 Гц), 7,26-7,50 (9H, м), 7,64-7,71 (3H, м), 7,87 (1H, д, J=3,2 Гц), 9,05 (1H, д, J=1,4 Гц), 11,08 (1H, с).
Справочный пример 61a
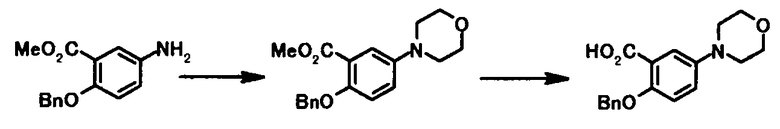
К раствору метил-5-амино-2-(бензилокси)бензоата (0,40 г) в N,N-диметилацетамиде (3,2 мл) последовательно добавляли карбонат калия (0,54 г), йодид калия (0,11 г), и бис(2-хлорэтил)эфир (0,22 мл), а затем перемешивали при 100°C в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 85-60% гексан/этилацетат] с получением 0,27 г метил-2-(бензилокси)-5-(морфолин-4-ил)бензоата в виде светло-желтого маслянистого вещества.
К раствору полученного метил-2-(бензилокси)-5-(морфолин-4-ил)бензоата (0,26 г) в этаноле (2,1 мл) добавляли 4 моль/л водный раствор гидроксида натрия (0,3 мл), а затем перемешивали при 50°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем последовательно добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,17 г 2-(бензилокси)-5-(морфолин-4-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 3,10-3,16 (4H, м), 3,82-3,89 (4H, м), 5,25 (2H, с), 7,04-7,13 (2H, м), 7,39-7,45 (5H, м), 7,73 (1H, д, J=2,9 Гц), 10,80-11,20 (1H, уширенный).
Справочный пример 62a
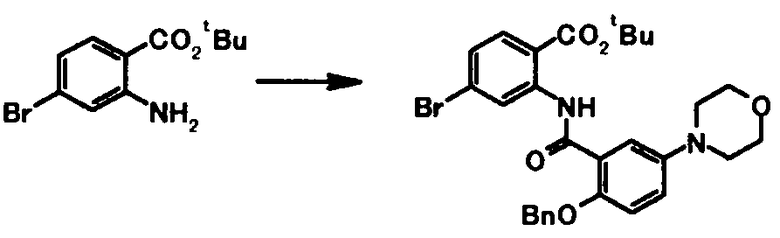
К раствору 2-(бензилокси)-5-(морфолин-4-ил)бензойной кислоты (11,4 г) в смеси тетрагидрофурана (57 мл) и N,N-диметилформамида (0,013 мл) добавляли оксалилхлорид (3,4 мл), затем перемешивали при комнатной температуре в течение 40 минут, а затем нагревали до температуры возгонки в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней тетрагидрофуран (23 мл), а затем нагревали с обратным холодильником в течение 30 минут. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку тетрагидрофуран (23 мл). Полученную смесь добавляли при охлаждении на льду к раствору трет-бутил-2-амино-4-бромбензоата (9,0 г) в смеси пиридина (6,7 мл) и тетрагидрофурана (45 мл), затем перемешивали при комнатной температуре в течение 30 минут, а затем при 50°C в течение 30 минут. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Нерастворимые вещества удаляли путем фильтрования, органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия, и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 90-60% гексан/этилацетат] с получением 13,8 г трет-бутил-2-(2-(бензилокси)-5-(морфолин-4-ил)бензамидо)-4-бромбензоата в виде светло-желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 1,46 (9H, с), 3,00-3,07 (4H, м), 3,69-3,77 (4H, м), 5,41 (2H, с), 7,09-7,17 (2H, м), 7,22-7,34 (3H, м), 7,40-7,50 (4H, м), 7,89 (1H, д, J=8,6 Гц), 9,03 (1H, д, J=2,0 Гц), 12,19 (1H, с).
Справочный пример 63a
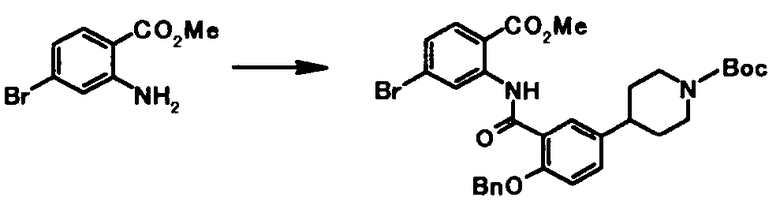
При охлаждении на льду к раствору 2-(бензилокси)-5-(1-(трет-бутоксикарбонил)пиперидин-4-ил)бензойной кислоты (0,93 г) в смеси хлористого метилена (9,0 мл) и N,N-диметилформамида (0,017 мл) добавляли оксалилхлорид (0,29 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (4,5 мл). Полученную смесь добавляли при охлаждении на льду к раствору метил-2-амино-4-бромбензоата (0,45 г) в смеси пиридина (0,40 мл) и хлористого метилена (9,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли хлороформ и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-70% гексан/этилацетат] с получением 0,65 г метил-2-(2-(бензилокси)-5-(1-(трет-бутоксикарбонил)пиперидин-4-ил)бензамидо)-4-бромбензоата в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 1,35-1,51 (2H, м), 1,41 (9H, с), 1,69-1,79 (2H, м), 2,65-2,90 (3H, м), 3,73 (3H, с), 4,00-4,12 (2H, м), 5,43 (2H, с), 7,18 (1H, д, J=8,8 Гц), 7,24-7,36 (3H, м), 7,38-7,48 (4H, м), 7,78 (1H, д, J=2,2 Гц), 7,90 (1H, д, J=8,6 Гц), 8,99 (1H, д, J=2,2 Гц), 12,00 (1H, с).
Справочный пример 64a
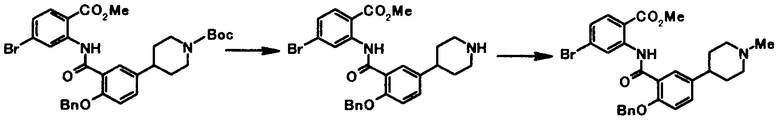
При охлаждении на льду к раствору метил-2-(2-(бензилокси)-5-(1-(трет-бутоксикарбонил)пиперидин-4-ил)бензамидо)-4-бромбензоата (0,65 г) в хлористом метилене (6,5 мл) добавляли трифторуксусную кислоту (1,3 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь добавляли при охлаждении на льду к насыщенному водному раствору бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором бикарбоната натрия и сушили над безводным сульфатом натрия. Растворитель выпаривали в условиях пониженного давления с получением 0,54 г метил-2-(2-(бензилокси)-5-(пиперидин-4-ил)бензамидо)-4-бромбензоата в виде белого твердого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-(пиперидин-4-ил)бензамидо)-4-бромбензоата (0,54 г) в тетрагидрофуране (5,4 мл) последовательно добавляли уксусную кислоту (0,12 мл), 37% водный раствор формальдегида (0,10 мл) и триацетоксиборгидрид натрия (0,54 г), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,48 г метил-2-(2-(бензилокси)-5-(1-метилпиперидин-4-ил)бензамидо)-4-бромбензоата в виде светло-желтого твердого вещества.
1H-ЯМР(CD3OD) δ: 1,70-1,91 (4H, м), 2,14-2,24 (2H, м), 2,34 (3H, с), 2,52-2,62 (1H, м), 2,97-3,05 (2H, м), 3,75 (3H, с), 5,43 (2H, с), 7,12 (1H, д, J=8,8 Гц), 7,22-7,40 (5H, м), 7,41-7,46 (2H, м), 7,89 (1H, д, J=2,4 Гц), 7,93 (1H, д, J=8,6 Гц), 9,09 (1H, д, J=2,0 Гц).
Справочный пример 1b
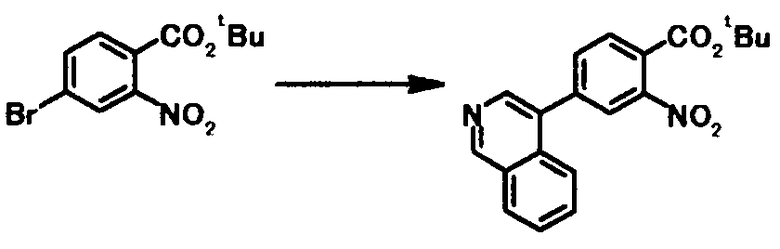
К раствору трет-бутил-4-бром-2-нитробензоата (5,0 г) в диметиловом эфире этиленгликоля (50 мл) добавляли воду (15 мл), карбонат натрия (4,6 г), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)изохинолин (5,1 г) и дихлорид бис(трифенилфосфин)палладия(II) (0,24 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и воду. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 85-75% гексан/этилацетат] с получением 5,8 г трет-бутил-4-(изохинолин-4-ил)-2-нитробензоата в виде коричневого маслянистого вещества.
1H-ЯМР(DMSO-d6) δ: 1,55 (9H, с), 7,76-7,83 (1H, м), 7,83-7,88 (2H, м), 7,99-8,02 (2H, м), 8,21 (1H, с), 8,28 (1H, д, J=8,0 Гц), 8,55 (1H, с), 9,44 (1H, с).
Справочный пример 2b
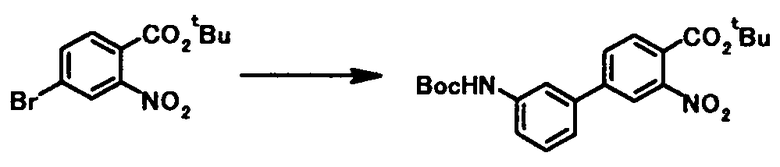
К раствору трет-бутил-4-бром-2-нитробензоата (0,15 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,6 мл), карбонат натрия (0,16 г), 3-(трет-бутоксикарбониламино)фенилбороновую кислоту (0,14 г) и тетракис(трифенилфосфин)палладий(0) (29 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-91% гексан/этилацетат] с получением 0,17 г трет-бутил-4-(3-(трет-бутоксикарбониламино)фенил)-2-нитробензоата в виде светло-желтого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,54 (9H, с), 1,58 (9H, с), 6,55-6,63 (1H, уширенный), 7,24-7,28 (1H, м), 7,33 (1H, д, J=8,6 Гц), 7,39 (1H, д, J=7,8 Гц), 7,74 (1H, с), 7,80 (1H, д, J=8,1 Гц), 7,84 (1H, дд, J=7,9, 1,6 Гц), 7,99 (1H, д, J=1,7 Гц).
Справочный пример 3b

Следующее соединение получали, как описано в Справочном примере 2b.
Метил-4-(фуран-2-ил)-2-нитробензоат
1H-ЯМР(CDCl3) δ: 3,92 (3H, с), 6,55 (1H, дд, J=3,4, 1,7 Гц), 6,87 (1H, д, J=3,4 Гц), 7,57 (1H, д, J=1,7 Гц), 7,80 (1H, д, J=8,1 Гц), 7,88 (1H, дд, J=8,1, 1,7 Гц), 8,08 (1H, д, J=1,7 Гц).
Справочный пример 4b
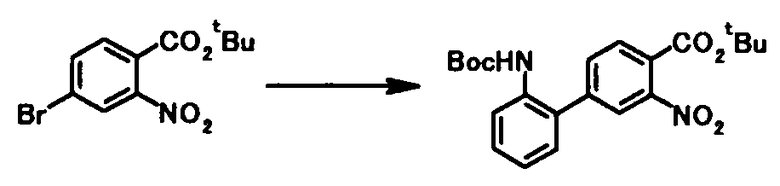
К раствору трет-бутил-4-бром-2-нитробензоата (0,15 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,6 мл), карбонат натрия (0,16 г), трет-бутил-2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенилкарбамат (0,19 г) и тетракис(трифенилфосфин)палладий(0) (29 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 91-80% гексан/этилацетат] с получением 0,21 г трет-бутил-4-(2-(трет-бутоксикарбониламино)фенил)-2-нитробензоата в виде желтого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,46 (9H, с), 1,60 (9H, с), 6,14-6,22 (1H, уширенный), 7,16-7,23 (2H, м), 7,38-7,45 (1H, м), 7,67 (1H, дд, J=8,1, 1,7 Гц), 7,84 (1H, д, J=8,1 Гц), 7,85 (1H, д, J=1,7 Гц), 7,96 (1H, д, J=8,5 Гц).
Справочный пример 5b
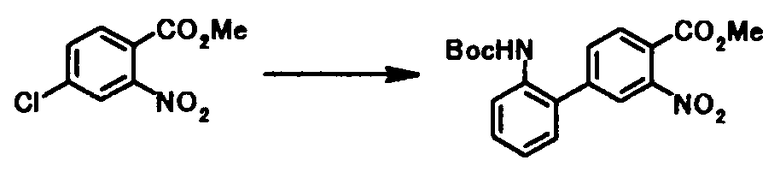
К раствору метил-4-хлор-2-нитробензоата (0,90 г) в диметиловом эфире этиленгликоля (10 мл) добавляли воду (3,0 мл), карбонат натрия (1,1 г), трет-бутил-2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенилкарбамат (1,5 г) и бис(ди-трет-бутил(4-диметиламинофенил)фосфин)палладия(II) дихлорид (30 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 1,5 г метил-4-(2-(трет-бутоксикарбониламино)фенил)-2-нитробензоата в виде светло-желтого твердого вещества.
1H-ЯМР(CDCl3): 1,45 (9H, с), 3,97 (3H, с), 6,13-6,22 (1H, уширенный), 7,17-7,25 (2H, м), 7,40-7,46 (1H, м), 7,71 (1H, дд, J=8,0, 1,7 Гц), 7,86 (1H, д, J=8,1 Гц), 7,91-7,97 (2H, м).
Справочный пример 6b
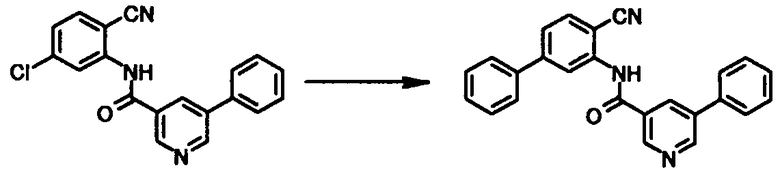
К суспензии N-(5-хлор-2-цианофенил)-5-фенилпиридин-3-карбоксамида (0,20 г) в толуоле (3,0 мл) добавляли фенилбороновую кислоту (88 мг), трикалийфосфат (0,28 г), 2-дициклогексилфосфино-2',6'-диметоксибифенил (2,5 мг) и ацетат палладия(II) (2,7 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 2-дициклогексилфосфино-2',6'-диметоксибифенил (2,5 мг) и ацетат палладия(II) (2,7 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 6 часов. После охлаждения реакционной смеси до комнатной температуры к ней добавляли этилацетат и 10% водный раствор лимонной кислоты, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,23 г N-(2-циано-5-фенилфенил)-5-фенилпиридин-3-карбоксамида в виде светло-желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,45-7,62 (6H, м), 7,75-7,83 (3H, м), 7,84-7,90 (2H, м), 7,96 (1H, д, J=1,7 Гц), 8,01 (1H, д, J=8,0 Гц), 8,65 (1H, дд, J=2,2, 2,2 Гц), 9,13-9,18 (2H, м), 11,01 (1H, с).
Справочный пример 7b
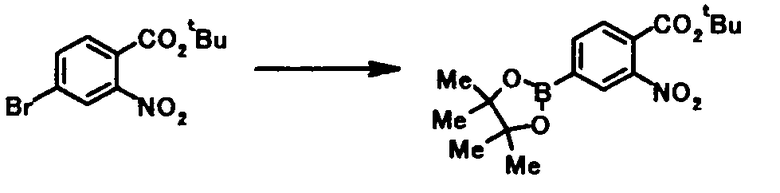
К раствору трет-бутил-4-бром-2-нитробензоат (2,0 г) в диоксане (20 мл) добавляли ацетат калия (2,0 г), бис(пинаколато)дибор (3,4 г) и комплекс (1,1'-бис(дифенилфосфино)ферроцен)палладия(II) дихлорида и хлористого метилена (0,27 г), а затем перемешивали в атмосфере азота при 95-100°C в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 80% гексан/этилацетат], а затем очищали по методу колоночной хроматографии [элюент: 95-90% гексан/этилацетат] с получением 2,0 г трет-бутил-2-нитро-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензоата в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,26 (12H, с), 1,36 (9H, с), 7,69 (1H, д, J=7,6 Гц), 7,99-8,06 (1H, м), 8,23-8,27 (1H, м).
Справочный пример 8b

Следующее соединение получали, как описано в Справочном примере 7b.
N,N-Диэтил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)анилин
1H-ЯМР(CDCl3) δ: 1,15 (6H, т, J=7,1 Гц), 1,33 (12H, с), 3,37 (4H, кв, J=7,1 Гц), 6,75-6,84 (1H, м), 7,07-7,17 (2H, м), 7,18-7,25 (1H, м).
Справочный пример 9b
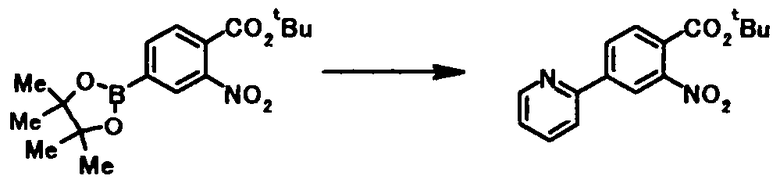
К раствору трет-бутил-2-нитро-4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензоата (1,0 г) в диметиловом эфире этиленгликоля (10 мл) добавляли воду (3 мл), карбонат натрия (0,76 г), 2-бромпиридин (0,42 мл) и тетракис(трифенилфосфин)палладий(0) (0,17 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 90-85% гексан/этилацетат] с получением 0,32 г трет-бутил-2-нитро-4-(пиридин-2-ил)бензоата в виде светло-желтого маслянистого вещества.
1H-ЯМР(CDCl3) δ: 1,59 (9H, с), 7,32-7,38 (1H, м), 7,78-7,87 (3H, м), 8,28 (1H, дд, J=8,1, 1,7 Гц), 8,50 (1H, д, J=1,7 Гц), 8,72-8,77 (1H, м).
Справочный пример 10b

Следующее соединение получали, как описано в Справочном примере 9b.
трет-Бутил-4-(2-(дифторметокси)фенил)-2-нитробензоат
1H-ЯМР(CDCl3): 1,59 (9H, с), 6,44 (1H, т, J=73,5 Гц), 7,24-7,37 (2H, м), 7,39-7,49 (2H, м), 7,74-7,82 (2H, м), 7,93-7,97 (1H, м).
Справочный пример 11b
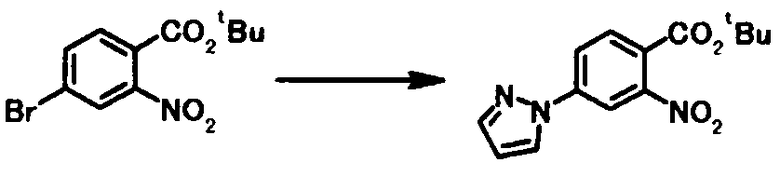
К раствору трет-бутил-4-бром-2-нитробензоата (0,50 г) в диметилсульфоксиде (5 мл) добавляли 1H-пиразол (0,14 г), карбонат калия (0,46 г), D-пролин (38 мг) и йодид меди(I) (32 мг), а затем перемешивали в атмосфере азота при 100°C в течение 3 часов. После охлаждения реакционной смеси до комнатной температуры к ней добавляли этилацетат и воду, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, последовательно промывали водой и насыщенным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 100-80% гексан/этилацетат] с получением 0,20 г трет-бутил-2-нитро-4-(1H-пиразол-1-ил)бензоата в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,57 (9H, с), 6,56 (1H, дд, J=2,6, 1,8 Гц), 7,79 (1H, д, J=1,8 Гц), 7,88 (1H, д, J=8,5 Гц), 7,95 (1H, дд, J=8,5, 2,1 Гц), 8,01 (1H, д, J=2,6 Гц), 8,15 (1H, д, J=2,1 Гц).
Справочный пример 12b

При охлаждении на льду к раствору трет-бутил-4-(3-(трет-бутоксикарбониламино)фенил)-2-нитробензоата (0,30 г) в тетрагидрофуране (5,0 мл) добавляли 60% гидрид натрия (43 мг), а затем перемешивали при той же температуре в течение 20 минут. К реакционной смеси при охлаждении на льду добавляли этилйодид (0,087 мл), затем перемешивали при той же температуре в течение 30 минут, а затем при комнатной температуре в течение 2 часов 40 минут. К реакционной смеси при комнатной температуре добавляли N,N-диметилформамид (3,0 мл), затем при охлаждении на льду к ней последовательно добавляли 60% гидрид натрия (14 мг) и этилйодид (0,058 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли воду и диэтиловый эфир, органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [элюент: 85-60% гексан/этилацетат] с получением 0,16 г трет-бутил-4-(3-((трет-бутоксикарбонил)(этил)амино)фенил)-2-нитробензоата в виде бесцветного маслянистого вещества.
1H-ЯМР(CDCl3) δ: 1,19 (3H, т, J=7,1 Гц), 1,46 (9H, с), 1,58 (9H, с), 3,73 (2H, кв, J=7,1 Гц), 7,26-7,32 (1H, м), 7,38-7,50 (3H, м), 7,80-7,83 (2H, м), 7,98 (1H, с).
Справочный пример 13b

При охлаждении на льду к раствору трет-бутил-4-(3-(трет-бутоксикарбониламино)фенил)-2-нитробензоат (0,17 г) в N,N-диметилформамиде (3,0 мл) добавляли 60% гидрид натрия (24 мг), затем перемешивали при той же температуре в течение 15 минут, а затем при комнатной температуре в течение 20 минут. К реакционной смеси при охлаждении на льду добавляли метилйодид (0,037 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли воду и диэтиловый эфир, органический слой разделяли, и экстрагировали водный слой диэтиловым эфиром. Органический слой и экстракт объединяли, полученную смесь последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 0,17 г трет-бутил-4-(3-((трет-бутоксикарбонил)(метил)амино)фенил)-2-нитробензоата в виде коричневого маслянистого вещества.
1H-ЯМР(CDCl3): 1,48 (9H, с), 1,58 (9H, с), 3,32 (3H, с), 7,30-7,36 (1H, м), 7,36-7,41 (1H, м), 7,42-7,53 (2H, м), 7,80-7,84 (2H, м), 7,99 (1H, с).
Справочный пример 14b

Следующее соединение получали, как описано в Справочном примере 13b.
Метил-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)-2-нитробензоат
1H-ЯМР(CD3OD): 1,06 (3H, т, J=7,1 Гц), 1,22-1,45 (9H, м), 2,85-3,05 (1H, уширенный), 3,50-3,70 (1H, уширенный), 3,91 (3H, с), 7,26-7,39 (1H, м), 7,42-7,54 (3H, м), 7,72-7,80 (1H, м), 7,88 (1H, д, J=7,8 Гц), 7,90-7,98 (1H, уширенный).
Справочный пример 15b

Следующее соединение получали, как описано в Справочном примере 13b.
Метил-4-(2-((трет-бутоксикарбонил)(изопропил)амино)фенил)-2-нитробензоат
1H-ЯМР(CD3OD): 0,73 (3H, д, J=6,8 Гц), 1,05 (3H, д, J=6,6 Гц), 1,26-1,50 (9H, уширенный), 3,91 (3H, с), 3,89-4,05 (1H, уширенный), 7,21-7,30 (1H, м), 7,46-7,54 (3H, м), 7,78 (1H, дд, J=7,9, 1,6 Гц), 7,88 (1H, д, J=7,9 Гц), 7,99 (1H, с).
Справочный пример 16b

При охлаждении на льду к раствору метил-4-(2-(этиламино)фенил)-2-нитробензоат (0,27 г) в N,N-диметилформамиде (3,0 мл) добавляли 60% гидрид натрия (54 мг), затем перемешивали при той же температуре в течение 5 минут, а затем при комнатной температуре в течение 15 минут. К реакционной смеси при охлаждении на льду добавляли метилйодид (0,083 мл), а затем перемешивали при комнатной температуре в течение 1 часа, а затем при 50°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней метилйодид (0,11 мл), а затем перемешивали при 40-50°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и диэтиловый эфир. Органический слой разделяли, промывали насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия последовательно и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 99-95% гексан/этилацетат] с получением 0,12 г метил-4-(2-((этил)(метил)амино)фенил)-2-нитробензоата в виде желтого маслянистого вещества.
1H-ЯМР(CDCl3): 0,92 (3H, т, J=7,2 Гц), 2,58 (3H, с), 2,80 (2H, кв, J=7,2 Гц), 3,94 (3H, с), 7,05-7,15 (2H, м), 7,23 (1H, дд, J=7,6, 1,7 Гц), 7,31-7,39 (1H, м), 7,78 (1H, д, J=8,0 Гц), 7,88 (1H, дд, J=8,0, 1,7 Гц), 8,18 (1H, д, J=1,7 Гц).
Справочный пример 17b

К раствору трет-бутил-4-(2-(трет-бутоксикарбониламино)фенил)-2-нитробензоата (0,27 г) в ацетоне (4,0 мл) добавляли карбонат калия (0,16 г) и диметилсульфат (0,094 мл), а затем нагревали с обратным холодильником в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат], а затем очищали по методу колоночной хроматографии [элюент: 91-85% гексан/этилацетат] с получением 0,061 г трет-бутил-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)-2-нитробензоата в виде бесцветного маслянистого вещества.
1H-ЯМР(DMSO-d6) δ: 0,99-1,28 (9H, м), 1,51 (9H, с), 3,00-3,11 (3H, м), 7,39-7,54 (4H, м), 7,74 (1H, д, J=8,3 Гц), 7,83-7,94 (2H, м).
Справочный пример 18b

К раствору метил-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)-2--нитробензоата (0,39 г) в хлористом метилене (2,0 мл) при комнатной температуре добавляли трифторуксусную кислоту (4,5 мл), а затем перемешивали при той же температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 91-85% гексан/этилацетат] с получением 0,27 г метил-4-(2-(этиламино)фенил)-2-нитробензоата в виде оранжевого маслянистого вещества.
1H-ЯМР(CDCl3): 1,16-1,23 (3H, м), 3,15 (2H, кв, J=7,1 Гц), 3,52-3,68 (1H, уширенный), 3,93-3,97 (3H, м), 6,74 (1H, д, J=8,3 Гц), 6,76-6,83 (1H, м), 7,03-7,09 (1H, м), 7,27-7,33 (1H, м), 7,74-7,79 (1H, м), 7,80-7,86 (1H, м), 7,95-7,99 (1H, м).
Справочный пример 19b

При нагревании с обратным холодильником к раствору N-(5-бром-4-метокси-2-метилфенил)ацетамида (1,0 г) в смеси воды (10 мл), трет-бутилового спирта (10 мл) и сульфата магния (0,79 г) добавляли перманганат калия (0,98 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 6 часов 20 минут. После охлаждения реакционной смеси до комнатной температуры нерастворимые вещества удаляли путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и этилацетат. Водный слой разделяли, и добавляли к нему 1 моль/л соляную кислоту (4 мл) и хлороформ. Органический слой разделяли, и экстрагировали водный слой хлороформом. Органический слой и экстракт объединяли, полученную смесь промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,36 г 2-(ацетамидо)-4-бром-5-метоксибензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 2,11 (3H, с), 3,86 (3H, с), 7,53 (1H, с), 8,68 (1H, с), 10,78 (1H, с).
Справочный пример 20b
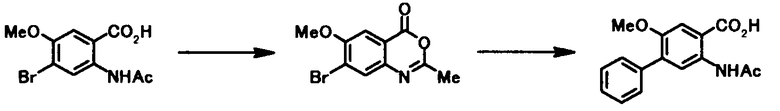
К раствору ди-трет-бутил-дикарбоната (0,75 г) в тетрагидрофуране (1,5 мл) при комнатной температуре добавляли 4-(диметиламино)пиридин (63 мг) и 2-ацетамид-4-бром-5-метоксибензойную кислоту (0,49 г), а затем перемешивали при той же температуре в течение 4 часов и 15 минут. К реакционной смеси при комнатной температуре добавляли тетрагидрофуран (2 мл), а затем перемешивали при той же температуре в течение 3 суток. К реакционной смеси при комнатной температуре добавляли ди-трет-бутил-дикарбонат (0,37 г), а затем перемешивали при той же температуре в течение 1 суток. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли гексан и диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,40 г 7-бром-6-метокси-2-метил-4H-3,1-бензоксазин-4-она в виде коричневого твердого вещества.
К суспензии полученного 7-бром-6-метокси-2-метил-4H-3,1-бензоксазин-4-она (0,40 г) в диметиловом эфире этиленгликоля (4 мл) добавляли воду (1,2 мл), фенилбороновую кислоту (0,22 г), карбонат натрия (0,38 г) и дихлорид бис(трифенилфосфин)палладия(II) (21 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Водный слой разделяли, и экстрагировали органический слой 2 моль/л водным раствором гидроксида натрия. Водный слой и экстракт объединяли, корректировали значение pH полученной смеси до 1 добавлением 6 моль/л соляной кислоты, и добавляли этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,27 г 2-ацетамид-5-метокси-4-фенилбензойной кислоты в виде желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 2,11 (3H, с), 3,78 (3H, с), 7,35-7,52 (5H, м), 7,57 (1H, с), 8,39 (1H, с), 10,79 (1H, с).
Справочный пример 21b
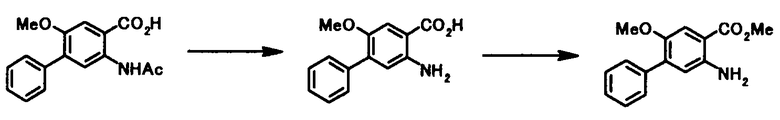
Раствор 2-ацетамид-5-метокси-4-фенилбензойной кислоты (0,41 г) в смеси диоксана (1,2 мл) и концентрированной соляной кислоты (1,2 мл) нагревали с обратным холодильником в течение 3 часов 40 минут. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду. После корректировки значения pH до 7 добавлением 1 моль/л водного раствора гидроксида натрия к смеси добавляли хлороформ. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления с получением 2-амино-5-метокси-4-фенилбензойной кислоты в виде коричневого твердого вещества.
При охлаждении на льду к суспензии полученной 2-амино-5-метокси-4-фенилбензойной кислоты в метаноле (10 мл) добавляли концентрированную серную кислоту (1 мл), а затем нагревали с обратным холодильником в течение 6 часов. Реакционную смесь охлаждали до комнатной температуры, корректировали значение pH до 8,0 добавлением насыщенного водного раствора бикарбоната натрия, и добавляли к ней хлороформ. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли гексан, и собирали твердое вещество путем фильтрования с получением 0,24 г метил-2-амино-5-метокси-4-фенилбензоата в виде коричневого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 3,65 (3H, с), 3,82 (3H, с), 6,35 (2H, с), 6,78 (1H, с), 7,30 (1H, с), 7,32-7,49 (5H, м).
Справочный пример 22b
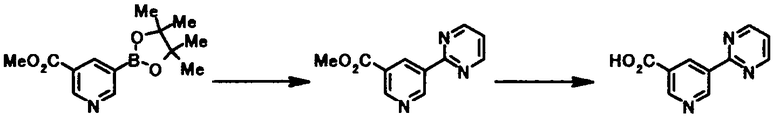
К раствору метил-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин-3-карбоксилата (0,10 г) в диметиловом эфире этиленгликоля (1 мл) добавляли 2-бромпиримидин (73 мг), карбонат натрия (81 мг), воду (0,3 мл) и дихлорид бис(трифенилфосфин)палладия(II) (5,3 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. После охлаждения реакционной смеси до комнатной температуры к ней добавляли этилацетат и воду, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-50% гексан/этилацетат] с получением 30 мг метил-5-(пиримидин-2-ил)пиридин-3-карбоксилата в виде желтого твердого вещества.
К раствору полученного метил-5-(пиримидин-2-ил)пиридин-3-карбоксилата (30 мг) в смеси диоксана (0,3 мл) и метанола (0,3 мл) при комнатной температуре добавляли 2 моль/л водный раствор гидроксида натрия (0,21 мл), а затем перемешивали при той же температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и толуол. Водный слой разделяли и корректировали значение pH до 3,8 добавлением 1 моль/л соляной кислоты. Твердое вещество собирали путем фильтрования с получением 7,0 мг 5-(пиримидин-2-ил)пиридин-3-карбоновой кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,58 (1H, т, J=4,9 Гц), 9,00 (2H, д, J=4,9 Гц), 9,13 (1H, дд, J=2,0, 2,0 Гц), 9,20 (1H, д, J=2,0 Гц), 9,68 (1H, д, J=2,0 Гц).
Справочный пример 23b
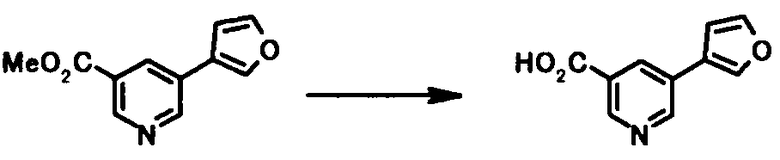
К раствору метил-5-(фуран-3-ил)пиридин-3-карбоксилата (0,54 г) в метаноле (10 мл) при комнатной температуре добавляли 4 моль/л водный раствор гидроксида натрия (2,0 мл), а затем перемешивали при той же температуре в течение 2 часов 50 минут. К реакционной смеси при комнатной температуре добавляли 10% водный раствор лимонной кислоты (8 мл), и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли воду, и собирали твердое вещество путем фильтрования с получением 0,33 г 5-(фуран-3-ил)пиридин-3-карбоновой кислоты в виде светло-желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,13-7,17 (1H, м), 7,80-7,84 (1H, м), 8,41-8,48 (2H, м), 8,92-8,96 (1H, м), 9,05-9,11 (1H, м).
Справочный пример 24b
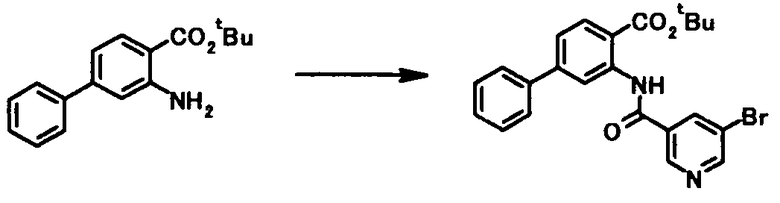
К суспензии 5-бромпиридин-3-карбоновой кислоты (0,23 г) в хлористом метилене (5 мл) при комнатной температуре добавляли N,N-диметилформамид (8,6 мкл) и оксалилхлорид (0,14 мл), а затем перемешивали при той же температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2,5 мл). Реакционную смесь при комнатной температуре добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,25 г) в смеси хлористого метилена (5 мл) и пиридина (0,19 мл), а затем перемешивали при той же температуре в течение 1 часа. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 100-80% гексан/этилацетат] с получением 0,39 г трет-бутил-2-(5-бромпиридин-3-карбоксамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,65 (9H, с), 7,37-7,45 (2H, м), 7,45-7,53 (2H, м), 7,68-7,74 (2H, м), 8,10 (1H, д, J=8,6 Гц), 8,52 (1H, дд, J=2,1, 2,1 Гц), 8,86 (1H, д, J=2,2 Гц), 9,17 (1H, д, J=2,0 Гц), 9,22 (1H, д, J=1,9 Гц), 12,52 (1H, с).
Справочные примеры 25b-27b
Соединения, представленные в Таблице 5b, получали, как описано в Справочном примере 24b.
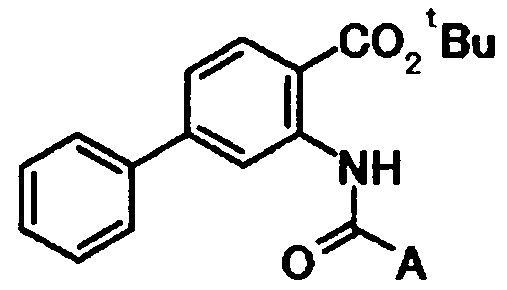
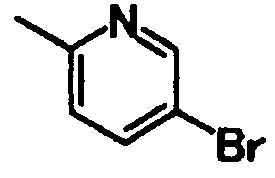
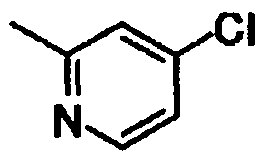
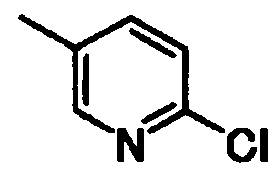
трет-Бутил-2-(5-бромпиридин-2-карбоксамидо)-4-фенилбензоат
1H-ЯМР(CDCl3) δ: 1,67 (9H, с), 7,35-7,43 (2H, м), 7,43-7,50 (2H, м), 7,69-7,75 (2H, м), 8,04 (1H, дд, J=8,5, 2,2 Гц), 8,09 (1H, д, J=8,3 Гц), 8,19 (1H, д, J=8,3 Гц), 8,84 (1H, д, J=2,0 Гц), 9,24 (1H, д, J=2,0 Гц), 12,90 (1H, с).
трет-Бутил-2-(4-хлорпиридин-2-карбоксамидо)-4-фенилбензоат
1H-ЯМР(CDCl3) δ: 1,68 (9H, с), 7,36-7,44 (2H, м), 7,44-7,53 (3H, м), 7,69-7,75 (2H, м), 8,09 (1H, д, J=8,3 Гц), 8,31 (1H, д, J=1,4 Гц), 8,67 (1H, д, J=5,2 Гц), 9,25 (1H, д, J=1,9 Гц), 12,94 (1H, с).
трет-Бутил-2-(6-хлорпиридин-3-карбоксамидо)-4-фенилбензоат
1H-ЯМР(DMSO-d6) δ: 1,55 (9H, с), 7,43-7,50 (1H, м), 7,51-7,58 (2H, м), 7,60 (1H, дд, J=8,3, 1,8 Гц), 7,71-7,76 (2H, м), 7,81 (1H, д, J=8,3 Гц), 8,02 (1H, д, J=8,3 Гц), 8,37 (1H, дд, J=8,3, 2,6 Гц), 8,60 (1H, д, J=1,8 Гц), 8,99 (1H, д, J=2,6 Гц), 11,56 (1H, с).
Справочный пример 28b
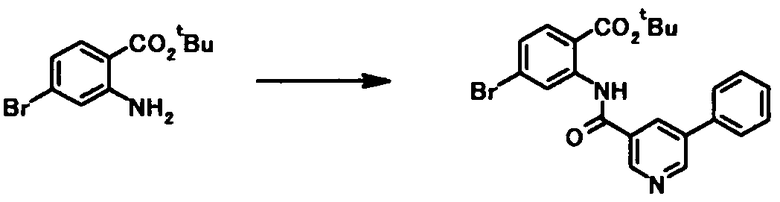
Следующее соединение получали, как описано в Справочном примере 24b.
трет-Бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоат
1H-ЯМР(CDCl3) δ: 1,64 (9H, с), 7,24-7,31 (1H, м), 7,43-7,49 (1H, м), 7,50-7,58 (2H, м), 7,66-7,73 (2H, м), 7,89 (1H, д, J=8,5 Гц), 8,56 (1H, дд, J=2,2, 2,2 Гц), 9,04 (1H, д, J=2,2 Гц), 9,17 (1H, д, J=1,9 Гц), 9,24 (1H, д, J=2,2 Гц), 12,52 (1H, с).
Справочный пример 29b
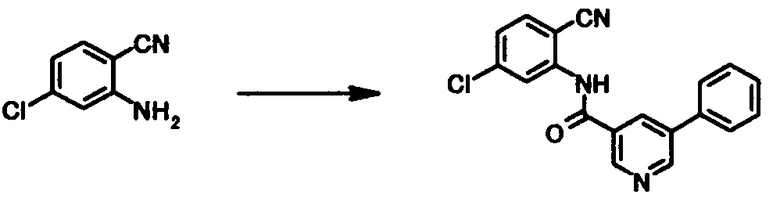
Следующее соединение получали, как описано в Справочном примере 24b.
N-(5-Хлор-2-цианофенил)-5-фенилпиридин-3-карбоксамид
1H-ЯМР(DMSO-d6) δ: 7,46-7,64 (4H, м), 7,78-7,90 (3H, м), 7,98 (1H, д, J=8,3 Гц), 8,59-8,64 (1H, м), 9,09-9,19 (2H, м), 11,03 (1H, с).
Справочный пример 30b

К раствору трет-бутил-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)-2-нитробензоата (57 мг) в смеси этилацетата (2,5 мл) и метанола (2,5 мл) добавляли 10% палладированый уголь (11 мг). Полученную смесь перемешивали при комнатной температуре в течение 3 часов в атмосфере водорода. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 48 мг трет-бутил-2-амино-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)бензоата в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 1,02-1,38 (9H, м), 1,54 (9H, с), 2,83-3,01 (3H, м), 6,44 (1H, дд, J=8,2, 1,3 Гц), 6,56-6,74 (3H, м), 7,26-7,43 (4H, м), 7,61-7,70 (1H, м).
Справочные примеры 31b-34b
Соединения, представленные в Таблице 6b, получали, как описано в Справочном примере 30b.
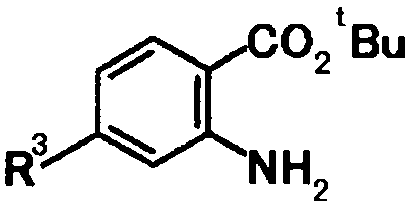
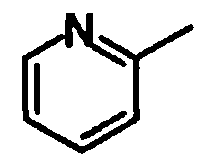
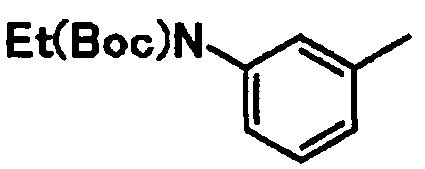
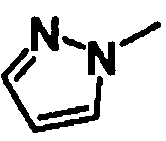
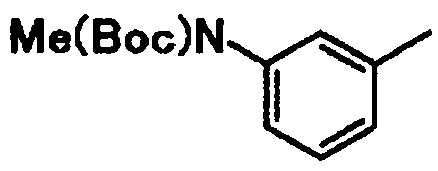
трет-Бутил-2-амино-4-(пиридин-2-ил)бензоат
1H-ЯМР(CDCl3) δ: 1,61 (9H, с), 5,74-5,86 (2H, уширенный), 7,18 (1H, дд, J=8,3, 1,7 Гц), 7,23-7,29 (1H, м), 7,36 (1H, д, J=1,4 Гц), 7,69-7,79 (2H, м), 7,90 (1H, д, J=8,3 Гц), 8,67-8,72 (1H, м).
трет-Бутил-2-амино-4-(1H-пиразол-1-ил)бензоат
1H-ЯМР(CDCl3) δ: 1,60 (9H, с), 5,82-5,95 (2H, уширенный), 6,47 (1H, дд, J=2,3, 2,0 Гц), 6,90 (1H, дд, J=8,8, 2,2 Гц), 7,08 (1H, д, J=2,2 Гц), 7,72 (1H, д, J=2,0 Гц), 7,88 (1H, д, J=8,8 Гц), 7,93 (1H, д, J=2,3 Гц).
трет-Бутил-2-амино-4-(3-((трет-бутоксикарбонил)(этил)амино)фенил)бензоат
1H-ЯМР(CDCl3) δ: 1,18 (3H, т, J=7,1 Гц), 1,45 (9H, с), 1,60 (9H, с), 3,71 (2H, кв, J=7,1 Гц), 5,78 (2H, с), 6,81-6,87 (2H, м), 7,15-7,24 (1H, м), 7,34-7,44 (3H, м), 7,84-7,90 (1H, м).
трет-Бутил-2-амино-4-(3-((трет-бутоксикарбонил)(метил)амино)фенил)бензоат
1H-ЯМР(CDCl3): 1,47 (9H, с), 1,60 (9H, с), 3,30 (3H, с), 5,72-5,83 (2H, уширенный), 6,81-6,86 (2H, м), 7,21-7,27 (1H, м), 7,34-7,41 (2H, м), 7,42-7,45 (1H, м), 7,84-7,89 (1H, м).
Справочный пример 35b
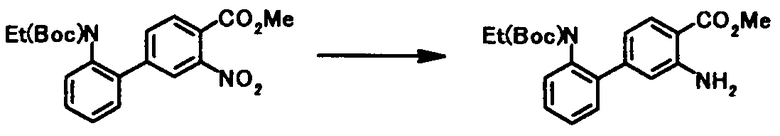
Следующее соединение получали, как описано в Справочном примере 30b.
Метил-2-амино-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)бензоат
1H-ЯМР(CD3OD): 0,96-1,11 (3H, м), 1,24-1,50 (9H, м), 2,77-2,95 (1H, м), 3,45-3,75 (1H, м), 3,86 (3H, с), 6,56 (1H, дд, J=8,3, 1,7 Гц), 6,73 (1H, д, J=1,7 Гц), 7,17-7,27 (1H, м), 7,33-7,42 (3H, м), 7,75-7,83 (1H, м).
Справочный пример 36b

Следующее соединение получали, как описано в Справочном примере 30b.
Метил-2-амино-4-(2-((трет-бутоксикарбонил)(изопропил)амино)фенил)бензоат
1H-ЯМР(CD3OD): 0,82 (3H, д, J=6,8 Гц), 0,93-1,13 (3H, м), 1,22-1,57 (9H, м), 3,80-4,07 (1H, м), 3,86 (3H, с), 6,60-6,70 (1H, м), 6,77 (1H, д, J=1,4 Гц), 7,08-7,24 (1H, уширенный), 7,33-7,44 (3H, м), 7,77 (1H, д, J=8,3 Гц).
Справочный пример 37b

Следующее соединение получали, как описано в Справочном примере 30b.
Метил-2-амино-4-(2-((этил)(метил)амино)фенил)бензоат
1H-ЯМР(CDCl3): 0,90 (3H, т, J=7,0 Гц), 2,61 (3H, с), 2,84 (2H, кв, J=7,0 Гц), 3,88 (3H, с), 6,85-6,91 (2H, м), 6,99 (1H, дд, J=7,4, 7,4 Гц), 7,03 (1H, д, J=8,3 Гц), 7,20 (1H, дд, J=7,6, 1,7 Гц), 7,23-7,30 (1H, м), 7,86 (1H, д, J=8,6 Гц).
Справочный пример 38b

К раствору трет-бутил-4-(2-(дифторметокси)фенил)-2-нитробензоата (0,18 г) в 2-пропаноле (2,1 мл) добавляли воду (0,53 мл), формиат натрия (0,13 г), уксусную кислоту (0,13 мл) и 10% палладированый уголь (35 мг), а затем нагревали с обратным холодильником в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и добавляли к смеси этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 99-91% гексан/этилацетат] с получением 0,15 г трет-бутил-2-амино-4-(2-(дифторметокси)фенил)бензоата в виде желтого маслянистого вещества.
1H-ЯМР(CDCl3): 1,60 (9H, с), 6,33 (1H, т, J=74,2 Гц), 6,72-6,78 (2H, м), 7,20-7,32 (2H, м), 7,33-7,42 (2H, м), 7,83-7,90 (1H, м).
Справочный пример 39b
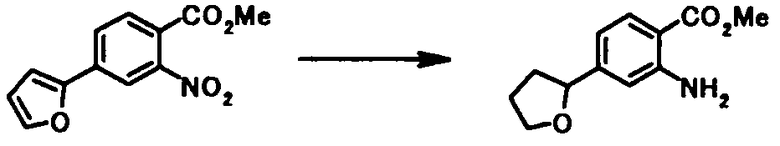
Следующее соединение получали, как описано в Справочном примере 38b.
Метил-2-амино-4-(тетрагидрофуран-2-ил)бензоат
1H-ЯМР(CDCl3): 1,70-1,82 (1H, м), 1,93-2,03 (2H, м), 2,25-2,37 (1H, м), 3,85 (3H, с), 3,89-3,97 (1H, м), 4,02-4,11 (1H, м), 4,82 (1H, дд, J=7,2, 7,2 Гц), 5,65-5,82 (2H, уширенный), 6,53-6,60 (1H, м), 6,64-6,70 (1H, м), 7,80 (1H, д, J=8,3 Гц).
Справочный пример 40b
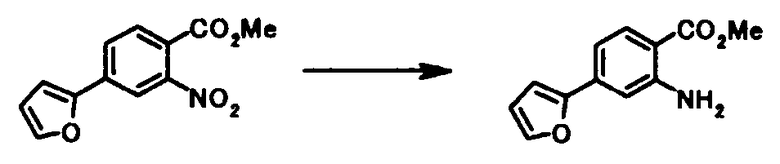
К суспензии метил-4-(фуран-2-ил)-2-нитробензоата (0,14 г) в этаноле (2,1 мл) добавляли воду (0,56 мл), хлорид аммония (18 мг) и порошковое железо (94 мг), а затем нагревали с обратным холодильником в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней хлорид аммония (18 мг), порошковое железо (31 мг) и воду (0,28 мл), а затем нагревали с обратным холодильником в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли насыщенный водный раствор бикарбоната натрия и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 99-95% гексан/этилацетат] с получением 78 мг метил-2-амино-4-(фуран-2-ил)бензоата в виде светло-желтого твердого вещества.
1H-ЯМР(CDCl3): 3,88 (3H, с), 5,72-5,86 (2H, уширенный), 6,49 (1H, дд, J=3,3, 1,8 Гц), 6,72 (1H, д, J=3,3 Гц), 6,94 (1H, дд, J=8,5, 1,7 Гц), 6,99 (1H, д, J=1,7 Гц), 7,47-7,51 (1H, м), 7,86 (1H, д, J=8,5 Гц).
Справочный пример 41b
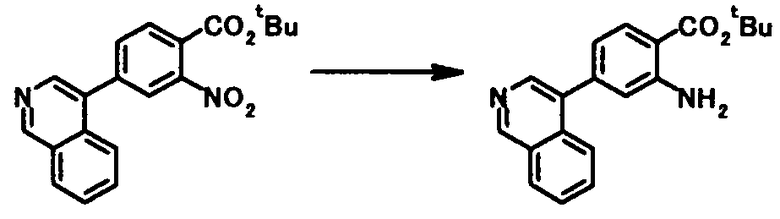
Следующее соединение получали, как описано в Справочном примере 40b.
трет-Бутил-2-амино-4-(изохинолин-4-ил)бензоат
1H-ЯМР(DMSO-d6) δ: 1,58 (9H, с), 6,64-6,72 (1H, м), 6,72-6,84 (2H, уширенный), 6,91 (1H, с), 7,72-7,96 (4H, м), 8,23 (1H, д, J=7,8 Гц), 8,42 (1H, д, J=1,0 Гц), 9,35 (1H, с).
Пример 1a
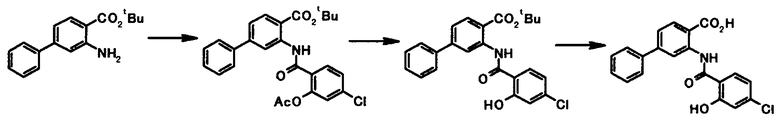
К суспензии 2-ацетокси-4-хлорбензойной кислоты (0,076 г) в хлористом метилене (1,6 мл) последовательно добавляли N,N-диметилформамид (2,7 мкл) и оксалилхлорид (0,046 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,080 г) в смеси пиридина (0,060 мл) и хлористого метилена (1,6 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Реакционную смесь очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 100-85% гексан/этилацетат] с получением 0,13 г трет-бутил-2-(2-ацетокси-4-хлорбензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-ацетокси-4-хлорбензамидо)-4-фенилбензоата (0,13 г) в смеси метанола (2,5 мл) и диоксана (2,5 мл) добавляли карбонат калия (0,12 г), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления с получением 0,11 г трет-бутил-2-(4-хлор-2-гидроксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(4-хлор-2-гидроксибензамидо)-4-фенилбензоата (0,11 г) в смеси трифторуксусной кислоты (5 мл) и хлористого метилена (2,5 мл) перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,077 г 2-(4-хлор-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,03-7,09 (2H, м), 7,43-7,58 (4H, м), 7,70-7,76 (2H, м), 7,93 (1H, д, J=9,0 Гц), 8,10 (1H, д, J=8,3 Гц), 9,02 (1H, д, J=1,7 Гц), 11,75-12,05 (1H, уширенный), 12,15-12,40 (1H, уширенный), 13,30-13,60 (1H, уширенный).
Примеры 2a-10a
Соединения, представленные в Таблице 9a, получали, как описано в Примере 1a.
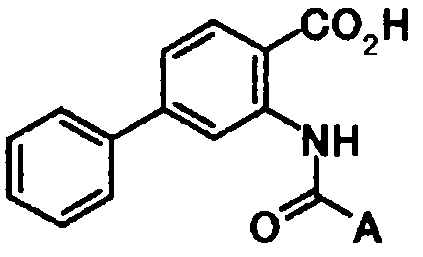
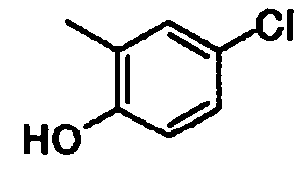
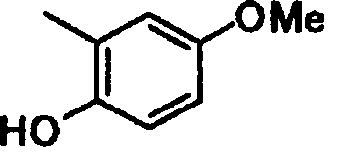
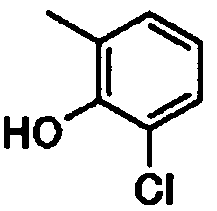
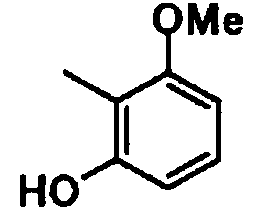
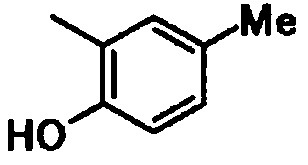
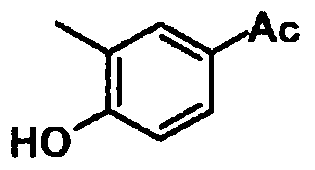
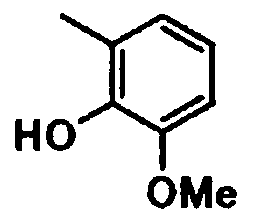
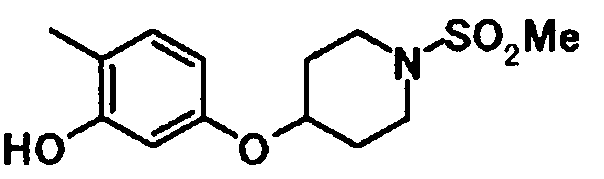
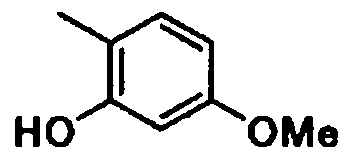
2-(5-Хлор-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 7,05 (1H, д, J=8,8 Гц), 7,43-7,58 (5H, м), 7,70-7,76 (2H, м), 7,90 (1H, д, J=2,9 Гц), 8,10 (1H, д, J=8,3 Гц), 9,00 (1H, д, J=1,7 Гц), 11,60-11,75 (1H, уширенный), 12,25-12,40 (1H, уширенный), 13,35-13,60 (1H, уширенный).
2-(3-Хлор-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 7,08 (1H, дд, J=7,9, 7,9 Гц), 7,44-7,50 (1H, м), 7,51-7,58 (2H, м), 7,60 (1H, дд, J=8,2, 1,8 Гц), 7,71 (1H, дд, J=7,9, 1,1 Гц), 7,72-7,78 (2H, м), 7,82-7,88 (1H, м), 8,14 (1H, д, J=8,2 Гц), 8,80 (1H, д, J=1,8 Гц), 12,25-12,50 (2H, уширенный).
2-(2-Гидрокси-5-метилбензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 2,28 (3H, с), 6,92 (1H, д, J=8,3 Гц), 7,26 (1H, дд, J=8,3, 1,7 Гц), 7,43-7,58 (4H, м), 7,69-7,76 (3H, м), 8,10 (1H, д, J=8,3 Гц), 9,01 (1H, д, J=1,7 Гц), 11,24 (1H, с), 12,30 (1H, с), 13,40-13,65 (1H, уширенный).
2-(2-Гидрокси-3-метоксибензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 3,81-3,87 (3H, м), 6,91-6,95 (1H, м), 7,17-7,23 (1H, м), 7,40-7,50 (2H, м), 7,50-7,58 (3H, м), 7,70-7,77 (2H, м), 8,11 (1H, дд, J=8,3, 2,4 Гц), 8,92-8,96 (1H, м), 11,25 (1H, с), 12,27 (1H, с).
2-(2-Гидрокси-4-метоксибензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 3,80 (3H, с), 6,53 (1H, д, J=2,3 Гц), 6,60 (1H, дд, J=8,9, 2,3 Гц), 7,42-7,57 (4H, м), 7,70-7,75 (2H, м), 7,85 (1H, д, J=8,9 Гц), 8,10 (1H, д, J=8,3 Гц), 8,97 (1H, д, J=1,7 Гц), 11,82 (1H, с), 12,21 (1H, с).
2-(2-Гидрокси-5-метоксибензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 3,76 (3H, с), 6,96 (1H, д, J=8,9 Гц), 7,08 (1H, дд, J=8,9, 3,1 Гц), 7,43-7,49 (2H, м), 7,49-7,58 (3H, м), 7,71-7,76 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,03 (1H, д, J=1,7 Гц), 11,00 (1H, с), 12,33 (1H, с), 13,35-13,65 (1H, уширенный).
2-(2-Гидрокси-6-метоксибензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 3,98 (3H, с), 6,59 (1H, дд, J=8,3, 1,0 Гц), 6,66 (1H, д, J=8,4 Гц), 7,40 (1H, дд, J=8,4, 8,3 Гц), 7,43-7,50 (1H, м), 7,51-7,58 (3H, м), 7,70-7,76 (2H, м), 8,11 (1H, д, J=8,1 Гц), 8,94 (1H, с), 12,35 (1H, с), 12,62 (1H, с), 13,60-13,78 (1H, уширенный).
2-(5-Ацетил-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 2,57 (3H, с), 7,12 (1H, д, J=8,7 Гц), 7,43-7,50 (1H, м), 7,51-7,58 (3H, м), 7,71-7,78 (2H, м), 8,04 (1H, дд, J=8,7, 2,2 Гц), 8,11 (1H, д, J=8,3 Гц), 8,58 (1H, д, J=2,2 Гц), 9,06 (1H, д, J=1,7 Гц), 12,25-12,48 (2H, м), 13,40-13,65 (1H, уширенный).
2-(2-Гидрокси-4-(1-(метилсульфонил)пиперидин-4-илокси)бензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6), (40°C) δ: 1,70-1,84 (2H, м), 1,96-2,10 (2H, м), 2,90 (3H, с), 3,10-3,22 (2H, м), 3,30-3,42 (2H, м), 4,59-4,70 (1H, м), 6,57 (1H, д, J=2,4 Гц), 6,65 (1H, дд, J=8,9, 2,4 Гц), 7,42-7,57 (4H, м), 7,69-7,75 (2H, м), 7,84 (1H, д, J=8,9 Гц), 8,10 (1H, д, J=8,3 Гц), 8,95 (1H, д, J=1,7 Гц), 11,79 (1H, с), 12,19 (1H, с).
Пример 11a
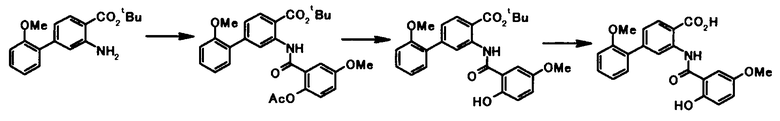
Следующее соединение получали, как описано в Примере 1a.
2-(2-Гидрокси-5-метоксибензамидо)-4-(2-метоксифенил)бензойная кислота
1H-ЯМР(DMSO-d6) δ: 3,75 (3H, с), 3,80 (3H, с), 6,95 (1H, д, J=9,0 Гц), 7,04-7,12 (2H, м), 7,16 (1H, д, J=8,6 Гц), 7,30-7,45 (4H, м), 8,03 (1H, д, J=8,3 Гц), 8,78 (1H, д, J=1,7 Гц), 11,00 (1H, с), 12,28 (1H, с).
Пример 12a
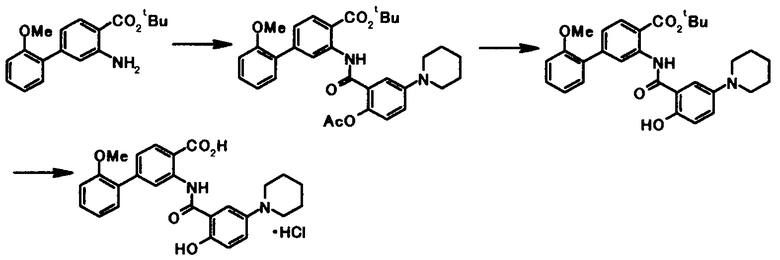
При охлаждении на льду к суспензии 2-ацетокси-5-(пиперидин-1-ил)бензойной кислоты (0,11 г) в хлористом метилене (2,0 мл) последовательно добавляли N,N-диметилформамид (0,010 мл) и оксалилхлорид (0,044 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2,0 мл). Полученную смесь добавляли при охлаждении на льду к раствору трет-бутил-2-амино-4-(2-метоксифенил)бензоата (0,10 г) и пиридина (0,054 мл) в хлористом метилене (1,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 91-80% гексан/этилацетат] с получением 0,11 г трет-бутил-2-(2-ацетокси-5-(пиперидин-1-ил)бензамидо)-4-(2-метоксифенил)бензоата в виде светло-желтого твердого вещества.
К полученному трет-бутил-2-(2-ацетокси-5-(пиперидин-1-ил)бензамидо)-4-(2-метоксифенил)бензоату (0,11 г) добавляли диоксан (4,0 мл) и 4 моль/л водный раствор гидроксида натрия (0,25 мл), а затем перемешивали при 50-55°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-60% гексан/этилацетат] с получением 0,025 г трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(2-метоксифенил)бензоата в виде желтого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(2-метоксифенил)бензоату (0,025 г) добавляли 4 моль/л раствор хлорводорода в диоксане (3,0 мл), затем перемешивали при комнатной температуре в течение 3 часов, а затем при 50-55°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,020 г гидрохлорида 2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(2-метоксифенил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР(CD3OD) δ: 1,72-1,84 (2H, м), 1,96-2,06 (4H, м), 3,52-3,62 (4H, м), 3,85 (3H, с), 7,03-7,16 (3H, м), 7,35-7,43 (3H, м), 7,64 (1H, дд, J=8,8, 2,7 Гц), 8,04-8,09 (1H, м), 8,15 (1H, д, J=8,3 Гц), 8,88 (1H, д, J=1,5 Гц).
Пример 13a
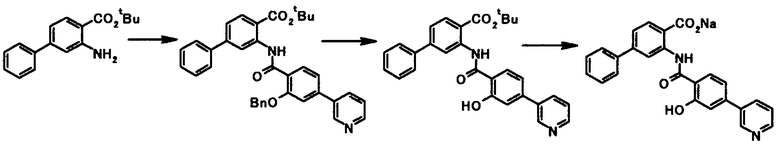
К суспензии 2-(бензилокси)-4-(пиридин-3-ил)бензойной кислоты (0,095 г) в хлористом метилене (1,4 мл) последовательно добавляли N,N-диметилформамид (2,4 мкл) и оксалилхлорид (0,040 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1,4 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,070 г) в смеси пиридина (0,053 мл) и хлористого метилена (1,4 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 1 моль/л водный раствор гидроксида натрия. Органический слой разделяли, промывали 1 моль/л водным раствором гидроксида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-50% гексан/этилацетат] с получением 0,13 г трет-бутил-2-(2-(бензилокси)-4-(пиридин-3-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-4-(пиридин-3-ил)бензамидо)-4-фенилбензоата (0,13 г) в смеси метанола (2 мл), диоксана (4 мл) и этилацетата (4 мл) добавляли 10% палладированый уголь (63 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-40% гексан/этилацетат] с получением 0,077 г трет-бутил-2-(2-гидрокси-4-(пиридин-3-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-4-(пиридин-3-ил)бензамидо)-4-фенилбензоата (0,077 г) в трифторуксусной кислоте (5 мл) перемешивали при комнатной температуре в течение 2 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду и этилацетат. После корректировки значения pH до 6,5 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли метанол (3 мл), диоксан (3 мл) и 2 моль/л водный раствор гидроксида натрия (0,073 мл). Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,063 г 2-(2-гидрокси-4-(пиридин-3-ил)бензамидо)-4-фенилбензоата натрия в виде светло-желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,31-7,43 (4H, м), 7,47-7,55 (3H, м), 7,66-7,72 (2H, м), 8,10-8,22 (3H, м), 8,60-8,65 (1H, м), 8,91 (1H, д, J=2,0 Гц), 8,99 (1H, д, J=1,9 Гц).
Примеры 14a-17a
Соединения, представленные в Таблице 10a, получали, как описано в Примере 13a.
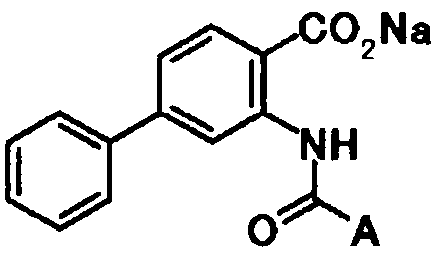
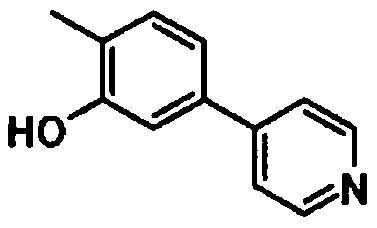
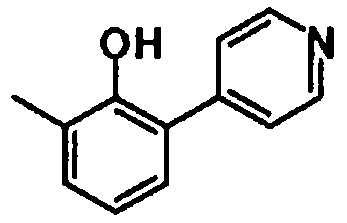
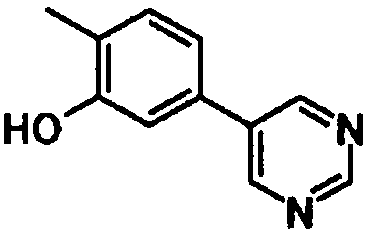
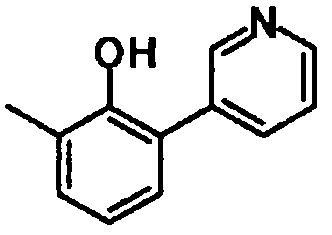
2-(2-Гидрокси-4-(пиридин-4-ил)бензамидо)-4-фенилбензоат натрия
1H-ЯМР(DMSO-d6) δ: 7,33-7,44 (4H, м), 7,47-7,54 (2H, м), 7,66-7,72 (2H, м), 7,76-7,83 (2H, м), 8,12 (1H, д, J=7,8 Гц), 8,15 (1H, д, J=8,3 Гц), 8,60-8,76 (2H, м), 8,91 (1H, д, J=1,7 Гц).
2-(2-Гидрокси-4-(пиримидин-5-ил)бензамидо)-4-фенилбензоат натрия
1H-ЯМР(DMSO-d6) δ: 7,34-7,54 (6H, м), 7,66-7,72 (2H, м), 8,12 (1H, д, J=8,1 Гц), 8,16 (1H, д, J=8,1 Гц), 8,91 (1H, д, J=1,7 Гц), 9,22-9,26 (3H, м).
2-(2-Гидрокси-3-(пиридин-3-ил)бензамидо)-4-фенилбензоат натрия
1H-ЯМР(DMSO-d6) δ: 7,12 (1H, дд, J=7,8, 7,8 Гц), 7,34-7,43 (2H, м), 7,45-7,53 (3H, м), 7,61 (1H, дд, J=7,4, 1,1 Гц), 7,65-7,71 (2H, м), 8,00-8,06 (1H, м), 8,10-8,16 (2H, м), 8,52-8,59 (1H, м), 8,79 (1H, д, J=1,7 Гц), 8,88 (1H, д, J=1,7 Гц).
2-(2-Гидрокси-3-(пиридин-4-ил)бензамидо)-4-фенилбензоат натрия
1H-ЯМР(DMSO-d6) δ: 7,04-7,21 (1H, м), 7,32-7,43 (2H, м), 7,46-7,54 (2H, м), 7,61-7,72 (5H, м), 8,06-8,22 (2H, м), 8,56-8,70 (2H, м), 8,86-8,92 (1H, м).
Пример 18a
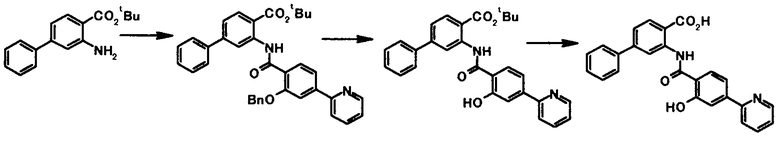
К суспензии 2-(бензилокси)-4-(пиридин-2-ил)бензойной кислоты (0,095 г) в хлористом метилене (1,4 мл) последовательно добавляли N,N-диметилформамид (2,4 мкл) и оксалилхлорид (0,040 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1,4 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,070 г) в смеси пиридина (0,053 мл) и хлористого метилена (1,4 мл), а затем перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли 1 моль/л водный раствор гидроксида натрия. Органический слой разделяли, промывали 1 моль/л водным раствором гидроксида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 95-60% гексан/этилацетат] с получением 0,13 г трет-бутил-2-(2-(бензилокси)-4-(пиридин-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-4-(пиридин-2-ил)бензамидо)-4-фенилбензоата (0,13 г) в смеси метанола (2 мл), диоксана (2 мл) и этилацетата (4 мл) добавляли 10% палладированый уголь (67 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 минут. К реакционной смеси добавляли хлороформ. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: хлороформ] с получением 0,11 г трет-бутил-2-(2-гидрокси-4-(пиридин-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-4-(пиридин-2-ил)бензамидо)-4-фенилбензоата (0,11 г) в трифторуксусной кислоте (5 мл) перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду и этилацетат. После корректировки значения pH до 6,0 добавлением насыщенного водного раствора бикарбоната натрия, твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли воду (4 мл), метанол (4 мл) и диоксан (4 мл), и при комнатной температуре пропускали через смесь газообразный углекислый газ. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. Твердое вещество собирали путем фильтрования с получением 0,072 г 2-(2-гидрокси-4-(пиридин-2-ил)бензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,40-7,58 (5H, м), 7,69 (1H, дд, J=8,3, 1,7 Гц), 7,72-7,77 (2H, м), 7,80 (1H, д, J=1,4 Гц), 7,93 (1H, ддд, J=7,8, 7,8, 1,8 Гц), 7,98-8,06 (2H, м), 8,11 (1H, д, J=8,3 Гц), 8,69-8,74 (1H, м), 9,05 (1H, д, J=1,7 Гц), 11,55-11,78 (1H, уширенный), 12,40-12,62 (1H, уширенный).
Пример 19a
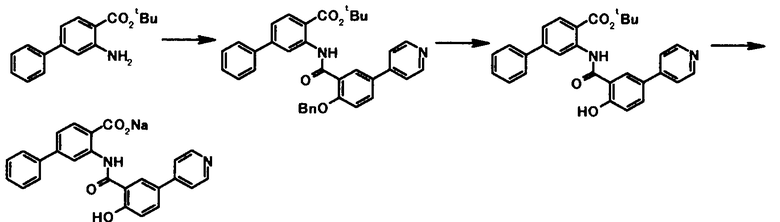
К суспензии 2-(бензилокси)-5-(пиридин-4-ил)бензойной кислоты (0,095 г) в хлористом метилене (2 мл) последовательно добавляли N,N-диметилформамид (2,4 мкл) и оксалилхлорид (0,040 мл), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1,5 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,070 г) в смеси пиридина (0,053 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 1 моль/л водный раствор гидроксида натрия. Органический слой разделяли, промывали 1 моль/л водным раствором гидроксида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-40% гексан/этилацетат] с получением 0,11 г трет-бутил-2-(2-(бензилокси)-5-(пиридин-4-ил)бензамидо)-4-фенилбензоата.
1H-ЯМР(DMSO-d6) δ: 1,51 (9H, с), 5,59 (2H, с), 7,26-7,42 (4H, м), 7,44-7,62 (6H, м), 7,67-7,80 (4H, м), 7,97 (1H, дд, J=8,8, 2,4 Гц), 8,07 (1H, д, J=8,3 Гц), 8,39 (1H, д, J=2,4 Гц), 8,58-8,67 (2H, м), 9,14 (1H, с), 12,25 (1H, с).
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(пиридин-4-ил)бензамидо)-4-фенилбензоата (0,11 г) в уксусной кислоте (2 мл) добавляли 10% палладированый уголь (0,11 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К остатку добавляли этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, последовательно промывали насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 5 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и этилацетат. После корректировки значения pH до 6,5 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования, и добавляли к полученному твердому веществу метанол (10 мл), диоксан (10 мл) и 2 моль/л водный раствор гидроксида натрия (0,078 мл). Затем, нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,067 г натрия 2-(2-гидрокси-5-(пиридин-4-ил)бензамидо)-4-фенилбензоата в виде желтого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,08 (1H, д, J=8,8 Гц), 7,36 (1H, дд, J=8,1, 1,7 Гц), 7,35-7,43 (1H, м), 7,47-7,54 (2H, м), 7,66-7,72 (2H, м), 7,73-7,79 (2H, м), 7,92-8,00 (1H, м), 8,12 (1H, д, J=8,1 Гц), 8,54 (1H, д, J=2,2 Гц), 8,60-8,70 (2H, м), 8,91 (1H, д, J=1,7 Гц).
Пример 20a
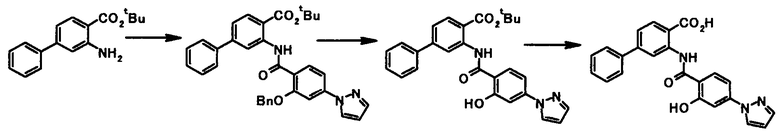
К суспензии 2-(бензилокси)-4-(1H-пиразол-1-ил)бензойной кислоты (0,092 г) в хлористом метилене (1,4 мл) последовательно добавляли N,N-диметилформамид (2,4 мкл) и оксалилхлорид (0,040 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1,4 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,070 г) в смеси пиридина (0,053 мл) и хлористого метилена (1,4 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия, и разделяли органический слой. Полученный органический слой очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 95-70% гексан/этилацетат] с получением 0,098 г трет-бутил-2-(2-(бензилокси)-4-(1H-пиразол-1-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-4-(1H-пиразол-1-ил)бензамидо)-4-фенилбензоата (0,098 г) в смеси этилацетата (2 мл), метанола (1 мл) и диоксана (1 мл) добавляли 10% палладированый уголь (49 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли хлороформ, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: хлороформ] с получением трет-бутил-2-(2-гидрокси-4-(1H-пиразол-1-ил)бензамидо)-4-фенилбензоата.
Раствор полученного трет-бутил-2-(2-гидрокси-4-(1H-пиразол-1-ил)бензамидо)-4-фенилбензоата в трифторуксусной кислоте (5 мл) перемешивали при комнатной температуре в течение 3 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку метанол. Твердое вещество собирали путем фильтрования с получением 0,056 г 2-(2-гидрокси-4-(1H-пиразол-1-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 6,60 (1H, дд, J=2,6, 1,8 Гц), 7,43-7,58 (6H, м), 7,71-7,77 (2H, м), 7,81 (1H, д, J=1,7 Гц), 8,03 (1H, д, J=8,8 Гц), 8,11 (1H, д, J=8,3 Гц), 8,58 (1H, д, J=2,4 Гц), 9,02 (1H, д, J=1,7 Гц), 11,90 (1H, с), 12,33 (1H, с), 13,38-13,64 (1H, уширенный).
Примеры 21a и 22a
Соединения, представленные в Таблице 11a, получали, как описано в Примере 20a.
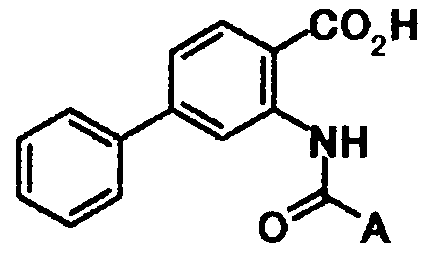
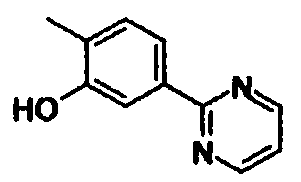
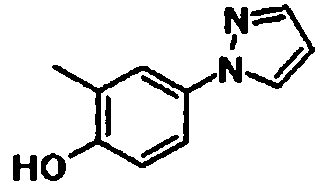
2-(2-Гидрокси-4-(пиримидин-2-ил)бензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 7,43-7,58 (5H, м), 7,71-7,77 (2H, м), 7,99 (1H, дд, J=8,4, 1,6 Гц), 8,04-8,14 (3H, м), 8,96 (2H, д, J=4,9 Гц), 9,07 (1H, д, J=1,7 Гц), 11,62 (1H, с), 12,42 (1H, с), 13,35-13,60 (1H, уширенный).
2-(2-гидрокси-5-(1H-пиразол-1-ил)бензамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 6,53 (1H, дд, J=2,1, 2,1 Гц), 7,14 (1H, д, J=9,0 Гц), 7,43-7,50 (1H, м), 7,51-7,58 (3H, м), 7,71-7,77 (3H, м), 7,90 (1H, дд, J=8,8, 2,9 Гц), 8,11 (1H, д, J=8,3 Гц), 8,34 (1H, д, J=2,7 Гц), 8,42 (1H, д, J=2,4 Гц), 9,06 (1H, д, J=1,7 Гц), 11,52-11,70 (1H, уширенный), 12,35-12,50 (1H, уширенный).
Пример 23a
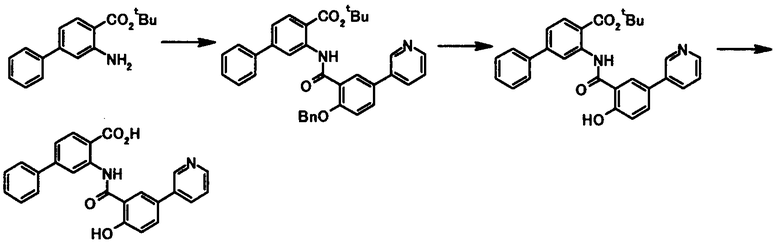
К суспензии 2-(бензилокси)-5-(пиридин-3-ил)бензойной кислоты (0,095 г) в хлористом метилене (2 мл) последовательно добавляли N,N-диметилформамид (2,4 мкл) и оксалилхлорид (0,040 мл), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1,5 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,070 г) в смеси пиридина (0,053 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 1 моль/л водный раствор гидроксида натрия. Органический слой разделяли, промывали 1 моль/л водным раствором гидроксида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-50% гексан/этилацетат] с получением 0,14 г трет-бутил-2-(2-(бензилокси)-5-(пиридин-3-ил)бензамидо)-4-фенилбензоата.
1H-ЯМР(DMSO-d6) δ: 1,51 (9H, с), 5,58 (2H, с), 7,26-7,42 (4H, м), 7,44-7,63 (7H, м), 7,70-7,78 (2H, м), 7,89 (1H, дд, J=8,8, 2,4 Гц), 8,04-8,13 (2H, м), 8,28 (1H, д, J=2,4 Гц), 8,56 (1H, дд, J=4,6, 1,4 Гц), 8,89 (1H, д, J=2,4 Гц), 9,12-9,17 (1H, м), 12,25 (1H, с).
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(пиридин-3-ил)бензамидо)-4-фенилбензоата (0,14 г) в смеси этилацетата (1 мл) и метанола (1 мл) добавляли 10% палладированый уголь (14 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа 30 минут. К реакционной смеси добавляли 10% палладированый уголь (14 мг). Реакционную смесь перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 минут. К реакционной смеси добавляли уксусную кислоту (2 мл) и 10% палладированый уголь (0,11 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К остатку добавляли этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия последовательно и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 5 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и этилацетат. После корректировки значения pH до 5 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования с получением 0,070 г 2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,16 (1H, д, J=8,5 Гц), 7,43-7,59 (5H, м), 7,70-7,78 (2H, м), 7,86 (1H, дд, J=8,5, 2,3 Гц), 8,05-8,11 (1H, м), 8,12 (1H, д, J=8,0 Гц), 8,26 (1H, д, J=2,3 Гц), 8,53-8,59 (1H, м), 8,91 (1H, д, J=2,0 Гц), 9,03 (1H, д, J=1,5 Гц).
Пример 24a
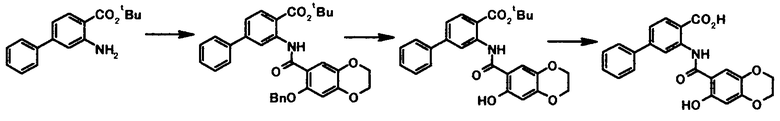
К суспензии 7-(бензилокси)-2,3-дигидробензо[1,4]диоксин-6-карбоновой кислоты (0,33 г) в хлористом метилене (3,0 мл) последовательно добавляли N,N-диметилформамид (8,8 мкл) и оксалилхлорид (0,15 мл), а затем перемешивали при комнатной температуре в течение 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (3 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,26 г) в смеси пиридина (0,20 мл) и хлористого метилена (3,0 мл), а затем перемешивали при комнатной температуре в течение 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 1 моль/л соляную кислоту и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 90-65% гексан/этилацетат] с получением 0,49 г трет-бутил-2-(7-(бензилокси)-2,3-дигидробензо[1,4]диоксин-6-карбоксамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(7-(бензилокси)-2,3-дигидробензо[1,4]диоксин-6-карбоксамидо)-4-фенилбензоата (0,49 г) в смеси метанола (4 мл) и этилацетата (4 мл) добавляли 10% палладированый уголь (0,24 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,37 г трет-бутил-2-(7-гидрокси-2,3-дигидробензо[1,4]диоксин-6-карбоксамидо)-4-фенилбензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(7-гидрокси-2,3-дигидробензо[1,4]диоксин-6-карбоксамидо)-4-фенилбензоата (0,37 г) в трифторуксусной кислоте (4 мл) перемешивали при комнатной температуре в течение 15 минут. К реакционной смеси добавляли хлористый метилен (10 мл), а затем перемешивали при комнатной температуре в течение 1 часа 15 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этилацетат. Твердое вещество собирали путем фильтрования с получением 0,30 г 2-(7-гидрокси-2,3-дигидробензо[1,4]диоксин-6-карбоксамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 4,18-4,26 (2H, м), 4,26-4,35 (2H, м), 6,48 (1H, с), 7,39 (1H, с), 7,41-7,57 (4H, м), 7,68-7,75 (2H, м), 8,08 (1H, д, J=8,3 Гц), 8,97 (1H, д, J=2,0 Гц), 11,24 (1H, с), 12,19 (1H, с), 13,35-13,60 (1H, уширенный).
Пример 25a
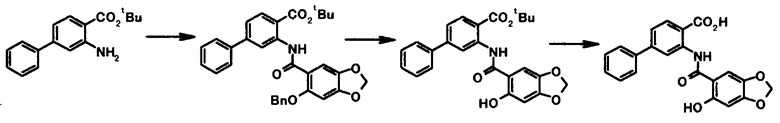
Следующее соединение получали, как описано в Примере 24a.
2-(6-Гидроксибензо[1,3]диоксазол-5-карбоксамидо)-4-фенилбензойная кислота
1H-ЯМР(DMSO-d6) δ: 6,07 (1H, с), 6,60 (1H, д, J=0,7 Гц), 7,34 (1H, д, J=0,7 Гц), 7,42-7,59 (4H, м), 7,68-7,78 (2H, м), 8,09 (1H, д, J=8,0 Гц), 8,90-8,96 (1H, м), 11,85 (1H, с), 12,17 (1H, с), 13,40-13,70 (1H, уширенный).
Пример 26a
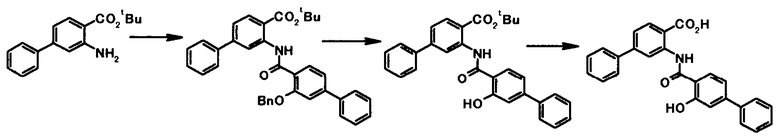
К раствору 2-(бензилокси)-4-фенилбензойной кислоты (0,18 г) в хлористом метилене (2 мл) последовательно добавляли N,N-диметилформамид (4,6 мкл) и оксалилхлорид (0,077 мл), а затем перемешивали при комнатной температуре в течение 25 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,14 г) в смеси пиридина (0,10 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Реакционную смесь очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 90-75% гексан/этилацетат → хлороформ] с получением 0,11 г трет-бутил-2-(2-(бензилокси)-4-фенилбензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-4-фенилбензамидо)-4-фенилбензоата (0,11 г) в смеси метанола (4 мл) и хлороформа (4 мл) добавляли 10% палладированый уголь (40 мг), затем перемешивали в атмосфере водорода при комнатной температуре в течение 5 часов 30 минут, а затем при 35°C в течение 1 часа. К реакционной смеси добавляли 10% палладированый уголь (40 мг), а затем перемешивали в атмосфере водорода при 35°C в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир гексан, и собирали твердое вещество путем фильтрования с получением трет-бутил-2-(2-гидрокси-4-фенилбензамидо)-4-фенилбензоата.
Раствор полученного трет-бутил-2-(2-гидрокси-4-фенилбензамидо)-4-фенилбензоата в смеси хлористого метилена (6 мл) и трифторуксусной кислоты (1 мл) перемешивали при комнатной температуре в течение 3 часов 10 минут. К реакционной смеси добавляли трифторуксусную кислоту (2 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,076 г 2-(2-гидрокси-4-фенилбензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,29 (1H, д, J=1,7 Гц), 7,31 (1H, дд, J=8,2, 1,8 Гц), 7,40-7,60 (7H, м), 7,66-7,79 (4H, м), 8,00 (1H, д, J=8,3 Гц), 8,11 (1H, д, J=8,1 Гц), 9,04 (1H, д, J=2,0 Гц), 11,66 (1H, с), 12,36 (1H, с), 13,35-13,70 (1H, уширенный).
Пример 27a
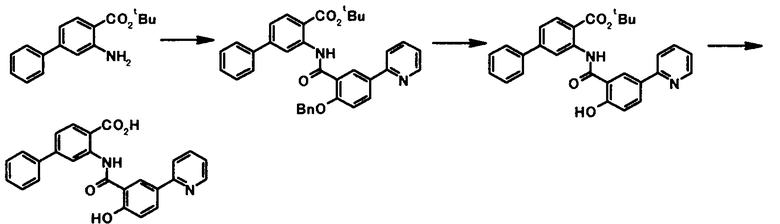
К суспензии 2-(бензилокси)-5-(пиридин-2-ил)бензойной кислоты (0,050 г) в хлористом метилене (2 мл) последовательно добавляли N,N-диметилформамид (1,5 мкл) и оксалилхлорид (0,023 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,053 г) в смеси пиридина (0,033 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [элюент: 95-70% гексан/этилацетат] с получением 0,038 г трет-бутил-2-(2-(бензилокси)-5-(пиридин-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР(CDCl3) δ: 1,53 (9H, с), 5,56 (2H, с), 7,08 (1H, д, J=8,8 Гц), 7,18 (1H, ддд, J=7,4, 4,8, 1,2 Гц), 7,23-7,52 (9H, м), 7,68-7,81 (4H, м), 8,07 (1H, д, J=8,3 Гц), 8,15 (1H, дд, J=8,8, 2,4 Гц), 8,61-8,66 (1H, м), 8,74 (1H, д, J=2,4 Гц), 9,31-9,35 (1H, м), 12,54 (1H, с).
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(пиридин-2-ил)бензамидо)-4-фенилбензоата (0,038 г) в смеси этилацетата (2 мл) и метанола (4 мл) добавляли 10% палладированый уголь (20 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 45 минут. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-70% гексан/этилацетат] с получением 0,021 г трет-бутил-2-(2-гидрокси-5-(пиридин-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-5-(пиридин-2-ил)бензамидо)-4-фенилбензоата (0,021 г) в смеси хлористого метилена (1 мл) и трифторуксусной кислоты (0,5 мл) перемешивали при комнатной температуре в течение 1 часа 10 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. После корректировки значения pH до 7 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования с получением 0,013 г 2-(2-гидрокси-5-(пиридин-2-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,15 (1H, д, J=8,6 Гц), 7,31-7,39 (1H, м), 7,43-7,60 (4H, м), 7,71-7,79 (2H, м), 7,86-8,00 (2H, м), 8,12 (1H, д, J=8,1 Гц), 8,18 (1H, дд, J=8,5, 2,2 Гц), 8,66 (1H, д, J=4,9 Гц), 8,69 (1H, д, J=2,0 Гц), 9,04-9,10 (1H, м), 11,81 (1H, с), 12,39 (1H, с).
Пример 28a
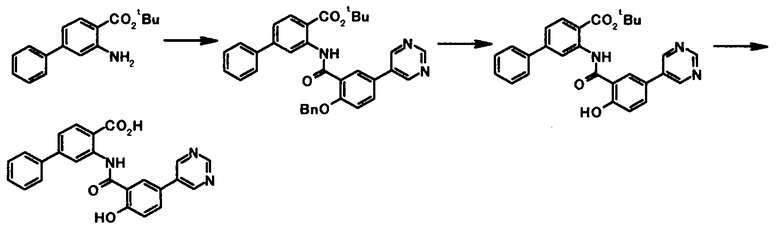
К суспензии 2-(бензилокси)-5-(пиримидин-5-ил)бензойной кислоты (0,80 г) в хлористом метилене (20 мл) последовательно добавляли N,N-диметилформамид (0,024 мл) и оксалилхлорид (0,40 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (20 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,74 г) в смеси пиридина (0,59 мл) и хлористого метилена (20 мл), а затем перемешивали при комнатной температуре в течение 1 часа 10 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 80-50% гексан/этилацетат] с получением 1,1 г трет-бутил-2-(2-(бензилокси)-5-(пиримидин-5-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного в трет-бутил-2-(2-(бензилокси)-5-(пиримидин-5-ил)бензамидо)-4-фенилбензоата (1,1 г) в смеси этилацетата (10 мл), метанола (20 мл) и диоксана (20 мл) добавляли 10% палладированый уголь (0,57 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 20 минут. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 70-0% гексан/этилацетат] с получением 0,73 г трет-бутил-2-(2-гидрокси-5-(пиримидин-5-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-5-(пиримидин-5-ил)бензамидо)-4-фенилбензоата (0,73 г) в смеси хлористого метилена (25 мл) и трифторуксусной кислоты (10 мл) перемешивали при комнатной температуре в течение ночи. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. После корректировки значения pH до 6,5 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования с получением 0,49 г 2-(2-гидрокси-5-(пиримидин-5-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,19 (1H, д, J=8,5 Гц), 7,43-7,50 (1H, м), 7,51-7,60 (3H, м), 7,70-7,78 (2H, м), 7,93 (1H, дд, J=8,5, 2,4 Гц), 8,12 (1H, д, J=8,3 Гц), 8,31 (1H, д, J=2,2 Гц), 9,04 (1H, д, J=1,7 Гц), 9,14 (2H, с), 9,17 (1H, с), 11,72-11,92 (1H, уширенный), 12,28-12,50 (1H, уширенный), 13,44-13,72 (1H, уширенный).
Пример 29a
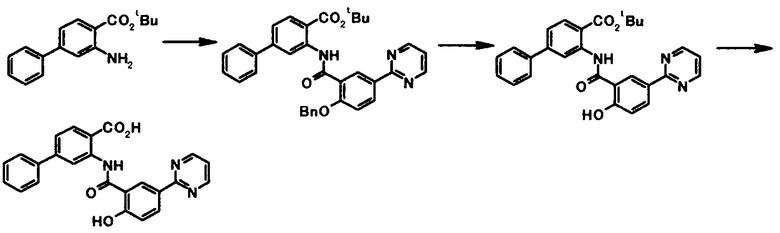
К суспензии 2-(бензилокси)-5-(пиримидин-2-ил)бензойной кислоты (0,64 г) в хлористом метилене (20 мл) последовательно добавляли N,N-диметилформамид (0,019 мл) и оксалилхлорид (0,32 мл), а затем перемешивали при комнатной температуре в течение 1 часа 10 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (20 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,59 г) в смеси пиридина (0,47 мл) и хлористого метилена (20 мл), а затем перемешивали при комнатной температуре в течение 1 часа 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 70-50% гексан/этилацетат] с получением 0,94 г трет-бутил-2-(2-(бензилокси)-5-(пиримидин-2-ил)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(пиримидин-2-ил)бензамидо)-4-фенилбензоата (0,072 г) в смеси этилацетата (4 мл) и метанола (4 мл) добавляли 10% палладированый уголь (36 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 45 минут. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 75-60% гексан/этилацетат] с получением 5 мг трет-бутил-2-(2-гидрокси-5-(пиримидин-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-5-(пиримидин-2-ил)бензамидо)-4-фенилбензоата (5 мг) в смеси хлористого метилена (2 мл) и трифторуксусной кислоты (0,50 мл) перемешивали при комнатной температуре в течение 3 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 4 мг 2-(2-гидрокси-5-(пиримидин-2-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,20-7,57 (6H, м), 7,64-7,77 (2H, м), 7,96-8,54 (2H, м), 8,64-9,14 (4H, м).
Пример 30a
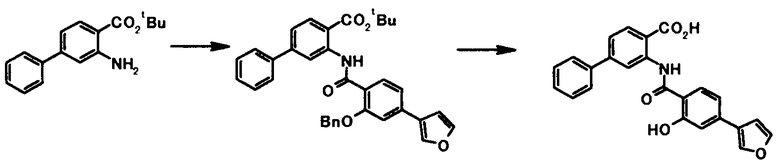
К 2-(бензилокси)-4-(фуран-3-ил)бензойной кислоте (0,099 г) добавляли хлористый метилен (2 мл), при охлаждении на льду последовательно добавляли N,N-диметилформамид (3 мкл) и оксалилхлорид (0,043 мл), затем перемешивали при той же температуре в течение 10 минут, а затем при комнатной температуре в течение 50 минут. К реакционной смеси при комнатной температуре добавляли оксалилхлорид (0,043 мл), а затем перемешивали при той же температуре в течение 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь при охлаждении на льду добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,075 г) в смеси пиридина (0,057 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 1 моль/л соляную кислоту и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-80% гексан/этилацетат] и дополнительно очищали по методу колоночной хроматографии на силикагеле [элюент: толуол] с получением 0,077 г трет-бутил-2-(2-(бензилокси)-4-(фуран-3-ил)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К полученному трет-бутил-2-(2-(бензилокси)-4-(фуран-3-ил)бензамидо)-4-фенилбензоату (0,076 г) добавляли тиоанизол (0,82 мл) и трифторуксусную кислоту (2,6 мл), а затем перемешивали при комнатной температуре в течение 3 часов 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 2 моль/л водный раствор гидроксида натрия и толуол. Водный слой разделяли и корректировали значение pH до 4,5 добавлением 6 моль/л соляной кислоты. Твердое вещество собирали путем фильтрования с получением 0,016 г 2-(4-(фуран-3-ил)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде коричневого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 6,98 (1H, с), 7,23 (1H, с), 7,28 (1H, д, J=8,3 Гц), 7,41-7,59 (4H, м), 7,68-7,82 (3H, м), 7,92 (1H, д, J=8,3 Гц), 8,11 (1H, д, J=8,3 Гц), 8,29 (1H, с), 8,99 (1H, с), 11,73 (1H, с), 12,38 (1H, с), 13,30-13,80 (1H, уширенный).
Пример 31a
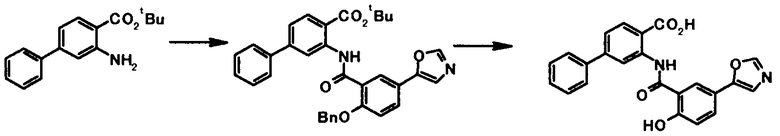
К суспензии 2-(бензилокси)-5-(оксазол-5-ил)бензойной кислоты (0,18 г) в хлористом метилене (2 мл) последовательно добавляли N,N-диметилформамид (4,6 мкл) и оксалилхлорид (0,077 мл), а затем перемешивали при той же температуре в течение 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,14 г) в смеси пиридина (0,10 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 1 часа 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 1 моль/л соляную кислоту, воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 70-50% гексан/этилацетат] с получением 0,22 г трет-бутил-2-(2-(бензилокси)-5-(оксазол-5-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному трет-бутил-2-(2-(бензилокси)-5-(оксазол-5-ил)бензамидо)-4-фенилбензоату (0,21 г) добавляли тиоанизол (2,3 мл) и трифторуксусную кислоту (7,7 мл), а затем перемешивали при комнатной температуре в течение 9 часов 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку метанол. Твердое вещество собирали путем фильтрования с получением 0,12 г 2-(2-гидрокси-5-(оксазол-5-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,14 (1H, д, J=8,8 Гц), 7,42-7,64 (5H, м), 7,69-7,87 (3H, м), 8,11 (1H, д, J=8,1 Гц), 8,28 (1H, с), 8,42 (1H, с), 9,07 (1H, с), 11,80 (1H, с), 12,38 (1H, с), 13,35-13,70 (1H, уширенный).
Пример 32a
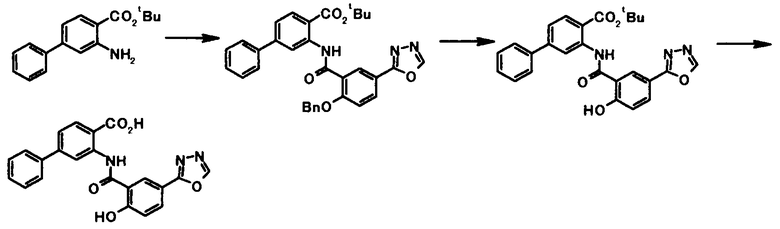
К суспензии 2-(бензилокси)-5-(1,3,4-оксадиазол-2-ил)бензойной кислоты (0,069 г) в хлористом метилене (1,2 мл) последовательно добавляли N,N-диметилформамид (1,8 мкл) и оксалилхлорид (0,030 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1,2 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,060 г) в смеси пиридина (0,045 мл) и хлористого метилена (1,2 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 10% водный раствор лимонной кислоты, органический слой разделяли, и очищали полученный органический слой по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-60% гексан/этилацетат] с получением 0,099 г трет-бутил-2-(2-(бензилокси)-5-(1,3,4-оксадиазол-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного в трет-бутил-2-(2-(бензилокси)-5-(1,3,4-оксадиазол-2-ил)бензамидо)-4-фенилбензоата (0,049 г) в смеси этилацетата (1 мл) и метанола (1 мл) добавляли 10% палладированый уголь (25 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли этилацетат, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,034 г трет-бутил-2-(2-гидрокси-5-(1,3,4-оксадиазол-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-5-(1,3,4-оксадиазол-2-ил)бензамидо)-4-фенилбензоата (0,034 г) в трифторуксусной кислоте (5 мл) перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,027 г 2-(2-гидрокси-5-(1,3,4-оксадиазол-2-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР(DMSO-d6) δ: 7,24 (1H, д, J=8,8 Гц), 7,43-7,51 (1H, м), 7,51-7,59 (3H, м), 7,71-7,78 (2H, м), 8,06-8,14 (2H, м), 8,61 (1H, д, J=2,2 Гц), 9,06 (1H, д, J=1,7 Гц), 9,31 (1H, с), 12,30 (1H, с), 12,43 (1H, с), 13,40-13,62 (1H, уширенный).
Пример 33a
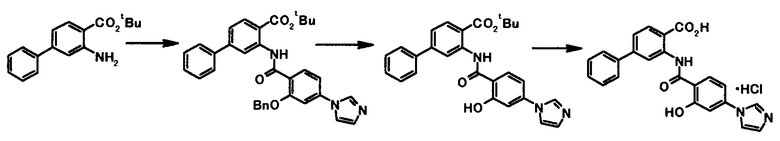
К суспензии гидрохлорида 2-(бензилокси)-4-(1H-имидазол-1-ил)бензойной кислоты (0,086 г) в хлористом метилене (1,4 мл) последовательно добавляли N,N-диметилформамид (2,0 мкл) и оксалилхлорид (0,033 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1,4 мл). Полученную смесь добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,070 г) в смеси пиридина (0,053 мл) и хлористого метилена (1,4 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный органический слой очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-20% гексан/этилацетат] с получением 0,12 г трет-бутил-2-(2-(бензилокси)-4-(1H-имидазол-1-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-4-(1H-имидазол-1-ил)бензамидо)-4-фенилбензоата (0,12 г) в смеси этилацетата (3,6 мл), метанола (1,8 мл) и диоксана (1,8 мл) добавляли 10% палладированый уголь (61 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли 10% палладированый уголь (30 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли хлороформ, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: хлороформ] с получением 0,084 г трет-бутил-2-(2-гидрокси-4-(1H-имидазол-1-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-4-(1H-имидазол-1-ил)бензамидо)-4-фенилбензоата (0,084 г) в трифторуксусной кислоте (5 мл) перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку диоксан (2 мл) и 4 моль/л раствор хлорводорода в диоксане (0,5 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Твердое вещество собирали путем фильтрования с получением 0,064 г 2-(2-гидрокси-4-(1H-имидазол-1-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,38-7,50 (3H, м), 7,51-7,59 (3H, м), 7,71-7,77 (2H, м), 7,84-7,88 (1H, м), 8,12 (1H, д, J=8,3 Гц), 8,13 (1H, д, J=8,5 Гц), 8,26 (1H, дд, J=1,7, 1,7 Гц), 9,02 (1H, д, J=1,7 Гц), 9,60 (1H, с), 12,23 (1H, с), 12,36 (1H, с).
Пример 34a
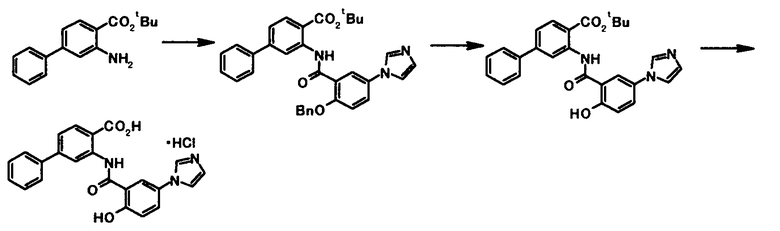
Следующее соединение получали, как описано в Примере 33a.
2-(2-Гидрокси-5-(1H-имидазол-1-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 7,27 (1H, д, J=8,8 Гц), 7,43-7,50 (1H, м), 7,51-7,58 (3H, м), 7,70-7,76 (2H, м), 7,83 (1H, дд, J=8,8, 2,9 Гц), 7,85-7,89 (1H, м), 8,11 (1H, д, J=8,3 Гц), 8,23 (1H, дд, J=1,7, 1,7 Гц), 8,29 (1H, д, J=2,9 Гц), 9,09 (1H, д, J=1,7 Гц), 9,58 (1H, с), 12,08 (1H, с), 12,42 (1H, с).
Пример 35a
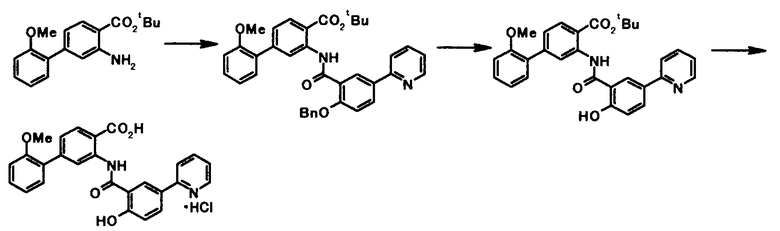
Следующее соединение получали, как описано в Примере 33a.
2-(2-Гидрокси-5-(пиридин-2-ил)бензамидо)-4-(2-метоксифенил)бензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 3,81 (3H, с), 7,06-7,12 (1H, м), 7,15-7,22 (2H, м), 7,32-7,46 (3H, м), 7,50-7,57 (1H, м), 8,05 (1H, д, J=8,3 Гц), 8,06-8,18 (2H, м), 8,16 (1H, дд, J=8,6, 2,3 Гц), 8,64 (1H, д, J=2,3 Гц), 8,69-8,73 (1H, м), 8,85 (1H, д, J=1,7 Гц), 11,99 (1H, с), 12,33 (1H, с).
Пример 36a
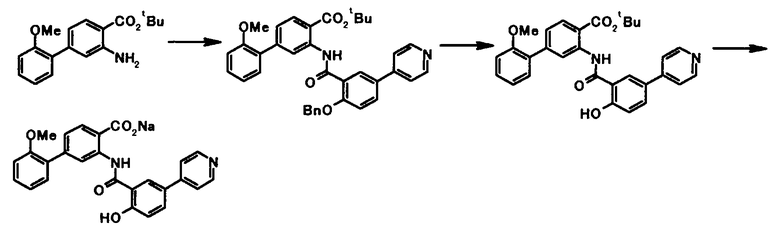
К суспензии 2-(бензилокси)-5-(пиридин-4-ил)бензойной кислоты (0,086 г) в хлористом метилене (1,5 мл) последовательно при охлаждении на льду добавляли N,N-диметилформамид (0,010 мл) и оксалилхлорид (0,031 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2,5 мл). Полученную смесь при охлаждении на льду добавляли к раствору трет-бутил-2-амино-4-(2-метоксифенил)бензоата (0,070 г) в смеси пиридина (0,028 мл) и хлористого метилена (1,0 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 50-0% гексан/этилацетат] с получением 0,094 г трет-бутил-2-(2-(бензилокси)-5-(пиридин-4-ил)бензамидо)-4-(2-метоксифенил)бензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(пиридин-4-ил)бензамидо)-4-(2-метоксифенил)бензоата (0,094 г) в смеси этилацетата (2,5 мл) и метанола (3,5 мл) добавляли 10% палладированый уголь (19 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. К реакционной смеси добавляли 10% палладированый уголь (19 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. Нерастворимые вещества удаляли путем фильтрования, и промывали остаток этилацетатом и тетрагидрофураном. Фильтрат и смывочную жидкость объединяли, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), PSQ100B(сферический), элюент: 65-45% гексан/этилацетат] с получением трет-бутил-2-(2-гидрокси-5-(пиридин-4-ил)бензамидо)-4-(2-метоксифенил)бензоата.
Раствор полученного трет-бутил-2-(2-гидрокси-5-(пиридин-4-ил)бензамидо)-4-(2-метоксифенил)бензоата в трифторуксусной кислоте (4,0 мл) перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,027 г 2-(2-гидрокси-5-(пиридин-4-ил)бензамидо)-4-(2-метоксифенил)бензойной кислоты в виде светло-желтого твердого вещества.
К полученной 2-(2-гидрокси-5-(пиридин-4-ил)бензамидо)-4-(2-метоксифенил)бензойной кислоте (0,027 г) добавляли диоксан (2,5 мл) и 2 моль/л водный раствор гидроксида натрия (0,031 мл), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. Твердое вещество собирали путем фильтрования с получением 0,012 г 2-(2-гидрокси-5-(пиридин-4-ил)бензамидо)-4-(2-метоксифенил)бензоата натрия в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 3,79 (3H, с), 7,02-7,16 (3H, м), 7,16-7,22 (1H, м), 7,30-7,41 (2H, м), 7,73-7,79 (2H, м), 7,97 (1H, дд, J=8,6, 2,2 Гц), 8,07 (1H, д, J=8,0 Гц), 8,53 (1H, с), 8,63-8,68 (2H, м), 8,68-8,71 (1H, м).
Пример 37a
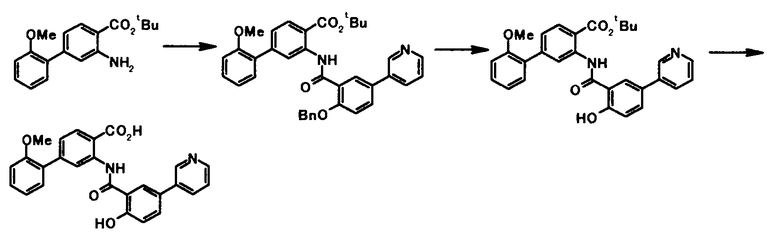
К суспензии 2-(бензилокси)-5-(пиридин-3-ил)бензойной кислоты (0,15 г) в тетрагидрофуране (2,0 мл) при охлаждении на льду последовательно добавляли N,N-диметилформамид (0,010 мл) и оксалилхлорид (0,053 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку тетрагидрофуран (3,0 мл). Полученную смесь при охлаждении на льду добавляли к раствору трет-бутил-2-амино-4-(2-метоксифенил)бензоата (0,12 г) в смеси пиридина (0,049 мл) и тетрагидрофурана (2,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 70-35% гексан/этилацетат] с получением 0,19 г трет-бутил-2-(2-(бензилокси)-5-(пиридин-3-ил)бензамидо)-4-(2-метоксифенил)бензоата в виде белого твердого вещества.
К раствору полученного в трет-бутил-2-(2-(бензилокси)-5-(пиридин-3-ил)бензамидо)-4-(2-метоксифенил)бензоата (0,19 г) в смеси этилацетата (5,0 мл) и метанола (5,0 мл) добавляли 10% палладированый уголь (39 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли 10% палладированый уголь (39 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 минут. К реакционной смеси добавляли тетрагидрофуран, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), PSQ100B (сферический), элюент: 100-91% хлороформ/метанол] с получением трет-бутил-2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)-4-(2-метоксифенил)бензоата в виде белого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)-4-(2-метоксифенил)бензоата в трифторуксусной кислоте (4,0 мл) перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли диоксан (2,0 мл) и 2 моль/л водный раствор гидроксида натрия (0,49 мл), а затем перемешивали при комнатной температуре в течение 45 минут. К реакционной смеси добавляли 10% водный раствор лимонной кислоты, и собирали твердое вещество путем фильтрования. К полученному твердому веществу добавляли этанол и воду, и собирали твердое вещество путем фильтрования с получением 0,053 г 2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)-4-(2-метоксифенил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 3,81 (3H, с), 7,06-7,12 (1H, м), 7,12-7,20 (2H, м), 7,33-7,39 (2H, м), 7,39-7,46 (1H, м), 7,46-7,52 (1H, м), 7,85 (1H, дд, J=8,6, 2,4 Гц), 8,02-8,10 (2H, м), 8,22 (1H, д, J=2,4 Гц), 8,55 (1H, дд, J=4,6, 1,5 Гц), 8,80 (1H, д, J=1,7 Гц), 8,90 (1H, д, J=1,9 Гц), 11,69-11,80 (1H, уширенный), 12,31-12,43 (1H, уширенный).
Пример 38a
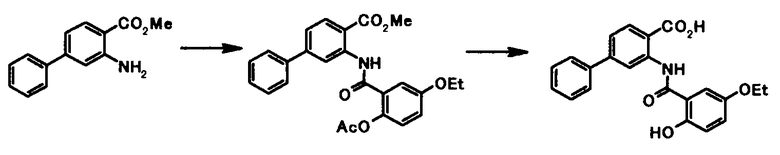
К суспензии 2-ацетокси-5-этоксибензойной кислоты (0,14 г) в хлористом метилене (2 мл) последовательно добавляли N,N-диметилформамид (4,6 мкл) и оксалилхлорид (0,077 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь добавляли к раствору метил-2-амино-4-фенилбензоата (0,11 г) в смеси пиридина (0,10 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 2 часов 10 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 90-70% гексан/этилацетат] с получением 0,082 г метил-2-(2-ацетокси-5-этоксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному метил-2-(2-ацетокси-5-этоксибензамидо)-4-фенилбензоату (0,082 г) добавляли метанол (4 мл) и 2 моль/л водный раствор гидроксида натрия (0,95 мл), затем перемешивали при комнатной температуре в течение 3 часов 30 минут, а затем нагревали до температуры возгонки в течение 30 минут. Реакционную смесь охлаждали до комнатной температуры и корректировали значение pH до 1,2 добавлением 6 моль/л соляной кислоты. Твердое вещество собирали путем фильтрования с получением 0,055 г 2-(5-этокси-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,33 (3H, т, J=6,9 Гц), 4,01 (2H, кв, J=6,9 Гц), 6,95 (1H, д, J=9,0 Гц), 7,07 (1H, дд, J=9,0, 3,2 Гц), 7,40-7,58 (5H, м), 7,70-7,78 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,01 (1H, д, J=1,7 Гц), 11,01 (1H, с), 12,33 (1H, с), 13,40-13,65 (1H, уширенный).
Пример 39a
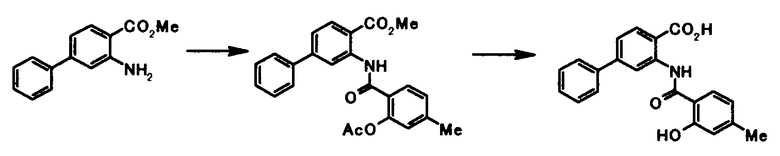
К раствору 2-ацетокси-4-метилбензойной кислоты (0,12 г) в хлористом метилене (2 мл) последовательно добавляли N,N-диметилформамид (4,6 мкл) и оксалилхлорид (0,077 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь добавляли к раствору метил-2-амино-4-фенилбензоата (0,11 г) в смеси пиридина (0,10 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 1 часа 10 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 90-70% гексан/этилацетат] с получением 0,14 г метил-2-(2-ацетокси-4-метилбензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному метил-2-(2-ацетокси-4-метилбензамидо)-4-фенилбензоату (0,14 г) добавляли диоксан (3 мл) и 2 моль/л водный раствор гидроксида натрия (1,7 мл), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. Значение pH реакционной смеси корректировали до 3,0 добавлением 6 моль/л соляной кислоты. Твердое вещество собирали путем фильтрования с получением 0,042 г 2-(2-гидрокси-4-метилбензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,31 (3H, с), 6,79-6,86 (2H, м), 7,42-7,58 (4H, м), 7,69-7,76 (2H, м), 7,80 (1H, д, J=7,8 Гц), 8,10 (1H, д, J=8,3 Гц), 9,00 (1H, д, J=1,7 Гц), 11,47 (1H, с), 12,29 (1H, с), 13,40-13,65 (1H, уширенный).
Пример 40a
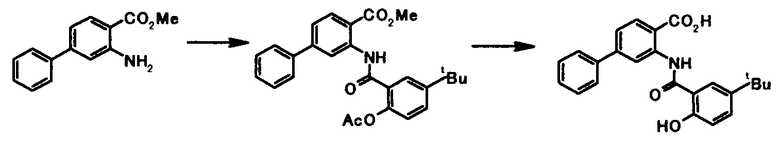
К раствору 2-ацетокси-5-трет-бутилбензойной кислоты (0,049 г) в хлористом метилене (1,5 мл) последовательно добавляли N,N-диметилформамид (2 мкл) и оксалилхлорид (0,026 мл), а затем перемешивали при комнатной температуре в течение 25 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь добавляли к раствору метил-2-амино-4-фенилбензоата (0,038 г) в смеси пиридина (0,034 мл) и хлористого метилена (1,5 мл), а затем перемешивали при комнатной температуре в течение 1 часа 15 минут. К реакционной смеси добавляли воду, 1 моль/л соляную кислоту и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 90-75% гексан/этилацетат] с получением 0,023 г метил-2-(2-ацетокси-5-трет-бутилбензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному метил-2-(2-ацетокси-5-трет-бутилбензамидо)-4-фенилбензоату (0,023 г) добавляли метанол (2 мл) и 2 моль/л водный раствор гидроксида натрия (0,26 мл), а затем перемешивали при комнатной температуре в течение 15 часов. К реакционной смеси добавляли толуол. Водный слой разделяли и корректировали значение pH до 3,0 добавлением 6 моль/л соляной кислоты. Твердое вещество собирали путем фильтрования с получением 0,010 г 2-(5-трет-бутил-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,31 (9H, с), 6,96 (1H, д, J=8,5 Гц), 7,42-7,60 (5H, м), 7,70-7,79 (2H, м), 7,93 (1H, д, J=2,4 Гц), 8,11 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,7 Гц), 11,35 (1H, с), 12,42 (1H, с), 13,45-13,80 (1H, уширенный).
Пример 41a
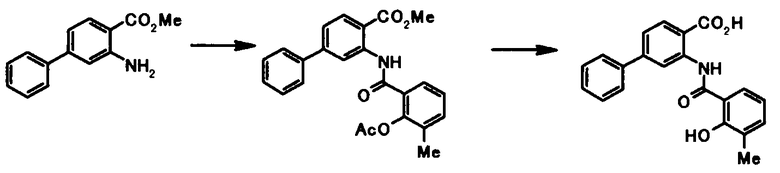
К раствору 2-ацетокси-3-метилбензойной кислоты (0,12 г) в хлористом метилене (2 мл) последовательно добавляли N,N-диметилформамид (4,6 мкл) и оксалилхлорид (0,077 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь добавляли к раствору метил-2-амино-4-фенилбензоата (0,11 г) в смеси пиридина (0,10 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 20 минут. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [элюент: 85-70% гексан/этилацетат] с получением 0,063 г метил-2-(2-ацетокси-3-метилбензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному метил-2-(2-ацетокси-3-метилбензамидо)-4-фенилбензоату (0,062 г) добавляли метанол (2 мл), диоксан (4 мл) и 2 моль/л водный раствор гидроксида натрия (0,77 мл), а затем перемешивали при комнатной температуре в течение 7 часов. Значение pH реакционной смеси корректировали до 1,1 добавлением 6 моль/л соляной кислоты. Твердое вещество собирали путем фильтрования с получением 0,044 г 2-(2-гидрокси-3-метилбензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,22 (3H, с), 6,95 (1H, дд, J=7,6, 7,6 Гц), 7,38-7,51 (2H, м), 7,51-7,63 (3H, м), 7,66-7,80 (3H, м), 8,14 (1H, д, J=8,3 Гц), 8,83-8,89 (1H, м), 8,85 (1H, с), 12,24 (1H, с), 12,34-12,46 (1H, уширенный).
Пример 42a
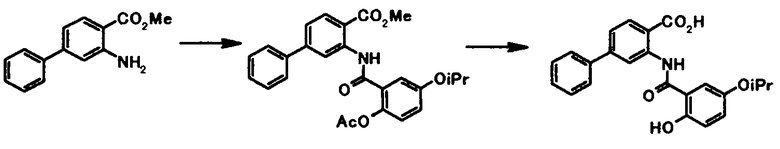
При охлаждении на льду к раствору 2-ацетокси-5-изопропоксибензойной кислоты (0,081 г) в смеси хлористого метилена (2,0 мл) и N,N-диметилформамида (0,010 мл) добавляли оксалилхлорид (0,040 мл), а затем перемешивали при комнатной температуре в течение 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2,0 мл). Полученную смесь при охлаждении на льду добавляли к раствору метил-2-амино-4-фенилбензоата (0,070 г) в смеси пиридина (0,037 мл) и хлористого метилена (1,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 45 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-80% гексан/этилацетат] с получением 0,072 г метил-2-(2-ацетокси-5-изопропоксибензамидо)-4--фенилбензоата в виде белого твердого вещества.
К полученному метил-2-(2-ацетокси-5-изопропоксибензамидо)-4-фенилбензоату (0,072 г) добавляли диоксан (5,0 мл) и 4 моль/л водный раствор гидроксида натрия (0,20 мл), а затем перемешивали при 50-60°C в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней 4 моль/л водный раствор гидроксида натрия (0,081 мл), а затем перемешивали при 55-60°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней 4 моль/л водный раствор гидроксида натрия (0,040 мл), а затем перемешивали при 60°C в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты (9 мл). Твердое вещество собирали путем фильтрования с получением 0,039 г 2-(2-гидрокси-5-изопропоксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,23-1,29 (6H, м), 4,45-4,56 (1H, м), 6,94 (1H, д, J=8,8 Гц), 7,03-7,10 (1H, м), 7,40-7,49 (2H, м), 7,49-7,58 (3H, м), 7,70-7,77 (2H, м), 8,10 (1H, д, J=8,3 Гц), 8,98-9,04 (1H, м), 11,03 (1H, с), 12,32 (1H, с), 13,40-13,64 (1H, уширенный).
Пример 43a
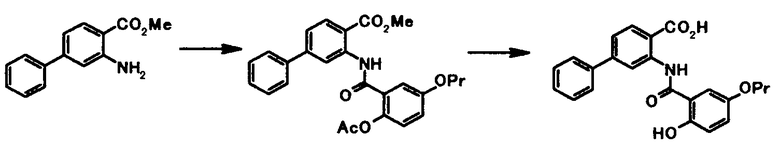
Следующее соединение получали, как описано в Примере 42a.
2-(2-Гидрокси-5-пропоксибензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 0,99 (3H, т, J=7,4 Гц), 1,66-1,79 (2H, м), 3,91 (2H, т, J=6,5 Гц), 6,95 (1H, д, J=8,8 Гц), 7,04-7,11 (1H, м), 7,41-7,49 (2H, м), 7,49-7,58 (3H, м), 7,69-7,77 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,01 (1H, с), 11,02 (1H, с), 12,33 (1H, с).
Пример 44a
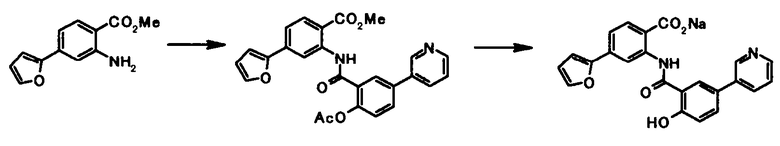
К суспензии 2-ацетокси-5-(пиридин-3-ил)бензойная кислота (0,15 г) в хлористом метилене (2 мл) добавляли N,N-диметилформамид (5 мкл) и оксалилхлорид (0,077 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь добавляли к раствору метил-2-амино-4-(фуран-2-ил)бензоата (0,11 г) в смеси пиридина (0,14 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 55-20% гексан/этилацетат] с получением 0,18 г метил-2-(2-ацетокси-5-(пиридин-3-ил)бензамидо)-4-(фуран-2-ил)бензоата в виде белого твердого вещества.
К полученному метил-2-(2-ацетокси-5-(пиридин-3-ил)бензамидо)-4-(фуран-2-ил)бензоату (0,18 г) добавляли диоксан (3 мл) и 2 моль/л водный раствор гидроксида натрия (0,19 мл), затем перемешивали при комнатной температуре в течение 3 часов 10 минут, а затем при 70°C в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, и корректировали значение pH до 6,0 добавлением 10% водного раствора лимонной кислоты. Твердое вещество собирали путем фильтрования, и добавляли к нему метанол (1,0 мл) и 1 моль/л водный раствор гидроксида натрия (0,055 мл). Твердое вещество собирали путем фильтрования с получением 0,044 г 4-(фуран-2-ил)-2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,62 (1H, дд, J=3,4, 2,0 Гц), 6,96 (1H, д, J=3,4 Гц), 7,10 (1H, д, J=8,7 Гц), 7,42 (1H, дд, J=8,1, 1,7 Гц), 7,52 (1H, ддд, J=7,9, 4,8, 0,7 Гц), 7,78-7,83 (1H, м), 7,89 (1H, дд, J=8,7, 2,3 Гц), 8,08 (1H, д, J=8,1 Гц), 8,08-8,15 (1H, м), 8,41 (1H, д, J=2,2 Гц), 8,58 (1H, дд, J=4,8, 1,6 Гц), 8,92-8,99 (2H, м).
Пример 45a
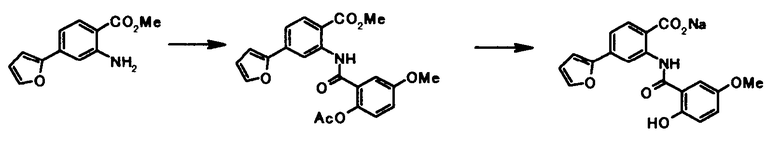
При охлаждении на льду к раствору 2-ацетокси-5-метоксибензойной кислоты (0,070 г) в смеси хлористого метилена (1,0 мл) и N,N-диметилформамида (0,010 мл) добавляли оксалилхлорид (0,036 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь при охлаждении на льду добавляли к раствору метил-2-амино-4-(фуран-2-ил)бензоата (0,060 г) в смеси пиридина (0,034 мл) и хлористого метилена (1,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 0,073 г метил-2-(2-ацетокси-5-метоксибензамидо)-4-(фуран-2-ил)бензоата в виде белого твердого вещества.
К полученному метил-2-(2-ацетокси-5-метоксибензамидо)-4-(фуран-2-ил)бензоат (0,073 г) добавляли диоксан (2,0 мл) и 4 моль/л водный раствор гидроксида натрия (0,22 мл), а затем перемешивали при 50-55°C в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты (6 мл). Твердое вещество собирали путем фильтрования с получением 0,062 г 4-(фуран-2-ил)-2-(2-гидрокси-5-метоксибензамидо)бензойной кислоты в виде белого твердого вещества.
К полученной 4-(фуран-2-ил)-2-(2-гидрокси-5-метоксибензамидо)бензойной кислоте (0,062 г) добавляли этанол (2,5 мл) и 1 моль/л водный раствор гидроксида натрия (0,17 мл), а затем перемешивали при комнатной температуре в течение 35 минут. Твердое вещество собирали путем фильтрования с получением 0,046 г 4-(фуран-2-ил)-2-(2-гидрокси-5-метоксибензамидо)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 3,78 (3H, с), 6,62 (1H, дд, J=3,4, 1,8 Гц), 6,90 (1H, д, J=9,0 Гц), 6,95 (1H, д, J=3,4 Гц), 7,10 (1H, дд, J=9,0, 3,0 Гц), 7,40 (1H, дд, J=8,0, 1,7 Гц), 7,58 (1H, д, J=3,0 Гц), 7,78-7,82 (1H, м), 8,06 (1H, д, J=8,0 Гц), 8,94 (1H, д, J=1,7 Гц).
Пример 46a
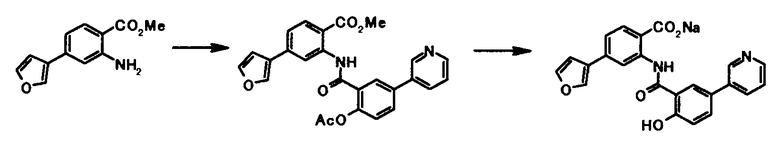
К суспензии 2-ацетокси-5-(пиридин-3-ил)бензойной кислоты (0,14 г) в тетрагидрофуране (4,0 мл) добавляли N,N-диметилформамид (0,010 мл) и оксалилхлорид (0,060 мл), а затем перемешивали при комнатной температуре в течение 50 минут. К реакционной смеси добавляли оксалилхлорид (0,060 мл), а затем перемешивали при комнатной температуре в течение 40 минут. К реакционной смеси добавляли оксалилхлорид (0,020 мл), а затем перемешивали при комнатной температуре в течение 15 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку тетрагидрофуран (3,0 мл). Полученную смесь при охлаждении на льду добавляли к раствору метил-2-амино-4-(фуран-3-ил)бензоата (0,10 г) в смеси пиридина (0,093 мл) и тетрагидрофурана (1,0 мл), а затем перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли и промывали насыщенным водным раствором хлорида натрия. Нерастворимые вещества удаляли путем фильтрования. Полученный фильтрат сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир и этилацетат. Твердое вещество собирали путем фильтрования с получением 0,11 г метил-2-(2-ацетокси-5-(пиридин-3-ил)бензамидо)-4-(фуран-3-ил)бензоата в виде белого твердого вещества.
К полученному метил-2-(2-ацетокси-5-(пиридин-3-ил)бензамидо)-4-(фуран-3-ил)бензоату (0,11 г) добавляли диоксан (5,0 мл) и 4 моль/л водный раствор гидроксида натрия (0,31 мл), а затем перемешивали при 50-55°C в течение 1 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты (6 мл). Твердое вещество собирали путем фильтрования с получением 0,081 г 4-(фуран-3-ил)-2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)бензойной кислоты в виде желтого твердого вещества.
К полученной 4-(фуран-3-ил)-2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)бензойной кислоте (0,081 г) добавляли этанол (1,5 мл) и 1 моль/л водный раствор гидроксида натрия (0,19 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Твердое вещество собирали путем фильтрования с получением 0,048 г 4-(фуран-3-ил)-2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,92-6,98 (1H, м), 7,13 (1H, д, J=8,5 Гц), 7,40 (1H, дд, J=8,1, 1,5 Гц), 7,50 (1H, дд, J=7,9, 4,7 Гц), 7,80 (1H, с), 7,87 (1H, дд, J=8,5, 2,2 Гц), 8,03-8,13 (1H, м), 8,06 (1H, д, J=8,3 Гц), 8,24 (1H, с), 8,34 (1H, д, J=1,7 Гц), 8,51-8,60 (1H, м), 8,83 (1H, д, J=1,4 Гц), 8,91-8,97 (1H, м).
Пример 47a
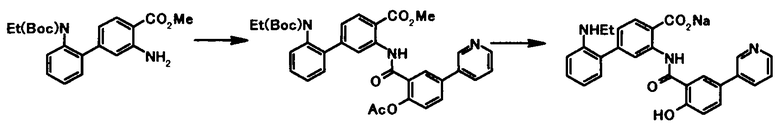
При охлаждении на льду к раствору 2-ацетокси-5-(пиридин-3-ил)бензойной кислоты (0,083 г) в смеси тетрагидрофурана (2,0 мл) и N,N-диметилформамида (0,010 мл) добавляли оксалилхлорид (0,035 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку тетрагидрофуран (3,0 мл). Полученную смесь при охлаждении на льду добавляли к раствору метил-2-амино-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)бензоата (0,10 г) в смеси пиридина (0,054 мл) и тетрагидрофурана (1,5 мл), а затем перемешивали при комнатной температуре в течение 1 часа 40 минут. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 70-45% гексан/этилацетат] с получением метил-2-(2-ацетокси-5-(пиридин-3-ил)бензамидо)-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)бензоата.
Раствор полученного метил-2-(2-ацетокси-5-(пиридин-3-ил)бензамидо)-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)бензоата в трифторуксусной кислоте (4,0 мл) перемешивали при комнатной температуре в течение 2 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли диоксан (4,0 мл) и 1 моль/л водный раствор гидроксида натрия (0,40 мл), а затем перемешивали при 50-55°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем корректировали значение pH до 7,4 добавлением 1 моль/л соляной кислоты. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. Твердое вещество собирали путем фильтрования с получением 0,032 г 4-(2-(этиламино)фенил)-2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)бензойной кислоты в виде белого твердого вещества.
К полученной 4-(2-(этиламино)фенил)-2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)бензойной кислоте (0,032 г) добавляли этанол (2,0 мл) и 1 моль/л водный раствор гидроксида натрия (0,067 мл), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. Твердое вещество собирали путем фильтрования с получением 0,024 г 4-(2-(этиламино)фенил)-2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,12 (3H, т, J=7,1 Гц), 3,06-3,15 (2H, м), 4,49 (1H, т, J=5,5 Гц), 6,65-6,72 (2H, м), 7,02-7,11 (3H, м), 7,16-7,22 (1H, м), 7,53 (1H, дд, J=7,9, 4,8 Гц), 7,84-7,92 (1H, м), 8,08-8,15 (2H, м), 8,39-8,45 (1H, м), 8,55-8,63 (2H, м), 8,93-8,99 (1H, м).
Пример 48a
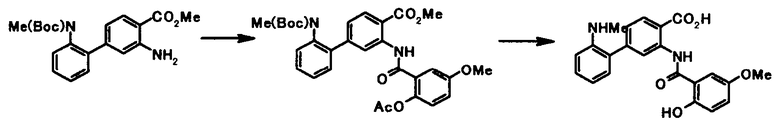
При охлаждении на льду к раствору 2-ацетокси-5-метоксибензойной кислоты (0,049 г) в смеси хлористого метилена (1,0 мл) и N,N-диметилформамида (0,010 мл) добавляли оксалилхлорид (0,026 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2,0 мл). Полученную смесь при охлаждении на льду добавляли к раствору метил-2-амино-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)бензоата (0,070 г) в смеси пиридина (0,024 мл) и хлористого метилена (1,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 91-60% гексан/этилацетат] с получением метил-2-(2-ацетокси-5-метоксибензамидо)-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)бензоата.
Раствор полученного метил-2-(2-ацетокси-5-метоксибензамидо)-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)бензоата в трифторуксусной кислоте (3,0 мл) перемешивали при комнатной температуре в течение 1 часа 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диоксан (3,0 мл) и 4 моль/л водный раствор гидроксида натрия (0,25 мл), затем перемешивали при 50-55°C в течение 1 часа 30 минут, а затем при 55-60°C в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду. После корректировки значения pH до 7,0 добавлением 1 моль/л соляной кислоты растворитель выпаривали в условиях пониженного давления. К полученному остатку добавляли воду, и собирали твердое вещество путем фильтрования с получением 0,025 г 2-(2-гидрокси-5-метоксибензамидо)-4-(2-(метиламино)фенил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,69 (3H, с), 3,75 (3H, с), 4,80-5,10 (1H, уширенный), 6,65 (1H, д, J=8,1 Гц), 6,70 (1H, дд, J=7,4, 7,4 Гц), 6,95 (1H, д, J=8,8 Гц), 7,01-7,10 (2H, м), 7,19-7,27 (2H, м), 7,40 (1H, д, J=3,2 Гц), 8,06 (1H, д, J=8,0 Гц), 8,70 (1H, д, J=1,2 Гц), 10,99 (1H, с), 12,32-12,43 (1H, уширенный), 13,24-13,66 (1H, уширенный).
Пример 49a
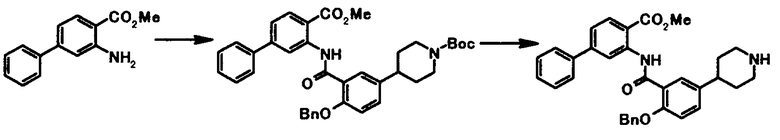
К раствору 2-(бензилокси)-5-(1-(трет-бутоксикарбонил)пиперидин-4-ил)бензойной кислоты (0,30 г) в хлористом метилене (3,0 мл) добавляли N,N-диметилформамид (5 мкл) и оксалилхлорид (0,093 мл), а затем перемешивали при комнатной температуре в течение 65 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (3,0 мл). Полученную смесь при охлаждении на льду добавляли к раствору метил-2-амино-4-фенилбензоата (0,14 г) в смеси пиридина (0,12 мл) и хлористого метилена (3,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 85-60% гексан/этилацетат] с получением 0,19 г метил-2-(2-(бензилокси)-5-(1-(трет-бутоксикарбонил)пиперидин-4-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-(1-(трет-бутоксикарбонил)пиперидин-4-ил)бензамидо)-4-фенилбензоата (0,19 г) в хлороформе (2,0 мл) добавляли трифторуксусную кислоту (1,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду. После корректировки значения pH до 7,4 добавлением насыщенного водного раствора бикарбоната натрия добавляли хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления с получением 0,15 г метил-2-(2-(бензилокси)-5-(пиперидин-4-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 1,50-1,92 (4H, м), 2,56-2,80 (3H, м), 3,10-3,26 (2H, м), 3,75 (3H, с), 5,42 (2H, с), 6,95 (1H, д, J=8,6 Гц), 7,20-7,52 (10H, м), 7,70-7,78 (2H, м), 8,02 (1H, д, J=2,4 Гц), 8,07 (1H, д, J=8,3 Гц), 9,29 (1H, д, J=1,7 Гц), 12,27 (1H, с).
Пример 50a
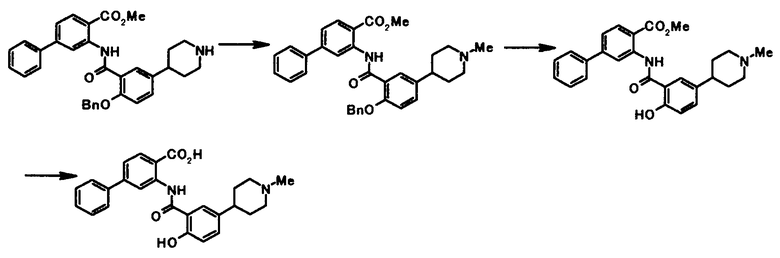
К раствору метил-2-(2-(бензилокси)-5-(пиперидин-4-ил)бензамидо)-4-фенилбензоата (0,10 г) в тетрагидрофуране (3,0 мл) последовательно добавляли 37% водный раствор формальдегида (6,3 мкл), уксусную кислоту (0,022 мл) и триацетоксиборгидрид натрия (0,10 г), а затем перемешивали при комнатной температуре в течение 3 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и хлороформ. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 98-90% хлороформ/метанол] с получением 0,086 г метил-2-(2-(бензилокси)-5-(1-метилпиперидин-4-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-(1-метилпиперидин-4-ил)бензамидо)-4-фенилбензоата (0,086 г) в метаноле (3,0 мл) добавляли 10% палладированый уголь (43 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 10 минут. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли этилацетат, и собирали твердое вещество путем фильтрования с получением 0,058 г метил-2-(2-гидрокси-5-(1-метилпиперидин-4-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К суспензии полученного метил-2-(2-гидрокси-5-(1-метилпиперидин-4-ил)бензамидо)-4-фенилбензоата (0,058 г) в метаноле (2,0 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (0,33 мл), а затем перемешивали при 60°C в течение 9 часов 20 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 6 моль/л соляную кислоту (0,11 мл). Растворитель выпаривали в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% хлороформ/метанол] с получением 0,019 г 2-(2-гидрокси-5-(1-метилпиперидин-4-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,83-2,11 (4H, м), 2,66-2,85 (4H, м), 2,87-3,11 (2H, м), 6,94 (1H, д, J=8,6 Гц), 7,33-7,44 (3H, м), 7,46-7,54 (2H, м), 7,64-7,72 (2H, м), 7,87-7,96 (1H, м), 8,13 (1H, д, J=8,0 Гц), 8,91 (1H, д, J=1,7 Гц).
1H-ЯМР (CF3COD) δ: 2,18-2,43 (4H, м), 2,95-3,38 (6H, м), 3,84-4,06 (2H, м), 7,17-7,29 (1H, м), 7,46-7,89 (8H, м), 8,38-8,50 (1H, м), 8,79-8,90 (1H, м).
Пример 51a
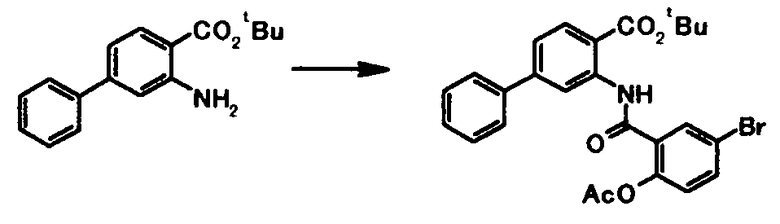
К суспензии 2-ацетокси-5-бромбензойной кислоты (5,0 г) в хлористом метилене (49 мл) добавляли N,N-диметилформамид (0,15 мл) и оксалилхлорид (2,5 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (10 мл). Полученную смесь при охлаждении на льду добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (4,9 г) в смеси пиридина (3,7 мл) и хлористого метилена (49 мл), а затем перемешивали при комнатной температуре в течение 30 минут. К реакционной смеси добавляли 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-80% гексан/этилацетат] с получением 8,9 г трет-бутил-2-(2-ацетокси-5-бромбензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 1,62 (9H, с), 2,30 (3H, с), 7,11 (1H, д, J=8,7 Гц), 7,36 (1H, дд, J=8,3, 1,8 Гц), 7,36-7,44 (1H, м), 7,44-7,51 (2H, м), 7,63 (1H, дд, J=8,7, 2,4 Гц), 7,67-7,73 (2H, м), 8,05 (1H, д, J=2,4 Гц), 8,07 (1H, д, J=8,3 Гц), 9,12 (1H, д, J=1,8 Гц), 11,89 (1H, с).
Примеры 52a-57a
Соединения, представленные в Таблице 12a, получали, как описано в Примере 51a.
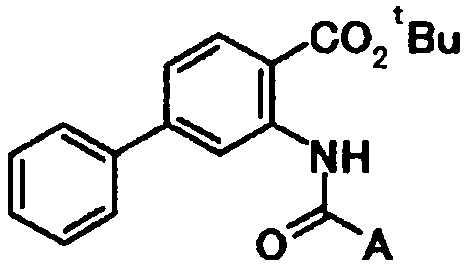
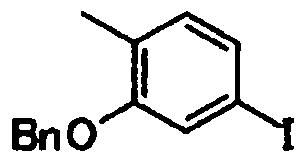
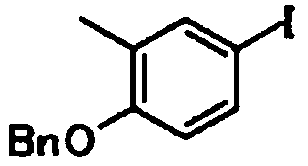
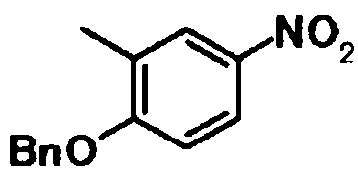
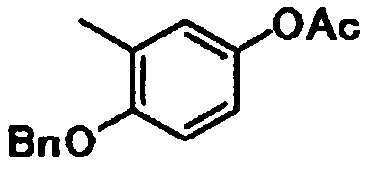
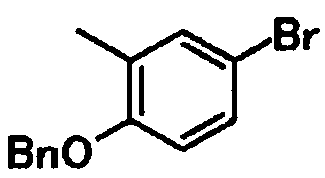
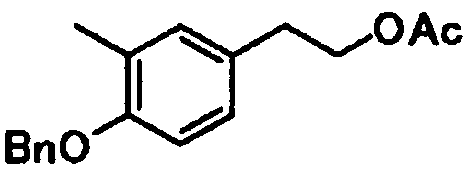
трет-Бутил-2-(2-(бензилокси)-4-йодбензамидо)-4-фенилбензоат
1H-ЯМР (DMSO-d6) δ: 1,49 (9H, с), 5,52 (2H, с), 7,25-7,37 (3H, м), 7,43-7,58 (7H, м), 7,61 (1H, д, J=1,2 Гц), 7,66-7,75 (3H, м), 8,05 (1H, д, J=8,3 Гц), 9,01-9,06 (1H, м), 12,08 (1H, с).
трет-Бутил-2-(2-(бензилокси)-5-нитробензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 1,55 (9H, с), 5,61 (2H, с), 7,05 (1H, д, J=9,3 Гц), 7,28-7,44 (5H, м), 7,44-7,53 (4H, м), 7,70-7,76 (2H, м), 8,09 (1H, д, J=8,3 Гц), 8,23 (1H, дд, J=9,3, 2,9 Гц), 9,09 (1H, д, J=2,9 Гц), 9,29 (1H, д, J=1,7 Гц), 12,60 (1H, с).
трет-Бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 1,53 (9H, с), 5,48 (2H, с), 6,83 (1H, д, J=8,8 Гц), 7,22-7,50 (10H, м), 7,70-7,75 (2H, м), 8,06 (1H, д, J=8,3 Гц), 8,29 (1H, д, J=2,7 Гц), 9,26 (1H, д, J=1,7 Гц), 12,49 (1H, с).
трет-Бутил-2-(2-(бензилокси)-5-йодбензамидо)-4-фенилбензоат
1H-ЯМР (DMSO-d6) δ: 1,50 (9H, с), 5,51 (2H, с), 7,08 (1H, д, J=8,8 Гц), 7,24-7,36 (3H, м), 7,44-7,58 (6H, м), 7,68-7,75 (2H, м), 7,81 (1H, дд, J=8,8, 2,3 Гц), 8,05 (1H, д, J=8,3 Гц), 8,21 (1H, д, J=2,3 Гц), 9,00-9,06 (1H, м), 12,15 (1H, с).
трет-Бутил-2-(5-ацетокси-2-(бензилокси)бензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 1,53 (9H, с), 2,28 (3H, с), 5,48 (2H, с), 6,94 (1H, д, J=9,0 Гц), 7,09 (1H, дд, J=9,0, 3,0 Гц), 7,24-7,51 (9H, м), 7,69-7,75 (2H, м), 7,89 (1H, д, J=3,0 Гц), 8,05 (1H, д, J=8,3 Гц), 9,25 (1H, д, J=1,9 Гц), 12,52 (1H, с).
трет-Бутил-2-(5-(2-ацетоксиэтил)-2-(бензилокси)бензамидо)-4-фенилбензоат
1H-ЯМР (DMSO-d6) δ: 1,49 (9H, с), 1,97 (3H, с), 2,88 (2H, т, J=6,8 Гц), 4,19 (2H, т, J=6,8 Гц), 5,48 (2H, с), 7,17 (1H, д, J=8,7 Гц), 7,23-7,36 (3H, м), 7,39 (1H, дд, J=8,7, 2,4 Гц), 7,43-7,59 (6H, м), 7,69-7,75 (2H, м), 7,84 (1H, д, J=2,4 Гц), 8,05 (1H, д, J=8,3 Гц), 9,06-9,11 (1H, м), 12,16 (1H, с).
Пример 58a
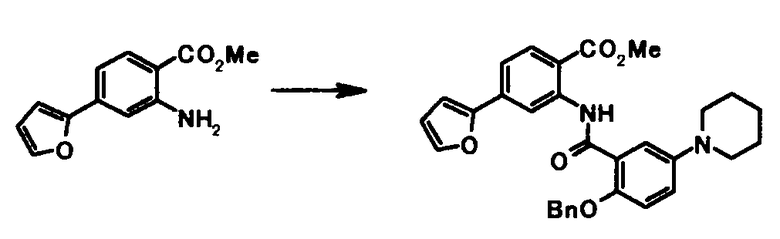
Следующее соединение получали, как описано в Примере 51a.
Метил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-(фуран-2-ил)бензоат
1H-ЯМР (CDCl3) δ: 1,40-2,50 (6H, м), 3,10-3,60 (4H, м), 3,77 (3H, с), 5,46 (2H, с), 6,53 (1H, дд, J=3,4, 1,6 Гц), 6,89 (1H, д, J=3,4 Гц), 6,98-7,12 (1H, м), 7,25-7,37 (4H, м), 7,40-7,49 (3H, м), 7,52-7,58 (1H, м), 8,00-8,22 (1H, м), 8,05 (1H, д, J=8,3 Гц), 9,30 (1H, д, J=1,4 Гц), 12,43 (1H, с).
Пример 59a
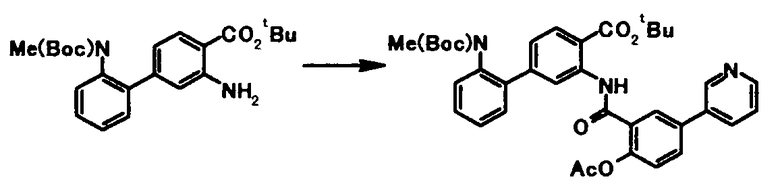
Следующее соединение получали, как описано в Примере 51a.
трет-Бутил-2-(2-ацетокси-5-(пиридин-3-ил)бензамидо)-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)бензоат
1H-ЯМР (CDCl3) δ: 1,21 (9H, с), 1,63 (9H, с), 2,32 (3H, с), 3,10 (3H, с), 7,05-7,13 (1H, м), 7,18-7,29 (1H, м), 7,31-7,48 (5H, м), 7,74 (1H, дд, J=8,4, 2,3 Гц), 7,95 (1H, ддд, J=7,9, 2,4, 1,7 Гц), 8,04 (1H, д, J=8,3 Гц), 8,15 (1H, д, J=2,2 Гц), 8,63 (1H, дд, J=4,8, 1,6 Гц), 8,88-8,98 (2H, м), 12,06 (1H, с).
Пример 60a
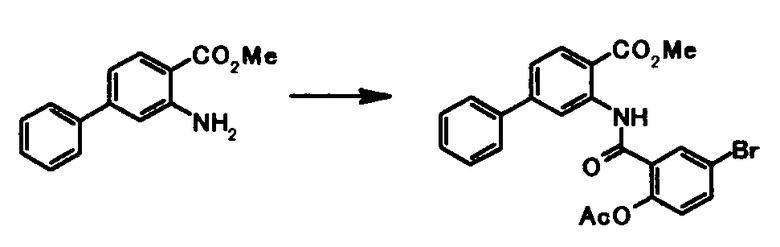
К суспензии 2-ацетокси-5-бромбензойной кислоты (0,16 г) в хлористом метилене (2 мл) добавляли N,N-диметилформамид (5 мкл) и оксалилхлорид (0,077 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Полученную смесь добавляли к раствору метил-2-амино-4-фенилбензоата (0,11 г) в смеси пиридина (0,10 мл) и хлористого метилена (2 мл), а затем перемешивали при комнатной температуре в течение 1 часа 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 70-50% гексан/этилацетат] с получением 0,23 г метил-2-(2-ацетокси-5-бромбензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 2,31 (3H, с), 3,96 (3H, с), 7,10 (1H, д, J=8,8 Гц), 7,36-7,53 (4H, м), 7,64 (1H, дд, J=8,8, 2,4 Гц), 7,67-7,74 (2H, м), 8,04 (1H, д, J=2,4 Гц), 8,13 (1H, д, J=8,3 Гц), 9,13 (1H, д, J=1,7 Гц), 11,75 (1H, с).
Примеры 61a и 62a
Соединения, представленные в Таблице 13a, получали, как описано в Примере 60a.
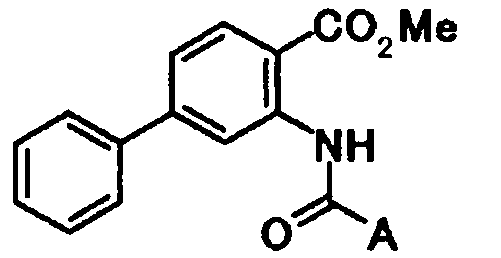
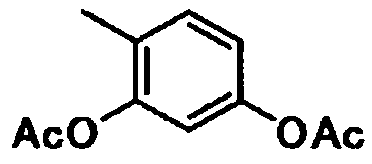
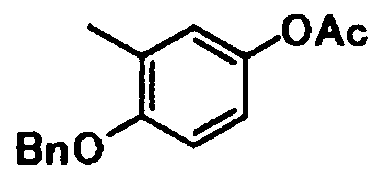
4-(2-(Метоксикарбонил)-5-фенилфенилкарбамоил)-1,3-фенилена диацетат
1H-ЯМР (CDCl3) δ: 2,32 (3H, с), 2,33 (3H, с), 3,95 (3H, с), 7,06 (1H, д, J=2,2 Гц), 7,16 (1H, дд, J=8,5, 2,2 Гц), 7,38 (1H, дд, J=8,4, 1,8 Гц), 7,38-7,44 (1H, м), 7,44-7,51 (2H, м), 7,68-7,74 (2H, м), 7,95 (1H, д, J=8,5 Гц), 8,12 (1H, д, J=8,6 Гц), 9,15 (1H, д, J=1,8 Гц), 11,75 (1H, с).
Метил-2-(5-ацетокси-2-(бензилокси)бензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 2,28 (3H, с), 3,77 (3H, с), 5,45 (2H, с), 6,98 (1H, д, J=9,0 Гц), 7,12 (1H, дд, J=8,9, 3,1 Гц), 7,26-7,51 (9H, м), 7,68-7,75 (2H, м), 7,89 (1H, д, J=3,0 Гц), 8,07 (1H, д, J=8,3 Гц), 9,25 (1H, д, J=2,0 Гц), 12,33 (1H, с).
Пример 63a
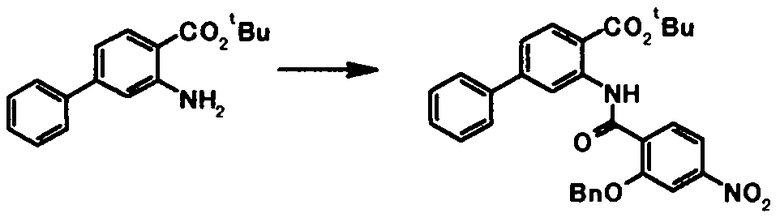
Следующее соединение получали, как описано в Примере 60a.
трет-Бутил-2-(2-(бензилокси)-4-нитробензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 1,55 (9H, с), 5,56 (2H, с), 7,24-7,57 (9H, м), 7,69-7,77 (2H, м), 7,85-7,94 (2H, м), 8,09 (1H, д, J=8,3 Гц), 8,28 (1H, д, J=8,3 Гц), 9,26 (1H, с), 12,55 (1H, с).
Пример 64a
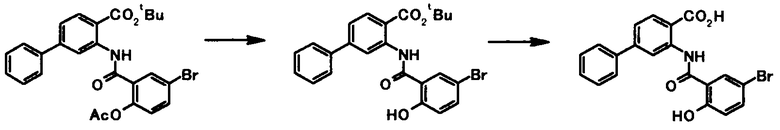
К раствору трет-бутил-2-(2-ацетокси-5-бромбензамидо)-4-фенилбензоата (0,060 г) в смеси метанола (1 мл) и диоксана (1 мл) добавляли карбонат калия (0,049 г), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку метанол. Твердое вещество собирали путем фильтрования с получением 0,034 г 2-(5-бром-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,00 (1H, д, J=8,7 Гц), 7,43-7,49 (1H, м), 7,50-7,58 (3H, м), 7,60 (1H, дд, J=8,7, 2,6 Гц), 7,70-7,75 (2H, м), 8,03 (1H, д, J=2,6 Гц), 8,09 (1H, д, J=8,0 Гц), 9,00 (1H, д, J=1,7 Гц), 11,62-11,80 (1H, уширенный), 12,24-12,40 (1H, уширенный), 13,38-13,60 (1H, уширенный).
Пример 65a
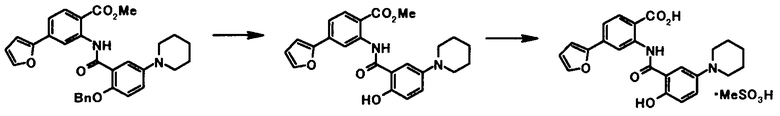
К раствору метил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-(фуран-2-ил)бензоата (0,085 г) в диоксане (1 мл) добавляли воду (0,20 мл), формиат натрия (0,045 г), уксусную кислоту (0,043 мл) и 10% палладированый уголь (8 мг), затем перемешивали при комнатной температуре в течение 3 часов 30 минут, а затем при 60°C в течение 50 минут. К реакционной смеси добавляли 10% палладированый уголь (8 мг), а затем перемешивали при 70°C в течение 50 минут. После охлаждения реакционной смеси до комнатной температуры нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,048 г метил-4-(фуран-2-ил)-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)бензоата.
К раствору полученного метил-4-(фуран-2-ил)-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)бензоата (0,043 г) в смеси метанола (1,0 мл) и диоксана (4,0 мл) добавляли 2 моль/л водный раствор гидроксида натрия (0,51 мл), а затем перемешивали при комнатной температуре в течение 5 часов. К реакционной смеси добавляли воду и толуол, и разделяли водный слой. После корректировки значения pH до 1,8 добавлением метансульфоновой кислоты путем фильтрования собирали 0,036 г твердого вещества. К полученному твердому веществу (0,036 г) добавляли этилацетат (2,0 мл) и метансульфоновую кислоту (5,7 мкл), и собирали твердое вещество путем фильтрования с получением 0,034 г метансульфоната 4-(фуран-2-ил)-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6-D2O) δ: 1,56-1,76 (2H, м), 1,83-1,98 (4H, м), 2,38 (3H, с), 3,46-3,57 (4H, м), 6,69 (1H, дд, J=3,4, 1,9 Гц), 7,11 (1H, д, J=3,4 Гц), 7,18 (1H, д, J=8,9 Гц), 7,57 (1H, дд, J=8,4, 1,8 Гц), 7,72 (1H, дд, J=8,9, 2,9 Гц), 7,87 (1H, д, J=1,2 Гц), 8,07 (1H, д, J=8,4 Гц), 8,14-8,22 (1H, м), 9,08 (1H, д, J=1,8 Гц).
Пример 66a
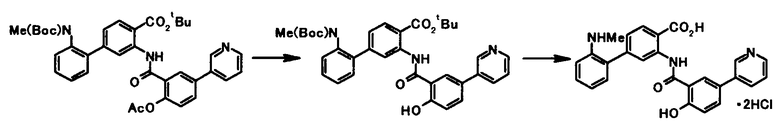
К раствору трет-бутил-2-(2-ацетокси-5-(пиридин-3-ил)бензамидо)-4-(2-((трет-бутоксикарбонил)(метил)амино)фенил)бензоата (0,28 г) в смеси метанола (2 мл) и диоксана (4 мл) добавляли 2 моль/л водный раствор гидроксида натрия (2,3 мл), а затем перемешивали при комнатной температуре в течение 6 часов. Значение pH реакционной смеси корректировали до 5,5 добавлением 10% водного раствора лимонной кислоты, и добавляли к ней хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли трифторуксусную кислоту (4 мл), а затем перемешивали при комнатной температуре в течение 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку 4 моль/л раствор хлорводорода в диоксане (5 мл), а затем перемешивали при комнатной температуре в течение 5 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку диэтиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,18 г дигидрохлорида 2-(2-гидрокси-5-(пиридин-3-ил)бензамидо)-4-(2-(метиламино)фенил)бензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,74 (3H, с), 6,86-7,02 (2H, м), 7,12-7,20 (1H, м), 7,25-7,39 (3H, м), 7,98 (1H, дд, J=8,7, 2,6 Гц), 8,05-8,15 (2H, м), 8,38 (1H, д, J=2,4 Гц), 8,75 (1H, д, J=1,7 Гц), 8,81-8,90 (2H, м), 9,25 (1H, д, J=2,0 Гц), 11,95-12,10 (1H, уширенный), 12,34 (1H, с).
Пример 67a
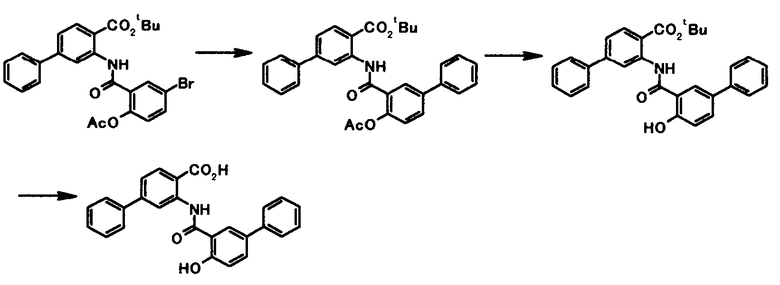
К трет-бутил-2-(2-ацетокси-5-бромбензамидо)-4-фенилбензоату (0,15 г) добавляли диметиловый эфир этиленгликоля (1,4 мл), воду (0,42 мл), фенилбороновую кислоту (0,045 г), бикарбонат натрия (0,063 г) и дихлорид бис(трифенилфосфин)палладия(II) (4 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 45 минут. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней карбонат калия (0,12 г), а затем перемешивали в атмосфере азота при комнатной температуре в течение 2 часов. К реакционной смеси добавляли воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли метанол (2 мл), диоксан (4 мл) и 2 моль/л водный раствор гидроксида натрия (1,5 мл), а затем перемешивали при комнатной температуре в течение 1 часа 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 1 моль/л соляную кислоту и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-80% гексан/этилацетат] и дополнительно очищали по методу колоночной хроматографии на силикагеле [элюент: хлороформ] с получением 0,086 г трет-бутил-2-(2-гидрокси-5-фенилбензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(2-гидрокси-5-фенилбензамидо)-4-фенилбензоата (0,085 г) в хлористом метилене (3 мл) добавляли трифторуксусную кислоту (1 мл), а затем перемешивали при комнатной температуре в течение 17 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат. Твердое вещество собирали путем фильтрования с получением 0,072 г 2-(2-гидрокси-5-фенилбензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,13 (1H, д, J=8,6 Гц), 7,31-7,39 (1H, м), 7,43-7,51 (3H, м), 7,51-7,58 (3H, м), 7,64-7,70 (2H, м), 7,72-7,77 (2H, м), 7,78 (1H, дд, J=8,6, 2,3 Гц), 8,12 (1H, д, J=8,3 Гц), 8,21 (1H, д, J=2,3 Гц), 9,05 (1H, д, J=1,7 Гц), 11,64 (1H, с), 12,40 (1H, с), 13,45-13,70 (1H, уширенный).
Пример 68a
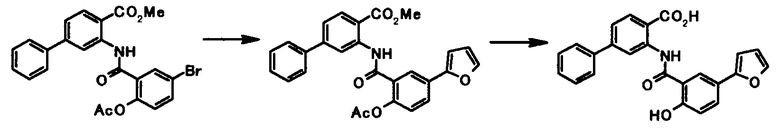
К суспензии метил-2-(2-ацетокси-5-бромбензамидо)-4-фенилбензоата (0,14 г) в диметиловом эфире этиленгликоля (1,4 мл) добавляли воду (0,42 мл), 2-фуранбороновую кислоту (0,040 г), бикарбонат натрия (0,060 г) и бис(трифенилфосфин)палладия(II) дихлорид (4 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 10 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-70% гексан/этилацетат] и дополнительно очищали по методу колоночной хроматографии на силикагеле [элюент: 90-70% гексан/этилацетат] с получением 0,073 г метил-2-(2-ацетокси-5-(фуран-2-ил)бензамидо)-4-фенилбензоата.
К полученному метил-2-(2-ацетокси-5-(фуран-2-ил)бензамидо)-4-фенилбензоату (0,072 г) добавляли диоксан (2 мл) и 2 моль/л водный раствор гидроксида натрия (0,79 мл), а затем перемешивали при комнатной температуре в течение 6 часов. Значение pH реакционной смеси корректировали до 1,5 добавлением 2 моль/л соляной кислоты, и собирали твердое вещество путем фильтрования с получением 0,055 г 2-(5-(фуран-2-ил)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,56-6,62 (1H, м), 6,83 (1H, д, J=3,4 Гц), 7,08 (1H, д, J=8,3 Гц), 7,42-7,60 (4H, м), 7,69-7,77 (3H, м), 7,78 (1H, дд, J=8,5, 2,2 Гц), 8,11 (1H, д, J=8,3 Гц), 8,25 (1H, д, J=1,9 Гц), 9,05 (1H, д, J=1,4 Гц), 11,55-11,80 (1H, уширенный), 12,30-12,60 (1H, уширенный), 13,45-13,65 (1H, уширенный).
Пример 69a
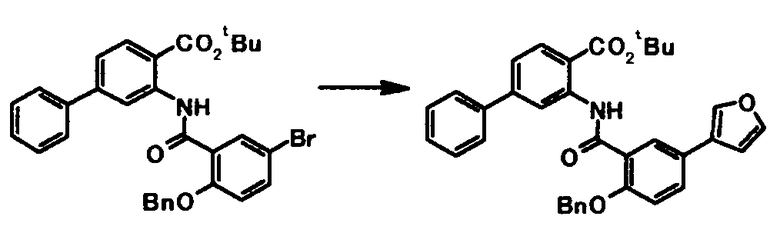
К раствору трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,17 г) в диметиловом эфире этиленгликоля (1,7 мл) добавляли воду (0,5 мл), 3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фуран (0,070 г), карбонат натрия (0,076 г) и дихлорид бис(трифенилфосфин)палладия(II) (4,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 40 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-80% гексан/этилацетат] с получением 0,14 г трет-бутил-2-(2-(бензилокси)-5-(фуран-3-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 1,53 (9H, с), 5,50 (2H, с), 6,67-6,73 (1H, м), 6,97 (1H, д, J=8,8 Гц), 7,24-7,53 (11H, м), 7,67-7,79 (3H, м), 8,07 (1H, д, J=8,3 Гц), 8,31 (1H, д, J=2,4 Гц), 9,31 (1H, д, J=1,7 Гц), 12,52 (1H, с).
Пример 70a
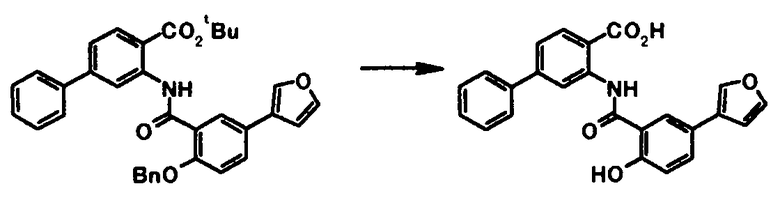
К трет-бутил-2-(2-(бензилокси)-5-(фуран-3-ил)бензамидо)-4-фенилбензоату (0,14 г) добавляли тиоанизол (1,6 мл) и трифторуксусную кислоту (5,2 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку диоксан. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат. Твердое вещество собирали путем фильтрования с получением 0,020 г 2-(5-(фуран-3-ил)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,89-6,95 (1H, м), 7,05 (1H, д, J=8,5 Гц), 7,42-7,50 (1H, м), 7,50-7,59 (3H, м), 7,70 (1H, дд, J=8,5, 2,4 Гц), 7,72-7,78 (3H, м), 8,08-8,15 (3H, м), 9,05 (1H, д, J=1,7 Гц), 11,45-11,58 (1H, уширенный), 12,30-12,50 (1H, уширенный), 13,45-13,65 (1H, уширенный).
Пример 71a
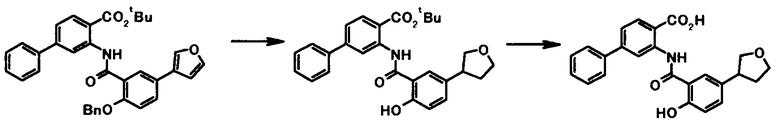
К раствору трет-бутил-2-(2-(бензилокси)-5-(фуран-3-ил)бензамидо)-4-фенилбензоата (0,048 г) в смеси метанола (2 мл) и диоксана (2 мл) добавляли 10% палладированый уголь (20 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 97-85% гексан/этилацетат] с получением 0,027 г трет-бутил-2-(2-гидрокси-5-(тетрагидрофуран-3-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(2-гидрокси-5-(тетрагидрофуран-3-ил)бензамидо)-4-фенилбензоата (0,027 г) в хлористом метилене (5 мл) добавляли трифторуксусную кислоту (2 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,023 г 2-(2-гидрокси-5-(тетрагидрофуран-3-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,85-2,00 (1H, м), 2,25-2,38 (1H, м), 3,27-3,44 (1H, м), 3,53 (1H, дд, J=7,9, 7,9 Гц), 3,81 (1H, ддд, J=7,8, 7,8, 7,8 Гц), 3,96 (1H, ддд, J=8,3, 8,3, 4,4 Гц), 4,04 (1H, дд, J=7,7, 7,7 Гц), 6,97 (1H, д, J=8,5 Гц), 7,37 (1H, дд, J=8,4, 2,3 Гц), 7,42-7,59 (4H, м), 7,70-7,77 (2H, м), 7,81 (1H, д, J=2,2 Гц), 8,10 (1H, д, J=8,3 Гц), 9,03 (1H, д, J=1,7 Гц), 11,35 (1H, с), 12,34 (1H, с), 13,45-13,65 (1H, уширенный).
Пример 72a
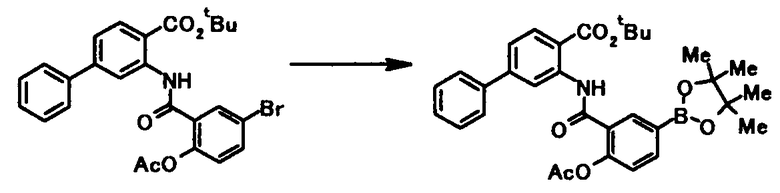
К суспензии трет-бутил-2-(2-ацетокси-5-бромбензамидо)-4-фенилбензоата (2,5 г) в диоксане (25 мл) последовательно добавляли ацетат калия (1,4 г), бис(пинаколато)дибор (1,5 г), и комплекс (1,1'-бис(дифенилфосфино)ферроцен)палладия(II) дихлорида и хлористого метилена (0,20 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней насыщенный водный раствор бикарбоната натрия и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Biotage AB, KP-Sil, элюент: 95-50% гексан/этилацетат] с получением 1,4 г трет-бутил-2-(2-ацетокси-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,32 (12H, с), 1,56 (9H, с), 2,25 (3H, с), 7,34 (1H, д, J=8,1 Гц), 7,43-7,50 (1H, м), 7,51-7,58 (3H, м), 7,68-7,74 (2H, м), 7,90 (1H, дд, J=8,1, 1,7 Гц), 8,03 (1H, д, J=8,3 Гц), 8,18 (1H, д, J=1,7 Гц), 8,78 (1H, д, J=1,7 Гц), 11,47 (1H, с).
Пример 73a
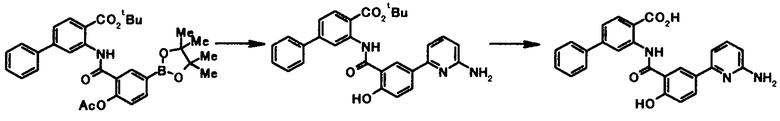
К суспензии трет-бутил-2-(2-ацетокси-5-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)бензамидо)-4-фенилбензоата (0,080 г) в диметиловом эфире этиленгликоля (1 мл) добавляли воду (0,3 мл), 2-амино-6-бромпиридин (0,037 г), бикарбонат натрия (0,036 г) и дихлорид бис(трифенилфосфин)палладия(II) (5,0 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней бис(трифенилфосфин)палладия(II) дихлорид (5,0 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней метанол (0,3 мл) и карбонат натрия (0,046 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 20 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 90-60% гексан/этилацетат] с получением 0,032 г трет-бутил-2-(5-(6-аминопиридин-2-ил)-2-гидроксибензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(5-(6-аминопиридин-2-ил)-2-гидроксибензамидо)-4-фенилбензоату (0,032 г) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 12 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли воду и этилацетат. После корректировки значения pH до 6 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования. В раствор полученного твердого вещества в смеси воды (1 мл), метанола (0,5 мл) и диоксана (0,5 мл) вводили углекислый газ, и собирали твердое вещество путем фильтрования с получением 0,018 г 2-(5-(6-аминопиридин-2-ил)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 5,90-6,15 (2H, уширенный), 6,41 (1H, д, J=8,0 Гц), 7,02 (1H, д, J=7,3 Гц), 7,07 (1H, д, J=8,6 Гц), 7,43-7,58 (5H, м), 7,71-7,77 (2H, м), 8,05 (1H, дд, J=8,6, 2,4 Гц), 8,11 (1H, д, J=8,3 Гц), 8,59 (1H, д, J=2,4 Гц), 9,06 (1H, д, J=1,7 Гц).
Пример 74a
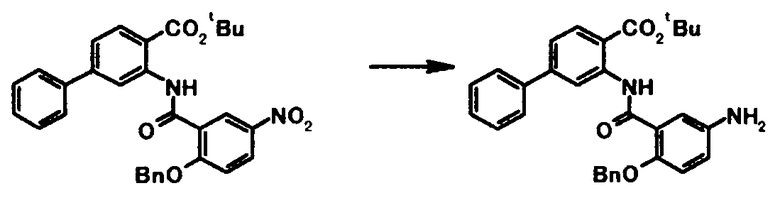
К раствору трет-бутил-2-(2-(бензилокси)-5-нитробензамидо)-4-фенилбензоата (0,14 г) в смеси метанола (1,4 мл) и уксусной кислоты (1,4 мл) добавляли порошковое железо (43 мг), а затем нагревали с обратным холодильником в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней порошковое железо (14 мг), а затем нагревали с обратным холодильником в течение 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней насыщенный водный раствор бикарбоната натрия и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, последовательно промывали насыщенным водным раствором бикарбоната натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 90-50% гексан/этилацетат] с получением 0,065 г трет-бутил-2-(5-амино-2-(бензилокси)бензамидо)-4-фенилбензоата в виде желтого твердого вещества.
1H-ЯМР (CDCl3) δ: 1,52 (9H, с), 5,38 (2H, с), 6,71 (1H, дд, J=8,7, 2,6 Гц), 6,79 (1H, д, J=8,7 Гц), 7,20-7,53 (10H, м), 7,70-7,75 (2H, м), 8,04 (1H, д, J=8,3 Гц), 9,25 (1H, д, J=1,7 Гц), 12,40 (1H, с).
Пример 75a
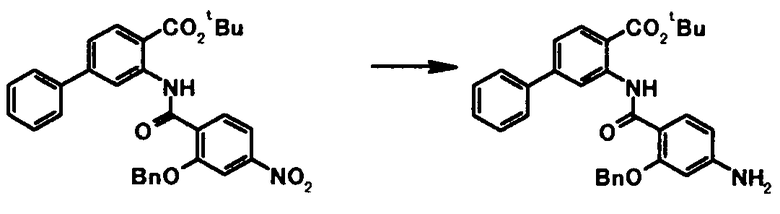
Следующее соединение получали, как описано в Примере 74a.
трет-Бутил-2-(4-амино-2-(бензилокси)бензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 1,51 (9H, с), 5,47 (2H, с), 6,16 (1H, д, J=2,2 Гц), 6,33 (1H, дд, J=8,5, 2,2 Гц), 7,25-7,41 (5H, м), 7,41-7,50 (4H, м), 7,70-7,76 (2H, м), 8,02 (1H, д, J=8,1 Гц), 8,05 (1H, д, J=8,5 Гц), 9,28 (1H, д, J=1,7 Гц), 12,36 (1H, с).
Пример 76a
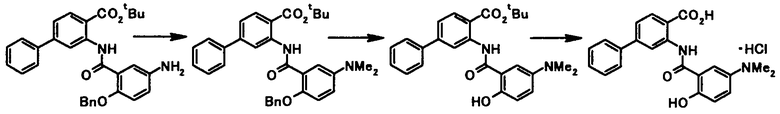
К раствору трет-бутил-2-(5-амино-2-(бензилокси)бензамидо)-4-фенилбензоата (0,064 г) в хлороформе (1,5 мл) последовательно добавляли 37% водный раствор формальдегида (0,24 мл) и триацетоксиборгидрид натрия (0,082 г), а затем перемешивали при комнатной температуре в течение 4 часов 30 минут. К реакционной смеси добавляли воду и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-70% гексан/этилацетат] с получением 0,063 г трет-бутил-2-(2-(бензилокси)-5-(диметиламино)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(диметиламино)бензамидо)-4-фенилбензоата (0,063 г) в смеси метанола (1,5 мл) и этилацетата (2,5 мл) добавляли 10% палладированый уголь (32 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли 10% палладированый уголь (13 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа 30 минут. К реакционной смеси добавляли этилацетат. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 0,036 г трет-бутил-2-(5-(диметиламино)-2-гидроксибензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(5-(диметиламино)-2-гидроксибензамидо)-4-фенилбензоату (0,036 г) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 12 часов. Растворитель выпаривали в условиях пониженного давления, добавляли этилацетат (1,5 мл) и 4 моль/л раствор хлорводорода в диоксане (0,5 мл), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. Твердое вещество собирали путем фильтрования с получением 0,029 г гидрохлорида 2-(5-(диметиламино)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 3,08 (6H, с), 7,08-7,16 (1H, м), 7,43-7,51 (2H, м), 7,51-7,58 (4H, м), 7,70-7,76 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,07 (1H, д, J=1,7 Гц), 12,37 (1H, с).
Пример 77a
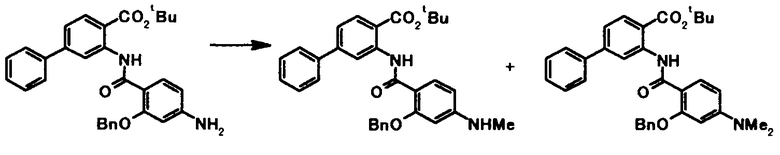
К раствору трет-бутил-2-(4-амино-2-(бензилокси)бензамидо)-4-фенилбензоата (0,15 г) в N,N-диметилацетамиде (1,5 мл) добавляли карбонат калия (0,084 г) и метилйодид (0,028 мл), затем перемешивали при комнатной температуре в течение 1 часа, а затем при 80°C в течение 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней карбонат калия (0,042 г) и метилйодид (0,019 мл), а затем перемешивали при 80°C в течение 20 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 90-70% гексан/этилацетат] с получением 0,056 г трет-бутил-2-(2-(бензилокси)-4-(метиламино)бензамидо)-4-фенилбензоата в виде белого твердого вещества и 0,049 г трет-бутил-2-(2-(бензилокси)-4-(диметиламино)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
трет-Бутил-2-(2-(бензилокси)-4-(метиламино)бензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 1,52 (9H, с), 2,77 (3H, с), 3,98-4,06 (1H, уширенный), 5,49 (2H, с), 6,05 (1H, д, J=2,1 Гц), 6,25 (1H, дд, J=8,7, 2,1 Гц), 7,22-7,41 (5H, м), 7,41-7,53 (4H, м), 7,70-7,76 (2H, м), 8,03 (1H, д, J=8,3 Гц), 8,08 (1H, д, J=8,7 Гц), 9,29 (1H, д, J=1,7 Гц), 12,37 (1H, с).
трет-Бутил-2-(2-(бензилокси)-4-(диметиламино)бензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 1,53 (9H, с), 2,91 (6H, с), 5,51 (2H, с), 6,11 (1H, д, J=2,3 Гц), 6,34 (1H, дд, J=9,0, 2,3 Гц), 7,22-7,40 (5H, м), 7,41-7,48 (2H, м), 7,50-7,55 (2H, м), 7,71-7,76 (2H, м), 8,03 (1H, д, J=8,3 Гц), 8,11 (1H, д, J=9,0 Гц), 9,31 (1H, д, J=2,0 Гц), 12,38-12,41 (1H, уширенный).
Пример 78a
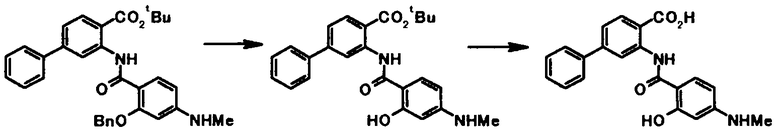
К раствору трет-бутил-2-(2-(бензилокси)-4-(метиламино)бензамидо)-4-фенилбензоата (0,053 г) в смеси метанола (1,5 мл), этилацетата (3 мл) и диоксана (4,5 мл) добавляли 10% палладированый уголь (27 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, а затем собирали твердое вещество путем фильтрования с получением 0,027 г трет-бутил-2-(2-гидрокси-4-(метиламино)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-4-(метиламино)бензамидо)-4-фенилбензоату (0,027 г) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и этилацетат, а затем корректировали значение pH до 6 добавлением насыщенного водного раствора бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли гексан и диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,014 г 2-(2-гидрокси-4-(метиламино)бензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,72 (3H, с), 5,99 (1H, д, J=2,1 Гц), 6,22 (1H, дд, J=8,9, 2,1 Гц), 6,50-6,64 (1H, уширенный), 7,42-7,49 (2H, м), 7,49-7,57 (2H, м), 7,58 (1H, д, J=8,9 Гц), 7,69-7,75 (2H, м), 8,09 (1H, д, J=8,3 Гц), 8,94 (1H, д, J=1,7 Гц), 12,03 (1H, с), 12,08-12,26 (1H, уширенный).
Пример 79a
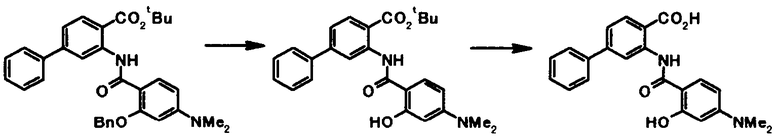
Следующее соединение получали, как описано в Примере 78a.
2-(4-(Диметиламино)-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,99 (6H, с), 6,14 (1H, д, J=2,7 Гц), 6,40 (1H, дд, J=9,0, 2,7 Гц), 7,42-7,50 (2H, м), 7,50-7,57 (2H, м), 7,68 (1H, д, J=9,0 Гц), 7,69-7,75 (2H, м), 8,10 (1H, д, J=8,3 Гц), 8,96 (1H, д, J=1,7 Гц), 11,95 (1H, с), 12,18-12,32 (1H, уширенный).
Пример 80a
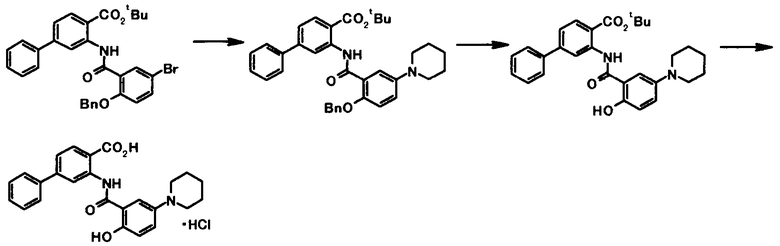
К суспензии трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,15 г) в толуоле (2,3 мл) добавляли пиперидин (0,040 мл), карбонат цезия (0,18 г), трис(дибензилиденацетон)дипалладий(0) (2,5 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней пиперидин (0,040 мл), карбонат цезия (0,18 г), трис(дибензилиденацетон)дипалладий(0) (2,5 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 5 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-70% гексан/этилацетат] с получением 0,13 г трет-бутил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-фенилбензоата в виде оранжевого маслянистого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-фенилбензоата (0,13 г) в смеси этилацетата (1 мл) и метанола (1 мл) 10% палладированый уголь (63 мг) добавляли, а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 минут. К реакционной смеси добавляли этилацетат, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,081 г трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-фенилбензоата в виде желтого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-фенилбензоату (0,081 г) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку этилацетат (2 мл) и 4 моль/л раствор хлорводорода в диоксане (0,5 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,066 г гидрохлорида 2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 1,75-1,88 (2H, м), 1,98-2,12 (4H, м), 3,65 (4H, дд, J=5,6, 5,6 Гц), 7,18 (1H, д, J=9,0 Гц), 7,40-7,46 (1H, м), 7,47-7,54 (3H, м), 7,70-7,76 (3H, м), 8,19 (1H, д, J=3,2 Гц), 8,22 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=2,0 Гц).
Примеры 81a-86a
Соединения, представленные в Таблице 14a, получали, как описано в Примере 80a.
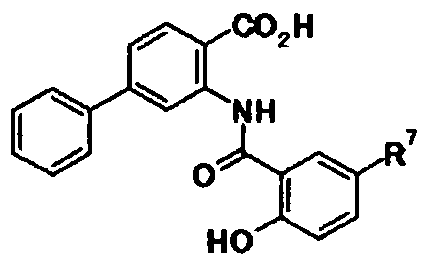
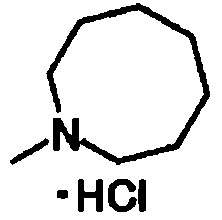
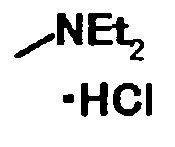
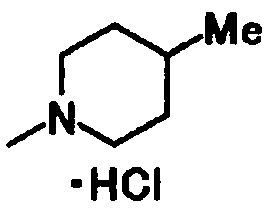
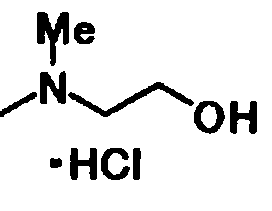
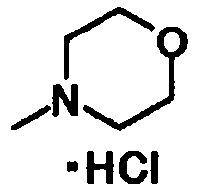
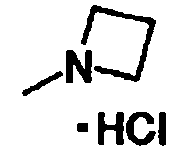
2-(2-Гидрокси-5-((октагидроазоцин)-1-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 1,42-1,61 (6H, м), 1,65-1,80 (4H, м), 3,36-3,50 (4H, м), 6,82-7,02 (2H, м), 7,08-7,30 (1H, м), 7,43-7,58 (4H, м), 7,70-7,77 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,04 (1H, д, J=1,9 Гц), 12,31 (1H, с).
2-(2-Гидрокси-5-(4-метилпиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (CD3OD) δ: 1,11 (3H, д, J=6,6 Гц), 1,64-1,78 (2H, м), 1,84-1,97 (1H, м), 2,02-2,13 (2H, м), 3,60-3,74 (4H, м), 7,18 (1H, д, J=9,0 Гц), 7,40-7,46 (1H, м), 7,47-7,54 (3H, м), 7,70-7,77 (3H, м), 8,18-8,24 (2H, м), 9,06 (1H, д, J=1,7 Гц).
2-(2-Гидрокси-5-(морфолин-4-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 3,16-3,27 (4H, м), 3,80-3,91 (4H, м), 7,03 (1H, д, J=9,0 Гц), 7,36-7,59 (5H, м), 7,67-7,78 (3H, м), 8,10 (1H, д, J=8,3 Гц), 9,03 (1H, д, J=1,7 Гц), 11,22-11,40 (1H, уширенный), 12,31 (1H, с).
2-(5-(Диэтиламино)-2-гидроксибензамидо)-4--фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 1,04 (6H, т, J=7,1 Гц), 3,43-3,68 (4H, м), 7,15-7,28 (1H, м), 7,43-7,50 (1H, м), 7,50-7,58 (3H, м), 7,68-7,86 (3H, м), 8,10 (1H, д, J=8,3 Гц), 8,16-8,34 (1H, м), 9,08 (1H, д, J=1,7 Гц), 11,93-12,15 (1H, уширенный), 12,39 (1H, с).
2-(2-Гидрокси-5-((2-гидроксиэтил)(метил)амино)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6), (50°C) δ: 3,04 (3H, с), 3,42-3,58 (4H, м), 7,02 (1H, д, J=9,0 Гц), 7,26-7,38 (1H, м), 7,41-7,57 (4H, м), 7,61-7,76 (3H, м), 8,10 (1H, д, J=8,3 Гц), 9,03 (1H, д, J=2,0 Гц), 12,17-12,35 (1H, уширенный).
2-(5-(Азетидин-1-ил)-2-гидроксибензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (CD3OD) δ: 2,66 (2H, qn, J=8,0 Гц), 4,57 (4H, т, J=8,0 Гц), 7,14 (1H, д, J=9,0 Гц), 7,39-7,46 (1H, м), 7,46-7,54 (3H, м), 7,59 (1H, дд, J=9,0, 2,8 Гц), 7,70-7,76 (2H, м), 7,96-8,02 (1H, м), 8,22 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=1,7 Гц).
Пример 87a
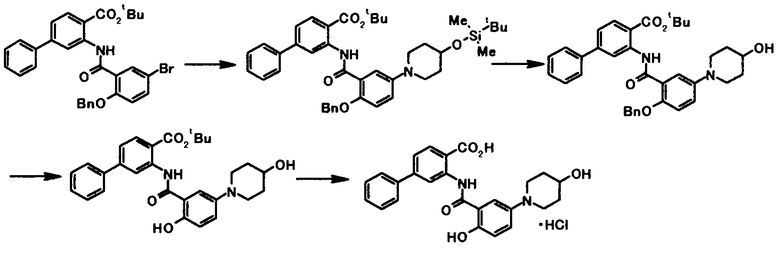
К раствору трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,30 г) в толуоле (4,5 мл) добавляли 4-(трет-бутилдиметилсилилокси)пиперидин (0,23 г), карбонат цезия (0,44 г), трис(дибензилиденацетон)дипалладий(0) (9,8 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (26 мг) и ацетат палладия(II) (4,8 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% гексан/этилацетат] с получением 0,32 г трет-бутил-2-(2-(бензилокси)-5-(4-(трет-бутилдиметилсилилокси)пиперидин-1-ил)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(4-(трет-бутилдиметилсилилокси)пиперидин-1-ил)бензамидо)-4-фенилбензоата (0,32 г) в тетрагидрофуране (3,2 мл) добавляли 1,0 моль/л раствор тетрабутиламмония фторида в тетрагидрофуране (0,56 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 1,0 моль/л раствор тетрабутиламмония фторида в тетрагидрофуране (0,28 мл), а затем перемешивали при комнатной температуре в течение 4 часов. К реакционной смеси при охлаждении на льду добавляли воду, и добавляли к ней хлороформ при комнатной температуре. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 90-40% гексан/этилацетат] с получением 0,23 г трет-бутил-2-(2-(бензилокси)-5-(4-гидроксипиперидин-1-ил)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(4-гидроксипиперидин-1-ил)бензамидо)-4-фенилбензоата (0,22 г) в смеси метанола (2,2 мл) и этилацетата (1,1 мл) добавляли 10% палладированый уголь (0,11 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа. К реакционной смеси добавляли этилацетат, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,18 г трет-бутил-2-(2-гидрокси-5-(4-гидроксипиперидин-1-ил)бензамидо)-4-фенилбензоата.
Раствор полученного трет-бутил-2-(2-гидрокси-5-(4-гидроксипиперидин-1-ил)бензамидо)-4-фенилбензоата (0,18 г) в трифторуксусной кислоте (5 мл) перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку этилацетат (2 мл) и 4 моль/л раствор хлорводорода в диоксане (0,5 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,15 г гидрохлорида 2-(2-гидрокси-5-(4-гидроксипиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (CD3OD) δ: 1,97-2,10 (2H, м), 2,18-2,32 (2H, м), 3,56-3,72 (2H, м), 3,78-3,94 (2H, м), 4,05-4,16 (1H, м), 7,18 (1H, д, J=9,0 Гц), 7,40-7,46 (1H, м), 7,47-7,54 (3H, м), 7,70-7,78 (3H, м), 8,19-8,24 (2H, м), 9,06 (1H, д, J=2,0 Гц).
Пример 88a
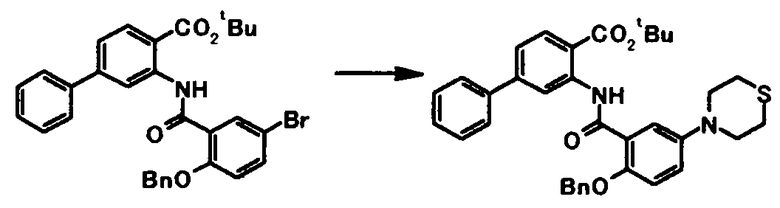
К раствору трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,50 г) в толуоле (5,0 мл) добавляли тиоморфолин (0,14 мл), карбонат цезия (0,58 г), трис(дибензилиденацетон)дипалладий(0) (8,2 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (21 мг) и ацетат палладия(II) (4,0 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней тиоморфолин (0,045 мл), карбонат цезия (0,15 г), трис(дибензилиденацетон)дипалладий(0) (8,2 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (21 мг) и ацетат палладия(II) (4,0 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-80% гексан/этилацетат] с получением 0,36 г трет-бутил-2-(2-(бензилокси)-5-(тиоморфолин-4-ил)бензамидо)-4-фенилбензоата в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,49 (9H, с), 2,65-2,73 (4H, м), 3,36-3,44 (4H, м), 5,42 (2H, с), 7,09-7,15 (2H, м), 7,23-7,35 (3H, м), 7,43-7,59 (7H, м), 7,69-7,76 (2H, м), 8,04 (1H, д, J=8,3 Гц), 9,08-9,12 (1H, м), 12,16 (1H, с).
Пример 89a
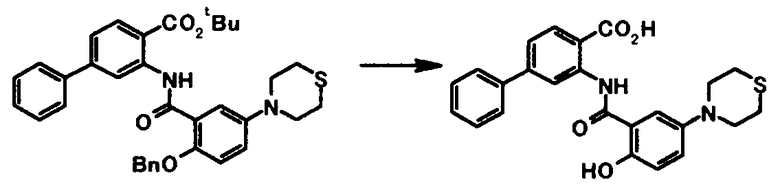
К раствору трет-бутил-2-(2-(бензилокси)-5-(тиоморфолин-4-ил)бензамидо)-4-фенилбензоата (0,10 г) в трифторуксусной кислоте (2,0 мл) добавляли тиоанизол (1,0 мл), а затем перемешивали при комнатной температуре в течение 24 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку 4 моль/л раствор хлорводорода в диоксане (0,5 мл) и этилацетат (1,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Твердое вещество собирали путем фильтрования, и добавляли к полученному твердому веществу воду и этилацетат. После корректировки значения pH до 6,5 добавлением насыщенного водного раствора бикарбоната натрия, органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: хлороформ] с получением 0,047 г 2-(2-гидрокси-5-(тиоморфолин-4-ил)бензамидо)-4-фенилбензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6), (40°C) δ: 2,70-2,76 (4H, м), 3,33-3,39 (4H, м), 6,92 (1H, д, J=8,8 Гц), 7,15 (1H, дд, J=8,8, 3,1 Гц), 7,41-7,57 (5H, м), 7,70-7,76 (2H, м), 8,10 (1H, д, J=8,1 Гц), 8,99 (1H, д, J=1,9 Гц), 10,99 (1H, с), 12,20-12,40 (1H, уширенный).
Пример 90a
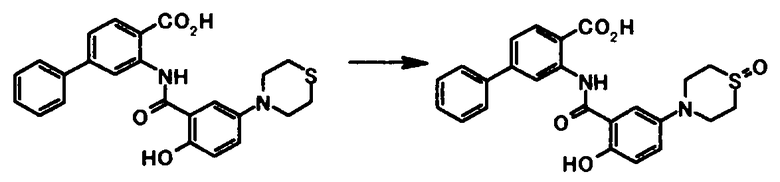
При охлаждении на льду к раствору 2-(2-гидрокси-5-(тиоморфолин-4-ил)бензамидо)-4-фенилбензойной кислоты (0,015 г) в смеси хлористого метилена (1,0 мл) и тетрагидрофурана (0,50 мл) добавляли мета-хлорпербензойную кислоту (7,9 мг), а затем перемешивали при комнатной температуре в течение 10 минут. К реакционной смеси добавляли 2-пропанол (2,0 мл), и собирали твердое вещество путем фильтрования с получением 0,011 г 2-(2-гидрокси-5-(1-оксидтиоморфолин-4-ил)бензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,71-2,84 (2H, м), 2,92-3,04 (2H, м), 3,38-3,50 (2H, м), 3,56-3,70 (2H, м), 6,95 (1H, д, J=9,0 Гц), 7,24 (1H, дд, J=9,0, 2,8 Гц), 7,42-7,57 (5H, м), 7,70-7,76 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,01 (1H, д, J=1,7 Гц), 11,07 (1H, с), 12,32-12,54 (1H, уширенный).
Пример 91a
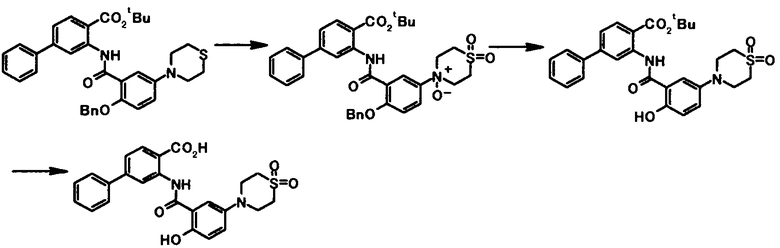
При охлаждении на льду к раствору трет-бутил-2-(2-(бензилокси)-5-(тиоморфолин-4-ил)бензамидо)-4-фенилбензоата (0,10 г) в хлористом метилене (1,5 мл) добавляли мета-хлорпербензойную кислоту (79 мг), а затем перемешивали при комнатной температуре в течение 30 минут. При охлаждении на льду к реакционной смеси добавляли мета-хлорпербензойную кислоту (20 мг), а затем перемешивали при комнатной температуре в течение 30 минут. При охлаждении на льду к реакционной смеси добавляли мета-хлорпербензойную кислоту (40 мг), а затем перемешивали при комнатной температуре в течение 30 минут. При охлаждении на льду к реакционной смеси добавляли мета-хлорпербензойную кислоту (20 мг), а затем перемешивали при комнатной температуре в течение 30 минут. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия и хлористый метилен. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,089 г трет-бутил-2-(2-(бензилокси)-5-(1,1,4-триоксидтиоморфолин-4-ил)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(1,1,4-триоксидтиоморфолин-4-ил)бензамидо)-4-фенилбензоата (0,086 г) в смеси метанола (2,0 мл) и этилацетата (3,0 мл) добавляли 10% палладированый уголь (43 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 минут. К реакционной смеси добавляли диоксан и этилацетат, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления с получением 0,061 г трет-бутил-2-(2-гидрокси-5-(1,1-диоксидтиоморфолин-4-ил)бензамидо)-4-фенилбензоата.
Раствор полученного трет-бутил-2-(2-гидрокси-5-(1,1-диоксидтиоморфолин-4-ил)бензамидо)-4-фенилбензоата (0,059 г) в трифторуксусной кислоте (5,0 мл) перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку воду и этилацетат, а затем корректировали значение pH до 6,5 добавлением насыщенного водного раствора бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,048 г 2-(2-гидрокси-5-(1,1-диоксидтиоморфолин-4-ил)бензамидо)-4-фенилбензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 3,13-3,25 (4H, м), 3,58-3,70 (4H, м), 6,95 (1H, д, J=8,9 Гц), 7,25 (1H, дд, J=8,9, 3,0 Гц), 7,42-7,57 (5H, м), 7,70-7,76 (2H, м), 8,10 (1H, д, J=8,0 Гц), 9,00 (1H, д, J=1,7 Гц), 11,04-11,20 (1H, уширенный).
Пример 92a
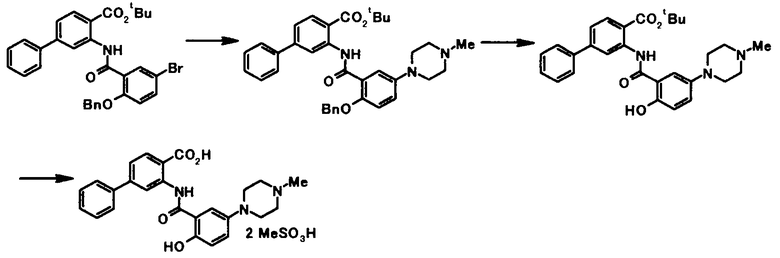
К раствору трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,30 г) в толуоле (4,5 мл) добавляли 1-метилпиперазин (0,089 мл), карбонат цезия (0,35 г), трис(дибензилиденацетон)дипалладий(0) (4,9 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (13 мг) и ацетат палладия(II) (2,4 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 1-метилпиперазин (0,060 мл), карбонат цезия (0,18 г), трис(дибензилиденацетон)дипалладий(0) (4,9 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (13 мг) и ацетат палладия(II) (2,4 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, последовательно промывали 1 моль/л водным раствором гидроксида натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,26 г трет-бутил-2-(2-(бензилокси)-5-(4-метилпиперазин-1-ил)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(4-метилпиперазин-1-ил)бензамидо)-4-фенилбензоата (0,26 г) в смеси метанола (2,6 мл) и этилацетата (1,3 мл) добавляли 10% палладированый уголь (0,26 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли хлороформ, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,13 г трет-бутил-2-(2-гидрокси-5-(4-метилпиперазин-1-ил)бензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(2-гидрокси-5-(4-метилпиперазин-1-ил)бензамидо)-4-фенилбензоату (0,13 г) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку метансульфоновую кислоту (0,034 мл) и этилацетат (3 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Твердое вещество собирали путем фильтрования с получением 0,12 г диметансульфоната 2-(2-гидрокси-5-(4-метилпиперазин-1-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,33 (6H, с), 2,84-2,98 (5H, м), 3,13-3,26 (2H, м), 3,49-3,57 (2H, м), 3,65-3,74 (2H, м), 6,97 (1H, д, J=8,9 Гц), 7,21 (1H, дд, J=8,9, 2,9 Гц), 7,43-7,58 (5H, м), 7,70-7,75 (2H, м), 8,09 (1H, д, J=8,3 Гц), 9,04 (1H, д, J=1,7 Гц), 9,48-9,62 (1H, уширенный), 10,94-11,06 (1H, уширенный), 12,27 (1H, с).
Пример 93a
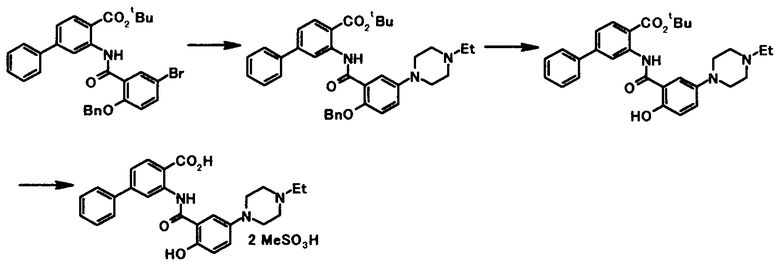
Следующее соединение получали, как описано в Примере 92a.
2-(5-(4-Этилпиперазин-1-ил)-2-гидроксибензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (DMSO-d6) δ: 1,26 (3H, т, J=7,3 Гц), 2,33 (6H, с), 2,87-2,98 (2H, м), 3,08-3,28 (4H, м), 3,54-3,65 (2H, м), 3,65-3,80 (2H, м), 6,98 (1H, д, J=9,0 Гц), 7,22 (1H, дд, J=9,0, 3,1 Гц), 7,43-7,57 (5H, м), 7,70-7,75 (2H, м), 8,09 (1H, д, J=8,3 Гц), 9,04 (1H, д, J=1,7 Гц), 9,26-9,38 (1H, уширенный), 10,94-11,04 (1H, уширенный), 12,27 (1H, с).
Пример 94a
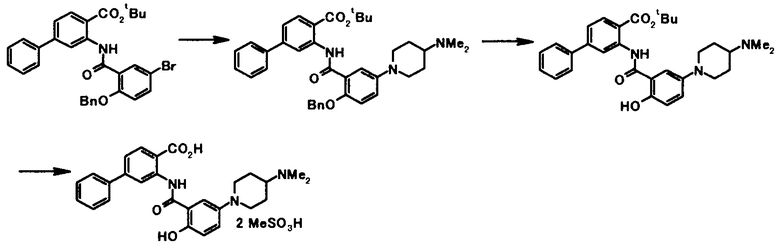
К раствору трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,15 г) в толуоле (2,3 мл) добавляли дигидрохлорид 4-(диметиламино)пиперидина (0,11 г), карбонат цезия (0,44 г), трис(дибензилиденацетон)дипалладий(0) (2,5 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, к реакционной смеси добавляли карбонат цезия (0,13 г), трис(дибензилиденацетон)дипалладий(0) (2,5 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 7 часов. Реакционную смесь охлаждали до комнатной температуры, к реакционной смеси добавляли трикалийфосфат (0,29 г), трис(дибензилиденацетон)дипалладий(0) (2,5 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и хлороформ. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,13 г трет-бутил-2-(2-(бензилокси)-5-(4-(диметиламино)пиперидин-1-ил)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(4-(диметиламино)пиперидин-1-ил)бензамидо)-4-фенилбензоата (0,13 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,13 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли хлороформ, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,066 г трет-бутил-2-(5-(4-(диметиламино)пиперидин-1-ил)-2-гидроксибензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(5-(4-(диметиламино)пиперидин-1-ил)-2-гидроксибензамидо)-4-фенилбензоату (0,066 г) добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 5 часов. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу обращенно-фазной колоночной хроматографии на силикагеле [YMC Co., Ltd., ODS-AM12S05-2520WT, элюент: 40-85% ацетонитрил/0,1% водный раствор трифторуксусной кислоты] с получением 0,060 г твердого вещества. К полученному твердому веществу (0,060 г) добавляли этилацетат (3,0 мл) и метансульфоновую кислоту (0,011 мл), а затем перемешивали при комнатной температуре в течение 5 часов. Твердое вещество собирали путем фильтрования с получением 0,045 г диметансульфоната 2-(5-(4-(диметиламино)пиперидин-1-ил)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 2,17-2,32 (2H, м), 2,36-2,50 (2H, м), 2,73 (6H, с), 2,98 (6H, с), 3,50-3,70 (3H, м), 3,82-3,94 (2H, м), 7,13 (1H, д, J=9,0 Гц), 7,39-7,46 (1H, м), 7,46-7,54 (3H, м), 7,64 (1H, дд, J=9,0, 2,9 Гц), 7,70-7,76 (2H, м), 8,06 (1H, д, J=2,9 Гц), 8,21 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=1,7 Гц).
Пример 95a
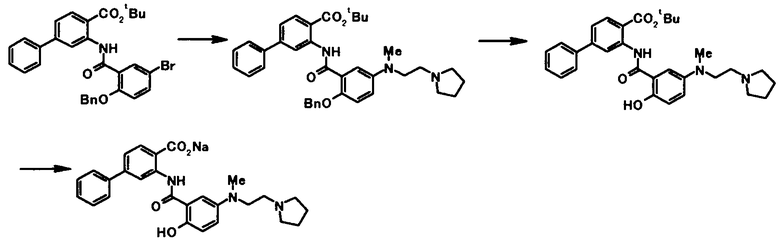
К раствору трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,15 г) в толуоле (2,3 мл) добавляли N-метил-2-(пирролидин-1-ил)этиламин (0,086 г), трикалийфосфат (0,17 г), трис(дибензилиденацетон)дипалладий(0) (2,5 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем к реакционной смеси добавляли N-метил-2-(пирролидин-1-ил)этиламин (0,017 г), трикалийфосфат (0,029 г), трис(дибензилиденацетон)дипалладий(0) (2,5 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 7 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем к реакционной смеси добавляли N-метил-2-(пирролидин-1-ил)этиламин (0,017 г), трикалийфосфат (0,029 г), трис(дибензилиденацетон)дипалладий(0) 2,5 мг, 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и хлороформ. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,097 г трет-бутил-2-(2-(бензилокси)-5-(метил(2-(пирролидин-1-ил)этил)амино)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(метил(2-(пирролидин-1-ил)этил)амино)бензамидо)-4-фенилбензоата (0,097 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,097 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли хлороформ, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-95% хлороформ/метанол] с получением 0,048 г трет-бутил-2-(2-гидрокси-5-(метил(2-(пирролидин-1-ил)этил)амино)бензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(2-гидрокси-5-(метил(2-(пирролидин-1-ил)этил)амино)бензамидо)-4-фенилбензоату (0,048 г) добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку воду и этилацетат, а затем корректировали значение pH до 7 добавлением насыщенного водного раствора бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли метанол (1,5 мл), диоксан (1,5 мл) и 1,0 моль/л водный раствор гидроксида натрия (0,067 мл), и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,028 г 2-(2-гидрокси-5-(метил(2-(пирролидин-1-ил)этил)амино)бензамидо)-4-фенилбензоата натрия в виде желтого твердого вещества.
1H-ЯМР (CD3OD) δ: 1,76-1,90 (4H, м), 2,58-2,78 (6H, м), 2,99 (3H, с), 3,43-3,54 (2H, м), 6,85 (1H, д, J=9,0 Гц), 7,06 (1H, дд, J=9,0, 2,9 Гц), 7,32-7,40 (3H, м), 7,43-7,50 (2H, м), 7,67-7,74 (2H, м), 8,18 (1H, д, J=8,1 Гц), 9,00 (1H, д, J=1,7 Гц).
Пример 96a
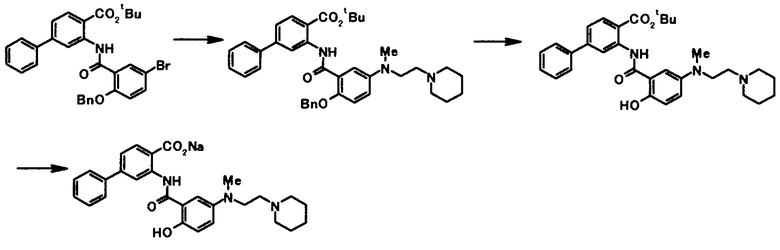
Следующее соединение получали, как описано в Примере 95a.
2-(2-Гидрокси-5-(метил(2-(пиперидин-1-ил)этил)амино)бензамидо)-4-фенилбензоат натрия
1H-ЯМР (CD3OD) δ: 1,42-1,54 (2H, м), 1,56-1,72 (4H, м), 2,46-2,68 (6H, м), 2,98 (3H, с), 3,45-3,56 (2H, м), 6,85 (1H, д, J=9,0 Гц), 7,06 (1H, дд, J=9,0, 2,9 Гц), 7,32-7,40 (3H, м), 7,43-7,50 (2H, м), 7,68-7,73 (2H, м), 8,18 (1H, д, J=8,3 Гц), 9,01 (1H, д, J=1,7 Гц).
Пример 97a
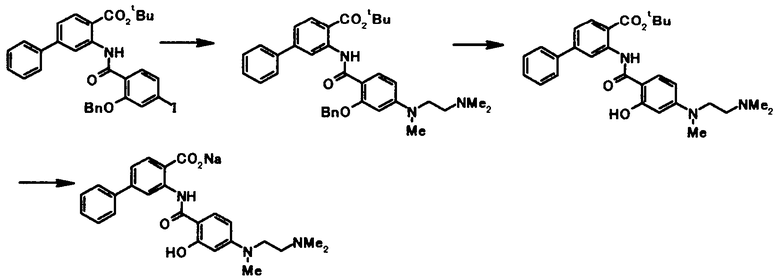
К суспензии трет-бутил-2-(2-(бензилокси)-4-йодбензамидо)-4-фенилбензоата (0,22 г) в толуоле (3,0 мл) добавляли N,N,N'-триметилэтилендиамин (0,12 мл), карбонат цезия (0,35 г), трис(дибензилиденацетон)дипалладий(0) (3,3 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (8,6 мг) и ацетат палладия(II) (1,6 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов 10 минут. Реакционную смесь охлаждали до комнатной температуры, затем к реакционной смеси добавляли N,N,N'-триметилэтилендиамин (0,12 мл), карбонат цезия (0,35 г), трис(дибензилиденацетон)дипалладий(0) (3,3 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (8,6 мг) и ацетат палладия(II) (1,6 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 8 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и хлороформ. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-93% хлороформ/метанол] с получением 0,072 г трет-бутил-2-(2-(бензилокси)-4-((2-(диметиламино)этил)(метил)амино)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-4-((2-(диметиламино)этил)(метил)амино)бензамидо)-4-фенилбензоата (0,071 г) в метаноле (3,0 мл) добавляли 10% палладированый уголь (0,035 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа 45 минут. К реакционной смеси добавляли метанол (2,0 мл) и хлороформ (1,0 мл), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли этилацетат, и собирали твердое вещество путем фильтрования с получением 0,045 г трет-бутил-2-(4-((2-(диметиламино)этил)(метил)амино)-2-гидроксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному трет-бутил-2-(4-((2-(диметиламино)этил)(метил)амино)-2-гидроксибензамидо)-4-фенилбензоату (0,045 г) добавляли трифторуксусную кислоту (2,0 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель удаляли в условиях пониженного давления, а затем добавляли к остатку метанол. После корректировки значения pH до 8,0 добавлением насыщенного водного раствора бикарбоната натрия, твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,028 г 2-(4-((2-(диметиламино)этил)(метил)амино)-2-гидроксибензамидо)-4-фенилбензоата натрия в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,70 (6H, с), 2,96 (3H, с), 3,00-3,10 (2H, м), 3,63-3,77 (2H, м), 6,15 (1H, д, J=2,2 Гц), 6,40 (1H, дд, J=9,0, 2,2 Гц), 7,35 (1H, дд, J=8,1, 1,7 Гц), 7,37-7,44 (1H, м), 7,46-7,55 (2H, м), 7,63-7,73 (2H, м), 7,77 (1H, д, J=9,0 Гц), 8,11 (1H, д, J=8,1 Гц), 8,89 (1H, д, J=1,7 Гц), 12,65-12,90 (1H, уширенный).
Пример 98a
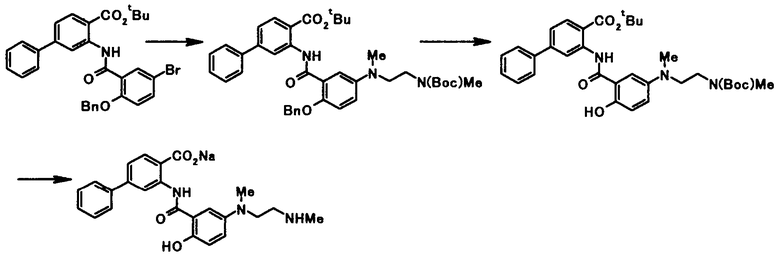
Следующее соединение получали, как описано в Примере 97a.
2-(2-Гидрокси-5-(метил(2-(метиламино)этил)амино)бензамидо)-4-фенилбензоат натрия
1H-ЯМР (DMSO-d6) δ: 2,66 (3H, с), 2,95 (3H, с), 3,05-3,16 (2H, м), 3,53-3,61 (2H, м), 6,88 (1H, д, J=8,9 Гц), 7,00 (1H, дд, J=8,9, 2,7 Гц), 7,36-7,46 (3H, м), 7,47-7,56 (2H, м), 7,65-7,75 (2H, м), 8,14 (1H, д, J=8,0 Гц), 8,89 (1H, д, J=1,7 Гц), 9,55-10,00 (1H, уширенный), 11,55-11,80 (1H, уширенный).
Пример 99a
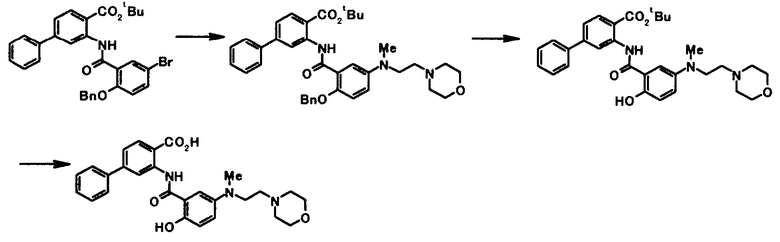
К раствору трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,15 г) в толуоле (2,3 мл) добавляли N-метил-2-(морфолин-4-ил)этиламин (0,097 г), трикалийфосфат (0,17 г), трис(дибензилиденацетон)дипалладий(0) (2,5 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем к реакционной смеси добавляли N-метил-2-(морфолин-4-ил)этиламин (0,019 г), трикалийфосфат (0,029 г), трис(дибензилиденацетон)дипалладий(0) (2,5 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (6,4 мг) и ацетат палладия(II) (1,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 6 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и хлороформ. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,12 г трет-бутил-2-(2-(бензилокси)-5-(метил(2-(морфолин-4-ил)этил)амино)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(метил(2-(морфолин-4-ил)этил)амино)бензамидо)-4-фенилбензоата (0,12 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,12 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 минут. К реакционной смеси добавляли этилацетат. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-95% хлороформ/метанол] с получением 0,074 г трет-бутил-2-(2-гидрокси-5-(метил(2-(морфолин-4-ил)этил)амино)бензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(2-гидрокси-5-(метил(2-(морфолин-4-ил)этил)амино)бензамидо)-4-фенилбензоату (0,074 г) добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. После корректировки значения pH до 7,0 добавлением насыщенного водного раствора бикарбоната натрия органический слой разделяли, и экстрагировали водный слой хлороформом. Органический слой и экстракт объединяли, и полученную смесь сушили над безводным сульфатом натрия. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,024 г 2-(2-гидрокси-5-(метил(2-(морфолин-4-ил)этил)амино)бензамидо)-4-фенилбензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6), (60°C) δ: 2,95 (3H, с), 3,00-3,14 (6H, м), 3,60-3,70 (2H, м), 3,96-4,08 (4H, м), 6,88 (1H, д, J=9,0 Гц), 6,99 (1H, дд, J=9,0, 2,9 Гц), 7,36 (1H, д, J=2,9 Гц), 7,38-7,45 (2H, м), 7,47-7,54 (2H, м), 7,66-7,73 (2H, м), 8,17 (1H, д, J=8,3 Гц), 8,93 (1H, д, J=2,0 Гц).
Пример 100a
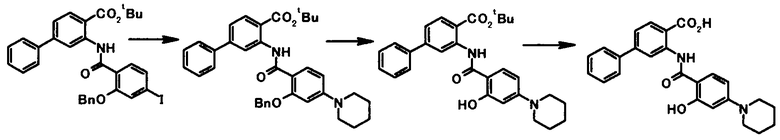
К суспензии трет-бутил-2-(2-(бензилокси)-4-йодбензамидо)-4-фенилбензоата (0,20 г) в толуоле (2,0 мл) добавляли пиперидин (0,049 мл), карбонат цезия (0,22 г), трис(дибензилиденацетон)дипалладий(0) (3,0 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (7,9 мг) и ацетат палладия(II) (1,5 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней пиперидин (0,033 мл), карбонат цезия (0,11 г), трис(дибензилиденацетон)дипалладий(0) (3,0 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (7,9 мг) и ацетат палладия(II) (1,5 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-85% гексан/этилацетат] с получением 0,13 г трет-бутил-2-(2-(бензилокси)-4-(пиперидин-1-ил)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-4-(пиперидин-1-ил)бензамидо)-4-фенилбензоата (0,13 г) в смеси метанола (1,5 мл) и этилацетата (3,0 мл) добавляли 10% палладированый уголь (0,063 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли этилацетат. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,084 г трет-бутил-2-(2-гидрокси-4-(пиперидин-1-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-4-(пиперидин-1-ил)бензамидо)-4-фенилбензоату (0,084 г) добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку воду и этилацетат, а затем корректировали значение pH до 6,5 добавлением насыщенного водного раствора бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,063 г 2-(2-гидрокси-4-(пиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6), (40°C) δ: 1,52-1,66 (6H, м), 3,26-3,40 (4H, м), 6,34 (1H, д, J=2,5 Гц), 6,58 (1H, дд, J=9,1, 2,5 Гц), 7,41-7,49 (2H, м), 7,49-7,56 (2H, м), 7,67 (1H, д, J=9,1 Гц), 7,69-7,74 (2H, м), 8,10 (1H, д, J=8,3 Гц), 8,94 (1H, д, J=1,7 Гц), 11,80-11,94 (1H, уширенный), 12,20-12,35 (1H, уширенный).
Пример 101a
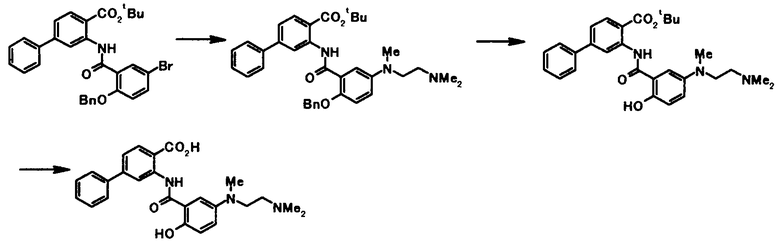
Следующее соединение получали, как описано в Примере 100a.
2-(5-((2-(Диметиламино)этил)(метил)амино)-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,83 (6H, с), 2,95 (3H, с), 3,16-3,26 (2H, м), 3,62-3,74 (2H, м), 6,89 (1H, д, J=9,0 Гц), 7,00 (1H, дд, J=9,0, 2,7 Гц), 7,36-7,45 (3H, м), 7,48-7,55 (2H, м), 7,67-7,73 (2H, м), 8,13 (1H, д, J=8,1 Гц), 8,88 (1H, д, J=2,0 Гц), 11,53-11,67 (1H, уширенный).
Пример 102a
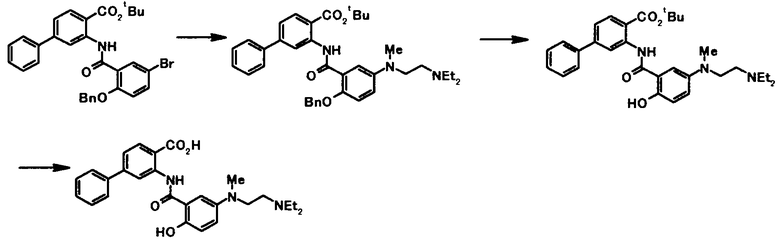
Следующее соединение получали, как описано в Примере 100a.
2-(5-((2-(Диэтиламино)этил)(метил)амино)-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,18-1,39 (6H, м), 2,97 (3H, с), 3,07-3,54 (6H, м), 3,63-3,80 (2H, м), 6,89 (1H, д, J=8,9 Гц), 7,00 (1H, дд, J=8,9, 2,4 Гц), 7,36-7,45 (3H, м), 7,47-7,55 (2H, м), 7,66-7,73 (2H, м), 8,15 (1H, д, J=8,0 Гц), 8,90 (1H, д, J=1,7 Гц), 11,56-11,70 (1H, уширенный).
Пример 103a
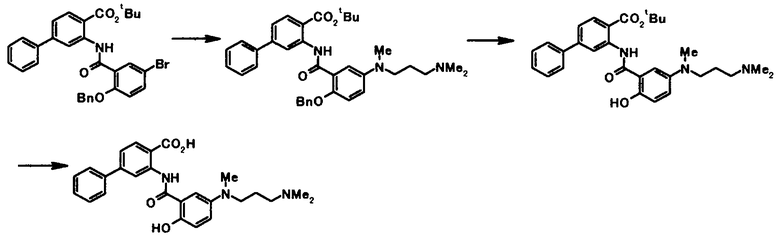
Следующее соединение получали, как описано в Примере 100a.
2-(5-((3-(Диметиламино)пропил)(метил)амино)-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР (CD3OD) δ: 2,07-2,21 (2H, м), 2,92 (6H, с), 2,95 (3H, с), 3,21 (2H, т, J=7,4 Гц), 3,37 (2H, т, J=8,3 Гц), 6,87 (1H, д, J=9,0 Гц), 7,01 (1H, дд, J=9,0, 3,0 Гц), 7,26 (1H, д, J=3,0 Гц), 7,35-7,42 (2H, м), 7,44-7,51 (2H, м), 7,68-7,74 (2H, м), 8,19 (1H, д, J=8,0 Гц), 9,03 (1H, д, J=2,0 Гц).
Пример 104a
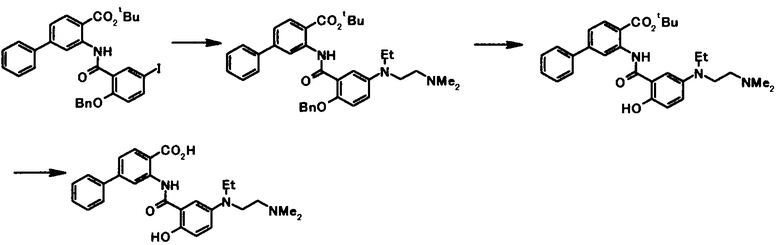
Следующее соединение получали, как описано в Примере 100a.
2-(5-((2-(Диметиламино)этил)(этил)амино)-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР (CD3OD) δ: 1,11 (3H, т, J=7,1 Гц), 2,95 (6H, с), 3,27-3,34 (2H, м), 3,40 (2H, кв, J=7,1 Гц), 3,64 (2H, т, J=7,1 Гц), 6,93 (1H, д, J=9,0 Гц), 7,15 (1H, дд, J=9,0, 2,8 Гц), 7,37-7,53 (5H, м), 7,69-7,75 (2H, м), 8,22 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,7 Гц).
Пример 105a
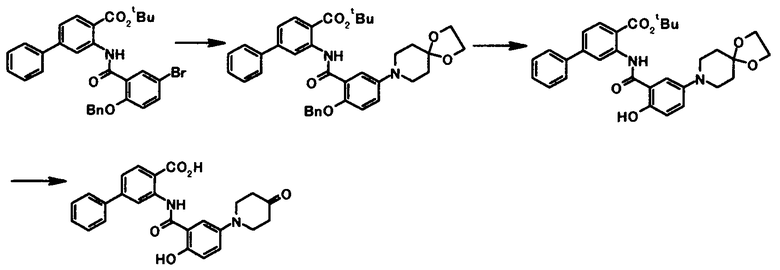
К раствору трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,20 г) в толуоле (3,0 мл) добавляли 1,4-диокса-8-азаспиро[4,5]декан (0,12 мл), карбонат цезия (0,35 г), трис(дибензилиденацетон)дипалладий(0) (3,3 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (8,5 мг) и ацетат палладия(II) (1,6 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем к реакционной смеси добавляли трис(дибензилиденацетон)дипалладий(0) (3,3 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (8,5 мг) и ацетат палладия(II) (1,6 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 5 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 90-65% гексан/этилацетат] с получением 0,18 г трет-бутил-2-(2-(бензилокси)-5-(1,4-диокса-8-азаспиро[4,5]декан-8-ил)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(1,4-диокса-8-азаспиро[4,5]декан-8-ил)бензамидо)-4-фенилбензоата (0,18 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,091 г), а затем перемешивали в атмосфере водорода при комнатной темпеартуре в течение 3 часов. К реакционной смеси добавляли этилацетат. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,12 г трет-бутил-2-(5-(1,4-диокса-8-азаспиро[4,5]декан-8-ил)-2-гидроксибензамидо)-4-фенилбензоата в виде желтого твердого вещества.
К полученному трет-бутил-2-(5-(1,4-диокса-8-азаспиро[4,5]декан-8-ил)-2-гидроксибензамидо)-4-фенилбензоату (0,070 г) добавляли диоксан (1,0 мл) и 6 моль/л соляную кислоту (1,0 мл), а затем нагревали с обратным холодильником в течение 25 минут. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней воду и этилацетат, а затем корректировали значение pH до 5,2 добавлением насыщенного водного раствора бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: хлороформ] с получением 0,026 г 2-(2-гидрокси-5-(4-оксопиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,46 (4H, т, J=6,0 Гц), 3,49 (4H, т, J=6,0 Гц), 6,96 (1H, д, J=8,8 Гц), 7,27 (1H, дд, J=8,8, 3,1 Гц), 7,43-7,57 (5H, м), 7,70-7,76 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,02 (1H, д, J=1,7 Гц), 10,97 (1H, с), 12,33 (1H, с).
Пример 106a
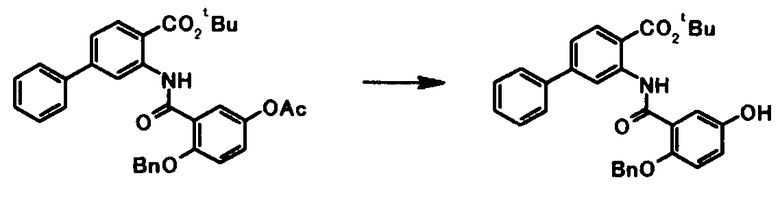
К раствору трет-бутил-2-(5-ацетокси-2-(бензилокси)бензамидо)-4-фенилбензоата (0,58 г) в смеси метанола (3,0 мл) и диоксана (2,0 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (1,6 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку воду и хлороформ, а затем корректировали значение pH до 4,0 добавлением 2,0 моль/л соляной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления с получением 0,52 г трет-бутил-2-(2-(бензилокси)-5-гидроксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 1,52 (9H, с), 5,41 (2H, с), 6,40 (1H, с), 6,80-6,93 (2H, м), 7,21-7,50 (9H, м), 7,72-7,79 (2H, м), 7,88 (1H, д, J=2,9 Гц), 8,01-8,08 (1H, м), 9,13 (1H, д, J=1,7 Гц), 12,51 (1H, с).
Пример 107a
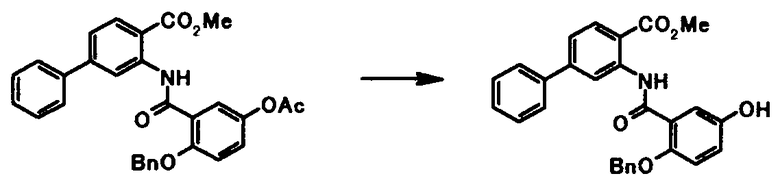
К раствору метил-2-(5-ацетокси-2-(бензилокси)бензамидо)-4-фенилбензоат (3,8 г) в смеси хлороформа (5,0 мл), метанола (10 мл) и ацетона (10 мл) добавляли карбонат калия (1,6 г), а затем перемешивали при комнатной температуре в течение 1 часа. Нерастворимые вещества удаляли путем фильтрования, затем выпаривали растворитель в условиях пониженного давления, и добавляли к остатку 1,0 моль/л соляную кислоту и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления с получением 3,4 г метил-2-(2-(бензилокси)-5-гидроксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 3,76 (3H, с), 5,36 (2H, с), 6,55 (1H, с), 6,85-6,95 (2H, м), 7,22-7,51 (9H, м), 7,70-7,81 (3H, м), 8,07 (1H, д, J=8,3 Гц), 9,16 (1H, д, J=1,7 Гц), 12,30 (1H, с).
Пример 108a
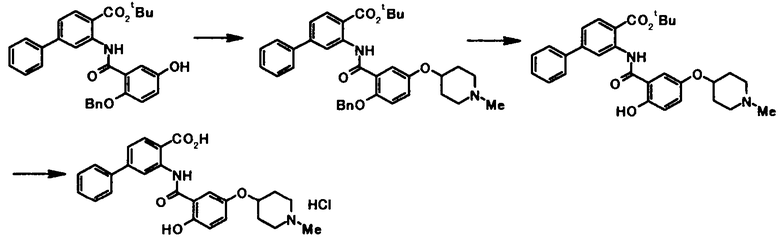
К раствору трет-бутил-2-(2-(бензилокси)-5-гидроксибензамидо)-4-фенилбензоата (0,15 г) в тетрагидрофуране (3,0 мл) добавляли 4-гидрокси-1-метилпиперидин (0,17 г), трифенилфосфин (0,39 г) и диизопропилазодикарбоксилат (0,30 мл), а затем перемешивали при комнатной температуре в течение 3 часов 20 минут. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [элюент: 60-50% гексан/этилацетат → 100-90% хлороформ/метанол] с получением трет-бутил-2-(2-(бензилокси)-5-((1-метилпиперидин-4-ил)окси)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-((1-метилпиперидин-4-ил)окси)бензамидо)-4-фенилбензоата в метаноле (5,0 мл) добавляли 10% палладированый уголь (0,11 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 40 минут. Нерастворимые вещества удаляли путем фильтрования, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,13 г трет-бутил-2-(2-гидрокси-5-((1-метилпиперидин-4-ил)окси)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-5-((1-метилпиперидин-4-ил)окси)бензамидо)-4-фенилбензоата (0,13 г) в трифторуксусной кислоте (2,0 мл) перемешивали при комнатной температуре в течение 2 часов 20 минут. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку 4,0 моль/л раствор хлорводорода в диоксане (2,0 мл), а затем перемешивали при комнатной температуре в течение 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,12 г гидрохлорида 2-(2-гидрокси-5-((1-метилпиперидин-4-ил)окси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,77-1,93 (1H, м), 2,00-2,12 (2H, м), 2,17-2,28 (1H, м), 2,72-2,86 (3H, м), 3,01-3,54 (4H, м), 4,39-4,68 (1H, м), 6,99 (1H, дд, J=8,9, 5,5 Гц), 7,10-7,22 (1H, м), 7,42-7,60 (5H, м), 7,68-7,78 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,03 (1H, д, J=2,0 Гц), 10,25-10,45 (1H, уширенный), 11,10 (1H, с), 12,25-12,40 (1H, м), 13,35-13,65 (1H, уширенный).
Пример 109a
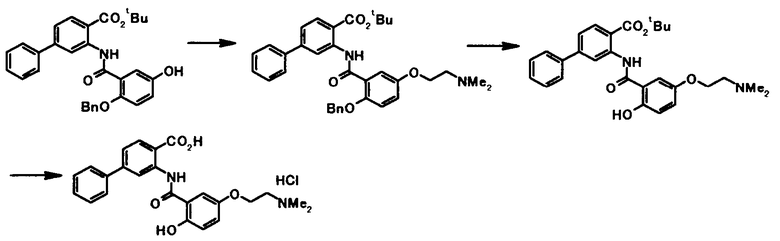
Следующее соединение получали, как описано в Примере 108a.
2-(5-(2-(диметиламино)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 2,86 (6H, с), 3,46-3,54 (2H, м), 4,34 (2H, т, J=5,0 Гц), 7,02 (1H, д, J=9,0 Гц), 7,15 (1H, дд, J=9,0, 3,2 Гц), 7,42-7,59 (5H, м), 7,67-7,78 (2H, м), 8,09 (1H, д, J=8,3 Гц), 9,04 (1H, д, J=1,7 Гц), 10,10-10,35 (1H, уширенный), 11,10 (1H, с), 12,33 (1H, с), 13,25-13,60 (1H, уширенный).
Пример 110a
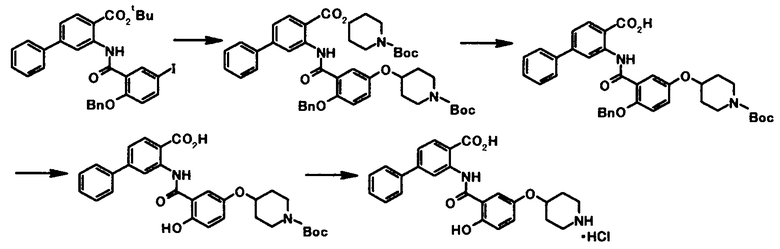
К раствору трет-бутил-2-(2-(бензилокси)-5-йодбензамидо)-4-фенилбензоата (0,070 г) в толуоле (1 мл) добавляли 1-(трет-бутоксикарбонил)-4-гидроксипиперидин (0,047 г), карбонат цезия (0,075 г), 1,10-фенантролин (4,2 мг) и йодид меди(I) (2,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры, затем к реакционной смеси добавляли 1-(трет-бутоксикарбонил)-4-гидроксипиперидин (0,047 г), карбонат цезия (0,075 г), 1,10-фенантролин (4,2 мг) и йодид меди(I) (2,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем к реакционной смеси добавляли 1,10-фенантролин (4,2 мг) и йодид меди(I) (2,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 5 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-60% гексан/этилацетат] с получением 0,074 г трет-бутил-4-(2-(2-(бензилокси)-5-((1-(трет-бутоксикарбонил)пиперидин-4-ил)окси)бензамидо)-4-фенилбензоилокси)пиперидин-1-карбоксилата.
К раствору полученного трет-бутил-4-(2-(2-(бензилокси)-5-((1-(трет-бутоксикарбонил)пиперидин-4-ил)окси)бензамидо)-4-фенилбензоилокси)пиперидин-1-карбоксилата (0,072 г) в смеси метанола (1 мл) и диоксана (1 мл) добавляли 2 моль/л водный раствор гидроксида натрия (0,13 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 2 моль/л водный раствор гидроксида натрия (0,089 мл), а затем нагревали с обратным холодильником в течение 20 минут. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. После корректировки значения pH до 3,5 добавлением 10% водного раствора лимонной кислоты добавляли этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К раствору полученного остатка добавляли 10% палладированый уголь (0,039 г) в метаноле (1,5 мл) и этилацетат (1,5 мл), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли этилацетат, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,024 г 2-(5-((1-(трет-бутоксикарбонил)пиперидин-4-ил)окси)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
К полученной 2-(5-((1-(трет-бутоксикарбонил)пиперидин-4-ил)окси)-2-гидроксибензамидо)-4-фенилбензойной кислоте (0,024 г) добавляли трифторуксусную кислоту (2 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку этилацетат (0,7 мл) и 4 моль/л раствор хлорводорода в диоксане (0,3 мл), а затем перемешивали при комнатной температуре в течение 5 часов. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,017 г гидрохлорида 2-(2-гидрокси-5-(пиперидин-4-илокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,78-1,89 (2H, м), 2,03-2,14 (2H, м), 3,02-3,14 (2H, м), 3,19-3,32 (2H, м), 4,51-4,60 (1H, м), 6,98 (1H, д, J=8,9 Гц), 7,14 (1H, дд, J=8,9, 3,2 Гц), 7,43-7,49 (1H, м), 7,49-7,58 (4H, м), 7,70-7,75 (2H, м), 8,09 (1H, д, J=8,3 Гц), 8,60-8,80 (2H, м), 9,02 (1H, д, J=1,7 Гц), 11,09 (1H, с), 12,30-12,40 (1H, уширенный), 13,35-13,60 (1H, уширенный).
Пример 111a
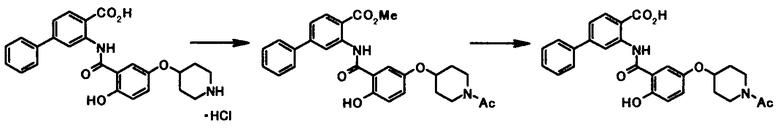
При охлаждении на льду к суспензии гидрохлорида 2-(2-гидрокси-5-(пиперидин-4-илокси)бензамидо)-4-фенилбензойной кислоты (0,030 г) в хлористом метилене (1 мл) последовательно добавляли пиридин (0,30 мл) и уксусный ангидрид (6,7 мкл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси последовательно добавляли пиридин (0,20 мл) и уксусный ангидрид (5,4 мкл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку метанол (0,5 мл) и 2 моль/л водный раствор гидроксида натрия (0,19 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 1 моль/л соляную кислоту (5 мл) и этилацетат. Органический слой разделяли, последовательно промывали добавлением 1 моль/л соляной кислоты, водой и насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диоксан (0,5 мл), метанол (0,5 мл) и 2 моль/л водный раствор гидроксида натрия (0,32 мл), а затем перемешивали при 70°C в течение 30 минут. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. После корректировки значения pH до 3 добавлением 6 моль/л соляной кислоты твердое вещество собирали путем фильтрования с получением 0,022 г 2-(5-(1-ацетилпиперидин-4-илокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,44-1,67 (2H, м), 1,83-2,06 (2H, м), 2,02 (3H, с), 3,19-3,40 (2H, м), 3,63-3,73 (1H, м), 3,79-3,89 (1H, м), 4,46-4,55 (1H, м), 6,95 (1H, д, J=8,8 Гц), 7,13 (1H, дд, J=8,8, 2,9 Гц), 7,43-7,58 (5H, м), 7,70-7,76 (2H, м), 8,10 (1H, д, J=8,1 Гц), 9,01 (1H, д, J=1,2 Гц), 11,07 (1H, с), 12,34 (1H, с), 13,40-13,57 (1H, уширенный).
Пример 112a
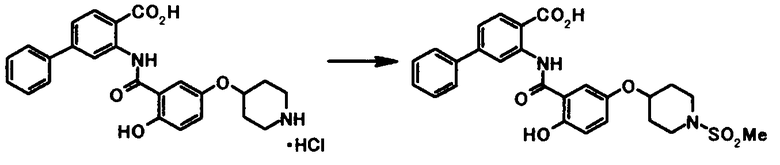
При охлаждении на льду к суспензии гидрохлорида 2-(2-гидрокси-5-(пиперидин-4-илокси)бензамидо)-4-фенилбензойной кислоты (0,030 г) в хлористом метилене (1 мл) последовательно добавляли пиридин (0,5 мл) и метансульфонилхлорид (9,9 мкл), а затем перемешивали при комнатной температуре в течение 5 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку метанол (0,5 мл) и 2 моль/л водный раствор гидроксида натрия (0,5 мл), а затем перемешивали при 70°C в течение 45 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 1 моль/л соляную кислоту (5 мл). Твердое вещество собирали путем фильтрования, и очищали полученное твердое вещество по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: хлороформ] с получением 8,0 мг 2-(2-гидрокси-5-(1-(метилсульфонил)пиперидин-4-илокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6), (40°C) δ: 1,67-1,82 (2H, м), 1,94-2,06 (2H, м), 2,90 (3H, с), 3,06-3,20 (2H, м), 3,32-3,44 (2H, м), 4,40-4,50 (1H, м), 6,95 (1H, д, J=9,0 Гц), 7,13 (1H, дд, J=9,0, 3,1 Гц), 7,42-7,56 (5H, м), 7,69-7,75 (2H, м), 8,10 (1H, д, J=8,1 Гц), 8,98 (1H, д, J=1,7 Гц).
Пример 113a
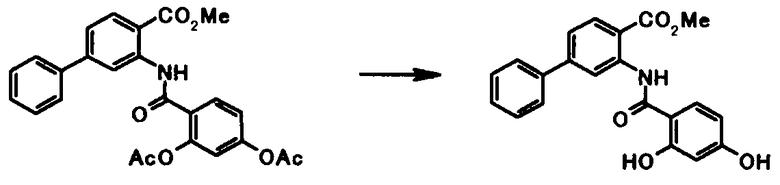
При охлаждении на льду к суспензии диацетата 4-(2-(метоксикарбонил)-5-фенилфенилкарбамоил)-1,3-фенилена (0,31 г) в метаноле (3,1 мл) добавляли 28% раствор метоксида натрия в метаноле (0,34 г), а затем перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь при охлаждении на льду добавляли к 0,5 моль/л соляной кислоте (20 мл), а затем добавляли этилацетат. Органический слой разделяли, последовательно промывали водой и насыщенным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир с получением 0,24 г метил-2-(2,4-дигидроксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 4,01 (3H, с), 5,26 (1H, с), 6,45 (1H, д, J=2,4 Гц), 6,49 (1H, дд, J=8,8, 2,4 Гц), 7,35-7,53 (4H, м), 7,67-7,74 (2H, м), 7,75 (1H, д, J=8,8 Гц), 8,15 (1H, д, J=8,3 Гц), 9,09 (1H, д, J=1,7 Гц), 12,14 (1H, с), 12,54 (1H, с).
Пример 114a
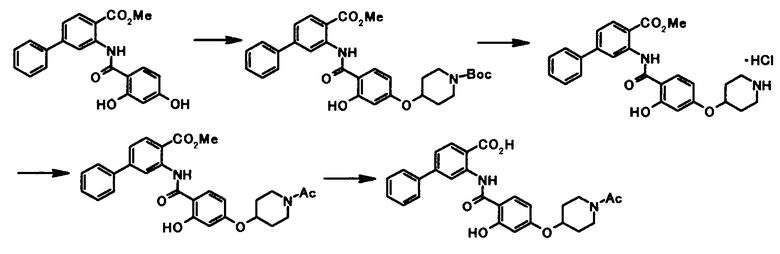
К суспензии метил-2-(2,4-дигидроксибензамидо)-4-фенилбензоата (0,24 г) в тетрагидрофуране (3,6 мл) добавляли 1-(трет-бутоксикарбонил)-4-гидроксипиперидин (0,15 г), трифенилфосфин (0,21 г) и диизопропилазодикарбоксилат (0,16 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 1-(трет-бутоксикарбонил)-4-гидроксипиперидин (0,066 г), трифенилфосфин (0,086 г) и диизопропилазодикарбоксилат (0,064 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [элюент: 100-75% гексан/этилацетат] с получением 0,050 г трет-бутил-4-(3-гидрокси-4-(2-(метоксикарбонил)-5-фенилфенилкарбамоил)фенокси)пиперидин-1-карбоксилата в виде белого твердого вещества.
К полученному трет-бутил-4-(3-гидрокси-4-(2-(метоксикарбонил)-5-фенилфенилкарбамоил)фенокси)пиперидин-1-карбоксилату (0,025 г) добавляли этилацетат (1 мл) и 4 моль/л раствор хлорводорода в диоксане (0,50 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,018 г метил-2-(2-гидрокси-4-(пиперидин-4-илокси)бензамидо)-4-фенилбензоата гидрохлорида в виде белого твердого вещества.
При охлаждении на льду к суспензии полученного метил-2-(2-гидрокси-4-(пиперидин-4-илокси)бензамидо)-4-фенилбензоата гидрохлорида (0,017 г) в хлористом метилене (1 мл) последовательно добавляли пиридин (0,010 мл) и уксусный ангидрид (4,0 мкл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси последовательно добавляли пиридин (0,49 мл) и уксусный ангидрид (4,0 мкл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления с получением 0,016 г метил-2-(4-((1-ацетилпиперидин-4-ил)окси)-2-гидроксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного метил-2-(4-((1-ацетилпиперидин-4-ил)окси)-2-гидроксибензамидо)-4-фенилбензоата (0,016 г) в смеси метанола (0,5 мл) и диоксана (0,5 мл) добавляли 2 моль/л водный раствор гидроксида натрия (0,082 мл), а затем перемешивали при 60°C в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем к реакционной смеси добавляли метанол (1 мл), диоксан (1 мл) и 2 моль/л водный раствор гидроксида натрия (0,082 мл), а затем перемешивали при 60°C в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли воду, а затем корректировали значение pH до 3 добавлением 6 моль/л соляной кислоты. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,014 г 2-(4-((1-ацетилпиперидин-4-ил)окси)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,46-1,70 (2H, м), 1,87-2,07 (2H, м), 2,02 (3H, с), 3,18-3,44 (2H, м), 3,63-3,74 (1H, м), 3,81-3,91 (1H, м), 4,64-4,74 (1H, м), 6,57 (1H, д, J=2,4 Гц), 6,66 (1H, дд, J=8,8, 2,4 Гц), 7,43-7,57 (4H, м), 7,70-7,75 (2H, м), 7,84 (1H, д, J=8,8 Гц), 8,10 (1H, д, J=8,3 Гц), 8,96 (1H, д, J=1,7 Гц), 11,81 (1H, с), 12,24 (1H, с).
Пример 115a
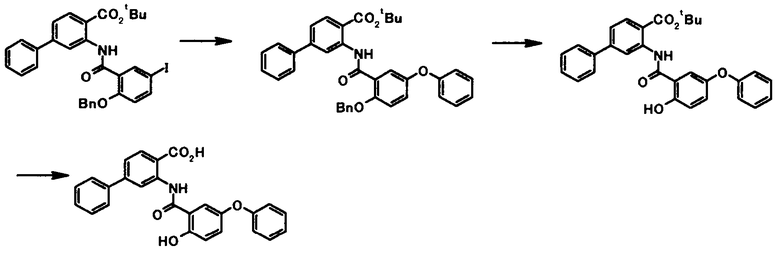
К раствору трет-бутил-2-(2-(бензилокси)-5-йодбензамидо)-4-фенилбензоата (0,10 г) в 1-метил-2-пирролидоне (0,60 мл) добавляли фенол (0,029 мл), карбонат цезия (0,11 г), 2,2,6,6-тетраметилгептан-3,5-дион (3,4 мкл) и хлорид меди(I) (8,2 мг), а затем перемешивали в атмосфере азота при 100°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 2,2,6,6-тетраметилгептан-3,5-дион (3,4 мкл) и хлорид меди(I) (8,2 мг), а затем перемешивали в атмосфере азота при 100°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-95% гексан/этилацетат] с получением 0,049 г трет-бутил-2-(2-(бензилокси)-5-феноксибензамидо)-4-фенилбензоата (0,049 г).
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-феноксибензамидо)-4-фенилбензоата (0,049 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,025 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли 10% палладированый уголь (0,050 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли этилацетат, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку гексан. Твердое вещество собирали путем фильтрования с получением 0,017 г трет-бутил-2-(2-гидрокси-5-феноксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-5-феноксибензамидо)-4-фенилбензоату (0,017 г) добавляли трифторуксусную кислоту (2,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,012 г 2-(2-гидрокси-5-феноксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,95-7,01 (2H, м), 7,07 (1H, д, J=8,8 Гц), 7,07-7,14 (1H, м), 7,21 (1H, дд, J=8,8, 2,9 Гц), 7,34-7,41 (2H, м), 7,41-7,48 (1H, м), 7,48-7,57 (4H, м), 7,68-7,75 (2H, м), 8,08 (1H, д, J=8,0 Гц), 8,98 (1H, д, J=1,7 Гц), 11,37 (1H, с), 12,26-12,44 (1H, уширенный), 13,30-13,55 (1H, уширенный).
Пример 116a
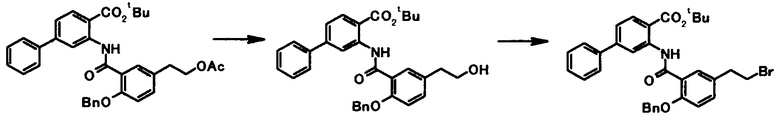
К раствору трет-бутил-2-(5-(2-ацетоксиэтил)-2-(бензилокси)бензамидо)-4-фенилбензоата (0,38 г) в смеси метанола (1,9 мл) и диоксана (1,9 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (0,37 мл), а затем перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси добавляли уксусную кислоту (0,012 мл). Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления с получением 0,35 г трет-бутил-2-(2-(бензилокси)-5-(2-гидроксиэтил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(2-гидроксиэтил)бензамидо)-4-фенилбензоата (0,17 г) в хлористом метилене (3,4 мл) добавляли трифенилфосфин (0,13 г) и тетрабромид углерода (0,16 г), а затем перемешивали при комнатной температуре в течение 50 минут. Реакционную смесь очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: хлороформ], а затем очищали по методу колоночной хроматографии [элюент: 100-85% гексан/этилацетат], с получением 0,16 г трет-бутил-2-(2-(бензилокси)-5-(2-бромэтил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,50 (9H, с), 3,12 (2H, т, J=7,0 Гц), 3,72 (2H, т, J=7,0 Гц), 5,49 (2H, с), 7,18 (1H, д, J=8,6 Гц), 7,24-7,37 (3H, м), 7,42 (1H, дд, J=8,6, 2,4 Гц), 7,43-7,60 (6H, м), 7,68-7,77 (2H, м), 7,87 (1H, д, J=2,4 Гц), 8,05 (1H, д, J=8,5 Гц), 9,06-9,14 (1H, м), 12,17 (1H, с).
Пример 117a
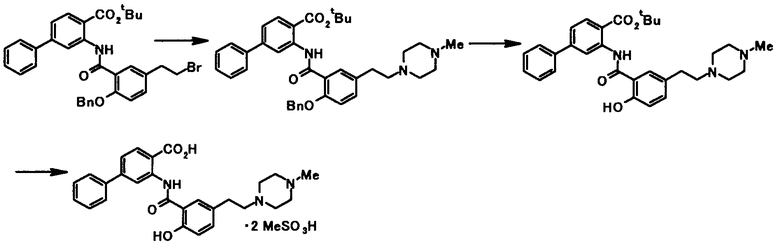
При охлаждении на льду к раствору трет-бутил-2-(2-(бензилокси)-5-(2-бромэтил)бензамидо)-4-фенилбензоата (0,10 г) в ацетоне (1,5 мл) добавляли 1-метилпиперазин (0,095 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Добавляли карбонат калия (0,035 г), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 1-метилпиперазин (0,095 мл) и карбонат калия (0,035 г), а затем перемешивали при комнатной температуре в течение 1 часа. Реакционную смесь оставляли отстаиваться в течение ночи. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,10 г трет-бутил-2-(2-(бензилокси)-5-(2-(4-метилпиперазин-1-ил)этил)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(2-(4-метилпиперазин-1-ил)этил)бензамидо)-4-фенилбензоата (0,10 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,10 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,056 г трет-бутил-2-(2-гидрокси-5-(2-(4-метилпиперазин-1-ил)этил)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-5-(2-(4-метилпиперазин-1-ил)этил)бензамидо)-4-фенилбензоату (0,056 г) добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 19 часов. Растворитель выпаривали в условиях пониженного давления, к остатку последовательно добавляли этилацетат (3,0 мл) и метансульфоновую кислоту (0,018 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,059 г диметансульфоната 2-(2-гидрокси-5-(2-(4-метилпиперазин-1-ил)этил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 2,74 (6H, с), 3,04 (3H, с), 3,09-3,17 (2H, м), 3,40-3,95 (10H, м), 7,00 (1H, д, J=8,5 Гц), 7,39-7,53 (5H, м), 7,69-7,76 (2H, м), 7,83 (1H, д, J=2,0 Гц), 8,22 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=1,9 Гц).
Пример 118a
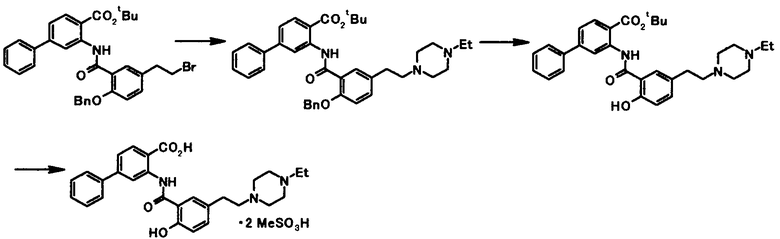
К раствору трет-бутил-2-(2-(бензилокси)-5-(2-бромэтил)бензамидо)-4-фенилбензоата (0,060 г) в ацетоне (1,2 мл) добавляли 1-этилпиперазин (0,065 мл) и карбонат калия (0,042 г), а затем перемешивали при комнатной температуре в течение 6 часов. К реакционной смеси добавляли 1-этилпиперазин (0,065 мл), а затем перемешивали при комнатной температуре в течение 9 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и хлороформ. Органический слой разделяли и сушили над безводным сульфатом натрия, а затем выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,062 г трет-бутил-2-(2-(бензилокси)-5-(2-(4-этилпиперазин-1-ил)этил)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(2-(4-этилпиперазин-1-ил)этил)бензамидо)-4-фенилбензоата (0,062 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,062 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 минут. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления с получением 0,047 г трет-бутил-2-(5-(2-(4-этилпиперазин-1-ил)этил)-2-гидроксибензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(5-(2-(4-этилпиперазин-1-ил)этил)-2-гидроксибензамидо)-4-фенилбензоату (0,047 г) добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, и последовательно добавляли к остатку этилацетат (3,0 мл) и метансульфоновую кислоту (0,013 мл), а затем перемешивали при комнатной температуре в течение 5 часов 30 минут. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,048 г диметансульфоната 2-(5-(2-(4-этилпиперазин-1-ил)этил)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,23 (3H, т, J=7,2 Гц), 2,34 (6H, с), 2,40-3,90 (14H, м), 7,00 (1H, д, J=8,3 Гц), 7,32-7,38 (1H, м), 7,43-7,58 (4H, м), 7,69-7,75 (2H, м), 7,83-7,91 (1H, м), 8,10 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,2 Гц), 11,31 (1H, с), 12,30 (1H, с).
Пример 119a
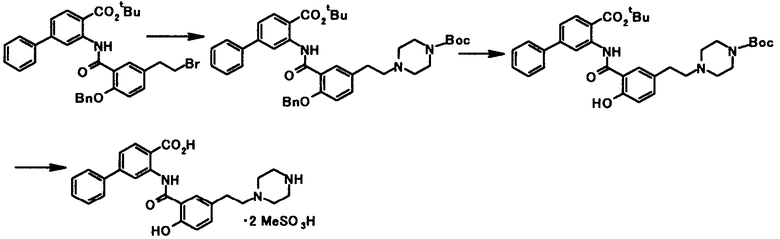
Следующее соединение получали, как описано в Примере 118a.
2-(2-Гидрокси-5-(2-(пиперазин-1-ил)этил)бензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (DMSO-d6) δ: 2,35 (6H, с), 2,80-3,70 (12H, м), 7,00 (1H, д, J=8,3 Гц), 7,36 (1H, дд, J=8,4, 2,3 Гц), 7,43-7,58 (4H, м), 7,69-7,75 (2H, м), 7,84-7,90 (1H, м), 8,10 (1H, д, J=8,3 Гц), 8,75-9,10 (1H, уширенный), 9,05 (1H, д, J=1,7 Гц), 11,31 (1H, с), 12,30 (1H, с).
Пример 120a
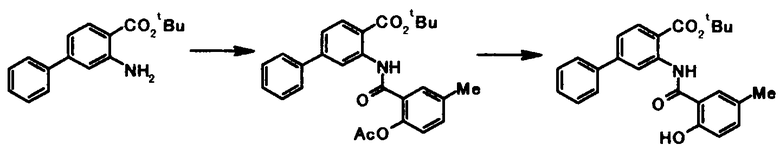
К суспензии 2-ацетокси-5-метилбензойной кислоты (0,48 г) в хлористом метилене (6,0 мл) последовательно добавляли N,N-диметилформамид (0,019 мл) и оксалилхлорид (0,32 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (6,0 мл). Полученную смесь добавляли при охлаждении на льду к раствору трет-бутил-2-амино-4-фенилбензоата (0,60 г) в смеси пиридина (0,45 мл) и хлористого метилена (6,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку метанол (5,0 мл) и карбонат калия (1,54 г), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,80 г трет-бутил-2-(2-гидрокси-5-метилбензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,56 (9H, с), 2,28 (3H, с), 6,93 (1H, д, J=8,3 Гц), 7,26 (1H, дд, J=8,3, 2,2 Гц), 7,42-7,49 (1H, м), 7,50-7,57 (3H, м), 7,69-7,78 (3H, м), 7,99 (1H, д, J=8,3 Гц), 8,81 (1H, д, J=1,7 Гц), 11,25 (1H, с), 11,81 (1H, с).
Пример 121a
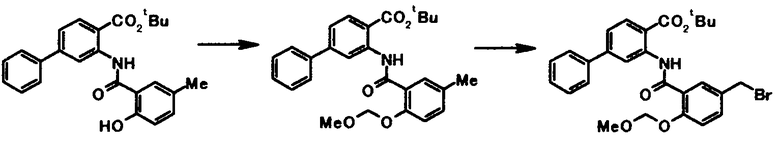
К суспензии трет-бутил-2-(2-гидрокси-5-метилбензамидо)-4-фенилбензоата (0,60 г) в ацетоне (9,0 мл) последовательно добавляли карбонат калия (0,51 г) и метоксиметилхлорид (0,23 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. К реакционной смеси последовательно добавляли карбонат калия (0,21 г) и метоксиметилхлорид (0,11 мл), а затем перемешивали при комнатной температуре в течение 2 часов. К реакционной смеси последовательно добавляли карбонат калия (0,51 г) и метоксиметилхлорид (0,23 мл), а затем перемешивали при комнатной температуре в течение 2 часов, а затем нагревали до температуры возгонки в течение 20 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-80% гексан/этилацетат] с получением 0,64 г трет-бутил-2-(2-(метоксиметокси)-5-метилбензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(метоксиметокси)-5-метилбензамидо)-4-фенилбензоата (0,63 г) в бензоле (6,3 мл) последовательно добавляли N-бромсукцинимид (0,25 г) и азобисизобутиронитрил (0,023 г), а затем нагревали с обратным холодильником в течение 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% гексан/этилацетат] с получением 0,51 г трет-бутил-2-(5-(бромметил)-2-(метоксиметокси)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,60 (9H, с), 3,49 (3H, с), 4,78 (2H, с), 5,52 (2H, с), 7,35 (1H, д, J=8,7 Гц), 7,42-7,58 (4H, м), 7,65 (1H, дд, J=8,7, 2,4 Гц), 7,70-7,76 (2H, м), 8,07 (1H, д, J=8,3 Гц), 8,13 (1H, д, J=2,4 Гц), 9,13 (1H, д, J=1,5 Гц), 12,17 (1H, с).
Пример 122a
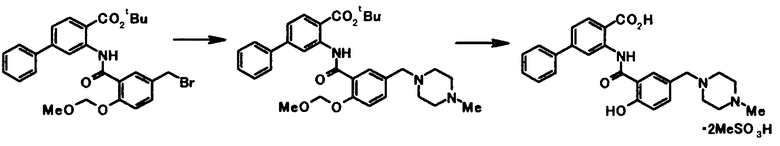
При охлаждении на льду к суспензии трет-бутил-2-(5-(бромметил)-2-(метоксиметокси)бензамидо)-4-фенилбензоата (0,15 г) в ацетоне (2,3 мл) добавляли 1-метилпиперазин (0,16 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 1,0 моль/л водный раствор гидроксида натрия и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-95% хлороформ/метанол] с получением 0,14 г трет-бутил-2-(2-(метоксиметокси)-5-((4-метилпиперазин-1-ил)метил)бензамидо)-4-фенилбензоата в виде желтого маслянистого вещества.
При охлаждении на льду к раствору полученного трет-бутил-2-(2-(метоксиметокси)-5-((4-метилпиперазин-1-ил)метил)бензамидо)-4-фенилбензоата (0,14 г) в хлористом метилене (3,0 мл) добавляли трифторуксусную кислоту (1,5 мл), а затем перемешивали при комнатной температуре в течение 4 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования, добавляли к полученному твердому веществу этилацетат (5,0 мл) и метансульфоновую кислоту (0,036 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,11 г диметансульфоната 2-(2-гидрокси-5-((4-метилпиперазин-1-ил)метил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 2,73 (6H, с), 3,01 (3H, с), 3,20-3,90 (8H, уширенный), 4,38 (2H, с), 7,10 (1H, д, J=8,6 Гц), 7,40-7,46 (1H, м), 7,46-7,54 (3H, м), 7,62 (1H, дд, J=8,6, 2,1 Гц), 7,69-7,75 (2H, м), 8,06 (1H, д, J=2,1 Гц), 8,22 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,7 Гц).
Примеры 123a и 124a
Соединения, представленные в Таблице 15a, получали, как описано в Примере 122a.
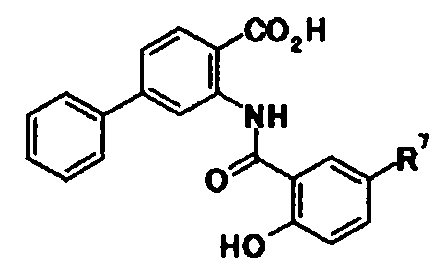
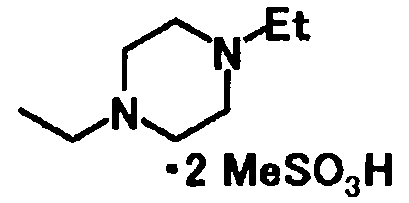
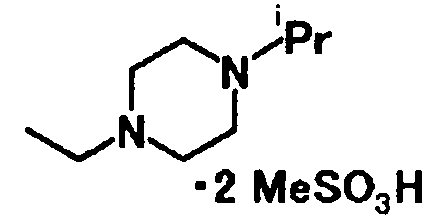
2-(5-((4-Этилпиперазин-1-ил)метил)-2-гидроксибензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (D2O) δ: 1,31 (3H, т, J=7,2 Гц), 2,79 (6H, с), 3,20-3,70 (10H, м), 4,10 (2H, с), 6,82 (1H, д, J=7,8 Гц), 6,98-7,15 (1H, м), 7,18-7,48 (7H, м), 7,58-7,72 (1H, м), 8,38 (1H, с).
2-(2-Гидрокси-5-((4-изопропилпиперазин-1-ил)метил)бензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (DMSO-d6) δ: 1,24 (6H, д, J=6,1 Гц), 2,33 (6H, с), 3,00-3,70 (11H, м), 7,08 (1H, д, J=8,8 Гц), 7,43-7,58 (5H, м), 7,68-7,76 (2H, м), 8,00-8,14 (1H, м), 8,10 (1H, д, J=8,6 Гц), 9,06 (1H, д, J=1,7 Гц), 11,52-11,75 (1H, уширенный), 12,33 (1H, с).
Пример 125a
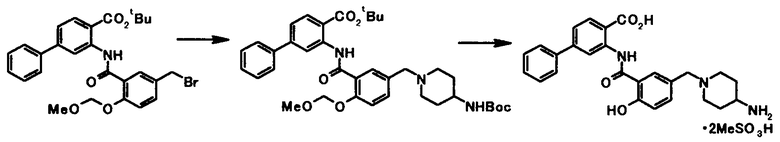
Следующее соединение получали, как описано в Примере 122a.
2-(5-((4-Аминопиперидин-1-ил)метил)-2-гидроксибензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (CD3OD) δ: 1,88-2,04 (2H, м), 2,23-2,34 (2H, м), 2,71 (6H, с), 3,12-3,27 (2H, м), 3,40-3,54 (1H, м), 3,58-3,70 (2H, м), 4,37 (2H, с), 7,11 (1H, д, J=8,6 Гц), 7,40-7,46 (1H, м), 7,47-7,54 (3H, м), 7,61 (1H, дд, J=8,6, 2,1 Гц), 7,70-7,75 (2H, м), 8,05 (1H, д, J=2,1 Гц), 8,22 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=1,7 Гц).
Пример 126a
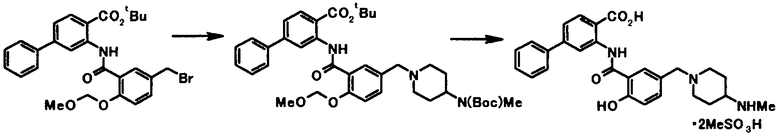
Следующее соединение получали, как описано в Примере 122a.
2-(2-Гидрокси-5-((4-(метиламино)пиперидин-1-ил)метил)бензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (DMSO-d6) δ: 1,64-1,80 (2H, м), 2,16-2,28 (2H, м), 2,38 (6H, с), 2,55-2,60 (3H, м), 2,90-3,07 (2H, м), 3,13-3,31 (1H, м), 3,42-3,56 (2H, м), 4,24-4,34 (2H, м), 7,11 (1H, д, J=8,5 Гц), 7,42-7,60 (5H, м), 7,68-7,76 (2H, м), 8,06-8,14 (2H, м), 8,62-8,76 (1H, м), 9,06 (1H, д, J=1,7 Гц), 9,46-9,63 (1H, уширенный), 11,76 (1H, с), 12,33 (1H, с).
Пример 127a
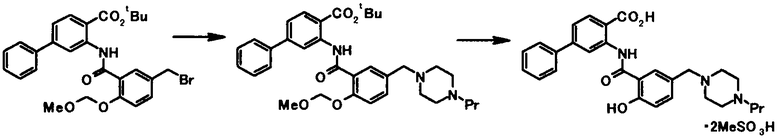
При охлаждении на льду к суспензии 1-пропилпиперазина дигидрохлорида (0,13 г) в ацетоне (1,8 мл) последовательно добавляли карбонат калия (0,19 г) и трет-бутил-2-(5-(бромметил)-2-(метоксиметокси)бензамидо)-4-фенилбензоат (0,12 г), а затем перемешивали при комнатной температуре в течение 5 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и хлороформ. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,088 г трет-бутил-2-(2-(метоксиметокси)-5-((4-пропилпиперазин-1-ил)метил)бензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(2-(метоксиметокси)-5-((4-пропилпиперазин-1-ил)метил)бензамидо)-4-фенилбензоату (0,088 г) добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку этилацетат (3,0 мл) и метансульфоновую кислоту (0,022 мл), а затем перемешивали при комнатной температуре в течение 2 часов 30 минут. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,067 г диметансульфоната 2-(2-гидрокси-5-((4-пропилпиперазин-1-ил)метил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 0,90 (3H, т, J=7,3 Гц), 1,55-1,69 (2H, м), 2,34 (6H, с), 2,90-3,70 (12H, м), 7,08 (1H, д, J=8,0 Гц), 7,43-7,59 (5H, м), 7,67-7,76 (2H, м), 7,99-8,15 (1H, м), 8,10 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=2,0 Гц), 11,55-11,75 (1H, уширенный), 12,33 (1H, с).
Пример 128a
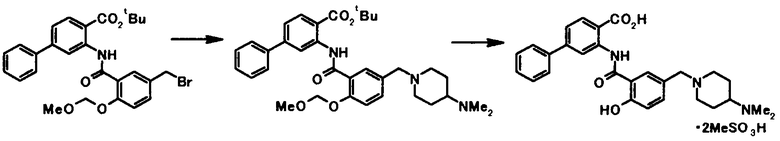
Следующее соединение получали, как описано в Примере 127a.
2-(5-((4-(Диметиламино)пиперидин-1-ил)метил)-2-гидроксибензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (CD3OD) δ: 1,96-2,13 (2H, м), 2,33-2,45 (2H, м), 2,72 (6H, с), 2,92 (6H, с), 3,10-3,23 (2H, м), 3,46-3,64 (1H, м), 3,66-3,78 (2H, м), 4,39 (2H, с), 7,12 (1H, д, J=8,5 Гц), 7,40-7,46 (1H, м), 7,47-7,54 (3H, м), 7,63 (1H, дд, J=8,5, 1,9 Гц), 7,70-7,76 (2H, м), 8,06 (1H, д, J=1,9 Гц), 8,22 (1H, д, J=8,6 Гц), 9,06 (1H, д, J=1,7 Гц).
Пример 129a
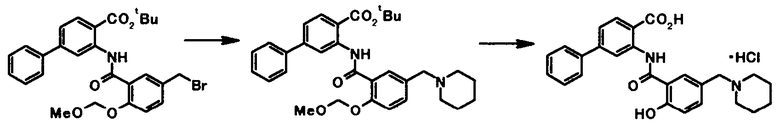
При охлаждении на льду к суспензии трет-бутил-2-(5-(бромметил)-2-(метоксиметокси)бензамидо)-4-фенилбензоата (0,10 г) в ацетоне (1,5 мл) добавляли пиперидин (0,094 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-95% хлороформ/метанол] с получением 0,080 г трет-бутил-2-(2-(метоксиметокси)-5-((пиперидин-1-ил)метил)бензамидо)-4-фенилбензоата.
При охлаждении на льду к раствору полученного трет-бутил-2-(2-(метоксиметокси)-5-((пиперидин-1-ил)метил)бензамидо)-4-фенилбензоата (0,080 г) в хлористом метилене (2,0 мл) добавляли трифторуксусную кислоту (1,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этилацетат. Твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли этилацетат (1,0 мл) и 4,0 моль/л раствор хлорводорода в диоксане (0,20 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,020 г гидрохлорида 2-(2-гидрокси-5-((пиперидин-1-ил)метил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 1,43-1,60 (1H, м), 1,65-1,90 (3H, м), 1,90-2,05 (2H, м), 2,92-3,06 (2H, м), 3,45-3,57 (2H, м), 4,31 (2H, с), 7,10 (1H, д, J=8,5 Гц), 7,40-7,46 (1H, м), 7,47-7,54 (3H, м), 7,58 (1H, дд, J=8,5, 2,2 Гц), 7,70-7,76 (2H, м), 8,02 (1H, д, J=2,2 Гц), 8,23 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=1,7 Гц).
Пример 130a
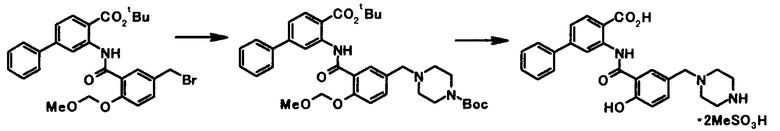
К трет-бутил-2-(5-(бромметил)-2-(метоксиметокси)бензамидо)-4-фенилбензоату (0,030 г) добавляли N,N-диметилформамид (1 мл), карбонат калия (0,039 г) и 1-(трет-бутоксикарбонил)пиперидин (0,053 г), а затем перемешивали при 90-100°C в течение 15 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и хлороформ. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли трифторуксусную кислоту (2 мл), а затем перемешивали при комнатной температуре в течение 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду. После корректировки значения pH до 6,7 добавлением насыщенного водного раствора бикарбоната натрия, твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли метанол и метансульфоновую кислоту (0,010 г). Твердое вещество собирали путем фильтрования с получением 0,015 г диметансульфоната 2-(2-гидрокси-5-((пиперазин-1-ил)метил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,34 (6H, с), 2,80-3,80 (10H, м), 7,09 (1H, д, J=7,8 Гц), 7,43-7,58 (5H, м), 7,69-7,75 (2H, м), 8,04-8,14 (1H, м), 8,10 (1H, д, J=8,3 Гц), 8,65-8,95 (1H, уширенный), 9,06 (1H, д, J=1,5 Гц), 11,60-11,80 (1H, уширенный), 12,33 (1H, с).
Примеры 131a-133a
Соединения, представленные в Таблице 16a, получали, как описано в Примере 130a.
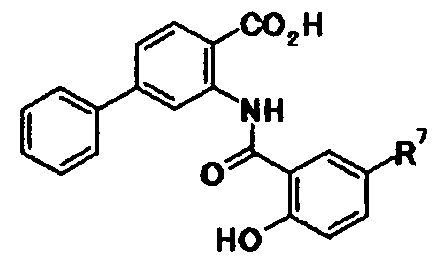
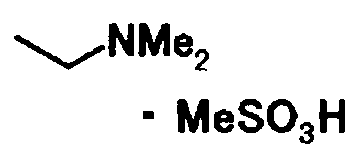
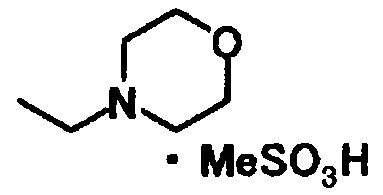
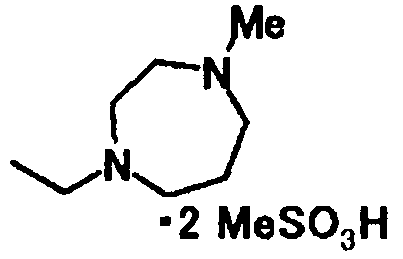
2-(5-((Диметиламино)метил)-2-гидроксибензамидо)-4-фенилбензойной кислоты метансульфонат
1H-ЯМР (DMSO-d6) δ: 2,30 (3H, с), 2,73 (6H, с), 4,26 (2H, с), 7,10 (1H, д, J=8,6 Гц), 7,44-7,58 (5H, м), 7,69-7,75 (2H, м), 8,08-8,13 (2H, м), 9,06 (1H, д, J=1,7 Гц), 9,42-9,58 (1H, уширенный), 11,68-11,78 (1H, уширенный), 12,28-12,38 (1H, уширенный).
2-(2-Гидрокси-5-((морфолин-4-ил)метил)бензамидо)-4-фенилбензойной кислоты метансульфонат
1H-ЯМР (DMSO-d6) δ: 2,32 (3H, с), 3,00-3,19 (2H, м), 3,20-3,46 (2H, м), 3,53-3,71 (2H, м), 3,88-4,05 (2H, м), 4,34 (2H, с), 7,11 (1H, д, J=8,5 Гц), 7,43-7,58 (5H, м), 7,69-7,75 (2H, м), 8,10 (1H, д, J=8,3 Гц), 8,12 (1H, д, J=2,2 Гц), 9,06 (1H, д, J=1,7 Гц), 9,62-9,85 (1H, уширенный), 11,74 (1H, с), 12,33 (1H, с).
2-(2-Гидрокси-5-((4-метил-1,4-диазепан-1-ил)метил)бензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (CD3OD) δ: 2,27-2,41 (2H, м), 2,73 (6H, с), 3,00 (3H, с), 3,24-3,88 (8H, м), 4,48 (2H, с), 7,13 (1H, д, J=8,5 Гц), 7,39-7,56 (4H, м), 7,65 (1H, дд, J=8,5, 2,1 Гц), 7,69-7,77 (2H, м), 8,08 (1H, д, J=2,1 Гц), 8,22 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,7 Гц).
Примеры 134a
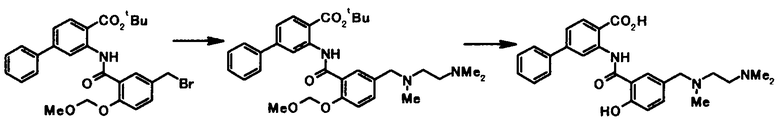
При охлаждении на льду к раствору N,N,N'-триметилэтилендиамина (0,089 мл) в ацетоне (1,8 мл) добавляли трет-бутил-2-(5-(бромметил)-2-(метоксиметокси)бензамидо)-4-фенилбензоат (0,12 г), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и хлороформ. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,070 г трет-бутил-2-(5-(((2-(диметиламино)этил)(метил)амино)метил)-2-(метоксиметокси)бензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(5-(((2-(диметиламино)этил)(метил)амино)метил)-2-(метоксиметокси)бензамидо)-4-фенилбензоату (0,070 г) добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 8 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и этилацетат. После корректировки значения pH до 6,3 добавлением насыщенного водного раствора бикарбоната натрия органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,045 г 2-(5-(((2-(диметиламино)этил)(метил)амино)метил)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 2,30 (3H, с), 2,91 (2H, т, J=5,9 Гц), 2,98 (6H, с), 3,37 (2H, т, J=5,9 Гц), 3,66 (2H, с), 6,90 (1H, д, J=8,3 Гц), 7,30 (1H, дд, J=8,3, 2,0 Гц), 7,35-7,43 (2H, м), 7,44-7,52 (2H, м), 7,68-7,74 (2H, м), 8,20 (1H, д, J=8,0 Гц), 8,32 (1H, д, J=2,0 Гц), 9,00 (1H, д, J=1,9 Гц).
Пример 135a
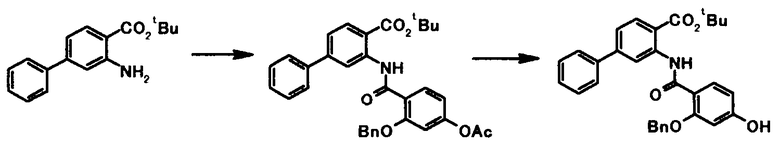
При охлаждении на льду к раствору 4-ацетокси-2-(бензилокси)бензойной кислоты (0,35 г) в смеси хлористого метилена (5,0 мл) и N,N-диметилформамида (0,020 мл) добавляли оксалилхлорид (0,15 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (3,0 мл). Полученную смесь при охлаждении на льду добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (0,30 г) в смеси пиридина (0,14 мл) и хлористого метилена (2,5 мл), а затем перемешивали при комнатной температуре в течение 3 часов 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 91-80% гексан/этилацетат] с получением 0,34 г трет-бутил-2-(4-ацетокси-2-(бензилокси)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-2-(4-ацетокси-2-(бензилокси)бензамидо)-4-фенилбензоата (0,34 г) в диоксане (5,0 мл) добавляли 4 моль/л водный раствор гидроксида натрия (0,47 мл), а затем перемешивали при 50-55°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты (15 мл) и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,29 г трет-бутил-2-(2-(бензилокси)-4-гидроксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,50 (9H, с), 5,49 (2H, с), 6,46-6,55 (2H, м), 7,25-7,38 (3H, м), 7,42-7,58 (6H, м), 7,68-7,75 (2H, м), 7,89 (1H, д, J=8,6 Гц), 8,03 (1H, д, J=8,3 Гц), 9,11 (1H, д, J=1,4 Гц), 10,25 (1H, с), 12,17 (1H, с).
Пример 136a
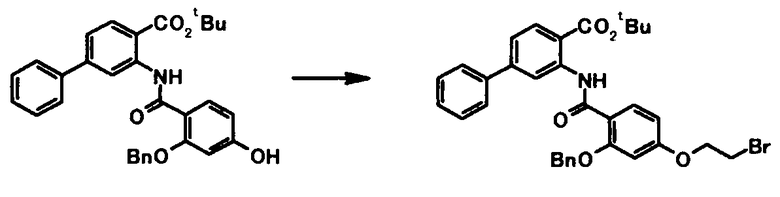
К раствору трет-бутил-2-(2-(бензилокси)-4-гидроксибензамидо)-4-фенилбензоата (0,29 г) в N,N-диметилформамиде (5,0 мл) добавляли карбонат калия (1,6 г) и 1,2-дибромэтан (2,6 мл), а затем перемешивали при 120°C в течение 1 часа 45 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-91% гексан/этилацетат] с получением 0,19 г трет-бутил-2-(2-(бензилокси)-4-(2-бромэтокси)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,50 (9H, с), 3,79 (2H, т, J=5,4 Гц), 4,37 (2H, т, J=5,4 Гц), 5,56 (2H, с), 6,71 (1H, дд, J=8,8, 2,2 Гц), 6,74 (1H, д, J=2,2 Гц), 7,24-7,37 (3H, м), 7,43-7,58 (6H, м), 7,68-7,75 (2H, м), 7,98 (1H, д, J=8,8 Гц), 8,04 (1H, д, J=8,3 Гц), 9,10 (1H, д, J=1,4 Гц), 12,17 (1H, с).
Пример 137a
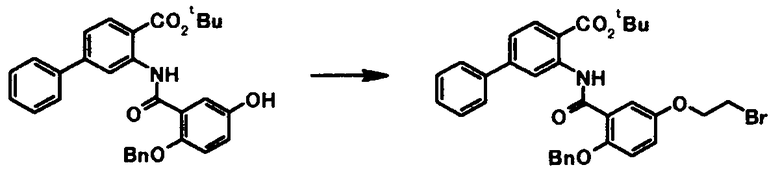
Следующее соединение получали, как описано в Примере 136a.
трет-Бутил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 1,52 (9H, с), 3,61 (2H, т, J=6,2 Гц), 4,30 (2H, т, J=6,2 Гц), 5,44 (2H, с), 6,90 (1H, д, J=9,0 Гц), 6,96 (1H, дд, J=9,0, 3,2 Гц), 7,26-7,50 (9H, м), 7,69-7,76 (3H, м), 8,06 (1H, д, J=8,3 Гц), 9,26 (1H, д, J=1,7 Гц), 12,50 (1H, с).
Пример 138a
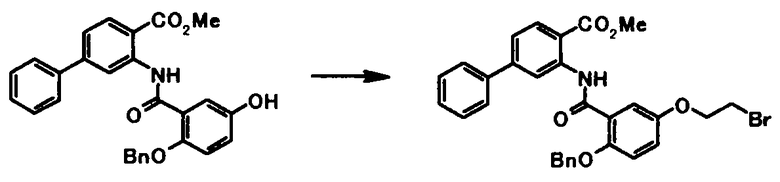
Следующее соединение получали, как описано в Примере 136a.
Метил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 3,62 (2H, т, J=6,2 Гц), 3,77 (3H, с), 4,31 (2H, т, J=6,2 Гц), 5,40 (2H, с), 6,95 (1H, д, J=9,0 Гц), 7,00 (1H, дд, J=9,0, 3,2 Гц), 7,23-7,52 (9H, м), 7,69-7,77 (3H, м), 8,08 (1H, д, J=8,3 Гц), 9,25 (1H, д, J=1,7 Гц), 12,33 (1H, с).
Пример 139a
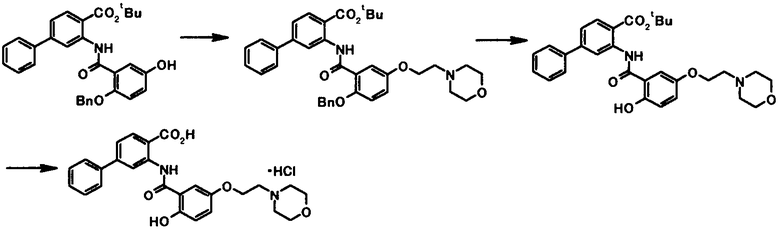
К раствору трет-бутил-2-(2-(бензилокси)-5-гидроксибензамидо)-4-фенилбензоата (0,090 г) в N,N-диметилацетамиде (1,8 мл) добавляли карбонат калия (0,075 г), йодид калия (0,090 г) и N-(2-хлорэтил)морфолина гидрохлорид (0,041 г), а затем перемешивали при 100°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором бикарбоната натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 80-25% гексан/этилацетат] с получением 0,058 г трет-бутил-2-(2-(бензилокси)-5-(2-(морфолин-4-ил)этокси)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(2-(морфолин-4-ил)этокси)бензамидо)-4-фенилбензоата (0,058 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,058 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли 10% палладированый уголь (0,029 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа. К реакционной смеси добавляли этилацетат. Затем, нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку этилацетат (2,5 мл) и 4,0 моль/л раствор хлорводорода в диоксане (0,30 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,033 г гидрохлорида 2-(2-гидрокси-5-(2-(морфолин-4-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 3,15-3,75 (4H, уширенный), 3,67 (2H, т, J=4,9 Гц), 3,75-4,20 (4H, уширенный), 4,43 (2H, т, J=4,9 Гц), 6,97 (1H, д, J=9,0 Гц), 7,21 (1H, дд, J=9,0, 3,1 Гц), 7,39-7,46 (1H, м), 7,46-7,55 (4H, м), 7,70-7,76 (2H, м), 8,21 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=2,0 Гц).
Пример 140a
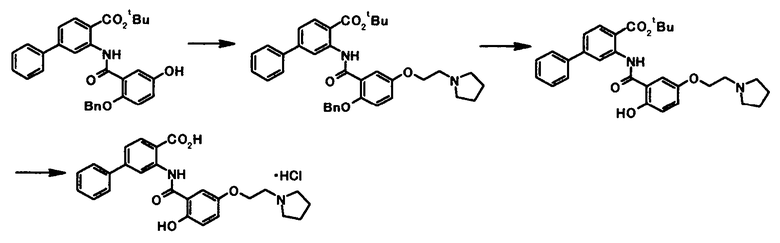
К раствору трет-бутил-2-(2-(бензилокси)-5-гидроксибензамидо)-4-фенилбензоата (0,060 г) в тетрагидрофуране (1,2 мл) добавляли 1-(2-гидроксиэтил)пирролидин (0,016 мл), трифенилфосфин (0,038 г) и диизопропилазодикарбоксилат (0,029 мл), а затем перемешивали при комнатной температуре в течение 25 минут. К реакционной смеси добавляли 1-(2-гидроксиэтил)пирролидин (0,016 мл), трифенилфосфин (0,038 г) и диизопропилазодикарбоксилат (0,029 мл), а затем перемешивали при комнатной температуре в течение 20 минут. К реакционной смеси добавляли 1-(2-гидроксиэтил)пирролидин (0,016 мл), трифенилфосфин (0,038 г) и диизопропилазодикарбоксилат (0,029 мл), а затем перемешивали при комнатной температуре в течение 30 минут. К реакционной смеси добавляли 1-(2-гидроксиэтил)пирролидин (0,016 мл), трифенилфосфин (0,038 г) и диизопропилазодикарбоксилат (0,029 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [элюент: 80-0% гексан/этилацетат] с получением 0,071 г трет-бутил-2-(2-(бензилокси)-5-(2-(пирролидин-1-ил)этокси)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(2-(пирролидин-1-ил)этокси)бензамидо)-4-фенилбензоата (0,071 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,071 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли трифторуксусную кислоту (5,0 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, добавляли к остатку этилацетат (2,5 мл) и 4,0 моль/л раствор хлорводорода в диоксане (0,30 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,036 г гидрохлорида 2-(2-гидрокси-5-(2-(пирролидин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде светло-коричневого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,82-2,10 (4H, м), 3,05-3,20 (2H, м), 3,52-3,66 (4H, м), 4,31 (2H, т, J=5,0 Гц), 7,01 (1H, д, J=8,9 Гц), 7,16 (1H, дд, J=8,9, 3,2 Гц), 7,43-7,58 (5H, м), 7,69-7,75 (2H, м), 8,09 (1H, д, J=8,3 Гц), 9,04 (1H, д, J=1,7 Гц), 10,10-10,30 (1H, уширенный), 11,08 (1H, с), 12,32 (1H, с), 13,30-13,55 (1H, уширенный).
Пример 141a
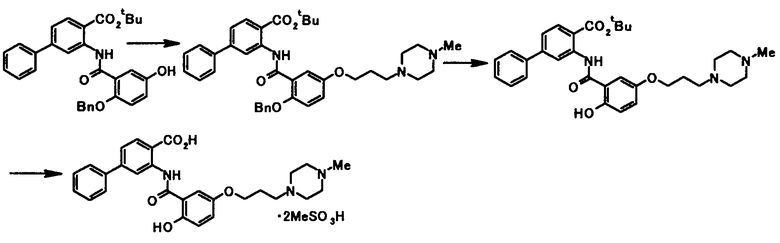
К трет-бутил-2-(2-(бензилокси)-5-гидроксибензамидо)-4-фенилбензоату (0,15 г) последовательно добавляли N,N-диметилформамид (3,0 мл), карбонат калия (0,12 г) и 1-(3-бромпропил)-4-метилпиперазин (0,30 г), а затем перемешивали при 100°C в течение 1 часа 20 минут. К реакционной смеси добавляли карбонат калия (0,12 г), а затем перемешивали при 100°C в течение 50 минут. К реакционной смеси добавляли воду и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-92% хлороформ/метанол] с получением 0,060 г трет-бутил-2-(2-(бензилокси)-5-(3-(4-метилпиперазин-1-ил)пропокси)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(3-(4-метилпиперазин-1-ил)пропокси)бензамидо)-4-фенилбензоата (0,059 г) в смеси метанола (1,0 мл) и хлороформа (1,0 мл) добавляли 10% палладированый уголь (0,023 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа 20 минут. К реакционной смеси добавляли 10% палладированый уголь (0,058 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. К реакционной смеси добавляли метанол (2,0 мл), хлороформ (2,0 мл) и 10% палладированый уголь (0,055 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 50 минут. К реакционной смеси добавляли 10% палладированый уголь (0,025 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 4 часов 30 минут. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,026 г трет-бутил-2-(2-гидрокси-5-(3-(4-метилпиперазин-1-ил)пропокси)бензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(2-гидрокси-5-(3-(4-метилпиперазин-1-ил)пропокси)бензамидо)-4-фенилбензоату (0,024 г) добавляли трифторуксусную кислоту (1,0 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и метанол. После корректировки значения pH до 7,5 добавлениеем насыщенного водного раствора бикарбоната натрия, твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли этилацетат (2,0 мл) и метансульфоновую кислоту (5,0 мкл), и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли этилацетат, и собирали твердое вещество путем фильтрования с получением 0,020 г диметансульфоната 2-(2-гидрокси-5-(3-(4-метилпиперазин-1-ил)пропокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 2,22-2,34 (2H, м), 2,72 (6H, с), 3,02 (3H, с), 3,36-3,90 (10H, м), 4,18 (2H, т, J=5,7 Гц), 6,94 (1H, д, J=9,0 Гц), 7,14 (1H, дд, J=9,0, 3,2 Гц), 7,39-7,54 (5H, м), 7,69-7,77 (2H, м), 8,22 (1H, д, J=8,3 Гц), 9,07 (1H, д, J=1,7 Гц).
Пример 142a
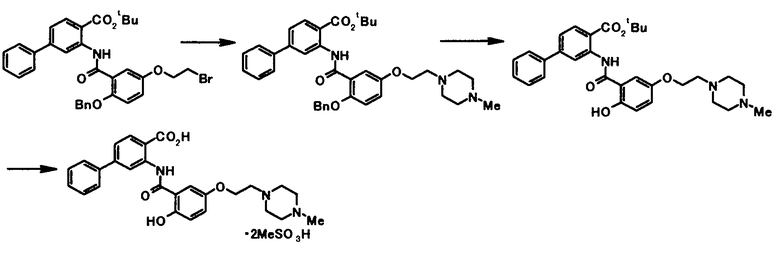
К раствору трет-бутил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоата (1,5 г) в ацетоне (7,5 мл) добавляли карбонат калия (1,0 г) и 1-метилпиперазин (0,83 мл), а затем нагревали с обратным холодильником в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней карбонат калия (0,34 г) и 1-метилпиперазин (0,28 мл), а затем нагревали с обратным холодильником в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Органический слой разделяли, и удаляли растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-95% хлороформ/метанол] с получением трет-бутил-2-(2-(бензилокси)-5-(2-(4-метилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(2-(4-метилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в метаноле (8,0 мл) добавляли 10% палладированый уголь (0,75 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 5 часов. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 1,2 г трет-бутил-2-(2-гидрокси-5-(2-(4-метилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата.
К полученному трет-бутил-2-(2-гидрокси-5-(2-(4-метилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоату (1,2 г) добавляли трифторуксусную кислоту (10 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 30% водный раствор метанола. После корректировки значения pH до 6,7 добавлением насыщенного водного раствора бикарбоната натрия, твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,86 г 2-(2-гидрокси-5-(2-(4-метилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты.
К раствору полученной 2-(2-гидрокси-5-(2-(4-метилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты (0,10 г) в смеси тетрагидрофурана (2,0 мл) и этанола (1,0 мл) добавляли воду (1,0 мл), метансульфоновую кислоту (0,029 мл) и активированный уголь (0,020 г), а затем перемешивали при комнатной температуре в течение 30 минут. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли ацетон, и собирали твердое вещество путем фильтрования с получением 0,095 г диметансульфоната 2-(2-гидрокси-5-(2-(4-метилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,36 (6H, с), 2,87 (3H, с), 2,99-4,05 (10H, м), 4,22-4,34 (2H, м), 7,00 (1H, д, J=9,0 Гц), 7,14 (1H, дд, J=8,7, 3,1 Гц), 7,43-7,59 (5H, м), 7,68-7,76 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,04 (1H, д, J=1,5 Гц), 10,99-11,10 (1H, уширенный), 12,32 (1H, с).
Пример 143a
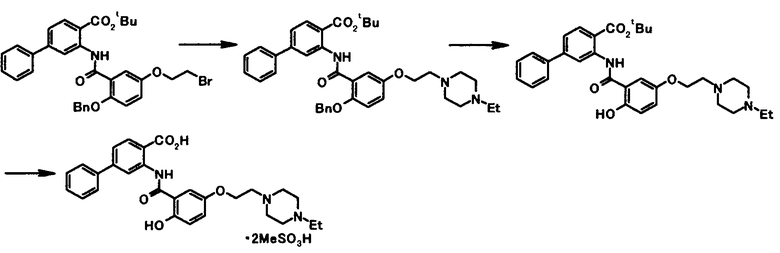
К раствору трет-бутил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоата (1,6 г) в ацетоне (8,0 мл) добавляли карбонат калия (1,5 г) и 1-этилпиперазин (1,0 мл), а затем нагревали с обратным холодильником в течение 5 часов. После охлаждения реакционной смеси до комнатной температуры нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением трет-бутил-2-(2-(бензилокси)-5-(2-(4-этилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в виде желтого маслянистого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(2-(4-этилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в метаноле (20 мл) добавляли 10% палладированый уголь (1,7 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 минут. К реакционной смеси добавляли 10% палладированый уголь (0,70 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления с получением трет-бутил-2-(5-(2-(4-этилпиперазин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному трет-бутил-2-(5-(2-(4-этилпиперазин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензоату добавляли трифторуксусную кислоту (10 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку 30% водный раствор метанола (16 мл). После корректировки значения pH до 6,5 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали из реакционной смеси путем фильтрования с получением 1,1 г 2-(5-(2-(4-этилпиперазин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
К суспензии полученной 2-(5-(2-(4-этилпиперазин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты (0,10 г) в этаноле (2,0 мл) добавляли метансульфоновую кислоту (0,027 мл), тетрагидрофуран (3,0 мл) и активированный уголь (0,020 г), а затем перемешивали при комнатной температуре в течение 30 минут. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли ацетон, и собирали твердое вещество путем фильтрования с получением 0,090 г диметансульфоната 2-(5-(2-(4-этилпиперазин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,23 (3H, т, J=7,3 Гц), 2,36 (6H, с), 3,02-3,78 (12H, м), 4,21-4,34 (2H, м), 7,00 (1H, д, J=9,0 Гц), 7,14 (1H, дд, J=9,0, 3,2 Гц), 7,42-7,59 (5H, м), 7,68-7,76 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,01-9,07 (1H, м), 10,99-11,09 (1H, уширенный), 12,32 (1H, с).
Пример 144a
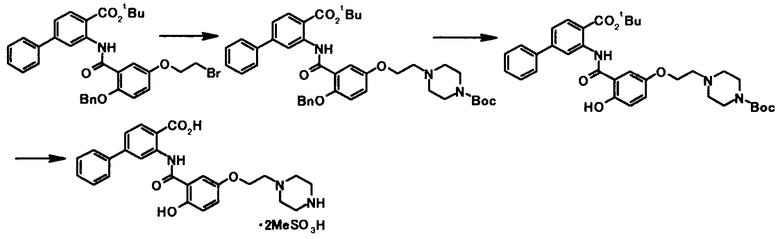
К N,N-диметилформамиду (1 мл) добавляли трет-бутил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоат (0,030 г), карбонат калия (0,10 г) и 1-(трет-бутоксикарбонил)пиперидин (0,093 г), а затем перемешивали при 90-100°C в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и хлороформ. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли тетрагидрофуран (1,5 мл), воду (0,1 мл), 10% палладированый уголь (0,060 г), формиат натрия (7,5 мг) и уксусную кислоту (7,5 мг), а затем перемешивали при 60°C в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К остатку добавляли насыщенный водный раствор бикарбоната натрия и хлороформ. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 80-50% гексан/этилацетат] с получением 0,025 г трет-бутил-4-(2-(3-(2-(трет-бутоксикарбонил)-5-фенилфенилкарбамоил)-4-гидроксифенокси)этил)пиперидин-1-карбоксилата.
К полученному трет-бутил-4-(2-(3-(2-(трет-бутоксикарбонил)-5-фенилфенилкарбамоил)-4-гидроксифенокси)этил)пиперидин-1-карбоксилату (0,025 г) добавляли трифторуксусную кислоту (2 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду. После корректировки значения pH до 6,3 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли метанол и метансульфоновую кислоту, а затем добавляли этилацетат. Твердое вещество собирали путем фильтрования с получением 0,010 г диметансульфоната 2-(2-гидрокси-5-(2-(пиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,31 (6H, с), 2,80-3,80 (10H, м), 4,16-4,32 (2H, м), 6,99 (1H, д, J=8,8 Гц), 7,08-7,17 (1H, м), 7,43-7,59 (5H, м), 7,68-7,76 (2H, м), 8,09 (1H, д, J=8,5 Гц), 9,01-9,07 (1H, м), 11,03 (1H, с), 12,32 (1H, с).
Пример 145a
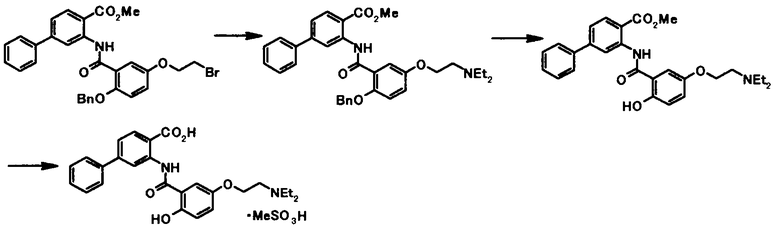
К раствору метил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоата (0,20 г) в ацетоне (2,0 мл) добавляли карбонат калия (0,15 г) и диэтиламин (0,11 мл), а затем нагревали с обратным холодильником в течение 4 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней карбонат калия (0,049 г) и диэтиламин (0,037 мл), а затем нагревали с обратным холодильником в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней карбонат калия (0,049 г) и диэтиламин (0,037 мл), а затем нагревали с обратным холодильником в течение 1 часа 15 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней карбонат калия (0,049 г) и диэтиламин (0,037 мл), а затем нагревали с обратным холодильником в течение 5 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду, насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-97% хлороформ/метанол] с получением 0,15 г метил-2-(2-(бензилокси)-5-(2-(диэтиламино)этокси)бензамидо)-4-фенилбензоата.
К раствору полученного метил-2-(2-(бензилокси)-5-(2-(диэтиламино)этокси)бензамидо)-4-фенилбензоата (0,15 г) в смеси метанола (3,0 мл) и этилацетата (3,0 мл) добавляли 10% палладированый уголь (0,030 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-96% хлороформ/метанол] с получением 0,087 г метил-2-(5-(2-(диэтиламино)этокси)-2-гидроксибензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному метил-2-(5-(2-(диэтиламино)этокси)-2-гидроксибензамидо)-4-фенилбензоату (0,087 г) добавляли диоксан (3,0 мл) и 4 моль/л водный раствор гидроксида натрия (0,19 мл), затем перемешивали при комнатной температуре в течение 2 часов 30 минут, а затем при 50-55°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры и корректировали значение pH до 6,9 добавлением метансульфоновой кислоты, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли воду, и собирали твердое вещество путем фильтрования с получением 0,079 г 2-(5-(2-(диэтиламино)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты.
К полученной 2-(5-(2-(диэтиламино)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоте (0,079 г) добавляли этанол (3,0 мл) и метансульфоновую кислоту (0,011 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,049 г метансульфоната 2-(5-(2-(диэтиламино)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 1,39 (6H, т, J=7,3 Гц), 2,69 (3H, с), 3,32-3,41 (4H, м), 3,62 (2H, т, J=4,9 Гц), 4,37 (2H, т, J=4,9 Гц), 6,96 (1H, д, J=9,0 Гц), 7,19 (1H, дд, J=9,0, 2,9 Гц), 7,39-7,45 (1H, м), 7,45-7,53 (4H, м), 7,69-7,75 (2H, м), 8,20 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,7 Гц).
Пример 146a
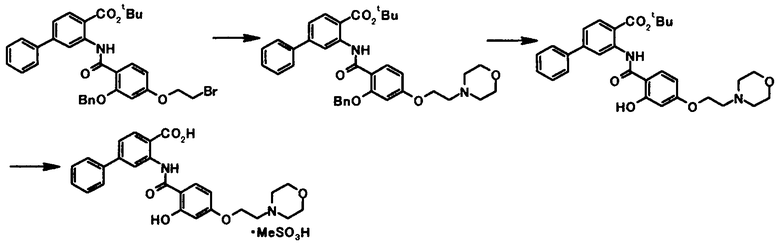
К раствору трет-бутил-2-(2-(бензилокси)-4-(2-бромэтокси)бензамидо)-4-фенилбензоата (0,094 г) в ацетоне (3,0 мл) добавляли карбонат калия (0,065 г) и морфолин (0,041 мл), а затем нагревали с обратным холодильником в течение 45 минут. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней карбонат калия (0,022 г) и морфолин (0,014 мл), а затем нагревали с обратным холодильником в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду, насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-91% хлороформ/метанол] с получением 0,059 г трет-бутил-2-(2-(бензилокси)-4-(2-(морфолин-4-ил)этокси)бензамидо)-4-фенилбензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-4-(2-(морфолин-4-ил)этокси)бензамидо)-4-фенилбензоата (0,059 г) в смеси метанола (2,0 мл) и этилацетата (2,0 мл) добавляли 10% палладированый уголь (0,012 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования. К полученному твердому веществу добавляли трифторуксусную кислоту (4,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. К реакционной смеси добавляли толуол, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования. К полученному твердому веществу добавляли этанол (4,0 мл). После корректировки значения pH до 7,7 добавлением 1 моль/л водного раствора гидроксида натрия твердое вещество собирали путем фильтрования с получением 0,011 г 2-(2-гидрокси-4-(2-(морфолин-4-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
К полученной 2-(2-гидрокси-4-(2-(морфолин-4-ил)этокси)бензамидо)-4-фенилбензойной кислоте (0,011 г) добавляли этанол (2,0 мл) и метансульфоновую кислоту (0,010 мл), а затем перемешивали при комнатной температуре в течение 3 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этанол. Твердое вещество собирали путем фильтрования с получением 6,1 мг метансульфоната 2-(2-гидрокси-4-(2-(морфолин-4-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,31 (3H, с), 3,10-4,10 (10H, м), 4,41 (2H, т, J=4,6 Гц), 6,61 (1H, д, J=2,4 Гц), 6,68 (1H, дд, J=9,0, 2,4 Гц), 7,42-7,58 (4H, м), 7,68-7,76 (2H, м), 7,90 (1H, д, J=9,0 Гц), 8,10 (1H, д, J=8,3 Гц), 8,98 (1H, д, J=1,7 Гц), 11,87 (1H, с), 12,25 (1H, с).
Пример 147a
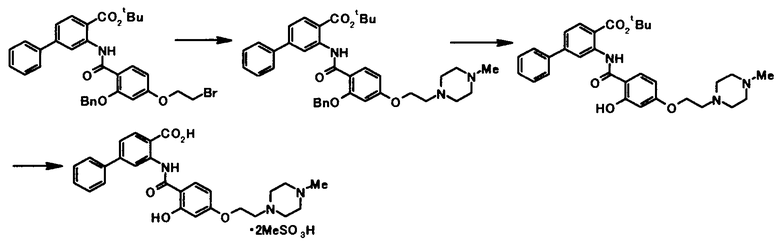
Следующее соединение получали, как описано в Примере 146a.
2-(2-Гидрокси-4-(2-(4-метилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (DMSO-d6) δ: 2,35 (6H, с), 2,86 (3H, с), 3,12-3,70 (10H, м), 4,24-4,38 (2H, м), 6,59 (1H, д, J=2,0 Гц), 6,62-6,70 (1H, м), 7,42-7,58 (4H, м), 7,68-7,76 (2H, м), 7,88 (1H, д, J=8,8 Гц), 8,10 (1H, д, J=8,3 Гц), 8,98 (1H, д, J=1,7 Гц), 11,86 (1H, с), 12,24 (1H, с).
Пример 148a
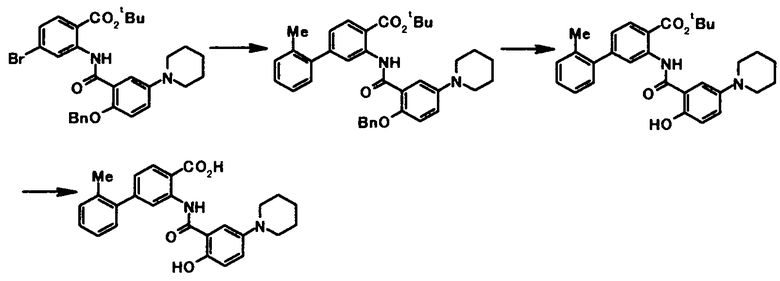
К раствору трет-бутил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-бромбензоата (0,10 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,60 мл), 2-метилфенилбороновую кислоту (0,029 г), карбонат натрия (0,047 г) и дихлорид бис(трифенилфосфин)палладия(II) (2,5 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 99-91% гексан/этилацетат] с получением 0,10 г трет-бутил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-(2-метилфенил)бензоата.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-(2-метилфенил)бензоата (0,10 г) в смеси метанола (2,0 мл) и этилацетата (2,0 мл) добавляли 10% палладированый уголь (0,020 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 45 минут. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 99-91% гексан/этилацетат] с получением 0,063 г трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(2-метилфенил)бензоата в виде желтого твердого вещества.
Раствор полученного трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(2-метилфенил)бензоата (0,063 г) в трифторуксусной кислоте (3,0 мл) перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли воду и этанол. После корректировки значения pH до 5,5 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования с получением 0,048 г 2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(2-метилфенил)бензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,46-1,56 (2H, м), 1,60-1,70 (4H, м), 2,29 (3H, с), 3,00-3,08 (4H, м), 6,91 (1H, д, J=9,0 Гц), 7,14-7,22 (2H, м), 7,24-7,38 (4H, м), 7,39-7,44 (1H, м), 8,08 (1H, д, J=8,1 Гц), 8,66 (1H, д, J=1,5 Гц), 10,91-11,08 (1H, уширенный), 12,24-12,40 (1H, уширенный).
Примеры 149a-155a
Соединения, представленные в Таблице 17a, получали, как описано в Примере 148a.
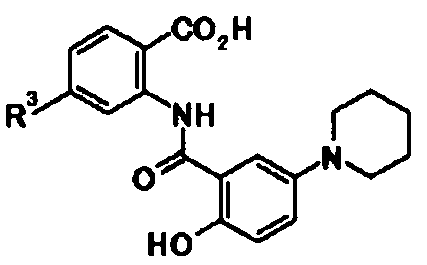
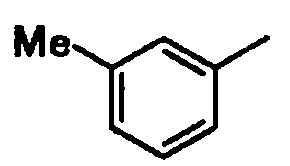
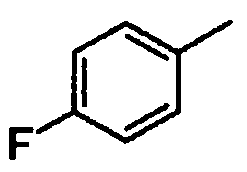
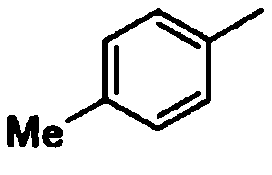
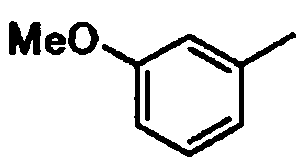
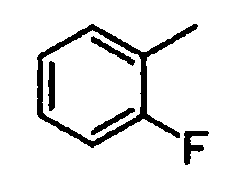
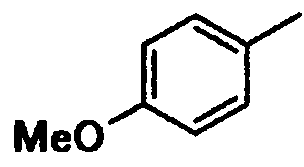
2-(2-Гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(3-метилфенил)бензойная кислота
1H-ЯМР (CDCl3) δ: 1,57-1,70 (2H, м), 1,91-2,05 (4H, м), 2,42 (3H, с), 3,30-3,43 (4H, м), 7,05 (1H, д, J=9,0 Гц), 7,19 (1H, д, J=7,6 Гц), 7,29-7,39 (3H, м), 7,41-7,47 (2H, м), 8,07 (1H, д, J=2,4 Гц), 8,11 (1H, д, J=8,3 Гц), 8,97 (1H, д, J=1,7 Гц).
2-(2-Гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(4-метилфенил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,47-1,56 (2H, м), 1,61-1,71 (4H, м), 2,38 (3H, с), 2,99-3,08 (4H, м), 6,91 (1H, д, J=8,9 Гц), 7,17 (1H, дд, J=8,9, 2,5 Гц), 7,34 (2H, д, J=7,9 Гц), 7,43 (1H, д, J=2,5 Гц), 7,46-7,52 (1H, м), 7,63 (2H, д, J=7,9 Гц), 8,08 (1H, д, J=8,3 Гц), 9,00 (1H, с), 10,95-11,09 (1H, уширенный), 12,29-12,43 (1H, уширенный).
4-(2-Фторфенил)-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,46-1,55 (2H, м), 1,60-1,69 (4H, м), 2,99-3,06 (4H, м), 6,90 (1H, д, J=9,0 Гц), 7,17 (1H, дд, J=9,0, 2,8 Гц), 7,33-7,44 (4H, м), 7,46-7,55 (1H, м), 7,56-7,64 (1H, м), 8,11 (1H, д, J=8,3 Гц), 8,90 (1H, с), 10,93-11,10 (1H, уширенный), 12,36-12,54 (1H, уширенный).
4-(3-Фторфенил)-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,47-1,56 (2H, м), 1,61-1,70 (4H, м), 3,00-3,07 (4H, м), 6,91 (1H, д, J=8,9 Гц), 7,17 (1H, дд, J=8,9, 2,9 Гц), 7,26-7,34 (1H, м), 7,44 (1H, д, J=2,9 Гц), 7,52-7,63 (4H, м), 8,10 (1H, д, J=8,3 Гц), 9,01 (1H, д, J=1,7 Гц), 10,92-11,12 (1H, уширенный), 12,28-12,48 (1H, уширенный).
4-(4-Фторфенил)-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,46-1,56 (2H, м), 1,60-1,71 (4H, м), 2,99-3,08 (4H, м), 6,91 (1H, д, J=8,9 Гц), 7,17 (1H, дд, J=8,9, 2,8 Гц), 7,33-7,41 (2H, м), 7,43 (1H, д, J=2,8 Гц), 7,46-7,53 (1H, м), 7,73-7,82 (2H, м), 8,09 (1H, д, J=8,3 Гц), 8,96-9,02 (1H, м), 10,96-11,08 (1H, уширенный), 12,31-12,46 (1H, уширенный).
2-(2-Гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(3-метоксифенил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,47-1,56 (2H, м), 1,61-1,70 (4H, м), 3,00-3,06 (4H, м), 3,85 (3H, с), 6,91 (1H, д, J=9,0 Гц), 7,01-7,07 (1H, м), 7,17 (1H, дд, J=9,0, 2,9 Гц), 7,22-7,25 (1H, м), 7,26-7,32 (1H, м), 7,41-7,49 (2H, м), 7,51 (1H, дд, J=8,3, 1,7 Гц), 8,09 (1H, д, J=8,3 Гц), 8,98 (1H, д, J=1,7 Гц), 10,92-11,12 (1H, уширенный), 12,30-12,50 (1H, уширенный).
2-(2-Гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(4-метоксифенил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,47-1,55 (2H, м), 1,61-1,69 (4H, м), 3,00-3,06 (4H, м), 3,83 (3H, с), 6,91 (1H, д, J=9,0 Гц), 7,07-7,12 (2H, м), 7,17 (1H, дд, J=9,0, 3,0 Гц), 7,42 (1H, д, J=3,0 Гц), 7,47 (1H, дд, J=8,3, 2,0 Гц), 7,66-7,71 (2H, м), 8,07 (1H, д, J=8,3 Гц), 8,97 (1H, д, J=2,0 Гц), 10,95-11,12 (1H, уширенный), 12,30-12,50 (1H, уширенный).
Пример 156a
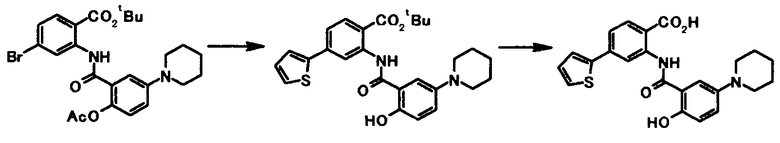
К раствору трет-бутил-2-(2-ацетокси-5-(пиперидин-1-ил)бензамидо)-4-бромбензоата (0,080 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,60 мл), тиофен-2-бороновую кислоту (0,024 г), карбонат натрия (0,041 г) и дихлорид бис(трифенилфосфин)палладия(II) (2,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-85% гексан/этилацетат] с получением 0,027 г трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(тиофен-2-ил)бензоата в виде желтого твердого вещества.
К раствору полученного трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(тиофен-2-ил)бензоата (0,027 г) в смеси диоксана (2,0 мл) и метанола (2,0 мл) добавляли 1 моль/л водный раствор гидроксида натрия (0,17 мл), а затем перемешивали при 50-55°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней 1 моль/л водный раствор гидроксида натрия (0,11 мл), а затем перемешивали при 50-55°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней 1 моль/л водный раствор гидроксида натрия (0,056 мл), а затем перемешивали при 55°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней 1 моль/л водный раствор гидроксида натрия (0,056 мл), а затем перемешивали при 60°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем корректировали значение pH до 7,7 добавлением 10% водного раствора лимонной кислоты, и добавляли воду и этилацетат. Органический слой разделяли, и экстрагировали водный слой хлороформом. Органический слой и экстракт объединяли, и сушили полученную смесь над безводным сульфатом магния. Растворитель выпаривали в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-80% хлороформ/метанол] с получением 0,011 г 2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(тиофен-2-ил)бензойной кислоты в виде оранжевого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,47-1,56 (2H, м), 1,61-1,70 (4H, м), 2,99-3,07 (4H, м), 6,90 (1H, д, J=8,8 Гц), 7,16 (1H, дд, J=8,8, 2,9 Гц), 7,21 (1H, дд, J=5,1, 3,7 Гц), 7,42 (1H, д, J=2,9 Гц), 7,52 (1H, дд, J=8,4, 2,0 Гц), 7,64 (1H, дд, J=3,7, 1,2 Гц), 7,69 (1H, дд, J=5,1, 1,2 Гц), 8,05 (1H, д, J=8,4 Гц), 9,04 (1H, д, J=2,0 Гц), 10,94-11,13 (1H, уширенный).
Пример 157a
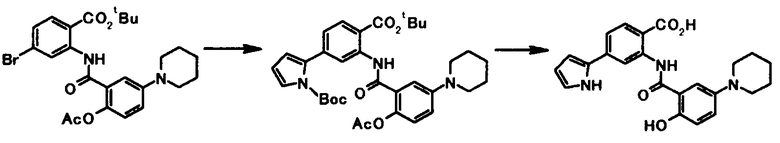
К раствору трет-бутил-2-(2-ацетокси-5-(пиперидин-1-ил)бензамидо)-4-бромбензоата (0,080 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,60 мл), 1-(трет-бутоксикарбонил)-1H-пиррол-2-бороновую кислоту (0,024 г), карбонат натрия (0,041 г) и дихлорид бис(трифенилфосфин)палладия(II) (2,2 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней карбонат натрия (0,016 г), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-80% гексан/этилацетат] с получением трет-бутил-2-(2-ацетокси-5-(пиперидин-1-ил)бензамидо)-4-(1-(трет-бутоксикарбонил)-1H-пиррол-2-ил)бензоата.
К раствору полученного трет-бутил-2-(2-ацетокси-5-(пиперидин-1-ил)бензамидо)-4-(1-(трет-бутоксикарбонил)-1H-пиррол-2-ил)бензоата в диоксане (2,0 мл) добавляли метанол (2,0 мл) и 4 моль/л водный раствор гидроксида натрия (0,19 мл), а затем перемешивали при 55°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 4 моль/л водный раствор гидроксида натрия (0,077 мл), а затем перемешивали при 60°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем корректировали значение pH до 7,8 добавлением 10% водного раствора лимонной кислоты, и добавляли воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-91% хлороформ/метанол] с получением 8 мг 2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-(1H-пиррол-2-ил)бензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,47-1,56 (2H, м), 1,61-1,70 (4H, м), 3,00-3,06 (4H, м), 6,16-6,22 (1H, м), 6,60-6,65 (1H, м), 6,89 (1H, д, J=9,0 Гц), 6,92-6,97 (1H, м), 7,17 (1H, дд, J=9,0, 2,8 Гц), 7,39-7,47 (1H, м), 7,41 (1H, д, J=2,8 Гц), 7,99 (1H, д, J=8,5 Гц), 8,85 (1H, д, J=1,5 Гц), 11,11-11,27 (1H, уширенный), 11,49-11,55 (1H, уширенный).
Пример 158a
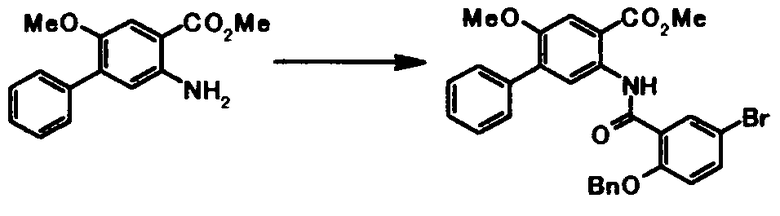
При охлаждении на льду к раствору 2-(бензилокси)-5-бромбензойной кислоты (0,074 г) в смеси хлористого метилена (2,0 мл) и N,N-диметилформамида (0,010 мл) добавляли оксалилхлорид (0,026 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2,0 мл). Полученную смесь добавляли к раствору метил-2-амино-5-метокси-4-фенилбензоата (0,052 г) в смеси пиридина (0,025 мл) и хлористого метилена (1,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Реакционную смесь очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 0,045 г метил-2-(2-(бензилокси)-5-бромбензамидо)-5-метокси-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 3,80 (3H, с), 3,85 (3H, с), 5,45 (2H, с), 6,87 (1H, д, J=8,8 Гц), 7,27-7,40 (4H, м), 7,40-7,47 (5H, м), 7,57 (1H, с), 7,62-7,66 (2H, м), 8,28 (1H, д, J=2,7 Гц), 8,92 (1H, с), 12,08 (1H, с).
Пример 159a
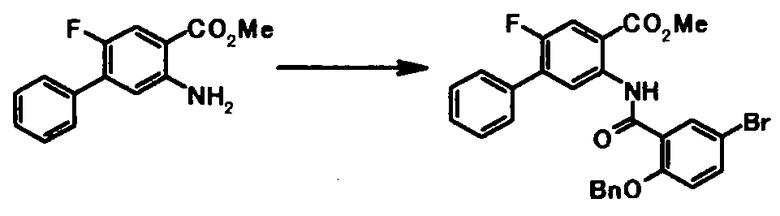
Следующее соединение получали, как описано в Примере 158a.
Метил-2-(2-(бензилокси)-5-бромбензамидо)-5-фтор-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 3,79 (3H, с), 5,46 (2H, с), 6,88 (1H, д, J=8,8 Гц), 7,22-7,37 (4H, м), 7,38-7,51 (5H, м), 7,64-7,72 (2H, м), 7,80 (1H, д, J=11,2 Гц), 8,25-8,31 (1H, м), 9,11 (1H, д, J=7,1 Гц), 12,15-12,24 (1H, уширенный).
Пример 160a
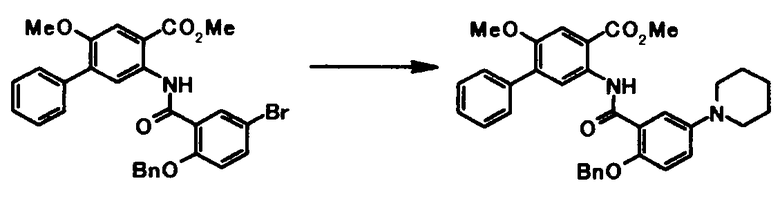
К раствору метил-2-(2-(бензилокси)-5-бромбензамидо)-5-метокси-4-фенилбензоата (0,045 г) в толуоле (2,0 мл) добавляли пиперидин (0,012 мл), карбонат цезия (0,054 г), трис(дибензилиденацетон)дипалладий(0) (2,3 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (5,9 мг) и ацетат палладия(II) (1,1 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 20 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней этилацетат и воду. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 0,034 г метил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-5-метокси-4-фенилбензоата в виде желтого твердого вещества.
1H-ЯМР (CDCl3) δ: 1,49-1,60 (2H, м), 1,64-1,74 (4H, м), 3,04-3,14 (4H, м), 3,76 (3H, с), 3,84 (3H, с), 5,36 (2H, с), 6,91 (1H, д, J=9,0 Гц), 6,99 (1H, дд, J=9,0, 2,9 Гц), 7,22-7,39 (4H, м), 7,39-7,46 (4H, м), 7,56 (1H, с), 7,61-7,68 (2H, м), 7,76 (1H, д, J=3,2 Гц), 8,92 (1H, с), 12,04 (1H, с).
Пример 161a
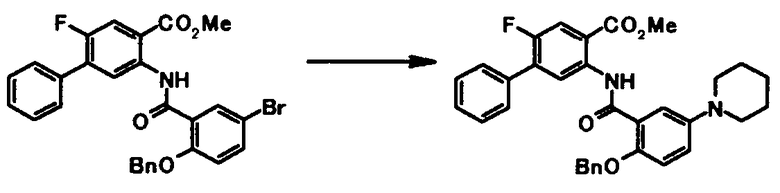
Следующее соединение получали, как описано в Примере 160a.
Метил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-5-фтор-4-фенилбензоат
1H-ЯМР (CDCl3) δ: 1,49-1,59 (2H, м), 1,65-1,74 (4H, м), 3,05-3,13 (4H, м), 3,75 (3H, с), 5,37 (2H, м), 6,92 (1H, д, J=8,9 Гц), 7,00 (1H, дд, J=8,9, 3,2 Гц), 7,23-7,34 (3H, м), 7,37-7,50 (5H, м), 7,64-7,72 (2H, м), 7,73-7,81 (2H, м), 9,12 (1H, д, J=7,3 Гц), 12,15 (1H, с).
Пример 162a
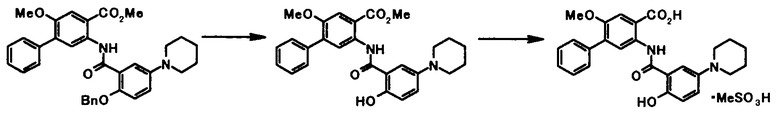
К раствору метил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-5-метокси-4-фенилбензоата (0,034 г) в смеси метанола (2,5 мл) и этилацетата (2,5 мл) добавляли 10% палладированый уголь (6,8 мг), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли гексан и диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,020 г метил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-5-метокси-4-фенилбензоата в виде желтого твердого вещества.
К полученному метил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-5-метокси-4-фенилбензоату (0,020 г) добавляли диоксан (3,0 мл) и 1 моль/л водный раствор гидроксида натрия (0,13 мл), а затем перемешивали при 50-55°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли этанол (2,0 мл) и метансульфоновую кислоту (0,010 мл), а затем перемешивали при комнатной температуре в течение 10 минут. Затем, твердое вещество собирали путем фильтрования с получением 0,012 г метансульфоната 2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-5-метокси-4-фенилбензойной кислоты в виде светло-коричневого твердого вещества.
1H-ЯМР (CD3OD) δ: 1,70-2,20 (6H, м), 2,70 (3H, с), 3,60-3,74 (4H, м), 3,86 (3H, с), 7,17 (1H, д, J=9,0 Гц), 7,34-7,50 (3H, м), 7,54-7,64 (2H, м), 7,68-7,75 (1H, м), 7,77 (1H, с), 8,18 (1H, д, J=2,9 Гц), 8,68 (1H, с).
Пример 163a
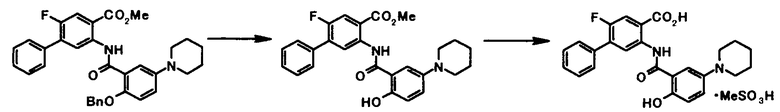
Следующее соединение получали, как описано в Примере 162a.
5-Фтор-2-(2-(гидрокси-5-(пиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты метансульфонат
1H-ЯМР (CD3OD) δ: 1,74-1,85 (2H, м), 1,97-2,07 (4H, м), 2,69 (3H, с), 3,57-3,65 (4H, м), 7,15 (1H, д, J=9,0 Гц), 7,42-7,47 (1H, м), 7,47-7,54 (2H, м), 7,61-7,66 (2H, м), 7,68 (1H, дд, J=9,0, 3,2 Гц), 7,91 (1H, д, J=11,2 Гц), 8,15 (1H, д, J=3,2 Гц), 8,92 (1H, д, J=7,6 Гц).
Пример 164a
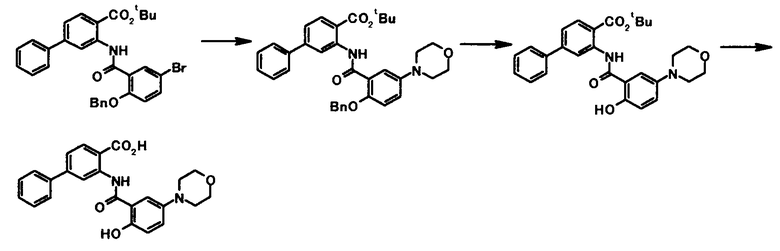
К раствору трет-бутил-2-(2-(бензилокси)-5-бромбензамидо)-4-фенилбензоата (0,060 г) в толуоле (0,90 мл) добавляли морфолин (0,014 мл), карбонат цезия (0,070 г), трис(дибензилиденацетон)дипалладий(0) (1,0 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (2,6 мг) и ацетат палладия(II) (0,5 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней морфолин (4,7 мкл), карбонат цезия (0,035 г), трис(дибензилиденацетон)дипалладий(0) (1,0 мг), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (2,6 мг) и ацетат палладия(II) (0,5 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-60% гексан/этилацетат] с получением 0,060 г трет-бутил-2-(2-(бензилокси)-5-(морфолин-4-ил)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(морфолин-4-ил)бензамидо)-4-фенилбензоата (0,060 г) в смеси этилацетата (1,5 мл) и метанола (1,5 мл) добавляли 10% палладированый уголь (0,030 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов 30 минут. К реакционной смеси добавляли этилацетат. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 0,036 г трет-бутил-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)-4-фенилбензоата в виде желтого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)-4-фенилбензоату (0,036 г) добавляли трифторуксусную кислоту (3 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду и 2-пропанол. После корректировки значения pH до 6,0 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования с получением 0,027 г 2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)-4-фенилбензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,99-3,08 (4H, м), 3,71-3,80 (4H, м), 6,94 (1H, д, J=9,0 Гц), 7,18 (1H, дд, J=9,0, 3,0 Гц), 7,40-7,58 (5H, м), 7,70-7,77 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,02 (1H, д, J=1,7 Гц), 10,99 (1H, с), 12,30-12,41 (1H, уширенный).
Примеры 165a и 166a
Соединения, представленные в Таблице 18a, получали, как описано в Примере 80a.
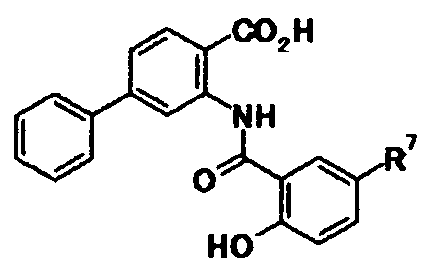
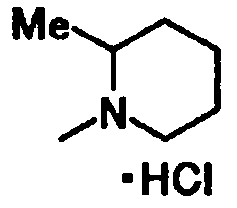
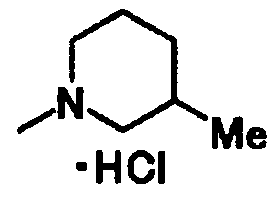
2-(2-Гидрокси-5-(2-метилпиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 1,00 (3H, д, J=6,4 Гц), 1,62-2,15 (6H, м), 3,39-3,70 (2H, м), 3,72-3,87 (1H, м), 7,21 (1H, д, J=8,6 Гц), 7,42-7,50 (1H, м), 7,50-7,58 (3H, м), 7,70-7,76 (2H, м), 7,86-7,98 (1H, м), 8,10 (1H, д, J=8,1 Гц), 8,34-8,45 (1H, м), 9,07 (1H, д, J=1,7 Гц), 11,66-11,86 (1H, уширенный), 11,94-12,11 (1H, уширенный), 12,37 (1H, с), 13,30-13,56 (1H, уширенный).
2-(2-Гидрокси-5-(3-метилпиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 0,94 (3H, д, J=6,6 Гц), 1,16-1,34 (1H, м), 1,74-2,27 (4H, м), 3,03-3,60 (4H, м), 7,17 (1H, д, J=8,8 Гц), 7,43-7,50 (1H, м), 7,51-7,59 (3H, м), 7,68-7,75 (2H, м), 7,77-7,88 (1H, уширенный), 8,11 (1H, д, J=8,0 Гц), 8,17-8,40 (1H, уширенный), 9,07 (1H, д, J=1,7 Гц), 11,76-12,09 (1H, уширенный), 12,36 (1H, с).
1H-ЯМР (DMSO-d6-D2O) δ: 0,97 (3H, д, J=6,6 Гц), 1,19-1,34 (1H, м), 1,76-2,16 (4H, м), 3,13-3,25 (1H, м), 3,35-3,60 (3H, м), 7,20 (1H, д, J=8,8 Гц), 7,45-7,63 (4H, м), 7,70-7,80 (3H, м), 8,13 (1H, д, J=8,1 Гц), 8,20 (1H, д, J=2,9 Гц), 9,01 (1H, д, J=1,5 Гц).
Примеры 167a-169a
Соединения, представленные в Таблице 19a, получали, как описано в Примере 87a.
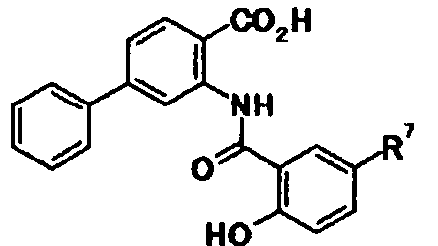
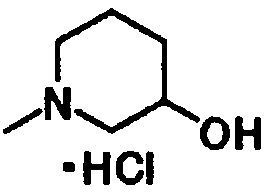
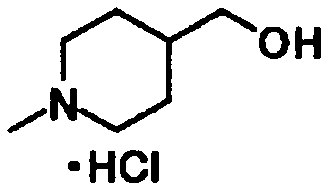
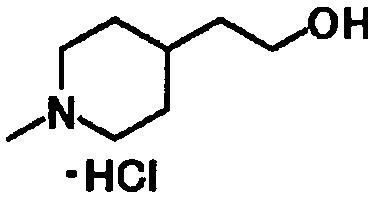
2-(2-Гидрокси-5-(3-гидроксипиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (CD3OD) δ: 1,80-2,01 (3H, м), 2,31-2,47 (1H, м), 3,45-3,62 (2H, м), 3,67-3,76 (2H, м), 4,19-4,26 (1H, м), 7,18 (1H, д, J=9,0 Гц), 7,39-7,45 (1H, м), 7,47-7,53 (3H, м), 7,70-7,78 (3H, м), 8,19-8,23 (2H, м), 9,05 (1H, д, J=1,7 Гц).
2-(2-Гидрокси-5-(4-(гидроксиметил)пиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (CD3OD) δ: 1,73-1,87 (2H, м), 1,90-2,01 (1H, м), 2,10-2,19 (2H, м), 3,56 (2H, д, J=5,8 Гц), 3,63-3,79 (4H, м), 7,18 (1H, д, J=9,0 Гц), 7,40-7,45 (1H, м), 7,47-7,53 (3H, м), 7,70-7,75 (2H, м), 7,76 (1H, дд, J=9,0, 3,1 Гц), 8,21 (1H, д, J=3,1 Гц), 8,21 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,7 Гц).
2-(2-Гидрокси-5-(4-(2-гидроксиэтил)пиперидин-1-ил)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (CD3OD) δ: 1,59-1,66 (2H, м), 1,68-1,83 (2H, м), 1,90-2,03 (1H, м), 2,10-2,20 (2H, м), 3,60-3,76 (6H, м), 7,17 (1H, д, J=9,0 Гц), 7,39-7,45 (1H, м), 7,47-7,53 (3H, м), 7,70-7,75 (2H, м), 7,76 (1H, дд, J=9,0, 2,9 Гц), 8,18-8,23 (2H, м), 9,05 (1H, д, J=1,7 Гц).
Пример 170a
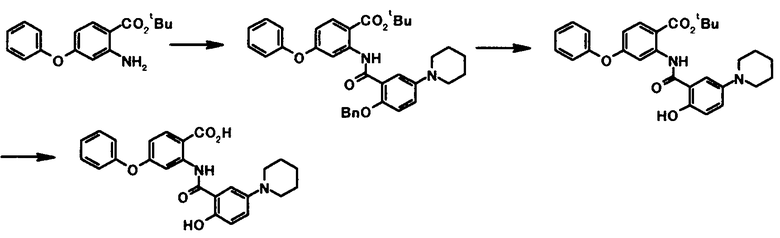
К раствору 2-(бензилокси)-5-(пиперидин-1-ил)бензойной кислоты (0,084 г) в хлористом метилене (1,4 мл) последовательно добавляли N,N-диметилформамид (2,1 мкл) и оксалилхлорид (0,032 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку толуол. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку хлористый метилен (1,0 мл). Полученную смесь при охлаждении на льду добавляли к раствору трет-бутил-2-амино-4-феноксибензоата (0,070 г) в смеси пиридина (0,070 мл) и хлористого метилена (1,4 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 10% водный раствор лимонной кислоты, органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 90-80% гексан/этилацетат] с получением 0,093 г трет-бутил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-феноксибензоата в виде желтого маслянистого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(пиперидин-1-ил)бензамидо)-4-феноксибензоата (0,093 г) в смеси этилацетата (1,5 мл) и метанола (1,5 мл) добавляли 10% палладированый уголь (0,047 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли хлороформ. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 80-70% гексан/этилацетат] с получением 0,067 г трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-феноксибензоата в виде желтого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-феноксибензоату (0,067 г) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и 2-пропанол. После корректировки значения pH до 6,0 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования с получением 0,053 г 2-(2-гидрокси-5-(пиперидин-1-ил)бензамидо)-4-феноксибензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,46-1,54 (2H, м), 1,59-1,68 (4H, м), 2,97-3,04 (4H, м), 6,76 (1H, дд, J=9,0, 2,6 Гц), 6,88 (1H, д, J=8,8 Гц), 7,11-7,20 (3H, м), 7,23-7,30 (1H, м), 7,32 (1H, д, J=2,7 Гц), 7,44-7,52 (2H, м), 8,04 (1H, д, J=9,0 Гц), 8,39 (1H, д, J=2,6 Гц), 10,79-10,94 (1H, уширенный), 12,40-12,58 (1H, уширенный).
Пример 171a
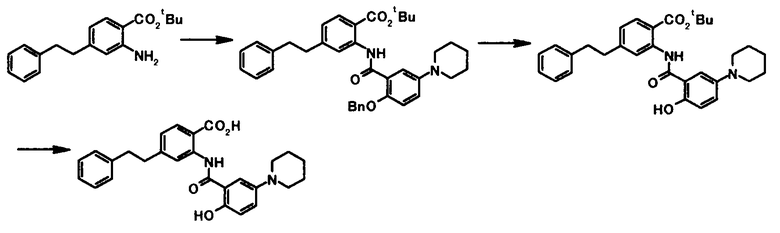
Следующее соединение получали, как описано в Примере 170a.
2-(2-Гидрокси-5-(пиперидин-1-ил)бензамидо)-4-феноксибензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,46-1,56 (2H, м), 1,59-1,70 (4H, м), 2,88-3,06 (8H, м), 6,89 (1H, д, J=9,0 Гц), 7,07 (1H, дд, J=8,2, 1,5 Гц), 7,13-7,22 (2H, м), 7,23-7,32 (4H, м), 7,36-7,40 (1H, м), 7,92 (1H, д, J=8,4 Гц), 8,57 (1H, д, J=1,5 Гц), 10,96-11,12 (1H, уширенный), 12,22-12,40 (1H, уширенный).
Пример 172a
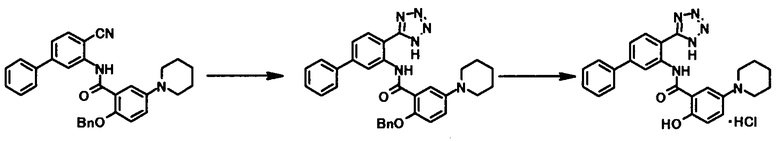
К суспензии 2-(бензилокси)-N-(4-цианобифенил-3-ил)-5-(пиперидин-1-ил)бензамид (0,25 г) в N,N-диметилформамиде (2,5 мл) добавляли азид натрия (0,065 г) и хлорид аммония (0,053 г), а затем перемешивали при 110°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней азид натрия (0,065 г) и хлорид аммония (0,053 г), а затем перемешивали при 110°C в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней затем азид натрия (0,032 г) и хлорид аммония (0,026 г), а затем перемешивали при 110°C в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней азид натрия (0,032 г) и хлорид аммония (0,026 г), а затем перемешивали при 110°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней хлороформ и воду. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол], а затем очищали по методу колоночной хроматографии [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-93% хлороформ/метанол], с получением 0,18 г 2-(бензилокси)-N-(5-фенил-2-(1H-тетразол-5-ил)фенил)-5-(пиперидин-1-ил)бензамида в виде коричневого твердого вещества.
К раствору полученного 2-(бензилокси)-N-(5-фенил-2-(1H-тетразол-5-ил)фенил)-5-(пиперидин-1-ил)бензамида (0,095 г) в смеси этилацетата (6,0 мл) и метанола (3,0 мл) добавляли 10% палладированый уголь (0,050 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 10% палладированый уголь (0,050 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли этилацетат (2,0 мл) и 4,0 моль/л раствор хлорводорода в этилацетате (2,0 мл), а затем перемешивали при комнатной температуре в течение 10 минут. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,016 г гидрохлорида 2-гидрокси-N-(5-фенил-2-(1H-тетразол-5-ил)фенил)-5-(пиперидин-1-ил)бензамида в виде коричневато-красного твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,56-1,74 (2H, м), 1,87-2,01 (4H, м), 3,24-3,70 (4H, м), 7,18 (1H, д, J=9,0 Гц), 7,43-7,50 (1H, м), 7,50-7,60 (2H, м), 7,72 (1H, дд, J=8,2, 1,8 Гц), 7,75-7,89 (3H, м), 8,05 (1H, д, J=8,0 Гц), 8,26-8,37 (1H, м), 8,86 (1H, д, J=2,0 Гц), 11,67 (1H, с), 11,82-12,09 (1H, уширенный).
1H-ЯМР (DMSO-d6-D2O) δ: 1,60-1,73 (2H, м), 1,86-1,98 (4H, м), 3,54 (4H, т, J=5,4 Гц), 7,22 (1H, д, J=9,0 Гц), 7,45-7,52 (1H, м), 7,53-7,62 (2H, м), 7,73 (1H, дд, J=8,1, 1,8 Гц), 7,73-7,82 (3H, м), 8,02 (1H, д, J=8,1 Гц), 8,23 (1H, д, J=3,0 Гц), 8,81 (1H, д, J=1,8 Гц).
Пример 173a
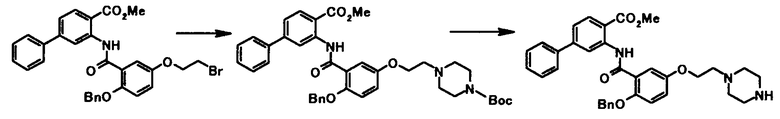
К раствору метил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоата (0,40 г) в 1-метил-2-пирролидоне (2,0 мл) добавляли карбонат калия (0,12 г) и 1-(трет-бутоксикарбонил)пиперидин (0,15 г), а затем перемешивали при 90°C в течение 45 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 80-0% гексан/этилацетат] с получением 0,36 г трет-бутил-4-(2-(4-(бензилокси)-3-(2-(метоксикарбонил)-5-фенилфенилкарбамоил)фенокси)этил)пиперидин-1-карбоксилата в виде белого твердого вещества.
При охлаждении на льду к раствору полученного трет-бутил-4-(2-(4-(бензилокси)-3-(2-(метоксикарбонил)-5-фенилфенилкарбамоил)фенокси)этил)пиперидин-1-карбоксилата (0,36 г) в хлористом метилене (5,0 мл) добавляли трифторуксусную кислоту (1,0 мл), а затем перемешивали при комнатной температуре в течение 4 часов. К реакционной смеси добавляли воду. После корректировки значения pH до 8,0 добавлением насыщенного водного раствора бикарбоната натрия органический слой разделяли, промывали насыщенным водным раствором бикарбоната натрия и сушили над безводным сульфатом натрия. Растворитель выпаривали в условиях пониженного давления с получением 0,30 г метил-2-(2-(бензилокси)-5-(2-(пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в виде желтого маслянистого вещества.
1H-ЯМР (CDCl3) δ: 2,48-2,63 (4H, м), 2,78 (2H, т, J=5,7 Гц), 2,91 (4H, т, J=4,9 Гц), 3,76 (3H, с), 4,12 (2H, т, J=5,7 Гц), 5,38 (2H, с), 6,91-7,01 (2H, м), 7,23-7,52 (9H, м), 7,68-7,77 (3H, м), 8,08 (1H, д, J=8,3 Гц), 9,26 (1H, д, J=1,7 Гц), 12,31 (1H, с).
Пример 174a
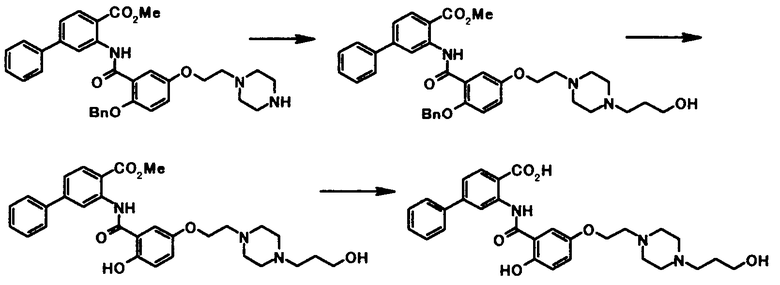
К раствору метил-2-(2-(бензилокси)-5-(2-(пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата (0,084 г) в 2-бутаноне (1,3 мл) добавляли карбонат калия (0,031 г) и 3-бром-1-пропанол (0,013 мл), а затем нагревали с обратным холодильником в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-91% хлороформ/метанол] с получением 0,036 г метил-2-(2-(бензилокси)-5-(2-(4-(3-гидроксипропил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в виде светло-желтого маслянистого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-(2-(4-(3-гидроксипропил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата (0,036 г) в смеси этилацетата (1,5 мл) и метанола (1,5 мл) добавляли 10% палладированый уголь (0,018 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 часов. К реакционной смеси добавляли 10% палладированый уголь (0,018 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,011 г метил-2-(2-гидрокси-5-(2-(4-(3-гидроксипропил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К раствору полученного метил-2-(2-гидрокси-5-(2-(4-(3-гидроксипропил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата (0,011 г) в смеси метанола (1,0 мл) и диоксана (1,0 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (0,031 мл), а затем перемешивали при 50°C в течение 1 часа. К реакционной смеси добавляли 2 моль/л водный раствор гидроксида натрия (0,031 мл), а затем перемешивали при 50°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду. После корректировки значения pH до 6,5 добавлением 1,0 моль/л соляной кислоты добавляли этилацетат. Органический слой разделяли, и экстрагировали водный слой этилацетатом. Органический слой и экстракт объединяли. Полученную смесь промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 6,5 мг 2-(2-гидрокси-5-(2-(4-(3-гидроксипропил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,70-1,84 (2H, м), 2,84-3,90 (14H, м), 4,15 (2H, т, J=4,8 Гц), 6,91 (1H, д, J=9,0 Гц), 7,15 (1H, дд, J=8,9, 2,8 Гц), 7,38-7,45 (2H, м), 7,48-7,55 (2H, м), 7,64 (1H, д, J=2,9 Гц), 7,67-7,73 (2H, м), 8,13 (1H, д, J=8,1 Гц), 8,92 (1H, д, J=1,7 Гц).
1H-ЯМР (DMSO-d6) δ: 1,72-1,87 (2H, м), 2,75-3,35 (12H, м), 3,49 (2H, т, J=6,1 Гц), 4,13-4,22 (2H, м), 6,94 (1H, д, J=9,0 Гц), 7,17 (1H, дд, J=9,0, 2,7 Гц), 7,38-7,48 (2H, м), 7,49-7,58 (2H, м), 7,57 (1H, д, J=2,7 Гц), 7,66-7,75 (2H, м), 8,14 (1H, д, J=8,0 Гц), 8,90 (1H, д, J=1,7 Гц).
Пример 175a
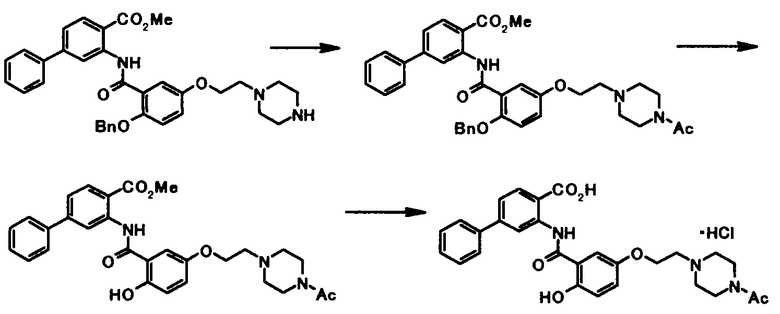
При охлаждении на льду к раствору метил-2-(2-(бензилокси)-5-(2-(пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата (0,12 г) в смеси хлористого метилена (2,4 мл) и пиридина (0,027 мл) добавляли уксусный ангидрид (0,025 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-95% хлороформ/метанол] с получением метил-2-(5-(2-(4-ацетилпиперазин-1-ил)этокси)-2-(бензилокси)бензамидо)-4-фенилбензоата в виде бесцветного маслянистого вещества.
К раствору полученного метил-2-(5-(2-(4-ацетилпиперазин-1-ил)этокси)-2-(бензилокси)бензамидо)-4-фенилбензоата в смеси этилацетата (1,5 мл) и метанола (1,5 мл) добавляли 10% палладированый уголь (0,15 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа 30 минут. К реакционной смеси добавляли хлороформ и метанол. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,083 г метил-2-(5-(2-(4-ацетилпиперазин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К суспензии полученного метил-2-(5-(2-(4-ацетилпиперазин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензоата (0,083 г) в 2-пропаноле (1,5 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (0,24 мл), а затем перемешивали при 50°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду. После корректировки значения pH до 6,5 добавлением 1,0 моль/л соляной кислоты растворитель выпаривали в условиях пониженного давления. К полученному остатку добавляли воду, и собирали твердое вещество путем фильтрования. К полученному твердому веществу добавляли этилацетат (2,0 мл) и 4,0 моль/л раствор хлорводорода в диоксане (0,10 мл), а затем перемешивали при комнатной температуре в течение 3 часов 30 минут. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,038 г гидрохлорида 2-(5-(2-(4-ацетилпиперазин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,05 (3H, с), 2,96-3,30 (3H, м), 3,44-3,84 (5H, м), 3,90-4,12 (1H, м), 4,34-4,49 (3H, м), 7,02 (1H, д, J=8,8 Гц), 7,15 (1H, дд, J=8,8, 2,9 Гц), 7,42-7,59 (5H, м), 7,70-7,76 (2H, м), 8,09 (1H, д, J=8,3 Гц), 9,02-9,06 (1H, м), 11,00-11,20 (2H, м), 12,31 (1H, с).
Пример 176a
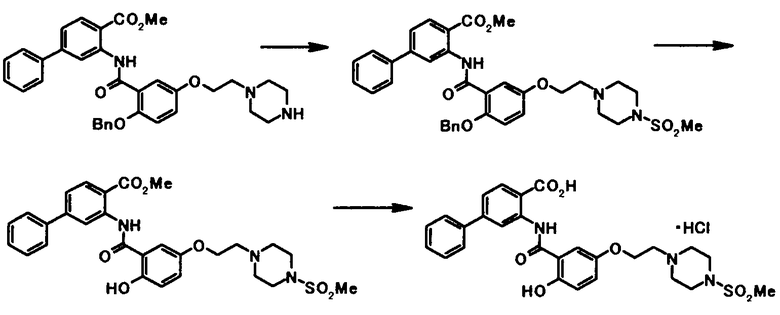
При охлаждении на льду к раствору метил-2-(2-(бензилокси)-5-(2-(пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата (0,11 г) в смеси хлористого метилена (2,2 мл) и пиридина (0,024 мл) добавляли метансульфонилхлорид (0,018 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси последовательно добавляли пиридин (0,016 мл) и метансульфонилхлорид (9,0 мкл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 50-0% гексан/этилацетат] с получением 0,085 г метил-2-(2-(бензилокси)-5-(2-(4-(метилсульфонил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-(2-(4-(метилсульфонил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата (0,085 г) в смеси этилацетате (3,0 мл), метанола (1,5 мл) и диоксан (6,0 мл) добавляли 10% палладированый уголь (0,085 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,063 г метил-2-(2-гидрокси-5-(2-(4-(метилсульфонил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К суспензии полученного метил-2-(2-гидрокси-5-(2-(4-(метилсульфонил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата (0,063 г) в 2-пропаноле (1,2 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (0,17 мл), а затем перемешивали при 50°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду. После корректировки значения pH до 6,5 добавлением 1,0 моль/л соляной кислоты твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли этилацетат (2,0 мл) и 4,0 моль/л раствор хлорводорода в диоксане (0,10 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,025 г гидрохлорида 2-(2-гидрокси-5-(2-(4-(метилсульфонил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 2,98 (3H, с), 3,46-3,74 (8H, м), 3,71 (2H, т, J=4,9 Гц), 4,44 (2H, т, J=4,9 Гц), 6,98 (1H, д, J=9,0 Гц), 7,22 (1H, дд, J=9,0, 3,2 Гц), 7,39-7,46 (1H, м), 7,47-7,53 (3H, м), 7,54 (1H, д, J=3,2 Гц), 7,70-7,75 (2H, м), 8,22 (1H, д, J=8,1 Гц), 9,06 (1H, д, J=1,7 Гц).
Пример 177a
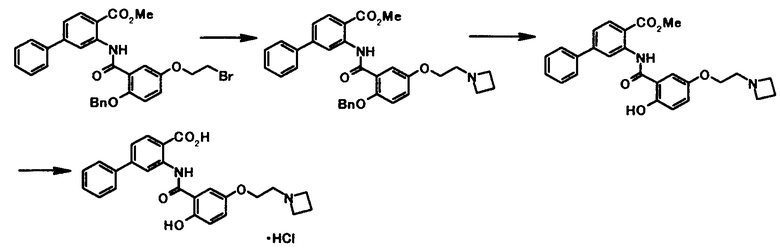
К раствору метил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоата (0,25 г) в 1-метил-2-пирролидоне (1,3 мл) добавляли карбонат калия (0,15 г) и азетидина гидрохлорид (0,046 г), а затем перемешивали при 90°C в течение 45 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,088 г метил-2-(5-(2-(азетидин-1-ил)этокси)-2-(бензилокси)бензамидо)-4-фенилбензоата в виде светло-желтого маслянистого вещества.
К раствору полученного метил-2-(5-(2-(азетидин-1-ил)этокси)-2-(бензилокси)бензамидо)-4-фенилбензоата (0,088 г) в смеси этилацетата (1,5 мл), метанола (1,5 мл) и диоксана (1,5 мл) добавляли 10% палладированый уголь (0,088 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли 10% палладированый уголь (0,088 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 3 часов. Нерастворимые вещества удаляли путем фильтрования, а затем выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,033 г метил-2-(5-(2-(азетидин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К суспензии полученного метил-2-(5-(2-(азетидин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензоата (0,032 г) в 2-пропаноле (1,0 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (0,11 мл), а затем перемешивали при 50°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду. После корректировки значения pH до 6,0 добавлением 1,0 моль/л соляной кислоты твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли этилацетат (1,5 мл) и 4,0 моль/л раствор хлорводорода в диоксане (0,10 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,021 г гидрохлорида 2-(5-(2-(азетидин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (CD3OD) δ: 2,40-2,55 (1H, м), 2,58-2,73 (1H, м), 3,66 (2H, т, J=4,9 Гц), 4,22-4,36 (6H, м), 6,96 (1H, д, J=9,0 Гц), 7,18 (1H, дд, J=9,0, 3,1 Гц), 7,39-7,47 (1H, м), 7,47-7,55 (4H, м), 7,70-7,76 (2H, м), 8,22 (1H, д, J=8,3 Гц), 9,07 (1H, д, J=1,7 Гц).
Примеры 178a-182a
Соединения, представленные в Таблице 20a, получали, как описано в Примере 177a.
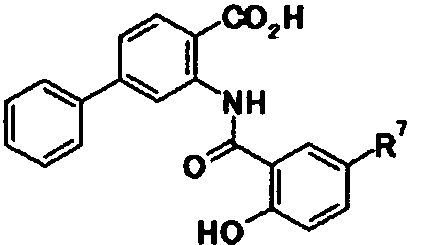
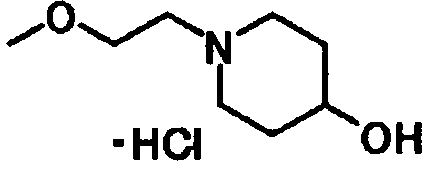
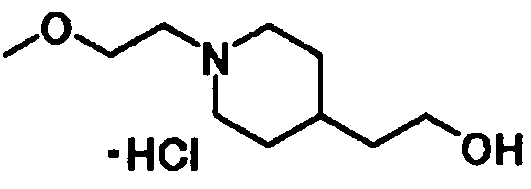
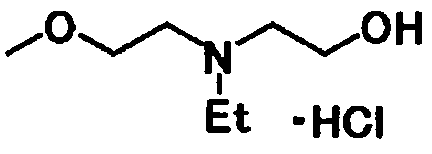
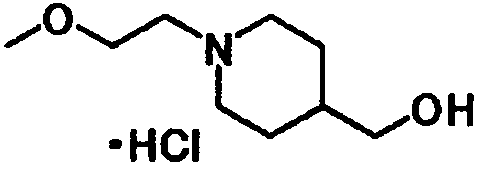
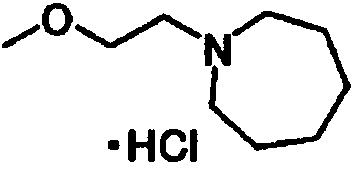
2-(2-Гидрокси-5-(2-(4-гидроксипиперидин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 1,60-1,82 (2H, м), 1,89-2,02 (2H, м), 2,98-3,72 (7H, м), 4,30-4,40 (2H, м), 4,94-5,14 (1H, м), 7,01 (1H, д, J=8,8 Гц), 7,15 (1H, дд, J=8,8, 3,2 Гц), 7,43-7,57 (5H, м), 7,70-7,75 (2H, м), 8,09 (1H, д, J=8,0 Гц), 9,03 (1H, д, J=1,7 Гц), 9,80-10,02 (1H, уширенный), 11,08 (1H, с), 12,36 (1H, с).
2-(2-Гидрокси-5-(2-(4-(2-гидроксиметил)пиперидин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 1,40-1,72 (3H, м), 1,78-1,90 (2H, м), 2,95-3,10 (2H, м), 3,18-3,64 (6H, м), 4,30-4,40 (2H, м), 4,58-4,74 (1H, уширенный), 7,01 (1H, д, J=9,0 Гц), 7,15 (1H, дд, J=9,0, 3,1 Гц), 7,43-7,58 (5H, м), 7,70-7,75 (2H, м), 8,10 (1H, д, J=8,0 Гц), 9,04 (1H, с), 9,60-9,88 (1H, уширенный), 11,09 (1H, с), 12,30-12,46 (1H, уширенный).
2-(2-Гидрокси-5-(2-(4-(гидроксиэтил)пиперидин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 1,30-1,74 (5H, м), 1,76-1,94 (2H, м), 2,93-3,09 (2H, м), 3,40-3,64 (6H, м), 4,28-4,56 (3H, м), 7,01 (1H, д, J=8,9 Гц), 7,14 (1H, дд, J=8,9, 3,0 Гц), 7,43-7,58 (5H, м), 7,70-7,75 (2H, м), 8,09 (1H, д, J=8,3 Гц), 9,04 (1H, д, J=1,7 Гц), 9,66-9,94 (1H, уширенный), 11,08 (1H, с), 12,35 (1H, с).
2-(5-(2-(Гомопиперидин-1-ил)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 1,53-1,73 (4H, м), 1,76-1,92 (4H, м), 3,18-3,60 (6H, м), 4,35 (2H, т, J=4,9 Гц), 7,01 (1H, д, J=9,0 Гц), 7,15 (1H, дд, J=9,0, 3,2 Гц), 7,42-7,58 (5H, м), 7,69-7,76 (2H, м), 8,09 (1H, д, J=8,3 Гц), 9,04 (1H, д, J=1,7 Гц), 9,98-10,14 (1H, уширенный), 11,08 (1H, с), 12,33 (1H, с), 13,30-13,52 (1H, уширенный).
2-(5-(2-(Этил(2-гидроксиэтил)амино)этокси)-2-гидроксибензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6) δ: 1,28 (3H, т, J=7,2 Гц), 3,18-3,42 (4H, м), 3,52-3,65 (2H, м), 3,79 (2H, т, J=5,0 Гц), 4,36 (2H, т, J=5,0), 5,26-5,49 (1H, уширенный), 7,02 (1H, д, J=8,9 Гц), 7,14 (1H, дд, J=8,9, 3,2 Гц), 7,43-7,58 (5H, м), 7,69-7,76 (2H, м), 8,09 (1H, д, J=8,0 Гц), 9,04 (1H, д, J=1,7 Гц), 9,72-10,00 (1H, уширенный), 11,10 (1H, с), 12,36 (1H, с).
Пример 183a
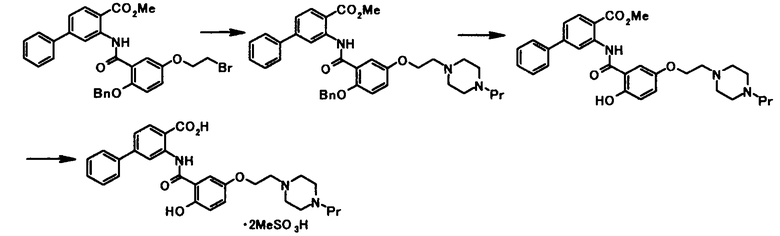
К раствору метил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоата (0,080 г) в ацетоне (1,6 мл) добавляли карбонат калия (0,14 г) и 1-пропилпиперазина дигидрохлорид (0,12 г), а затем нагревали с обратным холодильником в течение 4 часов. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и хлороформ. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,081 г метил-2-(2-(бензилокси)-5-(2-(4-пропилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в виде светло-желтого маслянистого вещества.
К раствору метил-2-(2-(бензилокси)-5-(2-(4-пропилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата (0,081 г) в смеси метанола (1,5 мл) и этилацетата (1,5 мл) добавляли 10% палладированый уголь (0,081 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов 30 минут. К реакционной смеси добавляли хлороформ. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,043 г метил-2-(2-гидрокси-5-(2-(4-пропилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоата в виде оранжевого твердого вещества.
К полученному метил-2-(2-гидрокси-5-(2-(4-пропилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензоату (0,043 г) добавляли метанол (2,0 мл) и 2,0 моль/л водный раствор гидроксида натрия (0,12 мл), а затем перемешивали при 50°C в течение 1 часа. К реакционной смеси добавляли 2 моль/л водный раствор гидроксида натрия (0,25 мл), а затем перемешивали при 50°C в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду. После корректировки значения pH до 6,0 добавлением 2,0 моль/л соляной кислоты твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли этилацетат (3,0 мл) и метансульфоновую кислоту (9,2 мкл), а затем перемешивали при комнатной температуре в течение 4 часов. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,035 г диметансульфоната 2-(2-гидрокси-5-(2-(4-пропилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 1,05 (3H, т, J=7,4 Гц), 1,74-1,88 (2H, м), 2,72 (6H, с), 3,17-3,26 (2H, м), 3,45-3,90 (10H, м), 4,43 (2H, т, J=4,9 Гц), 6,97 (1H, д, J=9,0 Гц), 7,22 (1H, дд, J=9,0, 3,2 Гц), 7,39-7,56 (5H, м), 7,69-7,76 (2H, м), 8,22 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=1,7 Гц).
Примеры 184a и 185a
Соединения, представленные в Таблице 21a, получали, как описано в Примере 183a.
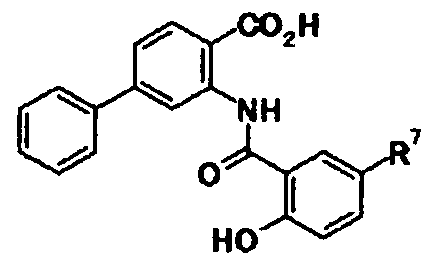
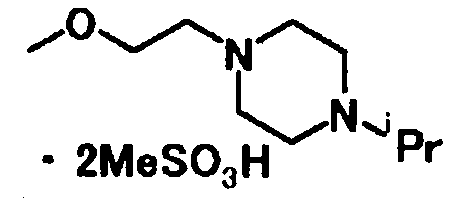
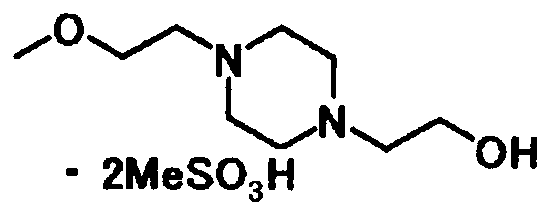
2-(2-Гидрокси-5-(2-(4-изопропилпиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (CD3OD) δ: 1,43 (6H, д, J=6,6 Гц), 2,72 (6H, с), 3,40-4,00 (11H, м), 4,43 (2H, т, J=4,9 Гц), 6,97 (1H, д, J=9,0 Гц), 7,22 (1H, дд, J=9,0, 2,9 Гц), 7,39-7,46 (1H, м), 7,47-7,56 (4H, м), 7,70-7,76 (2H, м), 8,22 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=1,7 Гц).
2-(2-Гидрокси-5-(2-(4-(2-гидроксиэтил)пиперазин-1-ил)этокси)бензамидо)-4-фенилбензойной кислоты диметансульфонат
1H-ЯМР (CD3OD) δ: 2,73 (6H, с), 3,39-3,47 (2H, м), 3,60-3,90 (10H, м), 3,90-3,98 (2H, м), 4,40-4,48 (2H, м), 6,97 (1H, д, J=9,0 Гц), 7,23 (1H, дд, J=9,0, 3,1 Гц), 7,39-7,55 (5H, м), 7,68-7,75 (2H, м), 8,20 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,7 Гц).
Пример 186a
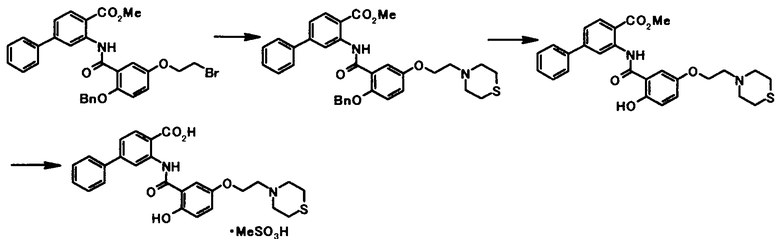
К раствору метил-2-(2-(бензилокси)-5-(2-бромэтокси)бензамидо)-4-фенилбензоата (2,0 г) в ацетоне (20 мл) добавляли карбонат калия (2,0 г) и тиоморфолин (1,1 мл), а затем нагревали с обратным холодильником в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней тиоморфолин (0,55 мл), а затем нагревали с обратным холодильником в течение 2 часов 30 минут. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и хлороформ. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 70-40% гексан/этилацетат] с получением 1,9 г метил-2-(2-(бензилокси)-5-(2-(тиоморфолин-4-ил)этокси)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному метил-2-(2-(бензилокси)-5-(2-(тиоморфолин-4-ил)этокси)бензамидо)-4-фенилбензоату (0,80 г) добавляли тиоанизол (3,2 мл) и трифторуксусную кислоту (10 мл), а затем перемешивали при комнатной температуре в течение 18 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку насыщенный водный раствор бикарбоната натрия и хлороформ. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 70-0% гексан/этилацетат 100-95% хлороформ/метанол] с получением 0,54 г метил-2-(2-гидрокси-5-(2-(тиоморфолин-4-ил)этокси)бензамидо)-4-фенилбензоата в виде коричневого твердого вещества.
К полученному метил-2-(2-гидрокси-5-(2-(тиоморфолин-4-ил)этокси)бензамидо)-4-фенилбензоату (0,15 г) добавляли метанол (5,0 мл) и 2,0 моль/л водный раствор гидроксида натрия (1,5 мл), а затем перемешивали при 40-50°C в течение 1 часа 30 минут. После охлаждения реакционной смеси до комнатной температуры и корректировки значения pH до 6,8 добавлением 10% водного раствора лимонной кислоты твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли этилацетат (5,0 мл) и метансульфоновую кислоту (0,015 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,12 г метансульфоната 2-(2-гидрокси-5-(2-(тиоморфолин-4-ил)этокси)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 2,69 (3H, с), 2,95-3,11 (4H, м), 3,50-3,83 (4H, м), 3,65 (2H, т, J=5,0 Гц), 4,41 (2H, т, J=5,0 Гц), 6,95 (1H, д, J=9,0 Гц), 7,19 (1H, дд, J=9,0, 3,2 Гц), 7,38-7,53 (5H, м), 7,68-7,74 (2H, м), 8,19 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,7 Гц).
Пример 187a
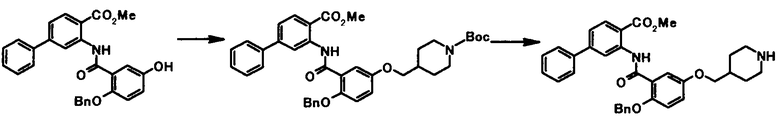
К раствору метил-2-(2-(бензилокси)-5-гидроксибензамидо)-4-фенилбензоата (0,50 г) в тетрагидрофуране (5,0 мл) добавляли трет-бутил-4-(гидроксиметил)пиперидин-1-карбоксилат (0,26 г), трифенилфосфин (0,35 г) и диизопропилазодикарбоксилат (0,26 мл), а затем перемешивали при комнатной температуре в течение 30 минут. К реакционной смеси добавляли трифенилфосфин (0,35 г) и диизопропилазодикарбоксилат (0,26 мл), а затем перемешивали при комнатной температуре в течение 30 минут. К реакционной смеси добавляли трифенилфосфин (0,35 г) и диизопропилазодикарбоксилат (0,26 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-70% гексан/этилацетат] с получением метил-2-(2-(бензилокси)-5-((1-(трет-бутоксикарбонил)пиперидин-4-ил)метокси)бензамидо)-4-фенилбензоата в виде желтого маслянистого вещества.
При охлаждении на льду к раствору полученного метил-2-(2-(бензилокси)-5-((1-(трет-бутоксикарбонил)пиперидин-4-ил)метокси)бензамидо)-4-фенилбензоата в хлористом метилене (9,4 мл) добавляли трифторуксусную кислоту (1,9 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Реакционную смесь при охлаждении на льду добавляли к насыщенному водному раствору бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором бикарбоната натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,30 г метил-2-(2-(бензилокси)-5-(пиперидин-4-илметокси)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6-D2O) δ: 1,10-1,23 (2H, м), 1,64-1,74 (2H, м), 1,74-1,86 (1H, м), 2,41-2,52 (2H, м), 2,89-2,98 (2H, м), 3,76 (3H, с), 3,79 (2H, д, J=6,3 Гц), 5,39 (2H, с), 7,11 (1H, дд, J=9,0, 3,2 Гц), 7,21 (1H, д, J=9,0 Гц), 7,25-7,35 (3H, м), 7,43-7,51 (4H, м), 7,52-7,59 (3H, м), 7,70-7,76 (2H, м), 8,07 (1H, д, J=8,3 Гц), 9,04 (1H, д, J=1,5 Гц).
Пример 188a
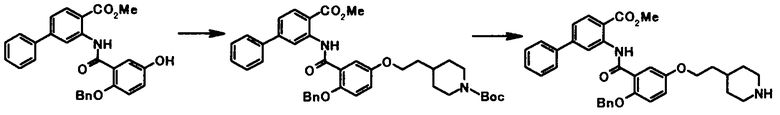
Следующее соединение получали, как описано в Примере 187a.
Метил-2-(2-(бензилокси)-5-(2-(пиперидин-4-ил)этокси)бензамидо)-4-фенилбензоат
1H-ЯМР (DMSO-d6) δ: 1,10-1,28 (2H, м), 1,57-1,77 (5H, м), 2,56-2,67 (2H, м), 3,00-3,10 (2H, м), 3,76 (3H, с), 3,96-4,06 (2H, м), 5,41 (2H, с), 7,10 (1H, дд, J=9,2, 3,2 Гц), 7,20 (1H, д, J=9,2 Гц), 7,24-7,36 (3H, м), 7,43-7,59 (7H, м), 7,70-7,77 (2H, м), 8,07 (1H, д, J=8,3 Гц), 9,04-9,09 (1H, м), 12,03 (1H, с).
Пример 189a
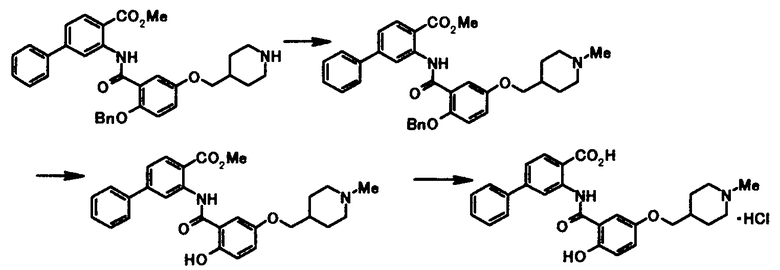
К раствору метил-2-(2-(бензилокси)-5-(пиперидин-4-илметокси)бензамидо)-4-фенилбензоата (0,13 г) в хлороформе (1,9 мл) последовательно добавляли 37% водный раствор формальдегида (0,17 мл) и триацетоксиборгидрид натрия (0,073 г), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия и хлороформ. Органический слой разделяли и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 100-90% хлороформ/метанол] с получением 0,11 г метил-2-(2-(бензилокси)-5-((1-метилпиперидин-4-ил)метокси)бензамидо)-4-фенилбензоата в виде бесцветного маслянистого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-((1-метилпиперидин-4-ил)метокси)бензамидо)-4-фенилбензоата (0,11 г) в смеси этилацетата (1,5 мл) и метанола (1,5 мл) добавляли 10% палладированый уголь (0,11 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа 30 минут. К реакционной смеси добавляли хлороформ. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,070 г метил-2-(2-гидрокси-5-((1-метилпиперидин-4-ил)метокси)бензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К суспензии полученного метил-2-(2-гидрокси-5-((1-метилпиперидин-4-ил)метокси)бензамидо)-4-фенилбензоата (0,070 г) в 2-пропаноле (1,0 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (0,37 мл), а затем перемешивали при 50°C в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду. После корректировки значения pH до 6,0 добавлением 1 моль/л соляной кислоты, твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли этилацетат (2,0 мл) и 4 моль/л раствор хлорводорода в диоксане (0,20 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,058 г гидрохлорида 2-(2-гидрокси-5-(1-метилпиперидин-4-илметокси)бензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,47-1,63 (2H, м), 1,82-2,04 (3H, м), 2,70-2,79 (3H, м), 2,88-3,03 (2H, м), 3,40-3,49 (2H, м), 3,82-3,89 (2H, м), 6,97 (1H, д, J=9,0 Гц), 7,08 (1H, дд, J=9,0, 3,1 Гц), 7,43-7,58 (5H, м), 7,69-7,76 (2H, м), 8,09 (1H, д, J=8,3 Гц), 9,02 (1H, д, J=1,7 Гц), 9,66-9,80 (1H, уширенный), 11,03 (1H, с), 12,28-12,38 (1H, уширенный), 13,38-13,52 (1H, уширенный).
Пример 190a
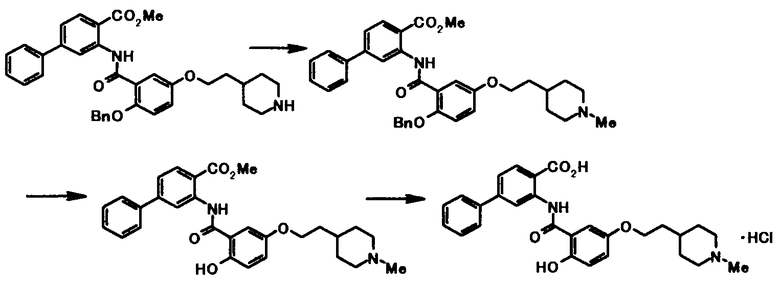
Следующее соединение получали, как описано в Примере 189a.
2-(2-Гидрокси-5-(2-(1-метилпиперидин-4-ил)этокси)бензамидо)-4-фенилбензойной кислоты гидрохлорид
1H-ЯМР (DMSO-d6-D2O) δ: 1,33-1,48 (2H, м), 1,64-1,88 (3H, м), 1,88-1,98 (2H, м), 2,74 (3H, с), 2,87-2,98 (2H, м), 3,36-3,45 (2H, м), 3,97-4,06 (2H, м), 6,97 (1H, д, J=8,8 Гц), 7,08 (1H, дд, J=8,8, 3,2 Гц), 7,42-7,50 (2H, м), 7,51-7,59 (3H, м), 7,70-7,76 (2H, м), 8,11 (1H, д, J=8,3 Гц), 9,01 (1H, д, J=1,7 Гц).
Примеры 191a-194a
Соединения, представленные в Таблице 22a, получали, как описано в Примере 164a.
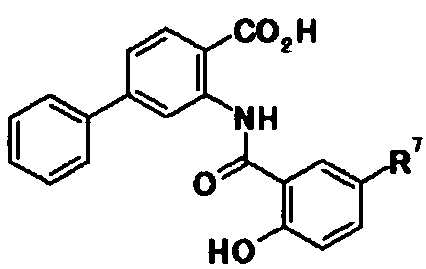
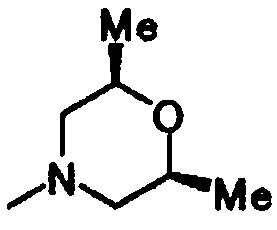
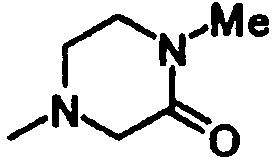
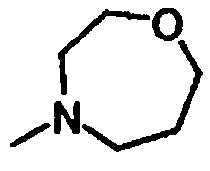
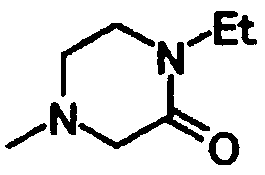
2-(5-((2S,6R)-2,6-Диметилморфолин-4-ил)-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,16 (6H, д, J=6,1 Гц), 2,22 (2H, дд, J=11,0, 10,6 Гц), 3,44 (2H, д, J=10,6 Гц), 3,67-3,78 (2H, м), 6,92 (1H, д, J=8,8 Гц), 7,16 (1H, дд, J=8,8, 3,0 Гц), 7,42-7,58 (5H, м), 7,70-7,76 (2H, м), 8,09 (1H, д, J=8,3 Гц), 9,03 (1H, д, J=1,7 Гц), 10,89 (1H, с), 12,24-12,36 (1H, уширенный).
2-(2-Гидрокси-5-(1,4-оксазепан-4-ил)бензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,88-1,98 (2H, м), 3,51-3,62 (6H, м), 3,71-3,77 (2H, м), 6,88 (1H, д, J=9,0 Гц), 6,98 (1H, дд, J=9,0, 2,9 Гц), 7,21 (1H, д, J=2,9 Гц), 7,42-7,58 (4H, м), 7,70-7,77 (2H, м), 8,10 (1H, д, J=8,3 Гц), 9,03 (1H, д, J=1,7 Гц), 10,68 (1H, с), 12,30-12,42 (1H, уширенный).
2-(2-Гидрокси-5-(4-метил-3-оксопиперазин-1-ил)бензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6+D2O) δ: 2,91 (3H, с), 3,36-3,48 (4H, м), 3,69 (2H, с), 6,98 (1H, д, J=9,0 Гц), 7,21 (1H, дд, J=9,0, 2,9 Гц), 7,43 (1H, д, J=2,9 Гц), 7,44-7,60 (4H, м), 7,70-7,78 (2H, м), 8,12 (1H, д, J=8,3 Гц), 8,97 (1H, д, J=1,7 Гц).
2-(5-(4-Этил-3-оксопиперазин-1-ил)-2-гидроксибензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,07 (3H, т, J=7,1 Гц), 3,15-3,48 (6H, м), 3,68 (2H, с), 6,94 (1H, д, J=8,9 Гц), 7,21 (1H, дд, J=8,9, 2,9 Гц), 7,40-7,57 (5H, м), 7,68-7,76 (2H, м), 8,10 (1H, д, J=8,3 Гц), 8,99 (1H, д, J=1,9 Гц), 11,02-11,22 (1H, уширенный).
1H-ЯМР (DMSO-d6-D2O) δ: 1,08 (3H, т, J=7,2 Гц), 3,34-3,50 (6H, м), 3,69 (2H, с), 6,97 (1H, д, J=9,0 Гц), 7,21 (1H, дд, J=9,0, 3,0 Гц), 7,42-7,59 (4H, м), 7,43 (1H, д, J=3,0 Гц), 7,70-7,77 (2H, м), 8,12 (1H, д, J=8,3 Гц), 8,97 (1H, д, J=1,7 Гц).
Пример 195a
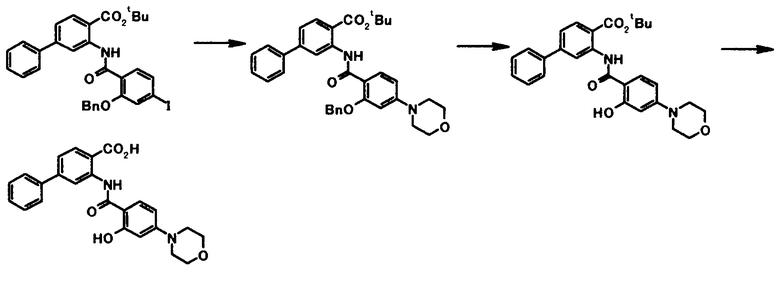
Следующее соединение получали, как описано в Примере 164a.
2-(2-Гидрокси-4-(морфолин-4-ил)бензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 3,22-3,29 (4H, м), 3,69-3,77 (4H, м), 6,40 (1H, д, J=2,4 Гц), 6,64 (1H, дд, J=9,3, 2,4 Гц), 7,42-7,57 (4H, м), 7,69-7,76 (3H, м), 8,10 (1H, д, J=8,3 Гц), 8,95 (1H, д, J=2,0 Гц), 11,85 (1H, с), 12,19-12,28 (1H, уширенный).
Пример 196a
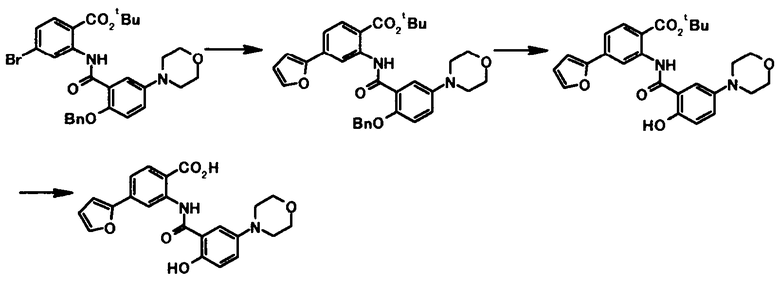
К трет-бутил-2-(2-(бензилокси)-5-(морфолин-4-ил)бензамидо)-4-бромбензоату (0,20 г) добавляли диметиловый эфир этиленгликоля (2,0 мл), воду (0,60 мл), фуран-2-бороновую кислоту (0,047 г), карбонат натрия (0,093 г) и дихлорид бис(трифенилфосфин)палладия(II) (4,9 мг), а затем перемешивали при 75°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней дихлорид бис(трифенилфосфин)палладия(II) (4,9 мг), а затем перемешивали при 75°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 85-70% гексан/этилацетат] с получением 0,14 г трет-бутил-2-(2-(бензилокси)-5-(морфолин-4-ил)бензамидо)-4-(фуран-2-ил)бензоата в виде светло-желтого твердого вещества.
К раствору полученного трет-бутил-2-(2-(бензилокси)-5-(морфолин-4-ил)бензамидо)-4-(фуран-2-ил)бензоата (0,14 г) в смеси метанола (2,0 мл) и этилацетата (2,0 мл) добавляли 10% палладированый уголь (0,029 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа. К реакционной смеси добавляли хлороформ. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 85-75% гексан/этилацетат] с получением 0,085 г трет-бутил-4-(фуран-2-ил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензоата в виде желтого твердого вещества.
К полученному трет-бутил-4-(фуран-2-ил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензоату (0,085 г) добавляли трифторуксусную кислоту (2,0 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку воду и 2-пропанол. После корректировки значения pH до 6,0 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования с получением 0,064 г 4-(фуран-2-ил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,99-3,08 (4H, м), 3,71-3,79 (4H, м), 6,68 (1H, дд, J=3,4, 1,5 Гц), 6,94 (1H, д, J=9,0 Гц), 7,12 (1H, д, J=3,4 Гц), 7,18 (1H, дд, J=9,0, 3,0 Гц), 7,42 (1H, д, J=3,0 Гц), 7,54 (1H, дд, J=8,3, 1,7 Гц), 7,88 (1H, д, J=1,5 Гц), 8,05 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=1,7 Гц), 10,99 (1H, с), 12,38 (1H, с).
Примеры 197a-210a
Соединения, представленные в Таблице 23a, получали, как описано в Примере 196a.
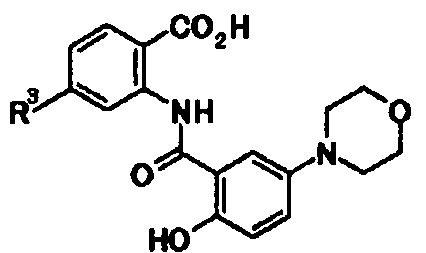
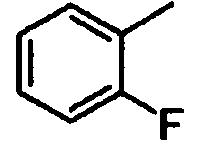
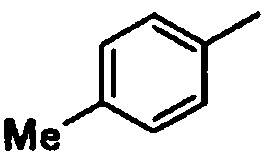
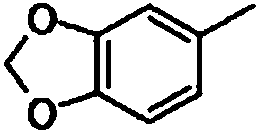
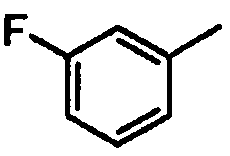
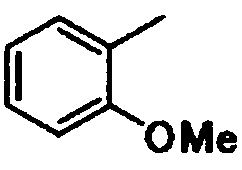
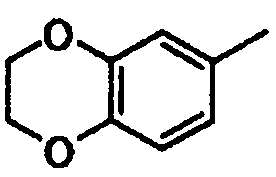
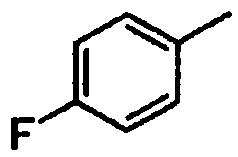
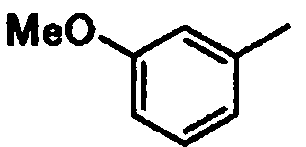
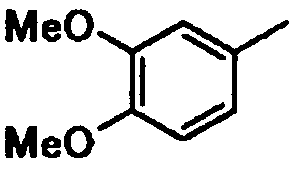
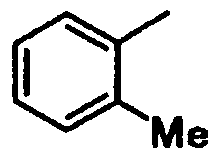
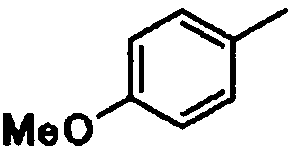
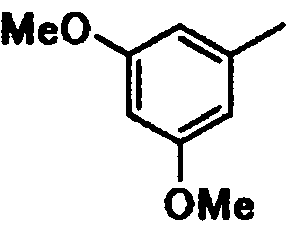
4-(2-Фторфенил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,98-3,09 (4H, м), 3,70-3,81 (4H, м), 6,94 (1H, д, J=9,0 Гц), 7,18 (1H, дд, J=9,0, 2,9 Гц), 7,32-7,45 (4H, м), 7,46-7,55 (1H, м), 7,56-7,64 (1H, м), 8,11 (1H, д, J=8,3 Гц), 8,91 (1H, с), 10,97 (1H, с), 12,29 (1H, с), 13,20-14,00 (1H, уширенный).
4-(3-Фторфенил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,99-3,08 (4H, м), 3,72-3,80 (4H, м), 6,94 (1H, д, J=8,9 Гц), 7,18 (1H, дд, J=8,9, 3,0 Гц), 7,26-7,35 (1H, м), 7,43 (1H, д, J=3,0 Гц), 7,52-7,63 (4H, м), 8,10 (1H, д, J=8,3 Гц), 9,02 (1H, д, J=2,0 Гц), 10,99 (1H, с), 12,32 (1H, с).
4-(4-Фторфенил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,98-3,08 (4H, м), 3,72-3,80 (4H, м), 6,94 (1H, д, J=9,0 Гц), 7,18 (1H, дд, J=9,0, 2,9 Гц), 7,33-7,41 (2H, м), 7,42 (1H, д, J=2,9 Гц), 7,47-7,53 (1H, м), 7,73-7,82 (2H, м), 8,09 (1H, д, J=8,3 Гц), 8,99 (1H, д, J=1,7 Гц), 10,99 (1H, с), 12,33 (1H, с).
2-(2-Гидрокси-5-(морфолин-4-ил)бензамидо)-4-(2-метилфенил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,29 (3H, с), 2,97-3,06 (4H, м), 3,70-3,79 (4H, м), 6,93 (1H, д, J=9,0 Гц), 7,13-7,22 (2H, м), 7,23-7,41 (5H, м), 8,07 (1H, д, J=8,1 Гц), 8,66 (1H, д, J=1,5 Гц), 10,95 (1H, с), 12,30 (1H, с), 13,25-13,85 (1H, уширенный).
2-(2-Гидрокси-5-(морфолин-4-ил)бензамидо)-4-(3-метилфенил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,41 (3H, с), 2,98-3,08 (4H, м), 3,70-3,80 (4H, м), 6,94 (1H, д, J=8,9 Гц), 7,18 (1H, дд, J=8,9, 2,9 Гц), 7,27 (1H, д, J=7,3 Гц), 7,37-7,58 (5H, м), 8,09 (1H, д, J=8,3 Гц), 8,99 (1H, д, J=1,7 Гц), 10,99 (1H, с), 12,33 (1H, с), 13,10-13,95 (1H, уширенный).
2-(2-Гидрокси-5-(морфолин-4-ил)бензамидо)-4-(4-метилфенил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,38 (3H, с), 2,97-3,08 (4H, м), 3,68-3,80 (4H, м), 6,94 (1H, д, J=8,9 Гц), 7,18 (1H, дд, J=8,9, 2,9 Гц), 7,34 (2H, д, J=8,0 Гц), 7,42 (1H, д, J=2,9 Гц), 7,49 (1H, дд, J=8,3, 1,8 Гц), 7,63 (2H, д, J=8,0 Гц), 8,08 (1H, д, J=8,3 Гц), 9,00 (1H, д, J=1,8 Гц), 11,00 (1H, с), 12,35 (1H, с).
2-(2-Гидрокси-5-(морфолин-4-ил)бензамидо)-4-(2-метоксифенил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,99-3,07 (4H, м), 3,71-3,78 (4H, м), 3,80 (3H, с), 6,93 (1H, д, J=8,8 Гц), 7,04-7,12 (1H, м), 7,13-7,20 (2H, м), 7,32 (1H, дд, J=8,2, 1,8 Гц), 7,35 (1H, дд, J=7,6, 1,7 Гц), 7,38-7,46 (2H, м), 8,03 (1H, д, J=8,2 Гц), 8,78 (1H, д, J=1,7 Гц), 11,05 (1H, с), 12,30-12,54 (1H, уширенный), 13,10-13,90 (1H, уширенный).
2-(2-Гидрокси-5-(морфолин-4-ил)бензамидо)-4-(3-метоксифенил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 3,00-3,07 (4H, м), 3,70-3,79 (4H, м), 3,85 (3H, с), 6,94 (1H, д, J=8,9 Гц), 7,01-7,07 (1H, м), 7,18 (1H, дд, J=8,9, 3,1 Гц), 7,21-7,26 (1H, м), 7,26-7,32 (1H, м), 7,43 (1H, д, J=3,1 Гц), 7,45 (1H, дд, J=7,9, 7,9 Гц), 7,52 (1H, дд, J=8,3, 1,8 Гц), 8,09 (1H, д, J=8,3 Гц), 8,99 (1H, д, J=1,8 Гц), 10,99 (1H, с), 12,31 (1H, с), 13,20-13,90 (1H, уширенный).
2-(2-Гидрокси-5-(морфолин-4-ил)бензамидо)-4-(4-метоксифенил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,99-3,08 (4H, м), 3,71-3,80 (4H, м), 3,83 (3H, с), 6,94 (1H, д, J=8,8 Гц), 7,06-7,13 (2H, м), 7,18 (1H, дд, J=8,8, 3,0 Гц), 7,42 (1H, д, J=3,0 Гц), 7,47 (1H, дд, J=8,3, 1,8 Гц), 7,65-7,72 (2H, м), 8,06 (1H, д, J=8,3 Гц), 8,98 (1H, д, J=1,8 Гц), 11,00 (1H, с), 12,33 (1H, с).
4-(Фуран-3-ил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,98-3,09 (4H, м), 3,70-3,81 (4H, м), 6,93 (1H, д, J=8,9 Гц), 6,94-7,00 (1H, м), 7,18 (1H, дд, J=8,9, 2,9 Гц), 7,42 (1H, д, J=2,9 Гц), 7,46 (1H, дд, J=8,3, 1,5 Гц), 7,80-7,85 (1H, м), 8,02 (1H, д, J=8,3 Гц), 8,30 (1H, с), 8,86 (1H, д, J=1,5 Гц), 11,02 (1H, с), 12,28 (1H, с).
4-(Бензо[1,3]диоксазол-5-ил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,99-3,08 (4H, м), 3,71-3,80 (4H, м), 6,11 (2H, с), 6,93 (1H, д, J=9,0 Гц), 7,07 (1H, д, J=8,1 Гц), 7,18 (1H, дд, J=9,0, 3,0 Гц), 7,23 (1H, дд, J=8,1, 1,8 Гц), 7,29 (1H, д, J=1,8 Гц), 7,42 (1H, д, J=3,0 Гц), 7,45 (1H, дд, J=8,3, 1,7 Гц), 8,05 (1H, д, J=8,3 Гц), 8,94 (1H, д, J=1,7 Гц), 10,99 (1H, с), 12,27-12,40 (1H, уширенный).
4-(2,3-Дигидробензо[1,4]диоксин-6-ил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 3,00-3,07 (4H, м), 3,72-3,79 (4H, м), 4,31 (4H, с), 6,93 (1H, д, J=9,0 Гц), 6,98-7,04 (1H, м), 7,18 (1H, дд, J=8,9, 3,0 Гц), 7,18-7,24 (2H, м), 7,42 (1H, д, J=3,0 Гц), 7,45 (1H, дд, J=8,4, 1,8 Гц), 8,04 (1H, д, J=8,4 Гц), 8,94 (1H, д, J=1,8 Гц), 10,97 (1H, с), 12,30 (1H, с).
4-(3,4-Диметоксифенил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,99-3,06 (4H, м), 3,70-3,77 (4H, м), 3,80 (3H, с), 3,84 (3H, с), 6,89 (1H, д, J=9,0 Гц), 7,04-7,12 (1H, м), 7,16 (1H, дд, J=9,0, 2,7 Гц), 7,20-7,26 (2H, м), 7,41 (1H, дд, J=8,3, 1,7 Гц), 7,47 (1H, д, J=2,7 Гц), 8,06 (1H, д, J=8,3 Гц), 8,89 (1H, д, J=1,7 Гц), 11,30-11,90 (1H, уширенный), 13,90-14,45 (1H, уширенный).
4-(3,5-Диметоксифенил)-2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,99-3,07 (4H, м), 3,71-3,79 (4H, м), 3,83 (6H, с), 6,60 (1H, дд, J=2,2, 2,2 Гц), 6,82 (2H, д, J=2,2 Гц), 6,94 (1H, д, J=9,0 Гц), 7,17 (1H, дд, J=9,0, 3,1 Гц), 7,42 (1H, д, J=3,1 Гц), 7,51 (1H, дд, J=8,3, 1,9 Гц), 8,07 (1H, д, J=8,3 Гц), 8,95 (1H, д, J=1,9 Гц), 10,98 (1H, с), 12,28 (1H, с), 13,30-13,80 (1H, уширенный).
Пример 211a
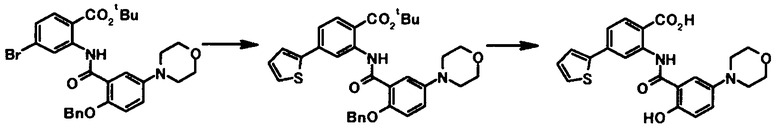
К трет-бутил-2-(2-(бензилокси)-5-(морфолин-4-ил)бензамидо)-4-бромбензоату (0,20 г) добавляли диметиловый эфир этиленгликоля (2,0 мл), воду (0,60 мл), тиофен-2-бороновую кислоту (0,054 г), карбонат натрия (0,093 г) и дихлорид бис(трифенилфосфин)палладия(II) (4,9 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 85-70% гексан/этилацетат] с получением 0,19 г трет-бутил-2-(2-(бензилокси)-5-(морфолин-4-ил)бензамидо)-4-(тиофен-2-ил)бензоата в виде светло-желтого твердого вещества.
К полученному трет-бутил-2-(2-(бензилокси)-5-(морфолин-4-ил)бензамидо)-4-(тиофен-2-ил)бензоату (0,19 г) добавляли тиоанизол (2,0 мл) и трифторуксусную кислоту (6,8 мл), а затем перемешивали при комнатной температуре в течение 24 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат. Твердое вещество собирали путем фильтрования, и добавляли к полученному твердому веществу воду и 2-пропанол. После корректировки значения pH до 6,0 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования с получением 0,11 г 2-(2-гидрокси-5-(морфолин-4-ил)бензамидо)-4-(тиофен-2-ил)бензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,98-3,09 (4H, м), 3,70-3,80 (4H, м), 6,94 (1H, д, J=9,0 Гц), 7,18 (1H, дд, J=9,0, 2,9 Гц), 7,21 (1H, дд, J=5,1, 3,7 Гц), 7,42 (1H, д, J=2,9 Гц), 7,53 (1H, дд, J=8,3, 1,7 Гц), 7,61-7,67 (1H, м), 7,67-7,73 (1H, м), 8,04 (1H, д, J=8,3 Гц), 9,06 (1H, д, J=1,7 Гц), 10,96 (1H, с), 12,36 (1H, с), 13,26-13,80 (1H, уширенный).
Пример 212a
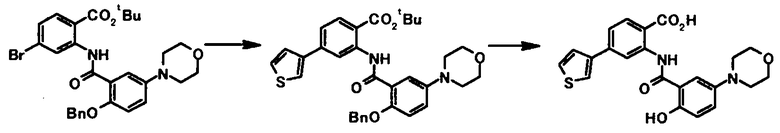
Следующее соединение получали, как описано в Примере 211a.
2-(2-Гидрокси-5-(морфолин-4-ил)бензамидо)-4-(тиофен-3-ил)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,98-3,08 (4H, м), 3,70-3,81 (4H, м), 6,94 (1H, д, J=8,9 Гц), 7,18 (1H, дд, J=8,9, 3,0 Гц), 7,42 (1H, д, J=3,0 Гц), 7,53-7,62 (2H, м), 7,72 (1H, дд, J=5,1, 2,9 Гц), 7,98-8,03 (1H, м), 8,05 (1H, д, J=8,3 Гц), 9,01 (1H, д, J=1,7 Гц), 11,01 (1H, с), 12,27 (1H, с), 13,20-13,80 (1H, уширенный).
Пример 213a
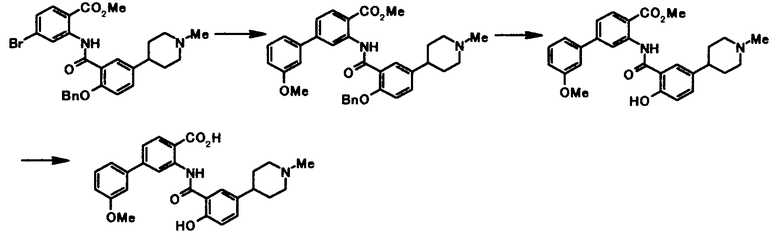
К метил-2-(2-(бензилокси)-5-(1-метилпиперидин-4-ил)бензамидо)-4-бромбензоату (0,090 г) добавляли диметиловый эфир этиленгликоля (0,90 мл), воду (0,27 мл), 3-метоксифенилбороновую кислоту (0,030 г), карбонат натрия (0,044 г) и дихлорид бис(трифенилфосфин)палладия(II) (2,3 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-92% хлороформ/метанол] с получением 0,093 г метил-2-(2-(бензилокси)-5-(1-метилпиперидин-4-ил)бензамидо)-4-(3-метоксифенил)бензоата в виде светло-коричневого твердого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-(1-метилпиперидин-4-ил)бензамидо)-4-(3-метоксифенил)бензоата (0,093 г) в смеси метанола (2,0 мл) и этилацетата (2,0 мл) добавляли 10% палладированый уголь (0,050 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли хлороформ. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-92% хлороформ/метанол] с получением 0,026 г метил-2-(2-гидрокси-5-(1-метилпиперидин-4-ил)бензамидо)-4-(3-метоксифенил)бензоата в виде белого твердого вещества.
К суспензии полученного метил-2-(2-гидрокси-5-(1-метилпиперидин-4-ил)бензамидо)-4-(3-метоксифенил)бензоата (0,026 г) в метаноле (1,0 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (0,27 мл), а затем перемешивали при 50°C в течение 3 часов. После охлаждения реакционной смеси до комнатной температуры и корректировки значения pH до 6,0 добавлением 2,0 моль/л соляной кислоты твердое вещество собирали путем фильтрования с получением 0,025 г 2-(2-гидрокси-5-(1-метилпиперидин-4-ил)бензамидо)-4-(3-метоксифенил)бензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6+D2O) δ: 1,85-2,12 (4H, м), 2,80-2,94 (1H, м), 2,83 (3H, с), 3,04-3,16 (2H, м), 3,47-3,59 (2H, м), 3,84 (3H, с), 6,96 (1H, д, J=8,3 Гц), 7,01 (1H, дд, J=8,3, 2,0 Гц), 7,16-7,22 (1H, м), 7,27 (1H, д, J=8,0 Гц), 7,38-7,50 (3H, м), 7,92 (1H, д, J=2,2 Гц), 8,15 (1H, д, J=8,1 Гц), 8,90 (1H, д, J=1,7 Гц).
Примеры 214a и 215a
Соединения, представленные в Таблице 24a, получали, как описано в Примере 213a.
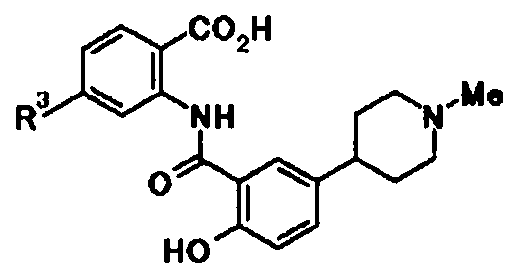
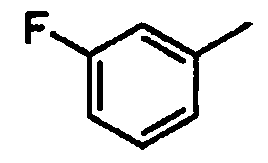
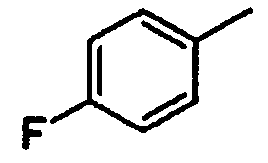
4-(3-Фторфенил)-2-(2-гидрокси-5-(1-метилпиперидин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6+D2O) δ: 1,84-2,12 (4H, м), 2,80-2,94 (1H, м), 2,83 (3H, с), 3,04-3,18 (2H, м), 3,48-3,60 (2H, м), 6,96 (1H, д, J=8,6 Гц), 7,21-7,30 (1H, м), 7,37-7,62 (5H, м), 7,92 (1H, д, J=1,9 Гц), 8,17 (1H, д, J=8,3 Гц), 8,92 (1H, д, J=1,7 Гц).
4-(4-Фторфенил)-2-(2-гидрокси-5-(1-метилпиперидин-4-ил)бензамидо)бензойная кислота
1H-ЯМР (DMSO-d6+D2O) δ: 1,83-2,12 (4H, м), 2,80-2,95 (1H, м), 2,83 (3H, с), 3,02-3,20 (2H, м), 3,46-3,60 (2H, м), 6,96 (1H, д, J=8,6 Гц), 7,31-7,44 (4H, м), 7,70-7,78 (2H, м), 7,93 (1H, д, J=1,9 Гц), 8,15 (1H, д, J=8,3 Гц), 8,89 (1H, д, J=1,9 Гц).
Пример 216a
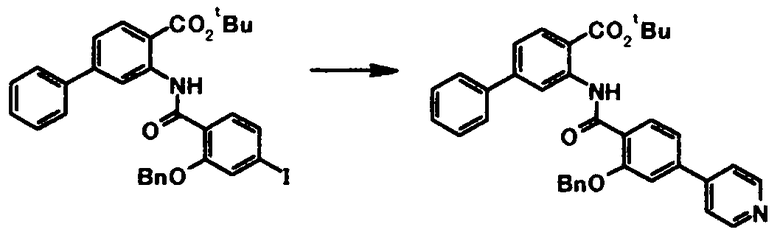
К трет-бутил-2-(2-(бензилокси)-4-йодбензамидо)-4-фенилбензоату (1,2 г) добавляли диметиловый эфир этиленгликоля (12 мл), воду (3,6 мл), 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (0,49 г), карбонат натрия (0,50 г) и дихлорид бис(трифенилфосфин)палладия(II) (14 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней дихлорид бис(трифенилфосфин)палладия(II) (28 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней дихлорид бис(трифенилфосфин)палладия(II) (28 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 80-60% гексан/этилацетат] с получением 0,55 г трет-бутил-2-(2-(бензилокси)-4-(пиридин-4-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,51 (9H, с), 5,66 (2H, с), 7,25-7,37 (3H, м), 7,44-7,49 (1H, м), 7,51-7,59 (6H, м), 7,62-7,66 (1H, м), 7,71-7,78 (4H, м), 8,04-8,11 (2H, м), 8,66-8,73 (2H, м), 9,07-9,12 (1H, м), 12,21 (1H, с).
Пример 217a

К раствору трет-бутил-2-(2-(бензилокси)-5-(пиридин-2-ил)бензамидо)-4-фенилбензоата (0,12 г) в уксусной кислоте (5 мл) добавляли 10% палладированый уголь (0,060 г), а затем перемешивали в атмосфере водорода (5 кг/см2) при 80°C в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней метанол и уксусную кислоту. Нерастворимые вещества удаляли путем фильтрования, и удаляли растворитель в условиях пониженного давления. К остатку добавляли хлороформ и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,062 г трет-бутил-2-(2-гидрокси-5-(пиперидин-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 1,46-1,75 (4H, м), 1,67 (9H, с), 1,81-1,98 (2H, м), 2,77-2,89 (1H, м), 3,14-3,25 (1H, м), 3,64 (1H, дд, J=10,8, 2,1 Гц), 6,97 (1H, д, J=8,4 Гц), 7,36 (1H, дд, J=8,4, 1,7 Гц), 7,38-7,44 (1H, м), 7,44-7,52 (3H, м), 7,66-7,73 (2H, м), 7,91 (1H, д, J=1,7 Гц), 8,08 (1H, д, J=8,3 Гц), 9,05 (1H, д, J=1,7 Гц), 12,55 (1H, с).
К раствору полученного трет-бутил-2-(2-гидрокси-5-(пиперидин-2-ил)бензамидо)-4-фенилбензоата (0,040 г) в хлористом метилене (1,5 мл) последовательно добавляли 37% водный раствор формальдегида (8,2 мкл), уксусную кислоту (9,7 мкл) и триацетоксиборгидрид натрия (0,045 г), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли хлороформ. Нерастворимые вещества удаляли путем фильтрования, а затем добавляли насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-92% хлороформ/метанол] с получением 0,040 г трет-бутил-2-(2-гидрокси-5-(1-метилпиперидин-2-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-5-(1-метилпиперидин-2-ил)бензамидо)-4-фенилбензоату (0,040 г) добавляли трифторуксусную кислоту (2,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку метанол и воду. После корректировки значения pH до 6,0 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,034 г 2-(2-гидрокси-5-(1-метилпиперидин-2-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6+D2O) δ: 1,56-1,73 (1H, м), 1,80-2,12 (5H, м), 2,48 (3H, с), 3,01-3,19 (1H, м), 3,45-3,59 (1H, м), 4,12-4,29 (1H, м), 7,09 (1H, д, J=8,6 Гц), 7,39-7,47 (2H, м), 7,48-7,62 (3H, м), 7,65-7,74 (2H, м), 8,00 (1H, д, J=1,7 Гц), 8,14 (1H, д, J=8,0 Гц), 8,89 (1H, д, J=1,5 Гц).
Пример 218a
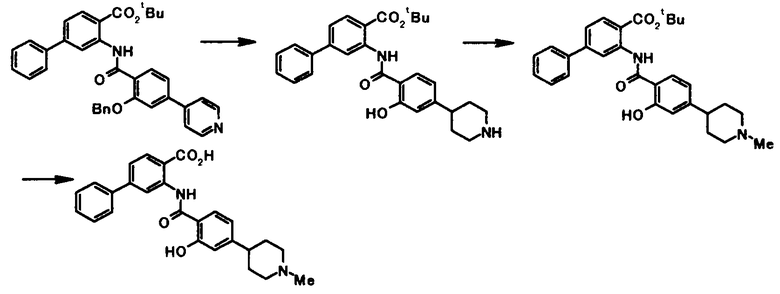
Следующее соединение получали, как описано в Примере 217a.
2-(2-Гидрокси-4-(1-метилпиперидин-4-ил)бензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 1,76-2,08 (4H, м), 2,72-2,84 (1H, м), 2,76 (3H, с), 2,87-3,02 (2H, м), 3,40-3,53 (2H, м), 6,74-6,84 (2H, м), 7,35-7,43 (2H, м), 7,46-7,54 (2H, м), 7,64-7,71 (2H, м), 7,88 (1H, д, J=8,1 Гц), 8,12 (1H, д, J=8,0 Гц), 8,87 (1H, д, J=1,7 Гц).
Пример 219a
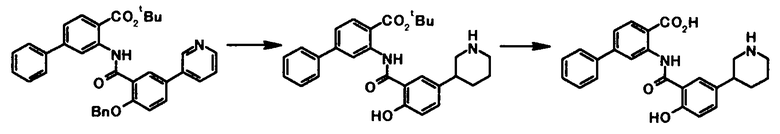
К раствору трет-бутил-2-(2-(бензилокси)-5-(пиридин-3-ил)бензамидо)-4-фенилбензоата (0,88 г) в уксусной кислоте (15 мл) добавляли 10% палладированый уголь (0,44 г), а затем перемешивали в атмосфере водорода (5 кг/см2) при 80°C в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней метанол и уксусную кислоту. Нерастворимые вещества удаляли путем фильтрования. Растворитель удаляли в условиях пониженного давления, и добавляли к остатку хлороформ и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,51 г трет-бутил-2-(2-гидрокси-5-(пиперидин-3-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному трет-бутил-2-(2-гидрокси-5-(пиперидин-3-ил)бензамидо)-4-фенилбензоату (0,10 г) добавляли трифторуксусную кислоту (2,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку метанол и воду. После корректировки значения pH до 6,0 добавлением насыщенного водного раствора бикарбоната натрия, твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,088 г 2-(2-гидрокси-5-(пиперидин-3-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6+D2O) δ: 1,68-2,04 (4H, м), 2,92-3,09 (3H, м), 3,26-3,41 (2H, м), 7,01 (1H, д, J=8,6 Гц), 7,40-7,50 (3H, м), 7,50-7,59 (2H, м), 7,67-7,74 (2H, м), 7,82 (1H, д, J=2,0 Гц), 8,15 (1H, д, J=8,1 Гц), 8,90 (1H, д, J=1,7 Гц).
Пример 220a
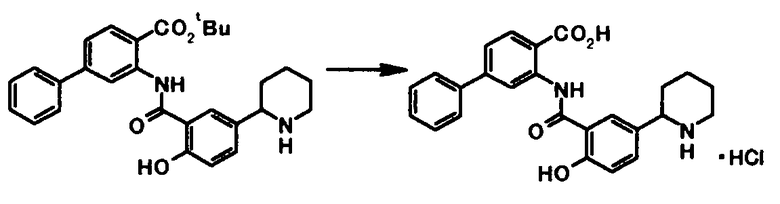
К трет-бутил-2-(2-гидрокси-5-(пиперидин-2-ил)бензамидо)-4-фенилбензоату (0,015 г) добавляли трифторуксусную кислоту (1,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку метанол и воду. После корректировки значения pH до 6,0 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали из реакционной смеси путем фильтрования. К твердому веществу добавляли этилацетат (1,0 мл) и 2,5 моль/л раствор хлорводорода в этилацетате (1,0 мл), а затем перемешивали при комнатной температуре в течение 30 минут. Твердое вещество собирали из реакционной смеси путем фильтрования с получением 0,010 г гидрохлорида 2-(2-гидрокси-5-(пиперидин-2-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6+D2O) δ: 1,56-1,78 (2H, м), 1,79-2,01 (4H, м), 2,98-3,12 (1H, м), 3,27-3,37 (1H, м), 4,20 (1H, дд, J=11,2, 3,2 Гц), 7,10 (1H, д, J=8,5 Гц), 7,44-7,60 (5H, м), 7,70-7,76 (2H, м), 8,09 (1H, д, J=2,4 Гц), 8,12 (1H, д, J=8,3 Гц), 9,03 (1H, д, J=2,0 Гц).
Пример 221a
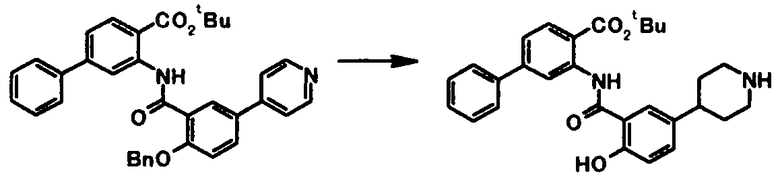
К раствору трет-бутил-2-(2-(бензилокси)-5-(пиридин-4-ил)бензамидо)-4-фенилбензоата (0,77 г) в уксусной кислоте (20 мл) добавляли 10% палладированый уголь (0,35 г), а затем перемешивали в атмосфере водорода (5 кг/см2) при 70-80°C в течение 7 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней уксусную кислоту, метанол и хлороформ. Нерастворимые вещества удаляли путем фильтрования. Растворитель удаляли в условиях пониженного давления, а затем добавляли к остатку хлороформ и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,36 г трет-бутил-2-(2-гидрокси-5-(пиперидин-4-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
1H-ЯМР (CDCl3) δ: 1,59-1,78 (2H, м), 1,67 (9H, с), 1,91-2,03 (2H, м), 2,60-2,74 (1H, м), 2,76-2,88 (2H, м), 3,19-3,32 (2H, м), 6,98 (1H, д, J=8,5 Гц), 7,33 (1H, дд, J=8,5, 2,2 Гц), 7,37 (1H, дд, J=8,4, 1,9 Гц), 7,38-7,53 (3H, м), 7,66-7,77 (3H, м), 8,09 (1H, д, J=8,4 Гц), 9,08 (1H, д, J=1,9 Гц), 12,57 (1H, с).
Пример 222a
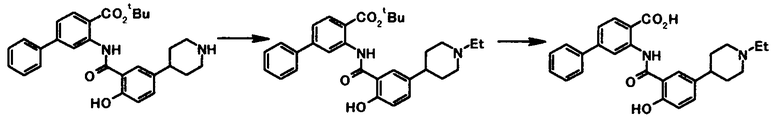
К суспензии трет-бутил-2-(2-гидрокси-5-(пиперидин-4-ил)бензамидо)-4-фенилбензоата (0,10 г) в хлористом метилене (1,0 мл) последовательно добавляли ацетальдегид (0,016 мл), уксусную кислоту (0,024 мл) и триацетоксиборгидрид натрия (0,11 г), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси последовательно добавляли ацетальдегид (0,016 мл) и триацетоксиборгидрид натрия (0,11 г), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат. После удаления нерастворимых веществ путем фильтрования добавляли насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,045 г трет-бутил-2-(5-(1-этилпиперидин-4-ил)-2-гидроксибензамидо)-4-фенилбензоата в виде светло-желтого твердого вещества.
К полученному трет-бутил-2-(5-(1-этилпиперидин-4-ил)-2-гидроксибензамидо)-4-фенилбензоату (0,040 г) добавляли трифторуксусную кислоту (2,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку метанол и воду. После корректировки значения pH до 6,0 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали из реакционной смеси путем фильтрования с получением 5,0 мг 2-(5-(1-этилпиперидин-4-ил)-2-гидроксибензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6+D2O) δ: 1,29 (3H, т, J=7,3 Гц), 1,85-2,15 (4H, м), 2,83-3,10 (3H, м), 3,10-3,23 (2H, м), 3,54-3,66 (2H, м), 6,96 (1H, д, J=8,3 Гц), 7,38-7,48 (3H, м), 7,50-7,57 (2H, м), 7,66-7,74 (2H, м), 7,94 (1H, д, J=1,2 Гц), 8,16 (1H, д, J=8,3 Гц), 8,92 (1H, д, J=1,7 Гц).
Пример 223a
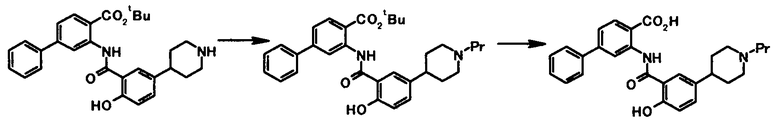
Следующее соединение получали, как описано в Примере 222a.
2-(2-Гидрокси-5-(1-пропилпиперидин-4-ил)бензамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6+D2O) δ: 0,95 (3H, т, J=7,5 Гц), 1,64-1,79 (2H, м), 1,88-2,12 (4H, м), 2,81-3,15 (5H, м), 3,49-3,67 (2H, м), 6,96 (1H, д, J=8,3 Гц), 7,37-7,47 (3H, м), 7,49-7,57 (2H, м), 7,66-7,74 (2H, м), 7,95 (1H, д, J=1,7 Гц), 8,16 (1H, д, J=8,1 Гц), 8,92 (1H, д, J=1,7 Гц).
Пример 224a
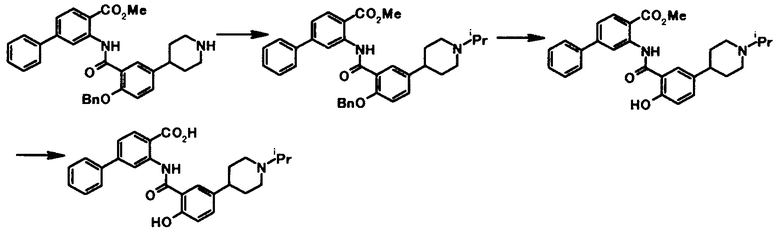
К суспензии метил-2-(2-(бензилокси)-5-(пиперидин-4-ил)бензамидо)-4-фенилбензоата (0,13 г) в ацетонитриле (1,9 мл) последовательно добавляли карбонат калия (0,033 мг) и изопропилйодид (0,024 мл), а затем нагревали с обратным холодильником в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, последовательно добавляли к ней карбонат калия (6,7 мг) и изопропилйодид (4,8 мкл), а затем нагревали с обратным холодильником в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом натрия, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-95% хлороформ/метанол] с получением 0,12 г метил-2-(2-(бензилокси)-5-(1-изопропилпиперидин-4-ил)бензамидо)-4-фенилбензоата в виде оранжевого маслянистого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-(1-изопропилпиперидин-4-ил)бензамидо)-4-фенилбензоата (0,12 г) в смеси этилацетата (1,5 мл) и метанола (1,5 мл) добавляли 10% палладированый уголь (0,12 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 1 часа. К реакционной смеси добавляли хлороформ, и удаляли нерастворимые вещества путем фильтрования. Растворитель выпаривали в условиях пониженного давления с получением 0,086 г метил-2-(2-гидрокси-5-(1-изопропилпиперидин-4-ил)бензамидо)-4-фенилбензоата в виде оранжевого твердого вещества.
К суспензии полученного метил-2-(2-гидрокси-5-(1-изопропилпиперидин-4-ил)бензамидо)-4-фенилбензоата (0,086 г) в 2-пропаноле (1,5 мл) добавляли 2,0 моль/л водный раствор гидроксида натрия (0,27 мл), а затем перемешивали при 50°C в течение 1 часа. К реакционной смеси добавляли 2 моль/л водный раствор гидроксида натрия (0,091 мл), а затем перемешивали при 50°C в течение 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней воду. После корректировки значения pH до 6,0 добавлением 1,0 моль/л соляной кислоты твердое вещество собирали путем фильтрования с получением 0,062 г 2-(2-гидрокси-5-(1-изопропилпиперидин-4-ил)бензамидо)-4-фенилбензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6-D2O) δ: 1,31 (6H, д, J=6,6 Гц), 1,91-2,13 (4H, м), 2,83-2,98 (1H, м), 3,03-3,19 (2H, м), 3,43-3,54 (3H, м), 6,95 (1H, д, J=8,6 Гц), 7,37-7,46 (3H, м), 7,49-7,57 (2H, м), 7,66-7,74 (2H, м), 7,98 (1H, д, J=2,0 Гц), 8,17 (1H, д, J=8,0 Гц), 8,92 (1H, д, J=1,7 Гц).
Пример 225a
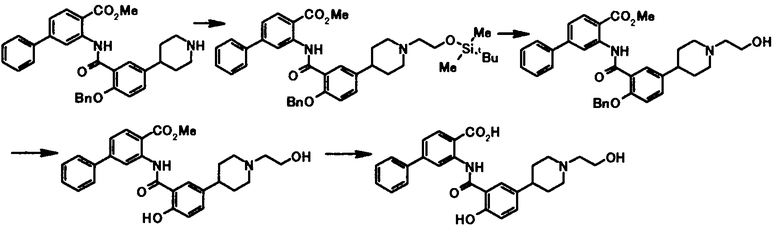
К раствору метил-2-(2-(бензилокси)-5-(пиперидин-4-ил)бензамидо)-4-фенилбензоата (0,11 г) в тетрагидрофуране (1,0 мл) последовательно добавляли уксусную кислоту (0,023 мл), 2-(трет-бутилдиметилсилилокси)ацетальдегид (0,046 мл) и триацетоксиборгидрид натрия (0,11 г), а затем перемешивали при комнатной температуре в течение 13 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат. После удаления нерастворимых веществ путем фильтрования добавляли насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-92% хлороформ/метанол] с получением 0,13 г метил-2-(2-(бензилокси)-5-(1-(2-(трет-бутилдиметилсилилокси)этил)пиперидин-4-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-(1-(2-(трет-бутилдиметилсилилокси)этил)пиперидин-4-ил)бензамидо)-4-фенилбензоата (0,13 г) в тетрагидрофуране (1,3 мл) добавляли 1,0 моль/л раствор фторида тетрабутиламмония в тетрагидрофуране (0,38 мл), а затем перемешивали при комнатной температуре в течение 4 часов. При охлаждении на льду к реакционной смеси добавляли воду и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия, сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-92% хлороформ/метанол] с получением 0,085 г метил-2-(2-(бензилокси)-5-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К раствору полученного метил-2-(2-(бензилокси)-5-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамидо)-4-фенилбензоата (0,085 г) в смеси этилацетата (1,0 мл) и метанола (1,0 мл) добавляли 10% палладированый уголь (0,040 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 2 часов. К реакционной смеси добавляли 10% палладированый уголь (0,040 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 4 часов. Нерастворимые вещества удаляли из реакционной смеси путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-92% хлороформ/метанол] с получением 0,035 г метил-2-(2-гидрокси-5-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамидо)-4-фенилбензоата в виде белого твердого вещества.
К полученному метил-2-(2-гидрокси-5-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамидо)-4-фенилбензоату (0,035 г) добавляли метанол (1,0 мл) и 2,0 моль/л водный раствор гидроксида натрия (0,37 мл), а затем перемешивали при 50°C в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры и корректировки значения pH до 6,0 добавлением 2,0 моль/л соляной кислоты твердое вещество собирали путем фильтрования с получением 0,030 г 2-(2-гидрокси-5-(1-(2-гидроксиэтил)пиперидин-4-ил)бензамидо)-4-фенилбензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6+D2O) δ: 1,92-2,13 (4H, м), 2,86-3,00 (1H, м), 3,05-3,27 (4H, м), 3,58-3,73 (2H, м), 3,77-3,87 (2H, м), 6,98 (1H, д, J=8,6 Гц), 7,40-7,49 (3H, м), 7,50-7,58 (2H, м), 7,67-7,75 (2H, м), 7,90 (1H, д, J=1,7 Гц), 8,16 (1H, д, J=8,0 Гц), 8,92 (1H, д, J=1,5 Гц).
Пример 1b
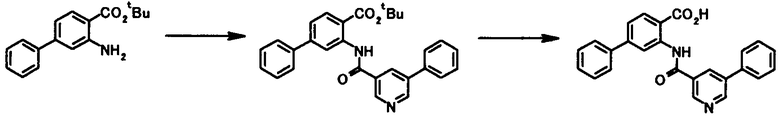
К суспензии 5-фенилпиридин-3-карбоновой кислоты (44 мг) в хлористом метилене (0,5 мл) при комнатной температуре добавляли N,N-диметилформамид (0,9 мкл) и оксалилхлорид (0,023 мл), а затем перемешивали при той же температуре в течение 1 часа. Реакционную смесь при комнатной температуре добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (40 мг) в смеси хлористого метилена (1 мл) и триэтиламина (0,17 мл), а затем перемешивали при той же температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Trikonex AB, FlashTube 2008, элюент: гексан/этилацетат = 2/1] с получением трет-бутил-4-фенил-2-(5-фенилпиридин-3-карбоксамидо)бензоата.
К полученному трет-бутил-4-фенил-2-(5-фенилпиридин-3-карбоксамидо)бензоату добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этилацетат. Твердое вещество собирали путем фильтрования с получением 40 мг 4-фенил-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,45-7,61 (7H, м), 7,72-7,78 (2H, м), 7,81-7,87 (2H, м), 8,15 (1H, д, J=8,3 Гц), 8,56 (1H, дд, J=2,2, 2,2 Гц), 9,02 (1H, д, J=1,7 Гц), 9,14 (1H, д, J=2,0 Гц), 9,15 (1H, д, J=2,0 Гц), 12,33 (1H, с).
Пример 2b
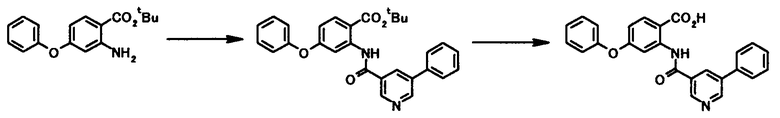
Следующее соединение получали, как описано в Примере 1b.
4-Фенокси-2-(5-фенилпиридин-3-карбоксамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 6,83 (1H, дд, J=8,8, 2,5 Гц), 7,17-7,22 (2H, м), 7,27-7,33 (1H, м), 7,46-7,59 (5H, м), 7,79-7,85 (2H, м), 8,09 (1H, д, J=8,8 Гц), 8,36 (1H, д, J=2,5 Гц), 8,49 (1H, дд, J=2,2, 2,1 Гц), 9,07 (1H, д, J=2,1 Гц), 9,13 (1H, д, J=2,2 Гц), 12,54 (1H, с).
Пример 3b
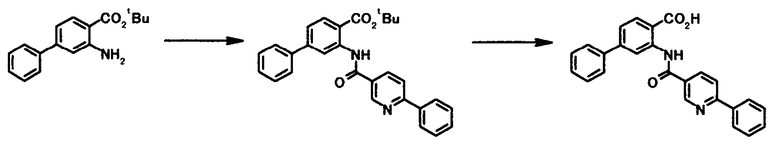
К суспензии 6-фенилпиридин-3-карбоновой кислоты (44 мг) в хлористом метилене (0,5 мл) при комнатной температуре добавляли N,N-диметилформамид (0,9 мкл) и оксалилхлорид (0,023 мл), а затем перемешивали при той же температуре в течение 1 часа. Реакционную смесь при комнатной температуре добавляли к раствору трет-бутил-2-амино-4-фенилбензоата (40 мг) в смеси хлористого метилена (1 мл) и триэтиламина (0,17 мл), а затем перемешивали при той же температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Trikonex AB, FlashTube 2008, элюент: гексан/этилацетат = 2/1] с получением трет-бутил-4-фенил-2-(6-фенилпиридин-3-карбоксамидо)бензоата.
К полученному трет-бутил-4-фенил-2-(6-фенилпиридин-3-карбоксамидо)бензоату добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку метанол. Твердое вещество собирали путем фильтрования с получением 53 мг 4-фенил-2-(6-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,44-7,60 (7H, м), 7,72-7,79 (2H, м), 8,16 (1H, д, J=8,3 Гц), 8,18-8,26 (3H, м), 8,39 (1H, дд, J=8,3, 2,4 Гц), 9,02-9,06 (1H, м), 9,24 (1H, д, J=1,7 Гц), 12,30 (1H, с).
Примеры 4b и 5b
Соединения, представленные в Таблице 7b, получали, как описано в Примере 3b.
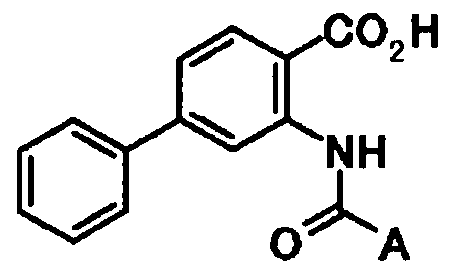
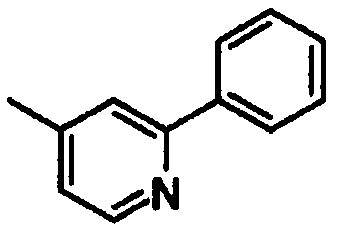
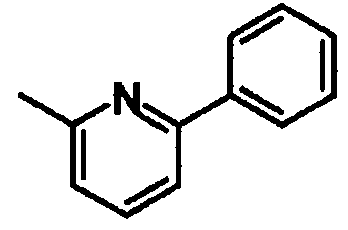
4-Фенил-2-(2-фенилпиридин-4-карбоксамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 7,45-7,62 (7H, м), 7,72-7,78 (2H, м), 7,84 (1H, дд, J=4,9, 1,6 Гц), 8,13-8,20 (3H, м), 8,41 (1H, с), 8,94 (1H, д, J=4,9 Гц), 9,02 (1H, д, J=1,7 Гц), 12,39 (1H, с).
4-Фенил-2-(6-фенилпиридин-2-карбоксамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 7,45-7,61 (7H, м), 7,73-7,80 (2H, м), 8,16-8,22 (3H, м), 8,29-8,36 (1H, м), 8,43-8,50 (2H, м), 9,28 (1H, д, J=1,7 Гц), 13,33 (1H, с), 13,60-13,80 (1H, уширенный).
Пример 6b
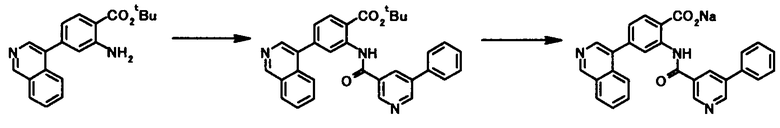
К суспензии 5-фенилпиридин-3-карбоновой кислоты (60 мг) в хлористом метилене (2 мл) при комнатной температуре добавляли N,N-диметилформамид (2,3 мкл) и оксалилхлорид (0,039 мл), а затем перемешивали при той же температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1,5 мл). Реакционную смесь при комнатной температуре добавляли к раствору трет-бутил-2-амино-4-(изохинолин-4-ил)бензоата (80 мг) в смеси хлористого метилена (2 мл) и пиридина (0,050 мл), а затем перемешивали при той же температуре в течение 1 часа. К реакционной смеси добавляли насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-50% гексан/этилацетат] с получением 0,10 г трет-бутил-4-(изохинолин-4-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде белого твердого вещества.
К полученному трет-бутил-4-(изохинолин-4-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату (0,10 г) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и воду. После корректировки значения pH до 6,5 добавлением 2 моль/л водного раствора гидроксида натрия твердое вещество собирали путем фильтрования с получением 81 мг 4-(изохинолин-4-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде светло-желтого твердого вещества.
К полученной 4-(изохинолин-4-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоте (81 мг) добавляли метанол (5 мл), диоксан (5 мл) и 2 моль/л водный раствор гидроксида натрия (0,091 мл), и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 83 мг 4-(изохинолин-4-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,21 (1H, дд, J=7,9, 1,8 Гц), 7,46-7,53 (1H, м), 7,54-7,61 (2H, м), 7,73-7,79 (1H, м), 7,80-7,87 (3H, м), 7,96-8,01 (1H, м), 8,20-8,28 (2H, м), 8,49 (1H, с), 8,60 (1H, дд, J=2,2, 2,2 Гц), 8,88 (1H, д, J=1,8 Гц), 9,09 (1H, д, J=2,2 Гц), 9,17 (1H, д, J=2,0 Гц), 9,37 (1H, с).
Пример 7b
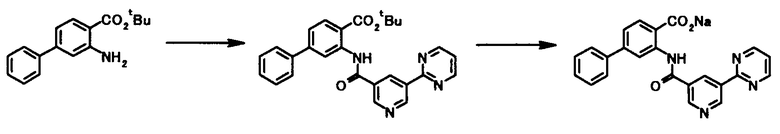
Следующее соединение получали, как описано в Примере 6b.
4-Фенил-2-(5-(пиримидин-2-ил)пиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 7,33 (1H, дд, J=8,1, 1,9 Гц), 7,37-7,43 (1H, м), 7,47-7,54 (2H, м), 7,60 (1H, т, J=4,9 Гц), 7,66-7,72 (2H, м), 8,12 (1H, д, J=8,1 Гц), 9,01-9,06 (3H, м), 9,28 (1H, дд, J=2,1, 2,0 Гц), 9,35 (1H, д, J=2,1 Гц), 9,67 (1H, д, J=2,0 Гц).
Пример 8b
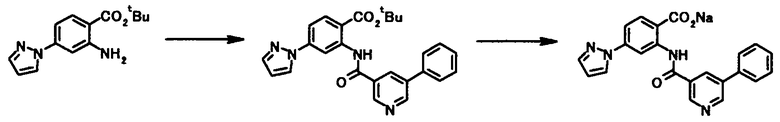
К суспензии 5-фенилпиридин-3-карбоновой кислоты (57 мг) в хлористом метилене (1,2 мл) при комнатной температуре добавляли N,N-диметилформамид (2,2 мкл) и оксалилхлорид (0,037 мл), а затем перемешивали при той же температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (1,2 мл). Реакционную смесь при комнатной температуре добавляли к раствору трет-бутил-2-амино-4-(1H-пиразол-1-ил)бензоата (62 мг) в смеси хлористого метилена (1,2 мл) и пиридина (0,048 мл), а затем перемешивали при той же температуре в течение 2 часов. К реакционной смеси добавляли хлористый метилен и 1 моль/л водный раствор гидроксида натрия. Органический слой разделяли, последовательно промывали 1 моль/л водным раствором гидроксида натрия и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-70% гексан/этилацетат] с получением 68 мг трет-бутил-2-(5-фенилпиридин-3-карбоксамидо)-4-(1H-пиразол-1-ил)бензоата в виде белого твердого вещества.
К полученному трет-бутил-2-(5-фенилпиридин-3-карбоксамидо)-4-(1H-пиразол-1-ил)бензоату (68 мг) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку метанол. Твердое вещество собирали путем фильтрования с получением 53 мг 2-(5-фенилпиридин-3-карбоксамидо)-4-(1H-пиразол-1-ил)бензойной кислоты.
К полученной 2-(5-фенилпиридин-3-карбоксамидо)-4-(1H-пиразол-1-ил)бензойной кислоте (53 мг) добавляли метанол (2 мл), диоксан (2 мл) и 2 моль/л водный раствор гидроксида натрия (0,083 мл), и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли воду и ацетон, и собирали твердое вещество путем фильтрования с получением 23 мг 2-(5-фенилпиридин-3-карбоксамидо)-4-(1H-пиразол-1-ил)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,56 (1H, дд, J=1,9, 1,9 Гц), 7,44-7,54 (2H, м), 7,55-7,62 (2H, м), 7,77 (1H, д, J=1,5 Гц), 7,81-7,87 (2H, м), 8,12 (1H, д, J=8,3 Гц), 8,45 (1H, д, J=2,4 Гц), 8,59-8,64 (1H, м), 9,10 (1H, д, J=2,2 Гц), 9,17-9,22 (2H, м).
Пример 9b
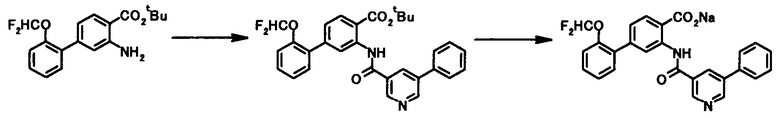
Следующее соединение получали, как описано в Примере 8b.
4-(2-Дифторметокси)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 6,96-7,42 (4H, м), 7,45-7,53 (3H, м), 7,53-7,61 (2H, м), 7,80-7,87 (2H, м), 8,11 (1H, д, J=7,8 Гц), 8,59 (1H, с), 8,82 (1H, с), 9,10 (1H, с), 9,17 (1H, с).
Пример 10b
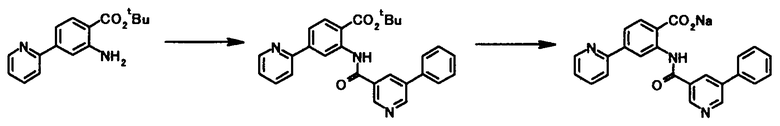
При охлаждении на льду к суспензии 5-фенилпиридин-3-карбоновой кислоты (0,11 г) в тетрагидрофуране (3,0 мл) добавляли N,N-диметилформамид (0,010 мл) и оксалилхлорид (0,059 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку тетрагидрофуран (5,5 мл). При охлаждении на льду реакционную смесь добавляли к раствору трет-бутил-2-амино-4-(пиридин-2-ил)бензоата (0,12 г) в смеси тетрагидрофурана (2,0 мл) и пиридина (0,073 мл), а затем перемешивали при комнатной температуре в течение 4 часов 30 минут. К реакционной смеси добавляли 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 80-55% гексан/этилацетат] с получением твердого вещества. К полученному твердому веществу добавляли этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,13 г трет-бутил-2-(5-фенилпиридин-3-карбоксамидо)-4-(пиридин-2-ил)бензоата в виде светло-желтого твердого вещества.
К полученному трет-бутил-2-(5-фенилпиридин-3-карбоксамидо)-4-(пиридин-2-ил)бензоату (0,13 г) добавляли трифторуксусную кислоту (4,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли диоксан (3,0 мл) и 2 моль/л водный раствор гидроксида натрия (0,19 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 10% водный раствор лимонной кислоты и этилацетат, и собирали твердое вещество путем фильтрования с получением 74 мг 2-(5-фенилпиридин-3-карбоксамидо)-4-(пиридин-2-ил)бензойной кислоты в виде белого твердого вещества.
К полученной 2-(5-фенилпиридин-3-карбоксамидо)-4-(пиридин-2-ил)бензойной кислоте (74 мг) последовательно добавляли этанол (2,0 мл) и 2 моль/л водный раствор гидроксида натрия (0,094 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Твердое вещество собирали путем фильтрования с получением 59 мг 2-(5-фенилпиридин-3-карбоксамидо)-4-(пиридин-2-ил)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,36-7,42 (1H, м), 7,47-7,54 (1H, м), 7,55-7,62 (2H, м), 7,74 (1H, дд, J=8,2, 1,7 Гц), 7,82-7,88 (2H, м), 7,89-7,97 (2H, м), 8,16 (1H, д, J=8,2 Гц), 8,63 (1H, дд, J=2,1, 2,0 Гц), 8,72 (1H, д, J=4,6 Гц), 9,11 (1H, д, J=2,1 Гц), 9,21 (1H, д, J=2,0 Гц), 9,45 (1H, д, J=1,7 Гц).
Пример 11b
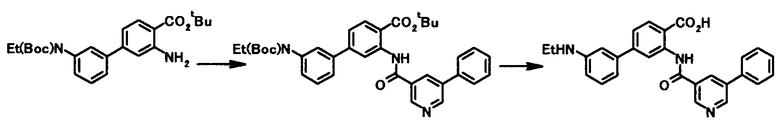
К суспензии 5-фенилпиридин-3-карбоновой кислоты (73 мг) в хлористом метилене (2 мл) при комнатной температуре добавляли N,N-диметилформамид (3 мкл) и оксалилхлорид (0,047 мл), а затем перемешивали при той же температуре в течение 40 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Реакционную смесь при комнатной температуре добавляли к раствору трет-бутил-2-амино-4-(3-((трет-бутоксикарбонил)(этил)амино)фенил)бензоата (0,13 г) в смеси хлористого метилена (2 мл) и пиридина (0,062 мл), а затем перемешивали при той же температуре в течение 20 минут. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [элюент: 90-60% гексан/этилацетат] с получением 0,15 г трет-бутил-4-(3-((трет-бутоксикарбонил)(этил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде белого твердого вещества.
К раствору полученного трет-бутил-4-(3-((трет-бутоксикарбонил)(этил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,15 г) в хлористом метилене (2,0 мл) при комнатной температуре добавляли трифторуксусную кислоту (2,0 мл), а затем перемешивали при той же температуре в течение 7 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку метанол (3 мл) и диоксан (1 мл). Значение pH корректировали до 13,0 добавлением 2 моль/л водного раствора гидроксида натрия, а затем до pH 4,6 добавлением 10% водного раствора лимонной кислоты. Твердое вещество собирали путем фильтрования с получением 0,10 г 4-(3-(этиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,21 (3H, т, J=7,1 Гц), 3,11 (2H, кв, J=7,1 Гц), 6,61-6,69 (1H, м), 6,84-6,93 (2H, м), 7,23 (1H, дд, J=7,8, 7,8 Гц), 7,45-7,62 (4H, м), 7,80-7,88 (2H, м), 8,12 (1H, д, J=8,3 Гц), 8,55 (1H, дд, J=2,1, 2,1 Гц), 8,98 (1H, д, J=1,7 Гц), 9,11-9,18 (2H, м), 12,37 (1H, с).
Примеры 12b и 13b
Соединения, представленные в Таблице 8b, получали, как описано в Примере 11b.
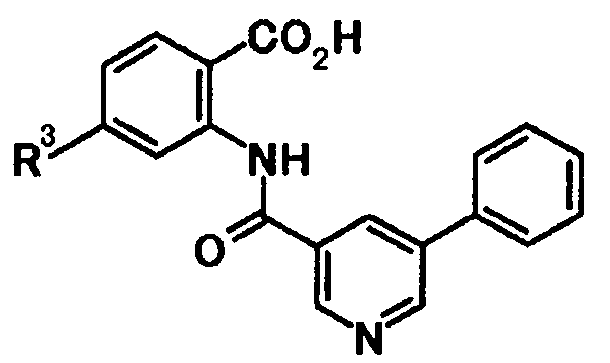
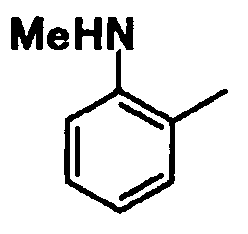
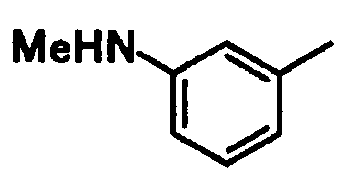
4-(2-(Метиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,70 (3H, с), 6,64-6,75 (2H, м), 7,02-7,09 (1H, м), 7,22-7,32 (2H, м), 7,46-7,53 (1H, м), 7,54-7,61 (2H, м), 7,80-7,87 (2H, м), 8,12 (1H, д, J=8,0 Гц), 8,50-8,55 (1H, м), 8,74 (1H, д, J=1,4 Гц), 9,11 (1H, д, J=2,2 Гц), 9,14 (1H, д, J=2,2 Гц), 12,38 (1H, с).
4-(3-(Метиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,75 (3H, с), 6,63 (1H, дд, J=8,2, 1,8 Гц), 6,85-6,92 (2H, м), 7,25 (1H, дд, J=7,8, 7,8 Гц), 7,46-7,54 (2H, м), 7,54-7,61 (2H, м), 7,81-7,87 (2H, м), 8,12 (1H, д, J=8,2 Гц), 8,56 (1H, дд, J=2,1, 2,1 Гц), 8,98 (1H, д, J=1,8 Гц), 9,14 (1H, д, J=2,1 Гц), 9,15 (1H, д, J=2,1 Гц), 12,36 (1H, с).
Пример 14b
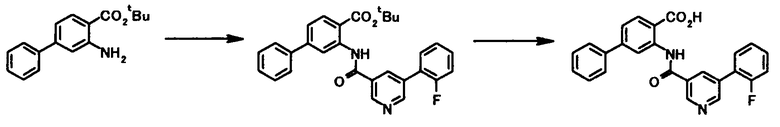
Следующее соединение получали, как описано в Примере 11b.
2-(5-(2-Фторфенил)пиридин-3-карбоксамидо)-4-фенилбензойная кислота
1H-ЯМР (DMSO-d6) δ: 7,38-7,51 (3H, м), 7,52-7,60 (4H, м), 7,70-7,78 (3H, м), 8,15 (1H, д, J=8,3 Гц), 8,47-8,52 (1H, м), 9,00-9,05 (2H, м), 9,18 (1H, д, J=2,2 Гц), 12,37 (1H, с).
Пример 15b
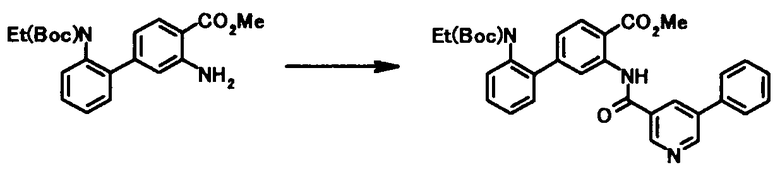
При охлаждении на льду к раствору 5-фенилпиридин-3-карбоновой кислоты (0,48 г) в смеси тетрагидрофурана (4,8 мл) и N,N-диметилформамида (0,010 мл) добавляли оксалилхлорид (0,23 мл), а затем перемешивали при комнатной температуре в течение 40 минут. Реакционную смесь при охлаждении на льду добавляли к раствору метил-2-амино-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)бензоата (0,80 г) в смеси тетрагидрофурана (8,0 мл) и пиридина (0,44 мл), а затем перемешивали при комнатной температуре в течение 1 часа 10 минут. К реакционной смеси добавляли этилацетат и воду. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 85-70% гексан/этилацетат] с получением 0,86 г метил-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде белого твердого вещества.
1H-ЯМР (CD3OD) δ: 1,02-1,16 (3H, м), 1,18-1,46 (9H, м), 2,83-3,02 (1H, м), 3,52-3,84 (1H, м), 4,00 (3H, с), 7,18-7,35 (2H, м), 7,39-7,59 (6H, м), 7,72-7,78 (2H, м), 8,09-8,20 (1H, м), 8,56-8,61 (1H, м), 8,77-8,90 (1H, м), 9,02 (1H, д, J=2,2 Гц), 9,12 (1H, д, J=2,2 Гц).
Пример 16b
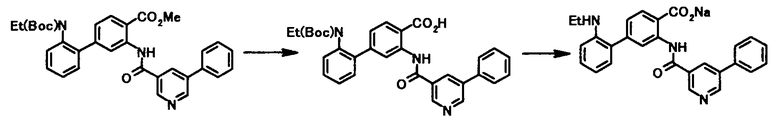
К раствору метил-4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,84 г) в смеси метанола (4,2 мл) и диоксана (4,2 мл) при комнатной температуре добавляли 2 моль/л водный раствор гидроксида натрия (3,8 мл), а затем перемешивали при той же температуре в течение 3 часов 10 минут. После корректировки значения pH до 4,9 добавлением 10% водного раствора лимонной кислоты добавляли хлороформ. Органический слой разделяли, последовательно промывали водой и насыщенным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 0,80 г 4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
К полученной 4-(2-((трет-бутоксикарбонил)(этил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоте (0,79 г) добавляли трифторуксусную кислоту (7,9 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку 30% водный раствор этанола. После корректировки значения pH до 5,0 добавлением 4,0 моль/л водного раствора гидроксида натрия твердое вещество собирали путем фильтрования с получением 0,61 г 4-(2-(этиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде желтого твердого вещества.
К полученной 4-(2-(этиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоте (0,60 г) последовательно добавляли этанол (18 мл) и 1,0 моль/л водный раствор гидроксида натрия (1,3 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку 10% водный раствор этанола. Твердое вещество собирали путем фильтрования с получением 0,57 г 4-(2-(этиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,12 (3H, т, J=7,1 Гц), 3,03-3,17 (2H, м), 4,41-4,52 (1H, м), 6,65-6,73 (2H, м), 7,00-7,08 (2H, м), 7,14-7,23 (1H, м), 7,45-7,62 (3H, м), 7,78-7,87 (2H, м), 8,11 (1H, д, J=7,8 Гц), 8,56-8,62 (1H, м), 8,68-8,73 (1H, м), 9,06-9,11 (1H, м), 9,14-9,19 (1H, м).
Пример 17b
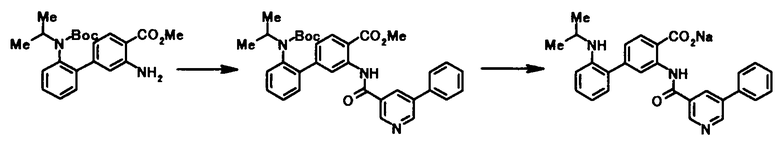
К раствору 5-фенилпиридин-3-карбоновой кислоты (26 мг) в смеси хлористого метилена (1,5 мл) и N,N-диметилформамида (0,010 мл) при комнатной температуре добавляли оксалилхлорид (0,014 мл), а затем перемешивали при той же температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2,0 мл). Реакционную смесь при комнатной температуре добавляли к раствору метил-2-амино-4-(2-((трет-бутоксикарбонил)(изопропил)амино)фенил)бензоата (42 мг) в смеси хлористого метилена (1,0 мл) и пиридина (0,013 мл), а затем перемешивали при той же температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 80-70% гексан/этилацетат] с получением метил-4-(2-((трет-бутоксикарбонил)(изопропил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата.
К полученному метил-4-(2-((трет-бутоксикарбонил)(изопропил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату добавляли трифторуксусную кислоту (3,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и к полученному остатку последовательно добавляли диоксан (3,0 мл) и 1 моль/л водный раствор гидроксида натрия (0,33 мл), затем перемешивали при комнатной температуре в течение 30 минут, а затем при 50°C в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 1 моль/л водный раствор гидроксида натрия (0,33 мл), а затем перемешивали при 50°C в течение 40 минут. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления. К полученному остатку добавляли воду, и собирали твердое вещество путем фильтрования с получением 24 мг 4-(2-(изопропиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,12 (6H, д, J=6,3 Гц), 3,59-3,70 (1H, м), 4,13 (1H, д, J=8,5 Гц), 6,68 (1H, дд, J=7,3, 7,3 Гц), 6,74 (1H, д, J=8,0 Гц), 7,00-7,08 (2H, м), 7,19 (1H, дд, J=7,6, 7,6 Гц), 7,50 (1H, дд, J=7,3, 7,3 Гц), 7,54-7,62 (2H, м), 7,80-7,87 (2H, м), 8,11 (1H, д, J=8,0 Гц), 8,59 (1H, с), 8,68-8,74 (1H, м), 9,09 (1H, д, J=1,9 Гц), 9,17 (1H, д, J=1,7 Гц).
Пример 18b
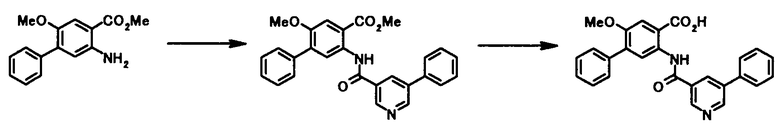
К раствору 5-фенилпиридин-3-карбоновой кислоты (84 мг) в смеси хлористого метилена (2 мл) и N,N-диметилформамида (3,2 мкл) при комнатной температуре добавляли оксалилхлорид (0,054 мл), а затем перемешивали при той же температуре в течение 1 часа 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2 мл). Реакционную смесь при комнатной температуре добавляли к раствору метил-2-амино-5-метокси-4-фенил)бензоата (90 мг) в смеси хлористого метилена (2 мл) и пиридина (0,071 мл), а затем перемешивали при той же температуре в течение 50 минут. Растворитель выпаривали в условиях пониженного давления, и очищали полученный остаток по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 75-30% гексан/этилацетат] с получением 0,12 г метил-5-метокси-4-фенил-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде коричневого твердого вещества.
К суспензии полученного метил-5-метокси-4-фенил-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,11 г) в метаноле (2,2 мл) при комнатной температуре добавляли 2 моль/л водный раствор гидроксида натрия (1,3 мл), а затем перемешивали при той же температуре в течение 30 минут. К реакционной смеси добавляли хлороформ (3 мл) и метанол (2 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этанол и воду. После корректировки значения pH до 1 добавлением 6 моль/л соляной кислоты твердое вещество собирали путем фильтрования с получением 88 мг 5-метокси-4-фенил-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 3,83 (3H, с), 7,38-7,62 (8H, м), 7,67 (1H, с), 7,80-7,89 (2H, м), 8,49-8,55 (1H, м), 8,58 (1H, с), 9,10 (1H, д, J=2,0 Гц), 9,13 (1H, д, J=2,2 Гц), 11,96 (1H, с).
Пример 19b
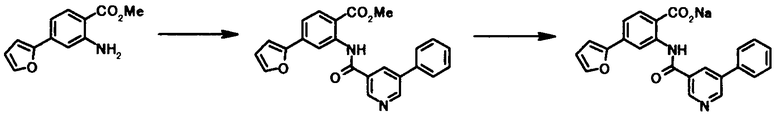
К раствору 5-фенилпиридин-3-карбоновой кислоты (86 мг) в смеси хлористого метилена (1,5 мл) и N,N-диметилформамида (0,010 мл) при комнатной температуре добавляли оксалилхлорид (0,047 мл), а затем перемешивали при той же температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2,0 мл). Реакционную смесь при комнатной температуре добавляли к раствору метил-2-амино-4-(фуран-2-ил)бензоата (78 мг) в смеси хлористого метилена (1,5 мл) и пиридина (0,044 мл), а затем перемешивали при той же температуре в течение 1 часа 20 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 80-20% гексан/этилацетат] с получением 76 мг метил-4-(фуран-2-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде светло-желтого твердого вещества.
К суспензии полученного метил-4-(фуран-2-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата (76 мг) в диоксане (3,0 мл) при комнатной температуре добавляли 2 моль/л водный раствор гидроксида натрия (0,19 мл), а затем перемешивали при той же температуре в течение 3 часов 20 минут. К реакционной смеси при комнатной температуре добавляли 2 моль/л водный раствор гидроксида натрия (0,19 мл), а затем перемешивали при 50-55°C в течение 4 часов. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления. К полученному остатку добавляли 1 моль/л соляную кислоту (1,5 мл). Твердое вещество собирали путем фильтрования с получением 69 мг 4-(фуран-2-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
К полученной 4-(фуран-2-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоте (69 мг) добавляли этанол (4,5 мл) и 2 моль/л водный раствор гидроксида натрия (0,085 мл), а затем перемешивали при комнатной температуре в течение 1 часа 20 минут. Твердое вещество собирали путем фильтрования с получением 31 мг 4-(фуран-2-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,63 (1H, дд, J=3,3, 1,7 Гц), 6,94 (1H, д, J=3,3 Гц), 7,39 (1H, дд, J=8,1, 1,7 Гц), 7,50 (1H, дд, J=7,3, 7,3 Гц), 7,54-7,62 (2H, м), 7,78-7,87 (3H, м), 8,08 (1H, д, J=8,1 Гц), 8,61 (1H, дд, J=2,1, 2,1 Гц), 9,06 (1H, д, J=1,5 Гц), 9,10 (1H, д, J=2,0 Гц), 9,18 (1H, д, J=1,7 Гц).
Пример 20b
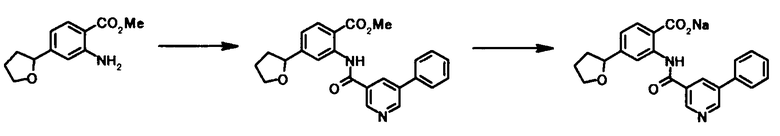
Следующее соединение получали, как описано в Примере 19b.
2-(5-Фенилпиридин-3-карбоксамидо)-4-(тетрагидрофуран-2-ил)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 1,64-1,75 (1H, м), 1,91-2,01 (2H, м), 2,27-2,38 (1H, м), 3,83 (1H, ддд, J=7,4, 7,4, 7,4 Гц), 4,01 (1H, ддд, J=7,1, 7,1, 7,1 Гц), 4,82 (1H, дд, J=7,2, 7,2 Гц), 6,97 (1H, д, J=8,1 Гц), 7,50 (1H, дд, J=7,2, 7,2 Гц), 7,54-7,61 (2H, м), 7,80-7,86 (2H, м), 8,00 (1H, д, J=7,8 Гц), 8,57-8,62 (1H, м), 8,67 (1H, с), 9,07-9,11 (1H, м), 9,15-9,19 (1H, м).
Пример 21b
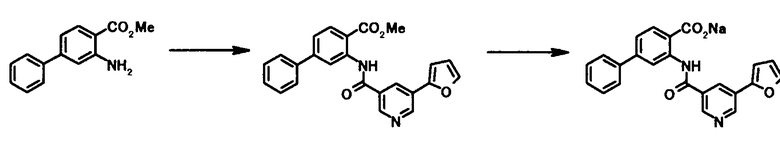
Следующее соединение получали, как описано в Примере 19b.
2-(5-(Фуран-2-ил)пиридин-3-карбоксамидо)-4-фенилбензоат натрия
1H-ЯМР (DMSO-d6) δ: 6,71 (1H, дд, J=3,4, 1,7 Гц), 7,25 (1H, д, J=3,4 Гц), 7,34 (1H, дд, J=8,1, 2,0 Гц), 7,40 (1H, дд, J=7,3, 7,3 Гц), 7,47-7,54 (2H, м), 7,66-7,72 (2H, м), 7,92 (1H, д, J=1,7 Гц), 8,12 (1H, д, J=8,1 Гц), 8,61 (1H, дд, J=2,0, 2,0 Гц), 9,02 (1H, д, J=2,0 Гц), 9,11 (1H, д, J=2,0 Гц), 9,14 (1H, д, J=2,0 Гц).
Пример 22b
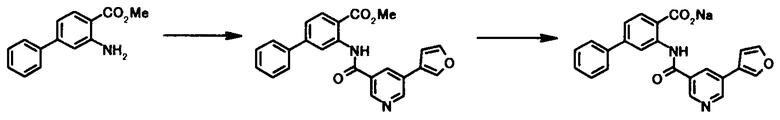
Следующее соединение получали, как описано в Примере 19b.
2-(5-(Фуран-3-ил)пиридин-3-карбоксамидо)-4-фенилбензоат натрия
1H-ЯМР (DMSO-d6) δ: 7,14 (1H, с), 7,31-7,37 (1H, м), 7,40 (1H, дд, J=7,1, 7,1 Гц), 7,47-7,55 (2H, м), 7,65-7,73 (2H, м), 7,87 (1H, д, J=1,5 Гц), 8,13 (1H, д, J=8,0 Гц), 8,42 (1H, с), 8,55 (1H, д, J=2,0 Гц), 9,01-9,05 (1H, м), 9,06-9,12 (2H, м).
Пример 23b
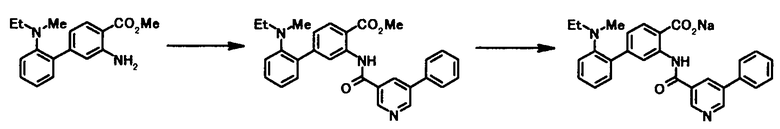
К раствору 5-фенилпиридин-3-карбоновой кислоты (83 мг) в смеси хлористого метилена (3,0 мл) и N,N-диметилформамида (0,010 мл) при комнатной температуре добавляли оксалилхлорид (0,046 мл), а затем перемешивали при той же температуре в течение 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлористый метилен (2,5 мл). Реакционную смесь при охлаждении на льду добавляли к раствору метил-2-амино-4-(2-((этил)(метил)амино)фенил)бензоата (99 мг) в смеси хлористого метилена (1,5 мл) и пиридина (0,042 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к остатку этилацетат и насыщенный водный раствор бикарбоната натрия. Органический слой разделяли, последовательно промывали 10% водным раствором лимонной кислоты и насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 0,10 г метил-4-(2-((этил)(метил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде желтого твердого вещества.
К раствору полученного метил-4-(2-((этил)(метил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в диоксане (3,0 мл) при комнатной температуре добавляли 1 моль/л водный раствор гидроксида натрия (0,67 мл), затем перемешивали при той же температуре в течение 1 часа, а затем при 55°C в течение 1 часа 30 минут. После охлаждения реакционной смеси до комнатной температуры и корректировки значения pH до 7,3 добавлением 1 моль/л соляной кислоты растворитель выпаривали в условиях пониженного давления. К полученному остатку добавляли воду, и собирали твердое вещество путем фильтрования. К полученному твердому веществу последовательно добавляли этанол (1,5 мл) и 1 моль/л водный раствор гидроксида натрия (0,091 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Затем, растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. Твердое вещество собирали путем фильтрования с получением 2,5 мг 4-(2-((этил)(метил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 0,86 (3H, т, J=7,0 Гц), 2,57 (3H, с), 2,81 (2H, кв, J=7,0 Гц), 7,04-7,11 (1H, м), 7,15 (1H, д, J=8,1 Гц), 7,24 (1H, дд, J=7,4, 1,6 Гц), 7,31-7,38 (1H, м), 7,44 (1H, дд, J=8,3, 1,7 Гц), 7,47-7,53 (1H, м), 7,54-7,61 (2H, м), 7,81-7,87 (2H, м), 8,09 (1H, д, J=8,3 Гц), 8,54 (1H, дд, J=2,1, 2,1 Гц), 8,87 (1H, д, J=1,7 Гц), 9,12 (1H, д, J=2,1 Гц), 9,14 (1H, д, J=2,1 Гц).
Пример 24b
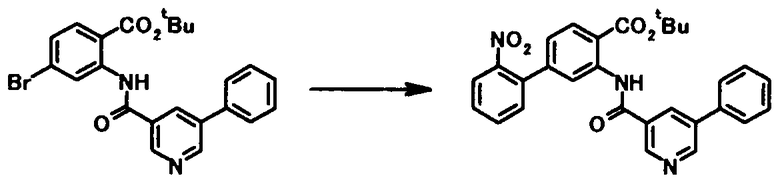
К раствору трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,6 мл), карбонат натрия (70 мг), 2-нитрофенилбороновую кислоту (44 мг) и тетракис(трифенилфосфин)палладий(0) (13 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней карбонат натрия (23 мг), 2-нитрофенилбороновую кислоту (37 мг), и тетракис(трифенилфосфин)палладий(0) (13 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 50 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 91-80% гексан/этилацетат] с получением 68 мг трет-бутил-4-(2-нитрофенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде светло-зеленого твердого вещества.
1H-ЯМР (CDCl3) δ: 1,66 (9H, с), 7,06 (1H, дд, J=8,2, 1,8 Гц), 7,43-7,49 (1H, м), 7,50-7,59 (4H, м), 7,64-7,73 (3H, м), 7,93-7,99 (1H, м), 8,09 (1H, д, J=8,2 Гц), 8,56 (1H, дд, J=2,2, 2,1 Гц), 8,99 (1H, д, J=1,7 Гц), 9,04 (1H, д, J=2,2 Гц), 9,26 (1H, д, J=2,1 Гц), 12,60 (1H, с).
Пример 25b
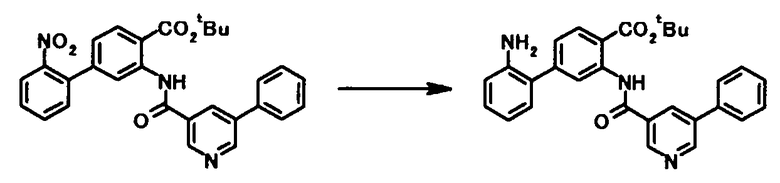
К раствору трет-бутил-4-(2-нитрофенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,28 г) в смеси хлороформа (3,0 мл) и метанола (2,0 мл) добавляли 10% палладированый уголь (0,13 г), а затем перемешивали в атмосфере водорода при комнатной температуре в течение 5 часов 40 минут. Нерастворимые вещества удаляли путем фильтрования, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 100-90% хлороформ/метанол] с получением 0,22 г трет-бутил-4-(2-аминофенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,55 (9H, с), 7,00-7,19 (2H, м), 7,21-7,36 (2H, м), 7,44 (1H, дд, J=8,2, 1,6 Гц), 7,47-7,62 (3H, м), 7,82-7,90 (2H, м), 8,00 (1H, д, J=8,2 Гц), 8,35 (1H, д, J=1,6 Гц), 8,62 (1H, дд, J=2,0, 2,0 Гц), 9,10-9,22 (2H, м), 11,62 (1H, с).
Пример 26b

К трет-бутил-4-(2-нитрофенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату (68 мг) добавляли трифторуксусную кислоту (3,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования, к полученному твердому веществу последовательно добавляли диоксан (3,0 мл) и 2 моль/л водный раствор гидроксида натрия (0,053 мл), а затем перемешивали при комнатной температуре в течение 1 часа 50 минут. К реакционной смеси добавляли воду. После корректировки значения pH до 6,3 добавлением 1 моль/л соляной кислоты твердое вещество собирали путем фильтрования с получением 47 мг 4-(2-нитрофенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,20-7,27 (1H, м), 7,50 (1H, дд, J=7,4, 7,4 Гц), 7,53-7,61 (2H, м), 7,64 (1H, д, J=7,8 Гц), 7,72 (1H, дд, J=7,8, 7,8 Гц), 7,80-7,89 (3H, м), 8,08 (1H, д, J=8,0 Гц), 8,14 (1H, д, J=8,1 Гц), 8,50-8,57 (1H, м), 8,66-8,72 (1H, м), 9,11 (1H, д, J=1,7 Гц), 9,14 (1H, д, J=1,7 Гц), 12,49-12,64 (1H, уширенный).
Пример 27b
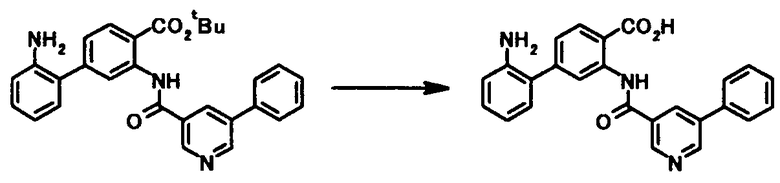
Следующее соединение получали, как описано в Примере 26b.
4-(2-Аминофенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 6,69 (1H, дд, J=7,3, 7,3 Гц), 6,81 (1H, д, J=7,8 Гц), 7,05-7,16 (2H, м), 7,33 (1H, д, J=8,1 Гц), 7,46-7,62 (3H, м), 7,80-7,87 (2H, м), 8,12 (1H, д, J=8,3 Гц), 8,53 (1H, с), 8,78 (1H, с), 9,09-9,17 (2H, м), 12,33 (1H, с).
Пример 28b
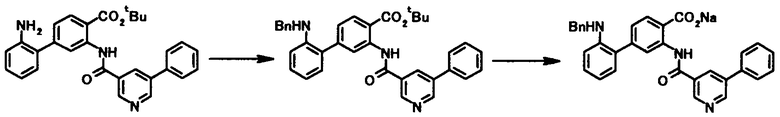
К суспензии трет-бутил-4-(2-аминофенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в хлористом метилене (1 мл) при комнатной температуре добавляли бензальдегид (0,027 мл) и триацетоксиборгидрид натрия (70 мг), а затем перемешивали при той же температуре в течение 3 часов 30 минут. К реакционной смеси при комнатной температуре добавляли хлористый метилен (2 мл), а затем перемешивали при той же температуре в течение 1 часа 50 минут. К реакционной смеси при комнатной температуре добавляли уксусную кислоту (0,013 мл) и триацетоксиборгидрид натрия (47 мг), а затем перемешивали при той же температуре в течение 2 часов 50 минут. К реакционной смеси при комнатной температуре добавляли триацетоксиборгидрид натрия (47 мг), хлористый метилен (3 мл) и бензальдегид (0,027 мл), а затем нагревали с обратным холодильником в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней триацетоксиборгидрид натрия (47 мг), а затем нагревали с обратным холодильником в течение 4 часов 40 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней хлороформ и воду. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент:85-60% гексан/этилацетат] с получением 78 мг трет-бутил-4-(2-(бензиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде светло-желтого твердого вещества.
К полученному трет-бутил-4-(2-(бензиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату (75 мг) добавляли трифторуксусную кислоту (1,0 мл), а затем перемешивали при комнатной температуре в течение 6 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку метанол (2 мл). После корректировки значения pH до 12,0 добавлением 2 моль/л водного раствора гидроксида натрия растворитель выпаривали в условиях пониженного давления. К полученному остатку добавляли воду, и собирали твердое вещество путем фильтрования с получением 68 мг 4-(2-(бензиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде светло-зеленого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 4,28-4,36 (2H, м), 5,36 (1H, т, J=5,5 Гц), 6,54 (1H, д, J=8,0 Гц), 6,61-6,69 (1H, м), 7,01-7,15 (3H, м), 7,17-7,24 (1H, м), 7,27-7,42 (4H, м), 7,45-7,62 (3H, м), 7,80-7,87 (2H, м), 8,14 (1H, д, J=8,0 Гц), 8,60 (1H, дд, J=2,1, 2,1 Гц), 8,81 (1H, д, J=1,7 Гц), 9,09 (1H, д, J=2,1 Гц), 9,18 (1H, д, J=2,1 Гц).
Пример 29b
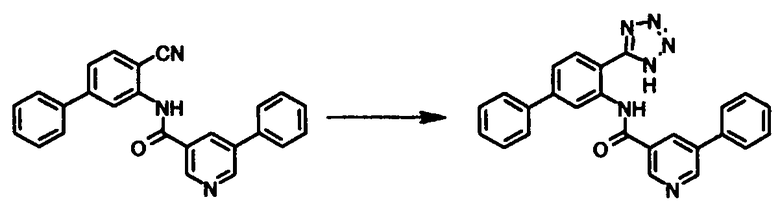
К раствору N-(2-циано-5-фенилфенил)-5-фенилпиридин-3-карбоксамида (0,11 г) в N,N-диметилформамиде (1,1 мл) при комнатной температуре добавляли азид натрия (38 мг) и хлорид аммония (31 мг), а затем перемешивали при 110°C в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 1,0 моль/л соляную кислоту (6,0 мл). Твердое вещество собирали путем фильтрования с получением 84 мг 5-фенил-N-(5-фенил-2-(1H-тетразол-5-ил)фенил)пиридин-3-карбоксамида в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,44-7,63 (6H, м), 7,75-7,83 (3H, м), 7,87-7,93 (2H, м), 8,13 (1H, д, J=8,0 Гц), 8,70-8,75 (1H, м), 8,78 (1H, д, J=1,5 Гц), 9,18 (1H, д, J=2,2 Гц), 9,20 (1H, д, J=2,0 Гц), 11,60 (1H, с).
Пример 30b
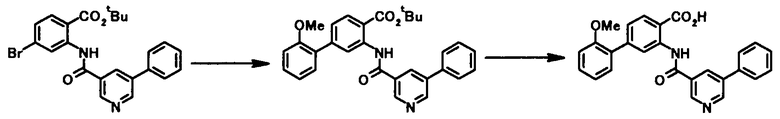
К суспензии трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,6 мл), карбонат натрия (70 мг), 2-метоксифенилбороновую кислоту (40 мг) и тетракис(трифенилфосфин)палладий(0) (13 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа. После охлаждения реакционной смеси до комнатной температуры нерастворимые вещества удаляли путем фильтрования, и добавляли к остатку 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 91-80% гексан/этилацетат] с получением 61 мг трет-бутил-4-(2-метоксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде белого твердого вещества.
К полученному трет-бутил-4-(2-метоксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату (61 мг) добавляли трифторуксусную кислоту (4,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования, и добавляли к полученному остатку диоксан (3,0 мл), воду и 2 моль/л водный раствор гидроксида натрия (0,080 мл). После корректировки значения pH до 7,6 добавлением 1 моль/л соляной кислоты твердое вещество собирали путем фильтрования с получением 32 мг 4-(2-метоксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 3,81 (3H, с), 7,09 (1H, дд, J=7,4, 7,4 Гц), 7,18 (1H, д, J=8,3 Гц), 7,33-7,40 (2H, м), 7,40-7,47 (1H, м), 7,50 (1H, дд, J=7,3, 7,3 Гц), 7,53-7,61 (2H, м), 7,80-7,87 (2H, м), 8,09 (1H, д, J=8,3 Гц), 8,52-8,56 (1H, м), 8,80-8,85 (1H, м), 9,12 (1H, д, J=2,0 Гц), 9,14 (1H, д, J=2,2 Гц), 12,35-12,49 (1H, уширенный).
Пример 31b
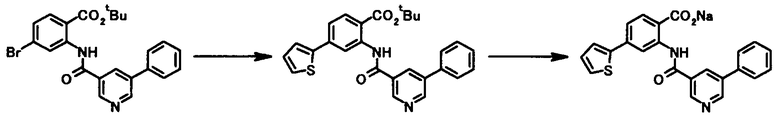
К суспензии трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,60 мл), 2-тиофенбороновую кислоту (34 мг), карбонат натрия (70 мг) и тетракис(трифенилфосфин)палладий(0) (13 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Kanto Chemical Co., Inc., силикагель 60 (сферический), элюент: 95-85% гексан/этилацетат] с получением трет-бутил-2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-2-ил)бензоата.
К полученному трет-бутил-2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-2-ил)бензоату добавляли трифторуксусную кислоту (4,0 мл), а затем перемешивали при комнатной температуре в течение 2 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 54 мг 2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-2-ил)бензойной кислоты в виде белого твердого вещества.
К суспензии полученной 2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-2-ил)бензойной кислоты (54 мг) в этаноле (4,0 мл) при комнатной температуре добавляли 1 моль/л водный раствор гидроксида натрия (0,13 мл), а затем перемешивали при той же температуре в течение 2 часов 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. Твердое вещество собирали путем фильтрования с получением 35 мг 2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-2-ил)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,15-7,21 (1H, м), 7,40 (1H, дд, J=8,1, 1,7 Гц), 7,46-7,63 (5H, м), 7,81-7,88 (2H, м), 8,08 (1H, д, J=8,1 Гц), 8,58-8,64 (1H, м), 9,06 (1H, д, J=1,7 Гц), 9,11 (1H, д, J=1,9 Гц), 9,19 (1H, д, J=1,7 Гц).
Примеры 32b-43b
Соединения, представленные в Таблице 9b, получали, как описано в Примере 31b.
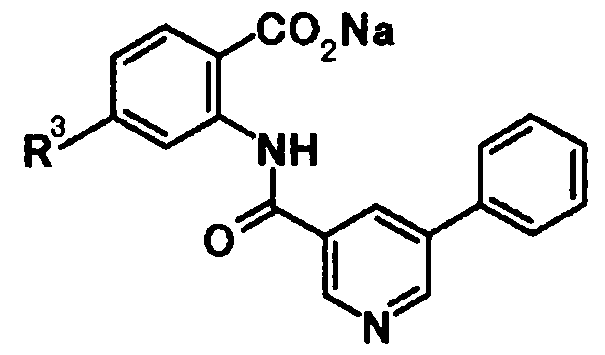
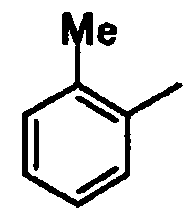
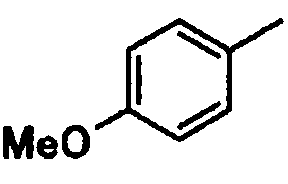
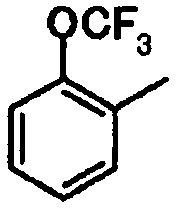
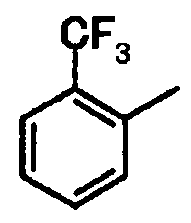
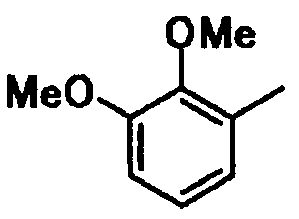
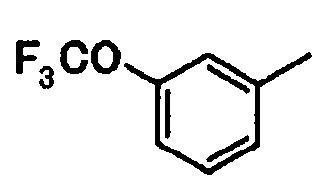
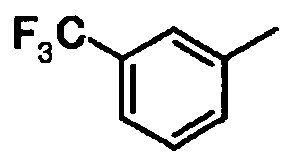
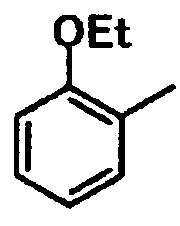
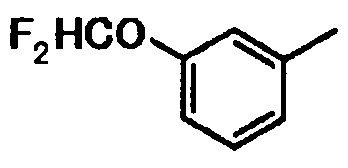
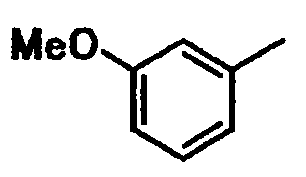
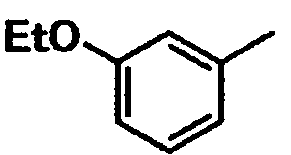
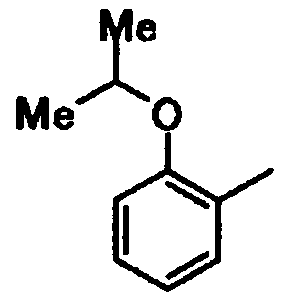
4-(2-Метилфенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 2,29 (3H, с), 7,00 (1H, дд, J=8,1, 1,7 Гц), 7,22-7,35 (4H, м), 7,46-7,53 (1H, м), 7,54-7,61 (2H, м), 7,80-7,86 (2H, м), 8,10 (1H, д, J=8,1 Гц), 8,59 (1H, дд, J=2,1, 2,1 Гц), 8,67 (1H, д, J=1,7 Гц), 9,09 (1H, д, J=2,1 Гц), 9,17 (1H, д, J=2,1 Гц).
2-(5-Фенилпиридин-3-карбоксамидо)-4-(2-(трифторметил)фенил)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 6,98 (1H, д, J=7,8 Гц), 7,44-7,53 (2H, м), 7,54-7,61 (2H, м), 7,64 (1H, дд, J=7,7, 7,7 Гц), 7,75 (1H, дд, J=7,4, 7,4 Гц), 7,80-7,90 (3H, м), 8,09 (1H, д, J=7,8 Гц), 8,56-8,62 (1H, м), 8,70 (1H, с), 9,09 (1H, д, J=1,5 Гц), 9,16 (1H, д, J=1,5 Гц).
2-(5-фенилпиридин-3-карбоксамидо)-4-(3-(трифторметил)фенил)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 7,44 (1H, д, J=8,3 Гц), 7,47-7,54 (1H, м), 7,55-7,63 (2H, м), 7,73-7,81 (2H, м), 7,82-7,89 (2H, м), 7,96 (1H, с), 7,99-8,06 (1H, м), 8,18 (1H, д, J=8,0 Гц), 8,61-8,67 (1H, м), 9,07-9,15 (2H, м), 9,21 (1H, с).
4-(3-Метоксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 3,85 (3H, с), 6,94-7,03 (1H, м), 7,20 (1H, с), 7,26 (1H, д, J=7,6 Гц), 7,31-7,37 (1H, м), 7,42 (1H, дд, J=7,9, 7,9 Гц), 7,50 (1H, дд, J=7,3, 7,3 Гц), 7,54-7,63 (2H, м), 7,81-7,89 (2H, м), 8,12 (1H, д, J=8,0 Гц), 8,62 (1H, с), 9,02 (1H, с), 9,10 (1H, д, J=1,7 Гц), 9,17-9,24 (1H, м).
4-(4-Метоксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 3,82 (3H, с), 7,04-7,11 (2H, м), 7,35 (1H, дд, J=8,2, 1,8 Гц), 7,46-7,53 (1H, м), 7,54-7,61 (2H, м), 7,62-7,69 (2H, м), 7,80-7,87 (2H, м), 8,10 (1H, д, J=8,2 Гц), 8,60 (1H, дд, J=2,1, 2,0 Гц), 9,00 (1H, д, J=1,8 Гц), 9,11 (1H, д, J=2,1 Гц), 9,18 (1H, д, J=2,0 Гц).
4-(2,3-Диметоксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 3,61 (3H, с), 3,86 (3H, с), 6,91-6,97 (1H, м), 7,06-7,19 (3H, м), 7,46-7,53 (1H, м), 7,54-7,62 (2H, м), 7,80-7,87 (2H, м), 8,07 (1H, д, J=8,0 Гц), 8,60 (1H, с), 8,82 (1H, с), 9,06-9,12 (1H, м), 9,15-9,20 (1H, м).
4-(2-Этоксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 1,31 (3H, т, J=7,0 Гц), 4,07 (2H, кв, J=7,0 Гц), 7,05 (1H, дд, J=7,3, 7,3 Гц), 7,12 (1H, д, J=8,6 Гц), 7,20 (1H, д, J=8,0 Гц), 7,30-7,40 (2H, м), 7,50 (1H, дд, J=7,2, 7,2 Гц), 7,54-7,63 (2H, м), 7,80-7,89 (2H, м), 8,07 (1H, д, J=8,0 Гц), 8,60 (1H, с), 8,89 (1H, с), 9,09 (1H, д, J=1,7 Гц), 9,16-9,23 (1H, м).
4-(3-Этоксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 1,38 (3H, т, J=7,0 Гц), 4,12 (2H, кв, J=7,0 Гц), 6,96 (1H, дд, J=8,1, 2,4 Гц), 7,16-7,20 (1H, м), 7,24 (1H, д, J=7,6 Гц), 7,33 (1H, дд, J=7,9, 1,4 Гц), 7,40 (1H, дд, J=7,9, 7,9 Гц), 7,46-7,53 (1H, м), 7,54-7,62 (2H, м), 7,81-7,87 (2H, м), 8,11 (1H, д, J=8,0 Гц), 8,62 (1H, дд, J=1,9, 1,8 Гц), 9,02 (1H, д, J=1,5 Гц), 9,10 (1H, д, J=1,9 Гц), 9,19 (1H, д, J=1,8 Гц).
2-(5-фенилпиридин-3-карбоксамидо)-4-(2-(трифторметокси)фенил)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 7,09-7,16 (1H, м), 7,46-7,62 (7H, м), 7,80-7,87 (2H, м), 8,11 (1H, д, J=8,0 Гц), 8,57-8,63 (1H, м), 8,81-8,86 (1H, м), 9,09 (1H, д, J=2,0 Гц), 9,17 (1H, д, J=2,0 Гц).
2-(5-Фенилпиридин-3-карбоксамидо)-4-(3-(трифторметокси)фенил)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 7,36-7,45 (2H, м), 7,47-7,54 (1H, м), 7,55-7,69 (4H, м), 7,72-7,78 (1H, м), 7,82-7,88 (2H, м), 8,15 (1H, д, J=8,0 Гц), 8,60-8,65 (1H, м), 9,06 (1H, д, J=1,7 Гц), 9,11 (1H, д, J=2,2 Гц), 9,20 (1H, д, J=1,9 Гц).
4-(3-(Дифторметокси)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 7,16-7,63 (9H, м), 7,81-7,88 (2H, м), 8,14 (1H, д, J=8,0 Гц), 8,60-8,65 (1H, м), 9,04 (1H, д, J=1,7 Гц), 9,10 (1H, д, J=2,2 Гц), 9,20 (1H, д, J=1,7 Гц).
4-(2-Изопропоксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 1,24 (6H, д, J=6,1 Гц), 4,58 (1H, гептет, J=6,1 Гц), 7,03 (1H, дд, J=7,4, 7,4 Гц), 7,12 (1H, д, J=8,3 Гц), 7,18 (1H, дд, J=8,0, 1,6 Гц), 7,29-7,37 (2H, м), 7,46-7,53 (1H, м), 7,54-7,61 (2H, м), 7,80-7,87 (2H, м), 8,05 (1H, д, J=8,0 Гц), 8,59 (1H, дд, J=2,2, 2,2 Гц), 8,88 (1H, д, J=1,6 Гц), 9,09 (1H, д, J=2,2 Гц), 9,17 (1H, д, J=2,2 Гц).
Пример 44b
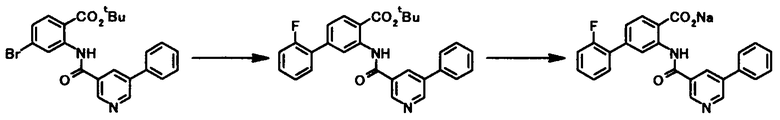
К суспензии трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в толуоле (2,1 мл) добавляли этанол (0,62 мл), воду (0,31 мл), карбонат натрия (70 мг), 2-фторфенилбороновую кислоту (37 мг) и тетракис(трифенилфосфин)палладий(0) (13 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 91-85% гексан/этилацетат] с получением трет-бутил-4-(2-фторфенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата.
К полученному трет-бутил-4-(2-фторфенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату добавляли трифторуксусную кислоту (3,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования. К полученному твердому веществу добавляли диоксан (3,0 мл) и 2 моль/л водный раствор гидроксида натрия (0,041 мл), а затем перемешивали при комнатной температуре в течение 1 часа. К реакционной смеси добавляли 10% водный раствор лимонной кислоты, и собирали твердое вещество путем фильтрования с получением 36 мг 4-(2-фторфенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
К полученной 4-(2-фторфенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоте (36 мг) последовательно добавляли этанол (1,5 мл) и 1 моль/л водный раствор гидроксида натрия (0,087 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Твердое вещество собирали путем фильтрования с получением 22 мг 4-(2-фторфенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,21 (1H, ддд, J=8,0, 1,8, 1,8 Гц), 7,30-7,38 (2H, м), 7,41-7,53 (2H, м), 7,53-7,61 (3H, м), 7,81-7,87 (2H, м), 8,13 (1H, д, J=8,0 Гц), 8,61 (1H, дд, J=2,2, 2,1 Гц), 8,90-8,94 (1H, м), 9,09 (1H, д, J=2,2 Гц), 9,18 (1H, д, J=2,1 Гц).
Пример 45b
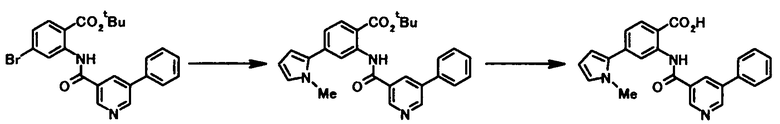
К раствору трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в толуоле (2,1 мл) добавляли этанол (0,62 мл), воду (0,31 мл), карбонат натрия (70 мг), 1-метил-2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол (55 мг) и тетракис(трифенилфосфин)палладий(0) (13 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней карбонат натрия (23 мг), 1-метил-2-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)-1H-пиррол (46 мг) и тетракис(трифенилфосфин)палладий(0) (13 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней толуол (1,0 мл), этанол (0,31 мл) и воду (0,16 мл), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 71 мг трет-бутил-4-(1-метил-1H-пиррол-2-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде светло-желтого твердого вещества.
К полученному трет-бутил-4-(1-метил-1H-пиррол-2-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату (71 мг) добавляли метанол (1,5 мл), диоксан (1,5 мл) и 2 моль/л водный раствор гидроксида натрия (0,24 мл), а затем перемешивали при 50-55°C в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты. Твердое вещество собирали путем фильтрования с получением 50 мг 4-(1-метил-1H-пиррол-2-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 3,79 (3H, с), 6,15 (1H, дд, J=3,0, 3,0 Гц), 6,38-6,43 (1H, м), 6,97 (1H, дд, J=2,1, 2,1 Гц), 7,36 (1H, дд, J=8,3, 1,6 Гц), 7,47-7,53 (1H, м), 7,54-7,61 (2H, м), 7,81-7,87 (2H, м), 8,07 (1H, д, J=8,3 Гц), 8,54 (1H, дд, J=2,1, 2,1 Гц), 8,84 (1H, д, J=1,6 Гц), 9,13 (1H, д, J=2,1 Гц), 9,15 (1H, д, J=2,1 Гц), 12,37 (1H, с).
Пример 46b
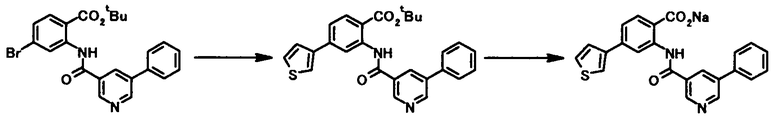
К раствору трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (80 мг) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,6 мл), карбонат натрия (47 мг), 3-тиофенбороновую кислоту (27 мг) и дихлорид бис(трифенилфосфин)палладия(II) (2,5 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 10 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением трет-бутил-2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-3-ил)бензоата.
К полученному трет-бутил-2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-3-ил)бензоату добавляли трифторуксусную кислоту (4,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 47 мг 2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-3-ил)бензойной кислоты в виде белого твердого вещества.
К суспензии полученной 2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-3-ил)бензойной кислоты (47 мг) в этаноле (4,0 мл) при комнатной температуре добавляли 1 моль/л водный раствор гидроксида натрия (0,10 мл), а затем перемешивали при той же температуре в течение 1 часа 10 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этанол и воду. Твердое вещество собирали путем фильтрования с получением 40 мг 2-(5-фенилпиридин-3-карбоксамидо)-4-(тиофен-3-ил)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,36-7,42 (1H, м), 7,46-7,54 (2H, м), 7,54-7,61 (2H, м), 7,65-7,70 (1H, м), 7,81-7,87 (3H, м), 8,04-8,10 (1H, м), 8,59-8,64 (1H, м), 9,01-9,05 (1H, м), 9,08-9,12 (1H, м), 9,17-9,21 (1H, м).
Пример 47b
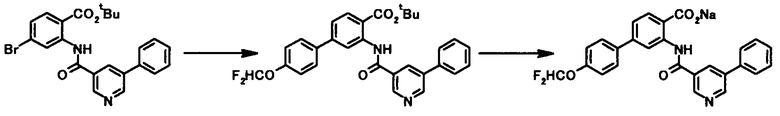
Следующее соединение получали, как описано в Примере 46b.
4-(4-(Дифторметокси)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 7,12-7,53 (5H, м), 7,54-7,62 (2H, м), 7,72-7,78 (2H, м), 7,81-7,87 (2H, м), 8,13 (1H, д, J=7,8 Гц), 8,59-8,65 (1H, м), 9,01-9,05 (1H, м), 9,11 (1H, д, J=1,5 Гц), 9,20 (1H, д, J=1,5 Гц).
Пример 48b
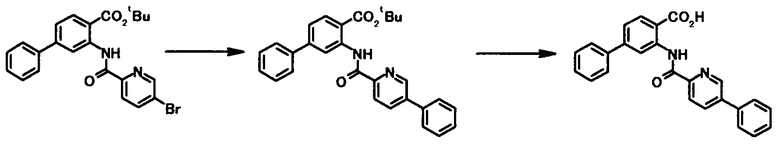
К суспензии трет-бутил-2-(5-бромпиридин-2-карбоксамидо)-4-фенилбензоата (0,12 г) в диметиловом эфире этиленгликоля (1,2 мл) добавляли карбонат натрия (55 мг), фенилбороновую кислоту (38 мг), воду (0,35 мл) и дихлорид бис(трифенилфосфин)палладия(II) (3,7 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней карбонат натрия (55 мг), фенилбороновую кислоту (38 мг) и дихлорид бис(трифенилфосфин)палладия(II) (3,7 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней этилацетат и воду. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-80% гексан/этилацетат] с получением 0,11 г трет-бутил-4-фенил-2-(5-фенилпиридин-2-карбоксамидо)бензоата в виде белого твердого вещества.
К полученному трет-бутил-4-фенил-2-(5-фенилпиридин-2-карбоксамидо)бензоату (0,11 г) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 4 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этилацетат и воду. После корректировки значения pH до 6,5 добавлением насыщенного водного раствора бикарбоната натрия органический слой разделяли, последовательно промывали водой и насыщенным раствором хлорида натрия, и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 90 мг 4-фенил-2-(5-фенилпиридин-2-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,44-7,60 (7H, м), 7,73-7,79 (2H, м), 7,85-7,91 (2H, м), 8,15 (1H, д, J=8,1 Гц), 8,29 (1H, д, J=8,3 Гц), 8,40 (1H, дд, J=8,2, 2,3 Гц), 9,08 (1H, д, J=2,0 Гц), 9,26 (1H, д, J=1,7 Гц), 13,23 (1H, с).
Пример 49b
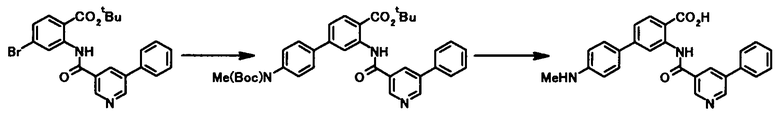
К раствору трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,15 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,60 мл), карбонат натрия (88 мг), трет-бутилметил-(4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенил)карбамате (0,13 г) и дихлорид бис(трифенилфосфин)палладия(II) (5,0 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-85% гексан/этилацетат] с получением 0,16 г трет-бутил-4-(4-((трет-бутоксикарбонил)(метил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде белого твердого вещества.
К полученному трет-бутил-4-(4-((трет-бутоксикарбонил)(метил)амино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату (0,16 г) добавляли трифторуксусную кислоту (4,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования, и добавляли к полученному твердому веществу этанол и воду. После корректировки значения pH до 5,5 добавлением 1 моль/л водного раствора гидроксида натрия твердое вещество собирали путем фильтрования с получением 0,11 г 4-(4-(метиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде светло-желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 2,74 (3H, с), 6,65-6,71 (2H, м), 7,43-7,61 (6H, м), 7,81-7,87 (2H, м), 8,05 (1H, д, J=8,3 Гц), 8,53-8,58 (1H, м), 8,97 (1H, д, J=1,5 Гц), 9,11-9,18 (2H, м), 12,39 (1H, с).
Пример 50b
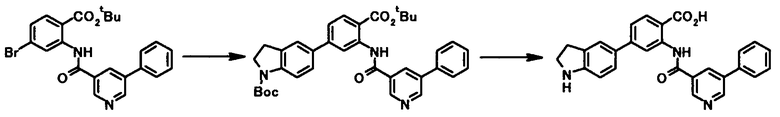
Следующее соединение получали, как описано в Примере 49b.
4-(Индолин-5-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 3,02 (2H, т, J=8,4 Гц), 3,51 (2H, т, J=8,4 Гц), 6,61 (1H, д, J=8,3 Гц), 7,37 (1H, д, J=8,3 Гц), 7,40-7,48 (2H, м), 7,50 (1H, дд, J=7,3, 7,3 Гц), 7,54-7,62 (2H, м), 7,80-7,89 (2H, м), 8,05 (1H, д, J=8,3 Гц), 8,56 (1H, с), 8,97 (1H, с), 9,07-9,23 (2H, м), 12,46 (1H, с).
Пример 51b
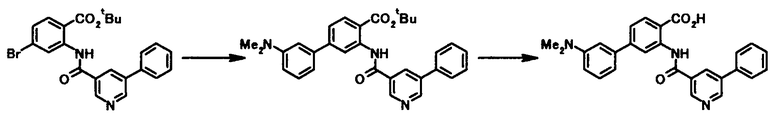
Следующее соединение получали, как описано в Примере 49b.
4-(3-(Диметиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойная кислота
1H-ЯМР (DMSO-d6) δ: 2,99 (6H, с), 6,79-6,87 (1H, м), 6,95-7,04 (2H, м), 7,34 (1H, дд, J=8,2, 8,2 Гц), 7,47-7,63 (4H, м), 7,81-7,89 (2H, м), 8,12 (1H, д, J=8,3 Гц), 8,56 (1H, дд, J=2,1, 2,1 Гц), 8,98 (1H, д, J=1,7 Гц), 9,11-9,19 (2H, м), 12,35 (1H, с).
Пример 52b
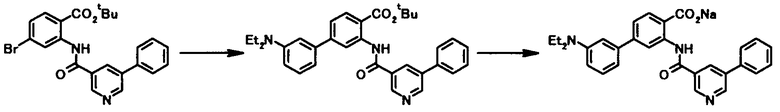
К раствору N,N-диэтил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)анилина (83 мг) в диметиловом эфире этиленгликоля (1,0 мл) добавляли трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоат (0,11 г), карбонат натрия (64 мг), воду (0,30 мл) и дихлорид бис(трифенилфосфин)палладия(II) (3,5 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 40 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней воду и хлороформ. Органический слой разделяли и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 90-70% гексан/этилацетат] с получением 0,12 г трет-бутил-4-(3-(диэтиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата в виде желтого твердого вещества.
К полученному трет-бутил-4-(3-(диэтиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату (0,12 г) добавляли трифторуксусную кислоту (1,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 10 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку метанол (2,0 мл). После корректировки значения pH до 12,7 добавлением 2 моль/л водного раствора гидроксида натрия твердое вещество собирали путем фильтрования с получением 99 мг 4-(3-(диэтиламино)фенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 1,15 (6H, т, J=7,0 Гц), 3,41 (4H, кв, J=7,0 Гц), 6,70 (1H, дд, J=8,4, 2,3 Гц), 6,81-6,92 (2H, м), 7,21-7,31 (2H, м), 7,46-7,62 (3H, м), 7,81-7,89 (2H, м), 8,09 (1H, д, J=7,8 Гц), 8,59-8,65 (1H, м), 8,98 (1H, д, J=1,7 Гц), 9,09 (1H, д, J=2,0 Гц), 9,19 (1H, д, J=2,0 Гц).
Пример 53b
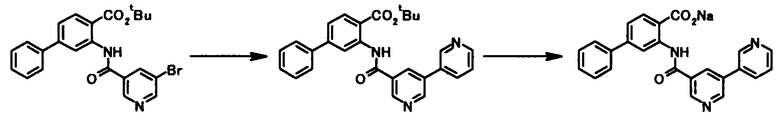
Следующее соединение получали, как описано в Примере 52b.
4-Фенил-2-(5-(пиридин-3-ил)пиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 7,34 (1H, дд, J=8,0, 1,8 Гц), 7,37-7,43 (1H, м), 7,47-7,54 (2H, м), 7,60 (1H, дд, J=8,0, 4,9 Гц), 7,66-7,72 (2H, м), 8,12 (1H, д, J=8,0 Гц), 8,26 (1H, ддд, J=8,0, 2,0, 2,0 Гц), 8,67 (1H, дд, J=2,2, 2,2 Гц), 8,70 (1H, дд, J=4,9, 1,4 Гц), 9,03 (1H, д, J=1,7 Гц), 9,05 (1H, д, J=1,9 Гц), 9,17 (1H, д, J=2,2 Гц), 9,24 (1H, д, J=2,0 Гц).
Пример 54b
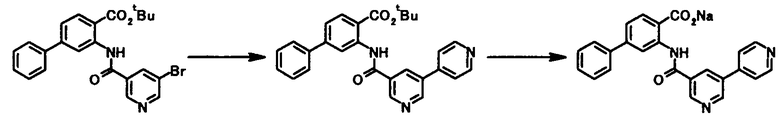
Следующее соединение получали, как описано в Примере 52b.
4-Фенил-2-(5-(пиридин-4-ил)пиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 7,31-7,36 (1H, м), 7,36-7,43 (1H, м), 7,47-7,54 (2H, м), 7,66-7,72 (2H, м), 7,87-7,92 (2H, м), 8,12 (1H, д, J=8,1 Гц), 8,71-8,78 (3H, м), 9,00-9,04 (1H, м), 9,21-9,24 (1H, м), 9,26-9,30 (1H, м).
Пример 55b
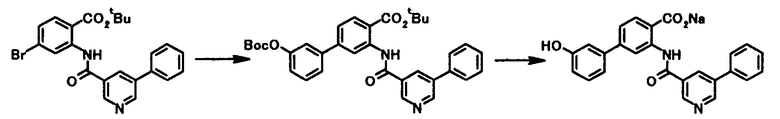
К суспензии трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в диметиловом эфире этиленгликоля (2,0 мл) добавляли воду (0,6 мл), карбонат натрия (58 мг), трет-бутил-3-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)фенилкарбонат (85 мг) и дихлорид бис(трифенилфосфин)палладия(II) (3,0 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 95-80% гексан/этилацетат] с получением трет-бутил-4-(3-(трет-бутоксикарбонил)оксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата.
К полученному трет-бутил-4-(3-(трет-бутоксикарбонил)оксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоату добавляли трифторуксусную кислоту (4,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 15 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования с получением 70 мг 4-(3-гидроксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде светло-желтого твердого вещества.
К полученной 4-(3-гидроксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоте (70 мг) последовательно добавляли этанол (4,0 мл) и 1 моль/л водный раствор гидроксида натрия (0,17 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этанол и воду. Твердое вещество собирали путем фильтрования с получением 26 мг 4-(3-гидроксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,76-6,83 (1H, м), 7,08-7,14 (2H, м), 7,25-7,33 (2H, м), 7,46-7,53 (1H, м), 7,54-7,62 (2H, м), 7,81-7,87 (2H, м), 8,10 (1H, д, J=8,1 Гц), 8,61 (1H, дд, J=2,2, 2,1 Гц), 9,00 (1H, д, J=1,7 Гц), 9,10 (1H, д, J=2,2 Гц), 9,18 (1H, д, J=2,1 Гц), 9,59 (1H, с).
Пример 56b
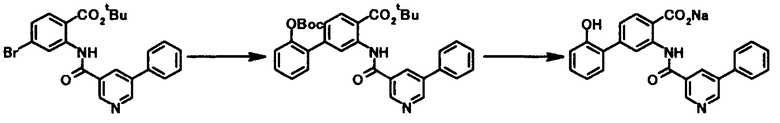
Следующее соединение получали, как описано в Примере 31b.
4-(2-Гидроксифенил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 6,90 (1H, дд, J=7,4, 7,4 Гц), 6,96 (1H, д, J=8,0 Гц), 7,14-7,26 (2H, м), 7,26-7,32 (1H, м), 7,49 (1H, дд, J=7,3, 7,3 Гц), 7,54-7,61 (2H, м), 7,80-7,87 (2H, м), 8,05 (1H, д, J=8,0 Гц), 8,60 (1H, дд, J=2,1, 2,1 Гц), 8,88 (1H, д, J=1,4 Гц), 9,09 (1H, д, J=2,0 Гц), 9,17 (1H, д, J=1,7 Гц), 9,54 (1H, с).
Пример 57b
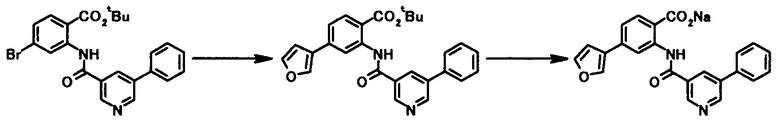
Следующее соединение получали, как описано в Примере 55b.
4-(Фуран-3-ил)-2-(5-фенилпиридин-3-карбоксамидо)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 6,91 (1H, с), 7,31 (1H, д, J=8,0 Гц), 7,45-7,63 (3H, м), 7,76-7,89 (3H, м), 8,06 (1H, д, J=7,8 Гц), 8,17 (1H, с), 8,61 (1H, с), 8,91 (1H, с), 9,10 (1H, с), 9,19 (1H, с).
Пример 58b
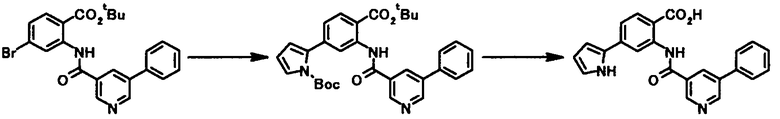
К раствору трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в толуоле (3,0 мл) добавляли трикалийфосфат (0,12 г), 1-(трет-бутоксикарбонил)-1H-пиррол-2-бороновую кислоту (56 мг), 2-дициклогексилфосфино-2',6'-диметоксибифенил (1 мг) и ацетат палладия(II) (1 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, добавляли к ней трикалийфосфат (47 мг), 1-(трет-бутоксикарбонил)-1H-пиррол-2-бороновую кислоту (47 мг), 2-дициклогексилфосфино-2',6'-диметоксибифенил (1 мг) и ацетат палладия(II) (1 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, и добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку последовательно добавляли диоксан (1,5 мл), метанол (1,5 мл) и 2 моль/л водный раствор гидроксида натрия (0,29 мл), а затем перемешивали при 50°C в течение 1 часа 30 минут. Реакционную смесь охлаждали до комнатной температуры, а затем последовательно добавляли к ней 10% водный раствор лимонной кислоты и этилацетат. Твердое вещество собирали путем фильтрования с получением 39 мг 2-(5-фенилпиридин-3-карбоксамидо)-4-(1H-пиррол-2-ил)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,18-6,24 (1H, м), 6,63-6,69 (1H, м), 6,95-7,01 (1H, м), 7,46-7,54 (2H, м), 7,54-7,62 (2H, м), 7,81-7,88 (2H, м), 8,03 (1H, д, J=8,3 Гц), 8,56 (1H, дд, J=2,1, 2,1 Гц), 8,90 (1H, д, J=1,7 Гц), 9,12-9,17 (2H, м), 11,61 (1H, с), 12,38 (1H, с), 13,50-13,82 (1H, уширенный).
Пример 59b
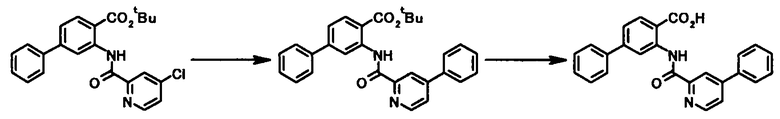
К раствору трет-бутил-2-(4-хлорпиридин-2-карбоксамидо)-4-фенилбензоата (60 мг) в толуоле (1,2 мл) добавляли фенилбороновую кислоту (21 мг), трикалийфосфат (69 мг), 2-дициклогексилфосфино-2',6'-диметоксибифенил (1,2 мг) и ацетат палладия(II) (1,3 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней фенилбороновую кислоту (5,4 мг), трикалийфосфат (16 мг), 2-дициклогексилфосфино-2',6'-диметоксибифенил (1,2 мг) и ацетат палладия(II) (1,3 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 100-85% гексан/этилацетат] с получением 65 мг трет-бутил-4-фенил-2-(4-фенилпиридин-2-карбоксамидо)бензоата в виде бесцветного маслянистого вещества.
К полученному трет-бутил-4-фенил-2-(4-фенилпиридин-2-карбоксамидо)бензоату (64 мг) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку этилацетат и воду. После корректировки значения pH до 6,5 добавлением насыщенного водного раствора бикарбоната натрия органический слой разделяли, последовательно промывали водой и насыщенным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли диизопропиловый эфир, и собирали твердое вещество путем фильтрования с получением 50 мг 4-фенил-2-(4-фенилпиридин-2-карбоксамидо)бензойной кислоты в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,44-7,51 (1H, м), 7,51-7,62 (6H, м), 7,73-7,78 (2H, м), 7,89-7,94 (2H, м), 8,04 (1H, дд, J=5,1, 1,9 Гц), 8,15 (1H, д, J=8,3 Гц), 8,48 (1H, д, J=1,2 Гц), 8,82 (1H, д, J=5,1 Гц), 9,27 (1H, д, J=1,7 Гц), 13,20 (1H, с).
Пример 60b
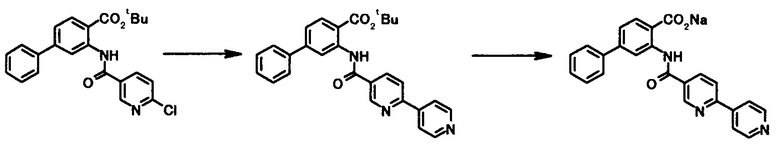
К суспензии трет-бутил-2-(6-хлорпиридин-3-карбоксамидо)-4-фенилбензоата (80 мг) в толуоле (1,6 мл) добавляли 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (48 мг), трикалийфосфат (91 мг), 2-дициклогексилфосфино-2',6'-диметоксибифенил (1,6 мг) и ацетат палладия(II) (1,8 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов 30 минут. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 4-(4,4,5,5-тетраметил-1,3,2-диоксаборолан-2-ил)пиридин (48 мг), трикалийфосфат (91 мг), 2-дициклогексилфосфино-2',6'-диметоксибифенил (1,6 мг) и ацетат палладия(II) (1,8 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 3 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней 2-дициклогексилфосфино-2',6'-диметоксибифенил (1,6 мг) и ацетат палладия(II) (1,8 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. После охлаждения реакционной смеси до комнатной температуры растворитель выпаривали в условиях пониженного давления, и добавляли к остатку хлороформ и воду. Нерастворимые вещества удаляли путем фильтрования. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [Fuji Silysia Chemical Ltd., PSQ100B (сферический), элюент: 90-15% гексан/этилацетат] с получением 25 мг трет-бутил-4-фенил-2-(6-(пиридин-4-ил)пиридин-3-карбоксамидо)бензоата в виде светло-желтого твердого вещества.
К полученному трет-бутил-4-фенил-2-(6-(пиридин-4-ил)пиридин-3-карбоксамидо)бензоату (25 мг) добавляли трифторуксусную кислоту (5 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. После корректировки значения pH до 5,5 добавлением насыщенного водного раствора бикарбоната натрия твердое вещество собирали путем фильтрования с получением 20 мг 4-фенил-2-(6-(пиридин-4-ил)пиридин-3-карбоксамидо)бензойной кислоты в виде желтого твердого вещества.
К полученной 4-фенил-2-(6-(пиридин-4-ил)пиридин-3-карбоксамидо)бензойной кислоте (20 мг) добавляли диоксан (2 мл), метанол (2 мл) и 2 моль/л водный раствор гидроксида натрия (0,025 мл), и выпаривали растворитель в условиях пониженного давления. К полученному остатку добавляли ацетон. Твердое вещество собирали путем фильтрования с получением 17 мг 4-фенил-2-(6-(пиридин-4-ил)пиридин-3-карбоксамидо)бензоата натрия в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 7,30-7,43 (2H, м), 7,46-7,54 (2H, м), 7,66-7,72 (2H, м), 8,08-8,20 (3H, м), 8,32-8,38 (1H, м), 8,49-8,55 (1H, м), 8,73-8,80 (2H, м), 9,00-9,04 (1H, м), 9,35 (1H, с).
Пример 61b
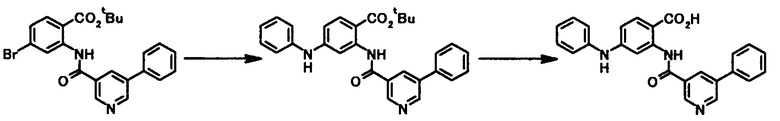
К раствору трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в толуоле (2,5 мл) добавляли карбонат цезия (0,14 г), анилин (0,030 мл), трис(дибензилиденацетон)дипалладий(0) (2 мг), ацетат палладия(II) (1 мг) и 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (5 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа 10 минут. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 91-80% гексан/этилацетат] с получением трет-бутил-4-анилино-2-(5-фенилпиридин-3-карбоксамидо)бензоата.
К полученному трет-бутил-4-анилино-2-(5-фенилпиридин-3-карбоксамидо)бензоату добавляли трифторуксусную кислоту (3,0 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования. К полученному твердому веществу последовательно добавляли диоксан (3,0 мл) и 2 моль/л водный раствор гидроксида натрия (0,068 мл), а затем перемешивали при комнатной температуре в течение 1 часа 30 минут. К реакционной смеси добавляли 10% водный раствор лимонной кислоты, и собирали твердое вещество путем фильтрования с получением 73 мг 4-анилино-2-(5-фенилпиридин-3-карбоксамидо)бензойной кислоты в виде желтого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 6,80 (1H, дд, J=8,8, 2,2 Гц), 7,00-7,07 (1H, м), 7,22-7,28 (2H, м), 7,33-7,40 (2H, м), 7,46-7,52 (1H, м), 7,53-7,60 (2H, м), 7,80-7,86 (2H, м), 7,91 (1H, д, J=8,8 Гц), 8,48-8,52 (1H, м), 8,55 (1H, д, J=2,2 Гц), 9,00 (1H, с), 9,10 (1H, д, J=1,7 Гц), 9,13 (1H, д, J=2,0 Гц), 12,67 (1H, с), 13,14-13,27 (1H, уширенный).
Пример 62b
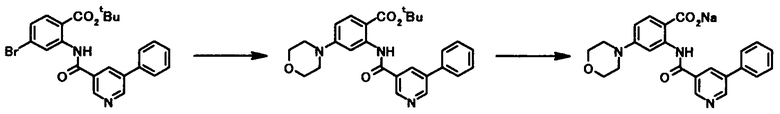
К раствору трет-бутил-4-бром-2-(5-фенилпиридин-3-карбоксамидо)бензоата (0,10 г) в толуоле (3,0 мл) добавляли карбонат цезия (0,14 г), морфолин (0,029 мл), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (5 мг), трис(дибензилиденацетон)дипалладий(0) (2 мг) и ацетат палладия(II) (1 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 1 часа. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней морфолин (0,029 мл), а затем нагревали с обратным холодильником в атмосфере азота в течение 2 часов. Реакционную смесь охлаждали до комнатной температуры, затем добавляли к ней карбонат цезия (72 мг), морфолин (0,029 мл), 2-дициклогексилфосфино-2',4',6'-триизопропилбифенил (5 мг), трис(дибензилиденацетон)дипалладий(0) (2 мг) и ацетат палладия(II) (1 мг), а затем нагревали с обратным холодильником в атмосфере азота в течение 4 часов. Реакционную смесь охлаждали до комнатной температуры, а затем добавляли к ней этилацетат и 10% водный раствор лимонной кислоты. Органический слой разделяли, промывали насыщенным водным раствором хлорида натрия и сушили над безводным сульфатом магния, и выпаривали растворитель в условиях пониженного давления. Полученный остаток очищали по методу колоночной хроматографии на силикагеле [элюент: 85-70% гексан/этилацетат] с получением трет-бутил-4-морфолино-2-(5-фенилпиридин-3-карбоксамидо)бензоата.
К полученному трет-бутил-4-морфолино-2-(5-фенилпиридин-3-карбоксамидо)бензоату добавляли трифторуксусную кислоту (3,0 мл), а затем перемешивали при комнатной температуре в течение 3 часов. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку диизопропиловый эфир. Твердое вещество собирали путем фильтрования, последовательно добавляли к полученному твердому веществу этанол (2,5 мл) и 1 моль/л водный раствор гидроксида натрия (0,44 мл), а затем перемешивали при комнатной температуре в течение 1 часа. Растворитель выпаривали в условиях пониженного давления, и добавляли к полученному остатку воду. Твердое вещество собирали путем фильтрования с получением 35 мг 4-морфолино-2-(5-фенилпиридин-3-карбоксамидо)бензоата натрия в виде белого твердого вещества.
1H-ЯМР (DMSO-d6) δ: 3,13-3,21 (4H, м), 3,73-3,81 (4H, м), 6,62 (1H, дд, J=8,8, 2,6 Гц), 7,46-7,52 (1H, м), 7,54-7,61 (2H, м), 7,80-7,86 (2H, м), 7,90 (1H, д, J=8,8 Гц), 8,37 (1H, д, J=2,6 Гц), 8,59 (1H, дд, J=2,1, 2,2 Гц), 9,08 (1H, д, J=2,2 Гц), 9,17 (1H, д, J=2,1 Гц).
Пример 63b
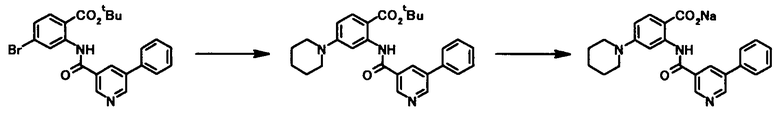
Следующее соединение получали, как описано в Примере 62b.
2-(5-Фенилпиридин-3-карбоксамидо)-4-(пиперидин-1-ил)бензоат натрия
1H-ЯМР (DMSO-d6) δ: 1,53-1,67 (6H, м), 3,18-3,25 (4H, м), 6,57 (1H, дд, J=8,9, 2,1 Гц), 7,46-7,53 (1H, м), 7,53-7,61 (2H, м), 7,79-7,87 (3H, м), 8,34 (1H, д, J=2,4 Гц), 8,58-8,63 (1H, м), 9,07 (1H, д, J=2,2 Гц), 9,16 (1H, д, J=2,0 Гц).
Применимость в промышленных условиях
Поскольку производное N-ацилантраниловой кислоты по настоящему изобретению или его соль обладает ингибирующим действием на продукцию коллагена, оно применимо для профилактики, лечения и тому подобное, заболеваний, ассоциированных с избыточной продукцией коллагена, таких как легочный фиброз, склеродермия, нефросклероз и цирроз печени.
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВОЕ ПРОИЗВОДНОЕ АНТРАНИЛОВОЙ КИСЛОТЫ ИЛИ ЕГО СОЛЬ | 2005 |
|
RU2394021C2 |
| КОНДЕНСИРОВАННОЕ ПРОИЗВОДНОЕ АМИНОДИГИДРОТИАЗИНА | 2009 |
|
RU2476431C2 |
| СИНТЕТИЧЕСКОЕ ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ 1-(2-ДЕЗОКСИ-2-ФТОР-4-ТИО-β-D-АРАБИНОФУРАНОЗИЛ)ЦИТОЗИНА, СИНТЕТИЧЕСКОЕ ПРОМЕЖУТОЧНОЕ СОЕДИНЕНИЕ ТИОНУКЛЕОЗИДА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2013 |
|
RU2633355C2 |
| АРИЛ-ЗАМЕЩЕННЫЕ КАРБОКСАМИДНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ БЛОКАТОРОВ КАЛЬЦИЕВЫХ ИЛИ НАТРИЕВЫХ КАНАЛОВ | 2010 |
|
RU2575168C2 |
| МОНОЦИКЛИЧЕСКОЕ ПИРИДИНОВОЕ ПРОИЗВОДНОЕ | 2014 |
|
RU2645352C2 |
| ПРОИЗВОДНЫЕ 4-АМИНОМЕТИЛБЕНЗОЙНОЙ КИСЛОТЫ | 2014 |
|
RU2673245C2 |
| ПРОИЗВОДНЫЕ АЦИЛБЕНЗОЛА | 2011 |
|
RU2585765C2 |
| АМИННОЕ СОЕДИНЕНИЕ И ЕГО ПРИМЕНЕНИЕ В МЕДИЦИНСКИХ ЦЕЛЯХ | 2006 |
|
RU2433117C2 |
| СОЕДИНЕНИЕ С-ФЕНИЛГЛИЦИТОЛА ДЛЯ ЛЕЧЕНИЯ ДИАБЕТА | 2007 |
|
RU2437876C2 |
| ПРОИЗВОДНОЕ ПИРАЗОЛА ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ | 2016 |
|
RU2687245C1 |
Изобретение относится к новому производному N-ацилантраниловой кислоты, представленному следующей общей формулой 1, или к его фармацевтически приемлемой соли, в которой R1, R2, R3, Х1, X2, X3, X4 и А определены в формуле изобретения. Изобретение также относится к ингибитору продукции коллагена, средству для лечения заболеваний, ассоциированных с избыточной продукцией коллагена, содержащим производное N-ацилантраниловой кислоты.
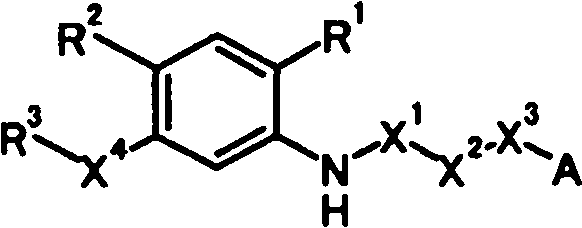
Формула 1
5 н. и 28 з.п. ф-лы, 34 табл.
1. Производное N-ацилантраниловой кислоты, представленное следующей общей формулой, или его фармацевтически приемлемая соль:
[Формула 1]

в которой
R1 представляет собой необязательно защищенную карбоксильную группу или 1Н-тетразол-5-ильную группу;
R2 представляет собой атом водорода, атом галогена, необязательно защищенную гидроксильную группу или алкоксигруппу;
R3 представляет собой необязательно замещенную арильную группу или необязательно замещенную гетероциклическую группу;
Х1 представляет собой карбонильную группу;
X2 представляет собой связь;
X3 представляет собой связь;
X4 представляет собой атом кислорода, иминогруппу, алкиленовую группу или связь; и
А представляет собой группу, представленную следующей общей формулой:
[Формула 2]
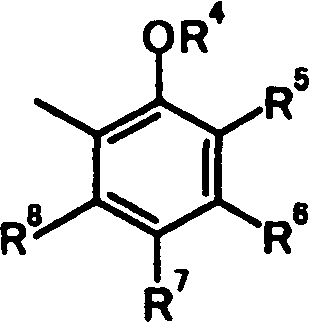
в которой
R4 представляет собой атом водорода или защитную группу фенольного гидроксила;
один из R5, R6, R7 и R8 представляет собой группу, представленную общей формулой -Y-R9,
в которой
R9 представляет собой атом галогена, нитрогруппу, необязательно защищенную гидроксильную группу, аминогруппу, алкиламиногруппу, необязательно замещенную диалкиламиногруппу, алкильную группу, алкоксигруппу, арильную группу, арилоксигруппу, необязательно замещенную гетероциклическую группу, необязательно замещенную гетероциклическую оксигруппу, ацильную группу или ацилоксигруппу;
Y представляет собой алкиленовую группу, связь, группу, представленную общей формулой -(CH2)m-O-(СН2)n-,
в которой m представляет собой целое число от 0 до 1; и n представляет собой целое число от 1 до 3, или общей формулой -(CH2)m-NR10-(CH2)n-,
в которой R10 представляет собой атом водорода или низшую алкильную группу; и m и n имеют те же определенные выше значения, и
каждый из оставшихся представляет собой атом водорода; или
каждый из R5 и R8 представляет собой атом водорода, и
каждый R6 и R7 вместе с атомами углерода, с которыми они связаны, представляют собой 5-7-членную гетероциклическую группу, или
группу, представленную следующей общей формулой:
[Формула 3]
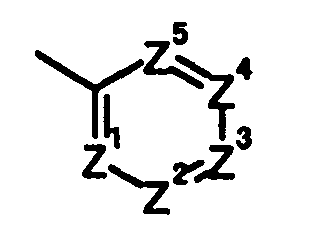
в которой
один из Z1, Z2, Z3, Z4 и Z5 представляет собой атом азота,
один из оставшихся четырех представляет собой группу, представленную общей формулой C-R11,
в которой R11 представляет собой необязательно замещенную арильную группу, азотсодержащую 6-членную ароматическую гетероциклическую группу или кислородсодержащую 5-членную ароматическую гетероциклическую группу,
каждый из оставшихся трех представляет собой группу, представленную общей формулой C-R12,
в которой R12 представляет собой атом водорода;
в которой заместители для арильной группы и гетероциклической группы R3 представляют собой один или несколько, выбранных из группы, состоящей из атома галогена, нитрогруппы, необязательно защищенных амино, алкиламино и гидроксильной групп, и алкильной, алкокси, алкиламино и диалкиламино групп, которые могут быть замещены одним или несколькими атомами галогена;
заместители для диалкиламиногруппы R9 представляют собой одну или несколько гидроксильных групп;
заместители для гетероциклической группы и гетероциклической оксигруппы R9 представляют собой один или несколько, выбранных из группы, состоящей из ацильной группы, алкилсульфонильной группы, оксогруппы, аминогруппы, гидроксильной группы, и алкильной, алкиламино и диалкиламиногрупп, которые могут быть замещены одной или несколькими гидроксильными группами;
заместители для арильной группы R11 представляют собой один или несколько, выбранных из группы, состоящей из атомов галогена;
карбоксилзащитная группа включает алкильную группу, арильную группу, аралкильную группу, ацилалкильную группу, арилтиоалкильную группу, арилсульфонилалкильную группу, кислородсодержащую гетероциклическую группу, алкилсилилалкильную группу, ацилоксиалкильную группу, азотсодержащую гетероциклическую алкильную группу, циклоалкильную группу, алкоксиалкильную группу, аралкилоксиалкильную группу, алкилтиоалкильную группу, алкенильную группу и замещенную силильную группу;
защитная группа фенольного гидроксила включает ацильную группу, алкильную группу, алкенильную группу, аралкильную группу, кислородсодержащую гетероциклическую группу, серосодержащую гетероциклическую группу, алкоксиалкильную группу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу;
аминозащитная группа включает ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, арилоксикарбонильную группу, аралкильную группу, алкоксиалкильную группу, аралкилоксиалкильную группу, арилтиогруппу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу;
и гидроксилзащитная группа включает ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, гетероциклическую оксикарбонильную группу, алкильную группу, алкенильную группу, аралкильную группу, кислородсодержащую гетероциклическую группу, серосодержащую гетероциклическую группу, алкоксиалкильную группу, аралкилоксиалкильную группу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу.
2. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по п.1, в котором А представляет собой группу, представленную следующей общей формулой:
[Формула 4]
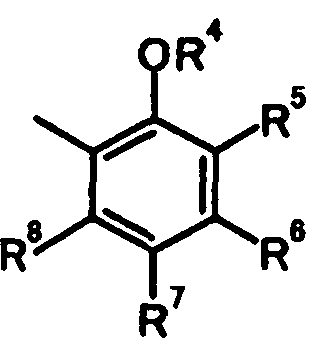
в которой
R4 представляет собой атом водорода или защитную группу фенольного гидроксила;
один из R5, R6, R7 и R8 представляет собой группу, представленную общей формулой -Y-R9,
в которой
R9 представляет собой атом галогена, нитрогруппу, необязательно защищенную гидроксильную группу, аминогруппу, алкиламиногруппу, необязательно замещенную диалкиламиногруппу, алкильную группу, алкоксигруппу, арильную группу, арилоксигруппу, необязательно замещенную гетероциклическую группу, необязательно замещенную гетероциклическую оксигруппу, ацильную группу или ацилоксигруппу;
Y представляет собой алкиленовую группу, связь, группу, представленную общей формулой -(СН2)m-O-(CH2)n-,
в которой m представляет собой целое число от 0 до 1; и n представляет собой целое число от 1 до 3, или
группу, представленную общей формулой -(СН2)m-NR10-(СН2)n-,
в которой R10 представляет собой атом водорода или низшую алкильную группу; и m и n имеют те же определенные выше значения, и
каждый из оставшихся представляет собой атом водорода; или
каждый из R5 и R8 представляет собой атом водорода, и
каждый R6 и R7 вместе с атомами углерода, с которыми они связаны, представляют собой 5-7-членную гетероциклическую группу;
в которой заместители для диалкиламиногруппы, гетероциклической группы и гетероциклической оксигруппы R9, защитная группа фенольного гидроксила и гидроксилзащитная группа определены в п.1.
3. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по п.2, в котором X4 представляет собой атом кислорода, иминогруппу или связь.
4. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по п.2 или 3, в котором R1 представляет собой необязательно защищенную карбоксильную группу;
в котором карбоксилзащитная группа определена в п.1.
5. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.2-3, в котором R2 представляет собой атом водорода или атом галогена.
6. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.2-3, в котором R3 представляет собой необязательно замещенную фенильную группу или фуранильную группу;
в котором заместители для фенильной группы R3 представляют собой один или несколько, выбранных из группы, состоящей из атома галогена, нитрогруппы, необязательно защищенных амино, алкиламино и гидроксильной групп, и алкильной, алкокси, алкиламино и диалкиламино групп, которые могут быть замещены одним или несколькими атомами галогена; и
аминозащитная группа и гидроксилзащитная группа определены в п.1.
7. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.2-3, в котором R4 представляет собой атом водорода.
8. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.2-3, в котором X4 представляет собой связь.
9. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.2-3, в котором
один из R5, R6, R7 и R8 представляет собой группу, представленную общей формулой -Ya-R9a,
в которой
R9a представляет собой атом галогена, нитрогруппу, необязательно защищенную гидроксильную группу, аминогруппу, алкиламиногруппу, необязательно замещенную диалкиламиногруппу, алкильную группу, алкоксигруппу, арильную группу, арилоксигруппу, необязательно замещенную гетероциклическую группу, необязательно замещенную гетероциклическую оксигруппу, ацильную группу или ацилоксигруппу; и
Ya представляет собой алкиленовую группу, связь, группу, представленную общей формулой -O-(СН2)n-,
в которой n представляет собой целое число от 1 до 3, или группу, представленную общей формулой NR10a-(СН2)n-,
в которой R10a представляет собой низшую алкильную группу; и n имеет те же значения, что и указанные выше, и
каждый из других оставшихся представляет собой атом водорода;
в котором заместители для диалкиламиногруппы R9a представляют собой одну или несколько гидроксильных групп;
заместители для гетероциклической группы и гетероциклической оксигруппы R9a представляют собой один или несколько, выбранных из группы, состоящей из ацильной группы, алкилсульфонильной группы, оксогруппы, аминогруппы, гидроксильной группы, и алкильной, алкиламино и диалкиламиногрупп, которые могут быть замещены одной или несколькими гидроксильными группами;
и гидроксилзащитная группа определена в п.1.
10. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.2-3, в котором
каждый R5, R6 и R8 представляет собой атом водорода, и
R7 представляет собой группу, представленную общей формулой -Yb-R9b,
в которой
R9b представляет собой необязательно замещенную гетероциклическую группу; и
Yb представляет собой алкиленовую группу, связь или группу, представленную общей формулой -O-(СН2)n-,
в которой n представляет собой целое число от 1 до 3;
в котором заместители для гетероциклической группы R9b представляют собой один или несколько, выбранных из группы, состоящей из ацильной группы, алкилсульфонильной группы, оксогруппы, аминогруппы, гидроксильной группы, и алкильной, алкиламино и диалкиламиногрупп, которые могут быть замещены одной или несколькими гидроксильными группами.
11. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.2-3, в котором
каждый R5, R6 и R8 представляет собой атом водорода, и
R7 представляет собой группу, представленную общей формулой -Yc-R9c,
в которой
R9c представляет собой гетероциклическую группу, которая может быть замещена низшей алкильной группой; и
Yc представляет собой метиленовую группу, связь или группу, представленную общей формулой -O-(СН2)2-.
12. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по п.1, в котором А представляет собой группу, представленную следующей общей формулой:
[Формула 5]
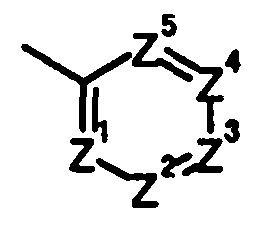
в которой
один из Z1, Z2, Z3, Z4 и Z5 представляет собой атом азота,
один из оставшихся четырех представляет собой группу, представленную общей формулой C-R11,
в которой R11 представляет собой необязательно замещенную арильную группу, азотсодержащую 6-членную ароматическую гетероциклическую группу или кислородсодержащую 5-членную ароматическую гетероциклическую группу, и
каждый из оставшихся трех представляет собой группу, представленную общей формулой C-R12,
в которой R12 представляет собой атом водорода;
в которой заместители для арильной группы R11 определены в п.1.
13. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по п.12, в котором X4 представляет собой атом кислорода, иминогруппу или связь.
14. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по п.12 или 13, в котором R1 представляет собой необязательно защищенную карбоксильную группу;
в котором карбоксилзащитная группа определена в п.1.
15. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.12-13, в котором R2 представляет собой атом водорода или атом галогена.
16. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по п.12, в котором X4 представляет собой связь.
17. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.12, 13 или 16, в котором R3 представляет собой необязательно замещенную фенильную группу или фуранильную группу;
в котором заместители для фенильной группы R3 представляют собой один или несколько, выбранных из группы, состоящей из атома галогена, нитрогруппы, необязательно защищенных амино, алкиламино и гидроксильной групп, и алкильной, алкокси, алкиламино и диалкиламино групп, которые могут быть замещены одним или несколькими атомами галогена; и
аминозащитная группа и гидроксилзащитная группа определены в п.1.
18. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.12, 13 или 16, в котором
Z1 представляет собой СН,
Z2 представляет собой атом азота,
Z3 представляет собой СН,
Z4 представляет собой группу, представленную общей формулой C-R11a,
в которой R11a представляет собой необязательно замещенную арильную группу, азотсодержащую 6-членную ароматическую гетероциклическую группу или кислородсодержащую 5-членную ароматическую гетероциклическую группу, и
Z5 представляет собой СН;
в котором заместители для арильной группы R11a представляют собой один или несколько атомов галогена.
19. Производное N-ацилантраниловой кислоты или его фармацевтически приемлемая соль по любому из пп.12, 13 или 16, в котором
Z1 представляет собой СН,
Z2 представляет собой атом азота,
Z3 представляет собой СН,
Z4 представляет собой C-C6H5, и
Z5 представляет собой СН.
20. Ингибитор продукции коллагена, содержащий производное N-ацилантраниловой кислоты, представленное следующей общей формулой, или его фармацевтически приемлемую соль, и носитель или эксципиент:
[Формула 6]
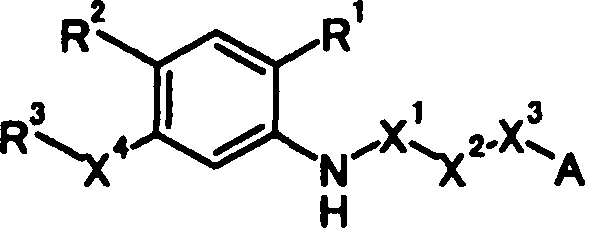
в которой
R1 представляет собой необязательно защищенную карбоксильную группу или 1H-тетразол-5-ильную группу;
R2 представляет собой атом водорода, атом галогена, необязательно защищенную гидроксильную группу или алкоксигруппу;
R3 представляет собой необязательно замещенную арильную группу или необязательно замещенную гетероциклическую группу;
Х1 представляет собой карбонильную группу;
X2 представляет собой необязательно замещенную алкиленовую группу, алкениленовую группу или связь;
X3 представляет собой связь;
X4 представляет собой группу, представленную общей формулой -Х5-Х6- или -Х6-Х5- (при условии, что связь с левой стороны каждой общей формулы связана с R3), в которой
X5 представляет собой атом кислорода, иминогруппу или связь; и
X6 представляет собой алкиленовую группу или связь; и
А представляет собой необязательно замещенную фенильную группу или необязательно замещенную гетероциклическую группу;
в которой заместители для арильной группы и гетероциклической группы R3 представляют собой один или несколько, выбранных из группы, состоящей из атома галогена, нитрогруппы, необязательно защищенных амино, алкиламино и гидроксильной групп, и алкила, алкокси, алкиламино, диалкиламино, циклической амино и гетероциклической групп, которые могут быть замещены одним или несколькими атомами галогена;
заместители для алкиленовых групп X2 представляют собой одну или несколько фенильных групп;
заместители для фенильной группы и гетероциклической группы А представляют собой один или несколько, выбранных из группы, состоящей из атома галогена, нитрогруппы, необязательно замещенных амино и гидроксильных групп, и необязательно замещенных алкильной, алкокси, фенильной, циклической амино и гетероциклической групп;
карбоксилзащитная группа включает алкильную группу, арильную группу, аралкильную группу, ацилалкильную группу, арилтиоалкильную группу, арилсульфонилалкильную группу, кислородсодержащую гетероциклическую группу, алкилсилилалкильную группу, ацилоксиалкильную группу, азотсодержащую гетероциклическую алкильную группу, циклоалкильную группу, алкоксиалкильную группу, аралкилоксиалкильную группу, алкилтиоалкильную группу, алкенильную группу и замещенную силильную группу;
защитная группа фенольного гидроксила включает ацильную группу, алкильную группу, алкенильную группу, аралкильную группу, кислородсодержащую гетероциклическую группу, серосодержащую гетероциклическую группу, алкоксиалкильную группу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу;
аминозащитная группа включает ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, арилоксикарбонильную группу, аралкильную группу, алкоксиалкильную группу, аралкилоксиалкильную группу, арилтиогруппу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу;
и гидроксилзащитная группа включает ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, гетероциклическую оксикарбонильную группу, алкильную группу, алкенильную группу, аралкильную группу, кислородсодержащую гетероциклическую группу, серосодержащую гетероциклическую группу, алкоксиалкильную группу, аралкилоксиалкильную группу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу.
21. Ингибитор продукции коллагена по п.20, в котором
R1 представляет собой необязательно защищенную карбоксильную группу,
R2 представляет собой атом водорода, и
R3 представляет собой необязательно замещенную фенильную группу, необязательно замещенную моноциклическую гетероциклическую группу или бициклическую гетероциклическую группу;
в котором заместители для фенильной группы и моноциклической гетероциклической группы R3 представляют собой один или несколько, выбранных из группы, состоящей из атома галогена, нитрогруппы, необязательно защищенных амино, алкиламино и гидроксильной групп, и алкила, алкокси, алкиламино, диалкиламино, циклической амино и гетероциклической групп, которые могут быть замещены одним или несколькими атомами галогена.
22. Ингибитор продукции коллагена по любому из пп.20 или 21, в котором X4 представляет собой атом кислорода, алкиленовую группу или связь.
23. Ингибитор продукции коллагена по любому из пп.20 или 21, в котором
А представляет собой необязательно замещенную фенильную группу или необязательно замещенную гетероциклическую группу, и
R3 представляет собой необязательно замещенную фенильную группу или бициклическую гетероциклическую группу;
в котором заместители для фенильной группы и гетероциклической группы А определены в п.20; и заместители для фенильной группы R3 определены в п.21.
24. Ингибитор продукции коллагена по п.23, в котором
X2 представляет собой связь,
X3 представляет собой связь, и
X4 представляет собой связь.
25. Ингибитор продукции коллагена по п.24, в котором
А представляет собой необязательно замещенную фенильную группу или необязательно замещенную пиридильную группу, и
R3 представляет собой необязательно замещенную фенильную группу;
в котором заместители для пиридильной группы А представляют собой одну или несколько групп, выбранных из фенильной, циклической амино и гетероциклической групп, которые могут быть замещены одним или несколькими атомами галогена;
заместители для фенильной группы А определены в п.20;
и заместители для фенильной группы R3 определены в п.21.
26. Средство для лечения заболеваний, ассоциированных с избыточной продукцией коллагена, содержащее производное N-ацилантраниловой кислоты, представленное следующей общей формулой, или его фармацевтически приемлемую соль, и носитель или эксципиент:
[Формула 7]
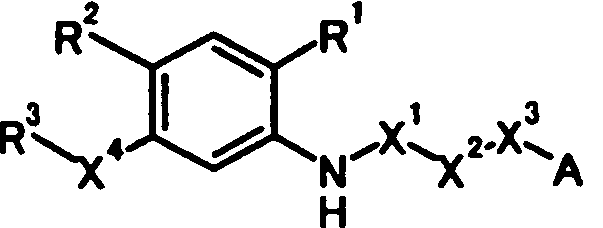
в которой
R1 представляет собой необязательно защищенную карбоксильную группу или 1H-тетразол-5-ильную группу;
R2 представляет собой атом водорода, атом галогена, необязательно защищенную гидроксильную группу или алкоксигруппу;
R3 представляет собой необязательно замещенную арильную группу или необязательно замещенную гетероциклическую группу;
X1 представляет собой карбонильную группу;
X2 представляет собой необязательно замещенную алкиленовую группу, алкениленовую группу или связь;
X3 представляет собой связь;
X4 представляет собой группу, представленную общей формулой -X5-X6- или -Х6-Х5- (при условии, что связь с левой стороны каждой общей формулы связана с R3), в которой
X5 представляет собой атом кислорода, иминогруппу или связь; и
X6 представляет собой алкиленовую группу или связь; и
А представляет собой необязательно замещенную фенильную группу или необязательно замещенную гетероциклическую группу;
в которой заместители для арильной группы и гетероциклической группы R3 представляют собой один или несколько, выбранных из группы, состоящей из атома галогена, нитрогруппы, необязательно замещенных амино, алкиламино и гидроксильной групп, и алкила, алкокси, алкиламино, диалкиламино, циклической амино и гетероциклической групп, которые могут быть замещены одним или несколькими атомами галогена;
заместители для алкиленовых групп X2 представляют собой одну или несколько фенильных групп;
заместители для фенильной группы и гетероциклической группы А представляют собой один или несколько, выбранных из группы, состоящей из атома галогена, нитрогруппы, необязательно замещенных амино и гидроксильных групп, и необязательно замещенных алкильной, алкокси, фенильной, циклической амино и гетероциклической групп;
карбоксилзащитная группа включает алкильную группу, арильную группу, аралкильную группу, ацилалкильную группу, арилтиоалкильную группу, арилсульфонилалкильную группу, кислородсодержащую гетероциклическую группу, алкилсилилалкильную группу, ацилоксиалкильную группу, азотсодержащую гетероциклическую алкильную группу, циклоалкильную группу, алкоксиалкильную группу, аралкилоксиалкильную группу, алкилтиоалкильную группу, алкенильную группу и замещенную силильную группу;
защитная группа фенольного гидроксила включает ацильную группу, алкильную группу, алкенильную группу, аралкильную группу, кислородсодержащую гетероциклическую группу, серосодержащую гетероциклическую группу, алкоксиалкильную группу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу;
аминозащитная группа включает ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, арилоксикарбонильную группу, аралкильную группу, алкоксиалкильную группу, аралкилоксиалкильную группу, арилтиогруппу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу;
и гидроксилзащитная группа включает ацильную группу, алкилоксикарбонильную группу, аралкилоксикарбонильную группу, гетероциклическую оксикарбонильную группу, алкильную группу, алкенильную группу, аралкильную группу, кислородсодержащую гетероциклическую группу, серосодержащую гетероциклическую группу, алкоксиалкильную группу, аралкилоксиалкильную группу, алкилсульфонильную группу, арилсульфонильную группу и замещенную силильную группу.
27. Средство для лечения заболеваний, ассоциированных с избыточной продукцией коллагена, по п.26, в котором
R1 представляет собой необязательно защищенную карбоксильную группу,
R2 представляет собой атом водорода, и
R3 представляет собой необязательно замещенную фенильную группу, необязательно замещенную моноциклическую гетероциклическую группу или бициклическую гетероциклическую группу;
в котором заместители для фенильной группы и моноциклической гетероциклической группы R3 представляют собой один или несколько, выбранных из группы, состоящей из атома галогена, нитрогруппы, необязательно замещенных амино, алкиламино и гидроксильной групп, и алкила, алкокси, алкиламино, диалкиламино, циклической амино и гетероциклической групп, которые могут быть замещены одним или несколькими атомами галогена.
28. Средство для лечения заболеваний, ассоциированных с избыточной продукцией коллагена, по любому из пп.26 или 27, в котором X4 представляет собой атом кислорода, алкиленовую группу или связь.
29. Средство для лечения заболеваний, ассоциированных с избыточной продукцией коллагена, по любому из пп.26 или 27, в котором
А представляет собой необязательно замещенную фенильную группу или необязательно замещенную гетероциклическую группу, и
R3 представляет собой необязательно замещенную фенильную группу или бициклическую гетероциклическую группу;
в котором заместители для фенильной группы и гетероциклической группы А определены в п.26; и заместители для фенильной группы R3 определены в п.27.
30. Средство для лечения заболеваний, ассоциированных с избыточной продукцией коллагена, по п.29, в котором
X2 представляет собой связь,
X3 представляет собой связь, и
X4 представляет собой связь.
31. Средство для лечения заболеваний, ассоциированных с избыточной продукцией коллагена, по п.30, в котором
А представляет собой необязательно замещенную фенильную группу или необязательно замещенную пиридильную группу, и
R3 представляет собой необязательно замещенную фенильную группу;
в котором заместители для пиридильной группы А представляют собой одну или несколько групп, выбранных из фенильной, циклической амино и гетероциклической групп, которые могут быть замещены одним или несколькими атомами галогена;
заместители для фенильной группы А определены в п.26;
и заместители для фенильной группы R3 определены в п.27.
32. Ингибитор продукции коллагена, содержащий производное N-ацилантраниловой кислоты или его фармацевтически приемлемую соль по любому из пп.1, 2, 3, 12, 13 или 16, и носитель или эксципиент.
33. Средство для лечения заболеваний, ассоциированных с избыточной продукцией коллагена, содержащее производное N-ацилантраниловой кислоты или его фармацевтически приемлемую соль по любому из пп.1, 2, 3, 12, 13 или 16, и носитель или эксципиент.
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Способ приготовления мыла | 1923 |
|
SU2004A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| RU 2006124794 A, 20.01.2008 | |||
Авторы
Даты
2014-10-10—Публикация
2010-01-29—Подача