Изобретение относится к области медицины и ветеринарии, в частности фармакологии и онкологии, и может быть использовано для торможения развития опухолей эпителиального происхождения (карцином), в частности карциномы Эрлиха.
В экспериментальной и клинической фармакологии достаточно широко используются противоопухолевые средства, относящиеся к разным химическим классам и типу действия. Наиболее часто с этой целью используют цитостатики, антиметаболиты, специальные антибиотики, цисплатин и гормональные средства [Руководство по химиотерапии опухолевых заболеваний. 2012. Практическая медицина. Под ред. Н.И.Переводчиковой].
Эффект этих веществ на опухолевый процесс определяется токсическим действием на митотическую активность клеток, в том числе опухолевых [Рак и его лечение. 2009. Бином. Лаборатория знаний. Соухами Р., Тобайс Дж.].
Для вторичной профилактики опухолевого роста (метастазирования) используют также стимуляторы иммунитета (интерлейкины, интерфероны) [Цитокины в терапии рака. В журнале «Цитокины и воспаление», Т.1, №3, 2002. С.27-30].
В последнее десятилетие в экспериментальной онкологии получило развитие новое направление профилактики и терапии опухолевых заболеваний. Оно основано на использовании природных и химически синтезированных М- и Н-холиноблокаторов, модулирующих функциональную активность холинергической системы млекопитающих [Neurotransmission and cancer: implications for prevention and therapy. // Anti-Cancer Drugs. 2008. Vol.19, p.655-671]. В работах этого направления установлено, что холиноблокаторы снижают митотическую активность нормальных и опухолевых клеток, подавляют ангиогенез и репаративные процессы в тканях. При всех достижениях, полученных в этих исследованиях, существенным ограничением для использования изученных холиноблокаторов в терапии онкозаболеваний является их высокая токсичность.
В отечественной фармакологии описана группа низкотоксичных соединений - производных диэтиламиноалкиловых эфиров бензиловой и дифенилуксусной кислот, которые обладают антигельминтным, спазмолитическим и холиноблокирующим действием (Патент РФ №2015696 от 15.07.94 г., Бюл. №13). Из изученных эффектов их влияния на организм не вытекает возможность оказывать какое-либо действие на опухолевый процесс.
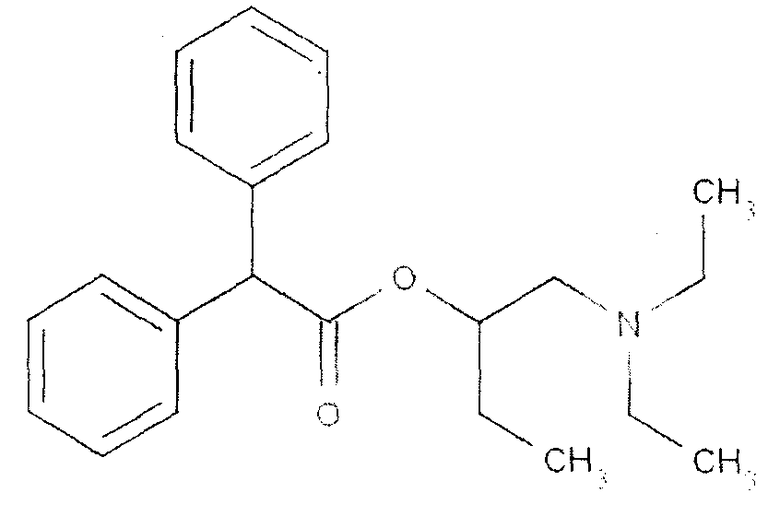
Химическая структура бета-этилдифацила
Задачей изобретения было изучение влияния использования Н-холиноблокатора - бета-этилдифацила (CAS 13426-07-8) в качестве средства торможения развития опухоли на экспериментальных моделях перевиваемых опухолей. Задача изобретения была достигнута установлением необходимых доз и режима применения бета-этилдифацила: в дозе 15-50 мг/кг, вводимого внутрибрюшинно бета-этилдифацила, начиная "до" или непосредственно "после" перевивания опухоли, препарат оказывает необходимое действие, то есть тормозит опухолевый процесс.
Биологические исследования
Для изучения действия заявляемого препарата в качестве экспериментальных животных-млекопитающих выбраны мыши. В качестве модели опухолевого процесса использовали опухоль - карциному Эрлиха, поддерживаемую в брюшной полости мышей-самцов гибридах первого поколения (СВА×С57В16) F1. В качестве перевиваемого материала использовали внутрибрюшинную перитонеальную жидкость с клетками (асцитная жидкость). Жидкость забирали не ранее, чем через 10-12 дней после очередной перевивки. Клетки, полученные из асцитной жидкости, осаждали мягким центрифугированием (400 g 5 мин), дважды промывали забуференным физиологическим раствором, после чего формировали сток-суспензию опухолевых клеток в физиологическом растворе в концентрации 106 (1 млн) клеток в 1 мл. Сток-суспензию в количестве 200 тыс. клеток в объеме 0,2 мл вводили мышам самцам массой 20-22 г подкожно в межлопаточную область. У мышей-реципиентов начинался рост опухоли, однозначно определяемый на 10-12 день после перевивки. Если не было фармакологического вмешательства, мыши с опухолью жили в среднем 40 дней после перевивки. При этом у них регистрировали типичный объемный процесс в межлопаточной области, динамично увеличивающуюся в объеме опухоль вплоть до смерти животного, сопровождающуюся асцитом и резким снижением основной массы тела, а также явно сниженным аппетитом.
В опыт включали 100 мышей-самцов (СВА×С57В16) F1 массой 20-22 г. В контрольной группе на 40,8±4,0-й день после перевивки опухоли погибли 100% мышей (n=20). При этом у них регистрировали все проявления опухолевого процесса (локальный рост опухоли, асцит, резкое снижение основной массы тела, резкая гиподинамия).
В группе мышей, которая получала бета-этилдифацил, 30 мг/кг внутрибрюшинно, курсом с интервалом 6-7 дней между введениями, начиная непосредственно после перевивки опухоли (не позже 24 ч), на 30-й день опыта регистрировали гибель только 20% мышей (n=20, р<0,02) с типичными признаками опухолевого процесса.
У остальных мышей динамика опухолевого роста была существенно замедлена, асцит практически не определялся, у животных сохранялись высокий аппетит и подвижность. У части мышей наблюдали некротизацию поверхности над опухолью с последующей быстрой эпителизацией (в течение 1-2 суток) и уменьшение объема опухоли. В дальнейшем оставшиеся в живых мыши опытной группы жили более 40 дней (в среднем 51,5±4,5 дней, хотя последняя мышь умерла на 78-й день после перевивки опухоли).
Аналогичные результаты были получены при профилактическом одноразовом введении бета-этилдифацила: 30 мг/кг до перевивки опухоли (за 2-24 ч) с последующим курсовым (1 раз в неделю) введением препарата.
Были поставлены дополнительные опыты, проведенные с использованием ряда холиноблокаторов (М-холиноблокаторы - метамизил, метацин; Н холиноблокатор - бензогесконий), с целью установления их влияния на опухолевый процесс.
Важно отметить, что другие холиноблокаторы (метамизил 2,5 мг/кг, n=20; метацин 2,5 мг/кг, n=20) потенцировали или не влияли (бензогексоний 50 мг/кг, n=20) на развитие опухолевого процесса (табл.1), при этом смертность мышей от опухолей наблюдали в более ранние сроки (как правило, до 20-го дня) в сравнении с контролем (введение физиологического раствора).
Таким образом, применение бета-этилдифацила, вводимого внутрибрюшинно, начиная на следующий день после перевивания опухоли, способствует торможению развития опухолевого процесса в модели перевиваемой карциномы Эрлиха у млекопитающих - мышей.
Аналогично ведут себя мыши в опыте при введении препарата "до" перевивания опухоли, то есть при профилактическом введении. Причем это введение осуществляют за 2-24 ч "до". Интерполируя срок продления жизни мышей на среднюю продолжительность их жизни, видно, что этот срок увеличивается на 30% при использовании заявляемого препарата. Причем наблюдения за состоянием и поведением экспериментальных мышей свидетельствуют, что их жизнь не отягощена прогрессией основной болезни. Эти экспериментальные данные дают основания предполагать, что в будущем возможно использование бета-этилдифацила в медицинской практике для торможения развития опухолей у людей, протекающего на фоне удовлетворительного качества жизни, и животных - в ветлечебницах.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ И АНАЛЬГЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 1996 |
|
RU2121839C1 |
| 2-/3-(2-ХЛОРЭТИЛ)-3-НИТРОЗОУРЕИДО/-1,3-ПРОПАНДИОЛ, ОБЛАДАЮЩИЙ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2068843C1 |
| ПРИМЕНЕНИЕ СОЕДИНЕНИЯ 2-[3-(2-ХЛОРЭТИЛ)-3-НИТРОЗОУРЕИДО]-1,3-ПРОПАНДИОЛ ДЛЯ ЛЕЧЕНИЯ КАРЦИНОМЫ ЭРЛИХА, САРКОМЫ 37, ЛИМФОСАРКОМЫ ЛИО-1, МЕЛАНОМЫ В16, ТРАНСПЛАНТИРОВАННЫХ В НИЖНЕЕ ВЕКО МЫШЕЙ В ЭКСПЕРИМЕНТЕ | 2020 |
|
RU2752083C1 |
| СРЕДСТВО ДЛЯ КОРРЕКЦИИ ЦИТОТОКСИЧЕСКИХ ЭФФЕКТОВ ПАРАНЕОПЛАСТИЧЕСКИХ ПРОЦЕССОВ И ХИМИОТЕРАПИИ, ОБЛАДАЮЩЕЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2447888C1 |
| СПОСОБ ФОТОДИНАМИЧЕСКОЙ ОБРАБОТКИ ОПУХОЛЕВЫХ КЛЕТОК ДЛЯ ПРИГОТОВЛЕНИЯ КЛЕТОЧНЫХ ПРЕПАРАТОВ | 2021 |
|
RU2775382C1 |
| СПОСОБ ЛЕЧЕНИЯ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2006 |
|
RU2320364C1 |
| Способ модификации развития аденокарциномы в эксперименте | 2020 |
|
RU2743960C1 |
| ПРИМЕНЕНИЕ СОЕДИНЕНИЯ 2-[3-(2-ХЛОРЭТИЛ)-3-НИТРОЗОУРЕИДО]-1,3-ПРОПАНДИОЛ ПРИ ЛЕЧЕНИИ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ ГЛАЗНИЦЫ В ЭКСПЕРИМЕНТЕ У МЫШЕЙ С ТРАНСПЛАНТИРОВАННОЙ ВНУТРИГЛАЗНИЧНО КАРЦИНОМОЙ ЭРЛИХА | 2023 |
|
RU2815639C1 |
| СПОСОБ ЛЕЧЕНИЯ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ | 2004 |
|
RU2269356C2 |
| Производное класса N-гликозидов индоло[2,3-а]пирроло[3,4-с]карбазол-5,7-дионов - N-{ 12-(β-D-ксилопиранозил)-5,7-диоксо-индоло[2,3-а]пирроло[3,4-с] карбазол-6-ил} пиридин-2-карбоксамид, обладающее цитотоксической и противоопухолевой активностью | 2017 |
|
RU2667906C1 |
Изобретение относится к фармакологии и онкологии, в частности к новому противоопухолевому средству. В качестве средства для торможения развития опухолей эпителиального происхождения (карцином) предложено применение бета-этилдифацила. Этилдифацил предлагается вводить в дозах 15-50 мг/кг как "до", так и "после" перевивки опухоли, курс лечения до 2 месяцев после перевивки опухоли с интервалом между введениями 6-7 дней, или для профилактического введения за 2-24 ч "до" перевивания опухоли. Технический результат состоит в продлении срока жизни млекопитающих с карциномой на 30%, причем эта жизнь не отягощена прогрессией основной болезни. 3 з.п. ф-лы, 1 табл.
1. Применение бета-этилдифацила в качестве средства для торможения развития карциномы Эрлиха - опухоли эпителиального происхождения.
2. Применение бета-этилдифацила по п.1, отличающееся тем, что препарат применяют в дозах 15-50 мг на кг веса млекопитающего.
3. Применение бета-этилдифацила по п.2, отличающееся тем, что интервал между введениями препарата составляет 6-7 дней.
4. Применение бета-этилдифацила по п.3, отличающееся тем, что курс лечения составляет от 2 до 60 дней после перевивки опухоли.
| CN101230015 A 30.07.2008 | |||
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ГЕЛЬМИНТОЗОВ | 1992 |
|
RU2015696C1 |
| КОНДРАТЕНКОВА Е.А | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| TKACHYENKO EI | |||
| [Effect of M- and N-cholinoblockers on excitability | |||
Авторы
Даты
2015-01-10—Публикация
2012-09-28—Подача