Изобретение относится к химико-фармацевтической промышленности и может быть использовано для стандартизации надземной части первоцвета весеннего (лекарственного) (Primula veris L., или Primula officinalis (L.) Hill.), используемого в качестве лекарственного поливитаминного и пищевого растительного сырья.
Первоцвет весенний используется в медицинской практике благодаря следующим фармакологическим свойствам: отхаркивающее, потогонное, мочегонное, спазмолитическое, седативное, противовоспалительное. Отмечена высокая антимикробная активность препаратов из первоцвета. Растение является богатым источником поливитаминов [В.К. Лавренов, Г.В. Лавренова. Важнейшие лекарственные растения. - Донецк: «Сталкер», 2004, с.324-325].
Согласно литературным данным листья первоцвета весеннего (лекарственного) (Primula veris L., или Primula officinalis (L.) Hill.) содержат витамин С, соединения фенольной природы: арбутин, умбеллиферон, галловая, хлорогеновая, кофейная, цикориевая, феруловая, коричная кислоты, рутин, апигенин, лютеолин-7-гликозид, дигидрокверцетин, витексин, байкалин; кемпферола дирамнозид, мирицетин, кверцетин, кемпферол. Антоцианы в гидролизате: дельфинидин, цианидин, тритерпеновые сапонины и др. биологически активные вещества (БАВ) [Романова З.Р. Фармакогностическое исследование первоцвета весеннего и первоцвета крупночашечного: автореф. дис. … канд. фарм. наук: (14.00.02) / З.Р. Романова; Башкирский гос. медицинский ун-т. - Курск, 2011. - 22 с.]. Цветки содержат эфирное масло, в его составе: 5-метоксиметилсалицилат, 4-метоксиметилсалицилат, примверин, примулаверин, витамин С. Флавоноиды: дирамнозид кемпферола (примулафлавонолозид), 3-генциобиозид кверцетина, метиловый эфир кверцетагетингликозида.
В зарубежной практике разрешены к применению иные виды первоцвета (первоцвет весенний, высокий и настоящий). В РФ разрешен к применению первоцвет весенний (лекарственный) (Primula veris L., или P. officinalis (L.) Hill.).
Существующая в РФ отечественная нормативная документация (НД) на первоцвет весенний по ГОСТ 3166-76 «Листья первоцвета весеннего (ангро), цельное сырье, поставляемое на экспорт» для его стандартизации предусматривает определение кислоты аскорбиновой. Стандартизация корневищ с корнями первоцвета весеннего (Primula veris или Primula elatior) согласно Европейской Фармакопее проводится по содержанию тритерпенового сапонина эсцина [European Pharmacopeia, 7th edition, 2010]. Кислота аскорбиновая и эсцин не являются специфическими соединениями для растений рода первоцвет.
Для стандартизации травы первоцвета весеннего известно количественное определение сапонинов в пересчете на эсцин [Борисова Д.С. Сравнительное исследование химического состава цветков, листьев и корневищ с корнями первоцвета лекарственного с целью контроля качества и стандартизации сырья: автореф. дис. … канд. фарм. наук: (14.00.02) / Д.С. Борисова; Первый Московский государственный медицинский университет им. И.М. Сеченова. - Курск, 2013. - 25 с.].
Наиболее близким аналогом изобретения является способ стандартизации травы первоцвета весеннего путем количественного определения суммы флавоноидов в пересчете на рутин [Романова З.Р. Фармакогностическое исследование первоцвета весеннего и первоцвета крупночашечного: автореф. дис. … канд. фарм. наук: (14.00.02) / З.Р. Романова; Башкирский гос. медицинский ун-т. - Курск, 2011. - 22 с.].
Однако эти вещества не являются специфическими для первоцвета весеннего.
Известно, что вещество рутин, относящееся к флавоноидам, широко распространено в природе и является маркером для стандартизации многих видов лекарственного растительного сырья; вещество эсцин, относящееся к сапонинам, также широко распространено в природе и используется для стандартизации сапонинсодержащих растений, например, конского каштана, листьев винограда и препаратов на их основе; кислота аскорбиновая используется для стандартизации плодов шиповника и др. витаминсодержащих растений.
Задачей изобретения является получение нового специфического маркера для стандартизации надземной части первоцвета весеннего (лекарственного) (Primula veris L., или Primula officinalis (L.) Hill.).
Технический результат при использовании изобретения - повышение специфичности стандартизации надземной части первоцвета весеннего (лекарственного).
Сущность изобретения: применение 3′,4′-метилендиокси-5′-метоксифлавона формулы:
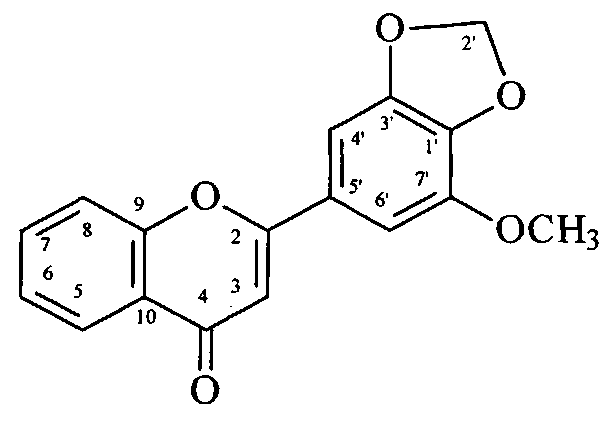
выделенного из травы первоцвета весеннего, в качестве специфического маркера для стандартизации надземной части первоцвета весеннего (лекарственного) (Primula veris L., или Primula officinalis (L.) Hill.)..
Выделение специфического маркера из травы первоцвета весеннего проводили совместно с кафедрой фармакогнозии ГБОУ ВПО «Самарский государственный медицинский университет», идентификацию выделенных веществ проводили на базе Института органической химии Уфимского научного центра РАН.
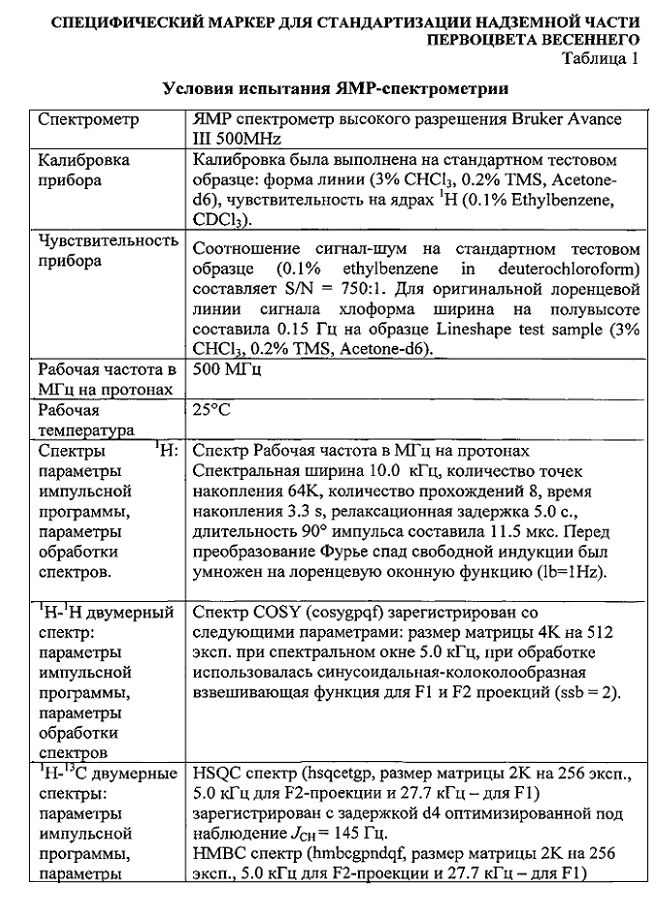
Препаративное разделение экстрактивных веществ осуществляли методом адсорбционной колоночной хроматографии. В качестве сорбентов был использован силикагель L 40/100 мкм (Wolem). Идентификацию выделенных веществ проводили методами УФ-, ЯМР1Н-, ЯМР13С - спектроскопии, условия испытания представлены в таблице 1.
МЕТОДИКА ВЫДЕЛЕНИЯ И ИДЕНТИФИКАЦИИ СПЕЦИФИЧЕСКОГО МАРКЕРА ИЗ ТРАВЫ ПЕРВОЦВЕТА ВЕСЕННЕГО
Соединение 3′,4′-метилендиокси-5′-метоксифлавон впервые выделено из травы первоцвета весеннего флоры европейской части РФ с использованием колоночной хроматографии на силикагеле.
Для препаративного выделения основных групп биологически активных веществ (БАВ) использовали сухое растительное сырье, измельченное до частиц размером 1-3 мм. Вещества экстрагировали спиртом этиловым различных концентраций. Извлечения концентрировали, очищали, вещества разделяли фракционированием по растворимости методом колоночной хроматографии. В качестве сорбентов был использован силикагель L 40/100 мкм (Wolem).
Для выделения БАВ сырье травы первоцвета весеннего, измельченного до размеров частиц, проходящих сквозь сито с отверстиями 3 мм (150,0 г), экстрагировали 70% раствором спирта этилового в соотношении 1:10 методом настаивания. Для очистки исследуемого извлечения от липофильных веществ полученный экстракт выдерживали в холодильнике в течение суток, образовавшийся осадок отфильтровывали. Полученное извлечение упаривали на вакуумном испарителе при температуре 40-60°С до получения густого остатка (около 50 мл). Сгущенное извлечение высушивали на силикагеле L 40/100 (50 г) и полученный порошок (извлечение + силикагель) наносили на слой силикагеля, сформированный в виде взвеси в хлороформе, и помещенный в хроматографическую колонку (высота сорбента - 3 см, диаметр - 5 см).
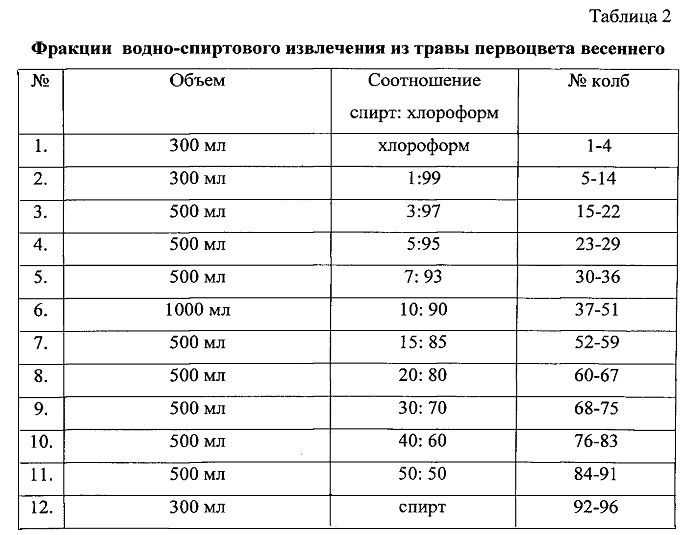
Элюирование колонки осуществляли в ступенчатом режиме хлороформом, а также хлороформом, содержащим в различных концентрациях спирт этиловый (1%, 3%, 5%, 7%, 10%, 15%, 20%, 30%, 40%, 50% и 96%). Дальнейшую очистку фракций проводили на микроколонках с силикагелем L 40/10, полиамидом и окисью алюминия. Процесс разделения полученных фракций веществ контролировали методом тонкослойной хроматографии (ТСХ) с использованием различных способов детекции. Для проведения ТСХ были использованы следующие системы: бутанол : уксусная кислота : вода (БУВ) 4:1:2; хлороформ : спирт этиловый : вода 26:16:3, наиболее оптимальной оказалась система БУВ 4:1:2. Результаты представлены в таблице 2.
Для установления структуры выделенных веществ использованы данные УФ-, ЯМР1Н-, ЯМР13С-спектроскопии.
Блок фракций (№8-11, элюент - спирт : хлороформ в соотношении 1:99), представлял собой густые маслянистые жидкости от желто-зеленого до темно-зеленого цветов. Полученные вещества в небольшом количестве элюента переносили по отдельности в хроматографическую колонку (сорбент - полиамид, высота сорбента - 3,0 см, диаметр - 5 см). Колонку элюировали хлороформом и смесью спирта этилового-хлороформа в различных соотношениях и спиртом этиловым. В результате было выделено вещество I, представляющее собой густую маслянистую жидкость темно-зеленого цвета.
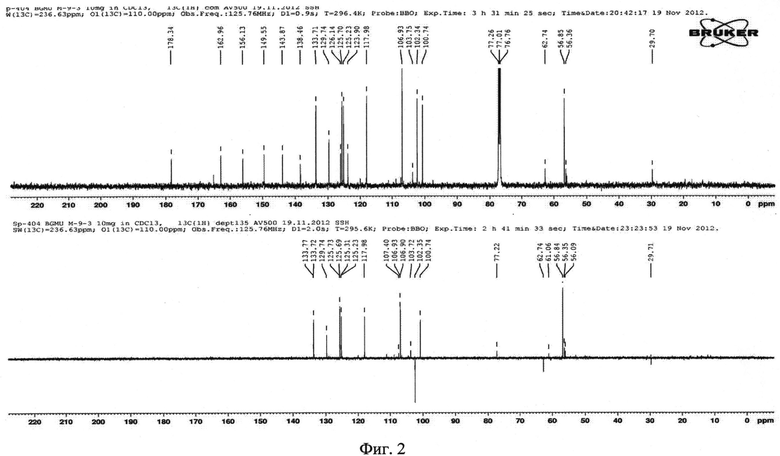
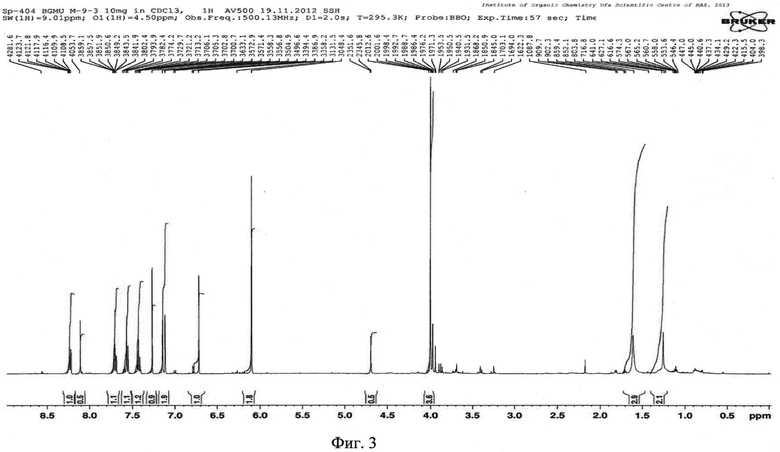
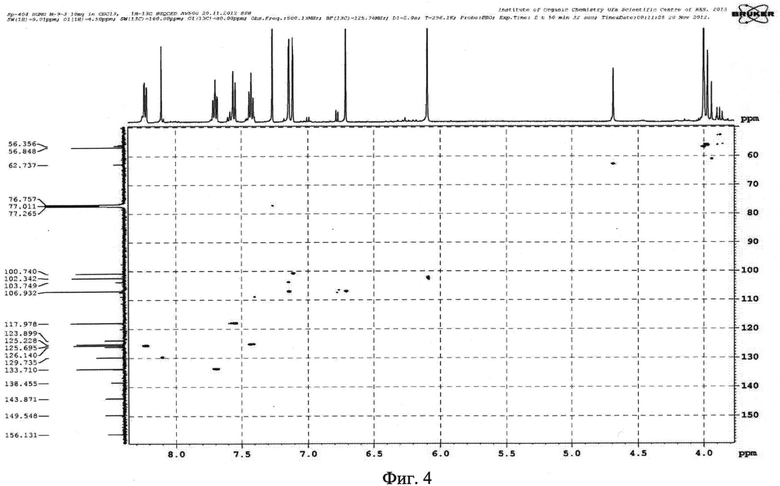
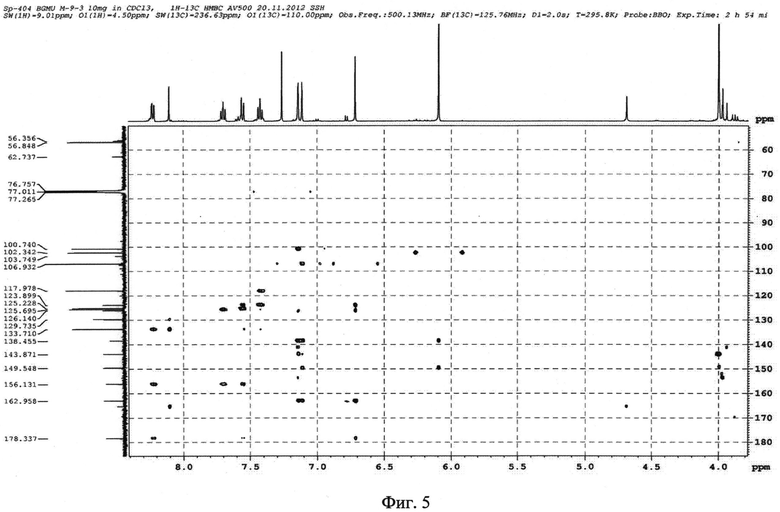
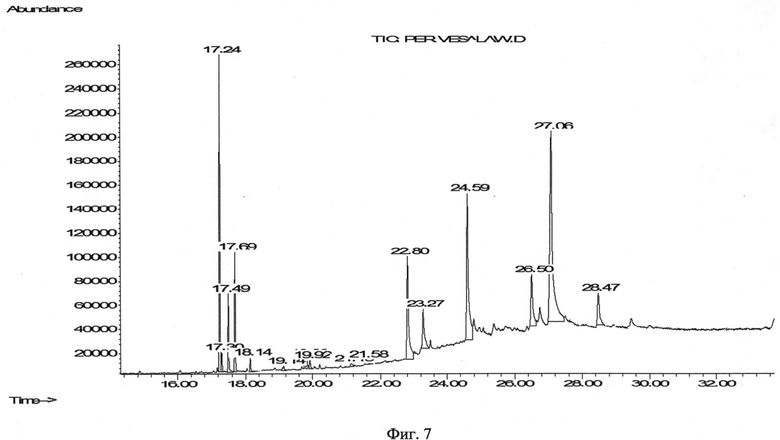
На фиг. 1 представлен УФ-спектр вещества I. Для идентификации структуры вещества I предложено сочетание современных методов ЯМР1H-, ЯМР13С-спектроскопии. На фиг. 2 представлен спектр ЯМР13С вещества I - 3′,4′-метилендиокси-5′-метоксифлавона в DMS. На фиг. 3 - спектр ЯМР1H вещества I в DMSO. На фиг. 4 - корреляционный спектр 1H-13CHSQCED вещества I в DMSO. На фиг. 5 - корреляционный спектр 1Н-13СНМВС вещества I в DMSO. На фиг. 6 - корреляционный спектр 1Н-1Н COSY вещества I в DMSO. На фиг. 7 - хроматограмма липофильной фракции первоцвета весеннего.
В спектрах ЯМР 13C представлены сигналы восьми четвертичных углеродных атомов, одной CH2-групп, семи CH- и одной OCH3-групп. Сигналы карбонильного C-4 (δС 178.34) углеродного атома, а также углеродных атомов двойной связи C-2 (δС 162.96) и C-3 (δС 106.93) обладают характеристичными значениями химических сдвигов 1,3-замещенной (т.е. положение 3 по отношению C=O) еноновой системы. Для протонированных углеродных атомов и их протонов положения сигналов установлены на основании анализа спектров COSY и HSQC.
Положение 7-метокси-1,3-бензодиоксольного заместителя в 4Н-хромен-4-оне установили на основании сильнопольных сигналов протона Н-3 (δН 6.72) и его углерода C-3 (δC 106.93). Это характерно для протона еноновой двойной связи находящегося в области экранирования магнитно-анизотропной группы C=O, что приводит к смещению сигнала в спектре в более сильное поле (если бы протон находился в положении C-2, а бензодиоксольный заместитель в C-3, то сигналы Н-2 регистрировались бы в более слабом поле в области 8.1-8.5 м.д.).
Корреляционные пики Н-2′/C-3′ и H-2′/С-1′ в спектре НМВС указывают на то, что диоксольный фрагмент находится в положении С-1′ и C-3′, а пик OMe/C-7′ является доказательством расположения метоксильной группы на углероде C-7′.
Кроме того, в спектрах масс-спектроскопии молекулярный ион M+ равен 296, что соответствует предполагаемой структуре 3′,4′-метилендиокси-5′-метоксифлавона.
Вещество I. Густая маслянистая жидкость темно-зеленого цвета состава
C17H12O5, УФ-спектр в спирте этиловом: λmax 219, 337, 410 нм. ЯМР 1H (500 MHz, CDCl3): 4.0 (3H, с, ОСН3), 6.10 (2H, с, Н-2′), 6.71 (1H, с, H-3), 7.11 (1H, д, J=1.5 Гц, Н-6′), 7.14 (1H, д, J=1.5 Гц, Н-4′), 7.43 (1Н, дд, J=7.9, 7.3 Гц, H-6), 7.55 (1H, д, J=8.2 Гц, H-8), 7.69 (1Н, ддд, J=8.2, 7.3, 1.5 Гц, Н-7), 8.22 (1Н, дд, J=7.9, 1.5 Гц, Н-5). ЯМР 13C (500 MHz, CDCl3): 56.36 (OCH3), 100.74 (С6′), 102.34 (С2′), 106.93 (C3, C4′), 117.98 (C8), 123.89 (C10), 125.23 (C6), 125.69 (C5), 126.14 (C5′), 133.71 (C7), 138.45 (C1′), 143.87 (C7′), 149.55 (C3′), 159.13 (C9), 162.96 (C2), 178.34 (С=O).
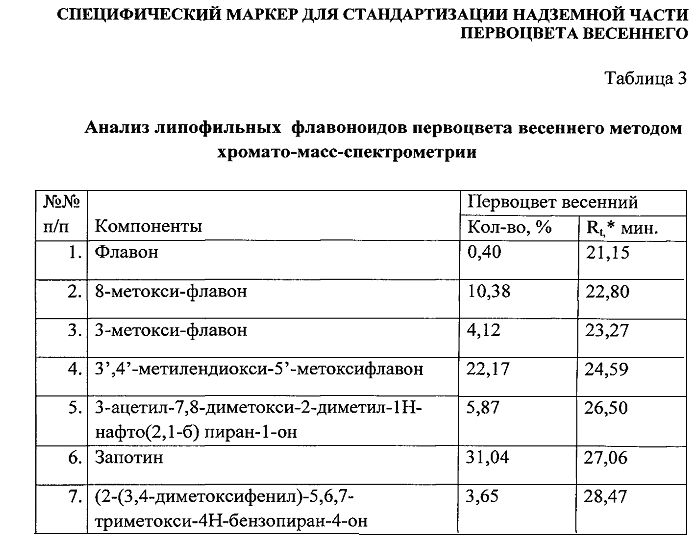
Кроме указанного вещества 3′,4′-метилендиокси-5′-метоксифлавона нами также были идентифицированы методом хромато-масс-спектрометрии иные липофильные флавоноиды первоцвета весеннего (таблица 3, фиг. 7)
По данным таблицы 3 и хроматограммы липофильной фракции первоцвета весеннего (фиг. 7) установлено высокое содержание (22,17%.) и наименьшее время удерживания вещества 3′,4′-метилендиокси-5′-метоксифлавона в данном образце сырья.
Таким образом, вещество 3′,4′-метилендиокси-5′-метоксифлавон является специфическим маркером для стандартизации надземной части первоцвета весеннего (Primula veris L.).

| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ, ОБЛАДАЮЩЕЕ ЭНДОТЕЛИОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ | 2014 |
|
RU2561064C1 |
| СРЕДСТВО РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ, ОБЛАДАЮЩЕЕ ГЕПАТОЗАЩИТНЫМ ДЕЙСТВИЕМ | 2014 |
|
RU2554493C1 |
| СРЕДСТВО РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ, ПРОЯВЛЯЮЩЕЕ КАРДИОТОНИЧЕСКУЮ АКТИВНОСТЬ ПРИ ХРОНИЧЕСКОЙ СЕРДЕЧНОЙ НЕДОСТАТОЧНОСТИ. | 2017 |
|
RU2654706C1 |
| СРЕДСТВО РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ, ОБЛАДАЮЩЕЕ АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ | 2007 |
|
RU2342942C1 |
| АНТИОКСИДАНТНОЕ СРЕДСТВО "КУРКУМЫ ЭКСТРАКТ ГУСТОЙ" | 2016 |
|
RU2650642C1 |
| СПОСОБ ПОЛУЧЕНИЯ РИККАРДИНА С | 2007 |
|
RU2340350C1 |
| РАСТИТЕЛЬНЫЙ СБОР, ОБЛАДАЮЩИЙ АНТИОКСИДАНТНЫМ, ПРОТИВОВОСПАЛИТЕЛЬНЫМ И КАПИЛЛЯРОУКРЕПЛЯЮЩИМ ДЕЙСТВИЕМ | 2020 |
|
RU2729784C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА С УСИЛЕННОЙ АКТИВНОСТЬЮ И ЛЕКАРСТВЕННОЕ СРЕДСТВО | 1999 |
|
RU2155062C1 |
| Средство, обладающее антиоксидантным и противовоспалительным действием и способ его получения | 2023 |
|
RU2807894C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНОЙ ДОБАВКИ ИЗ КАЛЕНДУЛЫ (CALENDULA OFFICINALIS 7) ДЛЯ КОСМЕТИЧЕСКИХ ИЗДЕЛИЙ | 1991 |
|
RU2008014C1 |


Изобретение относится к применению 3′,4′-метилендиокси-5′-метоксифлавона в качестве специфического маркера для стандартизации надземной части первоцвета весеннего (лекарственного) (Primula veris L., или Primula officinalis (L.) Hill.), что позволяет расширить перечень специфических веществ-маркеров для стандартизации лекарственного растительного сырья. 7 ил., 3 табл.
Применение 3',4'-метилендиокси-5'-метоксифлавона в качестве специфического маркера для стандартизации надземной части первоцвета весеннего (лекарственного) (Primula veris L., или Primula officinalis (L.) Hill.).
| Budzianowski Jaromir el al,Phytochemistry,2005,66(9),p.1033-1039 |
Авторы
Даты
2015-01-20—Публикация
2013-10-04—Подача