Изобретение относится к медицине, конкретно к клинической фармакологии, и может быть использовано для фармакологической коррекции заболеваний ЦНС, и касается лекарственных средств, обладающих церебропротекторным действием, получаемых из растительного сырья.
Проблема церебральной и цереброваскулярной патологии в современном мире является актуальной. В связи с ростом продолжительности жизни увеличивается и частота развития энцефалопатий, а также сосудистой деменции. В настоящее время этой патологией страдает более 157 млн. человек в мире, а за последние 5 лет на 17% увеличилось количество нейродегенеративных заболеваний. Психический, когнитивный и неврологический дефициты после перенесенных тяжелых нейроинфекций формируются с частотой до 45%. С другой стороны, рост заболеваемости с сочетанной психосоматической патологией также приводит к увеличению числа больных с вторичными неврологическими симптомами, обусловленными поражением внутренних органов и систем. Вместе с тем полноценное функционирование клеток и глиальных элементов ЦНС, поддержание в них адекватного церебрального кровотока является важнейшим условием нормальной жизнедеятельности человека. Расстройства церебральной гемодинамики влекут за собой угрозу для жизни больных или стойкую инвалидизацию. Основными особенностями нейронов головного мозга является высокий уровень энергозатрат и значительная активность метаболических процессов при малых резервах кислорода и энергетических субстратов. Одним из важных механизмов гипоксического (ишемического) повреждения является токсическое влияние продуктов метаболизма, обусловливающее дистрофические изменений клеток ЦНС, их некроз и апоптоз [1-4].
Поэтому актуальность решения проблемы адекватной фармакотерапии заболеваний, сопровождающихся церебральной патологией, является важной задачей, требующей для ее решения объединенных усилий специалистов разных профилей. Одновременно ограниченный ассортимент средств терапии данной патологии, служит основанием для разработки новых лекарственных препаратов, обладающих церебропротекторным действием.
Наиболее близким к предлагаемому решению является экстракт корня шлемника байкальского Scutellaria baicalensis Georgi сухой, содержащий флавоноиды и обладающий церебропротекторным действием (прототип) [5].
Задачей данного изобретения является расширение арсенала лекарственных средств из отечественного растительного сырья, обладающих церебропротекторной активностью.
Поставленную задачу решают применением тритерпеноидов и бутиролигнанов альфредии поникшей (Alfredia cernua (L.) Cass.) в качестве средства, обладающего церебропротекторным действием.
Новым является то, что впервые в качестве средства, обладающего церебропротекторным действием, используют тритерпеноиды и бутиролигнаны альфредии поникшей (Alfredia cernua (L.) Cass.).
В литературе отсутствуют данные о средстве, обладающим церебропротекторным действием и содержащим тритерпеноиды и бутиролигнаны альфредии поникшей (Alfredia cernua (L.) Cass.).
Применение тритерпеноидов и бутиролигнанов альфредии поникшей (Alfredia cernua (L.) Cass.) по предлагаемому назначению стало возможным благодаря выявлению их новых свойств в эксперименте, а именно способности улучшать функции ЦНС за счет церебропротекторного действия.
Отличительные признаки проявили в заявляемой совокупности новые свойства, явным образом не вытекающие из уровня техники в данной области и неочевидные для специалиста. Впервые установлено, что в качестве средства, обладающего церебропротекторным действием, можно использовать тритерпеноиды и бутиролигнаны альфредии поникшей (Alfredia cernua (L.) Cass.).
Идентичной совокупности признаков не обнаружено в патентной и научно-медицинской литературе.
Предлагаемое средство с успехом может быть использовано в практическом здравоохранении для коррекции заболеваний ЦНС.
Исходя из вышеизложенного следует считать предлагаемое изобретение соответствующим условиям патентоспособности «Новизна», «Изобретательский уровень», «Промышленная применимость».
Изобретение будет понятно из следующего описания.
Технологический процесс получения тритерпеноидов и бутиролигнанов, обладающих церебропротекторным действием, состоит из следующих этапов.
1. Экстракция растительного материала.
2. Фракционирование экстракта органическими растворителями в порядке увеличения их полярности (хлороформом).
3. Хроматографическое разделение хлороформной фракции и выделение тритерпеноидов и бутиролигнанов.
Пример 1.
Этап 1. Надземную часть альфредии поникшей собирали в фазу плодоношения. Высушенное воздушным способом сырье измельчали и просеивали через сито с диаметром отверстий 2 мм (влажность 11,8%). Экстракт получали обработкой измельченной надземной части растения метанолом на водяной бане с обратным холодильником в течение 2 ч при температуре 70°C и соотношении сырье-экстрагент 1:25. Полученные извлечения объединяли, фильтровали и упаривали в вакууме при температуре не выше 50°C.
Этап 2. Полученный экстракт (выход 15,7%) растворяли в воде (1:4) и исчерпывающе экстрагировали в делительной воронке хлороформом. Полученную хлороформную фракцию также упаривали в вакууме (выход 26,7%).
Этап 3. Разделение сложных смесей веществ и выделение индивидуальных соединений осуществляли, используя методы избирательной жидкостной экстракции, адсорбционной колоночной и флэш-хроматографии на силикагеле и полиамиде в сочетании с хроматографией на бумаге и в тонком слое сорбента, хромато-масс-спектрометрией (ГХ/МС), противоточным распределением и дробной кристаллизацией.
Разделение хлороформной фракции (20 г) осуществляли методом колоночной хроматографии на силикагеле (L 100/250 Lachema) в соотношении образец - сорбент 1:10, элюируя хлороформом и смесью хлороформ-этанол (с градиентным увеличением количества последнего, 98:2-80:20). В результате получено 4 подфракции (I-IV). Колоночному разделению на силикагеле подвергли подфракции II и III, содержащие преимущественно тритерпеновые и фенольные соединения, представляющие наибольший интерес.
В подфракции II (выход 39%), элюированной хлороформом, по данным хроматографии в тонком слое и ГХ/МС-анализа, обнаружили не менее четырех веществ тритерпеновой природы. При рехроматографии подфракции II на силикагеле (L 100/250 Lachema) в соотношении образец - сорбент 1:20, элюенты - гексан и смесь гексан-ацетон с возрастающим градиентом гидрофильности (98:2→90:10), выделили однородную, по хроматографической картине в тонком слое, смесь веществ I (тритерпеноиды) - белый мелкокристаллический порошок, Тпл. 160-161°C (этанол). УФ-спектр (C6H14), λmax, нм: 210, (220). ИК-спектр (KBr), νmax, см-1: 1043, 1072, 1085, 1110, 1138 (ОН), 1189, 1217, 1253, 1273, 1298, 1360, 1381, 1454, 1463 (CH3, CH2-, CH), 1641 (C=C), 2660, 2725 (ОН), 2872, 2962 (CH3, CH2, CH), 3387, 3614 (ОН). Выход - 1,7 г. Разделение указанной смеси явилось сложной экспериментальной задачей, поэтому для исследования применяли метод ГХ/МС. В результате во фракции идентифицировали β-амирин (олеан-12-ен-3-ол, 27,48%, tr 53,58 мин), α-амирин (урс-12-ен-3-ол, 27,52%, tr 57,72 мин), моретенол (гоп-22(29)-ен-3β-ол, 25,52%, tr 66,11 мин) и лупеол (луп-22(29)-ен-3β-ол, 19,48%, tr 66,96 мин).
Разделение подфракции III (выход 27%), элюированной смесью хлороформ-этанол 9,3:0,7-9:1 и содержащей не менее шести фенольных соединений, производили методом колоночной хроматографии на силикагеле (L 40/100 Lachema) при соотношении образец - сорбент 1:25. Элюирование проводили хлороформом, системой хлороформ-ацетон (с градиентным увеличением количества последнего, 98:2-50:50). При промывании колонки смесью хлороформ-ацетон 6:4 с последующим противоточным распределением в системе растворителей хлороформ-метанол-вода (5:6:4) из нижней фазы получили индивидуальные вещества II и III - доминирующие во фракции. Вещество II - белый мелкокристаллический порошок, C27H34O11; Тпл., °C (хлороформ-гексан 1:2): 86 (газ. выдел.), 250 (с разл.). УФ-спектр (C2H5OH), λmax, нм: 224, 255, (274), (298). ИК-спектр (в пленке CHCl3), νmax, см-1: 1026, 1074, 1140, 1157 (пиранозное кольцо), 1194, 1235, 1264 (C-O-C), 1332, 1349, 1383, 1421, 1453, 1464 (CH3, CH2, CH), 1515, 1592, 1606 (аром.), 1766 (γ-лактонный цикл, лактонный карбонил), 2855 (ОСН3 аром.), 2839, 2921 (CH3, CH2), 3419 (ОН). Выход 0,12 г. В продуктах кислотного гидролиза методом хроматографии в тонком слое и на бумаге обнаружили агликон с Rf 0,35 (вещество III) и 0,45 соответственно («Silufol UV-254», хлороформ-этанол 8:1 и этилацетат-этанол 8:1, диазореактив) и углеводный компонент - D-глюкоза (Rf 0,27, бумага «Ленинградская М», бутанол-1-пиридин-вода 6:4:3, анилинфталат). Относительная стереохимия молекулы II определена путем анализа спектров ROESY. транс-Расположение бензилильных заместителей по отношению к лактонному циклу следует из того, что в этих спектрах ROESY и NOESY отсутствуют кросс-пики между протонными сигналами групп C6 и C7. Протоны H3; H4 и H5α показывают взаимодействие с протонами H3′; H6′ и H3′′; H6′′ ароматических ядер, что свидетельствует о свободном вращении циклов по осям C6-C1′ и C7-C1′′. На основании физических, спектральных и хроматографических характеристик установлена структура вещества II - 3-(3-метокси-4-β-D-глюкопиранозилоксибензил)-4-(3,4-диметоксибензил)-бутиролактон (арктиин). Вещество III - бесцветные призматические кристаллы, C21H24O6 [m/z, 373,4190 (М+Н)+]; Тпл., °C (хлороформ-гексан 1:5):220, 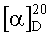
Фармакологические испытания проводили на аутбредных крысах-самцах CD (I категории, согласно сертификату) массой 200-220 г. Животные получены из отдела экспериментальных биологических моделей ФГБУ «НИИ фармакологии имени Е.Д. Гольдберга» СО РАМН. Эксперименты осуществляли в осенне-зимний период. Работы в рамках экспериментальных методик выполняли с 9 ч утра и заканчивали к 15 ч. Животных содержали в стандартных условиях вивария на обычном рационе кормления при свободном доступе к воде и пище (за исключением тех случаев, где иные условия оговариваются особо) в соответствии с правилами, принятыми Европейской Конвенцией по защите позвоночных животных, используемых для экспериментальных и научных целей (г. Страсбург, 1986). Эвтаназию осуществляли в соответствии с «Правилами проведения работ с использованием экспериментальных животных», утвержденными приказом МЗ РФ.
Фармакологические эффекты тритерпеноидов и бутиролигнанов оценивали по влиянию на выработку и воспроизведение сложного условного питьевого рефлекса у животных в «Т-образном лабиринте» на фоне ишемии головного мозга [6, 7].
Тритерпеноиды, бутиролигнаны, экстракт, фракцию и прототип вводили животным курсом ежедневно в течение семи дней однократно через зонд в желудок в виде раствора в воде, очищенной за 1 ч до тестирования. Интактные животные получали эквивалентное количество воды очищенной.
Полученные экспериментальные данные обрабатывали статистически. О достоверности различий судили методом проверки вероятности нулевой гипотезы с использованием t критерия Стьюдента и критерия Вилкоксона. Различия считали достоверными при p≤0,05.
Пример 2. Изучение влияния тритерпеноидов и бутиролигнанов на выработку и воспроизведение сложного условного питьевого рефлекса у животных проводили в шестизвенном Т-образном лабиринте в условиях ишемии головного мозга [6]. Опыты выполняли на крысах на фоне водной депривации. Лабиринт представляет собой установку, состоящую из одной стартовой камеры и двух систем коридоров, каждая из которых включает в себя по 3 Т-образных колена, спирально соединенных между собой и заканчивающихся целевыми камерами. Предварительно крыс оставляли без воды на одни сутки. Затем в течение 2 дней каждую крысу дважды в день на 20 мин с интервалом в 1 ч индивидуально помещали в лабиринт, где беспорядочно расставляли 6 поилок (первый этап обучения). На третий день животное помещали в стартовую камеру лабиринта, при этом все поилки из последнего убирали. Крыса начинала искать поилку, выходила из стартовой камеры и делала первый поворот в правую или левую часть лабиринта. Направление первого поворота фиксировали и считали предпочтительным направлением поворота для данного животного. Немедленно вслед за этим в целевую камеру, находящуюся в половине лабиринта противоположной, той в которую крыса повернула в первый раз, ставили поилку. При всех последующих побежках поилку ставили для данной крысы именно в эту целевую камеру. Это делали для того, чтобы при становлении условного рефлекса исключить влияние предпочтительного направления поворота на процесс обучения. Каждое животное тестировали в лабиринте таким образом в течение 15 мин, если оно не находило поилку раньше. Если животное не находило поилки в течение 15 мин, его помещали в целевую камеру, чтобы крыса могла напиться. Крыс, отказавшихся искать поилку в течение первых 4 побежек, из дальнейших экспериментов исключали. В тот же день животное через 1 ч совершало вторую побежку. Таким образом, каждую крысу обучали в течение 4 дней (2 этап обучения - 5-8 побежки и 3 этап обучения - 9-12 побежки). При этом регистрировали: продолжительность питья, характеризующую силу питьевой мотивации, время достижения поилки, количество ошибок (заходы в неправильные рукава лабиринта и тупики), количество вертикальных стоек и груминг. Выделяли также периоды полной неподвижности продолжительностью более 15 с, которые расценивали как фризинговые реакции. Их общую продолжительность регистрировали в качестве самостоятельного показателя. О качестве обучения судили по сокращению времени достижения поилки и количества ошибок. Груминг и вертикальные стойки характеризовали смещенную и ориентировочно-исследовательскую активность, соответственно. Отказ от поиска поилки, после двух успешных ее нахождений, отказ от питья после успешного обнаружения поилки оценивали как проявление невротической реакции [7], которое оценивали в виде отношения общего количества невротических реакций к общему числу побежек. Об эффекте веществ судили по усредненной разнице показателей 9-12 побежек между опытной и контрольной группами на протяжении третьего этапа обучения. Введение тритерпеноидов, бутиролигнанов, экстракта, фракции и прототипа начинали с момента лишения животных воды (всего 7 введений). Экспериментальную ишемию вызывали путем полной перевязки под гексобарбиталовым наркозом левой сонной артерии и ограничения кровотока в правой сонной артерии на 50% путем частичной перевязки. Операцию выполняли за 48 ч до первой побежки в лабиринте. Контролем служили ложнооперированные животные.
Курсовое введение тритерпеноидов и бутиролигнанов альфредии поникшей (Alfredia cernua (L.) Cass.) в условиях модели «Т-образного лабиринта» на фоне экспериментальной ишемии головного мозга снижает время достижения поилки, число ошибок, невротических реакций и представительство смещенной активности (груминг), увеличивает непосредственно время питья. Таким образом, тритерпеноиды и бутиролигнаны, способствуя улучшению выработки рефлекса у животных в условиях данного эксперимента, проявляет церебропротекторную активность (табл.1), превосходя эффект прототипа, экстракта альфредии и его фракции по влиянию на невротические реакции и груминг.
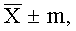
Таким образом, тритерпеноиды и бутиролигнаны проявляют выраженный церебропротекторный эффект.
На основании проведенных экспериментальных исследований можно сделать вывод о том, что применение тритерпеноидов и бутиролигнанов альфредии поникшей (Alfredia cernua (L.) Cass.) является перспективным для получения более высокого лечебного эффекта.
Положительный эффект достигнут благодаря использованию тритерпеноидов и бутиролигнанов альфредии поникшей (Alfredia cernua (L.) Cass.), обладающих перебропротекторным действием, что позволило расширить арсенал средств из отечественного растительного сырья, обладающих церебропротекторной активностью.
Литература
1. Камчатов П., Чугунов А., Умарова X., Бойко А. Хронические расстройства мозгового кровообращения: возможности терапии // Врач. - 2008. - №4. - С.14-17.
2. Ощепкова Е.В. Гипертоническая энцефалопатия: Проблема терапевта (кардиолога) или невролога? // Терапевтический архив. - 2009. - №1. - С.79-84.
3. Кушнир Г.М., Савчук Е.А. Дисциркуляторная энцефалопатия: Учебно-методическое пособие для врачей-слушателей циклов последипломного обучения, интернов-невропатологов, студентов медуниверситетов. - Симферополь, 2004. - 14 с.
4. Машковский М.Д. Лекарственные средства. - М.: Новая Волна, 2002. - Т.1. - С.388-392.
5. Гольдберг Е.Д., Дыгай A.M., Литвиненко В.И., Попова Т.П., Суслов Н.И. Шлемник байкальский. Фитохимия и фармакологические свойства. - Томск: Изд-во Томского ун-та, 1994. - С.151-180.
6. Азарашвили А.А. Исследование механизмов памяти с помощью физиологически активных соединений. - М.: Наука. - 1981. - 198 с.
7. Суслов Н.И. Патогенетическое обоснование психофармакологических эффектов препаратов природного происхождения (экспериментальное исследование): Дисс. докт. мед. наук. - Томск, 1995. - 98-100 с.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НООТРОПНЫМ ДЕЙСТВИЕМ | 2007 |
|
RU2347580C1 |
| Церебропротекторное средство | 2017 |
|
RU2648451C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКИМ ДЕЙСТВИЕМ | 2007 |
|
RU2354397C1 |
| Способ получения густого экстракта альфредии поникшей, обладающего противоневротическим действием | 2023 |
|
RU2823780C1 |
| ФАРМАЦЕВТИЧЕСКИЙ СОСТАВ, ОБЛАДАЮЩИЙ ЦЕРЕБРОПРОТЕКТОРНЫМ И ПРОТИВОНЕВРОТИЧЕСКИМ ДЕЙСТВИЕМ | 2013 |
|
RU2535024C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НОРМОТИМИЧЕСКИМ ДЕЙСТВИЕМ | 2010 |
|
RU2416421C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ НООТРОПНЫМ ДЕЙСТВИЕМ | 2011 |
|
RU2475250C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНКСИОЛИТИЧЕСКОЙ, НООТРОПНОЙ, ПРОТИВОСУДОРОЖНОЙ, АНТИДЕПРЕССИВНОЙ, ЦЕРЕБРОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ И СПОСОБНОСТЬЮ НОРМАЛИЗОВАТЬ ПРОЦЕССЫ ПЕРЕДАЧИ В СИНАПСАХ МОЗГА | 2007 |
|
RU2335293C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИОКСИДАНТНОЙ АКТИВНОСТЬЮ | 2005 |
|
RU2292214C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИГРИБКОВЫМ ДЕЙСТВИЕМ | 2014 |
|
RU2560517C1 |
Изобретение относится к клинической фармакологии, а именно к средству, обладающему церебропротекторным действием. Применение смеси тритерпеноидов, содержащей β-амирин 27,48 мас.%, α-амирин 27,52 мас.%, моретенол 25,52 мас.%, лупеол 19,48 мас.%, или бутиролигнанов - арктиина или арктигенина, выделенных из альфредии поникшей (Alfredia cemua (L.) Cass.), в качестве средства, обладающего церебропротекторным действием. Вышеописанная смесь тритерпеноидов или бутиролигнаны - арктиин или арктигенин, выделенные из альфредии поникшей (Alfredia cemua (L.) Cass., обладают выраженным церебропротекторным действием. 1 табл., 2 пр.
Применение смеси тритерпеноидов, содержащей β-амирин 27,48 мас.%, α-амирин 27,52 мас.%, моретенол 25,52 мас.%, лупеол 19,48 мас.% или бутиролигнанов - арктиина или арктигенина, выделенных из альфредии поникшей (Alfredia cemua (L.) Cass.), в качестве средства, обладающего церебропротекторным действием.
| Р.Н.МУСТАФИН и др | |||
| Антигипоксическое и стресспротекторное действие экстракта Альфредии поникшей //Химия растительного сырья, 2012, |
Авторы
Даты
2015-04-10—Публикация
2014-01-09—Подача