Изобретение относится к получению нового соединения N-(4-фениламинофенил)малеинимида, который может быть использован как химический модификатор многоцелевого назначения для резиновых смесей, а также в производстве термоустойчивых полимеров.
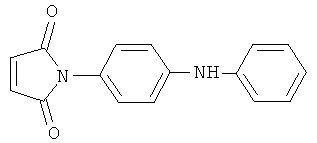
Известно, что ароматические соединения, содержащие в своем составе вторичные аминогруппы, являются эффективными стабилизаторами, антиоксидантами и термостабилизаторами различных видов синтетических и натурального каучуков (бутадиеновых, бутадиен-стирольных, изопреновых и др.) (Химические добавки к полимерам (справочник). 2-е изд., перераб. - М.: Химия, 1981). Примерами таких стабилизаторов являются следующие соединения: N-фенилнафтиламин-1 (там же, с.5), N-фенилнафтиламин-2 (там же, с.9-10), дифениламин (там же, с.13-14), N-алкил-N1-фенилфенилендиамин-1,4 (там же, с.26-27), N,N1-дифенилфенилендиамин-1,4 (там же, с.28-29) и многие другие. Ряд малеинимидов, в частности 1,3-фенилен-бис-малеинимид (торговое название малеид Ф), применяется в качестве химического модификатора многоцелевого назначения для резиновых смесей на основе непредельных каучуков, используемых в производстве крупногабаритных шин и шин массового ассортимента, а также является сырьем для получения термоустойчивых полимеров (там же, с.177-178).
Задачей изобретения является разработка способа получения N-(4-фениламинофенил)малеинимида, который может быть использован как химический модификатор многоцелевого назначения, т.е. сочетать в себе не только структурирующие свойства, но и функции стабилизатора широкого назначения.
Известно, что синтез малеинимидов и бис-малеинимидов обычно осуществляется в две стадии: первая включает в себя образование соответствующей малеаминовой или бис-малеаминовой кислоты, второй стадией является дегидроциклизация малеаминовой кислоты с образованием соответствующих малеинимидов. Дегидроциклизация может быть осуществлена различными способами. Прямая дегидроциклизация малеаминовой кислоты (А.с. 171593 ЧССР, кл. C07D 207/00, опубл. 1978; Пат. 3586697 США, кл.260-326.5, C07D 27/10, опубл. 1971) достигается нагреванием до температур, близких к 200°C, но в этих жестких условиях не всегда удается предотвратить образование побочных продуктов.
Известны способы получения малеинимидов, которые предусматривает дегидроциклизацию малеаминовой кислоты с использованием химических водоотнимающих средств: ангидридов низших карбоновых кислот, как правило в присутствии уксусного ангидрида (патент США 3960887, кл. C07D 207/44, опубл. 1976) или Ν,Ν-дициклогексилкарбодиимида (заявка Япония 61100534, кл. C07D 207/452, опубл. 1994) в присутствии катализатора. Процесс взаимодействия малеинового ангидрида с первичным моно- или диамином и последующую дегидроциклизацию образовавшейся кислоты проводят в среде органических разбавителей, в качестве которых используют, например, диметилформамид, диметилацетамид, диметилсульфоксид, N-метилпирролидон (патент США 3839358, опубл. 1974), кетоны, простые или сложные эфиры, хлорированные ароматические углеводороды (патент США 4154737, кл. C07D 403/10, опубл. 1979). Недостатком данных способов является образование побочных продуктов при получении N-(4-фениламинофенил)малеинимида за счет протекания реакции ацилирования вторичной аминогруппы уксусным ангидридом.
Наиболее удобным способом в данном случае является использование азеотропной отгонки воды в присутствии кислотного катализатора (Заявка Япония 61-76457, МКИ C07D 207/456, опубл. 1986; заявка Япония 499764, МКИ5 C07D 207/452, опубл. 1992). В качестве азеотропного растворителя чаще всего используется толуол, кипящий при 110°С, кроме того, с целью сокращения продолжительности реакции в реакционную смесь вводят полярный апротонный растворитель, напр. диметилформамид. Присутствие полярного растворителя облегчает протекание реакции вследствие увеличения полярности среды.
Известен способ получения N-фенилмалеинимида, который заключается во взаимодействии анилина с малеиновым ангидридом в среде ацетона, с последующей дигидроциклизацией образующегося фениламида малеиновой кислоты в среде толуола и диметилформамида в присутствии n-толуолсульфокислоты, с образованием N-фенилмалеинимида. Колямшин О.А., Данилов В.А., Кольцов Н.И. Особенности синтеза и свойства некоторых малеинимидов / Бутлеровские сообщения, 2012. Т. 32. №12. С. 26-30).
Однако заявляемое соединение данным способом не получают.
Наиболее близким по технической сущности является способ получения N-(4-фениламинофенил)малеинимида, включающий взаимодействие малеинового ангидрида с 4-аминофениланилином в среде ацетона и с последующей циклизацией уксусным ангидридом. Патент Китая №102775341, А, 14.11.2012 (реферат, стр. 4, 5).
Однако этим способом получают недостаточно чистый целевой продукт с пониженным выходом (91,5%).
Задачей изобретения является разработка нового способа получения N-(4-фениламинофенил)малеинимида, расширяющего арсенал способов данного назначения.
Техническим результатом заявляемого изобретения является увеличение выхода и чистоты целевого продукта.
Технический результат достигается способом получения N-(4-фениламинофенил)малеинимида формулы
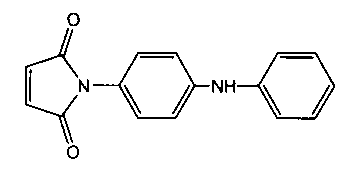
включающий взаимодействие малеинового ангидрида с 4-аминофениланилином в среде ацетона, дегидроциклизацию промежуточного амида, согласно изобретению, перед дегидроциклизацией проводят выделение промежуточного амида, путем его фильтрования в вакууме и сушки на воздухе в течение суток, а дегидроциклизацию проводят при кипячении в смеси толуола и диметилформамида в присутствии n-толуолсульфокислоты.
Способ осуществляли по следующей схеме:
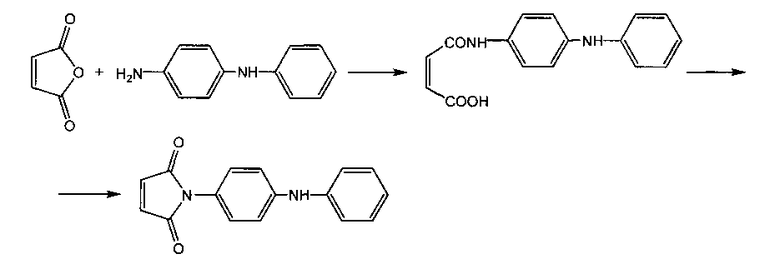
Пример. На первой стадии получали 4-фениламинофенилмалеаминовую кислоту.
К раствору 49,4 г (0,268 моль) 4-аминофениланилина в 250 мл ацетона постепенно в течение 20-25 мин при перемешивании приливали раствор 27,5 г (0,28 моль) малеинового ангидрида в 100 мл ацетона. Реакционную массу нагревали до 40-45°С и перемешивали 3 часа, осадок отфильтровывали в вакууме и промывали на фильтре 3 раза по 20 мл ацетона, сушили на воздухе в течение суток. Получили 59,6 г (78,8%) продукта в виде оранжевого порошка, т. пл. 196-197°С. Rf 0,56 (сп.). ИК-спектр, ν, см-1: 3380 (ΝΗ), 3261, 3203 (CONH), 1701 (С=O), 3056, 1596, 844, 745, 693 (ар. кольцо).
На второй стадии получали N-(4-фениламинофенил)малеинимид. Для этого смесь 56,5 г (0,2 моль) 4-фениламинофенилмалеаминовой кислоты, 2 г n-толуолсульфокислоты, 100 мл диметилформамида и 240 мл толуола кипятили с насадкой Дина-Старка до прекращения выделения воды (≈6 ч), большую часть растворителей отгоняли в вакууме водоструйного насоса, остаток размешивали с 1000 мл воды. Выделяющееся первоначально темное масло при перемешивании постепенно кристаллизуется. Осадок отфильтровывали в вакууме, промывали на фильтре 10 раз по 20 мл воды, сушили на воздухе, затем при 60°C в течение 4 ч. Получили 50,0 г (94,6%) продукта в виде желто-коричневого порошка, т.пл. 130-131°C (2×ИПС). Rf 0,55 (сп.). ИК-спектр, ν, см-1: 3387 (NH), 1706 (C=O), 3066, 1596, 826, 753, 687 (ар. кольцо). Спектр ЯМР 1Н, δ, м.д.: 7.14 с (2Н, СН=СН), 6.87 т (1Н, Ar-H, 3JHH 7), 7.13 м (6Н, Ar-H), 7.26 т (2Н, Ar-H, 3JHH 7).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 1,3-ФЕНИЛЕНБИСМАЛЕИМИДА | 2007 |
|
RU2333906C1 |
| СПОСОБ ПОЛУЧЕНИЯ 4,5-ДИЦИАНОФТАЛЕВОЙ КИСЛОТЫ | 2013 |
|
RU2540339C2 |
| Способ получения 4-замещенного 2-[2-оксо-1-пирролидинил] ацетамида | 2016 |
|
RU2629117C1 |
| СПОСОБ ПОЛУЧЕНИЯ N-[2-(МОРФОЛИН-4-ИЛ)ЭТИЛ]-4-ХЛОРБЕНЗАМИДА (ВАРИАНТЫ) | 2014 |
|
RU2570898C2 |
| СПОСОБ ПОЛУЧЕНИЯ АЦИКЛОВИРА | 1996 |
|
RU2111967C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-(АЗОЛ-1-ИЛ)ЭТАНАМИНОВ | 2006 |
|
RU2317984C2 |
| ЗАМЕЩЕННЫЕ 2-(1,2,4-ТРИАЗОЛ-1-ИЛМЕТИЛ)-6-БЕНЗИЛИДЕН-1,4-ДИОКСАСПИРО[4.5]ДЕКАНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 2006 |
|
RU2326878C1 |
| СПОСОБ ПОЛУЧЕНИЯ БОРИРОВАННЫХ ПОРФИРИНОВ | 2013 |
|
RU2551539C2 |
| Поли- -оксисукцинимиды, являющиеся полимерами-активаторами для синтеза пептидов в воде или водной среде | 1976 |
|
SU644800A1 |
| Хроматографический сорбент для анализа низкомолекулярных соединений в биологических жидкостях | 2023 |
|
RU2818021C1 |
Изобретение относится к получению N-(4-фениламинофенил)малеинимида, который может быть использован как химический модификатор многоцелевого назначения для резиновых смесей, а также в производстве термоустойчивых полимеров. Способ включает взаимодействие малеинового ангидрида с 4-аминофениланилином в среде ацетона, выделение промежуточного амида из раствора ацетона, путем его фильтрования в вакууме и сушки на воздухе в течение суток, и дегидроциклизацию выделенного амида кипячением в смеси толуола и диметилформамида в присутствии n-толуолсульфокислоты. 1 пр.
Способ получения N-(4-фениламинофенил)малеинимида формулы
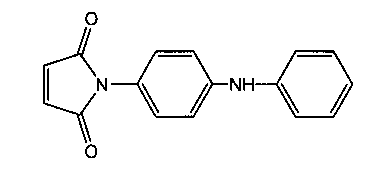
включающий взаимодействие малеинового ангидрида с 4-аминофениланилином в среде ацетона, дегидроциклизацию промежуточного амида, отличающийся тем, что перед дегидроциклизацией промежуточный амид выделяют из раствора ацетона, путем его фильтрования в вакууме и сушки на воздухе в течение суток, а дегидроциклизацию проводят при кипячении в смеси толуола и диметилформамида в присутствии n-толуолсульфокислоты.
| CN 102775341, A, 14.11.2012 | |||
| US 40154737, A1, 15.05.1979 | |||
| JP 62124134, A, 05.06.1987 | |||
| Жидкая лекарственная форма, содержащая лекарственное вещество, помещенное в биоразлагаемые полимеры | 2016 |
|
RU2649743C1 |
| Способ получения -замещенных малеимидов | 1976 |
|
SU667551A1 |
Авторы
Даты
2015-04-10—Публикация
2013-07-16—Подача