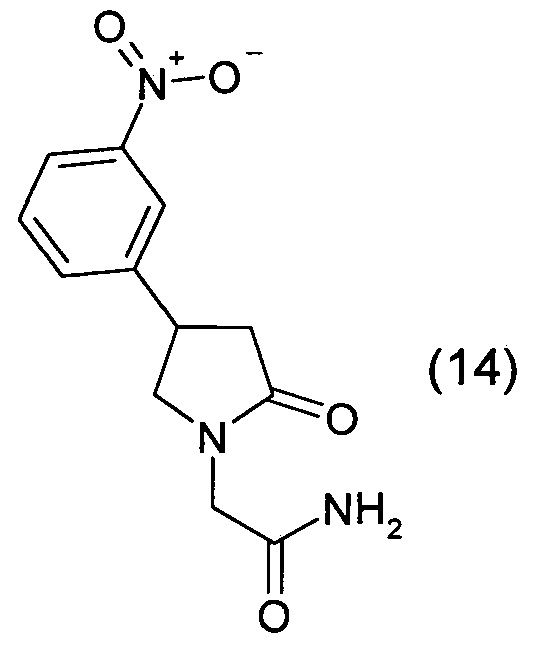
Изобретение относится к способу получения гетероциклического соединения, содержащего пятичленное кольцо, не конденсированное с другими кольцами, только с одним атомом азота в качестве гетероатома, а именно - к способу получения 2-[2-оксо-1-пирролидинил]ацетамида, замещенного в положений 4 пирролидинового Цикла радикалами R1 и R2, общей формулы

где
R1 обозначает Н,
R2 выбирают из Н, Ph, 2,4-диClPh, 4-ClPh, 4-CH3OPh, 3-NO2Ph;
или R1 и R2 совместно образуют С5Н10,
Соединения этой группы применяются в качестве терапевтических агентов, в частности, в лекарственных средствах, известных под названиями «пирацетам» и «фенотропил».
Известен способ получения этих соединений N-алкилированием замещенных и незамещенных 2-оксопирролидинов. Незамещенный или замещенный 2-оксопирролидин, при взаимодействии с сильными основаниями в безводных растворителях может образовывать соли щелочных металлов. Полученные соли используют в реакциях алкилирования алкилгалоидами по следующей схеме:
Схема 1

Защищен способ [Авт.св. СССР 797219, МКИ C07D 207/26, A61K 31/40, опубл. 25.07.1995] получения N-карбамоилметил-2-оксо-4-фенилпирролидина алкилированием 2-оксо-4-фенилпирролидина с последующим аминированием жидким аммиаком.
Для этого к раствору 4-фенил-2-оксопирролидина в растворе сухого бензола добавляют диспергированный металлический натрий. Смесь кипятят в течение 5 ч. Затем добавляют к ней этил хлорацетат, после чего поднимают температуру до 60°С и через несколько часов удаляют растворитель. Остаток перегоняют в вакууме, к полученному этил 2-[2-оксо-4-фенил-1-пирролидинил]ацетату при энергичном перемешивании приливают охлажденный водный аммиак. Через сутки выпавшие кристаллы N-карбамоилметил-2-оксо4-фенилпирролидина отфильтровывают и сушат, получают продукт с выходом 50%.
К недостаткам этого способа относится использование безводных легковоспламеняющихся органических растворителей и металлического натрия, что существенно повышает пожароопасность процесса. Стадия вакуумной перегонки является наиболее энергозатратной, что делает применение этого способа в крупном промышленном масштабе нерентабельным.
Описан способ [LV Pat. Appl. 13630; Chem. Abstr., 147, 365386 (2006)], по которому процесс проводят по схеме 2, превращая (4R)-2-оксо-4-фенилпирролидин действием гидрида натрия в натриевое производное, которое затем без выделения алкилировали этил бромацетатом. Полученный эфир подвергали аммонолизу, получая целевой продукт.
Схема 2

Главным недостатком этого способа является применение дорогостоящего и пожароопасного гидрида натрия. А также необходимость очистки промежуточных соединений.
Описан [патент США 4228179, МКИ C07D 209/00, опубл. 14.10.1980] способ получения 3-оксо-2-азаспиро-2-(N-метил)-ацетамидов, где в качестве алкилирующего агента применяются непосредственно N-замещенные галоалкиламиды.
Известен способ [патент США 7235579, МКИ A61K 31/40; C07D 409/00, опубл. 26.06.2007] с использованием в качестве основания гидрида натрия или литийдиизопропиламина с добавлением МФК (15-краун-5-эфира), причем процесс алкилирования замещенного 2-оксопирролидина проводят в безводных растворителях, таких, как ДМФА, ТГФ, ДМСО. Полученный эфир 2-оксо-1-пирролидинил уксусной кислоты гидролизуют до кислоты, обрабатывают хлористым тионилом или оксалилхлоридом для получения хлорангидрида. Взаимодействием хлорангидридов 2-оксо-1-пирролидинил уксусных кислот с замещенными алифатическими и ароматическими аминами получают конечный целевой продукт (Схема 3).
Схема 3
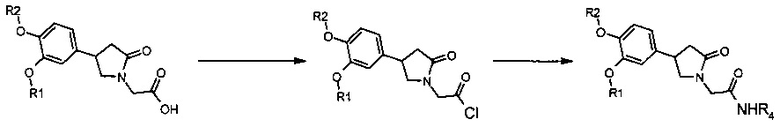
К недостаткам этих способов можно отнести применение катализаторов МФК и сильных дорогостоящих оснований. Очистка получаемых полупродуктов с помощью препаративной ВЭЖХ исключает использование данного способа в промышленном синтезе.
Известен способ [Авт. св. СССР №1265191, МКИ C07D 207/27, опубл. 23.10.1986], где в качестве альтернативы гидриду натрия используют металлорганические соединения, в частности, триметилгалогенсилан, для получения амида 2-оксо-4-фенил-1-пирролидинил уксусной кислоты из 2-оксо-4-фенилпирролидина. Способ включает взаимодействие 2-оксо-4-фенилпирролидина с избытком триметилбромсилана в присутствии триэтиламина в среде толуола при 60-80°С или с избытком гексаметилдисилазана в присутствии каталитических количеств соляной кислоты при температуре 30-150°С, образующееся производное 1-триметилсилил-2-оксо-4-фенил-пирролидина подвергают взаимодействию с метил бромацетатом при 130-175°C с одновременной отгонкой из смеси триметилбромсилана и последующим аммонолизом метил 2-оксо-4-фенил-1-пирролидинил ацетата водным аммиаком (Схема 4).
Схема 4
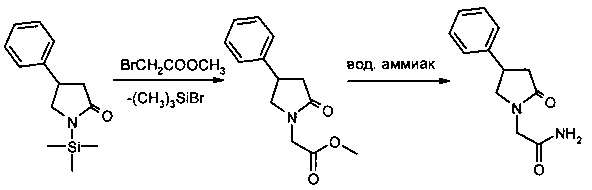
Данный способ, несмотря на хорошие выходы, имеет ряд недостатков, главный из которых - применение металлорганических соединений устойчивых только в отсутствии влаги. Триметилгалогенсилан легколетуч и пожаропасен. Кроме того, его применение предполагает использование коррозионостойких материалов.
К другим способам получения относится способ восстановления N-замещенных сукцинимидов [патент СССР 893131, МКИ C07D 297/26, опубл. 23.12.1981], в котором сукцинимид натрия, взаимодействием с 2-галоидзамещенными алкиламидами в этаноле, диметилформамиде, толуоле или другом подходящем растворителе при 80-150°С, превращают в N-алкиламиды-2,5-оксопирролидина. Эти соединения в дальнейшем подвергают электролитическому восстановлению в ячейке для электролиза с металлическим катодом (например, свинцовым) с применением диафрагмы в кислой среде. В качестве анода могут служить такие металлы, как платина или свинец (Схема 5). Обработка электролита щелочью, фильтрация и выпаривание фильтрата досуха в вакууме дает кристаллический сырой продукт, из которого с помощью подходящего растворителя можно экстрагировать желаемый продукт. Из полученного раствора после выпаривания можно получить чистый продукт перекристаллизацией.
Схема 5
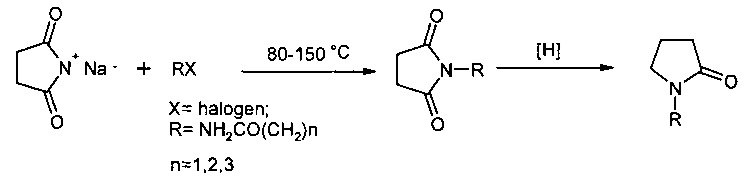
Применение электролитической ячейки существенно повышает себестоимость получаемого продукта. Низкая производительность, трудности, связанные с эксплуатацией электролитической установки, а также многостадийность процесса делают применение этого способа нецелесообразным.
Описан [патент РФ 2009126, МКИ C07D 207/26, опубл. 15.03.1994] усовершенствованный способ получения 5-пропил-N-карбамидометил-2-оксопирролидина, заключающийся в том, что этил 4-оксогептаноат подвергают гидроаминированию эквимолярным количеством амида глицина в среде метанола, содержащего 1% аммиака и 10% борида никеля от массы субстрата, при 80-100°С и начальном давлении водорода 8-10 МПа. Выходы целевого продукта достигают 70% (Схема 6).
Схема 6
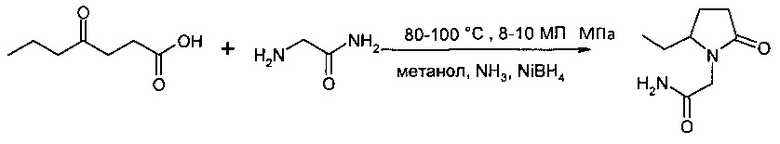
К преимуществам данного способа можно отнести одностадийность процесса и хороший выход. Среди недостатков следует отметить необходимость применения специализированного оборудования (автоклава), высоких давлений и газообразного водорода.
Еще один широко известный способ получения 4-замещенных 2-[2-оксо-1-пирролидинил]ацетамидов заключается в процессе внутримолекулярного ацилирования производных N-замещенных 4-аминомасляных кислот, в ходе которого происходит отщепление молекулы спирта или галогенводорода.
Данный способ рассматривается [патент СССР 1428195, МКИ C07D 207/26, A61K 31/4015, опубл. 30.09.1988] на примере получении этил 2-[2-оксо-1-пирролидин]ацетамида. Авторы патента описывают способ получения N-замещенных 4-аминомасляных кислот через реакцию N-алкилирования 2-аминобутанамидов функциональными производными 4-галогенбутановой кислоты. Процесс ведут в органических растворителях (толуол, ацетонитрил) в присутствии основных катализаторов, таких как, например, триэтиламин или поташ. Процесс циклизации полученных N-замещенных 4-аминомасляных кислот проводят также в среде органического растворителя в присутствии катализатора (ТБАБ, 2-оксипиридин). Авторы патента отмечают возможность циклизации полученных соединений при низких температурах, в том случае, если речь идет об использовании хлорангидридов 4-галогенбутановых кислот, так как в этом случае для отщепления молекулы хлороводорода достаточно добавить щелочной агент (Схема 7).
Схема 7

К недостаткам этого способа можно отнести необходимость отделения от раствора основного вещества примеси двойного продукта алкилирования 2-аминобутанамида, необходимость выделения технического продукта путем удаления растворителя при пониженном давлении и повторной кристаллизации. Очищение полупродуктов с использованием колоночной хроматографии и удаление воды с помощью молекулярного сита, а также использование измельченного или порошкообразного гидроксида калия делают этот способ крайне неудобным в условиях крупного производства.
Защищен способ получения 2-[4-гидрокси-2-оксо-1-пирролидинил]ацетамида (патент Испании 8601127. МКИ C07D 207/27, опубл. 16.02.1986), заключающийся во взаимодействии метилового эфира 3-гидрокси-4-аминомасляной кислоты с небольшим избытком амида моногалогенуксусной кислоты в ацетоне в присутствии поташа. Образующийся в ходе реакции метил 4-карбамоилметиламино-3-гидроксибутират без предварительной очистки циклизуют в среде органического растворителя с температурой кипения от 100 до 200°С (Схема 8).
Схема 8
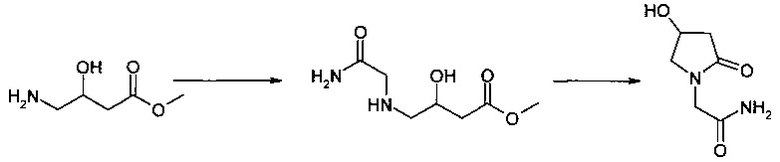
Учитывая способность N-алкилированных эфиров 4-аминомасляных кислот циклизоваться в N-алкил-2-оксопирролидины, был осуществлен [Химия гетероциклических соединений. 2012, №5. С. 775-778. М. Ворона, Г. Вейнберг и др.], синтез н-бутилового эфира 4-карбамоилметиламино-3-фенилмасляной кислоты и его циклизация в целевой продукт 2-[2-оксо-4-фенил-1-пирролидинил] ацетамид (Схема 9).
Схема 9
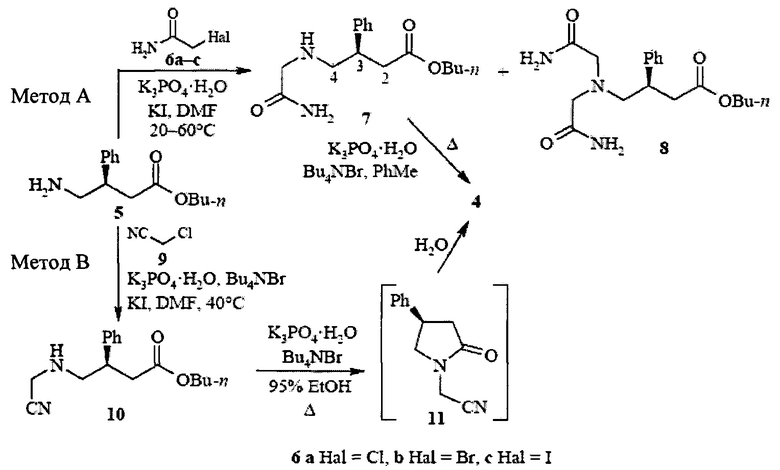
Авторы статьи алкилируют н-бутиловый эфир 4-аминомасляной кислоты галогензамещенными ацетамидами в присутствии фосфата калия моногидрата в полярном растворителе (ДМФА) при температуре от 20 до 60°C. Полученный таким образом н-бутил 4-карбамоилметиламино-3-фенилбутират циклизуют в конечный продукт 2-[2-оксо-4-фенил-1-пирролидинил] ацетамид с количественным выходом в среде толуола при температуре кипения в присутствии смеси фосфата калия моногидрата и тетрабутиламмония бромида. Чистое вещество получают, используя метод колоночной хроматографии или перекристаллизацией из воды, с выходом 63% и 48%, соответственно. В этой же статье описано использование хлорацетонитрила в качестве алкилирующего агента. Последующая за этим циклизация н-бутил 4-цианометиламино-3-фенилбутирата в среде 95%-ого этанола и гидролиз цианогруппы приводит к образованию 2-[2-оксо-4-фенил-1-пирролидинил] ацетамида с выходом 44%.
Это описание является наиболее близким по технической сущности к разработанному новому способу получения 4-замещенного 2-[2-оксо-1-пирролидинил]ацетамида.
Задача изобретения - создание нового, безопасного и технологичного способа получения 4-замещенного 2-[2-оксо-1-пирролидинил]ацетамида с использованием доступного сырья, применимого не только в лабораторном синтезе, но и в крупном промышленном производстве.
Сущность изобретения состоит в том, что разработан способ получения 2-[2-оксо-1-пирролидинил]ацетамида, замещенного в положении 4 пирролидинового цикла, включающий взаимодействие производного 4-аминомасляной кислоты в среде растворителя с галогензамещенным ацетамидом, с последующей циклизацией и выделением, отличающийся тем, что 2-[2-оксо-1-пирролидинил]ацетамид, замещенный в положении 4 пирролидинового цикла представляет собой соединение формулы
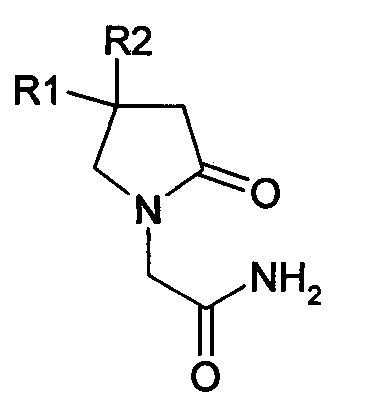
где
R1 обозначает Н,
R2 выбирают из Н, Ph, 2,4-диClPh, 4-ClPh, 4-CH3OPh, 3-NO2Ph;
или R1 и R2 совместно образуют С5Н10,
в качестве производного 4-аминомасляной кислоты используют калиевую соль 3-R1R2-4-аминомасляной кислоты, которая взаимодействует с хлорацетамидом в мольном соотношении 2:1 в спиртовой среде, затем выделяют N-карбамоилметил-3-R1R2-4-аминомасляную кислоту подкислением, с последующей ее циклизацией в среде высококипящего несмешивающегося с водой органического растворителя с температурой кипения от 140 до 200°C и отгонкой воды.
Описываемый процесс представлен на схеме:
Схема 10
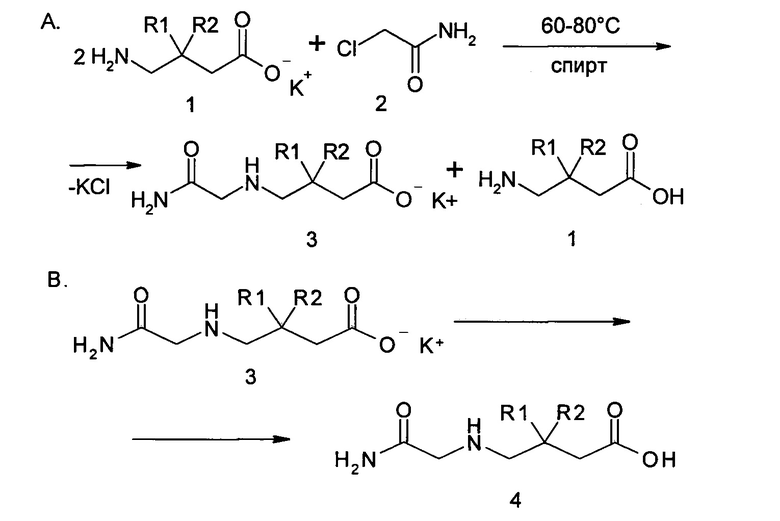
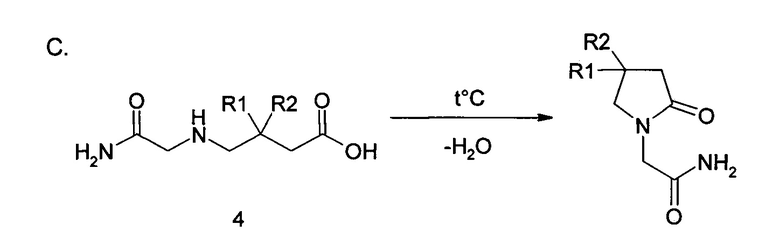
Таким образом, способ включает следующие стадии:
I. N-алкилирование 2 моль калиевой соли 3-R1R2-4-аминомасляной кислоты (1) 1 моль хлорацетамида (2) в спиртовой среде при температуре от 60 до 80°. (А)
II. Выделение фильтрацией от выпавшей в ходе нейтрализации 3-R1R2-4-аминомасляной кислоты (1) и/или образовавшегося в ходе реакции хлорида калия. (А)
III. Выделение из фильтрата промежуточного соединения N-карбамоилметил-3-R1R2-4-аминомасляной кислоты (4) из соответствующей калиевой соли (3) подкислением. (В)
IV. Циклизация полученной N-карбамоилметил-3-R1R2-4-аминомасляной кислоты (4) в среде высококипящего несмешивающегося с водой органического растворителя с температурой кипения от 140°C до 200°C, с отгонкой образующейся в ходе реакции воды. (С)
3-R1R2-4-аминомасляная кислота находится в растворе в виде цвиттер-иона или внутренней соли:
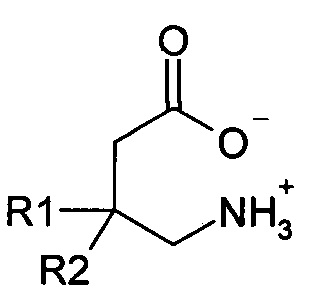
В таком виде нуклеофильность аминогруппы подавлена, вследствие чего, вещество не склонно вступать в реакцию N-алкилирования.
Для подавления образования внутренней соли 3-R1R2-4-аминомасляную кислоту можно перевести в эфир, как это было описано ранее, однако, нами был использован иной подход, а именно - использование калиевой соли 3-R1R2-4-аминомасляной кислоты в качестве исходного вещества.
Таким образом, аминогруппа становится свободной и легко вступает в реакцию с хлорацетамидом. При этом отсутствует опасность замыкания 4-аминомасляной кислоты в 2-оксипирролидин (как это часто случается при использовании эфиров 4-аминомасляных кислот), поскольку карбоксильная группа полностью инактивирована и не может взаимодействовать с аминогруппой.
К новизне разработанного нами метода относится и то, что в реакции N-алкилирования участвуют 2 моля 3-R1R2-4-аминомасляной кислоты в виде калиевой соли, рассчитан расход 1 моль непосредственно на реакцию алкилирования хлорацетамидом, еще 1 моль служит основанием для нейтрализации выделяющегося в ходе реакции алкилирования хлороводорода. В итоге в ходе нейтрализации выделяется осадок хлорида калия и/или осадок 3-R1R2-4-аминомасляной кислоты, последнюю можно использовать повторно.
Поскольку процесс идет в растворе, выбор калиевой щелочи определяется растворимостью получаемой соли 3-R1R2-4-аминомасляной кислоты в спиртах. В качестве растворителя может выступать этанол, изопропанол или смесь этих спиртов. Объем спирта берут из соотношения 4-9 мл спирта на 1 грамм 3-R1R2-4-аминомасляной кислоты. Время процесса составляет 2-4 часа при температуре 60-80°C.
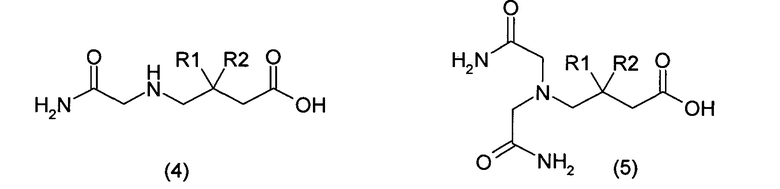
Еще одним преимуществом (нигде ранее не описанном) использования в качестве исходного сырья 3-R1R2-4-аминомасляной кислоты в виде калиевой соли состоит в том, что образующиеся полупродукты - калиевые соли N-карбамоилметил-3-R1R2-4-аминомасляной кислоты и N,N-бис(карбамоилметил)-3-R1R2-4-аминомасляной кислоты растворяются в спиртах. В то же время соответствующие им кислоты имеют существенное различие в растворимости.
Таким образом, после подкисления раствора выделяется только N-карбамоилметил-3-R1R2-4-аминомасляной кислота (4), в то время как N,N-бис(карбамоилметил)-3-R1R2-4-аминомасляная кислота остается в растворе (5). Выделившийся продукт можно отфильтровать, промыть и высушить. Таким образом, решается проблема выделения и очистки полупродуктов без применения вакуумной перегонки и колоночной хроматографии.
Выделенную N-карбамоилметил-3-R1R2-4-аминомасляную кислоту суспендируют в любом несмешивающемся с водой органическом растворителе с температурой кипения от 140 до 200°C для проведения процесса циклизации (например, о-ксилол, анизол, мезителен, фенетол, о-дихлорбензол). Преимуществом нашего способа является то, что выделяющаяся в процессе циклизации вода легко удаляется из реакционной массы путем азеотропной отгонки. При этом в отличие от описанных ранее способов, регенерация растворителя не представляет трудностей, так как удалить воду из органического растворителя значительно проще и не требуется применения ректификации. Все используемые растворители легкодоступны, так как являются крупнотоннажным сырьем.
Образующийся продукт кристаллизуют при комнатной температуре. Выделенный продукт представляет собой 2-[2-оксо-4-R1R2-1-пирролидинил] ацетамид. Таким образом, выделение конечного продукта не требует специальных приемов и многоступенчатых перекристаллизаций.
Выделенный по данному способу 2-[2-оксо-4-R1R2-1-пирролидинил] ацетамид может быть использован для дальнейших целей без предварительной очистки.
Учитывая вышесказанное, можно сделать вывод о том, что авторами патента была достигнута цель по разработке нового, безопасного и технологичного способа получения 4-замещенного 2-[2-оксо-1-пирролидинил]ацетамида с использованием доступного сырья, применимого не только в лабораторном синтезе, но и в крупном промышленном производстве.
ПРИМЕРЫ ПРОВЕДЕНИЯ СПОСОБА
Все используемые растворители и реагенты, кроме исходных 3-R1R2-4-аминомасляных кислот, коммерчески доступны и имеют марку ч. или х.ч., 3-R1R2-4-аминомасляные кислоты могут быть получены отдельно любым из известных способов. Результаты проведения способа приведены в примерах и сведены в Таблицу 1.
Пример 1
1. Получение N-карбамоилметил-3-фенил-4-аминомасляной кислоты
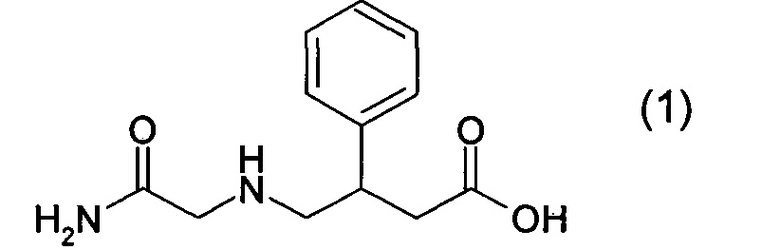
В трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником загружают 400 мл этанола и 17,04 г (0,273 моль) гидроксида калия (основное вещество 90%). Перемешивают до полного растворения. К полученному раствору загружают 50,00 г (0,279 моль) 3-фенил-4-аминомасляной кислоты, нагревают до 65°C и перемешивают до полного растворения. Затем загружают 12,72 г (0,136 моль) хлорацетамида. Смесь перемешивают при 65-70°C в течение 3 часов. По окончании выдержки суспензию охлаждают до комнатной температуры. Осадок 3-фенил-4-аминомасляной кислоты с примесью хлорида калия отфильтровывают, промывают этанолом. Смесь твердых продуктов промывают водой от хлористого калия, выделенную 3-фенил-4-аминомасляной кислоту промывают этанолом и используют повторно.
Фильтрат, содержащий калиевую соль N-карбамоилметил-3-фенил-4-аминомасляной кислоты, подкисляют 8,20 г (0,136 моль) уксусной кислоты. При комнатной температуре перемешивают 10-12 часов, осадок N-карбамоилметил-3-фенил-4-аминомасляной кислоты фильтруют (1) промывают на фильтре этанолом. Выход (1) 20,0 -20,6 г, 62-64% от теории.
2. Получение 2-[2-оксо-4-фенил-1-пирролидинил] ацетамида
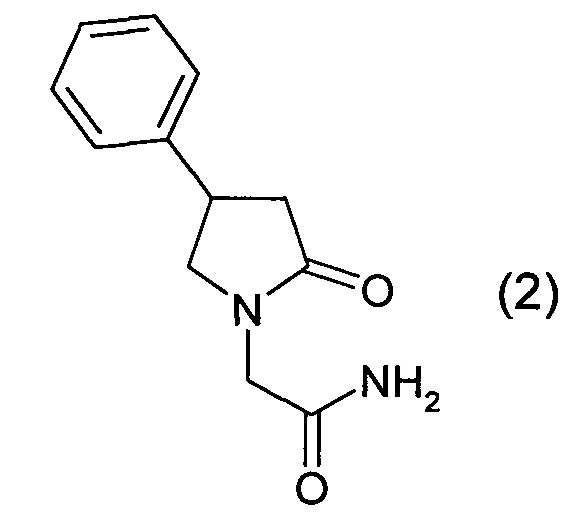
В колбу, загружают 40-45 мл анизола. Загружают N-карбамоилметил-3-фенил-4-аминомасляную кислоту (1), полученную ранее, включают нагрев и перемешивание. Суспензию греют до полного растворения твердого продукта. Процесс сопровождается отделением воды, которая удаляется из реакционной массы вместе с анизолом в виде азеотропа. Как только прекратилось отделение воды, отключают нагрев и оставляют массу на самоохлаждении. 2-[2-оксо-4-фенил-1-пирролидинил] ацетамид (2) выделяется из раствора в анизоле в течение нескольких часов при комнатной температуре, продукт отфильтровывают, промывают и сушат при температуре 70-80°C. Выход (2) 17,6-18,2 г, 95-97%, tпл=130-131°C.
Пример 2
1. Получение {1-[(карбамоилметиламино)метил]-циклогексил} уксусной кислоты
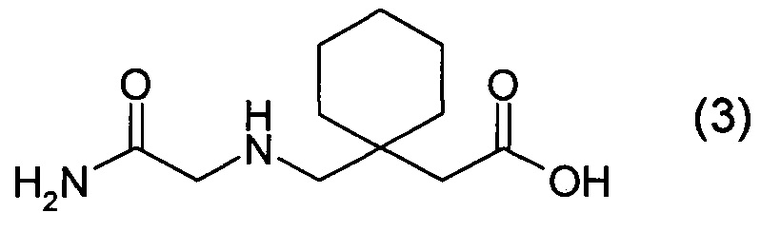
В трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником загружают 250 мл изопропанола и 18,00 г (0,289 моль) гидроксида калия (основное вещество 90%). Перемешивают до полного растворения при небольшом нагревании. К полученному раствору загружают 50,00 г (0,292 моль) (1-аминометил-циклогексил) уксусной кислоты, нагревают до 60°C и перемешивают до полного растворения. Затем загружают 13,50 г (0,144 моль) хлорацетамида. Смесь перемешивают при 75-80°C в течение 4 часов. По окончании выдержки суспензию охлаждают до комнатной температуры, фильтруют от хлорида калия.
Фильтрат, содержащий калиевую соль {1-[(карбамоилметиламино)метил]-циклогексил} уксусной кислоты, разбавляют 500 мл ацетона, подкисляют 8,65 г (0,144 моль) уксусной кислоты, охлаждают до -5°C и оставляют при этой температуре на сутки. Через 24 часа выпадает осадок (1-аминометил-циклогексил) уксусной кислоты. Осадок отфильтровывают, промывают ацетоном и сушат. Высушенный осадок (1-аминометил-циклогексил) уксусной кислоты можно использовать повторно.
Фильтрат, содержащий {1-[(карбамоилметиламино)метил]-циклогексил} уксусную кислотыу (3), концентрируют под вакуумом до 25% от объема первоначального раствора. Кубовый остаток охлаждают до -5°C в течение 24 часов. Выпавший осадок 1-[(карбамоилметил-амино)-метил]циклогексил уксусной кислоты (3) отфильтровывают, промывают ацетоном. Выход (3) 28,7 г, 80% от теории.
2. Получение 2-(3-оксо-2-аза-спиро[4.5]дец-2-ил)ацетамида
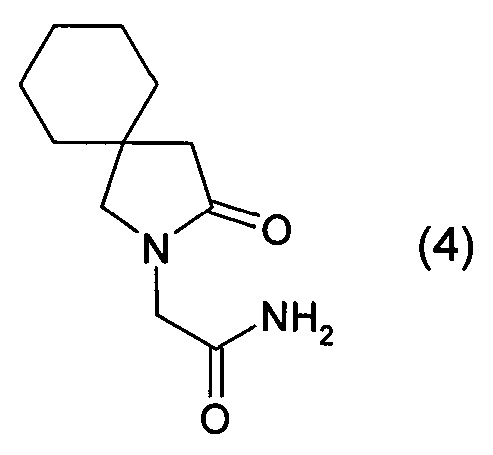
Процесс циклизации проводили аналогично получению соединения (2) в Примере 1, но вместо анизола использовали о-ксилол. Выход (4) 21 г, 83%, tпл=141,5-142,5°C.
Пример 3
1. Получение N-карбамоилметил-4-аминомасляной кислоты
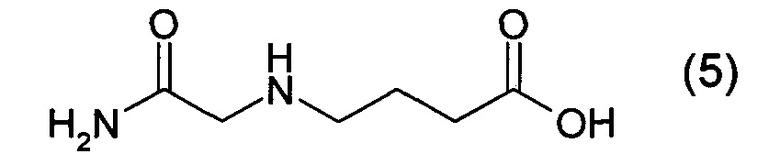
В трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником загружают 50 мл изопропанола и 100 мл этанола. К смеси спиртов загружают 12,00 г (0,192 моль) гидроксида калия (содержание основного вещества 90%). Перемешивают до полного растворения при небольшом нагревании. К полученному раствору загружают 20,00 г (0,194 моль) 4-аминомасляной кислоты (ГАМК), нагревают до 65°C и перемешивают до полного растворения. Затем загружают 9,00 г (0,096 моль) хлорацетамида. Смесь перемешивают при 65-70°C в течение 4 часов. По окончании выдержки суспензию охлаждают до 18°C и фильтруют осадок ГАМК с примесью хлорида калия.
Фильтрат, содержащий калиевую соль N-карбамоилметил-4-аминомасляной кислоты, подкисляют 11,53 г (0,192 моль) уксусной кислоты. Выпадает осадок N-карбамоилметил-4-аминомасляной кислоты (5) в виде уксуснокислой соли. Суспензию оставляют при комнатной температуре на 10-12 часов, затем фильтруют, осадок ацетата N-карбамоилметил-4-аминомасляной кислоты промывают на фильтре изопропанолом и сушат при температуре 65-70°С. Выход (5) 16,0 г, 62-64% от теории.
2. Получение 2-[2-оксо-1-пирролидинил] ацетамида

Данные приведены в Таблице 1.
Пример 4
1. Получение N-карбамоилметил-3-(4-хлорфенил)-4-аминомасляной кислоты
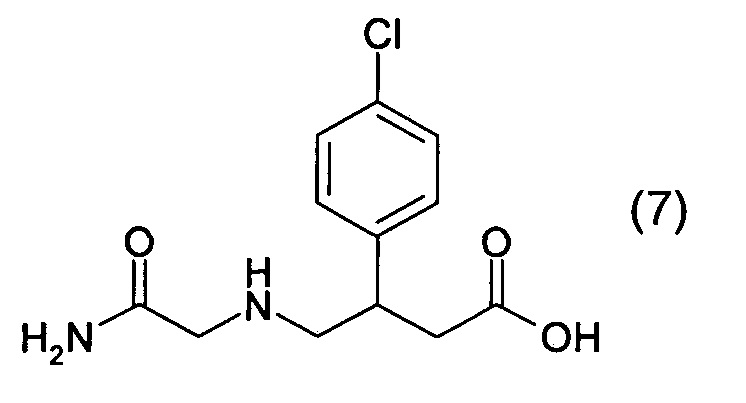
В трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником загружают 400 мл этанола и 14,40 г (0,233 моль) гидроксида калия (содержание основного вещества 90,7%). Перемешивают до полного растворения при небольшом нагревании. К полученному раствору загружают 50,00 г (0,234 моль) 3-(4-хлорфенил)-4-аминомасляной кислоты, нагревают до 65°C и перемешивают до полного растворения. Затем загружают 10,89 г (0,116 моль) хлорацетамида. Смесь перемешивают при 65-70°C в течение 3 часов. По окончании выдержки суспензию охлаждают до комнатной температуры. Осадок 3-(4-хлорфенил)-4-аминомасляной кислоты с примесью хлорида калия отфильтровывают, промывают спиртом. Смесь твердых продуктов промывают водой от хлористого калия, выделенную 3-(4-хлорфенил)-4-аминомасляную кислоту промывают этанолом и используют повторно.
Фильтрат, содержащий калиевую соль N-карбамоилметил-3-(4-хлорфенил)-4-аминомасляной кислоты, подкисляют 7,00 г (0,116 моль) уксусной кислоты. Выпадает осадок N-карбамоилметил-3-(4-хлорфенил)-4-аминомасляной кислоты (7). Суспензию оставляют при комнатной температуре на 10-12 часов, затем фильтруют, осадок N-карбамоилметил-3-фенил-4-аминомасляной кислоты (7) промывают на фильтре этанолом и сушат при температуре 65-70°C. Выход (7) 16,5-17,0 г, 52-53% от теории.
2. Получение 2-[2-оксо-4-(4-хлорфенил)-1-пирролидинил] ацетамида
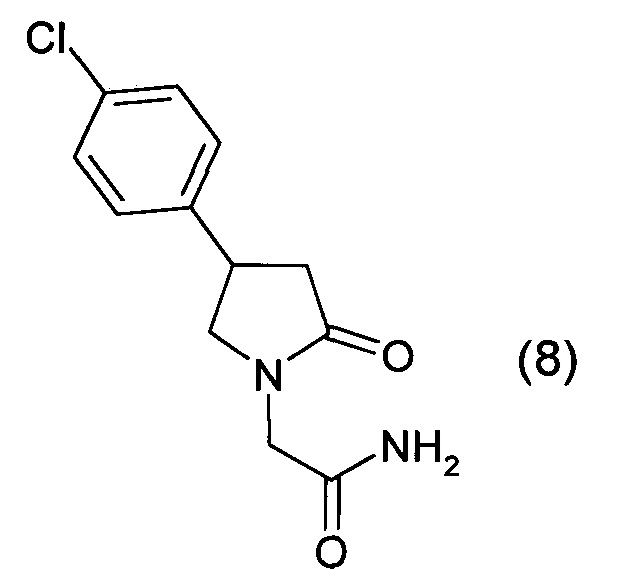
Данный приведены в Таблице 1.
Пример 5
1. Получение N-карбамоилметил-4-(4-метоксифенил)-4-аминомасляной кислоты
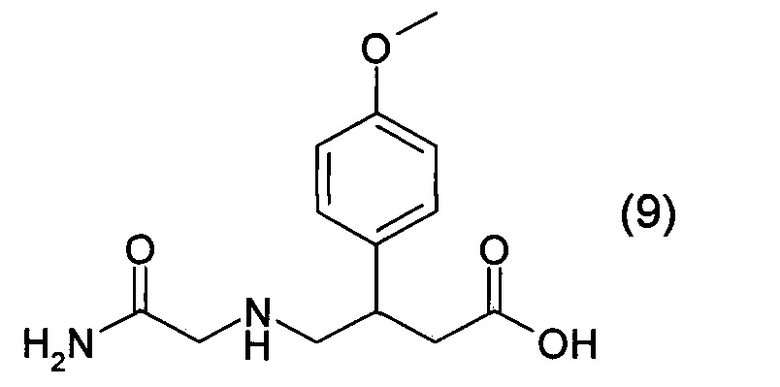
В трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником загружают 270 мл этанола, 135 мл изопропанола и 14,72 г (0,238 моль) гидроксида калия (содержание основного вещества 90,7%). Перемешивают до полного растворения при небольшом нагревании. К полученному раствору загружают 50,00 г (0,239 моль) 3-(4-метоксифенил)-4-аминомасляной кислоты, нагревают до 65°C и перемешивают до полного растворения. Затем загружают 11,13 г (0,119 моль) хлорацетамида. Смесь перемешивают при 65-70°C в течение 3 часов. По окончании выдержки суспензию охлаждают до комнатной температуры. Осадок 3-(4-метоксифенил)-4-аминомасляной кислоты с примесью хлорида калия отфильтровывают, промывают изопропанолом. Смесь твердых продуктов промывают водой от хлористого калия, выделенную 3-(4-метоксифенил)-4-аминомасляную кислоту промывают этанолом и используют повторно.
Фильтрат, содержащий калиевую соль N-карбамоилметил-3-(4-метоксифенил)-4-аминомасляной кислоты, подкисляют 7,14 г (0,119 моль) уксусной кислоты. Выпадает осадок N-карбамоилметил-3-(4-метоксифенил)-4-аминомасляной кислоты (9). Суспензию оставляют при комнатной температуре на 12-15 часов, затем фильтруют, осадок N-карбамоилметил-3-(4-метоксифенил)-4-аминомасляной кислоты (9) промывают на фильтре изопропанолом и сушат при температуре 65-70°C. Выход (9) 25,5-26,0 г, 68-70% от теории.
2. Получение 2-[2-оксо-4-(4-метоксифенил)-1-пирролидинил] ацетамида

Данные приведены в Таблице 1.
Пример 6
1. Получение N-карбамоилметил-3-(2,4-дихлорфенил)-4-аминомасляной кислоты

В трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником загружают 270 мл этанола, 135 мл изопропанола и 12,40 г (0,200 моль) гидроксида калия (содержание основного вещества 90,7%). Перемешивают до полного растворения при небольшом нагревании. К полученному раствору загружают 50,00 г (0,201 моль) 3-(2,4-дихлорфенил)-4-аминомасляной кислоты, нагревают до 65°C и перемешивают до полного растворения. Затем загружают 9,35 г (0,100 моль) хлорацетамида. Смесь перемешивают при 65-70°С в течение 3 часов. По окончании выдержки суспензию охлаждают до комнатной температуры. Осадок 3-(2,4-дихлорфенил)-4-аминомасляной кислоты с примесью хлорида калия отфильтровывают,промывают изопропанолом. Смесь твердых продуктов промывают водой от хлористого калия, выделенную 3-(2,4-дихлорфенил)-4-аминомасляную кислоту промывают этанолом и используют повторно.
Фильтрат, содержащий калиевую соль N-карбамоилметил-3-(2,4-дихлорфенил)-4-аминомасляной кислоты, подкисляют 6,00 г (0,100 моль) уксусной кислоты. Выпадает осадок N-карбамоилметил-3-(2,4-дихлорфенил)-4-аминомасляной кислоты (11). Суспензию оставляют при комнатной температуре на 10-12 часов, затем фильтруют, осадок N-карбамоилметил-3-(2,4-дихлорфенил)-4-аминомасляной кислоты промывают на фильтре этанолом и сушат при температуре 65-70°C. Выход (11) 15,0-16,0 г, 50-51% от теории.
2. Получение 2-[2-оксо-4-(2,4-дихлорфенил)-1-пирролидинил] ацетамида
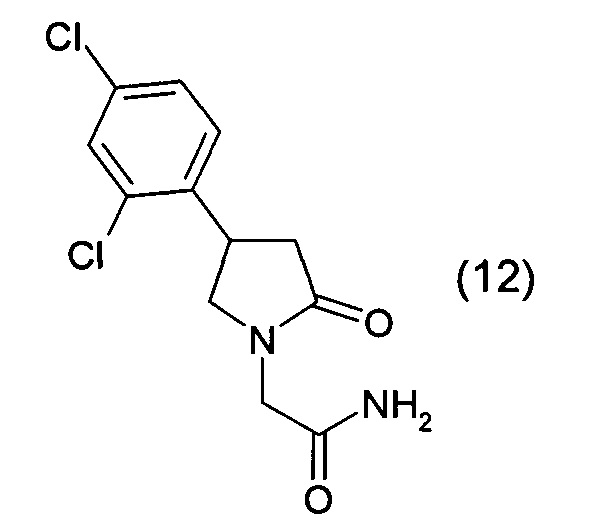
Данные приведены в Таблице 1.
Пример 7
1. Получение N-карбамоилметил-3-(3-нитрофенил)-4-аминомасляной кислоты

В трехгорлую колбу, снабженную мешалкой, термометром и обратным холодильником загружают 300 мл этанола и 150 мл изопропанола и 13,65 г (0,221 моль) гидроксида калия (содержание основного вещества 90,7%). Перемешивают до полного растворения при небольшом нагревании. К полученному раствору загружают 50,00 г (0,223 моль) 3-(3-нитрофенил)-4-аминомасляной кислоты, нагревают до 65°C и перемешивают до полного растворения. Затем загружают 10,33 г (0,110 моль) хлорацетамида. Смесь перемешивают при 75-80°C в течение 3 часов. По окончании выдержки суспензию охлаждают до комнатной температуры. Осадок 3-(3-нитрофенил)-4-аминомасляной кислоты с примесью хлорида калия отфильтровывают, промывают спиртом. Смесь твердых продуктов промывают водой от хлористого калия, выделенную 3-(3-нитрофенил)-4-аминомасляную кислоту промывают этанолом и используют повторно.
Фильтрат, содержащий калиевую соль N-карбамоилметил-3-(3-нитрофенил)-4-аминомасляной кислоты, подкисляют 6,60 г (0,110 моль) уксусной кислоты. Выпадает осадок N-карбамоилметил-3-(3-нитрофенил)-4-аминомасляной кислоты (13). Суспензию оставляют при комнатной температуре на 10-12 часов, затем фильтруют, осадок N-карбамоилметил-3-(3-нитрофенил)-4-аминомасляной кислоты промывают на фильтре этанолом и сушат при температуре 65-70°C. Выход (13) 20,0-21,0 г, 69-71% от теории.
2. Получение 2-[2-оксо-4-(3-нитрофенил)-1-пирролидинил] ацетамида
Данные приведены в Таблице 1.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ФОНТУРАЦЕТАМА ИЗ ФЕНИБУТА | 2024 |
|
RU2827339C1 |
| АМИДЫ АМИНОКАРБОНОВЫХ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2134683C1 |
| СПОСОБ ПОЛУЧЕНИЯ 1-КАРБАМОИЛМЕТИЛ-4-ФЕНИЛ-2-ПИРРОЛИДОНА | 2017 |
|
RU2663899C1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛОРОДСОДЕРЖАЩЕГО ПРОИЗВОДНОГО 6-ГАЛОГЕНХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2 | 2021 |
|
RU2827892C1 |
| ПРИМЕНЕНИЕ КИСЛОРОДСОДЕРЖАЩЕГО ПРОИЗВОДНОГО 6-ГАЛОГЕНХИНОЛИНА ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2021 |
|
RU2780245C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ВКЛЮЧАЮЩАЯ КИСЛОРОДСОДЕРЖАЩЕЕ ПРОИЗВОДНОЕ 6-ГАЛОГЕНХИНОЛИНА, ДЛЯ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ БЕТА-КОРОНАВИРУСОВ, ВКЛЮЧАЯ SARS-COV-2, И СПОСОБ ЕЕ ПРИМЕНЕНИЯ | 2021 |
|
RU2827893C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2 КАРБАМИД- ,3-ОКСИБЕНЗОФУРАНА | 1972 |
|
SU332626A1 |
| СПОСОБ ПОЛУЧЕНИЯ {2-[4-(АЛЬФА-ФЕНИЛ-П-ХЛОРБЕНЗИЛ)ПИПЕРАЗИН-1-ИЛ]-ЭТОКСИ}-УКСУСНОЙ КИСЛОТЫ И НОВЫЕ ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 2000 |
|
RU2248974C2 |
| Новый состав N-карбамоилметил-4-фенил-2-пирролидона | 2017 |
|
RU2696277C2 |
| ПРОИЗВОДНЫЕ ИМИДАЗОПИРИДИНОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1995 |
|
RU2156251C2 |
Изобретение относится к способу получения 2-[2-оксо-1-пирролидинил]ацетамида, замещенного в положении 4 пирролидинового цикла, в котором R1 обозначает Н, R2 выбирают из Н, Ph, 2,4-диClPh, 4-ClPh, 4-CH3OPh, 3-NO2Ph; или R1 и R2 совместно образуют С5Н10. Способ заключается во взаимодействии калиевой соли 3-R1R2-4-аминомасляной кислоты с хлорацетамидом в мольном соотношении 2:1 в спиртовой среде, выделении N-карбамоилметил-3-R1R2-4-аминомасляной кислоты подкислением, с последующей ее циклизацией в среде высококипящего несмешивающегося с водой органического растворителя с температурой кипения от 140 до 200°C и отгонкой воды. Способ безопасен и технологичен, использует доступное сырье и может применяться в крупном промышленном производстве. 1 з.п. ф-лы, 1 табл., 7 пр.

1. Способ получения 2-[2-оксо-1-пирролидинил]ацетамида, замещенного в положении 4 пирролидинового цикла, включающий взаимодействие производного 4-аминомасляной кислоты в среде растворителя с галогензамещенным ацетамидом, с последующей циклизацией и выделением, отличающийся тем, что 2-[2-оксо-1-пирролидинил]ацетамид, замещенный в положении 4 пирролидинового цикла представляет собой соединение формулы
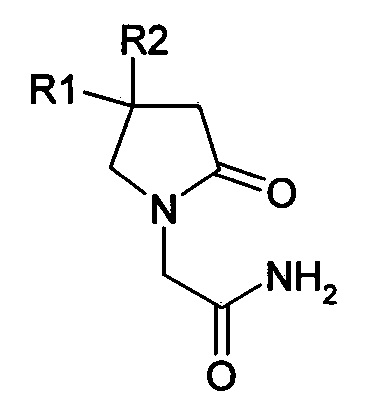
где R1 обозначает Н,
R2 выбирают из Н, Ph, 2,4-диClPh, 4-ClPh, 4-CH3OPh, 3-NO2Ph;
или R1 и R2 совместно образуют С5Н10,
в качестве производного 4-аминомасляной кислоты используют калиевую соль 3-R1R2-4-аминомасляной кислоты, которая взаимодействует с хлорацетамидом в мольном соотношении 2:1 в спиртовой среде, затем выделяют N-карбамоилметил-3-R1R2-4-аминомасляную кислоту подкислением, с последующей ее циклизацией в среде высококипящего несмешивающегося с водой органического растворителя с температурой кипения от 140 до 200°C и отгонкой воды.
2. Способ по п. 1, отличающийся тем, что получение 2-[2-оксо-4-фенил-1-пирролидинил]ацетамида проводят взаимодействием калиевой соли 3-фенил-4-аминомасляной кислоты с хлорацетамидом в среде этанола.
| Способ получения 2-оксопирролидин-N-алкиламидов | 1977 |
|
SU893131A3 |
| ПРОИЗВОДНЫЕ 2-ОКСО-1-ПИРРОЛИДИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ | 2001 |
|
RU2291860C2 |
| US 4228179 A1, 14.10.1980 | |||
| Циркуляционный клапан | 1982 |
|
SU1059137A2 |
| Vorona, M.et al "Novel methods for the synthesis of 2-[(4R)-2-oxo-4-phenylpyrrolidin-1-yl]-acetamide ((R)-phenotropil)." Chemistry of Heterocyclic Compounds 2012 (New York, NY, United States), 48(5), 720-723 (English). | |||
Авторы
Даты
2017-08-24—Публикация
2016-06-14—Подача