Заявляемая группа изобретений относится к области медицины, в частности к терапии онкологических заболеваний. Терапия занимает важное место в лечении, например, колоректального рака, и одним из основных средств ее является химиотерапия. Применяемые в настоящее время средства химиотерапии характеризуются не высокой эффективностью, но весьма значимой токсичностью, ограничивающей возможности длительного воздействия на опухоль. Наиболее современным средством в настоящее время является так называемая таргетная терапия, направленная на блокирование проявления конкретных генов. Препараты таргетной терапии (от английского слова target - цель, мишень) - созданный относительно недавно класс противоопухолевых лекарств, которые обладают способностью избирательно воздействовать на патогенетические молекулярные мишени. Известные способы и средства таргетной терапии для блокирования отдельных генов также несовершенны. Применение существующих коммерческих таргетных препаратов в качестве монотерапии далеко не всегда дает существенный эффект. Это привело к включению таких препаратов в состав комплексной терапии, сочетающей стандартные химиотерапевтические воздействия с применением таргетных препаратов.
Часть таргетных препаратов является малыми молекулами. К их недостаткам относится малая специфичность, что приводит к существенным неспецифическим эффектам, обусловливающим токсичность. В своем большинстве такие препараты являются антителами к белкам, кодируемым генами. Такие антитела являются инородными для организма веществами, имеют неполную специфичность и обладают большими размерами, затрудняющими их доставку к белку-мишени. Указанные свойства приводят к значительным побочным эффектам и недостаточной эффективности имеющихся таргетных препаратов. В противоположность этому, миРНК - природные вещества, функционирующие в клетках человека (и других млекопитающих). Искусственно введенные миРНК не будут инородными для организма веществами. Как природные, так и синтезированные миРНК обладают абсолютной специфичностью, позволяющей воздействовать именно на те гены, функция которых должна быть ингибирована. Они имеют малые размеры, облегчающие их эффективную доставку в раковую клетку. Кроме того, миРНК прерывают процесс функционального проявления генов на более ранней стадии, до синтеза белков, количество которых значительно больше, чем матричной РНК. Вследствие этого требуются меньшие количества вводимых в организм больного веществ.
Таргетные препараты, разработанные специально для применения совместно со стандартными химиопрепаратами, в настоящее время отсутствуют. В связи с этим актуально развитие новых таргетных препаратов и поиск альтернативных лечебных подходов. Одним из таких подходов является выявление генов, ингибирование которых способно приводить не только к снижению жизнеспособности раковой клетки, но и к усилению чувствительности опухоли к стандартному химиотерапевтическому лечению. Настоящее изобретение основано на новых подходах, базирующихся на последних достижениях «постгеномной эры».
Известен способ модулирования функции и/или экспрессии гена-супрессора опухолей в клетках или тканях млекопитающих in vivo или in vitro, включающий контактирование указанных клеток или тканей с по меньшей мере одним олигонуклеотидом короткой интерферирующей РНК (миРНК) длиной от 5 до 30 нуклеотидов, являющейся специфичной в отношении антисмыслового полинуклеотида гена-супрессора опухолей. Ген-супрессор опухолей (антионкоген, опухолевый супрессор) - ген, продукт которого обеспечивает профилактику опухолевой трансформации клеток. Белковые продукты генов-супрессоров называют белками-супрессорами или антионкобелками. Кроме того, антионкогены могут кодировать и микроРНК (RU №2011127196).
Известен многопрофильный промотор, обеспечивающий внутри раковых клеток экспрессию гена фермента, способного превращать внутри раковых клеток, но не в нормальных клетках, нетоксичное соединение - пролекарство в токсин, содержащий измененную или расширенную, по сравнению с известными промоторами, совокупность участков узнавания белков-факторов транскрипции, необходимый набор которых существует в большинстве раковых, но не в нормальных клетках, и представляющий тандемную комбинацию BIRC5 и TERT промоторов или производное тандемной комбинации BIRC5 и TERT промоторов, образованное в результате делении, замены, инсерции или иной мутации промотора, не влияющих на активность промотора, но при этом меняющих его структуру. Экспрессирующий вектор содержит многофункциональный промотор, соединенный с транскрибируемой последовательностью, которая при транскрипции продуцирует информационную РНК, кодирующую фермент, превращающий нетоксичное - пролекарство во внутриклеточный токсин. Экспрессирующий вектор представляет собой вирусный вектор или невирусный вектор. Там же известен способ избирательного убийства раковых, но не нормальных клеток, приводящий к синтезу токсинов внутри раковых клеток, включающий доставку в опухоль генной конструкции, состоящей из гена фермента, способного превращать внутри раковой клетки нетоксическое соединение - пролекарство в токсин, и многопрофильного промотора, или доставку двух генных конструкций, одна из которых состоит из гена фермента, способного превращать внутри раковой клетки нетоксичное соединение - пролекарство в токсин, и блокированного промотора, при деблокировании обеспечивающего экспрессию этого гена, а вторая является деблокирующей конструкцией, содержащей многопрофильный промотор, присоединенный к гену деблокатора, кодирующего белок деблокатор, способный деблокировать неактивный блокированный промотор, при этом синтезируемый внутри раковой клетки токсин диффундирует в окружающие раковые клетки (RU №2476596).
Известен способ индукции апоптоза в клетке-мишени и средство, в котором выделенная двухцепочечная молекула РНК, которая, по существу, соответствует части нуклеотидной последовательности мишеневой нуклеиновой кислоты, где каждая цепь РНК имеет длину 23 нуклеотида и, по меньшей мере, одна цепь имеет 3'-выступ из 1-5 нуклеотидов, причем указанная молекула РНК способна к мишень-специфической РНК-интерференции (RU №2470073).
Известна фармацевтическая композиция, содержащая дезинтегратор митоза/ингибитор биохимического пути polo-подобной киназы (Plk), в частности ON01910, ON01910-Na или миРНК, направленную на Plk1, и химиотерапевтический агент, представляющий собой нуклеотидный аналог, в эффективном количестве, а также фармацевтически и физиологически приемлемый носитель, для использования в качестве лекарственного средства для предупреждения развития резистентности к химиотерапевтическому агенту, представляющему собой нуклеотидный аналог, у субъекта, страдающего раком, или для использования в качестве лекарственного средства для лечения рака, резистентного к химиотерапевтическому агенту, представляющему собой нуклеотидный аналог, у нуждающегося в этом пациента. Химиотерапевтический агент представляет собой нуклеотидный аналог, выбран из группы, состоящей из кладрибина, клофарабина, флударабина, меркаптопурина, пентостатина, тиогуанина, капецитабина, цитарабина, децитабина, фторурацила, флоксуридина, сапацитабина и гемцитабина; или химиотерапевтический агент представляет собой нуклеотидный аналог, представляет собой гемцитабин (RU №2476239, прототип).
Недостатками известных способов и средств индукции апоптоза клеток злокачественной опухоли является недостаточная эффективность, большая длительность лечения до получения значимых результатов, высокая вероятность побочных явлений, характерных для химиотерапии, обусловленные тем, что в прототипе обеспечивают и оценивают снижение числа клеток, что может быть связано со снижением пролиферации, т.е. скорости размножения раковых клеток. Для этого, блокируя ген, увеличивают чувствительность к химиотерапии при ее стандартных дозах. Это позиционируется как преодоление резистентности. Задача снижения дозы химиопрепаратов не решается. Апоптотическая гибель уже образовавшихся клеток опухоли применяемыми средствами не обеспечивается в достаточной для лечения мере и не определяется. Использование для ингибирования гена малых молекул может иметь недостаточную специфичность, что приведет к существенным неспецифическим эффектам, обусловливающим дополнительную токсичность.
Технической задачей группы изобретений является создание эффективных способа и средства индукции апоптоза клеток злокачественной опухоли, а также расширение арсенала способов и средств индукции апоптоза клеток злокачественной опухоли.
Технический результат, обеспечивающий решение поставленной задачи, заключается в повышении эффективности, т.е. оптимизации и активизации воздействия платиносодержащего лекарственного средства на клетки опухоли колоректального рака за счет того, что блокированием соответствующих генов обеспечивается существенная апоптотическая гибель раковых клеток при дозе лекарственного средства, принципиально ниже стандартной. Таким образом, достигается снижение токсичности при сохранении или повышении эффективности терапии. Это достигается благодаря одновременному воздействию на конкретные антиапоптотические гены (ингибируемый ген-мишень, его мРНК, т.е. РНК-мишень) в клетке опухоли с помощью коротких петлевых интерферирующих РНК (миРНК, siRNA - small interfering RNA), что влечет за собой сокращение длительности лечения до получения значимых результатов, при снижении вероятности побочных явлений.
К числу широко используемых химиопрепаратов относятся производные платины, такие как цисплатин (цис-дихлородиамминплатина (II)), карбоплатин (Диамин [1,1-Циклобутандикарбоксилат]платина) и оксалиплатин ([(1R,2R)-1,2-Циклогександиамин-N,N'][оксалато(2)-O,O']платина), имеющие следующие химические структуры:
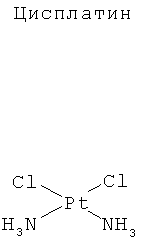
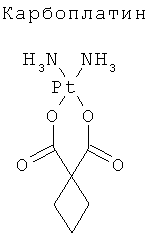
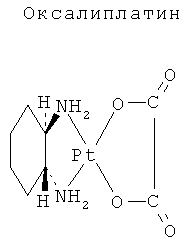
Все указанные соединения обладают сходным механизмом действия, обусловленным их способностью образовывать прочные специфические связи с ДНК, индуцирующие цитотоксичность.
Эти химиопрепараты имеют одинаковый механизм действия и применяются при широком круге онкологических заболеваний, включающих рак яичников, герминогенные опухоли у мужчин и женщин, рак легкого, злокачественные новообразования головы и шеи, рак шейки и тела матки, молочной железы, мочевого пузыря, саркома мягких тканей, меланома и колоректальный рак.
Однако указанные препараты при применении в стандартных дозировках обладают существенной токсичностью, ограничивающей их терапевтические возможности и наносящей вред организму человека. Токсические свойства указанных препаратов включают: желудочно-кишечные кровотечения, диарея, нарушение функции печени, тошнота, рвота, судороги, периферическая невропатия, неврит зрительного нерва, нарушения цветовосприятия, нарушение зрения, лейкопения, анемия, тромбоцитопения и др.
Снижение токсичности производных платины можно достичь снижением их дозировки. Обеспечение высокой эффективности терапевтического воздействия при низкой дозе химиопрепарата создаст существенный социально-экономический эффект в виде сохранения здоровья и деятельной жизни людей, сокращения затрат на лечение.
Применение выбранных малых интерферирующих РНК (миРНК) для подавления выбранных генов-мишеней является исходной основой технического результата, получаемого за счет использования заявляемого способа и противоопухолевого средства, позволяющего существенно снизить дозировку химиопрепарата - производного платины и, соответственно, свести к минимуму его побочное действие, при повышении эффективности терапии.
Сущность изобретения в части способа состоит в том, что способ индукции апоптоза клеток злокачественной опухоли колоректального рака предусматривает ингибирование функции генов клеток злокачественной опухоли с помощью препаратов малых интерферирующих РНК в присутствии химиотерапевтического платинового препарата, при котором производят ингибирование функции генов из группы: c-IAP2, Livin и МСМ4, для чего используют препараты малых интерферирующих миРНК-олигонуклеотидов из группы:
UGUGGACAAAGUCUCUUCCdTdT; CCUGUGGGUAAGAGAUGAGdTdT; UUCUCUCUCCUCUUCCCUUAdTdT.
Предпочтительно производят одновременное ингибирование функций двух генов из группы: C-IAP2, Livin и МСМ4, в одной из комбинаций генов: Livin и МСМ4; C-IAP2 и МСМ4; C-IAP2 и Livin, для чего используют препараты малых интерферирующих миРНК-олигонуклеотидов из группы:
UGUGGACAAAGUCUCUUCCdTdT; CCUGUGGGUAAGAGAUGAGdTdT; UUCUCUCUCCUCUUCCCUUAdTdT.
В частных случаях реализации производят одновременное ингибирование функций двух генов из группы: C-IAP2, Livin и МСМ4, в одной из комбинаций генов:
Livin и MCM4; C-IAP2 и МСМ4; C-IAP2 и Livin, для чего используют препараты малых интерферирующих миРНК-олигонуклеотидов в виде дуплексов прямой и обратной комплементарных цепей нуклеотидов следующей структуры:
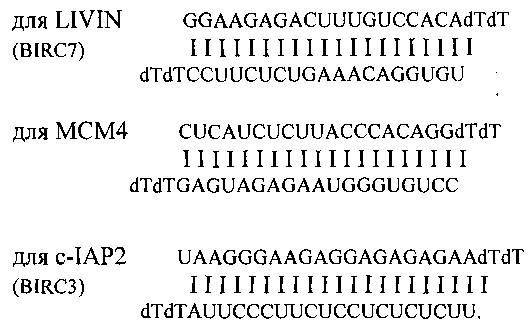
Как правило, используют миРНК дуплексы (duplex) синтезированные в прямом направлении (sense, (s)) и в обратном направлении (antisense, (as) на основе первичной структуры мРНК генов, выбранных из условия наибольшего подавления экспрессии гена при наименьшей концентрации миРНК, причем ингибирование функции двух генов клеток злокачественной опухоли осуществляют в присутствии химиотерапевтического препарата оксалиплатина.
Сущность изобретения в части средства состоит в том, что средство для осуществления вышеизложенного способа для индукции апоптоза клеток злокачественной опухоли колоректального рака содержит оксалиплатин и комбинацию комплементарных к мРНК в клетках злокачественной опухоли миРНК - олигонуклеотидов в виде коротких петлевых миРНК (shRNA), по меньшей мере, одной из следующих структур:
(Sense oligo)-CAAGAGA-(Antisense oligo), или:
(Sense oligo-dtdt)-(Sense oligo)-CAAGAGA-(Antisense oligo-dtdt)-(Antisense oligo), где: Sense oligo и Antisense oligo - пары олигонуклеотидов для каждого гена, (Sense oligo-dtdt) и (Antisense oligo-dtdt) - аналогичные последовательности РНК в парах олигонуклеотидов без dtdt.
Или:
(Antisense oligo-dtdt)-(Antisense oligo)-CAAGAGA-(Sense deoxyoligo-dtdt)-(Sense deoxyoligo), или:
CG-(Antisense deoxyoligo-dtdt)-(Antisense deoxyoligo)-CAAGAGA-(Sense deoxyoligo-dtdt)-(Sense deoxyoligo)-TTTTTTGGAAA, где: Antisense deoxyoligo и Sense deoxyoligo представляют собой последовательности нуклеотидов с заменой 8
рибонуклеотидов на дезоксирибонуклеотиды, (Antisense deoxyoligo-dtdt) и (Sense deoxyoligo-dtdt) - аналогичные последовательности ДНК в парах олигонуклеотидов без dtdt.
При этом (Sense oligo) и (Antisense oligo) выбираются в соответствии с ингибируемым геном из приведенных ниже:

Заявляемое средство выполнено в фармацевтической форме, пригодной для парентерального применения с целью индукции апоптоза клеток злокачественной опухоли колоректального рака.
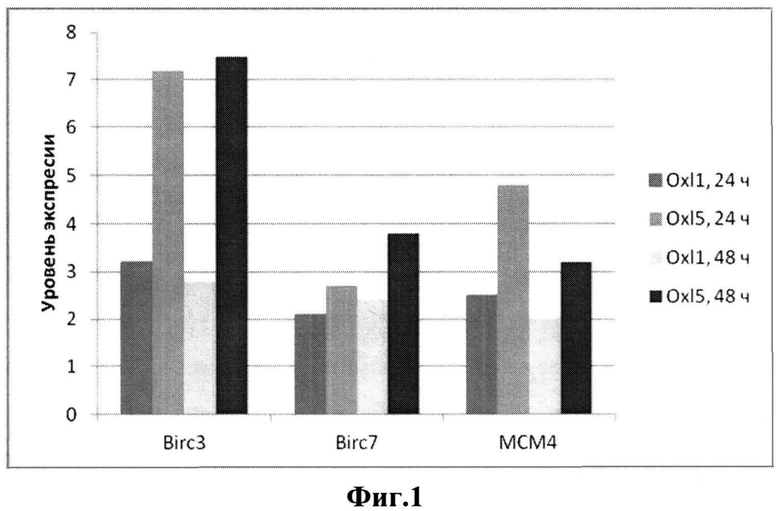
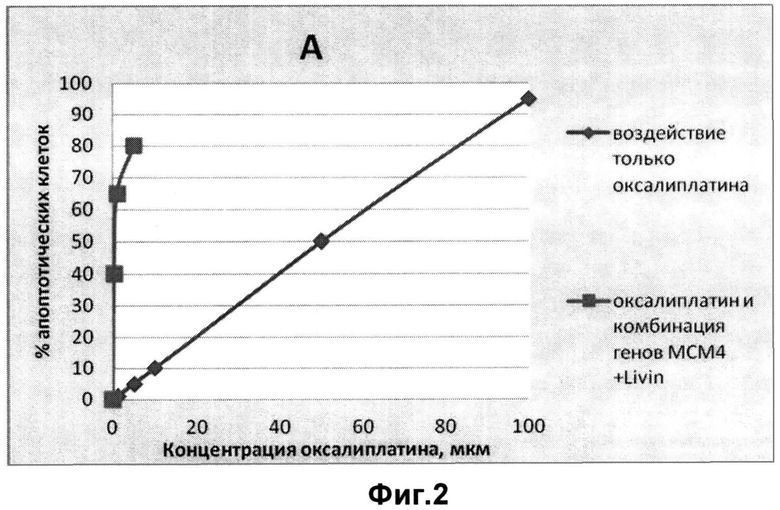
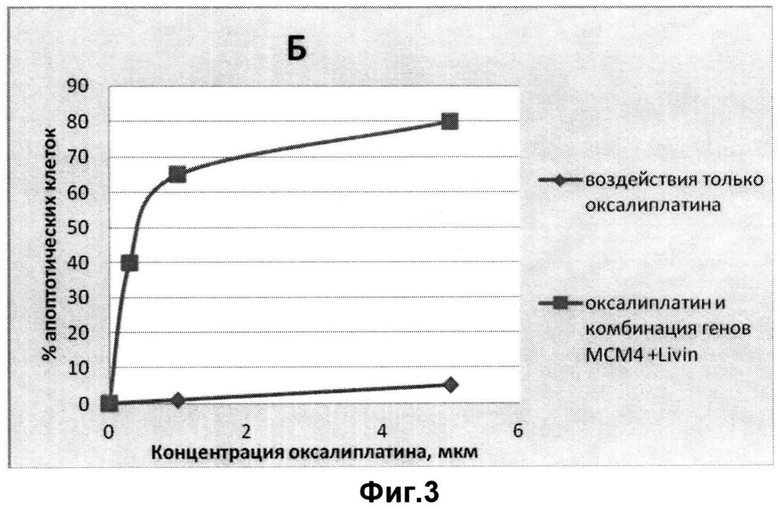
На чертеже фиг. 1. изображены диаграммы, демонстрирующие экспрессионный профиль генов C-IAP2 (BIRC3), Livin, (BIRC7) и МСМ4, в зависимости от времени и дозировки воздействия оксалиплатина (Ох) во временных интервалах 24 час и 48 часов. На фиг. 2, 3 изображены графики зависимости доли (%) апоптотических клеток в зависимости от концентрации оксалиплатина и наличия воздействия миРНК на гены Livin, и МСМ4. Графики с одними и теми же данными, но приведены фиг. 2, 3 в разных масштабах, на графике фиг. 2 приведен вид кривых, при концентрации оксалиплатина до 100 мкм, на графике фиг. 3 приведен вид кривых, при концентрации оксалиплатина до 5 мкм.
При этом технический результат заявляемых способа и средства основан на синергетическом действии апоптотического лекарственного платиносодержащего средства с одновременным блокированием неконтролируемого размножения раковых клеток, которое могло происходить в результате действия конкретных антиапоптотических генов клеток опухоли, с помощью конкретных выбранных миРНК, т.е. РНК-интерференции. В последние годы были обнаружены короткие фрагменты РНК (около 21-25 нуклеотидов), которые образованы из длинных молекул двухцепочечной РНК. Эти фрагменты называются малыми интерферирующими РНК (миРНК, siRNA - short interfering RNA). Такие миРНК в составе комплекса с белками образуют каталитические структуры, вызывающие направленную деградацию комплементарной им миРНК-мишени. Малые интерферирующие РНК (миРНК) или короткие интерферирующие РНК (англ. siRNA, small interfering RNA) - это класс двухцепочечных РНК, длиной 20-25 нуклеотидов. Малые интерферирующие РНК принимают участие в процессах РНК-интерференции (англ. RNAi), понижая экспрессию специфических генов. Интерферирующие РНК можно искусственно синтезировать и использовать для блокирования функции интересующего гена. Белки ингибиторы апоптоза - IAP (inhibitors of apoptosis proteins) играют очень важную роль в развитии апоптоза у большинства живых организмов. Достаточно часто клеточные мутации приводят к повышенной экспрессии генов ингибиторов апоптоза. Соответственно, мутантная раковая клетка не погибает, а начинает дальше размножаться. Индуцирование апоптоза в раковых клетках является одним из основных направлений в современной терапии рака. «Выключение» генов - ингибиторов апоптоза и их комбинаций должно приводить к запрограммированной гибели раковой клетки, особенно в условиях индукции апоптоза. Малые интерферирующие РНК (миРНК) обладают исключительной специфичностью действия по ингибированию функции генов. Молекулы миРНК в составе комплекса с белками образуют каталитические структуры, вызывающие направленную деградацию комплементарной им матричной РНК-мишени (мРНК). В результате настоящего изобретения сконструирован и синтезирован набор миРНК, внутриклеточными мишенями которых является ряд важных для жизнеспособности раковой клетки генов, включая антиапоптотические гены.
В соответствии с заявляемыми способом и средством предложена группа антиапоптотических генов, ингибирующих апоптоз клеток опухоли колоректального рака, и группа миРНК, блокирующее действие которых на указанные гены приводит к гибели клеток колоректального рака при действии малых доз платиносодержащего химиопрепарата (принципиально ниже терапевтических) за счет блокирования предложенных генов. Из трех генов: c-IAP2 (BIRC3), Livin, (BIRC7, ML-IAP) и МСМ4, миРНК для ингибирования которых используется в составе разрабатываемого средства, два - c-IAP2 и Livin - относятся к генам-ингибиторам апоптоза, преимущественно по внешнему и внутреннему путям, соответственно. Эти гены активируются в раковых клетках и слабо экспрессируются в нормальных тканях. Их блокирование устраняет функциональные препятствия на пути клетки в апоптоз при стрессовых условиях. Ген МСМ4 играет существенную роль в поддержании целостности генома, участвуя в процессе репликации ДНК и в остановке процесса деления клетки для репарации дефектов при нарушениях ДНК или остановке ее синтеза (checkpoint). Нарушение этих процессов ингибированием гена МСМ4 является критическим для жизнеспособности раковых клеток при дефектах ДНК, вызываемых, в частности, производными платины. Ингибирование указанных генов позволяет более чем на порядок величины уменьшить дозу химиопрепаратов - производных платины при сохранении вызываемого ими апоптотического эффекта раковых клеток, наблюдаемого при стандартной дозе.
Для подтверждения возможности получения указанного технического результата и предпочтительности выбранных для реализации способа и средства антиапоптотических генов была сформирована панель сравниваемых генов, каждый из этих генов потенциально мог играть важную роль в защите раковой клетки от воздействия химиопрепарата. В сформированную панель вошли гены:
- гены BIRC - семейства (baculoviral IAP repeat-containing proteins) - из группы ингибиторов апоптоза: с-IAP1 (Birc), с-IAP2 (Birc3), с-IAP3 (Birc4), с-IAP4 (Birc5), Livin (Birc7);
- ингибитор каспазы 8 - FLIP (FLIP, длинная и короткая изоформы) (FLIP, sCFL, LF);
- гены семейства Bcl-2 (Bcl-2, Bcl-XL);
- ген Trap1 (TNFR ассоциированный белок), ингибитор апоптоза путем блокирования митохондриального стресса;
- ген c-myc, усиливает пролиферацию раковых клеток;
- гены, участвующие в контроле целостности генома (МСМ4, NHEJ1, ERCC1);
- ген теплового шока (HspA5).
Для определения уровня экспрессии генов при различных дозировках оксалиплатина, были посеяны 12-луночные плашки с культурой клеток колоректального рака НТ-29. В экспериментальные лунки был внесен оксалиплатин в концентрациях 1 и 5 мкм. Для подтверждения результатов каждая такая лунка была повторена не менее 3 раз и каждый эксперимент был повторен не менее 3 раз.
Через 24 и 48 часов был произведен анализ экспрессии генов в изучаемых клетках с помощью метода ПЦР в реальном времени и получен экспрессионный профиль исследуемых генов.
На основе анализа полученных дозовых и временных зависимостей экспрессии указанных генов в ответ на химиотерапевтическое воздействие выявлены наиболее перспективные для терапевтического блокирования гены. Повышенную экспрессию при разных дозах химиопрепарата и на всем протяжении культивирования продемонстрировали три гена: c-IAP2, Livin и МСМ4.
На фиг.1 экспрессионный профиль генов c-IAP2, Livin, MCM4 в зависимости от времени и дозировки воздействия оксалиплатина показывает, что эти 3 гена реагируют повышением уровня экспрессии более чем в 2 раза и демонстрируют четкую зависимость от дозы в обоих из изученных временных интервалов.
Из полученных данных следует, что эти гены: c-IAP2, Livin, MCM4 имеют повышенную и связанную с дозой оксалиплатина экспрессию в течение всего времени инкубации, в отличие от других исследованных генов. Это подтверждает их особую роль в сохранении жизнеспособности клеток при воздействии оксалиплатина. То есть повышение экспрессии рассматриваемых трех генов не является промежуточным или побочным этапом в развитии процесса ответа на токсическое воздействие. Именно их повышенное функционирование необходимо для сохранения жизнеспособности раковых клеток в определенном интервале доз оксалиплатина на всем протяжении инкубации в его присутствии.
Следовательно, по характеристикам дозово-временных зависимостей в профиле экспрессии и по функциональному значению для жизнеспособности раковой клетки, гены c-IAP2, Livin, MCM4 правомерно выбраны в качестве терапевтических мишеней для преодоления резистентности к оксалиплатину клеток колоректального рака. Для ингибирования функции указанных генов были выбраны эффективно интерферирующие миРНК.
С целью проверочного функционального исследования было проведено ингибирование функции указанных генов с помощью миРНК. Первоначально был проверен апоптотический эффект от ингибирования функции генов c-IAP2, Livin и MCM4 по отдельности. В исследуемые лунки с культивируемыми клетками НТ-29 вносился оксалиплатин в изучаемых концентрациях 1 мкМ либо 5 мкМ и специфичные для указанных генов интерферирующие миРНК в концентрации 50 мкМ. Через 48 часов после добавления оксалиплатина и миРНК, клетки прижизненно окрашивались с использованием набора для определения апоптотических клеток Vybrant Apoptosis Assay Kit #5 (Invitrogen, USA), включающего флуоресцентные красители Hoechst 33342/Propidium Iodide. Число апоптотических клеток подсчитывали с помощью флуоресцентного микроскопа.
Наибольшим апоптотическим эффектом обладало блокирование гена МСМ4. Ингибирование малыми интерферирующими РНК генов c-IAP2, Livin и МСМ4 при 5 мкМ оксалиплатина приводит к апоптозу клеток колоректального рака на уровнях 40%, 50% и 60% от числа всех имеющихся в лунках клеток, соответственно.
При проверке действия различных приведенных ниже в таблице комбинаций миРНК, блокирующих исследуемые гены-мишени, показано синергетическое действие миРНК против пары генов Livin и МСМ4. Блокирование указанной пары генов приводит к апоптозу 80% клеток колоректального рака, устойчивых к действию оксалиплатина, при 5 мкМ оксалиплатина. Следовательно, использование разрабатываемого средства позволит достигать эффективного действия химиопрепарата при дозах, меньших приблизительно в 15 раз, или увеличить эффект низкой дозы химиопрепарата примерно на порядок величины. Другие комбинации миРНК, блокирующие пары генов c-IAP2 и Livin; c-IAP2 и МСМ4 продемонстрировали апоптоз на уровнях 60% и 65% от числа всех клеток в лунках, соответственно.
Для ингибирования функции генов были синтезированы выбранные миРНК-олигонуклеотиды, в прямом направлении (sense) и в обратном направлении (antisense). При этом миРНК sense - олигонуклеотид, 5'→3' и antisense - олигонуклеотид, 5'→3'. Последовательности олигонуклеотидов миРНК конструировали на основе последовательностей РНК генов (NCBI Reference Sequence: c-IAP2 - NM_001165.4; Livin - NM_022161.2; МСМ4 - NM_005914.3) с использованием известных способов, например, с употреблением специализированной программы BLOCK-iT™ RNAi Designer (Invitrogen, Life Technologies, USA).
С использованием олигонуклеотидов миРНК, синтезированных в прямом направлении (sense, s) и в обратном направлении (antisense, as) создавались дуплексы (duplex) миРНК.
Синтез олигонуклеотидов - это химический синтез фрагментов нуклеиновых кислот с заданной химической структурой (последовательностью). Синтез олигонуклеотидов осуществляли на автоматическом синтезаторе амидофосфитным методом (наиболее распространенный способ синтеза). Амидофосфиты - строительные блоки, которые являются реакционно-способными производными дезоксирибонуклеозидов (dA, dC, dG, Т) или рибонуклеозидов (A, C, G, U) и позволяют синтезировать короткие фрагменты ДНК и РНК, соответственно. Технология синтеза позволяет получать любые количества олигонуклеотидов. По завершении синтеза олигонуклеотид снимается с полимерного носителя, с него удаляются защитные группы (стадия деблокирования), и далее он подвергается очистке с помощью обращенно-фазовой ВЭЖХ или электрофореза в полиакриламидном геле.
Для каждого гена-мишени проверялось несколько вариантов миРНК, это позволяет утверждать, что заявляемое решение предусматривает наиболее эффективные. Эффективность определялась наибольшим подавлением экспрессии гена при наименьшей концентрации миРНК. Все выбранные олигонуклеотиды ингибировали соответствующий ген-мишень более чем на 75%, т.е. технический результат заявляемого способа и средства подтвержден.
В таблице приведены последовательности используемых олигонуклеотидов миРНК
Sense-олигонуклеотид, 5'→3'
Antisense-олигонуклеотид, 5'→3'
Какие-либо синтезированные олигонуклеотиды могут быть проверены на соответствие их первичной структуры последовательностям нуклеотидов, представленным в таблице, а также описанным ниже конструкциям на основе представленных в таблице олигонуклеотидов. Для этого используют специальные праймеры для обратной транскрипции, представляющие собой шпилечные структуры с выступающим концом, например, в 5-8 нуклеотидов, комплементарных по последовательности концевому участку определяемого олигонуклеотида миРНК.
После проведения реакции обратной транскрипции полученная кДНК может быть амплифицирована и затем секвенирована. Секвенирование - определение последовательности нуклеотидов в ДНК. Полученная последовательность нуклеотидов сравнивается с последовательностью в таблице.
Заявляемое средство представляет собой комбинацию указанных в таблице миРНК-олигонуклеотидов размером около 20 нуклеотидов - применяемых в виде дуплексов «рабочей» цепи и комплементарного к ней олигонуклеотида. Средство стабильно хранится длительное время (годы). Например, препарат для ингибирования гена c-IAP2, синтезированный 16.09.2010 г. сохранил работоспособность по 16.06.2013 г. (2 года и 9 месяцев). При введении в клетку миРНК снижение экспрессии антиапоптического гена - мишени сохраняется как минимум трое суток (72 часа). Возможность количественного определения массы олигонуклеотидов с помощью спектрофотометрии позволяет полностью стандартизовать количество и соотношения олигонуклеотидов в разных партиях. С использованием олигонуклеотидов миРНК, синтезированных в прямом направлении (sense, s) и в обратном направлении (antisense, as) создавались дуплексы (duplex) миРНК.
Получение дуплексов миРНК проводили в следующем растворе: 10 mM TRIS HCl; 20 mM NaCl; 1 mM EDTA (pH 8,0) при концентрации олигонуклеотидов 30-50 мкМ (http://ru-ru.invitrogen.com/site/ru/ru/home/Products-and-Services/Applications/Cell-Culture/Transfection/RNAi-Transfection/RNAi-Transfection-Protocols.html).
Помимо дуплексов использовали короткие шпилечные структуры, образованные на основе приведенных в таблице последовательностей sense и antisense олигонуклеотидов, обозначенных далее как Sense oligo и Antisense oligo, соответственно. Указанные шпилечные структуры были следующими:
(Sense oligo)-CAAGAGA-(Antisense oligo), или:
(Sense oligo-dtdt)-(Sense oligo)-CAAGAGA-(Antisense oligo-dtdt)-(Antisense oligo), где: Sense oligo и Antisense oligo - пары олигонуклеотидов для каждого гена, (Sense oligo-dtdt) и (Antisense oligo-dtdt) - аналогичные последовательности РНК в парах олигонуклеотидов без dtdt.
Или:
(Antisense oligo-dtdt)-(Antisense oligo)-CAAGAGA-(Sense deoxyoligo-dtdt)-(Sense deoxyoligo), или:
CG-(Antisense deoxyoligo-dtdt)-(Antisense deoxyoligo)-CAAGAGA-(Sense deoxyoligo-dtdt)-(Sense deoxyoligo)-TTTTTTGGAAA, предназначенное для экспрессии в раковой клетке соответствующих миРНК, где: Antisense deoxyoligo и Sense deoxyoligo представляют собой последовательности нуклеотидов с заменой рибонуклеотидов на дезоксирибонуклеотиды, (Antisense deoxyoligo-dtdt) и (Sense deoxyoligo-dtdt) - аналогичные последовательности ДНК в парах олигонуклеотидов без dtdt.
При этом (Sense oligo) и (Antisense oligo) выбираются в соответствии с ингибируемым геном из приведенных в таблице.
Трансфекцию клеток синтетическими олигонуклеотидами (миРНК) проводили липосомным методом согласно протоколу (www.invitrogen.com/…/lipofectamine-rnaimax) производителя с использованием реагентов Lipofectamine RNAiMAX ("Invitrogen", США). Эти реагенты коммерчески доступны. Данный реагент (Lipofectamine RNAiMAX) был выбран, исходя из его характеристик:
Основная характеристика Lipofectamine™ RNAiMAX: высокая эффективность трансфекции малых РНК (siRNA и miRNA) во все типы клеток, включая стабильные клеточные линии, первичные, стволовые и трудно трансфицируемые клетки. Трансфекция делалась прямым методом, т.е. смесь для трансфекции вносили непосредственно в среду с клетками. За 2 дня до эксперимента (трансфекции) клетки высевали на 12-луночные плашки, в концентрации 7,5·104 клеток в 1 мл среды. Перед трансфекцией питательную среду с 10% сывороткой заменяли на ту же среду с 1% сывороткой, согласно протоколу. Трансфекция - процесс введения нуклеиновой кислоты в клетки человека и животных невирусным методом
Для приготовления трансфецирующего реагента, дуплексы миРНК (10-50 пмоль) разводили с Lipofectamine RNAiMAX (2 мкл/лунку) в 200 мкл среды ДМЕМ с пониженным содержанием сыворотки (1%). Далее эта смесь в течение 20 мин перемешивалась при комнатной температуре. Полученную смесь вносили в плашку с клетками (конфлюентность - 20%-40%), плашка помещалась в термостат, через 20 мин добавлялось 800 мкл среды с нужной концентрацией химиопрепарата. Оксалиплатин наносился в различных концентрациях, в зависимости от цели эксперимента (0,3 мкм, 1 мкм, 5 мкм, 20 мкм, 50 мкм, 100 мкм, 150 мкм, 250 мкм). Подсчет результатов производили через 24, 48 и 72 часа после добавления оксалиплатина.
В результате показано, что средство, обеспечивающее совместное действие миРНК, ингибирующих гены Livin и МСМ4, при малых дозах оксалиплатина (5 мкм) дает соизмеримый эффект с отдельной дозировкой оксалиплатина, составляющей 80 мкм. Полученные данные демонстрируют, что заявляемое противоопухолевое средство на основе миРНК может рассматриваться в качестве эффективного инструмента для терапии рака, включая усиление терапевтического эффекта, вызываемого стандартной химиотерапией, и снижения ее нагрузки на организм пациента.
Стандартная однократная доза оксалиплатина для человека составляет примерно 150 мг (в соответствии с инструкцией на оксалиплатин-тева максимальная доза составляет 85 мг/1 м2 площади тела, средняя площадь тела 1,73 м2 - ru.wikipedia.org/wiki/плошадь_поверхности_тела). Исходя из количества крови у человека (в районе 5 л), введение 150 мг оксалиплатина приведет к его концентрации в крови, составляющей 30 мкг/мл, или 75 мкМ. То есть эффективная концентрация оксалиплатина в крови соответствует его концентрации в культуре раковых клеток, приводящей к их существенной гибели (фиг.2, 3). При использовании аналогичного расчета для дуплексов миРНК их доза, требуемая для достижения эффективного воздействия при лечении человека, составит около 8 мг при одновременном введении менее 10 мг оксалиплатина (в 15 раз меньше стандартной дозы). Оксалиплатин в стандартной дозировке вводят 1 раз в две недели в течение 12 циклов. Аналогично может вводиться и разработанное средство на основе миРНК. Однако существенное снижение дозировки оксалиплатина при одновременном использовании миРНК может позволить применять эти средства 1 раз в неделю в течение 12 циклов, что приведет к повышению эффективности терапии при одновременном сокращении ее длительности.
Предпочтительно, средство представляет собой стандартную дозировочную форму, включающую суточную дозу или стандартную, суточную субдозу или ее подходящую долю активного ингредиента.
Средство может применяться парентеральным способом, в форме фармацевтического состава, включающего активный ингредиент, в фармацевтически приемлемой лекарственной форме. В зависимости от заболевания и пациента, которому назначено лечение, а также способа введения, композиции могут применяться в различных дозах.
При лечении человека средство может применяться по отдельности, но в общем могут применяться в смеси с подходящим фармацевтическим наполнителем, разбавителем или носителем, выбранным по отношению к назначенному способу введения и стандартной фармацевтической практике.
Средство по настоящему изобретению можно также вводить с помощью липосомной доставки.
Средство можно также использовать в сочетании с растворимыми полимерами в качестве носителей. Такие полимеры могут включать поливинилпирролидон. сополимер пирана, полигидроксипропилметакриламидфенол, полигидроксиэтиласпартамидфенол или полиэтиленоксидполилизин. Средство можно использовать с биоразлагаемыми полимерами для контролируемого высвобождения лекарственного средства, например, метаболизируемыми липидами, содержащими производные глицерина, стеролов и длинноцепных спиртов; полимером молочной кислоты, полимером гликолевой кислоты, сополимерами молочной и гликолевой кислоты.
Например, средство может быть применено в форме капсул, растворов или суспензий, которые могут включать агенты, для применения с быстрым, замедленным или контролируемым высвобождением. Средство может также вводиться ректально или посредством интраопухолевой инъекции.
Средство может применяться в желатиновых капсулах. Предпочтительные в этом отношении вспомогательные вещества включают лактозу, крахмал, целлюлозу, молочный сахар, липиды или полиэтиленгликоли с высокой молекулярной массой. Для водных суспензий соединения изобретения могут быть объединены с различными агентами, с эмульгирующими и/или суспендирующими агентами и разбавителями, такими как вода, этанол, пропиленгликоль и глицерин, и их комбинациями.
Средство может применяться парентерально, например, внутривенно, интра-артериально, или могут применяться инфузионным способом. Наилучшим способом препарат может применяться в форме стерильного водного раствора, который может включать другие вещества, например, достаточное количество солей или глюкозы для обеспечения изотонии раствора с кровью. Водные растворы должны быть забуферены подходящим способом (предпочтительно до pH от 3 до 9), если необходимо. Приготовление подходящих парентеральных составов в стерильных условиях легко достигается стандартными фармацевтическими методиками, хорошо известными специалистам в данной области техники.
Составы могут быть представлены в контейнерах для стандартной дозы или множества доз, например, в запаянных ампулах и флаконах, и могут храниться в лиофилизированном состоянии, требующем только добавления стерильного жидкого носителя, например, воды для инъекций, немедленно перед применением. Растворы и суспензии для введения, готовящиеся непосредственно перед применением, могут быть приготовлены из стерильных порошков и гранул ранее описанного типа.
Для парентерального применения у пациентов-людей уровень разовой дозировки средства может обычно составлять от 0,1 мг/кг до 10 мг/кг. Так, например, капсулы из соединения изобретения могут включать дозу активного соединения для приема по отдельности или в двойном и большем объеме за один раз, как необходимо. Врач в каждом случае определяет необходимую дозировку, наиболее подходящую для любого отдельного пациента, и она может изменяться в зависимости от возраста, веса и ответа конкретного пациента. Вышеуказанные дозировки являются примерными для среднего случая. Могут, конечно, быть отдельные случаи, требуются более высокие или низкие диапазоны дозировки, и такие случаи относятся к области данного изобретения.
Для ветеринарного применения средство может применяться в виде подходящего состава в соответствии с нормальной ветеринарной практикой, и ветеринарный врач определяет режим дозирования и способ введения, наиболее подходящие для конкретного животного.
Результат изобретения состоит в оптимизации и активизации апоптотического воздействия платиносодержащего лекарственного средства на клетки опухоли колоректального рака за счет того, что блокированием соответствующих генов обеспечивается существенная апоптотическая гибель раковых клеток при дозе лекарственного средства, принципиально ниже стандартной. Таким образом, достигается снижение токсичности при сохранении или повышении эффективности терапии. Это достигается благодаря одновременному воздействию на конкретные антиапоптотические гены (ингибируемый ген-мишень, его мРНК, т.е. РНК-мишень) в клетке опухоли с помощью интерферирующих РНК (миРНК, siRNA - small interfering RNA), что влечет за собой сокращение длительности лечения до получения значимых результатов, при снижении вероятности побочных явлений.
Изобретение относится к биохимии. Описан способ индукции апоптоза клеток злокачественной опухоли колоректального рака. Производят ингибирование функции генов из группы: c-IAP2, Livin и MCM4. Для этого используют препараты малых интерферирующих миРНК-олигонуклеотидов из группы: UGUGGACAAAGUCUCUUCCdTdT; CCUGUGGGUAAGAAGAUGAGdTdT; UUCUCUCUCCUCUUCCCUUAdTdT. Предпочтительно производят одновременное ингибирование функций двух генов из группы: c-IAP2, Livin и MCM4, в одной из комбинаций генов: Livin и МСМ4; c-IAP2 и МСМ4; c-IAP2 и Livin. В частности производят одновременное ингибирование функций двух генов из группы: c-IAP2, Livin и МСМ4. Раскрыто средство для осуществления вышеизложенного способа, содержащее оксалиплатин и комбинацию комплементарных к мРНК в клетках злокачественной опухоли миРНК-олигонуклеотидов в виде коротких петлевых миРНК (shRNA). Изобретение позволяет оптимизировать и активизировать апоптотические воздействия платиносодержащего лекарственного средства на клетки опухоли колоректального рака, что обеспечивает существенную апоптотическая гибель раковых клеток при дозе лекарственного средства, принципиально ниже стандартной. 2 н. и 5 з.п. ф-лы, 3 ил., 1 табл.
1. Способ индукции апоптоза клеток злокачественной опухоли колоректального рака, предусматривающий ингибирование функции генов клеток злокачественной опухоли с помощью препаратов малых интерферирующих РНК в присутствии химиотерапевтического платинового препарата, при котором производят ингибирование функции генов из группы: C-IAP2, Livin и МСМ4, для чего используют препараты малых интерферирующих миРНК-олигонуклеотидов из группы: UGUGGACAAAGUCUCUUCCdTdT; CCUGUGGGUAAGAGAUGAGdTdT; UUCUCUCUCCUCUUCCCUUAdTdT.
2. Способ по п. 1, отличающийся тем, что производят одновременное ингибирование функций двух генов из группы: C-IAP2, Livin и МСМ4, в одной из комбинаций генов: Livin и МСМ4; C-IAP2 и МСМ4; C-IAP2 и Livin, для чего используют препараты малых интерферирующих миРНК-олигонуклеотидов из группы: UGUGGACAAAGUCUCUUCCdTdT; CCUGUGGGUAAGAAGAUGAGdTdT; UUCUCUCUCCUCUUCCCUUAdTdT.
3. Способ по любому из пп. 1, 2, отличающийся тем, что производят одновременное ингибирование функций двух генов из группы: C-IAP2, Livin и МСМ4, в одной из комбинаций генов: Livin и МСМ4; C-IAP2 и МСМ4; C-IAP2 и Livin, для чего используют препараты малых интерферирующих миРНК-олигонуклеотидов в виде дуплексов прямой и обратной комплементарных цепей нуклеотидов следующей структуры:
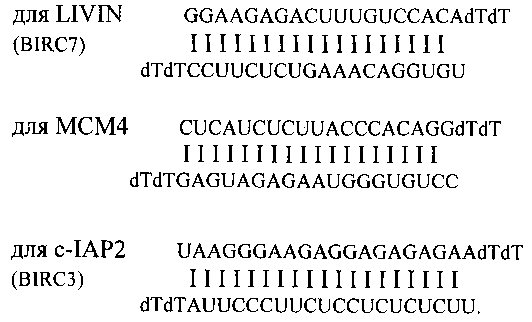
4. Способ по п. 3, отличающийся тем, что используют миРНК дуплексы (duplex), синтезированные в прямом направлении (sense, (s)) и в обратном направлении (antisense, (as) на основе первичной структуры мРНК генов, выбранных из условия наибольшего подавления экспрессии гена при наименьшей концентрации миРНК.
5. Способ по любому из пп. 1, 2, 4, отличающийся тем, что ингибирование функции двух генов клеток злокачественной опухоли осуществляют в присутствии химиотерапевтического препарата оксалиплатина.
6. Средство для осуществления способа по пп. 1-5 для индукции апоптоза клеток злокачественной опухоли колоректального рака, содержащее оксалиплатин и комбинацию комплементарных к мРНК в клетках злокачественной опухоли миРНК - олигонуклеотидов в виде коротких петлевых миРНК (shRNA), по меньшей мере, одной из следующих структур:
(Sense oligo)-CAAGAGA-(Antisense oligo), или:
(Sense oligo-dtdt)-(Sense oligo)-CAAGAGA-(Antisense oligo-dtdt)-(Antisense oligo), где: Sense oligo и Antisense oligo - пары олигонуклеотидов для каждого гена, (Sense oligo-dtdt) и (Antisense oligo-dtdt) - аналогичные последовательности РНК в парах олигонуклеотидов без dtdt.
Или:
(Antisense oligo-dtdt)-(Antisense oligo)-CAAGAGA-(Sense deoxyoligo-dtdt)-(Sense deoxyoligo), или:
CG-(Antisense deoxyoligo-dtdt)-(Antisense deoxyoligo)-CAAGAGA-(Sense deoxyoligo-dtdt)-(Sense deoxyoligo)-TTTTTTGGAAA, где: Antisense deoxyoligo и Sense deoxyoligo представляют собой последовательности нуклеотидов с заменой рибонуклеотидов на дезоксирибонуклеотиды, (Antisense deoxyoligo-dtdt) и (Sense deoxyoligo-dtdt) - аналогичные последовательности ДНК в парах олигонуклеотидов без dtdt.
При этом (Sense oligo) и (Antisense oligo) выбираются в соответствии с ингибируемым геном из приведенных ниже:

7. Средство по п. 6, отличающееся тем, что оно выполнено в фармацевтической форме, пригодной для парентерального применения с целью индукции апоптоза клеток злокачественной опухоли колоректального рака.
| МИКРООРГАНИЗМЫ В КАЧЕСТВЕ НОСИТЕЛЕЙ НУКЛЕОТИДНЫХ ПОСЛЕДОВАТЕЛЬНОСТЕЙ, КОДИРУЮЩИХ КЛЕТОЧНЫЕ АНТИГЕНЫ, ДЛЯ ЛЕЧЕНИЯ ОПУХОЛЕЙ | 2003 |
|
RU2319741C2 |
| WO 2007018309 A1, 15.02.2007 | |||
Авторы
Даты
2015-05-20—Публикация
2013-08-02—Подача