Данное изобретение относится к области биотехнологии. Изобретение может найти применение в биотехнологии, молекулярной биологии и фармакологии для деструкции рибонуклеиновых кислот (РНК) в биологических образцах.
В настоящее время для удаления РНК из биологических образцов, например при производстве вакцин, используют методы ферментативной деструкции РНК. В большинстве случаях деструкцию проводят, добавляя фермент (биокатализатор) в РНК-содержащий раствор. Однако данный подход нетехнологичен, так как сопряжен с потреблением больших количеств биокатализатора, загрязняющего целевой раствор. Более технологичными являются подходы, основанные на использовании иммобилизованных ферментов. Иммобилизация позволяет не только легко отделять биокатализатор от реакционной среды, но и использовать его многократно, что повышает эффективность технологического процесса.
В большинстве случаев применения иммобилизованных ферментов для решения тех или иных задач в качестве стационарной фазы используют сорбенты гелевого типа на основе природных [А.Д. Неклюдов, А.Н. Иванкин, О.П. Прошина, Г.Л. Олиференко. Способ получения иммобилизованной целлюлазы. 2010. Патент РФ №2388822] или синтетических полимеров [Г.И. Зверев, М.П. Лунин В.В. Способ получения иммобилизованных ферментов. 1996. Патент РФ 2054481].
Наиболее близким к заявляемому изобретению является способ деструкции РНК путем пропускания раствора через сорбент на основе целлюлозы или агарозы [A.Guissani born Trachtenberg, M.-N. Thang, Immobilized ribonuclease and alkaline phosphatase, 1977, US 4039382] или магнитного гидрогеля [Horak D., Rittich В.J., Safar A., Spanova J., Lenfeld N.J. Biotechnol. Prog. 17 (2001) 447], содержащих иммобилизованную рибонуклеазу.
Существенным недостатком данного способа является невысокая скорость процесса, обусловленная диффузионным механизмом межфазового массопереноса, а также непродолжительный срок службы сорбента вследствие ухудшения гидродинамических характеристик, являющихся следствием усадки геля. Кроме того, использование сорбентов гелевого типа не позволяет совместить процесс деструкции РНК со стадией анализа продуктов каталитической реакции в один технологический цикл в связи с существенным увеличением давления в системе.
Технической задачей и положительным результатом предлагаемого изобретения является способ деструкции РНК, сочетающий как стадию деструкции (биоконверсия), так и стадию мониторинга компонентов смеси (биосепарация) в одном непрерывном процессе. Указанная задача и технический результат достигаются в способе деструкции рибонуклеиновой кислоты, включающем проведение процесса в две последовательные непрерывные стадии, включающие биоконверсию и биосепарацию, где на первой стадии пропускают раствор образца, содержащего рибонуклеиновую кислоту сквозь макропористый полиметакрилатный сорбент монолитного типа, несущий иммобилизованную рибонуклеазу А, а на второй - адсорбцию компонентов образца на макропористом анионообменном сорбенте монолитного типа с их последующим градиентным элюированием. На первой стадии используют раствор А, представляющий собой 0.02 М буферный раствор трис(гидроксиметил)аминометана (ТрисHCl), pH 7.5, на второй стадии используют раствор Б, представляющий собой раствор А, содержащий 7 моль/л мочевины, а также линейное градиентное элюирование от 0 до 100% раствором В, представляющим собой раствор Б, содержащий 1 моль/л хлорида натрия. Детектирование продуктов деструкции проводят при длине волны 260 нм.
Заявляемый способ обладает совокупностью существенных признаков, которые включают:
(1) деструкцию РНК, которая происходит при пропускании раствора, содержащего РНК, сквозь макропористый полимерный сорбент монолитного типа, несущий иммобилизованную рибонуклеазу А;
(2) адсорбцию компонентов смеси, включая продукты деструкции РНК, на макропористом анионообменном сорбенте монолитного типа;
(3) селективную десорбцию компонентов смеси с поверхности сорбента в условиях градиентной элюции.
Положительный результат достигается вследствие использования на обеих стадиях процесса макропористых полимерных сорбентов монолитного типа со средним размером пор в пределах от 1.0 до 2.0 мкм и общей пористостью в пределах 55-65%. Данные сорбенты характеризуются высокой проницаемостью и доминированием конвективного массопереноса над диффузионным, что позволяет проводить процессы биоконверсии и биосепарации при высоких скоростях подвижной фазы (до 15 см/мин) и низких рабочих давлениях (от 0.1 до 1 МПа), и совмещать их в один технологический цикл.
Иммобилизация фермента через промежуточный альдегидсодержащий водорастворимый полимерный спейсер на основе функционального синтетического полимера улучшает доступность активного центра биокатализатора и, таким образом, повышает эффективность процесса биодеструкции. Использование данного способа иммобилизации позволяет сократить объем сорбента и количество иммобилизованного фермента, используемого на первой стадии, при сохранении эффективности процесса биодеструкции.
Пример 1. На первой стадии использовали макропористый полиметакрилатный сорбент монолитного типа со средним размером пор 1300±50 нм, пористостью 60±2% и объемом 0.83 мл, содержащий эпоксидные группы (сорбент 1). Иммобилизацию рибонуклеазы А проводили путем прямой реакции между аминогруппами фермента и эпоксидными группами сорбента. Для этого сквозь сорбент пропускали 1 мл раствора рибонуклеазы А в 0.1 M натрий-боратном буферном растворе, рН 8.4, с концентрацией 5 мг/мл, и инкубировали сорбент при температуре 22°С в течение 20 часов. После этого сорбент промывали 3 мл буфера в котором вели иммобилизацию, и затем 0.02 M буферным раствором трис(гидроксиметил)аминометана, рН 7.5, в течение 1 часа. Массу иммобилизованного фермента определяли по разности количества фермента в растворе до и после иммобилизации. Концентрацию фермента в растворе определи по методу Лоури-Фолина при длине волны 750 нм. Масса иммобилизованной рибонуклеазы составила 2.2±0.2 мг.
На второй стадии использовали макропористый анионообменный сорбент монолитного типа, со средним размером пор 1600 нм, пористостью 60±2% и объемом 0.34 мл, содержащий на поверхности диэтиламиноэтильные (ДЭАЭ) группы (сорбент 2).
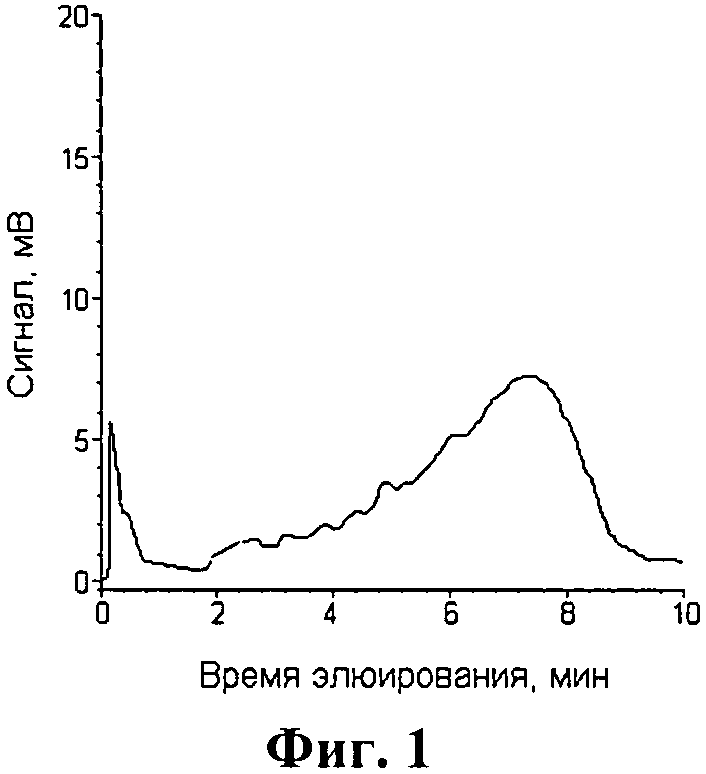
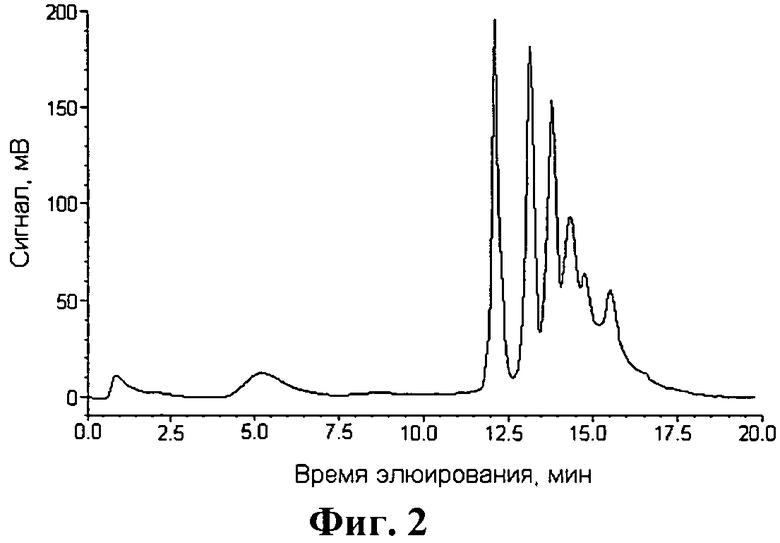
300 мкл раствора РНК (молекулярная масса 25 кДа) с концентрацией 0.15 мг/мл в 0.02 M буферном растворе трис(гидроксиметил)аминометана, рН 7.5, наносили на сорбент 1. Сорбент 1 последовательно соединяли с сорбентом 2. На фиг.1 представлен вид исходной РНК (не прошедшей стадию деструкции), элюируемой через сорбент 2. Процесс деструкции РНК проводили по следующей программе элюирования: (1) 0-5 мин - 100% элюента А, представляющего собой 0.02М буферный раствор трис(гидроксиметил)-аминометана, рН 7.5; (2) 5-10 мин - 100% элюента Б, представляющего собой раствор А, содержащий 7 моль/л мочевины; (3) 10-20 мин от 0 до 100% элюента В, представляющего собой раствор Б, содержащий 1 моль/л хлорида натрия. Детектирование проводили при длине волне 260 нм. Скорость элюирования составляла 1 мл/мин (соответствует линейной скорости 10 см/мин). Давление в системе составляло 0.7 МПа. Фиг. 2 подтверждает протекание процесса деструкции РНК, что выражается в исчезновении широкого пика РНК (рис. 1) и появлении набора пиков, характеризующих образование олигорибонуклеотидов. Ультрафильтрация собранного элюата через мембрану 10 кДа и последующий спектрофотометрический анализ высокомолекулярной фракции при длине волны 260 нм показал, что доля рибонуклеиновой кислоты, оставшейся после проведения реакции деструкции, составила 10±3%. Таким образом, предложенный способ позволял достичь степени деградации РНК, близкой к 90%.
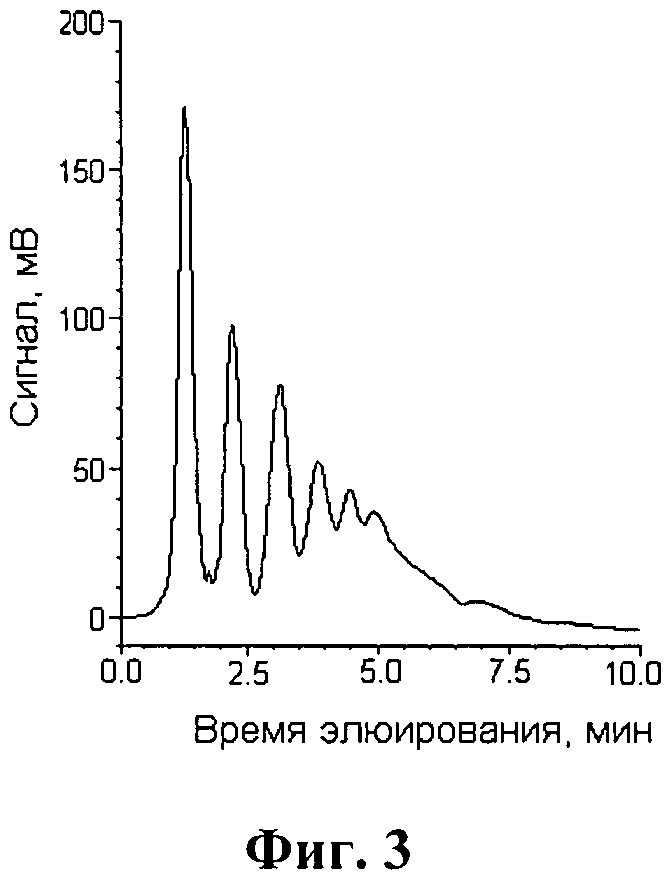
При этом олигонуклеотидная карта (фиг.3) совпадала с таковой, полученной при проведении процесса деструкции РНК рибонуклеазой А в растворе в течение 7 минут.
Пример 2. На первой стадии использовали макропористый полиметакрилатный сорбент монолитного типа со средним размером пор 1600+60 нм, пористостью 60±2% и объемом 0.34 мл, содержащий аминогруппы. Иммобилизацию фермента проводили в несколько стадий. На первой стадии сорбент заполняли 0.5 мл раствора альдегидсодержащего спейсера в 0.01 M натрий-фосфатном буфере, рН 7.0, с концентрацией 0.4 мг/мл и инкубировали при температуре 22°С в течение 1.5 часов. В качестве спейсера использовали раствор окисленного полимера М-метакрилоиламидо-О-глюкозы с молекулярной массой 22000 и содержанием альдегидных групп 25 мол.%. Затем сорбент промывали 0.01 M натрий-боратным буферным раствором, рН 8.4, и заполняли поровое пространство 0.5 мл раствора рибонуклеазы с концентрацией 5.0 мг/мл в том же буфере. Сорбент инкубировали при температуре 22°С в течение 1.5 часов. Образовавшиеся иминные связи восстанавливали раствором боргидрида натрия в воде с концентрацией 1 мг/мл в течение часа при температуре иммобилизации. Расчет количества иммобилизованного фермента проводили так же, как описано в Примере 1. Масса иммобилизованной рибонуклеазы составила 0.9±0.1 мг.
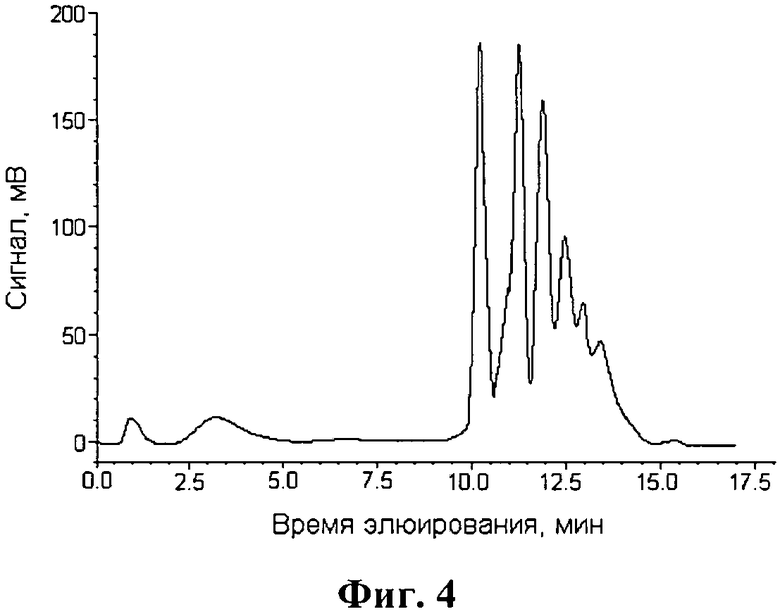
Процесс деструкции РНК проводили по следующей программе элюирования: (1) 0-2 мин - 100% элюента А; (2) 2-7 мин - 100% элюента Б; (3) 7-17 мин от 0 до 100% элюента В. Состав элюентов и остальные параметры процесса аналогичны таковым, приведенным в Примере 1. Фиг. 4 иллюстрирует профиль элюции набора олигорибонуклеотидов, образующихся при деструкции РНК. Доля РНК, не подвергшаяся деструкции, составила 8±2%.
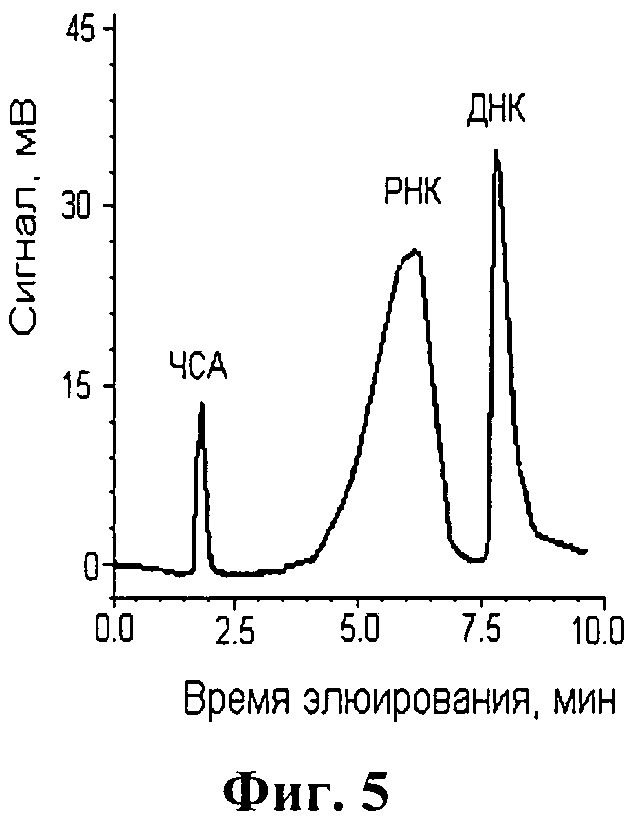
Пример 3. Для проведения процесса использовали сорбенты, описанные в Примере 1. При этом деструкцию РНК проводили, используя в качестве модели многокомпонентной биологической жидкости смесь РНК, ДНК и сывороточного альбумина человека (ЧСА). На фиг.5 представлен профиль элюции данной смеси из колонки 2, т.е. не включающий стадию деструкции целевого компонента.
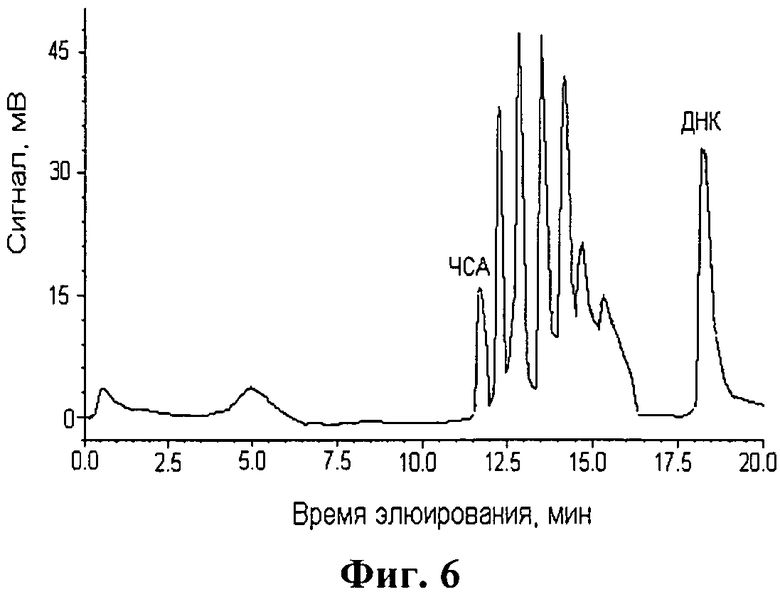
Для проведения процесса деструкции РНК в сорбент вносили 300 мкл указанной смеси, где концентрация каждого компонента составляла 0.15 мг/мл в 0.02 M буферном растворе трис(гидроксиметил)аминометана, рН 7.5. Далее процесс проводили так же, как описано в Примере 1. На фиг.6 представлен профиль элюции компонентов смеси биологических соединений, включающий как набор олигорибонуклеотидов, образовавшихся в результате деструкции РНК, так и исходные компоненты - ДНК и сывороточный альбумин человека. Доля РНК, не подвергшаяся деструкции, составила 10+4%. Очевидно, что присутствие дополнительных биологических компонентов не мешает протеканию процесса биоконверсии РНК.
Таким образом, вследствие использования на обеих стадиях процесса макропористых полимерных сорбентов монолитного типа описанный способ позволяет одновременно проводить деструкцию РНК и мониторинг продуктов реакции за короткий промежуток времени, при высоких скоростях подвижной фазы и низких рабочих давлениях с эффективностью, сопоставимой с биокаталитической реакцией в растворе. Использование способа иммобилизации фермента через полимерный спейсер позволяет сократить объем сорбента, используемого на первой стадии, при сохранении эффективности процесса биодеструкции.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ ковалентной иммобилизации лизоцима для последующего применения иммобилизованного лизоцима для снижения бактериальной обсемененности биологических жидкостей | 2018 |
|
RU2694883C1 |
| Способ удаления эндотоксинов из биологических жидкостей с помощью ковалентно иммобилизованного лизоцима в качестве лиганда | 2018 |
|
RU2684639C1 |
| СПОСОБ КОНЦЕНТРИРОВАНИЯ ВИРУСА | 1997 |
|
RU2130069C1 |
| Способ получения модифицированнойРибОНуКлЕиНОВОй КиСлОТы | 1978 |
|
SU810725A1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА, РЕКОМБИНАНТНЫЙ ШТАММ, РЕКОМБИНАНТНЫЙ БЕЛОК ВМР-7 И СПОСОБ ВЫДЕЛЕНИЯ РЕКОМБИНАНТНОГО БЕЛКА В ДИМЕРНОЙ ФОРМЕ | 2012 |
|
RU2499047C1 |
| РЕКОМБИНАНТНАЯ ПЛАЗМИДА, РЕКОМБИНАНТНЫЙ ШТАММ, РЕКОМБИНАНТНЫЙ БЕЛОК ВМР-2 И СПОСОБ ВЫДЕЛЕНИЯ РЕКОМБИНАНТНОГО БЕЛКА В ДИМЕРНОЙ ФОРМЕ | 2012 |
|
RU2499048C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАКРОПОРИСТОГО ПОЛИМЕРНОГО МАТЕРИАЛА МОНОЛИТНОГО ТИПА | 2009 |
|
RU2401693C1 |
| Способ культивирования мицелиальных грибов - продуцентов рибонуклеаз | 1986 |
|
SU1405310A1 |
| СОРБЕНТ ДЛЯ ХРОМАТОГРАФИИ ОПТИЧЕСКИХ ИЗОМЕРОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2006 |
|
RU2348455C2 |
| Способ получения водонерастворимых биологически активных соединений | 1977 |
|
SU689200A1 |
Изобретение относится к области биотехнологии. Предложен способ деструкции рибонуклеиновых кислот. Раствор, содержащий рибонуклеиновую кислоту, пропускают через макропористый полиметакрилатный сорбент монолитного типа, содержащий иммобилизованную рибонуклеазу А, а затем через макропористый анионообменный сорбент монолитного типа. Используют следующую программу элюирования при скорости подвижной фазы 10 см/мин: на первой стадии используют раствор А, представляющий собой 0,02 М ТрисНСl буферный раствор, pH 7,5, на второй стадии используют раствор Б, представляющий собой раствор А, содержащий 7 моль/л мочевины, а также линейное градиентное элюирование от 0 до 100% раствором В, представляющим собой раствор Б, содержащий 1 моль/л хлорида натрия. Преимуществом изобретения является одновременное эффективное проведение деструкции РНК и мониторинг продуктов реакции за короткий промежуток времени при высоких скоростях подвижной фазы и низких рабочих давлениях. 1 з.п. ф-лы, 6 ил., 3 пр.
1. Способ деструкции рибонуклеиновых кислот, включающий пропускание раствора, содержащего рибонуклеиновую кислоту, через сорбент с иммобилизованной рибонуклеазой А, отличающийся тем, что процесс ведут в две последовательные непрерывные стадии, включающие биоконверсию и биосепарацию, где сначала пропускают раствор образца, содержащего рибонуклеиновую кислоту, сквозь сорбент 1 - макропористый полиметакрилатный сорбент монолитного типа, содержащий иммобилизованную рибонуклеазу А, а затем сквозь сорбент 2 - макропористый анионообменный сорбент монолитного типа; для проведения деструкции рибонуклеиновых кислот используют следующую программу элюирования при скорости подвижной фазы 10 см/мин: на первой стадии используют раствор А, представляющий собой 0,02 М ТрисНCl буферный раствор, pH 7,5, на второй стадии используют раствор Б, представляющий собой раствор А, содержащий 7 моль/л мочевины, а также линейное градиентное элюирование от 0 до 100% раствором В, представляющим собой раствор Б, содержащий 1 моль/л хлорида натрия.
2. Способ по п.1, отличающийся тем, что на первой стадии пропускание раствора, содержащего рибонуклеиновую кислоту, осуществляется через сорбент с рибонуклеазой А, иммобилизованной на поверхности макропористого сорбента монолитного типа, содержащего аминогруппы, с использованием промежуточного альдегидсодержащего водорастворимого полимерного спейсера.
| US 4039382 A1, 02.08.1977 | |||
| HORAK D | |||
| ET AL | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Prog | |||
| Печь для сжигания твердых и жидких нечистот | 1920 |
|
SU17A1 |
| КОПИРОВАЛЬНЫЙ СТАНОК ДЛЯ ДЕРЕВА | 1921 |
|
SU447A1 |
| КОВАЛЕВ Н.А | |||
| Физико-химические свойства и механизм расщепления РНК соединениями, не содержащими функциональных групп, катализирующих реакцию трансэтерификации // | |||
Авторы
Даты
2015-05-20—Публикация
2013-08-08—Подача