Данное изобретение имеет отношение к таким композициям, а также к таким фармацевтическим композициям, которые включают поксвирусы, и более конкретно, к таким, которые влючают внеклеточные оболочечные вирусы. Данное изобретение также имеет отношение к способу, который является пригодным для того, чтобы продуцировать поксвирусы, а также к поксвирусам, полученным с помощью указанного способа. Кроме того, данное изобретение также имеет отношение к использованию указанных поксвирусов и указанной композиции для получения лекарственного средства.
Возникновение таких новых угроз (птичий грипп, западный нильский вирус, сибирская язва и т.д.) так же, как развитие генной терапии, увеличило со временем потребность в производстве и очищении поксвирусов в профилактических или терапевтических целях. Это особенно имеет место для такого вируса, которым является вирус Анкара млекопитающих (MVA). Этот поксвирус, который первоначально был использован для того, чтобы вакцинировать пациентов с иммунодефицитными состояниями против натуральной оспы, теперь также используется в качестве вектора в целях генной терапии. Например, MVA используется в качестве вектора для гена MUC 1 для того, чтобы вакцинировать пациентов против экспрессии опухоли Muc 1 (Scholl и др., 2003, J Biomed Biotechnol., 2003, 3, 194-201). MVA перенос гена, который кодирует антигены HPV, также используется в качестве вектора для терапевтического лечения карциномы яичников.
Поксвирусы - это группа оболочечных сложных вирусов, которые отличаются их преимущественно необычной морфологией, их большим геномом ДНК и их сайтом репликации, который является расположенным в цитоплазме. Геном нескольких членов Poxviridae, включая копенгагенский штамм вируса осповакцины (W) (Goebel и др., 1990, Virol. 179, 247-266 и 517-563; Johnson и др., 1993, Virol. 196. 381-401) и модифицированный штамм вирус осповакцины Анкара (MVA) (Antoine и др., 1998, Virol. 244, 365 - 396), был картированы и секвенирован. У копенгагенского штамма вируса осповакцины есть двухцепочечный геном ДНК, состоящий приблизительно из 192 КБ, предназначенный для кодирования приблизительно 200 белков, из которых приблизительно 100 вовлечены в сборку вируса. MVA является сильно аттенуированным штаммом вируса осповакцины, который произведен путем более чем 500 серийными пассажами штамма вируса осповакцины Анкара в культуре эмбрионов куриных фибробластов (Mayr и др., 1975, Infection 3, 6-16). Вирус MVA был депонирован в Национальной Коллекции Культур Микроорганизмов (CNCM) под депозитным номером N602 I - 721. Определение полной последовательности генома MVA и сравнения с геномом копенгагенского штамма вируса осповакцины позволяет точно идентифицировать те изменения, которые произошли в вирусном геноме и определить семь делеций (от I до VII), а также те многочисленные мутации, которые приводят к фрагментированию ORFs (открытая рамка считывания) (Antoine и др., 1998, Virology 244, 365-396).
Естественный метаболический путь внутриклеточного захвата оболочечных вирусов включает ряд таких этапов, которые состоят из закрепления вирусного полипептида, ориентированного на вирусной поверхности к клеточному рецептору, и этапа слияния между вирусной и клеточной мембранами, что приводит к тому, что вирусный геном высвобождается в цитоплазму зараженной клетки.
Однако, в особом случае для поксвирусов, точный анализ метаболического пути сложен тем, что существуют две морфологически отличные формы инфекционного вируса, которые имеют названия внутриклеточный зрелый вирус (IMV) и внеклеточный оболочечный вирус (EEV). Для формы IMV, среди других особенностей, характерно окруженное монолипидной оболочкой вирусное ядро и преимущественно локализация в цитоплазме зараженных клеток, хотя это может быть и для экстрацеллюларного, выпущенного после лизиса зараженных клеток. Многие из естественных полипептидов являются представленными на поверхности липидной оболочки IMV, были идентифицированы, такие, как, например, р 14 kDa и р 21 kDa белки, соответственно закодированные геном A27L (Rodriguez и др., 1985, J. Virol. 56, 482-488; Rodriguez и Estaban, 1987, J. Virol. 61, 3550-3554), и ген A17L, так же, который кодирует белки A14L, D8L, A9L (Yeh и др., 2000, J. Virol. 74. 9701-9711), E10R (Senkevich и др. 2000, Virol. 5, 244-252) и гены H3L. По сравнению с IMV у формы EEV есть дополнительная внешняя поверхность мембраны липида (двойной слой липида), которая получена из комплекса Гольджи. Это соответствует вирусной форме, выпущенной вне зараженных клеток. Мембранная поверхность EEV содержит приблизительно 10 белков, которые отсутствуют на поверхности IMV, такие как, например, закодированный В 5R, A34R и гемагглютининовые (ХА) генные продукты. Сосуществование указанного IMV и форм EEV было описано для большинства штаммов оспы (например, Копенгагенский и штамм MVA), так же как для других поксвирусов, таких как поксвирусы домашней птицы (Boulanger и др., 2000, J. Gen Virol. 81, 675-687).
Поскольку они являются самыми устойчивыми в окружающей среде, IMVs играют преобладающую роль в клетке хозяине, для того, чтобы быть готовыми для трансмиссии (Hooper и др. Virology 2003, 306, 181-185). С учетом этого, частицы IMV были традиционными векторами в целях генной терапии. Поэтому доступный процесс поксвирусной очистки позволяет обрабатывать только те вирусы, которые являются представленными на клетках (то есть IMV), тогда как от пула частиц EEV в среде культивирования невозможно избавиться. Из-за присутствия на его поверхности большего разнообразия полипептидов, чем на поверхности IMV, использование рекомбинантного EEVs было уже предложено и известно в назначении для инфицирования (US 20050208074; Galmiche и др. J. Gen. Virol., 1997, 78, 3019-3027). Однако, даже для этого определенного использования, частицы IMV особенно являются предпочтительными (US 20050208074, страница 4, глава 29).
Неожиданно, автор нашел, что EEVs без предназначенной инфекции специфически имеет большую терапевтическую и/или профилактическую эффективность по сравнению с IMV.
В этом аспекте, данное изобретение имеет отношение к поксвирусам и предпочтительно рекомбинантным поксвирусам, при этом поксвирусом является EEV, без выявленной специфики инфекционности. Данное изобретение также имеет отношение к композициям и предпочтительно фармацевтическим композициям, которые включают рекомбинантный EEV без выявленной специфики инфекционности.
В том значении, как используется везде по данному описанию, термин "один" используется в том смысле, что он подразумевает "по крайней мере один", "по крайней мере первое", "один или более" или "множество" компонентов, на которые ссылаются, или этапов, если из контекста явно не исходит иное. Например, термин "клетка" включает множество клеток, включая смеси клеток.
Термин "и/или" везде, там, где используется в данном описании, включает значение "и", "или" и "все или любая другая комбинация элементов, связанных указанным термином".
Термин "около" или "приблизительно", как используется в данном описании, означает в пределах 20%, предпочтительно в пределах 10% и более предпочтительно в пределах 5% данного интервала или диапазона.
Как используется в данном описании, термин "включающий" предназначен для того, чтобы уяснять, что продукты, композиции и методы включают компоненты, на которые ссылаются, или этапы, но не исключая при этом другие.
"Включающий по существу" используется тогда, когда необходимо определить продукты, композиции и методы, и он должен означать, что исключены другие компоненты или этапы, имеющие другое любое существенное значение. Таким образом, композиция, состоящая по существу из указанных компонентов, не исключает следовые количества контаминантов и фармацевтически приемлемые носители. "Включающий" должен означать, что исключены более чем микроэлементы, другие компоненты или этапы.
Семейство поксвирусов включает вирусы Chordo - поксвирус и подсемейство Entomo - поксвирус. Среди них поксвирус является представленным согласно изобретению и предпочтительно выбранным из группы, которая включает Ortho - поксвирусы, Para - поксвирусы, Avi - поксвирусы, Capri - поксвирусы, Lepori - поксвирусы, Sui - поксвирусы, Mollusci - поксвирусы, Yata - поксвирусы. Согласно более преимущественному воплощению, поксвирусом является Ortho - поксвирус.
Ortho - поксвирус - предпочтительно вирус осповакцины, и более предпочтительно им является измененный вирус осповакцины Анкара (MVA), точнее MVA 575 (ЕСАСС VO0 120707) и MVA-BN (ЕСАСС V 00083008).
Как ранее было указано, частица IMV включает вирусное ядро, включая вирусный геном, окруженный поверхностью монослоя из липидов. Термин "EEV" относится к частице IMV, окруженной дополнительной поверхностью, состоящей из двойного липидного слоя на ее поверхностных клеточных, а также и на вирусных полипептидах.
Термин "без выявленной специфики инфекционности" в том значении, в котором он используется здесь, касается контролируемой инфекционной специфичности, при которой поксвирусная частица сориентирована таким образом, чтобы выявить новое или расширенное сродство к целевым клеткам, по сравнению со связанными и не измененными поксвирусными частицами.
В результате поксвирусная частица с выявленной спецификой инфекционности показывает, что склонность инфицировать является специфичной для целевых клеток в отличие от таких же связанных и не измененных поксвирусных частиц, что означает, что поксвирусная частица с выявленной спецификой инфекционности заражает более эффективно или/и более быстро ее целевые клетки (является представленым на их поверхности антилиганд, выявленный половиной лиганда, проявленного на поверхности поксвирусной частицы согласно представленному изобретению), чем нецелевые клетки, и предназначена для клеток (которые не выявляют на их поверхности такой антилиганд), тогда как связанная поксвирусная частица без выявленной специфики инфекционности заражает, как выявилось, целевые клетки, с более низкой или подобной эффективностью, в сравнении, для того чтобы быть не предназначенной для клеток.
Термин "рекомбинантный вирус" относится к такому вирусу, который включает экзогенную последовательность, вставленную в ее геном. В значении, используемом здесь, экзогенная последовательность касается нуклеиновой кислоты, которая в природе не присутствует в родительском вирусе.
В одном из воплощений данного изобретения экзогенная последовательность кодирует молекулу, которая имеет прямо или косвенно опосредованную цитостатическую активность. Под "прямо или косвенно" цитостатическим мы подразумеваем, что молекула, которая закодирована экзогенной последовательностью, может самостоятельно быть токсичной (например рицин, фактор некроза опухоли, интерлейкин 2, интерферон гамма, рибонуклеаза, дезоксирибонуклеаза, экзотоксин Pseudomonas А), или указанная может быть метаболизирована, для того, чтобы образовать впоследствии токсичный продукт, или указанная может оказывать влияние на что-то еще, для того чтобы сформировать токсичный продукт. Последовательность рицина кДНК раскрыта Lamb и др. (Eur. J. Biochem., 1985, 148, 265-270) и включена здесь в качестве ссылки.
В преимущественном воплощении изобретения экзогенная последовательность - ген, является способным к самоуничтожению. Ген, который является способным к самоуничтожению, кодирует белок, который является способным преобразовать относительно нетоксичный препарат в токсичный препарат. Например, фермент цитозин дезаминаза преобразовывает 5-фторцитозин (5 FC) в 5-фтороурацил (5 FU) (Mullen и др. (1922) PNAS 89, 33); фермент тимидин киназа герпеса простого делает чувствительными клетки к обработке противовирусным средством ганцикловир (G CV) или ацикловир (Mooiten (1986) Cancer Res. 46, 5276; Ezzedine и др. (1991) New Biol 3, 608). Цитозин деаминаза любого организма, например, Е.coli или Saccharomyces cerevisiae, может быть здесь использована также.
Таким образом, в более преимущественном воплощении изобретения ген, который кодирует белок, который имеет цитозин деаминазную активность и, еще более предпочтительно, белок, такой, как описано в заявках на патент WO 2005007857 и WO 9954481.
Другие примеры пролекарственных ферментных комбинаций включают раскрытые Bagshawe и др. (WO 88/07378), а именно различные агенты алкилирования и Pseudomonas spp. Фермент CPG 2, и раскрытые Epenetos & Rowlinson-Busza (WO 91/11201), а именно цианогенные пролекарства (например амигдалин) и те, которые получены из растений, в частности бета-глюкозидаза.
Ферменты, которые являются применимыми в этом воплощении изобретения, включают, но не являются ограниченными, щелочную фосфатазу, которая является применимой для преобразования содержащих фосфат пролекарств в свободные лекарства; арилсульфатазу, которая является применимой для преобразования содержащих сульфат пролекарств в свободные лекарства; протеазы, такие как серная протеаза, термолизин, субилизин, карбоксипептидазы и катепсины (такие как, например, катепсины В и L), которые являются полезными для преобразования содержащих пептид пролекарств в свободные лекарства; D-аланилкарбоксипептидаза, которая является полезной для преобразования пролекарств, которые содержат заместители D-аминокислоты; гидратирующие углевод ферменты, такие как бета-галактозидаза и нейраминидаза, которая является применимой для преобразования глюкозилированных пролекарств в свободные лекарства; бета-лактамазу, которая является полезной для преобразования производных лекарств с бета-лактамами в свободные лекарства; и амидазы пенициллина, такие как пенициллин V амидаза или амидаза Г пенициллина, которая является полезной для преобразования производных лекарств в их азотистые амины с феноксиацетиловыми или фенилацетиловыми группами, соответственно, в свободные лекарства. Альтернативно, антитела с ферментативной активностью, также известной в уровне техники как абзимы, могут использоваться для того, чтобы преобразовать пролекарства изобретения в свободные активные лекарства (Massey R. и др., Nature, 1987, 328, 457-458).
Точно так же пролекарства включают, но не являются ограниченными, вышеупомянутые пролекарства - это перечисленные пролекарства, например, содержащие фосфат пролекарства, тиофосфат содержащие пролекарства, содержащие сульфат пролекарства, содержащие пептид пролекарства, D-амино кислотно-модифицированные пролекарства, гликозилированные пролекарства, бета-лактам содержащие пролекарства, произвольно замененный феноксиацетамид содержащие пролекарства или произвольно замененные фенилацетамид содержащие пролекарства, 5-фторцитозин и другие 5-фторированные пролекарства, которые могут быть преобразованы. Примерами таких цитотоксических препаратов, которые могут быть преобразованы в форму пропрепарата для использования в этом изобретении, включают, но не являются ограниченными, этопозид, тенипозид, адриамицин, дауномоцин, карминомицин, аминоптерин, дактиномицин, митомицин, цисплатину и аналоги цисплатины, блеомицин, эсперамицин (см., например, US 4,675,187), с 5-фтороурацилами, мелфалан и другие, связанные азотом иприта.
В дальнейшем воплощении экзогенный ген кодирует рибозим, который является способным расщеплять и предназначен для РНК или ДНК. Предназначенными РНК или ДНК, которые будут расщеплены, могут быть РНК или ДНК, которые являются существенными для функционирования клетки, и расщепление их приводит к некрозу клеток или РНК, или ДНК, которые будут расщеплены, может быть РНК или ДНК, которые кодирует нежелательный белок, например онкогенный продукт, и расщепление этой РНК или ДНК может препятствовать тому, чтобы клетка стала злокачественной.
Во всех следующих дальнейших воплощениях экзогенный ген кодирует антисмысловую РНК.
Под "антисмысловой РНК" мы подразумеваем такую молекулу РНК, которая скрещивается и интерферируется с экспрессией мРНК молекулы, которая кодирует белок, или другой молекулы РНК в пределах клетки, такой как пре-мРНК или тРНК или рРНК, или скрещивается и интерферируется с экспрессией гена.
В другом воплощении изобретения экзогенная последовательность заменяет функцию дефектного гена в целевой клетке. Есть несколько тысяч унаследованных генетических болезней млекопитающих, включая людей, которые вызваны такими дефектными генами. Примеры таких генетических болезней включают кистозный фиброз, при котором, как известно, происходит мутация в гене CFTR; мускулярную дистрофию Дюххенна, при которой, как известно, происходит мутация в дистрофичном гене; болезнь серповидных клеток, при которой, как известно, происходит мутация в гене HbA. Много типов рака вызваны дефектными генами, особенно протоонкогенными, и генами супрессора опухоли, которые подверглись мутации.
Примеры протоонкогенов - ras, src, bcl и так далее; примеры генов супрессора опухоли - р 53 и Rb.
В дальнейшем воплощении изобретения экзогенная последовательность кодирует опухоль ассоциированный антиген (ТАА). ТАА обращается к молекуле, которая обнаружена при более высокой частоте или плотности в клетках опухоли, чем в клетках неопухоли того же самого типа ткани. Примеры ТАА включают, но не являются ограниченными СЕА, MART - 1, MAGE - 1, MAGE - 3, GP - 100, MUC - 1, MUC - 2, указанный мутированный ras онкоген, нормальный, или точечно мутированный р 53, сверх экспрессированный р 53, СА - 125, PSA, С - erb / В2, BRCA I, BRCA II, PSMA, тирозиназа, TRP - 1, TRP - 2, NY - ESO - 1, TAG 72, KSA, HER-2/neu, Icг - aI. раз - fkhr, ews - fli - 1, сохранившийся и LRP. Согласно более преимущественному воплощению является представленным в данном изобретении ТАА MUC 1.
Рекомбинантный ген поксвируса может включать больше чем одну экзогенную последовательность, и каждая экзогенная последовательность может кодировать больше чем одну молекулу. Например, может быть пригодна проассоциировать в том же самом рекомбинантном гене поксвируса экзогенное секвенированное кодирование ТАА с экзогенной последовательностью, которая кодирует цитокин.
В другом воплощении изобретения экзогенный ген кодирует антиген.
В значении, используемом здесь, "антиген" касается лиганда, который может быть связан антителом; антиген должен не непосредственно быть иммуногенным.
Предпочтительно антиген получен из вируса, такого как, например, HIV - 1 (такой как gp 120 или gp 160), любой кошачий вирус иммунной недостаточности, человеческий или вирус герпеса животных, такие как gD или производные этого, или непосредственно ранний белок, такие как ICP 27 из HSV 1 или HSV 2, цитомегаловирус (такие как gB или производные этого). Varicella Zoster вирус (такие как gp 1, II или III), или из вируса гепатита, такие как вирус гепатита В, например антиген поверхности гепатита В или производная этого, вирус гепатита А, вирус гепатита С (предпочтительно не структурный белок от генотипа 1b штамма ja) и вирус гепатита Е, или из других вирусных болезнетворных микроорганизмов, таких как респираторно сцинцитиальный вирус, вирус папилломы человека (предпочтительно Е 6 и белок Е 7 из штамма HPV 16) или вирус гриппа, или полученный из бактериальных болезнетворных микроорганизмов, таких как сальмонелла, Neisseria, боррелия (например, Osp А или Osp В или производные указанных), или Chlamydia, или бордетелла, например Р.69, РТ и FHA, или полученный из паразитов, таких как плазмодий или токсоплазма.
В особенно преимущественном воплощении изобретения рекомбинантный ген поксвируса кодирует те же самые белки, что и TG 4010 (Rochlitz и др. J Gene Med, 2003 Aug; 5 (8): 690-900) и TG 4001 (Liu и др. Proc Nan Acad Sci США. 2004, 5 октября; 101 Suppl 2: 14567-14571). В другом особенно преимущественном воплощении изобретения у поксвируса согласно представленному изобретению есть последовательность, которая является на больше чем 90% гомологичной относительно последовательности TG 4010 или TG 4001.
Преимущественно, что рекомбинантный ген поксвируса далее включает элементы, необходимые для экспрессии экзогенной последовательности. Элементы, необходимые для экспрессии, включают набор таких элементов, которые позволяют реализовывать транскрипцию последовательности нуклеотида к РНК и трансформацию мРНК в полипептид, в особенности промоторные последовательности и/или регулирующие последовательности, которые являются эффективными в клетке, которая будет заражена рекомбинантным геном поксвируса согласно представленному изобретению, и произвольных последовательностей, требуемых для выделения или выражения на поверхности клеток для указанного полипептида. Эти элементы могут быть индуцибельными или конститутивными. Конечно, промотор может быть адаптирован к рекомбинантному гену поксвируса и подобран под клетку хозяина. Тут могут быть упомянуты, посредством примера, промоторы вируса осповакцины р 7.5К р H5R, р K1L, р 28, р 11 или комбинации указанных промоторов. Литература позволяет получить большое количество информации, касающейся таких последовательностей промотора.
Необходимые элементы могут, кроме того, включать дополнительные элементы, которые улучшают экспрессию экзогенной последовательности или ее существование в клетке хозяина. Тут могут быть упомянуты, в особенности, последовательности интрона (WO 94/29471), последовательности сигнальной секреции, ядерные последовательности локализации, внутренние участки для переинициирования трансляции IRES типа, поли А последовательности, предназначенные для завершения транскрипции.
Доступные способы производства поксвирусов включают репликацию вируса в клеточной линии (например, в Hela S 3), в эмбрионах яиц или в эмбрионах куриных фибробластов. После репликации вируса культуральная среда является непригодной, клетки являются лизированными, и поксвирус, который высвободился из клеток, очищают центрифугированием в градиенте плотности сахарозы (Kotwal and Abraham; Поксвирус growth, Purification and tittering in Vaccinia Virus and Poxvirology, 2004, 101-108, Humana Press Inc., Totowa; NJ; США). Согласно этим способам никакие EEVs не являются присутствующими в очищенной композиции.
Однако доступные способы вирусного производства не являются удовлетворительными. Во-первых, они включают использование композиций, происходящих из животных, таких как сыворотка и ферменты. При использовании композиций, происходящих из животных, в способах производства есть несколько недостатков. Например, химический состав этих композиций может изменяться между партиями, даже в том случае, если изготовитель является одним и тем же лицом. Композиции могут также быть загрязнены инфекционными агентами (например, микоплазмы и вирусы), что может серьезно негативно повлиять на состояние культивируемых клеток, в том случае, когда эти загрязненные примеси используются в композициях сред для клеточных культур.
Кроме того, использование дополнительной сыворотки для культуральных сред может усложнить и увеличить затраты очистки целевых веществ от культуральных сред из-за неспецифичной очистки сыворотки или извлекаемых белков. Наиболее важно то, что использование неопределенных композиций может препятствовать одобрению медицинскими агентствами фармацевтической композиции, полученной данным способом.
Данное изобретение далее описывает способ продуцирования поксвирусных частиц согласно данному изобретению, который включает следующие этапы:
a) приготовление культуры упаковываемых клеток,
b) инфицирование указанной клеточной культуры,
c) культивирование указанных зараженных клеток в течение соответствующего промежутка времени,
d) восстановление поксвирусных частиц, продуцируемых в супернатант культуры, и/или клеток с дефектом упаковки нуклеотидных последовательностей, и
e) произвольно, очистка восстановленных поксвирусных частиц.
Способ согласно данному изобретению предпочтительно является свободным от продуктов животного происхождения.
Способ согласно данному изобретению может также использоваться для производства дикого типа, и/или аттенуированного поксвируса.
В значении, как используется здесь, термин "аттенуированный поксвирус" относится к любому поксвирусу, который был изменен так, чтобы его патогенность относительно инфицированного предмета была существенно уменьшена. Предпочтительным является то, что поксвирус является аттенуированным по сути и является непатогенным с клинической точки зрения, иными словами, это означает, что выявленный поксвирус не проявляет статистически существенного увеличенного уровня патологических изменений относительно контрольных объектов.
Согласно преимущественному воплощению данного изобретения, аттенуированный вирус - это аттенуированный вирус осповакцины, такой как MVA.
Термин "инфекция" относится к передаче вирусной нуклеиновой кислоты к клетке, причем вирусная нуклеиновая кислота реплицируется, вирусные белки синтезируются или собираются новые вирусные частицы.
В значении, как используется здесь, термин "упаковываемая клетка" относится к клетке, которая может быть заражена поксвирусом, который будет произведен. Клетка с дефектом упаковки нуклеотидных последовательностей может быть первичной клеткой, рекомбинантной клеткой и/или клеточной линией. Например, может также быть использована рекомбинантная клетка, которая содержит элементы, необходимые для производства рекомбинантного вируса, которых нет в рекомбинантном вирусном векторе.
В одном воплощении изобретения клетка с дефектом упаковки нуклеотидных последовательностей - непрерывная линия клеток птиц.
В одном воплощении изобретения упаковываемая клетка - клетка DF1 (US 5,879,924), которая является спонтанно перевиваемой куриной клеточной линией, полученной из 10-дневных яиц старой Восточной Линии Лансинга (ELL - 0).
Непрерывная линия клеток птиц может быть получена из эмбриональных стволовых клеток прогрессирующим разведением ростовым фактором вырастающих слоев клеток, таким образом поддерживая особенности роста и особенность непрерывной продолжительности жизни недифференцированной линии. Например, куриная клеточная линия Ebx (WO 2005007840) была получена этим способом.
Согласно преимущественному воплощению, утиный эмбрион может также использоваться в качестве постоянной клеточной линии. Например, клеточная линия, определяемая как DEC 99 (Ivanov и др. Experimental Pathology And Parasitology, 4 / 2000 Bulgarian Academy of Sciences), была культивирована в течение более чем 140 последовательных пассажей, и это было не онкогенно для птиц. Клеточные линии DEC 99 - стандартная система клеточной культуры, которая использовалась для исследования и может быть использована для целей биотехнологии. Согласно более преимущественному воплощению, клетка с дефектом упаковки нуклеотидных последовательностей - клеточная линия, которая получена способом, раскрытым в заявке на патент ЕР 06360001.9.
Согласно другому преимущественному воплощению, клетка с дефектом упаковки нуклеотидных последовательностей является эмбрионами куриных фибробластов (CEF). Подготовка и использование CEF для производства вирусов известны специалисту, квалифицированному в данной области техники.
CEF предпочтительно являются экстрагированными из свободных от специфичных патогенов яиц (SPF). Яйца SPF являются коммерчески доступными, например от лабораторий Charles River (Уилмингтон, Массачусетс, США). Указанным яйцам предпочтительно больше чем 9 дней, более предпочтительно между 10 и 14 дней и еще более предпочтительно 12 дней.
Перед извлечением эмбриона яйцо предпочтительно дезинфицируют. Много методов и продуктов, предназначенных для дезинфекции яиц, доступны из предшествующего уровня техники. Инкубация в растворе формола (например, 2% формол, 1 мин) с последующим полосканием в 70% этаноле является особенно предпочтительной.
Клетки эмбрионов после этих процедур отделяют и очищают. Согласно преимущественному воплощению данного изобретения, клетки подвергают этапу ферментативного вываривания, что позволяет разрушать межклеточный матрикс. С этой целью использование фермента, способного расщепить межклеточный матрикс, особенно полезно. Такой фермент может быть выбран из группы, которая включает, но не ограничена трипсином, коллагеназой, проназой, диспазой, гиалуронидазой, нейраминидазой. Этот фермент может использоваться один или в комбинации. В особенно преимущественном воплощении изобретения диспаза и трипсин (например. Tryp LE, выбранный из Gibco™), используются в комбинации. Любое лицо, квалифицированное в данном уровне техники, в состоянии определить концентрацию фермента, температуру и длительность инкубации, позволяющие эффективное разделение клеток.
Согласно преимущественному воплощению способ согласно данному изобретению свободен от продуктов животного происхождения (кроме клеток с дефектом упаковки нуклеотидных последовательностей). С учетом этого фермент(ы), используемый для подготовки CEF, имеет(ют) предпочтительно рекомбинантное происхождение. В значении, используемом здесь, «продукты животных» означают любую композицию или коллекцию композиций, которая была произведена или клеткой животных, или в живом организме.
Подготовка CEF может далее включать этап фильтрации и/или этап центрифугирования, для того чтобы удалить загрязнители.
Эта первичная клетка CEF может использоваться или непосредственно, или после одного дальнейшего пассажа клетки как вторичная клетка CEF.
Любое лицо, квалифицированное в данном уровне техники, в состоянии выбрать наиболее соответствующую клетку для производства определенного вируса. Согласно преимущественному воплощению, способ согласно данному изобретению включает использование CEF или клетки согласно ЕР 06360001.9 для производства MVA.
Клетка с дефектом упаковки нуклеотидных последовательностей, используемая в способе согласно представленному изобретению, выращена в соответствующих культуральных средах. Возможно использовать больше чем одну культуральную среду в способе согласно представленному изобретению. Например, первая культуральная среда может использоваться во время подготовки клетки с дефектом упаковки нуклеотидных последовательностей (то есть во время этапа а) и вторая среда клеточной культуры - для инфекции (то есть во время этапа с и/или этап b).
Согласно преимущественному воплощению культуральные среды согласно данному изобретению свободны от продуктов животного происхождения.
Многие их культуральных сред, свободных от продуктов животного происхождения, были уже описаны, и некоторые из них являются коммерчески доступными. Например, 293 SFM II; 293 - F Cells, SFM Adapted; 293 - H Cells, SFM Adapted; 293 fectin™ Transfection Reagent; CD 293 AGT™; CD 293 Medium; FreeStyle™ 293 Expression System; FreeStyle™ 293 Medium; FreeStyle™ 293 - F Cells, SFM Adapted; Adenovirus Expression Medium (AEM) Growth Medium for PER.C6® Cells; CD 293 AGT™; CD 293 Medium; COS - 71 - Cells, SFM Adapted; EPISERF® Medium; OptiPro™ SFM; VP - SFM; VP - SFM AGT™ (все являются доступными и имеются в продаже) могут использоваться в качестве культуральных сред в способе согласно представленному изобретению.
Случаи, когда клетка с дефектом упаковки нуклеотидных последовательностей является CEF, VP - SFM (invitrogen) для этапа а) и минимальная среда для яиц (invitrogen) является средой культивирования для этапа b) и с), являются особенно предпочтительными.
Специфическим воплощением являются представленные согласно изобретению те случаи, когда клетки с дефектом упаковки нуклеотидных последовательностей являются CEF, и среда для клеточной культуры является выбранной между от 0.5 до 1.5 и предпочтительно является выбранной между 1.1 и 1.3 и более предпочтительным случаем является приблизительно 1.2 эмбрионов / литр среды клеточной культуры.
В этом воплощении CEF предпочтительно являются выращенными между 1 и 5 днями, более предпочтительно являются выращенными между 1 и 2 днями и еще более предпочтительно являются выращенными за 2 дня до инфекции.
Специфическим воплощением согласно данному изобретению, являются те случаи, когда поксвирус, который является пригодным для того, чтобы его продуцировать, является представленным MVA, при этом указанный вирус введен в среду клеточной культуры в MOI, который предпочтительно является расположенным между 0.001 и 0.1, более предпочтительно является расположенным между 0.03 и 0.07 и еще более предпочтительно является расположенным приблизительно 0.05.
Специфическим воплощением согласно данному изобретению являются те случаи, когда во время этапа с) клетки с дефектом упаковки нуклеотидных последовательностей выращены при температуре, которая ниже чем 37°С, предпочтительно при температуре между 30°С и 36.5°С или при температуре между приблизительно 32°С и о 36°С, более предпочтительно при температуре между 33°С и 35°С, наиболее предпочтительно при температуре, которая равняется 34°С.
Специфическим воплощением согласно данному изобретению являются те случаи, когда этап с) длится от одного до шести дней, более предпочтительно длится между двумя и четырьмя днями и наиболее предпочтительно длится приблизительно 72 ч.
После того как этап инфекции является совершенным, клетки, которые находятся в культуральной среде, и те из них, которые будут использованы для того, чтобы вырастить клетку с дефектом упаковки нуклеотидных последовательностей, собирают. Указанные клетки из культуральной среды включают также частицы EEV, элиминированные из зараженной клетки с дефектом упаковки нуклеотидных последовательностей.
Согласно преимущественному воплощению данного изобретения, после этапа инфекции, проводят этап сбора клеток из культуральной среды и клеток с дефектом упаковки нуклеотидных последовательностей. Среда, в которой были выращены клетки, и клетки с дефектом упаковки нуклеотидных последовательностей могут быть объединенными или сепарированными отдельно.
Для того чтобы получить поксвирусы, которые представлены на клетках с дефектом упаковки нуклеотидных последовательностей, способ согласно данному изобретению может включать этап, который позволяет их разрушить. Этот этап приводит к высвобождению поксвирусов из клеток с дефектом упаковки нуклеотидных последовательностей. Разрушение мембраны клеток с дефектом упаковки нуклеотидных последовательностей может быть произведено различными методами, известными тем лицам, которые являются квалифицированными в данной отрасли техники. Эти методы включают, но не являются ограниченными, разрушение ультразвуком, замораживание/таяние, гипотонический лизис, а также микрофлюидизацию.
Согласно преимущественному воплощению данного изобретения мембраны клеток с дефектом упаковки нуклеотидных последовательностей разрушают при использовании гомогенизатора высокой скорости. Гомогенизаторы высокой скорости являются коммерчески доступными от фирмы Silverson Machines Inc (East Longmeadow, США) или фирмы Ika - Labotechnik (Staufen, Германия). Согласно особенно преимущественному воплощению представленного изобретения гомогенизатором высокой скорости может являться гомогенизатор SILVERSON L4R.
В том случае, когда клетка с дефектом упаковки нуклеотидных последовательностей и среда культивирования клеток являются объединенными, разрушение мембраны клеток с дефектом упаковки нуклеотидных последовательностей не проводят методом замораживания/таяния, по той причине, что эта техника приводит к разрушению частиц EEV (Ichihashi у. и др. 1996, virology, 217 (2), 478-85).
Согласно преимущественному воплощению представленного изобретения, этап d) далее включает этап кларификации, который позволяет получить отделение клеточных осколков. Согласно более преимущественному воплощению данного изобретения, указанным выше этапом кларификации может быть этап глубинной фильтрации.
Процесс глубинной фильтрации включает, но не является ограниченным, использованием одного или более коммерчески доступных следующих продуктов: глубинные фильтры ряда АР CUNO Incorporated (примеры, которые включают АР 01), CUNO, глубинные фильтры CUNO Incorporated ряда (примеры, которые включают СР 10, СР 30, СР 50, СР 60, СР 70, СР 90), глубинные фильтры CUNO Incorporated ряда, например, которые включают HP 10, HP 30, HP 50, HP 60, HP 70, HP 90), глубинные фильтры CUNO Incorporated Халиф ряда (примеры, которые включают СА 10, СА 30, СА 50, СА 60, СА 70, СА 90), глубинные фильтры CUNO Incorporated SP ряда (примеры, которые включают SP 10, SP 30, SP 50, SP 60, SP 70, SP 90), глубинные фильтры CUNO Delipid и Delipid Плюс фильтры, Корпорация Millipore, ряда СЕ (примеры, которые включают СЕ 15, СЕ 20, СЕ 25, СЕ 30, СЕ 35, СЕ 40, СЕ 45, СЕ 50, СЕ 70, СЕ 75), глубинные фильтры Корпорации Millipore ряда DE (примеры, которые включают DE 25, DE 30, DE 35, DE 40, DE 45, DE 50, DE 55, DE 60, DE 65, DE 70, DE 75), фильтры НС Корпорации Millipore (примеры, которые включают А1 НС, В1 НС, СО НС), фильтры CUNO полинет (примеры, которые включают Полинет - ПБ, Millipore Clarigard и Polygard фильтры, CUNO Life Assure, глубинные фильтры Ассоциации Man Cel (примеры, которые включают, но не являются ограниченными, PR 12 UP, PR 12, PR 5 UP), и PALL или SeitzSchenk Incorporated фильтры. Для того чтобы улучшить способность к кларификации доступных единиц глубинных фильтров, может быть полезно соединить две или больше единицы с такими размерами пор, которые уменьшаются. В этом воплощении изобретения, смесь, которая будет кларифицирована, проходит через первую единицу глубинного фильтра, где остаются самые крупные контаминанты, и впоследствии проходит через вторую единицу глубинного фильтра. Согласно более преимущественному воплощению представленного изобретения, sartopure® (sartorius) с размером пор 8 мкм, соединенный с sartopure® с размером пор 5 мкм, можно также использовать для этапа глубинной фильтрации.
Согласно преимущественному воплощению представленного далее изобретения, способ включает этап концентрирования. Более предпочтительно, указанный этап концентрирования далее позволяет элиминировать те белки, которые находятся в смеси, полученной на ранее описанных этапах.
Согласно более преимущественному воплощению представленного изобретения, указанный этап концентрирования является этапом микрофильтрации. Микрофильтрация - это такой способ применения давления, относительно мембранных способов, благодаря которому может быть реализовано концентрирование, а также указанный способ позволяет очищать большие молекулы. Более преимущественно, раствор подают через полуводопроницаемую мембрану, размеры пор которой выбирают при этом таким образом, чтобы задержать большие частицы (вирусы) в слоях фильтрующего материала, и позволить маленьким молекулам (например, белкам) проходить через мембрану в пермиат. Микрофильтрация уменьшает объем того раствора, который подвержен концентрированию.
Согласно преимущественному воплощению представленного изобретения, этап микрофильтрации сопровождается этапом диафильтрации. Эти два этапа могут быть осуществлены с теми же самыми мембранами фильтрации. Диафильтрация является усовершенствованием процесса микрофильтрации и позволяет дилюировать концентрат раствора и привести к эффекту сокращения концентрирования примесей в концентрате. Растворение концентрата позволяет вымывать больше примесей из концентрата. Имеется в виду то, что диафильтрация может быть осуществлена в пакетном режиме, в полунепрерывном способе, или в непрерывном способе. Этап диафильтрации может быть с пользой использован для того, чтобы изменить буфер, в котором находится вирус. Например, может быть полезно изменить буфер, используемый в способе очистки, на буфер, который является приемлемым для фармацевтической продукции.
Предпочтительно, мембранами фильтрации, используемыми в микрофильтрации и/или в этапе диафильтрации, являются мембраны, которые включают размеры пор между 0.01 и 0.15 мкм, и более предпочтительно, которые включают размеры пор, приблизительно 0.1 мкм.
Нуклеиновые кислоты могут содержаться в полученных частицах клетки, таких как вирусы. С учетом этого, способ согласно данному изобретению, может произвольно далее включать этап, состоящий в удалении находящихся нуклеиновых кислот, в качестве контаминантов, в растворе. С этой целью могут быть использованы нуклеазы. Примеры нуклеаз включают бензоназу или любую другую дезоксирибонуклеазу или RN азу, которые обычно используют для целей данного отрасли техники, среди них бензоназа является особенно предпочтительной.
Бензоназа разрушает нуклеиновую кислоту и не имеет никакой протеолитической активности. При этом бензоназа быстро разрушает нуклеиновую кислоту, гидролизируя внутренние фосфодиэфирные связи между определенными нуклеотидами. После полного разрушения, является весь свободный пул нуклеиновых кислот в растворе уменьшенным до олигонуклеотидов размером из 2-4 оснований по длине. Бензоназа может быть использована при этапе конечного концентрирования, состоящего между 50 и 400 Ед/мл, предпочтительно состоящего между 100 и 300 Ед/мл и более предпочтительно состоящего между 150 и 250 Ед/мл. Обработка бензоназой может продлиться в течение 1 ч и 4 ч и еще более предпочтительно в течение 1.5 ч и 2.5 ч.
Однако в том случае, когда глубинная фильтрация, микрофильтрация и диафильтрация, ранее описанные, используются, использование нуклеаз, и более конкретно, использование бензоназы не является необходимым. С учетом этого, данное изобретение также касается способа такого производства поксвируса, в котором нуклеазы, и более конкретно, никакой бензоназы, не используется.
На данном этапе поксвирус, полученный согласно способу, ранее описанному, является достаточно очищенным. Возможным является изменение буфера, в котором находится вирус. Например, может быть целесообразным заменить буфер, используемый в способе очистки, на фармацевтически приемлемый буфер. Множество методов, пригодных к применению для того, чтобы заменить буфер, известны лицу, квалифицированному в данной отрасли техники. Среди таких методов особенно предпочтительным является способ тангенциальной фильтрации.
Способ тангенциальной фильтрации является такой техникой фильтрации, при которой та суспензия, которая будет отфильтрована на этом этапе, при высокой скорости ориентирована вдоль того направления, которое идет параллельно направлению поверхности фильтрования, для того чтобы создать турбулентность, которая предотвращает формирование комка фильтрования, и также довольно частое блокирование фильтра.
В то время как потоки суспензии направлены при высокой скорости, которая параллельна относительно проникающей поверхности, раствор проходит через и проникает сквозь поверхностные отверстия из-за разности давления и непрерывно при этом удаляется. Поверхностное фильтрование должно быть таким для того, чтобы не происходило механического сопротивления, чтобы дать возможным возникнуть градиенту давления в разных частях фильтрующей поверхности (то есть, разницы концентраций суспензии) и концентрата на поверхности (чистый отфильтрованный раствор, свободный от суспендированных частиц).
Различные этапы, из которых состоит способ согласно данному изобретению, могут быть осуществлены на разделенных рабочих местах и/или в различных периодах времени. Например, инфицирование клетки с дефектом упаковки нуклеотидных последовательностей и очистка поксвирусов могут быть осуществлены на различных рабочих местах. Также, клетки с дефектом упаковки нуклеотидных последовательностей и/или до тех пор будут реализованы, пока будет необходимо их очищать.
Данное изобретение также имеет отношение к таким композициям, которые могут быть получены согласно способу, ранее описанному, и к тем композициям, которые включают поксвирус согласно представленному изобретению. Предпочтительно, композиция, согласно представленному изобретению, включает больше чем 1%, предпочтительно больше чем 5%, еще более предпочтительно больше чем 10% и наиболее предпочтительно по крайней мере 20% поксвируса, который состоит в указанной композиции, при этом вирусом являются EEV.
Согласно преимущественному воплощению представленного изобретения, для композиции согласно представленному изобретению являются пригодными титры по крайней мере 105, предпочтительно по крайней мере 106, более предпочтительно по крайней мере 107, еще более предпочтительно по крайней мере 108 вирусных частиц на мл.
Согласно другому преимущественному воплощению представленного изобретения, для композиции являются пригодным титры по крайней мере 103, предпочтительно по крайней мере 104, более преимущественно по крайней мере 3∗103 вирусных частиц на микрограмм белка.
Данное изобретение также имеет отношение к таким фармацевтическим композициям, которые включают поксвирус, полученный по способу согласно данному изобретению, и/или композициям, согласно представленному изобретению. В том значении, в котором используется здесь, термин "фармацевтическая композиция" является такой композицией, которая включает фармацевтически приемлемые добавки.
Такие добавки являются предпочтительно изотоническими, гипотоническими или слабо гипертоническими и имеют относительно низкую ионную силу, такие как, например, раствор сахарозы.
Кроме того, такие добавки могут содержать любой растворитель, или водную или частично водную жидкость, такую как непирогенная стерильная вода. рН фактор фармацевтической композиции, кроме того, может быть адъюирован и буферизован, для того чтобы соответствовать требованиям использования в естественных условиях.
Фармацевтическая композиция может также включать фармацевтически приемлемый растворитель, адъювант или наполнитель, так же как и солюбилизирующие, стабилизирующие и сохраняющие агенты.
Для таких путей введения, как инъекции, для композиции предпочтительны водные, неводные или изотонические растворы. Это может быть обеспечено в единственной дозе или в мультидозе для формы жидкости или сухого состояния (порошок, лиофилизат и т.п.), которая может быть воссоздана во время непосредственного использования с соответствующим растворителем.
Данное изобретение также имеет отношение к поксвирусам и композициям, полученным способом согласно данному изобретению.
Данное изобретение также имеет отношение к использованию способа согласно представленному изобретению для производства вируса, композиции и/или фармацевтической композиции.
Данное изобретение также имеет отношение к использованию поксвируса, композиции и/или фармацевтической композиции согласно представленному изобретению для подготовки лекарственного средства.
Согласно преимущественному воплощению данного изобретения лекарство, согласно представленному изобретению, является лекарством для терапевтического или профилактического лечения рака.
Среди тех расстройств, которые могут быть предусмотрены, могут быть упомянуты раковые образования груди, матки (в особенности вызванные вирусами папилломы), простаты, легких, мочевого пузыря, печени, толстой кишки, поджелудочной железы, живота, пищевода, гортани, центральной нервной системы (в преимуществе глиомы) и крови (лимфомы, лейкемия и т.п.).
Композиция согласно представленному изобретению может быть произведена традиционно для таких путей введения, как местный, парентеральный или энтеральный пути.
Могут быть предусмотрены следующие способы введения: внутрижелудочный, подкожный, внутрисердечный, внутримышечный, внутривенный, внутрибрюшинный, внутриопухолевый, интраназальный, интралегочный или внутритрахеальный пути введения.
Для последних трех случаев введение аэрозолем или путем инстилляции является более выгодным.
Путь введения может быть представленным как единственная доза, или как разовая доза, или как доза в несколько раз после определенного временного интервала. Соответствующий путь введения и дозировка изменяются как функция различных параметров, например человека, болезни, которую будут рассматривать, или гена(-ов) заболевания, который будет передан.
Согласно первой возможности, лекарство может быть введено непосредственно в естественных условиях (например, внутривенная инъекция в доступную опухоль или в ее периферию, преимущественно для терапевтической или профилактической прививки). Также возможно принять его ex vivo подходом, который состоит в том, что получают клетки от пациента (стволовые клетки костного мозга, лимфоциты периферической крови, мышечные клетки и т.п.), транспортируют их или инфицируют их в пробирке согласно предшествующим методам, известным из уровня техники, и вводят их пациенту.
Кроме того, возможно предусмотреть способы, где соответственно и не отступая от предмета существующего изобретения, выполняют одновременные или последовательные пути введения, различными способами, различных компонентов, которые содержатся в фармацевтической композиции или в композиции согласно представленному изобретению.
Согласно преимущественному воплощению представленного изобретения, терапевтическое использование или метод лечения могут быть объединены с иным лечением пациента хирургическим путем (частичное или полное удаление опухоли), радиотерапией или химиотерапией. В данном случае, лечение согласно представленному изобретению может быть применено до, одновременно или в качестве последующего вслед за указанным иным лечением.
Предпочтительно, это лечение будет применено в качестве последующего вслед за указанным вторым лечением.
Согласно другому преимущественному воплощению данного изобретения лекарство предназначено для терапевтического или профилактического лечения инфекционных, в особенности болезней вирусного происхождения, вызванного гепатитом В или вирусом С, ВИЧ, герпесом, ретровирусами и т.п.
Примеры, которые следуют, предназначены для того, чтобы проиллюстрировать различные предметы существующего изобретения и, следовательно, не ограничивают его по сути.
Фиг.1: изображает норму выживания мышей С 57BL / 6, которым имплантирован с клетками ТС 1, экспрессирующими HPV 16 Е6 и Е7, онкоген C-Ha-ras. Различные группы мышей обрабатывали с помощью композиций, которые включают IMV и EEV, кодирующие антигены HPV, IMV, кодирующие антигены HPV или IMV и не кодирующие каких-либо антигенов.
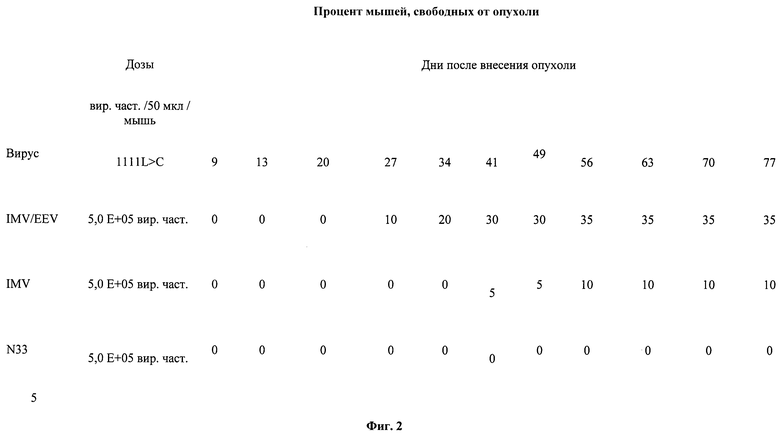
Фиг.2: изображает процент от мышей С 57BL / 6, свободных от опухоли после внесения с клетками ТС1, экспрессирующими HPV 16 Е6 и Е7 и онкоген C-Ha-ras. Различные группы мышей обрабатывали с помощью композиций, которые включают IMV и EEV, которые кодируют антигены HPV, IMV и которые кодируют антигены HPV или IMV, не экспрессирующий каких-либо антигенов.
Фиг.3: изображает норму выживания мышей С 57BL / 6, которым было имплантировано при помощи клеток ТС 1, которые экспрессируют MUC 1. Различные группы мышей обрабатывали при помощи композиций, которые включают IMV и EEV, который кодирует MUC 1 и IL 2, IMV, который кодирует MUC 1 и IL 2 или IMV, который не экспрессирует каких-либо антигенов.
Примеры
1. Приготовление композиций, которые включают IMV и EEV.
А. Подготовка CEF.
Шестьдесят шесть яиц SPF были инкубированы в течение 60 с в 2% растворе формола. После ополаскивания в 70%-ном этаноле яйца были вскрыты, эмбрионы были извлечены и были подвержены анализу. Полученные ткани были обработаны при 36.5°С в течение 120 минут диспазой (МЕд/мл) и втройне отселектированы (МЕд/мл). Смесь была отфильтрована для того, чтобы удалить необработанные ткани, и CEF собраны центрифугированием (2300 оборотов в минуту, в течение 15 мин).
В. Культивирование CEF и инфицирование.
CEF были инкубированы в 55 л VP-SFM (инвитрогенно) в течение 2 дней при 36.5°С. Среда культивирования для клеток была отобрана, и был далее добавлен поксвирус (0.05 MOI) в 55 л минимальной среды для яиц (инвитрогенная). Зараженные клетки с дефектом упаковки нуклеотидных последовательностей были далее инкубированы в течение трех дней.
С. Очистка поксвируса.
Клетки с дефектом упаковки нуклеотидных последовательностей и среда культивирования клеточной культуры были собраны.
Смесь далее была гомогенизирована в течение 15 мин в гомогенизаторе высокой скорости Silverson® L 4 R. Смесь, которая была получена, далее была кларифицирована методом глубинной фильтрации на ячейках 8 мкм (sartorius), соединенных с ячейками 5 мкм при расходе 1 литр/мин.
Смесь далее была сконцентрирована 18 раз через 0.1 мкм модуль микрофильтрации Prostak (относительно: PSWAG 021, Millipore).
Поксвирусная композиция далее была подвержена диафильтрации на том же самом модуле относительно желаемого фармацевтически приемлемого дополнительного агента.
2. Терапевтическая эффективность относительно композиций, которые включают EEV и IMV, и композиций, которые включают только IMV.
А. Терапевтическая обработка мышей, переносящих опухоль, которые экспрессируют антигены HPV.
Наименование и краткое описание каждой векторной конструкции
TG 4001: вектор MVA, несущий кодирующие последовательности для белков HPV, Е6 и Е7, (под контролем промотора р 7.5) и IL 2 (под контролем промотора рН 5R). Были проверены две партии, одна из которых включала IMV и EEV (подготовленный, как ранее раскрыто) и одна из которых включала только IMV.
N 33: пустой вектор MVA, который не экспрессирует ни белков HPV Е6 и Е7, ни IL 2, при этом он был использован в качестве отрицательного контроля.
Модель животного
Животные - самки мыши модели С57 BI / 6 в возрасте 6-8 недель были использованы в течение этого всего исследования. Указанные мыши были получены от Charles River (Руан, Франция).
Спецификация: животным было 6 недель в день прибытия. В начале эксперимента животным было меньше чем 8 недель.
Окружающая среда: животные были размещены в единственной, эксклюзивной комнате, которая была кондиционируема, для того чтобы обеспечить минимум 11 воздушных объемов в час. Диапазоны температурной и относительной влажности были расположены в пределах 18°С и 22°С и 40-70% соответственно. Освещение управлялось автоматическим путем, для того чтобы получать цикл 12 часов света и 12 часов темноты.
Специфичный патогенный свободный статус был проверен регулярным контролем окружающей среды.
Питание: в течение всего времени исследования у животных был свободный доступ к стерильному типу диеты D 04 (UAR, Epinay sur Orge, Франция). Вода была подана свободно через бутылки.
Акклиматизация и процедуры здоровья:
Всем животным был проведен клинический осмотр здоровья в момент прибытия. Они были акклиматизированы в специфичном свободном от патогенов средстве для животных (SPF) между одной и двумя неделями перед началом эксперимента, для того чтобы была гарантирована их пригодность для исследования.
Особенности клеток опухоли и условия использования:
Линия ТС 1 была получена из первичного легкого эпителиальных клеток мышей С57 BI / 6, которые были котрансформированы с HPV - 16 Е6 и Е7 и c-Ha-ras онкогенами Эти клетки растут в DMEM с глутамином (2 мМ), эмбриональной сывороткой теленка (10%), незаменимыми аминокислотами (0.1 мМ), в пирувате (1 мМ), парамеркаптоэтаноле (3 мкмМ, Hygromycine (0.2 мг/мл) и G 418 (0.5 мг/мл). После размораживания клетки были амплифицированы два раза, последний пасаж был выполнен за два дня до клеточной инъекции.
Клеточная инъекция
Клеточная инъекция была проведена в первый день эксперимента, клетки ТС 1 были введены под кожу мышам в дозе 2.0 Е + 05 клеток на мышь.
Вирусное инфицирование
По истечении 7 дней после инъекции клеток, 5.0 Е + 05 pfu / 50 мкл/мышь тестированных партий (TG 4001 IMV/EEV или IMV только) MVATGN 33 (пустой вектор) были введены в мышей. Двадцать мышей использовались как тестированная партия.
Вирусное инъецирование было выполнено под кожу, но на отдаленном участке от места инъекции клеток, и было выполнено 3 раза с 7-дневными интервалами.
Параметры контроля:
Рост опухоли был проверен в течение 90 дней после инъекции клеток с помощью кронциркуля. Мышей уничтожали по этическим причинам, когда размер опухоли превосходил 25 мм в диаметре, или тогда, когда они ощущали боль, даже если опухоль была меньшей.
Были зарегистрированы выживающие мыши.
Результаты
Все группы, которые были обработаны вектором MVA, который кодирует антиген HPV, показали более высокую норму выживания, чем группа, которая была обработана пустым вектором MVA. Мыши, которые были обработаны при помощи композиций, которые включают EEV и IMV, показали более высокую норму выживания, чем те мыши, которые были обработаны композициями, которые включали только IMV. Кроме того, 35% мышей, которых обрабатывали композицией, которая включала EEV и IMV, были свободны от опухоли спустя 77 дней после этого, будучи инъецированными по сравнению с только 10% мышей, которые были обработаны с помощью композиции, включающей только IMV.
В. Терапевтическое лечение мышей, переносящих опухоль, экспрессирующую MUC1.
Наименование и краткое описание каждой векторной конструкции
TG 4010: Вектор MVA, несущий кодирующие последовательности для белков MUC 1 (под контролем промотора р 7.5) и IL 2 (под контролем промотора рН 5R). Были проверены две партии, одно включение IMV и EEV и одно включение только IMV.
Пустой вектор MVATGN 33, который не экспрессирует ни MUC 1, ни IL 2, использовался в качестве отрицательного контроля.
Модель мыши и разновидности системы экспериментов животных
Штаммы и поставщик: самки мыши С 57BI / 6 в возрасте 6-8 недель использовались в течение всего этого исследования. Эти мыши были получены от Charles River (Руан, Франция).
Спецификация: животные находились в возрасте 6 недель в день прибытия. В начале эксперимента им было меньше чем 8 недель.
Окружающая среда: животные были размещены в единственной, эксклюзивной комнате, которая была кондиционируема для того, чтобы обеспечить минимум 11 воздушных объемов в час. Диапазоны температурной и относительной влажности были расположены в пределах 18°С и 22°С и 40-70% соответственно. Освещение управлялось автоматическим путем, для того чтобы дать цикл 12 часов света и 12 часов темноты. Животные были размещенными в общие группы по 10 на клетку 43×27×15 см, при этом закрытая площадь составляла 1161 см2.
Питание: в течение всего времени исследования у животных был свободный доступ к стерильному типу диеты D 04 (UAR, Epinay sur Orge, Франция). Вода была подана свободно через бутылки.
Акклиматизация и процедуры здоровья: Всем животным был проведен клинический осмотр для здоровья в момент прибытия. Они были акклиматизированы в специфичном свободном от патогенов средстве для животных (SPF) между одной и двумя неделями перед началом эксперимента, для того чтобы гарантировать их пригодность для исследования.
Особенности клеток опухоли и условия использования:
Линия опухоли RMA была получена из лимфомы С 57 В 1 / 6. Клетки RMA-MUC 1 были получены после трансфекции с плазмидой экспрессии, содержащей ген MUC 1а. Эти клетки были выращены в DMEM с глутамином (2 мМ), эмбриональной сывороткой теленка (10%), не заменимыми аминокислотами (0.1 мМ), пируватом (1 мМ), парамеркаптоэтанолом (36 мкМ) и гидромицином (550 мкг/мл). После размораживания клетки были амплифицированы два раза, последний пассаж был выполнен в день перед исследованием.
Иммунизация
Мыши были иммунизированы с 1.0 104 или 3.0 104 вирусных частиц/мышь для вируса TG 4010 и с 3.0 104 вирусных частиц/мышь для MVATGN 33.
20 мышей использовались как тестируемая партия.
Вирусные иммунизации были выполнены под кожу и выполнены 3 раза с 14-дневными интервалами.
Исследование опухоли
Спустя две недели после последней иммунизации, мышам было введено под кожу, в том же самом участке кожи, но на отдаленном участке от места вирусной инъекции, с 1.0 Е + 06 RMA - MUC 1 жизнеспособных клеток / 50 мкл/мышь.
Параметры контроля:
Рост опухоли был измерен в течение 6 недель после введения опухоли, с помощью кронциркуля. Мышей уничтожали по этическим причинам, в том случае, когда размер опухоли превосходил 25 мм в диаметре или когда они испытывали боль, даже если опухоль была меньшей по размеру.
Были зарегистрированы выживающие мыши.
20 мышей были использованы в качестве дозы.
Результаты
Все группы, которые были обработаны с помощью вектора MVA, который кодирует антиген MUC 1, показали более низкий рост опухоли и более высокую норму выживания, чем та группа, которая была обработана с помощью пустого вектора MVA. Мыши, которые были обработаны при помощи композиций, которые включали EEV и IMV, показали более низкий рост опухоли, чем те мыши, которые были обработаны при помощи композиций, которые включали только IMV.


Данное изобретение имеет отношение к таким композициям и фармацевтическим композициям, которые включают поксвирусы, и более конкретно, которые включают внеклеточные оболочечные вирусы. Данное изобретение также имеет отношение к такому способу, который предназначен для того, чтобы продуцировать поксвирусы, а также поксвирусы, полученные согласно этому изобретению. Кроме того, данное изобретение также имеет отношение к использованию указанного поксвируса и указанной композиции для приготовления лекарственного средства. 2 н. и 15 з.п. ф-лы, 3 ил.
1. Способ получения дикого типа или аттенуированного поксвируса, без выявленной инфекционной специфичности, который включает следующие этапы:
a) приготовление культуры клеток с дефектом упаковки нуклеотидных последовательностей,
b) инфицирование указанной культуры клеток для получения инфицированных клеток,
c) культивирование указанных инфицированных клеток в течение промежутка времени между одним и шестью днями для получения поксвирусных частиц,
d) выделение EEV и IMV продуцированных поксвирусных частиц из культурального супернатанта и клеток с дефектом упаковки нуклеотидных последовательностей, для получения смеси поксвирусных частиц,
e) этап очистки этой смеси поксвирусных частиц, который позволяет освободить ее от клеточных остатков, причем указанный этап очистки является этапом глубинной фильтрации, для получения очищенной смеси поксвирусных частиц,
f) этап концентрирования указанной очищенной смеси поксвирусных частиц, причем указанный этап концентрирования является этапом микрофильтрации для получения концентрированной смеси поксвирусных частиц, и
g) этап диафильтрации,
при этом указанный способ является свободным от продуктов животного происхождения.
2. Способ по п.1, в котором указанные клетки с дефектом упаковки нуклеотидных последовательностей представлены CEF.
3. Способ по п.1 или 2, в котором этап с) длится от двух до четырех дней.
4. Способ по п.1 или 2, в котором этап d) включает разрушение указанной клетки с дефектом упаковки нуклеотидных последовательностей при использовании гомогенизатора высокой скорости.
5. Способ по п.1 или 2, в котором не используется какая-либо нуклеаза и, более конкретно, в котором не используется какая-либо бензоназа.
6. Способ по п.1 или 2, в котором смесь поксовирусных частиц, полученная с помощью указанного способа, включает EEV и IMV с содержанием EEV более чем 1%.
7. Способ по п.1 или 2, дополнительно включающий этап смены буфера, используемого в способе очистки, в частности на этапе g), фармацевтически приемлемым буфером.
8. Способ по п.7, при котором указанный этап осуществляют с помощью тангенциальной фильтрации.
9. Способ по п.1 или 2, где указанный дикого типа или аттенуированный поксвирус является рекомбинантным поксвирусом.
10. Способ по п.1 или 2, где указанный дикого типа или аттенуированный поксвирус является вирусом осповакцины.
11. Способ по п.10, где указанный вирус осповакцины является модифицированным вирусом осповакцины Анкара (MVA) вирус.
12. Способ по п.1 или 2, где указанный дикого типа или аттенуированный поксвирус является рекомбинантным вирусом осповакцины.
13. Способ по п.12, где указанный рекомбинантный вирус осповакцины является рекомбинантным модифицированным вирусом осповакцины Анкара (MVA) вирус.
14. Способ по п.12, где указанный рекомбинантный MVA вирус включает по меньшей мере одну экзогенную последовательность, выбранную из:
гена самоуничтожения,
экзогенной последовательности, кодирующей опухоль ассоциированный антиген (TTA),
экзогенной последовательности, кодирующей опухоль ассоциированный антиген (TTA) и экзогенной последовательности, кодирующей цитокин, и
экзогенной последовательности, кодирующей антиген.
15. Применение поксвирусных частиц, полученных с помощью способа по п.1 или 2, для приготовления лекарственного средства.
16. Применение по п.15 для терапевтического или профилактического лечения рака.
17. Применение по п.15 для терапевтического или профилактического лечения инфекционных болезней.
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Контрольный стрелочный замок | 1920 |
|
SU71A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| US 2005208074 A1, 22.09.2005 | |||
| TREVOR K | |||
| T | |||
| ET AL: "Transduction of human | |||
Авторы
Даты
2015-06-10—Публикация
2007-06-15—Подача