Изобретение относится к экспериментальной клинической медицине, а именно к поиску новых лекарственных средств для комплексного лечения длительно незаживающих гнойных кожных язв и ран.
Лечение длительно незаживающих гнойных кожных язв и ран - одна из проблем практической медицины. Это обусловлено увеличением количества гнойных осложнений кожных ран и язв, прогрессирующим ростом антибиотик-устойчивых штаммов микроорганизмов, что приводит к осложнениям и увеличению сроков пребывания в стационаре. Однако существующее в настоящее время большое количество методов лечения подобных ран и язв не всегда дает хороший терапевтический эффект. Современные представления о биологическом процессе в ране, механизмах репарации и очищения раны или язвы от микробной загрязненности вызывает необходимость комплексного лечения, направленного с одной стороны на уничтожение инфекции в ране, а с другой стороны - на повышение механизмов регенерации с использованием биологических препаратов. Подобный метод был предложен (1), однако он имеет ряд недостатков, которые заключаются в следующем.
1. На рану наносят порошок фибрина, который не защищен антибактериальными препаратами и поэтому подвергается разрушительному действию микробов.
2. Проводимая антибактериальная предварительная обработка раны или язвы является непродолжительной, и из них эти средства вымываются тканевой жидкостью.
3. В связи с тем, что на рану или язву наносят порошок фибрина, он часто не задерживается на поверхности язвы или раны и поэтому через некоторое время это покрытие фибрином становится неполным.
Задачей изобретения является ускорение репаративных процессов в язве или ране с использованием биологических препаратов с одновременным постоянным воздействием на микрофлору дезинфицирующей мазью, что в конечном итоге приводит к более быстрому заживлению раны или язвы.
Сущность изобретения заключается в том, что в способе лечения длительно незаживающих гнойных кожных ран и язв путем наложения на их поверхность цинковой пасты и порошка фибрина, полученного из сгустка крови домашней свиньи, сухой порошок фибрина перемешивают с цинковой пастой в соотношении 1:5 за 25-30 мин до наложения.
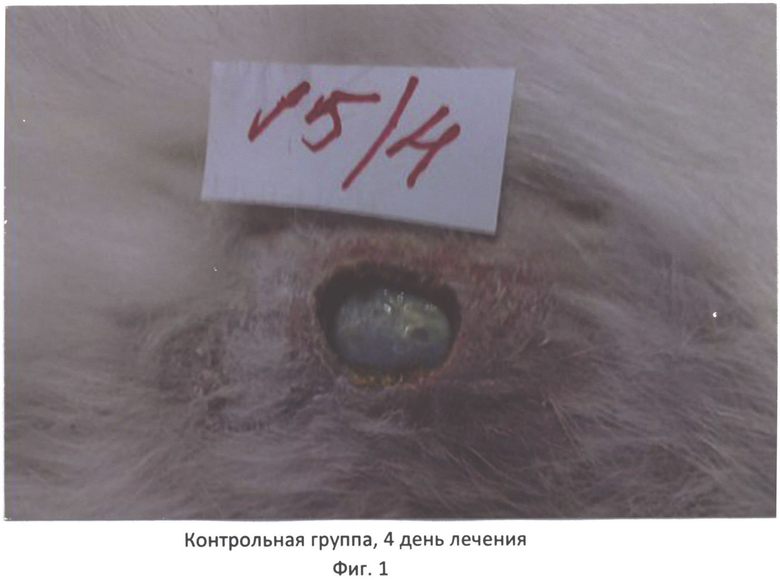
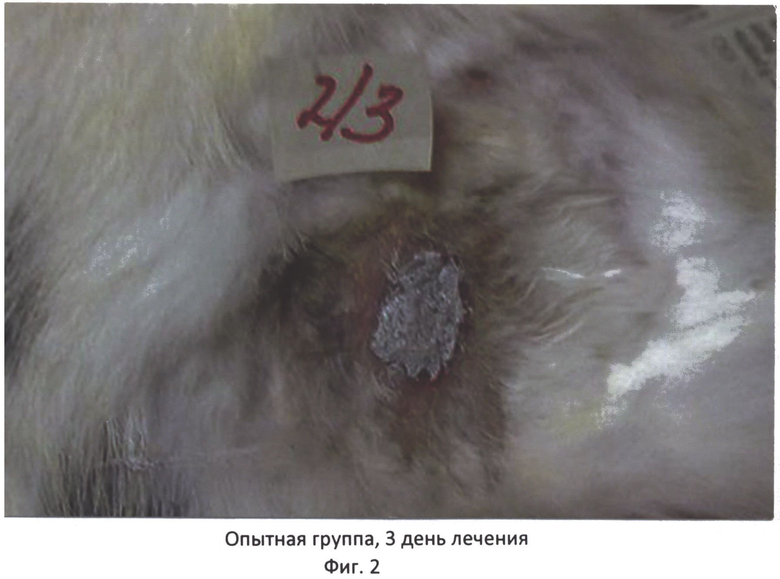
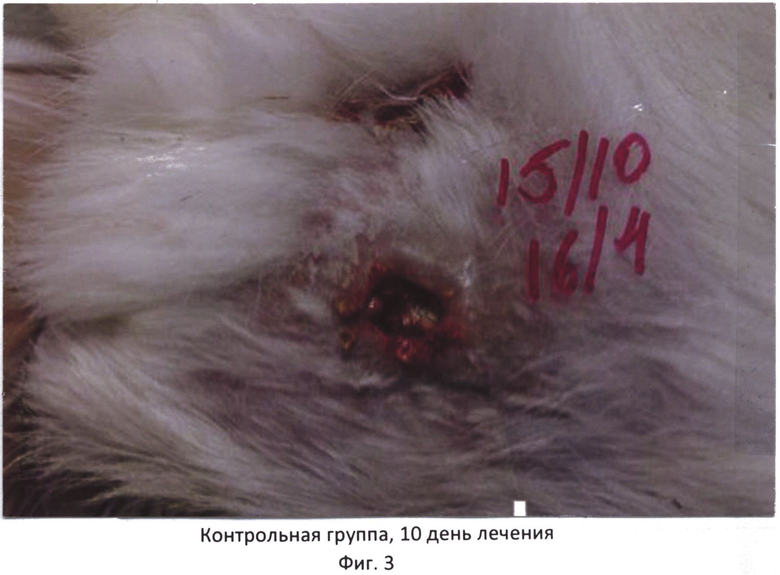
Способ иллюстрируется фотографиями, где на фиг.1 - контрольная группа, 4 день лечения, фиг.2 - опытная группа, 3 день лечения, фиг.3 - контрольная группа, 10 день лечения, фиг.4 - опытная группа, 10 день лечения.
Экспериментальные исследования по изучению влияния предлагаемого способа на раневой процесс проведены на 40 кроликах обоих полов в равных количествах массой 1,5-2,5 кг. Все животные содержались в индивидуальных клетках. Режим содержания и питания животных был одинаков во всех группах опытов. В качестве дезинфицирующей мази была избрана цинковая паста, не имеющая в своем составе антибиотиков. Цинковая паста смешивалась с порошком фибрина в соотношении 5:1 и готовилась за 25-30 минут до нанесения на язву или рану. В дальнейшем по тексту эта смешанная масса именуется как смесь. Сравнительная оценка результатов проведена в двух группах животных. Опытную группу (ОГ) составили 20 кроликов, которым для воздействия на экспериментальную рану местно применяли предлагаемую смесь. В контрольную группу (КГ) вошли 20 кроликов. Им для лечения экспериментальной раны применяли только цинковую пасту.
Экспериментальная модель длительно существующей раны была получена следующим способом. После предварительного удаления шерсти и обработки кожи с соблюдением требований асептики в условиях обезболивания за счет применения раствора рометара 0,2 мл в/м и местной инфильтрационной анестезии (раствор новокаина 0,25% 3 мл) на правом бедре задней лапы иссекали участок кожи с подкожной клетчаткой 2*2 см по трафарету, обрабатывали H2O2 и накладывали асептическую повязку. Цинковую пасту готовили в аптеке. Порошок фибрина получали по известному способу, разработанному и защищенному патентами России (2, 3). Полученный порошок фибрина и цинковую пасту брали в соотношении 1:5 и смешивали за 25-30 минут до нанесения на язву. Способ местного применения предлагаемой смеси и только цинковой пасты был следующим. На 3 сутки после создания экспериментальной модели раны снимали повязку и обрабатывали рану 3% раствором H2O2 и раствором 0,01% мирамистина. После чего у кроликов ОГ на рану наносили предлагаемую смесь, а у кроликов КГ - только цинковую пасту слоем 1-2 мм. Поверх пасты накладывали асептическую повязку. В случаях присоединения вторичной инфекции выполняли иссечение некротических тканей. Перевязки выполняли каждые 1-2 дня. Методы исследования язвы или раны были следующими.
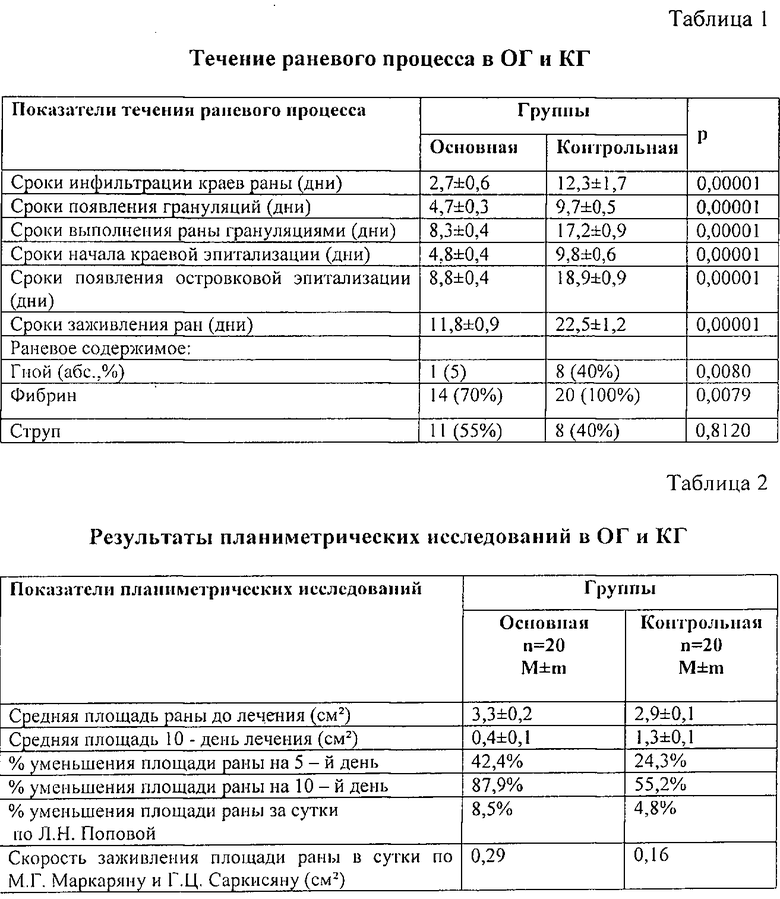
Исследование показателей течения раневого процесса проводили на основании: характера раневого содержимого, сроков воспалительной инфильтрации краев раны, сроков появления и выполнения раны грануляционной тканью, сроков начала краевой и островковой эпителизации раны, сроков заживления раны. Показатели течения раневого процесса оценивались при каждой перевязке животного (см. табл.1).
Планиметрические исследования проводили путем вычисления площади раны до лечения, на 5-е и 10-е сутки применения предлагаемой смеси и цинковой пасты. Контур раны наносили на прозрачную пленку, которую прикладывали к стандартному трафарету с нанесенными на него делениями в см2. Площадь раны определяли по формуле: N+n/2, где N - число полных квадратов; n - число неполных квадратов. Процент уменьшения площади раны определяли на 5-е и 10-е сутки. Определение процента уменьшения площади раны за сутки выполняли по формуле Л.Н. Поповой:
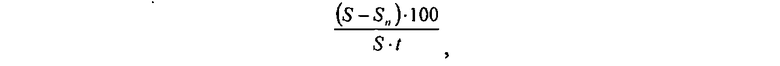
где S - площадь раны при предыдущем измерении;
Sn - площадь раны при данном измерении;
t - число дней между первым и последующим измерением.
Скорость заживления раны определяли по формуле М.Г. Маркаряна и Г.Ц. Саркисяна:
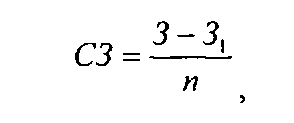
где СЗ - скорость заживления площади раны в сутки;
З - исходная площадь раны;
З1 - площадь ее к моменту измерения (см. табл.2).
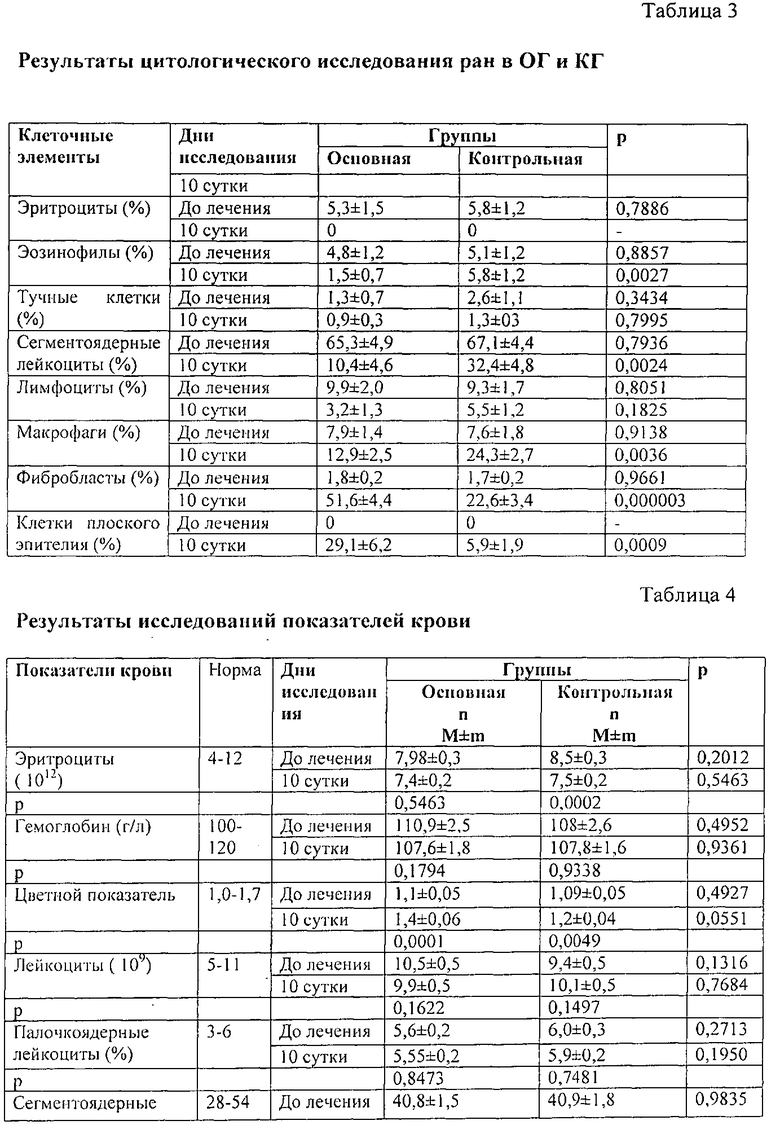
Цитологическое исследование проводили перед началом опыта и на 10-е сутки. Материал для исследования получали путем соскоба ткани из раневой поверхности (см. табл.3).
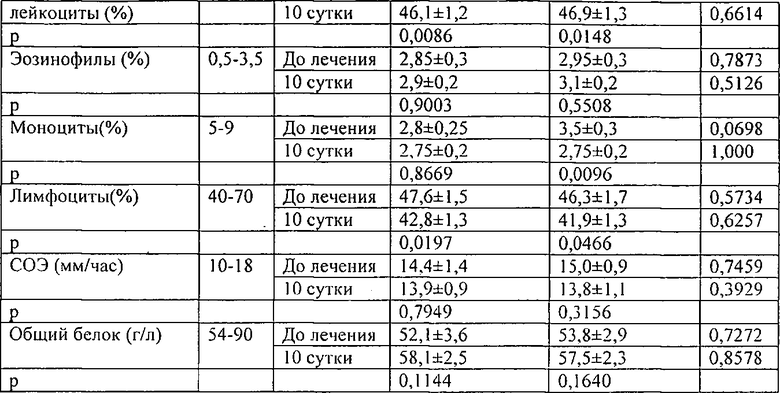
Исследование показателей крови. Клинический анализ крови и общий белок исследовали так же перед началом опыта и на 3 и 10-е сутки. Забор крови производили из вен уха животных до и после окончания лечения (см. табл.4).
Бактериологическое исследование включало изучение состава микрофлоры и ее количественное содержание в ране. Посевы микрофлоры из раны выполняли перед началом опыта и на 3 и 10-е сутки.
Математическую обработку результатов исследования осуществляли с помощью пакетов прикладных программ STATISTICA 6.0 на персональном компьютере. Все данные анализировали методами вариационной статистики. При нормальном распределении рядов данных применяли критерий Стьюдента. Если распределение существенно отличалось от нормального, использовали непараметрические методы: для сравнения независимых выборок - критерий Уитни-Манна, при анализе повторных изменений - критерий Вилкинсона, критерий знаков. Значимость различий качественных показателей определяли с помощью критерия и двухстороннего точного метода Фишера для четырехпольной таблицы. Все значения приведены в виде средней арифметической (М) и средней ошибки (т). Степень отличий считали значимой при p≤0,05.
Результаты бактериологических исследований
Как показали эти исследования, до применения пасты и смеси в ОГ и КГ микрофлора обнаруживалась у 8 (40%) и 9 (45%) кроликов соответственно, без значимых различий между группами (p=0,7421). Микробная обсемененность была одинаковой и составляла в ОГ 102.1 м.т. на 1 см2 и КГ - 102,2 м.т. на 1 см2 (p=0,9043). Значимых различий в структуре микрофлоры также не было обнаружено.
Результаты исследования форменных элементов крови и общего белка показали отсутствие значимых различий этих показателей у животных ОГ и КГ до лечения и в процессе лечения. Применение предлагаемой смеси в местном лечении не оказало отрицательного влияния на содержание форменных элементов крови и общего белка периферической крови.
Таким образом, проведенные исследования показывают:
1. На основании сравнительного анализа показателей течения раневого процесса и планиметрических исследований установлено более быстрое течение репаративных процессов и заживления экспериментальных ран у кроликов основной группы, получавших местное лечение смесью фибрина и цинковой пасты, по сравнению с контрольной группой кроликов, которым применяли только цинковую пасту.
2. При цитологическом исследовании экспериментальных ран у основной группы кроликов на 10-е сутки применения смеси обнаруживались признаки второй фазы регенерации, тогда как у кроликов контрольной группы чаще наблюдались признаки дегенеративно-воспалительного типа цитограмм или первой фазы регенерации.
3. При использовании смеси у основной группы кроликов число случаев выявления микрофлоры и микробная обсеменённость не возросли по сравнению с исходным уровнем и бактериологическими показателями контрольной группы.
4. Применение смеси фибрина сгустка крови свиньи и цинковой пасты в местном лечении экспериментальных ран не оказало отрицательного влияния на содержание форменных элементов крови и общего белка периферической крови у основной группы кроликов. Технический результат использования изобретения заключается в быстром заживлении гнойных кожных ран и язв.
Источники информации
1. Патент № 2001619. Способ лечения трофических язв. Авторы: В.А. Фигурнов., В.И. Точилин., А.В. Фигурнов.
2. Патент № 1573571. Способ получения фибрина сгустка крови. Авторы: В.А. Фигурнов., А.В. Фигурнов. 1990 г.
3. Патент № 1811845. Способ получения порошка фибрина. Авторы: В.А. Фигурнов., Е.В. Фигурнова.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ УСКОРЕНИЯ ЗАЖИВЛЕНИЯ КОЖНЫХ ПОВРЕЖДЕНИЙ | 2017 |
|
RU2663907C1 |
| СПОСОБ ЛЕЧЕНИЯ ТРОФИЧЕСКИХ ЯЗВ И ДЛИТЕЛЬНО НЕЗАЖИВАЮЩИХ РАН ЖИВОТНЫМИ ЖИРАМИ | 1998 |
|
RU2198667C2 |
| СПОСОБ ЛЕЧЕНИЯ ТРОФИЧЕСКИХ ЯЗВ И ДЛИТЕЛЬНО НЕЗАЖИВАЮЩИХ РАН | 1996 |
|
RU2144381C1 |
| СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКИХ РАНЕВЫХ ПРОЦЕССОВ | 2001 |
|
RU2189814C1 |
| Способ лечения труднозаживающих ран в эксперименте | 2019 |
|
RU2715145C1 |
| Способ лечения ран и гнойно-нектротических поражений пальцев у сельскохозяйственных животных | 1989 |
|
SU1706626A1 |
| СПОСОБ МОДЕЛИРОВАНИЯ ТРОФИЧЕСКОЙ РАНЫ В ЭКСПЕРИМЕНТЕ | 2013 |
|
RU2510083C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЛИТЕЛЬНО НЕЗАЖИВАЮЩИХ РАН У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ | 2008 |
|
RU2358757C1 |
| СПОСОБ СТИМУЛЯЦИИ ЗАЖИВЛЕНИЯ РАН РАЗЛИЧНОГО ГЕНЕЗА ПРИРОДНЫМ АНТИОКСИДАНТОМ ДИГИДРОКВЕРЦЕТИНОМ | 2012 |
|
RU2522214C1 |
| СПОСОБ ЛЕЧЕНИЯ ИНФИЦИРОВАННЫХ РАН У ЖИВОТНЫХ | 2007 |
|
RU2335281C1 |

Изобретение относится к экспериментальной клинической медицине, а именно к поиску новых лекарственных средств и способов для комплексного лечения длительно незаживающих гнойных кожных язв и ран. Сущность способа лечения длительно незаживающих гнойных кожных ран и язв путем наложения на их поверхность цинковой пасты и порошка фибрина, полученного из сгустка крови домашней свиньи, при этом сухой порошок фибрина перемешивают с цинковой пастой в соотношении 1:5 за 25-30 мин до наложения. Изобретение обеспечивает ускорение репаративных процессов в язве или ране с использованием биологических препаратов с одновременным постоянным воздействием на микрофлору дезинфицирующей мазью, что в конечном итоге приводит к более быстрому заживлению раны. 4 табл., 4 ил.
Способ лечения длительно незаживающих гнойных кожных ран и язв путем наложения на их поверхность цинковой пасты и порошка фибрина, полученного из сгустка крови домашней свиньи, отличающийся тем, что сухой порошок фибрина перемешивают с цинковой пастой в соотношении 1:5 за 25-30 мин до наложения.
| RU 2001619 C1, 30.10.1993 | |||
| АНТИМИКРОБНАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РАН И ОЖОГОВ | 2011 |
|
RU2481834C2 |
| МАЗЬ ДЛЯ ЛЕЧЕНИЯ ГНОЙНОВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ, ОЖОГОВ, ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ СУСТАВОВ, ТРОФИЧЕСКИХ ЯЗВ И ДЛИТЕЛЬНО НЕЗАЖИВАЮЩИХ РАН, СПОСОБ ЕЕ ПРИГОТОВЛЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 1997 |
|
RU2165754C2 |
| АЛЕКСЕЕВНИНА В.В | |||
| и др | |||
| Использование гетерогенного фибрина в лечении длительно существующих ран и язв | |||
| БЮЛЛЕТЕНЬ ВОСТОЧНО-СИБИРСКОГО НАУЧНОГО ЦЕНТРА СО РАМН | |||
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| RAVANTI L, KÄHÄRI V.M | |||
| Matrix metalloproteinases in wound repair (review) | |||
| Int J Mol Med | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Найдено в PubMed | |||
| PMID: 10998429 | |||
Авторы
Даты
2015-08-10—Публикация
2014-04-07—Подача