Настоящее изобретение относится к новому классу ингибиторов киназ, включая фармацевтически приемлемые соли, пролекарства и метаболиты упомянутых ингибиторов, которые применимы для модулирования активности протеинкиназ, с целью регулирования различных функций клеток, например, сигнальной трансдукции, пролиферации и секреции цитокинов. Более конкретно, в изобретении разработаны соединения, которые ингибируют, регулируют и/или модулируют активность киназ, в частности активность JAK3, и пути передачи сигнала, относящиеся к упомянутым выше видам клеточной активности. Кроме того, настоящее изобретение относится к фармацевтическим композициям, включающим указанные соединения, предназначенным, например, для лечения или профилактики иммунологических, воспалительных, аутоиммунных или аллергических расстройств или заболеваний, или отторжения трансплантата, или реакции «трансплантат против хозяина», а также к способам получения указанных соединений.
Киназы катализируют фосфорилирование белков, липидов, сахаров, нуклеозидов и других клеточных метаболитов, и играют ключевую роль во всех аспектах физиологии эукариотических клеток. Конкретно, протеинкиназы и липидкиназы принимают участие в актах передачи сигналов, которые регулируют активацию, рост, дифференцировку и выживание клеток в ответ на действие внеклеточных медиаторов или стимулов, например, факторов роста, цитокинов или хемокинов. Как правило, протеинкиназы подразделяют на две группы, а именно, протеинкиназы, которые преимущественно фосфорилируют тирозиновые остатки, и протеинкиназы, которые преимущественно фосфорилируют сериновые и/или треониновые остатки. Тирозин киназы включают трансмембранные рецепторы факторов роста, например, рецептор эпидермального фактора роста (EGFR), и цитозольные не рецепторные киназы, например, Янус-киназы (JAK).
Избыточно высокая активность протеинкиназ вовлечена во многие заболевания, в т.ч. рак, метаболические заболевания, аутоиммунные или воспалительные расстройства. Этот эффект может быть прямо или косвенно вызван нарушением управляющих механизмов вследствие мутации, избыточной экспрессии или неадекватной активации фермента. Ожидается, что во всех этих случаях, селективное ингибирование киназ окажет положительное действие.
Одной из групп киназ, на которой в последнее время сконцентрировано внимание специалистов по поиску новых лекарственных средств, является семейство не рецепторных тирозин киназ, именуемых Янус-киназами (JAK). У млекопитающих это семейство включает четыре белка, а именно JAK1, JAK2, JAK3 и тирозин киназу 2 (TYK2). Каждый из этих белков содержит киназный домен и каталитически неактивный псевдокиназный домен. Белки JAK связываются с рецепторами цитокинов через их амино-концевые домены FERM (домены группы белков-4.1, эзрина, радиксина, моэзина). После связывания цитокинов с соответствующими рецепторами, JAKs активируются и фосфорилируют рецепторы, в результате чего образуются участки, к которым прикрепляются сигнальные молекулы (сайты докинга), в особенности для членов семейств сигнальных белков и активаторов транскрипции (Stat) (Yamaoka et al., 2004. The Janus kinases (Jaks). Genome Biology 5(12):253).
У млекопитающих белки JAK1, JAK2 и TYK2 экспрессируются во всех тканях организма. В противоположность этому, экспрессия JAK3 происходит преимущественно в гематопоэтических клетках и жестко регулируется развитием и активацией клеток (Musso et al., 1995. 181(4):1425-31).
Исследование JAK-дефицитных линий клеток и мышей с направленными генетическими изменениями выявило основные, не дублируемые функции JAKs в передаче сигнала цитокинов. JAK1-нокаутированные мыши демонстрируют перинатальный летальный фенотип, вероятно связанный с неврологическими эффектами, которые мешают им осуществлять сосание (Rodig et al., 1998. Cell 93(3):373-83). Удаление гена JAK2 приводит к смерти эмбриона в возрасте 12,5 дней в результате нарушения эритропоэза (Neubauer et al., 1998. Cell 93(3):397-409). Интересно отметить, что дефицит JAK3 впервые был выявлен у людей в виде аутосомально рецессивного тяжелого комбинированного иммунодефицита (SCID) (Macchi et al., 1995. Nature 377(6544):65-68). У JAK3-нокаутированных мышей также проявляется SCID, но они не демонстрируют других нарушений, кроме иммунных, и это дает основание предположить, что ингибитор JAK3 в качестве иммуносупрессора мог бы иметь ограниченное действие in vivo и, следовательно, он является интересным потенциальным средством для подавления иммунитета (Papageorgiou and Wikman 2004, Trends in Pharmacological Sciences 25(11):558-62).
Активирующие мутации JAK3 наблюдались у пациентов с острым мегакариобластным лейкозом (AMKL) (Walters et al., 2006. Cancer Cell 10(1):65-75). Эти мутировавшие формы JAK3 могут трансформировать клетки Ba/F3, приводя к фактор-независимому росту, и вызывают признаки мегакариобластного лейкоза в мышиной модели.
Заболевания и расстройства, связанные с ингибированием JAK3, более подробно описаны, например, в WO 01/42246 и WO 2008/060301.
В литературе было описано несколько ингибиторов JAK3, которые могут найти применение в медицине (O'Shea et al., Nat.Rev.Drug Discov. 3(7):555-64). Сообщалось, что мощный ингибитор JAK3 (CP-690 550) продемонстрировал эффективность в животной модели трансплантации органа (Changelian et al., 2003, Science 302(5646):875-888) и клинических испытаниях (см. обзор в: Pesu et al., 2008. Immunol. Rev. 223, 132-142). Ингибитор CP-690 550 не проявляет селективность в отношении JAK3 киназы и практически с такой же эффективностью ингибирует киназу JAK2 (Jiang et al., 2008, J. Med. Chem. 51(24):8012-8018). Ожидается, что селективный ингибитор JAK3, который ингибирует JAK3 сильнее, чем JAK2, может иметь более благоприятные терапевтические свойства, поскольку ингибирование JAK2 может вызывать анемию (Ghoreschi et al., 2009, Nature Immunol. 4, 356-360).
Производные пиримидина, демонстрирующие способность ингибировать киназы JAK3 и JAK2, описаны в WO-A 2008/009458. В WO-A 2008/118822 и WO-A 2008/118823 описано применение пиримидиновых соединений в лечении состояний, при которых полезно модулирование сигнального пути JAK или ингибирование киназ JAK, в т.ч. JAK3.
Фторзамещенные пиримидиновые соединения в качестве ингибиторов JAK3 описаны в WO-A 2010/118986. Гетероциклильные аналоги пиразолопиримидина в качестве ингибиторов JAK описаны в WO-A 2011/048082.
Заявка WO-A 2008/129380 относится к производным сульфониламидов для лечения аномального роста клеток. В заявке WO-A 2006/117560 и работе J. of Molecular Graphics and Modelling (29) 2010, 309-320 описаны пиразолиламино-замещенные пиримидины и их применение в лечении рака. В EP 1054004 A1 описаны производные пиримидинов и их применение при воспалении.
Несмотря на то, что ингибиторы JAK известны в технике, существует потребность в разработке новых ингибиторв JAK, имеющих как минимум несколько более эффективные фармацевтические свойства, как, например, свойства, относящиеся к активности, селективности, особенно в отношении киназы JAK2, и ADME (всасывание, распределение, метаболизм и выведение).
Таким образом, цель настоящего изобретения заключается в разработке нового класса соединений, являющихся ингибиторами JAK, которые предпочтительно, проявляют селективность в отношении JAK2 и могут быть эффективными при лечении или профилактике расстройств, связанных с JAK.
Соответственно, настоящее изобретение относится к соединениям формулы (I)
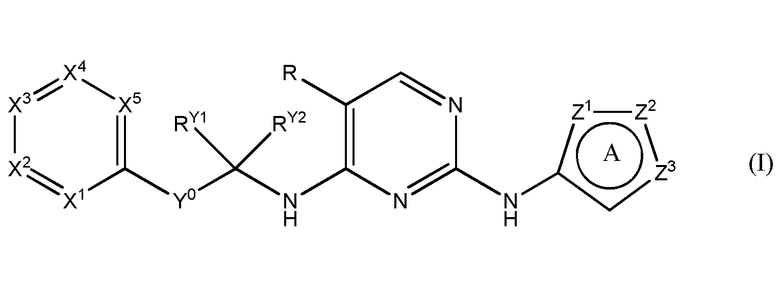
или их фармацевтически приемлемым солям или изотопным производным, где
R представляет собой H; F; Cl; Br; CN; CH3; CF3 или C(O)NH2;
цикл A представляет собой 5-членный ароматический гетероцикл, в котором Z1, Z2 и Z3 независимо выбраны из группы, состоящей из C(R1); N и N(R1), при условии, что, как минимум, одна из Z1, Z2, Z3 представляет собой N или N(R1);
каждый из R1 независимо представляет собой H, галоген; CN; C(O)OR2; OR2; C(O)R2; C(O)N(R2R2a); S(O)2N(R2R2a); S(O) N(R2R2a); S(O)2R2; S(O)R2; N(R2)S(O)2N(R2aR2b); N(R2)S(O)N(R2aR2b); SR2; N(R2R2a); NO2; OC(O)R2; N(R2)C(O)R2a; N(R2)S(O)2R2a; N(R2)S(O) R2a; N(R2)C(O)N(R2aR2b); N(R2)C(O)OR2a; OC(O)N(R2R2a); T1; C1-6алкил; C2-6алкенил; или C2-6алкинил, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R3, которые являются одинаковыми или различными;
R2, R2a, R2b независимо выбраны из группы, состоящей из H; T1; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R3, которые являются одинаковыми или различными;
R3 представляет собой галоген; CN; C(O)OR4; OR4; C(O)R4; C(O)N(R4R4a); S(O)2N(R4R4a); S(O)N(R4R4a); S(O)2R4; S(O)R4; N(R4)S(O)2N(R4aR4b); N(R4)S(O)N(R4aR4b); SR4; N(R4R4a); NO2; OC(O)R4; N(R4)C(O)R4a; N(R4)S(O)2R4a; N(R4)S(O)R4a; N(R4)C(O)N(R4aR4b); N(R4)C(O)OR4a; OC(O)N(R4R4a); или T1;
R4, R4a, R4b независимо выбраны из группы, состоящей из H; T1; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R5, которые являются одинаковыми или различными;
R5 представляет собой галоген; CN; C(O)OR5a; OR5a; C(O)R5a; C(O)N(R5aR5b); S(O)2N(R5aR5b); S(O)N(R5aR5b); S(O)2R5a; S(O)R5a; N(R5a)S(O)2N(R5bR5c); N(R5a)S(O)N(R5bR5c); SR5a; N(R5aR5b); NO2; OC(O)R5a; N(R5a)C(O)R5a; N(R5a)S(O)2R5b; N(R5a)S(O)R5b; N(R5a)C(O)N(R5bR5c); N(R5a)C(O)OR5b; или OC(O)N(R5aR5b);
R5a, R5b, R5c независимо выбраны из группы, состоящей из H; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими атомами галогенов, которые являются одинаковыми или различными;
T1 представляет собой C3-7циклоалкил; насыщенный 4-7-членный гетероциклил; или 7-11-членный гетеробициклил; где T1 необязательно замещен одним или несколькими R10, которые являются одинаковыми или различными;
Y0 представляет собой (CRY3RY4)n;
n означает 0; или 1;
один из RY1; RY2; RY3; RY4; представляет собой RY0, и другие выбраны из группы, состоящей из H; CH3; и CF3;
RY0 представляет собой незамещенный C1-4алкил; CH2CH2ORY5; CH2CH2C(O)TY1; CH2CH2C(O)ORY5; CH2CH2OC(O)RY5; CH2CH2N(RY5RY5a); CH2CH2N(RY5)C(O)RY5a; CH2CH2C(O)N(RY5RY5a); CH2ORY5; CH2C(O)TY1; CH2C(O)ORY5; CH2OC(O)RY5; CH2N(RY5RY5a); CH2N(RY5)C(O)RY5a; CH2C(O)N(RY5RY5a); C(O)TY1; C(O)ORY5; или C(O)N(RY5RY5a);
RY5, RY5a независимо выбраны из группы, состоящей из H; TY1; и C1-4алкила, где C1-4алкил необязательно замещен одним или несколькими RY6, которые являются одинаковыми или различными;
RY6 представляет собой галоген; ORY7; C(O)TY1; C(O)ORY7; OC(O)RY7; N(RY7RY7a); или N(RY7)C(O)RY7a;
RY7; RY7a независимо выбраны из группы, состоящей из H, C1-4алкила; или TY1, где C1-4алкил необязательно замещен одним или несколькими атомами галогена, которые являются одинаковыми или различными;
TY1 представляет собой незамещенный C3-7циклоалкил; незамещенный насыщенный 4-7-членный гетероциклил; или насыщенный 7-11-членный гетеробициклил;
X1 представляет собой C(R6a) или N; X2 означает C(R6b) или N; X3 означает CH, CF, COH или N; X4 означает C(R6c) или N; X5 означает C(R6d) или N; при условии, что не более чем два из числа X1, X2, X4, X5 являются атомами N;
R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из H, галогена; CN; C(O)OR7; OR7; C(O)R7; C(O)N(R7R7a); S(O)2N(R7R7a); S(O)N(R7R7a); S(O)2R7; S(O)R7; N(R7)S(O)2N(R7aR7b); N(R7)S(O)N(R7aR7b); SR7; N(R7R7a); NO2; OC(O)R7; N(R7)C(O)R7a; N(R7)S(O)2R7a; N(R7)S(O)R7a; N(R7)C(O)N(R7aR7b); N(R7)C(O)OR7a; OC(O)N(R7R7a); T2; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R11, которые являются одинаковыми или различными;
пара R6a/R6b необязательно объединена с образованием циклического фрагмента T3;
R7, R7a, R7b независимо выбраны из группы, состоящей из H; CN; T2; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R8, которые являются одинаковыми или различными;
R8 представляет собой галоген; CN; C(O)OR9; OR9; C(O)R9; C(O)N(R9R9a); S(O)2N(R9R9a); S(O)N(R9R9a); S(O)2R9; S(O)R9; N(R9)S(O)2N(R9aR9b); N(R9)S(O)N(R9aR9b); SR9; N(R9R9a); NO2; OC(O)R9; N(R9)C(O)R9a; N(R9)S(O)2R9a; N(R9)S(O)R9a; N(R9)C(O)N(R9aR9b); N(R9)C(O)OR9a; OC(O)N(R9R9a); или T2;
R9, R9a, R9b независимо выбраны из группы, состоящей из H; T2; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R12, которые являются одинаковыми или различными;
R10 представляет собой галоген; CN; C(O)OR13; OR13; оксо (=O), где цикл является по крайней мере частично насыщенным; C(O)R13; C(O)N(R13R13a); S(O)2N(R13R13a); S(O)N(R13R13a); S(O)2R13; S(O)R13; N(R13)S(O)2N(R13aR13b); N(R13)S(O)N(R13aR13b); SR13; N(R13R13a); NO2; OC(O)R13; N(R13)C(O)R13a; N(R13)S(O)2R13a; N(R13)S(O)R13a; N(R13)C(O)N(R13aR13b); N(R13)C(O)OR13a; OC(O)N(R13R13a); C1-6алкил; C2-6алкенил; или C2-6алкинил, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R14, которые являются одинаковыми или различными;
R13, R13a, R13b независимо выбраны из группы, состоящей из H; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R14, которые являются одинаковыми или различными;
R11, R12 независимо выбраны из группы, состоящей из галогена; CN; C(O)OR15; OR15; C(O)R15; C(O)N(R15R15a); S(O)2N(R15R15a); S(O)N(R15R15a); S(O)2R15; S(O)R15; N(R15)S(O)2N(R15aR15b); N(R15)S(O)N(R15aR15b); SR15; N(R15R15a); NO2; OC(O)R15; N(R15)C(O)R15a; N(R15)S(O)2R15a; N(R15)S(O)R15a; N(R15)C(O)N(R15aR15b); N(R15)C(O)OR15a; OC(O)N(R15R15a); или T2;
R15, R15a, R15b независимо выбраны из группы, состоящей из H; T2; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими галогенами, которые являются одинаковыми или различными;
R14 представляет собой галоген; CN; C(O)OR16; OR16; C(O)R16; C(O)N(R16R16a); S(O)2N(R16R16a); S(O)N(R16R16a); S(O)2R16; S(O)R16; N(R16)S(O)2N(R16aR16b); N(R16)S(O)N(R16aR16b); SR16; N(R16R16a); NO2; OC(O)R16; N(R16)C(O)R16a; N(R16)S(O)2R16a; N(R16)S(O)R16a; N(R16)C(O)N(R16aR16b); N(R16)C(O)OR16a; или OC(O)N(R16R16a);
R16, R16a, R16b независимо выбраны из группы, состоящей из H; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими галогенами, которые являются одинаковыми или различными;
T2 представляет собой фенил; нафтил; инденил; инданил; C3-7циклоалкил; 4-7-членный гетероциклил; или 7-11-членный гетеробициклил, где T2 необязательно замещен одним или несколькими R17, которые являются одинаковыми или различными;
T3 представляет собой фенил; C3-7циклоалкил; 4-7-членный гетероциклил; или 7-11-членный гетеробициклил, где T3 необязательно замещен одним или несколькими R18, которые являются одинаковыми или различными;
R17, R18 независимо выбраны из группы, состоящей из галогена; CN; C(O)OR19; OR19; оксо (=O), где цикл является по крайней мере частично насыщенным; C(O)R19; C(O)N(R19R19a); S(O)2N(R19R19a); S(O)N(R19R19a); S(O)2R19; S(O)R19; N(R19)S(O)2N(R19aR19b); N(R19)S(O)N(R19aR19b); SR19; N(R19R19a); NO2; OC(O)R19; N(R19)C(O)R19a; N(R19)S(O)2R19a; N(R19)S(O)R19a; N(R19)C(O)N(R19aR19b); N(R19)C(O)OR19a; OC(O)N(R19R19a); C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R20, которые являются одинаковыми или различными;
R19, R19a, R19b независимо выбраны из группы, состоящей из H; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими R20, которые являются одинаковыми или различными;
R20 представляет собой галоген; CN; C(O)OR21; OR21; C(O)R21; C(O)N(R21R21a); S(O)2N(R21R21a); S(O)N(R21R21a); S(O)2R21; S(O)R21; N(R21)S(O)2N(R21aR21b); N(R21)S(O)N(R21aR21b); SR21; N(R21R21a); NO2; OC(O)R21; N(R21)C(O)R21a; N(R21)S(O)2R21a; N(R21)S(O)R21a; N(R21)C(O)N(R21aR21b); N(R21)C(O)OR21a; или OC(O)N(R21R21a);
R21, R21a, R21b независимо выбраны из группы, состоящей из H; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одним или несколькими галогенами, которые являются одинаковыми или различными;
при условии, что из этого определения исключены следующие соединения:
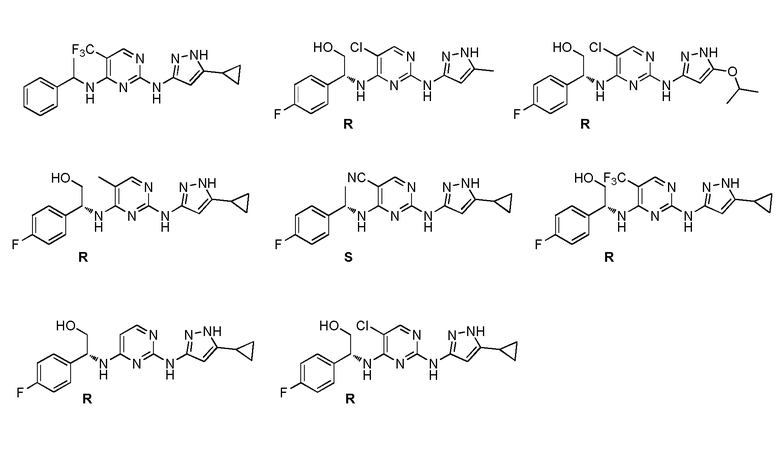 .
.
Соединения, исключенные из объема формулы (I), раскрыты в WO 2006/117560A в примерах на стр.27-29.
В случае, если переменный фрагмент или заместитель можно выбрать из группы различных вариантов, и этот переменный фрагмент или заместитель встречается в соединении более одного раза, варианты этого переменного фрагмента или заместителя могут быть одинаковыми или различными.
В рамках настоящего изобретения, следующие термины имеют указанные ниже значения:
Термин «необязательно замещенный» означает незамещенный или замещенный. Обычно, но не ограничиваясь этим, термин «один или несколько заместителей» означает один, два или три, предпочтительно, один или два и, более предпочтительно, один. Как правило, эти заместители могут быть одинаковыми или различными.
Термин «алкил» означает линейную или разветвленную углеводородную цепь. Каждый водород у атома углерода алкила может быть заменен заместителями, которые более подробно описаны в тексте заявки.
Термин «алкенил» означает линейную или разветвленную углеводородную цепь, которая включает как минимум одну двойную углерод-углеродную связь. Каждый водород у атома углерода алкенила может быть заменен заместителями, которые более подробно описаны в тексте заявки.
Термин «алкинил» означает линейную или разветвленную углеводородную цепь, которая включает как минимум одну тройную углерод-углеродную связь. Каждый водород у атома углерода алкенила может быть заменен заместителями, которые более подробно описаны в тексте заявки.
Термин «C1-4алкил» означает алкильную цепь, включающую 1-4 атома углерода, например, если алкильный радикал присутствует в концевой части молекулы: метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, или, если алкильная группа связывает две части молекулы, например, -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -CH(C2H5)-, -C(CH3)2-. Каждый водород у атома углерода C1-4алкила может быть заменен заместителями, которые более подробно описаны в тексте заявки. Соответственно определяется и термин «C2-4алкил».
Термин «C1-6алкил» означает алкильную цепь, включающую 1-6 атомов углерода, например, если алкильный радикал присутствует в концевой части молекулы: C1-4алкил, метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, н-гексил или, если алкильная группа связывает две части молекулы, например, -CH2-, -CH2-CH2-, -CH(CH3)-, -CH2-CH2-CH2-, -CH(C2H5)-, -C(CH3)2-. Каждый водород у атома углерода C1-6алкила может быть заменен заместителями, которые более подробно описаны в тексте заявки.
Термин «C2-6алкенил» означает алкенильную цепь, включающую 2-6 атомов углерода, например, если алкенильный радикал присутствует в концевой части молекулы: -CH=CH2, -CH=CH-CH3, -CH2-CH=CH2, -CH=CH-CH2-CH3, -CH=CH-CH=CH2 или, если алкенильная группа связывает две части молекулы, например, -CH=CH-. Каждый водород у атома углерода C2-6алкенила может быть заменен заместителями, которые более подробно описаны в тексте заявки.
Термин «C2-6алкинил» означает алкинильную цепь, включающую 2-6 атомов углерода, например, если алкинильный радикал присутствует в концевой части молекулы: -C≡CH, -CH2-C≡CH, -CH2-CH2-C≡CH, -CH2-C≡C-CH3 или, если алкинильная группа связывает две части молекулы, например, -C≡C-. Каждый водород у атома углерода C2-6алкинила может быть заменен заместителями, которые более подробно описаны в тексте заявки.
Термин «C3-7циклоалкил» означает циклический алкильный остаток, включающий 3-7 атомов углерода, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогексенил, циклогептил. Предпочтительно, термин «циклоалкил» относится к циклопропилу, циклобутилу, циклопентилу, циклогексилу или циклогептилу. Каждый водород у атома углерода C2-6алкинила может быть заменен заместителями, которые более подробно описаны в тексте заявки. Соответственно определяется и термин «C3-5циклоалкил».
Термин «галоген» означает фтор, хлор, бром или йод. Как правило, предпочтительно, чтобы галоген представлял собой фтор или хлор.
Термин «4-7-членный гетероциклил» или «4-7-членный гетероцикл» означает цикл, включающий 4, 5, 6 или 7 циклических атомов, которые могут содержать двойные связи в количестве вплоть до максимального (ароматический или неароматический цикл, который является полностью или частично ненасыщенным или насыщенным), где как минимум один и вплоть до четырех атомов цикла заменены гетероатомами, выбранными из группы, состоящей из серы (включая фрагменты -S(O)-, -S(O)2-), кислорода и азота (включая фрагмент =N(O)-), и где указанный цикл связан с остальной частью молекулы через атомы углерода или азота. Примерами 4-7-членных гетероциклов являются азетидин, оксетан, тиетан, фуран, тиофен, пиррол, пирролин, имидазол, имидазолин, пиразол, пиразолин, оксазол, оксазолин, изоксазол, изоксазолин, тиазол, тиазолин, изотиазол, изотиазолин, тиадиазол, тиадиазолин, тетрагидрофуран, тетрагидротиофен, пирролидин, имидазолидин, пиразолидин, оксазолидин, изоксазолидин, тиазолидин, изотиазолидин, тиадиазолидин, сульфолан, пиран, дигидропиран, тетрагидропиран, имидазолидин, пиридин, пиридазин, пиразин, пиримидин, пиперазин, пиперидин, морфолин, тетразол, триазол, триазолидин, тетразолидин, диазепан, азепин или гомопиперазин. Соответственно определяется и термин «5-6-членный гетероциклил» или «5-6-членный гетероцикл».
Термин «насыщенный 4-7-членный гетероциклил» или «насыщенный 4-7-членный гетероцикл» означает полностью насыщенный «4-7-членный гетероциклил» или «4-7-членный гетероцикл».
Термин «5-членный ароматический гетероциклил» или «5-членный ароматический гетероцикл» означает гетероцикл, являющийся производным циклопентадиенила, в котором как минимум один атом углерода заменен гетероатомом, выбранным из группы, состоящей из серы (включая фрагменты -S(O)-, -S(O)2-), кислорода и азота (включая фрагмент =N(O)-). Примерами таких гетероциклов являются фуран, тиофен, пиррол, имидазол, пиразол, оксазол, изоксазол, тиазол, изотиазол, тиадиазол, триазол, тетразол.
Термин «7-11-членный гетеробициклил» или «7-11-членный гетеробицикл» означает гетероциклическую систему из двух циклов, включающую от 7 до 11 циклических атомов, где как минимум один циклический атом входит в оба цикла, которая может содержать двойные связи в количестве вплоть до максимального (ароматический или неароматический цикл, который является полностью или частично ненасыщенным или насыщенным), где как минимум один и вплоть до шести циклических атомов заменены гетероатомами, выбранными из группы, состоящей из серы (включая фрагменты -S(O)-, -S(O)2-), кислорода и азота (включая фрагмент =N(O)-), и где указанная циклическая система связана с остальной частью молекулы через атом углерода или азота. Примерами 7-11-членных гетеробициклов являются индол, индолин, бензофуран, бензотиофен, бензоксазол, бензизоксазол, бензотиазол, бензизотиазол, бензимидазол, бензимидазолин, хинолин, хиназолин, дигидрохиназолин, хинолин, дигидрохинолин, тетрагидрохинолин, декагидрохинолин, изохинолин, декагидроизохинолин, тетрагидроизохинолин, дигидроизохинолин, бензазепин, пурин или птеридин. Термин «7-11-членный гетеробицикл» охватывает также спиро-структуры из двух циклов, такие как 1,4-диокса-8-азаспиро[4.5]декан или 2-окса-6-азаспиро[3.3]гептан-6-ил, или мостиковые гетероциклы, такие как 8-азабицикло[3.2.1]октан или 2,5-диазабицикло[2.2.2]октан-2-ил.
Термин «насыщенный 7-11-членный гетеробициклил» или «насыщенный 7-11-членный гетеробицикл» означает полностью насыщенный «7-11-членный гетеробициклил» или «7-11-членный гетеробицикл».
Предпочтительными соединениями формулы (I) являются такие соединения, в которых один или несколько входящих в них фрагментов имеют указанные ниже значения, причем все комбинации предпочтительных значений заместителей входят в объем настоящего изобретения. Что касается всех предпочтительных соединений формулы (I), настоящее изобретение включает также все таутомерные и стереоизомерные формы, а также их смеси во всех соотношениях, и, кроме того, фармацевтически приемлемые соли.
В предпочтительных вариантах осуществления настоящего изобретения, упомянутые ниже заместители независимо друг от друга принимают указанные ниже значения. Следовательно, один или несколько из этих заместителей могут иметь приведенные ниже предпочтительные или более предпочтительные значения.
Предпочтительно, n означает 0.
Предпочтительно, в формуле (I) фрагменты RY1, RY2 и Y0 определяются таким образом, что формула (I) принимает вид формул (Ia), (Ib), (Ic) или (Id):
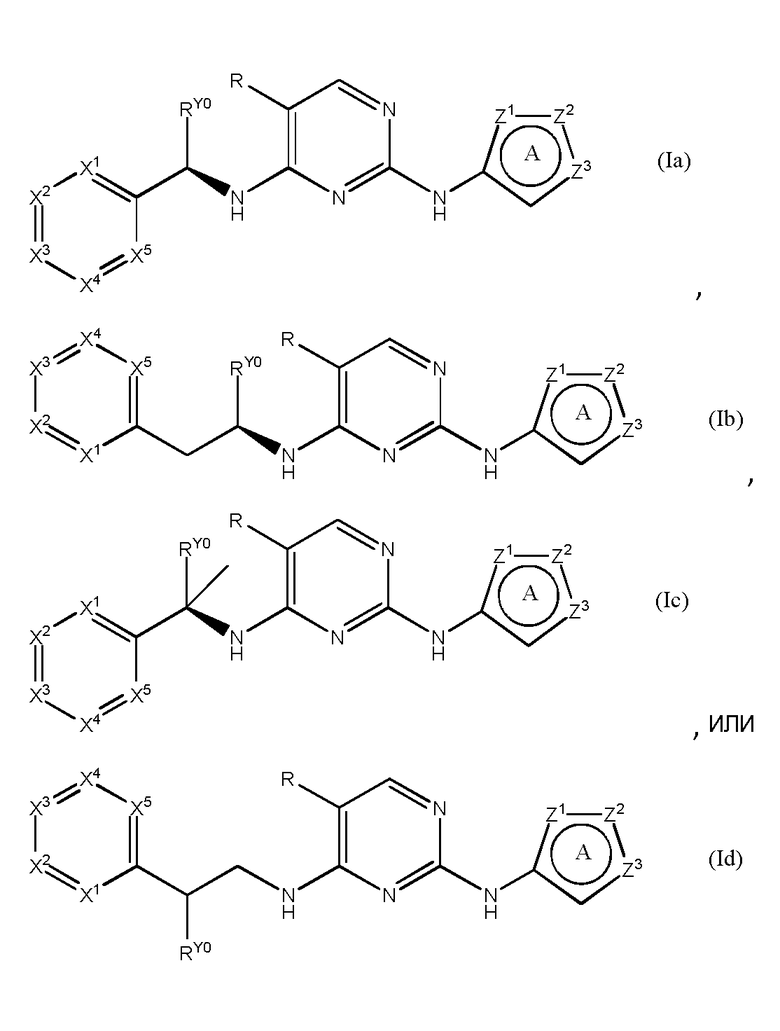 .
.
Предпочтительно, Z2 в формулах (Ia)-(Id) означает N(R1), где R1 не является H. Еще более предпочтительной является формула (Ia).
Предпочтительно, RY0 означает незамещенный C2-4алкил; CH2CH2ORY5; CH2CH2C(O)TY1; CH2CH2C(O)ORY5; CH2CH2OC(O)ORY5; CH2CH2N(RY5RY5a); CH2CH2N(RY5)C(O)RY5a; CH2CH2C(O)N(RY5RY5a); CH2ORY5; CH2C(O)TY1; CH2C(O)ORY5; CH2OC(O)RY5; CH2N(RY5RY5a); CH2N(RY5)C(O)RY5a; CH2C(O)N(RY5RY5a); C(O)TY1; C(O)ORY5; или C(O)N(RY5RY5a). Более предпочтительно, RY0 представляет собой CH2CH3; CH2ORY5; C(O)ORY5; C(O)N(RY5RY5a); или C(O)TY1. Еще более предпочтительно, RY0 представляет собой CH2ORY5, в частности CH2OH. Еще более предпочтительно, RY0 означает CH2OH; CH2CH3; C(O)OH; C(O)CH3; C(O)NHCH3; C(O)N(CH3)2; C(O)NHCH2CH3; C(O)NHCH2CH2CH2OCH3; пирролидин-1-илкарбонил; или пиперидин-1-илкарбонил. Еще более предпочтительно, RY0 означает CH2OCH3; циклопентиламинокарбонил; CH2CH2OH; или 2,2,2-трифторэтиламинокарбонил.
Предпочтительно, цикл A представляет собой пирролильный или пиразолильный цикл; более предпочтительно пиразолильный цикл. Еще более предпочтительно, цикл выбран из группы, состоящей из:
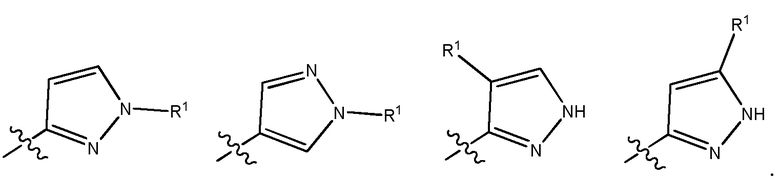
Еще более предпочтительно, цикл представляет собой
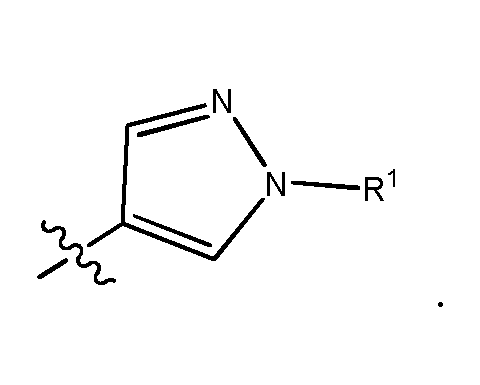
Предпочтительно, цикл A является незамещенным. Более предпочтительно, цикл A замещен одним или двумя (предпочтительно, одним) фрагментами R1, которые отличаются от H и являются одинаковыми или различными.
Предпочтительно, один из фрагментов Z1, Z2, Z3 представляет собой N(R1), и R1 не является H.
Предпочтительно, R1 представляет собой C(O)OR2; C(O)R2; или C(O)N(R2R2a) (предпочтительно C(O)NHR2). Предпочтительно, R1 означает морфолин-4-илкарбонил. Предпочтительно, R1 означает N-метилпирролидин-2-он-3-ил.
Предпочтительно, R1 означает незамещенный C1-4алкил (предпочтительно, метил); или C1-4алкил, замещенный одним или двумя (предпочтительно, одним) фрагментами R3, которые являются одинаковыми или различными.
Предпочтительно, R3 означает галоген; OR4; C(O)OR4; C(O)T1; или C(O)N(R4R4a). Также предпочтительно, R3 представляет собой OR4; C(O)OR4; или C(O)N(R4R4a). Более предпочтительно, R3 означает NH2 или галоген. Более предпочтительно, R3 означает C(O)N(R4R4a). Еще более предпочтительно, R3 означает OH; C(O)OC1-4алкил (предпочтительно, этил или 2-пропил); C(O)NHC1-4алкил (предпочтительно, метил); или C(O)N(C1-4алкил)2 (предпочтительно, диметил). Еще более предпочтительно, R3 означает C(O)NH2.
Более предпочтительно, R1 выбран из группы, включающей CH2CH2OH; CH2CH(OH)CH3; CH2C(O)OH; CH2C(O)OC1-4алкил (предпочтительно, этил или 2-пропил); CH2C(O)NHC1-4алкил (предпочтительно, метил); или CH2C(O)N(C1-4алкил)2 (предпочтительно, диметил). Еще более предпочтительно, R1 означает CH2C(CH3)2OH; (CH2)3OH; цикопропиламинокарбонилметил; CH2C(O)N(CH3)CH2CN; C(CH3)2C(O)NH2; CH2C(O)NH(CH2)2N(CH3)2; CH2C(O)NH(CH2)3N(CH3)2; морфолин-4-илкарбонилметил; 3-аминопропил; изопропилоксиэтил; CH2C(O)NHCH(CH3)2; CH2C(O)NHCH(CH3)CH2OH; или 2,2-дифторэтил. Еще более предпочтительно, R1 означает CH3 или CH2CH2OH. Еще более предпочтительно, R1 означает CH2C(O)NH2 или CH2C(O)NHCH3.
Предпочтительно, R означает F; Cl; CF3; или CH3. Более предпочтительно, R означает Cl.
Предпочтительно, ни один из фрагментов X1, X2, X4, X5 не является N. Предпочтительно, X3 означает CH. Более предпочтительно, X1, X2, X4, X5 представляют собой фрагменты CH.
Предпочтительно, не более трех (предпочтительно, не более двух, еще более предпочтительно, не более одного) фрагментов из числа R6a, R6b, R6c, R6d отличаются от H. Соответственно, в предпочтительном варианте осуществления, ни один из фрагментов R6a, R6b, R6c, R6d не отличается от H, и в другом предпочтительном варианте осуществления один из фрагментов R6a, R6b, R6c, R6d не является H.
Предпочтительно, фрагменты R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из H, галогена; CN; C(O)OR7; OR7; C(O)R7; C(O)N(R7R7a); S(O)2N(R7R7a); S(O)N(R7R7a); S(O)2R7; S(O)R7; SR7; N(R7R7a); NO2; OC(O)R7; N(R7)C(O)R7a; N(R7)C(O)N(R7aR7b); N(R7)C(O)OR7a; OC(O)N(R7R7a); T2; C1-6алкила; C2-6алкенила; и C2-6алкинила, где C1-6алкил; C2-6алкенил; и C2-6алкинил необязательно замещены одной или несколькими группами R11, которые являются одинаковыми или различными.
Предпочтительно, фрагменты R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из H, галогена (предпочтительно, F); или T2, например, 2-окса-6-азаспиро[3.3]гептан-6-ила, N-метилпиразол-4-ила. Предпочтительно, фрагменты R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из H; галогена; CF3; OR7, например, OCH3; или T2, например, N-метилпиразол-4-ила или морфолин-3-он-4-ила. Более предпочтительно, фрагменты R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из H; и галогена (предпочтительно, F).
Соединения формулы (I), в которых некоторые или все из упомянутых выше групп имеют предпочтительные значения, также являются предметом настоящего изобретения.
Еще более предпочтительные соединения по настоящему изобретению выбраны из группы, состоящей из:
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
2-((5-фтор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-фтор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(R)-5-хлор-N2-(1-метил-1H-пиразол-4-ил)-N4-(1-фенилпропил)пиримидин-2,4-диамина;
(S)-2-((2-((1-метил-1H-пиразол-4-ил)амино)-5-(трифторметил)пиримидин-4-ил)амино)-2-фенилэтанола;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилпропан-1-ола;
2-((2-((1-метил-1H-пиразол-4-ил)амино)-5-(трифторметил)пиримидин-4-ил)амино)-2-фенилпропан-1-ола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-3-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
2-((2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)-5-метилпиримидин-4-ил)амино)-2-фенилэтанола;
(S)-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиррол-2-ил)(морфолино)метанона;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-3-фенилпропан-1-ола;
метил 2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилацетата;
метил 2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилацетата;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилуксусной кислоты;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилуксусной кислоты;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-3-фенилпропан-1-ола;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-метил-2-фенилацетамида;
(S)-изопропил 2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетата;
(S)-этил 2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетата;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)уксусной кислоты;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N,N-диметил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N,N-диметил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-этил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-этил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-(2-метоксиэтил)-2-фенилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N,N-диметилацетамида;
2-(4-((5-хлор-4-((1-(2,6-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
2-(4-((5-хлор-4-((1-(3-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пирамидин-4-ил)амино)-2-фенил-1-(пирролидин-1-ил)этанона;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенил-1-(пирролидин-1-ил)этанона;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
1-(4-((5-хлор-4-((1-(3-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)пропан-2-ола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-3-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
1-(4-((5-хлор-4-((1-(2,6-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)пропан-2-ола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2,6-дифторфенил)этанола;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2,6-дифторфенил)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-3-ил)амино)пиримидин-4-ил)амино)-2-(2,6-дифторфенил)этанола;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-(2-гидроксиэтил)-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-(2-гидроксиэтил)-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-(2-метоксиэтил)-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенил-1-(пиперидин-1-ил)этанона;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-3-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенил-1-(пиперидин-1-ил)этанона; и
2-(3-(2-окса-6-азаспиро[3.3]гептан-6-ил)фенил)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола.
Другие предпочтительные соединения по настоящему изобретению выбраны из группы, состоящей из:
(S)-5-хлор-N4-(2-метокси-1-фенилэтил)-N2-(1-метил-1H-пиразол-4-ил)пиримидин-2,4-диамина;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
1-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-2-метилпропан-2-ола;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-циклопентил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-циклопентил-2-фенилацетамида;
1-(4-((5-хлор-4-((1-(3-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-2-метилпропан-2-ола;
1-(4-((5-хлор-4-((1-(2,6-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-2-метилпропан-2-ола;
3-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)пропан-1-ола;
(R)-3-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино-3-фенилпропан-1-ола;
(R)-2-(4-((5-хлор-4-((3-гидрокси-1-фенилпропил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-изопропилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-циклопропилацетамида;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-(1-метил-1H-пиразол-4-ил)фенил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-(цианометил)-N-метилацетамида;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(4-фторфенил)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(4-фторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-2-метилпропанамида;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-метоксифенил)этанола;
(S)-2-((2-((1H-пиразол-4-ил)амино)-5-хлорпиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
(S)-2-((2-((1H-пиразол-4-ил)амино)-5-хлорпиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-2-ил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(пиридин-2-ил)этил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-метоксифенил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(3-метоксифенил)этил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(3-фторфенил)-2-гидрокиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
(S)-2-((2-((1H-пиразол-4-ил-амино)-5-хлорпиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-(2-(диметиламино)этил)ацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-(3-(диметиламино)пропил)ацетамида;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-3-ил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-3-ил)этанола;
2-(3-бромфенил)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-(1-метил-1H-пиразол-4-ил)фенил)этанола;
(S)-2-((5-хлор-2-((1-этил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-этил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-этил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-3-ил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(2-метоксифенил)этил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(3-метоксифенил)этил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил) амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(2-метоксифенил)этил) амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(3-метоксифенил)этил) амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил) амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(пиридин-3-ил)этил) амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-((5-хлор-2-((1-изопропил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-изопропил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-изопропил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-3-ил)этанола;
(S)-2-(4-((5-фтор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
(S)-2-((5-хлор-2-((1-этил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-изопропил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-(4-((5-фтор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-фтор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-((2-((1-(3-аминопропил)-1H-пиразол-4-ил)амино)-5-хлорпиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-хлор-2-((1-(2-изопропиоксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-изопропилацетамида;
2-(4-((5-хлор-4-(((S)-1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино-1H-пиразол-1-ил)-N-((S)-1-гидроксипропан-2-ил)ацетамида;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-хлорфенил)этанола;
2-(4-((5-хлор-4-((1-(2-хлорфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
2-(4-((5-хлор-4-((1-(2-хлорфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-хлорфенил)этанола;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
2-(4-((5-хлор-4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
4-(3-(1-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-гидроксиэтил)фенил)морфолин-3-она;
5-хлор-N4-(1-(2-фторфенил)пропил)-N2-(1-метил-1H-пиразол-4-ил)пиримидин-2,4-диамина;
2-(4-((5-хлор-4-((1-(2-фторфенил)пропил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)-N,N-диметилацетамида;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)-N-(2,2,2-трифторэтил)ацетамида;
2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2,5-дифторфенил)этанола;
2-(4-((5-хлор-4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
2-(4-((5-хлор-4-((2-гидрокси-1-(2-(трифторметил)фенил)этил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
2-(4-((5-хлор-4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
(S)-2-(4-((4-((2-гидрокси-1-фенилэтил)амино)-5-метилпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((4-((2-гидрокси-1-фенилэтил)амино)-5-метилпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N,N-диметилацетамида;
3-(4-((5-хлор-4-(((S)-2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-1-метилпирролидин-2-она;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-(1-метил-1H-пиразол-4-ил)фенил)этанола;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фтор-5-(1-метил-1H-пиразол-4-ил)фенил)этанола;
(S)-4-(3-(1-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-гидроксиэтил)фенил)морфолин-3-она;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2,5-дифторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
(S)-2-(4-((5-хлор-4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
(S)-2-(4-((5-хлор-4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(2,5-дифторфенил)-2-((5-фтор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(2,5-дифторфенил)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(4-((4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(3-(1-метил-1H-пиразол-4-ил)фенил)-2-((5-метил-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-((5-фтор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фтор-5-(1-метил-1H-пиразол-4-ил)фенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-(1-метил-1H-пиразол-4-ил)фенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фтор-5-(1-метил-1H-пиразол-4-ил)фенил)этанола;
(S)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фтор-5-(1-метил-1H-пиразол-4-ил)фенил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(3-(1-метил-1H-пиразол-4-ил)фенил)этил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-фтор-4-((2-гидрокси-1-(3-(1-метил-1H-пиразол-4-ил)фенил)этил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((1-(3-фтор-5-(1-метил-1H-пиразол-4-ил)фенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-фтор-4-((1-(3-фтор-5-(1-метил-1H-пиразол-4-ил)фенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(3,5-дифторфенил)-2-((5-фтор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3,5-дифторфенил)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(4-((4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1H-пиразол-1-ил)ацетамида;
(S)-2-(4-((4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-4-(3-(1-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-гидроксиэтил)-2-фторфенил)морфолин-3-она;
(S)-2-(2,5-дифторфенил)-2-((5-метил-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3,5-дифторфенил)-2-((5-метил-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-((5-хлор-2-((1-(2,2-дифторэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((2-((1-(2,2-дифторэтил)-1H-пиразол-4-ил)амино)-5-метилпиримидин-4-ил)амино)-2-(2,5-дифторфенил)этанола;
(S)-2-((2-((1-(2,2-дифторэтил)-1H-пиразол-4-ил)амино)-5-метилпиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
2-((2-((1-(2,2-дифторэтил)-1H-пиразол-4-ил)амино)-5-метилпиримидин-4-ил)амино)-2-(2,6-дифторфенил)этанола;
2-(4-((4-((1-(2,6-дифторфенил)-2-гидроксиэтил)амино)-5-метилпиримидин-2-ил)амино-1H-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(пиридин-3-ил)этил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(3-бромфенил)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бром-5-фторфенил)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бромфенил)-2-((5-метил-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бром-5-фторфенил)-2-((5-фтор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бромфенил)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бром-5-фторфенил)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бром-5-фторфенил)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(4-((4-((1-(3-бромфенил)-2-гидроксиэтил)амино)-5-хлорпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((4-((1-(3-бромфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((4-((1-(3-бром-5-фторфенил)-2-гидроксиэтил)амино)-5-хлорпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((4-((1-(3-бром-5-фторфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида; и
2-(3-бромфенил)-2-((5-хлор-2-((1-метил-1H-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола.
Если может иметь место таутомерия, например, кето-енольная таутомерия, соединений общей формулы (I), индивидуальные формы, например, кетонная и енольная форма, включены в изобретение по отдельности и в виде смеси в любом соотношении. То же самое относится к стереоизомерам, например, энантиомерам, цис/транс-изомерам, конформерам и т.п.
Изотопно-меченые соединения («изотопные производные») формулы (I) также входят в объем настоящего изобретения. Способы введения изотопных меток известны в технике. Предпочтительными изотопами являются изотопы таких элементов, как H, C, N, O и S.
Если это желательно, изомеры можно разделить хорошо известными в технике способами, например, жидкостной хроматографией. Аналогично можно разделить и энантиомеры, с применением, например, хиральных неподвижных фаз. Кроме того, энантиомеры можно разделять, превращая их в диастереомеры, т.е. связывая их с энантиомерно чистым вспомогательным соединением с последующим разделением полученных диастереомеров и отщеплением остатка вспомогательного соединения. В качестве альтернативы, любой энантиомер соединения формулы (I) можно получить путем стереоселективного синтеза, используя оптически чистые исходные вещества.
Соединения формулы (I) могут существовать в кристаллической или аморфной форме. Кроме того, некоторые кристаллические формы соединений формулы (I) могут существовать в виде полиморфов, которые входят в объем настоящего изобретения. Полиморфные формы соединения формулы (I) можно охарактеризовать и дифференцировать с использованием целого ряда традиционных аналитических методик, включая, но не ограничиваясь этим, дифракцию рентгеновских лучей на порошке (XRPD), инфракрасные (IR, ИК) спектры, спектры комбинационного рассеяния, дифференциальную сканирующую калориметрию (DSC), термогравиметрический анализ (TGA) и твердотельный ядерный магнитный резонанс (ssNMR).
В случае если соединения формулы (I) содержат одну или несколько кислотных или основных групп, изобретение охватывает также соответствующие фармацевтически или токсикологически приемлемые соли, в частности, соли, применимые в фармацевтике. Так, например, соединения формулы (I), которые содержат кислотные группы, могут применяться согласно настоящему изобретению, например, в виде солей щелочных металлов, солей щелочноземельных металлов или солей аммония. Более конкретные примеры таких солей включают соли натрия, соли калия, соли кальция, соли магния, или соли аммония или органических аминов, например, этиламина, этаноламина, триэтаноламина или аминокислот. Соединения формулы (I), которые содержат одну или несколько основных групп, т.е. групп, которые могут быть протонированы, могут входить в объем настоящего изобретения и применяться в форме аддитивных солей с неорганическими или органическими кислотами. Примеры подходящих кислот включают хлористый водород, бромистый водород, фосфорную кислоту, серную кислоту, азотную кислоту, метансульфоновую ксилоту, п-толуолсульфоновую кислоту, нафталиндисульфоновые кислоты, щавелевую кислоту, уксусную кислоту, винную кислоту, молочную кислоту, салициловую кислоту, бензойную кислоту, муравьиную кислоту, пропионовую кислоту, пивалиновую кислоту, диэтилуксусную кислоту, малоновую кислоту, янтарную кислоту, пимелиновую кислоту, фумаровую кислоту, малеиновую кислоту, яблочную кислоту, сульфаминовую кислоту, фенилпропионовую кислоту, глюконовую кислоту, аскорбиновую кислоту, изоникотиновую кислоту, лимонную кислоту, адипиновую кислоту и другие кислоты, известные специалисту в данной области техники. Если в молекуле соединения формулы (I) одновременно содержатся кислотные и основные группы, изобретение также включает, помимо уже упомянутых солевых форм, внутренние соли или бетаины (цвиттерионы). Соответствующие соли соединений формулы (I) можно получать стандартными способами, которые известны специалисту в данной области техники, как, например, взаимодействием соединений формулы (I) с органическими или неорганическими кислотами или основаниями, в растворителе или дисперсионной среде, или путем анионного или катионного обмена с другими солями. Настоящее изобретение включает также все соли соединений формулы (I), которые из-за низкой физиологической совместимости, не подходят непосредственно для применения в фармацевтике, но могут применяться, например, в качестве интермедиатов для проведения химических реакций или для получения фармацевтически приемлемых солей.
В настоящем изобретении, термин «фармацевтически приемлемый» означает, что соответствующее соединение, носитель или молекула подходят для введения людям. Предпочтительно, этот термин означает одобрение регулирующим органом, например, EMEA (Европа) и/или FDA (Соединенные штаты) и/или любым другим национальным регулирующим органом для применения у животных, предпочтительно у людей.
Кроме того, настоящее изобретение включает все сольваты соединений по настоящему изобретению.
Согласно настоящему изобретению киназа «JAK» включает всех членов семейства JAK (например, JAK1, JAK2, JAK3 и TYK2).
Согласно настоящему изобретению, выражение «JAK1» или «JAK1 киназа» означает «Янус-киназа 1». Человеческй ген, кодирующий JAK1, локализован на хромосоме 1p31.3.
Согласно настоящему изобретению, выражение «JAK2» или «JAK2 киназа» означает «Янус-киназа 2». Человеческй ген, кодирующий JAK2, локализован на хромосоме 9p24.
Согласно настоящему изобретению, выражение «JAK3» или «JAK3 киназа» означает «Янус-киназа 3». Ген, кодирующий JAK3, локализован на человеческой хромосоме 19p13.1 и преимущественно находится в гематопоэтических клетках. JAK3 представляет собой цитоплазматическую протеин тирозин киназу, которая связывается с гамма-цепью рецептора интерлейкина 2 (IL-2). Эта цепь является также компонентом рецепторов ряда лимфотропных цитокинов, включая интерлейкины IL-4, IL-7, IL-9, IL-15 и IL-21 (Schindler et al., 2007, J. Biol. Chem. 282(28):29959-63). JAK3 играет ключевую роль в реакции иммунных клеток на цитокины, в частности в мастоцитах, лимфоцитах и макрофагах. Было показано, что ингибирование JAK3 оказывает благоприятное действие при профилактике отторжения трансплантата (Changelian et al., 2003, Science 302(5646):875-888).
Кроме того, согласно настоящему изобретению, выражение «JAK3» или «JAK3 киназа» включает мутантные формы JAK3, предпочтительно мутантные формы JAK3, которые обнаруживаются у пациентов с острым мегакариобластным лейкозом (AMKL). Более предпочтительно, эти мутантные формы включают мутации по одному аминокислотному остатку. Мутации, активирующие JAK3, наблюдалась у пациентов с острым мегакариобластным лейкозом (AMKL) (Walters et al., 2006. Cancer Cell 10(1):65-75). Таким образом, в предпочтительном варианте осуществления, выражение «JAK» включает также белок JAK3, имеющий мутации V7221 или P132T.
Согласно настоящему изобретению, выражение «TYK2» или «TYK2 киназа» означает «протеин тирозин киназа 2». Гены JAK3 и TYK2 сгруппированы на хромосоме 19p13.1 и 19p13.2, соответственно.
Как показано в примерах, соединения по настоящему изобретению были исследованы с точки зрения их селективности в отношении JAK3 киназы по сравнению с JAK2 киназой. При этом показано, что все испытанные соединения связывают JAK3 более селективно, чем JAK2 (см. приведенную ниже таблицу 8).
Поэтому считается, что соединения по настоящему изобретению применимы для профилактики или лечения заболеваний и расстройств, связанных с JAK, например, иммунологических, воспалительных, аутоиммунных или аллергических расстройств, отторжения трансплантата, реакции «трансплантат против хозяина», или пролиферативных заболеваний, например, рака.
В предпочтительных вариантах осуществления, соединения по настоящему изобретению являются селективными ингибиторами JAK3.
В равной степени предпочтительными являются двойные ингибиторы JAK1/JAK3.
Соединения по настоящему изобретению могут быть дополнительно охарактеризованы путем определения того, оказывают ли они влияние на JAK3, например, на его киназную активность (Changelian et al., 2003, Science 320(5646): 875-888 и online дополнение; Yang et al., 2007. Bioorg. Med. Chem.Letters 17(2):326-331).
Вкратце, киназную активность JAK3 можно измерить, используя рекомбинантный слитый белок GST-JAK3, включающий каталитический домен (JH1 каталитический домен). Киназную активность JAK3 измеряют с помощью ELISA следующим образом: планшеты в течение ночи покрывают статистическим сополимером L-глутаминовой кислоты и тирозина (4:1; 100 мкг/мл) в качестве субстрата. Планшеты промывают, инкубируют с рекомбинантным белком JAK3 JH1:GST (100 нг/лунку) в присутствии или в отсутствии ингибитора в течение 30 минут при комнатной температуре. Добавляют HPR-конъюгированное антитело PY20 против фосфорилтирозина (ICN) и проявляют TMB (3,3',5,'-тетраметилбензидином) (Changelian et al., 2003, Science 320(5646): 875-888 и online дополнение).
Была описана методика клеточного анализа (пролиферация клеток TF-1) для оценки ингибирующего влияния низкомолекулярных лекарственных средств на JAK2 или JAK3-зависимую передачу сигнала (Chen et al., 2006, Bioorg.Med.Chem.Letters 16(21):5633-5638).
Настоящее изобретение относится к фармацевтическим композициям, включающим соединение формулы (I), или его фармацевтически приемлемую соль или изотопное производное в качестве действующего ингредиента, наряду с фармацевтически приемлемым носителем, необязательно в комбинации с одним или несколькими другими фармацевтическими композициями.
Термин «фармацевтическая композиция» означает композицию, включающую один или несколько действующих ингредиентов, один или несколько инертных ингредиентов, которые образуют носитель, а также любые продукты, которые прямо или косвенно образуются в результате смешивания, комплексообразования или агрегирования любых двух или нескольких ингредиентов, или в результате диссоциации одного или нескольких ингредиентов, или в результате других типов реакций или взаимодействий одного или нескольких ингредиентов. Соответственно, фармацевтические композиции по настоящему изобретению охватывают любые композиции, полученные смешиванием соединения по настоящему изобретению и фармацевтически приемлемого носителя.
Термин «носитель» относится к разбавителю, адъюванту, эксципиенту или носителю, с которым вводится терапевтически активное вещество. Такие фармацевтические носители могут представлять собой стерильные жидкости, например, воду и масла, включая масла, полученные из нефти, растительного животного или синтетического происхождения, включая, но не ограничиваясь этим, масло арахиса, соевое масло, минеральное масло, кунжутное масло и т.п. Если фармацевтическая композиция вводится перорально, предпочтительным носителем является вода. Если фармацевтическая композиция вводится внутривенно, предпочтительными носителями являются физиологический раствор и водный раствор декстрозы. Физиологический раствор, а также водные растворы декстрозы и глицерина предпочтительно применяются в качестве жидких носителей в случае растворов для введения инъекцией. Походящие фармацевтические эксципиенты включают крахмал, глюкозу, лактозу, сахарозу, желатин, солод, рис, муку, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, обезжиренный молочный порошок, глицерин, пропиленгликоль, воду, этанол и т.п. Композиция, если это желательно, может также содержать небольшие количества смачивающих, эмульгирующих агентов или pH-буферных агентов. Эти композиции могут принимать форму растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, составов с длительным высвобождением и т.п. Композициям можно придавать форму суппозитория, включающего традиционные связующие вещества и носители, например, триглицериды. Пероральные составы могут включать стандартные носители, например, маннит, лактозу, крахмал, стеарат магния, натрий сахарин, целлюлозу, карбонат магния фармацевтического качества и т.д. Примеры подходящих фармацевтических носителей описаны E.W. Martin в “Remington's Pharmaceutical Sciences”. Композиции по настоящему изобретению будут содержать терапевтически эффективное количество действующего средства, предпочтительно, в очищенной форме, в сочетании с необходимым количеством носителя с тем, чтобы получить лекарственную форму, которую удобно вводить пациенту. Состав должен соответствовать выбранному пути введения.
Фармацевтическая композиция по настоящему изобретению может включать одно или несколько дополнительных соединений в качестве действующих ингредиентов, например, одно или несколько соединений формулы (I), которые не являются первым соединением в композиции, или других ингибиторов JAK. Дополнительные биологически активные соединения могут представлять собой стероиды, антагонисты лейкотриена, циклоспорин или рапамицин.
Соединения по настоящему изобретению или их фармацевтически приемлемые соли или изотопные производные и другие фармацевтически активные агенты можно вводить совместно или по отдельности и, в случае отдельного введения, это введение может осуществляться отдельно или последовательно в любом порядке. В случае объединения в одном и том же составе, следует иметь в виду, что два действующих соединения должны быть стабильны и совместимы друг с другом и другими компонентами состава. В случае включения соединений в отдельные составы, эти составы могут иметь любую удобную форму, обычно такую, которая известна в технике для этих соединений.
Кроме того, настоящее изобретение охватывает случаи, когда соединение формулы (I) или его фармацевтически приемлемую соль или изотопное производное, или фармацевтическую композицию, включающую соединение формулы (I), вводят в комбинации с другим лекарственным средством или фармацевтически активным агентом и/или когда фармацевтическая композиция по настоящему изобретению дополнительно включает такое лекарственное средство или фармацевтически активный агент.
В этом контексте, термин «лекарственное средство или фармацевтически активный агент» включает лекарственное средство или фармацевтический агент, который будет вызывать биологическую или медицинскую реакцию ткани, системы, животного или человека, которая подразумевалась, например, исследователем или клиницистом.
Термины «скомбинированный» или «в комбинации» или «комбинация» следует понимать, как функциональное комбинированное введение, где некоторые или все соединения можно вводить по отдельности в разных составах, разными путями (например, подкожным, внутривенным или пероральным) и в разное время. Индивидуальные соединения таких комбинаций можно вводить либо последовательно в составе отдельных фармацевтических композиций, а также одновременно, в составе комбинированных фармацевтических композиций.
Например, при лечении ревматоидного артрита, предусмотрена комбинация с другими агентами на основе химиотерапевтических средств или антител. Подходящие примеры фармацевтически активных агентов, которые могут применяться в комбинации с соединениями по настоящему изобретению и их солями для лечения ревматоидного артрита, включают: иммуносупрессоры, такие как амтолметина гуацил, мизорибин и римексолон; анти-TNFα агенты, такие как этанерцепт, инфликсимаб, адалимумаб, анакинра, абатацепт, ритуксимаб; ингибиторы тирозинкиназы, такие как лефлуномид; антагонисты клликреина, такие как субреум; агонисты интерлейкина 11, такие как опрелвекин; агонисты интерферона бета 1; агонисты гиалуроновой кислоты, такие как NRD-101 (Aventis); антагонисты рецептора интерлейкина 1, такие как анакинра; антагонисты CD8, такие как амиприлозы гидрохлорид; антагонисты предшественника бета-амилоидного белка, такие как реумакон; ингибиторы матриксных металлопротеиназ, такие как ципемастат, а также другие противоревматические средства, модифицирующие течение заболевания (DMARDs), такие как метотрексат, сульфасалазин, циклоспорин A, гидроксихлорохин, ауранофин, ауротиоглюкоза, ауротиомалат натрия и пеницилламин.
В частности, лечение по настоящему изобретению можно применять в качестве монотерапии или, в дополнение к введению соединений по настоящему изобретению, лечение может включать традиционное лечение с помощью хирургии, радиационной терапии или химиотерапии. Соответственно, соединения по настоящему изобретению можно также применять в комбинации с существующими терапевтическими агентами для лечения пролиферативных заболеваний, таких как рак. Походящие агенты, которые следует применять в таких комбинациях, включают:
(i) антипролиферативные/антинеопластические препараты и их комбинации, применяемые в лечении онкологических заболеваний, такие как алкилирующие агенты (например, цис-платин, карбоплатин, циклофосфамид, азотистый иприт, мелфалан, хлорамбуцил, бусульфан и нитрозомочевина); антиметаболиты (например, антифолаты, такие как фторпиримидины в т.ч. 5-фторурацил и тегафур, ралтитрексед, метотрексат, цитозина арабинозид, гидроксимочевина и гемцитабин); противоопухолевые антибиотики (например, антрацикилины, такие как адриамицин, блеомицин, доксорубицин, дауномицин, эпирубицин, идарубицин, митомицин-C, дактиномицин и митрамицин); антимитотические агенты (например, алкалоиды барвинка, такие как винкристин, винбластин, виндезин и винорелбин, и таксоиды, такие как паклитаксел и таксотере); а также ингибиторы топоизомеразы (например, эпиподофиллотоксины, такие как этопозид и тенипозид, амсакрин, топотекан и камптотекины);
(ii) цитостатические агенты, такие как антиэстрогены (например, тамоксифен, торемифен, ралоксифен, дролоксифен и йодоксифен), понижающие регуляторы рецептора эстрогена (например, фульвестрант), антиандрогены (например, бикалутамид, флутамид, нилутамид и ципротерона ацетат), антагонисты LHRH или агонисты LHRH (например, госерелин, леупрорелин и бусерелин), прогестогены (например, мегестерола ацетат), ингибиторы ароматазы (например, анастрозол, летрозол, воразол и эксеместан), а также ингибиторы 5α-редуктазы, такие как финастерид;
(iii) противоинвазивные средства (например, ингибиторы киназ семейства c-Src, такие как 4-(6-хлор-2,3-метилендиоксианилино)-7-[2-(метилпиперазин-1-ил)этокси]-5-тетрагидропиран -4-илоксихиназолин (AZD0530) и N-(2-хлор-6-метилфенил)-2-{6-[4-(2-гидроксиэтил)пиперазин-1-ил]-2-метилпиримидин-4-иламино}тиазол-5-карбоксамид (дазатиниб, BMS-354825), а также ингибиторы металлопротеиназы, такие как маримастат, и ингибиторы деятельности рецептора урокиназного активатора плазминогена);
(iv) ингибиторы деятельности факторов роста: например, такие ингибиторы включают антитела против факторов роста и антитела против рецепторов факторов роста (например, антитело против erbB2 трастузумаб [HerceptinTM] и антитело против erbB1 цетуксимаб [C225]); такие ингибиторы включают также, например, ингибиторы тирозин киназы, например, ингибиторы семейства эпидермальных факторов роста (например, ингибиторы тирозин киназ семейства EGFR, такие как N-(3-хлор-4-фторфенил)-7-метокси-6-(3-морфолинопропокси)хиназолин-4-амин (гефитиниб, ZD 1839), Λ/-(3-этинилфенил)-6,7-бис(2-метоксиэтокси)хиназолин-4-амин (эрлотиниб, OSI-774) и 6-акриламидо Λ/-(3-хлор-4-фторфенил)-7-(3-морфолинопропокси)хиназолин-4-амин (CI 1033), и ингибиторы erbB2 тирозин киназы, такие как лапатиниб), ингибиторы семейства факторов роста гепатоцитов, ингибиторы семейства факторов роста, вырабатываемых тромбоцитами, такие как иматиниб, ингибиторы серин/треонин киназ (например, ингибиторы сигнального пути Ras/Raf, например, ингибиторы фарнезил трансферазы, такие как сорафениб (BAY 43-9006)) и ингибиторы клеточной передачи сигнала через MEK и/или Akt киназы;
(v) антиангиогенные средства, например, ингибирующие действие сосудистого эндотелиального фактора роста, например, антитело против сосудистого эндотелиального фактора роста бевацизумаб (AvastinTM) и ингибиторы VEGF рецептора тирозин киназы, такие как 4-(4-бром-2-фторанилино)-6-метокси-7-(1-метилпиперидин-4-илметокси)хиназолин (ZD6474; пример 2 в заявке WO 01/32651), 4-(4-фтор-2-метилиндол-5-илокси)-6-метокси-7-(3-пирролидин-1-илпропокси)хиназолин (AZD2171; пример 240 в заявке WO 00/47212), ваталаниб (RTK787; WO 98/35985) и SUI 1248 (сунитиниб; WO 01/60814), а также соединения, которые действуют по другим механизмам (например, линомид, ингибиторы деятельности интегрина αvβ3 и ангиостатин);
(vi) агенты, поражающие сосуды опухолевой ткани, такие как комбрестатин A4 и соединения, раскрытые в международной заявке на патент WO 99/02166;
(vii) антисмысловые препараты, например, нацеленные на перечисленные выше мишени, такие как ISIS 2503 и анти-ras антисмысловой агент;
(viii) подходы, основанные на генной терапии, включая подходы, основанные на замене аномальных генов, например, аномальных генов p53, BRCA1 или BRCA2, методики GDEPT (ген-направленной ферментной пролекарственной терапии), например, в которых применяется цитозин деаминаза, тимидин киназа или бактериальный фермент нитроредуктаза, и подходы, направленные на увеличение переносимости химиотерапии или радиационной терапии пациентом, например, терапия, направленная на ген мультилекарственной устойчивости; и
(ix) иммунотерапевтические подходы, включая ex-vivo и in-vivo способы увеличения иммуногенности опухолевых клеток пациента, такие как трансфекция цитокинами, например, интерлейкином 2, интерлейкином 4 или колониестимулирующим фактором гранулоцитов и макрофагов, подходы, направленные на понижение толерантности T-клеток, подходы, использующие трансфецированные иммунные клетки, например, дендритные клетки, трансфецированные цитокинами, подходы, использующие опухолевые линии клеток, трансфецированных цитокинами, а также подходы, использующие анти-идиотипические антитела.
Дополнительные способы комбинированного лечения описаны в заявках WO-A 2009/0088992 и WO-A 2007/107318, которые включены в настоящее описание посредством ссылки.
Соответственно, индивидуальные соединения, образующие такие комбинации, можно вводить либо последовательно, в виде отдельных фармацевтических композиций, либо одновременно в составе объединенных фармацевтических композиций.
Фармацевтические композиции по настоящему изобретению включают композиции, подходящие для перорального, ректального, местного, парентерального (включая подкожное, внутримышечное и внутривенное), глазного (офтальмического), легочного (с помощью назальной или буккальной ингаляции) или назального введения, хотя наиболее удобный путь введения в каждом конкретном случае будет зависеть от природы и тяжести подвергаемого лечению состояния и от природы действующего ингредиента. Из композиций по настоящему изобретению имеет смысл получать дозированные лекарственные формы, что достигается любым из способов, хорошо известных в фармацевтической технике.
При практическом применении, соединения формулы (I) в качестве действующего ингредиента можно смешать до получения однородной смеси с фармацевтическим носителем, в соответствии с традиционными методиками получения фармацевтических смесей. Носитель может иметь широкий спектр форм, в зависимости от формы препарата, желательной для введения, например, пероральной или парентеральной (включая внутривенную). При получении композиций для пероральных дозированных форм, можно применять любую из традиционных фармацевтических сред, например, воду, гликоли, масла, спирты, вкусоароматические агенты, консерванты, красители и т.п. в случае жидких пероральных препаратов, например, суспензий, эликсиров и растворов; или такие носители, как крахмалы, сахара, микрокристаллическую целлюлозу, разбавители, гранулирующие агенты, смазывающие средства, связующие средства, дезинтегрирующие средства и т.п. в случае твердых пероральных препаратов, например, порошков, твердых или мягких капсул и таблеток, причем, твердые пероральные препараты являются предпочтительными по сравнению с жидкими препаратами.
Благодаря легкости введения, таблетки и капсулы представляют собой наиболее предпочтительные пероральные дозированные формы, при получении которых, очевидно, применяются твердые фармацевтические носители. Если это желательно, на таблетки можно нанести покрытие, с применением стандартных водных и неводных методик. Такие композиции и препараты должны содержать не менее 0,1 процента действующего соединения. Процентное содержание действующего соединения в этих композициях, безусловно, может изменяться и, как правило, находится в пределах от примерно 2 процентов до примерно 60 масс. процентов от массы единицы лекарственной формы. Количество действующего соединения в таких терапевтически применимых композициях является таким, чтобы можно было получить терапевтически эффективную дозу. Действующие соединения можно также вводить интраназально, например, в виде жидких капель или спрея.
Таблетки, пилюли, капсулы и подобные формы могут также содержать связующее вещество, например, камедь трагаканта, гуммиарабик, кукурузный крахмал или желатин; экципиенты, например, дикальцийфосфат; дезинтегрирующее средство, например, кукурузный крахмал, картофельный крахмал, альгиновую кислоту; смазывающее средство, например, стеарат магния; и подсластитель, например, сахарозу, лактозу или сахарин. Если дозированная лекарственная форма представляет собой капсулу, она, помимо материалов указанных выше типов, может содержать жидкий носитель, например, жирное масло.
В дозированной лекарственной форме может содержаться ряд других материалов, например, в качестве покрытия или предназначенных для модификации физической формы. Например, таблетки могут быть покрыты шеллаком, сахаром или обоими указанными материалами. Сироп или эликсир, помимо действующего ингредиента, может содержать сахарозу в качестве подсластителя, метил- и пропилпарабены в качестве консервантов, краситель и вкусоароматическую добавку, например, вишневый или апельсиновый ароматизатор.
Соединения формулы (I) можно также вводить парентерально. Растворы или суспензии этих действующих соединений можно получать в воде, смешанной с необходимым количеством ПАВ, например, гидроксипропилцеллюлозы. Дисперсии можно также готовить в глицерине, жидких полиэтиленгликолях и их смесях с маслами. При обычных условиях хранения и применения, эти препараты содержат консерванты для предотвращения развития микроорганизмов.
Фармацевтические формы, которые подходят для применения в виде инъекций, включают стерильные водные растворы или дисперсии и стерильные порошки для приготовления стерильных водных растворов или дисперсий непосредственно перед применением. В любом случае, лекарственная форма должна быть стерильной и обладать такой степенью текучести, чтобы ее можно было ввести с помощью шприца. Она должна быть стабильной в условиях производства и хранения и должна быть защищена от загрязняющего действия микроорганизмов, например, бактерий и грибков. Носитель может представлять собой растворитель или дисперсионную среду, содержащую, например, воду, этанол, полиол (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль), их подходящие смеси и растительные масла.
Для введения млекопитающему, в частности, человеку, эффективной дозы соединения по настоящему изобретению, может применяться любой подходящий путь введения. Например, может осуществляться пероральное, ректальное, местное, парентеральное, глазное, легочное, назальное и т.п. введение. Дозированные формы включают таблетки, пастилки, дисперсии, суспензии, растворы, капсулы, кремы, мази, аэрозоли и т.п. Предпочтительно, соединения формулы (I) вводят перорально.
Эффективная дозировка применяемого действующего ингредиента может меняться в зависимости от конкретного соединения, пути введения, подвергаемого лечению состояния и тяжести этого состояния. Такую дозировку может легко установить специалист в данной области техники.
Терапевтически эффективное количество соединения по настоящему изобретению обычно будет зависеть от ряда факторов, включающих, например, возраст и массу животного, конкретное состояние, требующее лечения, и его тяжесть, природу состава и путь его введения. Однако, эффективное количество соединения формулы (I) для лечения воспалительных заболеваний, например, ревматоидного артрита (RA), как правило, будет находиться в диапазоне от 0,1 до 100 мг/кг массы тела реципиента (млекопитающего) в день и, чаще, в диапазоне от 1 до 10 мг/кг массы тела в день. Таким образом, для взрослого млекопитающего массой 70 кг, необходимое количество соединения могло бы составлять от 70 до 700 мг в течение дня, причем это количество можно давать в виде одной дозы в день или, чаще, в виде нескольких (например, двух, трех, четырех, пяти или шести) меньших доз в течение дня, так, чтобы общая дневная дозировка оставалась той же самой. Эффективное количество фармацевтически приемлемой соли, пролекарства или метаболита соединения можно определить, исходя из соответствующей пропорции, по эффективному количеству самого соединения формулы (I). Предполагается, что аналогичные дозировки будут подходить для лечения других состояний, которые перечислены выше.
В настоящем описании, термин «эффективное количество» означает такое количество лекарственного средства или фармацевтического агента, которое вызовет биологическую или медицинскую реакцию ткани, системы, животного или человека, которая предполагалась, например, исследователем или клиницистом.
Кроме того, термин «терапевтически эффективное количество» означает любое количество, которое, при сравнении с соответствующим субъектом, который не получал такого количества, приводит к улучшению, излечению, предупреждению или облегчению заболевания, расстройства или побочного эффекта, или снижению скорости прогрессирования заболевания или расстройства. В рамки описываемого термина входят также количества, эффективные для улучшения нормальных физиологических функций.
Другой аспект настоящего изобретения относится к соединению по настоящему изобретению, его фармацевтически приемлемой соли или изотопному производному для применения в качестве лекарственного средства.
Еще один аспект настоящего изобретения относится к соединению по настоящему изобретению, его фармацевтически приемлемой соли или изотопному производному для применения в способе лечения или профилактики заболевания или расстройства, связанного с JAK.
В контексте настоящего изобретения, заболевание или расстройство, связанное с JAK, определяется, как заболевание или расстройство, в развитие которого вовлечена JAK.
В предпочтительном варианте осуществления, заболевание или расстройство, связанное с JAK, представляет собой иммунологическое, воспалительное, аутоиммунное или аллергическое расстройство или заболевание, связанное с отторжением трансплантата или реакцией «трансплантат против хозяина».
Таким образом, другой аспект настоящего изобретения относится к соединению или его фармацевтически приемлемой соли по настоящему изобретению для применения в способе лечения или профилактики иммунологического, воспалительного, аутоиммунного или аллергического расстройства или заболевания, связанного с отторжением трансплантата или реакцией «трансплантат против хозяина».
Воспаление ткани или органа имеет место при целом ряде расстройств и заболеваний и, в некоторых случаях происходит из-за активации рецепторов семейства цитокинов. Типовые примеры воспалительных расстройств, связанных с активацией JAK, включают, не ограничиваясь этим, воспаление кожи вследствие воздействия радиации, астму, аллергическое воспаление и хроническое воспаление.
В соответствии с настоящим изобретением, аутоиммунное заболевание представляет собой заболевание, которое по крайней мере частично вызвано иммунной реакцией организма против собственных компонентов, например, белков, липидов или ДНК. Примерами орган-специфичных аутоиммунных расстройств являются инсулин-зависимый диабет (I типа), который поражает поджелудочную железу, тиреоидит Хашимото и болезнь Грейвса, которые поражают щитовидную железу, злокачественная анемия, которая поражает желудок, болезнь Кушинга и болезнь Аддисона, которые поражают надпочечники, хронический активный гепатит, который поражает печень; синдром поликистозных яичников (PCOS), глютеиновая болезнь, псориаз, воспалительные заболевания кишечника (IBD) и анкилозирующий спондилит. Примерами не орган-специфичных аутоиммунных расстройств являются ревматоидный артрит, рассеянный склероз, системная красная волчанка и миастения gravis.
Диабет I типа возникает из-за селективной аутоиммунной агрессии аутореактивных T-клеток против бета-клеток островков Лангерганса, секретирующих инсулин. Нацеливание лекарственного средства на JAK3 при этом заболевании основано на данных о том, что многие цитокины, которые передают сигнал через путь JAK, участвуют в аутоиммунном разрушении бета-клеток, опосредованном T-клетками. Действительно, было показано, что JANEX-1, который является ингибитором JAK2, предупреждает развитие спонтанного аутоиммунного диабета в NOD мышиной модели диабета I типа.
В предпочтительном варианте осуществления, аутоиммунное заболевание выбрано из группы, состоящей из ревматоидного артрита (RA), воспалительного заболевания кишечника (IBD; болезни Крона и язвенного колита), псориаза, системной красной волчанки (SLE) и рассеянного склероза (MS).
Ревматоидный артрит (RA) представляет собой хроническое, прогрессирующее воспалительное заболевание с тяжелым течением, которым поражен примерно 1% населения планеты. RA является симметричным многосуставным артритом, который в первую очередь поражает мелкие суставы кистей рук и стоп. Помимо воспаления синовиального слоя и выстилки суставов (хряща), агрессивный фронт ткани, именуемой паннусом, проникает в локальные структуры суставов и разрушает их (Firestein 2003, Nature 423:356-361).
Воспалительная болезнь кишечника (IBD) характеризуется хроническим рецидивирующим воспалением кишечника. IBD подразделяют на фенотипы болезни Крона и язвенного колита. Болезнь Крона чаще всего затрагивает концевую область подвздошной кишки и ободочную кишку и является дискретной и трансмуральной (пронизывающей стенку кишечника). В противоположность этому, при язвенном колите воспаление является непрерывным и ограничивается слоем слизистой оболочки прямой и ободочной кишки. Примерно в 10% случаев воспалительных заболеваний, локализованных в прямой и ободочной кишке, нельзя провести явное различие между болезнью Крона и язвенным колитом, и эти случаи относят к «колитам неопределенной природы». Оба заболевания включают внекишечные воспаления кожи, глаз или суставов. Поражения, индуцированные нейтрофилами, можно предотвратить с помощью ингибиторов миграции нейтрофилов (Asakura et al., 2007, World J Gastroenterol. 13(15):2145-9).
Псориаз представляет собой хронический воспалительный дерматоз, которым поражено примерно 2% населения. Он характеризуется красными чешуйчатыми пятнами на коже, которые обычно появляются на волосистой части кожи головы, локтях и коленях, и может быть связан с тяжелым артритом. Эти поражения вызваны аномальной пролиферацией кератиноцитов и инфильтрацией воспалительных клеток в дерму и эпидермис (Schön et al., 2005, New Engl.J.Med. 352:1899-1912).
Системная красная волчанка (SLE) представляет собой хроническое воспалительное заболевание, вызванное активацией B-клеток, опосредованной T-клетками, которое приводит к гломерулонефриту и почечной недостаточности. На ранних стадиях SLE у людей характеризуется развитием долгоживущих аутореактивных клеток памяти CD4+ (D'Cruz et al., 2007, Lancet 369 (9561):587-596).
Рассеянный склероз (MS) представляет собой воспалительное и демиелинизирующее неврологическое заболевание. Его считали аутоиммунным расстройством, опосредованным T-хелперными клетками CD4+ типа 1, но современные исследования выявили определенную роль других иммунных клеток (Hemmer et al., 2002, Nat. Rev. Neuroscience 3, 291-301).
Мастоциты экспрессируют JAK3, и JAK3 является ключевым регулятором IgE-опосредованных реакций мастоцитов, в т.ч. высвобождения медиаторов воспаления. Было показано, что JAK3 является подходящей мишенью при лечении аллергических реакций, опосредованных мастоцитами. Аллергические реакции, связанные с активацией мастоцитов, включают немедленные аллергические реакции I типа, например, аллергический ринит (сенную лихорадку), аллергическую сыпь (крапивницу), ангиоэдему (отек Квинке), аллергическую астму и анафилаксию, например, анафилактический шок. Эти расстройства можно лечить или предупреждать ингибированием активности JAK3, например, введением ингибитора JAK3 по настоящему изобретению.
Отторжение трансплантата (отторжение аллотрансплантата) включает, не ограничиваясь этим, острое и хроническое отторжение аллотрансплантата после, например, трансплантации почки, сердца, печени, легкого, костного мозга, кожи и роговицы. Известно, что T-клетки играют основную роль в специфичном иммунном ответе, вызывающем отторжение аллотрансплантата. Можно лечить сверхострое, острое и хроническое отторжение трансплантата органа. Сверхострое отторжение проявляется в течение нескольких минут после трансплантации. Острое отторжение обычно возникает в течение шести-двенадцати месяцев нахождения трансплантата в организме. Сверхострое и острое отторжение обычно можно обратить при лечении иммуносупрессорами. Хроническое отторжение, характеризуемое постепенной потерей функции органа, является постоянной причиной для беспокойства реципиента трансплантата, т.к. оно может проявиться в любое время после трансплантации.
Реакция «трансплантат против хозяина» (GVHD) является основным осложнением при аллогенной трансплантации костного мозга (BMT). GVHD вызывается T-клетками донора, которые распознают и реагируют на отличия в системе комплекса гистосовместимости реципиента, что приводит к значительным осложнениям и смертности. JAK3 играет ключевую роль в индукции GVHD, и было показано, что лечение с помощью ингибитора JAK3, а именно JANEX-1, ослабляет тяжесть GVHD (см. обзор в Cetkovic-Cvrlje and Ucken, 2004).
В предпочтительном варианте осуществления настоящего изобретения, воспалительное заболевание представляет собой заболевание глаз.
Синдром сухого глаза (DES, известный также, как сухой кератоконъюнктивит) является одной из наиболее распространенных проблем, с которой сталкиваются глазные врачи. Иногда DES именуют синдромом нарушения слезоотделения (Jackson, 2009. Canadian Journal Ophthalmology 44(4), 385-394). DES поражает до 10% населения в возрасте от 20 до 45 лет, причем распространенность заболевания увеличивается с возрастом. Хотя имеется широкий спектр искусственных слез, эти продукты обеспечивают только временное облегчение симптомов. Поэтому существует потребность в средствах, композициях и терапевтических способов лечения сухости глаз.
В настоящей заявке имеется в виду, что термин «расстройство, связанное с сухостью глаз» охватывает болезненные состояния, суммированные в последнем официальном отчете международного семинара по сухому глазу (DEWS), которое определяет сухой глаз, как «многофакторное заболевание слезоотделения и поверхности глаза, которая приводит к ощущениям дискомфорта, нарушениям зрения и нестабильности слезной пленки с потенциальным ущербом для поверхности глаза. Оно сопровождается повышением осмоляльности слезной пленки и воспалением поверхности глаза». (Lemp, 2007. “The Definition and Classification oa Dry Eye Disease: Report of the Definition and Classification Subcommittee of the International Dry Eye Workshop”, The Ocular Surface, 5(2), 75-92). Сухой глаз иногда также именуют сухим кератоконъюнктивитом. В некоторых вариантах осуществления, лечение расстройств, связанных с сухостью глаз, включает облегчение конкретных симптомов расстройства, например, дискомфорта, нарушений зрения, нестабильности слезной пленки, гиперосмолярности слез и воспаления поверхности глаза.
Увеит является наиболее распространенной формой внутриглазного воспаления, и он остается значимой причиной потери зрения. Современные методики лечения увеита включают системное введение медикаментов, которые вызывают тяжелые побочные эффекты и в целом оказывают иммуносупрессорное действие. В клинической практике хронические прогрессирующие или рецидивирующие формы неифекционного увеита лечат местным и/или системным введением кортикостероидов. Кроме того, применяют макролиды, такие как циклоспорин и рапамицин, и, в некоторых случаях, цитотоксические средства, такие как циклофосфамид и хлорамбуцил, а также антиметаболиты, такие как азатиоприн, метотрексат и лефлуномид (Srivastava et al., 2010. Uveitis: Mechanisms and recent advances in therapy. Clinica Chimica Acta, doi:10.1016/j.cca.2010.04.017).
Другие заболевания глаз, способы комбинированного лечения и пути введения описаны, например, в заявке WO-A 2010/039939, которая включена в настоящее описание посредством ссылки.
В другом предпочтительном варианте осуществления, заболевание или расстройство, связанное с JAK, представляет собой пролиферативное заболевание, в частности рак.
Заболеваниями и расстройствами, связанными в том числе с JAK, являются пролиферативные расстройства или заболевания, в частности, рак.
Поэтому другой аспект настоящего изобретения относится к соединению, его фармацевтически приемлемой соли или изотопному производному по настоящему изобретению, для применения в способе лечения или профилактики пролиферативного заболевания, в частности, рака.
Термин «рак» охватывает группу заболеваний, характеризующихся неуправляемым ростом и распространением аномальных клеток. Все типы раковых заболеваний обычно включают определенные аномалии в регулировании роста, деления и выживания клеток, приводящие к злокачественному росту этих клеток. Ключевыми факторами, способствующими указанному злокачественному росту клеток, являются независимость от сигналов к росту, нечувствительность к сигналам прекращения роста, отключение апоптоза, неограниченный репликативный потенциал, постоянный ангиогенез, врастание опухолей и образование метастазов, а также неустойчивость генома (Hanahan and Weinberg, 2000. The Hallmarks of Cancer. Cell 100, 57-70).
Как правило, раковые заболевания подразделяются на гематологические виды рака (например, лейкозы и лимфомы) и солидные виды рака, например, саркомы и карциномы (например раковые заболевания мозга, груди, легких, ободочной кишки, желудка, печени, поджелудочной железы, простаты, яичников).
Ингибиторы JAK по настоящему изобретению могут также найти применение при лечении некоторых злокачественных заболеваний, включая рак кожи и гематологические злокачественные заболевания, такие как лимфомы и лейкемии.
В частности, ожидается, что на лечение ингибиторами JAK3 будут реагировать разновидности рака, при которых активирован путь передачи сигнала JAK-STAT, например, за счет активации JAK3. Примерами раковых заболеваний, включающих JAK3 мутации являются острый мегакариобластный лейкоз (AMKL) (Walters et al., 2006. Cancer Cell 10(1):65-75) и рак груди (Jeong et al., 2008, Clin.Cancer Res. 14, 3716-3721).
Пролиферативные заболевания или расстройства включают группу заболеваний, характеризующихся усиленным размножением клеток, которое наблюдается при миелопролиферативных расстройствах (MPD), например, при истинной полицитемии (PV).
Еще один аспект настоящего изобретения относится к применению соединения по настоящему изобретению, его фармацевтически приемлемой соли или изотопного производного для получения лекарственного средства, предназначенного для лечения или профилактики заболеваний и расстройств, связанных с JAK.
Следующий аспект настоящего изобретения относится к применению соединения по настоящему изобретению, его фармацевтически приемлемой соли или изотопного производного для получения лекарственного средства, предназначенного для лечения или профилактики иммунологических, воспалительных, аутоиммунных или аллергических расстройств или заболеваний, или отторжения трансплантата, или реакции «трансплантат против хозяина».
Другой аспект настоящего изобретения относится к применению соединения по настоящему изобретению, его фармацевтически приемлемой соли или изотопного производного для получения лекарственного средства, предназначенного для лечения или профилактики пролиферативного заболевания, в частности рака.
В контексте этих применений настоящего изобретения, заболевания и расстройства, связанные с JAK, включают перечисленные выше заболевания и расстройства.
Следующий аспект настоящего изобретения относится к способу лечения, регулирования, отсрочки наступления или профилактики у пациента из числа млекопитающих, у которого имеется такая необходимость, одного или нескольких состояний, выбранных из группы, состоящей из заболеваний и расстройств, связанных с JAK, где этот способ включает введение указанному пациенту терапевтически эффективного количества соединения по настоящему изобретению, его фармацевтически приемлемой соли или изотопного производного.
Еще один аспект настоящего изобретения относится к способу лечения, регулирования, отсрочки наступления или профилактики у пациента из числа млекопитающих, у которого имеется такая необходимость, одного или нескольких состояний, выбранных из группы, состоящей из иммунологических, воспалительных, аутоиммунных или аллергических расстройств или заболеваний, или отторжения трансплантата или реакции «трансплантат против хозяина», где этот способ включает введение указанному пациенту терапевтически эффективного количества соединения по настоящему изобретению или его фармацевтически приемлемой соли, или изотопного производного.
Другой аспект настоящего изобретения относится к способу лечения, регулирования, отсрочки наступления или профилактики у пациента из числа млекопитающих, у которого имеется такая необходимость, пролиферативного заболевания, в частности, рака, где этот способ включает введение указанному пациенту терапевтически эффективного количества соединения по настоящему изобретению, его фармацевтически приемлемой соли или изотопного производного.
В контексте этих способов по настоящему изобретению, заболевания и расстройства, связанные с JAK, включают перечисленные выше заболевания и расстройства.
Имеется в виду, что в настоящем изобретении термин «лечение», относится ко всем способам, которые способны замедлить, прервать, прекратить или остановить прогрессирование заболевания, но необязательно полностью устранить все его симптомы.
Все обсуждавшиеся выше варианты осуществления, относящиеся к фармацевтической композиции по настоящему изобретению, также относятся к первому или второму медицинскому применению или способам по настоящему изобретению.
Общие способы получения соединений по настоящему изобретению известны в технике (например, из WO 2006/117560 A1). В помещенном ниже экспериментальном разделе описаны методики получения, которые также можно применять в аналогичных способах, используя приемы, известные специалисту в данной области техники, в частности, методики защиты реакционноспособных функциональных групп или активации функциональных групп.
Аналитические методики
ЖХМС проводили на приборе Agilent 1100, UPLCMS (сверхэффективную ЖХМС) проводили на приборе Waters UPBINARY, используя воду и ACN (0,1% муравьиной кислоты для низких значений pH, 0,1% аммиака для высоких значений pH) при объеме впрыска 3 мкл. Детектирование осуществляли на длине волны 254 и 210 нм.
Методика A: UPLC низкие значения pH
Методика B: UPLC высокие значения pH
Колонка: Waters Acquity UPLC BEH C18, 30×2,1 мм, 1,7 мм, скорость потока 0,5 мл/мин
Методика C: ЖХМС низкие значения pH
Методика D: ЖХМС высокие значения pH
Колонка: Phenomenex Gemini-C18, 3×30 мм, 3 микрона, скорость потока 1,2 мл/мин
Методика E: ЖХМС низкие значения pH 16 минут
Колонка: Phenomenex Gemini-C18, 4,6×150 мм, 5 микронов, скорость потока 1,0 мл/мин, низкие значения pH
Методика F: UPLC, высокие значения pH, 6 минут
Колонка: Waters Acquity UPLC BEH C18, 2,1×50 мм, 1,7 микрона, скорость потока 0,5 мл/мин, низкие значения pH
Экспериментальная часть
Краткое описание типовых примеров путей синтеза соединений по настоящему изобретении приведено ниже на схемах A1-A4.
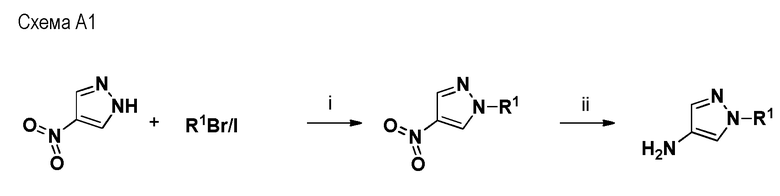
Условия: стадия i) K2CO3, ACN 60°C; стадия ii) 10% Pd/C, H2, MeOH.
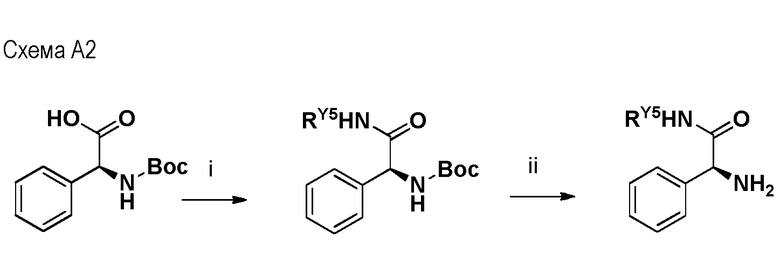
Условия: стадия i) RY5NH2, HATU, DIPEA, ДМФА; стадия ii) TFA, DCM.
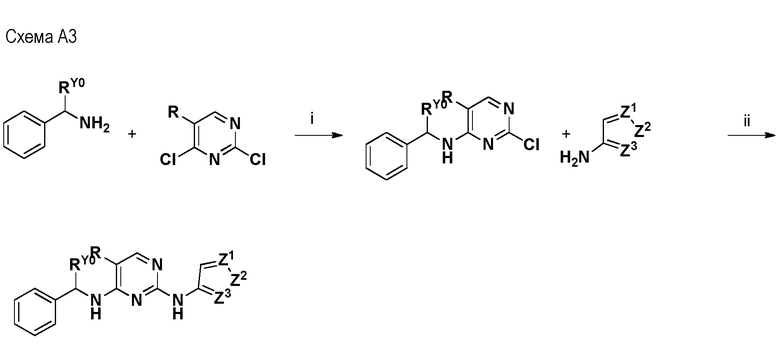
Условия: стадия i) IPA, DIPEA, время удерживания 24 ч; стадия ii) IPA, HCl, 80°C, 24 ч;
Соединения, у которых в формуле (I) n=1 можно получать аналогичным образом.
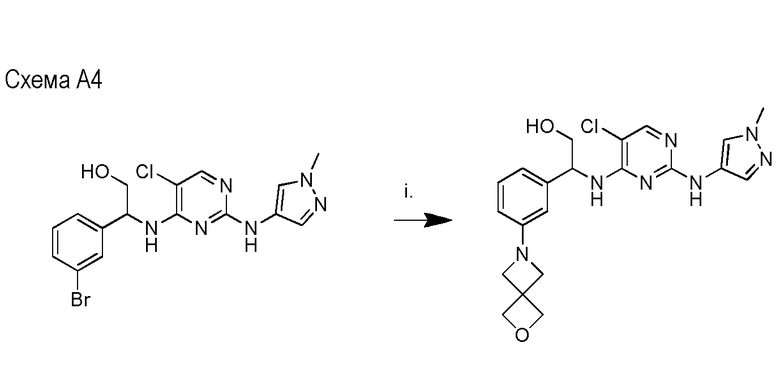
Условия: стадия i) Pd2(dba)3, Xantphos, Cs2CO3, Спироморфолин, 1,4-диоксан;
Общая методика синтеза 4-амино-1-N-алкилированных пиразолов
Схема A1, стадия 1
Раствор 4-нитропиразола (1,0 экв.), карбоната калия (2,0 экв.) и алкилирующего реагента (1,1 экв.) в ацетонитриле (10 объемов) нагревали при 60°C в течение 18 ч. После охлаждения до комнатной температуры, смесь разбавляли EtOAc и промывали водой. Органическую фазу собирали, сушили (MgSO4) и концентрировали в вакууме.
Стадия 2
Неочищенный остаток нитросоединения растворяли в метаноле (50 объемов), добавляли палладий на угле (10 масс.%) и перемешивали реакционную смесь в атмосфере H2 в течение 18 ч. Полученную смесь фильтровали через целит и фильтрат концентрировали в вакууме, получая желаемый продукт.
Общая методика получения амид-замещенных бензиламинов
Схема А2, стадия 1
При перемешивании к раствору N-(трет-бутоксикарбонил)-L-2-фенилглицина (1 экв.) в ДМФА (2 мл) добавляли соответствующий амин (1,1 экв.), HATU (1,3 экв.) и DIPEA (2 экв.). Затем реакционную смесь перемешивали в течение 1 ч при комнатной температуре. Реакционную смесь разбавляли DCM, промывали водой, сушили с помощью гидрофобной фритты и концентрировали в вакууме. Флэш-хроматография на обращенной фазе (30 г колонка C18, 5%-95% ACN с муравьиной кислотой в воде с муравьиной кислотой) позволяла получить желаемый амид.
Схема A2, стадия 2
BOC-аминометиламид перемешивали в течение 1 ч при комнатной температуре в TFA/DCM (1:4). Реакционную смесь переносили на картридж SPE с толуолсульфоновой кислотой и после промывания элюировали продукт 2н аммиаком в метаноле. Органические растворители удаляли в вакууме, получая желаемый продукт.
Схема A3, стадия 1
Общая методика синтеза промежуточных N-(2-хлор-5-фторпиримидин-4-ил)бензиламинов
К раствору 2,4-дихлор-5-фторпиримидина (1,0 экв.) и DIPEA (2,0 экв.) в пропан-2-оле (10 объемов) при 0°C по каплям добавляли замещенный бензиламин (1,0 экв.), и полученную смесь перемешивали в течение ночи при комнатной температуре. Затем реакционную смесь разбавляли EtOAc (20 объемов), водой (20 объемов) и насыщенным раствором соли (10 объемов). Органический слой собирали, сушили (MgSO4) и концентрировали при пониженном давлении.
Общая методика синтеза промежуточных N-(2-хлор-5-хлорпиримидин-4-ил)бензиламинов
К раствору 2,4,5-трихлорпиримидина (1,0 экв.) и DIPEA (2,0 экв.) в пропан-2-оле (10 объемов) при 0°C по каплям добавляли замещенный бензиламин (1,0 экв.), и полученную смесь перемешивали в течение ночи при комнатной температуре. Затем реакционную смесь разбавляли EtOAc (20 объемов), водой (20 объемов) и насыщенным раствором соли (10 объемов). Органический слой отделяли, сушили (MgSO4), концентрировали при пониженном давлении, получая желаемый продукт.
Общая методика синтеза промежуточных N-(2-хлор-5-метилпиримидин-4-ил)бензиламинов
К раствору 2,4-дихлор-5-метилпиримидина (1,0 экв.) и DIPEA (2,0 экв.) в пропан-2-оле (10 объемов) при 0°C по каплям добавляли замещенный бензиламин (1,0 экв.), и полученную смесь перемешивали в течение ночи при комнатной температуре. Затем реакционную смесь разбавляли EtOAc (20 объемов), водой (20 объемов) и насыщенным раствором соли (10 объемов). Органический слой отделяли, сушили (MgSO4), концентрировали при пониженном давлении, получая желаемый продукт.
Общие методики синтеза тестовых соединений
Схема A3, стадия 2
Смесь N-(2-хлор-5-хлорпиримидин-4-ил)бензиламина, замещенного 1H-пиразол-4-амина (1,0 экв.) и 4 М HCl в диоксане (0,1 экв.) перемешивали при 80°C в течение 18 ч в пропан-2-оле (5 объемов). Затем реакционную смесь разбавляли EtOAc (20 объемов) и NaHCO3 (10 объемов), органическую фазу отделяли, сушили (MgSO4) и упаривали, получая желаемый продукт. Затем полученные продукты при необходимости очищали флэш-хроматографией (EtOAc/петролейный эфир) или ВЭЖХ.
Общая методика получения аминозамещенных тестовых соединений
Схема A4
Суспензию арилбромида (1,0 экв.), спироморфолина (1,5 экв.), Pd2(dba)3 (0,01 экв.), XANTPHOS (0,05 экв.) и карбоната цезия (3,0 экв.) кипятили с обратным холодильником в дегазированном 1,4-диоксане (10 объемов) в течение ночи. Смесь охлаждали и фильтровали, фильтрат пропускали через PS-SH картридж и удаляли растворитель в вакууме. Очистку можно проводить хроматографией на обращенной фазе.
Ниже приведено более подробное описание типовых путей синтеза соединений по настоящему изобретению.
Общая методика синтеза 4-амино-1-N-алкилированных пиразолов 1.3.
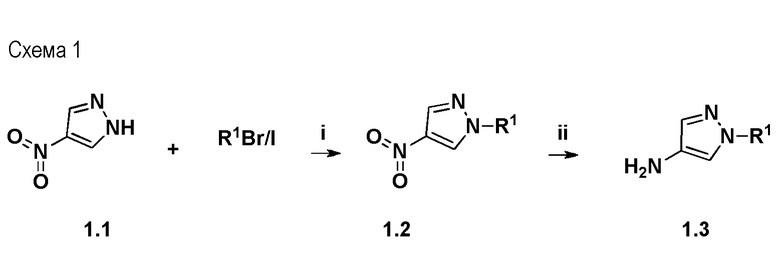
Условия: стадия i) K2CO3, ACN, 60°C, 18 ч; стадия ii) 10% Pd/C, H2, MeOH, время удерживания 18 ч.
Стадия 1
Раствор 4-нитропиразола (1,0 экв.), карбоната калия (2,0 экв.) и алкилирующего реагента (1,1 экв.) в ACN (10 объемов) нагревали при 60°C в течение 18 часов. После охлаждения до комнатной температуры, смесь разбавляли EtOAc и промывали водой. Органическую фазу отделяли, сушили (MgSO4) и концентрировали в вакууме.
Стадия 2
Алкилированный нитропиразол 1.2 растворяли в MeOH (50 объемов), добавляли палладий на угле (10 масс.%) и перемешивали реакционную смесь в атмосфере H2 в течение 18 ч. Полученную смесь фильтровали через целит и концентрировали фильтрат в вакууме, получая желаемый продукт.
Общая методика получения амидозамещенных бензиламинов 2.3.
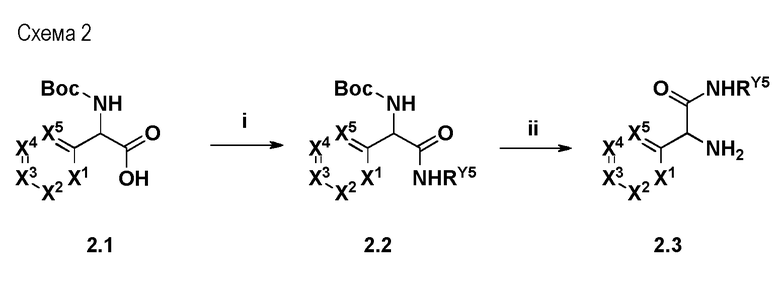
Условия: стадия i) RY5NH2, HATU, DIPEA, ДМФА, время удерживания 1 ч; стадия ii) TFA, DCM, 1 ч.
Стадия 1
К раствору соединения 2.1 (1,0 экв.) в ДМФА (2 мл) при перемешивании добавляли соответствующий амин RY5NH2 (1,1 экв.), HATU (1,3 экв.) и DIPEA (2,0 экв.). Затем реакционную смесь перемешивали в течение 1 ч при комнатной температуре. Реакционную смесь разбавляли DCM и промывали водой, сушили, используя гидрофобную фритту, и концентрировали в вакууме. Флэш-хроматография на обращенной фазе (30 г, колонка C18, 5-95% ACN с муравьиной кислотой в воде с муравьиной кислотой) позволяла получить желаемый амид 2.2.
Стадия 2
Амид 2.2 перемешивали в течение 1 ч при комнатной температуре в смеси TFA/DCM (1:4). Реакционныую смесь наносили на картридж SPE с толуолсульфоновой кислотой и, после промывания MeOH, элюировали продукт 2н. аммиаком в MeOH. Органические растворители удаляли в вакууме, получая желаемый продукт 2.3.
Общая методика получения морфолин-замещенных бензиламинов 3.2
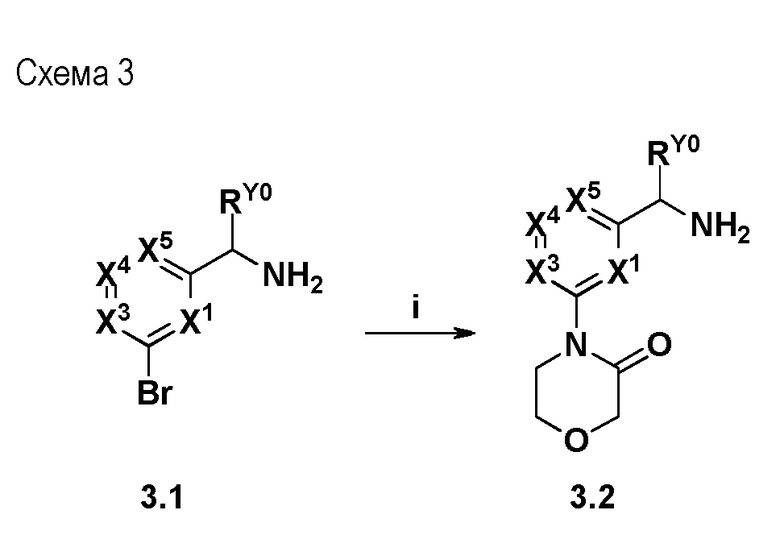
Условия: стадия i) CuI, морфолин-3-он, N,N'-диметилэтилен диамин, K2CO3, 1,4-диоксан.
Арилбромид 3.1 (1,0 экв.), морфолин-3-он (1,25 экв.), CuI (0,2 экв.), N,N'-диметилэтилендиамин (0,4 экв.) и K2CO3 (2,0 экв.) нагревали до 110°C в диоксане в течение 18 ч. Реакционную смесь охлаждали, разбавляли водой и EtOAc. Органический слой промывали (вода, насыщенный раствор соли), сушили (MgSO4) и концентрировали, получая соединение 3.2.
Общая методика синтеза интермедиатов 4.3.
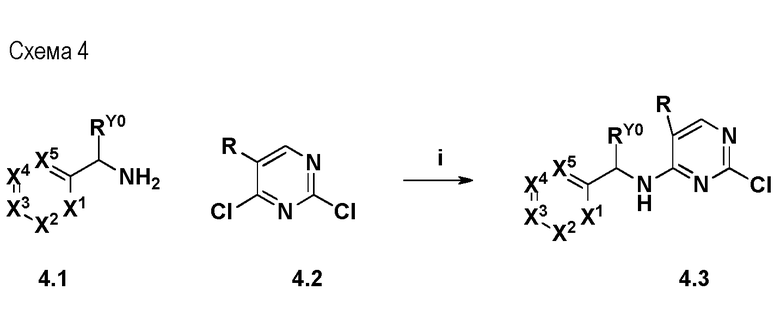
Условия: стадии i) IPA, DIPEA, время удерживания 18 ч.
К раствору 2,4-дихлор-5-замещенного пиримидина 4.2 (1,0 экв.) и DIPEA (2,0 экв.) в IPA (10 объемов) при 0°C по каплям добавляли альфа-замещенный бензиламин 4.1 (1,0 экв.) и полученную смесь перемешивали в течение ночи при комнатной температуре. Реакционную смесь разбавляли либо водой, собирая полученный осадок соединения 4.3 фильтрованием, либо EtOAc (20 объемов), водой (20 объемов) и насыщенным раствором соли (10 объемов). Органический слой отделяли, сушили (MgSO4) и концентрировали при пониженном давлении, получая соединение 4.3. При необходимости проводили очистку флэш-хроматографией на силикагеле (градиент EtOAc-петролейный эфир).
Альтернативная методика получения амидозамещенных интермедиатов 5.4
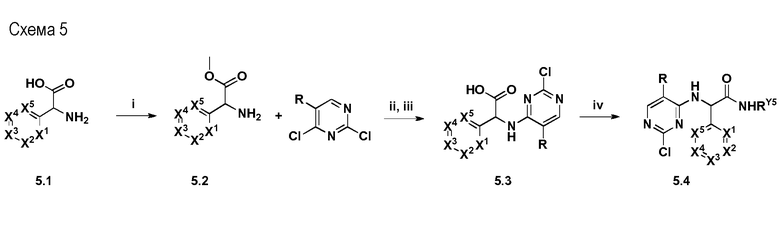
Условия: стадия i) AcCl, MeOH, 80°C; стадия ii) DIPEA, IPA, кт, 24 ч; стадия iii) 1 М LiOH, MeOH, время удерживания 24 ч; стадия iv) RY5NH2, HATU, DIPEA, ДМФА
Стадия 1
К раствору аминокислоты 5.1 (1,0 экв.) в MeOH (2 мл) при перемешивании добавляли ацетилхлорид (2,0 экв.). Реакционную смесь перемешивали в течение 15 мин при комнатной температуре и затем при 80°C в течение ночи. Реакционную смесь концентрировали в вакууме, остаток нейтрализовали насыщенным раствором NaHCO3 и экстрагировали EtOAc, получая аминоэфир 5.2.
Стадия 2
Аминоэфир 5.2 (1,2 экв.) при перемешивании добавляли к охлажденному (0°C) раствору 2,4-дихлор-5-замещенного пиримидина (1,0 экв.) и DIPEA (2,5 экв.) в IPA. Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение ночи. Реакционную смесь разбавляли водой и EtOAc. Органический слой промывали (насыщенным раствором соли), сушили (MgSO4) и концентрировали в вакууме, получая остаток, который использовали без дополнительной очистки.
Стадия 3
Остаток стадии 2 растворяли в MeOH и обрабатывали при комнатной температуре 1 М LiOH (3,0 экв.). Реакционную смесь перемешивали в течение ночи при комнатной температуре, затем нейтрализовали 2 М HCl, концентрировали и растирали с эфиром, получая кислоту 5.3 в виде не совсем белого твердого вещества.
Стадия 4
К раствору кислоты 5.3 (1,0 экв.) в ДМФА (2 мл) при перемешивании добавляли соответствующий амин RY5NH2 (1,1 экв.), HATU (1,3 экв.) и DIPEA (2,0 экв.). Затем реакционную смесь перемешивали в течение 1 ч при комнатной температуре. Реакционную смесь концентрировали в вакууме. Флэш-хроматография на обращенной фазе (30 г, колонка C18, 5%-95% ACN с аммиаком в воде с аммиаком) позволяла получить желаемый амид 5.4.
Общая методика синтеза тестовых соединений 6.1
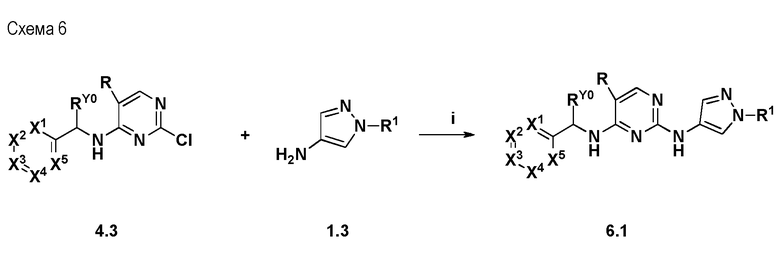
Условия: стадия i) IPA, HCl, 80°C, 18 ч
Смесь 2-хлорпиримидинового интермедиата 4.3 (1,0 экв.), замещенного 1H-пиразол-4-амина 1.3 (1,0 экв.) и 4 М HCl в диоксане (0,1 экв.) перемешивали при 80°C в течение 18 ч в IPA (5 объемов). Затем реакционную смесь разбавляли EtOAc (20 объемов) и NaHCO3 (10 объемов), органическую фазу отделяли, сушили (MgSO4) и концентрировали, получая желаемое тестовое соединение 6.1. которое при необходимости дополнительно очищали флэш-хроматографией (EtOAc/петролейный эфир) или ВЭЖХ.
Общая методика синтеза тестовых соединений 7.2
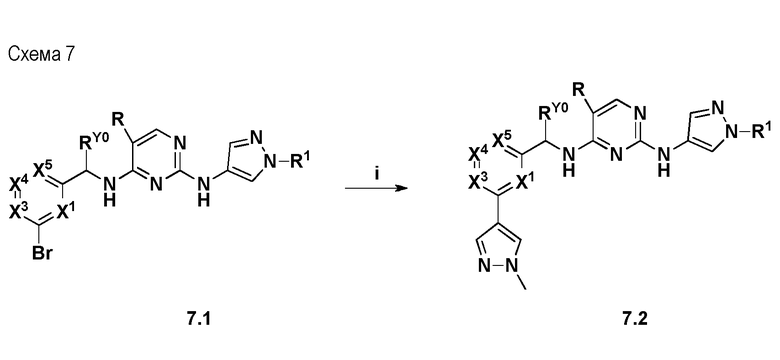
Условия: стадия i) метилпиразолбороновый эфир, Pd(dppf)Cl2, DCM, Na2CO3, ACN/H2O, 120°C, 30 мин
Арилбромид 7.1 (1,0 экв.), пинаколовый эфир 1-метилпиразол-4-бороновой кислоты (1,2 экв.), 2М Na2CO3 (2,0 экв.) и Pd(dppf)Cl2DCM (0,05 экв.) в ACN подвергали действию микроволнового излучения при 130°C в течение 30 минут. Реакционную смесь разбавляли MeOH и фильтровали. Фильтраты концентрировали и очищали препаративной ВЭЖХ, получая соединение 7.2.
Общая методика синтеза тестовых соединений 8.1
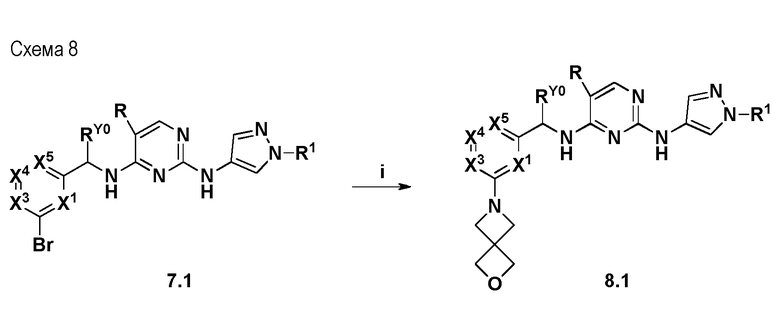
Условия: стадия i) Pd2(dba)3, Xantphos, Cs2CO3, спироморфолин, 1,4-диоксан, 110°C, 18 ч
Суспензию арилбромида 7.1 (1,0 экв.), спироморфолина (1,5 экв.), Pd2(dba)3 (0,01 экв.), XANTPHOS (0,05 экв.) и карбоната цезия (3,0 экв.) кипятили с обратным холодильником в дегазированном 1,4-диоксане (10 объемов) в течение ночи. Полученную смесь охлаждали и фильтровали. Фильтрат пропускали через PS-SH картридж, после чего удаяли растворитель в вакууме. Очистку продукта можно проводить с помощью хроматографии на обращенной фазе, получая тестовое соединение 8.1
Общая методика синтеза тестового соединения 9.2
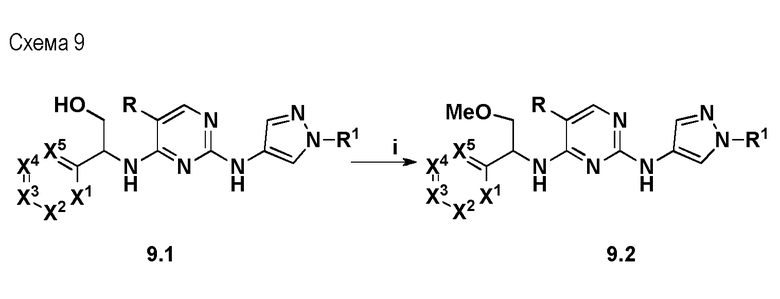
Условия: стадия i) NaH, MeI, ДМФА, кт, 2 ч
К раствору соединения 9.1 (20 мг) в ДМФА (2 мл) добавляли NaH (1,0 экв.) и затем MeI (1,5 экв.). Реакционную смесь перемешивали при комнатной температуре в течение 2 ч, после чего гасили MeOH, концентрировали и очищали препаративной ВЭЖХ, получая тестовое соединение 9.2.
Общая методика синтеза соединения 10.2 и превращения его в амид 10.3
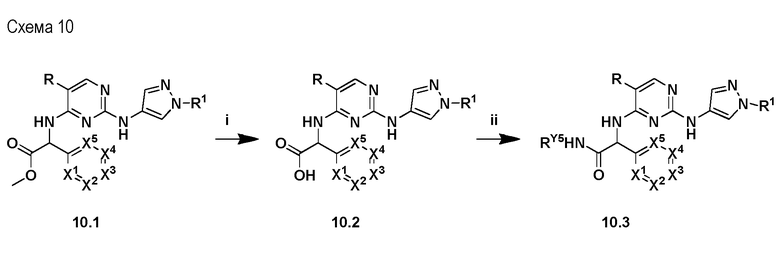
Условия: стадия i) NaOH, MeOH, время удерживания 18 ч; стадия ii) RY5NH2, HATU, DIPEA, ДМФА
Стадия 1
К раствору соединения 10.1 в MeOH добавляли 1 М NaOH (2 экв.). Реакционную смесь перемешивали в течение ночи при комнатной температуре, затем нейтрализовали 2 М HCl, концентрировали и растирали с эфиром, получая кислоту 10.2.
Стадия 2
К раствору 10.2 (1,0 экв.) в ДМФА (2 мл) при перемешивании добавляли соответствующий амин RY5NH2 (1,1 экв.), HATU (1,3 экв.) и DIPEA (2,0 экв.). Затем реакционную смесь перемешивали в течение 1 ч при комнатной температуре. Реакционную смесь разбавляли DCM, промывали (насыщенным раствором соли), сушили (MgSO4) и концентрировали в вакууме. Хроматография на обращенной фазе (30 г, колонка C18, 5%-95% ACN с муравьиной кислотой в воде с муравьиной кислотой) позволяла получить желаемый амид 10.3.
Общая методика синтеза тестовых соединений 11.1
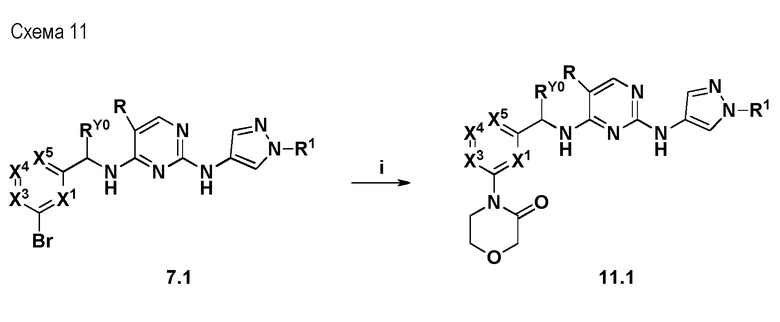
Условия стадии i) CuI, морфолин-3-он, N,N'-диметилендиамин, K2CO3, 1,4-диоксан.
Арилбромид 7.1 (1,0 экв.), морфолин-3-он (1,25 экв.), CuI (0,2 экв.), N,N'-диметилендиамин (0,4 экв.) и K2CO3 (2,0 экв.) нагревали при 110°C в диоксане в течение 18 ч. Реакционную смесь охлаждали, разбавляли водой и EtOAc. Органический слой промывали (водой, насыщенным раствором соли), сушили (MgSO4) и концентрировали, получая соединение 11.1. Очистку проводили хроматографией на обращенной фазе.
Практикующему специалисту в данной области ясно, как объединить или изменить описанные выше методики, в частности в комбинации с осуществлением активации или введением защитных химических групп.
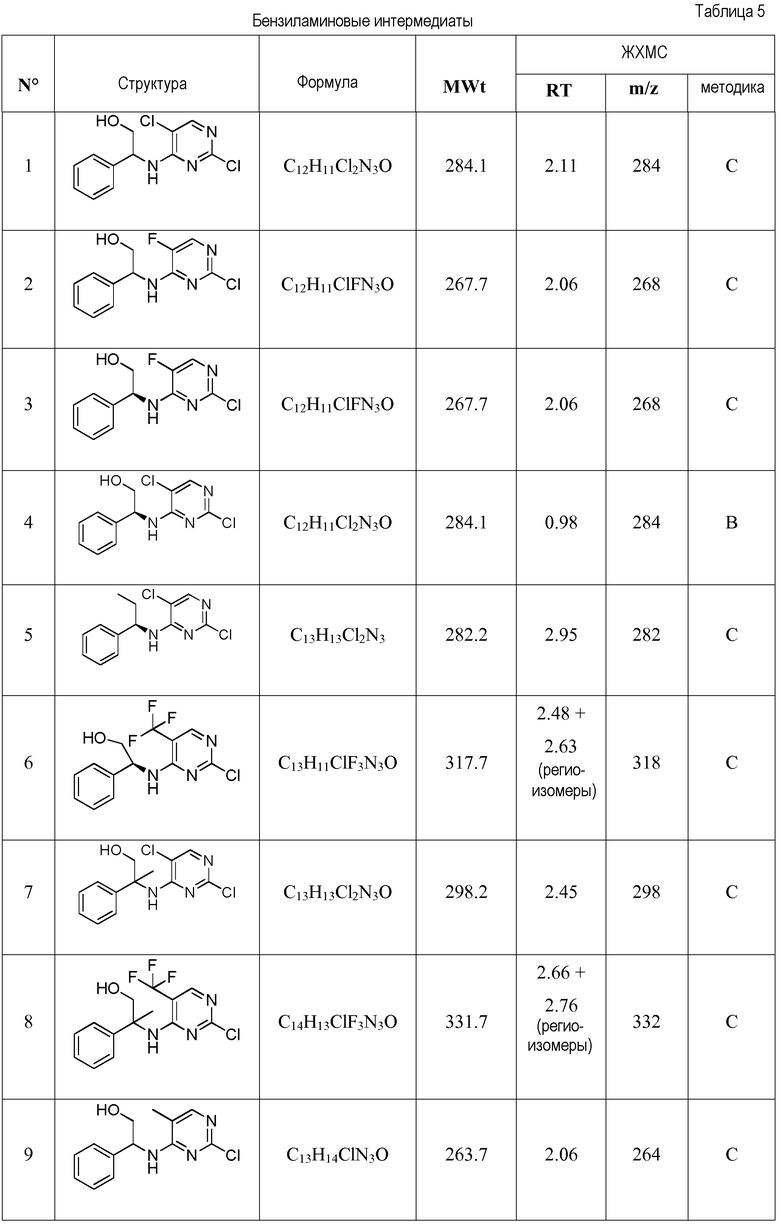
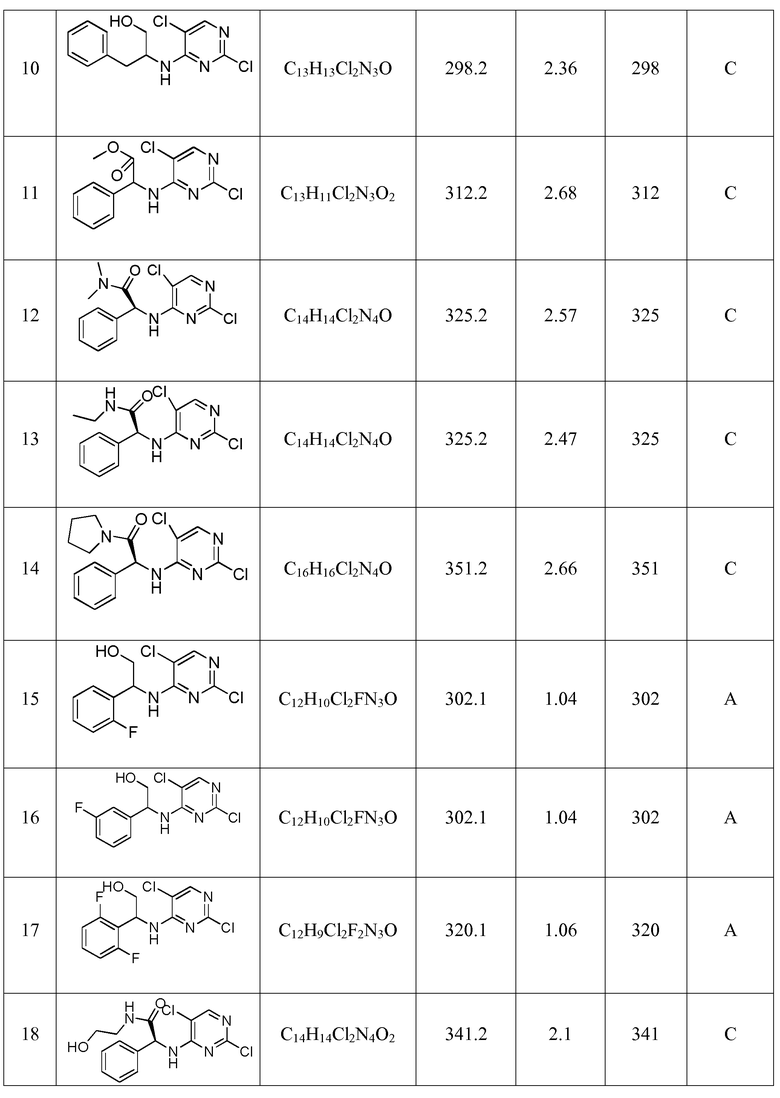
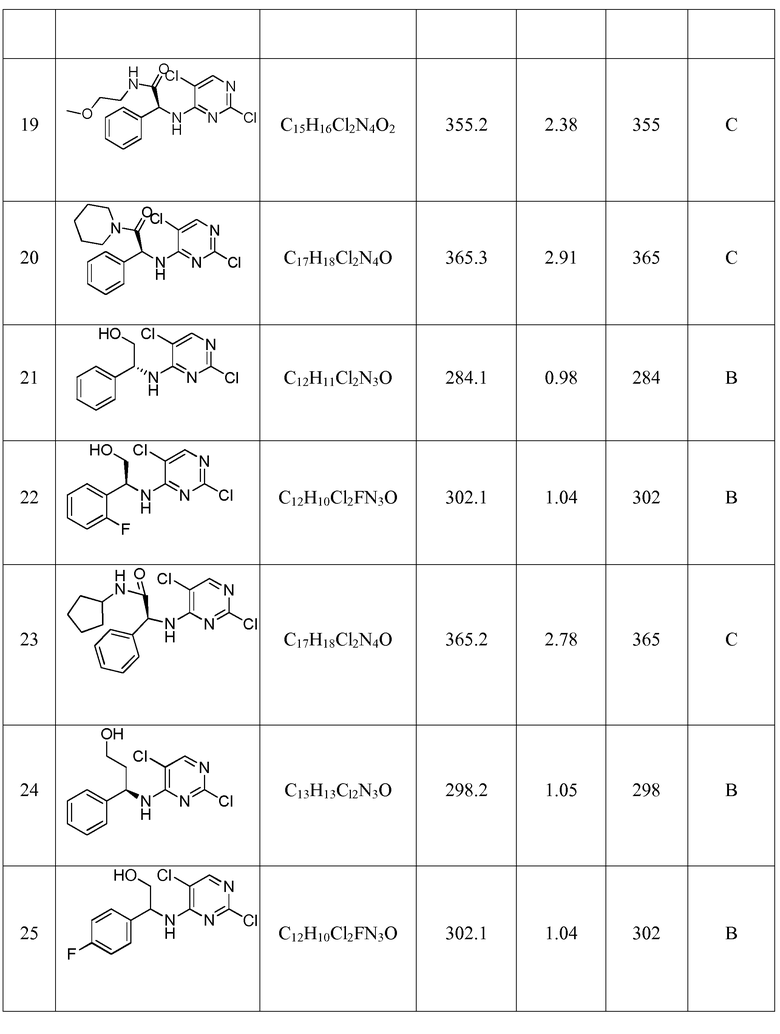
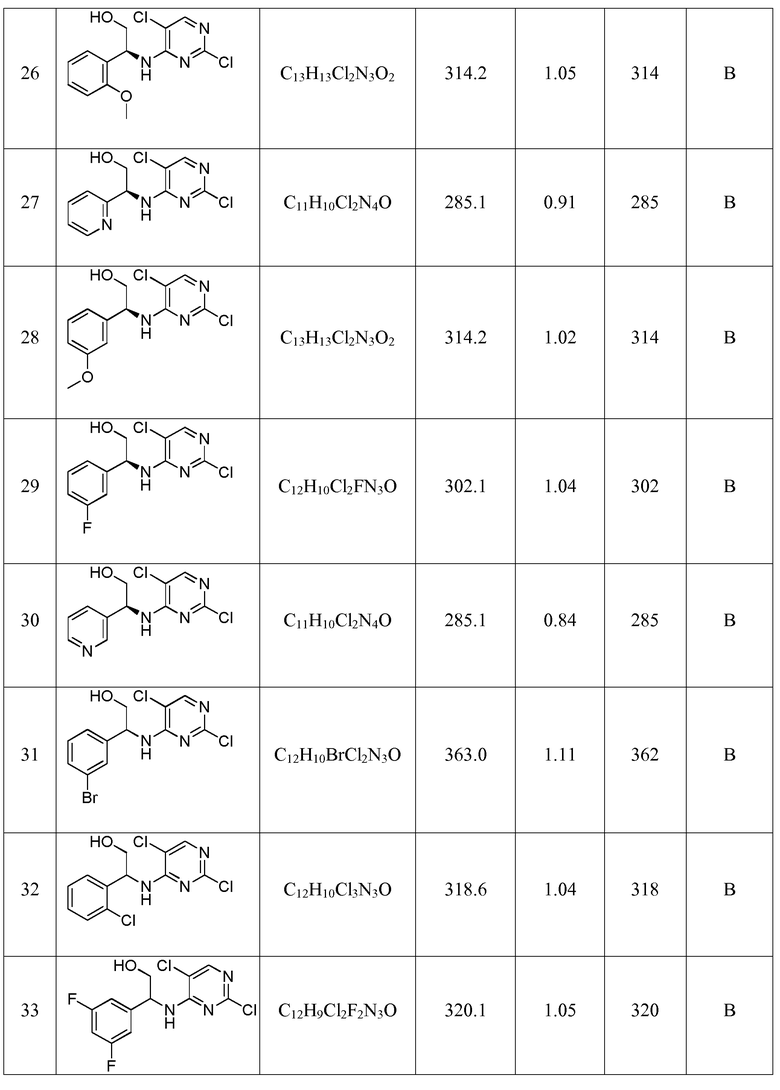
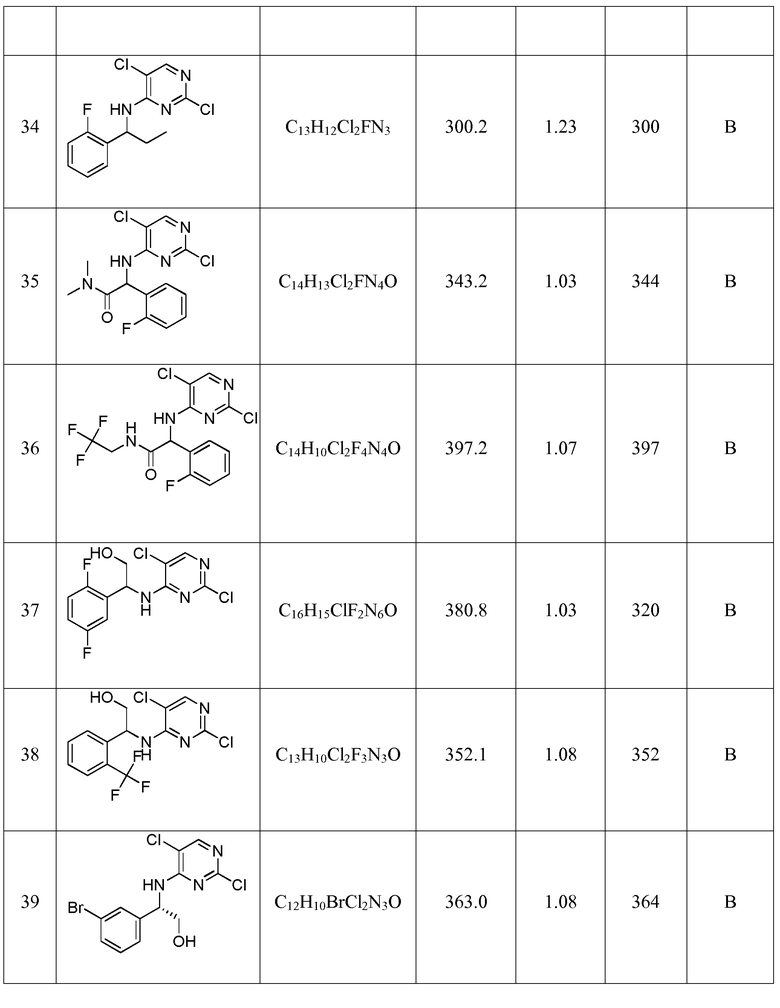
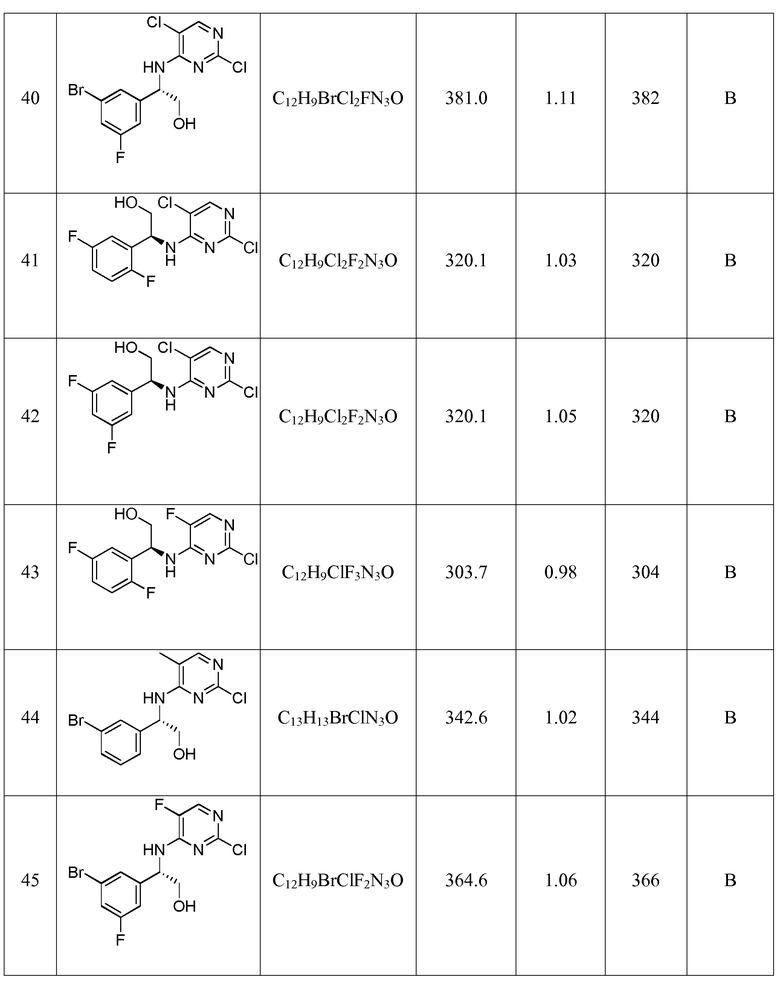
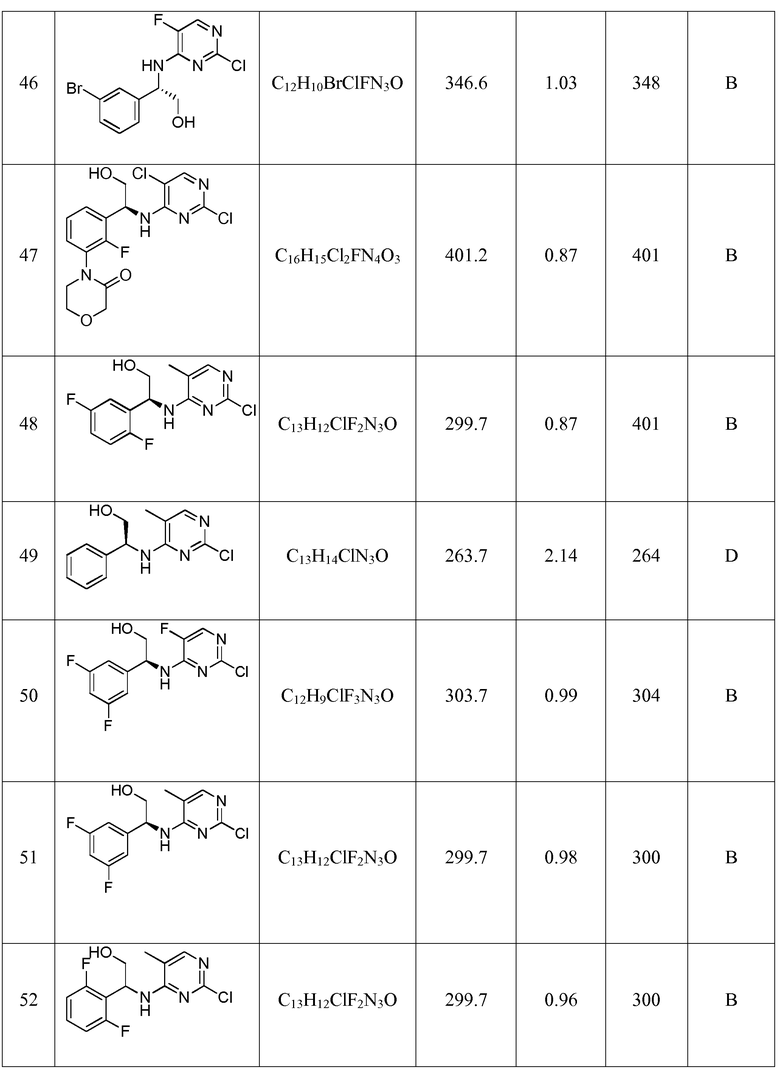
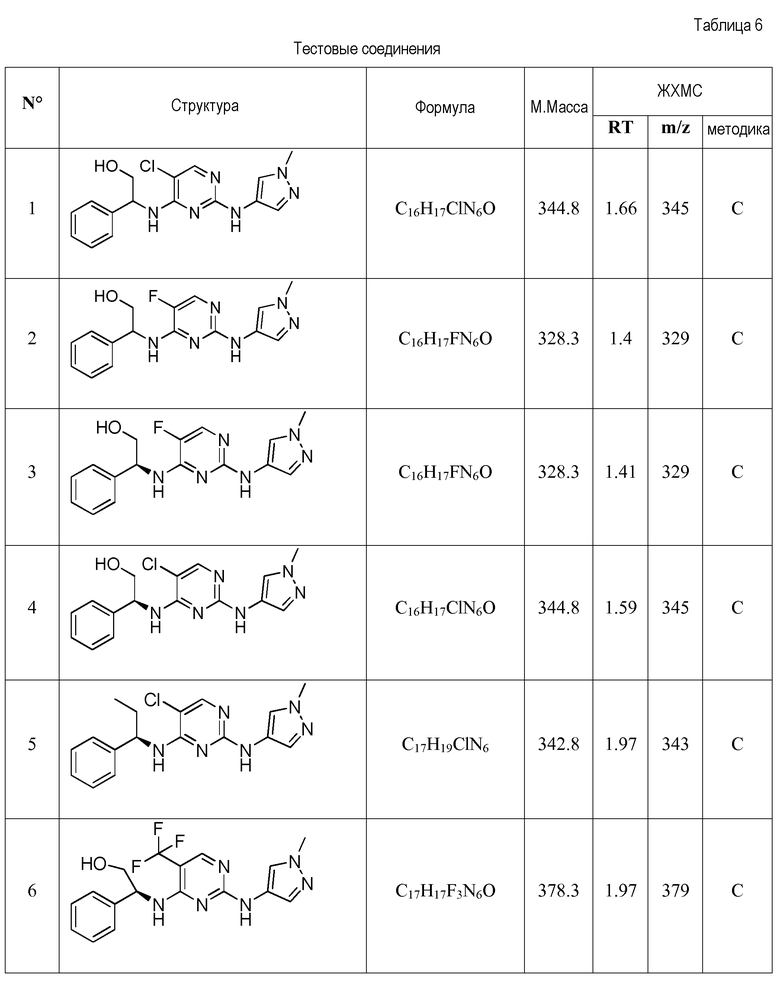
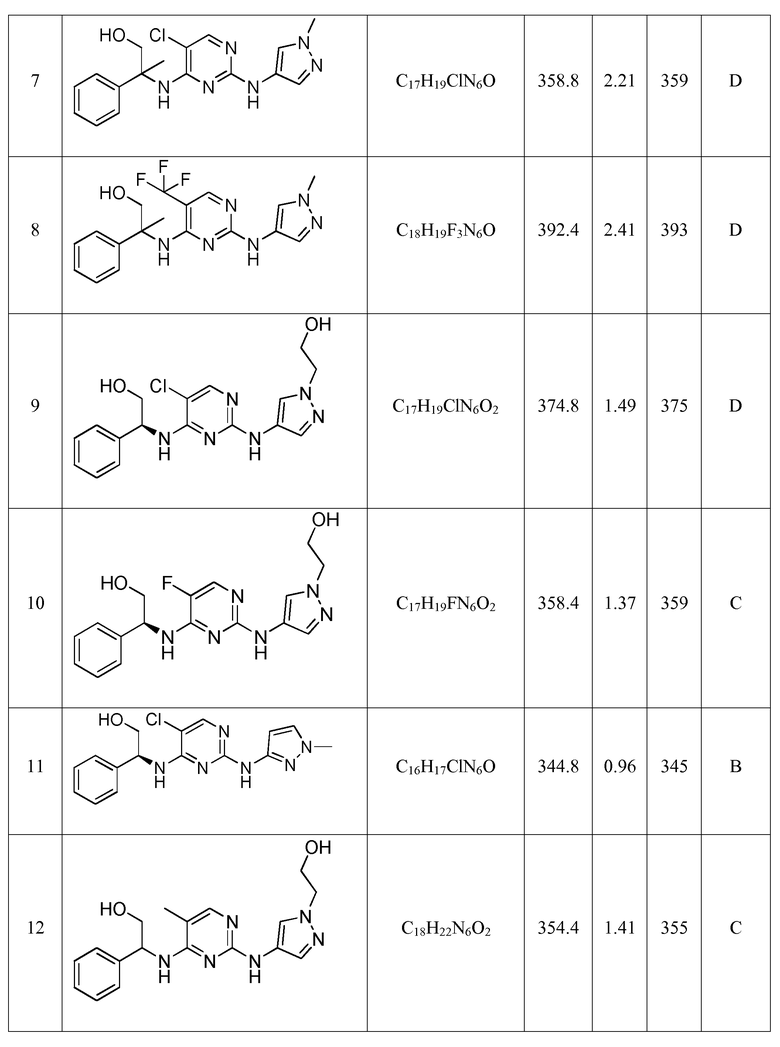
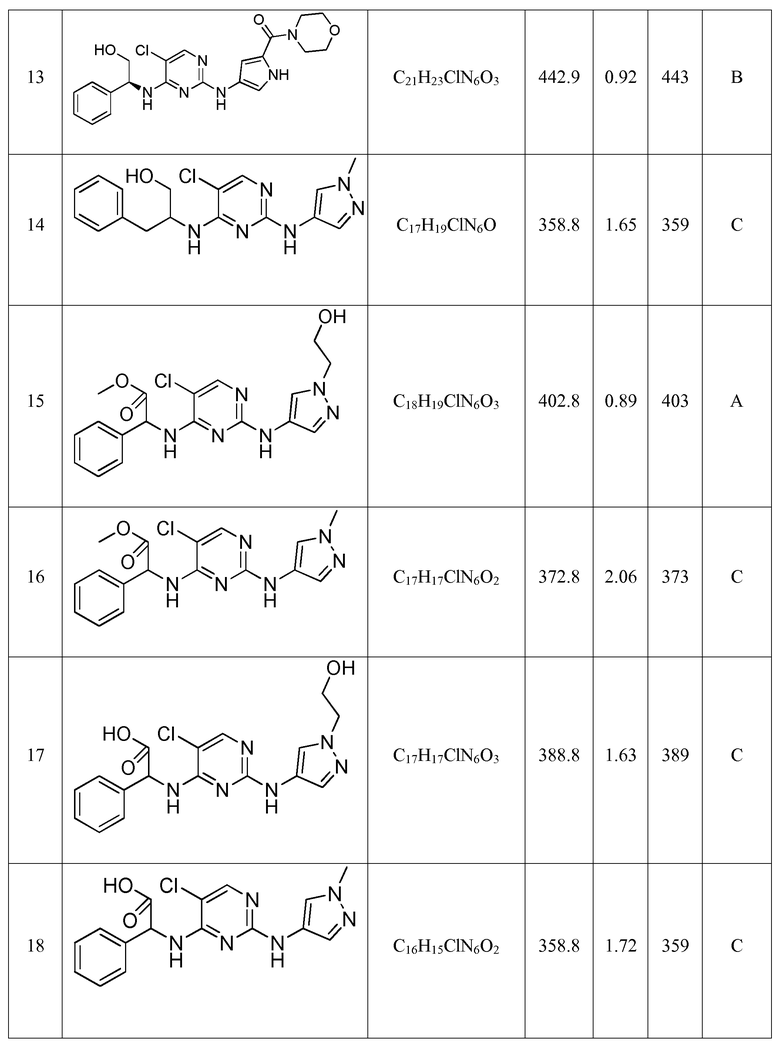
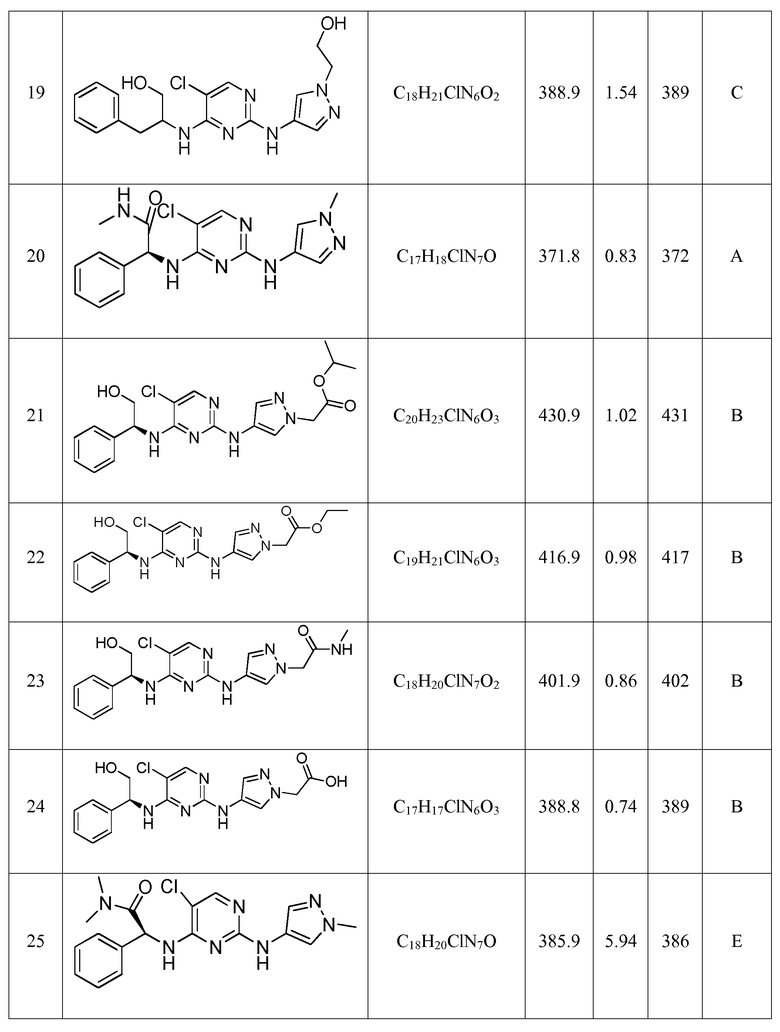
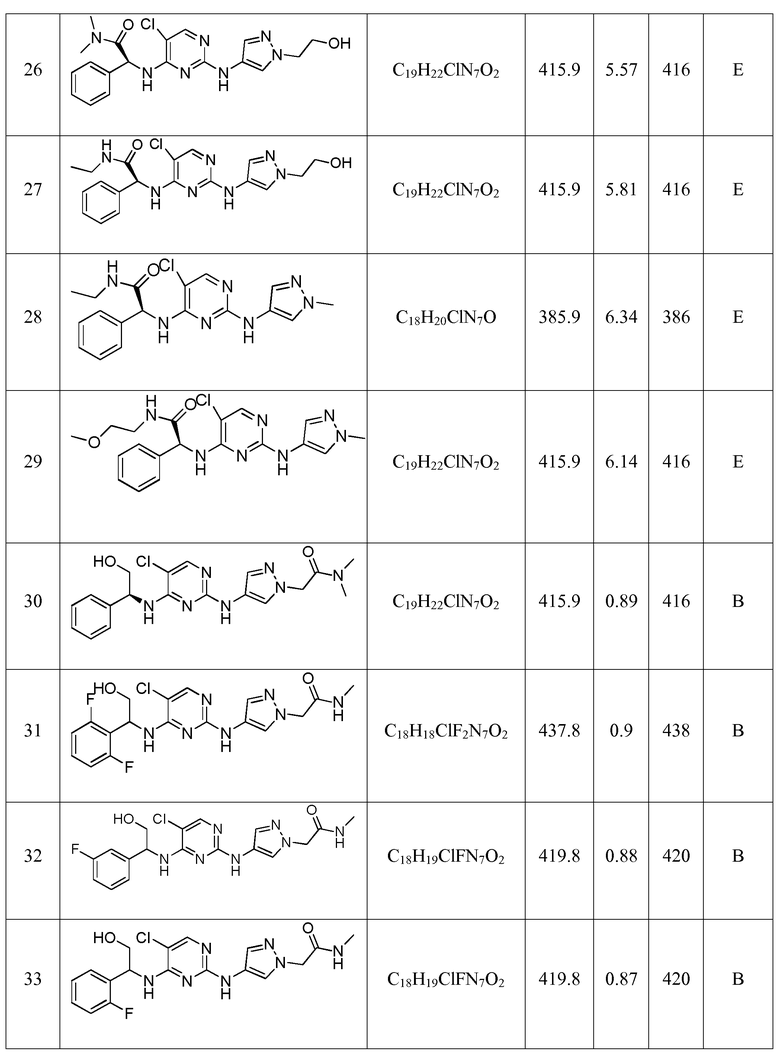
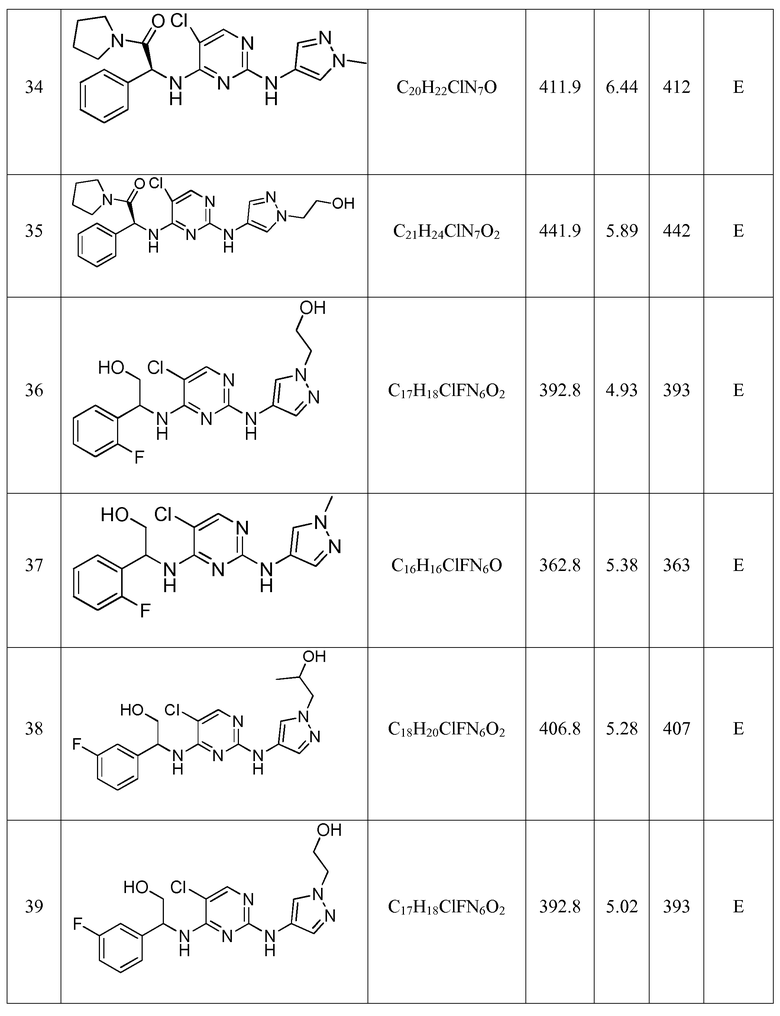
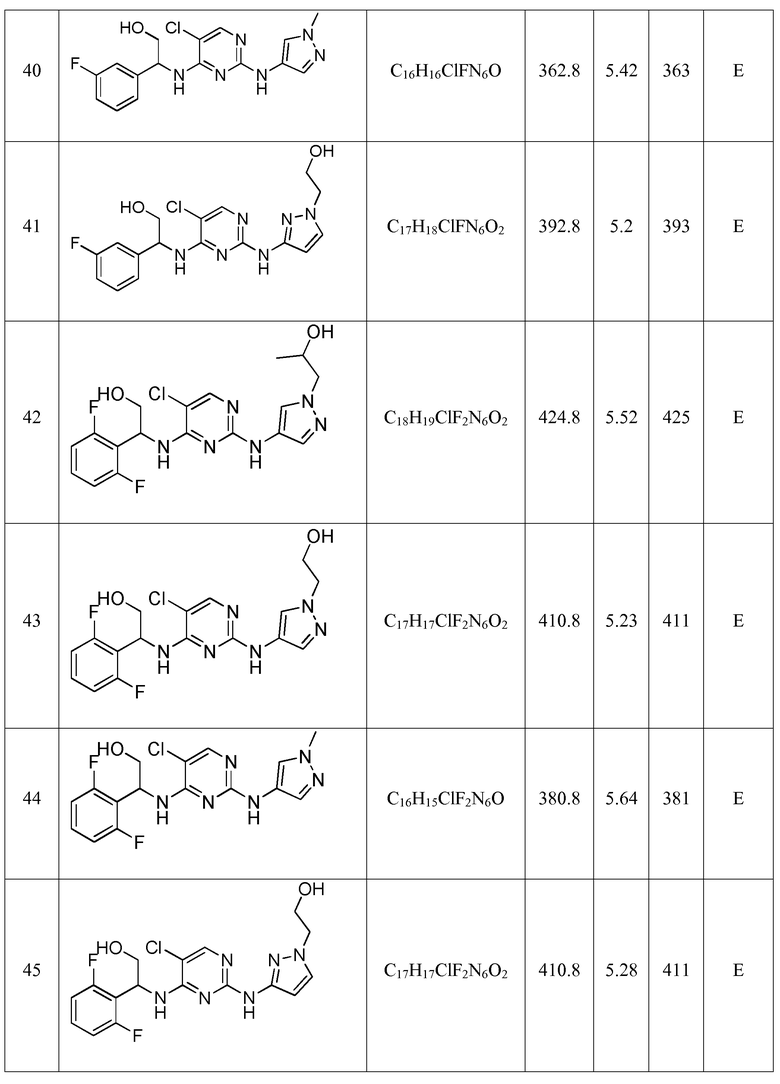
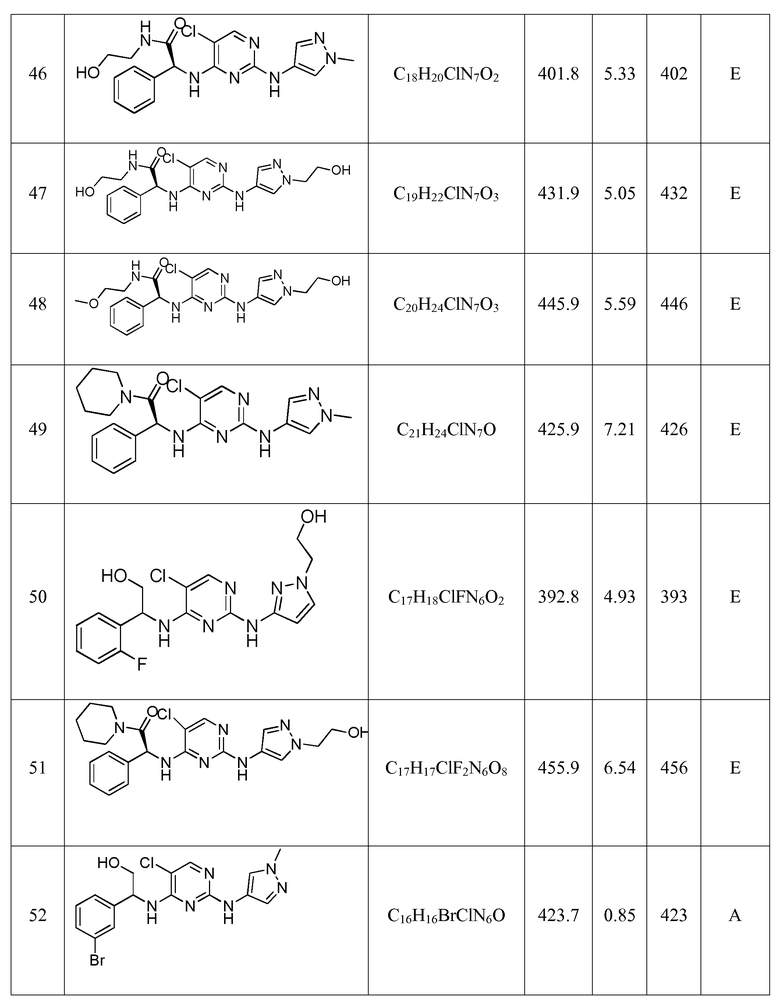
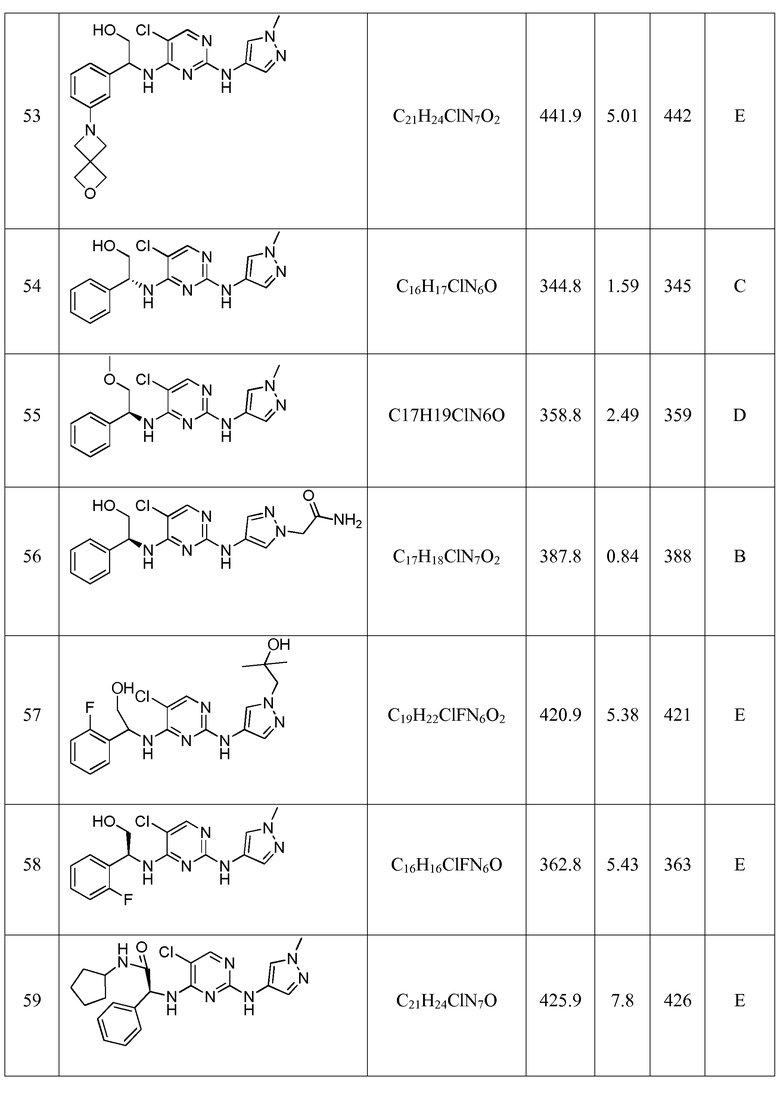
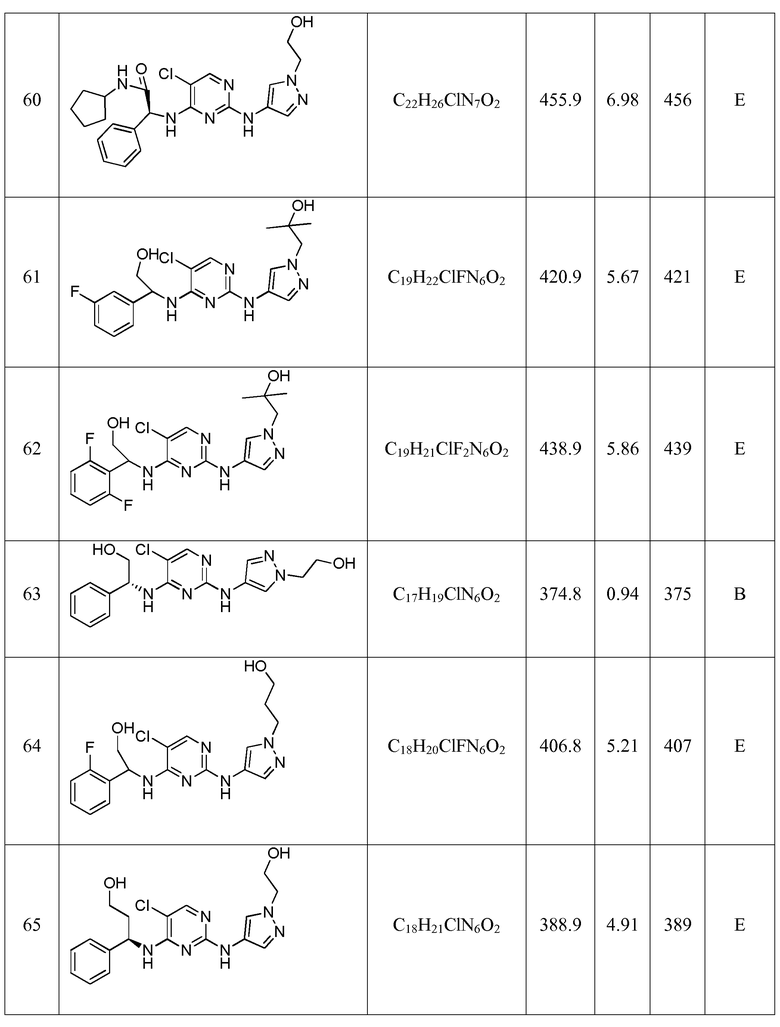
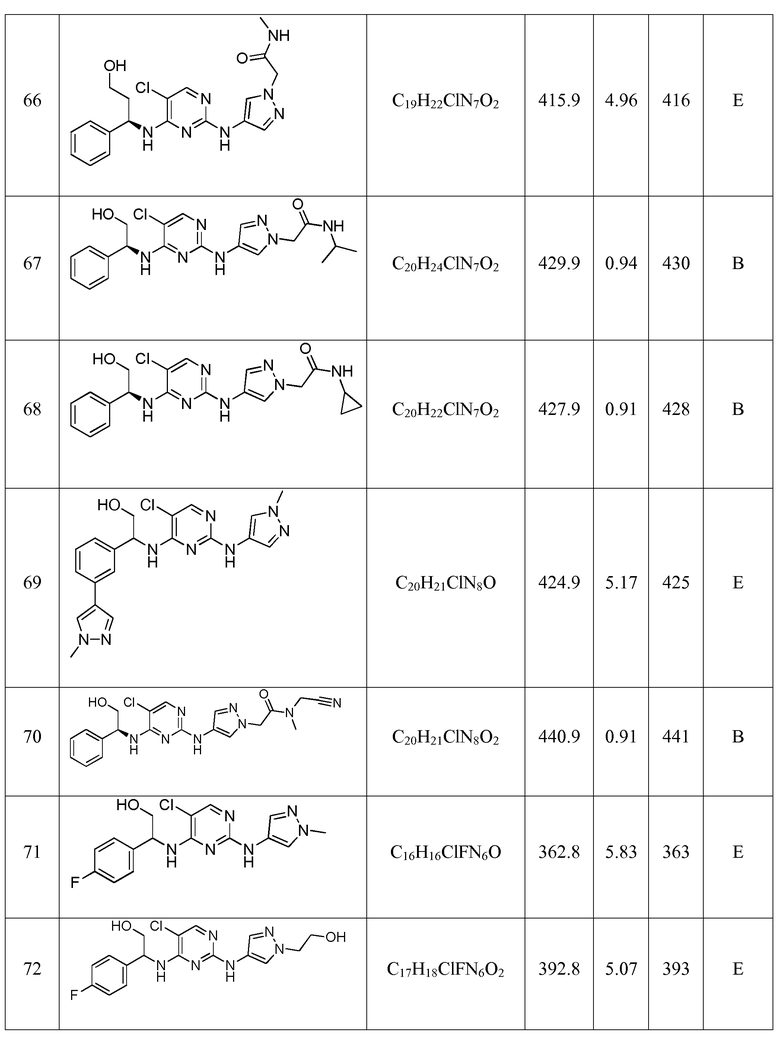
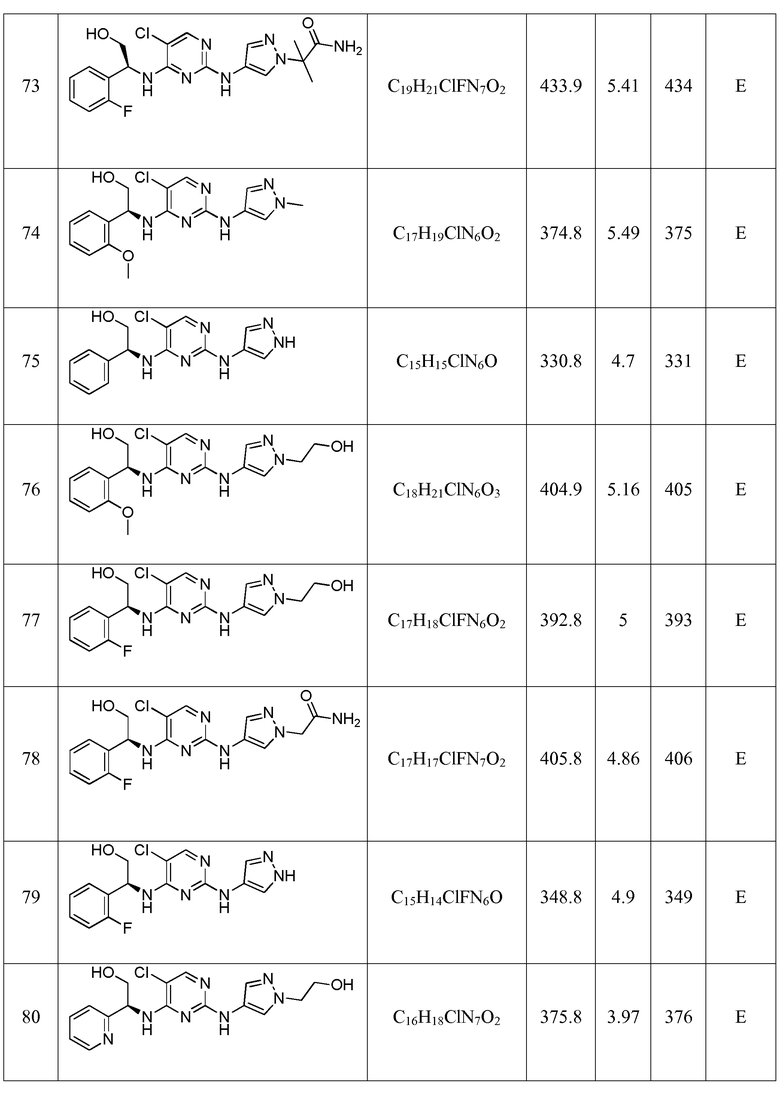
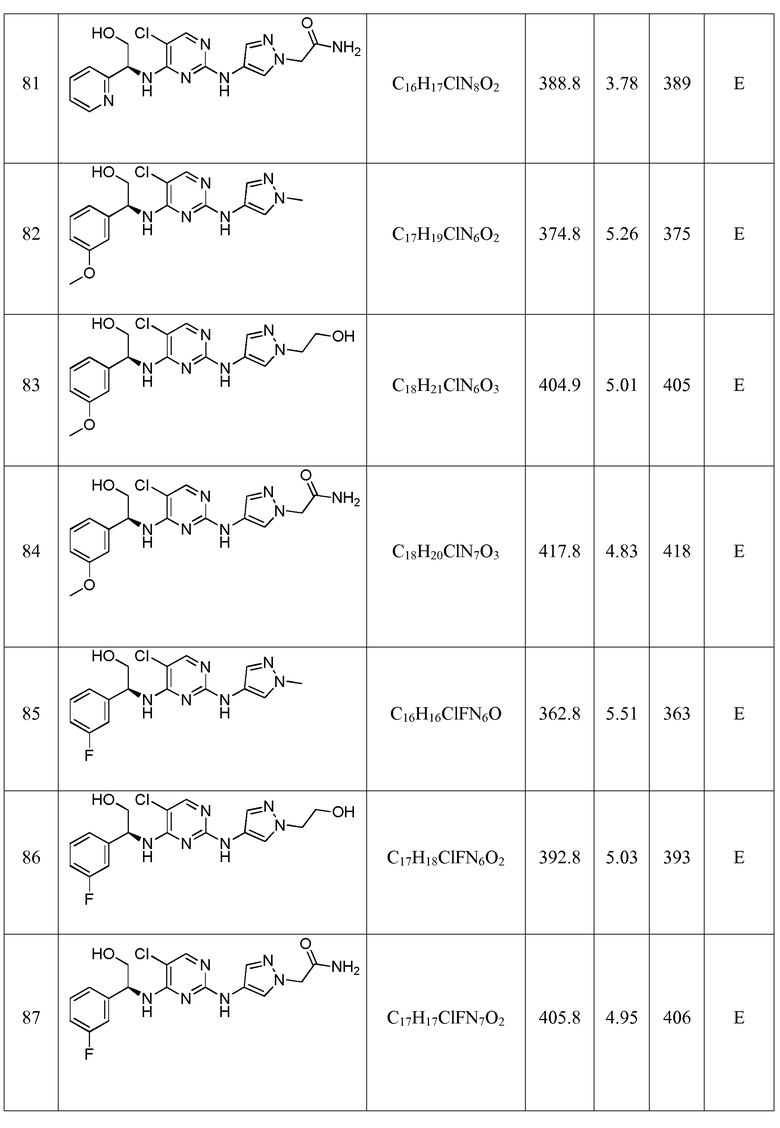
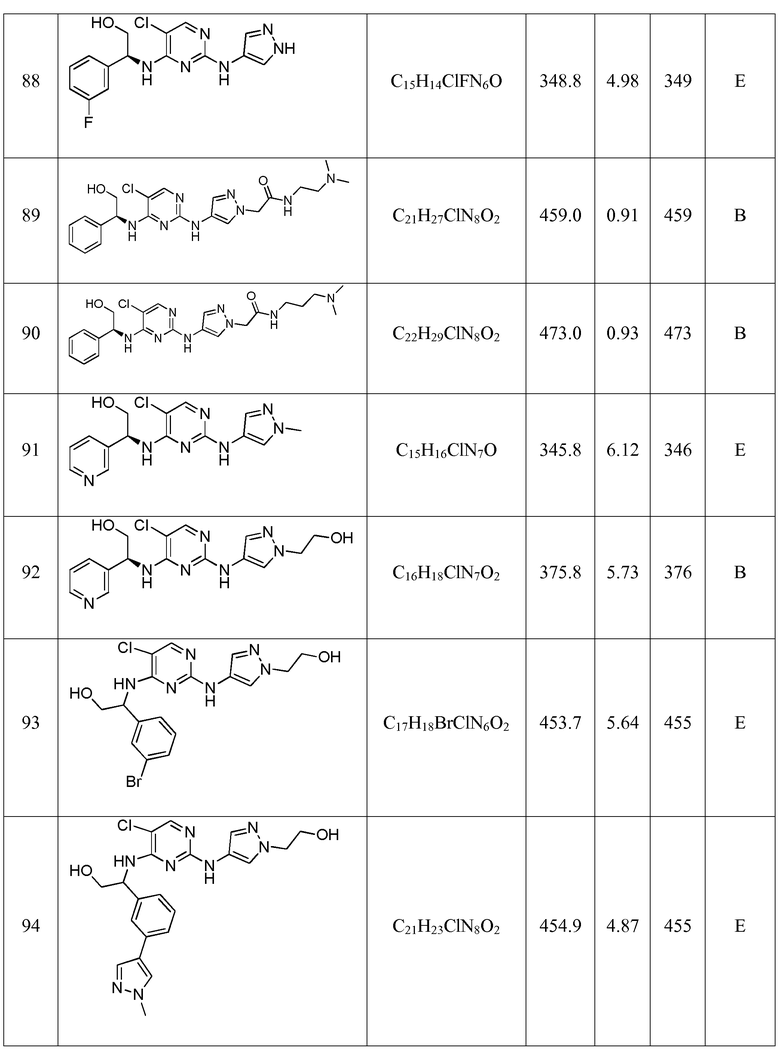
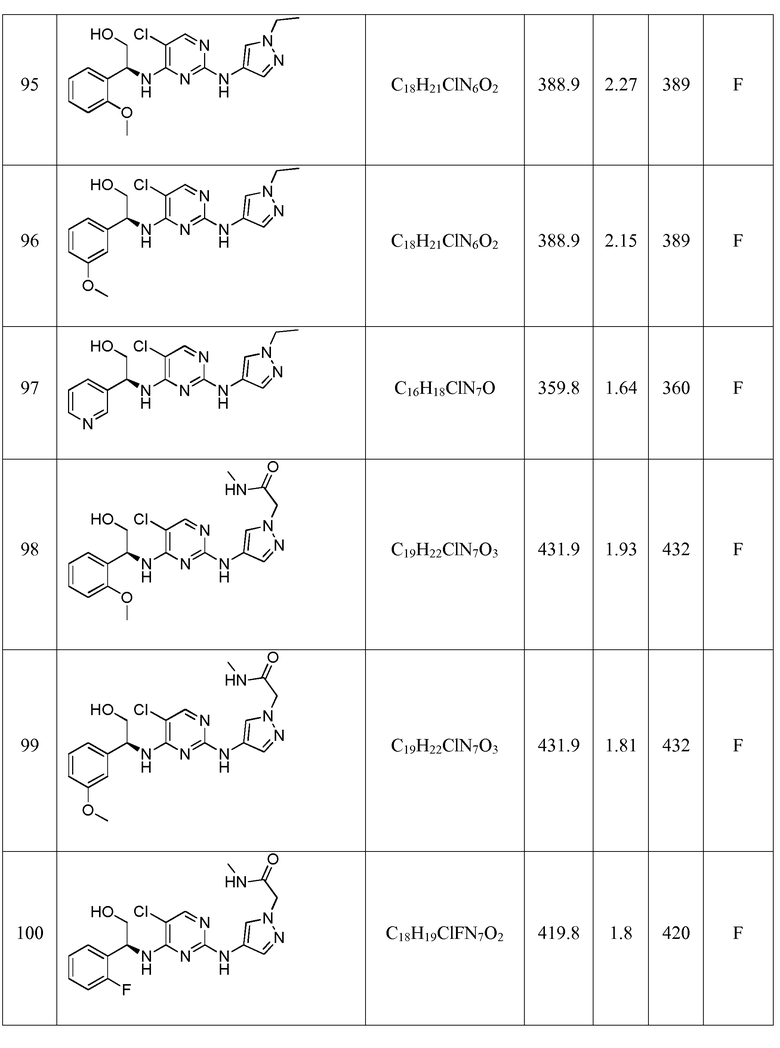
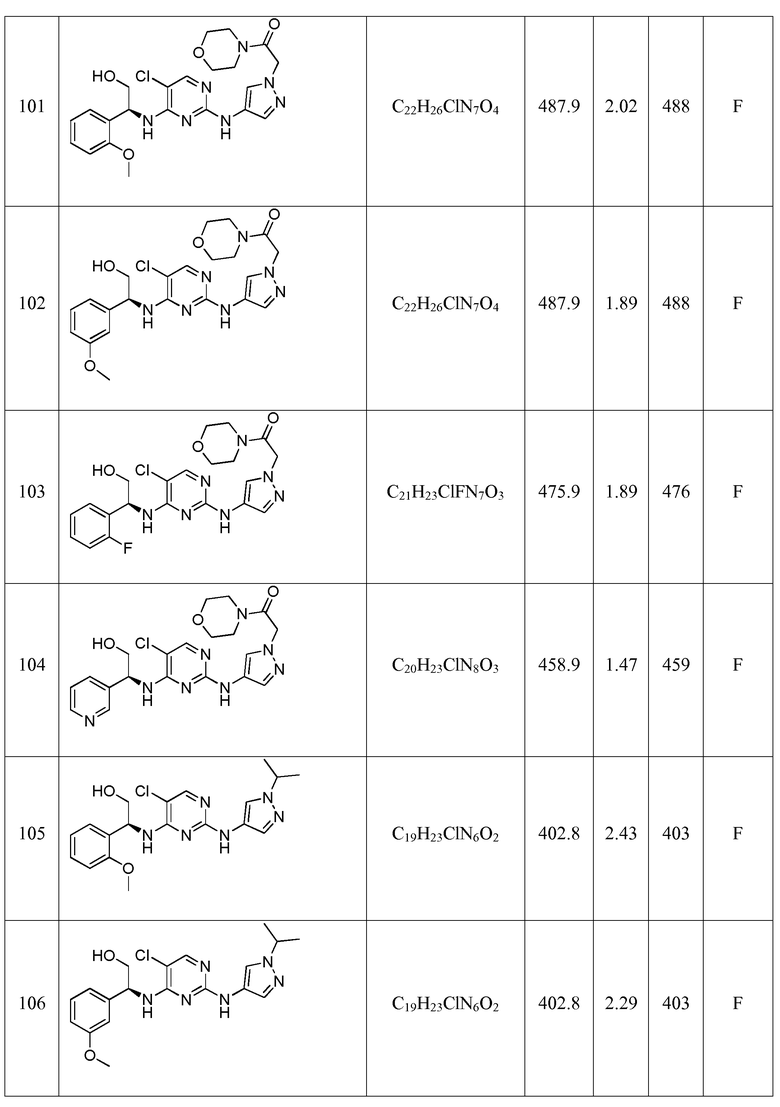
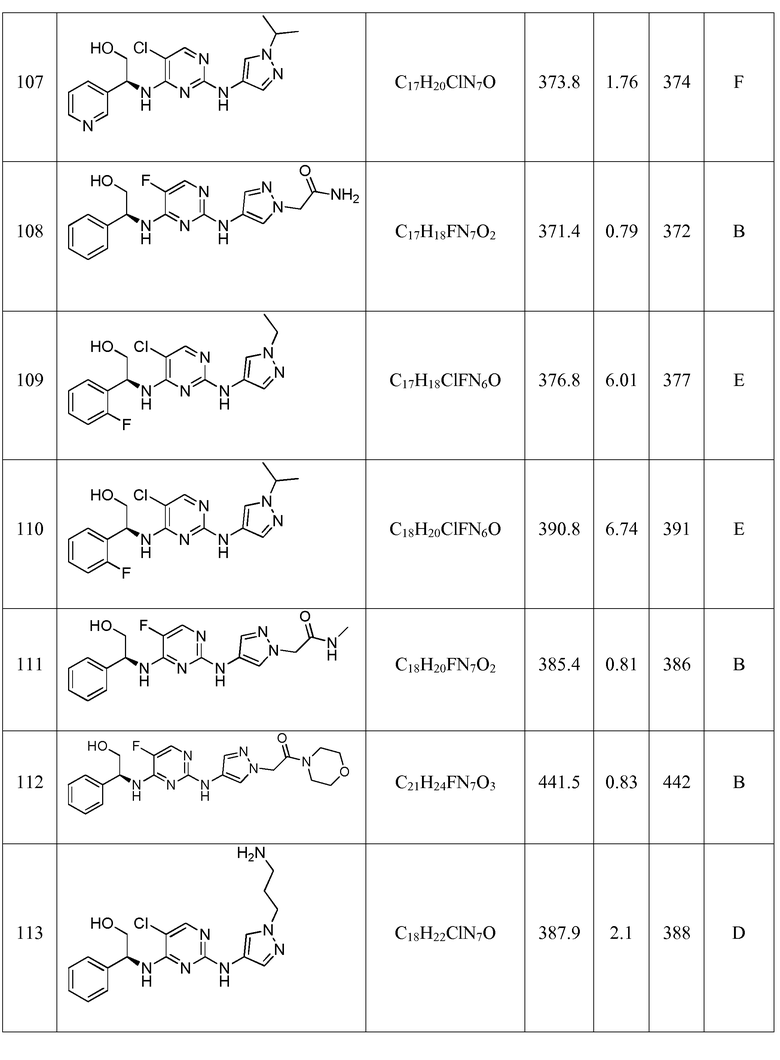
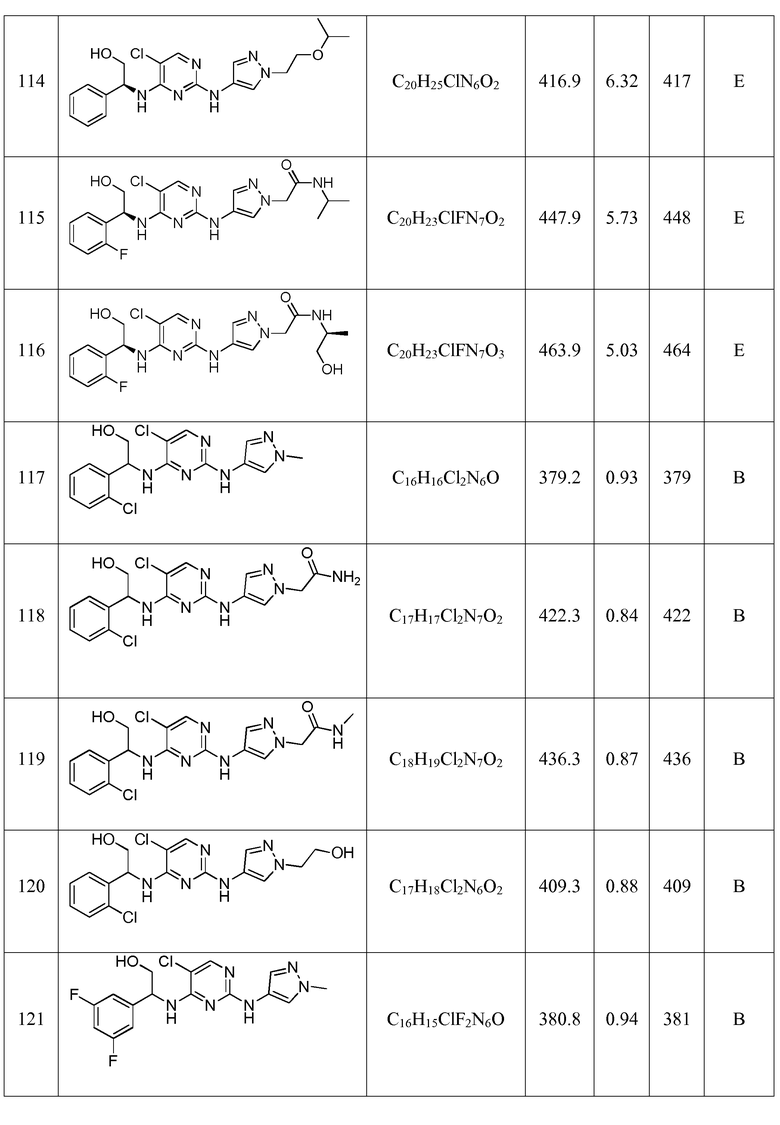
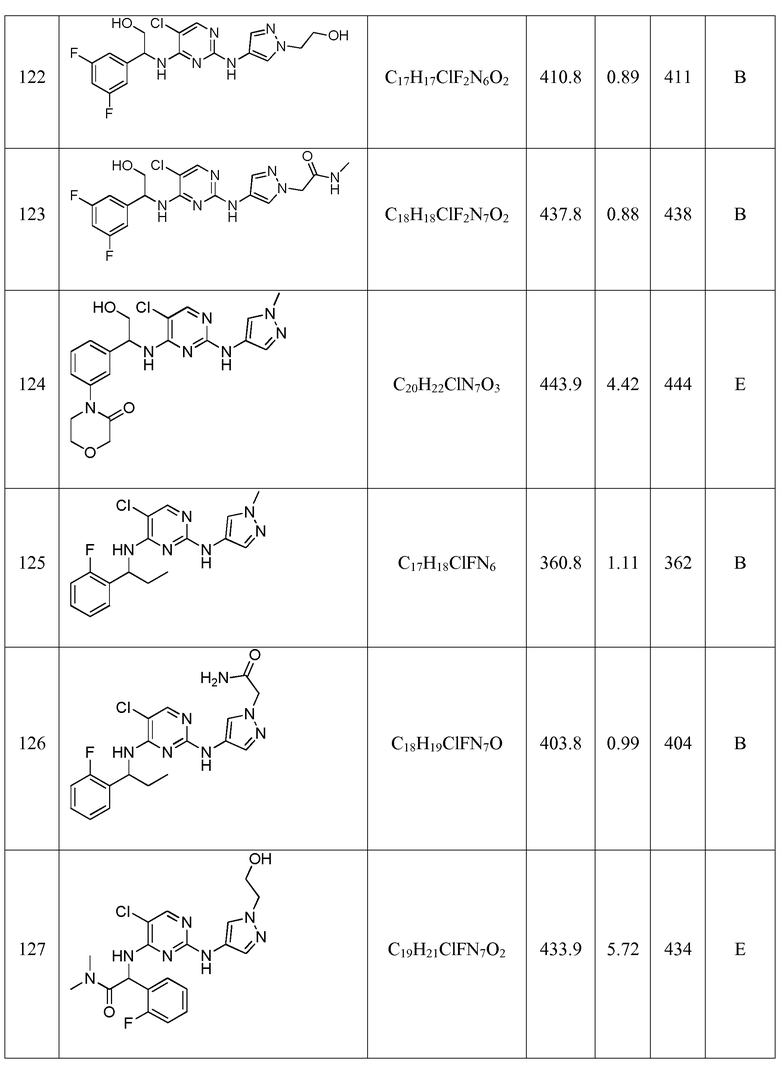
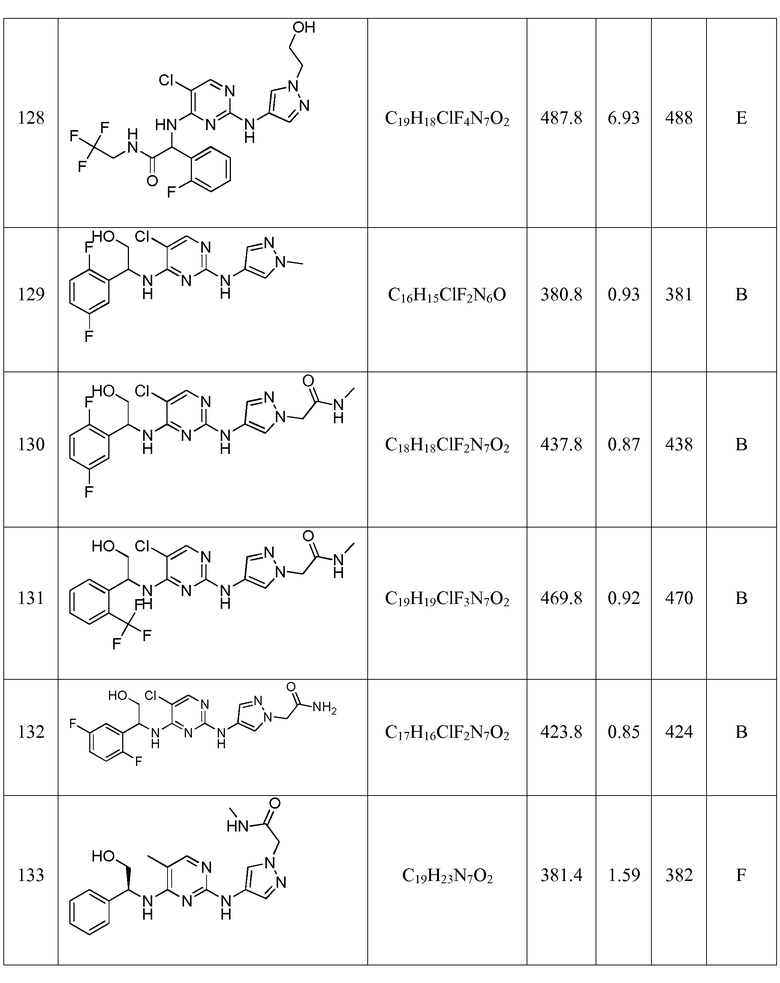
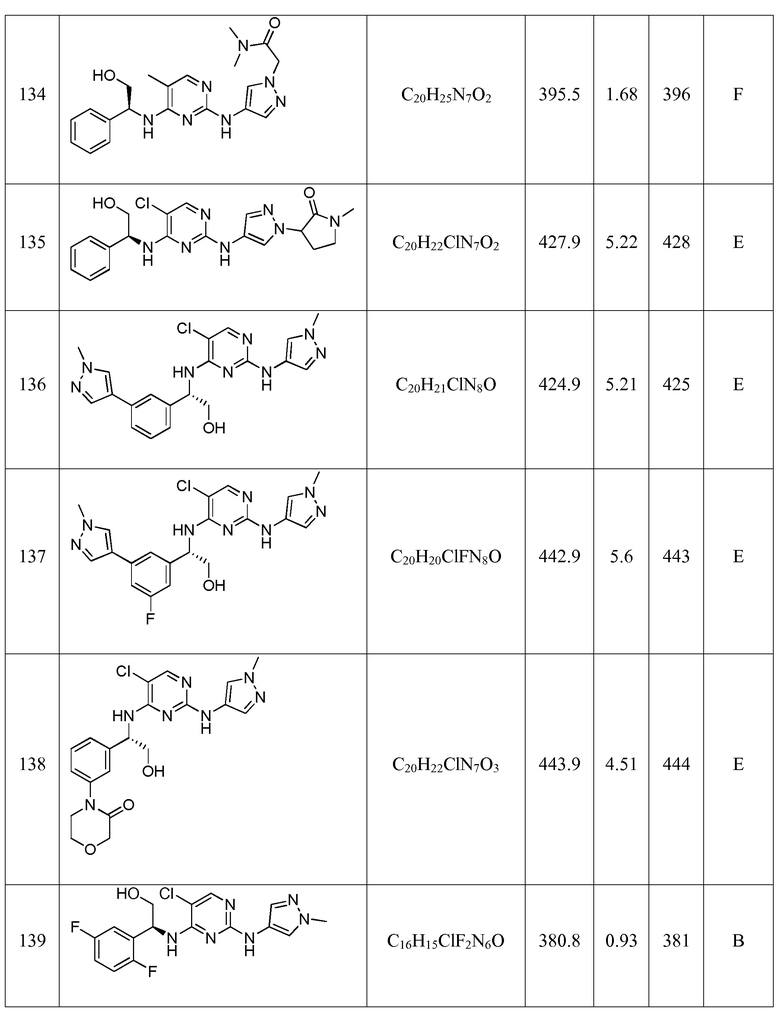
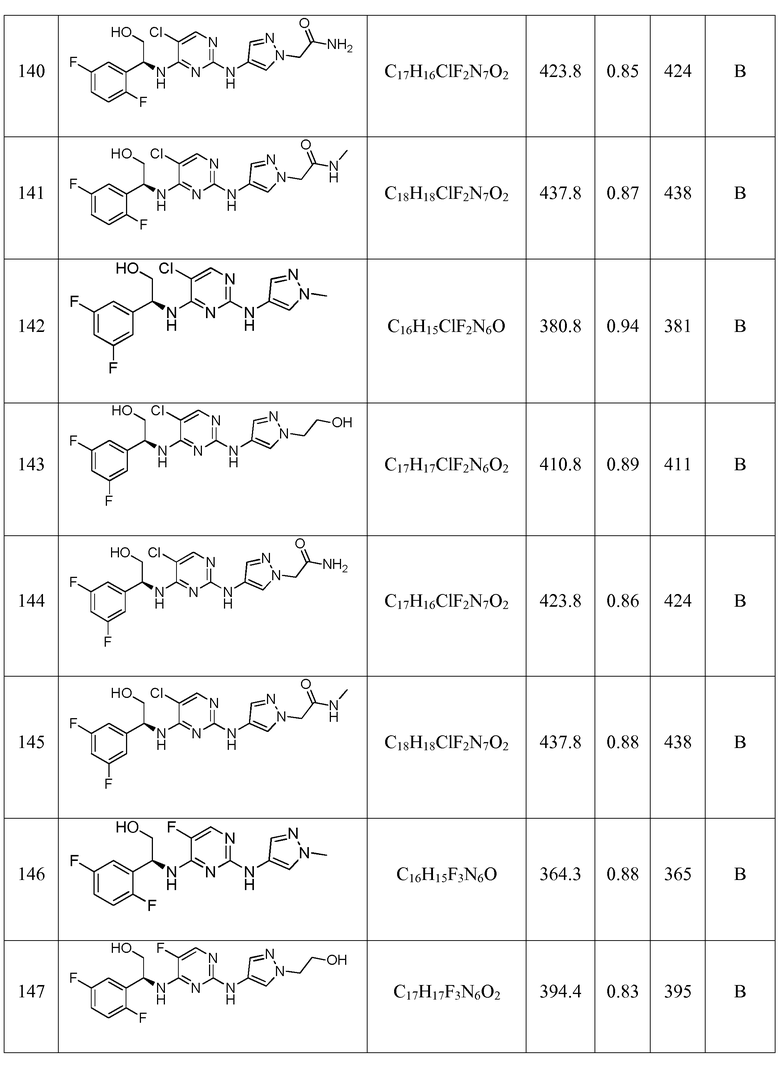
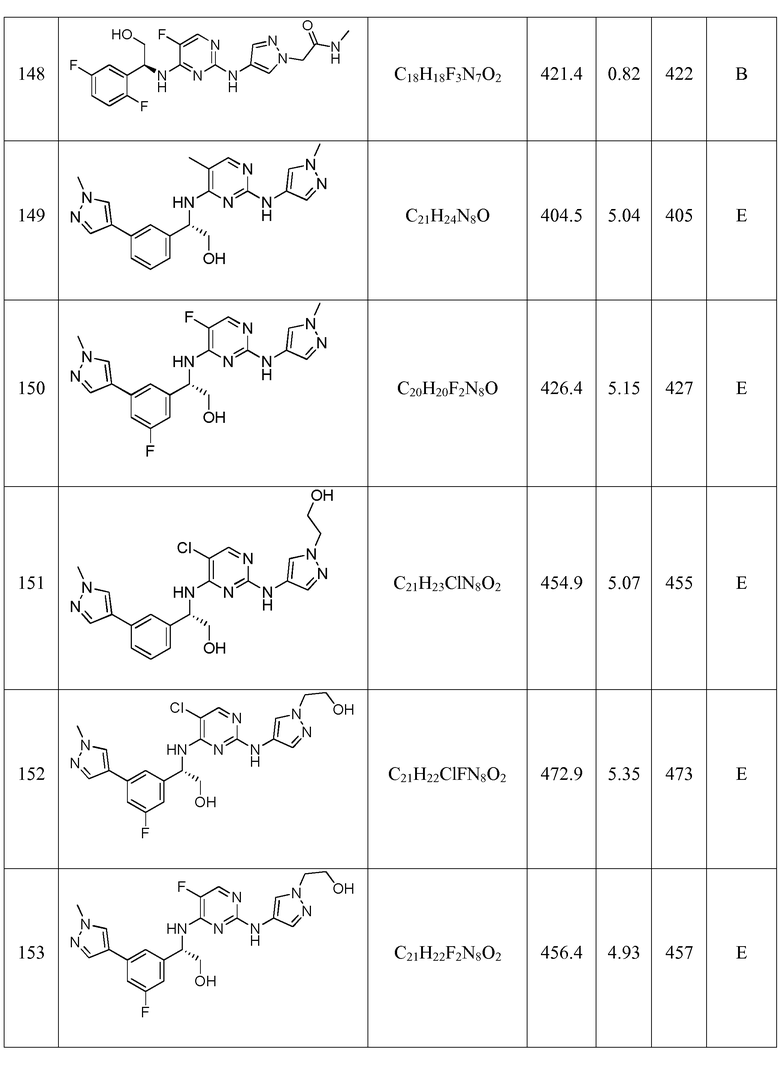
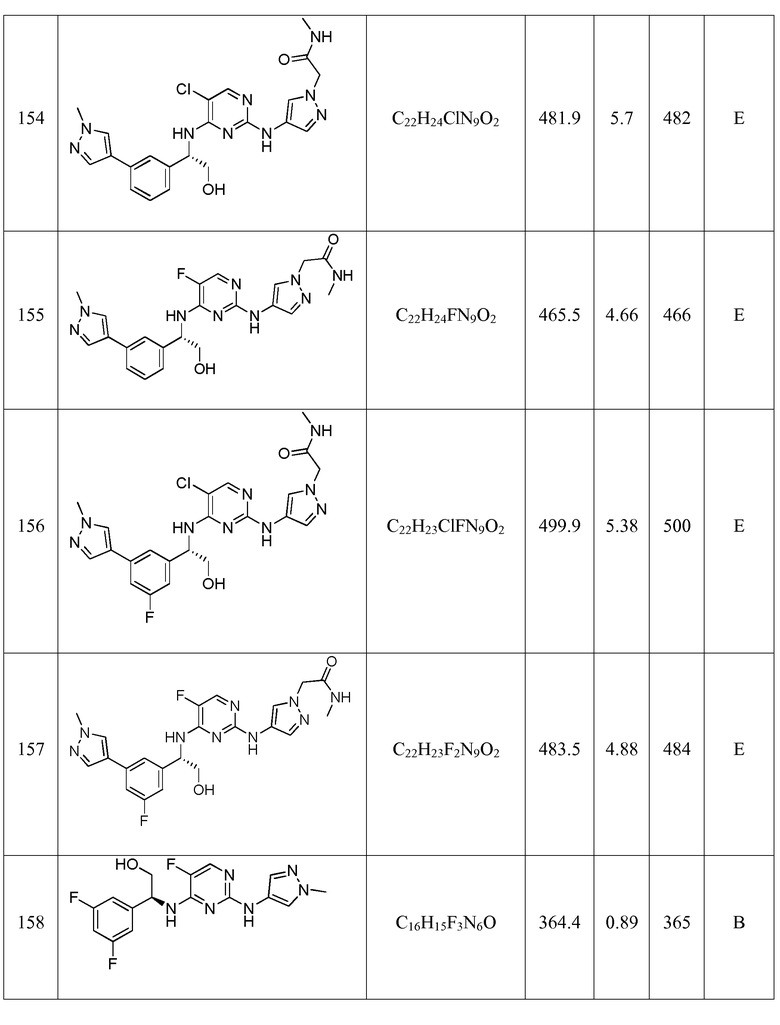
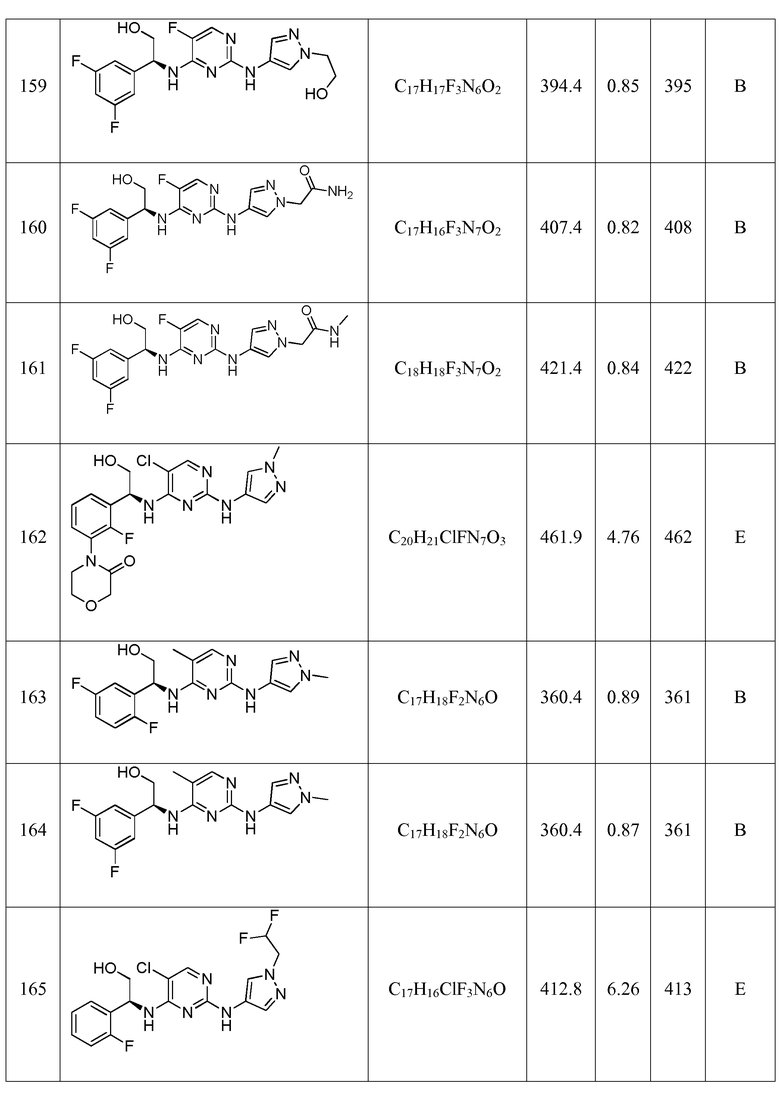
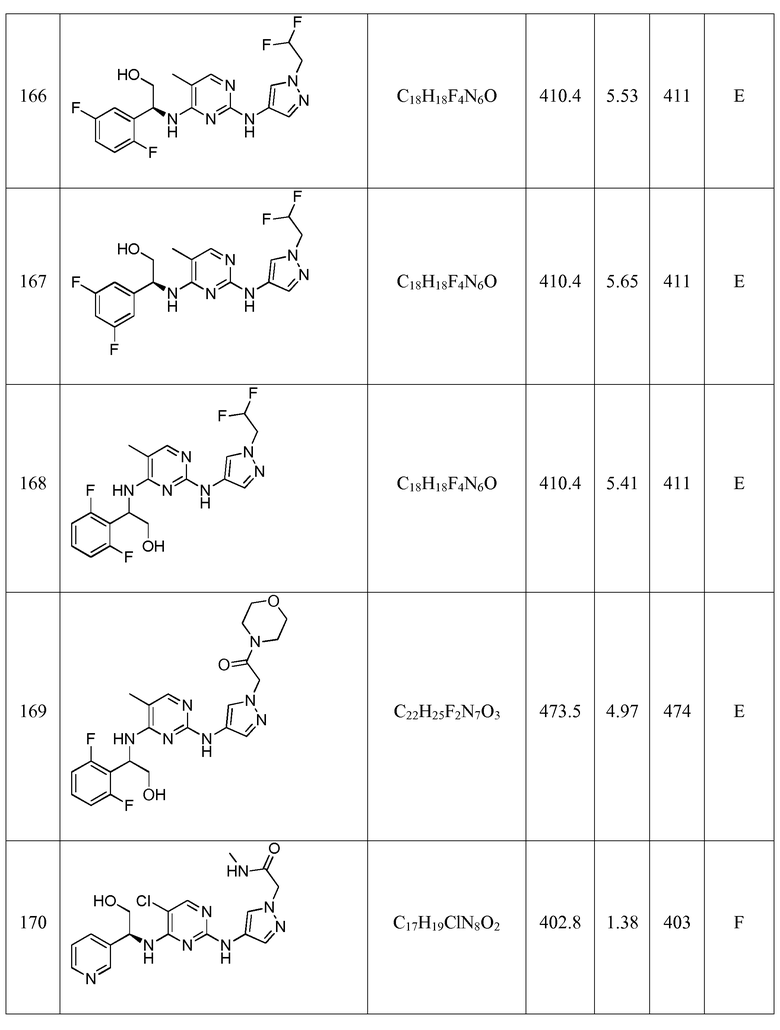
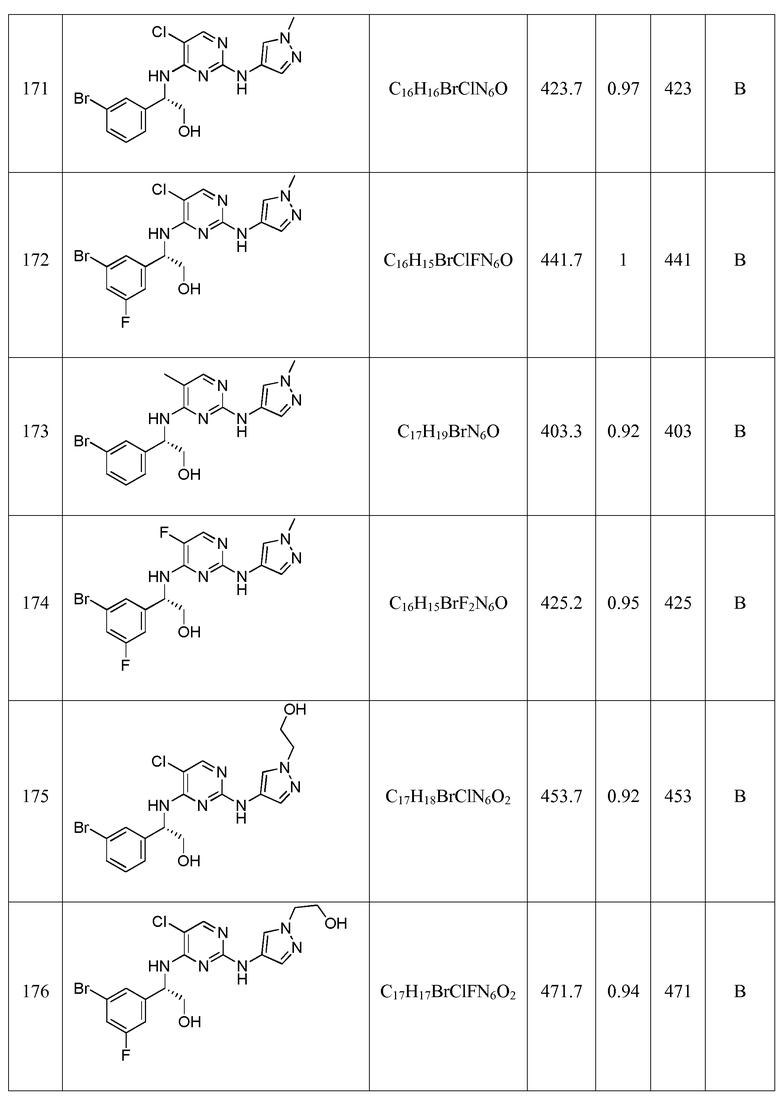
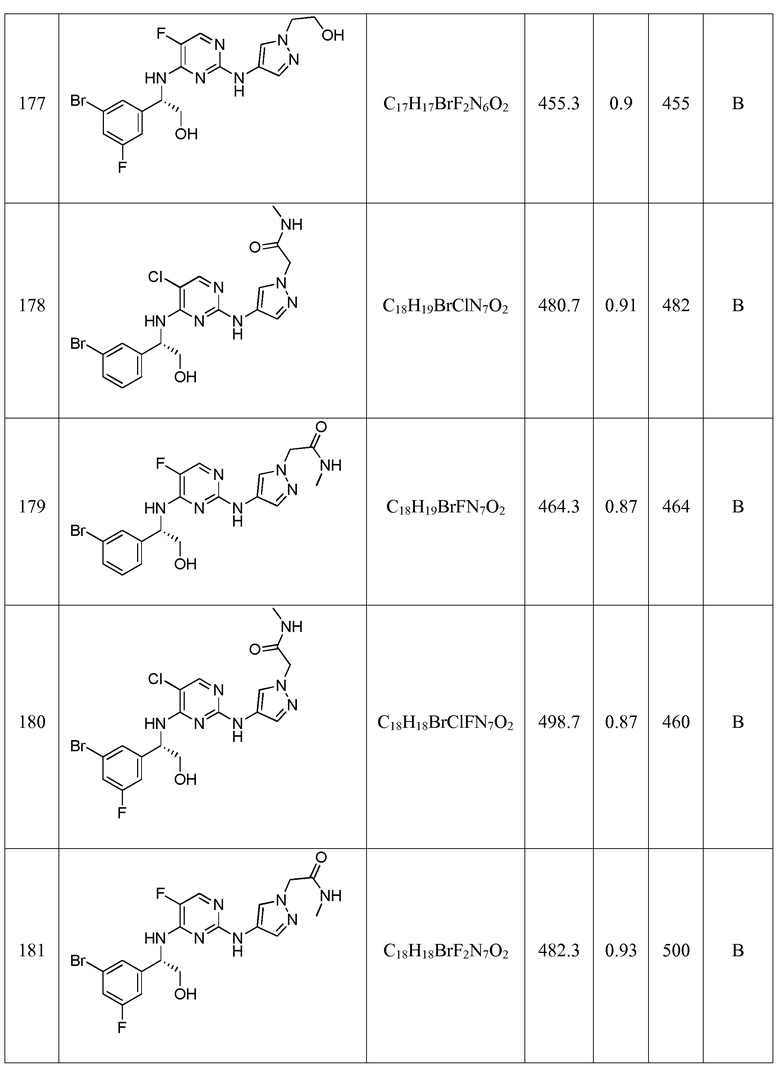
Получение (S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамида (23)
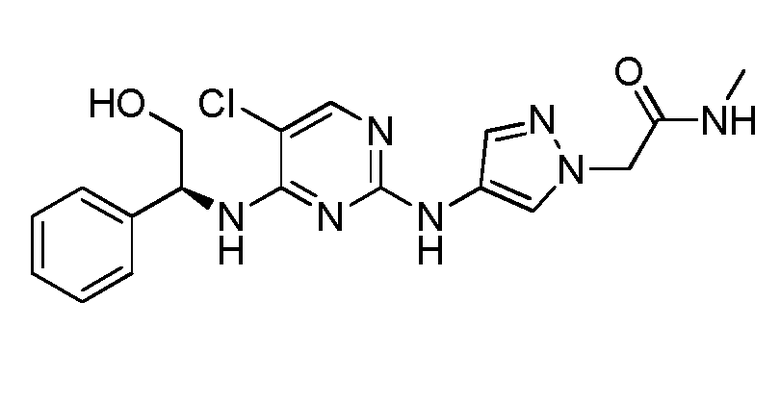
Стадия 1
К раствору 4-нитро-1H-пиразола (100 г, 0,88 моль) в ACN (2 л) добавляли K2CO3 (183,2 г, 1,33 моль) и метил 2-хлорацетат (95,6 г, 0,88 моль). Полученную смесь нагревали до 60°C и перемешивали в течение 5 ч. Затем смесь фильтровали и удаляли растворитель, получая метил 2-(4-нитро-1H-пиразол-1-ил)ацетат в виде твердого вещества белого цвета (150 г, 92%). 1H ЯМР (400 МГц, CDCl3): δ 8,28 (с, 1Н), 8,11 (с, 1H),4,98 (с, 2H), 3,84 (с, 3H).
Стадия 2
Раствор метил 2-(4-нитро-1H-пиразол-1-ил)ацетата (150 г, 0,81 моль) и метиламина в этаноле (2 л) нагревали до кипения с обратным холодильником и перемешивали в течение ночи. Затем реакционной смеси давали остыть и осуществляли ее фильтрование. Слой осадка промывали EtOAc (800 мл) и сушили в вакууме, получая N-метил-2-(4-нитро-1H-пиразол-1-ил)ацетамид в виде светло-желтого твердого вещества (148 г, 99%). 1H ЯМР (400 МГц, d6-ДМСО): δ 8,82 (с, 1Н), 8,24 (с, 1Н), 8,15 (д, J=4,4 Гц, 1Н), 4,85 (с, 2H), 2,61 (д, J=4,4 Гц, 3H).
Стадия 3
К раствору N-метил-2-(4-нитро-1H-пиразол-1-ил)ацетамида (80 г, 0,43 моль) в MeOH (1,5 л) в атмосфере N2 добавляли Pd-C (10%, 16 г). Полученную суспензию дегазировали в вакууме и несколько раз заполняли сосуд H2. Смесь перемешивали в атмосфере H2 (50 фунтов/кв.дюйм) при 30°C в течение ночи и затем фильтровали через слой целита, который промывали MeOH (3×300 мл). Объединенный фильтрат концентрировали досуха, получая 2-(4-амино-1H-пиразол-1-ил)-N-метилацетамид (441,7 г, выход 89%, 6 порций) в виде твердого вещества красного цвета, которое использовали без дополнительной очистки.
Стадия 4
К IPA (150 мл) при -78°C добавляли 2,4,5-трихлорпиримидин (1,34 г, 7,31 ммоль), (S)-2-фенилглицинол (1 г, 7,29 ммоль) и DIPEA (2,6 мл, 14,89 ммоль). Полученному раствору давали нагреться до комнатной температуры и перемешивали в течение ночи. Затем реакционную смесь выливали в воду (500 мл) при перемешивании, собирали полученный белый осадок фильтрованием и сушили в вакууме, получая (S)-2-((2,5-дихлорпиримидин-4-ил)амино)-2-фенилэтанол в виде твердого вещества белого цвета.
1H ЯМР (400 МГц, d6-ДМСО): δ 8,21 (с, 1Н), 8,04 (д, J=8,0 Гц, 1Н), 7,40 (д, J=8 Гц, 2H), 7,33 (т, J=8 Гц, 2H), 7,25 (т, J=8 Гц, 1Н), 5,21 (тд, J=8,2, 5,2 Гц, 1Н), 5,04 (т, J=6 Гц, 1Н), 3,87-3,81 (м, 1Н), 3,73-3,68 (м, 1Н). ЖХ-МС (методика B): время удержания = 0,98 мин, (ES+)284.
Стадия 4 (альтернативная методика)
К раствору 2,4,5-трихлорпиримидина (150 г, 0,818 моль) и (S)-2-фенилглицинола (112,2 г, 0,818 моль) в IPA (1,05 л) при перемешивании при 0°C медленно добавляли DIPEA (317,2 г, 2,45 моль). Реакционную смесь перемешивали при 0°C в течение 1 ч и давали нагреться до комнатной температуры. Реакционную смесь перемешивали в течение ночи при комнатной температуре. ТСХ Rf 0,6 (CH2Cl2/CH3OH=10/1) показала завершение реакции. Полученный осадок отделяли фильтрованием, промывали холодным IPA и затем сушили, получая (S)-2-((2,5-дихлорпиримидин-4-ил)амино)-2-фенилэтанол (550 г, выход: 78,8%, 3 порции) в виде белого твердого вещества.
Стадия 5
К (S)-2-((2,5-дихлорпиримидин-4-ил)амино)-2-фенилэтанолу (0,37 г, 1,30 ммоль) и 2-(4-амино-1H-пиразол-1-ил)-N-метилацетамиду (0,2 г, 1,30 моль) в IPA (15 мл) добавляли одну каплю концентрированной хлористоводородной кислоты. Полученный раствор нагревали в микроволновой печи при 140°C в течение 1 ч и оставляли стоять при комнатной температуре в течение ночи. Полученный белый осадок отделяли фильтрованием и сушили в вакууме, получая (S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамид в виде не совсем белого твердого вещества
1H ЯМР (400 МГц, d6-ДМСО): δ 10,28 (уш.с, 1Н), 8,62 (уш.с, 1H), 8,19 (уш.с, 1H), 8,04 (уш.с, 1Н), 7,74 (уш.с, 1H), 7,48 (с, 1Н), 7,40 (д, J=7,2 Гц, 2H), 7,33 (т, J=7,2 Гц, 2H), 7,25 (т, J=7,2 Гц, 1H), 5,33-5,28 (м, 1Н), 4,81-4,71 (м, 3H), 3,89 (дд, J=11,2, 8,6 Гц, 1Н), 3,74 (дд, J=11,2, 4,8 Гц, 1Н), 2,51 (д, J=2 Гц, 3H). ЖХ-МС (методика B): время удержания = 0,86 мин, (ES+)402.
Стадия 5 (альтернативная методика)
Смесь (S)-2-((2,5-дихлорпиримидин-4-ил)амино)-2-фенилэтанола (100 г, 0,352 моль) и 2-(4-амино-1H-пиразол-1-ил)-N-метилацетамида (0,352 моль) в IPA (1,5 л) перемешивали в течение ночи при 75°C. ТСХ Rf (CH2Cl2/CH3OH=10/1) показала, что реакция завершилась. Полученный осадок отделяли фильтрованием, промывали холодным IPA и затем сушили, получая белое твердое вещество. Затем это белое твердое вещество растворяли в воде и после этого доводили pH до 7 добавлением насыщенного водного раствора NaHCO3. Полученный остаток отделяли фильтрованием, промывали холодной водой и затем сушили, получая свободное основание. Объединяли несколько порций свободного основания (380 г) и растворяли в кипящем ацетоне (20 л). Смесь фильтровали для удаления нерастворимых примесей. Затем при быстром перемешивании к полученному горячему раствору по каплям добавляли HCl (4 М в диоксане, 250 мл, 1 моль). После этого реакционной смеси давали остыть до комнатной температуры и фильтровали. Слой отфильтрованного осадка промывали холодным ацетоном и сушили в вакууме, получая (S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1H-пиразол-1-ил)-N-метилацетамид в виде гидрохлорида (выход 324 г, 41,3%, 5 порций) в виде белого твердого вещества.
1H ЯМР (400 МГц, D2O): δ 2,600 (с, 3Н), 3,817-3,833 (д, J=2,4 Гц, 2H), 4,670-4,673 (м, 2Н), 5,097 (5, 1Н), 7,175-7,223 (м, 6H), 7,329 (с, 1Н), 7,723 (с, 1Н). ЖХ-МС: (M+H)+ 402.
Получение (S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино-1H-пиразол-1-ил)ацетамида (78)
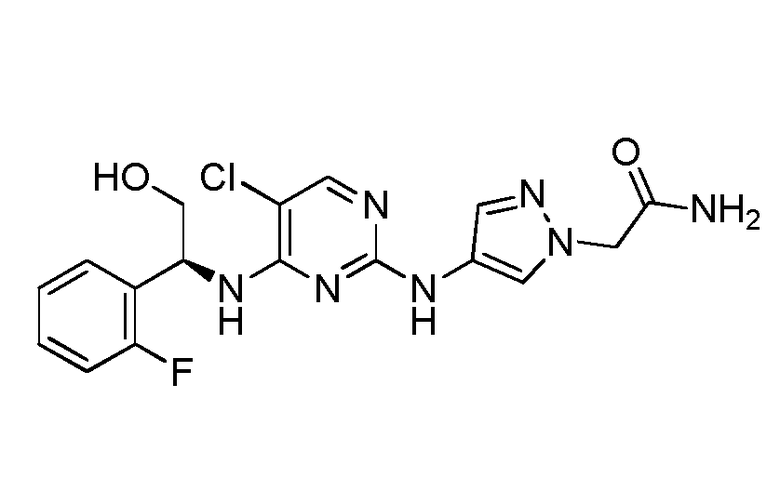
Стадия 1
К раствору 4-нитро-1H-пиразола (2 г, 17,68 ммоль) в ACN (200 мл) добавляли K2CO3 (4,9 г, 35,43 ммоль) и хлорацетамид (1,66 г, 17,75 ммоль). Смесь нагревали до 60°C и перемешивали в течение ночи. Смеси давали остыть, фильтровали и удаляли растворитель, получая 2-(4-нитро-1H-пиразол-1-ил)ацетамид в виде белого твердого вещества (3 г, 100%).
1H ЯМР (400 МГц, d6-ДМСО): δ 8,82 (с, 1Н), 8,26 (с, 1Н), 7,67 (уш.с, 1Н), 7,41 (уш.с, 1Н), 4,88 (с, 2H).
Стадия 2
К раствору 2-(4-нитро-1H-пиразол-1-ил)ацетамида (3 г, 17,64 ммоль) в MeOH (150 мл) в атмосфере N2 добавляли Pd-C (10%, 0,3 г). Суспензию дегазировали в вакууме и несколько раз заполняли реакционный сосуд H2. Смесь перемешивали в атмосфере H2 при атмосферном давлении и комнатной температуре в течение ночи и затем фильтровали через слой целита. Полученный фильтрат концентрировали досуха, получая 2-(4-амино-1H-пиразол-1-ил)ацетамид в виде твердого вещества бордового цвета, которое использовали без дальнейшей очистки.
1H ЯМР (400 МГц, d6-ДМСО): δ 7,17 (уш.с, 2H), 7,02 (с, 1Н), 6,93 (с, 1Н), 4,55 (с, 2H), 3,85 (уш.с, 2Н).
Стадия 3
К IPA (15 мл) при 0°C добавляли DIPEA (1,5 мл, 8,59 ммоль) и гидрохлорид (S)-2-амино-2-(2-фторфенил)этан-1-ола (0,5 г, 2,61 ммоль) и затем 2,4,5-трихлорпиримидин (0,45 г, 2,46 ммоль). Полученному раствору давали нагреться до комнатной температуры и перемешивали в течение ночи. Затем реакционную смесь выливали в воду (50 мл) при перемешивании, и полученный белый осадок собирали фильтрованием и сушили в вакууме, получая (S)-2-((2,5-дихлорпиримидин-4-ил)амино)-2-(2-фторфенил)этанол в виде не совсем белого/желтого твердого вещества (0,64 г, 86%), который использовали без дополнительной очистки.
1H ЯМР (400 МГц, d6-ДМСО): δ 8,23 (с, 1Н), 8,09 (д, J=8,0 Гц, 1Н), 7,48 (тд, J=7,6, 1,5 Гц, 1Н), 7,41-7,26 (м, 1Н), 7,26-7,08 (м, 2H), 5,51 (тд, J=8,1, 5,0 Гц, 1Н), 5,16 (т, J=5,9 Гц, 1Н), 3,92-3,75 (м, 1Н), 3,75-3,63 (м, 1Н). ЖХ-МС (методика B): время удержания = 1,04 мин, (ES+)302.
Стадия 4
К IPA (15 мл) добавляли (S)-2-((2,5-дихлорпиримидин-4-ил)амино)-2-(2-фторфенил)этанол (0,096 г, 0,32 ммоль) и 2-(4-амино-1H-пиразол-1-ил)ацетамид (0,07 г, 0,50 ммоль). Полученный раствор нагревали при 80°C в течение ночи, давали остыть и осаждали твердое вещество добавлением насыщенного раствора NaHCO3. Собранное твердое вещество очищали хроматографией на обращенной фазе, получая (S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино-1H-пиразол-1-ил)ацетамид в виде не совсем белого твердого вещества.
1H ЯМР (400 МГц, d6-ДМСО): δ 9,11 (с, 1Н), 7,94 (с, 1Н), 7,60 (с, 1Н), 7,40 (дд, J=15,1, 7,3 Гц, 2H), 7,35-7,25 (м, 2H), 7,23 (с, 1Н), 7,21-7,13 (м, 2H), 7,03 (с, 1Н), 5,53 (дд, J=13,2, 6,0 Гц, 1Н), 5,17 (с, 1Н), 4,64 (с, 2Н), 3,75 (т, J=5,8 Гц, 2H). ЖХ-МС (методика E): время удержания = 4,86 мин, (ES+)406.
Получение (S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино-1H-пиразол-1-ил)ацетамида (78) (альтернативная методика)
Путь синтеза
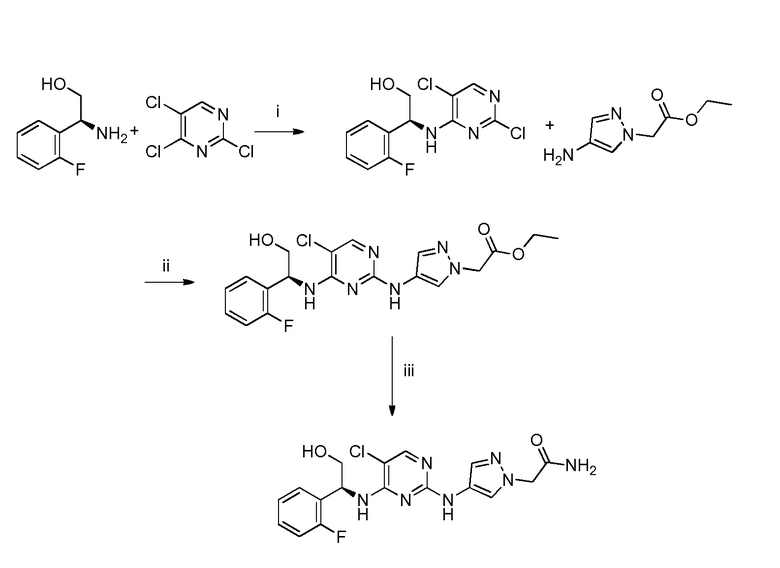
Стадия i) DIPEA, IPA 0°C 18 ч; стадия ii) 4,0М HCl диоксан, IPA, 60°C, 24-48 ч; стадия iii) 7н. NH3 MeOH, EtOH 18 ч.
(S)-2-((2,5-дихлорпиримидин-4-ил)амино)-2-(2-фторфенил)этанол
Раствор гидрохлорида (S)-2-амино-2-(2-фторфенил)этанола (500 мг, 2,62 ммоль) и DIPEA (1,1 мл, 3,0 экв.) в IPA (10 мл) перемешивали в течение 10 минут. Раствор охлаждали на бане с ледяной водой и затем добавляли 2,4,5-трихлорпиримидин (450 мг, 2,46 ммоль). Реакционной смеси давали нагреться до комнатной температуры и перемешивали в течение ночи. Добавляли воду (30 мл) и собирали образовавшийся осадок фильтрованием в виде не совсем белого/желтого твердого вещества (0,64 г, выход 87%). UPLC (высокое значение pH) время удержания 1,04 мин, m/z 302 (ES+);
1H ЯМР (400 МГц, d6-ДМСО): δ 8,23 (с, 1Н), 8,09 (д, J=8,0 Гц, 1Н), 7,48 (тд, J=7,6, 1,5 Гц, 1Н), 7,41-7,26 (м, 1Н), 7,26-7,08 (м, 2Н), 5,51 (тд, J=8,1, 5,0 Гц, 1Н), 5,16 (т, J=5,9 Гц, 1Н), 3,92-3,75 (м, 1Н), 3,75-3,63 (м, 1Н).
(S)-этил 2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-H-пиразол-1-ил)ацетат
(S)-2-((2,5-дихлорпиримидин-4-ил)амино)-2-(2-фторфенил)этанол (1,90 г, 6,3 ммоль) и этил 2-(4-амино-1H-пиразол-1-ил)ацетат (1,60 г, 1,5 экв.) перемешивали в EtOH (40 мл) с HCl в диоксане (4 М, 1,60 мл, 1,0 экв.) и нагревали до 50°C в течение 40 часов. Реакционную смесь упаривали, удаляя половину объема растворителя, и затем распределяли между EtOAc и NaHCO3 (водн.). Водный слой экстрагировали EtOAc, объединенные органические слои промывали насыщенным раствором соли, сушили над Na2SO4, фильтровали и упаривали, получая 3,0 г темно-красного твердого вещества. 169 мг этого красного твердого вещества дополнительно очищали флэш-хроматографией (оксид кремния 10 г, 50-100% EtOAc/петр.эфир), получая 124 мг (выход 73%) бесцветного твердого вещества.
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино-1H-пиразол-1-ил)ацетамид
(S)-этил 2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-H-пиразол-1-ил)ацетат (2,84 г, 6,53 ммоль) растворяли в 7н. растворе NH3 в MeOH (14 мл) и перемешивали при комнатной температуре в течение 64 часов. Полученный осадок собирали фильтрованием, затем растирали с IPA, вновь собирали фильтрованием, промывали IPA и в течение ночи сушили в вакуумной печи. ЖХМС (5) время удержания 4,81 минут m/z 406 (ES+).
1H ЯМР (400 МГц, d6-ДМСО): δ 9,11 (с, 1Н), 7,94 (с, 1Н), 7,60 (с, 1Н), 7,40 (дд, 15,1, 7,3 Гц, 2H), 7,35-7,25 (м, 2H), 7,23 (с, 1Н), 7,21-7,13 (м, 2H), 7,03 (с, 1Н), 5,53 (дд, J=13,2, 6,0 Гц, 1Н), 5,17 (с, 1H), 4,64 (с, 2H), 3,75 (т, J=5,8 Гц, 2H). Определяли, что процент ee энантиомерного избытка составил >98%.
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино-1H-пиразол-1-ил)ацетамид (альтернативные условия проведения реакции)
(S)-этил 2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-H-пиразол-1-ил)ацетат (822 мг, 1,89 ммоль) растворяли в 7н. растворе NH3 в MeOH (15 мл) и нагревали в микроволновой печи при 120°C в течение 30 мин. Реакционную смесь упаривали, получая 718 мг красного твердого вещества (выход 94%). Это твердое вещество растворяли в EtOAc с небольшим количеством MeOH для повышения растворимости и затем промывали NaHCO3 (водн.). Водный слой экстрагировали 2×EtOAc. Органические фазы объединяли и промывали насыщенным раствором соли, сушили над Na2SO4, фильтровали и упаривали, получая 647 мг (выход 84%) твердого вещества персикового цвета.
Образование солей с HCl
Соединение 78 в форме свободного основания (1,02 г, 2,51 ммоль) суспендировали в IPA (20 мл) при 60°C. К этой суспензии добавляли 2 М HCl (1,38 мл, 2,76 ммоль), получая бесцветный раствор. Этому раствору давали остыть до комнатной температуры после чего осторожно удаляли растворители, вначале ускоренным выпариванием в токе азота и затем в вакууме, получая 916 мг (выход 83%) UPLC при высоком значении pH. Время удержания 1,77 минут, m/z 406 (ES+), т.плавления (с разложением) 89°C, плавление 180°C.
Биологические исследования
Определение влияния соединений по настоящему изобретению на JAK
Соединения по настоящему изобретению, описанные в предыдущих примерах, исследовали в анализе KinobeadsTM, как описано для ZAP-70 (WO-A 2007/137867). Вкратце, тестируемые соединения (в различных концентрациях) и аффинную матрицу с иммобилизованным аминопиридопиримидиновым лигандом 24 добавляли к аликвотам клеточного лизата и давали связаться с белками в образце лизата. После инкубирования, гранулы со связанными белками отделяли от лизата. Затем связанные белки вымывали, определяли наличие JAK1, JAK2, JAK3 и TYK2 и осуществляли их количественное определение используя специфичные антитела в методике дотблоттинга и систему инфракрасного детектирования Odyssey. Строили зависимости реакции от дозы для индивидуальных киназ и рассчитывали значения IC50. Анализ KinobeadsTM для ZAP-70 (WO-A 2007/137867) и для определения профиля селективности в отношении киназ (WO-A 2006/134056) были описаны ранее.
Протоколы
Промывание аффинной матрицы
Аффинную матрицу два раза промывали 15 мл 1× буфера DP, содержащего 0,2% NP40 (IGEPAL® CA-630, Sigma, №13021) и затем ресуспендировали в 1× буфере DP, содержащем 0,2% NP40 (3% суспензия гранул).
5× буфер DP: 250 мМ Tris-HCl, pH 7,4, 25% глицерин, 7,5 мМ MgCl2, 750 мМ NaCl, 5 мМ Na3VO4; 5× DP буфер фильтровали через 0,22 мкм фильтр и хранили в виде аликвот при -80°C. 5х буфер DP разбавляли H2O до 1х буфера DP, содержащего 1 мМ DTT и 25 мМ NaF.
Получение тестовых соединений
Концентрированные растворы тестовых соединений готовили в ДМСО. В 96-луночном планшете готовили 30 мкл растворов разбавленных тестовых соединений в концентрации 5 мМ в ДМСО. Исходя из этих растворов готовили серии последовательных разбавлений 1:3 (9 ступеней). Для контрольных экспериментов (без тестовых соединений) использовали буфер, содержащий 2% ДМСО.
Клеточные культуры и получение клеточных лизатов
Клетки Molt4 (номер по каталогу ATCC CRL-1582) и клетки Ramos (номер по каталогу ATCC CRL-1596) выращивали в 1 л колбах Spinner (Integra Biosciences, №182101) в виде суспензии в среде RPMI 1640 (Invitrogen, №21875-034) c добавкой 10% сыворотки телят (Invitrogen) при плотности клеток от 0,15×106 до 1,2×106 клеток/мл. Клетки собирали центрифугированием, один раз промывали буфером 1×PBS (Invitrogen, №14190-094), замораживали осажденные клетки в жидком азоте и затем хранили при -80°C. Клетки гомогенизировали с помощью гомогенизатора Potter S в буфере для лизиса: 50 мМ Tris-HCl, 0,8% NP40, 5% глицерин, 150 мМ NaCl, 1,5 мМ MgCl2, 25 мМ NaF, 1 мМ ванадат натрия, 1 мМ DTT, pH 7,5. На 25 мл буфера добавляли одну полную, не содержащую EDTA, таблетку (коктейль ингибиторов протеаз, Roche Diagnostics, 1873580). Клеточный материал гомогенизировали 10 раз, используя моторизованный гомогенизатор Potter S, переносили в 50 мл пробирки falcon, инкубировали в течение 30 минут на льду и центрифугировали в течение 10 минут при 20000g при 4°C (10000 об/мин в предварительно охлажденной центрифуге Sorvall SLA600). Супернатант переносили в (UZ)-поликарбонатную пробирку для ультрацентрифуги (Beckmann, 355654) и центрифугировали в течение 1 ч при 100000 g при 4°C (33500 об/мин в предварительно охлажденной центрифуге Ti50.2). Супернатант переносили в новые 50 мл пробирки falcon, определяли концентрацию белка с помощью анализа Bradford (BioRad) и готовили образцы, содержащие 50 мг белка на аликвоту. Образцы немедленно использовали для проведения экспериментов или замораживали в жидком азоте и хранили в замороженном виде при -80°C.
Разбавление клеточных лизатов
Клеточные лизаты (примерно 50 мг белка на планшет) оттаивали на водяной бане при комнатной температуре и затем хранили на льду. К оттаявшему клеточному лизату добавляли 1×DP 0,8% буфера NP40, содержащего ингибиторы протеаз (1 таблетка на 25 мл буфера, коктейль ингибиторов протеаз, не содержащий EDTA; Roche Diagnostics 1873580) для достижения конечной концентрации белка 10 мг/мл общего содержания белка. Разбавленные клеточные лизаты хранили на льду. Смешанный лизат Molt4/Ramos готовили путем смешивания одного объема лизата Molt4 и двух объемов лизата Ramos (соотношение 1:2).
Инкубирование лизата с тестовым соединением и аффинной матрицей
В 96-луночные фильтровальные планшеты (Multiscreen HTS, BV Filter Plates, Millipore #MSBVN1250) добавляли на лунку: 100 мкл аффинной матрицы (3% суспензия гранул), 3 мкл раствора соединения и 50 мкл разбавленного лизата. Планшеты плотно закрывали и инкубировали в течение 3 часов в холодной комнате на шейкере для планшетов (Heidolph tiramax 1000) при 750 об/мин. После этого планшеты 3 раза промывали 230 мкл буфера для промывания (1×DP 0,4% NP40). Фильтровальные планшеты помещали наверх планшета для сбора образцов (Greiner bio-one, PP-microplate 96-луночный, V-образный 65120) и промывали гранулы 20 мкл буфера для образцов (100 мМ Tris, pH 7,4, 4% SDS, 0,00025% бромфеноловый синий, 20% глицерин, 50 мМ DTT). Элюат быстро замораживали при -80°C и хранили при -20°C.
Обнаружение и количественное определение элюированных киназ
Киназы в элюатах обнаруживали и количественно определяли нанесением пятна образца на нитроцеллюлозную мембрану с использованием первого антитела против интересующей киназы и флуоресцентно меченого второго антитела (антикроличьего IRDyeTM антитела 800 (Licor, #926-32211)). Систему получения инфракрасных изображений Odyssey от LI-COR Biosciences (Lincoln, Nebraska, USA) использовали согласно инструкциям производителя (Schutz-Geschwendener et al., 2004. Quantitative, two-color Western blot detection with infrared fluorescence. Опубликовано в мае 2004 LI-COR Biosciences, http://www.licor.com).
После нанесения пятна элюата, нитроцеллюлозные мембраны (BioTrace NT; PALL, #BTNT30R) во-первых, блокировали инкубированием с блокирующим буфером Odyssey (LICOR, 927-40000) в течение 1 часа при комнатной температуре. Затем блокированные мембраны инкубировали в течение 16 часов при температуре, указанной в таблице 4, с первым антителом, разбавленным блокирующим буфером Odyssey (LICOR #927-40000). После этого мембраны дважды в течение 10 минут промывали буфером PBS, содержащим 0,2% Tween 20 при комнатной температуре. Затем мембраны инкубировали в течение 60 минут при комнатной температуре с антителом для детектирования (антикроличье IRDyeTM антитело 800, Licor, #926-32211), разбавленным блокирующим буфером Odyssey (LICOR #927-40000). Затем мембраны дважды промывали в течение 10 минут буфером 1×PBS, содержащим 0,2% Tween 20 при комнатной температуре. Затем мембрану один раз промывали буфером PBS для удаления остатков Tween 20. Мембраны хранили в PBS буфере при 4°C и затем сканировали на приборе Odyssey. Флуоресцентные сигналы регистрировали и анализировали согласно инструкциям производителя.
Источники и разбавления антител
1:100
1:100
1:100
1:1000
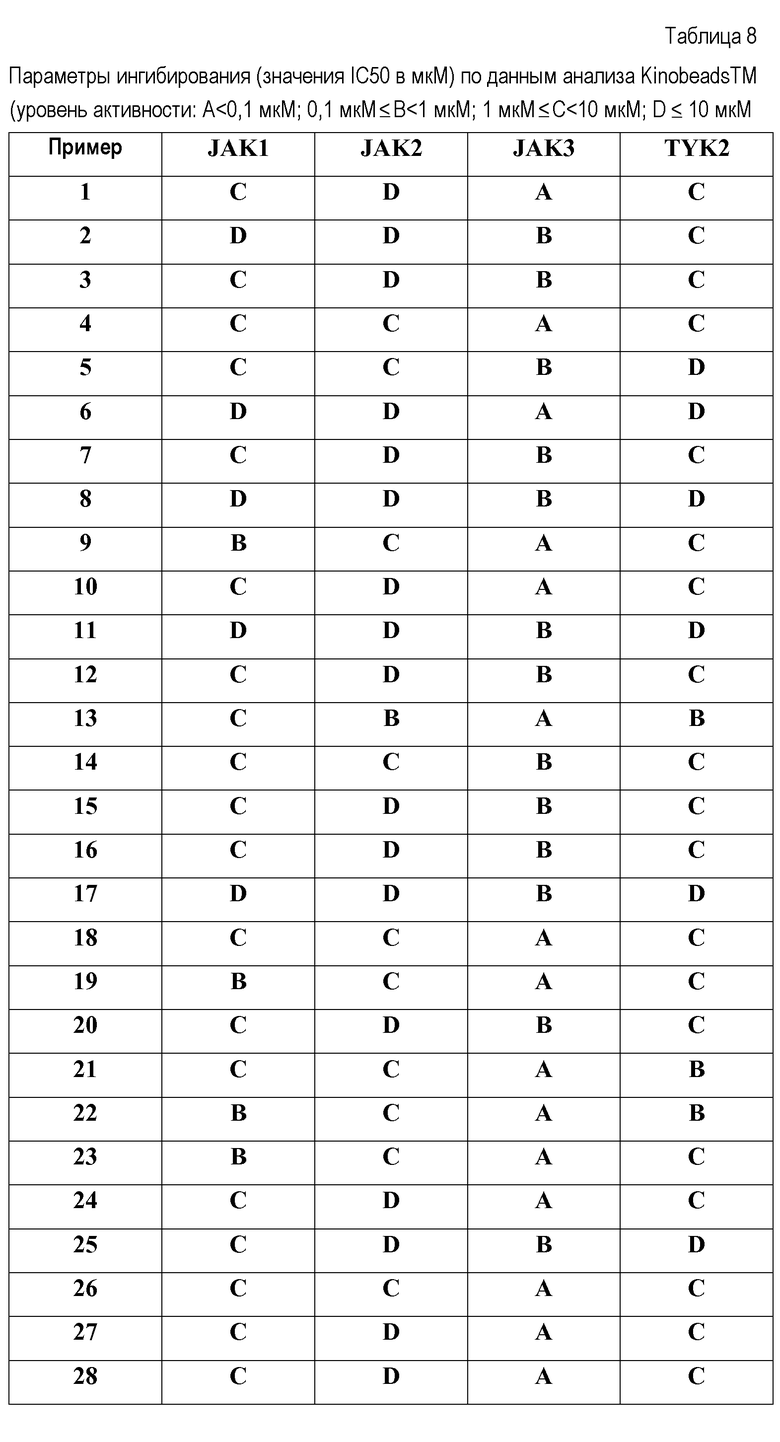
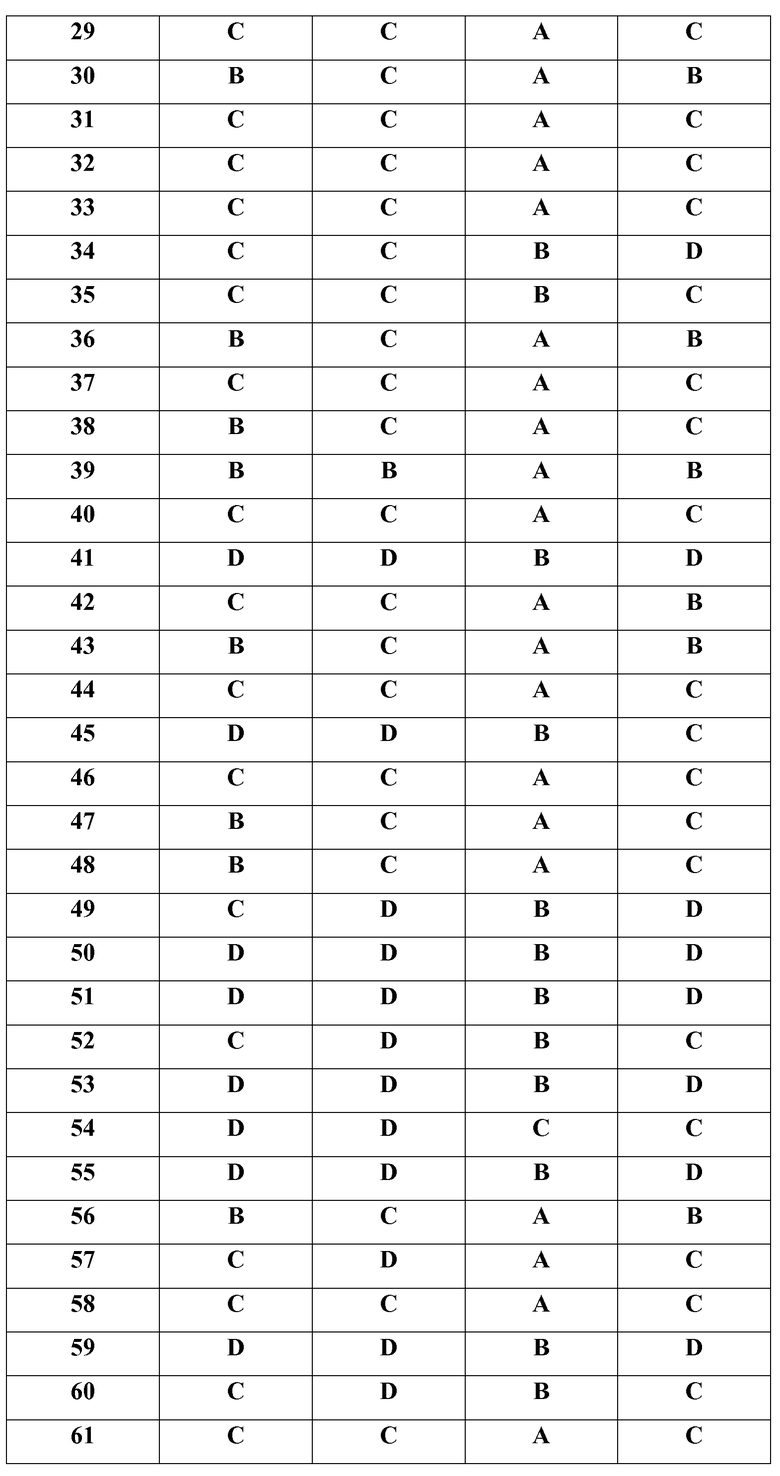
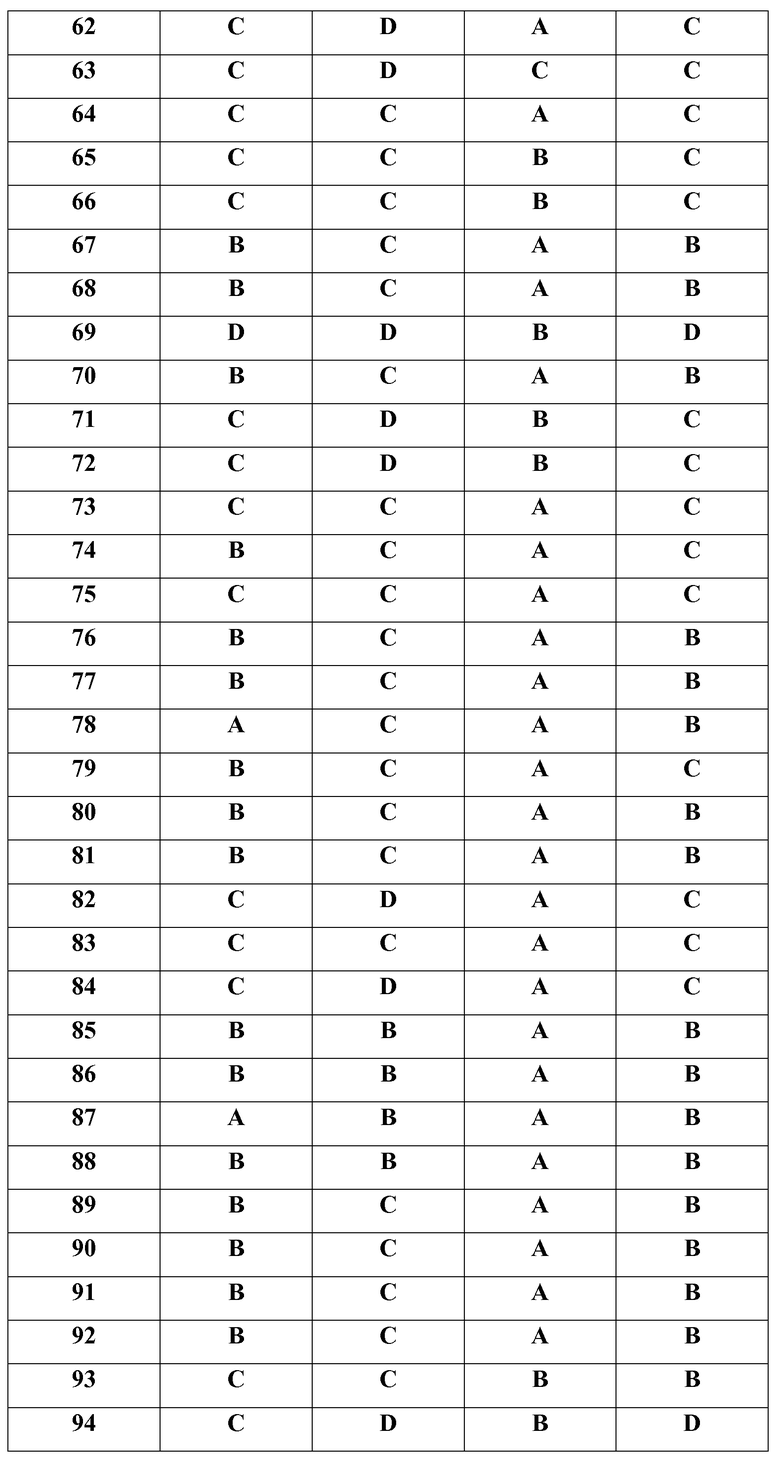
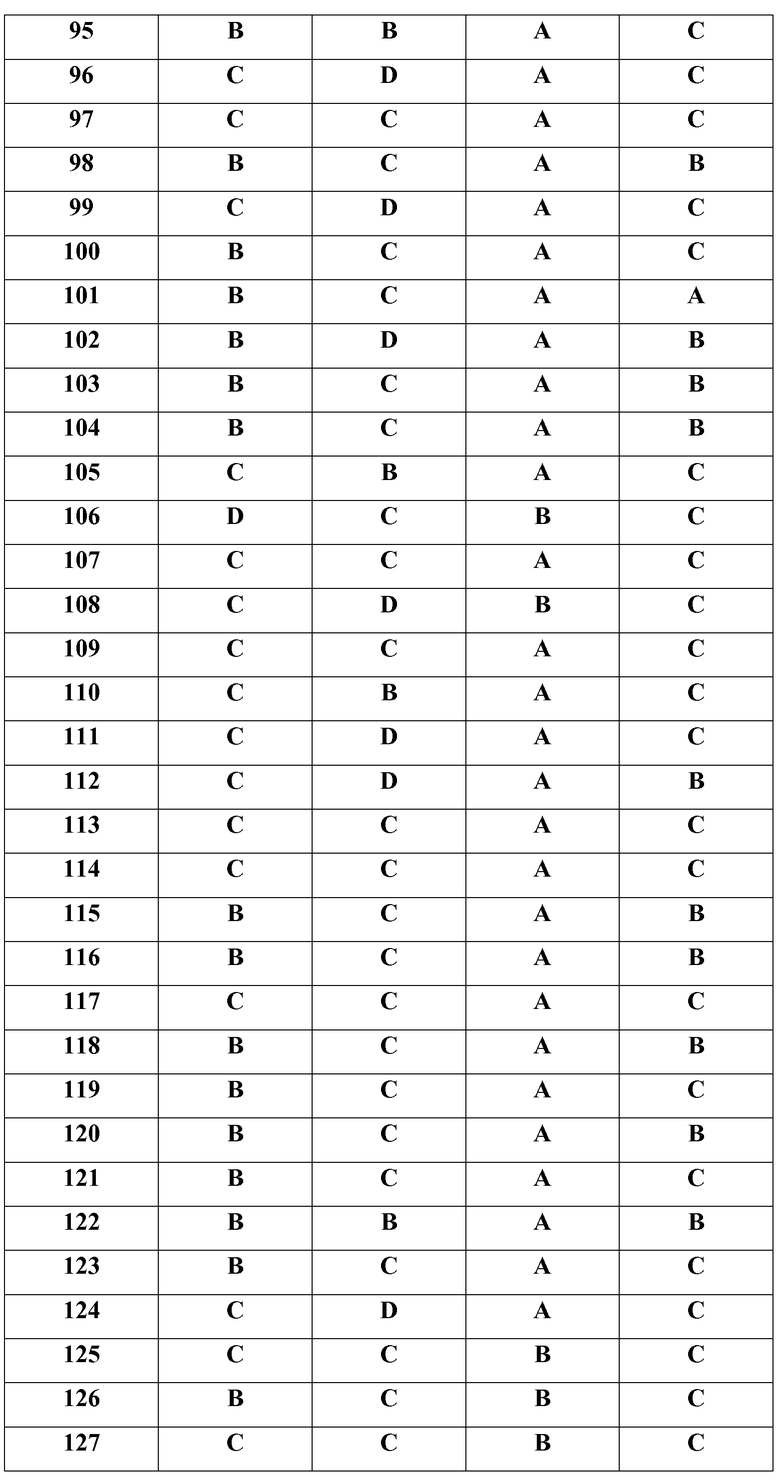
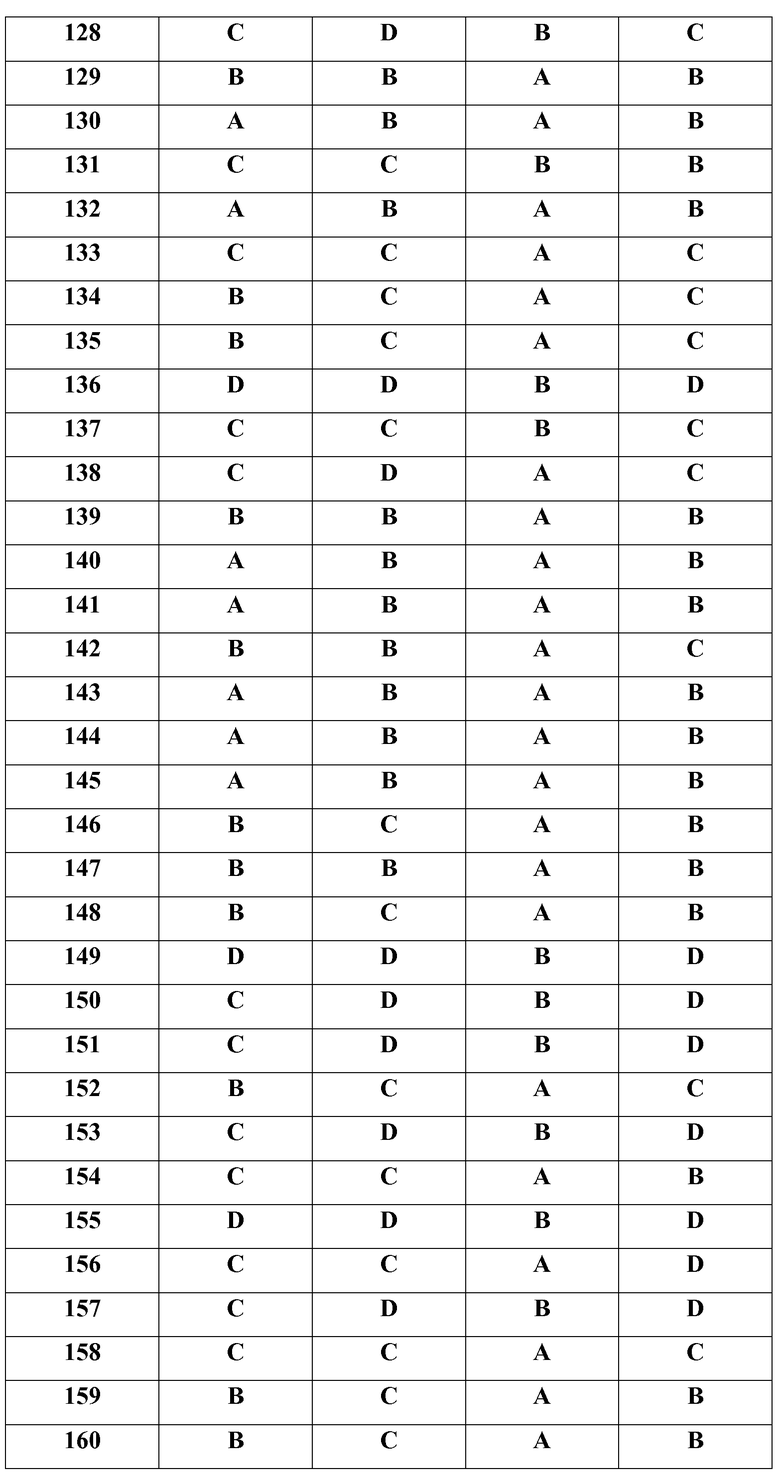
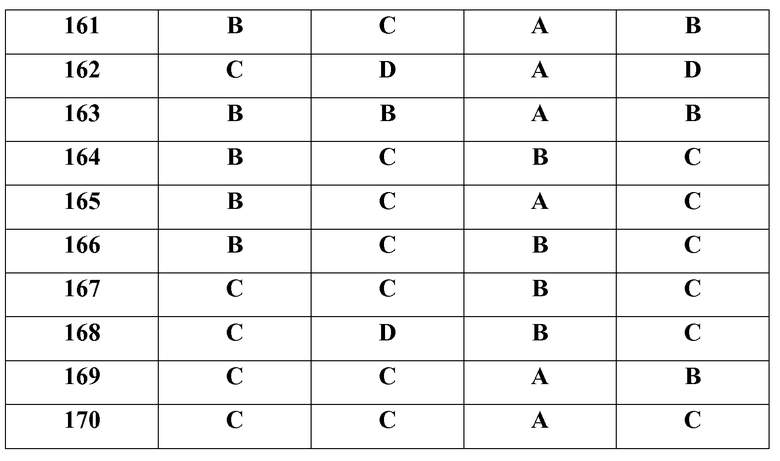
Клеточные анализы
pSTAT5 анализ
Принцип анализа
Фосфорилирование STAT5 представляет собой одно из ближайших событий в каскадной передаче сигнала, следующих за активацией JAK3. Поэтому фосфорилирование STAT5 является подходящим индикатором для оценки влияния ингибирования JAK3 на механизм передачи сигнала. Стимулирование человеческих клеток YT, которые являются NK-подобной клеточной линией, интерлейкином-2 (IL-2) приводит к фосфорилированию STAT5 по тирозиновому остатку 694 (Tyr694), которое можно измерить количественно путем иммунодетектирования с помощью специфичных антител и подходящей методики детектирования, в данном случае методики анализа AlphaScreen.
Протокол анализа
Культивирование и посев клеток
Человеческие клетки YT выращивали в среде RPMI (Lonza, BE12-167) с добавкой 2 мМ L-глутамина (Invitrogen, 25030-024) и 10% термически инактивированной FBS (Invitrogen, 10106-169) и хранили во влажном инкубаторе (37°C, 5% CO2). Клетки собирали центрифугированием, один раз промывали HBSS (Invitrogen, 14180-046), ресуспендировали в HBSS в концентрации 1,5×106 клеток/мл и высевали 0,9×104 клеток в объеме 6 мкл на лунку в 96-луночный белый планшет (PerkinElmer, 6005569).
Обработка тестовыми соединениями и стимулирование IL-2
Тестовые соединения растворяли в ДМСО и готовили серию образцов с последовательными разбавлениями 1:3 (9 ступеней). Для получения кривой зависимости реакции от дозы, 3 мкл соединения с концентрацией 4х в 4% ДМСО/HBSS добавляли к каждому образу клеток в 96 луночном планшете, получая конечную концентрацию ДМСО 1%. Клетки инкубировали в течение одного часа во влажном инкубаторе (37°C, 5% CO2). В каждую лунку добавляли 3 мкл раствора IL-2 с концентрацией 4х (рекомбинантный человеческий IL-2, Peprotech 200-02; 120 нМ раствор в HBSS) и инкубировали в течение 30 минут при комнатной температуре. Клетки подвергали лизису добавлением 3 мкл 5х буфера для лизиса (буфер для лизиса SureFire; Perkin Elmer, TGRS5S10K) и инкубировали при комнатной температуре в течение 10 минут при осторожном встряхивании.
Детектирование сигнала
Для детектирования сигнала в методике AlphaScreen® использовали набор SureFire Phospho-STAT5 (Tyr694/Tyr699) в соответствии с инструкцией производителя (Perkin Elmer, TGRS5S10K). Добавляли гранулы акцептора согласно рекомендациям производителя (реактивационный буфер/активационный буфер/акцепторные гранулы в соотношении 40:10:1) и инкубировали при комнатной температуре в течение 1,5 часов при осторожном встряхивании. Затем добавляли донорные гранулы, следуя рекомендациям (буфер для разбавления/донорные гранулы в соотношении 20:1) и инкубировали при комнатной температуре в течение 1,5 часов при осторожном встряхивании. Планшеты считывали на приборе Envision (Perkin Elmer) согласно протоколу AlphaScreen. Данные анализировали в программе BioAssay, используя нелинейную регрессию для сигмоидальной зависимости доза-реакция с переменным наклоном.
В таблице 9 приведены данные для избранных соединений по настоящему изобретению в клеточном анализе pSTAT5.
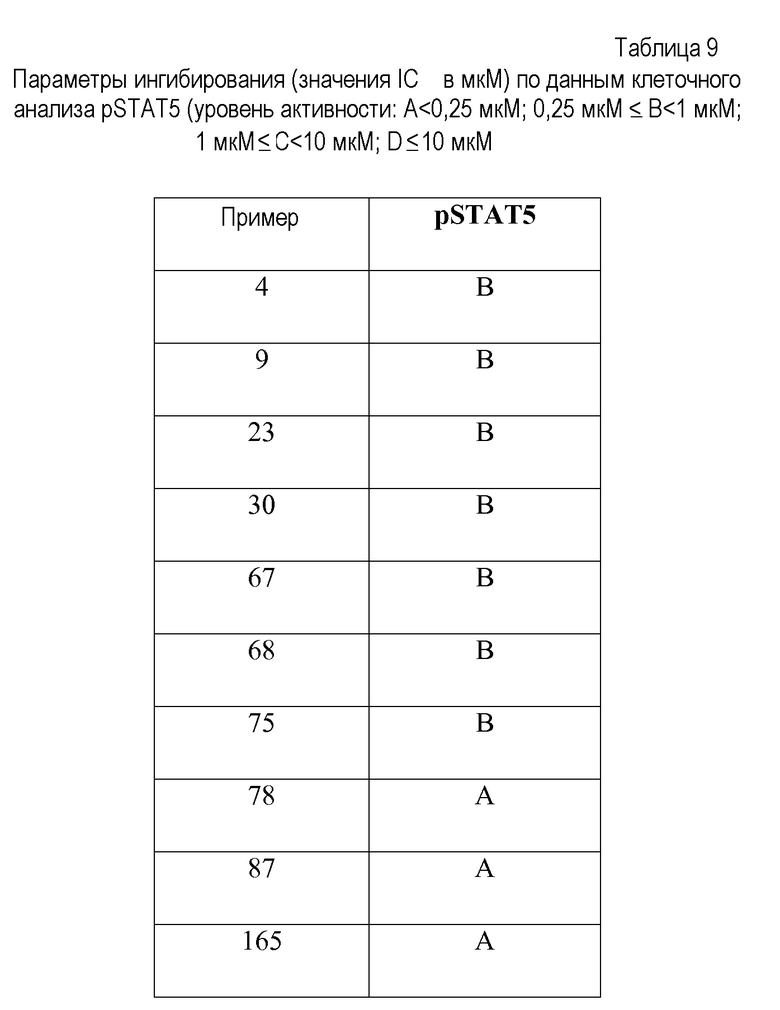
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЕТЕРОЦИКЛИЛЬНЫЕ ПИРИМИДИНОВЫЕ АНАЛОГИ В КАЧЕСТВЕ ИНГИБИТОРОВ Tук2 | 2013 |
|
RU2641895C2 |
| ПИРАЗОЛОПИРИМИДИНОВЫЕ СОЕДИНЕНИЯ-ИНГИБИТОРЫ JAK И СПОСОБЫ | 2009 |
|
RU2539568C2 |
| СОЕДИНЕНИЕ АМИНОПИРАЗОЛОПИРИМИДИНА, ИСПОЛЬЗУЕМОЕ В КАЧЕСТВЕ ИНГИБИТОРА ТИРОЗИНКИНАЗНОГО РЕЦЕПТОРА НЕЙРОТРОФИЧЕСКОГО ФАКТОРА | 2017 |
|
RU2764523C2 |
| ТИАЗОЛОПИРИМИДИНОНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ РЕЦЕПТОРОВ NMDA | 2014 |
|
RU2703273C2 |
| ИНГИБИТОРЫ СЕРИН/ТРЕОНИНОВЫХ КИНАЗ | 2013 |
|
RU2650501C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2015 |
|
RU2684102C2 |
| ИНГИБИРУЮЩИЕ JAK СОЕДИНЕНИЯ НА ОСНОВЕ ПИРАЗОЛОПИРИМИДИНА И СПОСОБЫ | 2010 |
|
RU2567238C2 |
| ИНГИБИРУЮЩИЕ JAK СОЕДИНЕНИЯ НА ОСНОВЕ ПИРАЗОЛОПИРИМИДИНА И СПОСОБЫ | 2010 |
|
RU2675857C2 |
| Селективный ингибитор киназы JAK1 | 2020 |
|
RU2818002C2 |
| ПРОИЗВОДНЫЕ ПИРИДАЗИНА В КАЧЕСТВЕ МОДУЛЯТОРОВ RORc | 2017 |
|
RU2757571C2 |
Изобретение относится к соединению структурной формулы (I), которое обладает ингибирующей активностью в отношении JAK киназ. В формуле (I) R представляет собой Н; F; Cl; СН3 или CF3; цикл А представляет собой 5-членный ароматический гетероцикл, в котором Z1, Z2 и Z3 независимо выбраны из группы, состоящей из C(R1); N и N(R1), при условии, что, как минимум, один из Z1, Z2, Z3 представляет собой N или N(R1); каждый из R1 независимо представляет собой Н, C(O)R2; Т1; C1-6алкил; где С1-6алкил необязательно замещен одним или несколькими R3, которые являются одинаковыми или различными; R2 выбран из Т1; R4, R4a независимо выбраны из группы, состоящей из Н; Т1; С1-6алкила; где С1-6алкил необязательно замещен одним или несколькими R5, которые являются одинаковыми или различными; Y0 представляет собой (CRY3RY4)n; n означает 0 или 1; одна из групп RY1; RY2; RY3; RY4 представляет собой RY0, и другие выбраны из группы, состоящей из Н и СН3; X1 представляет собой C(R6a) или N; X2 означает C(R6b) или N; X3 означает СН; X4 означает C(R6c); X5 означает C(R6d). Значения радикалов T1, R3, R5, RY5, RY5a, R6a, R6b, R6c, R6d, RY0, TY1 приведены в формуле изобретения. Изобретение также относится к фармацевтической композиции, содержащей указанные соединения, к соединению для применения в способе лечения или профилактики иммунологического, воспалительного, аутоиммунного или аллергического расстройства, или заболевания, связанного с отторжением трансплантата, и к способу лечения, регулирования, замедления начала или профилактики заболеваний и расстройств, связанных с JAK. 4 н. и 33 з.п. ф-лы, 9 табл.
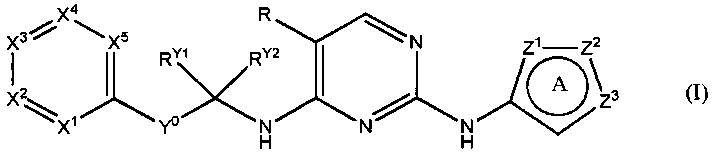
1. Соединение формулы (I)

или его фармацевтически приемлемая соль, где:
R представляет собой Н; F; Cl; СН3 или CF3;
цикл А представляет собой 5-членный ароматический гетероцикл, в котором Z1, Z2 и Z3 независимо выбраны из группы, состоящей из C(R1); N и N(R1), при условии, что, как минимум, один из Z1, Z2, Z3 представляет собой N или N(R1);
каждый из R1 независимо представляет собой Н, C(O)R2; Т1; C1-6алкил; где С1-6алкил необязательно замещен одним или несколькими R3, которые являются одинаковыми или различными;
R2 выбран из Т1;
R3 представляет собой галоген; С(О)OR4; OR4; C(O)R4; C(O)N(R4R4a) или N(R4R4a);
R4, R4a независимо выбраны из группы, состоящей из Н; Т1; С1-6алкила; где С1-6алкил необязательно замещен одним или несколькими R5, которые являются одинаковыми или различными;
R5 представляет собой CN; OR5a или N(R5aR5b);
R5a, R5b независимо выбраны из группы, состоящей из Н; C1-6алкила;
Т1 представляет собой С3циклоалкил; насыщенный 5-6-членный гетероциклил, содержащий 1-2 гетероатома, выбранные из N и О;
где группа Т1 необязательно замещена одним или несколькими R10, которые являются одинаковыми или различными;
Y0 представляет собой (CRY3RY4)n;
n означает 0 или 1;
одна из групп RY1; RY2; RY3; RY4 представляет собой RY0, и другие выбраны из группы, состоящей из Н и СН3;
RY0 представляет собой незамещенный С1-4алкил; CH2CH2ORY5; CH2ORY5; С(О)TY1; С(О)ORY5; или С(О)N(RY5RY5a);
RY5, RY5a независимо выбраны из группы, состоящей из Н; TY1; и С1-4алкила, где С1-4алкил необязательно замещен одним или несколькими RY6, которые являются одинаковыми или различными;
RY6 представляет собой галоген или ORY7;
RY7 выбран из С1-4алкила;
TY1 представляет собой незамещенный С5циклоалкил; или незамещенный насыщенный 5-6-членный гетероциклил, содержащий один гетероатом, выбранный из N;
X1 представляет собой C(R6a) или N; X2 означает C(R6b) или N; X3 означает СН; X4 означает C(R6c); X5 означает C(R6d);
R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из Н, галогена; OR7; Т2; С1-6алкила; где С1-6алкил необязательно замещен одним или несколькими R11, которые являются одинаковыми или различными;
R7 выбран из С1-6алкила;
R10 представляет собой оксо (=O) или С1-6алкил; R11 выбран из галогена;
Т2 представляет собой 5-6-членный гетероциклил, содержащий 2 гетероатома, выбранные из N или О; или 7-членный гетеробициклил, содержащий 2 гетероатома, выбранные из N или О, где фрагмент Т2 необязательно замещен одним или несколькими R17, которые являются одинаковыми или различными;
R17 выбран из группы, состоящей из оксо (=O), или C1-6алкила; при условии, что из этого определения исключены следующие соединения:
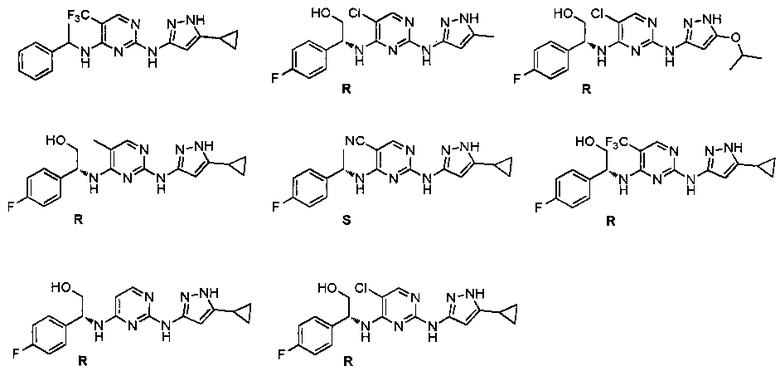
2. Соединение по п. 1, где n представляет собой 0.
3. Соединение по п. 1 или 2, где в формуле (I) RY1, RY2 и Y0 определяются таким образом, что формула (I) принимает вид формул (Ia), (Ib), (Ic) или (Id):
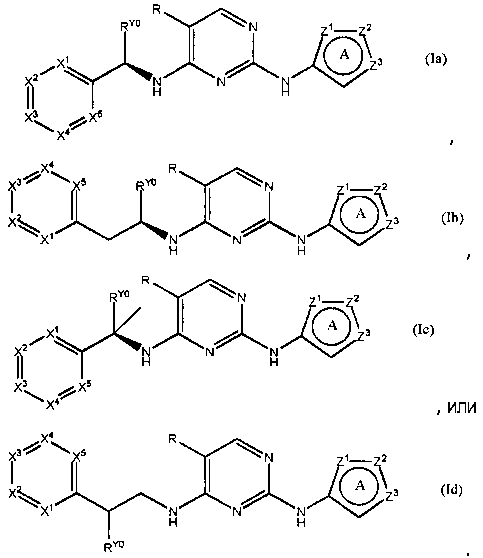
4. Соединение по п. 3, где Z2 представляет собой N(R1), причем R1 отличается от Н.
5. Соединение по п. 3, где в формуле (I) RY1, RY2 и Y0 определяются таким образом, что формула (I) принимает вид формулы (Ia).
6. Соединение по п. 1, где RY0 означает незамещенный С2-4алкил; CH2CH2ORY5; CH2ORY5; C(O)TY1; C(O)ORY5; или С(О)N(RY5RY5a).
7. Соединение по п. 1, где RY0 представляет собой СН2СН3; CH2ORY5; C(O)ORYS; С(О)N(RY5RY5a); или C(O)TY1.
8. Соединение по п. 1, где RY0 представляет собой CH2ORY5.
9. Соединение по п. 8, где RY0 представляет собой СН2ОН.
10. Соединение по п. 1, где цикл А является пирролильным или пиразолильным циклом.
11. Соединение по п. 1, где цикл А представляет собой
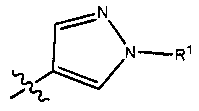 .
.
12. Соединение по п. 1, где цикл А является незамещенным или замещен одним или двумя заместителями R1, которые отличаются от Н и являются одинаковыми или различными.
13. Соединение по п. 1, где один из фрагментов Z1, Z2, Z3 представляют собой N(R1), и R1 отличается от Н.
14. Соединение по п. 1, где R1 означает незамещенный С1-4алкил; или С1-4алкил, замещенный одним или двумя фрагментами R3, которые являются одинаковыми или различными.
15. Соединение по п. 1, где R3 означает галоген; OR4; C(O)OR4; С(O)Т1; или C(O)N(R4R4a).
16. Соединение по п. 1, где R3 означает OR4; С(О)OR4; или C(O)N(R4R4a).
17. Соединение по п. 15 или 16, где R3 означает С(О)N(R4R4a).
18. Соединение по п. 1, где R означает F; Cl; CF3 или СН3.
19. Соединение по п. 18, где R означает Cl.
20. Соединение по п. 1, где ни один из фрагментов X1, X2, X4, X5 не является N.
21. Соединение по п. 1, где не более трех фрагментов из числа R6a, R6b, R6c, R6d отличаются от Н.
22. Соединение по п. 21, где ни один из фрагментов R6a, R6b, R6c, R6d не отличается от Н.
23. Соединение по п. 22, где один из фрагментов R6a, R6b, R6c, R6d отличается от Н.
24. Соединение по п. 1, где фрагменты R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из Н; галогена; CF3; OR7; или Т2.
25. Соединение по п. 1, где фрагменты R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из Н; галогена; или Т2.
26. Соединение по п. 1, где фрагменты R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из Н; и галогена.
27. Соединение по п. 26, где фрагменты R6a, R6b, R6c, R6d независимо выбраны из группы, состоящей из Н; и F.
28. Соединение по п. 1 или его фармацевтически приемлемая соль, выбранное из группы, состоящей из:
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
2-((5-фтор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-фтор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(R)-5-хлор-N2-(1-метил-1Н-пиразол-4-ил)-N4-(1-фенилпропил)пиримидин-2,4-диамина;
(S)-2-((2-((1-метил-1Н-пиразол-4-ил)амино)-5-(трифторметил)пиримидин-4-ил)амино)-2-фенилэтанола;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилпропан-1-ола;
2-((2-((1-метил-1Н-пиразол-4-ил)амино)-5-(трифторметил)пиримидин-4-ил)амино)-2-фенилпропан-1-ола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-3-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
2-((2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)-5-метилпиримидин-4-ил)амино)-2-фенилэтанола;
(S)-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиррол-2-ил)(морфолино)метанона;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-3-фенилпропан-1-ола;
метил 2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилацетата;
метил 2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилацетата;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилуксусной кислоты;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилуксусной кислоты;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-3-фенилпропан-1-ола;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-метил-2-фенилацетамида;
(S)-изопропил 2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетата;
(S)-этил 2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетата;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)уксусной кислоты;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N,N-диметил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N,N-диметил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-этил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-этил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-(2-метоксиэтил)-2-фенилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N,N-диметилацетамида;
2-(4-((5-хлор-4-((1-(2,б-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
2-(4-((5-хлор-4-((1-(3-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенил-1-(пирролидин-1-ил)этанона;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенил-1-(пирролидин-1-ил)этанона;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
1-(4-((5-хлор-4-((1-(3-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)пропан-2-ола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-3-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
1-(4-((5-хлор-4-((1-(2,6-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)пропан-2-ола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2,б-дифторфенил)этанола;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2,6-дифторфенил)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-3-ил)амино)пиримидин-4-ил)амино)-2-(2,6-дифторфенил)этанола;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-(2-гидроксиэтил)-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-(2-гидроксиэтил)-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-(2-метоксиэтил)-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенил-1-(пиперидин-1-ил)этанона;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-3-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенил-1-(пиперидин-1-ил)этанона;
2-(3-(2-окса-6-азаспиро[3.3]гептан-6-ил)фенил)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-5-хлор-N4-(2-метокси-1-фенилэтил)-N2-(1-метил-1Н-пиразол-4-ил)пиримидин-2,4-диамина;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
1-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-2-метилпропан-2-ола;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-циклопентил-2-фенилацетамида;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-N-циклопентил-2-фенилацетамида;
1-(4-((5-хлор-4-((1-(3-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-2-метилпропан-2-ола;
1-(4-((5-хлор-4-((1-(2,6-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-2-метилпропан-2-ола;
3-(4-((5-хлор-4-((1-(2-фторфнил)2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)пропан-1-ола;
(R)-3-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино-3-фенилпропан-1-ола;
(R)-2-(4-((5-хлор-4-((3-гидрокси-1-фенилпропил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-изопропилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-циклопропилацетамида;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-(1-метил-1Н-пиразол-4-ил)фенил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-(цианометил)-N-метилацетамида;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(4-фторфенил)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(4-фторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-2-метилпропанамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-метоксифенил)этанола;
(S)-2-((2-((1Н-пиразол-4-ил)амино)-5-хлорпиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
(S)-2-((2-((1Н-пиразол-4-ил)амино)-5-хлорпиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-2-ил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(пиридин-2-ил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-метоксифенил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(3-метоксифенил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(3-фторфенил)-2-гидрокиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
(S)-2-((2-((1Н-пиразол-4-ил)амино)-5-хлорпиримидин-4-ил)амино)-2-(3-фторфенил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-(2-(диметиламино)этил)ацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-(3-(диметиламино)пропил)ацетамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-3-ил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-3-ил)этанола;
2-(3-бромфенил)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-
пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-(1-метил-1Н-пиразол-4-ил)фенил)этанола;
(S)-2-((5-хлор-2-((1-этил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-этил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-этил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-3-ил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(2-метоксифенил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(3-метоксифенил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(2-метоксифенил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(3-метоксифенил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(пиридин-3-ил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-((5-хлор-2-((1-изопропил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-изопропил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-метоксифенил)этанола;
(S)-2-((5-хлор-2-((1-изопропил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(пиридин-3-ил)этанола;
(S)-2-(4-((5-фтор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
(S)-2-((5-хлор-2-((1-этил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((5-хлор-2-((1-изопропил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-(4-((5-фтор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-фтор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-((2-((1-(3-аминопропил)-1Н-пиразол-4-ил)амино)-5-хлорпиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-((5-хлор-2-((1-(2-изопропоксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-фенилэтанола;
(S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-изопропилацетамида;
2-(4-((5-хлор-4-(((S)-1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино-1Н-пиразол-1-ил)-N-((S)-1-гидроксипропан-2-ил)ацетамида;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-хлорфенил)этанола;
2-(4-((5-хлор-4-((1-(2-хлорфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
2-(4-((5-хлор-4-((1-(2-хлорфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-хлорфенил)этанола;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
2-(4-((5-хлор-4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
4-(3-(1-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-гидроксиэтил)фенил)морфолин-3-она;
5-хлор-N4-(1-(2-фторфенил)пропил)-N2-(1-метил-1Н-пиразол-4-ил)пиримидин-2,4-диамина;
2-(4-((5-хлор-4-((1-(2-фторфенил)пропил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)-N,N-диметилацетамида;
2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)-N-(2,2,2-трифторэтил)ацетамида;
2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2,5-дифторфенил)этанола;
2-(4-((5-хлор-4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
2-(4-((5-хлор-4-((2-гидрокси-1-(2-(трифторметил)фенил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
2-(4-((5-хлор-4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
(S)-2-(4-((4-((2-гидрокси-1-фенилэтил)амино)-5-метилпиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((4-((2-гидрокси-1-фенилэтил)амино)-5-метилпиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N,N-диметилацетамида;
3-(4-((5-хлор-4-(((S)-2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-1-метилпирролидин-2-она;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-(1-метил-1Н-пиразол-4-ил)фенил)этанола;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фтор-5-(1-метил-1Н-пиразол-4-ил)фенил)этанола;
(S)-4-(3-(1-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-гидроксиэтил)фенил)морфолин-3-она;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2,5-дифторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
(S)-2-(4-((5-хлор-4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
(S)-2-(4-((5-хлор-4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
(S)-2-(4-((5-хлор-4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(2,5-дифторфенил)-2-((5-фтор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(2,5-дифторфенил)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(4-((4-((1-(2,5-дифторфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(3-(1-метил-1Н-пиразол-4-ил)фенил)-2-((5-метил-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-((5-фтор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фтор-5-(1-метил-1Н-пиразол-4-ил)фенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-(1-метил-1Н-пиразол-4-ил)фенил)этанола;
(S)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фтор-5-(1-метил-1Н-пиразол-4-ил)фенил)этанола;
(S)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(3-фтор-5-(1-метил-1Н-пиразол-4-ил)фенил)этанола;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(3-(1-метил-1Н-пиразол-4-ил)фенил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-фтор-4-((2-гидрокси-1-(3-(1-метил-1Н-пиразол-4-ил)фенил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-хлор-4-((1-(3-фтор-5-(1-метил-1Н-пиразол-4-ил)фенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((5-фтор-4-((1-(3-фтор-5-(1-метил-1Н-пиразол-4-ил)фенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(3,5-дифторфенил)-2-((5-фтор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3,5-дифторфенил)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(4-((4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1Н-пиразол-1-ил)ацетамида;
(S)-2-(4-((4-((1-(3,5-дифторфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-4-(3-(1-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-гидроксиэтил)-2-фторфенил)морфолин-3-она;
(S)-2-(2,5-дифторфенил)-2-((5-метил-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3,5-дифторфенил)-2-((5-метил-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-((5-хлор-2-((1-(2,2-дифторэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)-2-(2-фторфенил)этанола;
(S)-2-((2-((1-(2,2-дифторэтил)-1Н-пиразол-4-ил)амино)-5-метилпиримидин-4-ил)амино)-2-(2,5-дифторфенил)этанола;
(S)-2-((2-((1-(2,2-дифторэтил)-1Н-пиразол-4-ил)амино)-5-метилпиримидин-4-ил)амино)-2-(3,5-дифторфенил)этанола;
2-((2-((1-(2,2-дифторэтил)-1Н-пиразол-4-ил)амино)-5-метилпиримидин-4-ил)амино)-2-(2,6-дифторфенил)этанола;
2-(4-((4-((1-(2,6-дифторфенил)-2-гидроксиэтил)амино)-5-метилпиримидин-2-ил)амино-1Н-пиразол-1-ил)-1-морфолиноэтанона;
(S)-2-(4-((5-хлор-4-((2-гидрокси-1-(пиридин-3-ил)этил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(3-бромфенил)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бром-5-фторфенил)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бромфенил)-2-((5-метил-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бром-5-фторфенил)-2-((5-фтор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бромфенил)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бром-5-фторфенил)-2-((5-хлор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(3-бром-5-фторфенил)-2-((5-фтор-2-((1-(2-гидроксиэтил)-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола;
(S)-2-(4-((4-((1-(3-бромфенил)-2-гидроксиэтил)амино)-5-хлорпиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((4-((1-(3-бромфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((4-((1-(3-бром-5-фторфенил)-2-гидроксиэтил)амино)-5-хлорпиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида;
(S)-2-(4-((4-((1-(3-бром-5-фторфенил)-2-гидроксиэтил)амино)-5-фторпиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамида; и
2-(3-бромфенил)-2-((5-хлор-2-((1-метил-1Н-пиразол-4-ил)амино)пиримидин-4-ил)амино)этанола.
29. Соединение по п. 1 или его фармацевтически приемлемая соль, которое представляет собой (S)-2-(4-((5-хлор-4-((2-гидрокси-1-фенилэтил)амино)пиримидин-2-ил)амино)-1Н-пиразол-1-ил)-N-метилацетамид:
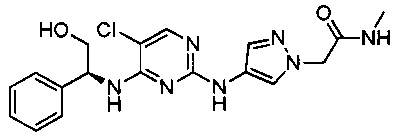
30. Соединение по п. 1 или его фармацевтически приемлемая соль, которое представляет собой (S)-2-(4-((5-хлор-4-((1-(2-фторфенил)-2-гидроксиэтил)амино)пиримидин-2-ил)амино-1Н-пиразол-1-ил)ацетамид:
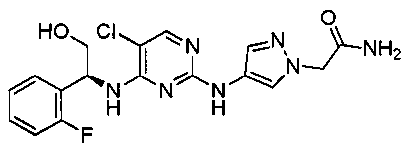
31. Фармацевтическая композиция, обладающая ингибирующей активностью в отношении JAK киназ, содержащая соединение, его фармацевтически приемлемую соль по любому из пп. 1-30, наряду с фармацевтически приемлемым носителем.
32. Соединение или его фармацевтически приемлемая соль по п. 1 для применения в качестве лекарственного средства, обладающего ингибирующей активностью в отношении JAK киназ.
33. Соединение или его фармацевтически приемлемая соль по п. 1 для применения в способе лечения или профилактики заболевания или расстройства, связанного с JAK.
34. Соединение или его фармацевтически приемлемая соль по п. 1 для применения в способе лечения или профилактики иммунологического, воспалительного, аутоиммунного или аллергического расстройства, или заболевания, связанного с отторжением трансплантата, или реакции «трансплантат против хозяина», опосредованного активностью JAK киназ.
35. Соединение или его фармацевтически приемлемая соль по п. 1 для применения в способе лечения или профилактики пролиферативного заболевания, опосредованного активностью JAK киназ.
36. Применение соединения по любому из пп. 1-30 или его фармацевтически приемлемой соли для получения лекарственного средства, предназначенного для лечения или профилактики заболеваний и расстройств, связанных с JAK.
37. Способ лечения, регулирования, замедления начала или профилактики у пациента из числа млекопитающих, при наличии такой необходимости, одного или нескольких состояний, выбранных из группы, состоящей из заболеваний и расстройств, связанных с JAK, включающий введение указанному пациенту терапевтически эффективного количества соединения по любому из пп. 1-30 или его фармацевтически приемлемой соли.
| CRTOMIR PODLIPNIK ET AL., DFG-in and DFG-out homology models of TrkB kinase receptor: Induced-fit and ensemble docking, Journal of molecular graphics and modeling, 29, 2010, p.309-320 | |||
| EA200901250 A1, 30.04.2010 | |||
| Устройство для контроля за процессом абразивно-электроэрозионной обработки | 1982 |
|
SU1054004A1 |
| WO2006117560 A1, 09.11.2006 | |||
| WO 2010146133 A1, 23.12.2010 | |||
Авторы
Даты
2015-09-27—Публикация
2012-07-24—Подача