ОБЛАСТЬ ТЕХНИКИ
[0001] Изобретение относится к активному материалу для положительного электрода натриевого аккумулятора и способу изготовления такого активного материала.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
[0002] В последние годы, в связи со стремительным распространением информационных устройств, таких, как персональные компьютеры, видеокамеры и мобильные телефоны, все более получает признание важность разработки усовершенствованных аккумуляторных батарей для использования в качестве источников питания в этих устройствах. В автомобильной промышленности также делаются успехи в разработке мощных и высокоемкостных аккумуляторных батарей для электрических и гибридных автомобилей. Из числа различных типов аккумуляторов, существующих в настоящее время, особенное внимание уделяется литиевым аккумуляторам в связи с их высокой энергоемкостью и мощностью.
[0003] В литиевом аккумуляторе активным материалом для положительного электрода в основном является сложный оксид лития, имеющий слоистую структуру, включающую, например, никелат лития и кобальтат лития. Активным материалом для отрицательного электрода обычно является, например, углеродный материал, способный интеркалировать и деинтеркалировать ионы лития, металлический литий или сплав лития. Электролит, помещенный между положительным и отрицательным электродами в основном является, например, раствором электролита, содержащим в себе растворенную литиевую соль, или литий-содержащим твердым электролитом.
Несмотря на то, что литиевые аккумуляторы обладают, как указано выше, отличной энергоемкостью и мощностью, растущая цена на литий, связанная с постоянно повышающимся спросом на литиевые аккумуляторы и тем фактом, что геологические резервы лития ограничены, является узким местом для массового производства и расширения производства.
[0004] В связи с этим проводятся исследования в области натриевых аккумуляторов, использующих натрий - природные месторождения которого обширны, а стоимость низка - вместо лития (см., например, Патентный документ 1 и Непатентные документы с 1 по 4).
Например, Патентный документ 1 описывает активные материалы для положительного электрода для вторичных батарей с безводным электролитом следующей формулы: MaxMbyP2O7 (где Ma - это Na, Li, Ca или Mg, Mb - является переходным металлом, имеющим постоянную валентность от 4 и выше, 0≤x≤4; 0,5≤y≤3 и 6≤z≤14). В демонстрационных примерах Патентного документа №1 было описано изготовление и дана оценка материала MoP2O7.
[0005] Патентный документ 1: Публикация японской патентной заявки №2004-158348
Патентный документ 2: Публикация японской патентной заявки №2005-183395
[0006] Непатентный документ 1: Реферат №389, 218-я Конференция Электрохимического общества (ECS), Электрохимическое общество (2010)
Непатентный документ 2: LiBD-5 2011 - Электродные материалы - Аркашон, Франция; 12-17 июня 2011 г.
Непатентный документ 3: Electrochemistry Communications, 12 (2010), 355-358
Непатентный документ 4: Nature Материалы DOI; 10.1038/NMAT2920
Непатентный документ 5: Richiumu niji-denchi (Lithium secondary batteries), written and edited by Zenpachi OGUMI (Ohmsha), p.77
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0007] Однако, когда материалы MoP2O7, изготовленные и оцененные в демонстрационных примерах Патентного документа 1, используются как активный материал для положительного электрода в натриевых аккумуляторах, существенным недостатком является низкое рабочее напряжение. Кроме того, как указано в Непатентных документах с 1 по 4, активные материалы для положительного электрода натриевых аккумуляторов, которые широко используются в настоящее время, обеспечивают в лучшем случае рабочее напряжение около 3,5 В.
[0008] Патентный документ 2 описывает в качестве активного материала для литиевых аккумуляторов (Li4Ni3(PO4)2(P2O7), однако этот материал не является активным материалом для положительного электрода натриевых аккумуляторов, а Непатентный документ 5 описывает LiCoO2 с рабочим напряжением около 4 В.
[0009] Поскольку MoP2O7, изготовленный и оцененный в Патентном документе 1, не содержит Na, при его использовании в качестве активного материала для положительного электрода в натриевом аккумуляторе работа натриевого аккумулятора должна начинаться с захвата ионов Na (разряжающей реакции). По этой причине активный материал для отрицательного электрода должен использоваться совместно с таким активным материалом для положительного электрода, который уже содержит Na. Однако в настоящее время не известен Na-содержащий активный материал для отрицательного электрода, который работает при низком напряжении и способен обеспечить достаточную электродвижущую силу, и разработка такого активного материала для практического использования сопряжена с существенными трудностями.
[0010] Настоящее изобретение разрабатывалось в свете вышеизложенных обстоятельств. Задачей изобретения является создание активного материала для положительного электрода для натриевых аккумуляторов, который имеет высокое рабочее напряжение и может быть заряжаем и разряжаем при высоком напряжении; другой задачей изобретения является разработка способа изготовления такого активного материала.
[0011] Активный материал для положительного электрода натриевого аккумулятора, согласно настоящему изобретению, представлен ниже общей формулой (1):
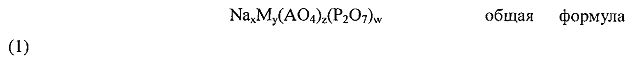
(В формуле (1) М представляет, по меньшей мере, один из элементов, выбранный из группы, состоящей из титана (Ti), ванадия (V), хрома (Cr), марганца (Mn), железа (Fe), кобальта (Со), никеля (Ni), меди (Cu) и цинка (Zn); А - по меньшей мере, один из элементов, выбранный из группы, состоящей из алюминия (Al), кремния (Si), фосфора (Р), серы (S), титана (Ti), ванадия (V) и вольфрама (W); x удовлетворяет условию 4≥x≥2; y удовлетворяет условию 4≥y≥1, z удовлетворяет условию 4≥z≥0; w удовлетворяет условию 1≥w≥0; и, по меньшей мере, один из индексов z и w больше или равен 1.)
[0012] Активный материал для положительного электрода натриевого аккумулятора, согласно настоящему изобретению, имеет высокое рабочее напряжение и обеспечивает высокую энергоемкость натриевого аккумулятора.
[0013] В приведенной выше формуле (1) предпочтительно, чтобы М был двухвалентным до зарядки по той причине, что М во время зарядки становится трехвалентным или более высокой степени окисления, что делает возможным для аккумулятора работать при высоком напряжении.
[0014] Предпочтительно, чтобы активный материал для положительного электрода натриевого аккумулятора, согласно настоящему изобретению, имел кристаллическую структуру, принадлежащую к пространственной группе Pn21a. Это обусловлено тем, что, когда активный материал для положительного электрода имеет кристаллическую структуру, принадлежащую к пространственной группе Pn21a, все ионы Na внутри кристаллической структуры ориентированы в направлении оси «а», оси «b» или оси «c», что является очень благоприятным для переноса ионов Na.
[0015] В предпочтительном варианте активного материала для положительного электрода натриевого аккумулятора согласно настоящему изобретению, М в приведенной выше формуле (1) является, по меньшей мере, одним из элементов, выбранным из группы, состоящей из Mn, Co и Ni, при этом его некоторая часть может быть заменена, по меньшей мере, одним из элементов, который отличается от М, и который выбран из группы, состоящей из Ti, V, Cr, Mn, Fe, Со, Ni, Cu и Zn. Активный материал для положительного электрода натриевого аккумулятора, согласно настоящему варианту осуществления изобретения, изначально имеет кристаллическую структуру, принадлежащую к пространственной группе Pn21a, и имеет прекрасную проводимость ионов Na.
В наиболее предпочтительном варианте осуществления активного материала для положительного электрода натриевого аккумулятора, согласно настоящему изобретению, M в приведенной выше формуле (1) представлен Ni, при этом некоторая часть Ni может быть заменена, по меньшей мере, одним из элементов, выбранным из группы, состоящей из Ti, V, Cr, Mn, Fe, Co, Cu и Zn.
[0016] В другом предпочтительном варианте осуществления активного материала для положительного электрода натриевого аккумулятора, согласно настоящему изобретению, A в приведенной выше формуле (1) является, по меньшей мере, одним из элементов, выбранным из группы, состоящей из Si, Р и S, при этом его некоторая часть может быть заменена, по меньшей мере, одним из элементов, который отличается от A, и который выбран из группы, состоящей из Al, Si, Р, S, Ti, V и W. Активный материал для положительного электрода натриевого аккумулятора, согласно настоящему варианту осуществления изобретения, изначально имеет кристаллическую структуру, принадлежащую к пространственной группе Pn21a, и имеет прекрасную проводимость ионов Na.
В наиболее предпочтительном варианте осуществления активного материала для положительного электрода натриевого аккумулятора, согласно настоящему изобретению, a в формуле (1) представляет собой Р, при этом некоторая часть Р может быть заменена, по меньшей мере, одним из элементов, выбранным из группы, состоящей из Al, Si, S, Ti, V и W.
[0017] Примеры активного материала для положительного электрода натриевого аккумулятора, согласно настоящему изобретению, включают соединения, представленные общей формулой Na4Ni3(PO4)2(P2O7), соединения, представленные общей формулой Na4Mn3(PO4)2(P2O7), соединения, представленные общей формулой Na4Co3(PO4)2(P2O7), соединения, представленные общей формулой Na4Co(3-a)Mna(PO4)2(P2O7) (где 'а' удовлетворяет условию 0,3≤а≤0,8) и соединения, представленные общей формулой Na4Co(3-b-c)MnbNic(PO4)2(P2O7) (где 'b' удовлетворяет условию 0,3≤b≤1,0, и 'с' удовлетворяет условию 0,3≤с≤1,0).
[0018] Способ изготовления активного материала для положительного электрода натриевого аккумулятора по настоящему изобретению включает:
этап предварительного обжига смеси исходных материалов, содержащей, по меньшей мере, Na-содержащее соединение, M-содержащее соединение, включающее вышеупомянутый элемент M, A-содержащее соединение, включающее вышеупомянутый элемент A, и P-содержащее соединение в атмосферном воздухе при температуре от 150 до 500°C; и
этап основного обжига полученного таким образом предварительно обожженного материала в атмосферном воздухе при температуре от 500 до 800°C после выполнения этапа предварительного обжига.
Способ изготовления активного материала для положительного электрода натриевого аккумулятора по настоящему изобретению может также включать перед этапом предварительного обжига, этап уменьшения размера частиц Na-содержащего соединения, M-содержащего соединения, A-содержащего соединения и P-содержащего соединения.
[0019] Настоящее изобретение обеспечивает возможность создания активного материала для положительного электрода для натриевых аккумуляторов, который имеет высокое рабочее напряжение и может быть заряжаем и разряжаем при высоком напряжении. Использование активного материала для положительного электрода для натриевых аккумуляторов по настоящему изобретению делает возможным достижение высокой энергоемкости в натриевых аккумуляторах.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
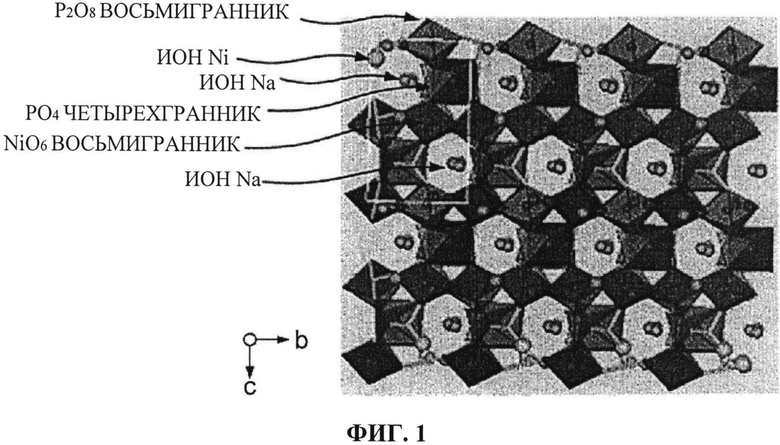
[0020] [ФИГ. 1] ФИГ. 1 отображает кристаллическую структуру пространственной группы Pn21a, вид по оси «а».
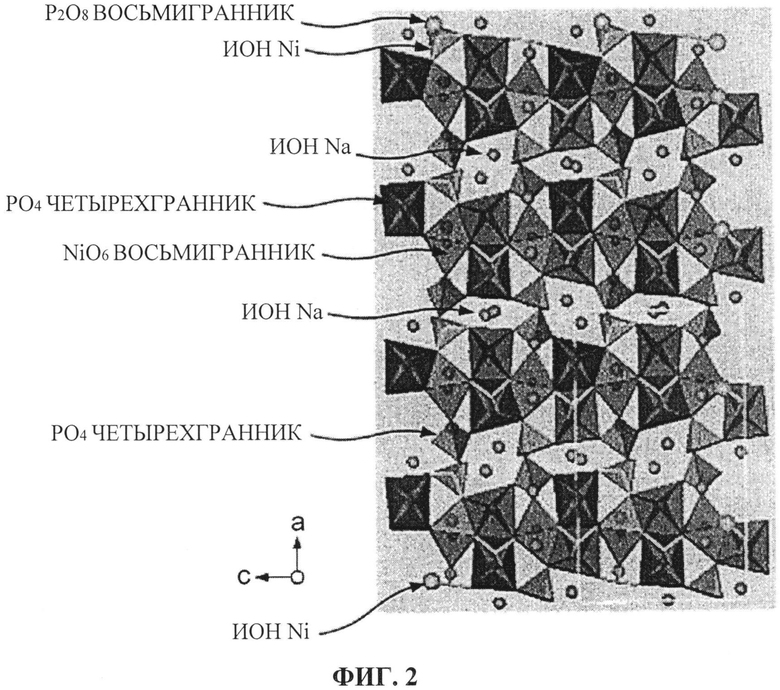
[ФИГ. 2] ФИГ. 2 отображает кристаллическую структуру пространственной группы Pn21a, вид по оси «b».
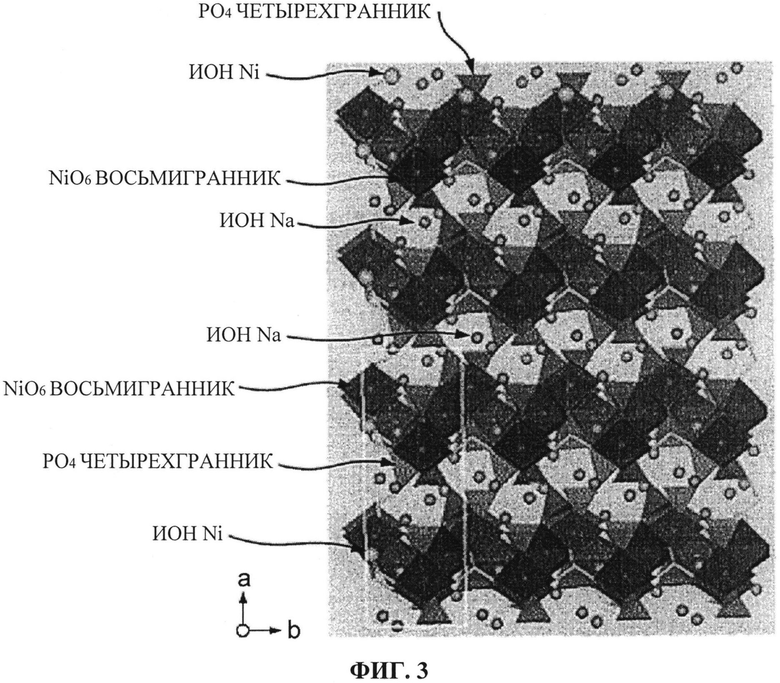
[ФИГ. 3] ФИГ. 3 отображает кристаллическую структуру пространственной группы Pn21a, вид по оси «c».
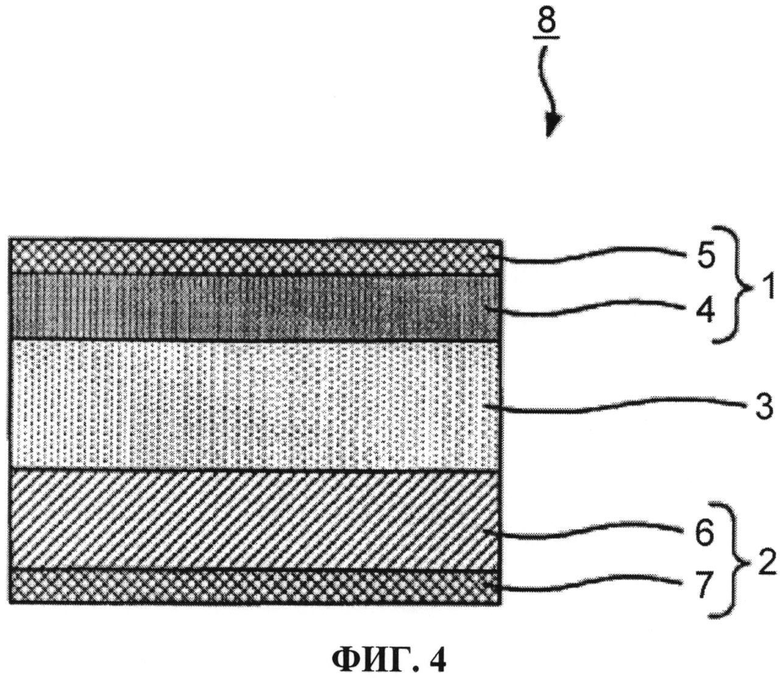
[ФИГ. 4] ФИГ. 4 представляет собой схематический вид в поперечном разрезе одного из вариантов осуществления натриевого аккумулятора.
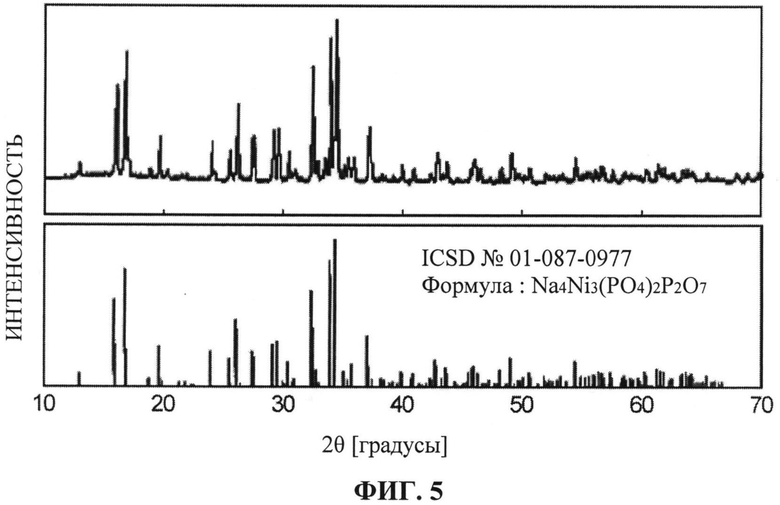
[ФИГ. 5] ФИГ. 5 отображает рентгенограмму для активного материала для положительного электрода, синтезированного в Примере 1.
[ФИГ. 6] ФИГ. 6 отображает результаты измерений силы тока от напряжения при металлическом Na, выполняющим функцию противоэлектрода, при использовании положительного электрода, изготовленного с использованием активного материала для положительного электрода, синтезированного в Примере 1.
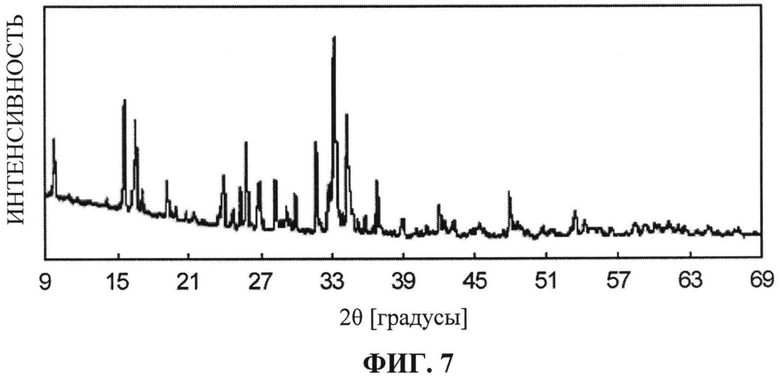
[ФИГ. 7] ФИГ. 7 отображает рентгенограмму для активного материала для положительного электрода, синтезированного в Примере 2.
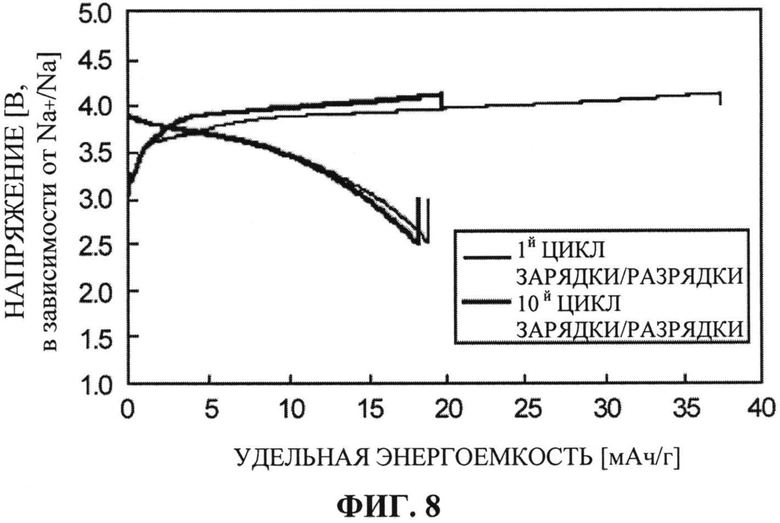
[ФИГ. 8] ФИГ. 8 отображает зарядно-разрядные характеристики (удельная энергоемкость по отношению к напряжению) при использовании положительного электрода, изготовленного из активного материала для положительного электрода, синтезированного в Примере 2.
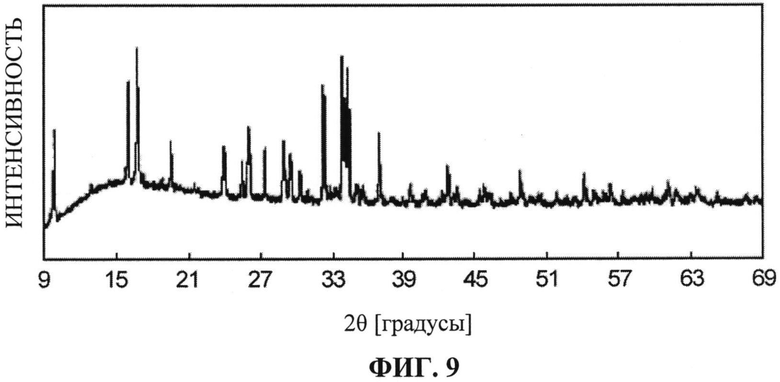
[ФИГ. 9] ФИГ. 9 отображает рентгенограмму для активного материала для положительного электрода, синтезированного в Примере 3.
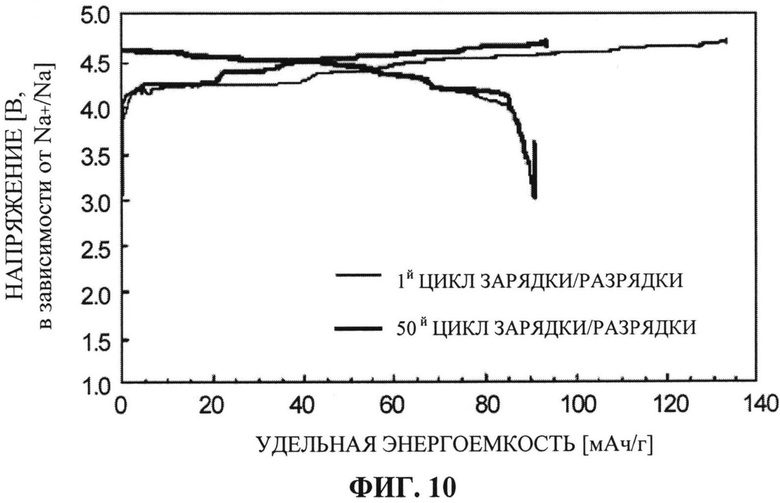
[ФИГ. 10] ФИГ. 10 отображает зарядно-разрядные характеристики (удельная энергоемкость по отношению к напряжению) при использовании положительного электрода, изготовленного из активного материала для положительного электрода, синтезированного в Примере 3.
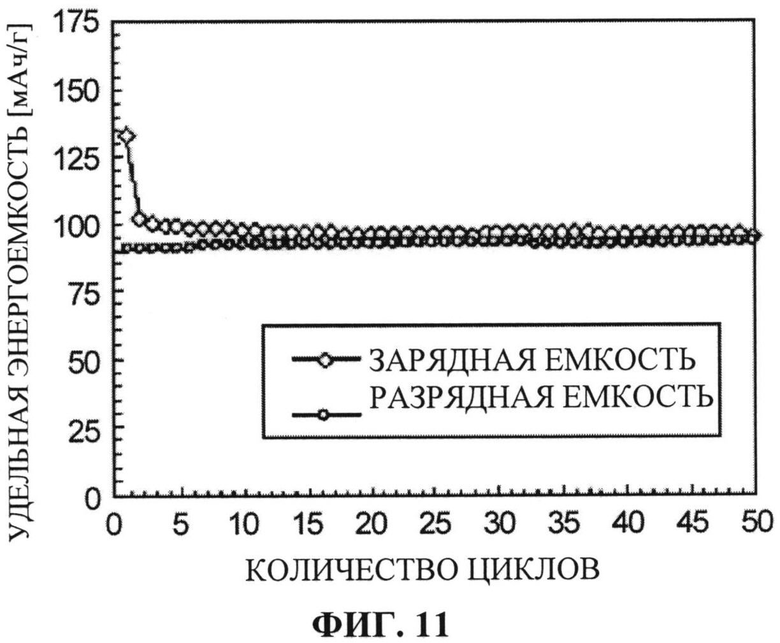
[ФИГ. 11] ФИГ. 11 отображает поцикловую характеристику (количество циклов по отношению к зарядно-разрядной удельной энергоемкости) при использовании положительного электрода, изготовленного из активного материала для положительного электрода, синтезированного в Примере 3.
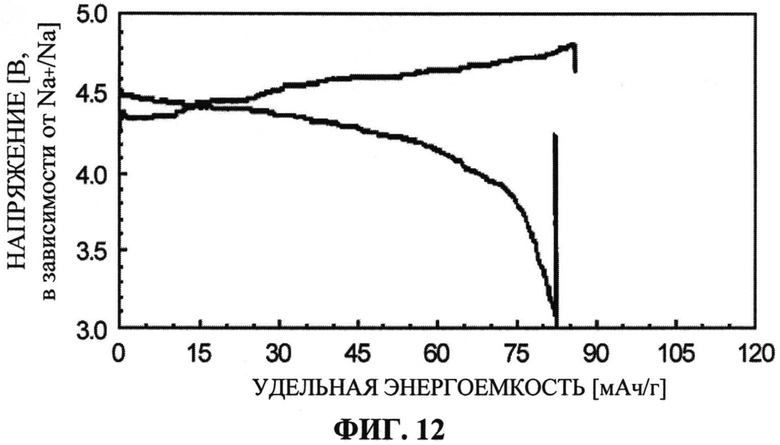
[ФИГ. 12] ФИГ. 12 отображает зарядно-разрядные характеристики (удельная энергоемкость по отношению к напряжению) при использовании положительного электрода, изготовленного из активного материала для положительного электрода, синтезированного в Примере 3.
[ФИГ. 13] ФИГ. 13 отображает результаты оценочных испытаний зарядно-разрядных характеристик при использовании положительных электродов, изготовленных с применением активных материалов для положительного электрода, синтезированных в Примерах с 4 по 8.
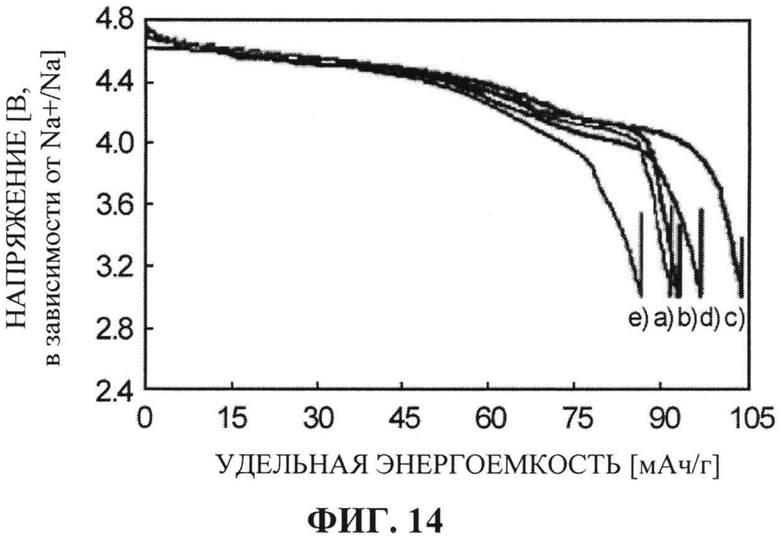
[ФИГ. 14] ФИГ. 14 отображает кривые разрядки при использовании положительных электродов, изготовленных с применением активных материалов для положительного электрода, синтезированных в Примерах с 4 по 8.
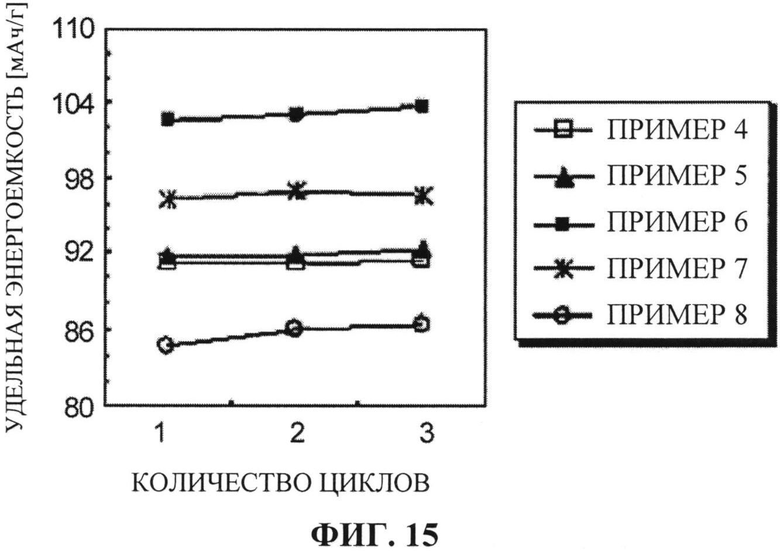
[ФИГ. 15] ФИГ. 15 отображает поцикловые характеристики при использовании положительных электродов, изготовленных с применением активных материалов для положительного электрода, синтезированных в Примерах с 4 по 8.
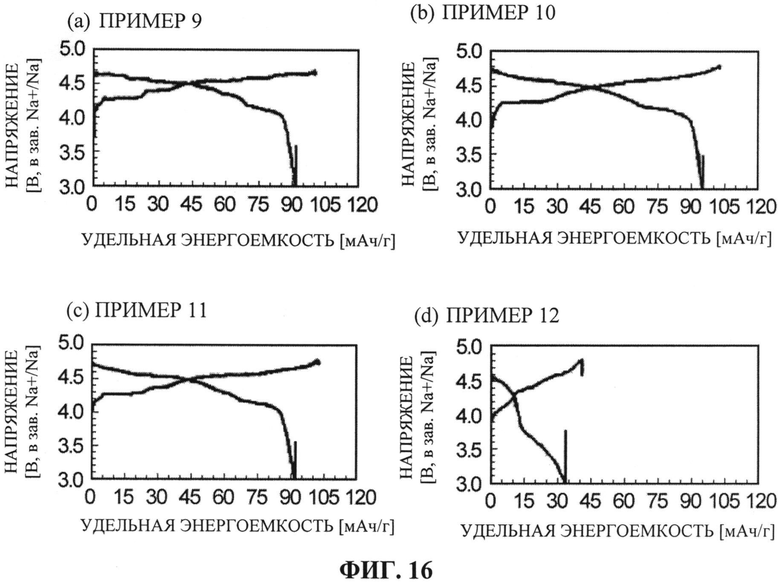
[ФИГ. 16] ФИГ. 16 отображает результаты оценочных испытаний зарядно-разрядных характеристик положительных электродов, изготовленных с применением активных материалов для положительного электрода, синтезированных в Примерах с 9 по 12.
ПРИМЕРЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
[0021] Активный материал для положительного электрода натриевого аккумулятора по настоящему изобретению (время от времени именуемый далее как просто «активный материал для положительного электрода») и способ изготовления такого материала по настоящему изобретению детально описаны ниже.
[0022] [Активный материал для положительного электрода натриевого аккумулятора]
активный материал для положительного электрода натриевого аккумулятора по настоящему изобретению характеризуется представленной ниже общей формулой (1).
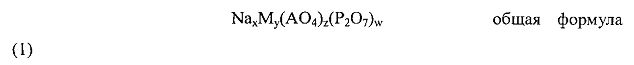
(в формуле (1) M является, по меньшей мере, одним из элементов, выбранным из группы, состоящей из Ti, V, Cr, Mn, Fe, Со, Ni, Cu и Zn; А является, по меньшей мере, одним из элементов, выбранным из группы, состоящей из Al, Si, Р, S, Ti, V и W; х удовлетворяет условию 4≥x≥2; y удовлетворяет условию 4≥y≥1, z удовлетворяет условию 4≥z≥0; w удовлетворяет условию 1≥w≥0; и, по меньшей мере, один из индексов z и w больше или равен 1).
[0023] Как указано выше, традиционные активные материалы для положительного электрода для натриевых аккумуляторов имеют рабочее напряжение около 3,5 В или менее, в результате чего невозможно получить натриевые аккумуляторы достаточной энергоемкости.
Когда Li в составе активного материала для литиевого аккумулятора заменяется Na, рабочее напряжение значительно снижается. Например, как упоминается в Непатентном документом 5, указанном выше, LiCoO2 характеризуется напряжением около 4 В, в то время как, согласно Непатентному документу 4, среднее напряжение для Na(x)CoO2 составляет около 2,9 В, что значительно ниже, чем в случае LiCoO2.
Кроме того, поскольку ионы Na имеют больший ионный радиус, чем ионы Li, когда Li в составе Li-содержащего активного материала заменяется Na, считается, что движение ионов Na становится более затрудненным.
В силу таких причин бытует мнение, что полезный активный материал для натриевых аккумуляторов, который работал бы при высоком напряжении, не может быть получен в результате простой замены лития в активном материале для литиевых аккумуляторов натрием.
[0024] Однако изобретатели провели всесторонние исследования и в конечном итоге открыли, что соединение с формулой Na4Ni3(PO4)2(P2O7) может применяться как активный материал для положительного электрода натриевого аккумулятора, более того, работающего при высоком напряжении от 4,6 до 4,9 В. Кроме того, поскольку разложение раствора электролита, используемого совместно с активным материалом для положительного электрода, можно сдерживать при таких высоких напряжениях от 4,6 до 4,9 В посредством использования активного материала для положительного электрода по настоящему изобретению, существует возможность создания натриевого аккумулятора, который показывает стабильный заряд батареи в течение длительного времени. Автор настоящего изобретения также открыл, что соединение с формулой Na4Mn3(PO4)2(P2O7), соединение с формулой Na4Co3(PO4)2(P2O7), соединение с формулой Na4Co(3-a)Mna(PO4)2(P2O7) и соединение с формулой Na4Co(3-b-c)MncNic(PO4)2(P2O7) могут использоваться как активные материалы для положительного электрода для натриевых аккумуляторов и работать при высоком напряжении, превышающем 4 В.
Более того, активные материалы для положительного электрода по настоящему изобретению, способны к функционированию при высоких напряжениях даже при относительно низкой температуре в 25°C.
[0025] Соединения с приведенной выше общей формулой (1) NaxMy(AO4)z(P2O7)w, такие, как представленное выше соединение Na4Ni3(PO4)2(P2O7), способны работать при высоком напряжении в качестве активного материала для положительного электрода натриевого аккумулятора. Объяснение этого приводится далее.
В общей формуле (1) М является электрохимически активным переходным металлом с валентностью, равной 2 или более, и это либо Ni, либо другой металл, имеющий ионный радиус, близкий к ионному радиусу Ni.
В общей формуле (1) А - это P, или другой элемент, который, подобно Р, изначально имеет тетраэдрическую структуру. В данном контексте «тетраэдрическая структура» подразумевает структуру в виде четырехгранника с четырьмя атомами кислорода в вершинах, содержащего в пространстве внутри четырехгранника, единственный атом А, который ковалентно связан с четырьмя атомами кислорода.
В отношении полианионных групп (AO4) и (P2O7), при условии, что, по меньшей мере, один из нижних индексов: z, представляющий собой число структурных единиц (AO4), и w, представляющий собой число структурных единиц (P2O7), - активного материала для положительного электрода больше или равен единице, считается, что полученный в результате активный материал для положительного электрода работает при высоком напряжении благодаря индукционным влияниям связей М-О за счет, по меньшей мере, одной из групп (AO4) и (P2O7). «Индукционные влияния» означают что, вследствие высокой ковалентной способности связей А-О, формирующих (AO4) и связей Р-О, формирующих (P2O7), электроны связей М-О перемещаются к стороне связи А-О и связи Р-О, способность к образованию ковалентной химической связи между М и О снижается, при этом ширина запрещенной энергетической зоны гибридной орбитали становится меньше, в результате чего редокс-уровень М падает, разность энергий с натрием становится больше, а редокс-потенциал по отношению к натрию возрастает.
[0026] Химический состав активного материала для положительного электрода по настоящему изобретению подробно описан далее.
В составе активного материала для положительного электрода по настоящему изобретению М является, по меньшей мере, одной разновидностью металла, выбранной из группы, состоящей из Ti, V, Cr, Mn, Fe, Со, Ni, Cu и Zn. Из этой группы предпочтение отдается металлам, которые являются двухвалентными до зарядки. Это обусловлено тем, что в случаях, когда М представляет собой разновидность металла, являющегося двухвалентным до зарядки, такая разновидность металла переходит во время зарядки в сильно окисленное состояние с валентностью, равной 3 или выше, что позволяет активному материалу работать при высоком напряжении.
[0027] Из числа перечисленных выше металлов М предпочтительно выбирать по меньшей мере, одним из металлов, выбранным из группы, состоящей из Mn, Со и Ni. Это связано с тем, что Mn, Со и Ni являются двухвалентными до зарядки, а также тем, что Mn и Со способны образовывать кристаллические структуры, сходные с кристаллическими структурами Ni. В приведенной выше общей формуле (1) NaxMy(AO4)z(P2O7)w в качестве М может быть Ni, Mn и Со. В случаях, когда остаточное соотношение (значения x, y, z и w, а также А) не меняется, доказано, что соединение имеет такую же кристаллическую структуру.
Некоторая часть этих металлов Mn, Со и Ni может быть заменена по крайней мере одним из элементов, отличающимся от М (который является, по меньшей мере, одним, выбранным из Mn, Со и Ni), элементом, который выбирают из группы, состоящей из Ti, V, Cr, Mn, Fe, Co, Ni, Cu и Zn.
[0028] Когда M в приведенной выше формуле (1) - это Ni, можно получить активный материал для положительного электрода с высокой электронной проводимостью. Есть основания полагать, что это обусловлено тем, что в случаях, когда редокс-элементом, то есть элементом, который является донором и акцептором электронов, является Ni, с экстракцией ионов Na во время зарядки, в сложных оксидах Ni, имеющих обычную кристаллическую структуру типа оливина, ионы Ni переходят из двухвалентного состояния в трехвалентное. В противоположность этому, в активном материале для положительного электрода по настоящему изобретению ионы Ni переходят из двухвалентного состояния в состояние более, чем трехвалентное (например, в случае Na4Ni3(PO4)2(P2O7), валентность приблизительно равна 3,3), и поэтому большее количество электронов перемещается. Ni может быть заменен, по меньшей мере, одним из элементов, выбранным из группы, состоящей из Ti, V, Cr, Mn, Fe, Co, Cu и Zn.
[0029] Когда M в приведенной выше формуле (1) представлен Mn, по сравнению с тем, когда М=Ni, можно получить активный материал для положительного электрода, имеющий высокую обратимость кристаллической структуры и высокую стабильность во время зарядки и разрядки, а также относительно низкое рабочее напряжение. Поскольку рабочее напряжение относительно низкое, разложение и ухудшение свойств раствора электролита может быть в дальнейшем задержано. Следовательно, когда М - это Mn, по сравнению с тем, когда М=Ni, обратимость кристаллической структуры и стабильность повышается, а ухудшение свойств раствора электролита замедляется, что позволяет достичь высокой поцикловой характеристики. Некоторая часть Mn, может быть заменена по крайней мере одним из элементов, выбранным из группы, состоящей из Ti, V, Cr, Fe, Со, Ni, Cu и Zn.
[0030] Когда М в приведенной выше формуле (1) представлен Со, по сравнению с тем, когда М=Ni, то можно получить активный материал для положительного электрода, имеющий высокую обратимость кристаллической структуры и высокой стабильностью во время зарядки и разрядки, а также относительно низкое рабочее напряжение. Поскольку рабочее напряжение относительно низкое, разложение и ухудшение свойств раствора электролита может быть в дальнейшем задержано. Более того, когда М представлен Со, благодаря лучшей обратимости кристаллической структуры, лучшей стабильности и эффектам, замедляющим ухудшение свойств раствора электролита, активный материал для положительного электрода может продемонстрировать большую способность к обратимости. В результате, когда М представлен Со, по сравнению с тем, когда М=Ni, аккумулятор позволяет достичь очень хорошей поцикловой характеристики и очень хорошей емкостной характеристики.
Некоторая часть Со, может быть заменена по крайней мере одним из элементов, выбранным из группы, состоящей из Ti, V, Cr, Mn, Fe, Ni, Cu и Zn.
[0031] Когда М в приведенной выше формуле (1) представлен Со, при этом часть Со заменена Mn, емкостная характеристика аккумулятора будет даже лучше, чем в том случае, когда М представлен только Со. Есть основания полагать, что причина этого в том, что при замещении части Со2+ узлов на Mn2+ замещающий Mn2+ может быть зарядно компенсирован не только до Mn2+/3+, но даже до Mn3+/4+. Кроме того, некоторое количество Со и Mn может быть замещено, по меньшей мере, одним из элементов, выбранным из группы, состоящей из Ti, V, Cr, Mn, Fe, Со, Ni, Cu и Zn.
[0032] Когда М в приведенной выше формуле (1) представлен Со, при этом часть Со замещена Mn и Ni, может быть продемонстрировано даже более высокое рабочее напряжение, чем когда часть Со замещена только Mn. Есть основания полагать, что причина этого в том, что замещающий Mn2+ может быть зарядно компенсирован не только до Mn2+/3+, но даже до Mn3+/4+, а также потому, что некоторое количество Со замещено Ni, для которого компенсация заряда (Ni2+→Ni3+) при высоком напряжении происходит намного легче, чем для Со. Некоторая часть Со, Mn и Ni может быть замещена, по меньшей мере, одним из элементов, выбранным из группы, состоящей из Ti, V, Cr, Mn, Fe, Co, Ni, Cu и Zn.
[0033] В составе активного материала для положительного электрода по настоящему изобретению А является по меньшей мере, одним из элементов, выбранным из группы, состоящей из Al, Si, Р, S, Ti, V и W, при этом предпочтительно, чтобы это был, по меньшей мере, один из элементов, выбранный из группы, состоящей из Si, Р и S. Это обусловлено тем, что Si, Р и S легко образуют, в частности, тетраэдрическую структуру, a Si и S способны образовывать кристаллическую структуру, аналогичную кристаллической структуре Р. По этой причине наиболее предпочтительно, чтобы А был представлен Р. Некоторая часть Si, Р и S может быть замещена по меньшей мере, одним из элементов, отличным от А (то есть Si, Р и S), и выбранным из группы, состоящей из Al, Si, Р, S, Ti, V и W.
[0034] В формуле (1), х удовлетворяет условию 4≥х≥2, y удовлетворяет условию 4≥y≥1, z удовлетворяет условию 4≥z≥0, w удовлетворяет условию 1≥w≥0, и, по меньшей мере, один из индексов z и w больше или равен 1.
В случаях, когда z и w оба равны или больше 1, поскольку полианионная группа включает четырехгранник АО4 и Р2О7, который имеет один общий атом кислорода с четырехгранником АО4, индукционное влияние связей М-O кислорода с четырехгранником АО4, индукционное влияние связей М-O больше, что приводит к желаемому результату получения активного материала для положительного электрода, имеющего более высокий потенциал.
[0035] В рамках настоящего изобретения наиболее предпочтительным активным материалом для положительного электрода является соединение с формулой Na4Ni3(PO4)2(P2O7). Поскольку Na4Ni3(PO4)2(P2O7) включает Ni в качестве редокс-элемента, а полианионная группа включает (PO4) и (P2O7), это соединение, в сочетании с отмеченной выше высокой электронной проводимостью, имеет способность работать при высоком напряжении благодаря высокому индукционному влиянию.
Кроме этого, Na4Ni3(PO4)2(P2O7) имеет кристаллическую структуру, принадлежащую к пространственной группе Pn21a. ФИГ. с 1 по 3 отображают кристаллическую структуру (Na4Ni3(PO4)2(P2O7)), принадлежащую к пространственной группе Pn21a, вид по оси «а» (ФИГ. 1), вид по оси «b» (ФИГ. 2) и вид по оси «с» (ФИГ. 3). Используя Na4Ni3(PO4)2(P2O7) для целей иллюстрации, ФИГ. с 1 по 3 отображают кристаллическую структуру, принадлежащую к пространственной группе Pn21a. Однако на ФИГ. с 1 по 3, при замещении Ni другим видом металла, представленным описанным выше элементом М (например, Со или Mn), показана кристаллическая структура другого активного материала для положительного электрода, имеющего кристаллическую структуру, принадлежащую к пространственной группе Pn21a.
Как видно из ФИГ. с 1 по 3, в кристаллической структуре, принадлежащей к пространственной группе Pn21a, все ионы Na в кристаллической структуре ориентированы в направлении оси «а», оси «b» или оси «с», благодаря чему достигается очень высокая подвижность ионов Na. Таким образом, кристаллическая структура, принадлежащая к пространственной группе Pn21a, очень благоприятна для переноса ионов Na, в результате чего захват и испускание ионов Na происходит беспрепятственно.
В силу подобных причин предпочтительно, чтобы активный материал для положительного электрода по настоящему изобретению имел кристаллическую структуру, принадлежащую к пространственной группе Pn21a.
[0036] В настоящем изобретении дополнительные примеры наиболее предпочтительных активных материалов для положительного электрода включают соединения с общей формулой Na4Mn3(PO4)2(P2O7), соединения с общей формулой Na4Co3(PO4)2(P2O7), соединения с общей формулой Na4Co(3-a)Mna(PO4)2(P2O7) и соединения с общей формулой Na4Co(3-b-c)MnbNic(PO4)2(P2O7). Все эти соединения имеют кристаллические структуры, принадлежащие к пространственной группе Pn21a, показанной на ФИГ. с 1 по 3.
[0037] Как уже было отмечено ранее, соединение Na4Mn3(PO4)2(P2O7), содержащее Mn в качестве редокс-элемента (М), благодаря улучшению обратимости кристаллической структуры, повышению стабильности и замедлению ухудшения свойств раствора электролита, способно обеспечить высокую поцикловую характеристику.
[0038] Как уже было отмечено ранее, соединения с общей формулой Na4Co3(PO4)2(P2O7), содержащие Со в качестве редокс-элемента (М), благодаря улучшению обратимости кристаллической структуры, повышению стабильности, замедлению ухудшения свойств раствора электролита и повышению обратимой емкости обеспечивают очевидную очень хорошую поцикловую характеристику и очень хорошую емкостную характеристику.
[0039] Кроме того, как уже ранее было отмечено выше, соединения с формулой Na4Co(3-a)Mna(PO4)2(P2O7), которые включают Со в качестве редокс-элемента (М), и в которых некоторое количество Со замещено Mn, посредством компенсации заряда за счет Mn, способны к обеспечению даже лучшей емкостной характеристики, чем Na4Co3(PO4)2(P2O7).
В соединениях с общей формулой Na4Co(3-a)Mna(PO4)2(P2O7) нижний индекс 'а', который обозначает количество замещений Mn, должен быть меньше 3, предпочтительно, в пределах 0,01≤а≤0,8, еще лучше в пределах 0,3≤а≤0,8, а наиболее предпочтительное значение нижнего индекса 'а' - это 0,6.
[0040] Кроме того, как уже было отмечено выше, в соединениях с общей формулой Na4Co(3-b-c)MnbNic(PO4)2(P2O7), которые включают Со в качестве редокс-элемента (М), и в которых некоторое количество Со замещено Mn и Ni, влияние компенсации заряда за счет Mn и, дополнительно, влияние компенсации заряда в диапазоне высоких напряжений за счет Ni дает возможность таким соединениям показывать более высокое рабочее напряжение по сравнению с Na4Co(3-a)Mna(PO4)2(P2O7).
В соединениях с общей формулой Na4Co(3-b-c)MnbNic(PO4)2(P2O7) нижний индекс 'b', обозначающий количество замещений Mn, и нижний индекс 'с', обозначающий количество замещений Ni, должны быть такими, чтобы сумма (b+c) не превышала 3, предпочтительно, в пределах 0,01≤b≤1,0 и 0,01≤с≤1,0, а более предпочтительно в пределах 0,3≤b≤1,0 и 0,3≤с≤1,0.
[0041] [Способ изготовления активного материала для положительного электрода]
Способ изготовления активного материала для положительного электрода изобретения особым образом не ограничивается, хотя пример предпочтительного способа является единственным, в котором активный материал для положительного электрода по настоящему изобретению изготавливают, как описано ниже.
[0042] Способ изготовления активного материала для положительного электрода натриевого аккумулятора по настоящему изобретению характеризуется тем, что включает этапы в следующем порядке:
этап предварительного обжига, который включает в себя нагрев смеси исходных материалов, содержащей, по меньшей мере, одно Na-содержащее соединение, соединение, содержащее М, соединение, содержащее А и Р-содержащее соединение, на открытом атмосферном воздухе при температуре от 150 до 500°C; и
этап основного обжига, который включает в себя нагрев предварительно обожженного материала при температуре от 500 до 800°C на открытом атмосферном воздухе.
[0043] Как указано выше, однофазный активный материал для положительного электрода может быть синтезирован путем предварительного обжига смеси исходных материалов при температуре от 150 до 500°C, которая ниже, чем температура на этапе основного обжига, затем выполняется этап основного обжига при температуре от 500 до 800°C так, чтобы реакция протекала равномерно.
[0044] Каждый этап способа изготовления активного материала для положительного электрода по настоящему изобретению последовательно описан ниже.
(Этап предварительного обжига)
На этапе предварительного обжига смесь исходных материалов, содержащая, по меньшей мере, Na-содержащее соединение, M-содержащее соединение, А-содержащее соединение и P-содержащее соединение, обжигается на открытом атмосферном воздухе при температуре от 150 до 500°C.
[0045] Na-содержащее соединение, M-содержащее соединение, A-содержащее соединение и P-содержащее соединение являются исходными материалами для активного материала для положительного электрода NaxMy(AO4)z(P2O7)w и служат, соответственно, источником Na, источником М, источником А и источником Р.
[0046] Na-содержащее соединение, M-содержащее соединение, A-содержащее соединение и P-содержащее соединение могут быть подходящим образом выбраны без особых ограничений. Каждое из этих соединений может быть типом вещества, используемым само по себе, либо быть комбинацией двух или более типов. Также отдельное соединение может включать два или более элементов из числа Na, М, А и Р. В случаях, когда М и А содержат общие атомы, М-содержащее соединение и А-содержащее соединение могут быть одним и тем же соединением. В случаях, когда А представлен Р, А-содержащее соединение и Р-содержащее соединение могут быть одним и тем же соединением.
[0047] В качестве примеров Na-содержащих соединений, служащих источниками Na, можно привести Na2CO3, Na2O, Na2O2, Na3PO4, Na4P2O7 и CH3COONa.
[0048] В качестве примеров М-содержащих соединений, служащих источником М, можно привести Ti-содержащие соединения, такие, как TiO2 и Ti2O3, V-содержащие соединения, такие, как V2O3, V2O5 и NH4VO3, Cr-содержащие соединения, такие, как Cr2O3 и Cr(NO3)3, Mn-содержащие соединения, такие, как MnCO3 и (CH3COO)2Mn, Fe-содержащие соединения, такие, как FeO, Fe2O3 и Fe(NO3)3, Co-содержащие соединения, такие, как CoCO3, (СН3СОО)2Со, СоО и Co2O3, Ni-содержащие соединения, такие, как (CH3COO)2Ni, NiCO3 и NiO, Cu-содержащие соединения, такие, как (СН3СОО)2Cu и CuO, и Zn-содержащие соединения, такие, как (CH3COO)2Zn и ZnO.
[0049] В качестве примеров А-содержащих соединений, служащих источником А, можно привести Al-содержащие соединения, такие, как Al(NO3)3, Al2O3 и Al(ОН)3, Si-содержащие соединения, такие, как SiO2 и SiO, Р-содержащие соединения, такие, как NH4H2PO4, (NH4)2HPO4, H3PO4, Na2P2O7 и Na3PO4, S-содержащие соединения, такие, как (NH4)2SO4, Na2SO4 и H2SO4, Ti-содержащие соединения, такие, как TiO2 и Ti2O3, V-содержащие соединения, такие, как V2O3, V2O5 и NH4VO3, и W-содержащие соединения, такие, как WO3 и Na2WO4.
[0050] В качестве примеров P-содержащих соединений, служащих источником Р, можно привести NH4H2PO4, (NH4)2HPO4, H3PO4, Na4P2O7 и Na3PO4.
[0051] В смеси исходных материалов соотношение составных частей смеси вышеперечисленных Na-содержащего соединения, M-содержащего соединения, А-содержащего соединения и Р-содержащего соединения может быть подходящим образом установлено согласно индексам x, y, z и w в синтезируемом соединении NaxMy(AO4)z(P2O7)w. Обычно соответствующие соединения могут быть смешаны так, чтобы соотношение (молярное отношение) Na, М, А и Р в смеси исходных материалов удовлетворяла условию: Na:M:A:P=x:y:z:2w.
[0052] Нет каких-либо специальных ограничений относительно способа приготовления смеси исходных материалов. Например, может применяться любой подходящий способ смешивания или способ перетирания.
Несмотря на то, что размеры частиц соответствующих соединений в смеси исходных материалов ничем специально не ограничены, то поскольку желательно увеличить площадь контактной поверхности между частицами, чтобы реакция протекала равномерно, предпочтительно подвергнуть каждое из соединений измельчению до начала этапа предварительного обжига. То есть, до начала этапа предварительного обжига предпочтительно выполнить этап измельчения, на котором уменьшить размеры частиц Na-содержащего соединения, М-содержащего соединения, А-содержащего соединения и Р-содержащего соединения в смеси исходных материалов. На этапе измельчения может быть проведено измельчение нескольких соединений одновременно или каждого соединения по отдельности. Более того, нет каких-либо специальных ограничений относительно способа измельчения на этапе измельчения. Может применяться любой способ измельчения; можно даже применить способ, комбинирующий смешивание и перетирание смеси исходных материалов с измельчением. Например, шаровая мельница, бисерная мельница способны смешивать и перетирать смесь исходных материалов при этом одновременно подвергая смесь измельчению.
[0053] Температура на этапе предварительного обжига ниже температуры на этапе основного обжига и должна быть в пределах от 150 до 500°C, предпочтительно от 180 до 450°C, а еще более предпочтительно от 250 до 350°C. Время предварительного обжига специально не ограничено и может быть подходящим образом установлено, например, примерно от 1 до 5 часов.
Под открытым атмосферным воздухом, служащим воздушной средой на этапе предварительного обжига, здесь понимается любая кислородсодержащая газовая среда.
[0054] (Этап основного обжига)
На этапе основного обжига предварительно обожженный материал, полученный на этапе предварительного обжига, обжигают на открытом атмосферном воздухе при температуре от 500 до 800°C.
Температура обжига на этапе основного обжига предпочтительно должна быть от 550 до 750°C. Время обжига на этом этапе специально не ограничено и может быть подходящим образом установлена, например, примерно от 1 до 30 часов.
Открытый атмосферный воздух, служащим воздушной средой на этапе основного обжига аналогичен открытому атмосферному воздуху на этапе предварительного обжига.
[0055] (Другие способы изготовления)
Способ изготовления активного материала для положительного электрода по настоящему изобретению не ограничен изложенным далее. Например, изготовление также возможно с применением способа, в котором предварительно Na-содержащие соединение, служащее источником Na, М-содержащее соединение, служащее источником М, А-содержащее соединение, служащее источником А, и Р-содержащее соединение, служащее источником Р, растворяют и нагревают вместе с гелеобразующим агентом в кислом растворе, чтобы приготовить гель, затем полученный в результате гель подвергают обжигу на открытом атмосферном воздухе.
[0056] В этом способе Na-содержащее соединение, M-содержащее соединение, A-содержащее соединение и P-содержащее соединение могут быть подходящим образом выбраны при условии, что они растворимы в кислом растворе. Каждое из этих соединений может быть типом вещества, используемым само по себе, либо быть комбинацией двух или более типов. Также отдельное соединение может включать два или более элементов из числа Na, М, А и Р. В случаях, когда М и А содержат общие атомы, M-содержащее соединение и А-содержащее соединение могут быть одним и тем же соединением. В случаях, когда А представлен Р, А-содержащее соединение и Р-содержащее соединение могут быть одним и тем же соединением.
[0057] В качестве примеров Na-содержащих соединений можно привести Na4P2O7, CH3COONa, Na2CO3, Na2O и Na2O2.
[0058] В качестве примеров М-содержащих соединений можно привести Ti-содержащие соединения, такие, как Ti(NO3)4, TiO2 и Ti2O3, V-содержащие соединения, такие, как V2O3 и V2O5, Cr-содержащие соединения, такие, как Cr(NO3)3, Mn-содержащие соединения, такие, как (СН3СОО)2Mn и MnCO3, Fe-содержащие соединения, такие, как Fe(NO3)3, FeC2O4 и (CH3COO)3Fe, Co-содержащие соединения, такие, как (СН3СОО)2Со, CoCO3, Со2О3 и СоО, Ni-содержащие соединения, такие, как (CH3COO)2Ni, NiO и NiCO3, Cu-содержащие соединения, такие, как (СН3СОО)2Cu, и Zn-содержащие соединения, такие, как (CH3COO)2Zn.
[0059] В качестве примеров А-содержащих соединений можно привести Al-содержащие соединения, такие, как Al(NO3)3, Si-содержащие соединения, такие, как Si(OCH2CH3)4, Р-содержащие соединения, такие, как NH4H2PO4, (NH4)2HPO4 и H3PO4, S-содержащие соединения, такие, как H2SO4 и Na2SO4, Ti-содержащие соединения, такие, как Ti(NO3)4, TiO2 и Ti2O3, V-содержащие соединения, такие, как V2O3 и V2O5, и W-содержащие соединения, такие, как WO3 и Na2WO4.
[0060] В качестве примеров Р-содержащих соединений можно привести NH4H2PO4, (NH4)2HPO4 и H3PO4.
[0061] Соотношение составных частей смеси вышеперечисленных Na-содержащего соединения, М-содержащего соединения, А-содержащего соединения и Р-содержащего соединения может быть подходящим образом установлено согласно индексам х, y, z и w в синтезируемом соединении NaxMy(AO4)z(P2O7)w. Обычно соответствующие соединения могут быть смешаны так, чтобы соотношение (молярное отношение) Na, М, А и Р в смеси исходных материалов удовлетворяла условию: Na:M:A:P=x:y:z:2w.
[0062] Гелеобразующим агентом может быть, например, гликолевая кислота. Кислотным растворителем может быть, например, водный раствор азотной кислоты.
[0063] Температура нагрева при приготовлении геля должна быть такой, чтобы обеспечить растворение каждого из перечисленных выше соединений в кислом растворе и обеспечить возможность приготовления геля, и может быть установлена, например, от 60 до 120°C.
Температура обжига геля может быть установлена от 500 до 800°C, предпочтительно от 550 до 750°C. Открытый атмосферный воздух во время обжига геля аналогичен открытому атмосферному воздуху на этапе предварительного обжига, который описан выше.
[0064] [Натриевый аккумулятор]
Активный материал для положительного электрода по настоящему изобретению может успешно применяться как активный материал для положительного электрода в натриевом аккумуляторе. Натриевый аккумулятор может быть как первичным источником питания, так и перезаряжаемым аккумулятором. Используя натриевый аккумулятор в целях иллюстрации, ниже приводится описание натриевого аккумулятора, который использует активный материал для положительного электрода по настоящему изобретению.
[0065] ФИГ. 4 представляет собой схематический вид в разрезе одного из вариантов осуществления натриевого перезаряжаемого аккумулятора. Как показано на ФИГ. 4, натриевый перезаряжаемый аккумулятор 8 обычно имеет структуру, в которой слой электролита 3 расположен между отрицательным электродом 1 и положительным электродом 2. Отрицательный электрод 1 включает слой активного материала для отрицательного электрода 4, содержащий активный материал для отрицательного электрода, токосборник отрицательного электрода 5, который осуществляет аккумуляцию заряда применительно к слою активного материала для отрицательного электрода 4. Положительный электрод 2 включает слой активного материала для положительного электрода 6, содержащего активный материал для положительного электрода, и токосборник положительного электрода 7, который осуществляет аккумуляцию заряда применительно к слою активного материала для положительного электрода 6.
В следующие параграфах поясняется каждый элемент структуры.
[0066] Отрицательный электрод содержит активный материал для отрицательного электрода, способный захватывать и испускать ионы натрия. Отрицательный электрод обычно содержит слой активного материала для отрицательного электрода, который включает, по меньшей мере, один активный материал для отрицательного электрода. Там, где это необходимо, он также может включать токосборник отрицательного электрода, который осуществляет аккумуляцию заряда применительно к слою активного материала для отрицательного электрода.
[0067] В качестве примеров активного материала для отрицательного электрода можно привести твердый углерод, металлический Na и олово.
Слой активного материала для отрицательного электрода может содержать только активный материал для отрицательного электрода или может, в дополнение к активному материалу для отрицательного электрода, также содержать связующее вещество, электропроводный материал, электролит и т.п. Например, в случаях, когда активный материал для отрицательного электрода представлен в виде тонкого листа или фольги, он может быть включен в слой отрицательного электрода, содержащего только активный материал для отрицательного электрода. С другой стороны, в случаях, когда активный материал для отрицательного электрода представлен в виде порошка, он может быть включен в слой активного материала для отрицательного электрода, включающего связующее вещество в дополнение к активному материалу для отрицательного электрода.
В качестве примеров связующего вещества можно привести поливинилиденфторид (ПВДФ), политетрафторэтилен (ПТФЭ) и стироль-бутадиеновый каучук (СБК). В качестве примеров электропроводный материала можно привести углеродные материалы, такие, как технический углерод, активированный уголь, углеродное волокно (например, углеродные нанотрубки, углеродные нановолокна) и графит.
[0068] Положительный электрод содержит активный материал для положительного электрода, способный захватывать и испускать ионы натрия. Положительный электрод обычно содержит слой активного материала для положительного электрода, включающий, по меньшей мере, один активный материал для положительного электрода. Там, где это необходимо, он также может включать токосборник положительного электрода, который осуществляет аккумуляцию заряда применительно к слою активного материала для положительного электрода.
[0069] В качестве активного материала для положительного электрода может использоваться вышеописанный активный материал для положительного электрода по настоящему изобретению или активный материал для положительного электрода, изготовленный способом по настоящему изобретению.
Как и в случае слоя активного материала для отрицательного электрода, слой активного материала для положительного электрода может содержать только активный материал для положительного электрода или может в дополнение к активному материалу для положительного электрода, также включать электропроводный материал, связующее вещество, электролит, электродный катализатор и т.п. Поскольку в активном материале для положительного электрода в качестве электропроводного материала и связующего вещества могут применяться материалы, аналогичные активным материалам в материале для отрицательного электрода, их дальнейшее описание будет опущено.
[0070] Слой активного материала для электродов (как слой активного материала для отрицательного электрода, так и слой активного материала для положительного электрода) может быть создан с использованием любого подходящего способа нанесения покрытий, таким, как метод погружения, метод напыления, нанесение покрытия валиком, нанесение покрытия ножевым устройством, нанесение покрытия с помощью гравированного цилиндра или нанесение покрытия трафаретом для нанесения, сушки и, как вариант, методом прокатки шликера, содержащего соответствующие материалы.
[0071] В отношении материала, структуры или формы токосборника положительного электрода и токосборника отрицательного электрода не предусмотрено никаких особенных ограничений, при условии что, они являются материалами, обладающими желаемой электронной проводимостью и не вызывающими реакций легирования/насыщения ионами натрия во внутренней среде аккумулятора.
В качестве примеров материала для изготовления токосборника положительного электрода можно привести металлические материалы, такие, как нержавеющая сталь, никель, алюминий, железо, титан и медь; углеродные материалы, такие, как углеродное волокно и углеродная бумага, а также керамические материалы, обладающие высокой электронной проводимостью, такие, как нитрид титана. Корпус аккумулятора также может функционировать как токосборник положительного электрода.
В качестве примеров материала для изготовления токосборника отрицательного электрода можно привести медь, нержавеющую сталь, никель и алюминий. Корпус аккумулятора также может функционировать как токосборник отрицательного электрода.
Как токосборник положительного электрода, так и токосборник отрицательного электрода могут быть изготовлены в виде, например, тонкого листа, фольги или сетки, из которых сетка является наиболее предпочтительным вариантом.
[0072] Слой электролита включает, по меньшей мере, электролит, который обеспечивает условия проводимости ионов натрия между положительным электродом и отрицательным электродом.
Электролит должен быть одним из веществ, обеспечивающих проводимость ионов натрия, и, как пример, это могут быть растворы электролита, гелеобразные электролиты, полученные путем загущения раствора электролита с использованием полимера или подобного вещества, а также твердые электролиты.
В качестве примеров растворов электролита, обеспечивающих электоропроводимость ионов натрия, можно привести растворы электролита, полученные путем растворения соли натрия в водном растворителе или в безводном растворителе.
[0073] В качестве примеров неводного растворителя, но не ограничивая их только перечисляемым далее, можно привести циклические карбонаты, такие, как пропиленкарбонат (ПК), этиленкарбонат (ЭК) и фторэтиленкарбонат (ФЭК), циклические эфиры, такие, как γ-бутиролактон (ГБЛ), а также ациклические карбонаты, такие, как диметилкарбонат (ДМК), диэтилкарбонат (ДЭК) и этилметилкарбонат (ЭМК). Эти неводные растворители могут быть использованы как сами по себе, так и в комбинации из двух или более веществ. Кроме того, нитрильное соединение, включающее группу CN, имеющую концевую связь с ациклическим насыщенным углеводородным соединением, может использоваться в качестве добавки к неводному растворителю. Путем добавления нитрильного соединения в раствор электролита с растворителем неводного типа можно получить стабильный неводный раствор электролита на основе неводного растворителя, который устойчив и не разлагается даже в диапазоне высоких напряжений, при которых функционирует активный материал для положительного электрода натриевых аккумуляторов по настоящему изобретению.
[0074] В качестве примеров соли натрия, но не ограничивая их только перечисляемым далее, можно привести NaPF6, NaBF4, NaClO4, NaCF3SO3, (CF3SO2)2NNa, NaN(FSO2) и NaC(CF3SO2)3. Эти соли натрия могут быть использованы как сами по себе, так и в комбинации из двух или более веществ. NaPF6, которая устойчива также и при высоких напряжениях, наиболее предпочтительна.
Нет каких-либо специальных ограничений относительно концентрации соли натрия в неводном растворе электролита.
[0075] Неводный раствор электролита может также использоваться после загущения путем добавлением полимера. Примером способа загущения неводного раствора электролита может служить способ, который включает добавление полимера, такого, как полиэтиленоксид (ПЭО), полиакрилнитрил (ПАН), ПВДФ или полиметилметакрилат (ПММА), в неводный раствор электролита.
[0076] В случаях, когда в качестве электролита используется раствор электролита, изоляция между положительным электродом и отрицательным электродом может осуществляться путем размещения изолирующего пористого тела как разделителя между положительным электродом и отрицательным электродом, и пропитыванием разделителя раствором электролита. Примером разделителя могут служить пористые мембраны, такие, как полиэтиленовые пористые мембраны и полипропиленовые пористые мембраны, а также нетканые материалы, такие, как полимерная нетканая ткань и нетканая ткань из стекловолокна.
[0077] Корпус аккумулятора, используемый, чтобы вместить отрицательный электрод, слой электролита и положительный электрод, может быть любым, имеющим традиционную форму, т.е. быть корпусом монетного типа, в форме плоской пластины, трубчатым или корпусом слоистого типа.
В аккумуляторах, имеющих конструкцию, в которой слои положительного электрода, слоя электролита и слоя отрицательного электрода, расположенные в указанном порядке, повторно наложены, образуя многослойную структуру, то в целях безопасности между соседними положительным и отрицательным электродами могут быть помещены разделители, состоящие из изолирующего материала. В качестве примеров таких разделителей можно привести пористые мембраны, такие, как полиэтиленовые пористые мембраны и полипропиленовые пористые мембраны; а также нетканые материалы, такие, как полимерная нетканая ткань и нетканая ткань из стекловолокна.
Кроме того, на токосборниках соответствующих электродов могут быть установлены клеммы, функционирующие в качестве соединителей с внешними устройствами.
[0078] [Пример 1]
(Синтез активного материала для положительного электрода натриевого аккумулятора)
Na2CO3 (Na-содержащее соединение), (CH3COO)2Ni (Ni-содержащее соединение) и NH4H2PO4 (Р-содержащее соединение) были смешаны в молярном отношении Na:Ni:Р=4:3:4. Смесь подверглась измельчению с использованием шаровой мельницы, затем предварительному обжигу на открытом атмосферном воздухе при температуре 300°C и основному обжигу в течение 15 часов при температуре 700°C.
Кристаллическая структура синтезированного материала, полученного на этапе основного обжига, была подвергнута анализу с использованием рентгеновского дифрактометра (РД). Результаты анализа представлены на ФИГ. 5. Верхняя часть ФИГ. 5 изображает рентгенограмму синтезированного материала, а нижняя часть - рентгенограмму Na4Ni3(PO4)2P2O7 в Базе данных кристаллических структур неорганических веществ (ICSD №01-087-0977). На основании ФИГ. 5 можно подтвердить, что полученный синтезированный материал действительно представляет собой Na4Ni3(PO4)2P2O7. Кроме того, было подтверждено, что синтезированный материал (Na4Ni3(PO4)2P2O7) имеет кристаллическую структуру, принадлежащую к пространственной группе Pn21a.
[0079] (Испытание активного материала для положительного электрода натриевого аккумулятора)
<Изготовление положительного электрода>
Был приготовлен шликер путем смешивания Na4Ni3(PO4)2P2O7 (активного материала для положительного электрода), полученного в Примере 1, углерода (электропроводной добавки) и ПВДФ (связующего вещества) в весовой пропорции 75:20:5, затем смесь была диспергирована в N-метил-2-пирролидоне (диспергирующем агенте).
Этот шликер был нанесен на алюминиевую фольгу (токосборник), высушен и раскатан, в результате чего был изготовлен положительный электрод, состоящий из токосборника и слоя активного материала для положительного электрода в виде последовательных слоев.
[0080] <Изготовление тестового образца>
Сначала получили верхний электрод посредством штамповки фольги из металлического натрия.
В порядке отдельной процедуры в смешанный растворитель, полученный смешиванием ЭК и ДМК в объемной пропорции 1:1, была добавлена натриевая соль (NaPF6), в результате чего был получен неводный раствор электролита с концентрацией соли натрия, равной 1,0 моль/дм3.
Положительный электрод, изготовленный, как было описано выше, пористая мембрана (разделитель), изготовленная из полипропиленовой пористой мембраны, полиэтиленовой пористой мембраны и полипропиленовой пористой мембраны, расположенных последовательными слоями в указанном порядке, и верхний электрод были наложены друг на друга в указанном порядке. Положительный электрод был расположен внутри этого пакета таким образом, чтобы слой активного материала для положительного электрода лежал на боковой поверхности вышеуказанного разделителя.
Вышеописанным раствором электролита на базе неводного растворителя был пропитан разделитель вышеописанного пакета, и таким образом был получен тестовый образец монетного типа.
[0081] <Метод испытания>
Циклическая вольтамперометрия (CV) с использованием вышеупомянутого тестового образца была произведена при следующих условиях. Результаты испытания представлены на ФИГ. 6.
- Диапазон напряжений: Напряжение разомкнутой цепи (НРЦ) до 4,9 В
- Скорость сканирования: 0,2 мВ/с
- Температура: 25°C.
[0082] Как показано на ФИГ. 6, пики реакции окисления, которая соответствует зарядке, и реакции восстановления, которая соответствует разрядке, были подтверждены в диапазоне сверхвысокого напряжения от 4,6 до 4.9 В как в первом цикле, так и во втором. Таким образом, было подтверждено, что синтезированный материал, полученный в Примере 1, может быть использован как активный материал для положительного электрода натриевого перезаряжаемого аккумулятора, и, более того, что он функционирует при высоком напряжении. Кроме того, способность функционировать при высоком напряжении, о которой шла речь выше, проявилась при низкой температуре 25°C.
[0083] [Пример 2]
(Синтез активного материала для положительного электрода натриевого аккумулятора)
Na4P2O7 (Na- и Р-содержащее соединение), (СН3СОО)2Mn (Mn-содержащее соединение) и NH4H2PO4 (Р-содержащее соединение) были добавлены вместе с гликолевой кислотой (гелеобразующим агентом) в кислый раствор (водный раствор азотной кислоты) в молярном отношении Na:Mn:Р=4:3:4 и растворены в нем; раствор был перемешан при температуре 80°C. Полученный в результате гель был подвергнут обжигу на открытом атмосферном воздухе при температуре 700°C в течение 15 часов.
Кристаллическая структура синтезированного материала, полученного в результате обжига, была подвергнута анализу с использованием РД. Результаты анализа показаны на ФИГ. 7. На основании ФИГ. 7 подтверждено, что полученный синтезированный материал является Na4Mn3(PO4)2P2O7. Подтверждено также, что полученный синтезированный материал (Na4Mn3(PO4)2P2O7) имеет кристаллическую структуру, принадлежащую к пространственной группе Pn21a, показанную на ФИГ. с 1 по 3.
[0084] (Испытание активного материала для положительного электрода натриевого аккумулятора)
<Изготовление положительного электрода>
Был приготовлен шликер путем перемешивания Na4Mn3(PO4)2P2O7 (активного материала для положительного электрода), полученного в Примере 2, углерода (электропроводной добавки) и ПВДФ (связующего вещества) в весовой пропорции 75:20:5, затем смесь диспергировали в N-метил-2-пирролидоне (диспергирующем агенте).
Этот шликер был нанесен на алюминиевую фольгу (токосборник), высушен и раскатан, в результате чего был изготовлен положительный электрод, состоящий из токосборника и слоя активного материала для положительного электрода в виде последовательных слоев.
[0085] <Изготовление тестового образца>
Кроме использования ДЭК вместо ДМК, тестовый образец монетного типа был получен тем же способом, что и в Примере 1.
[0086] <Метод испытания>
Десять циклов зарядки-разрядки вышеупомянутого тестового образца было произведено при следующих условиях, и были оценены его зарядно-разрядные характеристики. Соотношение между удельной энергоемкостью и напряжением в первом цикле и в десятом цикле показано на ФИГ. 8.
- Диапазон напряжений: от 2,5 В до 4,1 В
- Плотность тока: 8,5 мА/г
- Температура: 25°C.
[0087] Как показано на ФИГ. 8, даже после десяти циклов зарядка и разрядка возможны в том же диапазоне напряжений, что и в первом цикле. Более того, удалось подтвердить, что удельная энергоемкость при разрядке также может быть сохранена (сохранение энергоемкости, 96%; емкость при повторном использовании, 18 мАч/г). Таким образом, было установлено, что активный материал для положительного электрода из Примера 2 обеспечивает зарядку и разрядку в диапазоне напряжений, в котором раствор электролита сохраняет устойчивость, и при этом поцикловая характеристика очень хорошая.
[0088] [Пример 3]
(Синтез активного материала для положительного электрода натриевого аккумулятора)
Na4P2O7 (Na- и Р-содержащее соединение), (СН3СОО)2Со (Со-содержащее соединение) и NH4H2PO4 (Р-содержащее соединение) были добавлены вместе с гликолевой кислотой (гелеобразующим агентом) в кислый раствор (водный раствор азотной кислоты) в молярном отношении Na:Со:Р=4:3:4 и растворены в нем; раствор был перемешан при температуре 80°C. Полученный в результате гель был подвергнут обжигу на открытом атмосферном воздухе при температуре 700°C в течение 15 часов.
Кристаллическая структура синтезированного материала, полученного в результате обжига, была подвергнута анализу с использованием РД. Результаты анализа показаны на ФИГ. 9. На основании ФИГ. 9 подтверждено, что полученный синтезированный материал является Na4Co3(PO4)2P2O7. Подтверждено также, что полученный синтезированный материал (Na4Co3(PO4)2P2O7) имеет кристаллическую структуру, принадлежащую к пространственной группе Pn21a, показанную на ФИГ. с 1 по 3.
[0089] (Испытание активного материала для положительного электрода натриевого аккумулятора)
<Изготовление положительного электрода>
Был приготовлен шликер путем перемешивания Na4Co3(PO4)2P2O7 (активного материала для положительного электрода), полученного в Примере 3, углерода (электропроводной добавки) и ПВДФ (связующего вещества) в весовой пропорции 75:20:5, затем смесь диспергировали в N-метил-2-пирролидоне (диспергирующем агенте).
Этот шликер был нанесен на алюминиевую фольгу (токосборник), высушен и раскатан, в результате чего был изготовлен положительный электрод, состоящий из токосборника и слоя активного материала для положительного электрода в виде последовательных слоев.
[0090] <Изготовление тестового образца>
Тестовый образец монетного типа был изготовлен тем же способом, что и в Примере 2.
[0091] <Метод испытания>
Пятьдесят циклов зарядки-разрядки вышеупомянутого тестового образца было произведено при следующих условиях, и были оценены его зарядно-разрядные характеристики. Соотношение между удельной энергоемкостью и напряжением в первом цикле и в пятидесятом цикле показано на ФИГ. 10. Кроме того, на ФИГ. 11 показано количество циклов в зависимости от удельной энергоемкости при зарядке и удельной энергоемкости при разрядке.
- Диапазон напряжений: от 3,0 В до 4,7 В
- Плотность тока: 17 мА/г
- Температура: 25°C.
Циклическое повторение зарядки-разрядки вышеупомянутого тестового образца было произведено также при описанных ниже условиях, и были оценены его зарядно-разрядные характеристики. Кривая зарядки и кривая разрядки в десятом цикле показаны на ФИГ. 12.
- Диапазон напряжений: от 3,0 В до 4,8 В
- Плотность тока: 1700 мА/г
- Температура: 25°C.
[0092] Как показано на ФИГ. 10, даже после пятидесяти циклов зарядка и разрядка могут осуществляться в том же самом диапазоне напряжений, что и в первом цикле. Также, в сравнении с Примером 1 и 2, было подтверждено повышение емкости при повторном использовании. Более того, как показано на ФИГ. 11, было подтверждено, что даже после пятидесяти циклов удельная энергоемкость сохраняется. Таким образом, было подтверждено, что активный материал для положительного электрода из Примера 3 обладает высокой емкостью при повторном использовании (около 90 мАч/г) в диапазоне напряжений, в котором раствор электролита остается стабильным, и, более того, имеет очень хорошую поцикловую характеристику. Как показано на ФИГ. 12, даже при очень высокой плотности тока, равной 1700 мАч/г, обнаруживается способность к емкости при повторном использовании около 82 мАч/г. Таким образом, учитывая то, что уменьшение емкости было незначительным, несмотря на то, что плотность тока стала в 100 раз больше, чем в вышеописанном испытательном цикле зарядки-разрядки при плотности тока 17 мА/г, активный материал для положительного электрода из Примера 3 может рассматриваться как материал, обладающий наибольшими преимуществами для достижения более высоких исходных и выходных параметров аккумулятора.
[0093] [Примеры с 4 по 8]
(Синтез активного материала для положительного электрода для натриевых аккумуляторов)
Na4P2O7 (Na- и Р-содержащее соединение), (СН3СОО)2Со (Со-содержащее соединение), (СН3СОО)2Mn (Mn-содержащее соединение) и NH4H2PO4 (Р-содержащее соединение) были добавлены вместе с гликолевой кислотой (гелеобразующим агентом) в кислый раствор (водный раствор азотной кислоты) в количествах вещества, показанных в таблице 1, чтобы получить молярные отношения Na, Со, Mn и Р, показанные в таблице 1, и растворены в нем; растворы были перемешаны при температуре 80°C. Полученные в результате гели были подвергнуты обжигу на открытом атмосферном воздухе при температуре 700°C в течение 15 часов.
[0094] [Таблица 1]
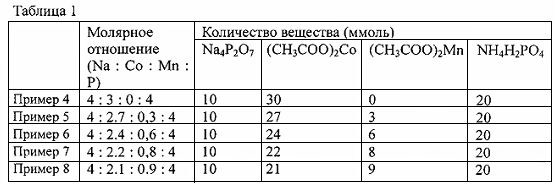
[0095] Кристаллические структуры синтезированных материалов, полученных в результате обжига в Примерах с 4 по 8, были подвергнуты анализу с использованием РД. Результаты анализа показаны в Таблице 2.
Было подтверждено, что синтезированные материалы, полученные в Примерах с 4 по 8, представляют собой, соответственно, Na4Co3(РО4)2Р2О7 (Пример 4), Na4Co2.7Mn0,3(PO4)2P2O7 (Пример 5), Na4Co2.4Mn0,6(PO4)2P2O7 (Пример 6), Na4Co2.2Mn0,8(PO4)2P2O7 (Пример 7) и Na4Co2.1Mn0.9(PO4)2P2O7 (Пример 8). Подтверждено также, что материалы, синтезированные в Примерах с 4 по 8, имеют кристаллическую структуру, принадлежащую к пространственной группе Pn21a, показанной на ФИГ. с 1 по 3.
[0096] [Таблица 2]

[0097] (Исследование активного материала для положительного электрода для натриевых аккумуляторов)
<Изготовление положительных электродов>
Были приготовлены шликеры путем перемешивания активных материалов для положительного электрода, полученных в приведенных выше Примерах с 4 по 8, (Na4Co3.0(PO4)2P2O7 (Пример 4), Na4Co2.7Mn0,3(PO4)2P2O7 (Пример 5), Na4Co2.4Mn0,6(PO4)2P2O7 (Пример 6), Na4Co2.2Mn0.8(PO4)2P2O7 (Пример 7), Na4Co2.1Mn0.9(PO4)2P2O7 (Пример 8)), с углеродом (электропроводной добавкой) и ПВДФ (связующим веществом) в весовой пропорции 75 (активный материал для положительного электрода):20(электропроводная добавка):5(связующее вещество), затем смесь диспергировали в N-метил-2-пирролидоне (диспергирующим агенте).
Эти шликеры были нанесены на алюминиевую фольгу (токосборник), высушены и раскатаны, в результате чего были изготовлены положительные электроды, состоящие из токосборника и слоя активного материала для положительного электрода в виде последовательных слоев.
[0098] <Изготовление тестовых образцов>
Тестовые образцы монетного типа были изготовлены таким же способом, что и в Примере 2, с использованием вышеописанных положительных электродов, содержащих активные материалы для положительного электрода из Примеров с 4 по 8.
[0099] <Метод испытания>
Три цикла зарядки-разрядки вышеупомянутых тестовых образцов было произведено при описанных ниже условиях, и были оценены их зарядно-разрядные характеристики.
- Диапазон напряжений: Пример 4: от 3,0 В до 4,7 В; Примеры с 5 по 8: от 3,0 В до 4,8 В
- Плотность тока: 17 мА/г
- Температура: 25°C.
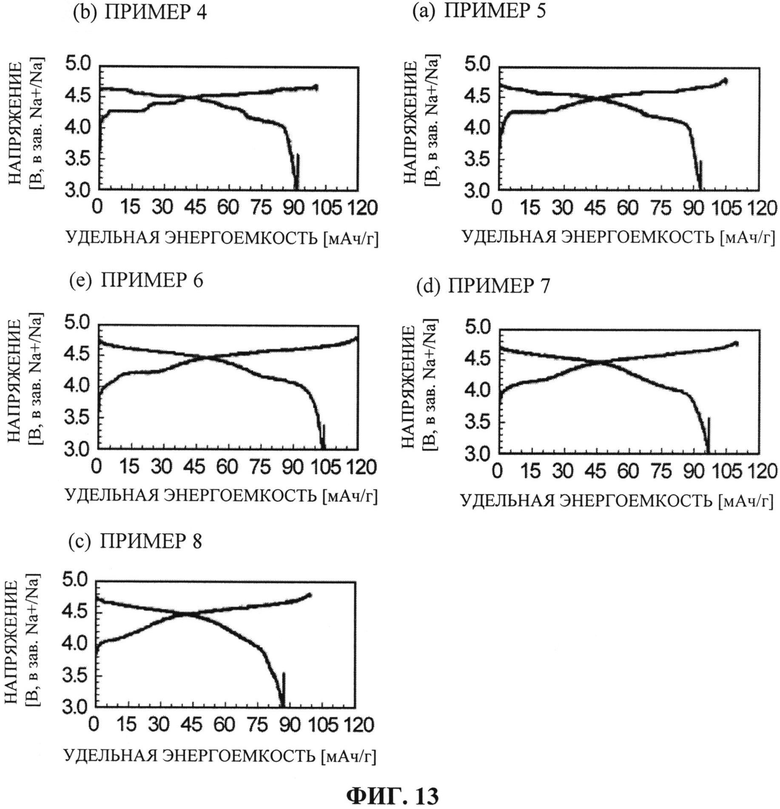
[0100] ФИГ. 13 отображает соотношение между удельной энергоемкостью и напряжением в третьем цикле (кривая разрядки и кривая зарядки). ФИГ. 13, (а) отображает результаты Примера 4, (b) отображает результаты Примера 5, (с) отображает результаты Примера 6, (d) отображает результаты Примера 7, и (е) отображает результаты Примера 8.
На ФИГ. 14 показаны кривые разрядки в третьем цикле для Примеров с 4 по 8. На ФИГ. 14, пункты с (а) по (е) соответствуют пунктам с (а) по (е) на ФИГ. 13.
ФИГ. 15 отображает поцикловые характеристики (количество циклов по отношению к удельной энергоемкости) для Примеров с 4 по 8.
[0101] Как показано на ФИГ. 13 и 14, все Примеры с 4 по 8 продемонстрировали очень хорошую разрядную емкость, от 90 мАч/г до 103 мАч/г в диапазоне высоких напряжений от 3,0 до 4,8 В.
В частности, в Примерах с 5 по 7, где некоторая часть Со2+ в составе Na4Co3.0(PO4)2P2O7 была замещена Mn2+ при 0,3≤а≤0,8 в общей формуле Na4CO(3-a)Mna(PO4)2(P2O7), наблюдалось улучшение параметров как емкостной характеристики, так и характеристики напряжения, по сравнению с Примером 4 (Na4Co3.0(PO4)2P2O7). Есть основание полагать, что это в значительной степени является следствием того факта, что в случаях, когда коэффициент замещения Со2+ марганцем Mn2+ находится в вышеуказанном диапазоне (0,3≤а≤0,8), замещающий Mn2+ может быть компенсирован по заряду не только до Mn2+/3+, но даже до Mn3+/4+ в диапазоне напряжений от 4,7 В и выше.
Более того, в Примере 8, где в общей формуле Na4Co(3-a)Mna(PO4)2(P2O7) кобальт Со2+ был замещен марганцем Mn2+ при а=0,9, стало понятно, что, по причине снижения электронной проводимости активного материала для положительного электрода из-за Mn2+, сопротивление аккумулятора повысилось и, по сравнению с Примером 4 (Na4Co3.0(PO4)2P2O7), снизились параметры как емкостной характеристики, так и характеристики напряжения.
[0102] Кроме того, как показано на ФИГ. 15, во всех Примерах с 4 по 8 сохранилась высокая емкость в пределах приблизительно от 85 мАч/г до 103 мАч/г в течение всех трех циклов, в дополнение к чему подтвердились хорошие поцикловые характеристики.
[0103] Более того, при сопоставлении результатов из Примера 3 с результатами из Примера 2, было выявлено, что, по сравнению с активным материалом для положительного электрода, в котором М=Со, активный материал для положительного электрода, в котором М=Mn, обладает худшей емкостной характеристикой и более низким рабочим напряжением. Это подтверждает общепризнанное мнение, что замена некоторого количества Со марганцем Mn ведет к ухудшению эксплуатационных качеств аккумулятора. Таким образом, тот факт, что за счет замещения Со2+ марганцем Mn2+ при 0,3≤а≤0,8 в общей формуле Na4CO(3-a)Mna(PO4)2(P2O7), как в вышеприведенных Примерах с 5 по 7, можно улучшить показатели емкостной характеристики и рабочего напряжения, является дополнительным полезным эффектом изобретения.
[0104] [Примеры с 9 по 12]
(Синтез активных материалов для положительного электрода для натриевых аккумуляторов)
Na2P2O7 (Na- и Р-содержащее соединение), (СН3СОО)2Со (Со-содержащее соединение), (СН3СОО)2Mn (Mn-содержащее соединение), (CH3COO)2Ni (Ni-содержащее соединение) и NH4H2PO4 (Р-содержащее соединение) были добавлены вместе с гликолевой кислотой (гелеобразующим агентом) в кислый раствор (водный раствор азотной кислоты) в количествах вещества, показанных в таблице 3, чтобы получить молярные отношения Na, Со, Mn, Ni и Р, показанные в таблице 3, и растворены в нем; растворы были перемешаны при температуре 80°C. Полученные в результате гели были подвергнуты обжигу на открытом атмосферном воздухе при температуре 700°C в течение 15 часов.
[0105] [Таблица 3]
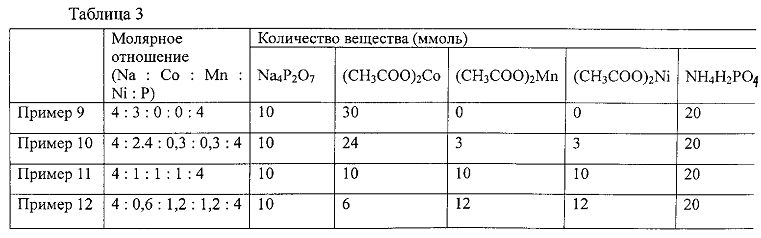
[0106] Кристаллические структуры материалов, синтезированных в результате обжига в Примерах с 9 по 12, были подвергнуты анализу с использованием РД. Результаты анализа показаны в Таблица 4.
Было подтверждено, что синтезированные материалы, полученные в Примерах с 9 по 12, являются, соответственно, Na4Co3(PO4)2P2O7 (Пример 9), Na4Co2.4Mn0.3Ni0.3(PO4)2P2O7 (Пример 10), Na4Co1.0Mn1.0Ni1.0(PO4)2P2O7 (Пример 11) и Na4Co0.6Mn1.2Ni1.2(PO4)2P2O7 (Пример 12). Также подтвердилось, что синтезированные материалы, полученные в Примерах с 9 по 12, имеют кристаллические структуры, принадлежащие к пространственной группе Pn21a, показанной на ФИГ. с 1 по 3.
[0107] [Таблица 4]

[0108] (Исследование активных материалов для положительного электрода для натриевых аккумуляторов)
<Изготовление положительных электродов>
Были приготовлены шликеры путем перемешивания активных материалов для положительного электрода, полученных в Примерах с 9 по 12 (Na4Co3.0(PO4)2P2O7 (Пример 9), Na4Co2.4Mn0.3Ni0.3(PO4)2P2O7 (Пример 10), Na4Co1.0Mn1.0Ni1.0(PO4)2P2O7 (Пример 11), Na4Co0.6Mn1.2Ni1.2(PO4)2P2O7 (Пример 12)), с углеродом (электропроводной добавкой) и ПВДФ (связующим веществом) в весовой пропорции 75 (активный материал для положительного электрода):20 (электропроводная добавка):5 (связующее вещество), затем смесь диспергировали в N-метил-2-пирролидоне (диспергирующем агенте).
Эти шликеры были нанесены на алюминиевую фольгу (токосборник), высушены и раскатаны, в результате чего были изготовлены положительные электроды, состоящие из токосборника и слоя активного материала для положительного электрода в виде последовательных слоев.
[0109] <Изготовление тестовых образцов>
Тестовые образцы монетного типа были изготовлены таким же способом, что и в Примере 2, с использованием вышеописанных положительных электродов, содержащих активные материалы для положительного электрода из Примеров с 9 по 12.
[0110] <Метод испытания>
Три цикла зарядки-разрядки вышеупомянутых тестовых образцов было произведено при описанных ниже условиях, и были оценены их зарядно-разрядные характеристики.
- Диапазон напряжений: Пример 9: от 3,0 В до 4,7 В; Примеры с 10 по 12: от 3,0 В до 4,8 В
- Плотность тока: 17 мА/г
- Температура: 25°C.
[0111] ФИГ. 16 отображает соотношение между удельной энергоемкостью и напряжением в третьем цикле (кривая разрядки и кривая зарядки). На ФИГ. 16, (а) отображает результаты Примера 9, (b) отображает результаты Примера 10, (с) отображает результаты Примера 11, и (d) отображает результаты Примера 12.
Как показано на ФИГ. 16, все Примеры с 9 по 11 продемонстрировали очень хорошие параметры разрядной емкости в пределах от 90 мАч/г до 95 мАч/г в диапазоне высоких напряжений от 3,0 В до 4,8 В. Пример 12 показал разрядную емкость, равную 35 мАч/г, в диапазоне высоких напряжений от 3,0 В до 4,8 В.
[0112] В частности, в Примерах 10 и 11, где некоторая часть Со2+ в составе Na4Co3,0(PO4)2P2O7 была замещена марганцем Mn2+ и никелем Ni2+ при 0,3≤b≤1,0 и 0,3≤с≤1,0 в общей формуле Na4Co(3-b-c)MnbNic(PO4)2(P2O7), было отмечено улучшение как емкостной характеристики, так и характеристики напряжения, по сравнению с Примером 9 (Na4Co3.0(PO4)2P2O7). Это, по-видимому, обусловлено тем, что в случаях, когда коэффициенты замещения Со2+ марганцем Mn2+ и никелем Ni2+ находятся в указанных диапазонах (0,3≤b≤1,0, 0,3≤с≤1,0), замещающий Mn2+ может быть компенсирован по заряду не только до Mn2+/3+, но даже до Mn3+/4+ в диапазоне напряжений от 4,7 В и выше, а замещающий Ni2+ становится Ni3+ при высоком напряжении так, что зарядная компенсация Ni2+/3+ происходит при высоком напряжении.
[0113] В Примере 8 где, в общей формуле Na4CO(3-a)Mna(PO4)2(P2O7), Со2+ был замещен Mn2+ при а (индекс/коэффициент Mn)=0,9, наблюдалось снижение емкостной характеристики и характеристики напряжения по сравнению с Примерами 5 по 7. И напротив, при замещении некоторой части Со никелем Ni в дополнение к Mn, даже когда b (индекс/коэффициент Mn)=1,0, как в Примере 11, подтвердилось улучшение емкостной характеристики и характеристики напряжения. На основании этих результатов, несмотря на то, что замещение Со2+ марганцем Mn2+ должно было, как ожидалось, повлечь за собой снижение электронной проводимости активного материала, можно предположить, что благодаря замещению Со2+ марганцем Mn2+ и дополнительно никелем Ni2+, который имеет относительно высокую электронную проводимость, можно компенсировать снижение электронной проводимости активного материала, вызываемое Mn2+.
[0114] Таким образом, при сопоставлении результатов Примера 3 с результатами Примеров 1 и 2, становится очевидно, что как активные материалы для положительного электрода, в которых М=Ni, так и активные материалы для положительного электрода, в которых М=Mn, отличаются худшими емкостными характеристиками, по сравнению с активными материалами для положительного электрода, в которых М=Со. Вероятно, именно поэтому принято считать, что замещение некоторого количества Со марганцем Mn или никелем Ni приводит к ухудшению эксплуатационных параметров аккумулятора. Таким образом, тот факт, что за счет замещения Со2+ марганцем Mn2+ и никелем Ni2+ при 0,3≤b≤1,0 и 0,3≤с≤1,0 в общей формуле Na4Co(3-b-c)MnbNic(PO4)2(P2O7), как указано выше в Примерах 10 и 11, можно улучшить как емкостные характеристики, так и параметры рабочего напряжения, является дополнительным полезным эффектом изобретения.
[0115] 1: Отрицательный электрод
2: Положительный электрод
3: Слой электролита
4: Слой активного материала для отрицательного электрода
5: Токосборник отрицательного электрода
6: Слой активного материала для положительного электрода
7: Токосборник положительного электрода
8: Натриевый перезаряжаемый аккумулятор.
Изобретение относится к активному материалу для положительного электрода натриевого аккумулятора, имеющего кристаллическую структуру, принадлежащую к пространственной группе Pn21a, представленному приведенной ниже общей формулой (1):
 где М представляет, по меньшей мере, один из элементов, выбранный из группы, состоящей из: марганца, железа, кобальта и никеля; А представляет, по меньшей мере, один из элементов, выбранный из группы, состоящей из: кремния, фосфора или серы; x удовлетворяет условию 4≥х≥2; y удовлетворяет условию 4≥y≥1, и оба индекса z и w больше или равны 1. Также изобретение относится к способу получения материала. Предложенный материал имеет высокое рабочее напряжение и может быть заряжаем и разряжаем при высоком напряжении. 2 н. и 11 з.п. ф-лы, 4 табл., 12 пр., 16 ил.
где М представляет, по меньшей мере, один из элементов, выбранный из группы, состоящей из: марганца, железа, кобальта и никеля; А представляет, по меньшей мере, один из элементов, выбранный из группы, состоящей из: кремния, фосфора или серы; x удовлетворяет условию 4≥х≥2; y удовлетворяет условию 4≥y≥1, и оба индекса z и w больше или равны 1. Также изобретение относится к способу получения материала. Предложенный материал имеет высокое рабочее напряжение и может быть заряжаем и разряжаем при высоком напряжении. 2 н. и 11 з.п. ф-лы, 4 табл., 12 пр., 16 ил. 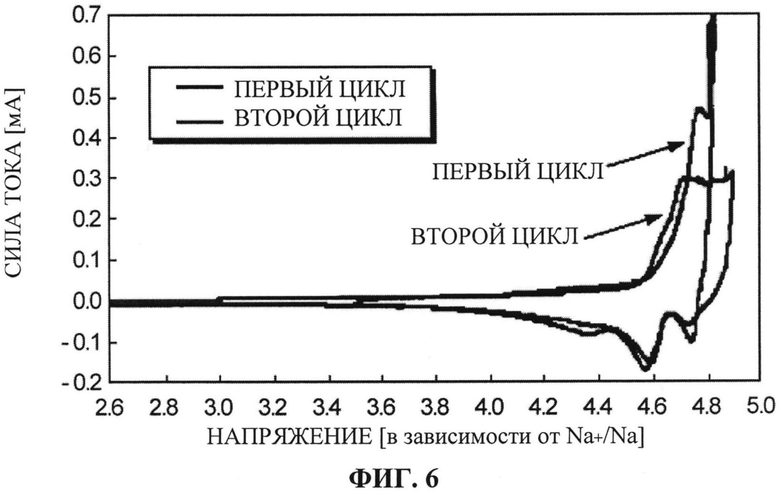
1. Активный материал для положительного электрода натриевого аккумулятора, имеющий кристаллическую структуру, принадлежащую к пространственной группе Pn21a, представленный приведенной ниже общей формулой (1):

где М представляет, по меньшей мере, один из элементов, выбранный из группы, состоящей из: марганца, железа, кобальта и никеля; А представляет, по меньшей мере, один из элементов, выбранный из группы, состоящей из: кремния, фосфора или серы; x удовлетворяет условию 4≥х≥2; y удовлетворяет условию 4≥y≥1, и оба индекса z и w больше или равны 1.
2. Активный материал для положительного электрода по п. 1, в котором элемент М в формуле (1) до зарядки является двухвалентным.
3. Активный материал для положительного электрода по п. 1, в котором М в формуле (1) представляет, по меньшей мере, один из элементов, выбранный из группы, состоящей из: марганца, кобальта и никеля, при этом некоторая часть такого элемента замещена, по меньшей мере, одним из элементов, который отличается от М, и который представлен, по меньшей мере, одним из элементов, выбранным из группы, состоящей из: марганца, железа, кобальта и никеля.
4. Активный материал для положительного электрода по п. 1, в котором М в формуле (1) представлен никелем, при этом некоторая часть никеля замещена, по меньшей мере, одним из элементов, выбранным из группы, состоящей из: марганца, железа и кобальта.
5. Активный материал для положительного электрода по п. 1, в котором А в формуле (1) представлен, по меньшей мере, одним из элементов, выбранным из группы, состоящей из: кремния, фосфора и серы, при этом некоторая часть такого элемента замещена, по крайней мере, одним из элементов, отличающимся от А, и который представлен, по меньшей мере, одним из элементов, выбранным из группы, состоящей из: кремния, фосфора и серы.
6. Активный материал для положительного электрода по п. 1, в котором А в формуле (1) представлен фосфором, при этом некоторая часть фосфора замещена, по меньшей мере, одним из элементов, выбранным из группы, состоящей из: кремния и серы.
7. Активный материал для положительного электрода по п. 1, представленный общей формулой Na4Ni3(PO4)2(P2O7).
8. Активный материал для положительного электрода по п. 1, представленный общей формулой Na4Mn3(PO4)2(P2O7).
9. Активный материал для положительного электрода по п. 1, представленный общей формулой Na4Co3(PO4)2(P2O7).
10. Активный материал для положительного электрода по п. 1, представленный общей формулой Na4Co(3-a)Mna(PO4)2(P2O7), (где "а" удовлетворяет условию 0,3≤а≤0,8).
11. Активный материал для положительного электрода по п. 1, представленный общей формулой Na4Co(3-b-c)MnbNic(PO4)2(P2O7) (где "b" удовлетворяет условию 0,3≤b≤1,0 и "с" удовлетворяет условию 0,3≤с≤1,0).
12. Способ изготовления активного материала для положительного электрода по любому из пп. с 1 по 11,
включающий:
этап предварительного обжига, на котором осуществляется обжиг смеси исходных материалов, включающей, по меньшей мере, Na-содержащее соединение, М-содержащее соединение, в которое входит указанный элемент М, А-содержащее соединение, в которое входит указанный элемент А, и Р-содержащее соединение, на открытом атмосферном воздухе при температуре от 150 до 500°C; и
этап основного обжига, на котором осуществляется обжиг полученного таким образом предварительно обожженного материала на открытом атмосферном воздухе при температуре от 500 до 800°C после завершения этапа предварительного обжига.
13. Способ по п. 12, который дополнительно включает этап уменьшения размера частиц Na-содержащего соединения, М-содержащего соединения, А-содержащего соединения и Р-содержащего соединения до этапа предварительного обжига.
| JP 2010015782 A, 21.01.2010 | |||
| ПНЕВМАТИЧЕСКОЕ УСТРОЙСТВО УДАРНОГО ДЕЙСТВИЯ С ДРОССЕЛЬНЫМ ВОЗДУХОРАСПРЕДЕЛЕНИЕМ | 2005 |
|
RU2301890C2 |
| Вторичный химический источник тока | 1985 |
|
SU1691914A1 |
Авторы
Даты
2015-10-20—Публикация
2012-06-13—Подача