Изобретение относится к области клеточной биологии и биотехнологии, конкретно к предифференцировке некоммитированных стволовых клеток стромы костного мозга в тирозингидроксилаза - позитивные клетки.
Стромальные клетки костного мозга выделяют из образцов красного костного мозга, полученных из гребня подвздошной кости. Образцы измельчают, культивируют в среде, содержащей культуральные среды RPMI 1640, F12, эмбриональную сыворотку теленка в соотношении 4:4:2 (среда 1). После образования монослоя прикрепленных клеток их рассевают на культуральные сосуды, содержащие среду следующего состава: среда 1-50%, супернатант культуры ножек мозга эмбриона свиньи шестой недели гестации - 50% (среда 2). В процессе культивирования популяция клеток костного мозга обогащалась клетками, несущими тирозингидроксилазу. Как известно, такие клетки могут быть предшественниками дофамин-продуцирующих нейронов, локализующихся в нигростриальной системе мозга. Уменьшение количества или активности этих нейронов приводит к снижению синтеза дофамина, что влечет за собой серьезное поражение нервной системы, носящее название болезнь Паркинсона. Таким образом, настоящее изобретение позволяет получить аутологичную культуру клеток стромы костного мозга, обогащенную прекоммитированными стволовыми клетками, несущими тирозингидроксилазный маркер. Эти клетки могут найти применение в клеточной терапии болезни Паркинсона.
Изобретение относится к области клеточной биологии, биотехнологии и трансплантационной терапии, конкретно к предифференцировке некоммитированных стволовых клеток стромы костного мозга в тирозингидроксилаза-позитивные клетки.
В последние годы появились многочисленные данные, свидетельствующие о высокой пластичности клеток высших животных, наличии скрытых резервов обновления соматических клеток в постнатальном онтогенезе благодаря поддержанию пула стволовых клеток - предшественниц различных ветвей клеточной дифференцировки. На сегодня сформулировано понятие как о тотипотентной (зиготе), так и мультипотентной стволовой клетке. Мультипотентная стволовая клетка наделена неизменной способностью к самообновлению, поддерживаемой на протяжении всей жизни организма. Эти клетки превосходят все другие клетки организма по пролиферативному потенциалу. К хорошо изученным представлениям о гематопоэтической стволовой клетке добавились многочисленные исседования, посвященные свойствам мезенхимальных и эпидермальных стволовых клеток. В дальнейшем было показано наличие нейральной стволовой клетки в головном мозге млекопитающих как у эмбрионов, так и у взрослых организмов. Активно пролиферирующие нейральные предшественники персистируют в специфических зонах центральной нервной системы взрослых млекопитающих. Они локализованы в субэпендимальной зоне, зубчатой извилине гиппокампа и обонятельной луковице головного мозга. Эти клетки дают начало нейронам и глии и способны поддерживать локальный нейрогенез в течение всей жизни. Не так давно такие зоны были обнаружены в других областях ЦНС. Нейральные предшественники включают в себя гетерогенную популяцию клеток, включающую мультипотентные стволовые клетки и их олиго- и унипотентных потомков.
Известно, что доступным источником аутологичных стволовых клеток для трансплантации является костный мозг пациента. Также известно, что возможна предифференцировка этих клеток в нестин-позитивные клетки, по многим данным, являющиеся предшественниками нейральных клеток разных стадий дифференцировки.
Мы предположили, что факторы, выделяемые клетками определенной стадии развития эмбрионального мозга, могут предифференцировать мезинхимально-подобные клетки стромы костного мозга в прогенитальные клетки, могущие в дальнейшем дифференцироваться в дофамин-продуцируюшие нейроны или клетки, производящие тирозингидроксилазу. Этот фермент, который является ключевым ферментом синтеза дофамина, производится в аркуатном ядре недофаминергическими нейронами. Показано, что эти нейроны участвуют в кооперативном синтезе дофамина, что рассматривается, с одной стороны, как новый уровень химической интеграции мозга, а с другой - как адаптивная реакция при функциональной недостаточности дофаминергической системы. Известно, что маркером таких клеток является фермент тирозингидроксилаза.
Уровень техники
Известен способ нейральной предифференцировки мезенхимальных стволовых клеток костного мозга в нейроны in vivo под действием 27-суточного культивирования в среде ,содержащей эпидермальный ростовой фактор (EGF) в концентрации 2 нг/мл (Земчихина В., Цитология, т. 47, 2005, № 7, с. 644-648). Однако этот способ не приводит к образованию тирозинкиназа-позитивных клеток.
Наиболее близким способом, использованным нами как прототип, является способ нейральной предифференцировки стромы костного мозга для лечения болезни Паркинсона под действием ретиноевой кислоты (Щегельская Е. и др. Дифференцировка in vitro клеток стромы костного мозга мыши в клетки-предшественники нейронов и гепатоцитов. Экспериментальная и клиническая медицина, № 1, с. 16-20, Валошина и др. Аутотерапия стромальными клетками костного мозга (КСКМ), индуцированными в нервные, у больных с хроническими заболеваниями ЦНС (рассеянный склероз, болезнь Паркинсона). 2003, Украiнський нейрохiрургiчний журнал, № 3, с. 54-61). Строму костного мозга индуцировали в предифференцировку добавлением различных количеств низкомолекулярного гидрофобного агента - ретиноевой кислоты. Однако данный способ не приводит к образованию тирозингидроксилаза-позитивных клеток.
Поэтому нами предложен способ обогащения культуры стромы костного мозга тирозингидроксилаза-позитивными клетками. Известно, что дофамин в мозгу продуцируют клетки Пуркинье, локализованные в нигростриальной системе ножек мозга. Там же локализованы и тирозинкиназа-продуцирующие клетки. Поэтому нами была получена первичная культура ножек мозга свиньи. Свинья была использована, как одно из животных, мозг которого наиболее близок к человеческому по многим параметрам. Кроме того, в связи с тем, что человек употребляет в пищу мясо и субпродукты свиньи, в том числе мозг, человеческий организм адаптирован к большей части вирусов свиньи. Так как для получения препарата мозга использовали эмбрион свиньи, полученный в стерильных условиях, и культура проверялась на бактериальный пророст, то возможность бактериального заражения при получении препаратов исключалась.
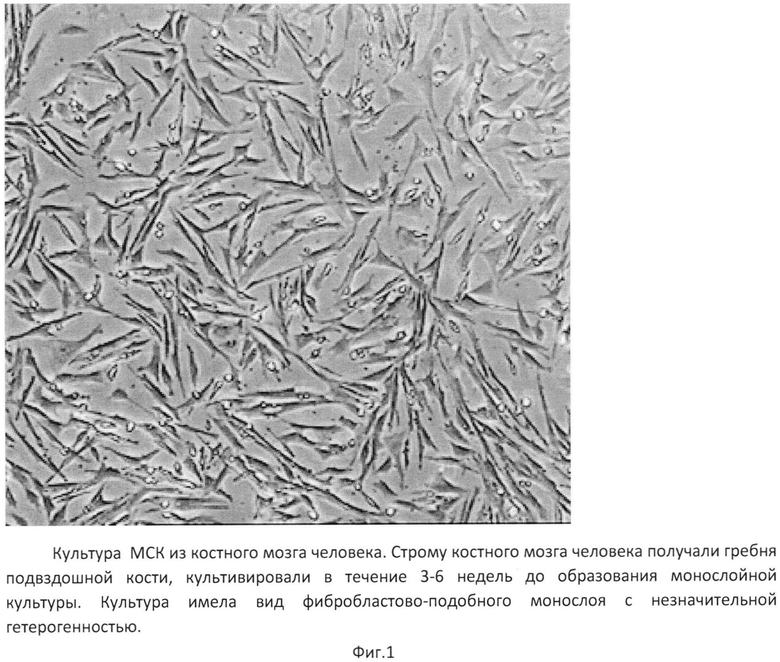
Препарат ножек мозга, содержащего нигростриальную систему, эмбрионов шестинедельных поросят переводили в культуру путем их коллагеназной обработки и дальнейшего культивирования в монослойной культуре. Супернатант монослойной культуры на разных сроках культивирования использовали для попыток предифференцировки костного мозга человека. Строму костного мозга человека получали следующим образом: 1 мл красного костного мозга из подвздошной кости измельчали и культивировали в течение 3-6 недель в плоскодонных флаконах до образования монослойной культуры. Культура имела вид фибробласто-подобного монослоя с незначительной гетерогенностью (фиг. 1). Полученные клетки переносили для опыта в плоскодонные культуральные флаконы и подвергали обработке средой, содержащей супернатант от культуры ножек мозга эмбриона свиньи. После семидневной инкубации клетки фиксировали, проводили иммуноцитохимию на наличие тирозингидроксилазы. Для этого фиксированные метанолом клетки монослоя стромы костного мозга обрабатывали моноклональными антителами к тирозингидроксилазе, а затем коньюгатом кроличьих антител против иммуноглобулинов мыши, меченных флуоресцеином. Реакцию учитывали под люминесцентным микроскопом при увеличении ×400.
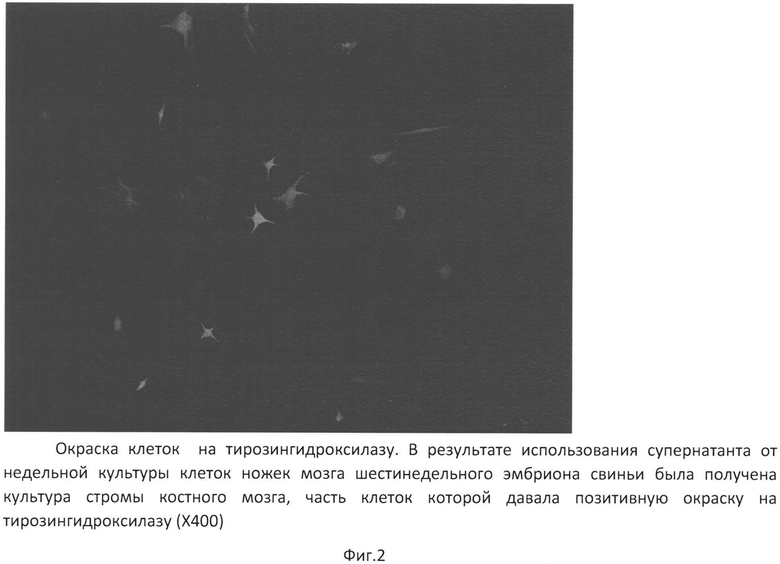
В результате использования супернатанта от недельной культуры клеток ножек мозга шестинедельного эмбриона свиньи была получена культура стромы костного мозга, часть клеток которой давала позитивную окраску на тирозингидроксилазу (фиг. 2). Это свидетельствует о прошедшей предифференцировке в направлении клеток, обладающих потенцией стимулировать продукцию дофамина клетками Пуркинье. Супернатант от 3-4-недельной культуры ножек мозга эмбриона свиньи не обладал свойством предифференцировать клетки костного мозга человека в тирозинкиназа-позитивные клетки.
Сущность изобретения
Предложенный нами способ получения культура аутологичных клеток стромы костного мозга может в дальнейшем быть использован для попыток терапии нейродегенеративных заболеваний, в первую очередь болезни Паркинсона, путем их трансплантации в мозг пациентов с дисбалансом в синтезе тирозингидроксилазы и дофамина. Ранее показано на моделях животных с паркинсонизмом, что инъекция векторов на основе аденоассоциированных вирусов, несущих ген тирозингидроксилазы в стриатум, удается получить синтез этого фермента de novo и опосредованное повышение синтеза дофамина (Haque N., Isacson O. (1997). Exp. Neurol. 144(1). Р. 139-146). При этом снимаются проблемы, связанные с аллогенной и ксеногенной трансплантацией аналогичных клеток.
Пример
Культуру стромы костного мозга человека получали следующим образом.
Пример 1. Фрагменты костного мозга получили трепанацией гребня подвздошной кости пациента 65-летнего возраста. На надкостнице был произведен п-образный надрез размером 1,5×1,5×1,5 см. Надкостницу отогнули и ложкой Фольксмана извлекли 1,5 мл красного костного мозга. Затем надкостницу вернули в исходное положение и заклеили медицинским клеем. Образец был помещен в транспортную среду следующего состава: RPMI 1640 - 97%, фетальная сыворотка теленка - 3%, гентамицин - 200 мг на мл. В течение не более 120 мин фрагменты костного мозга транспортировали в ламинарный бокс для дальнейшей обработки в стерильных условиях. Затем фрагменты извлекли и поместили в стерильную чашку Петри, содержащую среду следующего состава среда RPMI 1640 97%, фетальная бычья сыворотка 3%, гентамицин 100 мг/мл, а также фунгизон и глютамин. Транспортную среду с вымытыми в нее отдельными клетками центрифугировали 10 минут при 1000 оборотах в минуту. Супернатант удалили и ресуспендировали осадок в свежей порции среды того же состава для отмывки. После третьего центрифугирования осадок ресуспендировали в среде для культивирования следующего состава: RPMI 1640, DMEM и фетальную сыворотку в соотношении 4:4:2, пенициллин 100 ед./мл, стрептомицин 100 мг/мл, амфотерицин 0,25 мг/мл, L-глутамина 2 мМ из расчета 250-500 тысяч ядросодержащих клеток в мл. Фрагменты измельчили и интенсивно промыли, отделяя от свободных клеток. Затем фрагменты и предварительно отцентрифугированные свободные клетки поместили в отдельные культуральные сосуды в среде для культивирования, описанной выше. После суточного культивирования неприкрепившиеся клетки удалили, центрифугировали и поместили для культивирования в отдельные флаконы со средой, описанной выше. Клетки культивировали 6 недель до образования монослоя. Смену среды проводили каждые двое суток. Монослойные культуры объединяли и использовали для опытов.
Культуру ножек мозга получали следующим образом. Эмбрионы, не вскрывая матки, доставляли в стерильный бокс в течение часа после извлечения из матери. Затем рога матки вскрывали и извлекали эмбрионы. После удаления свода черепа и вышележащей части мозга извлекали ножки мозга и помещали в среду следующего состава: RPMI 1640 - 97%, фетальная сыворотка теленка - 3%, гентамицин - 200 мг/мл. Затем ткань ножек мозга измельчали на фрагменты диаметром 1-2 мм и подвергали коллагеназному расщеплению в течение 20-120 минут при температуре +37°С в атмосфере, содержащей 6% СО2. Клетки однократно отмывали средой того же состава и помещали для культивирования в плоскодонные культуральные сосуды, содержащие среду следующего состава: RPMI 1640, DMEM и фетальная сыворотка теленка в соотношении 4:4:2, пенициллин 100 ед./мл, стрептомицин 100 мг/мл, амфотерицин 0,25 мг/мл, L-глутамина 2 мМ из расчета 250-500 тысяч ядросодержаших клеток в мл. Среду меняли каждые два-три дня. Супернатант с культуры замораживали при температуре -40°С и в дальнейшем использовали для опытов, предварительно фильтруя его через фильтр с диаметром пор 0,22 мкм для стерилизации и удаления детрита.
Для опытов по предифференцировке клетки стромы костного мозга рассевали из расчета 200 тыс. клеток в мл на 12-луночные полистироловые плашки. После образования монослоя прикрепленных клеток их рассевали на культуральные сосуды, содержащие среду следующего состава: среда 1-50%, супернатант культуры ножек мозга эмбриона свиньи шестой недели гестации - 50% (среда 2). Окраску на тирозингидроксилазу производили с помощью моноклональных антител против тирозинкиназы методом непрямой иммунофлюоресценции.
Изобретение относится к области биотехнологии. Описан способ предифференцировки стромальных стволовых клеток костного мозга. Способ предусматривает получение монослойной культуры стромы костного мозга человека, получение культурального супернатанта ножек мозга эмбриона свиньи шестой недели гестации и использование этой среды для обогащения популяции тирозингидроксилаза-позитивными клетками культуры стромы костного мозга путем инкубации его в среде, содержащей 50% супернатанта трехдневной культуры ножек мозга эмбриона свиньи. Полученные аутологичные клетки стромы костного мозга могут быть использованы для терапии нейродегенеративных заболеваний. Изобретение может быть использовано в медицине. 2 ил., 1 пр.
Способ предифференцировки стромальных стволовых клеток костного мозга, отличающийся тем, что для обогащения популяции тирозингидроксилаза-позитивными клетками монослой инкубируют в среде, содержащей 50% супернатанта трехдневной культуры ножек мозга эмбриона свиньи шестой недели гестации.
| ЩЕГЕЛЬСКАЯ Е, и др., "Дифференцировка in vitro клеток стромы костного мозга мыши в клетки предшественники нейронов и гепатоцитов", Экспериментальная и клиническая медицина, N1, с.16-20.ЗЕМЧИХИНА В.Н | |||
| и др., "СПОСОБНОСТЬ МЕЗЕНХИМНЫХ СТВОЛОВЫХ КЛЕТОК К НЕЙРАЛЬНОЙ ДИФФЕРЕНЦИРОВКЕ IN VITRO", Цитология, т.47 N7, 2005, с.644-648.RU 2368378 C1, 27.09.2009.RU 2249039 C2, 27.03.2005 |
Авторы
Даты
2015-11-10—Публикация
2014-08-22—Подача