Область техники, к которой относится изобретение
Настоящее изобретение относится к области водной биотехнологии, в частности, к применению композиций, содержащих PACAP, и PACAP, для лечения вирусных инфекций или инфекционных заболеваний, вызываемых вирусами, у водных организмов. Оно также относится к применению PACAP в комбинации с противовирусными средствами для лечения инфекций, вызываемых вирусом.
Уровень техники, предшествующий изобретению
В настоящее время ежегодный вклад культуры водных видов в общей объем производства рыбы и моллюсков увеличился. Однако более высокие плотности приводят к тому, что эти животные обитают в условиях стресса, и в основном они являются более восприимчивыми к инфекциям. Вспышки вызываемых патогенами заболеваний в аквакультуре приводят к крупным экономическим потерям и даже иногда приводят к удалению определенной культуры из конкретного региона.
Поражения, вызываемые вирусом инфекционного панкреатического некроза (IPNV), вирусом вирусной геморрагической септицемии (VHSV), вирусом инфекционной анемии лососевых (ISAV) и вирусом инфекционного гематопоэтического некроза (IHNV), у лососевых являются основной причиной вспышек заболеваний в их культуре (Marroqui et al. (2008) Antiviral Research 80:332-338). Например, предполагают, что производство чилийского лосося к концу 2010 года упадет на 38,7% (с 403000 тонн в 2009 году до 245000 тонн в 2010 году) в результате смертности, вызванной ISAV (http://www.aqua.cl).
Кроме того, ракообразные являются одним из наиболее важных экономических секторов в мировой аквакультуре, привнося вклад более 10 миллиардов ежегодно. Креветки в культуре восприимчивы к широкому спектру патогенов, включая вирусы. По оценке, в середине 90-х годов приблизительно 40% мирового производства (эквивалентного 3 миллиардам долларов США) было потеряно вследствие заболеваний. Пять вирусов являются основными факторами этих потерь: вирус синдрома белых пятен (WSSV), вирус синдрома желтой головы (YHV), вирус синдрома Таура (TSV), вирус инфекционного гематопоэтического некроза (IHNNV) и монодон-бакуловирус (MBV) (описано Johnson et al. (2008) Vaccine 26:4885-4992).
Двустворчатые моллюски являются важной частью мирового производства моллюсков. Эти организмы, характеризующиеся тем, что являются фильтратами, являются основными резервуарами вирусов, таким образом, их культура может переживать эпизоотии, которые угрожают их производству. Описана массовая гибель взрослых устриц Crassostrea angulata, ассоциированная с вирусными инфекциями, сходными с иридовирусами. Кроме того, другие вирусы семейств Herpesviridae, Papovaviridae, Togaviridae, Retroviridae, Reoviridae, Birnaviridae и Picornaviridae способны инфицировать культуры двустворчатых моллюсков. Однако вследствие отсутствия клеточных линий, полученных у моллюска, и ограничивающих существующих средств молекулярной биологии для этих организмов, вирусология двустворчатых моллюсков все еще остается примитивной наукой, основанной преимущественно на морфологических исследованиях и незначительном количестве экспериментальных исследования (описано T. Renault and B. Novoa (2004) Aquat. Living Resour. 17:397-409).
Противовирусные лекарственные средства представляют собой химические соединения, используемые для лечения инфекций, вызываемых вирусами. Первые экспериментальные противовирусные средства были описаны в начале 60-х годов. Они были получены на основе метода "проб" и "ошибок". Однако после середины 80-х годов наука существенно изменилась, и в последние годы получено и зарегистрировано много новых противовирусных лекарственных средств, главным образом для лечения вируса иммунодефицита человека (ВИЧ). Однако вследствие того, что эти соединения не всегда являются эффективными или хорошо переносимыми, существует много аспектов, которые необходимо улучшать. Дополнительными причинами для совершенствования разработки и применения этих лекарственных средств является возникновение устойчивости вирусов или ассоциированных с ней побочных эффектов (De Clercq (2002) Nature Reviews Drug Discovery 1:13-25). При разработке противовирусного лекарственного средства в качестве основных мишеней выступают вирусные белки или белки клетки-хозяина. Первая стратегия приводит к более специфичным и менее токсичным соединениям, но с более узким спектром противовирусной активности и более высокой вероятностью развития устойчивости. Вторая стратегия приводит к открытию противовирусных соединений с более широким спектром активности, меньшей вероятностью развития устойчивости, но более высокой вероятностью оказания токсического действия на клетки. Выбор стратегии зависит от природы вируса и потенциальных мишеней в вирусе или в клетках-хозяевах (De Clercq (2002) Nature Reviews Drug Discovery 1:13-25).
Рибавирин представляет собой противовирусное соединение широкого спектра действия с активностью против широкого диапазона ДНК- и РНК-вирусов. Он представляет собой нуклеозидный аналог, который после внутриклеточного фосфорилирования становится конкурентным ингибитором инозинмонофосфатдегидрогеназы (IMPDH), клеточного фермента вовлеченного в синтез гуанозинмонофосфата (GMP) (Graci and Cameron, (2006) обзор в Medical Virology 16:49-63, Parker, (2005) Virus Research 107:165-171). В дополнение к ингибированию этого фермента существует три других механизма, которые были предложены для объяснения противовирусной активности этого соединения: прямым ингибированием вирусной РНК-полимеразы (Toltzis et al. (1988) Antimicrobial Agents and Chemotherapy 32:492-497), ингибированием добавления кэпа на 5'-конце вирусной матричной РНК (мРНК) (Goswami et al. (1979) Biochemical and Biophysical Research Communications 89:830-836) и накоплением мутаций (Graci y Cameron, (2002) Virology 298:175-180).
К настоящему времени не существует специфических противовирусных лекарственных средств, одобренных для лечения вирусных заболеваний у водных организмов. В Чили дочерняя компания Diagnotec SA, именуемая Andromaco, разработала новое противовирусное соединение, называемое VIROTOP, для лечения вирусных заболеваний у рыб. Это противовирусное средство рассматривают для утверждения "Servicio Agricola y Ganadero" (SAG) (http://www.aqua.cl). Однако значительное количество соединений оценивали in vitro и in vivo (Hudson et al. (1988) Antiviral Research 9:379-385, Jasher et al. (2000) Antiviral Research 45:9-17, Kamei and Aoki, (2007) Archives of Virology 152:861-869, LaPatra et al. (1998) Fish and Shellfish Immunology 8:435-446, Mas et al. (2006) Antiviral Research 72:107-115, Micol et al. (2005) Antiviral Research 66:129-136, Moya et al. (2000) Antiviral Research 48:125-130), для которых показаны различные степени эффективности.
На личинках кижуча (Oncorhynchus kisutch) и радужной форели (Oncorhynchus mykiss), экспериментально инфицированных IPNV, оценивали in vivo введение аналога рибавирина, 5-этинил-1-β-D-рибофуранозилимидазолкарбоксамида (EICAR) (Moya et al. (2000) Antiviral Research 48:125-130). Лечение состояло из ежесуточных погружений в ванны с раствором 0,4 и 0,8 мкг/мл EICAR в течение двух часов на протяжении 20 суток. Результаты указывают на то, что выживаемость инфицированных и получавших лечение EICAR групп являлась сходной с выживаемостью в не инфицированных вирусом группах. Анализ вирусной нагрузки в печени и селезенки проводили с применением способа полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР). Этим анализом было продемонстрировано снижение вирусной нагрузки у животных, получавших лечение противовирусным средством. Из этого исследования сделали вывод, что EICAR является ингибитором репликации IPNV, таким образом, его применение для снижения вирусной нагрузки и предотвращения смертности рыб является полезным средством для увеличения продуктивности культур. Однако противовирусное лечение не пригодно для селекционного отбора, т.к. инфицированная и получавшая лечение рыба все еще несет вирус и может передавать его потомству. С другой стороны, выявлено, что одним из нарушений, вызываемых некоторыми вирусными инфекциями, является потеря массы инфицированной рыбы (Wolf (1986) The fish viruses. In: Espinosa de los Monteros, J. Labarta U. (Eds.), Patologia en Acuicultura. Industrias graficas, Espana, SL, pp. 93-95, Moya et al. (2000) Antiviral Research 48:125-130).
Дополнительное преимущество использования противовирусных средств заключается в том, что такая потеря массы является намного ниже у получавшей лечение рыбы. Этот эффект был наиболее заметен у форели, чем у кижуча (Moya et al. (2000) Antiviral Research 48:125-130).
Активирующий аденилатциклазу гипофиза полипептид (PACAP) принадлежит к суперсемейству секретин/глюкагон/вазоактивному интестинальному пептиду. Этот пептид впервые был выделен из гипоталамуса быка в 1989 году. Была показана его способность стимулировать выделение гормона роста посредством активации аденилатциклазы и последующей стимуляции продукции аденозинмонофосфата (цАМФ) (Miyata et al (1989) Biochem. Biophys. Res. Commun. 164:567-574). PACAP представляет собой многофункциональный нейропептид, который играет важную роль в качестве нейромедиатора, нейротрансмиттера и вазодилататора у млекопитающих (Arimura A. (1998) Japanese Journal of Physiology 48:301-31). Была показана его функция в регуляции клеточного деления, дифференцировке и гибели клеток (Sherwood et al. (2000) Endocrine Review 21:619-670). Этот пептид существует в двух различных молекулярных формах: 27 а/к (PACAP27) и 38 а/к (PACAP38) (Miyata et al. (1990) Biochemical and Biophysical Research Communications 170:643-8). Эффекты PACAP проявляются через семейство трех рецепторов VIP/PACAP, которые принадлежат к связанному с G-белком рецептору типа секретина. Рецепторы VPAC-1 и VPAC-2 обладают сходными аффинностями к двум нейропептидам VIP и PACAP, тогда как рецептор PACAP (PAC-1) обладает более высокой аффинностью к PACAP, чем к VIP (Vaudry et al. (2000) Pharmacol. Rev. 52:269-324).
PACAP широко распространен в головном мозге млекопитающих, в основном в гипоталамусе, паравентрикулярном и дорсомедиальном ядрах таламуса, в перегородке, коре головного мозга, миндалевидном теле, гиппокампе и мозжечке (Montero et al. (2000) Journal of Molecular Endocrinology 25:157-168). Наиболее широко распространенной формой в центральной нервной системе и периферических тканях является PACAP38. В проведенных на млекопитающих исследованиях показано содержание PACAP также в половых железах (Shioda et al. (1994) Endocrinology 135:818-825), надпочечниках (Arimura et al. (1991) Endocrinology 129:2787-2789), паращитовидных железах (Vaudry et al. (2000) Pharmacol. Rev. 2000;52:269-324), эндокринной поджелудочной железе (Arimura and Shioda (1995) Neuroendocrinology 16:53-88) и желудочно-кишечном тракте (Arimura et al. (1991) Endocrinology 129:2787-2789, Vaudry et al. (2000) Pharmacol. Rev. 52:269-324, Hannibal et al. (1998) Cell Tissue Res. 291: 65-79).
PACAP и экспрессия его рецепторов в иммунных клетках выявлена только частично (Gaytan et al. (1994) Cell Tissue Res. 276:223-7, Abad et al. (2002) NeuroImmunoModulation 10:177-86). У млекопитающих выявлена конститутивная экспрессия рецептора VPAC-1 в лимфоцитах периферической крови людей и в лимфоцитах и макрофагах мышей, тогда как экспрессия VPAC-2 является индуцируемой в этих клетках. Кроме того, выявлена конститутивная экспрессия рецептора PAC-1 в перитонеальных макрофагах крысы и в клеточной линии миеломоноцитов человека THP-1. Кроме того, опубликована экспрессия PACAP в тимоцитах, различных подтипах T-клеток, B-клеток, спленоцитах и лимфоузлах у крыс (Delgado et al. (2001) J. Biol. Chem. 276:369-80, Pozo et al. (2003) Trends Mol. Med. 9:211-7).
PACAP описан в центральной нервной системе (в частности, в гипоталамусе, головном мозге и спинном мозге) и периферической нервной системе, иннервированных глазах, гипофизе, дыхательных путях, слюнных железах, желудочно-кишечном тракте, половом пути, поджелудочной железе и мочевыводящих путях у рыб (Sherwood et al. (2000) Endocrine Review 21:619-670).
PACAP ингибирует спонтанный апоптоз тимоцитов у крыс (Delgado (1996) Blood 87:5152-5161). Тот факт, что PACAP регулирует пролиферацию тимоцитов позволяет предположить, что этот пептид является важным регулятором созревания иммунных клеток (Delgado (1996) Blood 87:5152-5161).
Этот пептид оказывает опосредованное действие на созревание лимфоцитов посредством стимуляции высвобождения интерлейкина 6 (IL-6) фолликулярными клетками в гипофизе. IL-6 стимулирует рост и дифференцировку B-клеток и промотирует синтез и секрецию иммуноглобулинов этими клетками (Tatsuno et al. (1991) Endocrinology 129:1797-1804, Yada et al. (1993) Peptides 14:235-239). Кроме того, PACAP активирует и подавляет воспалительный ответ посредством регуляции IL-6 и IL-10 (Martinez et al. (1996) J. Immunol. 156(11):4128-36, Martinez et al. (1998) J. Neuroimmunol. 85(2):155-67), Martinez et al. (1998) J. Leukoc. Biol. 63(5):591-601). В активированных макрофагах PACAP ингибирует провоспалительные цитокины и стимулирует продукцию противовоспалительных цитокинов, обеспечивая гомеостаз иммунной системы. Кроме того, PACAP уменьшает экспрессию ко-стимулирующих молекул B7.1/B7.2 и последующую активацию T-хелперов (Th). С другой стороны, PACAP ингибирует продукцию IL-6 через свой рецептор PAC-1 в активированных макрофагах, подавляя воспаление (Martinez et al. (1998) J. Neuroimmunol. 85(2):155-67, Martinez et al. (1998) J. Leukoc. Biol. 1998 May, 63(5):591-601). Ингибиторное действие PACAP на транскрипцию IL-6 в ответ на значительные воспалительные стимулы или интоксикацию способствуют защите тканей и гомеостазу иммунной системы (Martinez et al. (1998) J. Neuroimmunol. 85(2):155-67, Martinez et al. (1998) J. Leukoc. Biol. 1998 May, 63(5):591-601). Наоборот, PACAP индуцирует экспрессию B7.2 и промотирует клеточную дифференцировку до Th2 в неактивированных макрофагах (Delgado and Ganea (2001) Arch. Immunol. Ther. Exp. (Warsz) 49(2):101-10).
В основном, функция PACAP в модуляции иммунной системы млекопитающего только частично была выявлена в последние годы. Этими исследованиями продемонстрировано, что PACAP регулирует врожденный и приобретенный иммунный ответ и модулирует про- и противовоспалительный ответ. Однако имеется недостаточно информации об эффекте этого пептида на противовирусный ответ. В последние годы было показано увеличение в плазме уровней PACAP-38 у пациентов с хроническим гепатитом B при устранении виремии вследствие лечения ламивудином (Elefsiniotis et al. (2003) European Journal of Gastroenterology and Hepatology 15:1209-1216). Это открытие позволяет предполагать действие на T-клеточный иммунный ответ, которое приводит к биохимической и гистологической ремиссии заболевания в печени пациента.
Опубликованные до настоящего времени исследования in vivo биологической функции PACAP у рыб в основном связаны с размножением (Canosa et al. (2008) American Journal of Physiology (Regul. Integr. Comp. Physiol.) 295:1815-21), развитием головного мозга (Sherwood et al. (2007) Peptides 28:1680-7) и аппетитом (Matsuda et al. (2005) Peptides 26:1611-6, Maruyama et al. (2006) Peptides 27:1820-6). В последние годы была показана биологическая функция этого нейропептида в росте и развитии личинок различных видов костистых рыб (Lugo et al. (2008) Journal of Endocrinology 197:583-97).
Знания о функции PACAP в модулировании иммунного ответа рыб ограничены исследованиями, проводимыми исследовательской группой авторов изобретения. Авторы продемонстрировали, что введение рекомбинантного PACAP Clarias gariepinus посредством погружения в ванны или инъекции не только способствует росту, а также стимулирует параметры врожденного иммунного ответа (лизоцим, производные оксида азота метаболиты и антиоксидантную защиту) и приобретенного иммунитета (IgM) у получавших лечение личинок и молоди (Carpio et al. (2008) Fish and Shellfish Immunology 25:439-45, Lugo et al. (2010) Fish and Shellfish Immunology 29:513-520). Эти новые свойства были описаны в патентной заявке "Neuropeptidos para el cultivo de organismos acuaticos" (WO2007/059714).
Одной из первых линий защиты против вирусных инфекций у позвоночных является система интерферона (IFN) I типа. Эта система активируется индукцией вирусом интерферонов I типа (IFNα и IFNβ) через рецептор IFN-α/β, который инициирует передачу опосредованного JAK-STAT сигнала. Индуцированные цитокины вызывают противовирусное состояние клетки, вызывая экспрессию белков с противовирусной активностью, таких как 2',5'-олигоаденилатсинтетаза, киназа R и ГТФазы Mx (Goodbourn et al. (2000) Journal of General Virology 81:2341- 2364). По полученным в последние годы сведениям установлено, что рыбы обладают системой IFN, аналогичной млекопитающим (Robertsen (2006) Fish and Shellfish Immunology 20:172-191, Robertsen (2008) Fish and Shellfish Immunology 25:351-357). Клонированы интерфероны некоторых видов рыб, таких как данио рерио (Danio rerio), североамериканский канальный сом (Ictalurus punctatus) и атлантический лосось (Salmo salar) (Altmann et al. (2003) Journal of Virology 77:1992-2002, Lutfalla et al. (2003) BMC Genomics 4:29, Robertsen et al. (2003) Journal of Interferon and Citokine Research 23:601-612, Long et al. (2006) Fish and Shellfish Immunology 21:42-59). Кроме того, установлены некоторые регуляторные факторы IFN, молекулы пути передачи сигнала JAK-STAT, белки Mx и другие гены, активируемые IFN у различных видов рыб. Сообщается о противовирусной активности, опосредованной белками Mx у Salmo salar и Paralichtys olivaceus (описано Robertsen (2006) Fish and Shellfish Immunology 20: 172-191).
Несмотря на то, что еще не открыты IFN-подобные гены у ракообразных, выявлена отрицательная регуляция молекул STAT (они представляют собой молекулы, которые активируются при IFN-ответе у позвоночных) в ответ на инфекцию WSSV. Отрицательная регуляция STAT при вирусной инфекции противоположна IFN-ответу I типа у млекопитающих (описано Johnson et al. (2008) Vaccine 26:4885-4992). Знания о противовирусном ответе у двустворчатых моллюсков еще меньше. Существуют данные о противовирусной активности в гемолимфе этих организмов, и высказано предположение о существовании IFN-подобного механизма (Olicarda et al. (2005) Antiviral Research 66(2-3):147-152, Defer et al. (2009) Aquaculture 293(1-2):1-7).
Для аквакультуры чрезвычайный интерес представляет получение новых соединений или композиций, которые можно использовать в борьбе с вирусными инфекциями, вследствие ущерба, который они вызывают в этом виде деятельности.
Описание изобретения
Настоящее изобретение относится к решению описанной выше задачи, предоставляя новую альтернативу борьбе с вирусными инфекциями в аквакультуре путем использования PACAP при получении композиций для лечения вирусных инфекций и вызываемых вирусом инфекционных заболеваний у водных организмов.
Термин "лечение" в контексте настоящего изобретения относится к любому положительному эффекту на ремиссию заболевания, которая включает ослабление, снижение или уменьшение патологического развития после начала заболевания.
Термин "противовирусное средство" в настоящем изобретении включает любую молекулу, определяемую как противовирусное средство в предшествующем уровне техники, или ее аналоги, функциональные производные или активные фрагменты.
Термин "активирующий аденилатциклазу гипофиза полипептид (PACAP)" в настоящем изобретении включает такую молекулу в любой форме (PACAP27 или PACAP38), как выделенную из природного источника, так и синтетическую, или полученную посредством технологии рекомбинантных ДНК.
В одном из вариантов осуществления изобретения виды нейропептида PACAP вводят отдельно или в комбинации с известной противовирусной молекулой рыбам, ракообразным и двустворчатым моллюскам посредством погружения в ванны с интервалом 2-3 суток. PACAP также вводят в виде пищевой добавки отдельно или в комбинации с известной противовирусной молекулой.
В настоящем изобретении продемонстрировано, что содержащие PACAP композиции, вводимые посредством погружения в ванны, инъекции или пероральным путем являлись эффективными, увеличивая выживаемость водного организма, инфицированного вирусом и получавшего лечение такими композициями. Не наблюдали снижение массы получавших лечение рыб. В некоторых случаях получали увеличение общей массы у инфицированных и получавших лечение животных по сравнению с инфицированными и не получавшими лечение. Анализом образцов ткани и восприимчивых органов ОТ-ПЦР показано снижение вирусной нагрузки у инфицированных и получавших лечение животных.
До настоящего изобретения не существовало знаний о том, модулирует или нет PACAP противовирусный ответ у рыб, ракообразных и двустворчатых моллюсков, и о вовлеченных механизмах. В настоящем изобретении впервые показана in vitro и in vivo взаимосвязь между PACAP и ответом на вирус у рыб, ракообразных и двустворчатых моллюсков. Кроме того, авторы изобретения впервые описывают неожиданное положительно действие на PACAP участвующих в противовирусном ответе молекул, таких как белок Mx, интерферон-гамма (IFN-γ) и Toll-подобный рецептор 9 (TLR9), а также регуляцию на дифференцировку этого пептида и его рецепторов в клетках иммунной системы рыб, обработанных вирусом и/или поли(I:C) in vitro и in vivo.
Лечение вирусных инфекций у рыб, ракообразных и двустворчатых моллюсков введением PACAP или комбинацией PACAP и молекулы с известным противовирусным действием у рыб ранее не описывали или не предполагали в существующем уровне техники.
В контексте настоящего изобретения введение PACAP и противовирусной молекулы может быть одновременным (в одном составе), последовательным или разделенным во времени. Препараты вводят водным организмам пероральным путем, посредством инъекции или погружения в ванны.
В настоящем изобретении рыб, ракообразных и двустворчатых моллюсков обрабатывают PACAP и препаратами, содержащими противовирусные молекулы, объединенные с PACAP. Неожиданно наблюдали, что нейропептид PACAP обладает противовирусным действием у рыб, ракообразных и двустворчатых моллюсков. С другой стороны, показано, что комбинация PACAP с веществами с известным противовирусным действие вызывает более высокий противовирусный ответ (синергическое действие) по сравнению с одним PACAP in vitro и in vivo. До настоящего времени не были определены биологические функции PACAP в противовирусном ответе у рыб. Кроме того, до настоящего времени ни PACAP, ни другой пептид, принадлежащий к суперсемейству секретина и глюкагона, не были выделены у креветки или моллюска. Современные знания об этих пептидах у этих таксомических групп основаны только на экспериментальных данных стимуляции роста креветок посредством экзогенного введения рекомбинантного PACAP рыбы (международная публикация патентной заявки номер WO2007/059714). Таким образом, до настоящего изобретения не существует знаний о его возможной взаимосвязи с ответом на вирус у ракообразных и двустворчатых моллюсков.
Другой целью настоящего изобретения является композиция для лечения вирусных и инфекционных заболеваний, вызываемых вирусами, у водных организмов, которая содержит "активирующий аденилатциклазу гипофиза полипептид" (PACAP). В одном из вариантов осуществления изобретения PACAP в виде части композиции получают выделением из природного источника, синтетически или посредством технологии рекомбинантных ДНК. Его вводят перорально, посредством инъекции или погружения в ванны. В одном из вариантов осуществления изобретения PACAP представляет собой полипептидную последовательность, выделяемую у рыб.
Настоящее изобретение также относится к ветеринарной комбинации, которая содержит "активирующий аденилатциклазу гипофиза полипептид" (PACAP) и противовирусную молекулу. В одном из вариантов осуществления изобретения противовирусная молекула представляет собой рибавирин или аналог рибавирина. Элементы, которые являются частью смеси, противовирусную молекулу и PACAP вводят одновременно, раздельно или последовательно во время одного и того же лечения. В одном из вариантов осуществления изобретения смесь используют при лечении вирусных и инфекционных заболеваний, вызываемых вирусами, у водных организмов. При этом PACAP и противовирусное средство вводят перорально, посредством инъекции или погружением в ванны.
В одном из вариантов осуществления изобретения PACAP используют в виде рецептированного корма в концентрации 50-750 мг/кг корма и противовирусную молекулу в концентрации от 100 до 2000 мг/кг корма. Во втором варианте осуществления изобретения PACAP используют в качестве части ветеринарной комбинации у рыб посредством инъекции в концентрации 0,1-10 мкг на грамм массы тела и противовирусное средство в концентрации 1-50 мкг/г. В другом варианте осуществления изобретения в таком составе PACAP используют у рыб или ракообразных посредством погружения в ванны в концентрации 50-1000 мкг на литр воды, и концентрация противовирусного средства составляет 100-2000 мкг/л. В изобретении PACAP, когда его используют в качестве противовирусного средства или в комбинации с известной противовирусной молекулой, используют у ряда водных организмов. Например, они включают лососевых, жгутиковых креветок и двустворчатых моллюсков.
Композиция, содержащая PACAP, и состав с противовирусной молекулой являются пригодными для терапевтического лечения вирусных инфекций, вызываемых вирусами, семейств Herpesviridae, Papovaviridae, Togaviridae, Retroviridae, Reoviridae, Birnaviridae и Picornaviridae.
В изобретении PACAP, когда его используют в качестве противовирусного средства, и состав с противовирусной молекулой используют для борьбы с инфекциями, вызванными IPNV, VHSV и ISAV. Также их используют при терапевтическом лечении вирусных инфекций, вызываемых WSSV, YHV, TSV, IHNNV и MBV.
Также частью настоящего изобретения является способ борьбы с вирусными инфекциями в управлении аквакультуры, включающему введение PACAP или содержащих PACAP ветеринарных комбинаций водным организмам в культуре.
Краткое описание чертежей
Фиг.1. Анализ экспрессии ПЦР в реальном времени рецептора PAC-1 в лейкоцитах предпочки у радужной форели (Oncorhynchus mykiss), обработанных поли(I:C) (30 мкг/мл) или инфицированных IPNV (множественность заражения, m.o.i. 0,1), через 4, 24 и 48 часов после начала эксперимента. Культуру лейкоцитов обрабатывали в двух повторениях, и анализировали уровни экспрессии кПЦР в трех повторениях. Данные представлены в виде среднего значения относительной экспрессии PAC-1 относительно эндогенного фактора элонгации EF1α ± стандартное отклонение (SD). *(p<0,05).
Фиг.2. Анализ экспрессии ПЦР в реальном времени рецептора PAC-1 в клеточной линии макрофагов O. mykiss RTS-11, инфицированных in vitro VHSV (m.o.i 0,1), через 1, 4 и 8 ч после начала эксперимента. Эксперимент проводили в двух повторениях, и уровни экспрессии анализировали кПЦР в трех повторениях. Данные представлены в виде среднего значения относительной экспрессии PAC-1 относительно эндогенного фактора элонгации EF1α ± стандартное отклонение (SD). *(p<0,05).
Фиг.3. Анализ экспрессии ПЦР в реальном времени рецептора VPAC-1 в лейкоцитах предпочки у радужной форели (O. mykiss), обработанных поли(I:C) (30 мкг/мл) или инфицированных IPNV (множественность заражения, m.o.i. 0,1), через 4, 24 и 48 часов после начала эксперимента. Культуру лейкоцитов обрабатывали в двух повторениях, и анализировали уровни экспрессии кПЦР в трех повторениях. Данные представлены в виде среднего значения относительной экспрессии VPAC-1 относительно эндогенного фактора элонгации EF1α ± стандартное отклонение (SD). *(p<0,05).
Фиг.4. Анализ экспрессии ПЦР в реальном времени рецептора PAC-1 в лейкоцитах предпочки (A) и селезенки (B) у радужной форели (O. mykiss), экспериментально инфицированных in vivo VHSV (100 мкл 1×107 TCID50 (титр вируса в супернатанте культуры/мл на рыбу)). В случайном порядке отбирали образцы из пяти совокупностей тотальной РНК из предпочки и селезенки 5 рыб через 3, 7 и 10 суток после вирусной инфекции. Уровни экспрессии анализировали кПЦР в трех повторениях. Данные представлены в виде среднего значения относительной экспрессии PAC-1 относительно эндогенного фактора элонгации EF1α ± стандартное отклонение (SD). *(p<0,05).
Фиг.5. Анализ экспрессии ПЦР в реальном времени рецептора VPAC-1 в лейкоцитах предпочки (A) и селезенки (B) у радужной форели (O. mykiss), экспериментально инфицированной in vivo VHSV (100 мкл 1×107 TCID50 (титр вируса в супернатанте культуры/мл на рыбу)). В случайном порядке отбирали образцы из пяти совокупностей тотальной РНК из предпочки и селезенки 5 рыб через 3, 7 и 10 суток после вирусной инфекции. Уровни экспрессии анализировали кПЦР в трех повторениях. Данные представлены в виде среднего значения относительной экспрессии VPAC-1 относительно эндогенного фактора элонгации EF1α ± стандартное отклонение (SD). *(p<0,05).
Фиг.6. Анализ экспрессии ПЦР в реальном времени PACAP в лейкоцитах селезенки у радужной форели (O. mykiss), экспериментально инфицированной in vivo VHSV (100 мкл 1×107 TCID50/мл на рыбу). В случайном порядке отбирали образцы из пяти совокупностей тотальной РНК из селезенки 5 рыб через 3, 7 и 10 суток после вирусной инфекции. Уровни экспрессии анализировали кПЦР в трех повторениях. Данные представлены в виде среднего значения относительной экспрессии PACAP относительно эндогенного фактора элонгации EF1α ± стандартное отклонение (SD). *(p<0,05).
Фиг.7. Анализ экспрессии ПЦР в реальном времени эффекта in vitro PACAP38 на транскрипцию кодирующего белок Mx гена в лейкоцитах периферической крови (A) и предпочки (B) здоровой радужной форели. Эффекты введения PACAP в концентрации 10-10, 10-9 и 10-8 M оценивали через 48 часов после обработки. Эксперимент повторяли 4 раза. Культуру лейкоцитов обрабатывали в двух повторениях, и кПЦР проводили в трех повторениях. Данные представлены в виде среднего значения относительной экспрессии Mx относительно эндогенного фактора элонгации EF1α ± стандартное отклонение (SD). *(p<0,05).
Фиг.8. Анализ экспрессии ПЦР в реальном времени эффекта in vitro PACAP38 на транскрипцию кодирующего IFN-γ гена в лейкоцитах периферической крови (A) и предпочки (B) здоровой радужной форели. Эффекты введения PACAP в концентрации 10-10, 10-9 и 10-8 M оценивали через 48 часов после обработки. Эксперимент повторяли 4 раза. Культуру лейкоцитов обрабатывали в двух повторениях, и кПЦР проводили в трех повторениях. Данные представлены в виде среднего значения относительной экспрессии IFN-γ относительно эндогенного фактора элонгации EF1α ± стандартное отклонение (SD). *(p<0,05).
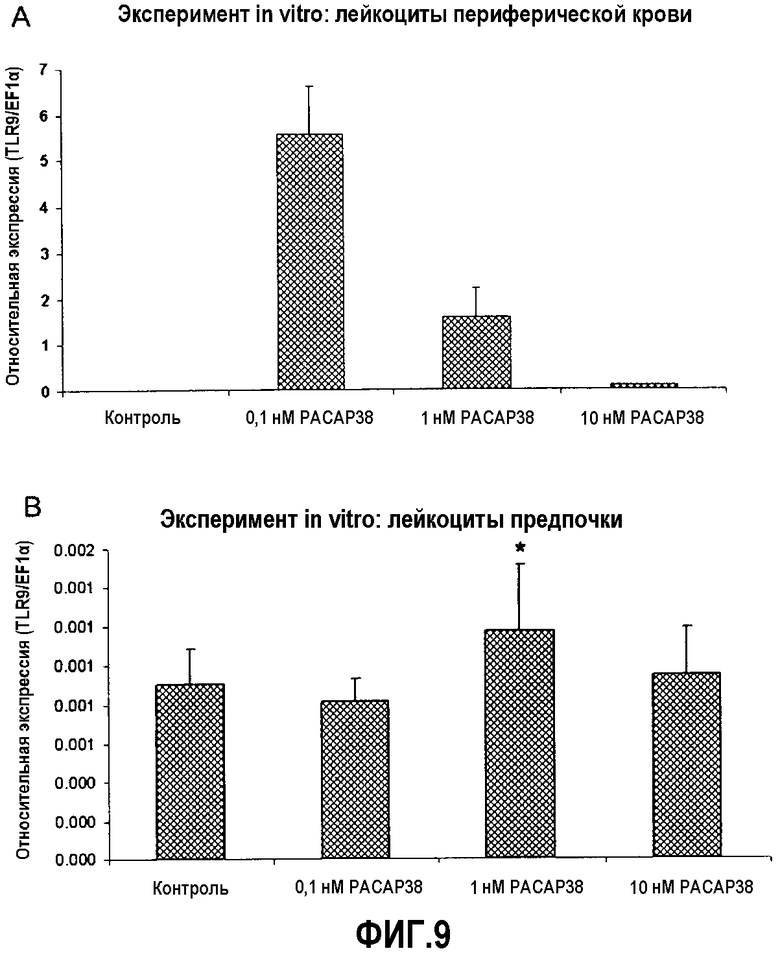
Фиг.9. Анализ экспрессии ПЦР в реальном времени эффекта in vitro PACAP38 на транскрипцию кодирующего TLR9 гена в лейкоцитах периферической крови (A) и предпочки (B) здоровой радужной форели. Эффекты введения PACAP в концентрации 10-10, 10-9 и 10-8 M оценивали через 48 часов после обработки. Эксперимент повторяли 4 раза. Культуру лейкоцитов обрабатывали в двух повторениях, и кПЦР проводили в трех повторениях. Данные представлены в виде среднего значения относительной экспрессии TLR9 относительно эндогенного фактора элонгации EF1α ± стандартное отклонение (SD). *(p<0,05).
Фиг.10. Анализы in vitro для определения противовирусного действия комбинаций PACAP-рибавирин (Rib-PACAP). За 24 часа до вирусной инфекции клетки обрабатывали "противовирусным средством" или комбинациями PACAP-противовирусные средства. Положительный контроль (c+): инфицированные вирусом клетки без противовирусной обработки. Отрицательный контроль (c-): неинфицированные необрабатываемые клетки. Клетки инфицировали вирусом в течение 30 минут для обеспечения адсорбции. Затем их отмывали PBS и добавляли различные виды средств лечения. Ингибирование цитопатического действия (CPE) оценивали с применением окрашивания кристаллическим фиолетовым (оптическая плотность при 550 нм).
Примеры
Пример 1. Экспрессия рецептора PAC-1 в лейкоцитах из предпочки клеток радужной форели (O. mykiss), обработанных поли(I:C) и IPNV, и в клеточной линии макрофагов радужной форели (O. mykiss) RTS-11, инфицированных in vitro VHSV
Авторы использовали молодь радужной форели (O. mykiss) от 9 до 12 грамм и в возрасте 7 месяцев, не инфицированную VHSV и IPNV. Рыб содержали при 14°C при циркуляции воды. Корм давали дважды в сутки неограниченно. Вирус VHSV (штамм 0771) и IPNV (штамм Sp) выращивали на клеточной линии половых желез радужной форели RTG-2 (Sena and Rio (1975) Infect. Immun. 11:815-22). Клетки выращивали на минимальной питательной среде (MEM, Invitrogen, USA) с добавлением 10% эмбриональной телячьей сыворотки (FCS, Invitrogen), содержащей 100 мкг/мл пенициллина и 100 мкг/мл стрептомицина. Вирусы инокулировали в клетки RTG-2, растущие на MEM с антибиотиками и 2% FCS при 14°C. Когда наблюдали выраженное цитопатическое действие, собирали супернатанты культур и центрифугировали для удаления продуктов распада клеток. Для экспериментов авторы использовали осветленные супернатанты культур. Титры вирусов определяли в 96-луночных планшетах, как описано Reed and Muench (Reed and Muench (1998) J. Hyg. 27:280-9).
Лейкоциты предпочки выделяли у 4 форелей следующим ниже способом, описанным Graham and Secombes (Graham and Secombe (1998) Immunology 65:293-7). В кратком изложении, в стерильных условиях удаляли переднюю почку и пропускали через нейлоновое сито с размером ячеек 100 мкм с использованием среды Лейбовитца (L-15, Gibco, UK) с добавлением пенициллина 100 мкг/мл, стрептомицина (100 мг/мл), гепарина (10 единиц/мл) и 2% FCS. Получаемую клеточную суспензию аккуратно помещали в градиент перколла до 51%. Кольцо клеток, соответствующих лейкоцитам, аккуратно удаляли, дважды промывали в L-15, содержащей 0,1% FCS. Клетки ресуспендировали в L-15 с 5% FCS в концентрации 5×106 клеток на мл и разливали в 24-луночные планшеты по 1 мл на лунку. Инфицированные лейкоциты экспонировали 30 мкг/мл поли(I:C) (Sigma) или инфицировали IPNV при MOI 0,1 и инкубировали при 14°C в течение 4 часов, 24 часов и 48 часов.
В заключении тотальную РНК выделяли из культур лейкоцитов способом, описанным Chomczynski and Sacchi (Chomczynski and Sacchi (1987) Anal. Biochem. 162:156-9), для оценки уровней экспрессии рецептора PAC-1 на лейкоцитах, не обработанных и обработанных поли(I:C) или инфицированных вирусами. Образцы обрабатывали RQ1 RNase-free DNase (Promega) для удаления содержащейся в образцах геномной ДНК. Для синтеза комплементарной ДНК (кДНК) использовали коммерческий реагент SuperScript III (Invitrogen) на основе обратной транскриптазы. Для реакций количественной ПЦР (кПЦР) использовали смесь ПЦР из коммерческих источников: Power SYBR Green PCR Master Mix (Applied Biosystems). Результаты кПЦР нормализовали на конститутивную экспрессию эндогенного гена, специфического фактора элонгации 1α (EF1α), и проводили в трех повторениях. Результаты выражали в виде 2-ΔCt, где ΔCt равно разности значения Ct гена минус вычисленное значение Ct гена нормализации (EF1α).
Результат представлял собой такой, что уровни PAC-1 являлись сверхэкспрессированными в культивируемых лейкоцитах, обрабатываемых поли(I:C) через 4, 24 и 48 часов эксперимента, свидетельствуя о том, что рецептор PAC-1 вовлечен в ответ на вирус у рыб, учитывая что поли(I:C) представляет собой молекулу, которая структурно является аналогичной двухцепочечной РНК, сходный с вирусной инфекцией эффект (многие вирусы обладают РНК-геномами). Эти результаты представлены на фиг.1. Поли(I:C) взаимодействует с Toll-подобным рецептором 3 (TLR3), который экспрессируется во внутриклеточных компартментах B-клеток и дендритных клеток. В природе вирусы стимулируют TLR-3.
Кроме того, уровни экспрессии PAC-1 становились детектируемыми значениями для лейкоцитов в необрабатываемых культурах до недетектируемых уровней в культурах лейкоцитов, инфицированных IPNV, через 4, 24 и 48 часов после инфекции, подтверждая участие этого рецептора, который специфически связывается с PACAP, в противовирусном ответе у рыб (фиг.1). Различия, наблюдаемые между эффектами вирусного миметика поли(I:C) и вируса IPNV, могут быть ассоциированы со специфическим действием вируса в инфицированных клетках, вероятно, с его преимуществом.
Кроме того, авторы оценивали уровни экспрессии PAC-1 в клеточной линии макрофагов форели (O. mykiss) RTS-11, инфицированных VHSV, способ инфекции вирусом линии RTS-11 являлся аналогичным тому, который описан выше для линии RTG-2. Аналогично, авторы наблюдали снижение уровней экспрессии PAC-1 через 4 и 8 суток после инфицекции VHSV (фиг.2).
Пример 2. Экспрессия рецептора VPAC-1 в лейкоцитах из передней почки клеток радужной форели (Oncorhynchus mykiss), обработанных поли(I:C) и VHSV
Для оценки уровней экспрессии рецептора VPAC-1 составляли план эксперимента, аналогичный тому, который описан в примере 1.
Результат представлял собой такой, что уровни VPAC-1 являются сверхэкспрессированными в культивируемых лейкоцитах, обрабатываемых поли(I:C), через 4, 24 и 48 часов эксперимента, свидетельствуя о том, что рецептор VPAC-1, как и PAC-1, вовлечен в ответ на вирус у рыб, учитывая то, что поли(I:C) считают молекулой-вирусным миметиком (фиг.3).
Кроме того, уровни экспрессии VPAC-1 являлись недетектируемыми в культурах лейкоцитов, инфицированных VHSV, через 4, 24 и 48 часов после инфекции, подтверждая участие этого рецептора, который связывается с PACAP и VIP с одинаковой аффинностью, в противовирусном ответе у рыб (фиг.3).
Как наблюдали для рецептора PAC-1 в культивируемых лейкоцитах передней почки, инфицированных IPNV, наблюдаемые различия в регуляции VPAC-1 при обработке лейкоцитов in vitro поли(I:C) и инфицированных VHSV, могут быть ассоциированы со специфическим действием вируса как биологического организма, оказываемым в инфицированных клетки, вероятно, с его преимуществом.
Пример 3. Экспрессия PACAP и рецепторов PAC-1 и VPAC-1 в лейкоцитах из селезенки и передней почки радужной форели (Oncorhynchus mykiss), инфицированных in vivo VHSV
VHSV (штамм 0771) выращивали на клеточной линии RTG-2 (Sena and Rio (1975) Infect. Immun. 11:815-22). В кратком изложении, вирусы инокулировали на клеточной линии RTG-2, растущей на MEM с антибиотиками (100 МЕ/мл пенициллина и 100 мкг/мл стрептомицина) и 2% FCS при 14°C. Когда наблюдали выраженное цитопатическое действие, собирали супернатанты культуры и центрифугировали для удаления продуктов распада клеток. Для инфицирования форели использовали осветленные супернатанты культур. Титры вирусов определяли в 96-луночных планшетах, как описано Reed and Muench (Reed and Muench (1998) J. Hyg. 27:280-9).
Авторы использовали молодь радужной форели (O. mykiss) от 9 до 12 грамм и в возрасте 7 месяцев и не инфицированную VHSV и IPNV. Рыб содержали при 14°C при циркуляции воды. Корм давали дважды в сутки неограниченно. Формировали две экспериментальные группы по 20 форелей в каждой группе, одну группу инъецировали раствором вируса (100 л 1×107 TCID50/мл на рыбу) и другую группу (используемую в качестве отрицательного контроля) инъецировали средой для культивирования RTG-2, не инфицированной VHSV.
На 1, 3, 7 и 10 сутки после инъекции в случайном порядке выбирали 5 форелей и умерщвляли посредством передозировки анестетиком MS-22. Затем удаляли почки и селезенку для проведения выделения тотальной РНК из этих органов способом, описанным Chomczynski and Sacchi (Chomczynski and Sacchi (1987) Anal. Biochem. 162:156-9). Синтез кДНК и реакции количественной ПЦР проводили, как описано в примере 1.
Для реакций обратной транскрипции (ОТ) объединяли пять образцов тотальной РНК пяти индивидуумов из каждой экспериментальной группы, выбранных в случайном порядке на 1, 3, 7 и 10 сутки эксперимента.
Результат представлял собой такой, что в селезенке рецепторы PAC-1 и VPAC-1 являются сверхэкспрессированными на 3 сутки после инъекции по сравнению с отрицательным контролем. Уровни экспрессии являются ниже, чем в контрольной группе на 10 сутки после инъекции. Уровни экспрессии рецепторов PAC-1 и VPAC-1 во внешней почке ниже в контрольной группе на 1 и 3 сутки, где значения VPAC-1 на 10 сутки являются недетектируемыми. На 7 сутки у обоих рецепторов повышаются уровни их экспрессии по сравнению с группой отрицательного контроля. Также выявлено, что оба рецептора обладают сходным профилем экспрессии во времени после инфекции вирусом (фиг.4 и 5).
Значения экспрессии PACAP на 1 сутки были ниже по сравнению со значениями отрицательного контроля. На 7 сутки эти значения экспрессии являются наиболее высокими. Эти результаты коррелируют с результатами для двух его рецепторов VPAC-1 и PAC-1 в том смысле, что для уровней экспрессии рецептора выявлена тенденция быть ниже (1 сутки) и выше (7 сутки) по сравнению с группой отрицательного контроля. На 10 сутки значения экспрессии PACAP ниже по сравнению с группой отрицательного контроля (фиг.4, 5 и 6).
Изменение уровней экспрессии PACAP и его рецепторов PAC-1 и VPAC-1 в селезенке и передней почки рыб, экспериментально инфицированных VHSV и IPNV, свидетельствуют об участии обоих рецепторов в противовирусном ответе in vivo у рыб. Это подтверждалось в экспериментах с нагрузкой, в которых авторы наблюдали положительное действие PACAP в противовирусном ответе у лососевых, увеличивавшее выживаемость инфицированной рыбы, усиливавшее иммунный ответ против вирусной инфекции и удалявшее вирус из органов и жидкостей, способных осуществлять репликацию вируса.
Пример 4. Эффект PACAP на транскрипцию белков Mx, IFN и TLR9 в лейкоцитах периферической крови и передней почки здоровой радужной форели (Oncorhynchus mykiss)
Авторы использовали молодь радужной форели (O. mykiss) приблизительно 50 граммов, не инфицированных VHSV и IPNV. Рыб (n=5) анестезировали солью метансульфоновой кислоты (Sigma, USA) и в стерильных условиях удаляли сначала периферическую кровь из хвостовой вены, а затем переднюю почку.
Выделяли лейкоциты из периферической крови, из передней почка и независимо из 5 форелей способом, описанным Graham and Secombe (Graham and Secombe (1998) Immunology 65:293-7).
Периферическую кровь каждой рыбы разбавляли 4 раза в половине среды Лейбовитца (L-15, Gibco, UK) с добавлением пенициллина 100 МЕ/мл, стрептомицина (100 мкг/мл), гепарина (10 единиц/мл) и 2% FCS, и аккуратно помещали в градиент перколля до 51%. Кольцо клеток, соответствующих лейкоцитам, аккуратно удаляли, дважды промывали в L-15, содержащей 0,1% FCS.
Переднюю почку пропускали через нейлоновое сито 100 микрометров в среде Лейбовитца (L-15, Gibco, UK) с добавлением пенициллина 100 МЕ/мл, стрептомицина (100 мг/мл), гепарина (10 единиц/мл) и 2% FCS. Получаемую клеточную суспензию разбавляли 1:4 в той же среде с добавками L-15 и аккуратно помещали в градиент перколля до 51%. Кольцо клеток, соответствующих лейкоцитам, аккуратно удаляли, дважды промывали в L-15, содержащей 0,1% FCS.
Клетки суспендировали в L-15 с 5% FCS в концентрации 5×106 клеток на мл и разливали в 24-луночные планшеты по 1 мл на лунку. Лейкоциты обрабатывали 3 дозами PACAP38 Clarias gariepinus, получаемого химическим синтезом, (10-10 M, 10-9 M и 10-8 M) в двух повторениях и в качестве отрицательного контроля использовали необработанные лейкоциты, разлитые в двух повторениях.
Уровни Mx, IFN и TLR9 оценивали через 48 часов после обработки. Для этого выделяли тотальную РНК из культур лейкоцитов, обработанных PACAP способом, описанным Chomczynski and Sacchi (Chomczynski and Sacchi (1987) Anal. Biochem. 162:156-9).
Праймеры, сконструированные для амплификации Mx, IFN-γ и TLR9, отжигаются на кДНК и геномной ДНК, обрабатывали тотальные РНК, выделяемые из различных тканей ДНК-нуклеазой, конкретно RQ1 RNase-free DNase (Promega) для удаления содержащейся в образцах геномной ДНК.
Для синтеза кДНК использовали коммерческий набор реагентов на основе обратной транскриптазы SuperScript III (Invitrogen). В дальнейшем для реакций количественной ПЦР (кПЦР) использовали смесь для ПЦР из коммерческих источников: Power SYBR Green PCR Master Mix (Applied Biosystems). Результаты кПЦР нормализовали на конститутивную экспрессию эндогенного гена, специфического фактора элонгации 1α (EF1α), и проводили в трех повторениях. Результаты выражали в виде 2-ΔCt, где ΔCt равно разности значения Ct гена минус вычисленное значение Ct гена нормализации (EF1α).
Уровни белка Mx увеличиваются через 48 часов после обработки в культурах лейкоцитов периферической крови, обработанных 10-10 M PACAP38. При дозе 10-9 M также существует стимулирующее действие PACAP38 на транскрипцию белков Mx относительно отрицательного контроля, но детектируемые уровни экспрессии являлись ниже уровней, получаемых при дозе 10-10 M. При дозе 10-8 M не выявлено различий в уровнях экспрессии белка Mx относительно отрицательного контроля. Эти результаты свидетельствуют о положительном действие PACAP38 на транскрипцию белков Mx при низких концентрациях в диапазоне (10-9-10-10 M) (фиг.7). В лейкоцитах передней почки действие PACAP38 на белок Mx является более умеренным, чем в лейкоцитах периферической крови, проявляя стимулирующее действие при дозе 10-9 M (фиг.7B).
Кроме того, авторы выявили стимулирующее действие PACAP38 на экспрессию TLR9, от недетекитуемых уровней TLR9 в культивируемых лейкоцитах периферической крови, активированных PACAP, до детектируемых уровней в культурах, активированных PACAP38 в диапазоне (10-10-10-8 M). Наиболее высокие значения получали при дозе 10-10 M (фиг.8A). В лейкоцитах передней почки, как ранее наблюдалось с экспрессией белка Mx, действие было более умеренным. При промежуточной дозе 10-9 M уровни экспрессии TLR9 являлись значительно выше, чем в отрицательном контроле (фиг.8B).
Уровни IFN-γ являлись недетектируемыми в необрабатываемых культурах лейкоцитов периферической крови. В культурах, обработанных 3 дозами PACAP38, выявляли детектируемые уровни экспрессии с наиболее высоким уровнем экспрессии при промежуточной дозе 10-9 M (фиг.9A). Кроме того, в культивируемых лейкоцитах передней почки авторы выявили, что PACAP38 стимулирует транскрипцию IFN-γ. Уровни экспрессии IFN-γ являлись значительно выше по сравнению с контрольной группой при дозах 10-9 и 10-8 M, получая наилучшие результаты при наиболее высокой дозе 10-9 M (фиг.9B).
Пример 5. Эффект in vitro введения PACAP в комбинации с рибавирином на инфекцию IPNV
Авторы использовали супернатант из клеточной культуры (штамм ATCC VR-299), инфицированной IPNV, в виде изолированного вируса. Подтверждение вирусной инфекции проводили специфичной ПЦР. Для анализов in vitro авторы использовали клеточную линию CHSE-214 (эмбрионы чавычи) (ECACC No 00/F/031). Ее поддерживали при 18°C в среде MEM с добавлением солей Игла, 10% эмбриональной телячьей сыворотки (FBS), 2 мМ глутамина и антибиотиков.
Вирусный инокулят выращивали при 15°C и 2% FBS, и до анализов определяли титр вируса в супернатанте культуры (TCID 50) способом Reed and Muench (Reed and Muench (1938) The American Journal of Hygiene 27:493497). Из вирусного инокулята получали разбавление 0,1 m.o.i. Планшеты на 96 лунок засевали CHSE-214, поддерживаемой при 18°C на MEM (соли Игла) с добавлением 10% FBS, 2 мМ глутамина и антибиотиков. Авторы оценивали различные концентрации рибавирина и 3 различные концентрации PACAP (0,1, 1 и 10 нМ). За 24 часа до инфекции клетки обрабатывали противовирусным средством или комбинациями PACAP-противовирусное средство, устанавливая положительные контроли (клетки, инфицированные вирусом без противовирусной обработки) и отрицательные контроли (неинфицированные и необрабатываемые клетки, и неинфицированные клетки, обрабатываемые противовирусным средством или различными дозами PACAP). Клетки инфицировали вирусным инокулятом в течение 30 минут для адсорбции. Затем клетки отмывали PBS. Лекарственные средства разбавляли в MEM с добавлением 2% FBS и антибиотиков и снова добавляли. Тест завершали, когда автора наблюдали цитопатическое действие (CPE) в положительном контроле. Оценку проводили микроскопией и окрашиванием кристаллическим фиолетовым (оптическая плотность определения 550 нм). CPE в положительном контроле наблюдали через 3 суток после инфекции. Результаты ингибирования CPE в отношении необрабатываемых и инфицированных контрольных клеток, получаемые из значений оптической плотности при окрашивании кристаллическим фиолетовым, представлены на фиг.10. Анализ противовирусного действия рибавирина в комбинации с PACAP проводили с использованием программы Calcusyn для Windows (Biosoft). Значение получаемого комбинационного индекса Чоу свидетельствует о синергизме двух лекарственных средств при тестируемых значениях концентраций.
Пример 6. Эффект введения PACAP и комбинации PACAP плюс рибавирин у радужной форели (O. mykiss), экспериментально инфицированной IPNV
Эксперимент проводили для оценки эффекта введения PACAP и комбинации PACAP-рибавирина у радужной форели, экспериментально инфицированной IPNV. Авторы формировали 8 экспериментальных групп по 50 рыб с массой тела 1,6±0,4 г каждой рыбы. Температуру воды поддерживали при 10-12°C.
Группа 1: не получающие обработку рыбы, которых не подвергают действию вируса.
Группа 2: не получающие обработку рыбы, которых подвергают действию вируса.
Группа 3: группа, получающая обработку рибавирином в дозе 400 мкг/л воды, которую подвергают действию вируса.
Группа 4: группа, получающая обработку рибавирином в дозе 800 мкг/л воды, которую подвергают действию вируса.
Группа 5: группа, получающая обработку PACAP в дозе 100 мкг/л воды, которую подвергают действию вируса.
Группа 6: группа, получающая обработку PACAP в дозе 200 мкг/л воды, которую подвергают действию вируса.
Группа 7: группа, получающая обработку комбинацией 1 (рибавирин 400 мкг/л - PACAP 100 мкг/л, которую подвергают действию вируса.
Группа 8: группа, получающая обработку комбинацией 2 (рибавирин 800 мкг/л - PACAP 200 мкг/л, которую подвергают действию вируса.
Животных кормили дважды в сутки в количестве, эквивалентном 3% общей массы тела в каждом резервуаре. Рыб подвергали действию вируса, помещая их в воду при 10-12°C, содержащую приблизительно 105 бляшкообразующих единиц (БОЕ)/мл IPNV (штамм ATCC VR-299), в течение 2 часов. Рыб в группах 1 и 2 подвергали аналогичной стрессовой обработке без противовирусного соединения или без комбинации PACAP-противовирусное соединение. Рыбы группы 1 получали аналогичные процедуры со средой для культивирования клеток вместо вируса. Определение вируса проводили ОТ-ПЦР в почке и селезенке способом, описанным Lopez-Lastra et al. (1994) Journal of Fish Diseases 17:269-282. Обработки PACAP или комбинацией PACAP-противовирусное средство проводили 3 раза в неделю в течение 20 суток. Первые обработки проводили через 2 часа после инфекции вирусом. Экспериментальные наблюдения проводили в течение первых 20 суток обработок и через 25 суток после их завершения. Во время эксперимента (45 суток) не наблюдали смертности и аномального поведения рыб.
У инфицированных IPNV рыб, которых не подвергали обработке, выявляли характерные признаки инфекционного панкреатического некроза через 6 суток после инфекции. Первая гибель наступала на 7 сутки после инфекции, сопровождающаяся усугублением признаков заболевания у всех рыб и высокой смертностью на 11, 12 и 13 сутки после инфекции. У рыб, инфицированных и получавших обработку рибавирином или PACAP, признаки заболевания детектировали на 8 сутки. В группе, которую обрабатывали комбинацией рибавирин-PACAP и подвергали действию вируса, не выявляли признаков заболевания в течение всего периода эксперимента.
К рыбам, которых не обрабатывали и инфицировали, возвращался аппетит на 15 сутки после инфекции. К рыбам, которых обрабатывали противовирусным средством, возвращался аппетит на 13 сутки, тогда как рыбы, которых обрабатывали PACAP и комбинациями PACAP-рибавирин, проявляли его на 9 сутки эксперимента. Рыбы неифицированного контроля демонстрировали нормальное поведение, и в этой группе не отмечали смертности в течение всего периода эксперимента. Кумулятивная смертность у не получавших обработку рыб и инфицированных IPNV рыб составляла 40 рыб из 50 (20% выживаемости). У рыб, получавших обработку рибавирином и инфицированных, выживаемость составила 68 и 70% для групп 3 и 4, соответственно. У рыб, получавших обработку PACAP и инфицированных, выживаемость составила 50 и 55% для групп 5 и 6, соответственно. В группах, которые обрабатывали комбинацией PACAP-рибавирин, выживаемость составляла 97 и 99% в группах 7 и 8, соответственно. В образцах ткани мертвых рыб выявляли наличие IPNV. Вирус не детектировали в образцах, получаемых у групп, которых не обрабатывали и не инфицировали.
В таблице 1 показаны средние массы тела на 45 сутки после инфекции. У инфицированных и не получавших обработку рыб увеличение массы составляло меньше по сравнению с неинфицированными рыбами. Эта потеря массы была компенсирована в группах, которые обрабатывали, и еще больше в группах, которые обрабатывали комбинацией PACAP-рибавирин.
Проводили ANOVA с последующей проверкой критерием Тьюки. Различные буквы соответствуют статистически значимым отличиям.
Пример 7. Эффект введения PACAP и составленной в сополимере молочной и гликолевой кислот комбинации PACAP плюс рибавирин радужной форели (O. mykiss), экспериментально инфицированной IPNV
Эксперимент проводили для оценки эффекта введения PACAP и композиции PACAP-рибавирин, содержащейся в сополимере молочной и гликолевой кислот (PLGA), радужной форели, экспериментально инфицированной IPNV. Формировали восемь экспериментальных групп по 30 рыб с массой 30±4 г каждая рыба, и содержали в воде при 10-12°C.
Группа 1: получавшие инъекцию PLGA рыбы, которых не подвергали действию вируса.
Группа 2: получавшие инъекцию PLGA рыбы, которых подвергали действию вируса.
Группа 3: группа, получавшая инъекции рибавирином в дозе 4 мкг/г рыбы, которую подвергали действию вируса.
Группа 4: группа, получавшая инъекции рибавирином в дозе 8 мкг/г рыбы, которую подвергали действию вируса.
Группа 5: группа, получавшая инъекции PACAP в дозе 0,1 мкг/г рыбы, которую подвергали действию вируса.
Группа 6: группа, получавшая инъекции PACAP в дозе 0,2 мкг/г рыбы, которую подвергали действию вируса.
Группа 7: группа, получавшая инъекции комбинацией 1 (рибавирин 4 мкг/г - PACAP 0,1 мкг/г), которую подвергали действию вируса.
Группа 8: группа, получавшая инъекции комбинацией 2 (рибавирин 8 мкг/г - PACAP 0,2 мкг/г), которую подвергали действию вируса.
Наночастицы, содержащие PACAP или комбинацию PACAP-рибавирин, вводили посредством интраперитонеальной инъекции через 2 часа после инфекции вирусом. Экспериментальные наблюдения проводили в течение 30 суток. Получали результаты коэффициентов выживаемости, аналогичные тем, что описаны в примере 6.
Пример 8. Эффект введения PACAP и комбинации PACAP плюс рибавирин у атлантического лосося (Salmo salat), экспериментально инфицированного IPNV
Эксперимент проводили для оценки введение PACAP и комбинации PACAP-рибавирин у лосося (Salmo salar), экспериментально инфицированного IPNV. Формировали восемь экспериментальных групп по 50 рыб и массой 1,2±0,3 г каждая рыба, и содержали в воде при 10-12°C.
Группа 1: не получавшие обработку рыбы, которых не подвергали действию вируса.
Группа 2: не получавшие обработку рыбы, которых подвергали действию вируса.
Группа 3: группа, получавшая обработку рибавирином в дозе 400 мкг/л воды, которую подвергали действию вируса.
Группа 4: группа, получавшая обработку рибавирином в дозе 800 мкг/л воды, которую подвергали действию вируса.
Группа 5: группа, получавшая обработку PACAP в дозе 100 мкг/л воды, которую подвергали действию вируса.
Группа 6: группа, получавшая обработку PACAP в дозе 200 мкг/л воды, которую подвергали действию вируса.
Группа 7: группа, получавшая обработку комбинацией рибавирина 400 мкг/л - PACAP 100 мкг/л, которую подвергали действию вируса.
Группа 8: группа, получавшая обработку комбинацией рибавирина 800 мкг/л - PACAP 200 мкг/л, которую подвергали действию вируса.
Животные кормили дважды в сутки в количестве, эквивалентном 3% общей массы тела в каждом резервуаре. Рыб подвергали действию вируса, помещая их в воду при 10-12°C, содержащую приблизительно 105 БОЕ/мл IPNV (штамм ATCC VR-299), в течение 2 часов. Обработки проводили 3 раза в неделю в течение 20 суток. Экспериментальные наблюдения проводили в течение этого периода и через 25 суток после последних обработок. В течение 45 суток эксперимента не наблюдали гибели и аномального поведения рыб. Рыб в группах 1 и 2 подвергали аналогичному стрессу, вызываемому при обработке противовирусным соединением или комбинацией PACAP-противовирусное соединение. Рыбы в группе 1 получали аналогичные процедуры со средой для культивирования клеток вместо вируса. Определение вируса проводили ОТ-ПЦР в почке и селезенке способом, описанным Lopez-Lastra et al. (1994) Journal of Fish Diseases 17:269-282.
У инфицированных IPNV и не получавших обработку рыб выявляли характерные признаки инфекционного панкреатического некроза через 6 суток после инфекции. Первая гибель наступала на 8 сутки после инфекции, сопровождающаяся усугублением признаков заболевания у всех рыб и высокой смертностью между 11 и 15 сутками после инфекции. Процент выживаемости в этой группе составлял 30%. Наблюдали потерю аппетита на 10 и 11 сутки у всех групп, инфицированных вирусом, за исключением групп, получавших обработку PACAP, комбинацией PACAP-рибавирин и неинфицированной группы. У рыб, инфицированных и получавших обработку обоими дозами рибавирина, ранние признаки заболевания детектировали на 10 сутки, и выживаемость составляла 70-76% для низкой и высокой доз, соответственно. У рыб, инфицированных и получавших обработку PACAP, выживаемость составляла 56-60% для низкой и высокой доз, соответственно. В группе, получавшей обработку комбинацией рибавирин-PACAP и подвергавшейся действию вируса, выживаемость составляла 96-98%. В неинфицированной и не получавшей обработку группе процент выживаемости составлял 98%. В образцах ткани мертвой рыбы выявляли наличие IPNV.
В таблице 2 представлены средние массы тела на 45 сутки после инфекции. Инфицированные и не получавшие обработку рыбы обладали более низким приростом массы тела по сравнению с неинфицированными рыбами. Эта потеря массы была компенсирована в группах, получавших обработку, и еще больше в группах, получавших обработку PACAP и комбинациями PACAP-рибавирин.
Проводили ANOVA с последующей проверкой критерием Тьюки. Различные буквы соответствуют статистически значимым отличиям.
Пример 9. Эффект введения PACAP и комбинации PACAP плюс рибавирин у атлантического лосося (Salmo salar), экспериментально инфицированного ISAV
Эксперимент проводили для оценки эффекта введения PACAP и комбинации PACAP-рибавирин для лосося (Salmo salar), экспериментально инфицированного ISAV. Формировали восемь экспериментальных групп по 25 рыб и массой 50±10 г каждая рыба. Группы содержали в морской воде при 10-12°C.
Группа 1: рыбы, не получавшие обработку, не подвергавшиеся действию вируса ISA.
Группа 2: не получавшие обработку рыбы, подвергавшиеся действию вируса ISA.
Группа 3: группа, получавшая обработку рибавирина в дозе 400 мкг/л воды, которую подвергали действию вируса.
Группа 4: группа, получавшая обработку рибавирина в дозе 800 мкг/л воды, которую подвергали действию вируса.
Группа 5: группа, получавшая обработку PACAP в дозе 100 мкг/л воды, которую подвергали действию вируса.
Группа 6: группа, получавшая обработку PACAP в дозе 200 мкг/л воды, которую подвергали действию вируса.
Группа 7: группа, получавшая обработку комбинацией рибавирина 400 мкг/л - PACAP 100 мкг/л, которую подвергали действию вируса.
Группа 8: группа, получавшая обработку комбинацией рибавирина 800 мкг/л - PACAP 200 мкг/л, которую подвергали действию вируса.
Для получения достаточного количества вируса для экспериментов с нагрузкой культивировали клетки SHK-1 и инфицировали их штаммом Glesvaer (номер доступа AJ012285, Krossoy et al. (1999) Journal of Virology 73:2136-2142) в 175 см2 флаконах в течение 5 суток.
Рыб подвергали действию вируса посредством совместного обитания с рыбами, инъецированными интраперитонеально 0,3 мл среды для культивирования, содержащей приблизительно 104 БОЕ/мл ISAV. Группа 1: рыбы, которые получали равный объем среды для культивирования. Процент смертности в группе 1 (не получавшей обработку, не подвергавшей действию вируса ISA) составлял 4% и в группе 2 (подвергавшей действию вируса и не получавшей обработку) составлял 92%. В группах 3 и 4 смертность составляла 52 и 36%, соответственно, тогда как в группах 5 и 6 составляла 60 и 72%, соответственно. В группах 7 и 8, получавших обработку комбинацией PACAP-рибавирин, процент смертности составлял 8 и 4%, соответственно. В образцах ткани мертвых рыб выявляли наличие ISAV. Вирус не детектировали в образцах от не получавшей обработку и неинфицированной группы.
Пример 10. Эффект введения PACAP и комбинации PACAP-амантадин у радужной форели (O. mykiss), экспериментально инфицированной IHNV
Эксперимент проводили для оценки эффекта введения PACAP и комбинации PACAP-амантадин у радужной форели, экспериментально инфицированной IHNV. Формировали восемь экспериментальных групп по 50 рыб массой 50±5 г каждая рыба и содержали в воде при 10-12°C.
Группа 1: не получавшие обработку рыбы, не подвергавшиеся действию вируса.
Группа 2: не получавшие обработку рыбы, подвергавшиеся действию вируса.
Группа 3: группа, получавшая обработку амантадином в дозе 400 мкг/л воды, которую подвергали действию вируса.
Группа 4: группа, получавшая обработку амантадином в дозе 800 мкг/л воды, которую подвергали действию вируса.
Группа 5: группа, получавшая обработку PACAP в дозе 100 мкг/л воды, которую подвергали действию вируса.
Группа 6: группа, получавшая обработку PACAP в дозе 200 мкг/л воды, которую подвергали действию вируса.
Группа 7: группа, получавшая обработку комбинацией 1 (амантадин 400 мкг/л - PACAP 100 мкг/л), которую подвергали действию вируса.
Группа 8: группа, получавшая обработку combination 2 (амантадин 800 мкг/л - PACAP 200 мкг/л), которую подвергали действию вируса.
Экспериментальные условия являлись аналогичными экспериментам, описанным в предшествующих примерах. Рыб заражали погружением в 20 л воды с аэрацией с 5,9×103 БОЕ/мл вируса в течение 1 часа. В результате эксперимента наблюдали выживаемость 26% у рыб, не получавших обработку и инфицированных IHNV. У рыб, получавших обработку амантадином и инфицированных IHNV, выживаемость составляла 46%. У рыб, получавших обработку PACAP и инфицированных IHNV, выживаемость составляла 36%. В группах, получавших обработку комбинацией PACAP-амантадин, выживаемость составляла 96-98%.
Пример 11. Эффект введения PACAP и комбинации PACAP плюс рибавирин у тихоокеанской белой креветки (Litopenaeus vannamei), экспериментально инфицированной вирусом синдрома белых пятен (WSSV)
Эксперимент проводили для оценки эффекта введения PACAP и комбинации PACAP-рибавирин у тихоокеанской белой креветки Litopenaeus vannamei, экспериментально инфицированной WSSV. Формировали четыре экспериментальные группы по 50 креветок массой 5±0,5 г каждая креветка и содержали в морской воде при 28°C.
Креветок кормили дважды в сутки в количестве, эквивалентном 8% общей биомассы на группу. Экспериментальные группы являлись следующими:
Группа 1: не получавшие обработку, не подвергавшиеся действию вируса WSSV;
Группа 2: не получавшие обработку, подвергавшиеся действию вируса WSSV;
Группа 3: получавшие обработку рибавирином, подвергавшиеся действию вируса WSSV;
Группа 4: получавшие обработку PACAP, подвергавшиеся действию вируса WSSV;
Группа 5: получавшие обработку комбинацией рибавирин-PACAP, подвергавшиеся действию вируса WSSV.
Для выделения и распространения вируса использовали краба Orconectes limosus. WSSV выделяли из только что выделенной гемолимфы центрифугированием в градиенте сахарозы, как описано Van Hulten et al in 2001 (Van Hulten et al. (2001) Virology 285:228-33).
Образцы вируса хранили при -80°C до использования.
Для сведения к минимуму естественных путей инфекции WSSV и получения воспроизводимого протокола использовали погружение для индицирования экспериментальной вирусной инфекции. До проведения вирусной инфекции определяли титр вируса и количество, необходимое для вызывания 75% смертности. Для этого креветок экспериментально инфицировали различными разбавлениями вируса во время инкубационного периода 7 часов.
После вирусной инфекции креветок отмывали морской водой, не содержащей вирус, и помещали в новые контейнеры в соответствии с планом экспериментальных групп, описанных выше.
Обработки вводили 3 раза в неделю в течение 30 суток в дозе (500 мкг противовирусного средства/л воды) или (500 мкг противовирусного средства плюс PACAP 200 мкг/л воды) после инфекции. Для группы, получавшей обработку PACAP, используемая доза составляла 200 мкг/л воды. Креветок в группах 1 и 2 подвергали стрессу, аналогичному при введении обрабатывающих веществ. В течение 30 суток эксперимента наблюдали за гибелью в каждой экспериментальной группе.
Процент смертности в группе 2 (не получавшей обработку, подвергавшейся действию вируса) составлял 60%, в группе 1 (не получавшей обработку, не подвергавшейся действию вируса) составлял 0%, в группе 3 (получавшей обработку рибавирином, подвергавшейся действию вируса) смертность составляла 16%, в то время как в группе, получавшей обработку PACAP, смертность составляла 26%. В группе, подвергавшейся обработке композицией PACAP-рибавирин, процент смертности составлял 2%. В образцах ткани мертвых креветок детектировали WSSV ОТ-ПЦР.
Пример 12. Эффект введения PACAP и комбинации PACAP плюс рибавирин у устриц вида Pecten maximus, экспериментально инфицированных IPNV
Эксперимент проводили для оценки эффекта введения PACAP и комбинации PACAP-рибавирин у устриц вида Pecten maximus, экспериментально инфицированных IPNV. Формировали восемь экспериментальных группы по 30 взрослых устриц в каждой группе, и содержали в 250 л фильтрованной морской воды при 10°C. Вирус не детектировали в образцах гепатопанкреаса, собранных до начала эксперимента. Экспериментальные группы являлись следующими:
Группа 1: не получавшая обработку, не подвергавшаяся действию вируса;
Группа 2: не получавшая обработку, подвергавшаяся действию вируса;
Группа 3: группа, получавшая обработку рибавирином в дозе 400 мкг/л воды, подвергавшаяся действию вируса;
Группа 4: группа, получавшая обработку рибавирином в дозе 800 мкг/л воды, подвергавшаяся действию вируса;
Группа 5: группа, получавшая обработку PACAP в дозе 100 мкг/л воды, подвергавшаяся действию вируса;
Группа 6: группа, получавшая обработку PACAP в дозе 200 мкг/л воды, подвергавшаяся действию вируса;
Группа 7: группа, получавшая обработку комбинацией 1 (рибавирин 400 мкг/л - PACAP 100 мкг/л), подвергавшаяся действию вируса;
Группа 8: группа, получавшая обработку комбинацией 2 (рибавирин 800 мкг/л - PACAP 200 мкг/л), подвергавшаяся действию вируса.
Обработки проводили 3 раза в неделю в течение 20 суток. Устриц заражали экспозицией в 25 л воды, содержащей 107 TCID50 мл-1 в резервуаре на 80 л. Через 6 часов воду заменяли при медленном потоке 1 л/мин и через 12 часов поток увеличивали до 3 л/мин.
Через две недели после заражения получали образцы гепатопанкреаса и определяли титр вируса. Результаты демонстрировали снижение вирусной нагрузки у животных, получавших обработку рибавирином и PACAP. Такое снижение было выше в группах, получавших обработку комбинацией (таблица 3).
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ РАСАР В КАЧЕСТВЕ МОЛЕКУЛЯРНОГО АДЪЮВАНТА ДЛЯ ВАКЦИН | 2012 |
|
RU2580294C2 |
| НЕЙРОПЕПТИДЫ ДЛЯ КУЛЬТУРЫ ВОДНЫХ ОРГАНИЗМОВ | 2006 |
|
RU2409027C2 |
| ПОСТОЯННАЯ ЛИНИЯ КЛЕТОК OMG ИЗ ГОНАД РАДУЖНОЙ ФОРЕЛИ (ONCORHYNCHUS MYKISS) | 2012 |
|
RU2495120C1 |
| ИНАКТИВИРОВАННАЯ ВАКЦИНА ПРОТИВ ОРТОРЕОВИРУСА РЫБ | 2020 |
|
RU2827386C1 |
| ВАКЦИНА ПРОТИВ ВНУТРИКЛЕТОЧНОГО ПАТОГЕНА, НЕ СОДЕРЖАЩАЯ СЫВОРОТКИ | 2019 |
|
RU2818370C2 |
| Средство, обладающее противовирусным действием в отношении герпесвируса человека I типа и энтеровируса В | 2022 |
|
RU2798659C1 |
| СПОСОБ ЛЕЧЕНИЯ ВИРУСНОГО ГЕПАТИТА С | 2012 |
|
RU2496512C1 |
| ПРОТИВОВИРУСНЫЕ КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ИНФЕКЦИЙ, СВЯЗАННЫХ С КОРОНАВИРУСАМИ | 2017 |
|
RU2753534C2 |
| Средство, обладающее противовирусным действием в отношении коронавируса SARS-CoV-2 | 2022 |
|
RU2788762C1 |
| МУТАНТНЫЕ ШТАММЫ MYCOPLASMA HYOPNEUMONIAE | 2013 |
|
RU2689671C2 |









Настоящее изобретение относится к применению активирующего аденилатциклазу гипофиза полипептида (PACAP) в лечении вирусных заболеваний и инфекционных заболеваний, вызываемых вирусами, у водных организмов. Показана эффективность PACAP отдельно или в комбинации с противовирусной молекулой, проявляющаяся в увеличении выживаемости рыб или ракообразных, инфицированных вирусами, где его вводили перорально, посредством инъекции или посредством погружения в ванны. Кроме того, наблюдали, что получавшие лечение организмы сохраняют или увеличивают свою массу по сравнению с инфицированными и не получавшими лечение организмами. PACAP или содержащие PACAP комбинации снижают вирусную нагрузку в тканях и органах, восприимчивых к вирусным инфекциям, как определено ОТ-ПЦР. 4 н. и 14 з.п. ф-лы, 3 табл., 10 ил., 12 пр.
1. Применение "активирующего аденилатциклазу гипофиза полипептида" (РАСАР) в качестве противовирусного соединения для лечения вирусных инфекций и инфекционных заболеваний, вызываемых вирусами, у водных организмов.
2. Применение по п. 1, где РАСАР получают: а) выделением из его природного источника, b) синтетически или с) технологией рекомбинантных ДНК.
3. Применение по п. 2, где РАСАР представляет собой полипептидную последовательность, выделяемую у рыб.
4. Применение по пп. 1-3, где РАСАР используют у водного организма, выбранного из группы, состоящей из лососевых, жгутиковых креветок и двустворчатых моллюсков.
5. Применение по п. 1, где РАСАР используют при терапевтическом лечении вирусных инфекций, вызываемых вирусами семейств Herpesviridae, Papovaviridae, Togaviridae, Retroviridae, Reoviridae, Birnaviridae и Picornaviridae.
6. Композиция для лечения вирусных заболеваний и инфекционных заболеваний, вызываемых вирусами, у водных организмов, содержащая "активирующий аденилатциклазу гипофиза полипептид" (РАСАР).
7. Композиция по п. 6, где РАСАР получают: а) выделением из его природного источника, b) синтетически или с) технологией рекомбинантных ДНК.
8. Композиция по п. 6, которую вводят перорально, посредством инъекции или посредством погружения в ванны.
9. Композиция по пп. 7 и 8, в которой РАСАР представляет собой полипептидную последовательность, выделяемую из рыб.
10. Ветеринарная комбинация для лечения вирусных заболеваний и инфекционных заболеваний, вызываемых вирусами, у водных организмов, содержащая "активирующий аденилатциклазу гипофиза полипептид" (РАСАР) и противовирусную молекулу, выбранную из группы, состоящей из рибавирина, аналога рибавирина, 5-этинил-1-β-D-рибофуранозилимидазолкарбоксамида (EICAR) и амантадина.
11. Комбинация по п. 10, где РАСАР получают: а) выделением из его природного источника, b) синтетически или с) технологией рекомбинантных ДНК.
12. Комбинация по п. 10, где РАСАР и противовирусную молекулу вводят одновременно, раздельно или последовательно при одном и том же лечение.
13. Комбинация по пп. 10-12, отличающаяся тем, что ее используют при лечении вирусных заболеваний и инфекционных заболеваний, вызываемых вирусами, у водных организмов.
14. Комбинация по п. 13, где РАСАР и противовирусную молекулу вводят перорально, посредством инъекции или посредством погружения в ванны.
15. Комбинация по п. 14, которую используют в качестве части рецептированного корма, где РАСАР содержится в концентрации 50-750 мкг/кг корма, и противовирусное соединение содержится в концентрации от 100 до 2000 мкг/кг корма.
16. Комбинация по п. 14, которую используют посредством инъекции, где РАСАР используют в концентрации 0,1-10 мкг на грамм массы тела (г массы тела) и противовирусную молекулу - в концентрации 1-50 мкг/г массы тела.
17. Комбинация по п. 14, которую используют посредством погружения в ванны, где РАСАР используют в концентрации 50-1000 мкг на литр воды и противовирусную молекулу используют в концентрации 100-2000 мкг/л воды.
18. Способ борьбы с вирусными инфекциями в аквакультуре, включающий введение РАСАР или ветеринарных комбинаций, содержащих РАСАР, культивируемым водным организмам.
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Приспособление для автоматической односторонней разгрузки железнодорожных платформ | 1921 |
|
SU48A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2015-11-10—Публикация
2011-11-30—Подача