ПРИОРИТЕТ
[0001] Данная заявка претендует на приоритет Временной Заявки США №61/238,903, поданной 1 сентября 2009 г., Временной Заявки США №61/308,524, поданной 26 февраля 2010 г., и Временной Заявки США №61/310,952, поданной 10 марта 2010 г. Данное описание базируется на полном содержании перечисленных заявок, которое включено в данную заявку путем ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Изобретение касается конъюгатов жирных кислот и ниацина;
композиций, которые содержат эффективное количество конъюгатов жирных кислот и ниацина; и способов лечения или профилактики метаболических заболеваний, которые включают введение эффективного количества конъюгата жирной кислоты и ниацина.
УРОВЕНЬ ТЕХНИКИ
[0003] Жир холодноводных рыб, таких как лосось, форель, сельдь и тунец, является источником пищевых омега-3 жирных кислот морского происхождения - эйкозапентаеновой кислоты (ЭПК) и докозагексаеновой кислоты (ДГК), которые представляют собой ключевые омега-3 жирные кислоты морского происхождения. Как ниацин, так и омега-3 жирные кислоты морского происхождения (ЭПК и ДГК) продемонстрировали способность уменьшать встречаемость сердечно-сосудистых заболеваний, заболеваний коронарных сосудов сердца, атеросклероза, а также уменьшать смертность среди больных дислипидемией, гиперхолестеринемией или диабетом 2 типа, а также метаболические заболевания. Показано, что ниацин в высокой дозе (1,5-4 г в сутки) снижает уровни липопротеинов очень низкой плотности ("ЛПОНП") путем снижения уровня Аполипопротеина В ("АроВ") и повышает уровни липопротеинов высокой плотности ("ЛПВП") путем повышения уровня Аполипопротеина A1 ("ApoA1") в печени. Ниацин также может ингибировать диацилглицеринацилтрансферазу-2, ключевой фермент для синтеза триглицеридов (ТГ) (Kamanna, V.S.; Kashyap, М.L. Am. J. Cardiol. 2008, 101 (8A), 20B-26B). К сожалению, ниацин вызывает многочисленные эффекты за пределами печени, которые снижают его терапевтическую пользу. Наиболее распространенным побочным эффектом ниацина являются приливы, которые могут ограничить переносимую дозу для больного. Считается, что приливы являются следствием наличия рецептора GPR109 в сосудах.
[0004] Показано, что омега-3 жирные кислоты улучшают чувствительность к действию инсулина и толерантность глюкозы у нормогликемических мужчин и лиц с ожирением. Также показано, что омега-3 жирные кислоты уменьшают инсулинорезистентность у больных ожирением и лиц с нормальной массой тела и воспалительным фенотипом. Показано, что метаболизм липидов, глюкозы и инсулина улучшается у гипертонических субъектов с избыточной массой тела в результате лечения омега-3 жирными кислотами. Также показано, что омега-3 жирные кислоты (ЭПК/ДГК) уменьшают уровни триглицеридов и снижают риск внезапной смерти, вызванной сердечными аритмиями, а также уменьшают смертность среди больных, у которых присутствует риск сердечно-сосудистых катастроф. Омега-3 жирные кислоты как часть диеты в виде биологически активных добавок дополняют лечение дислипидемии.
[0005] Способность ниацина и омега-3 жирной кислоты действовать синергично могла бы обеспечить значительную пользу в лечении вышеупомянутых заболеваний.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0006] Изобретение частично базируется на открытии конъюгатов ниацина и жирных кислот и их продемонстрированном влиянии для обеспечения более эффективного лечения, которое не может быть обеспечено введением ниацина или жирных кислот, отдельно или в комбинации. Указанные новые конъюгаты пригодны для лечения или профилактики атеросклероза, в том числе метаболических заболеваний, дислипидемии, заболевания коронарных сосудов сердца, гиперхолестеринемии, диабета 2 типа, повышенного уровня холестерина, метаболического синдрома и сердечно-сосудистого заболевания.
[0007] Соответственно, в одном из аспектов описан молекулярный конъюгат, который включает ниацин, ковалентно связанный с жирной кислотой, где жирная кислота выбрана из группы, состоящей из омега-3 жирных кислот и жирных кислот, которые метаболизируются in vivo с образованием омега-3 жирных кислот, где конъюгат включает как минимум один амид, и конъюгат способен гидролизоваться с образованием свободного ниацина и свободной жирной кислоты.
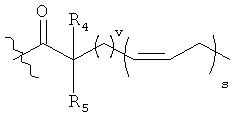
[0008] В другом аспекте описаны соединения Формулы I:
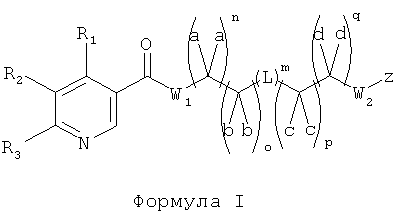
и их фармацевтически приемлемые соли, гидраты, сольваты, пролекарства, энантиомеры и стереоизомеры;
где
каждый из R1, R2 и R3 независимо выбран из группы, состоящей из: -Н, -D, -Сl, -F, -CN, -NH2, -NH(C1-C3 алкил), -N(С1-С3 алкил)2, -NH(C(O)C1-C3 алкил), -N(C(O)C1-С3 алкил)г, -С(O)Н, -С(O)С1-С3 алкила, -С(O)OC1-С3 алкила, -C(O)NH2, -С(O)NH(С1-С3 алкил), -C(O)N(C1-C3 алкил)2, -C1-С3 алкила, -O-C1-С3 алкила, -S(O)С1-С3 алкила и -S(O)2C1-C3 алкила;
каждый из W1 и W2 независимо представляет собой нуль, О, S, NH, NR, или W1 и W2 вместе могут образовывать имидазолидиновую или пиперазиновую группу, при условии, что W1 и W2 не могут одновременно представлять собой О;
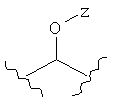
каждый из а, b, с и d независимо представляет собой -Н, -D, -СН3, -ОСН3, -ОСН2СН3, -C(O)OR, или -O-Z, или бензил, или два из а, b, с и d, вместе с одинарным атомом углерода, к которому они присоединены, могут образовывать циклоалкил или гетероцикл;
каждый из n, о, p и q независимо равен 0 или 1;
каждый L независимо представляет собой -O-, -S-, -S(O)-, -S(O)2-, -S-S-,
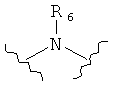 ,
, 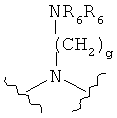 ,
, 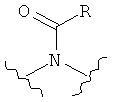 ,
, 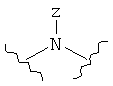 ,
, 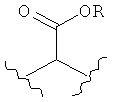 ,
,  ,
, 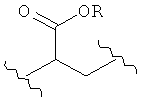 ,
,
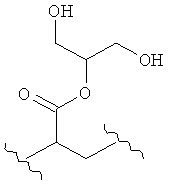 ,
, 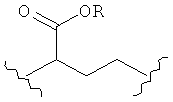 ,
, 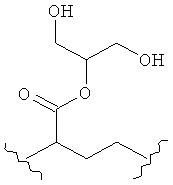 ,
, 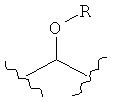 ,
, 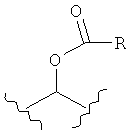 ,
,
 ,
, 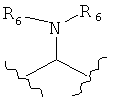 ,
, 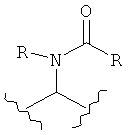 ,
, 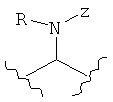 ,
, 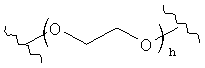 ,
, 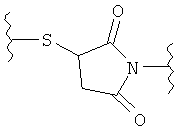 ,
,
или 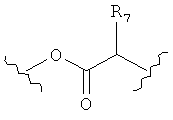 :
:
где представление L не ограниченно изображенным направлением слева направо, скорее, левая сторона или правая сторона L может быть присоединена к стороне W1 соединения Формулы I;
каждый g независимо равен 2, 3 или 4;
каждый h независимо равен 1, 2, 3 или 4;
m равно 0, 1, 2, или 3;
каждый R6 независимо представляет собой Н или C1-C6 алкил, или обе группы вместе с атомом азота, к которому они присоединены, могут образовывать гетероцикл;
каждый R7 независимо представляет собой е, Н, или неразветвленный или разветвленный C1-С10 алкил, который может быть необязательно замещен ОН, NH2, CO2R, CONH2, фенилом, C6H4OH, имидазолом или аргинином;
каждый е независимо представляет собой Н или любую из боковых цепей природных аминокислот;
каждый Z независимо представляет собой -Н, или
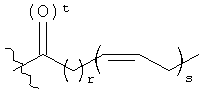 , или
, или
при условии, что в соединении присутствует по меньшей мере один
 , или
, или  ;
;
каждый r независимо равен 2, 3, или 7;
каждый s независимо равен 3, 5, или 6;
каждый t независимо равен 0 или 1;
каждый v независимо равен 1, 2, или 6;
каждый из R4 и R5 независимо представляет собой -Н, -D, -С, -С1-C4 алкил, -галоген, -ОН, -C(O)C1-C4 алкил, -O-арил, -O-бензил, -OC(O)C1-C4 алкил, -C1-С3 алкен, -C1-С3 алкин, -С(O)С1-С4 алкил, -NH2, -NH(С1-C3 алкил), -N(C1-C3 алкил)2, -NH(C(O)C1-C3 алкил), -N(C(O)C1-C3 алкил)2, -SH, -S(C1-C3 алкил), -S(O)С1-С3 алкил, -S(O)2C1-C3 алкил; но
каждый R независимо представляет собой -Н, -С(O)-С1-С3 алкил, или неразветвленный или разветвленный C1-C4 алкил, необязательно замещенный OR, NR2 или галогеном;
при условии, что
если каждый из m, n, о, p и q равен 0, каждый из W1 и W2 представляет собой нуль, и Z представляет собой
 .
.
то t должно равняться 0; и
если каждый из m, n, о, p и q равен 0, и каждый из W1 и W2 представляет собой нуль, то Z не должен представлять собой

[0009] В Формуле I, любой один или больше из Н может быть замещен дейтерием. Также следует понимать, что в Формуле I метиловый заместитель может быть заменен C1-С6 алкилом.
[0010] Также описаны фармацевтические композиции, содержащие как минимум одно ниациновое производное жирной кислоты.
[0011] Также описаны способы лечения заболевания, поддающегося лечению ниациновым производным жирной кислоты, у пациента, который нуждается в таком лечении, путем введения пациенту эффективного количества ниацинового производного жирной кислоты.
[0012] Также в данном описании описаны способы лечения метаболических заболеваний путем введения пациенту, который нуждается в таком лечении, эффективного количества ниацинового производного жирной кислоты.
[0013] Изобретение также включает фармацевтические композиции, содержащие эффективное количество ниацинового производного жирной кислоты и фармацевтически приемлемый носитель. Композиции пригодны для лечения или профилактики метаболического заболевания. Изобретение включает ниациновое производное жирной кислоты в форме фармацевтически приемлемых пролекарств, гидрата, соли, энантиомера, стереоизомера или их смеси.
[0014] Подробное описание изобретения приведено ниже. Хотя способы и материалы, подобные или эквивалентные описанным в данном описании, могут использоваться в практике или тестировании данного изобретения, в данном описании описаны иллюстративные способы и материалы. Другие признаки, объекты и преимущества изобретения будут очевидными из описания и формулы изобретения. В описании и приложенной формуле изобретения, форма единственного числа также включает множественное число, если контекст не указывает четко на противоположное. Если не указано иное, все технические и научные термины, использованные в данном описании, имеют такое же значение, которое им обычно придает средний специалист в области техники, к которой принадлежит данное изобретение. Все патенты и публикации, процитированные в данном описании, включены в данное описание путем ссылки в полном объеме.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На Фиг.1 изображено влияние соединения 1-7 на секрецию АроВ в клетках HepG2.
На Фиг.2 изображено влияние ниациновых производных жирных кислот на целевые гены SREBP-1c.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0015] Метаболические заболевания - это широкий спектр медицинских расстройств, которые препятствуют метаболизму в организме субъекта. Метаболизм - это способ, которым организм субъекта превращает еду в энергию. Метаболизм в организме субъекта с метаболическим заболеванием определенным образом нарушен. Ниациновые производные жирных кислот обладают способностью лечить или предупреждать метаболические заболевания.
[0016] Ниациновые производные жирных кислот разработаны таким образом, чтобы вводить вместе аналоги ниацина и омега-3 жирные кислоты в одном молекулярном конъюгате. Активность ниациновых производных жирных кислот значительно выше, чем суммарная активность индивидуальных компонентов молекулярных конъюгатов, указывая на то, что активность, индуцируемая ниациновыми производными жирных кислот, является синергичной.
ОПРЕДЕЛЕНИЯ
[0017] Следующие определения используются в связи с ниациновыми производными жирных кислот:
[0018] Термин "ниациновые производные жирных кислот" включает любые и все возможные изомеры, стереоизомеры, энантиомеры, диастереомеры, таутомеры, фармацевтически приемлемые соли, гидраты, сольваты и пролекарства ниациновых производных жирных кислот, описанных в данном описании.
[0019] Неопределенные артикли используются в данном описании для обозначения одного или больше грамматических объектов (то есть, как минимум одного). Например, "элемент" обозначает один элемент или больше, чем один элемент.
[0020] Термин "и/или" используется в данном описании для обозначения любого из "и" и "или", если не указано другое.
[0021] Если конкретно не определено другое, термин "арил" обозначает циклические, ароматические углеводородные группы, которые включают 1-2 ароматических кольца, в том числе моноциклические или бициклические группы, такие как фенил, бифенил или нафтил. В случаях двух ароматических колец (бициклические, и т.п.), ароматические кольца арильной группы могут быть соединены в одинарной точке (например, бифенил), или могут быть конденсированными (например, нафтил). Арильная группа необязательно может быть замещена одним или больше заместителями, например, может содержать 1-5 заместителей, присоединенных в любом положении. Заместители сами по себе необязательно могут быть замещенными.
[0022] "C1-С3 алкил" обозначает неразветвленную или разветвленную насыщенную углеводородную цепь, которая содержит 1-3 атома углерода. Примеры группы C1-С3 алкил включают, не ограничиваясь ими, метил, этил, пропил и изопропил.
[0023] "С1-С4 алкил" обозначает неразветвленную или разветвленную насыщенную углеводородную цепь, которая содержит 1-4 атома углерода. Примеры группы C1-C4 алкил включают, не ограничиваясь ими, метил, этил, пропил, бутил, изопропил, изобутил, втор-бутил- и трет-бутил.
[0024] "C1-C5 алкил" обозначает неразветвленную или разветвленную насыщенную углеводородную цепь, которая содержит 1-5 атомов углерода. Примеры группы С1-С5 алкил включают, не ограничиваясь ими, метил, этил, пропил, бутил, пентил, изопропил, изобутил, втор-бутил- и трет-бутил, изопентил и неопентил.
[0025] "C1-С6 алкил" обозначает неразветвленную или разветвленную насыщенную углеводородную цепь, которая содержит 1-6 атомов углерода. Примеры группы C1-C6 алкил включают, не ограничиваясь ими, метил, этил, пропил, бутил, пентил, гексил, изопропил, изобутил, втор-бутил, трет-бутил, изопентил, и неопентил.
[0026] Термин "циклоалкил" обозначает циклический углеводород, который содержит 3-6 атомов углерода. Примеры циклоалкильных групп включают, не ограничиваясь ими, циклопропил, циклобутил, циклопентил и циклогексил. Следует понимать, что любой из пригодных для замещения атомов водорода в циклоалкиле может быть замещен группами галоген, C1-С3 алкил, гидроксил, алкокси и циано.
[0027] Термин "гетероцикл" в данном описании обозначает циклический углеводород, который содержит 3-6 атомов углерода, где как минимум один из атомов представляет собой О, N или S. Примеры гетероциклов включают, не ограничиваясь ими, азиридин, оксиран, тииран, азетидин, оксетан, тиетан, пирролидин, тетрагидрофуран, тетрагидротиофен, пиперидин, тетрагидропиран, тиан, имидазолидин, оксазолидин, тиазолидин, диоксолан, дитиолан, пиперазин, оксазин, дитиан и диоксан.
[0028] Термин "любая из боковых цепей природных аминокислот" в данном описании обозначает боковую цепь любой из следующих аминокислот: изолейцин, аланин, лейцин, аспарагин, лизин, аспартат, метионин, цистеин, фенилаланин, глютамат, треонин, глютамин, триптофан, глицин, валин, пролин, аргинин, серии, гистидин и тирозин.
[0029] Термин "жирная кислота" в данном описании обозначает омега-3 жирную кислоту и жирные кислоты, которые in vivo метаболизируются до омега-3 жирных кислот. Неограничивающие примеры - это все-цис-7,10,13-гексадекатриеновая кислота, α-линоленовая кислота (АЛК или все-цис-9,12,15-октадекатриеновая кислота), стеаридоновая кислота (СТД или все-цис-6,9,12,15-октадекатетраеновая кислота), эйкозатриеновая кислота (ЭТЕК или все-цис-11,14,17-эйкозатриеновая кислота), эйкозатетраеновая кислота (ЭТК или все-цис-8,11,14,17-эйкозатетрае новая кислота), эйкозапентаеновая кислота (ЭПК или все-цис-5,8,11,14,17-эйкозапентаеновая кислота), докозапентаеновая кислота (ДПК, клупанодоновая кислота или все-цис-7,10,13,16,19-докозапентаеновая кислота), докозагексаеновая кислота (ДГК или все-цис-4,7,10,13,16,19-докозагексаеновая кислота), тетракозапентаеновая кислота (все-цис-9,12,15,18,21-докозагексаеновая кислота) или тетракозагексаеновая кислота (низиновая [nisinic] кислота или все-цис-6,9,12,15,18,21-тетракозеноевая кислота).
[0030] Термин "ниацин" в данном описании обозначает молекулу, известную как ниацин, а также любое ее производное.
[0031] "Субъект" - это млекопитающее, например, человек, мышь, крыса, морская свинка, собака, кот, лошадь, корова, свинья, или негуманоидный примат, такой как мартышка, шимпанзе, бабуин или макака резус, и термины "субъект" и "больной (пациент)" используются в данном описании равнозначным образом.
[0032] Изобретение также включает фармацевтические композиции, содержащие эффективное количество ниацинового производного жирной кислоты и фармацевтически приемлемый носитель. Изобретение включает ниациновое производное жирной кислоты в форме фармацевтически приемлемых пролекарств, гидрата, соли, например, фармацевтически приемлемой соли, энантиомеров, стереоизомеров или смеси указанных компонентов.
[0033] Характерные "фармацевтически приемлемые соли" включают, например, растворимые и нерастворимые в воде соли, такие как ацетат, амзонат (4,4-диаминостильбен-2,2-дисульфонат), бензолсульфонат, бензоат, бикарбонат, бисульфат, битартрат, борат, бромид, бутират, кальций, кальция эдетат, камзилат, карбонат, хлорид, цитрат, клавуланат, дигидрохлорид, эдетат, эдизилат, эстолат, эзилат, фумарат, глюцептат, глюконат, глутамат, гликолиларсанилат, гексафторфосфат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, йодид, изетионат, лактат, лактобионат, лаурат, магний, малат, малеат, манделат, мезилат, метилбромид, метилнитрат, метилсульфат, муцат, напзилат, нитрат, N-метилглюкамина аммониевую соль, 3-гидрокси-2-нафтоат, олеат, оксалат, пальмитат, памоат (1,1-метен-бис-2-гидрокси-3-нафтоат, эйнбонат), пантотенат, фосфат/дифосфат, пикрат, полигалактуронат, пропионат, n-толуолсульфонат, салицилат, стеарат, субацетат, сукцинат, сульфат, субсалицилат, сурамат, таннат, тартрат, теоклат, тозилат, триэтийодид и валерат.
[0034] Термин "метаболическое заболевание" в данном описании обозначает расстройства, заболевания и синдромы, которые включают дислипидемию; при этом фразы «метаболическое расстройство», «метаболическое заболевание» и «метаболический синдром» используется в данном описании равнозначным образом.
[0035] "Эффективное количество" в связи с ниациновым производным жирной кислоты обозначает количество, эффективное для лечения или профилактики метаболического заболевания.
[0036] Термин "носитель" в данном описании охватывает носители, вспомогательные вещества и разбавители и обозначает материал, композицию или носитель, например, жидкий или твердый наполнитель, разбавитель, вспомогательное вещество, растворитель или инкапсулирующий материал, участвующий в переносе или транспортировке фармацевтического агента от одного органа или части тела в другой орган или часть тела.
[0037] Термин "лечение" в связи с субъектом означает улучшение как минимум одного симптома расстройства у субъекта. Лечение может вылечивать, улучшать или как минимум частично улучшать состояние больного при расстройстве.
[0038] Термин "расстройство", если не указано иное, употребляется в данном описании для обозначения заболевания, патологического состояния или болезни, и используется равнозначным образом с последними.
[0039] Термины "вводить" или "введение" в данном описании обозначают или непосредственное введение соединения или фармацевтически приемлемой соли соединения или композиции субъекту, или введение производного в форме пролекарств или аналога соединения или фармацевтически приемлемой соли соединения или композиции субъекту, которые могут образовывать эквивалентное количество активного соединения в организме субъекта.
[0040] Термин "пролекарство" в данном описании обозначает соединение, которое превращается in vivo метаболическими средствами (например, гидролизом) в ниациновое производное жирной кислоты.
[0041] Следующие сокращения используются в данном описании и имеют следующие определения: Воc и ВОС - трет-бутоксикарбонил, Вос2О - ди-трет-бутил-дикарбонат, АТС - альбумин телячьей сыворотки, КДИ - 1,1′-карбонилдиимидазол, ДЦК - N,N-дициклогексилкарбодиимид, ДИЭА - N,N-диизопропилэтиламин, ДМАП - 4-диметиламинопиридин, МДСИ - модифицированная Дульбекко среда Игла, ДМФ - N,N-диметилформамид, ДОСН - диоктилсульфосукцинат натрий, ЭДК и ЭДКИ - 1-этил-3-(3-диметиламинопропил)карбодиимида гидрохлорид, ELISA - иммуносорбентный анализ с использованием ферментов, EtOAc - этилацетат, СТЭ - сыворотка телячьего эмбриона, час - час, ГАТУ - 2-(7-аза-1H-бензотриазол-1-ил)-1,1,3,3-тетраметилурония гексафторфосфат, ВИЧ - вирус иммунодефицита человека, ГПМЦ - гидроксипропилметилцеллюлоза, оксон - калия пероксимоносульфат, Pd/C -палладий на угле, ТФУ - трифторуксусная кислота, ТПГС - токоферол пропиленгликольсукцинат, и ТГФ - тетрагидрофуран.
СОЕДИНЕНИЯ
[0042] Соответственно, в одном из аспектов данного изобретения предлагается молекулярный конъюгат, который включает ниацин и ковалентно связанную с ним жирную кислоту, где жирная кислота выбрана из группы, состоящей из омега-3 жирных кислот и жирных кислот, которые метаболизируются in vivo до омега-3 жирных кислот, где конъюгат включает как минимум один амид, и конъюгат способен гидролизоваться с образованием свободного ниацина и свободной жирной кислоты.
[0043] В некоторых вариантах, жирная кислота выбрана из группы, состоящей из все-цис-7,10,13-гексадекатриеновой кислоты, α-линоленовой кислоты, стеаридоновой кислоты, эйкозатриеновой кислоты, эйкозатетраеновой кислоты, эйкозапентаеновой кислоты (ЭПК), докозапентаеновой кислоты, докозагексаеновой кислоты (ДГК), тетракозапентаеновой кислоты и тетракозапентаеновой кислоты. В других вариантах, жирная кислота выбрана из эйкозапентаеновой кислоты и докозагексаеновой кислоты. В некоторых вариантах, гидролиз является ферментным.
[0044] В другом аспекте данного изобретения предлагаются ниациновые производные жирных кислот в соответствии с Формулой I:

и их фармацевтически приемлемые соли, гидраты, сольваты, пролекарства, энантиомеры и стереоизомеры;
где R1, R2, R3, R4, R5, R6, R7, R, W1, W2, L, а, с, b, d, e, g, h, m, n, o, p, q, Z, r, s, t и v являются такими, как определено выше для Формулы I,
при условии, что в соединении присутствует по меньшей мере один
 или
или 
[0045] В некоторых вариантах R3 представляет собой Cl, F или CN.
[0046] В некоторых вариантах R3 представляет собой -СН3 или -СН2СН3.
[0047] В некоторых вариантах W1 представляет собой NH.
[0048] В некоторых вариантах W2 представляет собой NH.
[0049] В некоторых вариантах W1 представляет собой О.
[0050] В некоторых вариантах W2 представляет собой О.
[0051] В некоторых вариантах каждый из а и с независимо представляет собой Н или СН3.
[0052] В некоторых вариантах m равно 0.
[0053] В других вариантах m равно 1.
[0054] В некоторых вариантах L представляет собой -S, или -S-S-.
[0055] В некоторых вариантах L представляет собой -O-,
[0056] В некоторых вариантах L представляет собой
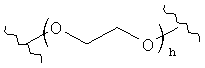
[0057] В некоторых вариантах L представляет собой

[0058] В некоторых вариантах L представляет собой
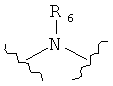
[0059] В некоторых вариантах L представляет собой
 ,
,  , или
, или  .
.
[0060] В некоторых вариантах L представляет собой
 ,
,  или
или  .
.
[0061] В некоторых вариантах L представляет собой
 ,
,  или
или  .
.
[0062] В некоторых вариантах один из b представляет собой O-Z, Z представляет собой
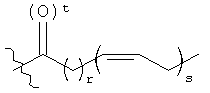
и t равно 1.
[0063] В некоторых вариантах один из d представляет собой C(O)OR.
[0064] В некоторых вариантах каждый из n, о, p и q равен 1.
[0065] В некоторых вариантах два из n, о, p и q равны 1.
[0066] В других вариантах три из n, о, p и q равны 1.
[0067] В некоторых вариантах один из Z представляет собой
 .
.
и r равно 2.
[0068] В некоторых вариантах один из Z представляет собой
 ;
;
и r равно 3.
[0069] В некоторых вариантах один из Z представляет собой

и r равно 7.
[0070] В других вариантах один из Z представляет собой

и s равно 3.
[0071] В некоторых вариантах один из Z представляет собой
 .
.
и s равно 5.
[0072] В некоторых вариантах один из Z представляет собой
 ;
;
и s равно 6.
[0073] В некоторых вариантах один из Z представляет собой
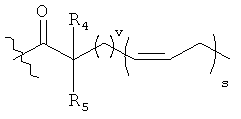
и v равно 1.
[0074] В других вариантах один из Z представляет собой

и v равно 2.
[0075] В некоторых вариантах один из Z представляет собой

и v равно 6.
[0076] В некоторых вариантах один из Z представляет собой

и s равно 3.
[0077] В некоторых вариантах один из Z представляет собой

и s равно 5.
[0078] В других вариантах один из Z представляет собой

и s равно 6.
[0079] В некоторых вариантах t равно 1.
[0080] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, m равно 1, каждый из n, о, p и q равен 1, и L представляет собой О.
[0081] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, m равно 1, каждый из n, о, p и q равен 1, и L представляет собой -S-S-.
[0082] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, m равно 1, каждый из n и о равен 0, каждый из p и q равен 1, и L представляет собой

[0083] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, m равно 1, каждый из n, о, p и q равен 0, и L представляет собой

[0084] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, каждый из m, n и о равен 0, и каждый из p и q равен 1.
[0085] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, m равно 1, каждый из n и о равен 0, каждый из p и q равен 1, и L представляет собой

[0086] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, m равно 1, каждый из n и о равен 1, каждый из р и q равен 0, и L представляет собой

[0087] В некоторых вариантах r равно 2, s равно 6, m равно 1, каждый из n и о равен 0, каждый из р и q равен 1, и L представляет собой

[0088] В некоторых вариантах r равно 2, s равно 6, m равно 1, каждый из n и о равен 1, каждый из р и q равен 0, и L представляет собой

[0089] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, m равно 1, каждый из n, о, р и q равен 1, и L представляет собой

[0090] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, m равно 1, каждый из n, о, р и q равен 1, и L представляет собой NR6.
[0091] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, каждый из m, n и о равен 0, каждый из р и q равен 1, и один из с представляет собой -СН3, и другой с представляет собой -СН3.
[0092] В некоторых вариантах r равно 2, s равно 6, каждый из W1 и W2 представляет собой NH, m равно 1, каждый из n и о равен 1, каждый из р и q равен 0, и L представляет собой
 .
.
[0093] В некоторых вариантах r равно 3, s равно 5, и L представляет собой -S-S-.
[0094] В некоторых вариантах r равно 3, s равно 5, и L представляет собой -O-.
[0095] В некоторых вариантах r равно 3, s равно 5, и L представляет собой

[0096] В некоторых вариантах r равно 3, s равно 5, и L представляет собой

[0097] В некоторых вариантах r равно 3, s равно 5, и L представляет собой

 или
или  .
.
[0098] В некоторых вариантах r равно 3, s равно 5, и L представляет собой
 ,
,  или
или  .
.
[0099] В некоторых вариантах r равно 3, s равно 5, и каждый из n, о, p и q равен 1.
[0100] В некоторых вариантах r равно 3, s равно 5, и два из n, о, р и q равны 1.
[0101] В некоторых вариантах r равно 3, s равно 5, и каждый из W1 и W2, представляет собой NH.
[0102] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n, о, р и q равен 1, и L представляет собой О.
[0103] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n, о, р и q равен 1, и L представляет собой - S-S-.
[0104] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n и о равен 0, каждый из р и q равен 1, и L представляет собой

[0105] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n, о, р и q равен 0, и L представляет собой

[0106] В некоторых вариантах r равно 3, s равно 5, каждый из m, n и о равен 0, и каждый из р и q равен 1.
[0107] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n и о равен 1, каждый из р и q равен 0, и L представляет собой

[0108] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n и о равен 0, каждый из р и q равен 1, и L представляет собой

[0109] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n и о равен 0, каждый из р и q равен 1, и L представляет собой

[0110] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n и о равен 1, каждый из р и q равен 0, и L представляет собой

[0111] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n, о, р и q равен 1, и L представляет собой NR6.
[0112] В некоторых вариантах r равно 3, s равно 5, каждый из m, n и о равен 0, каждый из р и q равен 1, один из с представляет собой -СН3, и другой с представляет собой -СН3.
[0113] В некоторых вариантах r равно 3, s равно 5, m равно 1, каждый из n и о равен 1, каждый из р и q равен 0, и L представляет собой

[0114] В Формуле I, любой один или больше из Н могут быть заменены на дейтерий. Также следует понимать, что в Формуле I метальный заместитель может быть заменен на C1-С6 алкил.
[0115] В других альтернативных вариантах, соединения Формулы I являются такими, как определено ниже:
[0116] N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтокси)этил)никотинамид (I-1);
[0117] N-(2-((2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(метил)амино)этил)никотинамид(I-2);
[0118] N-(2-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)дисульфанил)этил)никотинамид(I-3);
[0119] N-(2-(1-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)-2,5-диоксопирролидин-3-илтио)этил)никотинамид(I-4);
[0120] метил-3-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоацэтокси)-2-(никотинамидо)бутаноат(I-5);
[0121] 1,3-дигидроксипропан-2-ил-6-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-(никотинамидо)гексаноат (I-6);
[0122] N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)никотинамид (I-7);
[0123] N-(2-(5Z,8Z,llZ,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидоэтил)никотинамид (I-8);
[0124] (2S,3R)-метил-3-((S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропаноилокси)-2-(никотинамидо)бутаноат(I-9);
[0125] (2S,3R)-метил-3-((S)-2-((5Z,8Z,11Z,14Z,17Z)-икоза-5,8,11,14,17-пентаенамидо)пропаноилокси)-2-(никотинамидо)бутаноат (I-10);
[0126] (S)-метил-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)гексаноат (I-11);
[0127] (S)-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)гексановая кислота (I-12);
[0128] (S)-метил-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-6-(никотинамидо)гексаноат (I-13);
[0129] (S)-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-6-(никотинамидо)гексановая кислота (I-14);
[0130] (S)-метил-6-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-2-(никотинамидо)гексаноат (I-15);
[0131] (S)-6-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-2-(никотинамидо)гексановая кислота (I-16);
[0132] (S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-6-(никотинамидо)гексановая кислота (I-1);
[0133] (S)-5-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)пентановая кислота (I-18);
[0134] (S)-2-((4Z,7Z,10Z,13Z,16Z,19z)-докоза-4,7,10,13,16,19-гексаенамидо)-5-(никотинамидо)пентановая кислота (I-19);
[0135] 4-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-(никотинамидо)бутановая кислота (I-20);
[0136] 2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-4-(никотинамидо)бутановая кислота (I-21);
[0137] 3-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-(никотинамидо)пропановая кислота (I-22);
[0138] 2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-3-(никотинамидо)пропановая кислота (I-23);
[0139] 2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)-4-(никотинамидо)бутановая кислота (I-24);
[0140] (S)-1,3-дигидроксипропан-2-ил-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-6-(никотинамидо)гексаноат (I-25);
[0141] (S)-1,3-дигидроксипропан-2-ил-5-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)пентаноат (I-26);
[0142] (S)-1,3-дигидроксипропан-2-ил-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-5-(никотинамидо)пентаноат(I-27);
[0143] 1,3-дигидроксипропан-2-ил-4-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-(никотанамидо)бутаноат (I-28);
[0144] 1,3-дигидроксипропан-2-ил-2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-4-(никотинамидо)бутаноат (I-29);
[0145] 1,3-дигидроксипропан-2-ил-3-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-(никотинамидо)пропаноат (I-30);
[0146] 1,3-дигидроксипропан-2-ил-2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-3-(никотинамидо)пропаноат (I-31);
[0147] 1,3-дигидроксипропан-2-ил-2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)-4-(никотинамидо)бутаноат(1-32);
[0148] N-(4-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидобутил)никотинамид (I-33);
[0149] N-(3-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидопропил)никотинамид (I-34);
[0150] N-(1-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-метилпропан-2-ил)никотинамид (I-35);
[0151] N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-метилпропил)никотинамид (I-36);
[0152] N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтиламино)этил)никотинамид(I-37);
[0153] N-(3-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтиламино)пропил)никотинамид (I-38);
[0154] N-(2-(3-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидопропиламино)этил)никотинамид (I-39);
[0155] N-(2-((3-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидопропил)(этил)амино)этил)никотинамид (I-40);
[0156] N-(2-((2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(изобутил)амино)этил)никотинамид (I-41);
[0157] N-(2-(N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)ацетамидо)этил)никотинамид (I-42);
[0158] N-(2-((2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(2-морфолиноетил)амино)этил)никотинамид (I-43);
[0159] N-(2-((2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(3-(пиперазин-1-ил)пропил)амино)этил)никотинамид (I-44);
[0160] N-(3-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-оксопропил)никотинамид (I-45);
[0161] N-(3-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-морфолинопропил)никотинамид (I-46);
[0162] N-(3-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-(пиперазин-1-ил)пропил)никотинамид (I-47);
[0163] N-(3-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-(4-метилпиперазин-1-ил)пропил)никотинамид (I-48);
[0164] N-(5-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-3-гидроксипентил)никотинамид (I-49);
[0165] N-(5-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-3-морфолинопентил)никотинамид (I-50);
[0166] N-(5-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-3-(пиперазин-1-ил)пентил)никотинамид (I-51);
[0167] (S)-((R)-1-(никотинамидо)пропан-2-ил)-2-((5Z,8Z,HZ,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)пропаноат (I-52);
[0168] (S)-((R)-1-(никотинамидо) пропан-2-ил)-2-((5Z,8Z,10Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-3-метилбутаноат (I-53);
[0169] N-(2-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтокси)этокси)этил)никотинамид (I-54);
[0170] N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтилтио)этил)никотинамид (I-55);
[0171] (4Z,7Z,10Z,13Z,16Z,19Z)-1-(никотинамидо)пропан-2-ил-докоза-4,7,10,13,16,19-гексаеноат (I-56);
[0172] (4Z,7Z,10Z,13Z,16Z,19Z)-4-мэтокси-3-(никотинамидо)-4-оксобутан-2-илдокоза-4,7,10,13,16,19-гексаеноат (I-57);
[0173] N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)-6-метилникотинамид (I-58);
[0174] N-(2-(5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидоэтил)-6-метилникотинамид (I-59);
[0175] N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)-6-этилникотинамид (I-60);
[0176] 6-этил-N-(2-(5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидоэтил)никотинамид (I-61);
[0177] 6-хлор-N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)никотинамид (I-62);
[0178] 6-хлор-N-(2-(5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидоэтил)никотинамид (I-63);
[0179] N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)-6-фторникотинамвд (I-64);
[0180] 6-фтор-N-(2-(5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидоэтил)никотинамид (I-65);
[0181] 6-циано-N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)никотинамид (I-66);
[0182] 6-циано-N-(2-(5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидоэтил)никотинамид (I-67);
[0183] (S)-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(2-метилникотинамидо)гексановая кислота (I-68);
[0184] (S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-6-(2-метилникотинамидо)гексановая кислота (I-69);
[0185] (S)-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(2-этилникотинамидо)гексановая кислота (I-70);
[0186] (S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-6-(2-этилникотинамидо)гексановая кислота (I-71);
[0187] (S)-2-(2-хлорникотинамвдо)-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)гексановая кислота (I-72);
[0188] (S)-6-(2-хлорникотинамидо)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)гексановая кислота (I-73);
[0189] (S)-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(2-фторникотинамидо)гексановая кислота (I-74);
[0190] (S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-6-(2-фторникотинамидо)гексановая кислота (I-75);
[0191] (S)-2-(2-цианоникотинамидо)-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)гексановая кислота (I-76);
[0192] (S)-6-(2-цианоникотинамидо)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)гексановая кислота (I-77);
[0193] N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтокси)этил)-6-метилникотинамид (I-78);
[0194] N-(2-((2-(4Z.7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(метил)амино)этил)-6-метилникотинамид (I-79);
[0195] N-(2-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)дисульфанил)этил)-6-метилникотинамид (I-80);
[0196] N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтокси)этил)-6-этилникотинамид (I-81);
[0197] N-(2-((2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(метил)амино)этил)-6-этилникотинамид (I-82);
[0198] N-(2-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)дисульфанил)этил)-6-этилникотинамид (I-83);
[0199] 6-хлор-N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтокси)этил)никотинамид (I-84);
[0200] 6-хлор-N-(2-((2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(метил)амино)этил)никотинамид (I-85);
[0201] 6-хлор-N-(2-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)дисульфанил)этил)никотинамид (I-86);
[0202] 6-циано-N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтокси)этил)никотинамид (I-87);
[0203] 6-циано-N-(2-((2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(метил)амино)этил)никотинамид (I-88);
[0204] 6-циано-N-(2-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)дисульфанил)этил)никотинамид (I-89).
Способы с применением ниациновых производных жирных кислот
[0205] Изобретение также включает способы лечения метаболических заболеваний, например, лечение или профилактику атеросклероза, в том числе метаболических заболеваний, дислипидемии, заболевания коронарных сосудов сердца, гиперхолестеринемии, диабета 2 типа, повышенного уровня холестерина, метаболического синдрома и сердечно-сосудистого заболевания.
[0206] В одном из вариантов, способ включает обеспечение контакта клетки с ниациновым производным жирной кислоты в количестве, достаточном для уменьшения высвобождения триглицеридов или ЛПОНП или ЛПНП или увеличение обратного транспорта холестерина, или увеличение уровня ЛПВП.
[0207] Также в изобретении предложен способ ингибирования, профилактики или лечения метаболического заболевания или симптомов метаболического заболевания у субъекта. Примеры таких расстройств включают, не ограничиваясь ими, атеросклероз, дислипидемию, гипертриглицеридемию, повышенное артериальное давление, сердечную недостаточность, сердечные аритмии, низкие уровни ЛПВП, высокие уровни ЛПНП, внезапную смерть, стабильную стенокардию, заболевание коронарных сосудов сердца, острый инфаркт миокарда, вторичную профилактику инфаркта миокарда, кардиомиопатию, эндокардит, диабет 2 типа, инсулинорезистентность, сниженную переносимость глюкозы, гиперхолестеринемию, инсульт, гиперлипидемию, гиперлипопротеинемию, хроническое заболевание почек, перемежающуюся хромоту, гиперфосфатемию, атеросклероз сонной артерии, заболевание периферических артерий, диабетическую нефропатию, гиперхолестеринемию в ВИЧ-инфицированных, острый коронарный синдром (ОКС), неалкогольное жировое заболевание печенки, окклюзионное заболевание артерий, мозговой артериосклероз, сердечно-сосудистые расстройства, ишемию миокарда и автономную диабетическую невропатию.
[0208] В некоторых вариантах, субъекту вводят эффективное количество ниацинового производного жирной кислоты.
[0209] Изобретение также включает фармацевтические композиции, пригодные для лечения или профилактика метаболического заболевания, или для подавления метаболического заболевания, или для более чем одного из указанного. Композиции могут быть пригодными для приема внутрь и содержать эффективное количество ниацинового производного жирной кислоты и фармацевтически приемлемый носитель. Ниациновые производные жирных кислот являются особенно пригодными, поскольку они демонстрируют самую низкую периферическую токсичность или даже отсутствие периферической токсичности.
[0210] Каждое из ниациновых производных жирных кислот можно вводить в количествах, достаточных для лечения или предупреждения метаболического заболевания или предупреждения развития указанных состояний у субъектов.
[0211] Введение ниациновых производных жирных кислот может быть осуществлено любым способом введения терапевтических агентов. Указанные способы включают системное введение или местное применение, например, пероральный, назальный, парентеральный, трансдермальный, подкожный, влагалищный, буккальный, ректальный способы введения или местное применение.
[0212] В зависимости от предусмотренного способа введения, композиции могут быть изготовлены в твердой, полутвердой или жидкой лекарственной форме, например, инъекционные препараты, таблетки, суппозитории, пилюли, капсулы с замедленным высвобождением, эликсиры, настойки, эмульсии, сиропы, порошки, жидкости, суспензии, и тому подобное, иногда в виде дозированных лекарственных форм, в соответствии с традиционными фармацевтическими способами. Также, они могут быть введены в форме для внутривенного (как болюс, так и инфузия), внутрибрюшинного, подкожного или внутримышечного введения; все используемые формы хорошо известных специалистам в области фармации.
[0213] Иллюстративные фармацевтические композиции - это таблетки и желатиновые капсулы, содержащие ниациновое производное жирной кислоты и фармацевтически приемлемый носитель, такой как: а) разбавитель, например, вода очищенная, триглицеридные масла, в том числе гидрогенизированное или частично гидрогенизированное масло, или их смеси, кукурузное масло, оливковое масло, подсолнечное масло, сафлоровое масло, рыбий жир, в том числе ЭПК или ДГК, или их эфиры или триглицериды, или смеси указанных компонентов, омега-3 жирные кислоты или их производные, лактоза, глюкоза, сахароза, маннит, сорбит, целлюлоза, натрия сахаринат, глюкоза и/или глицин; б) смазывающее вещество, например, кремния диоксид, тальк, стеариновая кислота, ее магниевая или кальциевая соль, натрия олеат, натрия стеарат, магния стеарат, натрия бензоат, натрия ацетат, натрия хлорид и/или полиэтиленгликоль; в частности, для таблеток; в) связующее средство, например, алюминия магния силикат, крахмальный клейстер, желатин, трагакантовая камедь, метилцеллюлоза, натрий карбоксиметилцеллюлоза, магния карбонат, природные сахара, например, глюкоза или бета-лактоза, кукурузные подсластители, природная и синтетическая камедь, например, акациевая, трагакантовая камедь или натрия альгинат, воск и/или поливинилпирролидон, по желанию; г) дезинтегрант, например, различные виды крахмала, агар, метилцеллюлоза, бентонит, ксантановая камедь, альгиновая кислота или ее натриевая соль, или шипучие смеси; д) абсорбент, краситель, ароматизатор и подсластитель; е) эмульгатор или диспергирующее средство, например, Твин 80, Лабразол, ГПМЦ. ДОСН, капроил 909, лабрафак, лабрафил, пецеол, транскутол, капмул МСМ, капмул PG-12, катекст 355, гелюцир, витамин Е ТГПС или другой приемлемый эмульгатор; и/или ж) агент, который увеличивает абсорбцию соединения, например, циклодекстрин, гидроксипропилциклодекстрин, PEG400, PEG200.
[0214] Жидкая композиция, в частности, для инъекций, может, например, быть получена растворением, диспергированием, и т.п.Например, ниациновое производное жирной кислоты растворяют или смешивают с фармацевтически приемлемым растворителем, таким как вода, раствор соли, водный раствор глюкозы, глицерин, этанол, и т.п, с получением таким способом изотонического инъекционного раствора или суспензии. Белки, такие как альбумин, хиломикронные частицы или белки сыворотки, могут быть использованы для солюбилизации ниациновых производных жирных кислот.
[0215] Ниациновые производные жирных кислот также могут быть введены в суппозиторий, который может быть получен на основе жировых эмульсий или суспензий; с использованием в качестве носителя полиалкиленгликоля, такого как пропиленгликоль.
[0216] Ниациновые производные жирных кислот могут также быть введены в форме липосомальных систем доставки, таких как маленькие однослойные везикулы, большие однослойные везикулы и многослойные везикулы. Липосомы могут быть образованы из разнообразных фосфолипидов, содержащих холестерин, стеариламин или фосфатидилхолины. В некоторых вариантах, пленку липидных компонентов гидратируют водным раствором лекарственного средства с образованием липидного слоя, в котором инкапсулировано лекарственное средство, как описано в патенте США 5262564, содержание которого включено в данное описание путем ссылки в полном объеме.
[0217] Ниациновые производные жирных кислот могут также быть введены с использованием моноклональных антител как индивидуальных носителей, к которым присоединенные Ниациновые производные жирных кислот. Ниациновые производные жирных кислот могут также быть соединены с растворимыми полимерами как пригодными для нацеливания носителями лекарственных средств. Такие полимеры могут включать поливинилпирролидон, сополимер пирана, полигидроксипропилметилакриламид-фенол, полигидроксиэтиласпанамидфенол или полиэтиленоксидполилизин, замещенный пальмитоильными остатками. Кроме того, ниациновые производные жирных кислот могут быть присоединены к классу биоразлагаемых полимеров, пригодных для обеспечения контролируемого высвобождения лекарственного средства, таких как полимолочная кислота, полиэпсилон капролактон, полигидроксимасляная кислота, полиортоэфиры, полиацеталь, полидигидропираны, полицианоакрилаты и поперечно-сшитые или амфипатические блок-сополимеры гидрогелей. В одном из вариантов, ниациновые производные жирных кислот не соединены ковалентно с полимером, например, полимером поликарбоновой кислоты или полиакрилатом.
[0218] Парентеральное инъекционное введение в целом применяют для подкожной, внутримышечной или внутривенной инъекции и инфузии. Инъекционные препараты могут быть получены в традиционных формах, как жидкие растворы или суспензии, или как твердые формы, пригодные для растворения в жидкости перед инъекцией.
[0219] Композиции могут быть получены в соответствии с традиционными способами смешивания, гранулирования или нанесения покрытия, соответственно, и такие фармацевтические композиции могут содержать от приблизительно 0,1% до приблизительно 80%, от приблизительно 5% до приблизительно 60%, или от приблизительно 1% до приблизительно 20% ниацинового производного жирной кислоты (масс. или об.).
[0220] Схему лечения с использованием ниацинового производного жирной кислоты выбирают в соответствии с разнообразными факторами, в том числе, тип, вид, возраст, масса тела, пол и медицинское состояние больного; тяжесть состояния, которое подлежит лечению; способ введения; функция почек или печени у больного; и конкретное ниациновое производное жирной кислоты, которое применяют. Средний врач или ветеринар может легко определить и назначить эффективное количество лекарственного средства, необходимое для предупреждения, противодействия или остановки прогрессирования состояния.
[0221] Эффективные дозы по данному изобретению, при применение в соответствии с инструкцией, варьируют от приблизительно 20 мг до приблизительно 5000 мг ниацинового производного жирной кислоты в сутки. Композиции для применения in vivo или in vitro могут содержать приблизительно 20, 50, 75, 100, 150, 250, 500, 750, 1000, 1250, 2500, 3500 или 5000 мг ниацинового производного жирной кислоты. В одном из вариантов, композиции находятся в форме таблетки, на которую может быть нанесена риска. Эффективные уровни в плазме ниацинового производного жирной кислоты могут варьировать от приблизительно 0,002 мг до приблизительно 100 мг на кг массы тела в сутки. Соответствующие дозы ниациновых производных жирных кислот могут быть определены, как указано в Goodman, L.S.; Gilman, A. The Pharmacological Basis of Therapeutics, 5th ed.; MacMillan: New York, 1975, pp.201-226.
[0222] Ниациновые производные жирных кислот можно вводить один раз в сутки, или общую суточную дозу можно вводить в несколько приемов, то есть 2, 3 или 4 раза в сутки. Кроме того, ниациновые производные жирных кислот можно вводить в интраназальной форме путем местного применения пригодного для интраназального введения носителя, или трансдермальным путем, с использованием трансдермальных пластырей, хорошо известных среднему специалисту в данной области. При введении с помощью формы для трансдермальной доставки, доза может вводиться непрерывно вместо перемежающегося введения в ходе схемы лечения. Другие иллюстративные препараты для местного применения включают кремы, мази, лосьоны, аэрозоль для распыления и гели, где концентрация ниацинового производного жирной кислоты варьирует от приблизительно 0,1% до приблизительно 15%, масс/масс или масс/об.
СПОСОБЫ ПОЛУЧЕНИЯ
Способы получения ниациновых производных жирных кислот
[0223] Примеры путей синтеза, пригодных для получения ниациновых производных жирных кислот Формулы I, приведены в Примерах ниже и обобщены на Схемах 1-9.
Схема 1
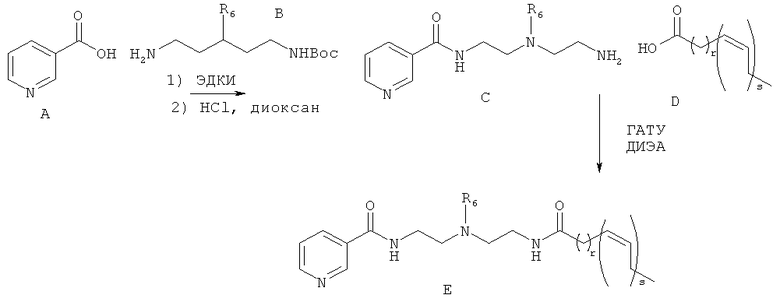
Где Re r и s являются такими, как определено выше.
[0224] Моно-ВОС-защищенный амин формулы В может быть получен из коммерческих источников или изготовлен в соответствии с методиками, описанными в Krapcho et al. Synthetic Communications 1990, 20, 2559-2564. Соединение А может быть амидировано амином В с использованием реагента сочетания, такого как ДЦК, КДИ, ЭДК, или, необязательно, основания и/или катализатора на базе третичного амина, например, ДМАП, с последующим удалением защитной группы ВОС с использованием кислот, таких как ТФУ или НСl, в растворителе, таком как CH2Cl2 или диоксан, с образованием сочетанного Соединения С.Активация Соединения С с использованием агента сочетания, такого как ГАТУ, в присутствии амина, такого как ДИЭА, с последующим прибавлением жирной кислоты формулы D, дает соединения формулы Е.
Схема 2
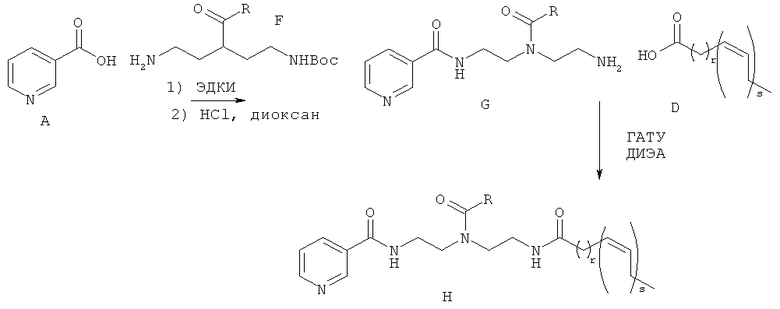
где R, r и s являются такими, как определено выше.
[0225] Ацилированный амин формулы F может быть получен с использованием методик, описанных в Andruszkiewicz et al. Synthetic Communications 2008, 38, 905-913. Соединение А может быть амидировано амином F с использованием реагента сочетания, такого как ДЦК, КДИ, ЭДК, или, необязательно, основания и/или катализатора на базе третичного амина, например, ДМАП, с последующим удалением защитной группы ВОС с помощью кислот, таких как ТФУ или НСl, в растворителе, таком как CH2Cl2 или диоксан, с образованием сочетанного Соединения G. Активация соединения G с использованием агента сочетания, такого как ГАТУ, в присутствии амина, такого как ДИЭА, с последующим добавлением жирной кислоты формулы D дает соединения формулы Н.
Схема 3
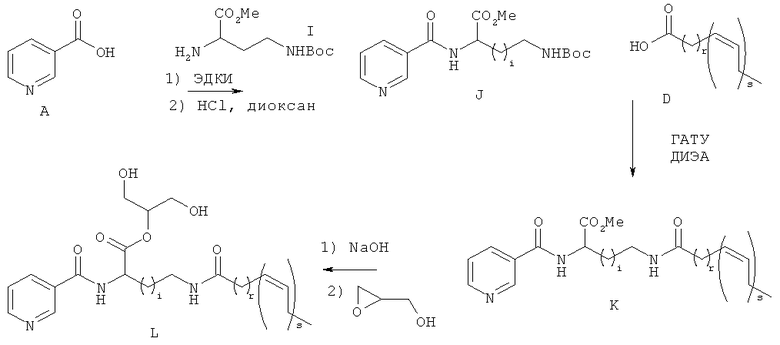
где r и s являются такими, как определено выше.
[0226] Соединение А может быть амидировано соответствующим амином I (где i=0, 1, 2 или 3) с использованием реагента сочетания, такого как ДЦК, КДИ, ЭДК, или, необязательно, основания и/или катализатора на базе третичного амина, например, ДМАП, с последующим удалением защитной группы ВОС с помощью кислот, таких как ТФУ или, НСl в растворителе, таком как СН2Cl2 или диоксан, с образованием сочетанного Соединения J. Активация соединения J с использованием агента сочетания, такого как ГАТУ, в присутствии амина, такого как ДИЭА, с последующим добавлением жирной кислоты формулы D дает соединения формулы К. Гидролиз сложного эфира в основных условиях, которые обеспечиваются, например, NaOH или LiOH, дает соответствующую кислоту, для которой может быть осуществлено сочетание с глицидолом с получением соединений формулы L.
Схема 4
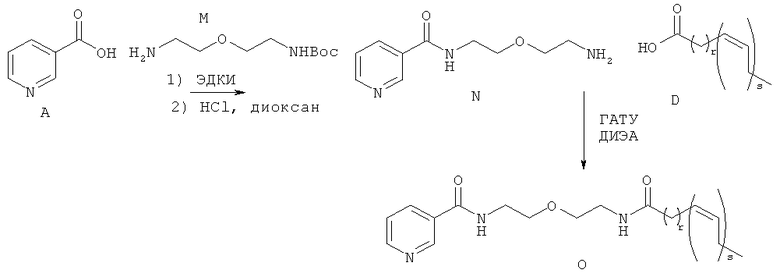
где r и s являются такими, как определено выше.
[0227] Амин М может быть получен в соответствии с методиками, описанными в Dahan et al. J. Org. Chem. 2007, 72, 2289-2296. Для Соединения А может быть осуществлено сочетание с амином М с использованием реагента сочетания, такого как ДЦК, КДИ, ЭДК, или, необязательно, основания и/или катализатора на базе третичного амина, например, ДМАП, с последующим удалением защитной группы ВОС с помощью кислот, таких как ТФУ или НСl, в растворителе, таком как CH2Cl2 или диоксан, с образованием сочетанного Соединения N. Активация Соединения N с использованием агента сочетания, такого как ГАТУ, в присутствии амина, такого как ДИЭА, с последующим добавлением жирной кислоты формулы D дает соединения формулы О.
Схема 5
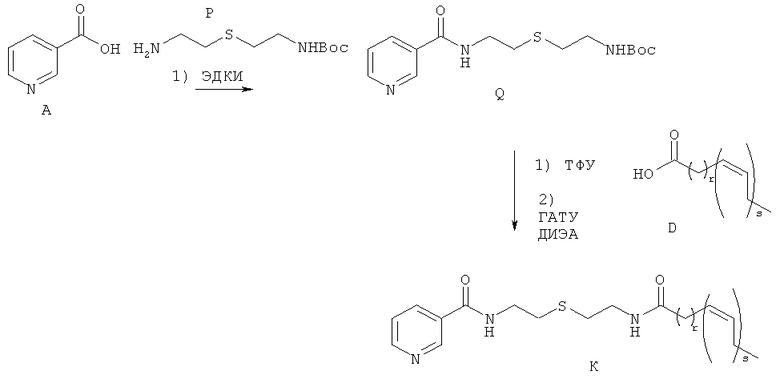
где г и s являются такими, как определено выше.
[0228] Соединение А может быть амидировано коммерчески доступным амином Р с использованием реагента сочетания, такого как ДЦК, КДИ, ЭДК, или, необязательно, основания и/или катализатора на базе третичного амина, например, ДМАП, с получением Соединения Q. Защитная группа ВОС может быть удалена из Соединения Q с помощью кислот, таких как ТФУ или НСl, в растворителе, таком как СН2Сl2 или диоксан, и полученный амин может быть соединен с жирной кислотой формулы D с использованием агента сочетания, такого как ГАТУ, в присутствии амина, такого как ДИЭА, с получением соединений формулы R. Специалисты в данной области могут осуществить окислении серосодержащей группы в формуле Q до соответствующего сульфоксида или сульфона с использованием окислителя, такого Н2О2 или оксон.
Схема 6
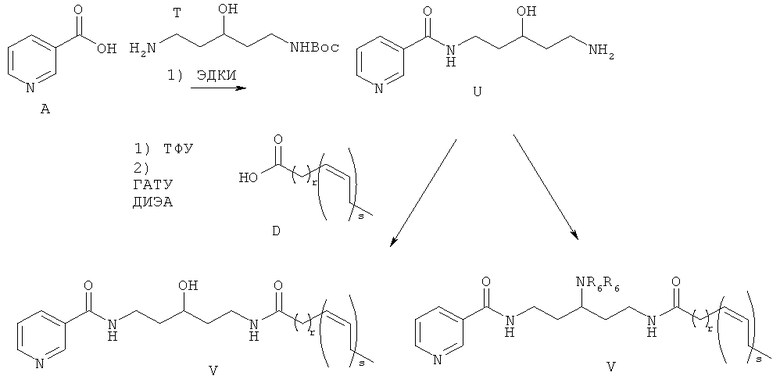
где R6 r и s являются такими, как определено выше.
[0229] Амин Т может быть получен из коммерчески доступного диамина в соответствии с методиками, описанными в Dahan et al. J. Org. Chem. 2007, 72, 2289-2296. Соединение А может быть амидировано амином Т с использованием реагента сочетания, такого как ДЦК, КДИ, ЭДК, или, необязательно, основания и/или катализатора на базе третичного амина, например, ДМАП, с получением Соединения U. Защитная группа ВОС из соединения U может быть удалена с помощью кислот, таких как ТФУ или НСl, в растворителе, таком как CH2Cl2 или диоксан, и может быть осуществлено сочетание полученного амина с жирной кислотой формулы D с использованием ГАТУ, в присутствии амина, такого как ДИЭА, с получением соединений формулы V. Специалисты в данной отрасли могут дополнительно осуществить ацилированне гидроксильной группы в Соединении U или превращение ее в аминогруппу стандартной реакцией мезилировання с последующим вытеснением с использованием натрия азида и гидрогенизацией над катализатором, таким как Pd/C. Амин может быть дополнительно ацилирован или алкилирован, с последующим удалением группы ВОС. Для полученного амина может быть осуществлено сочетание с жирной кислотой формулы D с получением соединений формулы W.
Схема 7
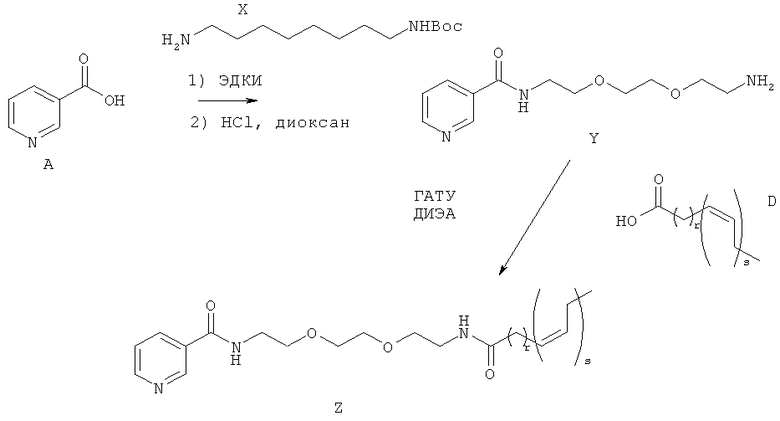
где r и s являются такими, как определено выше.
[0230] Соединение А может быть амидировано коммерчески доступным амином Х с использованием реагента сочетания, такого как ДЦК, КДИ, ЭДК, необязательно с использованием основания и/или катализатора на базе третичного амина, например, ДМАП, с получением Соединения Y. Защитная группа ВОС в Соединении В может быть удалена с помощью кислот, таких как ТФУ или НСl, в растворителе, таком как CH2Cl2 или диоксан. Для полученного амина может быть осуществлено сочетание с жирной кислотой формулы D с использованием реагента сочетания, такого как ГАТУ, в присутствии амина, такого как ДИЭА, с получением соединений формулы Z.
Схема 8
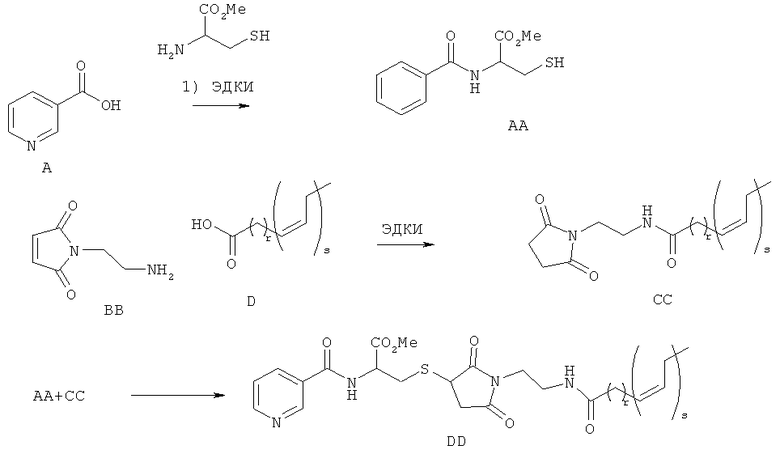
где r и s являются такими, как определено выше.
[0231] Соединение А может быть амидировано коммерчески доступным метиловым эфиром цистеина с использованием реагента сочетания, такого как ДЦК, КДИ, ЭДК, или, необязательно, основания и/или катализатора на базе третичного амина, например, ДМАП, с получением Соединения АА. Коммерчески доступное производное малеинимида ВВ может быть соединено с жирной кислотой формулы D с использованием агента сочетания, такого как ГАТУ или ЭДКИ, с получением соединений формулы СС. Для Соединения АА может быть осуществлено сочетание с соединениями формулы СС в растворителе, таком как ацетонитрил, с получением соединений формулы DD.
Схема 9
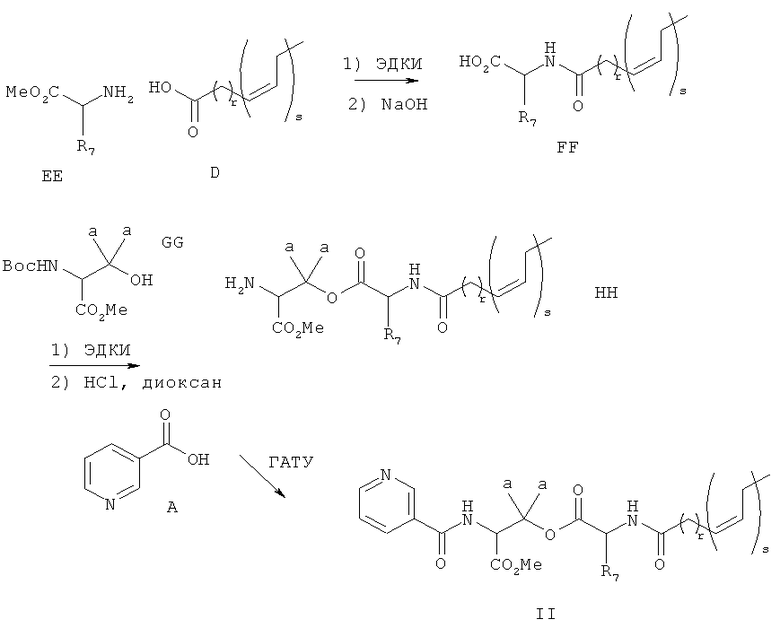
где R7, a, r и s являются такими, как определено выше.
[0232] Для коммерчески доступных эфиров аминокислот ЕЕ может быть осуществлено сочетание с жирной кислотой формулы D с использованием агента сочетания, такого как ЭДКИ или ГАТУ, с последующим щелочным гидролизом метилового эфира с получением соединений формулы FF. Для соединений формулы FF может быть осуществлено сочетание с коммерчески доступными производными ВОС-аминокислоты GG с использованием агента сочетания, такого как ЭДКИ или ГАТУ. Защитная группа ВОС может быть удалена путем обработки кислотами, такими как ТФУ или НСl, с получением соединений формулы НН, для которых далее может быть осуществлено сочетание с Соединением А с получением соединений формулы II.
ПРИМЕРЫ
[0233] Описание дополнительно проиллюстрировано следующими примерами, которые не должны интерпретироваться как ограничивающие контекст или дух данного изобретения конкретными методиками, описанными в данном описании. Следует понимать, что примеры приведены для иллюстрации некоторых вариантов и не предназначены для ограничения границ изобретения. Также следует понимать, что может быть осуществлена пересортировка с получением разнообразных других вариантов, модификаций и эквивалентов изобретения, которые могут прийти в голову специалистам в данной отрасли без отхода от духа данного описания и/или границ, определенных приложенной формулой изобретения.
Пример 1
Влияние ниациновых производных жирных кислот на секрецию АроВ в клетках HepG2
[0234] Сообщалось, что ниацин in vivo повышает уровни в сыворотке ЛПВП по сравнению с уровнями ЛПНП. Подобным образом, сообщалось, что ниацин повышает секрецию ApoA1 (Jin, F-Y. et al. Arterioscler. Thromb. Vase. Biol. 1997, 17 (10), 2020-2028), при этом ингибируя секрецию АроВ (Jin, F-Y. et al. Arterioscler. Thromb. Vase. Biol. 1999, 19, 1051-1059) в супернатантах сред культур HepG2. Независимо, ДГК также продемонстрировала способность к снижению уровней АроВ (Pan, M. et al. J. Clin. Invest. 2004, 113, 1277-1287) по совершенно другому механизму. Таким образом, секреция АроВ клетками HepG2 является потенциальной моделью для клеточного анализа влияния конъюгатов ниацин-ДГК, а также их производных.
[0235] Клетки HepG2 (АТСС) высевали с плотностью 10000 клеток/лунку на 96-луночные планшеты. После прикрепления на протяжении ночи, среду культивирования (10% СТЭ в МДСИ) удаляли, и клетки лишали сыворотки на 24 час в МДСИ, содержащей 0,1% свободного от жирных кислот альбумина телячьей сыворотки (АТС, Sigma). Далее клетки обрабатывали соединением. Ниацин в концентрации 5 мМ использовали как положительный контроль. Все виды обработки осуществляли в трех повторениях. Одновременно с обработкой соединением, секрецию АроВ стимулировали добавлением 0,1 олеата в комплексе со свободной от жирных кислот АТС, в молярном соотношении 5:1. Инкубацию с соединением и олеатом осуществляли на протяжении 24 час. Супернатанты среды удаляли, и концентрацию АроВ измеряли с использованием наборов ELISA (Mabtech АВ). Процент ингибирования секреции АроВ определяли, нормализуя данные к результатам обработанных растворителем клеток. Для данного соединения, значение IC50 (концентрация, при которой секреция АроВ ингибируется на 50%) определяли с использованием модели 4-хпараметрической аппроксимации кривой ингибирования (Graph Pad Prism®). В ходе каждого эксперимента определяли жизнеспособность клеток с использованием набора ATPlite 1-Step (Perkin Elmer) для контроля цитотоксического влияния соединения.
Конъюгат ниацина и жирной кислоты I-7 оценивали на клетках HepG2 в 3-х концентрациях (50, 100 и 200 мкМ). Уровень секреции АроВ сравнивали с уровнем секреции при добавлении ниацина в концентрации 5 мМ. По сравнению с ниацином, конъюгат ниацина и жирной кислоты I-7 продемонстрировал выраженное ингибирование АроВ при намного более низкой концентрации лекарственного средства.
Пример 2
Влияние ниациновых производных жирных кислот на целевые гены SREBP-Ic
Клетки HepG2 (АТСС) высевали с плотностью 20000 клеток/лунку на 96-луночные планшеты. После прикрепления на протяжении ночи, среду культивирования (10% СТЭ в МДСИ) удаляли, и клетки лишали сыворотки на 24 час в МДСИ, содержащей 1% свободного от жирных кислот альбумина телячьей сыворотки (АТС, Sigma). Далее клетки обрабатывали одним из 4-х веществ в конечной концентрации 50 мкМ в 1% растворе АТС или 0,1% олеата в комплексе со свободным от жирных кислот АТС в молярном соотношении 5:1 (4 вещества представляли собой: соединение I-7, соединение I-8, комбинацию свободного ниацина и свободной ДГК, или комбинацию свободного ниацина и свободной ЭПК). Клетки инкубировали на протяжении 6 час, после чего промывали фосфатным буферным раствором (ФБР). С использованием клеток осуществляли обратную транскрипцию РНК до реагентов кДНК в соответствии со стандартными протоколами (отображены в протоколах ПЦР в реальном времени Applied Biosystem StepOne). ПЦР транскриптов в реальном времени осуществляли в анализах Taqman для 4-х специфических генов FASN (синтетаза жирной кислоты), SCD (стероил-КоА-десатураза) и АроА1 (аполипопротеин А1). Во всех 3-х случаях использовали 18S-VIC® как контроль для нормализации. Как показано на фиг.2, статистически значимое ингибирование экспрессии генов FASN и SCD и увеличение экспрессии гена АроА1 наблюдались при стимуляции клеток HepG2 олеатом в присутствии 50 мкМ соединения I-7 и соединения I-8. Две группы, которые содержали комбинацию свободного ниацина и свободной ДГК или ниацина и свободной ЭПК, не продемонстрировали значительных изменений экспрессии указанных 3-х специфических генов в конечной концентрации 50 мкМ.
Соединения
[0236] Следующие неограничивающие примеры соединений служат для иллюстрации дополнительных вариантов ниациновых производных жирных кислот. Следует понимать, что любые варианты, приведенные в разделе «Примеры» являются вариантами ниациновых производных жирных кислот, и, таким образом, пригодны для применения в описанных выше способах и композициях.
Пример 3
Получение N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)никотинамида (I-7)
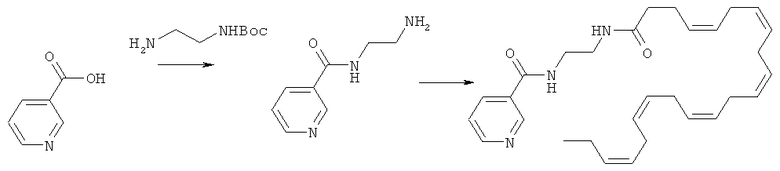
[0237] В типичном случае, никотиновую кислоту (2,0 г, 16,2 ммоль) переносят в CH2Cl2 (20 мл) вместе с оксалилхлоридом (1,4 мл, 16,2 ммоль). После этого добавляют несколько капель ДМФА, реакционную смесь перемешивают при комнатной температуре до полного растворения твердых веществ и прекращения выделения газа (1 час). Полученный свежеприготовленный раствор хлорангидрида кислоты добавляют по каплям при температуре 0°С к раствору, содержащему трет-бутил-2-аминоэтилкарбамат (2,6 г, 16,2 ммоль) и Et3N (3,4 мл, 24,2 ммоль) в СН2Сl2 (200 мл). Полученную реакционную смесь нагревают до комнатной температуры и перемешивают на протяжении 2 часов. Далее ее промывают солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (CH2Cl2) дает трет-бутил-2-(никотинамидо)этилкарбамат (3,1 г, 74%).
[0238] трет-Бутил-2-(никотинамидо)этилкарбамат (3,1 г, 11,7 ммоль) переносят в 25% ТФУ в CH2Cl2 (10 мл). Полученную реакционную смесь оставляют при комнатной температуре на 1 час. В этой точке образуется значительное количество осадка, после чего прозрачный фильтрат удаляют. Остаток твердого вещества сушат с получением соли ТФУ N-(2-аминоэтил)никотинамида (1,6 г).
[0239] Соль ТФУ N-(аминоэтил)никотинамида (5,0 ммоль) переносят в СН3СN (20 мл) вместе с (4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаеновой кислотой (5,0 ммоль), ГАТУ (5,5 ммоль) и ДИЭА (15 ммоль). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 час и разбавляют этилацетатом. Органическую фракцию промывают насыщенным водным раствором NaHCO3, солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (5% МеОН/СН2Сl2) дает N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)никотинамид. МС: вычислено для С30H41N3O2 475,32; найдено [М+Н]+ 476.
Пример 4
Получение N-(2-(5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидоэтил)никотинамида (I-8)
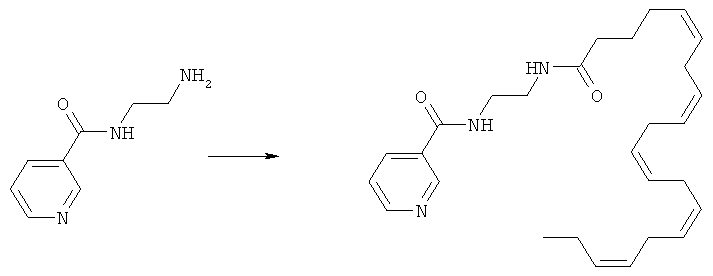
[0240] Соль ТФУ N-(2-аминоэтил)никотинамида (1,6 г, 5,7 ммоль) переносят в CH3CN (15 мл) вместе с (5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаеновой кислотой (1,7 г, 5,7 ммоль), ГАТУ (2,4 г, 6,3 ммоль) и ДИЭА (3 мл, 17 ммоль). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 час и разбавляют этилацетатом. Органическую фракцию промывают насыщенным водным раствором NaHCO3, солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (5% MeOH/CH2Cl2) дает N-(2-(5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидоэтил)никотинамид (1,6 г, 62%). МС: вычислено для C28H39N3O2: 449,3; найдено [М+Н]+ 450.
Пример 5
Получение N-(2-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)дисульфанил)этил)никотинамида (I-3)
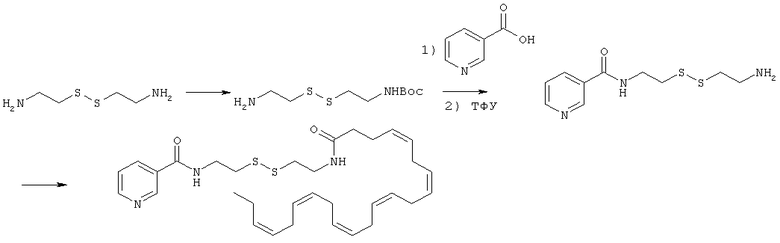
[0241] Цистамина дигидрохлорид (1,0 г, 4,44 ммоль) растворяют в метаноле (50 мл). Триэтиламин (1,85 мл, 3 экв.) добавляют при комнатной температуре, с последующим добавлением по каплям Вос2О (0,97 г, 4,44 ммоль) в виде раствора в метаноле (5 мл). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 3 час. Далее ее упаривают при сниженном давлении, и полученный остаток переносят в 1М водный раствор NaH2PO4 (20 мл). Водную фракцию промывают смесью пентан/ЕtOАс (1:1, 10 мл), подщелачивают до рН 9 с помощью 1М водного раствора NaOH и экстрагируют этилацетатом. Объединенные органические фракции промывают солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении с получением трет-бутил-2-(2-(2-аминоэтил)дисульфанил)этилкарбамата (500 мг, 44%).
[0242] Отдельно, никотиновую кислоту (246 мг, 2,0 ммоль) переносят в CH3CN (10 мл) вместе с трет-бутил-2-(2-(2-аминоэтил)дисульфанил)этилкарбаматом (503 мг, 2,0 ммоль), ЭДКИ (422 мг, 2,2 ммоль). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 4 час, после чего разбавляют этилацетатом. Органическую фракцию промывают разбавленным водным раствором NaHCO3, солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (CH2Cl2) дает трет-бутил-2-(2-(2-(никотинамидо)этил)дисульфанил)этилкарбамат (400 мг, 56%).
[0243] трет-Бутил-2-(2-(2-(никотинамидо)этил)дисульфанил)этилкарбамат (200 мг, 0,56 ммоль) переносят в 25% раствор ТФУ в CH2Cl2 (5 мл) и оставляют при комнатной температуре на 4 час. Реакционную смесь далее упаривают при сниженном давлении с получением соли ТФУ N-(2-(2-(2-аминоэтил)дисульфанил)этил)никотинамида. Полученный материал переносят в CH3CN (10 мл) вместе с (4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаеновой кислотой (184 мг, 0,56 ммоль), ГАТУ (234 мг, 0,62 ммоль) и ДИЭА (0,30 мл). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 час. Далее ее разбавляют этилацетатом и промывают последовательно насыщенным водным раствором NaHCO3 и солевым раствором. Органическую фракцию сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (5% MeOH/CH2Cl2) дает (N-(2-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4.7.10,13,16,19-гексаенамидоэтил)дисульфанил)этил)никотинамид (300 мг, 86%). МС: вычислено для C32H45N3O2S2: 567,3; найдено [М+Н]+ 568.
Пример 6
Получение N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтокси)этил)никотинамида (I-1)
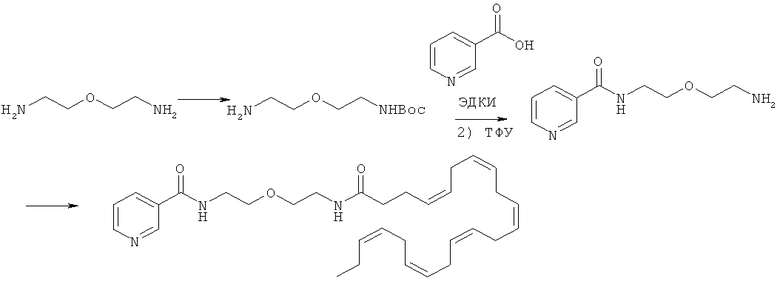
[0244] В типичном случае, натрия гидроксид (400 мг, 10 ммоль) растворяют в метаноле (70 мл), и добавляют 2-(2-аминоэтокси)этанамина дигидрохлорид (1,0 г, 5,65 ммоль). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 30 мин. Затем раствор, содержащий Вос2О (740 мг, 3,40 ммоль) в ТГФ (15 мл) добавляют по каплям при комнатной температуре в течение 15 мин. Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 18 час. Далее ее упаривают при сниженном давлении. Полученный остаток переносят в CH2Cl2 (200 мл) и энергично перемешивают при комнатной температуре на протяжении 4 час. Смесь фильтруют, и фильтрат упаривают при сниженном давлении с получением трет-бутил-2-(7-аминоэтокси)этилкарбамата (850 мг, 74%).
[0245] трет-Бутил-2-(2-аминоэтокси)этилкарбамат (420, 2,06 ммоль) далее переносят в CH3CN (20 мл) вместе с никотиновой кислотой (253 мг, 2,06 ммоль) и ЭДКИ (434 мг, 2,3 ммоль). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 18 час. Далее ее разбавляют этилацетатом (20 мл), промывают насыщенным водным раствором NaHCO3, солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Полученный остаток очищают хроматографией на силикагеле (СН2Сl2/МеОН, 9:1) с получением трет-бутил-2-(2-(никотинамидо)этокси)этилкарбамата (280 мг, 44%). МС: вычислено для С15H23N3O4: 309,17; найдено [М+Н]+ 310.
[0246] трет-Бутил-2-(2-(никотинамидо)этокси)этилкарбамат (140 мг, 0,453 ммоль) переносят в 25% ТФУ в CH2Cl2 (10 мл). Реакционную смесь оставляют при комнатной температуре на 2 час, после чего упаривают при сниженном давлении с получением соли ТФУ N-(2-(2-аминоэтокси)этил)никотинамида. Полученный материал далее переносят в CH3CN (10 мл) вместе с (4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаеновой кислотой (148 мг, 0,453 ммоль), ГАТУ (190 мг, 0,498 ммоль) и ДИЭА (0,24 мл). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 час. Далее ее разбавляют этилацетатом и промывают последовательно насыщенным водным раствором NaHCO3 и солевым раствором. Органическую фракцию сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (CH2Cl2/MeOH, 9:1) дает N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтокси)этил)никотинамид (75 мг, 31%). МС: вычислено для C31H46N2O5: 526,34; найдено [М+Н]+ 527.
Пример 7
Получение N-(2-((2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(метил)амино)этил)никотинамида (I-2)
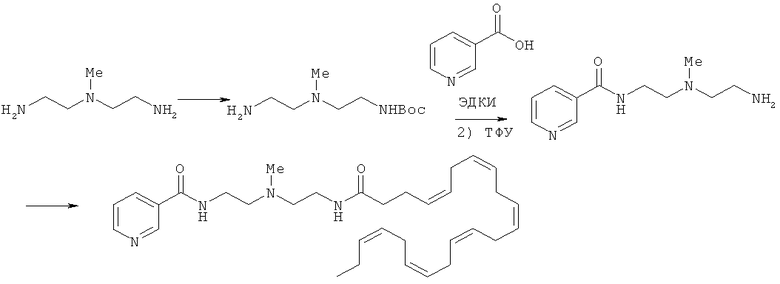
[0247] N1-(2-Aминoэтил)-N1-мeтилэтaн-1,2-диaмин (5,0 г, 42,7 ммоль) растворяют в CH2Cl2 (100 мл) и охлаждают до 0°С. Далее раствор Вос2O (0,93 г, 4,27 ммоль) в СН2Сl2 (10 мл) добавляют по каплям при температуре 0°С на протяжении 15 мин. Полученную реакционную смесь перемешивают при 0°С, выдерживая при этой температуре на протяжении 30 мин, после чего нагревают до комнатной температуры. После перемешивания при комнатной температуре в течение протяжении 2 час, реакционную смесь разбавляют CH2Cl2 (100 мл). Органическую фракцию промывают солевым раствором (3×25 мл), сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении с получением трет-бутил-2-((2-аминоэтил)(метил)амино)этилкарбамата (1,1 г).
[0248] трет-Бутил-2-((2-аминоэтил)(метил)амино)этилкарбамат (400 мг, 1,84 ммоль) переносят в CH3CN (10 мл) вместе с никотиновой кислотой (227 мг, 1,84 ммоль) и ЭДКИ (353 мг, 2,02 ммоль). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 18 час, после чего разбавляют этилацетатом. Органическую фракцию промывают насыщенным водным раствором NаНСО3, солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Полученный остаток очищают хроматографией на силикагеле (5% MeOH/CH2Cl2) с получением трет-бутил-2-(метил(2-(никотинамидо)этил)амино)этилкарбамата (180 мг, 30%). МС: вычислено для С16Н26Н4O3: 322,2; найдено [М+Н]+ 323.
[0249] трет-Бутил-2-(метил(2-(никотинамидо)этил)амино)этилкарбамат (90 мг, 0,279 ммоль) переносят в 25% раствор ТФУ в CH2Cl2 (5 мл) и оставляют при комнатной температуре на протяжении 3 час. Реакционную смесь упаривают при сниженном давлении с получением соли ТФУ N-(2-((2-аминоэтил)(метил)амино)этил)никотинамида. Полученный материал переносят в CH3CN (10 мл) вместе с (4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаеновой кислотой (90 мг, 0,279 ммоль), ГАТУ (117 мг, 0,31 ммоль) и ДИЭА (0,15 мл). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 час. Далее ее разбавляют этилацетатом и промывают последовательно насыщенным водным раствором NaHCO3 и солевым раствором. Органическую фракцию сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (5% MeOH/CH2Cl2) дает N-(2-((2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)(метил)амино)этил)никотинамид (30 мг, 20%). МС: вычислено для C33H48N4O2: 532,38; найдено [М+Н]+ 533.
Пример 8
Получение (2S,3R)-метил-3-((S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропаноилокси)-2-(никотинамидо)бутаноата (I-9)
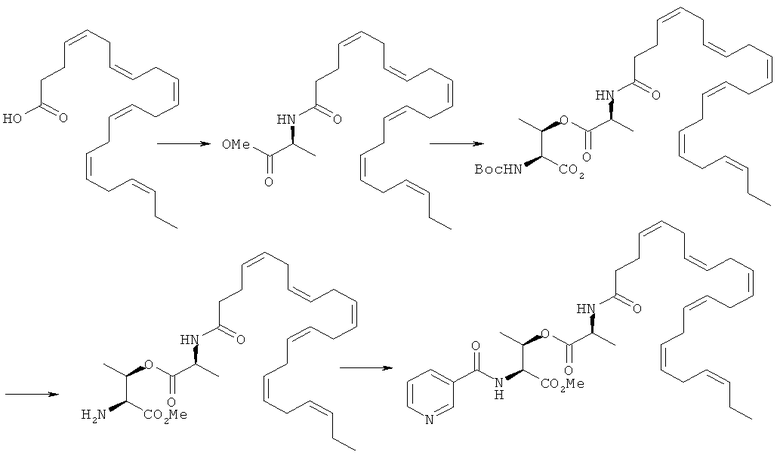
[0250] Гидрохлорид метилового эфира L-аланина (0,85 г, 6,1 ммоль) переносят в СН3СN (20 мл) вместе с (4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаеновой кислотой (2,0 г, 6,1 ммоль), ЭДКИ (1,3 г, 6,72 ммоль) и ДИЭА (1,3 мл). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 часов. Далее ее разбавляют этилацетатом, промывают разбавленным водным раствором NaНСО3 и солевым раствором. Органическую фракцию сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении с получением (S)-метил-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропаноата (2,0 г, 79%).
[0251] (S)-Метил-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропаноат (2,0 г, 4,8 ммоль) переносят в ТГФ (8 мл) вместе с 5 М водным раствором NaOH (5 мл), и энергично перемешивают при комнатной температуре на протяжении 3 час. Реакционную смесь разбавляют водой и упаривают при сниженном давлении. Далее прибавляют достаточное количество 6 н НСl до рН 2. Полученную смесь экстрагируют этилацетатом. Объединенные органические фракции сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении с получением (S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропановой кислоты, которую переносят в CH3CN (15 мл) вместе с метиловым эфиром N-Boc-L-треонина (1,11 г, 4,78 ммоль), ГАТУ (2,0 г, 5,3 ммоль) и ДИЭА (1,2 мл). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 6 час и разбавляют EtOAc. Органическую фракцию промывают NaHCO3, солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (CH2Cl2) дает (25,3R)-метил-2-(трет-бутоксикарбонил)-3-((S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропаноилокси)бутаноат (1,0 г).
[0252] (2S,3R)-Метил-2-(трет-бутоксикарбонил)-3-((S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропаноилокси)бутаноат (300 мг, 0,488 ммоль) переносят в 4 М НСl в диоксане (2 мл) и оставляют при комнатной температуре на 10 мин. Реакционную смесь далее разбавляют этилацетатом и упаривают при сниженном давлении с получением соли (2S,3R)-метил-2-амино-3-((S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропаноилокси)бутаноата НСl. Полученный материал переносят в CH3CN (5 мл) вместе с никотиновой кислотой (60 мг, 0,488 ммоль), ГАТУ (204 мг, 0,54 ммоль) и ДИЭА (0,25 мл, 1,46 ммоль). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 1 час и упаривают при сниженном давлении. Полученный маслянистый остаток очищают хроматографией на силикагеле (СН2Сl2/МеОН, 9:1) с получением (2S,3R)-метил-3-((S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропаноилокси)-2-(никотинамидо)бутаноата (120 мг, 40%). МС: вычислено для С36Н49N3О6: 619,36; найдено [М+Н]+ 620.
Пример 9
Получение (2S,3R)-метил-3-((S)-2-((5Z,8Z,11Z,14Z,17Z)-икоза-5,8,11,14,17-пентаенамидо)пропаноилокси)-2-(никотинамидо)бутаноата (I-10)
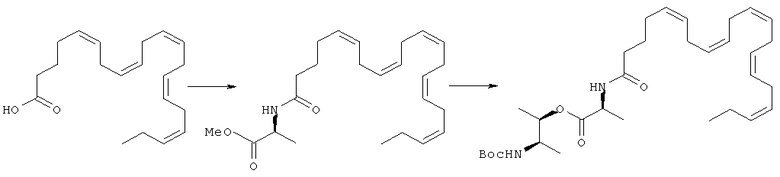
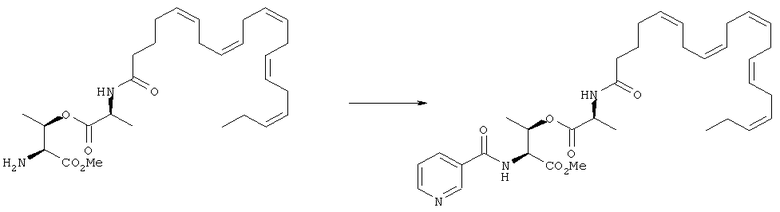
[0253] Применяют последовательность синтеза, идентичную описанной выше для получения (2S,3R)-метил-3-((S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)пропаноилокси)-2-(никотинамидо)бутаноата, за исключением использования (5Z,8Z,11Z,14Z,17Z)-докоза-5,8,11,14,17-пентаеновой кислоты (ЭПК) вместо ДГК. МС: вычислено для С34H47N3O6: 593,35; найдено [М+Н]+ 594.
Пример 10
Получение (S)-метил-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)гексаноата (I-11)
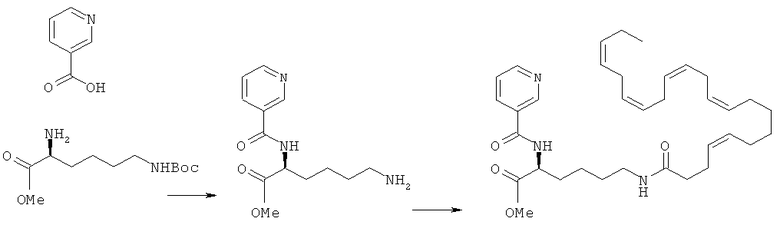
[0254] Н-Лизин-(ВОС)-ОМе гидрохлорид (500 мг, 1,68 ммоль) переносят в СН3СN (10 мл) вместе с никотиновой кислотой (207 мг, 1,68 ммоль), ЭДКИ (354 мг, 1,85 ммоль) и ДИЭА (0,90 мл). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 18 час и разбавляют этилацетатом. Органическую фракцию промывают разбавленным водным раствором NаНСО3, солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (СН3Сl2) дает (S)-метил-6-(трет-бутоксикарбонил)-2-(никотинамидо)гексаноат (520 мг, 85%).
[0255] (S)-Метил-6-(трет-бутоксикарбонил)-2-(никотинамидо)гексаноат (260 мг, 0,71 ммоль) переносят в 4 М НСl в диоксане (2 мл) и оставляют при комнатной температуре на 1 час. Реакционную смесь разбавляют этилацетатом и упаривают при сниженном давлении с получением соли (5)-метил-6-амино-2-(никотинамидо)гексаноата НСl. Полученный материал переносят в СН3СN (5 мл) вместе с (4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаеновой кислотой (233 мг, 0,71 ммоль), ГАТУ (297 мг, 0,78 ммоль) и ДИЭА (0,4 мл). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 час и разбавляют этилацетатом. Органическую фракцию промывают разбавленным водным раствором NaHCO3, солевым раствором, сушат над натрия сульфатом, фильтруют и упаривают при сниженном давлении. Очистка хроматографией на силикагеле (СН2Сl/МеОН, 9:1) дает (S)-метил-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)гексаноат (280 мг, 72%). МС: вычислено для C35H49N3O4: 575,37; найдено [М+Н]+ 576.
Пример 11
Получение (S)-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)гексановой кислоты (I-12)
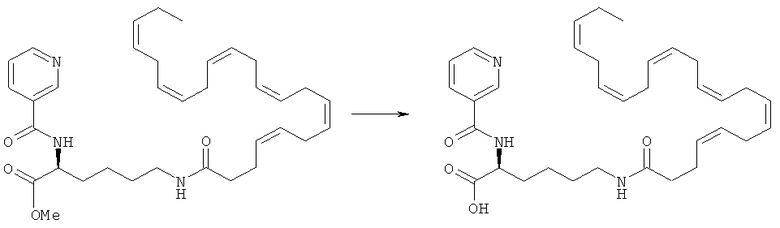
(S)-Метил-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)гексаноат (40 мг, 0,0695 ммоль) переносят в 2 мл тетрагидрофурана вместе с 80 мкл 5 М раствора NaOH. Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 час. Далее ее подкисляют до рН 4 с помощью 2 н НСl, после чего экстрагируют этилацетатом. Объединенные органические фракции сушат (Na2SO4) и упаривают при сниженном давлении с получением 31 мг (S)-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)гексановой кислоты. МС: вычислено для C34H47N3O4: 561,36; найдено [М+Н]+ 562.
Пример 12
Получение (S)-метил-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-6-(никотинамидо)гексаноата(I-13)
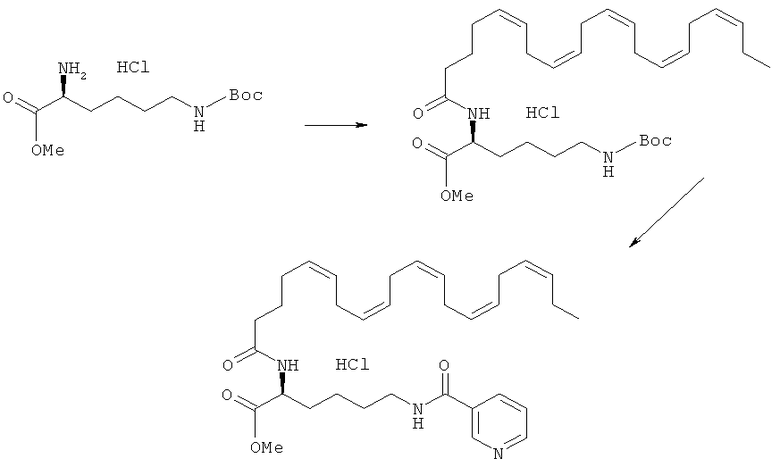
Н-Лизин-(ВОС)-ОМе гидрохлорид (500 мг, 1,68 ммоль) переносят в 25 мл CH3CN вместе с (5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаеновой кислотой (ЭПК, 509 мг, 1,68 ммоль), ГАТУ (702 мг, 1,85 ммоль) и ДИЭА (880 мкл, 5,04 ммоль). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 час. Далее ее разбавляют этилацетатом (70 мл) и промывают солевым раствором (20 мл). Органическую фракцию сушат (Na2SO4) и упаривают при сниженном давлении. Полученный остаток очищают хроматографией на силикагеле (CH2Cl2, элюация с градиентом до 90% CH2Cl2, 10% МеОН), с получением 870 мг (S)-метил-6-(трет-бутоксикарбонил)-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)гексаноата (выход 95%). МС: вычислено для C32H52N2O5: 544,39; найдено [М+Н]+ 545.
(S)-Метил-6-(трет-бутоксикарбонил)-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)гексаноат (870 мг, 1,60 ммоль) переносят в 4 мл 4 н НСl в диоксане и оставляют при комнатной температуре на протяжении 10 мин. Реакционную смесь разбавляют 10 мл этилацетата и упаривают при сниженном давлении с получением соли (S)-метил-6-амино-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)гексаноата НСl. Полученный остаток переносят в 5 мл CH3CN вместе с никотиновой кислотой (197 мг, 1,60 ммоль), ГАТУ (669 мг, 1,76 ммоль) и ДИЭА (836 мл, 4,8 ммоль). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 час и разбавляют этилацетатом (20 мл). Органическую фракцию промывают солевым раствором (20 мл), сушат (Na2SO4) и упаривают при сниженном давлении. Полученный остаток очищают хроматографией (95% СН2Сl2, 5% МеОН) с получением 300 мг (S)-метил-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-6-(никотинамидо)гексаноата. МС: вычислено для C33H47N3O4: 549,36; найдено [М+Н]+ 550.
Пример 13
Получение (S)-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-6-(никотинамидо)гексановой кислоты (I-14)
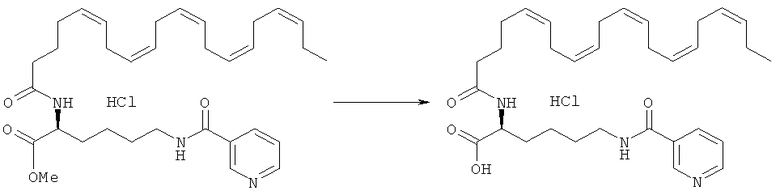
(S)-Mетил-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-6-(никотинамидо)гексаноат (140 мг, 0,225 ммоль) переносят в 2 мл тетрагидрофурана вместе с водным раствором NaOH (35 мг в 2 мл воды). Полученную реакционную смесь перемешивают при комнатной температуре на протяжении 2 часов. Далее ее подкисляют до рН 4 с помощью 2 н НСl, после чего экстрагируют этилацетатом. Объединенные органические фракции сушат (Na2SO4) и упаривают при сниженном давлении с получением 31 мг (S)-2-((5Z,8Z,HZ,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-6-(никотинамидо)гексановой кислоты. МС: вычислено для С34Н47N3O4: 561,36; найдено [М+Н]+ 562. МС: вычислено для С32Н45N3O4: 535,34; найдено [М+Н]+ 536.
[0256] Данное изобретение не ограничивается границами конкретных вариантов, описанных в примерах, которые предназначены для иллюстрации некоторых аспектов изобретения, и любые варианты, которые являются функционально эквивалентными, находятся в пределах данного изобретения. Напротив, разнообразные модификации изобретения, в добавление к показанным и описанным в данном описании, будут очевидными для специалистов в данной отрасли и находятся в пределах приложенной формулы изобретения.
ЭКВИВАЛЕНТЫ
[0257] Специалисты в данной отрасли распознают или смогут распознать, с использованием не более чем шаблонного экспериментирования, многочисленные эквиваленты конкретных вариантов, конкретно описанных в данном описании. Предусматривается, что такие эквиваленты включены в пределы приложенной формулы изобретения.
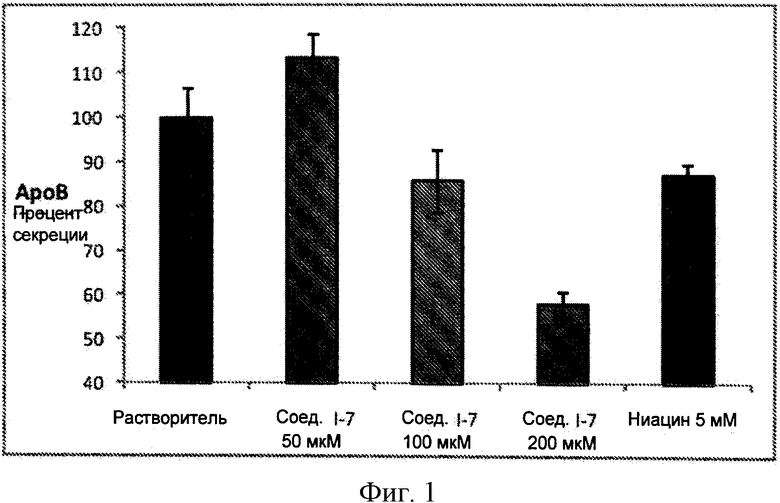
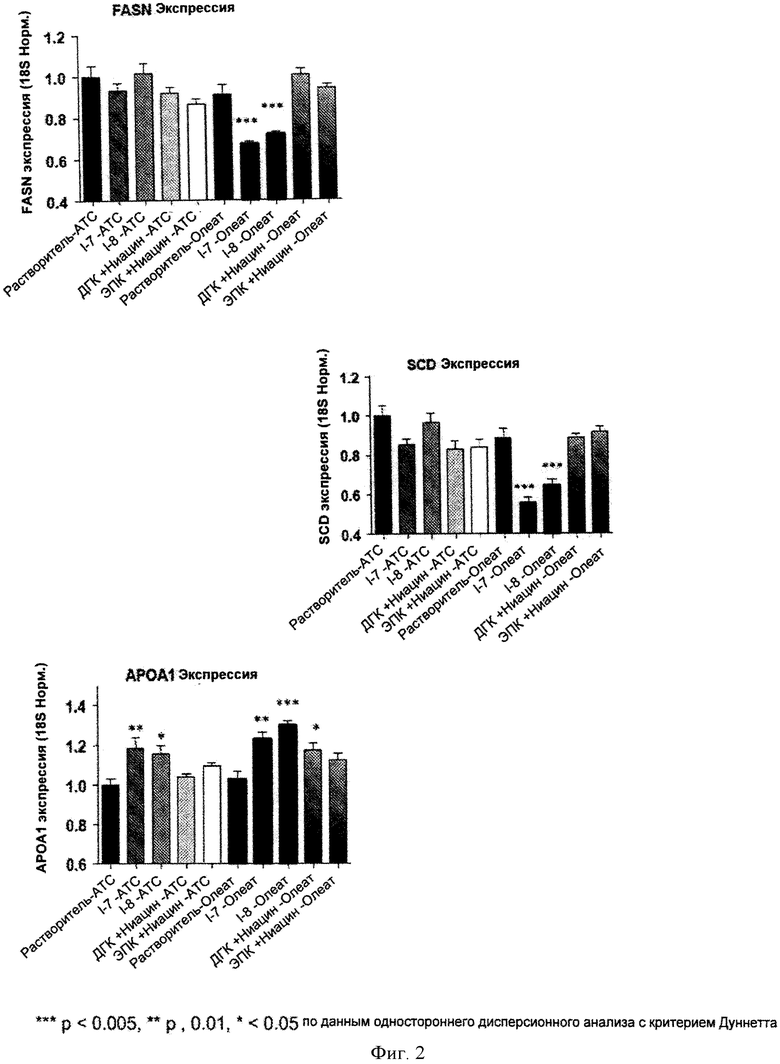
Изобретение относится к соединению формулы I:
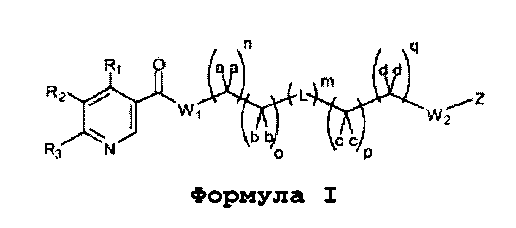
или его фармацевтически приемлемой соли, или стереоизомеру;
где каждый из R1; R2 и R3 независимо выбран из группы, состоящей из -Н, -D, -CI, -F и -С1-С3алкила; каждый из W1 и W2 представляет собой NR, или W1 и W2 вместе могут образовывать имидазолидиновую или пиперазиновую группу; каждый a, b, с и d независимо представляет собой -Н, -D, -СН3 или -С(О)OR, или два из а, b, с и d, вместе с одинарным атомом углерода, к которому они присоединены, могут образовывать циклоалкил; каждый n, о, р и q независимо равен 0 или 1; каждый L независимо представляет собой -О-,-S-,-S-S-, 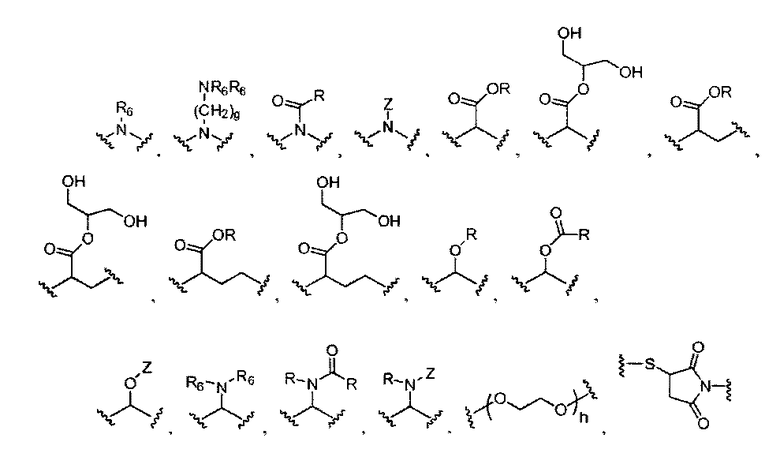
или
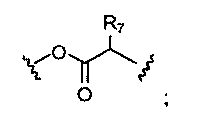
m равен 0 или 1; каждый R6 независимо представляет собой Н или С1-С6алкил; каждый R7 независимо представляет собой Н или неразветвленный или разветвленный С1-С10алкил; каждый Z независимо представляет собой
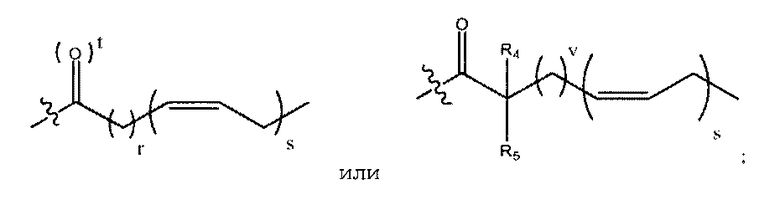
каждый r независимо равен 2, 3 или 7; каждый s независимо равен 3, 5 или 6; t равен 1; каждый v независимо равен 1 или 2; каждый из R4 и R5 независимо представляет собой водород, дейтерий или -С1-С4алкил; и каждый R независимо представляет собой -Н или -С1-С3алкил. Соединения могут быть использованы для лечения или профилактики метаболического расстройства. 3 н. и 35 з.п. ф-лы, 13 пр.
1. Соединение Формулы I:

или его фармацевтически приемлемая соль или стереоизомер;
где
каждый из R1; R2 и R3 независимо выбран из группы, состоящей из -Н, -D, -CI, -F и -С1-С3алкила;
каждый из W1 и W2 представляет собой NR или W1 и W2 вместе могут образовывать имидазолидиновую или пиперазиновую группу/
каждый a, b, c и d независимо представляет собой -Н, -D, -СН3 или -С(О)OR, или два из а, b, с и d, вместе с одинарным атомом углерода, к которому они присоединены, могут образовывать циклоалкил;
каждый n, о, р и q независимо равен 0 или 1;
каждый L независимо представляет собой -О-, -S- -S-S-,

или

m равен 0 или 1;
каждый R6 независимо представляет собой Н или С1-С6алкил;
каждый R7 независимо представляет собой Н или неразветвленный или разветвленный С1-С10алкил; каждый Z независимо представляет собой

каждый r независимо равен 2, 3 или 7;
каждый s независимо равен 3, 5 или 6;
t равен 1;
каждый v независимо равен 1 или 2;
каждый из R4 и R5 независимо представляет собой водород, дейтерий или -С1-С4алкил; и
каждый R независимо представляет собой -Н или -С1-С3алкил.
2. Соединение по п. 1, отличающееся тем, что Z представляет собой
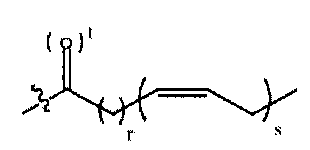
3. Соединение по п. 2, отличающееся тем, что t равно 1.
4. Соединение по п. 3, отличающееся тем, что r равно 2, и s равно 6.
5. Соединение по п. 3, отличающееся тем, что r равно 3, и s равно 5.
6. Соединение по п. 3, отличающееся тем, что r равно 7, и s равно 3.
7. Соединение по п. 4, отличающееся тем, что L представляет собой -S-S-
8. Соединение по п. 4, отличающееся тем, что L представляет собой -О-.
9. Соединение по п. 4, отличающееся тем, что L представляет собой
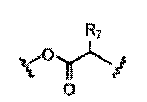
10. Соединение по п. 5, отличающееся тем, что L представляет собой
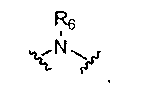
11. Соединение по п. 4, отличающееся тем, что L представляет собой
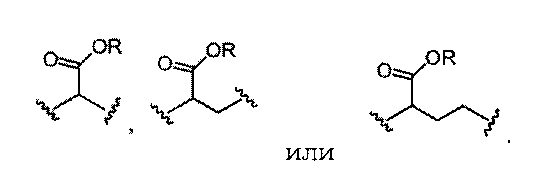
12. Соединение по п. 4, отличающееся тем, что каждый из n, о, р и q равен 1.
13. Соединение по п. 4, отличающееся тем, что два из n, о, р и q равны 1.
14. Соединение по п. 4, отличающееся тем, что каждый из W1 и W2 представляет собой NH.
15. Соединение по п. 4, отличающееся тем, что m равно 1, каждый из n, о, р и q равен 1, и L представляет собой О.
16. Соединение по п. 4, отличающееся тем, что m равно 1, каждый из n, о, р и q равен 1, и L представляет собой -S-S-.
17. Соединение по п. 4, отличающееся тем, что m равно 1, каждый из n и о равен 0, каждый из р и q равен 1, и L представляет собой
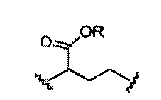
18. Соединение по п. 4, отличающееся тем, что m равно 1, каждый из n и о равен 1, каждый из р и q равен 0, и L представляет собой
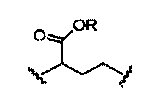
19. Соединение по п. 4, отличающееся тем, что m равно 1, каждый из n, о, р и q равен 1, и L представляет собой NR6.
20. Соединение по п. 4, отличающееся тем, что m равно 1, каждый из n и о равен 1, каждый из р и q равен 0, и L представляет собой
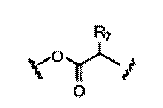
21. Соединение по п. 1, выбранное из группы, состоящей из N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидозтокси)этил)никотинамида; N-(2-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)дисульфанил)этил)никотинамида; и N-(2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтиламино)этил)никотинамида.
22. Соединение по п.1, выбранное из группы, состоящей из N-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13, 16, 19-гексаенамидоэтил)никотинамида; N-(2-(5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидоэтил)никотинамида; и N-(1-(4Z, 7Z, 10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо-2-метилпропан-2-ил)никотинамида.
23. Соединение по п. 1, выбранное из группы, состоящей из (S)-6-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-2-(никотинамидо)гексановой кислоты; (S)-2-((4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидо)-6-(никотинамидо)гексановой кислоты; (S)-6-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-2-(никотинамидо)гексановой кислоты; (S)-2-
((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-6-(никотинамидо)гексановой кислоты; и 2-(2-(4Z,7Z,10Z,13Z,16Z,19Z)-докоза-4,7,10,13,16,19-гексаенамидоэтил)-4-(никотинамидо)бутановой кислоты.
24. Соединение по п. 1, выбранное из группы, состоящей из (S)-((R)-1-(никотинамидо)пропан-2-ил)-2-((5Z,8Z,11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)пропаноата; и (S)-((R)-1-(никотинамид)пропан-2-ил) - 2-((5Z, 8Z, 11Z,14Z,17Z)-эйкоза-5,8,11,14,17-пентаенамидо)-3-мэтилбутаноата.
25. Соединение по п. 1, представляющее собой 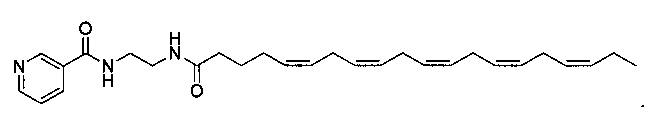
26. Соединение по п. 1, где m равно 0.
27. Соединение по п. 1, где каждый из n, о, р и q равен 1.
28. Соединение по п. 1, где каждые два из n, о, р и q равны 1.
29. Соединение по п. 1, где r равен 3, s равен 5 и каждые два из n, о, р и q равны 1.
30. Соединение по п. 1, где r равен 3, s равен 5 и каждый из W1 и W2 представляет собой NH.
31. Соединение по п. 1, где L представляет собой -S-S-
32. Соединение по п. 1, где L представляет собой -О-.
33. Соединение по п. 1, где L представляет собой
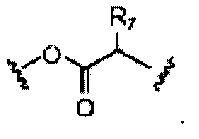
34. Соединение по п. 1, где L представляет собой NR6.
35. Соединение по п. 1, где L представляет собой 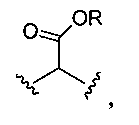
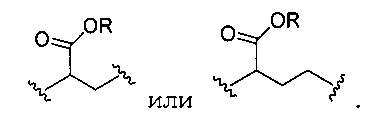
36. Фармацевтическая композиция, содержащая соединение по любому из пп. 1-35 и фармацевтически приемлемый носитель для лечения метаболического расстройства, выбранного из гипертриглицеридемии, гиперхолестеринемии, жирового заболевания печенки, атеросклероза, заболевания коронарных сосудов сердца, диабета 2 типа, диабетической нефропатии, диабетической невропатии, диабетической ретинопатии, метаболического синдрома или сердечно-сосудистого заболевания.
37. Способ лечения метаболического расстройства, включающий введение пациенту, который нуждается в таком лечении, эффективного количества соединения по любому из пп. 1-35, где метаболическое расстройство выбрано из гипертриглицеридемии, гиперхолестеринемии, жирового заболевания печени, атеросклероза, заболевания коронарных сосудов сердца, диабета 2 типа, диабетической нефропатии, диабетической невропатии, диабетической ретинопатии, метаболического синдрома или сердечно-сосудистого заболевания.
38. Способ по п. 37, где метаболическое расстройство представляет собой гипертриглицеридемию или гиперхолестеринемию.
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Очаг для массовой варки пищи, выпечки хлеба и кипячения воды | 1921 |
|
SU4A1 |
| Способ крашения тканей | 1922 |
|
SU62A1 |
| Прибор для подсчета сдачи при уплате денег | 1928 |
|
SU10802A1 |
Авторы
Даты
2015-11-20—Публикация
2010-08-31—Подача