Предпосылки изобретения
Люди выращивают кукурузу с целью получения продуктов питания и энергии. Насекомые поедают и повреждают растения кукурузы и тем самым подрывают эти усилия человека.
Современный трансгенный контроль этих вредителей в растении достигается за счет экспрессии в растении гена кристаллического (Cry) дельта-эндотоксина, кодирующего белок Cry1Fa Bacillus thuringiensis. Cry1Fa представляет собой белковый токсин, в настоящее время присутствующий в трансгенных семенах кукурузы марки HerculexTM Dow AgroSciences (Herculex, Herculex-Extra, и Herculex-RW), которые устойчивы к насекомым-вредителям FAW и ECB. Этот белок действует путем связывания со специфическим рецептором(ами), расположенным в кишечнике насекомых, и образует поры в клетках кишечника. Формирование этих пор мешает насекомым регулировать осмотический баланс, что приводит к их гибели.
Тем не менее, существует некоторое опасение, что насекомые могут быть в состоянии вырабатывать устойчивость к действию Cry1Fa благодаря генетическим изменениям рецепторов в своем кишечнике, которые связывают Cry1Fa. Насекомые, которые продуцируют рецепторы с пониженной способностью связывать Cry1Fa, могут быть устойчивы к активности Cry1Fa и поэтому выживать на растениях, которые экспрессируют этот белок.
С одним Cry-токсином, постоянно присутствующим в растении в условиях его роста, существует опасение, что насекомые могут приобрести устойчивость к активности этого белка благодаря генетическим изменениям рецептора, который связывается с токсином Cry1Fa в кишечнике насекомых. Уменьшение связывания токсина из-за этих изменений рецептора приведет к снижению токсичности Cry1Fa, возможно, ведущей в конечном итоге к снижению эффективности белка при экспрессии в сельскохозяйственной культуре.
КРАТКОЕ ОПИСАНИЕ
Настоящее изобретение относится, в частности, к комплектованию белка Cry1Ab и белка Cry2Aa, чтобы сделать растения (в частности, зерновые и кукурузу) более устойчивыми и менее подверженными тому, чтобы дать возможность развиваться насекомым, которые устойчивы к активности какого-либо из этих двух токсинов. Эти комплекты можно применять специфически против европейского кукурузного мотылька (ECB).
ПОДРОБНОЕ ОПИСАНИЕ
Настоящее изобретение относится, в частности, к комплектованию инсектицидного белка Cry1Ab и инсектицидного белка Cry2Aa, чтобы сделать растения (в частности, зерновые и кукурузу) более устойчивыми и менее подверженными тому, чтобы дать возможность развиваться насекомым, которые устойчивы к активности какого-либо из этих двух токсинов. Эти комплекты можно применять специфически против европейского кукурузного мотылька (ECB; Ostrinia nubilalis).
Настоящее изобретение также относится, в частности, к тройным комплектам или «пирамидам» из трех (или более) белковых токсинов, с белком Cry1Ab и белком Cry2Aa, составляющими основную пару. (Под «раздельными участками воздействия» подразумевается, что любой из данных белков не вызывает перекрестной устойчивости друг с другом). Добавление третьего белка, который нацелен против ECB, может обеспечить белок с третьим участком воздействия против ECB. В некоторых предпочтительных вариантах осуществления, третий белок может быть выбран из группы, состоящей из DIG-3 (смотри US 2010-00269223), Cry1I, Cry1Be, Cry2Aa и Cry1Fa. Смотри, например, USSN 61/284278, поданную 16 декабря 2009 года. Смотри также US 2008-0311096.
Таким образом, в некоторых предпочтительных вариантах осуществления выбранные токсины обладают тремя раздельными участками воздействия против ECB. Опять же, предпочтительные «многоуровневые» комбинации представляют собой пару белков плюс третий IRM-белок по изобретению.
Пары и/или тройные комплекты (активные в отношении ECB) по изобретению также можно комбинировать с дополнительными белками - для нацеливания, например, против травяной совки (FAW). Такие белки могут включать, например, Vip3, Cry1C, Cry1D и/или Cry1E. CryBe и/или Cry1Fa может также применять для нацеливания против FAW и ECB.
Для получения последовательностей любых генов и белков, раскрытых или упомянутых в настоящем документе, можно использовать GENBANK. Смотри Приложение А.
Настоящее изобретение также относится к трем инсектицидным белкам (белки Cry в некоторых предпочтительных вариантах осуществления), которые активны в отношении отдельных вредителей-мишеней, но не приводят к перекрестной устойчивости друг против друга.
Растения (и участок, засаженный этими растениями), которые продуцируют эти три (как минимум) токсина, включены в область охвата настоящего изобретения. Можно также добавить дополнительные токсины/гены, но эти специфические тройные комплекты, в соответствии с настоящим изобретением, могли бы выгодно и неожиданно обеспечить три участка воздействия против ECB.
Пары или тройные комплекты (и/или комбинации дополнительных белков) по настоящему изобретению могут помочь уменьшить или ликвидировать требования для рефугийного участка (например, менее 40%, менее 20%, меньше чем 10%, менее 5%, или даже 0% рефугия). Поэтому засеянное таким образом поле площадью более 10 акров включено в настоящее изобретение. Полинуклеотид(ы) по изобретению, предпочтительно, находится в генетической конструкции под контролем промотора(ов), отличного от промотора(ов) Bacillus thuringiensis. Полинуклеотиды по изобретению могут содержать кодоны для увеличения экспрессии в растении.
Для того чтобы противодействовать способности насекомых вырабатывать устойчивость к белку Cry, авторы идентифицировали Cry-токсины, которые неконкурентно связываются с белковыми рецепторами в пищеварительной системе ECB. Было обнаружено, что Cry1Ab не вытесняет Cry2Aa, связанный с рецепторами, расположенными в кишечнике личинок насекомого ECB.
Авторы обнаружили, что Cry2Aa и Cry1Ab являются токсичными для личинок ECB, но все же они не в полной мере взаимодействуют с одним и тем же рецепторным участком(ами); это показывает, что их токсичность не будет подвергаться перекрестной устойчивости в ECB.
Таким образом, насекомые с развившейся устойчивостью к Cry1Ab будут по-прежнему чувствительны к токсичности Cry2Aa-белков, например, тех, которые связываются с альтернативными рецепторными участками. Авторы получили биохимические данные, которые подтверждают это. Комбинация этих белков, экспрессированных в трансгенных растениях, обеспечивает полезный и ценный механизм снижения вероятности развития устойчивости насекомых в поле и, таким образом, приводит к снижению требований для рефугиев. Данные, описанные в настоящем документе ниже, демонстрируют, что Cry2Aa-белок взаимодействует с отдельным по сравнению с Cry1Ab участком(ами)-мишенью в кишечнике насекомого, и поэтому может стать отличным партнером по комплектации.
Если устойчивость наступала благодаря изменениям в аффинности рецепторов кишечника насекомого, которые связываются с Cry-токсинами, изменения должны были произойти по крайней мере в двух различных рецепторах одновременно, чтобы дать возможность насекомым выжить на растениях, экспрессирующих несколько белков. Вероятность такого события крайне мала, что увеличивает, таким образом, устойчивость трансгенного продукта к защите от насекомых, обладающих способностью развития толерантности к белкам.
Авторы метили белок Cry1Ab радиоактивным йодом и использовали способы анализа радиорецепторного связывания для определения их связывания с предполагаемыми рецепторными белками, расположенными в мембранах кишечника насекомого. Мембраны кишечника подготавливали как мембранные везикулы щеточной каймы (BBMV) способом Волферсбергера. Иодирование токсинов проводили с использованием либо Iodo-Beads или обработанных пробирок Iodo-gen от Pierce Chemicals. Удельная активность радиоактивно меченного токсина составляла приблизительно 1-4 мкКи/мкг белка. Исследования по связыванию проводили, в основном, при помощи методики Лян (1995).
Данные, представленные в настоящем документе, показывают, что токсины воздействуют на отдельный по сравнению с Cry1Ab участок-мишень в кишечнике насекомых и, таким образом, могли бы стать отличными партнерами по комплектации.
Настоящее изобретение можно применять с множеством растений. Примеры включают зерновые (кукурузу), сою и хлопок.
Гены и токсины, пригодные в соответствии с настоящим изобретением, включают не только раскрытые полноразмерные последовательности, но также фрагменты этих последовательностей, варианты, мутанты и слитые белки, которые сохраняют характерную пестицидную активность токсинов, специфически представленных в настоящем документе. Как используется в настоящем документе, термины «варианты» или «вариации» генов относятся к нуклеотидным последовательностям, которые кодируют те же токсины или которые кодируют эквивалентные токсины, обладающие пестицидными активностями. Как используется в настоящем документе, термин «эквивалентные токсины» относится к токсинам, обладающим такой же или, по существу, такой же биологической активностью в отношении вредителей-мишеней, что и заявленные токсины.
Как используется в настоящем документе, границы составляют приблизительно 95% (например, Cry1Ab и Cry2Aa), 78% (например, Cry1A и Cry2A) и 45% (Cry1 и Cry2) идентичности последовательностей, согласно «Revision of the Nomenclature for the Bacillus thuringiensis Pesticidal Crystal Proteins», N. Crickmore, D.R. Zeigler, J. Feitelson, E. Schnepf, J. Van Rie, D. Lereclus, J. Baum, and D.H. Dean. Microbiology and Molecular Biology Reviews (1998) Vol 62: 807-813. Эти уровни можно также применять только для основных белков.
Фрагменты и эквиваленты, которые сохраняют пестицидную активность типичных токсинов, находятся в границах настоящего изобретения. Кроме того, в силу вырожденности генетического кода множество последовательностей ДНК могут кодировать аминокислотные последовательности, раскрытые в настоящем документе. Это находится в пределах компетенции специалиста в области создания таких альтернативных последовательностей ДНК, кодирующих такие же или, по существу, такие же токсины. Эти варианты последовательностей ДНК находятся в рамках настоящего изобретения. Как используется в настоящем документе, ссылка на «по существу, такая же» последовательность относится к последовательностям, которые имеют аминокислотные замены, делеции, добавления или вставки, которые существенно не влияют на пестицидную активность. Фрагменты генов, кодирующих белки, которые сохранили пестицидную активность, также включены в это определение.
Еще одним способом идентификации генов, кодирующих токсины, и частей генов, полезных в соответствии с настоящим изобретением, является способ с использованием олигонуклеотидных зондов. Эти зонды являются детектируемыми нуклеотидными последовательностями. Эти последовательности можно определить посредством соответствующей метки или можно сделать флуоресцентными по своей природе, как описано в Международной заявке No. WO93/16094. Как известно в данной области, если молекула зонда и образец нуклеиновой кислоты гибридизуются, образуя прочную связь между двумя молекулами, можно резонно предположить, что зонд и образец имеют значительную гомологию. Предпочтительно, гибридизация проводится в жестких условиях при помощи способов, известных в данной области, как описано, например, в Keller, G. H., M. M. Manak (1987) DNA Probes, Stockton Press, New York, N.Y., pp. 169-170. Далее представлены некоторые примеры концентраций соли и температурных условий (в порядке увеличения жесткости): 2X SSPE или SSC при комнатной температуре; 1X SSPE или SSC при 42ºC; 0,1X SSPE или SSC при 42ºC; 0,1X SSPE или SSC при 65ºC. Детектирование зонда предоставляет средства для определения известным способом, произошла ли гибридизация. Такой зондовый анализ предоставляет быстрый способ определения генов, кодирующих токсин, по настоящему изобретению. Нуклеотидные сегменты, которые используются в качестве зондов в соответствии с изобретением, могут быть синтезированы с использованием ДНК-синтезатора и стандартных процедур. Эти нуклеотидные последовательности можно также использовать в качестве ПЦР-праймеров, чтобы амплифицировать гены по настоящему изобретению.
Определенные белки по настоящему изобретению подробно рассмотрены в настоящем изобретении. Поскольку эти белки являются просто типичными белками по изобретению, то должно быть очевидно, что настоящее изобретение включает вариантные или эквивалентные белки (и нуклеотидные последовательности, кодирующие эквивалентные белки) с пестицидной активностью, такой же или сходной с пестицидной активностью типичного белка. Эквивалентные белки должны иметь аминокислотную гомологию с типичным белком. Эта аминокислотная идентичность, как правило, должна быть больше чем 75%, больше чем 90% и может быть больше чем 91, 92, 93, 94, 95, 96, 97, 98 или 99%. Аминокислотная идентичность будет наиболее высокой в критических областях белка, которые ответственны за биологическую активность или вовлечены в установление пространственной конфигурации, которая, в конечном счете, отвечает за биологическую активность. При этом некоторые аминокислотные замены являются приемлемыми и можно ожидать, что эти замены находятся в областях, которые не являются критическими для активности или являются консервативными аминокислотными заменами, которые не влияют на трехмерную структуру молекулы. Например, аминокислоты можно отнести к следующим классам: неполярных, незаряженных полярных, основных и кислых аминокислот. Консервативные замены, при которых аминокислота одного класса заменяется другой аминокислотой того же типа, находятся в границах настоящего изобретения, при условии, что замена существенным образом не меняет биологической активности соединения. Ниже приведен список примеров аминокислот, принадлежащих к каждому классу. В некоторых случаях, также можно делать неконсервативные замены. Критическим фактором является то, что эти мутации не должны существенно уменьшать биологическую активность белка.
Трансформация растений. Предпочтительным рекомбинантным хозяином для продуцирования инсектицидных белков по настоящему изобретению является трансформированное растение. Гены, кодирующие белки Bt-токсина, как раскрыто в настоящем документе, могут быть встроены в клетки растений с использованием разнообразных способов, которые хорошо известны в данной области. Например, большое количество векторов для клонирования, содержащих систему репликации в Escherichia coli и маркер, который позволяет проводить селекцию трансформированных клеток, доступны для подготовки к введению чужеродных генов в высшие растения. Векторы включают, например, pBR322, серии pUC, серии M13mp, pACYC184, в частности. Соответственно, фрагмент ДНК, имеющий последовательность, кодирующую белок Bt-токсина, можно встраивать в вектор по подходящему сайту рестрикции. Полученную в результате плазмиду используют для трансформации в E. coli. Клетки E. coli культивируют в подходящей питательной среде, а затем собирают и лизируют. Плазмиду выделяют. Анализ последовательности, рестрикционный анализ, электрофорез и другие биохимические, молекулярно-биологические способы, как правило, проводят как способы анализа. После каждой манипуляции, используемую последовательность ДНК можно расщеплять и присоединять к следующей последовательности ДНК. Каждая плазмидная последовательность может быть клонирована в ту же или другие плазмиды. В зависимости от способа встраивания нужных генов в растение, могут быть необходимы другие последовательности ДНК. Если, например, для трансформации растительной клетки используется плазмида Ti и Ri, то, по крайней мере, правая граница, а часто, правая и левая границы Т-ДНК плазмиды Ti и Ri должны быть соединена как фланкирующая область генов, который следует вставить. Использование Т-ДНК для трансформации растительных клеток было интенсивно исследовано и достаточно описано в EP 120 516, Lee and Gelvin (2008), Hoekema (1985), Fraley et al., (1986), and An et al., (1985), и является принятым в данной области.
После того как встроенная ДНК была интегрирована в геном растения, она является относительно стабильной. Трансформационный вектор обычно содержит селективный маркер, который придает трансформированным клеткам растений устойчивость к биоциду или антибиотику, такому как Bialaphos, канамицин, G418, блеомицин или гигромицин, в частности. Индивидуально действующий маркер, соответственно, должен давать возможность селектировать трансформированные клетки, а не клетки, которые не содержат встроенной ДНК.
Для встраивания ДНК в растительную клетку-хозяин доступно большое количество способов. Эти способы включают в себя трансформацию Т-ДНК, используя Agrobacterium tumefaciens или Agrobacterium rhizogenes в качестве трансформационного агента, слияние, инъекции, биолистику (бомбардировка микрочастицами) или электропорацию, а также другие возможные способы. Если для трансформации используются Agrobacteria, предназначенную для встраивания ДНК необходимо клонировать в специальные плазмиды, а именно либо в промежуточный вектор, либо в бинарный вектор. Промежуточные векторы могут быть интегрированы в плазмиду Ti или Ri при помощи гомологичной рекомбинации благодаря последовательностям, гомологичным последовательностям в Т-ДНК. Плазмида Ti или Ri также содержит vir-область, необходимую для передачи Т-ДНК. Промежуточные векторы не могут самостоятельно реплицироваться в Agrobacteria. Промежуточные векторы можно передать в Agrobacterium tumefaciens посредством плазмиды-хелпера (конъюгация). Бинарные векторы могут самостоятельно реплицироваться как в E. coli, так и в Agrobacteria. Они содержат ген селективного маркера и линкер или полилинкер, который ограничен правой и левой граничными областями Т-ДНК. Они могут быть трансформированы непосредственно в Agrobacteria (Holsters et al., 1978). Agrobacterium, использованные в качестве клетки-хозяина, должны содержать плазмиду, несущую vir-область. Vir-область необходима для передачи Т-ДНК в клетки растений. Могут содержаться дополнительные Т-ДНК. Таким образом, трансформированные бактерии используются для трансформации клеток растений. Эксплантаты растений можно успешно выращивать с Agrobacterium tumefaciens или Agrobacterium rhizogenes для передачи ДНК в клетки растений. Целые растения затем можно регенерировать из инфицированного растительного материала (например, кусочки листьев, сегменты стебля, корней, а также протопласты или культивируемые в суспензии клетки) в подходящей среде, которая может содержать антибиотики или биоциды для селекции. Полученные таким образом растения затем можно проверить на наличие встроенной ДНК. В случае инъекции и электропорации никаких специальных манипуляций с плазмидами не осуществляют. Можно использовать исходные плазмиды, такие как, например, производные pUC.
Трансформированные клетки выращивают внутри растения обычным образом. Они могут образовывать половые клетки и передавать трансформированный признак(и) растениям-потомкам. Такие растения можно выращивать обычным образом и скрещивать с растениями, имеющими такие же трансформированные наследственные факторы или иные наследственные факторы. Полученные в результате гибридные особи обладают соответствующими фенотипическими свойствами.
В предпочтительном варианте осуществления настоящего изобретения, растения трансформируют генами, у которых коэффициент использования кодонов был оптимизирован для растений. Смотри, например, Патент США No. 5380831, который включен в настоящее описание посредством ссылки. Хотя некоторые укороченные токсины приведены в настоящем документе, в Bt-области известно, что токсины типа 130 кДа (полноразмерные) содержат N-концевую половину, которая представляет собой основной токсин, и C-концевую половину, которая представляет собой «хвост» протоксина. Таким образом, соответствующие «хвосты» можно использовать с укороченными/основными токсинами по настоящему изобретению. Смотри, например, Патент США No. 6218188 и Патент США No. 6673990. Кроме того, способы создания синтетических Bt-генов для использования в растениях известны в данной области (Stewart and Burgin, 2007). Одним неограничивающим примером предпочтительного трансформированного растения является плодовитое растение кукурузы, содержащее экспрессируемый в растении ген, кодирующий белок Cry1Da, а также содержащее второй экспрессируемый в растении ген, кодирующий белок Cry1Be.
Перенос (или интрогрессию) определяемого Cry1Da и Cry1Be признака(ов) в инбредные линии кукурузы можно достичь путем периодического отбора, селекции, например, при помощи обратного скрещивания. В этом случае, необходимый рекуррентный родитель сначала скрещивают с донорным инбредом (нерекуррентным родителем), который несет соответствующий ген(ы) для определяемых Cry1D- и Cry1C признаков. Затем проводят возвратное скрещивание потомства этого скрещивания с рекуррентным родителем с последующей селекцией в образуемом потомстве на желаемый признак(и), который передается от нерекуррентного родителя. После трех, предпочтительно четырех, более предпочтительно пяти или более поколений возвратных скрещиваний с рекуррентным родителем с селекцией на желаемый признак(и), потомство будет гетерозиготным по локусу, контролирующему передаваемый признак(и), но будет похоже на рекуррентного родителя по большинству или почти всем другим генам (смотри, например, Poehlman & Sleper (1995) Breeding Field Crops, 4th Ed., 172-175; Fehr (1987) Principles of Cultivar Development, Vol.1 : Theory and Technique, 360-376).
Стратегии борьбы с устойчивостью насекомых (IRM). Roush et al., например, описывает двухтоксинные стратегии, также называемые «пирамидированием» или «комплектованием», для агротехники инсектицидных трансгенных культур (The Royal Society. Phil. Trans. R. Soc. Lond. B. (1998) 353, 1777-1786).
На своем сайте Агентство по охране окружающей среды США (epa.gov/oppbppd1/biopesticides/pips/bt_corn_refuge_2006.htm) публикует следующие требования для обеспечения нетрансгенных (т.е., не содержащих B.t.) рефугиев (раздел Bt-несодержащих сельскохозяйственных культур и кукурузы) для использования с трансгенными сельскохозяйственными культурами, продуцирующими один Bt-белок, активный в отношении вредителей-мишеней.
«Специфические структурные требования для продуктов из Bt(Cry1Ab или Cry1F)-кукурузы, защищенной от кукурузного мотылька, представляют собой следующие:
Структурные рефугии: 20% рефугия кукурузы, не содержащей Bt против чешуекрылых, в кукурузном поясе;
50% рефугия, не содержащего Bt против чешуекрылых, в поясе хлопчатника
Блоки
Внутренний (т.е., в Bt-поле)
Внешние (т.е., отдельные поля в пределах 1/2 мили (1/4 мили, если возможно) Bt-поля для того, чтобы максимизировать случайное скрещивание)
Полосы в поле
Полосы должны представлять собой не менее 4 борозд в ширину (предпочтительно, 6 борозд), чтобы снизить эффект от движения личинок
Кроме того, Национальная ассоциация кукурузоводов на своем сайте:(ncga.com/insect-resistance-management-fact-sheet-bt-corn) также предоставляет аналогичные руководства в отношении требований к рефугиям. Например:
«Требования для IRM от кукурузного мотылька:
- засадить по крайней мере 20% от ваших акров с кукурузой рефугийными гибридами;
- в регионах, производящих хлопок, рефугий должен составлять 50%;
- должно быть посажено в пределах 1/2 мили рефугийных гибридов;
- рефугий можно высадить полосами в пределах Bt-поля; рефугийные полосы должны быть не менее 4 борозд в ширину;
- рефугий можно обрабатывать традиционными пестицидами только в случае, если экономические границы достигают насекомых-мишеней;
- поддающиеся разбрызгиванию инсектициды на основе Bt не могут применяться на рефугийной кукурузе;
- соответствующий рефугий должен быть посажен на каждой ферме с Bt-кукурузой».
Как указано в Roush et al. (правая колонка на страницах 1780 и 1784, например), комплектование или «пирамидирование» из двух различных белков, каждый из которых эффективен против вредителей-мишеней и с небольшой или отсутствием перекрестной устойчивости, может позволить использование меньшего рефугия. Рош предполагает, что для успешного комплекта рефугийный размер менее 10% рефугия может обеспечить агротехнику с сопоставимой устойчивостью для около 50% рефугия для одного («немногоуровневого») признака. Для доступных в настоящее время продуктов «многоуровневой» Bt-кукурузы Агентство по защите окружающей среды США требует, чтобы было посажено значительно меньше (обычно 5%) структурированного рефугия не содержащей Bt кукурузы, чем для продуктов с одним признаком (обычно 20%).
Существуют различные способы обеспечения IRM-эффектов рефугия, включая различные геометрические схемы посадки в полях (как упоминалось выше) и упакованные семенные смеси, как дополнительно отмечается в Roush et al. (выше) и Патенте США No. 6551962.
Указанные выше проценты, или аналогичные коэффициенты рефугиев, могут быть использованы для рассматриваемых двойных или тройных комплектов или пирамид. Для тройных комплектов с тремя участками воздействия против одного вредителя-мишени целью был бы нулевой рефугий (или менее чем 5%-рефугий, например). Это особенно верно для коммерческих площадей - более 10 акров, например.
Все патенты, заявки на патенты, предварительные заявки и публикации, упомянутые или цитируемые в настоящем описании, включены посредством ссылки в полном объеме в той мере, пока они не являются несовместимыми с конкретными идеями данной спецификации.
За исключением случаев, когда это специально оговорено или следует из контекста, грамматические формы единственного числа следует понимать как означающие “по крайней мере один”.
Ниже приводятся примеры, иллюстрирующие процедуры для практикующих изобретение. Эти примеры не следует истолковывать в качестве ограничивающих. Все процентные соотношения приводятся по массе и все пропорции смесей растворителей - по объему, если не указано иное. Все температуры в градусах Цельсия.
ПРИМЕРЫ
Пример 1. 125 I-мечение белков Cry
Иодирование Cry-токсинов. Очищенные усеченные Cry-токсины йодировали с помощью Iodo-Beads или Iodo-gen (Pierce). Вкратце, два Iodo-Bead промывали два раза 500 мкл забуференного фосфатом солевого раствора PBS (20 мМ фосфата натрия, 0,15 М NaCl, рН 7,5) и помещали в 1,5-мл центрифужную пробирку за свинцовой защитой. К этому прибавляли еще 100 мкл PBS. За защитой и при использовании надлежащих приемов обращения с радиоактивностью, 0,5 мкКи Na125I (17,4 Ки/мг, Lot 0114, Amersham) добавляли к раствору PBS с Iodo-Beads. Компонентам была предоставлена возможность реагировать в течение 5 минут при комнатной температуре, затем 2-25 мкг высокоочищенного укороченного Cry-белка добавляли в раствор и давали возможность реагировать в течение еще 3-5 минут. Реакцию прекращали удалением раствора от Iodo-Beads и нанесением его на 0,5-мл обессоливающую колонку Zeba spin (InVitrogen), уравновешенную PBS. Каждый из Iodo-Bead промывали два раза по 10 мкл PBS и промывочный раствор также наносили на обессоливающую колонку. Радиоактивный раствор элюировали через обессоливающую колонку путем центрифугирования при 1000 x g в течение 2 мин. С помощью этой процедуры, Cry-токсин в 100 мМ фосфатном буфере (pH 8) сначала очищали от липополисахаридов (LPS) путем его пропускания несколько раз через небольшую 0,5-мл полимиксиновую колонку. К пробирке с Iodo-gen (Pierce Chem. Co.) добавляли 20 мкг не содержащего LPS Cry1Da-токсина, затем 0,5 мкКи Na125I. Реакционную смесь встряхивали в течение 15 мин при 25ºC. Раствор удаляли из пробирки и добавляли 50 мкл 0,2 М нерадиоактивно меченного NaI, чтобы подавить реакцию. Белок диализовали против PBS с 3 сменами буфера для полного удаления несвязанного 125I.
Радио-чистоту йодированных Cry-белков определяли при помощи электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия (SDS-PAGE), образования изображения в фосфоимеджере и гамма-радиометрии. Вкратце, 2 мкл радиоактивного белка разделяли при помощи SDS-PAGE. После разделения гели высушивали с помощью прибора BioRad для сушки гелей в соответствии с инструкциями производителя. Высушенные гели визуализировали путем заворачивания их в пленку Mylar (12 мкм в толщину) и выдерживания их под экраном Molecular Dynamics storage phosphor screen (35 см×43 см) в течение 1 часа. Пластины проявляли с помощью фосфоимеджера Molecular Dynamics Storm 820 и изображение анализировали с использованием программного обеспечения ImageQuantTM. Радиоактивную полосу вместе с областями, расположенными непосредственно выше и ниже полосы, вырезали из геля с помощью лезвия и подсчитывали в гамма-счетчике. Радиоактивность детектировалась только в полосе Cry-белка и в областях ниже полосы. Выше полосы никакой радиоактивности не детектировалось, что указывает на то, что все радиоактивное загрязнение состоит из меньших белковых компонентов, чем укороченный Cry-белок. Эти компоненты, скорее всего, представляют собой продукты деградации.
Пример 2. Протокол подготовки BBMV
Подготовка и фракционирование растворимых BBMV. Личинки Spodoptera frugiperda, Ostrinia nubilalis или Heleothis zea поздней возрастной стадии подвергали голоданию в течение ночи, а затем утром рассекали после охлаждения на льду в течение 15 минут. Ткань средней кишки удаляли из полости тела, оставляя сзади заднюю кишку, прикрепленную к кожным покровам. Среднюю кишку помещали в 9X объем охлажденного во льду буфера для гомогенизации (300 мМ маннитол, 5 мМ EGTA, 17 мМ Трис-основание, рН 7,5) с добавлением Protease Inhibitor Cocktail (конечная концентрация компонентов коктейля (в мкМ) составляет AEBSF (500), EDTA (250 мМ), Бестатин (32), Е-64 (0,35), лейпептин (0,25), апротинин (0,075)) (Sigma P-2714) в разведении, рекомендованном поставщиком. Ткань гомогенизировали за 15 ходов стеклянного гомогенизатора для ткани. BBMV подготавливали способом MgCl2-преципитации Wolfersberger (1993). Вкратце, равный объем 24 мМ раствора MgCl2 в 300 мМ маннитоле смешивали с гомогенатом среднего кишечника, перемешивали в течение 5 минут и оставляли на льду в течение 15 мин. Раствор центрифугировали при 2500 x g в течение 15 мин при 4ºC. Супернатант сохраняли и осадок суспендировали в исходном объеме 0,5-х разведенного буфера для гомогенизации и центрифугировали снова. Два супернатанта объединяли, центрифугировали при 27000 x g в течение 30 мин при 4ºC для образования фракции BBMV. Осадок суспендировали в 10 мл буфера для гомогенизации с добавлением ингибиторов протеаз и центрифугировали снова при 27000 x g в течение 30 мин при 4ºC для промывки BBMV. Полученный в результате осадок суспендировали в буфере для хранения BBMV (10 мМ HEPES, 130 мМ KC1, 10% глицерин, pH 7,4) до концентрации примерно 3 мг/мл белка. Концентрацию белка определяли с помощью способа Брэдфорда (1976) с бычьим сывороточным альбумином (BSA) в качестве стандарта. Определение щелочной фосфатазы проводили перед замораживанием образцов с помощью теста от Sigma, следуя инструкциям производителя. Удельная активность этого маркерного фермента во фракции BBMV, как правило, увеличивается в 7 раз по сравнению с тем, что обнаруживается для фракции гомогената среднего кишечника. Фракцию BBMV распределяли по аликвотам в образцы 250 мкл, быстро замораживали в жидком азоте и хранили при -80ºC.
Пример 3. Способ определения связывания 125 I-белков Cry с белков BBMV
Связывание 125 I-белков Cry с BBMV. Для определения оптимального количества белка BBMV для использования в анализах по связыванию была построена кривая насыщения. Радиоактивно меченый 125I белок Cry (0,5 нМ) инкубировали в течение 1 часа при 28ºC с разными количествами белка BBMV в диапазоне от 0 до 500 мкг/мл в буфере для связывания (8 мМ NaHPO4, 2 мМ H2PO4, 150 мМ NaCl, 0,1% бычьего сывороточного альбумина, pH 7,4). Общий объем составлял 0,5 мл. Связанный с 125I Cry-белок отделяли от несвязанного путем отбора 150 мкл реакционной смеси в трех повторностях из 1,5-мл центрифужной пробирки в 500-мкл центрифужную пробирку и центрифугирования образцов при 14000 x g в течение 6 минут при комнатной температуре. Супернатант аккуратно отбирали и осадок аккуратно промывали три раза охлажденным во льду буфером для связывания. Нижнюю часть центрифужной пробирки, содержащую осадок, отделяли и помещали в стеклянную пробирку для культивирования размером 13×75 мм. Каждый образец обсчитывали в течение 5 минут в гамма-счетчике. Данные, содержащиеся в выборке, вычитали из фоновых значений (реакция без какого-либо белка) и строили график зависимости от концентрации белка BBMV. Оптимальное количество белка для использования, как было определено, составляло 0,15 мг белка BBMV на мл.
Для определения кинетики связывания была построена кривая насыщения. Вкратце, BBMV (150 мкг/мл) инкубировали в течение 1 часа при 28ºC с 125I Cry-токсинов в возрастающей концентрации в диапазоне от 0,01 до 10 нМ. Общее связывание определяли путем отбора по 150 мкл для каждой концентрации в трех повторностях, центрифугирования образца и подсчета, как описано выше. Неспецифическое связывание определяли таким же образом, с добавлением 1000 нМ гомологичного трипсинизированного нерадиоактивного Cry-токсина, добавленного в реакционную смесь, для насыщения всех участков неспецифического связывания с рецепторами. Специфическое связывание рассчитывали как разницу между общим связыванием и неспецифическим связыванием.
Гомологичные и гетерологичных тесты по конкурентному связыванию проводили с использованием 150 мкг/мл белка BBMV и 0,5 нМ радиоактивно меченного 125I белка Cry. Концентрация конкурентного, не меченного радиоактивно Cry-токсина, добавленного к реакционной смеси, варьировала от 0,045 до 1000 нМ, и его добавляли в то же время, что и радиоактивный лиганд, чтобы обеспечить истинную конкуренцию связывания. Инкубации проводили в течение 1 часа при 28ºC и количество 125I белка Cry, связанного с его рецептором токсина, определяли, как описано выше, с вычитанием неспецифического связывания. Сто процентов общего связывания определялось в отсутствие какого-либо конкурентного лиганда. Результаты были представлены на полулогарифмическом графике в виде зависимости процента общего специфического связывания от концентрации добавленного конкурентного лиганда.
Пример 4. Краткое описание результатов
Фигура 1 показывает процент специфического связывания 125I CryAb (0,5 нМ) в BBMV ECB против конкуренции немеченого гомологичного Cry1Ab(♦) и гетерологичного Cry2Aa (□). Смещение кривой для гомологичной конкуренции на Cry1Ab приводит к сигмоидальной кривой, демонстрирующей 50% смещение радиолиганда при около 3 нМ Cry1Ab. Cry2Aa при концентрации 1000 нМ (в 2000 раз больше, чем вытесненный 125I Cry1Ab) приводит к менее чем 50%-смещению. Планки погрешностей представляют диапазон значений, полученных из определения трех повторностей.
ССЫЛКИ

Приложение A
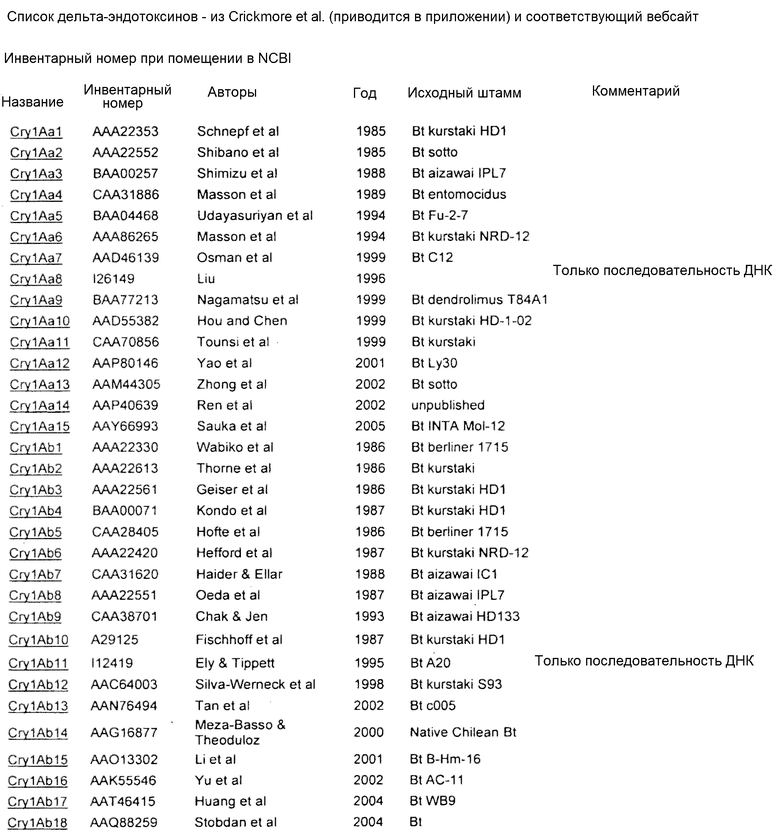
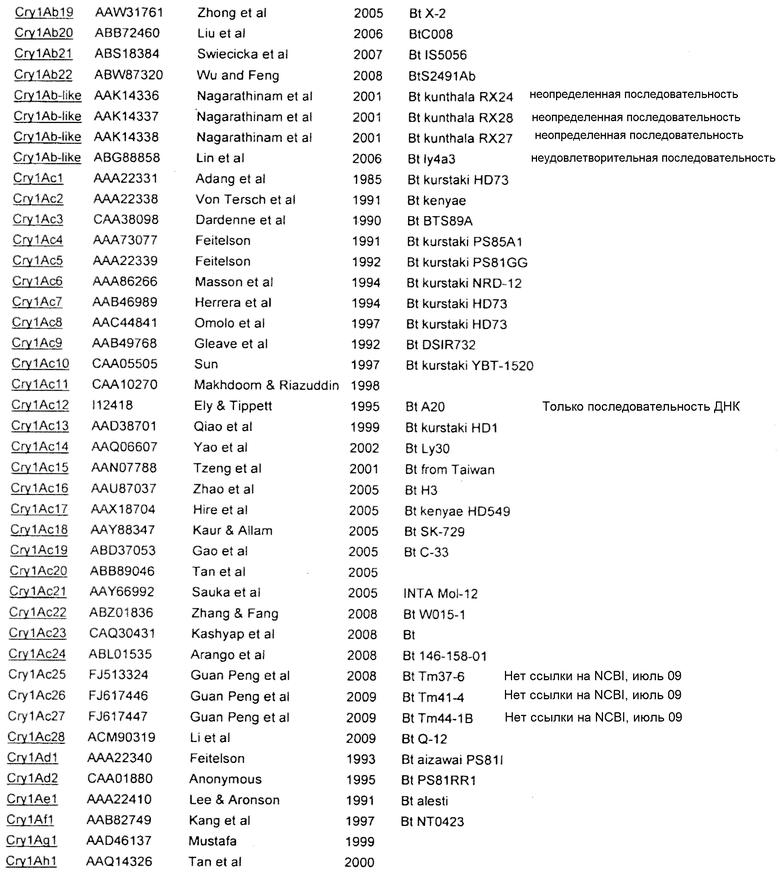



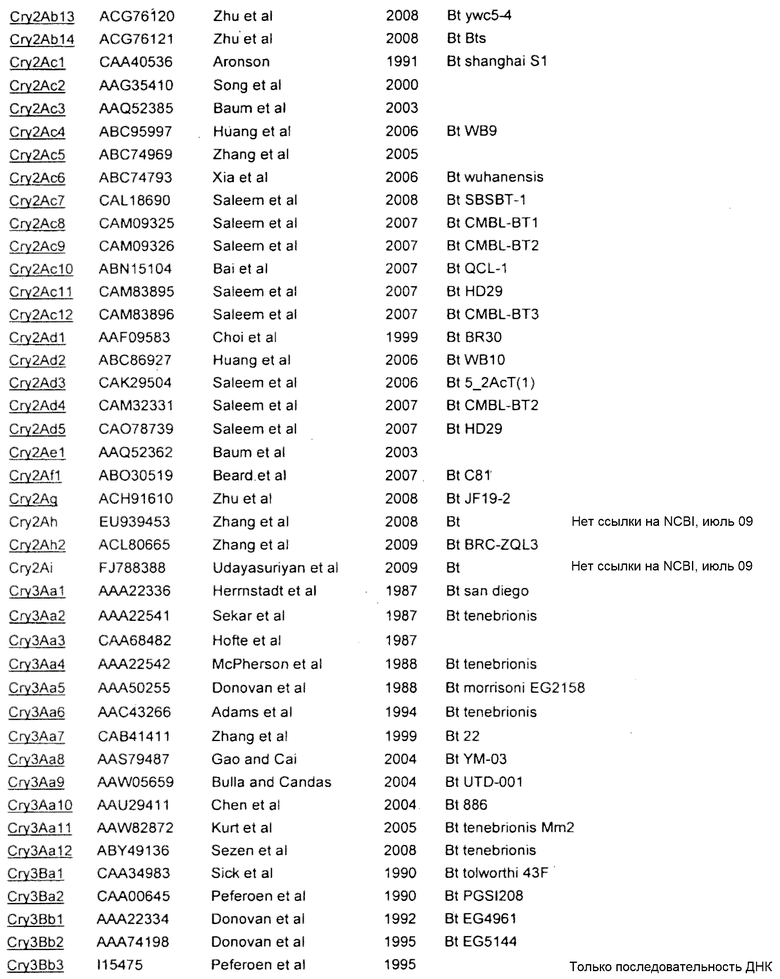
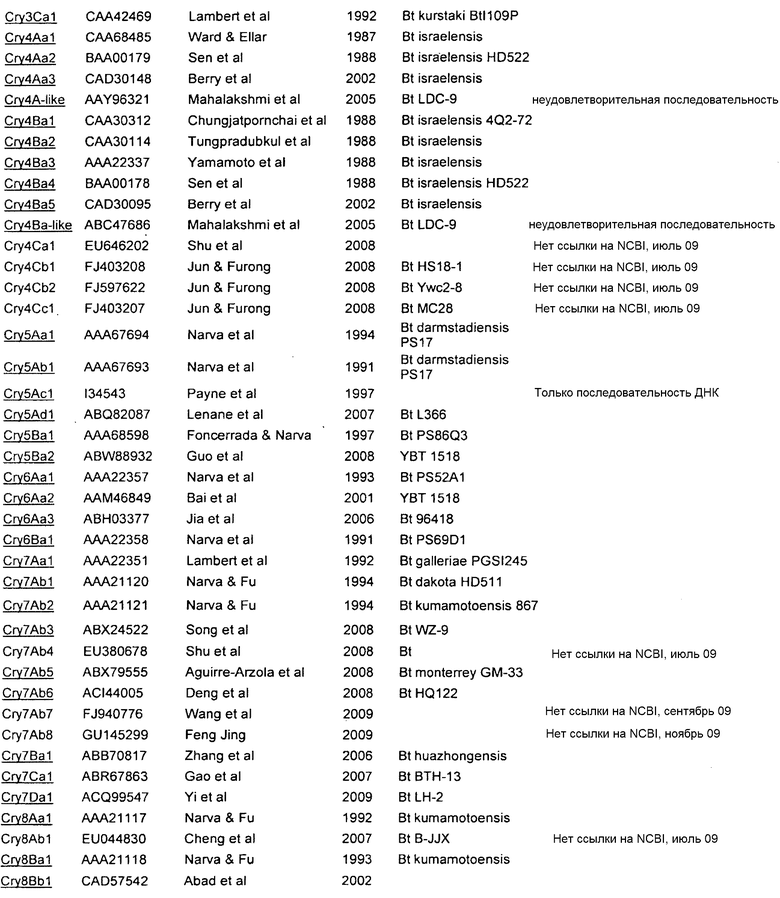
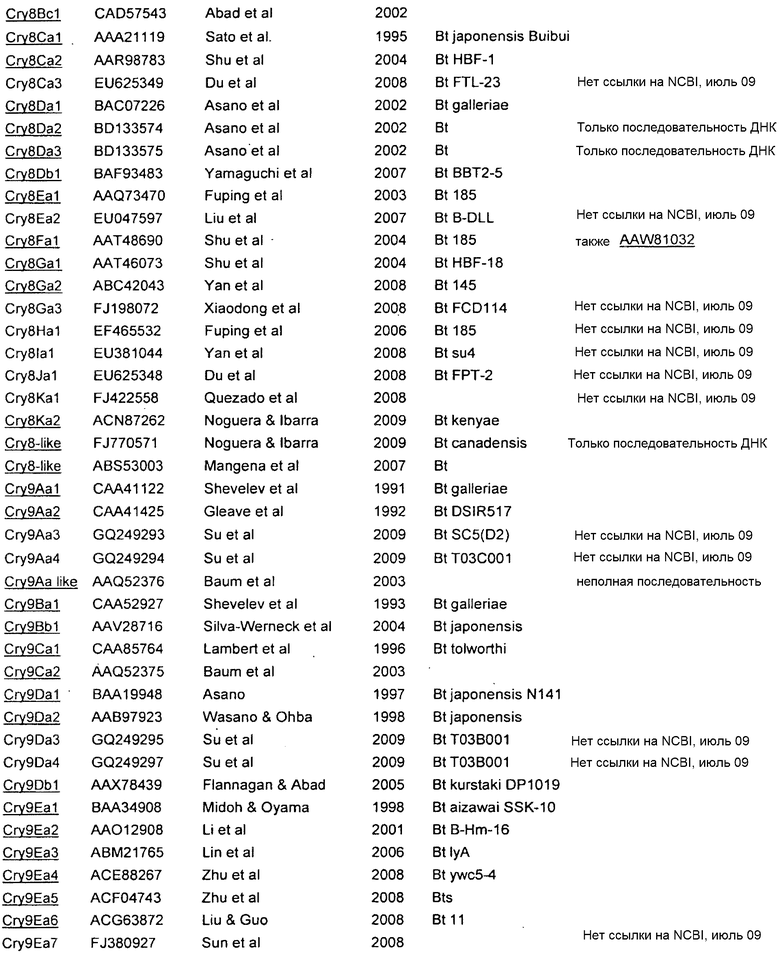


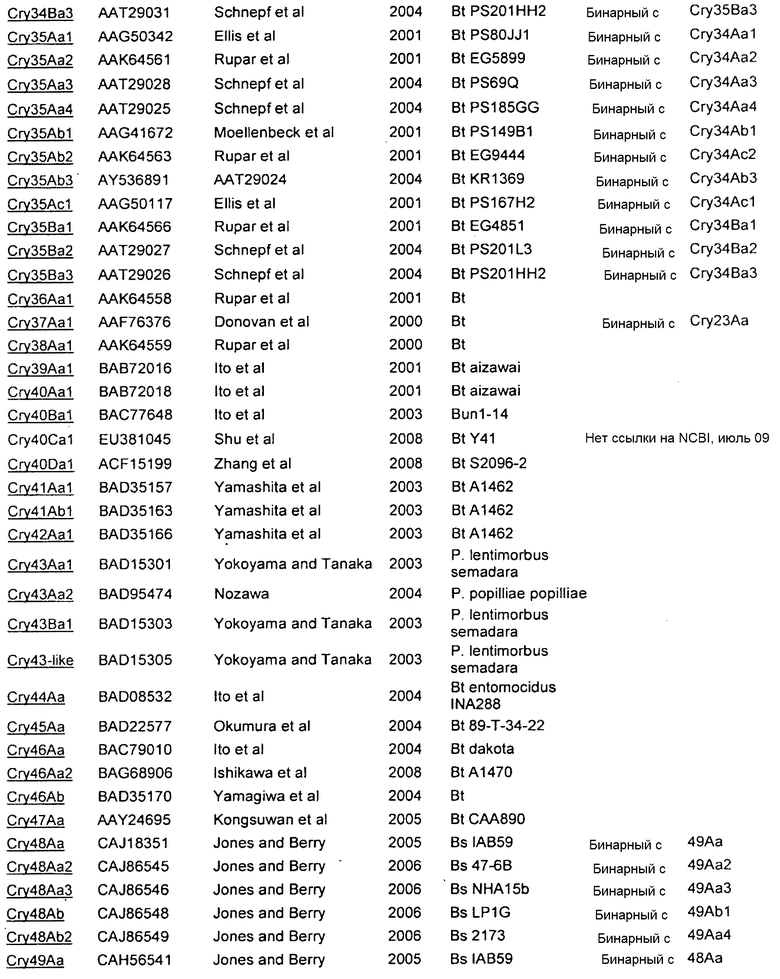
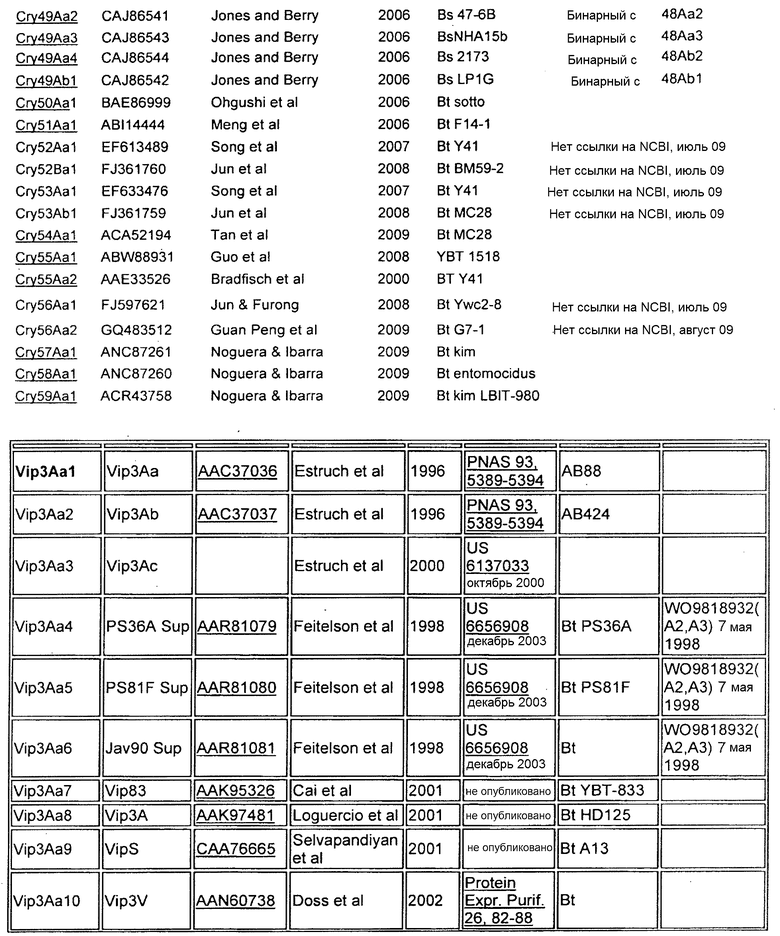
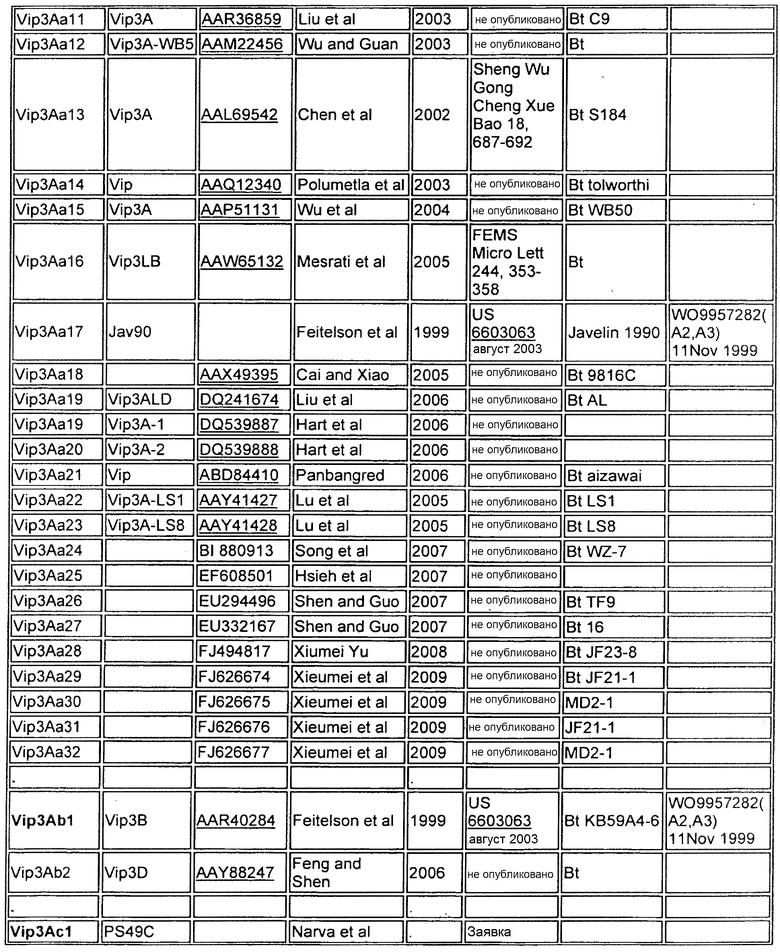
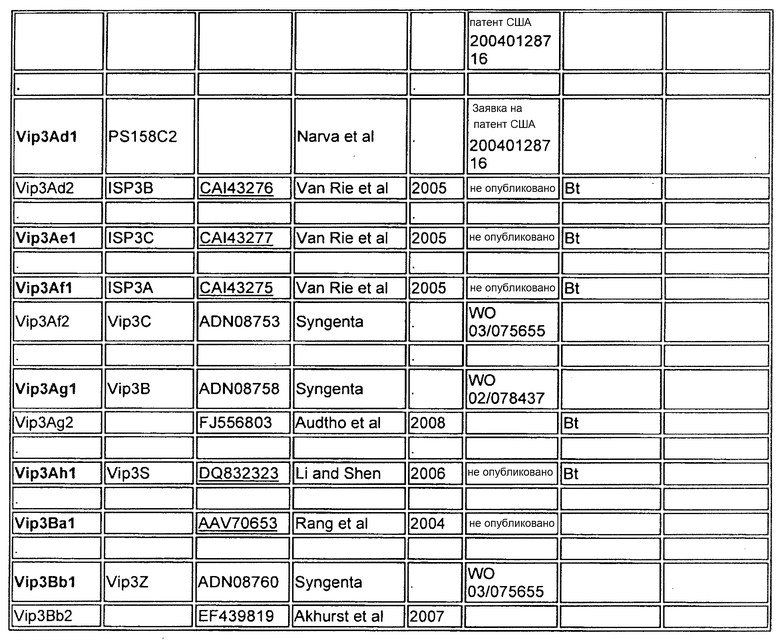
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНСЕКТИЦИДНЫЕ КОМБИНАЦИИ БЕЛКОВ ДЛЯ БОРЬБЫ С СОВКОЙ ТРАВЯНОЙ И КУКУРУЗНЫМ МОТЫЛЬКОМ И СПОСОБЫ УПРАВЛЕНИЯ УСТОЙЧИВОСТЬЮ НАСЕКОМЫХ | 2010 |
|
RU2577141C2 |
| ПРИМЕНЕНИЕ Cry1Da В СОЧЕТАНИИ С Cry1Ca ДЛЯ УПРАВЛЕНИЯ УСТОЙЧИВЫМИ НАСЕКОМЫМИ | 2010 |
|
RU2569108C2 |
| ПРИМЕНЕНИЕ Cry1Da В СОЧЕТАНИИ С Cry1Be ДЛЯ УПРАВЛЕНИЯ УСТОЙЧИВЫМИ НАСЕКОМЫМИ | 2010 |
|
RU2590592C2 |
| ПРИМЕНЕНИЕ ИНСЕКТИЦИДНОГО КРИСТАЛЛИЧЕСКОГО БЕЛКА DIG3 В КОМБИНАЦИИ С CRY1AB ДЛЯ РЕГУЛИРОВАНИЯ УСТОЙЧИВОСТИ К КУКУРУЗНОМУ МОТЫЛЬКУ | 2012 |
|
RU2624031C2 |
| ПРИМЕНЕНИЕ CRY1AB В КОМБИНАЦИИ С CRY1BE ДЛЯ УПРАВЛЕНИЯ РЕЗИСТЕНТНОСТЬЮ НАСЕКОМЫХ | 2010 |
|
RU2583288C2 |
| КОНТРОЛЬ УСТОЙЧИВОСТИ НАСЕКОМЫХ С ПОМОЩЬЮ КОМБИНАЦИИ БЕЛКОВ Cry1Be И Cry1F | 2010 |
|
RU2575611C2 |
| ПРИМЕНЕНИЕ Vip3Ab В СОЧЕТАНИИ С Cry1Ca ДЛЯ УПРАВЛЕНИЯ УСТОЙЧИВЫМИ НАСЕКОМЫМИ | 2010 |
|
RU2575084C2 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ VIP3AB И CRY1AB ДЛЯ РЕГУЛИРОВАНИЯ УСТОЙЧИВЫХ НАСЕКОМЫХ | 2011 |
|
RU2608500C2 |
| КОМБИНИРОВАННОЕ ПРИМЕНЕНИЕ БЕЛКОВ Cry1Da И Cry1Fa ДЛЯ ВЫРАБАТЫВАНИЯ РЕЗИСТЕНТНОСТИ К НАСЕКОМЫМ | 2010 |
|
RU2603257C2 |
| КОМБИНИРОВАННОЕ ИСПОЛЬЗОВАНИЕ БЕЛКОВ CRY1Ca И CRY1Ab ДЛЯ КОНТРОЛЯ УСТОЙЧИВОСТИ НАСЕКОМЫХ | 2010 |
|
RU2596406C2 |







Изобретение относится к области биохимии, в частности к трансгенному растению кукурузы, которое обладает устойчивостью к насекомым-вредителям европейским кукурузным мотылькам, а также к его семени. Раскрыто множество растений кукурузы на поле, включающее не содержащие Bacillus thuringiensis (не содержащие Bt) растения, которые не экспрессируют трансгенные инсектицидные белки, и множество трансгенных растений, которые обладают устойчивостью к насекомым-вредителям европейским кукурузным мотылькам, а также раскрыта смесь семян кукурузы, включающая семена от не содержащих Bt растений, которые не экспрессируют трансгенные инсектицидные белки, и множество семян, содержащих ДНК, кодирующую инсектицидный белок Cry1Ab, и ДНК, кодирующую инсектицидный белок Cry2Аа. Также раскрыт способ снижения развития устойчивости к белку Cry1Ab или белку Cry2Аа у насекомых европейских кукурузных мотыльков. Изобретение позволяет эффективно бороться с насекомыми-вредителями европейским кукурузным мотыльком. 5 н. и 14 з.п. ф-лы, 1 ил., 4 пр.
1. Трансгенное растение кукурузы, которое обладает устойчивостью к насекомым-вредителям европейским кукурузным мотылькам (ЕСВ: Ostrinia nubilalis), содержащее ДНК, кодирующую инсектицидный белок Cry1Ab с SEQ ID NO: 1, и ДНК, кодирующую инсектицидный белок Cry2Аа с SEQ ID NO: 2.
2. Трансгенное растение по п. 1, дополнительно содержащее ДНК, кодирующую третий инсектицидный белок, где указанный третий белок выбран из группы, состоящей из Cry1Fa, Cry1Be, Cry1I и DIG-3.
3. Трансгенное растение по п. 2, где указанный третий белок выбран из группы, состоящей из Cry1Fa и Cry1Be, и указанное растение дополнительно содержит ДНК, кодирующую четвертый и пятый инсектицидные белки, выбранные из группы, состоящей из Cry1Ca, Cry1Da, Cry1E и Vip3Ab.
4. Семя растения, по любому из пп. 1-3, содержащее ДНК, кодирующую инсектицидный белок Cry1Ab с SEQ ID NO: 1, и ДНК, кодирующую инсектицидный белок Cry2Аа с SEQ ID NO: 2, где указанное семя засеивают с целью контроля развития у кукурузной листовой совки устойчивости к инсектицидным белкам.
5. Множество растений кукурузы на поле, включающее не содержащие Bacillus thuringiensis (не содержащие Bt) растения, которые не экспрессируют трансгенные инсектицидные белки, и множество трансгенных растений, которые обладают устойчивостью к насекомым-вредителям европейским кукурузным мотылькам, по любому из пп. 1-3, где указанные трансгенные растения содержат ДНК, кодирующую инсектицидный белок Cry1Ab с SEQ ID NO: 1, и ДНК, кодирующую инсектицидный белок Cry2Аа с SEQ ID NO: 2, где указанные не содержащие Bt растения, которые не экспрессируют трансгенные инсектицидные белки, составляют менее 40% от всех культурных растений в указанном множестве растений, где указанное множество растений противодействует выработке устойчивости к белку Cry1Ab или белку Cry2Аа насекомыми европейскими кукурузными мотыльками, где указанное множество растений включает по меньшей мере одно не содержащее Bt растение, которое не экспрессирует трансгенные инсектицидные белки.
6. Множество растений на поле по п. 5, где указанные не содержащие Bt растения составляют менее 30% от всех культурных растений в указанном множестве растений.
7. Множество растений на поле по п. 5, где указанные не содержащие Bt растения составляют менее 20% от всех культурных растений в указанном множестве растений.
8. Множество растений на поле по п. 5, где указанные не содержащие Bt растения составляют менее 10% от всех культурных растений в указанном множестве растений.
9. Множество растений на поле по п. 5, где указанные не содержащие Bt растения составляют менее 5% от всех культурных растений в указанном множестве растений.
10. Множество растений на поле по п. 5, где указанные не содержащие Bt растения расположены в блоках или полосах.
11. Смесь семян кукурузы, включающая семена от не содержащих Bt растений, которые не экспрессируют трансгенные инсектицидные белки, и множество семян, содержащих ДНК, кодирующую инсектицидный белок Cry1Ab с SEQ ID NO: 1, и ДНК, кодирующую инсектицидный белок Cry2Аа с SEQ ID NO: 2, где указанные не содержащие Bt семена составляют менее 40% всех семян в смеси, где указанную смесь семян засеивают для контроля выработки устойчивости к белку Cry1Ab или белку Cry2Аа европейским кукурузным мотыльком, где указанная смесь семян включает по меньшей мере одно не содержащее Bt семя, которое не экспрессирует трансгенные инсектицидные белки.
12. Смесь семян по п. 11, где указанные не содержащие Bt семена составляют менее 30% всех семян в смеси.
13. Смесь семян по п. 11, где указанные не содержащие Bt семена составляют менее 20% всех семян в смеси.
14. Смесь семян по п. 11, где указанные не содержащие Bt семена составляют менее 10% всех семян в смеси.
15. Смесь семян по п. 11, где указанные не содержащие Bt семена составляют менее 5% всех семян в смеси.
16. Способ снижения развития устойчивости к белку Cry1Ab или белку Cry2Аа у насекомых европейских кукурузных мотыльков, включающий засевание семян для получения множества трансгенных растений кукурузы, содержащих ДНК, кодирующую инсектицидный белок Cry1Ab с SEQ ID NO: 1, и ДНК, кодирующую инсектицидный белок Cry2Аа с SEQ ID NO: 2, и приведение указанного насекомого в контакт с указанным множеством трансгенных растений.
17. Множество растений кукурузы по любому из пп. 5-10, где указанные растения занимают более 10 акров.
18. Растение по любому из пп. 1-3, где указанное растение представляет собой растение кукурузы.
19. Растение по любому из пп. 1-3, где указанный инсектицидный белок Cry1Ab характеризуется SEQ ID NO: 1, и указанный инсектицидный белок Cry2Аа содержит SEQ ID NO: 2.
Авторы
Даты
2015-11-27—Публикация
2010-12-16—Подача