Группа изобретений относится к области органической и медицинской химии, а именно к новым индивидуальным соединениям класса мезоионных гетероциклических систем - замещенным хлоридам 2-[(1Z)-1-(3,5-диарил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия общей формулы I и способу их получения, которые могут быть использованы для синтеза новых гетероциклических соединений и в медицине в качестве потенциального антимикробного средства.
 ,
,
где R=3,5-диFC6H4; R1=4-FC6H4 (Ia - хлорид 2-[(1Ζ)-1-(3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-3-ия);
R=4-FC6H4; R1=Ph (Iб - хлорид 2-[(1Z)-1-(3-(4-фторфенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(4-фторфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=3,5-диFC6H4; R1=Ph (Iв - хлорид 2-[(1Ζ)-1-(3-(3,5-дифторфенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(3,5-дифторфенил)-5-фенил-1,3,4-тиадиазол-3-ия);
R=3,5-диClС6Н4; R1=Ph (Iг - хлорид 2-[(1Ζ)-1-(3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазол-3-ия);
R=4-NO2C6H4; R1=Ph (Iд - хлорид 2-[(1Z)-1-(3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=Bn; R1=Ph (Ie - хлорид 2-[(1Z)-1-(3-бензил-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-бензил-5-фенил-1,3,4-тиадиазол-3-ия).
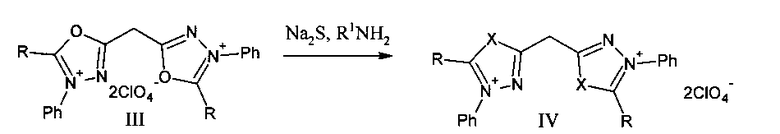
Описаны перхлораты 5,5′-метиленбис(2-метил(фенил)-3-фенил-1,3,4-оксадиазол-3-ия) III, которые были получены взаимодействием N′1,N′3-дифенилпропандигидразида II с ангидридами уксусной и бензойной кислот (R=Me, Ph). Под действием Na2S и аминов R1NH2 (R1=Ph, 4-CH3Ph, CH2Ph, 1-Naph) происходила трансформация 1,3,4-оксадиазольных циклов в 1,3,4-тиадиазольные и 1,2,4-триазольные с образованием соединений общей формулы IV (X=S, NR1). Обработка некоторых соединений IV (X=S, R=Ph; X=NPh, R=Me) водными растворами аммиака или гидроксида натрия приводила к отщеплению одной молекулы хлорной кислоты и получению перхлоратов 2-[(4,5-дифенил-1,3,4-тиадиазол-4-ий-2-ил)метилиден]-4,5-дифенил-1,3,4-тиадиазол-3-ид-4-ия и 5-[(1,4-дифенил-5-метил-4H-1,2,4-триазол-1-ий-3-ил)метилиден]-2,4-дифенил-3-метил-4,5-дигидро-1,2,4-триазол-1-ид-2-ия соответственно (соединения общей формулы V) [Чуйгук, В.А. Мезоионные метановые красители бичетвертичных солей дигетероарилметанов - производные 1,3,4-окса(тиа)диазолов и 1,2,4-триазолов / В.А. Чуйгук, А.Г. Немазаный // Украинский химический журнал. - 1984. - №5. - с. 519-524]:


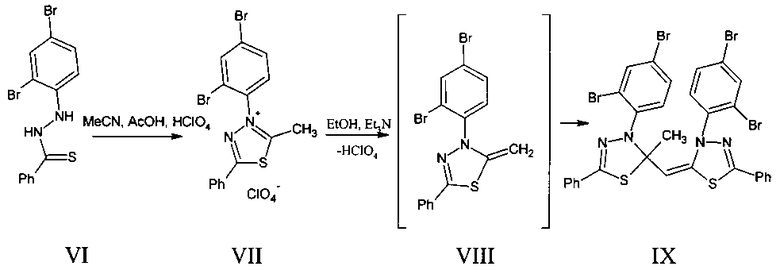
Описан 5-фенил-2-[(5-фенил-3-(2,4-дибромфенил)-1,3,4-тиадиазол-2(3H)-илиден)метил]-2-метил-3-(2,4-дибромфенил)-2,3-дигидро-1,3,4-тиадиазол IX, полученный димеризацией 3-(2,4-дибромфенил)-2-метилиден-5-фенил-2,3-дигидро-1,3,4-тиадиазола VIII in situ [Mastalerz, Η. 2-Alkyl-3,5-diaryl-1,3,4-thiadiazolim perchlorates and reactions thereof / H. Mastalerz, M.S. Gibson // Journal of Chemical Society, Perkin Trans. 1 - 1983. - №2. - P. 245-249].
В литературе описаны 2-алкил-3-фенил-1,3,4-тиадиазол-3-ий-5-тиолаты XIII, обладающие примерно равной активностью с пенициллином G в отношение грамположительных бактерий Staphylococcus aureus и Diplococcus pneumoniae (R=Me, Et, Pr, i-Pr) [Pat. 3337398 US Mesoionic thiadiazole bactericides]:

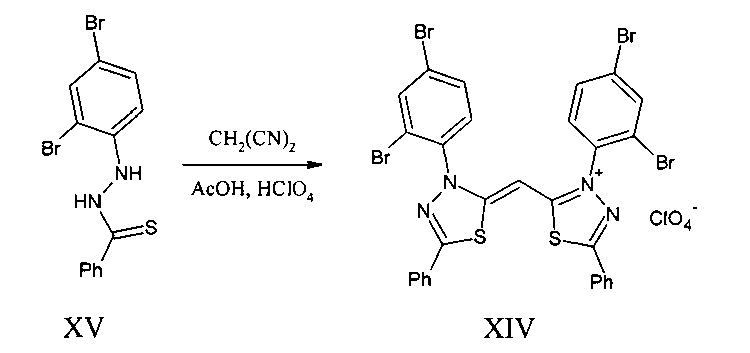
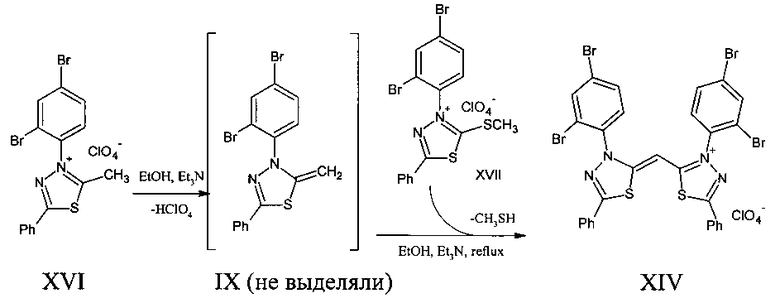
Известен перхлорат 2-[(Z)-(3-(2,4-дибромфенил)-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(2,4-дибромфенил)-5-фенил-1,3,4-тиадиазол-3-ия XIV, полученный взаимодействием N′-(2,4-дибромфенил)тиобензгидразида XV с динитрилом малоновой кислоты в уксусной кислоте в присутствии хлорной кислоты. Он же был синтезирован кипячением смеси перхлората 3-(2,4-дибромфенил)-2-метил-5-фенил-1,3,4-тиадиазол-3-ия XVI и перхлората 3-(2,4-дибромфенил)-2-метилсульфанил-5-фенил-1,3,4-тиадиазол-3-ия XVII в этаноле в присутствии триэтиламина [Mastalerz, Η.A 2-methylthio-3,5-diaryl-1,3,4-thiadiazolim cation; its reactions, and further exploration of the chemistry of 2-alkyl-3,5-diaryl-1,3,4-thiadiazolium cations / H. Mastalerz, T. Mohammad, M.S. Gibson // Canadian Journal of Chemistry. - 1987. - №12. - P. 2713-2716]:
К недостаткам приведенных решений относится то, что данными способами невозможно получить хлорид 2-[(1Z)-1-(3,5-дифенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-дифенил-1,3,4-тиадиазол-3-ия, а перхлорат-ионы, играющие роль противоионов у вышеперечисленных соединений, являются фармакологически неприемлемыми. Известно, что, будучи антагонистами иода, они нарушают его обмен в организме человека.
Описан метод получения хлорида 2-[(1Z)-1-(3,5-дифенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-дифенил-1,3,4-тиадиазол-3-ия XIX путем взаимодействия N′-фенилтиобензгидразида XVIII с незамещенным малонилдихлоридом в соотношении 1:1 в среде безводного неполярного органического растворителя при температуре кипения реакционной массы с последующим выделением целевого продукта по схеме:
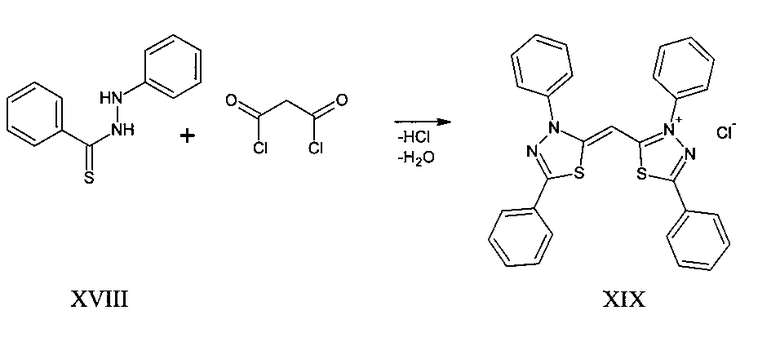
К недостаткам данного метода получения относится токсичность веществ, необходимы дополнительные меры по обеспечению безопасности технологического процесса [Пат. 2402550 РФ. Хлорид 2-[(1Z)-1-(3,5-дифенил-1,3,4-тиадиазол-2(3н)-илиден)метил]-3,5-дифенил-1,3,4-тиадиазол-3-ия и способ его получения].
Задачей предлагаемой группы изобретений является разработка способа и создание новых не описанных в литературе соединений - замещенных хлоридов 2-[(1Z)-1-(3,5-диарил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия (I), что позволит расширить ассортимент потенциальных антимикробных средств.
Техническими результатами, на решение которых направлена группа изобретений, являются получение новых соединений - замещенных хлоридов 2-[(1Ζ)-1-(3,5-диарил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия общей формулы I, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в медицине, например в качестве антимикробных средств; разработка простого способа их получения с высоким выходом продукта.
Поставленная задача осуществляется путем взаимодействия замещенного N′-арилтиобензгидразида с малондинитрилом в соотношении 2:1 в среде полярного органического растворителя (диметилформамида) и хлористого водорода, причем изначально насыщают реакционную смесь сухим хлористым водородом, а затем, не прекращая подачи хлористого водорода, нагревают до 60°C и выдерживают в течение часа при температуре кипения реакционной массы с последующим выделением целевого продукта по схеме:
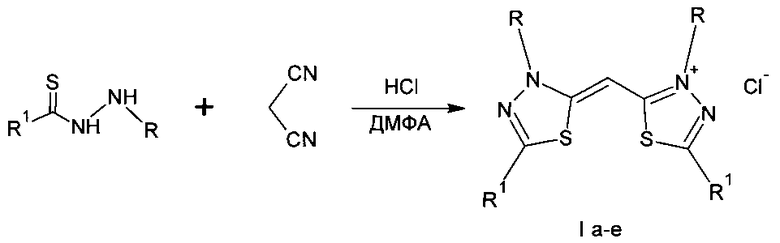
R=3,5-диFC6H4; R1=4-FC6H4 (Ia - хлорид 2-[(1Ζ)-1-(3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-3-ия);
R=4-FC6H4; R1=Ph (Iб - хлорид 2-[(1Z)-1-(3-(4-фторфенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(4-фторфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=3,5-диFC6H4; R1=Ph (Iв - хлорид 2-[(1Ζ)-1-(3-(3,5-дифторфенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(3,5-дифторфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=3,5-диClC6H4; R1=Ph (Iг - хлорид 2-[(1Ζ)-1-(3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=4-NO2C6H4; R1=Ph (Iд - хлорид 2-[(1Z)-1-(3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=Bn; R1=Ph (Ie - хлорид 2-[(1Z)-1-(3-бензил-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-бензил-5-фенил-1,3,4-тиадиазол-3-ия).
Поставленная задача осуществляется еще и тем, что для выделения продукта охлажденную реакционную смесь выливают на тонкоизмельченный лед, перемешивают и отфильтровывают выпавший осадок.
Способ получения замещенных хлоридов 2-[(1Z)-1-(3,5-диарил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия изучен и проведен в лабораторных условиях на стандартном товарном сырье.
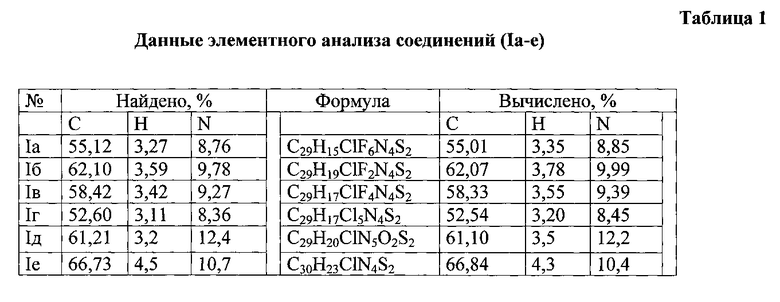
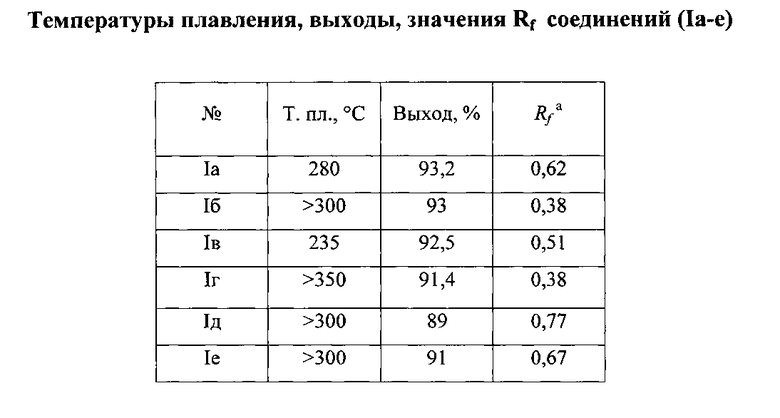
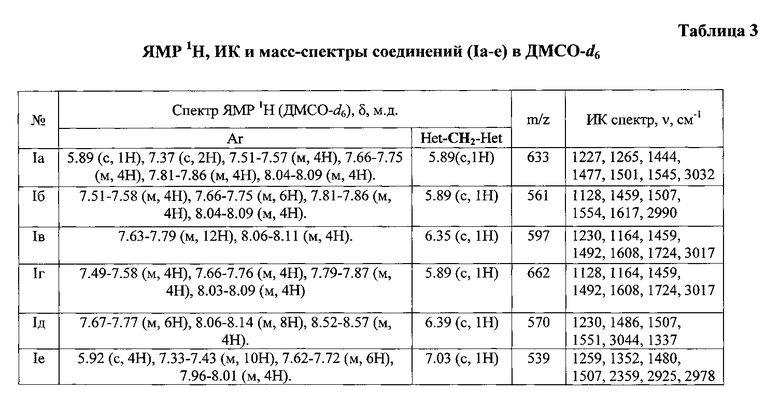
Данные элементного анализа приведены в табл. 1, выходы продуктов реакций, температуры плавления и величины Rf приведены в табл. 2, спектральные характеристики полученных соединений сведены в табл. 3 и 4, антимикробная активность - в табл. 5.
Пример 1. Хлорид 2-[(1Z)-1-(3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-3-ия (Iа). В трехгорлую круглодонную колбу емкостью 250 мл, снабженную мешалкой, обратным холодильником и трубкой для подачи газа, загружают 22,83 г (0,1 моль) N′-(3,5-дифторфенил)тио-4-фторбензгидразида 3,3 г (0,05 моль) малондинитрила и 100 мл диметилформамида (ДМФА). Включают мешалку и насыщают реакционную смесь сухим хлористым водородом в течение 30 мин. Затем, не прекращая подачи HCl, нагревают колбу до 60°C и выдерживают при этой температуре в течении часа. Охлажденную реакционную смесь выливают на 1 кг тонкоизмельченного льда, перемешивают и отфильтровывают выпавший осадок. Осадок промывают сначала три раза холодной водой, затем три раза этилацетатом и сушат при 70°C. Выход продукта Iа 29,5 г (93,2% от теоретического из расчета на N′-(3,5-дифторфенил)тио-4-фторбензгидразид) в виде ярко-желтых мелких игольчатых кристаллов. Т. пл. 280°C разл. Продукт хроматографически однороден - Rf=0.62 (хлороформ-метанол 2:1).
Состав синтезированного соединения подтвержден элементным анализом. Брутто-Формула: C29H15ClF6N4S2. Найдено, %: С - 55.12, Η - 3.27, N - 8.76. Вычислено, %: С - 55.01, Н - 3.35, N - 8.85.
Строение синтезированного вещества было доказано физико-химическими методами идентификации органических соединений: ЯМР 1Н и 13С, ИК-спектроскопией.
В ИК-спектрах вещества (таблетки KBr) наиболее характеристической является область 1540-1440 см-1, где наблюдаются полосы поглощения, соответствующие валентным колебаниям связей C=C и C=N сопряженной системы. Аналогичные колебания С-Н связей бензольных колец находятся в диапазоне 3100-3000 см-1.
В спектре ЯМР 1Н полученного соединения в ДМСО-d6 присутствуют сигналы протонов бензольных колец (δ 7.59-7.73 (м, 16Н), 8.04 (д, 4Н, J=6.9Hz)) и протона метанового мостика между 1,3,4-тиадиазольными циклами (δ 6.01 с 1Н).
Спектр ЯМР 13С этого соединения характеризуется сигналами ядер углерода бензольных колец (δ 125.4-136.2 м.д.), тиадиазольных циклов (δ 162.9 и 168.5 м.д.) и метанового мостика между 1,3,4-тиадиазольными циклами (δ 79.26 м.д.).
Также строение полученного вещества было доказано с помощью масс-спектрометрии. Рассчитанная молекулярная масса полностью совпала с экспериментально полученной (М+=633).
Пример 2. Хлорид 2-[(1Z)-1-(3-(4-фторфенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(4-фторфенил)-5-фенил-1,3,4-тиадиазолил-3-ия (Iб). В трехгорлую круглодонную колбу емкостью 250 мл, снабженную мешалкой, обратным холодильником и трубкой для подачи газа, загружают 24,63 г (0,1 моль) N′-(4-фторфенил)тиобензгидразида, 3,3 г (0,05 моль) малондинитрила и 100 мл ДМФА. Включают мешалку и насыщают реакционную смесь сухим хлористым водородом в течение 30 мин. Затем, не прекращая подачи HCl, нагревают колбу до 60°C и выдерживают при этой температуре в течении часа. Охлажденную реакционную смесь выливают на 1 кг тонкоизмельченного льда, перемешивают и отфильтровывают выпавший осадок. Осадок промывают сначала три раза холодной водой, затем три раза этилацетатом и сушат при 70°C. Выход продукта Iб 26,1 г, 93% от теоретического из расчета на N′-(4-фторфенил)тиобензгидразид.
Пример 3. Хлорид 2-[(1Z)-1-(3-(3,5-дифторфенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(3,5 -дифторфенил)-5-фенил-1,3,4-тиадиазолил-3-ия (Iв). В трехгорлую круглодонную колбу емкостью 250 мл, снабженную мешалкой, обратным холодильником и трубкой для подачи газа, загружают 26,43 г (0,1 моль) N′-(3,5-дифторфенил)тиобензгидразида, 3,3 г (0,05 моль) малондинитрила и 100 мл ДМФА. Включают мешалку и насыщают реакционную смесь сухим хлористым водородом в течение 30 мин. Затем, не прекращая подачи HCl, нагревают колбу до 60°C и выдерживают при этой температуре в течение часа. Охлажденную реакционную смесь выливают на 1 кг тонкоизмельченного льда, перемешивают и отфильтровывают выпавший осадок. Осадок промывают сначала три раза холодной водой, затем три раза этилацетатом и сушат при 70°C. Выход продукта Iв 27,6 г, 92,5% от теоретического из расчета на Ν′-(3,5-дифторфенил)тиобензгидразида.
Пример 4. Хлорид 2-[(1Z)-1-(3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазолил-3-ия (Iг). В трехгорлую круглодонную колбу емкостью 250 мл, снабженную мешалкой, обратным холодильником и трубкой для подачи газа, загружают 29,72 г (0,1 моль) N′-(3,5-дихлорфенил)тиобензгидразида, 3,3 г (0,05 моль) малондинитрила и 100 мл ДМФА. Включают мешалку и насыщают реакционную смесь сухим хлористым водородом в течение 30 мин. Затем, не прекращая подачи НСl, нагревают колбу до 60°C и выдерживают при этой температуре в течение часа. Охлажденную реакционную смесь выливают на 1 кг тонкоизмельченного льда, перемешивают и отфильтровывают выпавший осадок. Осадок промывают сначала три раза холодной водой, затем три раза этилацетатом и сушат при 70°C. Выход продукта Iг 30,3 г, 91,4% от теоретического из расчета на Ν′-(3,5-дихлорфенил)тиобензгидразид.
Пример 5. Хлорид 2-[(1Z)-1-(3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазолил-3-ия (Iд). В трехгорлую круглодонную колбу емкостью 250 мл, снабженную мешалкой, обратным холодильником и трубкой для подачи газа, загружают 27,33 г (0,1 моль) N′-(4-нитрофенил)тиобензгидразида, 3,3 г (0,05 моль) малондинитрила и 100 мл ДМФА. Включают мешалку и насыщают реакционную смесь сухим хлористым водородом в течение 30 мин. Затем, не прекращая подачи HCl, нагревают колбу до 60°C и выдерживают при этой температуре в течение часа. Охлажденную реакционную смесь выливают на 1 кг тонкоизмельченного льда, перемешивают и отфильтровывают выпавший осадок. Осадок промывают сначала три раза холодной водой, затем три раза этилацетатом и сушат при 70°C. Выход продукта Iд 24,1 г, 89% от теоретического из расчета на N′-(4-нитрофенил)тиобензгидразид.
Пример 6. Хлорид 2-[(1Z)-1-(3-бензил-5-фенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3-бензил-5-фенил-1,3,4-тиадиазол-3-ия (Iе). В трехгорлую круглодонную колбу емкостью 250 мл, снабженную мешалкой, обратным холодильником и трубкой для подачи газа, загружают 24,23 г (0,1 моль) Ν′-(бензил)тиобензгидразида, 3,3 г (0,05 моль) малондинитрила и 100 мл ДМФА. Включают мешалку и насыщают реакционную смесь сухим хлористым водородом в течение 30 мин. Затем, не прекращая подачи HCl, нагревают колбу до 60°C и выдерживают при этой температуре в течение часа. Охлажденную реакционную смесь выливают на 1 кг тонкоизмельченного льда, перемешивают и отфильтровывают выпавший осадок. Осадок промывают сначала три раза холодной водой, затем три раза этилацетатом и сушат при 70°C. Выход продукта Iе 25,1 г, 91% от теоретического из расчета на N′-(бензил)тиобензгидразид.
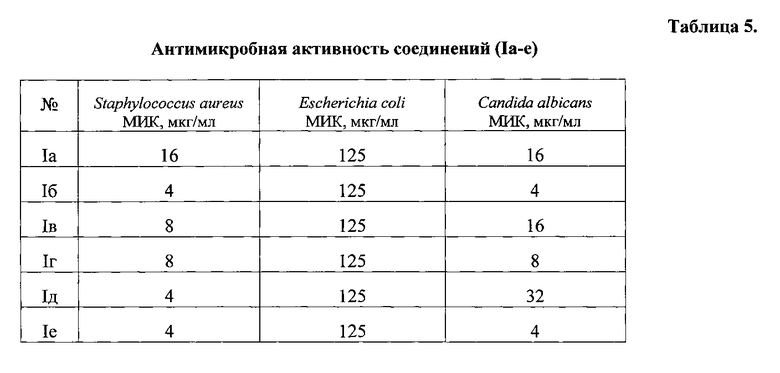
Пример 8. Определение минимально ингибирующих концентраций (МИК) - табл. 5.
Проводили методом серийных разведений в мясопептонном бульоне в отношении тест-культур микроорганизмов Staphylococcus aureus (штамм 209-Р), Escherichia coli (штамм 1257), Candida albicans (штамм АТСС 885-635), рекомендованных Государственной Фармакопеей [Государственная Фармакопея РФ XII. М.: Научный центр экспертизы средств медицинского применения, 2007. С. 105-109]. Исследуемые соединения ограниченно растворяются в воде, поэтому в качестве растворителя использовали 20% раствор ДМСО, не подавляющий роста ни одной из использованных тест-культур в условиях эксперимента. Минимальные ингибирующие концентрации соединений I на Е. coli и С. albicans соответствуют допустимым и на St. aureus находятся на уровне широко используемых на практике антибиотиков (эдицин - 10-20 мкг/мл, ванкомицин и тейкопланин - 0,3-12,5 мкг/мл).
Получены новые соединения - замещенные хлориды 2-[(1Ζ)-1-(3,5-диарил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия общей формулы I, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в медицине, например в качестве антимикробных средств. Разработан простой одностадийный способ их синтеза с высоким выходом. Способ занимает мало времени, не требует дорогого оборудования, основан на использовании доступного дешевого сырья.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения замещенных хлоридов 2-[(1Z)-1-(3,5-диарил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия | 2017 |
|
RU2637926C1 |
| ХЛОРИД 2-[(1Z)-1-(3,5-ДИФЕНИЛ-1,3,4-ТИАДИАЗОЛ-2(3Н)-ИЛИДЕН)МЕТИЛ]-3,5-ДИФЕНИЛ-1,3,4-ТИАДИАЗОЛ-3-ИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2402550C1 |
| Способ получения ангидро-2-меркапто1,3,4-тиадиазолий-гидроксидов | 1975 |
|
SU560532A3 |
| Способ количественного определения хлорида 2-[(Z)-1-(3,5-дифенил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-дифенил-1,3,4-тиадиазол-3-ия в биологических объектах | 2019 |
|
RU2702330C1 |
| ИНГИБИТОРЫ ТИРОЗИНФОСФАТАЗЫ БЕЛКА ЧЕЛОВЕКА И СПОСОБЫ ПРИМЕНЕНИЯ | 2007 |
|
RU2435763C2 |
| Способ получения производных -(1,3,4-тиадиазол-2ил) бензамида | 1977 |
|
SU706023A3 |
| 6-(3,5-Дифенил-1,3,4-тиадиазол-2(3Н)-илиден)-2,4-дифенил-4Н-1,3,4-тиадиазин-5-он и способ его получения | 2016 |
|
RU2659574C2 |
| ПРОИЗВОДНЫЕ 2-ПИРРОЛИДИН-2-ИЛ-[1,3,4]ОКСАДИАЗОЛА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ АНТИДЕПРЕССАНТОВ | 2003 |
|
RU2324694C2 |
| Замещенные 3-арил-5-фенил-3Н-1,2,3,4-дитиадиазол-2-оксиды и способ их получения | 2016 |
|
RU2659789C2 |
| ПРОИЗВОДНЫЕ 1,3,4-ТИОДИАЗОЛ-2-КАРБОНОВЫХ КИСЛОТ | 1992 |
|
RU2050357C1 |
Изобретение относится к области органической и медицинской химии, а именно к новым индивидуальным соединениям класса мезоионных гетероциклических систем - замещенным хлоридам 2-[(1Z)-1-(3,5-диарил-1,3,4-тиадиазол-2(3Н)-илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия общей формулы I, где: R=3,5-диFC6H4; R1=4-FC6H4 (Ia); R=4-FC6H4; R1=Ph (Iб); R=3,5-диFC6H4; R1=Ph (Iв); R=3,5-диClC6H4; R1=Ph (Iг); R=4-NO2C6H4; R1=Ph (Iд); R=Bn; R1=Ph (Ie). Замещенные хлориды, представленные формулой (I), получают путем взаимодействия замещенного N′-арилтиобензгидразида с малонилдинитрилом в соотношении 2:1 в среде полярного органического растворителя (диметилформамида) и хлористого водорода, причем изначально насыщают реакционную смесь сухим хлористым водородом, а затем, не прекращая подачи хлористого водорода, нагревают до 60°C и выдерживают в течение часа с последующим выделением продукта. При этом для выделения продукта охлажденную реакционную смесь выливают на тонкоизмельченный лед, перемешивают и отфильтровывают выпавший осадок. Технический результат - получение новых соединений, которые могут быть использованы в медицине, в качестве антимикробных средств, с высоким выходом. 2 н. и 1 з.п. ф-лы, 5 табл., 8 пр.
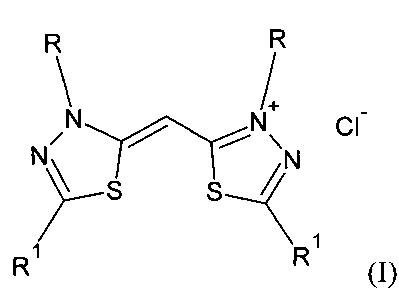
1. Замещенные хлориды 2-[(1Z)-1-(3,5-диарил-1,3,4-тиадиазол-2(3H)илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия общей формулы I
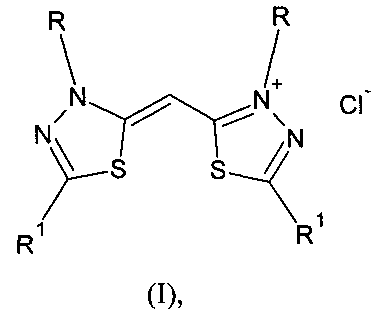
где R=3,5-диFC6H4; R1=4-FC6H4 (Iа - хлорид 2-[(1Z)-1-(3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-3-ия);
R=4-FC6H4; R1=Ph (Iб - хлорид 2-[(1Z)-1-(3-(4-фторфенил)-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(4-фторфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=3,5-диFC6H4; R1=Ph (Iв - хлорид 2-[(1Z)-1-(3-(3,5-дифторфенил)-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(3,5-дифторфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=3,5-диClC6H4; R1=Ph (Iг - хлорид 2-[(1Z)-1-(3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=4-NO2C6H4; R1=Ph (Iд - хлорид 2-[(1Z)-1-(3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=Bn; R1=Ph (Iе - хлорид 2-[(1Z)-1-(3-бензил-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-бензил-5-фенил-1,3,4-тиадиазол-3-ия).
2. Способ получения замещенных хлоридов 2-[(1Z)-1-(3,5-диарил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия общей формулы I

где R=3,5-диFC6H4; R1=4-FC6H4 (Iа - хлорид 2-[(1Z)-1-(3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(3,5-дифторфенил)-5-(4-фторфенил)-1,3,4-тиадиазол-3-ия);
R=4-FC6H4; R1=Ph (Iб - хлорид 2-[(1Z)-1-(3-(4-фторфенил)-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(4-фторфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=3,5-диFC6H4; R1=Ph (Iв - хлорид 2-[(1Z)-1-(3-(3,5-дифторфенил)-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(3,5-дифторфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=3,5-диClC6H4; R1=Ph (Iг - хлорид 2-[(1Z)-1-(3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(3,5-дихлорфенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=4-NO2C6H4; R1=Ph (Iд - хлорид 2-[(1Z)-1-(3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-(4-нитрофенил)-5-фенил-1,3,4-тиадиазолил-3-ия);
R=Bn; R1=Ph (Iе - хлорид 2-[(1Z)-1-(3-бензил-5-фенил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3-бензил-5-фенил-1,3,4-тиадиазол-3-ия) путем взаимодействия замещенного N′-арилтиобензгидразида с малонилдинитрилом в соотношении 2:1 в среде полярного органического растворителя (диметилформамида) и хлористого водорода, причем изначально насыщают реакционную смесь сухим хлористым водородом, а затем, не прекращая подачи хлористого водорода, нагревают до 60°C и выдерживают в течение часа с последующим выделением продукта.
3. Способ получения замещенных хлоридов 2-[(1Z)-1-(3,5-диарил-1,3,4-тиадиазол-2(3H)-илиден)метил]-3,5-диарил-1,3,4-тиадиазол-3-ия общей формулы I по п. 2, отличающийся тем, что для выделения продукта охлажденную реакционную смесь выливают на тонкоизмельченный лед, перемешивают и отфильтровывают выпавший осадок.
| ХЛОРИД 2-[(1Z)-1-(3,5-ДИФЕНИЛ-1,3,4-ТИАДИАЗОЛ-2(3Н)-ИЛИДЕН)МЕТИЛ]-3,5-ДИФЕНИЛ-1,3,4-ТИАДИАЗОЛ-3-ИЯ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2402550C1 |
| US 3337398 A, 22.08.1967 | |||
| MASTALERZ Н | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2015-12-20—Публикация
2014-10-07—Подача