Область техники, к которой относится изобретение
Настоящее изобретение относится к фармацевтическому средству для предотвращения и/или лечения гепатоклеточной карциномы.
Уровень техники
В 2009 году 344000 человек в Японии умерли от злокачественных новообразований, которые являются главной причиной смерти. Среди них количество умерших от гепатоклеточной карциномы превышает 30000. Количество смертей из-за гепатоклеточной карциномы увеличивается из года в год и почти утроилось в течение последних 20 лет.
Среди случаев гепатоклеточной карциномы в Японии, 90% или более, как сообщается, представляют собой стойкую инфекцию (хронический гепатит), вызываемую вирусом гепатита B (HBV, далее может упоминаться как HBV) и вирусом гепатита C (HCV, далее может упоминаться как HCV). Таким образом, вирусный гепатит представляет собой ключевое заболевание для появления гепатоклеточной карциномы. В то же время неалкогольный стеатогепатит (далее может сокращенно упоминаться как "NASH") представляет собой один из типов гепатита, возникающего из-за аккумуляции жира в печени. Оксидативный стресс при ожирении печени, стойкость к инсулину, провоспалительные цитокины и тому подобное, приводят к переходу от ожирения печени или от обострения патологического состояния. В последние годы участились случаи метаболического синдрома, и существуют проблемы с увеличением возникновения NASH, и с последующим переходом к фиброзу печени, циррозу и гепатоклеточной карциноме. Таким образом, NASH, как и вирусный гепатит, представляет собой ключевое заболевание, вовлеченное в появление гепатоклеточной карциномы.
В настоящее время гепатоклеточную карциному лечат, например, посредством методик, включающих хирургическую терапию (например, гепатэктомию и трансплантацию печени); местную медицинскую терапию, включая терапию с чрескожной инъекцией этанола, радиочастотную абляцию и чрескожную микроволновую коагуляционную терапию; катетеризацию, такую как чрескатетерная артериальная эмболизация или терапия с инфузией в печеночную артерию с использованием имплантированного резервуара, и химиотерапию, такую как терапия с использованием лекарственных средств, нацеленных на молекулярные мишени. Однако даже на современной стадии, когда доступны эти виды терапии, гепатоклеточная карцинома возобновляется с высокой частотой. В частности, в течение 2 лет со времени установления диагноза внутрипеченочный рецидив (вторичный канцерогенез) наблюдают у 28,8% пациентов с гепатоклеточной карциномой (непатентный документ 1), и повторение рецидива приводит к гибели многих пациентов. По этой причине, в дополнение к раннему выявлению и лечению гепатоклеточной карциномы, ингибирование перехода от хронического гепатита к гепатоклеточной карциноме и ингибирование рецидивов гепатоклеточной карциномы после их лечения, как считается, становятся важными проблемами, и терапия, положительно ингибирующая рецидивы гепатоклеточной карциномы в печени после ее лечения, считается очень важной. Однако в настоящее время нет установленных терапевтических способов ингибирования рецидивов гепатоклеточной карциномы.
В то же время одно из фармацевтических средств, используемых при химиотерапии гепатоклеточной карциномы, представляет собой лекарственное средство, нацеленное на молекулярную мишень, сорафениб (торговое наименование: Nexavar (зарегистрированная торговая марка)). Это лекарственное средство используют только при системной химиотерапии для неоперабельной гепатоклеточной карциномы, и при этом сообщается о различных тяжелых вредных побочных воздействиях. В дополнение к этому, не существует установленной эффективности и безопасности вспомогательной химиотерапии после хирургической или местной лекарственной терапии для гепатоклеточной карциномы. По этой причине имеется насущная потребность в эффективном и безопасном лекарственном средстве, которое можно использовать после хирургической или местной лекарственной терапии для гепатоклеточной карциномы.
Поскольку другое соединение, (2E,4E,6E,10E)-3,7,11,15-тетраметилгексадека-2,4,6,10,14-пентаеновая кислота (далее может упоминаться как "перетиноин"), как показано, обладает ингибиторным действием на рецидив гепатоклеточной карциномы, из клинических исследований следует, что рецидив гепатоклеточной карциномы после ее радикального лечения значительно ингибируется посредством долговременного введения этого соединения в течение одного года. В дополнение к этому, перетиноин по существу не вызывает расстройств печени и не дает значительных вредных побочных воздействий, которые дают другие ретиноиды, тем самым он служит как безопасное лекарственное средство (непатентный документ 2).
В то же время аминокислоты с разветвленной цепью используют для облегчения энцефалопатии, сопутствующей хроническим расстройствам печени, для облегчения гипоальбуминемии пациентов с декомпенсированным циррозом, которые страдают от гипоальбуминемии даже при условиях достаточной диеты, и для облегчения других состояний. Сообщается также, что лекарственное средство, содержащее три аминокислоты с разветвленной цепью, изолейцин, лейцин и валин, обладают ингибиторным воздействием на появление и развитие гепатоклеточной карциномы у пациентов с циррозом, возникающим в результате HCV. Однако указанное выше исследование ограничивается пациентами-мужчинами в возрасте 25-75 лет, и не сообщается о воздействиях по отношению к пациентам-женщинам или пациентам-мужчинам вне этого диапазона возрастов. В дополнение к этому, это сообщение не может описать или доказать, что эти лекарственные средства являются эффективными при ингибировании рецидива гепатоклеточной карциномы после ее радикального лечения (Патентный документ 1). Кроме того, имеется сообщение, описывающее, что лекарственное средство, содержащее аминокислоты с разветвленной цепью, не является сильнодействующим при ингибировании рецидивов гепатоклеточной карциномы после ее радикального лечения, с точки зрения либо кумулятивной частоты рецидивов рака, либо частоты выживания (Непатентный документ 3). Таким образом, показано, что ингибирование рецидива гепатоклеточной карциномы после ее лечения является более сложным, чем ингибирование появления и развития гепатоклеточной карциномы.
Документы, известные из литературы
Патентные документы
Патентный документ 1: WO2006/006729
Непатентные документы
Непатентный документ 1: 18th Follow-Up Survey Report of Primary Liver Cancer, Liver Cancer Study Group of Japan (2009)
Непатентный документ 2: N. Eng. J. Med. 334(24), 1561-1567 (1996)
Непатентный документ 3: Br. J. Surg. 84, 1525-1531 (1997)
Сущность изобретения
Проблемы, которые должны решаться с помощью изобретения
Настоящее изобретение относится к получению фармацевтического средства, пригодного для предотвращения и/или лечения гепатоклеточной карциномы.
Средства для решения проблемы
Авторы настоящего изобретения осуществили широкие исследования для решения указанной выше проблемы и обнаружили, что использование ациклического ретиноида, такого как перетиноин, в сочетании с аминокислотой с разветвленной цепью, приводит к значительному ингибиторному воздействию на рецидив гепатоклеточной карциномы после ее лечения, при этом сочетание ациклического ретиноида и аминокислоты с разветвленной цепью может служить в качестве фармацевтического средства, пригодного для предотвращения и/или лечения гепатоклеточной карциномы. Настоящее изобретение осуществлено на основе этих данных.
В частности, настоящее изобретение предлагает фармацевтическое средство для предотвращения и/или лечения гепатоклеточной карциномы, средство содержит ациклический ретиноид, его соль или сольват любого из них, в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них.
Настоящее изобретение направлено на следующее.
[1] Фармацевтическое средство для предотвращения и/или лечения гепатоклеточной карциномы, средство содержит ациклический ретиноид, его соль или сольват любого из них, в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них.
[2] Фармацевтическое средство, как описано в [1] выше, где ациклический ретиноид представляет собой перетиноин.
[3] Фармацевтическое средство, как описано в [1] или [2] выше, где аминокислота с разветвленной цепью содержит сочетание изолейцина, лейцина и валина.
[4] Фармацевтическое средство, как описано в любом из [1]-[3] выше, где предотвращение и/или лечение гепатоклеточной карциномы представляет собой ингибирование рецидива гепатоклеточной карциномы после ее лечения.
[5] Фармацевтическое средство, как описано в любом из [1]-[4] выше, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
[6] Фармацевтическое средство, как описано в [5] выше, где вирус гепатита представляет собой вирус гепатита C или вирус гепатита B.
[7] Фармацевтическое средство, как описано в любом из [1]-[6] выше, которое находится в форме одного препарата (сочетанного лекарственного средства), содержащего ациклический ретиноид, его соль или сольват любого из них, в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них.
[8] Фармацевтическое средство, как описано в любом из [1]-[6] выше, которое находится в форме набора препаратов, содержащего препарат, содержащий ациклический ретиноид, его соль или сольват любого из них, в сочетании с препаратом, содержащим аминокислоту с разветвленной цепью, ее соль или сольват любой из них.
[9] Фармацевтическое средство содержит ациклический ретиноид, его соль или сольват любого из них, которое должно вводиться в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них, для предотвращения и/или лечения гепатоклеточной карциномы.
[10] Фармацевтическое средство, как описано в [9] выше, которое находится в форме набора, содержащего следующие компоненты (1) и (2):
(1) фармацевтическое средство для предотвращения и/или лечения гепатоклеточной карциномы, средство содержит ациклический ретиноид, его соль или сольват любого из них; и
(2) инструкцию, которая описывает введение фармацевтического средства, которое должно вводиться в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них.
[11] Фармацевтическое средство, содержащее аминокислоту с разветвленной цепью, ее соль или сольват любой из них, которое должно вводиться в сочетании с ациклическим ретиноидом, его солью или сольватом любого из них, для предотвращения и/или лечения гепатоклеточной карциномы.
[12] Фармацевтическое средство, как описано в [11] выше, которое находится в форме набора, содержащего следующие компоненты (1) и (2):
(1) фармацевтическое средство для предотвращения и/или лечения гепатоклеточной карциномы, средство содержит аминокислоту с разветвленной цепью, ее соль или сольват любой из них; и
(2) инструкцию, которая описывает введение фармацевтического средства, которое должно вводиться в сочетании с ациклическим ретиноидом, его солью или сольватом любого из них.
[13] Фармацевтическое средство, как описано в любом из [9]-[12] выше, где ациклический ретиноид представляет собой перетиноин.
[14] Фармацевтическое средство, как описано в любом из [9]-[13] выше, где аминокислота с разветвленной цепью содержит сочетание изолейцина, лейцина и валина.
[15] Фармацевтическое средство, как описано в любом из [9]-[14] выше, где предотвращение и/или лечение гепатоклеточной карциномы представляет собой ингибирование рецидива гепатоклеточной карциномы после ее лечения.
[16] Фармацевтическое средство, как описано в любом из [9]-[15] выше, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
[17] Фармацевтическое средство, как описано в [16] выше, где вирус гепатита представляет собой вирус гепатита C или вирус гепатита B.
[18] Способ предотвращения и/или лечения гепатоклеточной карциномы, включающий введение эффективного количества ациклического ретиноида, его соли или сольвата любого из них и эффективного количества аминокислоты с разветвленной цепью, ее соли или сольвата любой из них, пациенту, нуждающемуся в этом, одновременно или раздельно, в различные моменты времени.
[19] Способ, как описано в [18] выше, где ациклический ретиноид представляет собой перетиноин.
[20] Способ, как описано в [18] или [19] выше, где аминокислота с разветвленной цепью включают сочетание изолейцина, лейцина и валина.
[21] Способ, как описано в любом из [18]-[20] выше, где предотвращение и/или лечение гепатоклеточной карциномы представляет собой ингибирование рецидива гепатоклеточной карциномы после ее лечения.
[22] Способ, как описано в любом из [18]-[21] выше, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
[23] Способ, как описано в [22] выше, где вирус гепатита представляет собой вирус гепатита C или вирус гепатита B.
[24] Применение ациклического ретиноида, его соли или сольвата любого из них, в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них, для получения фармацевтического средства для предотвращения и/или лечения гепатоклеточной карциномы.
[25] Применение, как описано в [24] выше, где ациклический ретиноид представляет собой перетиноин.
[26] Применение, как описано в [24] или [25] выше, где аминокислота с разветвленной цепью содержит сочетание изолейцина, лейцина и валина.
[27] Применение, как описано в любом из [24]-[26] выше, где предотвращение и/или лечение гепатоклеточной карциномы представляет собой ингибирование рецидива гепатоклеточной карциномы после ее лечения.
[28] Применение, как описано в любом из [24]-[27] выше, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
[29] Применение, как описано в [28] выше, где вирус гепатита представляет собой вирус гепатита C или вирус гепатита B.
[30] Ациклический ретиноид, его соль или сольват любого из них, который должен вводиться в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них, для предотвращения и/или лечения гепатоклеточной карциномы.
[31] Ациклический ретиноид, его соль или сольват любого из них, как описано в [30] выше, где ациклический ретиноид представляет собой перетиноин.
[32] Ациклический ретиноид, его соль или сольват любого из них, как описано в [30] или [31] выше, где аминокислота с разветвленной цепью содержит сочетание изолейцина, лейцина и валина.
[33] Ациклический ретиноид, его соль или сольват любого из них, как описано в любом из [30]-[32] выше, где предотвращение и/или лечение гепатоклеточной карциномы представляет собой ингибирование рецидива гепатоклеточной карциномы после ее лечения.
[34] Ациклический ретиноид, его соль или сольват любого из них, как описано в любом из [30]-[33] выше, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
[35] Ациклический ретиноид, его соль или сольват любого из них, как описано в [34] выше, где вирус гепатита представляет собой вирус гепатита C или вирус гепатита B.
[36] Аминокислота с разветвленной цепью, ее соль или сольват любой из них, которая должна вводиться в сочетании с ациклическим ретиноидом, его солью или сольватом любого из них, для предотвращения и/или лечения гепатоклеточной карциномы.
[37] Аминокислота с разветвленной цепью, ее соль или сольват любой из них, как описано в [36] выше, где ациклический ретиноид представляет собой перетиноин.
[38] Аминокислота с разветвленной цепью, ее соль или сольват любой из них, как описано в [36] или [37] выше, где аминокислота с разветвленной цепью содержит сочетание изолейцина, лейцина и валина.
[39] Аминокислота с разветвленной цепью, ее соль или сольват любой из них, как описано в любом из [36]-[38] выше, где предотвращение и/или лечение гепатоклеточной карциномы представляет собой ингибирование рецидива гепатоклеточной карциномы после ее лечения.
[40] Аминокислота с разветвленной цепью, ее соль или сольват любой из них, как описано в любом из [36]-[39] выше, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
[41] Аминокислота с разветвленной цепью, ее соль или сольват любой из них, как описано в [40] выше, где вирус гепатита представляет собой вирус гепатита C или вирус гепатита B.
Эффекты изобретения
Настоящее изобретение делает возможным получение превосходного фармацевтического средства для предотвращения и/или лечения гепатоклеточной карциномы. В частности, фармацевтическое средство по настоящему изобретению демонстрирует замечательное ингибиторное воздействие на рецидив гепатоклеточной карциномы после ее лечения, чтобы тем самым уменьшить частоту рецидивов гепатоклеточной карциномы, которые имеют плохой прогноз.
Краткое описание чертежа
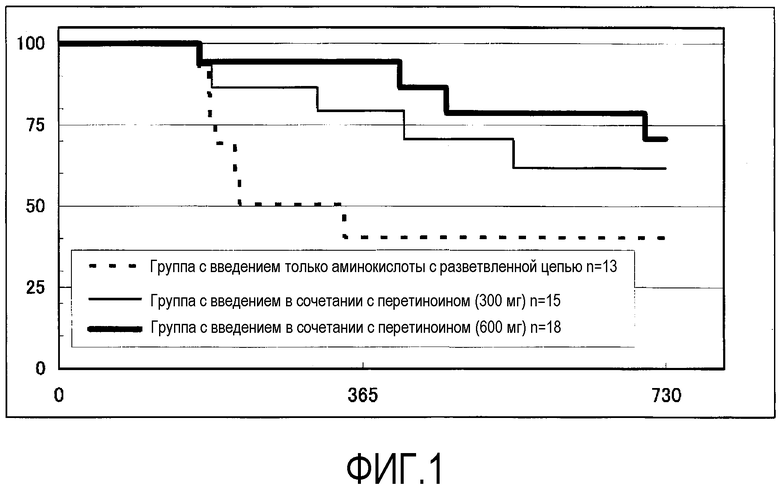
[Фиг.1] График, показывающий соотношение между кумулятивным временем без рецидивов и объединенным воздействием, где горизонтальная ось обозначает дни, прошедшие от исследования, а вертикальная ось обозначает кумулятивное время без данного (%) рецидивов.
Способы осуществления изобретения
Определения терминов, используемых в настоящем описании, являются такими, как следует далее. Если не указано иного, все технические и научные термины, используемые в описании, должны иметь значения, как правило, понимаемые специалистами в данной области, к которой относится настоящее изобретение.
В одном из вариантов осуществления настоящего изобретения предлагается фармацевтическое средство для предотвращения и/или лечения гепатоклеточной карциномы, средство содержит ациклический ретиноид, его соль или сольват любого из них, в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них (далее, фармацевтическое средство может упоминаться как "комбинированное фармацевтическое средство по настоящему изобретению"). А именно, комбинированное фармацевтическое средство по настоящему изобретению представляет собой фармацевтическое средство для предотвращения и/или лечения гепатоклеточной карциномы; и ациклический ретиноид, его соль или сольват любого из них, и эффективное количество аминокислоты с разветвленной цепью, ее соли или сольвата любой из них могут вводиться пациенту, нуждающемуся в этом, одновременно или раздельно, в различные моменты времени.
Класс ретиноидов включает витамин A (ретинол) и его гомологические соединения. Эти соединения вовлечены в морфогенез, дифференциацию клеток, контроль пролиферации клеток, и тому подобное, в организме. С точки зрения их структуры, ретиноиды классифицируются как циклические ретиноиды и ациклические ретиноиды (ретиноид/каротеноид, 14-20 (1997), опубликовано Nanzan-Do). Примеры циклического ретиноида включают указанный выше ретинол, ретиналь, полностью транс-ретиноевую кислоту (третиноин), 9-цис-ретиноевую кислоту (алитретиноин) и 13-цис-ретиноевую кислоту (изотретиноин). В широком смысле, класс ретиноидов включает синтетические соединения, демонстрирующие сродство связывания с рецептором ретиноевой кислоты, даже если соединения имеют химическую структуру, полностью отличающуюся от структуры витамина A.
В настоящем изобретении термин "ациклический ретиноид" относится, среди указанных выше ретиноидов в более широком смысле, к ретиноиду, не имеющему циклической структуры в своей молекуле. Конкретные примеры ациклического ретиноида включает геранилгераниевую кислоту, перетиноин, 2,3-дигидрогеранилгераниевую кислоту, 4,5-дидегидро-10,11-дигидрогеранилгераниевую кислоту, 4,5,8,9-тетрадегидрогеранилгераниевую кислоту, 4,5-дидегидро-10,11,14,15-тетрагидрогеранилгераниевую кислоту, 14,15-дигидрогеранилгераниевую кислоту, метапреновую кислоту, гидропреновую кислоту и фитановую кислоту. Эти ациклические ретиноиды можно использовать раздельно или в сочетании двух или более видов. А именно, геранилгераниевая кислота, которая является элементом ациклических ретиноидов и представляет собой компонент, содержащийся в лекарственных растениях, как известно, повышает уровень керамидов мембранных липидов и индуцирует апоптоз раковых клеток печени, возможно, служа тем самым в качестве профилактического и терапевтического средства против рака (J. Lipid Res., 45 1092-1103 (2004)).
В настоящем изобретении можно также использовать соль ациклического ретиноида. Когда ациклический ретиноид служит в качестве основного соединения, примеры его соли включают кислотно-аддитивные соли с неорганической кислотой (например, хлористо-водородной кислотой, бромисто-водородной кислотой, йодисто-водородной кислотой, серной кислотой, азотной кислотой или фосфорной кислотой) или с органической кислотой (например, муравьиной кислотой, уксусной кислотой, пропионовой кислотой, щавелевой кислотой, малоновой кислотой, янтарной кислотой, фумаровой кислотой, малеиновой кислотой, молочной кислотой, яблочной кислотой, винной кислотой, лимонной кислотой, метансульфоновой кислотой, этансульфоновой кислотой, п-толуолсульфоновой кислотой, аспарагиновой кислотой или глютаминовой кислотой). Когда ациклический ретиноид служит в качестве кислотного соединения, примеры соли включают неорганические соли (например, соли натрия, соли калия, соли лития, соли бария, соли кальция и соли магния) и органические соли (например, соли пиридиния, соли пиколиния и соли триэтиламмония).
В настоящем изобретении можно также использовать сольват ациклического ретиноида или сольват соли ациклического ретиноида. Не накладывается никаких особенных ограничений на растворитель, который образует сольват, и можно использовать воду или физиологически приемлемый органический растворитель (например, этанол, ацетон, этилацетат или гексан).
Когда используют несколько видов ациклических ретиноидов в сочетании, соли ретиноидов или их сольваты могут быть идентичными или отличными друг от друга.
Указанный выше ациклический ретиноид, его соль и сольват любого из них, в частности указанные выше соединения, все они являются известными соединениями и могут быть получены с помощью известного способа. Например, перетиноин может быть получен с помощью способа, описанного в JP-A-1981-140949. Альтернативно, в настоящем изобретении можно также использовать коммерческие продукты ациклических ретиноидов.
В настоящем изобретении "ациклический ретиноид, его соль или сольват любого из них" предпочтительно представляет собой перетиноин, его соль или сольват любого из них, особенно предпочтительно, перетиноин.
В настоящем изобретении примеры "аминокислоты с разветвленной цепью" включают α-аминокислоты, имеющие разветвленный углерод в боковой цепи изолейцина, лейцина, валина, и тому подобное. В настоящем изобретении эти аминокислоты можно использовать раздельно или в сочетании двух или более видов. Также, аминокислота с разветвленной цепью может находиться в D-форме, L-форме или представлять собой их смесь. В настоящем изобретении предпочтительной является L-форма.
В настоящем изобретении также можно использовать соль аминокислоты с разветвленной цепью. Когда аминокислота с разветвленной цепью служит в качестве основного соединения, примеры соли включают кислотно-аддитивные соли с неорганической кислотой (например, хлористо-водородной кислотой, бромисто-водородной кислотой, йодисто-водородной кислотой, серной кислотой, азотной кислотой или фосфорной кислотой) или с органической кислотой (например, муравьиной кислотой, уксусной кислотой, пропионовой кислотой, щавелевой кислотой, малоновой кислотой, янтарной кислотой, фумаровой кислотой, малеиновой кислотой, молочной кислотой, яблочной кислотой, винной кислотой, лимонной кислотой, метансульфоновой кислотой, этансульфоновой кислотой, п-толуолсульфоновой кислотой, аспарагиновой кислотой или глютаминовой кислотой). Когда аминокислота с разветвленной цепью служит в качестве кислотного соединения, примеры соли включают основно-аддитивные соли, такие как неорганические соли (например, соли натрия, соли калия, соли лития, соли бария, соли кальция и соли магния) и органические соли (например, соли пиридиния, соли пиколиния и соли триэтиламмония).
В настоящем изобретении можно также использовать сольват аминокислоты с разветвленной цепью или сольват соли аминокислоты с разветвленной цепью. Не накладывается никаких особенных ограничений на растворитель, который образует сольват, и можно использовать воду или физиологически приемлемый органический растворитель (например, этанол, ацетон, этилацетат или гексан).
Когда используют несколько видов аминокислот с разветвленной цепью в сочетании, соли аминокислот с разветвленной цепью или их сольваты могут быть идентичными или отличными друг от друга.
Указанная выше аминокислота с разветвленной цепью, ее соль, и сольват любой из них представляют собой известные соединения и могут быть получены с помощью известного способа. Альтернативно, можно также использовать коммерческие продукты аминокислот с разветвленной цепью.
В настоящем изобретении "аминокислота с разветвленной цепью, ее соль или сольват любой из них" предпочтительно представляет собой аминокислоту с разветвленной цепью, содержащую, по меньшей мере, одну кислоту, выбранную из группы, состоящей из изолейцина, лейцина и валина, их соли или сольвата любой из них, более предпочтительно, аминокислоту с разветвленной цепью, содержащую три аминокислоты: изолейцин, лейцин и валин, их соль или сольват любой из них, особенно предпочтительно, аминокислоту с разветвленной цепью, состоящую из трех аминокислот: изолейцина, лейцина и валина. Когда аминокислота с разветвленной цепью, ее соль или сольват любой из них содержит изолейцин, лейцин и валин, не накладывается никаких особенных ограничений на композиционные пропорции между этими тремя компонентами. Предпочтительно, массовые пропорции изолейцина (свободная форма):лейцина (свободная форма):валина (свободная форма) составляют от 1:0,5 до 3:0,4 до 2, более предпочтительно от 1:1 до 2:0,8 до 1,4.
В одном из предпочтительных вариантов осуществления настоящего изобретения "аминокислота с разветвленной цепью, ее соль или сольват любой из них" имеет массовые композиционные пропорции среди трех аминокислот с разветвленной цепью (то есть изолейцина, лейцина и валина), составляющие: изолейцин (свободная форма), 952 массовых частей: лейцин (свободная форма), 1904 массовых частей: валин (свободная форма), 1144 массовых частей. Отдельная композиция, содержащая изолейцин (свободную форму), лейцин (свободную форму) и валин (свободную форму) при указанных выше массовых пропорциях, является особенно предпочтительной. Композиция может быть получена с помощью известного способа как пероральный препарат или парентеральный препарат.
Особенно предпочтительно, композиция содержит изолейцин (952 мг), лейцин (1904 мг) и валин (1144 мг). Предпочтительно, композиция вводится три раза в день. Хотя композиция может быть получена с помощью известного способа, можно использовать коммерческий продукт композиции (например, изолейцин (952 мг), лейцин (1904 мг) и валин (1144 мг) в одной упаковке). Примеры коммерческого продукта включают комбинированные гранулы Aminovact (зарегистрированное торговое наименования) (продукт Nichi-Iko Pharmaceutical Co., Ltd.), комбинированные гранулы Aminomylan (продукт Mylan Seiyaku), комбинированные гранулы Coveneal (зарегистрированное торговое наименования) (продукт Yoshindo Inc.), гранулы Branute (зарегистрированное торговое наименования) (продукт Nihon Pharmaceutical Co., Ltd.), комбинированные гранулы Hepaact (зарегистрированное торговое наименования) (продукт Toa Pharmaceuticals Co., Ltd.), комбинированные гранулы Lickle (зарегистрированное торговое наименования) (продукт Sawai Pharmaceutical Co., Ltd.), комбинированные гранулы Livact (зарегистрированное торговое наименования) (продукт Ajinomoto Pharmaceuticals Co., Ltd.), комбинированные гранулы Liverevan (зарегистрированное торговое наименования) (продукт Medisa Shinyaku Inc.) и комбинированные гранулы Leovacton (зарегистрированное торговое наименования) (в разделенных дозах) (продукт Choseido Pharmaceutical Co., Ltd.). Любой из указанных выше коммерческих продуктов предпочтительно вводится, три раза в день, в одной упаковке как одна доза.
В настоящем изобретении не накладывается никаких особенных ограничений на отношение количества ациклического ретиноида, его соли или сольвата любого из них к количеству аминокислоты с разветвленной цепью, ее соли или сольвата любой из них, и отношение может подбираться соответствующим образом с тем, чтобы можно было получить представляющее интерес воздействие на предотвращение и/или лечение гепатоклеточной карциномы. В случае, когда ациклический ретиноид представляет собой перетиноин, а аминокислота с разветвленной цепью содержит изолейцин, лейцин и валин, их соль или сольват любого из них, общее количество изолейцина (свободная форма), лейцина (свободная форма) и валина (свободная форма) предпочтительно составляет от 1 до 5000 массовых частей, по отношению к 1 доле массовой перетиноина (свободная форма), более предпочтительно, от 5 до 200 массовых частей, особенно предпочтительно, от 10 до 100 массовых частей.
В настоящем изобретении выражение "предотвращение и/или лечение гепатоклеточной карциномы" относится к концепции, охватывающей предотвращение появления гепатоклеточной карциномы, ингибирование развития гепатоклеточной карциномы, лечение гепатоклеточной карциномы и ингибирование рецидива гепатоклеточной карциномы после ее лечения. Фармацевтическое средство по настоящему изобретению можно соответствующим образом использовать в качестве фармацевтического средства для ингибирования рецидива гепатоклеточной карциномы после ее лечения, в частности, для ингибирования рецидива гепатоклеточной карциномы после ее радикального лечения. При "ингибировании рецидива гепатоклеточной карциномы после ее лечения" примеры терапевтического способа против гепатоклеточной карциномы включают хирургическую терапию, такую как гепатэктомия, полная трансплантация печени и частичная трансплантация печени; чрескожную местную терапию, такую как чрескожная терапия с инъекцией этанола (PEIT), чрескожную терапию с микроволновой коагуляцией (PMCT) и радиочастотную абляцию (RFA); чрескатетерную артериальную инфузию (TAI); чрескатетерную артериальную эмболизацию (TAE), при которой артериальную эмболизацию осуществляют с помощью эмболизирующего вещества, такого как желатиновая губка, пористые желатиновые гранулы, Embosephere (трисакриловые-желатиновые сферические частицы), суперпоглощающие полимерные микросферы (SAP-MS), HepaSphere, Embozene (акриловый гидрогель, обработанный с помощью специального фтористого покрытия) или поливиниловый спирт; чрескатетерную артериальную химиоэмболизацию (TACE), при которой эмболизацию осуществляют посредством использования противоракового средства, такого как эпирубицин гидрохлорид, цисплатин, доксорубицин гидрохлорид или митомицин C, и посредством использования указанного выше эмболизирующего вещества после липидизации или посредством использования шариков, элюирующих лекарственное средство (противораковое средство) (DEB); и фармакотерапию, использующую глицирризиновую кислоту, shosaikoto, интерферон, пегинтерферон, рибавирин, 5-фторурацил, цисплатин, оксалиплатин, доксорубицин гидрохлорид, эпирубицин гидрохлорид, митоксантрон гидрохлорид, этопозид, иринотекан гидрохлорид, гемцитабин гидрохлорид, доцетаксель гидрат, сорафениб тозилат, эрлотиниб гидрохлорид, питавастатин кальция, и тому подобное.
Фармацевтическое средство по настоящему изобретению может вводиться до и после предотвращения/лечения гепатоклеточной карциномы или в ходе его. Не накладывается никаких особенных ограничений на способ терапии гепатоклеточной карциномы, и можно использовать указанные выше способы. Можно объединить два или более способов. По настоящему изобретению хирургическая терапия и местное лекарственное лечения являются предпочтительными.
В настоящем изобретении не накладывается никаких особенных ограничений на причину гепатоклеточной карциномы, и примеры таких причин включают хронический гепатит и цирроз (вирусный, алкогольный, от ожирения печени, неалкогольный). Настоящее изобретение может соответствующим образом применяться к гепатоклеточной карциноме, вызываемой вирусом гепатита или неалкогольным стеатогепатитом, более целесообразно, к гепатоклеточной карциноме, вызываемой вирусом гепатита (предпочтительно, к гепатоклеточной карциноме, положительной по вирусу гепатита), еще более целесообразно, к гепатоклеточной карциноме, вызываемой, по меньшей мере, одним вирусом, выбранным из группы, состоящей из вируса гепатита B и вируса гепатита C (предпочтительно, к гепатоклеточной карциноме положительной, по меньшей мере, по одному вирусу, выбранному из группы, состоящей из вируса гепатита B и вируса гепатита C), особенно целесообразно, к гепатоклеточной карциноме, вызываемой вирусом гепатита C (предпочтительно, к гепатоклеточной карциноме, положительной по вирусу гепатита C). Как конкретно описано в Примере, фармацевтическое средство по настоящему изобретению демонстрирует превосходное ингибиторное воздействие на рецидивы в отношении пациентов после лечения гепатоклеточной карциномы, вызываемой вирусом гепатита, таким как вирус гепатита C, тем самым улучшая прогноз. По этой причине фармацевтическое средство по настоящему изобретению может особенно целесообразно применяться для ингибирования рецидивов гепатоклеточной карциномы, вызываемой вирусом гепатита, таким как вирус гепатита C, после ее лечения.
В дополнение к этому, поскольку фармацевтическое средство по настоящему изобретению может ингибировать рецидивы гепатоклеточной карциномы после ее лечения, может быть предотвращено дальнейшее вмешательство при лечении рецидива гепатоклеточной карциномы. Таким образом, фармацевтическое средство по настоящему изобретению может целесообразно применяться в качестве фармацевтического средства для ингибирования рецидивов гепатоклеточной карциномы после ее лечения.
Фармацевтическое средство по настоящему изобретению может дополнительно содержать, в дополнение к ациклическому ретиноиду, его соль или сольват любого из них, и аминокислоту с разветвленной цепью, ее соль или сольват любой из них, "аминокислоту с неразветвленной цепью, ее соль или сольват любой из них". Могут вводиться ингредиенты, комбинированные таким образом.
В настоящем изобретении примеры "аминокислоты с неразветвленной цепью" включают аминокислоты, иные, чем указанная выше "аминокислота с разветвленной цепью", такие как глицин, аланин, серин, треонин, аспарагиновая кислота, глютаминовая кислота, лизин, аргинин, цистеин, цистин, метионин, фенилаланин, тирозин, триптофан, гистидин и пролин. Эти аминокислоты можно использовать раздельно или в сочетании двух или более видов. Среди них, глицин, аланин, серин, треонин, лизин, аргинин, метионин, фенилаланин, триптофан, гистидин и пролин являются предпочтительными в качестве аминокислот с неразветвленной цепью, используемых в настоящем изобретении. Аминокислота с неразветвленной цепью может находиться в D-форме, L-форме или представлять собой их смесь, и среди них, предпочтительной является L-форма.
В настоящем изобретении можно использовать соль аминокислоты с неразветвленной цепью. Можно также использовать такой же тип солей, как рассмотрено по отношению к аминокислотам с разветвленной цепью. Также можно использовать сольват аминокислоты с неразветвленной цепью или сольват соли аминокислоты с неразветвленной цепью. Можно также использовать такой же тип сольватов, как рассмотрено по отношению к аминокислотам с разветвленной цепью.
Когда используют несколько видов аминокислот с неразветвленной цепью в сочетании, соли или сольваты аминокислоты с неразветвленной цепью могут быть идентичными или отличными друг от друга. Аминокислота с неразветвленной цепью, ее соль и сольват любой из них представляют собой известные соединения и могут быть получены с помощью известного способа. Альтернативно, можно также использовать коммерческие продукты аминокислот с неразветвленной цепью.
В настоящем изобретении, в случае, когда аминокислота с неразветвленной цепью, ее соль или сольват любой из них, вводится вместе с основными ингредиентами, можно использовать композицию, содержащую, по меньшей мере, аминокислоту с разветвленной цепью, ее соль или сольват любой из них, и аминокислоту с неразветвленной цепью, ее соль или сольват любой из них.
Конкретные примеры таких композиций включают следующие (i)-(iii).
(i) Композиция, содержащая изолейцин (0,9 массовых частей), лейцин (1,1 массовых частей) и валин (0,84 массовых частей); и треонин (0,45 массовых частей), серин (0,5 массовых частей), пролин (0,8 массовых частей), цистеин гидрохлорид гидрат (0,04 массовых частей, 0,03 массовых частей цистеина), глицин (0,9 массовых частей), аланин (0,75 массовых частей), метионин (0,1 массовых частей), фенилаланин (0,1 массовых частей), триптофан (0,07 массовых частей), лизин гидрохлорид (0,76 массовых частей, 0,61 массовых частей лизина), гистидин гидрохлорид (0,32 массовых частей, 0,24 массовых частей гистидина) и аргинин гидрохлорид (0,73 массовых частей, 0,6 массовых частей аргинина).
Композиция может быть получена с помощью известного способа в качестве перорального препарата или парентерального препарата. Можно также использовать коммерческий продукт композиции.
Другой предпочтительный вариант осуществления настоящего изобретения представляет собой парентеральную композицию (парентеральный препарат), содержащий изолейцин (0,9% масс/объем), лейцин (1,1% масс/объем) и валин (0,84% масс/объем), и аминокислоты с неразветвленной цепью: треонин (0,45% масс/объем, серин (0,5% масс/объем), пролин (0,8% масс/объем), цистеин гидрохлорид гидрат (0,04% масс/объем, 0,03% масс/объем цистеина), глицин (0,9% масс/объем), аланин (0,75% масс/объем), метионин (0,1% масс/объем), фенилаланин (0,1% масс/объем), триптофан (0,07% масс/объем), лизин гидрохлорид (0,76% масс/объем, 0,61% масс/объем лизина), гистидин гидрохлорид (0,32% масс/объем, 0,24% масс/объем гистидина), и аргинин гидрохлорид (0,73% масс/объем, 0,6% масс/объем аргинина). Можно также использовать коммерческие продукты композиции для инъекции, такие как препарат для внутривенных вливаний Aminoleban (зарегистрированное торговое наименования) (продукт Otsuka Pharmaceutical Factory, Inc.), препарат для внутривенных вливаний Terufis (зарегистрированное торговое наименования) (продукт Terumo Corporation), препарат для инъекций Hikarilevan (зарегистрированное торговое наименования) (продукт Hikari Pharmaceutical Co., Ltd.) и препарат для внутривенных вливаний Morihepamin (зарегистрированное торговое наименования) (продукт Ajinomoto Pharmaceuticals Co., Ltd.). Указанный выше препарат для внутривенных вливаний Aminoleban предпочтительно вводят как одну дозу из 500-1000 мл. Препарат для внутривенных вливаний Terufis предпочтительно вводят как одну дозу из 500-1000 мл. Препарат для внутривенных вливаний Hikarilevan предпочтительно вводят как одну дозу из 500-1000 мл. Препарат для внутривенных вливаний Morihepamin предпочтительно вводят как одну дозу из 500 мл.
(ii) Композиция, содержащая изолейцин (1,9225 массовых частей), лейцин (2,037 массовых частей) и валин (1,602 массовых частей); и лизин гидрохлорид (0,2425 массовых частей), треонин (0,133 массовых частей), аргинин гидрохлорид (0,302 массовых частей), гистидин гидрохлорид (0,1875 массовых частей) и триптофан (0,0735 массовых частей).
Композиция может быть получена с помощью известного способа как пероральный препарат или парентеральный препарат. Также можно использовать коммерческий продукт композиции, такой как EN комбинированный порошок Aminoleban (зарегистрированное торговое наименования) (продукт Otsuka Pharmaceutical Co., Ltd.), одна упаковка которого (50 г) содержит изолейцин (1,9225 г), лейцин (2,037 г) и валин (1,602 г); и лизин гидрохлорид (0,2425 г), треонин (0,133 г), аргинин гидрохлорид (0,302 г), гистидин гидрохлорид (0,1875 г) и триптофан (0,0735 г). EN комбинированный порошок Aminoleban предпочтительно вводят три раза в день как одну дозу из одной упаковки.
(iii) Не содержащая BCAA композиция, содержащая изолейцин (1730 массовых частей), лейцин (2122 массовых частей) и валин (1615 массовых частей); и лизин гидрохлорид (974 массовых частей), метионин (117 массовых частей), фенилаланин (117 массовых частей), треонин (436 массовых частей), триптофан (56 массовых частей), гистидин (306 массовых частей), аргинин (1647 массовых частей), аргинин гидрохлорид (108 массовых частей), аланин (978 массовых частей), глицин (430 массовых частей), пролин (522 массовых частей) и серин (257 массовых частей).
Композиция может быть получена с помощью известного способа как пероральный препарат или парентеральный препарат. Также можно использовать коммерческий продукт композиции, такой как комбинированное внутреннее лекарственное средство Hepan ED (зарегистрированное торговое наименования) (продукт Ajinomoto Pharmaceuticals Co., Ltd.), одна упаковка которого (80 г) содержит изолейцин (1730 мг), лейцин (2122 мг) и валин (1615 мг); и лизин гидрохлорид (974 мг), метионин (117 мг), фенилаланин (117 мг), треонин (436 мг), триптофан (56 мг), гистидин (306 мг), аргинин (1647 мг), аргинин гидрохлорид (108 мг), аланин (978 мг), глицин (430 мг), пролин (522 мг) и серин (257 мг). Комбинированное внутреннее лекарственное средство Hepan ED предпочтительно вводят дважды в день как одну дозу из одной упаковки.
Дополнительные неограничивающие примеры композиции, содержащей разветвленные аминокислоты, включают Aminosyn (продукт HOSPIRA), Branchamin (продукт BAXTER HEALTHCARE), Hepatasol (продукт BAXTER HEALTHCARE), Novamine (продукт HOSPIRA), Prosol (продукт BAXTER HEALTHCARE) и Travasol (продукт BAXTER HEALTHCARE).
Не накладывается никаких особенных ограничений на форму комбинированного фармацевтического средства по настоящему изобретению, и конкретные примеры формы включают следующие (I) и (II):
(I) форма отдельного препарата (комбинированное лекарственное средство), содержащего ациклический ретиноид, его соль или сольват любого из них, в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них, и
(II) форма раздельного введения препарата, содержащего ациклический ретиноид, его соль или сольват любого из них, и препарата, содержащего аминокислоту с разветвленной цепью, ее соль или сольват любой из них.
В случае формы (II), препарат может вводиться пациенту, нуждающемуся в этом, одновременно или раздельно, в различные моменты времени с соответствующим интервалом, и можно использовать соответствующий режим дозирования с тем, чтобы можно было получить воздействие, представляющее интерес, на предотвращение и/или лечение гепатоклеточной карциномы. Форма для раздельного введения препарата, содержащего ациклический ретиноид, его соль или сольват любого из них, и препарата, содержащего аминокислоту с разветвленной цепью, ее соль или сольват любой из них, может быть предусмотрена как набор препаратов, содержащий два препарата в сочетании в одной упаковке.
Не накладывается никаких особенных ограничений на способ введения фармацевтического средства по настоящему изобретению, можно использовать либо пероральное введение, либо парентеральное введение. В случае указанной выше формы (II), один препарат может представлять собой пероральный препарат, а другой может представлять собой парентеральный препарат. Примеры перорального препарата включают таблетку, капсулу, гранулу, порошок и сироп, а примеры парентерального препарата включают препарат для инъекций, суппозиторий, ингаляцию, лекарственное средство для чрескожного поглощения, наружное лекарственное средство для кожи, капли для глаз и капли в нос. Среди этих форм для введения предпочтительными являются пероральные препараты, при этом таблетка, капсула, гранула, порошок, сироп и тому подобное являются особенно предпочтительными.
Такие пероральные препараты и парентеральные препараты могут быть получены вместе с известными добавками для приготовления лекарственных средств с помощью известного способа, описанного, например, в "The Japanese Pharmacopoeia 15th Edition, General Rules for Preparations".
Не накладывается никаких особенных ограничений на дозу фармацевтического средства по настоящему изобретению, и доза может устанавливаться соответствующим образом в зависимости от различных состояний, таких как возраст, масса тела и симптомы пациента, форма введения и частота введения. В случае, когда ациклический ретиноид представляет собой перетиноин, а аминокислота с разветвленной цепью содержит изолейцин, лейцин и валин, в сочетании, ежедневная доза перетиноина (свободная форма) для взрослого составляет от 10 мг до 10 г, предпочтительно от 100 мг до 5 г, более предпочтительно от 300 мг до 1 г, особенно предпочтительно от 500 мг до 900 мг. Подобным же образом, ежедневная доза аминокислоты с разветвленной цепью, как общее количество изолейцина (свободная форма), лейцина (свободная форма) и валина (свободная форма), составляет от 1 г до 50 г, предпочтительно от 5 г до 35 г, более предпочтительно от 10 г до 30 г. При введении доза может представлять собой ежедневную дозу или делиться на множество порций.
В другом варианте осуществления настоящего изобретения предлагается фармацевтическое средство, содержащее ациклический ретиноид, его соль или сольват любого из них, для ведения в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них, для предотвращения и/или лечения гепатоклеточной карциномы. Фармацевтическое средство по этому варианту осуществления содержит, в качестве ингредиента, ациклический ретиноид, его соль или сольват любого из них и вводится вместе с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них, пациенту, нуждающемуся в этом, одновременно или раздельно в различные моменты времени, для предотвращения и/или лечения гепатоклеточной карциномы. Конкретный пример фармацевтического средства этого варианта осуществления представляет собой набор для предотвращения и/или лечения гепатоклеточной карциномы,
набор содержит следующие компоненты (1) и (2):
(1) фармацевтическое средство для предотвращения и/или лечения гепатоклеточной карциномы, средство содержит ациклический ретиноид, его соль или сольват любого из них, и
(2) инструкцию, которая описывает введение фармацевтического средства, которое должно вводиться в сочетании с аминокислотой с разветвленной цепью, ее солью или сольватом любой из них. Конкретные примеры инструкции включают так называемое описание (вставку в упаковку), описывающее воздействие, эффективность, указание для применения, дозу и тому подобное.
В этом варианте осуществления значения терминов, количества ингредиентов, способов получения лекарственных средств и тому подобное являются такими же, как описано выше.
В другом варианте осуществления настоящего изобретения предлагается фармацевтическое средство, содержащее аминокислоту с разветвленной цепью, ее соль или сольват любой из них, которое должно вводиться в сочетании с ациклическим ретиноидом, его солью или сольватом любого из них, для предотвращения и/или лечения гепатоклеточной карциномы. Фармацевтическое средство по этому варианту осуществления содержит, в качестве ингредиента, аминокислоту с разветвленной цепью, ее соль или сольват любой из них и вводится вместе с ациклическим ретиноидом, его солью или сольватом любого из них, пациенту, нуждающемуся в этом, одновременно или раздельно в различные моменты времени, для предотвращения и/или лечения гепатоклеточной карциномы. Конкретный пример фармацевтического средства этого варианта осуществления представляет собой набор для предотвращения и/или лечения гепатоклеточной карциномы,
набор содержит следующие компоненты (1) и (2):
(1) фармацевтическое средство для предотвращения и/или лечения гепатоклеточной карциномы, средство содержит аминокислоту с разветвленной цепью, ее соль или сольват любой из них; и
(2) инструкцию, которая описывает введение фармацевтического средства, которое должно вводиться в сочетании ациклическим ретиноидом, его солью или сольватом любого из них. Конкретные примеры инструкции включают так называемое описание (вставку в упаковку), описывающее воздействие, эффективность, указание для применения, дозу и тому подобное.
Значения терминов, количества ингредиентов, способы получения лекарственных средств и тому подобное являются такими же, как описано выше.
Примеры
Настоящее изобретение будет теперь описываться более подробно с помощью примеров, которые не должны рассматриваться в качестве ограничивающих настоящее изобретение.
Пример 1
[Используемые лекарственные средства]
В качестве ациклического ретиноида используют перетиноин, полученный с помощью известного способа. В качестве аминокислоты с разветвленной цепью используют коммерческий препарат, содержащий изолейцин, лейцин и валин, в сочетании.
[Процедура]
Исследуют сорок шесть субъектов (возраст: 49-80 лет). Субъекты являются положительными по HCV, подвергаются радикальному лечению (хирургической терапии или местной лекарственной терапии) первичного возникновения или первого рецидива гепатоклеточной карциномы, которая имеет оценку Child-Pugh A или B, и не имеют статической значимости для ее причины перед введением. В качестве препарата, содержащего аминокислоту с разветвленной цепью, используют комбинированный порошок EN (для парентерального введения) Aminoleban (зарегистрированное торговое наименования) или комбинированные гранулы Livact (зарегистрированное торговое наименования), которые вводят при описываемом количестве в течение периода исследования. Ежедневная доза Aminoleban составляет 150 г (ежедневная доза включает L-изолейцин (5,7675 г), L-лейцин (6,111 г) и L-валин (4,806 г)), а ежедневная доза Livact составляет 12,45 г (ежедневная доза включает L-изолейцин (2,856 г), L-лейцин (5,712 г) и L-валин (3,432 г)). В качестве ациклического ретиноида субъектам вводят перетионин в сочетании с аминокислотой с разветвленной цепью. Субъектов разделяют на следующие группы:
1: перетиноин, 600 мг (ежедневная доза, это же относится к тому, что изложено ниже), объединенная группа: 18 субъектов (мужчин: 11, женщин: 7),
2: перетиноин, 300 мг объединенная группа: 15 субъектов (мужчин: 9, женщин: 6), и
3: группа с введением только аминокислоты с разветвленной цепью: 13 субъектов (мужчин: 8, женщин: 5).
Ежедневную дозу перетиноина делят на две порции. Каждый день в течение 96 недель после начала исследования перетиноин вводят перорально после еды.
Радикальное излечение и рецидивы гепатоклеточной карциномы подтверждают посредством динамического CT, измеряемого каждые 12 недель после начала исследований. Сочетанное воздействие на кумулятивное время без рецидивов оценивают с помощью log-рангового теста.
Фиг.1 показывает результаты. Также Таблица 1 показывает данные по интервалу, содержащему 50% отсутствия рецидивов (то есть интервалу времени, в течение которого рецидивы гепатоклеточной карциномы наблюдаются у 50% субъектов) и для интервала, содержащего 75% отсутствия рецидивов (то есть интервала времени, в течение которого рецидивы гепатоклеточной карциномы наблюдаются у 25% субъектов).
Как ясно из Фиг.1, заметное улучшение с точки зрения кумулятивного времени с отсутствием рецидивов наблюдают в группе с сочетанием с 600 мг перетиноина и в группе с сочетанием 300 мг перетиноина. В частности, кумулятивное время отсутствия рецидивов для группы с сочетанием с 600 мг значительно улучшается, по сравнению с группой, которой вводили только аминокислоту с разветвленной цепью (P=0,020, Log-ранговый тест).
Как ясно из Таблицы 1, интервал, когда 75% не имеют рецидивов, как обнаружено, увеличивается на 517 дней (группа, которой вводили 600 мг) и на 227 дней (группа, которой вводили 300 мг), по сравнению с группой, которой вводили только аминокислоту с разветвленной цепью. В группах с сочетанием перетиноина и аминокислоты с разветвленной цепью, интервал, когда 50% не имеют рецидивов, как обнаружено, увеличивается более чем вдвое, по сравнению с группой, которой вводили только аминокислоту с разветвленной цепью.
По этой причине, введение перетиноина в сочетании с аминокислотой с разветвленной цепью, как обнаружено, уменьшает время с отсутствием рецидивов гепатоклеточной карциномы. В частности, когда вводят в сочетании перетиноин (600 мг) и аминокислоту с разветвленной цепью, кумулятивное время с отсутствием рецидивов, как обнаружено, значительно улучшается, по сравнению со случаем введения только лишь аминокислоты с разветвленной цепью.
Результаты приведенных выше исследований показывают, что применение ациклического ретиноида в сочетании с аминокислотой с разветвленной цепью дает значительно превосходящее воздействие ингибирования рецидивов гепатоклеточной карциномы после ее лечения. Таким образом, сочетание ациклического ретиноида и аминокислоты с разветвленной цепью, как показано, служит в качестве фармацевтического средства, пригодного для предотвращения и/или лечения гепатоклеточной карциномы.
Промышленное применение
Фармацевтическое средство по настоящему изобретению можно использовать в качестве фармацевтического средства для предотвращения и/или лечения гепатоклеточной карциномы. Таким образом, настоящее изобретение имеет промышленное применение.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОР ВОЗНИКНОВЕНИЯ И РАЗВИТИЯ РАКА ПЕЧЕНИ ДЛЯ ПРИМЕНЕНИЯ У ПАЦИЕНТОВ-ЛЮДЕЙ С ЦИРРОЗОМ ПЕЧЕНИ, ПОЛОЖИТЕЛЬНЫХ ПО ВИРУСУ ГЕПАТИТА С | 2005 |
|
RU2372900C2 |
| КОНЪЮГАТ АНТИТЕЛО-ЛЕКАРСТВЕННОЕ СРЕДСТВО, НАГРУЖЕННЫЙ БИНАРНЫМИ ТОКСИНАМИ, И ЕГО ПРИМЕНЕНИЕ | 2021 |
|
RU2795148C2 |
| ФОСФОРАМИДАТНЫЕ ПРОИЗВОДНЫЕ НУКЛЕОЗИДОВ | 2010 |
|
RU2553656C2 |
| Препарат для магнитно-резонансной томографии, содержащий дейтерированную природную аминокислоту с разветвленной боковой цепью, и способ диагностики с использованием этого препарата | 2018 |
|
RU2738850C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ДЛЯ ЛЕЧЕНИЯ РАКА | 2013 |
|
RU2699546C2 |
| СОСТАВ ДЛЯ ЛЕЧЕНИЯ САХАРНОГО ДИАБЕТА | 2016 |
|
RU2679602C1 |
| КОМПОЗИЦИИ И СПОСОБЫ УСИЛЕНИЯ ЭНЕРГЕТИЧЕСКОГО ОБМЕНА | 2013 |
|
RU2655794C2 |
| Новая композиция, содержащая аминокислоты с разветвленными боковыми цепями | 2020 |
|
RU2817963C2 |
| КОМПОЗИЦИИ, СОДЕРЖАЩИЕ АМИНОКИСЛОТЫ, ДЛЯ ПРИМЕНЕНИЯ В ЛЕЧЕНИИ ЗАБОЛЕВАНИЙ, АССОЦИИРОВАННЫХ С МИТОХОНДРИАЛЬНЫМИ ДИСФУНКЦИЯМИ | 2018 |
|
RU2778296C2 |
| Пептиды с противоопухолевой активностью | 2024 |
|
RU2840111C1 |
Изобретение относится к фармацевтической промышленности и представляет собой Фармацевтическое средство для ингибирования рецидива гепатоклеточной карциномы после ее лечения, содержащее перетиноин в сочетании с L-изолейцином, L-лейцином и L-валином. Изобретение обеспечивает эффективное ингибирование рецидива гепатоклеточной карциномы после ее лечения. 6 н. и 14 з.п. ф-лы, 1 пр., 1 табл., 1 ил.
1. Фармацевтическое средство для ингибирования рецидива гепатоклеточной карциномы после ее лечения, содержащее перетиноин в сочетании с L-изолейцином, L-лейцином и L-валином.
2. Фармацевтическое средство по п. 1, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
3. Фармацевтическое средство по п. 2, где вирус гепатита представляет собой вирус гепатита С или вирус гепатита В.
4. Фармацевтическое средство по любому из пп. 1-3, которое находится в форме одного препарата (комбинированное лекарственное средство), содержащего перетиноин в сочетании с L-изолейцином, L-лейцином и L-валином.
5. Фармацевтическое средство по любому из пп. 1-4, которое находится в форме набора, содержащего препарат, содержащий перетиноин в сочетании с препаратом, содержащим сочетание L-изолейцина, L-лейцина и L-валина.
6. Фармацевтическое средство для ингибирования рецидива гепатоклеточной карциномы после ее лечения, содержащее перетиноин, которое должно вводиться в сочетании с L-изолейцином, L-лейцином и L-валином.
7. Фармацевтическое средство по п. 6, которое находится в форме набора, содержащего следующие компоненты (1) и (2):
(1) фармацевтическое средство для ингибирования рецидива гепатоклеточной карциномы после ее лечения, содержащее перетиноин; и
(2) инструкцию, которая описывает введение фармацевтического средства, которое должно вводиться в сочетании с L-изолейцином, L-лейцином и L-валином.
8. Фармацевтическое средство для ингибирования рецидива гепатоклеточной карциномы после ее лечения, содержащее сочетание L-изолейцина, L-лейцина и L-валина, которое должно вводиться в сочетании с перетиноином.
9. Фармацевтическое средство по п. 8, которое находится в форме набора, содержащего следующие компоненты (1) и (2):
(1) фармацевтическое средство для ингибирования рецидива гепатоклеточной карциномы после ее лечения, содержащее сочетание L-изолейцина, L-лейцина и L-валина; и
(2) инструкцию, которая описывает введение фармацевтического средства, которое должно вводиться в сочетании с перетиноином.
10. Фармацевтическое средство по п. 6 или 8, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
11. Фармацевтическое средство по п. 10, где вирус гепатита представляет собой вирус гепатита С или вирус гепатита В.
12. Способ ингибирования рецидива гепатоклеточной карциномы после ее лечения, включающий введение эффективного количества перетиноина и эффективного количества сочетания L-изолейцина, L-лейцина и L-валина пациенту, нуждающемуся в этом, одновременно или раздельно в различные моменты времени.
13. Способ по п. 12, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
14. Способ по п. 13, где вирус гепатита представляет собой вирус гепатита С или вирус гепатита В.
15. Применение перетиноина в сочетании с L-изолейцином, L-лейцином и L-валином для получения фармацевтического средства для ингибирования рецидива гепатоклеточной карциномы после ее лечения.
16. Применение по п. 15, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
17. Применение по п. 16, где вирус гепатита представляет собой вирус гепатита С или вирус гепатита В.
18. Сочетание L-изолейцина, L-лейцина и L-валина для введения в сочетании с перетиноином для ингибирования рецидива гепатоклеточной карциномы после ее лечения.
19. Сочетание L-изолейцина, L-лейцина и L-валина по п. 18, где гепатоклеточная карцинома вызывается вирусом гепатита или неалкогольным стеатогепатитом.
20. Сочетание L-изолейцина, L-лейцина и L-валина по п. 19, где вирус гепатита представляет собой вирус гепатита С или вирус гепатита В.
| ИНГИБИТОР ВОЗНИКНОВЕНИЯ И РАЗВИТИЯ РАКА ПЕЧЕНИ ДЛЯ ПРИМЕНЕНИЯ У ПАЦИЕНТОВ-ЛЮДЕЙ С ЦИРРОЗОМ ПЕЧЕНИ, ПОЛОЖИТЕЛЬНЫХ ПО ВИРУСУ ГЕПАТИТА С | 2005 |
|
RU2372900C2 |
| Muto Y et | |||
| all | |||
| " Prevention of second primary tumors by an acyclic retinoid, polyprenoic acid, in patients with hepatocellular carcinoma | |||
| Hepatoma Prevention Study Group", N Engl J Med | |||
| Предохранительное устройство для паровых котлов, работающих на нефти | 1922 |
|
SU1996A1 |
| "Теория химического строения А.М.Бутлерова", А.И.Артеменко "Органическая химия", 2-ое издание, Москва | |||
Авторы
Даты
2016-01-27—Публикация
2011-08-10—Подача