Изобретение относится к клинической биохимии, кардиологии, неврологии и может быть использовано для определения литической активности (атерогенности) множественно модифицированных липопротеинов низкой плотности (ммЛНП) как для прогноза течения атеросклеротического процесса в организме человека, так и для разработки препаратов, уменьшающих патогенность ммЛНП и предупреждающих развитие эндотелиальной дисфункции на ранних стадиях атеросклероза.
Атеросклероз является сложным, периодически обостряющимся хроническим воспалительным процессом повреждения сосудов, развивающимся на фоне нарушений холестеринового обмена, который приводит к структурной модификации сосудистого эндотелия и разрастанию соединительной ткани, обуславливая формирование атеросклеротической бляшки. Атеросклероз и его осложнения - ишемическая болезнь сердца, инсульт, поражение сосудов нижних конечностей продолжают оставаться наиболее частой причиной инвалидизации и смертности населения в экономически развитых странах Европы, США и особенно России [European Guidelines on Cardiovascular Disease // Eur. Heart J. - 2003. - V. 24, №17. - P. 1601-1610; NCEP. Adult Treatment Panel III Guidelines // Circulation. - 2004. - V. 110. - P. 227-239; ВНОК. Российские рекомендации. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. М. - 2004. - 36 с.].
В прогрессировании атеросклеротического процесса важную роль играет сосудистая эндотелиальная дисфункция, которая в настоящее время рассматривается как независимый фактор риска атеросклероза и атеротромбоза [Нагорнев В.А. Патогенез атеросклероза. М.: СПб. - 2006].
Заболевание начинается с накопления липопротеинов, в первую очередь липопротеинов низкой плотности (ЛНП), во внеклеточном матриксе сосуда. Данные частицы ЛНП агрегируют и подвергаются модификации в результате окисления. Модифицированные окислением ЛНП (моЛНП) являются токсичными и повреждают сосуды, вызывая воспаление и фиброз [Steinberg D. The LDL modification hypothesis of atherogenesis: an update // J. Lipid Res. - 2009. - V. 50. - P. S376 - S381].
Наиболее убедительные доказательства участия моЛНП в развитии атеросклероза подтверждаются следующими данными:
1) моЛНП обнаруживают в атеросклеротической бляшке, но не в нормальных артериях [Rosenfeld М.Е., Palinski W., Yla-Herttuala S., Butler S., Witztum J.L. Distribution of oxidation specific lipid-protein adducts and apolipoprotein В in atherosclerotic lesions of varying severity from WHHL rabbits // Atherosclerosis. - 1990. - V. 10. - P. 336-349];
2) аутоантитела, образующиеся против неоэпитопов моЛНП, определяются в крови, и титр этих антител коррелирует с тяжестью атеросклероза и рассматривается в качестве маркера заболевания [Itabe Н., Mori М., Higashi Y., and Takano Т. Minimally modified LDL is an oxidized LDL enriched with oxidized phosphatidylcholines // J Biochem. - 2003. - V. 134. - P. 459-465; Tsimikas S. Oxidative biomarkers in the diagnosis and prognosis of cardiovascular disease // Am J Cardiol. - 2006. - V. 98. - P. 9P - 17P];
3) в исследованиях на животных при моделировании атеросклероза было показано, что антиоксиданты (витамин Е, пробукол, аналоги пробукола и KoQ) оказывают протективное действие, хотя в клинических испытаниях на людях с использованием витамина Е эти данные не были полностью подтверждены [Witztum J.L. and Steinberg D. The oxidative modification hypothesis of atherosclerosis: Does it hold for humans? // Trends Cardiovasc Med. - 2001. - V. 11. - P. 93-102];
4) было обнаружено, что у мышей генетический нокаут различных скавенд-жер-рецепторов значительно подавляет развитие атеросклероза [Kuchibhotla S., Vanegas D., Kennedy D.J., Guy E, Nimako G, Morton RE, Febbraio M. at al. Absence of CD36 protects against atherosclerosis in ApoE knock-aut mice with no additional protection provided by absence of scavenger receptor AI/II // Cardiovasc Res. - 2008. - V. 78. - P. 185-196; Manning-Tobin J.J., Moore K.J., Seimon T.A., Bell SA, Sharuk M, Alvarez-Leite JI. at al. Loss of SA-A and CD36 activity reduces atherosclerotic lesion complexity without abrogating foam cell formation in hyperlipidemic mice // Arterioscler Thromb Vase Biol. - 2009. - V. 29. - P. 19-26; Mehta J.L., Sanada N., Hu C.P., Chen J, Dandapat A, Sugawara F at al. Deletion of LOX-1 reduces atherogenesis in LDLR knockout mice fed high cholesterol diet // Circ Res. - 2007. - V. 100. - P. 1634-1642; de Winther M.P.J., van Dijk K.W., Havekes L.M., and Hofker M.H. Macrophage scavenger receptor Class A: A multifunctional receptor in a Atherosclerosis // Artherioscler Thromb Vase Biol. - 2000. - V. 20. - P. 290-297], что указывает на значимость этих рецепторов и их лигандов (моЛНП) в развитии повреждения артерий;
5) установлено также, что истощение фермента 12/15-липооксигеназы, который является физиологическим окисляющим агентом ЛНП, замедляет развитие атеросклероза [HuoY., Zhao L., Hyman M.C., Shashkin P, Harry BL, Burcin T at al. Critical role of macrophage 12/15-lipooxygenese for atherosclerosis in apolipoprotein E-deficient mice // Circulation. - 2004. - V. 110. - P. 2024-2031], в то время как его повышенная экспрессия ускоряет атеросклероз [Harats D., Shaish A., Geoege J., Mulkins M, Kurihara H, Levkovitz H. at al. Overexpression of 15-lipooxygenase in vascular endothelium accelerates early atherosclerosis in LDL receptor-deficient mice // Arterioscler Thromb Vase Biol. - 2000. - V. 20. - P. 2100-2105], свидетельствуя о важной роли окислительной модификации ЛНП в развитии данного заболевания;
6) Като и соавт. (2009) в исследованиях на апоЕ-дефицитных мышах показали, что повышение плазменного уровня окисленных ЛНП предшествует развитию повреждений артерий [Kato R., Mori С, Kitazato K., Arata S, Obama T, Mori M. at al. Transient increase in plasma oxidized LDL during the progression of atherosclerosis in apolipoprotein E knockout mice // Arterioscler Thromb Vase Biol. - 2009. - V. 29. - P. 33-39];
7) было показано, что специфическое снижение плазменного уровня моЛНП при увеличении экспрессии скавенджер-рецептора (LOX-1) в печени предотвращает прогрессирование атеросклеротического повреждения у апоЕ-дефицитных мышей даже при наличии тяжелой гиперхолестеринемии [Ishi-gaki Y., Katagiri H., Gao J., Yamada T, Imai J, Uno K. at al. Impact of plasma oxidized low-density lipoprotein removal on atherosclerosis // Circulation. - 2008. - V. 118. - Р. 75-83].
Таким образом, учитывая важную патогенетическую роль моЛНП, а в целом - множественно модифицированных ЛНП при атеросклерозе, остается актуальной разработка простых, доступных способов определения литической активности (атерогенности) ммЛНП как для прогноза течения и эффективности лечения, так и для разработки новых подходов терапии атеросклеротических заболеваний и эндотелиальной дисфункции на ранних стадиях.
Известен способ определения атерогенности сыворотки крови по ее способности вызывать накопление холестерина в культивируемых клетках [Tertov V.V., Orekhov A.N., Nikitina N.A. Perova NV, Lyakishev AA, Serebrennikov SG et al. Peritoneal macrophages: a model for detecting atherogenic potential in patiens blood serum // Ann. Med. - 1989. - V. 21(6). - Р. 455-459]. Недостатком этого способа являются трудоемкость, высокая себестоимость, сложность и длительность проведения исследования.
Также известен способ определения литической активности липопротеинов, содержащих лизофосфатидилхолин (лФХ), в инкубированной мышиной плазме [Suzuki A., Kawakami М. A hemolytic lipoprotein containing lyso-phosphatidylcholine prodused in incubated mouse plasma // Biochimica et Biophysica Acta. - 1983. - V. 753. - P. 236-243]. В плазме крови человека и крыс большое количество лФХ также присутствует в липопротеинах очень высокой плотности в виде комплекса с альбумином [Switzer S., Eder Н.А. Transport of lysolecithin by albumin in human and rat plasma // J. Lipid Res. - 1965. - V. 6. - P. 506-511; Wille L.E., Heiberg A., Gjone E. Studies on serum pre-alpha-lipoprotein. An albumin-ApoA-I-lysolecithin-containing lipoprotein family (AAL) // Scand. J. Clin. Lab. Invest. - 1978. - V. 38, Suppl. 150. - P. 59-65], однако логическая активность лФХ не была показана.
В настоящее время показано, что лФХ является большим плазменным липидом, который узнается как важный клеточно-сигнализирующая молекула и продуцируется в физиологических условиях при действии фосфолипазы А2 (ФлА2) на лФХ. лФХ транспортирует глицерофосфолипидные компоненты, такие как жирные кислоты, фосфатидилглицерол и холин между тканями, является лигандом для специфического белок-G-связанного рецептора и активирует некоторые вторичные мессенджеры. лФХ является также большим фосфолипидным компонентом моЛНП и признается критическим фактором для проявления атерогенной активности моЛНП [Schmitz G., Rueb-saamen K. Metabolism and atherogenic desease association of lysophosphatidyl-choline // Atherosclerosis. - 2010. - V. 208. - P. 10-18].
Методы, разработанные для определения лФХ, в основном связаны с определением активности ФлА2 [Aasman van den В.Н. A review on methods of phospholipase A determination // Agents Action. - 1979. - V. 9. - P. 382-389]. Однако потенциальные эффекты детергента в составе буфера на активность фермента, также как и структура фосфолипидного бислоя, не учитываются. Наряду с масс-спектрометрией для анализа лизофосфолипидов существует ряд методов, основанных на хроматографии [Choi S., Lee Y.S., Na D.S., Yoo Y.S. Determination of enzymatic activity and properties of secretory phospholipase A2 by capillary electrophoresis // J. Chromatogr. - 1999. - V. 853. - P. 285-293; Lai C.S., Zhang J.Z., Joseph J. Spin-label assay for phospholipase A2 // Anal Biochem. - 1988. - V. 172. - P. 397-402], ультрафиолетовой и флуоресцентной спектроскопии [Rawyler A., Siegenthaler Р.А. A single and continuous spectro-photometric assay for various lipolytic enzimes, using natural, non-labelled substrates // Biochim Biophys Acta. - 1989. - V. 1004. - P. 337-344], ядерно-магнитно-резонансной спектроскопии [Fuchs В., Schiller J., Wagner U., Hantzschel H., Arnold K. The phosphatidylcholine/lysophosphatidylcholine ratio in human plasma is an indicator of the severity of rheumatoid arthritis: investigations by 31P NMR and MALDI-TOF MS // Clin. Biochem. - 2005. - V. 38. - P. 925-933] и радиоактивности [Catz S.D., Sterin-Speziale N.B. Bradykinin stimulates phosphoinositide turnover and phospholipase С but not phospholipase D and NADPH oxidase in human neutrophils // J. Leukoc. Biol. - 1996. - V. 59. - P. 591-597]. Большинство опубликованных методов, используемых для анализа лФХ, включают разделение их с помощью тонкослойной хроматографии [Wang W.Q., Gustafson A. One-dimensional thin-layer chromatographic separation of phospholipids and lysophospholipids from tissue lipid extracts // J. Chromatogr. - 1992. - V. 581. - P. 139-142; Yokoyama K., Shimizu F., Setaka M. Simultaneous separation of lysophospholipids from the total lipid fraction of crude biological samples using two-dimensional thin-layer chromatography // J. Lipid. Res. - 2000. - V. 41. - P. 142-147] или высокоэффективной жидкостной хроматографии [Guan Z., Grunler J., Piao S., Sindelar P.J. Separation and quantitation of phospholipids and their ether analogues by high-performance liquid chromatography // Anal. Biochem. - 2001. - V. 297. - P. 137-143; Suchocka Z., Gronostajska D., Suchocki P., Pachecka J. New HPLC method for separation of blood plasma phospholipids // J. Pharm. Biomed. Anal. - 2003. - V. 32. - P. 859-865]. Использование этих методов в рутинной практике ограничено из-за их сложности, длительности процедуры, а также высокой себестоимости анализов.
Техническим результатом предлагаемого способа является устранение вышеуказанных недостатков, расширение арсенала способов определения литической активности (атерогенности) ммЛНП для раннего прогноза течения, проведения и контроля эффективности патогенетической терапии атеросклероза в условиях клинико-диагностических лабораторий за счет упрощения технологии, а также его многократного удешевления.
Этот результат достигается тем, что определение литической активности ммЛНП проводят путем обработки сыворотки крови 20% раствором поливинилпирролидона с молекулярной массой 35000 (ПВП-35000) при объемном соотношении сыворотка: ПВП (1:0,84), инкубируют 10 мин при комнатной температуре, агрегаты ммЛНП осаждают центрифугированием, декантируют, осадок ммЛНП растворяют в буфере без ПВП, добавляют аутологичные, отмытые стандартизованные эритроциты человека, инкубируют в течение 48 часов при комнатной температуре, измеряют оптическую плотность на фотометре при длине волны 620 нм, по калибровочному графику определяют степень лизиса и при лизисе более 10% констатируют повышенную литическую активность ммЛНП.
Подписи к рисункам
Рис. 1. Калибровочный график для определения степени лизиса эритроцитов человека по оптической плотности при длине волны 620 нм.
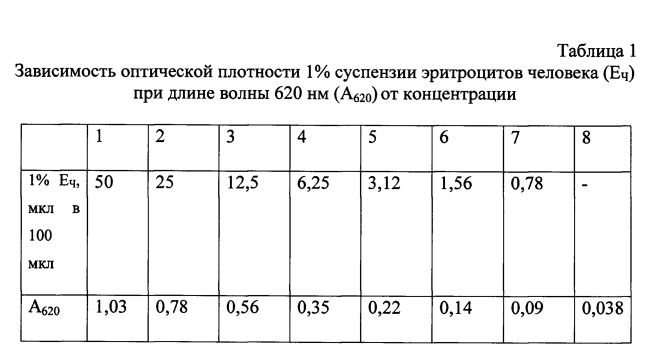
Пример 1. Определение оптимальной концентрации эритроцитов человека для теста определения литической активности ммЛНП. Эритроциты человека (ЕЧ) 3 раза отмывают в вероналовом солевом буфере (VBS2+) центрифугированием в течение 10 мин при 2500 об/мин. Строят график зависимости оптической плотности суспензии эритроцитов (при длине волны 620 нм) от концентрации эритроцитов. Для этого 1% суспензию эритроцитов прогрессивно разводят в плоскодонной 96-луночной иммунологической планшете в объеме 100 мкл 0,15М NaCl. Тщательно перемешивают и измеряют на фотометре для иммуноферментного анализа при длине волны 620 нм. Результаты представлены в таблице 1. Как видно из данных, представленных в таблице 1, наблюдается линейная зависимость оптической плотности суспензии от концентрации ЕЧ в растворе до А620, равной 0,56 ЕД. Свыше 0,56 ЕД при А620 данная зависимость - нелинейная. Поэтому для теста определения литической активности ммЛНП нами выбрана концентрация суспензии ЕЧ, которая в объеме 100 мкл в 96-луночных планшетах дает оптическую плотность, равную 0,40-0,56 ЕД. Для определения степени лизиса эритроцитов нами предложен калибровочный график, в котором динамику лизиса эритроцитов оценивают по снижению оптической плотности при длине волны 620 нм. За 0% лизиса принимают оптическую плотность контроля эритроцитов на спонтанный лизис (30 мкл ЕЧ + 70 мкл VBS2+), соответственно за 100% лизис принимают оптическую плотность контроля на полный лизис (30 мкл ЕЧ + 70 мкл Н2О). Степень лизиса эритроцитов оценивают через 48 часов инкубации при комнатной температуре по калибровочному графику, представленному на рис. 1.
Как видно из рис. 1, калибровочный график позволяет определять степень лизиса эритроцитов в процентах по оптической плотности пробы без стадии центрифугирования и измерения гемоглобина в супернатанте и последующего расчета степени лизиса эритроцитов по формуле, что существенно упрощает регистрацию результатов анализа литической активности ммЛНП в рутинных исследованиях.
Пример 2. Выделение мм ЛНП из сыворотки крови больных с инструментально подтвержденным атеросклерозом каротидных артерий.
Выделение ммЛНП проводят, как описано в работе [Шойбонов Б.Б., Шойбонова Б.В. Способ определения атерогенности крови человека // Патент РФ №2497116 от 27.10.2013 г.], с незначительной модификацией. Буфер-1 для агрегации мм ЛНП готовят растворением 20 г ПВП-35000 в 100 мл 0,01М Трис-HCl-буфера (pH 7,4), содержащего 0,15 М NaCl; Буфер-2, в отличие от Буфера-1, не содержит ПВП-35000. К 100 мкл пулированной сыворотки крови (10 больных с атеросклерозом каротидных артерий и 10 здоровых доноров) добавляют по 84 мкл Буфера-1, тщательно перемешивают и инкубируют при комнатной температуре в течение 10 мин. Агрегированные ммЛНП осаждают центрифугированием при 3100 g в течение 10 мин при 23°С, декантируют, преципитат ммЛНП растворяют в 100 мкл Буфера-2. После растворения осадка в приготовленных ПВП-преципитатах определяют содержание холестерина, триацилглицерида (ТАГ) и общих белков с использованием коммерческих ферментных наборов. Полученные результаты представлены в таблице 2.
Как видно из данных, представленных в таблице 2, в ПВП-преципитате пулированной сыворотки больных атеросклерозом каротидных артерий содержание холестерина в 5,3 раза, а ТАГ - в 16 раз больше, чем в ПВП-преципитате из сыворотки здоровых доноров. Содержание общего белка в 1,3 раза выше в ПВП-преципитате больных.
Таким образом, наличие холестерина, ТАГ и белка в ПВП-преципитатах из сывороток свидетельствует о липопротеиновой природе агрегатов, образующихся в присутствии 9,1% ПВП 35000±5000 в условиях 54% сыворотки. Повышенный уровень ПВП-преципитата, содержащего мЛПНП у больных с атеросклерозом каротидных артерий, подтверждает патологическую роль мЛПНП при атеросклеротическом процессе.
Пример 3. Определение литической активности ммЛНП, приготовленных из сыворотки крови больных с атеросклерозом каротидных артерий, с использованием аутологичных эритроцитов.
Для подтверждения литической активности (патогенности) ммЛНП, приготовленных из индивидуальных сывороток больных с инструментально подтвержденным атеросклерозом каротидных артерий, были приготовлены аутологичные суспензии эритроцитов для теста, как описано выше (см. пример 1). Положительные результаты теста должны свидетельствовать о патогенности ммЛНП в тесте лизиса аутологичных (собственных) эритроцитов.
Тест литической активности ммЛНП проводят в 96-луночных плоскодонных иммунологических планшетах по 3 повтора. Вначале по 10 мкл (×3) ммЛНП вносят в лунки, потом добавляют 60 мкл (×3) буфера VBS2+ и 30 мкл (×3) суспензии стандартизованных в этом же буфере аутологичных эритроцитов больного. Параллельно ставят контроли: 3 контроля на полный лизис (30 мкл суспензии аутологичных эритроцитов + 70 мкл H2O); 3 контроля на спонтанный лизис эритроцитов (30 мкл аутологичных эритроцитов + 70 мкл буфера VBS2+). Тщательно перемешивают и сразу измеряют оптическую плотность на фотометре для иммуноферментного анализа при длине волны 620 нм (бланк устанавливают против воздуха). После измерения планшеты герметично заклеивают пленкой и оставляют на 48 часов при комнатной температуре. После 48-ми часовой инкубации планшеты тщательно перемешивают и измеряют оптическую плотность при тех же условиях. Проведено исследование литической активности 6 проб ммЛНП, приготовленных из индивидуальных сывороток больных, с использованием в качестве мишеней аутологичные (собственные) отмытые и стандартизованные эритроциты. Полученные результаты представлены в таблице 3.
Как видно из данных, представленных в таблице 3, в пробах 1-5 разброс оптической плотности после 48-часовой инкубации колебался от 0,8% до 5,3%. Только в пробе №6 разброс составил 11%. При определении степени лизиса по калибровочному графику, приведенному в примере 1, максимальная ошибка в пробе №6 составила ± 7,9%.
Таким образом, ошибка по трем точкам не превышает 10%, поэтому наличие литического эффекта ммЛНП можно констатировать при лизисе более 10%.
Выявление литического действия ммЛНП, приготовленных из сыворотки крови больного с атеросклерозом каротидных артерий, и лизис собственных эритроцитов свидетельствует о высокой патогенности ммЛНП и об отсутствии ингибирующих факторов в пробе в виде альбумина и липопротеинов высокой плотности, которые были представлены в работе Suzuki А., Kawakami М. (1983). Авторами показано, что основными факторами, оказывающими литическое действие на эритроциты мыши, являются ФлА2 и лФХ, который является продуктом гидролиза сложноэфирной связи во втором положении фосфатидилхолина и превращении его в лФХ. Для уточнения литического фактора в составе ммЛНП нами проведены следующие исследования.
Пример 4. Влияние повышенной температуры на литическое действие ммЛНП. Для проведения данных исследований были отобраны 8 проб сыворотки крови больных атеросклерозом каротидных артерий и приготовлены ммЛНП, как описано выше. Пробы ммЛНП делили на 2 пробы и одну из них прогревали при 58°С в течение 20 мин для термоинактивации липопротеин ассоциированной ФлА2 (ла-ФлА2), а вторая часть ммЛНП служила контролем. Результаты проведенного теста на литическую активность ммЛНП представлены в таблице 4.
Как видно из данных, представленных в таблице 4, во всех 8 сыворотках содержится повышенный уровень ммЛНП, который определяли по содержанию холестерина в ПВП-преципитатах (от 10 до 33,7 мг/дл), т.е. в 100% мы выявляем количественно атерогенные (множественно модифицированные) ЛНП. Определение литической активности в мм ЛНП в 50% выявляет высокую активность, у 25% - пограничное значение (на уровне 10% литическая активность), и только в 2 пробы ммЛНП не обладали литической активностью. Известно, что инкубация при 58°С в течение 20 мин вызывает инактивацию ла-ФлА2 (Suzuki A., Kawakami М., 1983). Термостабильность литической активности свидетельствует о наличии в составе ммЛНП лФХ, который обладает детергентными свойствами. Как видно из данных, приведенных в таблице 4, инкубация ммЛНП при 58°С действительно вызывает снижение литической активности частично или почти на 50% (проба №8). В то же время обнаружено, что для пробы №7 температурное воздействие не оказывает ингибирующего эффекта на литическую активность ммЛНП. Следовательно, литическая активность ммЛНП (№7) обусловлена наличием термостабильных молекул лФХ.
Таким образом, инкубация препаратов ммЛНП позволяет выявить природу литического фактора для оценки тяжести (остроты) атеросклеротического процесса в организме человека. Наличие же высокоактивной ла-ФлА2 в ммЛНП свидетельствует об острой воспалительной реакции в организме больного с субклиническим или клиническим атеросклерозом и требует интенсивной противовоспалительной терапии. Известно, что основным источником ФлА2 являются активированные макрофаги. Отсутствие литической активности ммЛНП является благоприятным прогнозом для обследуемого и свидетельствует о медленном прогрессировании атеросклеротического процесса, требует дальнейшего наблюдения и проведения стандартной антиатеросклеротической терапии. Термостабильность литического фактора в составе ммЛНП №7 свидетельствует о высокой концентрации лФХ, генерированного по альтернативному пути, без участия ла-ФлА2. Данный механизм, возможно, протекает при дефиците антиоксидантов в организме из-за повышенного их расхода или же связан с нарушением питания и требует дальнейших исследований.
Определение литической активности ммЛНП позволяет проводить диагностику течения атеросклеротического процесса, определение литического фактора при термоинактивации ммЛНП расширяет возможности для коррекции проводимой терапии под контролем уровня литической активности ммЛНП. Определение литической активности ммЛНП открывает новый подход к оценке атерогенности от количественных показателей к качественным (функциональным) показателям. То есть при нормальном уровне ммЛНП, наличие субклинического атеросклероза может быть обусловлено высокой литической активностью (атерогенностью) ммЛНП.
Предлагаемый способ отличается простотой, так как, кроме специального буфера для выделения ммЛНП, остальные компоненты являются рутинным материалом диагностических лабораторий. Для регистрации лизиса эритроцитов человека не требуется стадия центрифугирования. Использование простого и информативного способа определения литической активности ммЛНП позволяет проводить скрининг и выявлять людей с острым течением атеросклеротического процесса, и на доклинических стадиях заболевания, и при клиническом атеросклерозе. Дальнейшие углубленные исследования таких пациентов позволят установить индивидуальную причину атерогенности крови и проводить этиотропную терапию.



| название | год | авторы | номер документа |
|---|---|---|---|
| МЕТОД ВЫДЕЛЕНИЯ И КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ МНОЖЕСТВЕННО МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИНОВ НИЗКОЙ ПЛОТНОСТИ | 2015 |
|
RU2592238C1 |
| Способ оценки характера аутоиммунной реакции организма человека на множественно модифицированные липопротеины низкой плотности в литическом тесте | 2017 |
|
RU2680848C1 |
| СПОСОБ ЭКСПРЕСС-ОПРЕДЕЛЕНИЯ РЕЗИСТЕНТНОСТИ К ОКИСЛЕНИЮ ЛИПОПРОТЕИНОВ НИЗКОЙ ПЛОТНОСТИ СЫВОРОТКИ КРОВИ ЧЕЛОВЕКА | 2015 |
|
RU2578027C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ СОСУДИСТОЙ ДИСТОНИИ У КРЫС ПО ГИПОТЕНЗИВНОМУ ТИПУ | 2014 |
|
RU2614521C2 |
| СПОСОБ ВЫДЕЛЕНИЯ И ИССЛЕДОВАНИЯ АТЕРОГЕННОСТИ ИММУННЫХ КОМПЛЕКСОВ, СОДЕРЖАЩИХ МНОЖЕСТВЕННО МОДИФИЦИРОВАННЫЕ ЛИПОПРОТЕИНЫ | 2016 |
|
RU2632118C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АТЕРОГЕННОСТИ ИММУННЫХ КОМПЛЕКСОВ | 2013 |
|
RU2549467C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АТЕРОГЕННОСТИ КРОВИ ЧЕЛОВЕКА | 2012 |
|
RU2497116C1 |
| СПОСОБ ЭКСПРЕСС-ОПРЕДЕЛЕНИЯ ХОЛЕСТЕРИНА В ИММУННЫХ КОМПЛЕКСАХ | 2013 |
|
RU2538685C1 |
| СПОСОБ ИЗМЕРЕНИЯ КОНЦЕНТРАЦИИ ЦИРКУЛИРУЮЩИХ МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИДОВ НИЗКОЙ ПЛОТНОСТИ В СЫВОРОТКЕ КРОВИ ЧЕЛОВЕКА | 2016 |
|
RU2659211C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МИНИМАЛЬНО МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИНОВ НИЗКОЙ ПЛОТНОСТИ В СЫВОРОТКЕ ИЛИ ПЛАЗМЕ КРОВИ ЧЕЛОВЕКА | 2012 |
|
RU2501013C1 |

Изобретение относится к клинической биохимии и представляет собой способ определения литической активности множественно модифицированных липопротеинов низкой плотности (ммЛНП) путем обработки сыворотки крови 20% раствором поливинилпирролидона с молекулярной массой 35000 (ПВП-35000) при объемном соотношении сыворотка: ПВП (1:0,84), инкубируют 10 мин при комнатной температуре, агрегаты ммЛНП осаждают центрифугированием, декантируют, осадок ммЛНП растворяют в буфере без ПВП, добавляют аутологичные отмытые стандартизованные эритроциты человека, инкубируют в течение 48 часов при комнатной температуре, измеряют оптическую плотность на фотометре при длине волны 620 нм, по калибровочному графику определяют степень лизиса и при лизисе более 10% констатируют повышенную литическую активность ммЛНП. Изобретение обеспечивает расширение арсенала способов определения литической активности ммЛНП. 4 пр., 4 табл., 1 ил.
Способ определения литической активности множественно модифицированных липопротеинов низкой плотности (ммЛНП) путем обработки сыворотки крови 20% раствором поливинилпирролидона с молекулярной массой 35000 (ПВП-35000) при объемном соотношении сыворотка : ПВП (1:0,84), инкубируют 10 мин при комнатной температуре, агрегаты ммЛНП осаждают центрифугированием, декантируют, осадок ммЛНП растворяют в буфере без ПВП, добавляют аутологичные, отмытые, стандартизованные эритроциты человека, инкубируют в течение 48 часов при комнатной температуре, измеряют оптическую плотность на фотометре при длине волны 620 нм, по калибровочному графику определяют степень лизиса и при лизисе более 10% констатируют повышенную литическую активность ммЛНП.
| ШОЙБОНОВ Б.Б | |||
| и др | |||
| / Определения холестерина в иммунных комплексах / Клин | |||
| лаб | |||
| диаг | |||
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| СРЕДА И СПОСОБ ОПРЕДЕЛЕНИЯ МНОЖЕСТВЕННО МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИНОВ СЫВОРОТКИ КРОВИ ЧЕЛОВЕКА | 2010 |
|
RU2444014C1 |
| Способ определения литической активности веществ | 1980 |
|
SU1116394A1 |
| OREKHOV A.N | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2016-03-20—Публикация
2015-01-15—Подача