Изобретение относится к клинической биохимии и может быть использовано в лабораторной диагностике для выделения множественно модифицированных липопротеинов низкой плотности (ммЛНП) и определения холестерина множественно модифицированных липопротеинов низкой плотности (Х-ммЛНП).
Атеросклероз представляет собой хроническое заболевание, которое вызывает утолщение внутреннего слоя (интимы) крупных артерий и артерий среднего размера. Заболевание начинается с накопления липопротеинов, в первую очередь, липопротеина низкой плотности (ЛНП), во внеклеточном матриксе сосуда. Молекулы ЛНП агрегируют и подвергаются множественной модификации (ммЛНП), становятся токсичными и вызывают повреждения сосудов (Itabe Н. Oxidative modification of LDL: its pathological role in atherosclerosis. // Clin Rev Allergy Immunol. - 2009. - V. 37, №1. - P. 4-11.).
Учитывая ключевую роль ммЛНП при атеросклерозе, остается актуальной разработка простых, доступных как для рутинных, так и для фундаментальных научных исследований, методов выделения и количественного определения их.
В настоящее время наиболее широко распространены три основных способа выделения и очистки липопротеинов отдельных классов сыворотки крови в препаративных количествах: ультрацентрифугирование в солевых растворах, хроматография и осаждение. Электрофорез используется в основном в аналитических целях. Наиболее часто используется первый способ, способ последовательного центрифугирования при различных плотностях водного растворителя. Метод основан на процедуре, предложенной Хавелом и соавт. (Havel R.J., Eder Н., Bragdon J. The distribution and chemical composition of ultracentrifugally separated lipoproteins in human serum. // J. Clin. Invest. - 1955. - V. 347. - P. 1345-1353.), и детально разработан Линдгреном (Lindgren F.T. Analysis of lipids and lipoproteins (Perkins E.G., ed.) // American oil Chemists Soc., Champaign, SL., USA. 1975. P. 204-223.). Принцип метода состоит в том, что гидратированная плотность плазмы или сыворотки крови доводится до нижнего предела плотности фракции, которую необходимо выделить, и затем проба центрифугируется при 100000 g несколько часов. Липопротеины (ЛП), имеющие плотность, меньшую плотности растворителя, флотируют к верхней части центрифужной пробирки, а другие седиментируют на дно. Осадки встряхивают и их гидратированную плотность доводят до верхнего предела следующей требуемой плотности ЛП фракции. Центрифугирование повторяют вплоть до выделения необходимой фракции в верхней части пробирки (в супернатанте). Фракция липопротеинов высокой плотности (ЛВП) выделяется после предварительного отделения фракций липопротеинов очень низкой плотности (ЛОНП) и ЛНП, и для ее выделения требуется проводить центрифугирование в течение не менее 24-36 часов при 40000-100000 g. К достоинствам центрифугирования следует отнести то, что этот способ обладает значительной гибкостью, так как дает возможность изолировать и выделить почти любое требуемое количество фракций, которые можно охарактеризовать в пределах двух интервалов плотности водного растворителя. В целом этот способ характеризуется высокой точностью и воспроизводимостью.
К недостаткам центрифугирования относятся необходимость использования (для обеспечения заданной плотности растворителя) таких солей, как NaCl, CsCl, KBr или NaBr и проведение специальных процедур для их последующего удаления из готовых растворов фракций ЛП с помощью диализа. Кроме того, необходимо использовать высокоскоростные, термостатируемые ультрацентрифуги, а время выделения, например, фракции ЛВП составляет более 36 часов. Кроме того, метод ультрацентрифугирования не позволяет отделить ммЛНП от нативных ЛНП.
Известен хроматографический метод очистки белков (Холодова Ю. Д., Чаяло П.П. Липопротеины крови. Киев: Наукова думка. - 1990. - С. 26-33]. Его обычно применяют для разделения и очистки всех или отдельных фракций липопротеинов, полученных другими методами, в частности ультрацентрифугированием, либо осаждением. Используются в основном адсорбционная, ионообменная, аффинная и гель-фильтрационная хроматографии. Сущность этого способа заключается в пропускании исходной плазмы или сыворотки крови через колонку, наполненную специальным сорбентом, по-разному взаимодействующим с разделяемыми белками. Достоинством этого способа является относительная простота реализации и использование недорого оборудования.
К недостаткам этого метода следует отнести трудность отделения липопротеинов от других белков сыворотки крови, длительность процедуры и большое разведение выделенных фракций липопротеинов.
Наиболее широко используемым способом является химическое осаждение белков (Холодова Ю. Д., Чаяло П.П. Липопротеины крови. Киев: Наукова думка. 1990. С. 22-26.), основанное на том, что такие анионы, как сульфированные полисахариды (гепарин, декстрансульфат и др.) в комбинации с некоторыми двухвалентными катионами (Mn2+, Со2+, Mg2+, Са2+ и др.) способны осаждать ЛНП при значениях рН, близких к 7, образуя их нерастворимые комплексы. Сущность этого способа заключается в добавлении к плазме или сыворотке крови растворов гепарина и солей типа MnCl2 при определенных их концентрациях. Далее эти смеси встряхивают и центрифугируют при 6000g. Фракции ЛОНП и ЛНП при этом выпадают в осадок, а супернатант, содержащий фракцию ЛВП, очищают далее путем диализа против нескольких порций нейтрального буфера в течение 48 часов.
К достоинствам этого способа относится простота и использование только низкоскоростного центрифугирования. Метод преципитации ЛОНП и ЛНП широко используется в рутинных исследованиях определения содержания холестерина в ЛВП, а содержание холестерина в ЛНП рассчитывают по расчетной формуле Фридвальда (Friedewald WT, Levy RI, Fredrickson DS. Estimation of the concentration of low-density lipoprotein cholesterol in plasma, without use of the preparative ultracentrifuge // Clin Chem. - 1972. - V. 18. - P. 499-502.).
Однако у методов химического осаждения имеются и ряд недостатков:
1) часть сывороточных белков коопреципитируют вместе с ЛОНП и ЛНП, а часть остается в супернатанте с ЛВП;
2) трудность и длительность удаления преципитирующих агентов, необходимость стадии диализа;
3) нарушение нативности липопротеиновых частиц;
4) метод пригоден только для аналитических исследований холестерина во фракциях липопротеинов.
Известен также метод выделения десиалированных ЛНП с использованием аффинного сорбента, сефарозы с иммобилизованным лектином из Ricinus Communis (RCA120) (Tertov V.V., Sobenin I.A., Tonevitsky A.G., et al. Isolation of atherogenic modified (desialated) low density lipoprotein from blood of atherosclerotic patients: separation from native lipoprotein by affinity chromatography // Biochem. Biophys. Res. Coramun. - 1990. - V. 167. - P. 1122-1127.). В настоящее время метод не нашел применения в рутинных исследованиях из-за трудоемкости, определения только десиалированных ЛНП из всего пула множественно модифицированных ЛНП.
Таким образом, известные методы выделения фракции липопротеинов из образцов сыворотки крови трудоемки, длительны, требуют использования дорогостоящего оборудования, а также использования химически активных реактивов, влияющих на целостность структуры как липопротеинов.
Наиболее близким техническим решением является определение множественно модифицированных липопротеинов низкой плотности (ммЛНП) в сыворотке крови человека путем обработки ее буфером, содержащим поливинилпирролидон с молекулярной массой 35000 (ПВП-35000), и последующей регистрацией помутнения по сравнению с контрольной пробой. Наличие помутнения, обусловленного агрегацией ммЛНП, свидетельствует об атерогенности крови (Шойбонов Б.Б., Шойбонова Б.В. Способ определения атерогенности крови человека // Патент РФ №2497116 от 27.10.2013 г.).
Недостатками данного метода являются то, что способ выявляет не только ммЛНП, но и частично наблюдается агрегация циркулирующих иммунных комплексов, которые при турбидиметрии завышают уровень содержания ммЛНП, метод выявляет ммЛНП полуколичественно и при повышенном уровне иммунных комплексов может давать ложно положительный результат при диагностике субклинического атеросклероза.
Задачей настоящего изобретения является расширение арсенала реагентов для выделения и определения количества ммЛНП, ключевого маркера субклинического атеросклероза.
Поставленная задача решается путем добавления к сыворотке крови человека буферного раствора, содержащего поливинилпирролидон с молекулярной массой 35000 (ПВП-35000), осаждения агрегированных ммЛНП центрифугированием, декантации супернатанта, растворения преципитата в буфере без ПВП и определения холестерина с использованием стандартных коммерческих китов.
Техническим результатом, получаемым при реализации изобретения, является расширение арсенала способов и реагентов для выделения ммЛНП и определения в них холестерина с целью ранней биохимической диагностики субклинического атеросклероза, а также исследования молекулярного состава атерогенных ммЛНП у конкретных индивидумов для оценки тяжести патологического процесса и разработки прогностических критериев сосудистых осложнений на доклинической стадии атеросклероза. Этот результат достигается тем, что выделение ммЛНП из сыворотки крови человека и определение количества холестерина ммЛНП проводят путем обработки ее буфером, содержащим ПВП-35000, инкубации пробы в течение 10 мин при комнатной температуре, осаждения агрегированных ммЛНП центрифугированием, декантацией, растворением преципитированных ммЛНП в буфере без ПВП и определения холестерина в преципитате, при уровне холестерина более 6,6 мг/дл констатируют повышенный уровень ммЛНП у обследуемого индивидуума.
Выделение ммЛНП и определение холестерина ммЛНП с использованием ПВП-35000 (ООО «АК Синтвита», Россия). Буфер-1 для агрегации ммЛНП готовят растворением 20,0 г ПВП-35000 в 100 мл 0,01М Трис-HCl-буфера, рН 7,4, содержащего 0,15 М NaCl. Буфер-2, в отличие от Буфера-1, не содержит ПВП-35000.
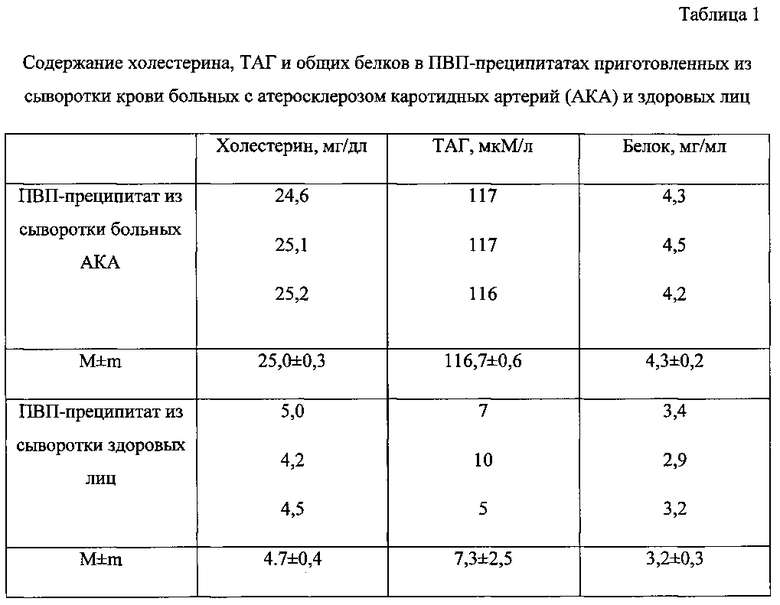
Пример 1. Определение содержания холестерина, триацилглицеридов (ТАГ) и общих белков в ПВП-преципитатах. Для подтверждения наличия ммЛНП в индивидуальных ПВП-преципитатах, приготовленных из сыворотки крови больных с атеросклерозом каротидных артерий и относительно здоровых людей, проходящих плановое медицинское обследование, были проведены следующие эксперименты. К 100 мкл сыворотки крови человека в пробирках типа «эппендорф» добавляют 84 мкл 20% ПВП-35000 (соотношение сыворотки к 20% ПВП (1,0:0,84), тщательно перемешивают и после 10-минутной инкубации при комнатной температуре, агрегированные ммЛНП осаждают путем центрифугирования при 9000 об/мин в течение 10 мин при 23°С в угловом роторе для микропробирок. ПВП-преципитат тщательно декантируют и ресуспендируют в 100 мкл буфера-2. После растворения осадка в полученных ПВП-преципитатах определяют содержание холестерина, ТАГ и общих белков с использованием коммерческих ферментных наборов. Полученные результаты представлены в таблице 1.
Как видно из данных, представленных в таблице 1, в ПВП-преципитате пулированной сыворотки больных с АКА содержание холестерина в 5,3 раз, а ТАГ - в 16 раз больше, чем в ПВП-преципитате из сыворотки здоровых лиц. Содержание общего белка в 1,3 раза выше в ПВП-преципитате больных.
Таким образом, наличие холестерина, ТАГ и белка в ПВП-преципитатах из сывороток свидетельствует о липопротеиновой природе агрегатов, образующихся в среде, содержащей 9,1% ПВП-35000 и 54% сыворотки крови человека. Повышенный уровень ПВП-преципитата, содержащего ммЛНП у больных с АКА, подтверждает патологическую роль ммЛНП при атеросклеротическом процессе.
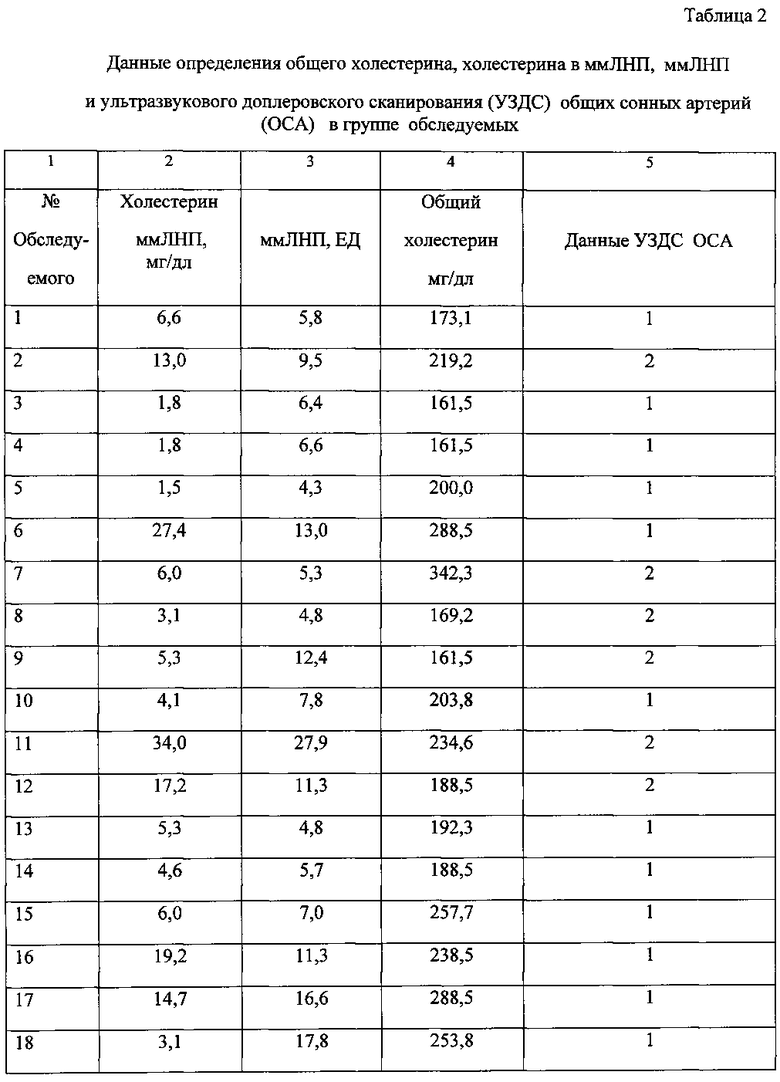
Пример 2. Определение уровня содержания холестерина в ммЛНП в сыворотке обследуемых лиц. Проведены исследования содержания холестерина в ммЛНП предлагаемым способом и прототипом в сыворотке 31 относительно здоровых людей. По предлагаемому способу, как описано в примере 1, определяли холестерин в ПВП-преципитатах. Данные по содержанию холестерина в ммЛНП представлены в таблице 2.
В прототипе использовали 10% ПВП 35000 (ООО «АК Синтвита», Россия) в 0,01 М Трис-HCl-буфере, содержащем 0,15 М NaCl, рН 7,4, как описано в работе (Шойбонов Б.Б., Шойбонова Б.В. // Патент РФ №2497116).
Кратко: 15 мкл исследуемой сыворотки добавляли 150 мкл буфера, содержащего 10% ПВП-35000 в 0,01 М Трис-HCl-буфере, содержащем 0,15 М NaCl, рН 7,4, тщательно перемешивали и инкубировали при комнатной температуре в течение 10 мин в 96-ти луночных плоскодонных иммунологических планшетах. Степень помутнения определяли турбидиметрически при длине волны 450 нм. В качестве бланка использовали пробы сыворотки с соответствующим количеством буфера без ПВП. Рассчитывали уровень содержания ммЛНП по формуле, описанной в прототипе. Полученные результаты по определению ммЛНП приведены в таблице 2.
Для определения общего холестерина в сыворотке крови использовали коммерческий ферментный набор «Холестерин» (ООО «ЭКОлаб», Россия). Данные представлены в таблице 2.
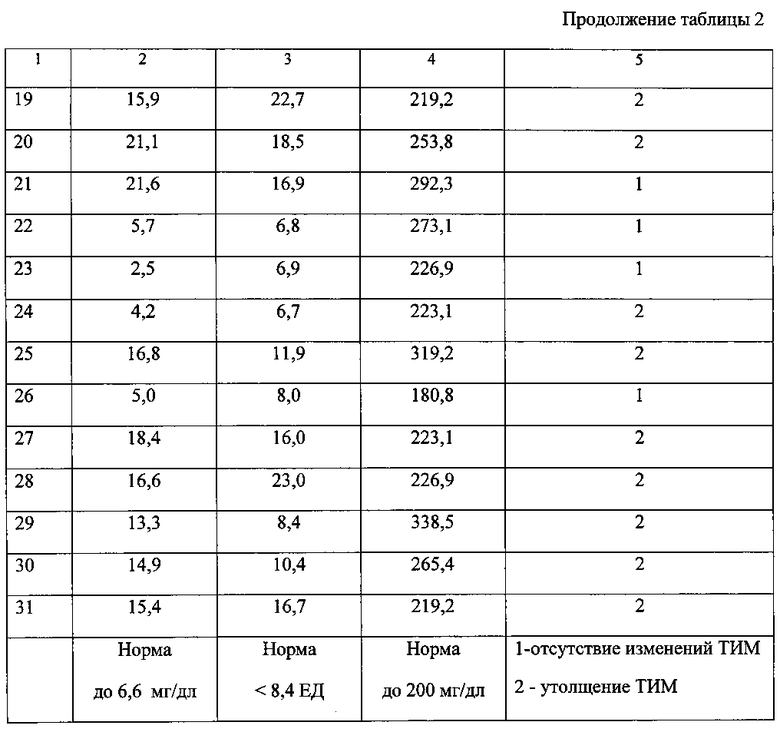
Для оценки состояния стенки сонных артерий (СА) использовали ультрасонографию высокого разрешения в В-режиме с применением линейного сосудистого датчика с частотой 7,5 МГц на ультразвуковом сканере «SonoScape SSI-1000» (Китай). Протокол обследования включал сканирование левой и правой общих СА (ОСА) с фокусировкой на задней стенке артерии в трех фиксированных проекциях - переднее-боковой, боковой и заднебоковой. Измерение толщины интима-медиа (ТИМ) осуществляли на участке ОСА длиной 10 мм, противолежащем началу каротидного синуса. ТИМ задней стенки ОСА определяли как расстояние от ведущего края первой эхогенной зоны до ведущего края второй эхогенной зоны. Среднее значение трех измерений рассматривали как интегральный показатель ТИМ. При значениях ТИМ, превышающих 0,9 мм для общих сонных артерий диагностируют атеросклеротическое поражение и при отсутствии симптомов ставится диагноз: «Субклинический атеросклероз». Данные ультразвукового доплеровского сканирования общих сонных артерий у обследованных лиц (31 человек) представлены в таблице 2. Отсутствие изменений ТИМ в таблице обозначено цифрой - 1, наличие утолщения ТИМ - цифра 2.
I. Как видно из данных, представленных в таблице 2, у 15 обследованных лиц по данным ультразвукового доплеровского сканирования (УЗДС) общих сонных артерий были выявлены изменения толщины интима-медиа в виде утолщения более 0,9 мм. Таким образом, по данным УЗДС общих сонных артерий у 48% обследованных выставлен диагноз «Субклинический атеросклероз». Установлено, что при ссужении артерий более 70% просвета сосуда появляются признаки ишемии, проявляющиеся разными симптомами, обусловленными гипоксией головного мозга.
II. Данные исследования уровня содержания множественно модифицированных ЛНП в сыворотке крови по прототипу выявили:
1. Из 15 человек с субклиническим атеросклерозом у 3 из них уровень содержания ммЛНП был в пределах нормальных величин (<8,4 ЕД), что составляет 20% ошибки;
2. Из 16 обследованных без изменений в сосудах (здоровые лица) у 4 из них был выявлен повышенный уровень ммЛНП, что составило 31% (гипердиагностика);
3. По данным УЗДС за нормальный уровень ммЛНП по данному контингенту можно считать величину менее 8,4 ЕД.
III. Исследования холестерина в ммЛНП по предлагаемому способу дали следующие результаты:
1. Из 15 человек с субклиническим атеросклерозом у 4 из них холестерин в ммЛНП был в пределах нормальных величин (<6,6 мг/дл), что составляет 27% ошибки;
2. Из 16 обследованных без изменений в сосудах у 4 из них был выявлен повышенный уровень холестерина в мм ЛНП, что составило 31% (гипердиагностика);
3. По данным УЗДС за нормальный уровень холестерина в ммЛНП по данному контингенту можно считать величину менее 6,6 мг/дл.
Таким образом, полученные результаты исследования атерогенности крови с использованием способа-прототипа и предлагаемого способа, дали следующие расхождения:
1. Нормальный уровень содержания холестерин в ммЛНП в 1 случае не совпал с повышенным уровнем ммЛНП (прототип) и наличием субклинического атеросклероза, подтвержденного инструментальным методом (УЗДС общих сонных артерий);
2. Нормальный уровень содержания холестерина в ммЛНП и нормальный уровень содержания ммЛНП (прототип) у 3 обследованных лиц не совпал с субклиническим атеросклерозом;
3. Оба метода у 4 обследованных лиц выявили повышенные уровни ммЛНП и холестерина в ммЛНП (совпадение), хотя инструментально не были выявлены изменения интима-медиального комплекса общих сонных артерий. Следует отметить, что у всех лиц с «гипердиагностикой» атеросклероза по предлагаемому способу и прототипу выявлены повышенные уровни общего холестерина.
Полученные результаты с использованием двух методов определения атерогенности крови (ммЛНП и холестерин ммЛНП) свидетельствуют о том что, 20-30% ошибки биохимической диагностики субклинического атеросклероза связаны с повышенной атерогенностью данных меркеров.
Разработанный способ был авторами использован для исследования атерогенности выделенных ммЛНП в гемолитическом тесте с использованием аутологичных эритроцитов человека в качестве мишеней. Полученные результаты свидетельствуют о том, что при одинаковом содержании холестерина в ммЛНП, приготовленных из индивидуальных сывороток больных с атеросклерозом каротидных артерий, в новом тесте определения атерогенности по лизису собственных эритроцитов различаются по литической активности.
Таким образом, выделение ммЛНП из сыворотки крови человека позволяет исследовать его функциональную активность и тем самым от характеристики количественных характеристик данного ключевого маркера атеросклероза перейти к оценке качественных характеристик, т.е. степени патогенности. Оценка степени патогенности (литической активности) позволит прогнозировать скорость (тяжесть) течения атеросклеротического процесса, с одной стороны, контролировать эффективность терапии, с другой стороны.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ЛИТИЧЕСКОЙ АКТИВНОСТИ МНОЖЕСТВЕННО МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИНОВ НИЗКОЙ ПЛОТНОСТИ | 2015 |
|
RU2577719C1 |
| СПОСОБ ВЫДЕЛЕНИЯ И ИССЛЕДОВАНИЯ АТЕРОГЕННОСТИ ИММУННЫХ КОМПЛЕКСОВ, СОДЕРЖАЩИХ МНОЖЕСТВЕННО МОДИФИЦИРОВАННЫЕ ЛИПОПРОТЕИНЫ | 2016 |
|
RU2632118C1 |
| СПОСОБ ЭКСПРЕСС-ОПРЕДЕЛЕНИЯ РЕЗИСТЕНТНОСТИ К ОКИСЛЕНИЮ ЛИПОПРОТЕИНОВ НИЗКОЙ ПЛОТНОСТИ СЫВОРОТКИ КРОВИ ЧЕЛОВЕКА | 2015 |
|
RU2578027C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АТЕРОГЕННОСТИ ИММУННЫХ КОМПЛЕКСОВ | 2013 |
|
RU2549467C1 |
| Способ оценки характера аутоиммунной реакции организма человека на множественно модифицированные липопротеины низкой плотности в литическом тесте | 2017 |
|
RU2680848C1 |
| СПОСОБ ИЗМЕРЕНИЯ КОНЦЕНТРАЦИИ ЦИРКУЛИРУЮЩИХ МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИДОВ НИЗКОЙ ПЛОТНОСТИ В СЫВОРОТКЕ КРОВИ ЧЕЛОВЕКА | 2016 |
|
RU2659211C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ АТЕРОГЕННОСТИ КРОВИ ЧЕЛОВЕКА | 2012 |
|
RU2497116C1 |
| СПОСОБ ЭКСПРЕСС-ОПРЕДЕЛЕНИЯ ХОЛЕСТЕРИНА В ИММУННЫХ КОМПЛЕКСАХ | 2013 |
|
RU2538685C1 |
| СПОСОБ МОДЕЛИРОВАНИЯ СОСУДИСТОЙ ДИСТОНИИ У КРЫС ПО ГИПОТЕНЗИВНОМУ ТИПУ | 2014 |
|
RU2614521C2 |
| ЭКСПРЕСС-СПОСОБ ОПРЕДЕЛЕНИЯ АТЕРОГЕННОСТИ ИММУННЫХ КОМПЛЕКСОВ СЫВОРОТКИ КРОВИ ЧЕЛОВЕКА | 2013 |
|
RU2549466C1 |
Изобретение относится к клинической биохимии и может быть использовано для выделения и определения холестерина множественно модифицированных липопротеинов низкой плотности (ммЛНП) в сыворотке крови человека. Способ заключается в том, что сыворотку крови обрабатывают 20%-ным буферным раствором поливинилпирролидона с молекулярной массой 35000 (ПВП-35000) при объемном соотношении сыворотка:ПВП (1,0:0,84), с последующей инкубацией в течение 10 мин при комнатной температуре, агрегаты ммЛНП осаждают центрифугированием при 9000 об/мин в течение 10 мин при 23°С, декантируют, осадок ммЛНП растворяют в буфере без ПВП-35000 и определяют холестерин в преципитате. При уровне содержания холестерина в ммЛНП более 6,6 мг/дл констатируют повышенный уровень ммЛНП у обследуемого индивидуума. Изобретение может быть использовано для установления наличия субклинического атеросклероза у обследуемого индивидуума, оценки тяжести патологического процесса и разработки прогностических критериев сосудистых осложнений. 2 табл., 2 пр.
Способ выделения и определения холестерина множественно модифицированных липопротеинов низкой плотности (ммЛНП) в сыворотке крови человека, заключающийся в том, что сыворотку крови обрабатывают 20%-ным буферным раствором поливинилпирролидона с молекулярной массой 35000 (ПВП-35000) при объемном соотношении сыворотка:ПВП (1,0:0,84), с последующей инкубацией в течение 10 мин при комнатной температуре, агрегаты ммЛНП осаждают центрифугированием при 9000 об/мин в течение 10 мин при 23°С, декантируют, осадок ммЛНП растворяют в буфере без ПВП-35000 и определяют холестерин в преципитате и при уровне содержания холестерина в ммЛНП более 6,6 мг/дл констатируют повышенный уровень ммЛНП у обследуемого индивидуума.
| СПОСОБ ОПРЕДЕЛЕНИЯ МИНИМАЛЬНО МОДИФИЦИРОВАННЫХ ЛИПОПРОТЕИНОВ НИЗКОЙ ПЛОТНОСТИ В СЫВОРОТКЕ ИЛИ ПЛАЗМЕ КРОВИ ЧЕЛОВЕКА | 2012 |
|
RU2501013C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ РИСКА ФОРМИРОВАНИЯ КЛИНИЧЕСКИХ ОСЛОЖНЕНИЙ АТЕРОСКЛЕРОЗА | 2011 |
|
RU2498307C2 |
| Tertov V.V., Orekhov A.N., Nikitina N.A | |||
| et al | |||
| Peritoneal macrophages: a model for detecting atherogenic potential in patiens' blood serum // Ann | |||
| Med | |||
| Механизм для сообщения поршню рабочего цилиндра возвратно-поступательного движения | 1918 |
|
SU1989A1 |
| Выбрасывающий ячеистый аппарат для рядовых сеялок | 1922 |
|
SU21A1 |
| P | |||
| Снеговая лыжа для самолетов | 1913 |
|
SU455A1 |
| Мельниченко А | |||
| А | |||
| Механизмы и роль атерогенной модификации липопротеидов в атерогенезе | |||
| Автореф | |||
| дисс | |||
| д.б.н. | |||
Авторы
Даты
2016-07-20—Публикация
2015-01-15—Подача