Область техники
Изобретение относится к неводному жидкому электролиту для вторичных аккумуляторов и к аккумулятору с металлическим анодом, содержащему жидкий неводный электролит.
Уровень техники
Из уровня техники (ЕР 1173899 А1, 23.01.2002) известен неводный жидкий электролит для литиевых аккумуляторов, содержащий соль лития - LiClO4, LiPF6 и др., растворенную в растворителе- органические карбонаты, эфиры и др.
Такие электролиты стабильны до 4-4,5 В и обладают проводимостью по литию порядка 10-2-10-3 См/см. Тем не менее, образование дендритов при перезаряде аккумулятора приводит к деградации его емкости и сокращению срока службы.
Наиболее близким аналогом заявленного изобретения является неводный жидкий электролит, раскрытый в US 2013/0202920 А1, 08.08.2013. Для снижения дендритообразования электролит содержит смесь двух растворов солей: LiPF6 и CsPF6.
Недостатками данного технического решения являются:
- Невысокая емкость аккумулятора - менее 250 мАч/г;
- потеря емкости составляет до 40% за 100 циклов перезарядки;
- растворимость CsPF6 в апротонных растворителях невысока, что не позволяет повышать равномерность осаждения лития за счет дальнейшего увеличения его концентрации в электролите;
- при повышении концентрации CsPF6 потенциал осаждения цезия из раствора приближается к потенциалу осаждения лития, что может привести к осаждению цезия и снижению кулоновской эффективности переосаждения.
Раскрытие изобретения
Задача предлагаемого технического решения состоит в разработке электролита для вторичных аккумуляторов, эффективно подавляющего образование дендритов и увеличивающего кулоновскую эффективность перезаряда.
Техническим результатом изобретения является увеличение емкости и срока службы аккумулятора за счет электролита, способствующего снижению дендритообразования и увеличению кулоновской эффективности перезаряда.
Данный технический результат достигается за счет того, что в отличие от известного электролита, содержащего смесь растворов двух солей, в предложенном жидком электролите для вторичного аккумулятора содержится смесь двух солей, растворенных в органическом растворителе, при этом первая соль содержит катион металла, совпадающий с материалом анода, и анион, выбранный из группы: 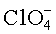
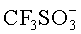
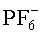
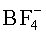
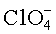
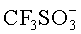
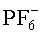
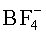
Катион металла первой соли выбран из группы: Li+, Na+, K+, Mg2+, Са2+, Zn2+, Al3+, Fe2+.
Концентрация первой соли в растворе составляет 0,01-2 М.
Концентрация второй соли в растворе составляет 0,001-2 М.
В качестве растворителя используют выбранные из группы: пропиленкарбонат, этиленкарбонат, бутиленкарбонат, диметилкарбонат, этилметилкарбонат, диэтилкарбонат, 1,2-диметоксиэтан, 1,3-диоксолан, тетрагидрофуран, диметиловый эфир диэтиленгликоля, диметиловый эфир триэтиленгликоля, дибутиловый эфир диэтиленгликоля, диметилсульфоксид, гексафторфосфат 1-этил-3-метилимидазолия, тетрафторборат 1-этил-3-метилимидазолия, бис-трифторметилсульфонилимид 1-этил-3-метилимидазолия, гексафторфосфат 1-бутил-3-метилимидазолия, бис-трифторметилсульфонилимид 1-бутил-3-метилимидазолия, гексафторфосфат 1-метил-1-пропилпиперидиния, бис-трифторметилсульфонилимид 1-метил-1-пропил пиперидиния или их различные смеси, при их различном соотношении в смеси.
Кроме того, данный технический результат достигается за счет того, что вторичный аккумулятор содержит металлический анод, катод и раскрытый выше жидкий электролит.
Материал анода включает металл, выбранный из группы: Li, Na, K, Mg, Са, Zn, Al, Fe.
Материал катода выбран из группы: ацетиленовая сажа, графен, углеродные нанотрубки, оксиды переходных металлов, соединения со структурой перовскита, оливина или шпинели.
Краткое описание чертежей
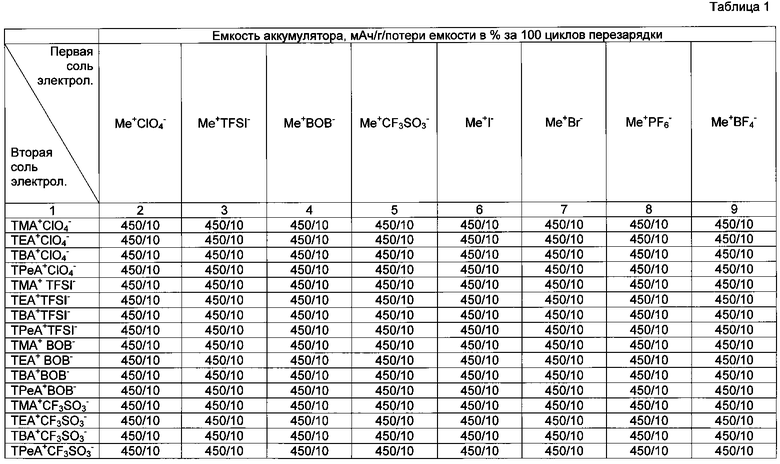
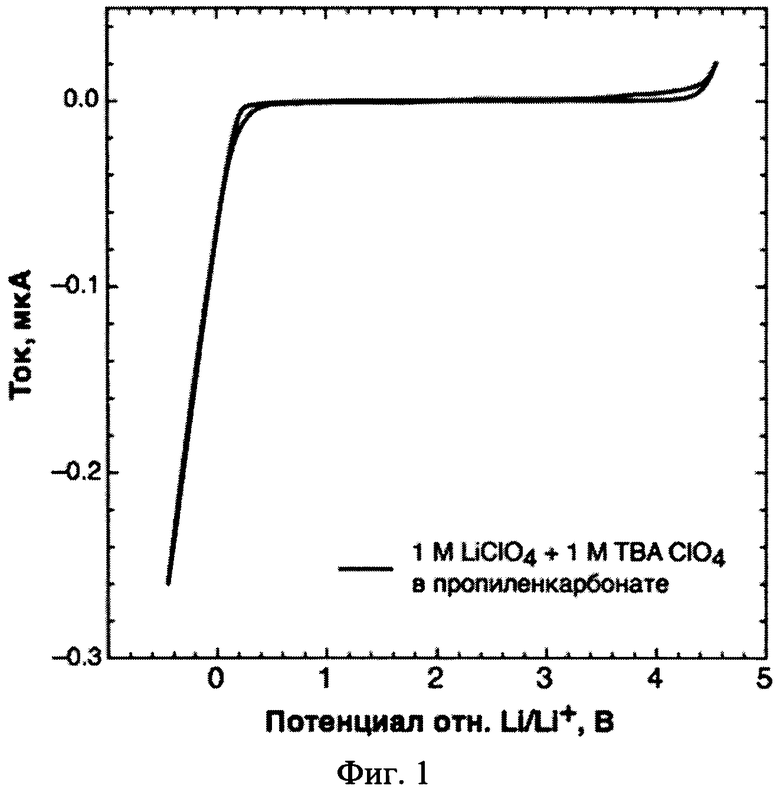
Фиг. 1 - Циклические вольтамперограммы электрохимической ячейки с электролитом, содержащим 1 М LiClO4 и 1 М TBAClO4 в пропиленкарбонате.
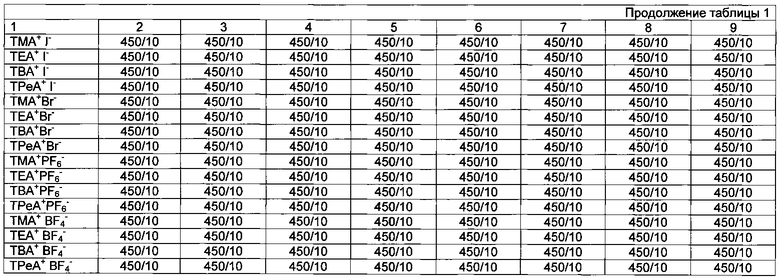
Фиг. 2 - Циклические вольтамперограммы электрохимической ячейки с электролитом, содержащим 1 М LiClO4 и 1 М TBAClO4 в тетрагидрофуране.
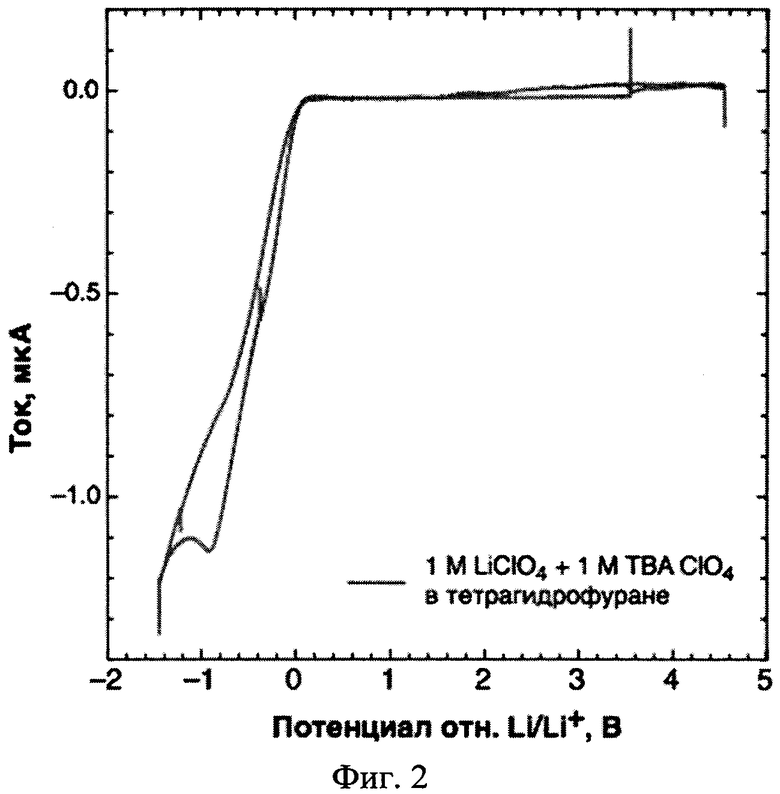
Фиг. 3 - Циклические вольтамперограммы электрохимической ячейки с электролитом, содержащим 1 М LiClO4 в растворителе, содержащем пропиленкарбонат и диметоксиэтан в соотношении 7:3 по объему, соответственно.
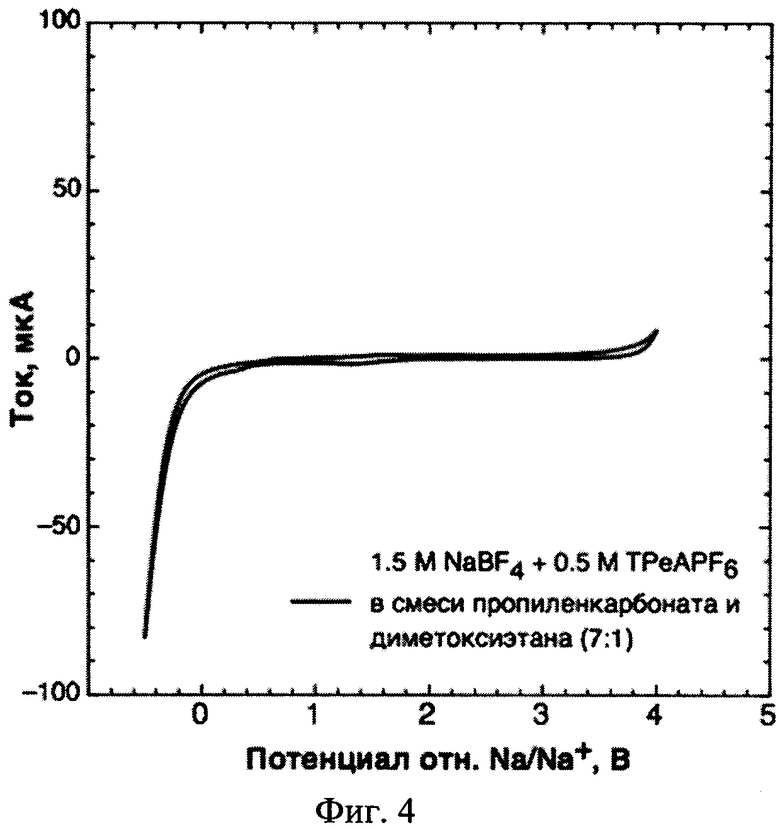
Фиг. 4 - Циклические вольтамперограммы электрохимической ячейки с электролитом, содержащим 1 М концентрации NaBF4 и 0,5 М концентрации TPeAPF6 в растворителе, содержащем пропиленкарбонат и диметоксиэтан в соотношении 7:1 по объему, соответственно.
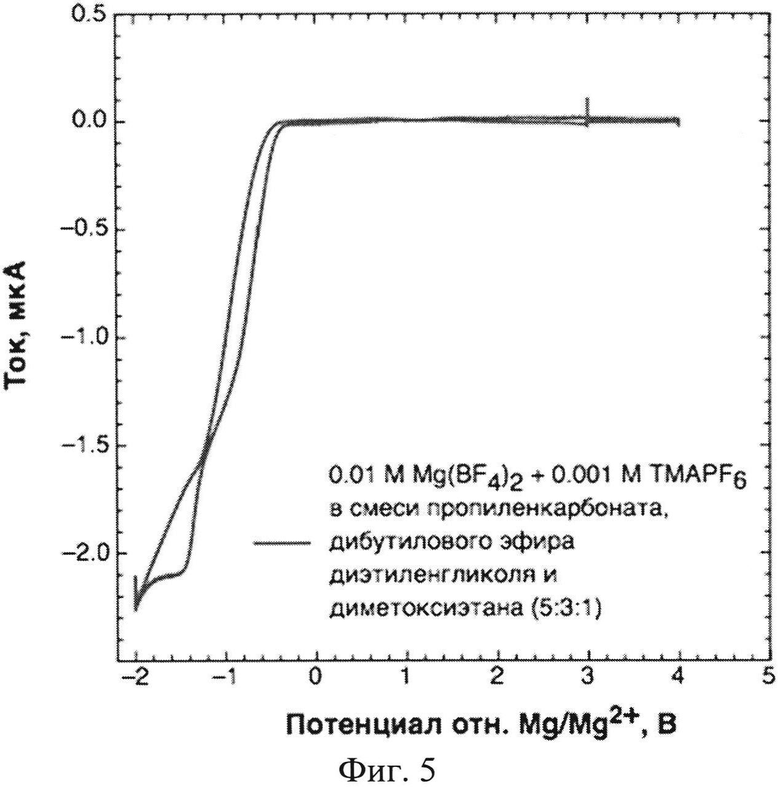
Фиг. 5 - Циклические вольтамперограммы электрохимической ячейки с электролитом, содержащим 0,01 М концентрации Mg(BF4)2 и 0,001 М концентрации TMAPF6 в растворителе, содержащем пропиленкарбонат, дибутиловый эфир диэтиленгликоля и диметоксиэтан в соотношении 5:3:1 по объему, соответственно.
Фиг. 6 - Фотографии поверхности металлического лития после перезаряда в пропиленкарбонате с добавлением различных солей.
Фиг. 7 - Фотографии поверхности металлического натрия до и после осаждения натрия (до и после перезаряда) в электролите, содержащем 1 М концентрации NaBF4 и 0,5 М концентрации TPeAPF6 в растворителе, содержащем пропиленкарбонат и диметоксиэтан в соотношении 7:1 по объему, соответственно.
Фиг. 8 - Фотографии поверхности металлического магния до и после осаждения магния (до и после перезаряда) в электролите, содержащем 0,01 М концентрации Mg(BF4)2 и 0,001 М концентрации TMAPF6 в растворителе, содержащем пропиленкарбонат, дибутиловый эфир диэтиленгликоля и диметоксиэтан в соотношении 5:3:1 по объему соответственно.
Осуществление изобретения
Жидкий электролит для вторичного аккумулятора включает смесь двух солей, растворенных в органическом растворителе. При этом первая соль с концентрацией 0,01-2 М в растворе содержит катион металла, совпадающий с материалом анода, и анион, выбранный из группы: 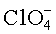
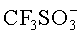
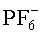
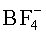
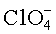
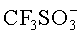
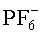
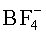
При концентрации первой соли менее 0,01 М и более 2 М проводимость электролита по ионам металла будет слишком низкой, что приведет к ухудшению характеристик аккумулятора.
Концентрация второй соли 0,001-2 М обеспечивает получение первой соли в растворе с концентрацией 0,01-2 М, при этом концентрация второй соли менее 0,001 М приведет к ухудшению характеристик аккумулятора в связи с очень малым содержанием катионов (ТВА+ или др.) в электролите, а концентрация второй соли выше 2 М не позволит растворить необходимое количество первой соли, обеспечивающее в растворе концентрацию первой соли 0,01-2 М.
Аккумулятор содержит корпус, выполненный с возможностью размещения в нем катода и анода, находящихся на расстоянии друг от друга и помещенных в электролит, которым заполняют корпус аккумулятора.
Пример 1
Для получения необходимого объема неводного жидкого электролита растворяют порошки солей LiClO4 и TBAClO4 в пропиленкарбонате, с получением 1 М концентрации LiClO4 и 1 М концентрации TBAClO4 в растворе. Полученный электролит используют в аккумуляторе с анодом из металлического Li. Из фиг. 1, на которой изображена циклическая вольтамперограмма, видно, что при содержании в аккумуляторе электролита, содержащего вышеуказанные соли, указанные соли электрохимически стабильны при потенциалах осаждения металлического лития, что приводит к снижению образования побочных продуктов и дендритов в аккумуляторе, а следовательно, к увеличению емкости и количества циклов перезарядки аккумулятора. По сравнению с фиг. 3, на которой изображена циклическая вольтамперограмма для электролита с 1 М раствором LiClO4, добавление второй соли в электролит приводит к увеличению электрохимической стабильности. Из фиг. 2 видно, что даже при малых концентрациях в электролите вышеуказанные соли способствуют снижению дендритообразования, по сравнению с электролитами, содержащими другие соли.
Пример 2
Для получения необходимого объема неводного жидкого электролита растворяют порошки солей LiClO4 и TBAClO4 в тетрагидрофуране, с получением 1 М концентрации LiClO4 и 1 М концентрации TBAClO4 в растворе. Полученный электролит используют в аккумуляторе с анодом из металлического Li.
Из фиг. 2, на которой изображена циклическая вольтамперограмма, видно, что при содержании в аккумуляторе электролита, содержащего вышеуказанные соли, указанные соли электрохимически стабильны при потенциалах осаждения металлического лития, что приводит к снижению образования побочных продуктов и дендритов в аккумуляторе, а следовательно, к увеличению емкости и срока службы аккумулятора.
Пример 3
Для получения необходимого объема неводного жидкого электролита растворяют порошки солей NaBF4 и TPeAPF6 в растворителе, содержащем пропиленкарбонат и диметоксиэтан в соотношении 7:1 по объему, соответственно, с получением 1,5 М концентрации NaBF4 и 0,5 М концентрации TPeAPF6 в растворе. Полученный электролит используют в аккумуляторе с анодом из металлического Na.
Из фиг. 4, на которой изображена циклическая вольтамперограмма, видно, что при содержании в аккумуляторе электролита, содержащего вышеуказанные соли, указанные соли электрохимически стабильны при потенциалах осаждения металлического лития, что приводит к снижению образования побочных продуктов и дендритов в аккумуляторе, а следовательно, к увеличению емкости и количества циклов перезарядки аккумулятора. Из фиг. 7 видно, что использование в аккумуляторе электролита, содержащего вышеуказанные соли, способствует снижению дендритообразования.
Пример 4
Для получения необходимого объема неводного жидкого электролита растворяют порошки солей Mg(BF4)2 и TMAPF6 в растворителе, содержащем пропиленкарбонат, дибутиловый эфир диэтиленгликоля и диметоксиэтан в соотношении 5:3:1 по объему, соответственно, с получением 0,01 М концентрации Mg(BF4)2 и 0,001 М концентрации TMAPF6 в растворе. Полученный электролит используют в аккумуляторе с анодом из металлического Mg.
Из фиг. 5, на которой изображена циклическая вольтамперограмма, видно, что при содержании в аккумуляторе электролита, содержащего вышеуказанные соли, указанные соли электрохимически стабильны при потенциалах осаждения металлического лития, что приводит к снижению образование побочных продуктов и дендритов в аккумуляторе, а следовательно, к увеличению емкости и количества циклов перезарядки аккумулятора. Из фиг. 8 видно, что использование в аккумуляторе электролита, содержащего вышеуказанные соли, способствует снижению дендритообразования.
Пример 5
Аккумулятор с анодом из металлического Li, катодом из ацетиленовой сажи и электролитом, содержащим 1 М LiClO4 и 1 М TBAClO4 в пропиленкарбонате, работает следующим образом. При разряде аккумулятора литиевый анод растворяется с образованием ионов Li+, которые переходят в электролит, содержащий 1 М LiClO4 и 1 М TBAClO4 в пропиленкарбонате. За счет наличия в электролите соли LiClO4 ионы Li+ внедряются в структуру катодного материала с образованием литий-содержащих фаз. При заряде ионы Li+ выходят из структуры катодного материала, поступают в электролит и затем равномерно осаждаются в виде металла на поверхность анода. Соль TBAClO4 препятствует росту дендритов, способствуя равномерному заполнению поверхности анода при осаждении.
Таким образом, предлагаемое изобретение позволяет получить аккумулятор, имеющий более высокую емкость и количество циклов перезарядки аккумулятора.
Изобретение было раскрыто выше со ссылкой на конкретный вариант его осуществления. Для специалистов могут быть очевидны и иные варианты осуществления изобретения, не меняющие его сущности, как она раскрыта в настоящем описании. Соответственно, изобретение следует считать ограниченным по объему только нижеследующей формулой изобретения.
Me - Li+, Na+, K+, Mg+, Ca2+, Zn2+, Al3+, Fe2+.
| название | год | авторы | номер документа |
|---|---|---|---|
| АНОДНЫЙ МАТЕРИАЛ С ПОКРЫТИЕМ И АККУМУЛЯТОР С МЕТАЛЛИЧЕСКИМ АНОДОМ | 2014 |
|
RU2579357C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КАТОДНОГО МАТЕРИАЛА, КАТОДНЫЙ МАТЕРИАЛ И ЛИТИЙ-ИОННЫЙ АККУМУЛЯТОР | 2014 |
|
RU2585176C1 |
| ПОРИСТЫЙ ЛИТИЕВЫЙ АНОД | 2016 |
|
RU2626457C1 |
| ЛИТИЙ-ВОЗДУШНЫЙ АККУМУЛЯТОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2012 |
|
RU2591203C2 |
| Высокорастворимый католит на основе трифениламина и электрохимический источник тока на его основе | 2020 |
|
RU2752762C1 |
| ДОБАВКИ ДЛЯ ГАЛЬВАНИЧЕСКИХ БАТАРЕЙ | 2013 |
|
RU2665552C2 |
| ГЕЛЬ-ПОЛИМЕРНЫЙ ЭЛЕКТРОЛИТ ДЛЯ ЛИТИЙ-ИОННОГО АККУМУЛЯТОРА | 2011 |
|
RU2457587C1 |
| СПОСОБ ПОЛУЧЕНИЯ АНОДА ПЕРЕЗАРЯЖАЕМОГО ЛИТИЕВОГО ИСТОЧНИКА ТОКА | 1995 |
|
RU2082261C1 |
| ЛИТИЙ-ВОЗДУШНЫЙ АККУМУЛЯТОР И СПОСОБ ЕГО ИЗГОТОВЛЕНИЯ | 2012 |
|
RU2578196C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ЛИТИЕВЫХ АККУМУЛЯТОРОВ ЭЛЕКТРОХИМИЧЕСКОЙ СИСТЕМЫ ЛИТИЙ-ЛИТИРОВАННЫЙ ДИОКСИД МАРГАНЦА | 2000 |
|
RU2179771C1 |



Изобретение относится к жидкому электролиту для вторичного аккумулятора, включающему смесь двух солей, растворенных в органическом растворителе. При этом первая соль содержит катион металла, совпадающий с материалом анода, и анион, выбранный из группы: 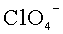
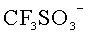
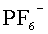
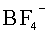
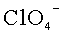
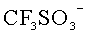
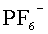
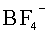
1. Жидкий электролит для вторичного аккумулятора, включающий смесь двух солей, растворенных в органическом растворителе, при этом первая соль содержит катион металла, совпадающий с материалом анода и анион, выбранный из группы: 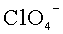
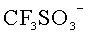
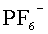
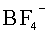
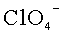
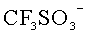
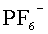
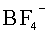
2. Электролит по п.1, отличающийся тем, что катион металла первой соли выбран из группы: Li+, Na+, К+, Mg+, Са2+, Zn2+, Al3+, Fe2+.
3. Электролит по п. 1, отличающийся тем, что концентрация первой соли в растворе составляет 0,01-2 М.
4. Электролит по п. 1, отличающийся тем, что в качестве растворителя используют выбранные из группы: пропиленкарбонат, этиленкарбонат, бутиленкарбонат, диметилкарбонат, этилметилкарбонат, диэтилкарбонат, 1,2-диметоксиэтан, 1,3-диоксолан, тетрагидрофуран, диметиловый эфир диэтиленгликоля, диметиловый эфир триэтиленгликоля, дибутиловый эфир диэтиленгликоля, диметилсульфоксид, гексафторфосфат 1-этил-3-метилимидазолия, тетрафторборат 1-этил-3-метилимидазолия, бис-трифторметилсульфонилимид 1-этил-3-метилимидазолия, гексафторфосфат 1-бутил-3-метилимидазолия, бис-трифторметилсульфонилимид 1-бутил-3-метилимидазолия, гексафторфосфат 1-метил-1-пропилпиперидиния, бис-трифторметилсульфонилимид 1-метил-1-пропилпиперидиния или их различные смеси, при их различном соотношении в смеси.
5. Вторичный аккумулятор, включающий металлический анод, катод и жидкий электролит по пп. 1-4.
6. Аккумулятор по п. 5, отличающийся тем, что материал анода включает металл, выбранный из группы: Li, Na, К, Mg, Са, Zn, Al, Fe.
7. Аккумулятор по п. 5, отличающийся тем, что материал катода выбран из группы: ацетиленовая сажа, графен, углеродные нанотрубки, оксиды переходных металлов, соединения со структурой перовскита, оливина или шпинели.
| Многоступенчатая активно-реактивная турбина | 1924 |
|
SU2013A1 |
| JP 2009158240 A, 16.07.2009 | |||
| JP 07065842 A, 10.03.1995 | |||
| Регулятор двух взаимосвязанных электрических величин | 1958 |
|
SU129709A1 |
Авторы
Даты
2016-04-10—Публикация
2014-09-15—Подача