Изобретение относится к области медицины, а именно к клинической иммунологии, и может быть использовано для определения сенсибилизации организма к антигенам HLA-G.
Известно, что на поверхности практически всех клеток организма представлены молекулы (белки), которые носят название антигенов главного комплекса гистосовместимости (HLA-антигены). Эти молекулы выполняют роль своеобразных "антенн" на поверхности клеток, которые позволяют организму распознавать собственные и чужие клетки (бактерии, вирусы, раковые клетки и т.д.) и при необходимости запускать иммунный ответ, обеспечивающий выработку специфических антител и удаление чужеродного агента из организма. Кроме того, доказана взаимосвязь между HLA-антигенами и предрасположенностью человека к ряду заболеваний, таких как анкилозирующий спондилит, синдром Рейно, сахарный диабет и т.д., а несовместимость супругов по HLA-антигенами и отличие плода от материнского организма является важным моментом, необходимым для сохранения и вынашивания беременности.
Известен способ молекулярно генетического определения HLA-фенотипа с использованием полимеразной цепной реакции (ПЦР), при котором очищенную ДНК размещают на рабочей станции PROTRANS в планшет с лиофилизированными праймерами из набора Protrans HLA-А, В, DRBI и Tag полимеразой, осуществляя амплификацию в термоцикле по установленной программе (Пат. 2423524 Рос. Федерация: МПК C12N 15/10. Способ HLA - типирования цельной крови [Текст] / А.Б. Смолянинов, Е.А. Котелевская, С.А. Смирнова и др.; заявитель и правообладатель Смолянинов A.B. (RU), ООО «Покровский банк стволовых клеток» (RU). - №2009149410/10; заяв. 29.12.2009; опубл. 10.07.2011. - Бюл. №19. - 5 с.). Визуализацию результатов ПЦР осуществляют методом электрофореза агарозным гелем, подкрашенным бромистым этидием и размещенным в электрофоретической ячейке. Под действием тока молекулы ДНК проходят через гель. По наличию продукта в лунке планшета со специфическими праймерами определяют HLA-генотип.
Недостатком известного способа является то, что он не позволяет достоверно оценить перекрестную совместимость доноров и реципиентов при трансплантации органов, а также прогнозировать вероятность иммунологических репродуктивных потерь в супружеских парах.
Известен способ иммунологического исследования сыворотки крови реципиента для выявления антител к антигенам HLA системы с помощью методики Luminex, при котором в качестве носителя (твердой фазы) используют полистироловые микросферы с интегрированными в их состав двумя флуорофорами и покрытые очищенными рекомбинантными HLA-антигенами (Руководство по диагностическому лабораторному обеспечению трансплантации солидных органов, оригинал документа доступен на сайте: www.beaumont.ie). При наличии в сыворотке антител на поверхности микросферы образуется комплекс АГ-АТ. После добавления к сыворотке коньюгата проводят ее исследование в потоке направляющей жидкости, при этом каждая микросфера подвергается облучению двумя лазерами с разной длиной волны и сигнал, испускаемый флуорофорами, регистрируется датчиками прибора. Таким образом, анализируется одновременно тип микросферы и наличие (концентрация) искомого аналита на соответствующем типе частиц.
Недостатком известного способа является то, что он позволяет проводить идентификацию антител к классическим HLA-антигенам I (А, В и С) и II (DR, DQ) классов и не определяет низко полиморфные молекулы главного комплекса гистосовместимости - HLA-G и HLA-Е.
Надо отметить, что в настоящее время отводится особая роль эмбриональным HLA-антигенам в регуляции иммунитета при репродукции. Молекулы HLA-G и HLA-E презентируют антигены трофобласта γσТ-клеткам, ограничивая иммунный ответ к ним. Кроме того, через взаимодействие HLA-G с киллингингибирующими рецепторами NK-лимфоцитов (CD94+NKG2A+) происходит ингибирование NK-активности, что способствует вынашиванию беременности (Grzywacz М., Gorski В., Jakubowska A. et al. Association between HLA-G01018 allele pregnancy complications // J. Reprod. Immunol. 2003. V. 58. №2. P. 162; King A., Allan D.S., Bowen M. et al. HLA-E expressed on trophoblast and interacts with CD94/NKG2 receptors on decidual NK cells // Eur. J. Immunol. 2000. V. 30. P. 1623-1631; Kovats S., Main E., Librach C. HLA-G expressed in human trophoblast // Science. 1990. V. 248. P. 220-223; Тарбаева Д.А., Кузник Б.И., Загородняя Э.Д., Иозефсон С.А. Функция HLA в репродуктивной системе // Забайкальский медицинский вестник. - 2009. - №1. - с. 6-19). С этих позиций разработка современных методов определения антител в сыворотке крови к HLA-G является актуальной задачей клинической иммунологии.
Наиболее близким к предлагаемому изобретению является способ оценки перекрестной совместимости (cross-match) донора и реципиента с использованием проточной цитофлуорометрии (The National Histocompatibility And Immunogenetics Service For Solid Organ Transplantation-NHISSOT - 8 издание, Beaumont Hospital, Дублин, Ирландия, 2011). Перекрестную пробу на совместимость проводят путем инкубации лимфоцитов донора, полученных из периферической крови с сывороткой реципиента, после чего выполняют окрашивание клеток флуоресцентными красителями или флюоресцирующими моноклональными антителами. Далее с помощью проточной цитофлуорометрии проводят анализ на наличие антител к HLA-антигенам донора.
Недостатком способа является отсутствие стандартизации при интерпритации полученных данных между разными лабораториями, а также отсутствие рекомендаций по определению антител к аллоНLА-G.
Техническим результатом предложенного изобретения является повышение качества и достоверности определения сенсибилизации донора к аллоНLА-G, за счет определения экспрессии молекул HLA-G на поверхности мононуклеров крови и расчета коэффициента подавления в опытных и контрольных образцах по субпопуляциям CD3+HLA-G+ и CD3-HLA-G+.
Ввиду того, что антитела к HLA-G индуцируются во время беременности и максимально представлены у многорожавших женщин, предложенный способ определения антител к аллоHLA-G исследовали у 13 семейных пар, имеющих двух и более детей, а также не имеющих общих антигенов HLA I и II классов. Соответственно наличие антител к HLA-G исследовали в женской сыворотке крови, а в качестве донаторов аллоНLА-G использовали мононуклеары их супругов (мужей). В качестве контроля принимали образцы мононуклеаров, обработанные отрицательным реагентом, не содержащим антител к HLA-G. Исследование проведено на базе ЗАО «Современные медицинские технологии» г. Кемерово.
Способ осуществляют следующим образом. Для получения мононуклеаров венозную кровь, полученную от мужчины (супруга) в объеме 3 мл, инкубируют в вакутейнере с антикоагулянтом (ЭДТА). А для получения исследуемой сыворотки кровь женщины в объеме 4 мл забирают в вакутейнер с активаторами свертывающей системы.
Кровь, полученную от донора моноклеаров (мужчины), разводят в 2 раза, добавляя 3 мл раствора однократного натрий-фосфатного буфера (PBS). Разведенную венозную кровь в объеме 6 мл переносят в центрифужную пробирку, содержащую 3 мл раствора фиколл-верографина плотностью 1,077. Центрифугирование пробирки (с уравновешиванием), содержащей фиколл-верографин, и разведенную венозную кровь проводят на 500 g, 30 минут при температуре +10°C. По окончании центрифугирования из пробирки отбирают интерфазное кольцо, содержащее мононуклеары, и выполняют их отмывку от раствора фиколл-верографина. Для этого в новую центрифужную пробирку переносят отобранные мононуклеары и добавляют 7 мл однократного PBS, последовательно выполняя пипетирование мононуклеаров и центрифугирование пробирки на 500 g в течение 7 минут при температуре +10°С. После этого надосадочную жидкость удаляют, а процедуру отмывки повторяют еще раз. После последней отмывки мононуклеары разводятся в 1000 мкл однократного PBS - окончательное разведение мононуклеаров.
Кровь от донора сыворотки (женщины) инкубируют в течение 35 минут при комнатной температуре, после чего центрифугируют в течение 30 минут при температуре +10°С на 500 g. Полученную сыворотку отбирают в отдельную пластиковую пробирку в объеме 1,5-2 мл.
Подготовленные мононуклеары донора разносят в четыре разные пробирки по 200 мкл в каждую. В первые две пробирки (1 и 2) к мононуклеарам добавляют по 50 мкл исследуемой сыворотки (опытные образцы), а в последующие две (3 и 4) по 50 мкл однократного PBS (контрольные образцы). Все образцы инкубируют в строго одинаковых условиях при температуре 37°С в течение 30 минут.
Далее выполняют двукратную отмывку мононуклеаров в опытных и контрольных образцах, для чего в каждую пробирку добавляют по 2 мл однократного PBS, мононуклеары пипетируют и центрифугируют на 500 g, 5 минут при температуре 10°С. Надосадочную жидкость удаляют, при этом остаточный объем жидкости не должен превышать 50 мкл.
Для проведения проточной цитофлуорометрии во все четыре пробирки вносят по 5 мкл смеси моноклональных антител с различными флуоресцентными красителями к:
- HLA-G конъюгированных с фикоэритрином (РЕ),
- CD3 с флуорисцеином изотиоцианатом (FITC),
- CD45 конъюгированных с алофикоцианином (АРС).
Далее все четыре пробирки с мононуклеарами инкубируют при 37°С, в течение 30 минут, и осуществляют двухкратную отмывку от не связавшихся моноклональных антител. После этого в каждую пробирку добавляют 200 мкл однократного фиксатора связи моноклональных антител с соответствующими рецепторами на мононуклеарах.
Окрашивание клеток крови через маркер CD45 позволяет выделить лейкоцитарные клетки, а добавление маркера CD3 позволяет дополнительно выделить CD3+ лимфоциты (Т-лимфоциты). Именно на Т-лимфоцитах экспрессируется HLA-G и это позволит увидеть снижение Т-лимфоцитов, экспрессирующих HLA-G при наличии антител к ним в опытной постановке по отношению к контрольной.
Проточную цитофлуорометрию мононуклеаров проводят поочередно в опытной постановке по пробиркам 1 и 2 (для дублирования) и контрольной постановке по пробиркам 3 и 4 (для дублирования).
При наличии антител к аллоНLА-G в исследуемой сыворотке во время инкубации образуются иммунные комплексы и дополнительное внесение в опытные образцы моноклональных антител к HLA-G не приведет к специфическому взаимодействию, поскольку молекулы HLA-G уже блокированы сывороточными аллоантителами. Напротив, в контрольных образцах процесс образования иммунных комплексов с моноклональными антителами HLA-G будет идти активно, так как молекулы HLA-G на них свободны.
Для оценки сенсибилизации по HLA-G значимыми являются субпопуляции CD3-HLA-G+ и CD3+HLA-G+. Поэтому выявленные при проточной цитофлуорометрии скопления мононуклеаров с маркером CD45 из каждой пробирки дополнительно анализируют по этим двум субпопуляциям.
После снятия результатов для каждой субпопуляции рассчитывают коэффициент подавления (КП) по формуле:

где HLA-Gоп - суммарное относительное число субпопуляций экспрессирующих HLA-G: (CD3-HLA-G+ + CD3+HLA-G+) в опытной постановке, %;
HLA-Gконт - суммарное относительное число субпопуляций экспрессирующих HLA-G: (CD3-HLA-G+ + CD3+HLA-G+) в контрольной постановке, %.
Коэффициент подавления - это процентное снижения удельного веса субпопуляций, экспрессирующих HLA-G, опытной постановки по отношению к таковому в контрольной постановке.
Наличие сенсибилизации к аллогенным HLA-G диагностируют при отрицательном значении КПHLA-G, рассчитанного из соотношения суммарных популяций CD3-HLA-G+ и CD3+HLA-G+, в опытной и контрольной постановках.
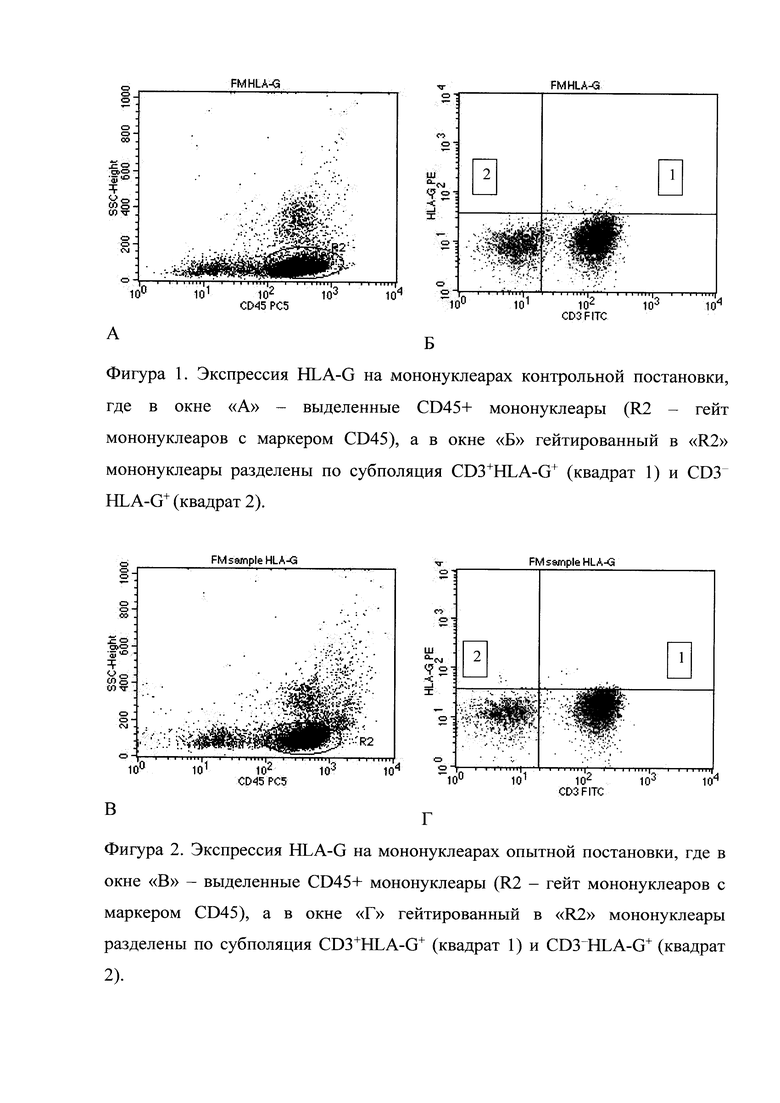
Сущность изобретения поясняется чертежами, где на фиг. 1 изображен протокол проточной цитофлуорометрии в контрольной постановке, а на фиг. 2 - протокол в опытной постановке, при этом А и В - точечная диаграмма мононуклеаров с маркером CD45, R2 - гейт мононуклеаров с маркером CD45, Б и Г - выделение монуклеаров по субполяции CD3+HLA-G+ и CD3-HLA-G+.
При проведении перекрестной реакции с исследуемой женской сывороткой, мононуклеарами супруга и моноклональными антителами к HLA-G выявлено достоверно значимое различие между удельным весом HLA-G+ мононуклеаров в опытной и контрольной постановках.
По результатам исследования уровень CD3+HLA-G+ в опытной группе составил 2,33±0,17%, в то время как в контроле он был равен 5,04+0,11% (p<0,05). Относительное количество CD3-HLA-G+ в опытной группе было 0,29±0,11%, в то время как в контроле этот показатель был равен 0,53±0,09% (p<0,05) (таблица 1).
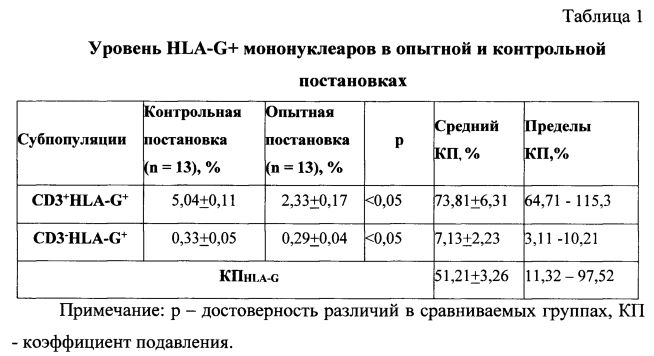
Представленные данные указывают на то, что с помощью предложенного способа в неродственных по HLA семейных парах антитела к HLA-G определяются в 100% случаев.
В исследовании для каждой семейной пары были выявлены средние значения коэффициентов подавления (КП) для субпопуляции CD3+HLA-G+ и для CD3-HLA-G+. Был рассчитан процент отклонения от среднего значения как для максимального значения КП, так и для минимального КП. В таблице 2 представлены значения среднего отклонения для субпопуляций CD3+HLA-G+ и CD3-HLA-G+.

Также указаны данные о максимальном и минимальном отклонении для каждой субпопуляции. Проведенное исследование показало, что воспроизводимость метода для субпопуляции CD3+HLA-G+ составляет 96%, а для субпопуляции CD3-HLA-G+ - 91%.
Ниже представлены примеры реализации предложенного способа.
Представим пример №1 определения антител к аллоНLА-G в семейных парах, имеющих двух детей и неродственных по HLA.
Семейная пара П.А.М. и П.О.И. проходила обследования в ЗАО «Современные медицинские технологии» (амбулаторная карта ЗАО «Современные медицинские технологии» №5-14-631 ж/м). Донором мононуклеаров выступил супруг П.А.М., мужчина, 32 лет. Исследовалась на наличие антител к аллоНLА сыворотка крови женщины (супруги) П.О.И., 25 лет. У данной семейной пары было двое общих детей. По данным клинико-лабораторных исследований оба супруга были здоровы и не имели урогенитальных инфекций. Молекулярно-генетическое типирование локуса HLA-DRB1 выявило, что у мужчины был генотип HLA-DRB1*11,13; а у женщины - HLA-DRB1*01,17. В данной семейной паре общих аллелей не обнаружено.
Кроме того, проведено типирование гена HLA-G на полиморфизм HLA-G 3′UTR 14 bp - делеция / 14 bp - инсерция. Наборы разработаны в лаборатории фармакогеномики (зав. лаб. - к.б.н. М.Л. Филиппенко) НИИХБФМ СО РАН (директор - академик В.В. Власов). Результаты генотипирования представлены на рисунке 1 (женщина П.О.И., дорожка на электрофорезе №3207; супруг П.А.М., дорожка на электрофорезе №3206). Как видно из рисунка, женщина имеет делецию в гомозиготном состоянии в гене HLA-G, а муж имеет гетерозиготное носительство делеции и инсерции. Тем самым их генотипы HLA-G не схожи.
В сыворотке крови женщины проведено исследование антител к аллоНLА-G, экспрессированных на мононуклеарах мужчины. В ходе проведенного исследования получены результаты, на основании которых был рассчитан коэффициент подавления (КПHLA-G), согласно вышеописанной формуле:
КПHLA-G=(((CD3+HLA-G+оп+CD3-HLA-G+оп)-(CD3+HLA-G+конт+CD3-HLA-G+конт))/(CD3+HLA-G+конт+CD3-HLA-G+конт))*100=(((4,07%+3,11%)-(5,26%+4,22%))(5,26%+4,22%))*100=-24,26%.
Тем самым, на основании полученного отрицательного КПHLA-G можно документировать наличие антител к аллоНLА-G супруга.
Пример 2. Семейная пара Н.О.С и Н.Е.В. проходила прегравидарную подготовку в ЗАО «Современные медицинские технологии» на этапе планирования беременности (амбулаторная карта ЗАО «Современные медицинские технологии» №5-14-983/ж). Клиническое обследование показало, что женщина Н.О.С (34 лет) не имеет хронической соматической и генитальной патологии. Обследование на заболевания, передающиеся половым путем, не выявило инфекций. Было проведено молекулярно-генетическое типирование гена HLA-DRB1 коммерческими наборами НПФ «ДНК-технология» (г. Москва). Выявлено, что у женщины обнаружен генотип HLA-DRB1*14,15.
Мужчина Н.Е.В., 35 лет, также не имеет трансплацентарных и урогенильных инфекций, осмотрен терапевтом и урологом. Диагноз - здоров. Молекулярно-генетическое типирование локуса HLA-DRB1 выявило у него следующий генотип HLA-DRB1*04,10.
Проведено типирование гена HLA-G на полиморфизм HLA-G 3′UTR 14 bp - делеция / 14 bp - инсерция. Результаты представлены на рисунке 1 (женщина Н.О.С., дорожка на электрофорезе №3209; супруг Н.Е.В., дорожка на электрофорезе №3208). Как видно из рисунка, женщина имеет делецию в гомозиготном состоянии в гене HLA-G, а муж имеет гетерозиготное носительство делеции и инсерции. Это показывает, что их генотипы HLA-G не схожи.
Тем самым в семейной паре в целом - общих HLA аллелей не обнаружено.
В сыворотке крови женщины проведено исследование антител к аллоНLА-G, экспрессированных на мононуклеарах мужчины. В ходе проведенного исследования получены результаты, на основании которых был рассчитан коэффициент подавления (КПHLA-G), согласно вышеописанной формуле:
КПHLA-G=(((CD3+HLA-G+оп+CD3-HLA-G+оп)-(CD3+HLA-G+конт+CD3-HLA-G+конт))/(CD3+HLA-G+конт+CD3-HLA-G+конт))*100=(((2,11%+3,21%)-(4,33%+5,02%))(4,33%+5,02%))*100=-43,11%.
Тем самым, на основании полученного отрицательного КПHLA-G можно документировать наличие антител к аллоНLА-G супруга.
В качестве примера, где антител к HLA-G не должно быть, представляем исследования сыворотки крови двух близнецов.
Пример №3. Донор X. (№1), 21 год мужчина проходил лабораторное обследование в ЗАО «Современные медицинские технологии» (амбулаторная карта ЗАО «Современные медицинские технологии» №3-14-711). Донор С. (№2), 21 год (брат-близнец донора №1), также проходил лабораторное обследование в ЗАО «Современные медицинские технологии» (амбулаторная карта ЗАО «Современные медицинские технологии» №3-14-712). Обоим донорам было проведено молекулярно-генетическое типирование гена HLA-DRB1 коммерческими наборами НПФ «ДНК-технология» (г. Москва). Выявлено, что у донора №1 и донора №2 общий генотип HLA-DRB1*15,16.
Проведено типирование гена HLA-G на полиморфизм HLA-G 3′UTR 14 bp - делеция / 14 bp - инсерция. Результаты представлены на рисунке 1 (донор X., дорожка на электрофорезе №3210; донор С, дорожка на электрофорезе №3211). Как видно из рисунка, оба донора (брата) имеют и делецию, и инсерцию. Тем самым их генотипы HLA-G схожи.
При проведении исследований антител к аллоНLА-G были получены следующие результаты.
Используя известную формулу, выявили следующие коэффициенты для пары (I) «мононуклеары донора №2 - сыворотка донора №1», и наоборот - (II) «мононуклеары донора №1 - сыворотка донора №2»:
(I) КПHLA-G=(((CD3+HLA-G+оп+CD3-HLA-G+оп)-(CD3+HLA-G+конт+CD3-HLA-G+конт))/(CD3+HLA-G+конт+CD3-HLA-G+конт))*100=(((3,23%+3,71%)-(3,21%+3,59%))(3,21%+3,59%))*100=+2,05%.
(II) КПHLA-G=(((CD3+HLA-G+оп+CD3-HLA-G+оп)-(CD3+HLA-G+конт+CD3-HLA-G+конт))/(CD3+HLA-G+конт+CD3-HLA-G+конт))*100=(((3,45%+3,58%)-(3,44%+3,36%))(3,44%+3,36%))*100=+3,38%.
Тем самым, по всем коэффициентам, рассчитанных для определения антител к аллоHLA-G в сыворотке крови донор №1 на мононуклеары донора №2 и, наоборот, в сыворотке крови донора №2 - к мононуклеарам донора №1 были получены положительные коэффициенты. Это указывает на то, что в сыворотках отсутствуют антитела к аллоHLА-G и они не блокируют соответствующие молекулы. Поэтому субпопуляции контрольных и опытных постановок были сопоставимы, более того в опытных пробах удельный вес субпопуляций, экспрессирующих HLA-G, было больше чем в контроле. Эти данные вполне справедливы, так как выбранные доноры были братья-близнецы, имели общий HLA-генотип и не могли сенсибилизировать друг друга по антигенам тканевой совместимости. Факт общности доноров по HLA был документирован молекулярно-генетическим типированием на коммерческих наборах НПФ «ДНК-технологии» и наборами НИИХБФМ СО РАН.
Метод исследования является скрининговым и достаточно специфичным для лабораторных исследований сенсибилизации к аллогенным HLA-G, что можно использовать при обследовании супругов, для диагностики иммунных причин репродуктивных потерь.
Предлагаемый способ является нетрудоемким, и может быть использован в клинико-диагностических лабораториях. Показана 100% эффективность и 91% воспроизводимость метода.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОЦЕНКИ АЛЛОГЕННОГО ИММУННОГО ОТВЕТА В КРАТКОВРЕМЕННОЙ СМЕШАННОЙ КУЛЬТУРЕ МОНОНУКЛЕАРОВ НЕРОДСТВЕННЫХ ДОНОРОВ | 2014 |
|
RU2581925C2 |
| Способ получения гамма-глобулиновой фракции человека для прегравидарной профилактики врожденных пороков сердца в последующем поколении | 2023 |
|
RU2817352C1 |
| СПОСОБ ПРЕГРАВИДАРНОГО ПРОГНОЗИРОВАНИЯ РИСКА ФОРМИРОВАНИЯ СПОРАДИЧЕСКИХ СЕПТАЛЬНЫХ ВРОЖДЕННЫХ ПОРОКОВ СЕРДЦА БЕЗ ХРОМОСОМНЫХ ЗАБОЛЕВАНИЙ В ПОСЛЕДУЮЩИХ ПОКОЛЕНИЯХ | 2018 |
|
RU2709610C1 |
| СПОСОБ ПРЕГРАВИДАРНОГО ПРОГНОЗИРОВАНИЯ РИСКА ФОРМИРОВАНИЯ СЕПТАЛЬНЫХ ФОРМ ВРОЖДЕННЫХ ПОРОКОВ СЕРДЦА У ПЛОДА | 2016 |
|
RU2617249C1 |
| Способ выявления антиотцовских антител после иммунизации женщин с идиопатическим привычным выкидышем лимфоцитами полового партнера | 2016 |
|
RU2614729C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ РИСКА ПРОГРЕССИРОВАНИЯ ЛАТЕНТНОЙ ТУБЕРКУЛЕЗНОЙ ИНФЕКЦИИ У ДЕТЕЙ | 2009 |
|
RU2405151C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СПЕЦИФИЧЕСКОГО КЛЕТОЧНОГО ИММУННОГО ОТВЕТА К АНТИГЕНАМ ВИРУСА КОРИ И КРАСНУХИ | 2011 |
|
RU2464571C1 |
| Способ оценки риска образования анти-HLA антител при трансфузиях компонентов крови | 2022 |
|
RU2793843C1 |
| Способ определения и количественной оценки специфического клеточного иммунитета к антигенам S-белка вируса SARS-COV-2 | 2021 |
|
RU2762616C1 |
| Способ активации цитотоксических Т-лимфоцитов в популяции мононуклеарных клеток крови при помощи мембранных везикул, полученных из генетически модифицированных опухолевых клеток меланомы М14 со сверхэкспрессией интерлейкина 2 | 2022 |
|
RU2790867C1 |

Изобретение относится к медицине, а именно к иммунологии, и может быть использовано для определения антител к аллогенным HLA-G в сыворотки крови. Для этого используют тест перекрестной совместимости (cross match) мононуклеаров донора с сывороткой реципиента. Проводят анализ субпопуляций мононуклеаров с помощью проточной цитофлуорометрии на связывание моноклональных антител HLA-G и оценивают степень экспрессии HLA-G на опытных и контрольных мононуклеарах донора. При этом значимыми являются субпопуляции CD3-HLA-G+ и CD3+HLA-G+, по которым рассчитывают коэффициент подавления (КП) в опытной постановке по отношению к контрольной по формуле:

где HLA-Gоп - суммарное относительное число субпопуляций экспрессирующих HLA-G: (CD3-HLA-G++CD3+HLA-G+) в опытной постановке, %; HLA-Gконт - суммарное относительное число субпопуляций экспрессирующих HLA-G: (CD3-HLA-G++CD3+HLA-G+) в контрольной постановке, %. При этом наличие сенсибилизации к аллогенным HLA-G диагностируют при отрицательном значении КПHLA-G. Использование данного способа позволяет выявлять аллогенную сенсибилизацию к HLA-G с помощью проточной цитофлуориметрии, определяя субпопуляции CD3-HLA-G+ и CD3+HLA-G+. 3 пр., 3 ил., 2 табл.
Способ определения антител к аллогенным HLA-G, включающий выполнение теста перекрестной совместимости (cross match) мононуклеаров донора с сывороткой реципиента, анализ субпопуляций мононуклеаров с помощью проточной цитофлуорометрии на связывание моноклональных антител HLA-G, отличающийся тем, что дополнительно оценивают степень экспрессии HLA-G на опытных и контрольных мононуклеарах донора, при этом значимыми являются субпопуляции CD3-HLA-G+ и CD3+HLA-G+, по которым рассчитывают коэффициент подавления (КП) в опытной постановке по отношению к контрольной по формуле:

где HLA-Gоп - суммарное относительное число субпопуляций экспрессирующих HLA-G: (CD3-HLA-G++CD3+HLA-G+) в опытной постановке, %;
HLA-Gконт - суммарное относительное число субпопуляций экспрессирующих HLA-G: (CD3-HLA-G++CD3+HLA-G+) в контрольной постановке, %,
при этом наличие сенсибилизации к аллогенным HLA-G диагностируют при отрицательном значении КПHLA-G, рассчитанного из соотношения суммарных популяций CD3-HLA-G+ и CD3+HLA-G+, в опытной и контрольной постановках.
| БЕЛЕНКОВА О.В | |||
| и др | |||
| Показатели аллогенных взаимодействий лимфоцитов супругов как дополнительные диагностические и прогностические критерии иммунных форм репродуктивных потерь // Саратовский научно-медцинский журнал, 2013, т.9, N4, стр.649-652 | |||
| СПОСОБ HLA-ТИПИРОВАНИЯ ЦЕЛЬНОЙ КРОВИ | 2009 |
|
RU2423524C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ БЛОКИРУЮЩЕГО ЭФФЕКТА АУТОЛОГИЧНОЙ ЖЕНСКОЙ СЫВОРОТКИ | 2009 |
|
RU2396566C1 |
| CN 101493462 A, 29.07.2009. | |||
Авторы
Даты
2016-05-27—Публикация
2015-01-19—Подача