Область техники, к которой относится изобретение
Данное изобретение касается катализатора для использования в каталитическом способе получения водорода, особенно в процессе реформинга, пористого катализатора, который может применяться в таком способе, а также способа получения самого такого пористого катализатора.
Уровень техники изобретения
Применение никелевых катализаторов в паровом реформинге известно в технике. US 6416731, например, описывает способ каталитического парового реформинга углеродистого сырья с улучшенной устойчивостью к отравлению серой и спеканию, отличающийся взаимодействием сырья с никелевым катализатором, нанесенным на магний-алюминевую шпинель MgO.xAl2O3, где шпинельный носитель имеет удельную площадь поверхности Asp [м2/г] выше, чем 400*exp(-Tc/400ºC), полученную прокаливанием при температуре Tc [°С].
WO 2008/049266 описывает способ превращения углеводородов в водород и один или несколько оксидов углерода, включающий взаимодействие углеводорода с паром и/или кислородом в присутствии кристаллического катализатора с фазой шпинели, содержащего каталитически активный металл. Также описывается способ изготовления катализатора, пригодного для превращения углеводородов в водород и один или несколько оксидов углерода, включающий добавление осадителя к раствору или суспензии тугоплавкого оксида или его предшественника и соединения, содержащего каталитический металл, с образованием осадка, который прокаливают в кислородсодержащей атмосфере, получая кристаллическую фазу с высокой дисперсностью каталитического металла. Дополнительно описывается кристаллический катализатор, содержащий элементы никель, магний, алюминий и лантаноид, в котором кристаллическая фаза является шпинельной фазой.
Каталитические условия (окислительного) парового реформинга в комбинации с мембраной и/или поглощающим сепаратором могут существенно отклоняться от обычных условий в промышленном получении водорода и/или синтез-газа (без такого сепаратора). При использовании процессов, усиленных за счет разделения, в которых эндотермическая реакция может ускоряться путем отделения продукта эндотермической реакции, общая рабочая температура ниже, чем в обычных условиях в промышленном получении водорода и/или синтез-газа. Это вызывает желание обеспечить альтернативные катализаторы, которые могут термически активироваться при меньших температурах. Часто стабильность катализатора в бедных водородом и богатых углеводородом условиях может благоприятствовать образованию богатых углеродом отложений (например, графита, графена, сажи и подобного), которые могут действовать как каталитический яд. Это также вызывает желание обеспечить альтернативные катализаторы, которые более стабильны в таких условиях.
Обычно катализатор парового реформинга углеводородов для получения водорода и/или синтез-газа в промышленном масштабе основан предпочтительно на никеле (Ni). В некоторых современных приложениях, однако, никель оказывается нестабильным и/или недостаточно реакционно-способным. Альтернативно могут применяться благородные металлы, но они более дороги, что может быть менее желательно.
Сущность изобретения
Следовательно, задачей данного изобретения является обеспечение альтернативного катализатора для получения водорода (включая получение синтез-газа) путем парового реформинга, который, по меньшей мере, частично избавлен от одного или нескольких из вышеуказанных недостатков. Такой катализатор может применяться в сплошном широком температурном режиме, который применяется в различных конфигурациях парового реформинга (например, низкотемпературный реформинг, обычно включающий конвекционный реформинг и реформинг бионефтепродуктов (компонентов), предварительный реформинг, высокотемпературный основной реформинг и т.д.). Данный катализатор особенно подходит для использования в паровом реформинге, усиленном разделением.
Дополнительной задачей данного изобретения является обеспечить альтернативный способ получения водорода (включая образование синтез-газа), особенно усиленный разделением способ. Еще одной задачей данного изобретения является обеспечение катализатора с высокой каталитической активностью и стабильностью, даже в условиях разделения при усилении разделением, который может особенно применяться в способе данного изобретения.
Наконец, данное изобретение обеспечивает катализатор, содержащий Ni, В и Mg, для получения водорода (Н2) и синтез-газа, особенно для каталитического (окислительного) парового реформинга углеводородсодержащего газа (такого как метан, природный газ и т.д.), особенно применяемого в комбинации с сепаратором, который является селективным для заданного продукта реакции, такого как СО2, например, с помощью мембраны, селективной для СО2. В одном варианте осуществления, альтернативно, необязательный сепаратор является селективным для заданного продукта реакции, такого как Н2, например, с помощью мембраны, селективной для Н2.
Данный катализатор представляет собой пористый катализатор, особенно имеющий поры с размером пор в интервале 0,1-50 нм, особенно 0,1-30 нм, например, 0,1-20 нм, еще более особенно 4-30 нм, например, 5-15 нм или 4-8 нм.
Подробное описание
Согласно первому аспекту, данное изобретение обеспечивает пористый катализатор, основанный на, по меньшей мере, оксиде алюминия и одном или нескольких компонентах из оксида магния, кальция, титана, циркония, хрома, марганца и железа, предпочтительно оксида магния, где данный пористый катализатор дополнительно содержит бор и никель, и где данный пористый катализатор содержит поры, имеющие средний размер пор в интервале 0,1-50 нм, особенно 0,1-30 нм, например, 0,1-20 нм, еще более конкретно 4-30 нм, например, 5-15 нм. Катализатор, содержащий поры, далее называется "пористый катализатор" или "катализатор".
Согласно дополнительному аспекту, данное изобретение обеспечивает способ получения водорода (Н2), в котором углеводородсодержащий газ подвергают реакции реформинга в реакционной камере в присутствии катализатора и, необязательно, в присутствии сепаратора, селективного для заданного продукта реакции реформинга, такого как мембрана, селективная для заданного продукта реакции реформинга, с получением водородсодержащего газа, где данный катализатор предпочтительно является пористым и основан на, по меньшей мере, оксиде магния и оксиде алюминия, где данный катализатор дополнительно содержит бор и никель, и где данный катализатор предпочтительно содержит поры, имеющие размер пор в интервале 0,1-50 нм.
В особом варианте осуществления, где применяют сепаратор, данный способ может дополнительно содержать селективное удаление, по меньшей мере, части заданного продукта реакции из реакционной камеры с помощью данного сепаратора. Следовательно, в особом варианте осуществления, данное изобретение обеспечивает способ получения водорода, в котором углеводородсодержащий газ подвергают реакции реформинга в реакционной камере в присутствии катализатора и мембраны (в качестве "сепаратора"), селективной для заданного продукта реакции реформинга, с получением водородсодержащего газа и селективным удалением, по меньшей мере, части заданного продукта реакции из реакционной камеры с помощью данной мембраны, где данный катализатор содержит предпочтительно пористый катализатор, определенный выше и ниже.
Преимуществом данного способа, сопутствующим применению данного катализатора, является то, что температура реакции может быть ниже, например, приблизительно 400-750°С, например, 500-700°С, при том, что катализатор данного изобретения может быть таким же эффективным, как современные катализаторы, которые могут иметь рабочие температуры приблизительно 850-1000°С. Неожиданно оказалось, что данный катализатор и снижает образование углерода (на Ni), и сохраняет желаемый размер (частиц) катализатора предположительно посредством ограничивающих эффектов в порах носителя. Кроме того, присутствие Mg оказывает положительный эффект на производительность и стабильность катализатора, и помогает предотвращать образование нежелательных шпинельных кристаллов.
В отсутствие сепаратора, такого как селективная мембрана, условия данного способа могут включать в себя температуру выше 700°С, например, приблизительно 850-1000°С, особенно приблизительно 900-1000°С. Также в этих условиях катализатор данного изобретения может демонстрировать свои преимущества в отношении стабильности. Следовательно, в данном изобретении также подвергают углеводородсодержащий газ реакции реформинга в реакционной камере в присутствии описанного здесь катализатора при температуре в интервале 700-1000°С, особенно 850-1000°С (в отсутствие сепаратора, такого как селективная мембрана).
Здесь термин "углеводородсодержащий газ" относится к газу, который содержит один или несколько типов углеводородов. Например, углеводородсодержащий газ может содержать природный газ или состоять из него, т.е. содержать метан. Однако углеводородсодержащий газ может также содержать один или несколько высших углеводородов, таких как этан или пропан, или полученные из биомассы (древесные) нефтепродукты. Данный газ может также содержать один или несколько ненасыщенных углеводородов и оксигенатов (полученных из) спиртов, простых эфиров и/или кислот, сложных эфиров, альдегидов, кетонов и т.д. Кроме того, данный газ может содержать одно или несколько (органо-)сернистых соединений. В особенности, углеводородсодержащий газ содержит метан (СН4).
Углеводородсодержащий газ подвергают реакции реформинга. Это означает, что углеводородсодержащий газ смешивают с водяным паром. В другом варианте осуществления, где применяют СО2 реформинг, это может означать, что углеводородсодержащий газ смешивают с СО2-содержащим газом.
В условиях реформинга и в присутствии катализатора, по меньшей мере, часть углеводорода углеводородсодержащего газа превращается в Н2 и другие компоненты, особенно СО и/или СО2. Реакция реформинга является эндотермической реакцией. Поэтому выгодно, когда используют сепаратор, который селективно отделяет один компонент от продуктов реакции реформинга, т.е. разделение усиливает паровой реформинг. Как указано выше, образующимися компонентами могут быть, например, Н2 или СО, или СО2. Необязательно, сепаратор может быть селективным для Н2 и СО, но не для СО2, или для СО и СО2, но не для Н2. В первом случае с помощью сепаратора (особенно мембраны) удаляют синтез-газ, который может быть использован для дальнейшего получения желаемых углеводородов. В последнем случае может быть получен газ, который сравнительно чист от Н2. Как будет ясно специалисту в данной области техники, сепаратор также может быть селективным для Н2. В зависимости от желаемого продукта реакции может быть использован конкретный тип сепаратора. Сепаратор может быть сорбентом, особенно приспособленным поглощать или адсорбировать один или несколько продуктов реакции. В другом варианте осуществления сепаратор может быть мембраной, селективной для одного или нескольких продуктов реакции.
Углеводородсодержащий газ и пар (или СО2-содержащий газ) вводят в реакционную камеру реактора. Эта реакционная камера может быть единственной камерой или множеством камер. Если применяют множество камер, они могут быть расположены параллельно или последовательно.
В одном варианте осуществления реакционная камера также включает в себя сепаратор. Такие конструкции известны в технике и, например, описаны в WO 2004/021495 или WO 2006/034086. Примером подходящей технологии отделения СО2 является, например, усиленная сорбцией и мембраной реакция сдвига водяного газа и усиленная сорбцией и мембраной реакция реформинга.
Углеводородсодержащий газ может подвергаться реакции реформинга при температуре в интервале 400-750°С, особенно 500-700°С. Благодаря присутствию катализатора данного изобретения, а также благодаря присутствию сепаратора, температура может быть в этих, относительно низкотемпературных областях, все еще обеспечивая относительно эффективное превращение углеводорода в Н2.
В отсутствие сепаратора температура может быть, например, в интервале 400-1000°С, например, 700-1000°С, например, 750-950°С. Следовательно, в одном варианте осуществления углеводородсодержащий газ может подвергаться реакции реформинга при температуре в интервале 700-1000°С, особенно 750-950°С, особенно в отсутствие такого сепаратора, как это может быть в случае промышленных способов парового реформинга.
Следовательно, в общем, углеводородсодержащий газ может подвергаться реакции реформинга при температуре в интервале 400-1000°С, где с сепаратором температура может быть в интервале 400-900°С, даже 400-800°С, даже 400-750°С, и где без сепаратора температура может быть в интервале 700-1000°С.
Здесь термин "реформинг" в одном варианте осуществления может также относиться к предварительному реформингу.
Следовательно, в дополнительном аспекте, данное изобретение также обеспечивает применение описанного здесь катализатора, чтобы позволять, по меньшей мере, части углеводородсодержащего газа реагировать по реакции реформинга до водородсодержащего газа, особенно при температуре реакции в интервале 400-1000°С. Таким образом, углеводород в углеводородсодержащем газе может быть превращен в Н2 (и СО и/или СО2). В одном варианте осуществления это может быть реакция реформинга, в другом варианте осуществления это может быть реакция предварительного реформинга. В еще одном варианте осуществления это может быть реформинг, усиленный сорбцией, например, сорбентом или мембраной (селективной для заданного продукта реакции реформинга).
Катализатор данного изобретения предпочтительно содержит пористый несущий материал. Как показано здесь, катализатор может состоять, по существу, из такого катализатора. Здесь термин «пористый» в особенности относится к порам размера 0,1-50 нм, особенно 0,1-30 нм, например, 0,1-20 нм. Способ Barrett-Joyner-Halenda (BJH) использовали с данными адсорбции-десорбции N2 при 77 К, чтобы получать данные о размере пор. В особенности, пористый катализатор содержит поры, имеющие средний размер пор в интервале 1-30 нм, например, 1-20 нм, например, по меньшей мере, 2 нм, более предпочтительно размер пор в интервале 4-30 нм, например, 5-15 нм, особенно 4-13 нм, например, 4-8 нм или 8-13 нм. Кроме того, предпочтительно, по меньшей мере, 20% Ni, более предпочтительно, по меньшей мере, 50% Ni (в виде восстановленного Ni) находится в таких порах. Здесь проценты относятся к полному количеству Ni, содержащегося в пористом катализаторе (т.е. мас.%). В особом варианте осуществления катализатор имеет высокую площадь поверхности (чаще всего от 50 до 300 м2/г, особенно от 100 до 300 м2/г), большую ширину пор (8-13 нм), относительно большой объем пор (0,3-1,4 см3/г).
В одном варианте осуществления пористый катализатор содержит (пористый) магний-алюминиевый смешанный оксидный материал, такой как MgAl2O4, Al2O3, MgO, MgO-Al2O3, Ni-MgO-Al2O3 и т.д. В особенности, пористый катализатор содержит смешанный оксид MgAl2O4 и MgO-Al2O3, но, как указано выше, другой тип материала также может применяться. В остальной части текста смешанный оксид обозначается как Mg(Al)O.
Пористый катализатор может (дополнительно) содержать не только Ni и В, но также может содержать другие материалы (т.е. иные чем магний, алюминий, никель и бор). Вместо или в добавление к магнию пористый катализатор может дополнительно содержать один или несколько элементов из Ti (титан), Са (кальций), Cr (хром), Fe (железо) и Mn (марганец). В частности, катализатор содержит один или несколько элементов из Са и Ti (и Mg). Эти металлы предпочтительно присутствуют в виде своих оксидов или смесей оксидов. В особенности, такие материалы могут дополнительно увеличивать стабильность катализатора и/или улучшать производительность катализатора. Такие элементы могут преимущественно присутствовать в качестве структурного материала (см. также ниже).
Предпочтительно, катализатор содержит по меньшей мере 30 мас.%, вплоть до 95 мас.% комбинации оксида магния (в расчете на MgO) и оксида алюминия (в расчете на Al2O3). Более предпочтительно, полный уровень оксидов магния и алюминия составляет от 50 до 95 мас.%, наиболее предпочтительно 70-90 мас.%. Массовое отношение оксида магния (в расчете на MgO) к оксиду алюминия (в расчете на Al2O3) предпочтительно составляет от 2:98 до 60:40, более предпочтительно от 9:91 до 40:60. Атомное отношение Mg:Al предпочтительно составляет от 5:95 до 63:27, более предпочтительно от 11:89 до 46:54. Если металлы, выбранные из Са, Ti, Zr, Cr, Mn и Fe, присутствуют вместо или в добавление к Mg, атомное отношение (Mg+Ca+Ti+Zr+Cr+Mn+Fe): Al аналогично предпочтительно составляет от 2:98 до 60:40, более предпочтительно от 9:91 до 40:60, а массовое отношение в расчете на оксиды вычисляют соответственно. Доля оксида алюминия от всей массы катализатора предпочтительно составляет 30-75 мас.%, более предпочтительно 45-65 мас.%, а доля оксида магния или других оксидов металлов от всей массы катализатора предпочтительно составляет 8-50 мас.%, более предпочтительно 15-35 мас.%.
В одном варианте осуществления пористый катализатор дополнительно содержит благородный металл (такой как Rh, Pt, Ru, Pd и др.), особенно Rh. Дополнительно или альтернативно, пористый катализатор также содержит один или несколько элементов из La, Cu, Sn, Mo, Ce, Y, K, Re, V, (щелочных металлов) Na, K, Cs и (щелочноземельных металлов) Be, Sr и Ва (т.е. катализатор содержит дополнительное соединение металла), в особенности все (оксиды, соли и др.) металлов имеют температуру восстановления ниже чем 600°С. Следовательно, в одном варианте осуществления Ni-В пористый катализатор может быть активирован (т.е. это, главным образом, неструктурные элементы, см. также ниже) с помощью одного или нескольких элементов из Rh, Pt, Ru, Pd, La, Cu и Sn и др. Эти элементы могут быть введены в пористый катализатор таким же образом, как Ni (см. ниже). Термин (благородный) металл не означает, что данный элемент присутствует в форме металла. Он также может присутствовать, например, в виде оксида. Однако в восстановительных условиях данное соединение металла может восстанавливаться до металла. Преимуществом от присутствия одного или нескольких таких металлов, как Rh, Pt, Ru, Pd, La, Cu, Sn и Fe может быть снижение энергии, необходимой для восстановления (преобладающих никелевых компонентов в свежесинтезированном или окисленном катализаторе) до Ni, хотя также имеются преимущества относительно небольшого размера частиц Ni благодаря присутствию В. В особом варианте осуществления данный катализатор представляет собой пористый катализатор, основанный на, по меньшей мере, оксиде магния и оксиде алюминия, где данный пористый катализатор дополнительно содержит бор и никель, и дополнительно один или несколько элементов из Rh, Pt, Ru, Pd, La, Cu и Sn. Количество этого дополнительного элемента предпочтительно составляет 0,01-5 мас.% в расчете на массу всего (сухого) катализатора, предпочтительно 0,05-3 мас.%, наиболее предпочтительно 0,1-2 мас.%, тогда как количество одного или нескольких благородных металлов (Rh, Pt, Ru, Pd) предпочтительно составляет 0,01-4 мас.%, более предпочтительно 0,05-1 мас.%.
В другом особом варианте осуществления пористый катализатор не содержит иных активаторов, чем Ni (и В).
Фраза "основанный на, по меньшей мере, оксиде магния и оксиде алюминия" означает, что эти материалы являются основой структуры пористого катализатора. В особенности, пористый катализатор представляет собой магний-алюминиевый оксидный материал, как указано выше, т.е. смешанный оксид. Ti, Ca, Cr, Fe, Zr и Mn также могут быть использованы в качестве структурного материала, но также могут быть неструктурным материалом, и могут присутствовать в порах. В особенности, Ni не является структурным материалом и, по существу, присутствует в порах. В может быть структурным материалом или может быть в порах (в виде неструктурного материала). Фраза "где пористый катализатор дополнительно содержит бор и никель" означает, что эти материалы могут присутствовать в виде соединения, такого как оксид бора или борная кислота, и, например, оксид никеля. Пористый катализатор на основе оксида магния и оксида алюминия может быть пропитан никелевыми и/или борными материалами, например, солью никеля и/или борной кислотой. Они могут присутствовать (по меньшей мере) в порах пористого катализатора.
В одном варианте осуществления бор может обеспечиваться в катализаторе с помощью физического смешения, например, путем применения порошка бора или любого из других соединений бора, упомянутых здесь.
Массу никеля относительно всей массы пористого катализатора предпочтительно выбирают в интервале 4-70 мас.%, предпочтительно 10-45 мас.%, наиболее предпочтительно 15-25 мас.%. Полная масса пористого катализатора, таким образом, относится к пористому катализатору, включая бор, никель и, необязательно, другие (чем Ni) активаторы. Здесь масса никеля относится к элементарному никелю, а не к оксиду никеля (хотя, как здесь указано, обычно не в условиях реакции никель будет присутствовать в виде оксида никеля, а в условиях реакции в виде металлического никеля).
Кроме того, массу бора (В) относительно полной массы пористого катализатора предпочтительно выбирают в интервале 0,1-20мас.%. предпочтительно 0,5-5мас.%. Полная масса пористого катализатора, таким образом, относится к пористому катализатору, включая бор, никель и, необязательно, другие (чем Ni) активаторы. Здесь масса бора относится к элементарному бору, а не к борной кислоте.
Оказывается, что такой катализатор обеспечивает желаемые каталитические свойства. При бóльших порах, никель все еще имеет достаточное пространство в порах и спекается слишком много, и образование сажи может быть слишком большим. При меньших порах, в таких порах образуются очень маленькие частицы никеля с очень высокой активностью, но большая доля никеля будет находиться на внешней поверхности носителя, делая его склонным к спеканию. При меньшем содержании Ni активность может быть слишком низкой, а при более высоком содержании Ni образование сажи опять может быть слишком высоким. Особенно хорошие результаты могут быть получены с порами, имеющими размер в интервале 4-30 нм, например, 4-15 нм, например, 5-15 нм.
Как указано выше, никель может присутствовать в виде оксида никеля. Однако в реакционных условиях никель предпочтительно присутствует в виде металлического никеля. Внутри пор могут формироваться частицы металлического никеля, имеющие размеры, которые определяются размером пор. Поэтому, в особом варианте осуществления, до того, как углеводородсодержащий газ подвергают реакции реформинга в реакционной камере, катализатор подвергают восстановительным условиям. И также по этой причине размер пор предпочтительно находится в интервале 4-30 нм, например, 4-15 нм, например, 5-15 нм, например, 4-8 нм или 8-13 нм, так как потом могут быть получены относительно хорошие результаты с точки зрения стабильности, образования сажи и выхода. Также количество никеля относительно полной массы пористого катализатора предпочтительно выбирают в интервале 15-25 мас.%, предпочтительно равное или ниже чем 22,5 мас.% относительно полной массы пористого катализатора.
Когда пористый катализатор подвергают восстановительным условиям, полученные таким образом частицы Ni имеют размер частиц в интервале 0,1-50 нм, например, 1-30 нм, например, 4-30 нм, соответственно. Размер пор может диктовать размеры данных частиц. Здесь термин "размеры" относится к длине, ширине и высоте, но в случае, по существу, сферических частиц он может также относиться к диаметру. Катализатор, который был подвергнут восстановительным условиям, может быть достаточно стабильным для хранения и транспортировки. Стабильность может быть улучшена с помощью этапа пассивации, чтобы снизить пирофорную природу реакционно-способных металлов, таких как никель. Это может быть вызвано, например, путем обеспечения тонкого оксидного или карбонатного слоя на металле.
Следовательно, данное изобретение также обеспечивает пористый катализатор, основанный, по меньшей мере, на оксиде магния и оксиде алюминия, где данный пористый катализатор дополнительно содержит бор и никель, и где данный пористый катализатор подвергают восстановительным условиям, причем полученные таким образом частицы Ni имеют размер частиц в интервале 0,1-50 нм, например, 0,1-30 нм, например, 1-30 нм, например, 4-30 нм соответственно, и где данный пористый катализатор предпочтительно содержит поры, имеющие размер пор в интервале 0,1-50 нм, например, 0,1-30 нм, например, 1-30 нм, например, 4-30 нм соответственно.
Пористый катализатор содержит поры, имеющие размер пор в интервале 0,1-50 нм, особенно 0,1-30 нм, например, 0,1-20 нм, например, 1-30 нм, возможно 1-20 нм, возможно 4-15 нм, например, 5-15 нм, возможно 8-13 нм. В особенности, пористый катализатор содержит магний-алюминиевый оксидный материал (обозначаемый Mg(Al)O), такой как смешанный оксид MgO-Al2O3 и MgAl2O4. Пористый катализатор может дополнительно содержать один или несколько элементов из Ti, Ca, Cr, Fe, Zr, Mn, например, один или несколько элементов из Са и Ti, как описано выше (и ниже).
В еще одном аспекте данное изобретение также обеспечивает способ получения пористого катализатора, где данный способ содержит: обеспечение соединения магния или других соединений элементов из группы Mg, Ca, Ti, Zr, Cr, Mn, Fe, соединения алюминия, соединения никеля, соединения бора и порообразователя (структуро-направляющий агент), формирование в процессе формирования пористого материала путем объединения, по меньшей мере, соединения Mg, Ca, Ti, Zr, Cr, Mn, Fe, соединения алюминия и порообразователя, и воздействие на эти соединения условий кристаллизации, чтобы обеспечить пористый материал, и прокаливание образованного таким образом пористого материала, где (1) соединение бора присутствует во время процесса формирования и/или где соединение бора наносят на пористый материал, полученный с помощью процесса формирования, и где (2) соединение никеля присутствует во время процесса формирования и/или где соединение никеля наносят на пористый материал, полученный с помощью процесса формирования. Таким образом формируют пористый катализатор.
Также могут вводиться другие элементы. Например, системы Ni-В, описанные здесь, могут объединяться с промоторами, известными для промышленных катализаторов парового реформинга.
Ni может промотироваться одним или несколькими промоторами, или промоторы могут иметь другое преимущественное действие, такое как стабилизация катализатора и/или стабилизация размера частиц. Примерами этого могут быть один или несколько элементов, выбранных из (1) одного или нескольких щелочных элементов, (2) одного или нескольких элементов благородных металлов, (3) одного или нескольких элементов 3-11 групп периодической таблицы элементов, (4) одного или нескольких лантаноидных элементов и (5) одного или нескольких актиноидных элементов. Например, в качестве дополнительного элемента (например, в качестве промотора), в добавление к В и Ni, один или несколько элементов могут быть выбраны из группы, состоящей из Li, Na, K, Rb, Cs, Be, Mg, Ca, Sr, Ba, Sc, Y, La, Ce, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Ti, Zr, Hf, V, Nb, Ta, Cr, Mo, W, Mn, Re, Fe, Ru, Os, Co, Rh, Pd, Pt, Cu, Ge и Sn. Опять-таки, термин "элемент" не обязательно означает, что эти элементы присутствуют в своей элементарной форме, но эти элементы также могут присутствовать в форме оксида или соли (и могут быть введены, например, пропиткой в поры).
Щелочной элемент (как неструктурный элемент), такой как Na, К, Rb и Cs, например, присутствующий в форме оксида или соли (или их комбинации), может, например, увеличивать адсорбцию пара, помогать предшественникам газификации углерода, предотвращать отложение углерода.
Щелочноземельный элемент (как неструктурный элемент), такой как Ве, Mg, Ca, Sr и Ва, а также такой элемент, как Ge или Sn, например, присутствующий в форме оксида или соли (или их комбинации), может, например, уменьшать подвижность атомов и тем самым снижать спекание.
Элемент группы скандия или лантаноид (как неструктурный элемент), такой как Sc, La, Ce, Pr, Nd, Pm, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb и Lu, например, присутствующий в форме оксида или соли (или их комбинации), может, например, увеличивать адсорбцию пара, помогать предшественникам газификации углерода, предотвращать отложение углерода.
В особенности, используют те элементы, которые, когда присутствуют в форме соли, имеют температуру восстановления ниже чем 600°С, например, чтобы помогать восстановлению никелевого компонента до металлического Ni.
Например, один или несколько элементов из Rh, Pt, Ru, Pd, La, Cu, Sn и Fe и др. могут присутствовать как соединение Rh, Pt, Ru, Pd, La, Cu, Sn и Fe (и др.) во время процесса формирования и/или могут наноситься на пористый материал, полученный в процессе формирования. Обычно соединения Ni, а также возможное соединение Rh, Pt, Ru, Pd, La, Cu, Sn и Fe (и др.) могут наноситься (вместе или последовательно) на пористый материал, полученный в процессе формирования, например, пропиткой. Эти элементы могут вводиться, например, в форме оксидов и т.д. В восстановительных условиях могут формироваться металлические частицы.
Полное количество благородных металлов может, например, составлять 0,01-4 мас.%, особенно 0,05-1 мас.% относительно полной массы пористого катализатора. Неблагородные металлы могут присутствовать в количестве, например, 0,01-20 мас.%, более предпочтительно 0,1-10мас.%.
Таким образом, например, пористый катализатор на основе, по меньшей мере, оксида Mg, Ca, Ti, Zr, Cr, Mn и/или Fe и оксида алюминия содержит В и Ni (где Ni может присутствовать в виде металла после восстановления) и, например, один или несколько других промоторов, описанных выше, таких как Rh или Pt, или Cu, или Sn, или Fe, или комбинация одного или нескольких таких элементов. Такие другие элементы могут промотировать каталитическую реакцию на основе Ni.
Процесс формирования может, в особенности, представлять собой мокрую химическую технологию, в частности, золь-гель способ. Гидролиз алкоксида алюминия предпочтительно спиртом, подобным этанолу, происходит в присутствии органического структуро-направляющего агента, который способен формировать мезо-размерные мицеллы, которые соединяются с помощью гидролизующегося алкоксида алюминия. Надлежащее время процесса золь-гель синтеза составляет от 1,5 до 12 дней, и температура синтеза от комнатной температуры и выше в зависимости от типа сополимера.
В одном варианте осуществления процесса формирования соединение алюминия содержит алюминийорганическое соединение, такое как изопропоксид, втор-бутоксид, ацетилацетонат алюминия и т.п. Соединение магния может быть растворимой солью магния, такой как нитрат магния (Mg(NO3)2.6H2O) или ацетат и т.п. Другие металлы могут использоваться в процессе формирования в виде своих растворимых или диспергируемых солей, таких как нитраты, ацетаты и др., например, алкоксиды, нитрат или хлорид титана, хлорид или нитрат кальция, алкоксид, нитрат или галогениды циркония, нитраты хрома, марганца или железа, или подобные. Примерами подходящих соединений никеля являются растворимые соли никеля, например, нитрат никеля, ацетат никеля и др. В одном варианте осуществления соединение никеля содержит нитрат никеля, такой как Ni(NO3)2.6Н2О.
Соединение бора предпочтительно содержит одно или несколько соединений, выбранных из группы, состоящей из (1) борной кислоты, (2) боратных солей, таких как бура (декагидрат тетрабората натрия) или другие гидраты, и водорастворимое борсодержащее соединение, такое как минералы бура (Na2B4O5(ОН)4·8(Н2О)), колеманит (СаВ3О4(ОН)3·(Н2О)), улексит (NaCaB5O6(ОН)6·5(Н2О)) и кернит (Na2B4O6(ОН)3·3(Н2О)), (3) галогенида бора, такого как трифторид бора (BF3), трихлорид бора (BCl3) и боргалогенид щелочного металла, такой как борфторид натрия (NaBF4), (4) раствора комплекса диметилсульфид трибромид бора в метиленхлориде (СН3)2S·BBr3, (5) борогидрида щелочного металла, такого как, например, раствор КВН4, (5) оксида бора, (6) алкилбората, (7) цианборгидрида натрия NaBH3(CN) и (8) порошка бора.
Как указано выше, никель предпочтительно присутствует в порах. Это может достигаться, например, путем нанесения (водного) раствора или возможно водной суспензии соли никеля на пористый материал. Это также может достигаться получением пористого материала в присутствии соединения никеля. После получения катализатора, включая прокаливание и восстановление, никель может, в особенности, присутствовать в виде металлического никеля. Следовательно, соединение никеля может присутствовать во время процесса формирования (пористого материала) и/или соединение никеля может наноситься на пористый материал, полученный в процессе формирования. Никель также может альтернативно или дополнительно присутствовать на поверхности пористого материала.
Как указано выше, бор может присутствовать в порах. Это может достигаться, например, путем нанесения соединения бора, (водной) жидкой композиции с соединением бора или, возможно, водной суспензии с соединением бора на пористый материал. Это также может достигаться путем получения пористого материала в присутствии соединения бора. После получения катализатора, включая прокаливание и восстановление, бор может, в особенности, присутствовать в виде борида никеля, хотя небольшие количества элементарного бора и оксида бора также могут присутствовать. Следовательно, бор может присутствовать в порах, но альтернативно или дополнительно также может присутствовать на поверхности пористого материала. Бор, в одном варианте осуществления, также может обеспечиваться в катализаторе путем физического смешения соединения бора, например, путем использования порошка бора или любых других соединений бора, упомянутых здесь, с пористым материалом.
В еще одном варианте осуществления данное соединение бора содержит борную кислоту. В еще одном варианте осуществления, где порообразователь содержит триблоксополимер, имеющий молекулярную массу в интервале 3000-18000 Да, такой как Pluronic® 123 (НО(СН2СН2О)20(СН2СН(СН3)О)70(СН2СН2О)20Н, что соответствует молекулярной массе приблизительно 5800 Да) или Pluronic® F127 (молекулярная масс приблизительно 12600 Да). Другими вариантами являются Pluronic® F87, F68 и F108. Прокаливание, предпочтительно выше 500°С, является особенно преимущественным для удаления остаточного органического материала из пор. В еще одном варианте осуществления мезопоры формируются в присутствии сахаров, сахаридов, например, глюкозы, сахарозы, крахмала, малкодекстринов и циклодекстринов, или других олигосахаридов (MW 300-3000) или полисахаридов (MW выше 3000) в качестве порообразователей.
Другие элементы, такие как один или несколько из Rh, Pt, Ru, Pd, La, Cu, Sn и Fe, а также другие вышеупомянутые элементы, могут вводиться таким же образом, как Ni. Неструктурный материал может присутствовать в порах и может вводиться, например, пропиткой.
Если по причинам особого применения размер пор несущего материала (на основе Mg, Al) не является очень критичным, преимущества синергизма между Ni, В и Mg также могут быть получены другими методами синтеза, в которых Ni, В нанесенные катализаторы получают нанесением Ni и В на MgAl2O4, и синтезируют носитель на основе MgAl2O4 другими способами, чем золь-гель способ, известными специалисту в данной области техники, например, прокаливанием механической смеси оксидов и/или солей Mg и Al, методом осаждения, аэрозольным методом, цитрат-нитратным методом, пиролизом комплексных соединений алюминия и магния с триэтаноламином, технологией PVA испарения, синтезом со сгоранием, с использованием мочевины и сахарозы в качестве топлива и др.
Термин "по существу", применяемый здесь, будет понятен специалисту в данной области техники. Термин "по существу", может также включать в себя варианты осуществления с "совершенно", "полностью", "все" и т.п. Поэтому в вариантах осуществления выражение "по существу" также может отсутствовать. Где применимо, термин "по существу" может также означать 90% или выше, например, 95% или выше, особенно 99% или выше, особенно 99,5% или выше, включая 100%. Термин "содержит" включает в себя также варианты осуществления, где термин "содержит" означает "состоит из".
Следует заметить, что вышеупомянутые варианты осуществления скорее иллюстрируют, а не ограничивают данное изобретение, и что специалисты в данной области техники будут способны разработать многие альтернативные варианты осуществления без отклонения от объема приложенной формулы изобретения. В пунктах формулы изобретения любые символы, помещенные между скобками, не следует понимать, как ограничение данного пункта. Применение глагола "содержать" и его спряжений не исключает присутствия других элементов или этапов, чем указанные в данном пункте. Единственное число, относящееся к элементу, не исключает присутствия множества таких элементов. Тот факт, что определенные меры указываются в разных взаимозависимых пунктах, не означает, что комбинация этих мер не может преимущественно использоваться.
Фигуры
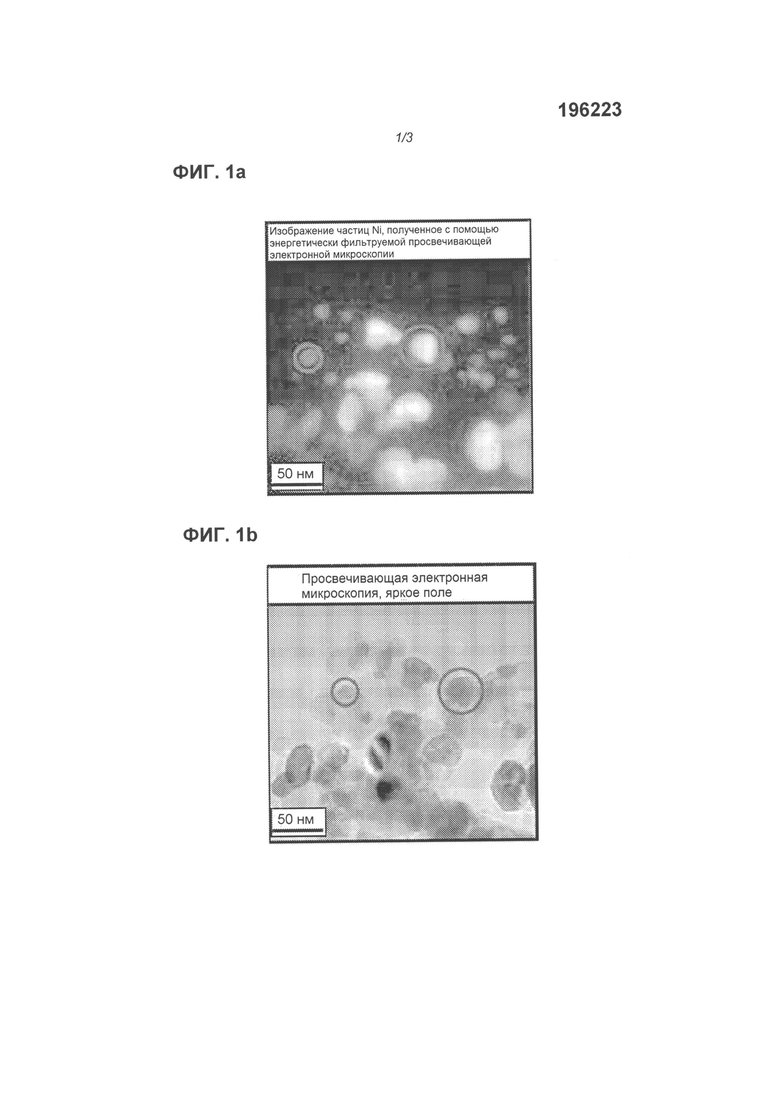
Фиг.1а/1b показывают ТЭМ изображения 40,1 мас.%. Ni со средним размером частиц 20 нм (мерная черта 50 нм);
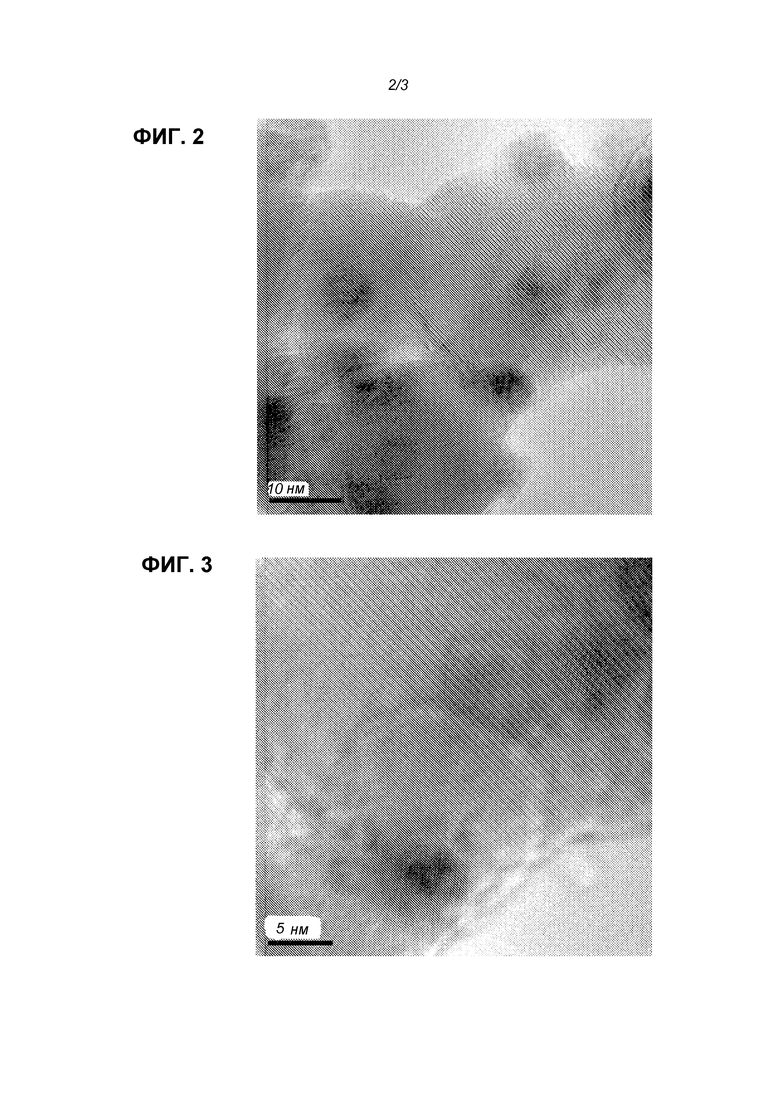
Фиг.2 показывает ТЭМ изображение 40,1 мас.%. Ni - 2,8 мас.%. В со средним размером частиц 7 нм (мерная черта 10 нм);
Фиг.3 показывает ТЭМ изображение 18 мас.% Ni - 1,2 мас.%. В со средним размером частиц 5 нм (мерная черта 5 нм); и
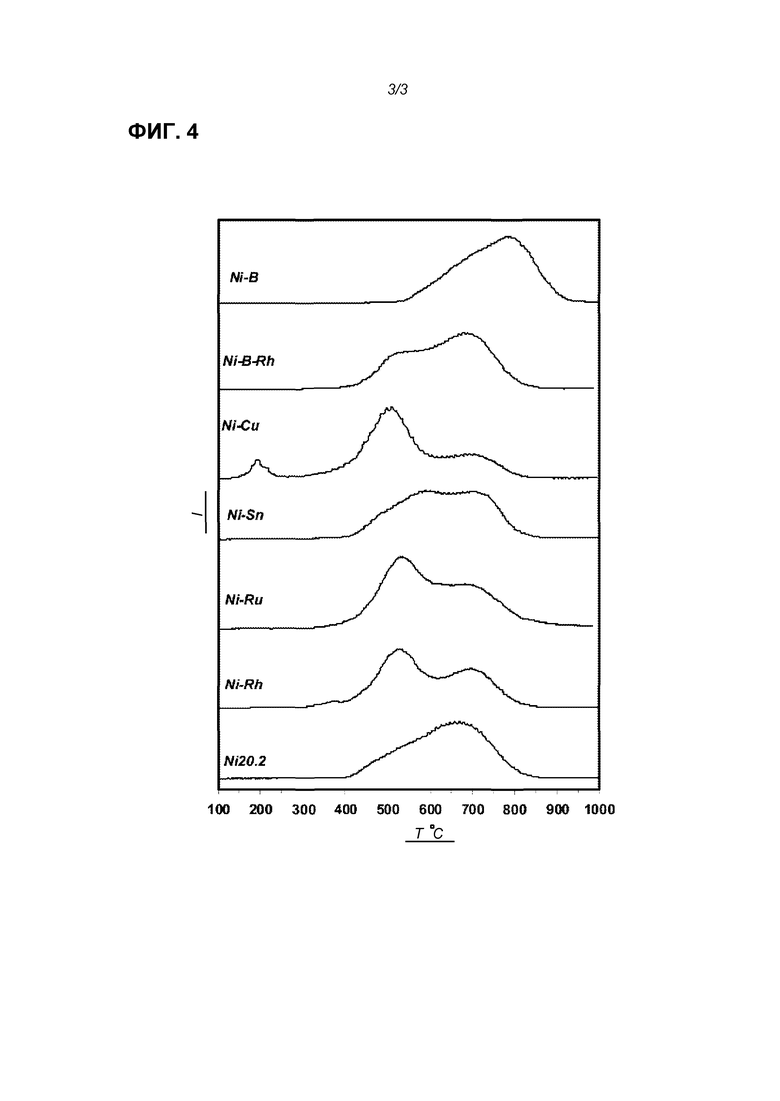
Фиг.4 показывает некоторые ТПВ результаты никелевых катализаторов (интенсивность (отн. ед.) от температуры (°С)).
ПРИМЕРЫ
ПРИМЕР 1: Размер частиц никеля
Пропитывали никелем носитель MgAl2O4 (30 нм частицы, 60 м2/г), используя исходный раствор, приготовленный растворением Ni(NO3)2.6Н2О в 100 мл дистиллированной воды (100 г/100 мл). Для пропитки данный раствор добавляли к носителю по каплям, чтобы достичь 19,8 мас.% и 40 мас.% Ni в случае двух независимых пропиток. После пропитки образец снова прокаливали в режиме 0,5°С/мин-600°С-4 ч.
Альтернативно, меньшие частицы никеля готовили с помощью гомогенного осаждения (HDP). Для HDP сначала 1 или 2 г MgAl2O4 перемешивали в большом количестве воды (150 мл). Затем добавляли соль никеля в количестве, необходимом, чтобы получить 5, 15 и 20 мас.% никеля (рН ≈ 7-9). рН доводили до 2 1М раствором HNO3. Данную суспензию перемешивали и нагревали при 90°С. Водный раствор мочевины (20 мл) добавляли, чтобы начать осаждение. рН контролировали во время осаждения, и обычно после 16-24 ч осаждение заканчивали, затем смесь охлаждали и фильтровали. Высушенный в сушильном шкафу образец прокаливали в режиме 0,5°С/мин-600°С-4 ч.
ПРОВЕРКА СТАБИЛЬНОСТИ:
Проверка стабильности катализаторов в 2 условиях при 600°С, 1 атм.: условия с Н/С=10 (RC1: 7,5% СН4, 22,5% Н2О) периодически заменяли на Н/С=2,9 (RC3: 1,3% СН4, 0,14% СО, 11,6% СО2, 16% Н2О); последний набор условий отражает условия с мембраной (низкое Н/С). Катализаторы разбавляли инертным оксидом алюминия, чтобы измерять истинную каталитическую активность, т.е. далеко от равновесного превращения.
Размер частиц Ni относительно активности превращения метана и дезактивации выражали с помощью -Kd (ч-1), последнее отражает наклон снижения в направлении меньшей конверсии. Х исходная представляет собой активность превращения метана в процентах превращенного метана после 10 мин в потоке. См. таблицу 1 ниже.
Активны два пути дезактивации: углеродная дезактивация, больше углерода при большем размере частиц, и спекание придают важность частицам меньшего размера, как видно из анализа ТПВ и EXAFS. Поэтому существует оптимальный размер частиц, чтобы предотвращать интенсивную дезактивацию: большие частицы производят углерод, меньшие частицы дают спекание/реструктуризацию. С помощью исследований XAS и ТПВ/ТПО сделали вывод, что окисление восстановленных Ni металлических активных центров при реакции не происходит. Из этого исследования 10-13 нм (в среднем) частицы, полученные пропиткой нитратом никеля в количестве, соответствующем 19-20 мас.% Ni, оказываются особенно хорошим выбором для высокой конверсии и улучшенной стабильности. Стабильность однако может быть еще улучшена путем закрепления частиц Ni в пористой структуре Mg(Al)O, чтобы уменьшить их чувствительность к миграции и спеканию. Чтобы дополнительно подавить активность образования углерода Ni-Mg(Al)O катализатора, изучали действие промоторов, см. пример 2.
ПРИМЕР 2: Синтез MgAl2O4 носителя с никелем и вторыми металлами (пропитка Sn, Pt, Cu, Pd, La, Ce, Pr, Gd, бором)
Пропитывали никелем носитель MgAl2O4, используя исходный раствор, приготовленный растворением Ni(NO3)2.6Н2О в 100 мл дистиллированной воды (100 г/100 мл). Для пропитки данный раствор добавляли к носителю по каплям, чтобы достичь 20 мас.% или 40 мас.% Ni. После пропитки образец снова прокаливали в режиме 0,5°С/мин-600°С-4 ч.
Вторым металлическим компонентом пропитывали никельсодержащий MgAl2O4, используя раствор соли металла. После пропитки образец снова прокаливали в режиме 0,5°С/мин-600°С-4 ч.
ПРОВЕРКА СТАБИЛЬНОСТИ:
Проверка стабильности катализаторов в 2 условиях при 600°С, 1 атм.: условия с Н/С=10 обозначали "сравнительные условия RC", используя 7,5% СН4, 22,5% Н2О, остальное N2, и периодически заменяли на Н/С=2,9 (1,3% СН4, 0,14% СО, 11,6% СО2, 16% Н2О, остальное N2); последний набор условий отражает смоделированные условия с мембраной (низкое Н/С). RC1 и RC3 обозначают соответственно первый и третий период, когда катализатор взаимодействует со сравнительными условиями (RC3: во время RC3 катализатор взаимодействовал с двумя предыдущими периодами сравнительных условий и 2 периодами смоделированных условий с мембраной).
Катализаторы разбавляли инертным оксидом алюминия (1:27), чтобы измерять истинную каталитическую активность, т.е. далеко от равновесного превращения. Объемная скорость (SV) = 1290000 ч-1. См. таблицу 2:
Только лантан и бор стабилизируют Ni катализатор от дезактивации после повторного взаимодействия с моделированными условиями с мембраной и продолжительного времени эксплуатации. При использовании бора для носителя MgAl2O4 более высокие количества никеля являются предпочтительными для катализатора. Система с 40 мас.% Ni страдает только из-за дезактивации углеродом, и действие бора, главным образом, блокирует отложение углерода на катализаторе и, следовательно, углеродный путь дезактивации (заметим, что вклад спекания в системе с 40 мас.% Ni является незначительным вследствие большего размера частиц).
Однако в дезактивации катализатора с меньшим содержанием Ni преобладает спекание частиц Ni, и действие бора заметно только при продолжительных временах в потоке, когда размер частиц Ni увеличивается во время RC1 (высокий -Kd) и преобладающая дезактивация переходит от спекания к углеродной дезактивации, которая, в свою очередь, эффективно блокируется В, см. низкий -Kd во время RC3. Как известно из литературы, лантан демонстрирует очень хорошее поведение при газификации углерода и, следовательно, высокую стабильность, но проблемой является конверсия: начальная конверсия существенно падает после внесения La в Ni-катализатор.
ПРИМЕР 3: Синтез никельсодержащего пористого Mg(Al)О катализатора
Раствор 1) готовили при комнатной температуре: Pluronic 123 растворяли в 10-20 мл этанола при интенсивном перемешивании.
Раствор 2) готовили при комнатной температуре: Компоненты нитрат магния (1 грамм), изопропоксид алюминия (3,2 грамма) и нитрат никеля (2 грамма) объединяли в стакане в вытяжном шкафу и сначала добавляли этанол (10 мл), затем азотную кислоту (2,6 мл) (65%). Соли растворяли при интенсивном перемешивании.
Раствор 2 добавляли к раствору 1, закрывали ПЭ-пленкой и перемешивали в течение 5 ч при комнатной температуре. После 5 ч раствор помещали в масляную баню и нагревали до 60°С. Инициировали кристаллизацию при испарении в течение 48 ч в небольшом потоке воздуха. После 48 ч образец прокаливали в трубчатой печи в режиме 1°С/мин до 650°С-700°С в потоке воздуха 50 мл/мин и выдерживали там в течение 4 ч. Результаты даны в таблице 3.
ПРИМЕР 4: Синтез никельсодержащего пористого Mg(Al)О катализатора, впоследствии пропитанного бором
Никельсодержащий пористый MgO-Al2O3 смешанный оксидный катализатор, приготовленный в пример 3, пропитывали бором. Пропитывали бором никельсодержащий пористый алюминат магния, используя 2-3 мл борной кислоты (приблизительно 0,6М). После пропитки образец снова прокаливали в режиме 0,5°С/мин-600°С-4 ч. Результаты даны в таблице 3.
ПРИМЕР 5: Синтез пористого Mg(Al)O носителя, пропитанного никелем
Раствор 1) готовили при комнатной температуре: Pluronic 123 растворяли в 10-20 мл этанола при интенсивном перемешивании.
Раствор 2) готовили при комнатной температуре: Компоненты нитрат магния (1 грамм) и изопропоксид алюминия (3,2 грамма) объединяли в стакане в вытяжном шкафу и сначала добавляли этанол (10 мл), затем азотную кислоту (2,6 мл) (65%). Соли растворяли при интенсивном перемешивании.
Раствор 2 добавляли к раствору 1, закрывали ПЭ-пленкой и перемешивали в течение 5 ч при комнатной температуре. После 5 ч раствор помещали в масляную баню и нагревали до 60°С. Инициировали кристаллизацию при испарении в течение 48 ч в небольшом потоке воздуха. После 48 ч образец прокаливали в трубчатой печи в режиме 1°С/мин до 650°С-700°С в потоке воздуха 50 мл/мин и выдерживали там в течение 4 ч.
Типичная петля гистерезиса на изотермах адсорбции азота дает информацию о пористости материалов. Формирование упорядоченных гексагональных пористых структур с p6mm симметрией также можно было наблюдать из спектров рентгеновской дифракции.
Прокаленный носитель пропитывали никелем, используя исходный раствор, приготовленный растворением Ni(NO3)2.6Н2О в 100 мл дистиллированной воды (100 г/100 мл). Для пропитки данный раствор добавляли к носителю по каплям, чтобы достичь 19 мас.% Ni. После пропитки образец снова прокаливали в режиме 0,5°С/мин-600°С-4 ч. Результаты даны в таблице 3.
ПРИМЕР 6: Синтез пористого носителя MgO-Al2O3, пропитанного никелем и затем пропитанного бором
Пропитанный никелем, пористый MgO-Al2O3 катализатор, приготовленный в примере 5, пропитывали бором. Пропитывали бором никельсодержащий пористый алюминат магния, используя 2-3 мл борной кислоты (приблизительно 0,6М). После пропитки образец снова прокаливали в режиме 0,5°С/мин-600°С-4 ч. Результаты даны в таблице 3.
ПРИМЕР 7: Синтез никель- и борсодержащего пористого MgO-Al2O3 катализатора
Раствор 1) готовили при комнатной температуре: Pluronic 123 растворяли в 10-20 мл этанола при интенсивном перемешивании.
Раствор 2) готовили при комнатной температуре: Компоненты нитрат магния (1 г), изопропоксид алюминия (3,2 г), нитрат никеля (2 г) и 2-3 мл борной кислоты (приблизительно 0,6М) объединяли в стакане в вытяжном шкафу и сначала добавляли этанол (10 мл), затем азотную кислоту (2,6 мл) (65%). Соли растворяли при интенсивном перемешивании.
Раствор 2 добавляли к раствору 1, закрывали ПЭ-пленкой и перемешивали в течение 5 ч при комнатной температуре. После 5 ч раствор помещали в масляную баню и нагревали до 60°С. Инициировали кристаллизацию при испарении в течение 48 ч в небольшом потоке воздуха. После 48 ч образец прокаливали в трубчатой печи в режиме 1°С/мин до 650°С-700°С в потоке воздуха 50 мл/мин и выдерживали там в течение 4 ч. Результаты даны в таблице 3.
ПРИМЕР 8: Синтез никелевого катализатора, нанесенного на Al2O3
Оксид алюминия Al-4172Р (гамма оксид алюминия ~328 м2/г, BASF/Engelhard) использовали в качестве носителя. Прокаленный носитель пропитывали никелем, используя исходный раствор, приготовленный растворением Ni(NO3)2.6Н2О в 100 мл дистиллированной воды (100 г/100 мл). Для пропитки данный раствор добавляли к носителю по каплям, чтобы достичь содержания 19 мас.% Ni. После пропитки образец снова прокаливали в режиме 0,5°С/мин-600°С-4 ч (пример 8а).
Часть пропитанного никелем Al2O3 катализатора пропитывали бором (пример 8b). Никельсодержащий Al2O3 пропитывали бором, используя 2,19 мл раствора Н3ВО3 (1,885 г Н3ВО3 в 50 мл) для 0,496 г пропитанного никелем Al2O3. После пропитки образец снова прокаливали в режиме 0,5°С/мин-600°С-4 ч. Результаты даны в таблице 3.
ПРИМЕР 9: Синтез никелевого катализатора, нанесенного на MgO
Оксид магния (MgO, 99%, Sigma Aldrich, SA 100 м2/г) использовали в качестве носителя. Прокаленный носитель пропитывали никелем, используя исходный раствор, приготовленный растворением Ni(NO3)2.6Н2О в 100 мл дистиллированной воды (100 г/100 мл). Для пропитки данный раствор добавляли к носителю по каплям, чтобы достичь 19 мас.% Ni. После пропитки образец снова прокаливали в режиме 0,5°С/мин-600°С-4 ч (пример 8а). Результаты даны в таблице 3.
ПРИМЕР 10: Тесты стабильности для пористых Mg(Al)O катализаторов
Проверка стабильности катализаторов в 2 условиях при 600°С, 1 атм.: условия с Н/С=10 обозначали "сравнительные условия RC", используя 7,5% СН4, 22,5% Н2О, остальное N2, и периодически заменяли на Н/С=2,9 (1,3% СН4, 0,14% СО, 11,6% СО2, 16% Н2О, остальное N2); последний набор условий отражает смоделированные условия с мембраной (низкое Н/С). RC1 и RC3 обозначают соответственно первый и третий период, когда катализатор взаимодействует со сравнительными условиями (RC3: во время RC3 катализатор взаимодействовал с двумя предыдущими периодами сравнительных условий и 2 периодами смоделированных условий с мембраной). Катализаторы разбавляли инертным оксидом алюминия (1:27), чтобы измерять истинную каталитическую активность, т.е. далеко от равновесного превращения. SV=1190000 ч-1, Treduction 650°С. Результаты даны в таблице 3.
Все пористые Ni и Ni-В катализаторы, нанесенные на Mg(Al)О, демонстрируют очень высокую конверсию и очень хорошую стабильность. Присутствие бора также явно улучшает стабильность по сравнению с системами, содержащими только Ni. По сравнению с MgAl2O4 Ni-B (пример 2) носитель Mg(Al)О с пористым характером превосходит по стабилизации небольшие Ni частицы, полученные при малых содержаниях Ni (19 мас.%).
Комбинация Ni металлического активного центра и решетки магний-алюминиевого носителя приводит к синергизму, увеличивающему конверсию. В случае Ni-B Mg(Al)О бор, при условии, что количество бора превышает 2,5 мас.%, облегчает восстановление NiO до металлического Ni (активные центры для этапа активации метана, определяющего скорость) в противоположность Ni-В-Al2O3, описанному в современной литературе по Ni-В катализаторам, в котором образуется алюминат Ni и В не влияет на степень восстановления Ni. Усиленное восстановление никеля дает большее количество центров металлического никеля после восстановления при 650°С и отчасти увеличивает конверсию для Ni-В комбинированных катализаторов.
Также бор может адсорбироваться на носителе γ-Al2O3, образуя борат алюминия (9 Al2O3-2В2О3). Сравнительный катализатор, нанесенный на MgO, не показывает какой-либо конверсии в этих условиях. Заметим, что и сравнительный MgO, и сравнительный Al2O3 имели более высокую площадь поверхности и доступную площадь поверхности никеля по сравнению с MgAl2O4. Никель, нанесенный на MgAl2O4, следовательно, неожиданно является гораздо более активным, чем аналогичные катализаторы, нанесенные на оксид алюминия и MgO, в конкретных условиях.
ПРИМЕР 11: Агломерация частиц Ni при повышенных температурах
Т(подъема) и Т(снижения): 300-750-300°С
Т(прокаливания) 650°С; Т(восстановления) 650°С: SV = 955000 ч-1
7,5% СН4, 22,5% Н2О, остальное N2.
Температурный гистерезис обнаружили в случае MgAl2O4 материала: высокая температура реакции 700-750°С заставляет частицы никеля, расположенные на внешней поверхности, увеличиваться в размере, что отражается в потере конверсии метана при повторном выполнении измерений при меньшей температуре. В случае, когда частицы никеля нанесены в порах, частицы никеля стабилизируются от спекания/роста частиц внутри пор, и не замечается такой потери конверсии после работы при высокой температуре. Стабилизация частиц Ni также выгодна для регулирования углерода: большие частицы никеля также более активно образуют углерод и будут требовать больше бора, чтобы предотвращать вызываемую углеродом дезактивацию. Высокотемпературная устойчивость пористых Ni катализаторов на основе Mg(Al)О также подает надежду для применения в (высокотемпературных) условиях промышленного реформинга и каталитического реформинга в устройствах обработки топлива.
ДОПОЛНИТЕЛЬНЫЕ ПРИМЕРЫ
Катализаторы готовили с никелем, различными промоторами, например, B, La, Cu, Sn, Rh, Pt, Pd и др., и наносили на смешанный оксид MgO-Al2O3. Катализаторы изучали с помощью просвечивающей электронной микроскопии (ПЭМ), температурно-программируемого восстановления (ТПВ) и измерения каталитической активности и стабильности.
Средний размер частиц никеля для разных катализаторов составлял от 4 до 30 нм. Показано, что В очень полезен для получения очень маленьких частиц Ni в интервале 4-8 нм в зависимости от содержания Ni и В. Небольшие частицы никеля могут быть менее склонны к образованию углерода, чем большие частицы никеля. Стабильность Ni-В катализатора в паровом реформинге лучше, чем Ni катализатора. В демонстрирует тенденцию к соединению с Ni подобно С и поэтому, как считается, избирательно блокирует центры на ступеньках и под поверхностью и предотвращает образование центров зародышеобразования углерода, создавая сильную помеху диффузии атомов С.
Однако меньшие частицы труднее восстанавливать, чем большие частицы. При использовании типичной температуры восстановления 600°С для активации никелевого катализатора в мембранных реакторах приблизительно только 10-20% никеля, в зависимости от восстановительной среды и времени восстановления, восстанавливается в Ni-В комбинированном катализаторе. Тем не менее, конверсия метана, выражаемая формулой:
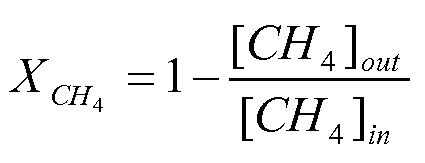
при 600°С очень хорошая по сравнению с конверсией на Ni катализаторе, имеющем долю восстановленного никеля в 4-5 раз выше. Катализаторы, модифицированные бором, демонстрируют гораздо меньший размер частиц Ni, гораздо более высокую дисперсность Ni и активность поверхностных атомов Ni.
Степень восстановления частиц никеля при 600°С сильно увеличивается при объединении никеля с промоторами La, Rh, Pd, Pt, благородными металлами в общем, а также с неблагородными металлами, как например, Cu и Sn. Объединение никеля с промоторами La, Rh, Pd, Pt, благородными металлами в общем, а также с неблагородными металлами, например, Cu и Sn, вместе с В дает дополнительные преимущества, в особенности для реформинга, усиленного разделением, при низких температурах. Преимуществами могут быть:
1) Степень восстановления никелевых частиц в Ni-В катализаторе при 600°С сильно увеличивается в присутствии третьего компонента (La, Rh, Pd, Pt, благородные металлы в общем, а также неблагородные металлы, например, Cu и Sn). В результате, количество металлического никеля, присутствующего в реакции реформинга между 400 и 900°С после восстановления при 600°С, значительно выше. Следовательно (более высокая) конверсия достигается при меньших температурах.
2) Катализатор также активен в реакции реформинга после восстановления при температурах ниже чем 600°С. В зависимости от выбора 3го компонента - промотора и точного состава катализатора в общем, конверсия метана уже является значительной после восстановления (активации) при таких низких температурах, как 500°С или даже ниже. Заметим, что даже наименьшая конверсия может резко увеличиваться, когда катализатор объединяют с водород-селективной мембраной, чтобы тянуть реакцию к завершению. Меньшая температура восстановления может быть желательна в случае, если свойства мембраны (носителя), объединенной с катализатором в реакторе с мембраной, не допускают высоких температур.
ПРИМЕР 12: Ni катализаторы с промоторами: размер частиц Ni
Стандартные медные сетки погружали в дисперсию нанесенных наночастиц в этаноле и затем сушили на воздухе. FEI Tecnai 20 ПЭМ, оборудованный нитью LaB6 и энергетическим фильтром Gatan GIF200, применяли при 200 кВ. Результаты ПЭМ анализа изображены для 40,1 мас.% Ni образца на фиг.1а/1b. Идентификацию Ni частиц выполняли с помощью ЭФПЭМ изображения (ПЭМ с фильтрацией энергии) (путем использования ЭФПЭМ изображений с конкретными величинами потерь энергии становится возможным создавать изображения/карты, которые отражают присутствие конкретного элемента, т.е. изображения являются яркими там, где присутствует данный элемент, и темными, где он отсутствует). Определение диаметров частиц возможно в светлопольной ПЭМ (вместе со статистической оценкой распределения диаметров частиц). Распределения размера частиц определяли путем анализа, по меньшей мере, 100 металлических частиц на, по меньшей мере, четырех разных микрофотографиях.
Ni частицы становятся больше и распределение размера частиц уширяется с увеличением содержания Ni. В противоположность ожиданиям, В-промотирование оказывает отчетливое влияние на размер частиц никеля. Фиг.2-3 показывают ПЭМ изображения двух других образцов (40,1 мас.% Ni/2,8 мас.% В со средним размером частиц 7 нм; и 18 мас.% Ni/1,2 мас.% В со средним размером частиц 5 нм, соответственно). Использование маленького количества Rh также приводило к небольшому уменьшению размера частиц Ni. Однако это изменение очень мало по сравнению с В-промотированием. См. таблицу 5 ниже.
ПРИМЕР 13: Ni и (другие) каталитические промоторы: влияние промоторов на легкость восстановительной активации Ni катализатора и активность катализатора
Эксперименты с температурно-программируемым восстановлением (ТПВ) выполняли в проточном устройстве, оборудованном реактором с неподвижным слоем, регулируемой компьютером печью и детектором теплопроводности. Обычно некоторое количество катализатора помещали между двумя тампонами из кварцевой ваты в кварцевом реакторе. Образец восстанавливали в 10 об.% Н2 в аргоне при скорости потока 30 мл/мин, нагревая от КТ до 1000°С со скоростью 10°С/мин. Сигнал Н2 калибровали, используя сравнительный катализатор CuO/SiO2.
Конверсию измеряли между 300 и 900°С при атмосферных условиях при исходном газе 7,5% СН4, 22,5% Н2О (Н/С=10). Катализатор разбавляли инертным оксидом алюминия на уровне порошка, чтобы измерять истинную каталитическую активность, т.е. вдали от равновесной конверсии. Разбавленный катализатор испытывали в виде отсеянной фракции 0,212-0,425 мм в кварцевом реакторе с внутренним диаметром 6 мм.
Фиг.4 показывает профили температурно-программируемого восстановления для Ni катализатора, нанесенного на MgAl2O4, и катализаторов с комбинациями Ni-промотор. Две верхние кривые показывают катализаторы Ni-В; другие кривые приведены, чтобы показать эффект совместного введения (но в отсутствие В). Они свидетельствуют, что присутствие второго компонента возле никеля сдвигает начало восстановления никеля в сторону меньшей температуры, причем степень сдвига изменяется с промотором. Заметим, что площадь преобладающего пика, видимого на фиг.В1, относится к восстановлению никелевых частиц: восстановление родия заметно в Ni-Rh, небольшое плечо при 350°С; в Ni-Cu заметно восстановление CuO при 200°С. Явным исключением, однако, является катализатор с комбинацией Ni-В, демонстрирующий начало восстановления никеля приблизительно при 600°С. Из интенсивностей полос следует, что данное восстановление должно быть вследствие восстановления оксида никеля. Более высокая температура восстановления связана с меньшими частицами никеля в Ni-В катализаторе. Высокая температура указывает на очень сильное взаимодействие Ni-В. Начало восстановления Ni в Ni-В снова сдвигается, однако, к меньшей температуре при введении небольшого количества родия в катализатор. Таким образом, добавление родия (и других благородных металлов, а также неблагородных металлов) к Ni-В катализаторам делает возможной восстановительную активацию катализатора на основе никеля при меньших температурах.
Долю металлического Ni после восстановления до 600°С определяли для некоторых образцов, см. таблицу ниже. Из нее следует, что восстановление Ni в В-промотированных катализаторах действительно очень затруднено; доля восстановленного Ni, участвующего в реакции парового реформинга, будет довольно небольшой в случае восстановления при 600°С. Некоторые ТПВ результаты суммированы в таблице 6 ниже.
(ммоль/гкат)
2Доля металлического Ni после восстановления до 600°С
Величина конверсии может быть исправлена в соответствии с дисперсностью металла и долей металлического металла, чтобы сделать сравнение значимым. Дисперсность Ni определяли с помощью ПЭМ анализа. Долю металлического Ni, определенную с помощью ТПВ после восстановления при 600°С, использовали, чтобы скорректировать количество невосстановленного Ni и вычислить активность на атом поверхности. Некоторые скорости парового реформинга суммированы в таблице ниже.
В-промотированный катализатор демонстрирует гораздо более высокую активность. В-промотирование действительно приводит к гораздо большей реакционной способности поверхностных атомов Ni. Активность Rh-промотированных катализаторов подобна активности непромотированных Ni катализаторов. Это заставляет предположить, что Rh промотор не вовлекается в реакцию иначе, чем влияя на дисперсность и степень восстановления Ni фазы.
Таблица 8 показывает активность Ni-В, Ni-В-Rh и Ni-В-Cu катализаторов в паровом реформинге метана после восстановления при разных температурах. В соответствие с более высоким началом восстановительной активации, показанной на фиг.4 для Ni-В катализатора, Ni-В катализатор требует более жесткой восстановительной обработки для активации по сравнению с аналогичным Ni катализатором. При использовании 40% водорода в азоте и продолжительности 5 ч в потоке требовалась температура 585°С, чтобы активировать Ni-В катализатор. Это немного выше, чем для аналогичного катализатора с одним никелем. Ni-B-Rh-MgAl2O4 катализатор активируется гораздо легче, и, в результате, активность после восстановления при 500°С подобна активности Ni-В катализатора после восстановления при 605°С. Ni-B-Rh-MgAl2O4 имеет преимуществом более высокое восстановление при 530°С (т.е. активность увеличивает по сравнению с ситуацией после восстановления при 500°С), тогда как температуры восстановления выше чем 530°С не вызывают дополнительной активности. Ясно, что температура восстановления 530°С достаточна для полного восстановления всего активного никеля в Ni-B-Rh-MgAl2O4 катализаторе. Добавление Cu с получением Ni(18)B(1,2)Cu(2) также отчасти улучшает восстановительную активацию, как показано в таблице.
Резюмируя, В является прекрасным структурным промотором для получения маленьких частиц Ni. Борный промотор оказывает очень благоприятное влияние на размер частиц Ni и их стабильность в паровом реформинге метана. Несмотря на ингибирование восстановления Ni за счет В, В-промотированные Ni катализаторы демонстрируют такие же скорости реакции на единицу массы, как стандартный Ni катализатор аналогичной дисперсности, но с улучшенной стабильностью. Кроме того, скорость реакции на Ni-В катализаторе дополнительно улучшается путем увеличения участия восстановленного металлического никеля, что может достигаться путем добавления благородных или неблагородных металлов.
| название | год | авторы | номер документа |
|---|---|---|---|
| КАТАЛИЗАТОР РИФОРМИНГА ГАЗООБРАЗНОГО УГЛЕВОДОРОДНОГО СЫРЬЯ (ВАРИАНТЫ) | 2013 |
|
RU2549878C1 |
| КАТАЛИЗАТОР ОКИСЛИТЕЛЬНОЙ КОНВЕРСИИ УГЛЕВОДОРОДНЫХ ГАЗОВ С ПОЛУЧЕНИЕМ ОКСИДА УГЛЕРОДА И ВОДОРОДА | 2013 |
|
RU2532924C1 |
| КАТАЛИЗАТОР РЕФОРМИНГА | 2011 |
|
RU2558150C2 |
| СПОСОБ ПОЛУЧЕНИЯ ОКСИДНЫХ КАТАЛИЗАТОРОВ НА ПОДЛОЖКЕ | 2003 |
|
RU2329100C2 |
| ФОРМОВАННЫЕ ГЕТЕРОГЕННЫЕ КАТАЛИЗАТОРЫ | 2009 |
|
RU2488443C2 |
| ФОРМОВАННЫЕ ГЕТЕРОГЕННЫЕ КАТАЛИЗАТОРЫ | 2009 |
|
RU2488444C2 |
| ПОЛУЧЕНИЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ И СИНТЕЗ-ГАЗА ИЗ МЕТАНА | 2007 |
|
RU2458899C2 |
| ФОРМОВАННЫЕ ГЕТЕРОГЕННЫЕ КАТАЛИЗАТОРЫ | 2009 |
|
RU2487757C2 |
| СПОСОБ ИЗГОТОВЛЕНИЯ КАТАЛИЗАТОРА | 2011 |
|
RU2774626C2 |
| СПОСОБ КОНВЕРСИИ НИТРАТА МЕТАЛЛА | 2007 |
|
RU2437717C2 |
Изобретение относится к пористому катализатору для получения водорода путем парового реформинга. Предлагаемый пористый катализатор содержит алюминий и магний, а также дополнительно содержит бор и никель. Бор присутствует в количестве 0,1-20 мас.% в расчете на общую массу катализатора. Данный пористый катализатор содержит поры, имеющие средний размер пор в интервале 0,1-50 нм. Предлагаемый катализатор обладает высокой каталитической активностью и стабильностью. Изобретение относится также к способу получения указанного катализатора и способу получения водорода по реакции парового реформинга в присутствии этого катализатора. 3 н. и 16 з.п. ф-лы, 8 табл., 4 ил., 13 пр.
1. Пористый катализатор получения водорода, содержащий алюминий и магний, где данный пористый катализатор дополнительно содержит бор и никель, причем бор присутствует в количестве 0,1-20 мас.% в расчете на общую массу катализатора, и где данный пористый катализатор содержит поры, имеющие средний размер пор в интервале 0,1-50 нм.
2. Катализатор по п.1, где магний присутствует в виде оксида магния.
3. Катализатор по п.2, где данный пористый катализатор содержит MgAl2O4.
4. Катализатор по любому из пп.1-3, где данный пористый катализатор содержит поры, имеющие размер пор в интервале 4-30 нм.
5. Катализатор по любому из пп.1-3, где данный катализатор содержит 15-45 мас.% Ni и 0,5-5 мас.% В.
6. Катализатор по любому из пп.1-3, где данный пористый катализатор дополнительно содержит один или несколько элементов, выбранных из Li, Na, K, Rb, Cs, Be, Sr, Ba, Sc, Y, La, Ce, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm, Yb, Hf, V, Nb, Та, Mo, W, Re, Ru, Os, Co, Rh, Pd, Ir, Pt, Cu, Ge и Sn.
7. Катализатор по п.5, где данный пористый катализатор дополнительно содержит благородный металл, предпочтительно Rh, Ru, Pd, Ir или Pt, особенно Rh, предпочтительно с долей 0,01-4 мас.% от массы катализатора.
8. Катализатор по п.6, где данный пористый катализатор дополнительно содержит благородный металл, предпочтительно Rh, Ru, Pd, Ir или Pt, особенно Rh, предпочтительно с долей 0,01-4 мас.% от массы катализатора.
9. Катализатор по любому из пп.1-3, где данный пористый катализатор дополнительно содержит один или несколько элементов из La, Cu, Sn и Fe.
10. Катализатор по любому из пп.1-3, где, когда данный пористый катализатор был подвергнут восстановительным условиям, полученные таким образом частицы Ni имеют размер частиц в интервале 0,1-50 нм, предпочтительно в интервале 4-30 нм.
11. Катализатор по любому из пп.1-3, где масса никеля составляет 4-70 мас.% в расчете на общую массу пористого катализатора.
12. Способ получения пористого катализатора по любому из пп.1-11, где
a) формируют, в процессе формирования, пористый материал путем объединения по меньшей мере соединения алюминия, соединения магния, порообразователя, причем данный порообразователь содержит триблоксополимер, имеющий молекулярную массу в интервале 3000-18000 Да, соединения никеля и соединения бора, а также, необязательно, соединения дополнительного металла, и подвергают эти соединения условиям кристаллизации, что обеспечивает пористый материал;
b) обеспечивают присутствие соединения никеля и соединения бора в данном пористом материале или добавление соединения никеля и/или соединения бора к данному пористому материалу, полученному с помощью процесса формирования, и
c) прокаливают сформированный таким образом пористый материал.
13. Способ по п.12, где соединение магния содержит растворимую соль магния, где соединение алюминия содержит алюминийорганическое соединение, где соединение никеля содержит растворимую соль никеля, где соединение бора содержит боратную соль или, в особенности, борную кислоту.
14. Способ получения водорода, где углеводородсодержащий газ подвергают реакции парового реформинга в присутствии катализатора реформинга в реакционной камере, где данный катализатор реформинга представляет собой катализатор по любому из пп.1-11, в котором частицы Ni имеют размер частиц в интервале 0,1-50 нм.
15. Способ по п.14, где перед тем, как подвергают углеводородсодержащий газ реакции реформинга в реакционной камере, данный пористый катализатор подвергают восстановительным условиям, и полученные таким образом частицы Ni имеют размер частиц в интервале 4-30 нм.
16. Способ по п.14 или 15, где по меньшей мере часть заданного продукта реакции, в частности Н2 или CO2, селективно удаляют из реакционной камеры с помощью сепаратора, в частности мембраны, которая является селективно проницаемой для упомянутого продукта реакции.
17. Способ по п.16, где данный углеводородсодержащий газ подвергают реакции реформинга при температуре в интервале 400-750°С, особенно 500-700°С.
18. Способ по п.14 или 15, где данный углеводородсодержащий газ содержит СН4.
19. Способ по п.14 или 15, где данный пористый катализатор дополнительно содержит благородный металл, особенно Rh.
| US 5399537 A, 21.03.1995 | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
| ЯДЕРНЫЙ ГОМОГЕННЫЙ РЕАКТОР | 1997 |
|
RU2125743C1 |
| КАТАЛИЗАТОР ДЛЯ ПРОЦЕССА ФИШЕРА-ТРОПША (ВАРИАНТЫ) И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2292238C2 |
Авторы
Даты
2016-05-27—Публикация
2011-11-15—Подача