РОДСТВЕННАЯ ЗАЯВКА
Настоящая заявка является родственной заявке на патент Великобритании номер 10010700, поданной 22 января 2010 года, содержание которой полностью включено в настоящую заявку посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
Настоящее изобретение в целом относится к области лекарственных соединений и, в частности, к конкретным пирувамидным соединениям (которые в настоящей заявке для удобства в целом называют «PVA соединениями»), которые, в числе прочего, ингибируют аллерген пылевых клещей 1 группы, представляющий собой пептидазу (например, Der p 1, Der f 1, Eur m 1). Настоящее изобретение также относится к фармацевтическим композициям, содержащим указанные соединения, и применению указанных соединений и композиций, как in vitro, так и in vivo, для ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу, и для лечения заболеваний и нарушений, опосредованных аллергеном пылевых клещей 1 группы, представляющим собой пептидазу; которые можно облегчить путем ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу; астмы; ринита; аллергического конъюнктивита; атопического дерматита; аллергического состояния, вызванного пылевыми клещами; аллергического состояния, вызванного аллергеном пылевых клещей 1 группы, представляющим собой пептидазу; и атопии у собак.
УРОВЕНЬ ТЕХНИКИ
В настоящей заявке цитируется ряд патентов и публикаций для более подробного описания и раскрытия изобретения и уровня техники, к которому относится настоящее изобретение. Каждая из указанных цитат в настоящей заявке полностью включена посредством ссылки в настоящее изобретение, в той же мере, как если бы было конкретно и отдельно указано, что каждая отдельная цитата включена посредством ссылки.
Следует понимать, что во всей настоящей заявке, включая формулу изобретения, которая представлена далее, если иное не следует из контекста, под словом «включают» и такими его формами, как «включает» и «включающий», подразумевается включение указанного числа или этапа или группы указанных чисел или этапов, но не подразумевается исключение любого другого числа или этапа или группы чисел или этапов.
Необходимо отметить, что в настоящей заявке и приложенной формуле изобретения употребление предмета в единственном числе включает множественное число указанного предмета, если иное не следует из контекста. Таким образом, например, ссылка на «фармацевтический носитель» включает смеси двух или более таких носителей и т.д.
В настоящей заявке диапазоны часто представлены от «примерно» одного конкретного значения и/или до «примерно» другого конкретного значения. Когда представлен такой диапазон, другой вариант реализации изобретения включает значения от указанного одного конкретного значения и/или до указанного другого конкретного значения. Подобным образом, когда значения представлены в виде приблизительных значений путем использования предшествующего указанному значению слова «примерно», следует понимать, что конкретное значение представляет собой другой вариант реализации изобретения.
Настоящее изобретение включает данные, которые могут использоваться для понимания настоящего изобретения. Не следует допускать, что любые из представленных в настоящей заявке данных являются предшествующим уровнем техники или относятся к заявленному в настоящей заявке изобретению, или что любая публикация, на которую непосредственно или косвенно есть ссылка в настоящей заявке, является предшествующим уровнем техники.
Аллергические заболевания
Аллергические заболевания, такие как астма, ринит, конъюнктивит и экзема, представляют собой усугубляющуюся проблему всемирного здравоохранения, не охваченную существующими способами лечения. Клинические состояния возникают и развиваются у генетически предрасположенных субъектов при воздействии ряда разнообразных веществ, известных как аллергены. Существует множество источников аллергенов, но те источники, которые связаны с жилыми помещениями, являются особо важными возбудителями заболевания, так как люди подвергаются их воздействию в течении длительных периодов времени. Среди аллергенов жилых помещений в целом наиболее важной причиной аллергических заболеваний являются аллергены, происходящие от клещей домашней пыли (HDM). Указанные клещи в большом количестве обнаруживаются в домах, на рабочих местах, на развлекательных площадках и в общественных и личных транспортных средствах. Хроническая сенсибилизация к аллергенам HDM может возникать в любое время жизни, и последующие обострения, вызванные повторным воздействием аллергена, повышают вероятность перехода несущественных состояний, таких как аллергический ринит, в астму, которая является более серьезным заболеванием. Кроме того, клещи домашней пыли вызывают проблемы со здоровьем у животных, которые живут вместе с людьми. Например, состояние атопии у собак представляет собой наследственное заболевание, которое вызывает совокупность аллергических состояний кожи, носа и глаз (Sture et al., 1995). Круглогодичные симптомы обычно связаны с сенсибилизацией и последующим повторным воздействием аллергенов пылевых клещей. Хорошо известно, что клещи домашней пыли считаются важными возбудителями круглогодичных аллергических симптомов у собак, вызывающих необходимость ветеринарного лечения для облегчения симптомов заболевания. Симптомы, которые наблюдаются у собак, значительно сходны с симптомами атопического дерматита и конъюнктивита у человека.
Важное значение аллергенов клещей домашней пыли как возбудителей аллергических состояний вызвало необходимость понимания причины их аллергенности. Исследования молекулярных механизмов аллергенности показали, что аллерген HDM, имеющий наибольшую клиническую значимость, представляет собой цистеиновую пептидазу. Неожидано оказалось, что указанная пептидазная активность вносит решающий вклад в развитие аллергии на аллергены HDM в целом и на другие неспецифические аллергены, не родственные аллергенам HDM.
Известно несколько видов пылевых клещей (например, Dermatophagoides pteronyssinus, Dermatophagoides farinae, Dermatophagoides siboney и Euroglyphus maynei), представители каждого из которых продуцируют множество аллергенных белков. Аллергены различных видов можно разделить на отдельные группы, аллергенов, которые обладают перекрестной иммунологической реактивностью, так как они являются белками, сильно сходными с консервативными аминокислотными последовательностями. В случае HDM, аллергены 1 группы (например, Der р 1, Der f 1, Eur m 1) отвечают за >95% аллергических реакций, вызванных HDM, и представляют собой высоко консервативное семейство цистеиновых пептидаз. В норме указанные цистеиновые пептидазы у клещей выполняют функцию пищеварительных ферментов, которые способны переваривать устойчивые структурные белки в сухих чешуйках отшелушивающейся кожи, являющейся важным компонентом питания HDM. Аминокислотные последовательности аллергенов 1 группы, представляющих собой цистеиновые пептидазы HDM, являются настолько консервативными (>90%), что указанные пептидазы можно считать функционально идентичными и рассматривать их как единственную терапевтическую мишень при подборе лекарственных средств. Также известно, что клинически значимый аллерген другого клеща, Blomia tropicalis, имеющего более ограниченное географическое распределение, представляет собой родственную цистеиновую пептидазу и обладает перекрестной иммунологической реактивностью с аллергенами клещей домашней пыли 1 группы. Указанные данные дают основание полагать, что ингибитор аллергенов HDM 1 группы может в целом являться применимым в качестве ингибитора родственных молекул всех видов клещей, вызывающих аллергию.
Аллергены HDM 1 группы являются важными возбудителями астмы и других аллергических состояний. При вдыхании указанных аллергенов в результате их пептидазной активности расщепляются белки, что приводит к (i) повышению проницаемости эпителия воздухоносных путей, обеспечивающему доступ указанным и другим не пептидазным аллергенам к дендритным антиген-презентирующим клеткам и (ii) активации сигнальных каскадов, переключающих иммунологический ответ на Th2-фенотип.Оба указанных события вызывают аллергию и должны повторяться для ее поддержания. Блокирование указанных существенных и сложных этапов аллергической сенсибилизации путем ингибирования активности аллергена 1 группы, представляющего собой цистеиновую пептидазу, таким образом, могло бы лежать в основе уникального подхода к лечению и предотвращению аллергии.
Аллергены HDM 1 группы как терапевтическая мишень
Люди подвергаются воздействию аллергенов клещей домашней пыли (HDM) до 23 часов в сутки каждый день; поэтому указанные аллергены имеют большое клиническое значение в ряду клинических состояний, для которых общим молекулярным маркером заболевания является повышенный уровень IgE. Многолетние и охватывающие разные группы населения популяционные исследования демонстрируют, что положительная кожная проба на антитела IgE к аллергенам HDM связана с астмой, персистентным ринитом, аллергическим конъюнктивитом или атопическим дерматитом (Arruda et al., 1991; Gelber et al., 1993; Miyamoto et al., 1968; Peat et al., 1996; Peat et al., 1991; Pollart et al., 1989; Smith et al., 1969; Sporik et al., 1990). У генетически предрасположенных субъектов первый контакт с указанными аллергенами может провоцировать начало заболевания в любой момент времени, а при повторных воздействиях в течение жизни неопасные состояния могут перерастать в серьезное заболевание. Таким образом, вероятность развития астмы повышается в 10-20 раз после установленного ринита. Более того, самое крупное из проведенных исследований астмы у взрослых показало, что в отличие от ранее существующих убеждений, аллергия на HDM имеет настолько же большое значение для взрослых, как и для детей (Jaakkola et al., 2006).
Риск возникновения и тяжесть аллергии являются дозозависимыми от уровня воздействия аллергена, что повышает интерес к способам фармакологического воздействия, направленного на аллергены HDM 1 группы. Клинические данные решительно подтверждают существование порогового уровня воздействия, выше которого становится вероятной сенсибилизация субъектов, находящихся в группе риска. Более того, существует зависимость доза-ответ между концентрациями указанных аллергенов в домах (и, таким образом, уровнем воздействия на человека) и значимостью указанной сенсибилизации для развития астмы (Gelber et al., 1993; Peat et al., 1991; Platts-Mills et al., 1997; Platts-Mills et al., 1987; Dowse et al., 1985; Charpin et al., 1991). Указанные наблюдения дают основание полагать, что избежание или инактивация указанных ключевых аллергенов (т.е., путем снижения дозы функционального аллергена, воздействию которого подвергается субъект), вероятно, приводит к снижению сенсибилизации, вызывая облегчение симптомов и улучшение клинического прогноза. Уменьшение воздействия указанных аллергенов лежит в основе стратегий избежания физического контакта с аллергенами, которые исследовались в качестве способов контроля аллергии. Эффективность избежания физического контакта с аллергеном подтверждается контролируемыми исследованиями, в которых люди перемещались в условия (например, альпийский санаторий), в которых мог быть организован строгий режим избежания аллергена (Dowse et al., 1985; Platts-Mills et al., 2000; Vervloet et al., 1982; Peroni et al., 1994). Эффект строгого режима избежания аллергена является быстрым на начальных этапах, при этом пациенты проявляют значительное снижение маркеров воспаления или уменьшение использования медикаментов в пределах от 2 до 4 недель (van Velzen et al., 1996; Schultze-Werninghaus, 2006; Bodini et al., 2004; Gourgoulianis et al., 2001; Piacentini et al., 1999; Piacentini et al., 1998). Однако указанные меры избежания физического контакта в целом являются неосуществимыми на практике, и благоприятные эффекты снижаются при возвращении к повседневной жизни.
Учитывая участие протеолитической активности в аллергической сенсибилизации, разработка средств ингибирования пептидазной активности аллергенов 1 группы могла бы обеспечить фармакологическую инактивацию аллергена, имитирующую эффекты физического избежания аллергена. Предполагается, что оптимальными средствами достижения указанной цели является местное или системное лечение пациентов указанными ингибиторами. Одним преимуществом такого подхода является тот факт, что фармакологическая инактивация аллергена не устраняется при перемещениях субъекта, подвергаемого лечению (т.е., лечение является «мобильным»), с достижением эффекта длительного избежания аллергена, который не достигается при использовании мер физического избежания аллергена. Помимо применения в качестве медикаментов, ингибиторы пептидазных аллергенов 1 группы, вероятно, могут иметь дополнительную ценность в качестве акарицидов, применимых для обработки окружающей среды. Путем инактивации ключевых ферментов, вовлеченных в переваривание пищи HDM, указанные ингибиторы могли бы лишить клещей источника питания, предотвратив их размножение.
Аллергены и пептидазная активность
Два наблюдения относятся к оценке вклада пептидазной активности в реакцию аллергической сенсибилизации. Первым из них является демонстрация того, что протеолитическая активность малого количества ферментативных аллергенов является необходимой для аллергической сенсибилизации через дыхательные пути. Вторым наблюдением является способность пептидаз инициировать аллергическую сенсибилизацию к неспецифическим аллергенам, у которых отсутствует протеолитическая активность. При отдельном введении и в отсутствии адъювантов такие не ферментативные неспецифические аллергены даже при системной иммунизации не вызывают ответ, вызывают устойчивость или только слабые lgG-опосредованные реакции, (Seymour et al., 1998; van Halteren et al., 1997; McMillan et al., 2004; McCusker et al., 2002; Hellings et al., 2001). Так как большинство аллергенов не обладает протеолитической активностью, способность отдельных пептидаз оказывать значительное влияние на развитие сенсибилизации к неспецифическим аллергенам создает привлекательную возможность терапевтического применения ингибиторов клещевых аллергенов 1 группы.
Предыдущие исследования показали, что протеолитическая активность аллергенов HDM 1 группы вносит существенный вклад в аллергическую реакцию по двум основным механизмам, которые являются основными для инициации и поддержания аллергического состояния. Указанные механизмы представляют собой:
- Облегчение доставки аллергена через поверхность слизистых оболочек, обеспечивающее, таким образом, доступ к антиген-презентирующим клеткам (например, дендритным клеткам в легких) (Holt et al., 1990; Holt, 2002; Huh et al., 2003; Lambrecht et al., 2003a; Lambrecht et al., 2002; Lambrecht et al., 2003b; Wan et al., 2000).
- Активацию путей передачи сигнала, которые способствуют развитию аллергии у субъектов, имеющих генетическую предрасположенность (Hellings et al., 2001; Comoy et al., 1998; Stewart et al., 2003).
Пептидазные аллергены HDM, таким образом, проявляют значительные независимые от IgE эффекты, но оказывающие существенное воздействие на lgE-зависимую сенсибилизацию и аллергические ответы (King et al., 1998; Asokananthan et al., 2002). Указанные эффекты обеспечивают сенсибилизацию к стимулирующему пептидазному аллергену, но поскольку эффекты описанных общих механизмов по существу являются не специфичными к аллергену, как описано выше, также возникает сенсибилизация к не ферментативным неспецифическим аллергенам (Stewart et al., 2003; Wan et al., 1999).
Доставка аллергена
Дендритные клетки представляют собой основные антиген-презентирующие клетки в дыхательных путях (Holt et al., 1990; Holt, 2002; Huh et al., 2003; Lambrecht et al., 2003a; Lambrecht et al., 2002; Lambrecht et al., 2003b). Однако для развития и поддержания эффективного lgE-ответа вероятность контакта с антигенами должна быть повышена (Lambrecht et al., 2003b). Существенный этап в выявлении аллергена может быть облегчен благодаря активности аллергена 1 группы, представляющего собой цистеиновую пептидазу клещей, расщепляющей трансмембранные белки адгезии плотных соединений в эпителии, облегчая параклеточную доставку любого аллергена к дендритным клеткам (Wan et al., 1999; Wan et al., 2000; Winton et al., 1998).
IgE-независимая активация клеток
Считается, что пептидазные аллергены вносят вклад во врожденный иммунитет и активируют различные клетки по множеству IgE-независимых механизмов. Сигнальные пути, активируемые расщеплением связанных с лигандами рецепторов на эпителиальных клетках, являются одним из таких механизмов, вносящих вклад в хроническое высвобождение гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) и интерлейкина 6 (IL-6). Указанные цитокины присутствуют в повышенном количестве в дыхательных путях при аллергической астме и рините (Broide et al., 1992; Fahy et al., 1995; Muraguchi et al., 1988; Vercelli., 1989). Они обеспечивают аллергический ТП2-СДВИГ несколькими путями. Например, IL-6 является важным для созревания В-клеток и IL-4-зависимого синтеза IgE (Muraguchi et al., 1988; Vercelli., 1989). GM-CSF генерирует сигналы, заставляющие дендритные клетки мигрировать из эпителия дыхательных путей в региональные лимфатические узлы для представления захваченных антигенов (Stick et al., 2003). Таким образом, протеолитическая активность, обеспечивающая расщепление связанных с лигандом рецепторов, связана с рядом событий, существенных как для инициации аллергический сенсибилизации, так и для ее поддержания. Пептидазные аллергены активируют тучные клетки по IgE-независимым механизмам, и, следовательно, их вклад в острый бронхоспазм, вызванный сенсибилизацией к аллергену, должен обеспечиваться указанной зависимой от пептидазы активацией, что указывает на то, что ингибиторы пептидазных аллергенов 1 группы должны ослаблять острый аллергический бронхоспазм. Другие IgE-независимые механизмы включают расщепление рецепторов цитокина и рецепторов IgE, связанное с распространением аллергии (Ghaemmaghami et al., 2002), инактивацию системы антипептидазной защиты (которая может уже быть нарушенной при аллергии) и расщепление других защитных факторов, таких как поверхностно-активные белки (Deb et al., 2007).
Вклад протеолитических аллергенов в аллергию
Потенциальная ценность пептидазных аллергенов как мишени для лечения аллергии показана на основании их способности быстро и непосредственно вызывать IgE-опосредованную сенсибилизацию и на основании исследований с использованием стандартных ингибиторов цистеиновых пептидаз на экспериментальных животных.
Сильная аллерген-специфичная IgE-опосредованная сенсибилизация может быть достигнута путем подвержения мышей неинвазивному воздействию Der p 1 с высокой специфической протеолитической активностью в отсутствии адъювантов (Zhang et al., 2009). На крысах Brown Norway образование специфичного к Der p 1 IgE и аллергическая реактивность также возникают без необходимости в дополнительных адъювантах. Напротив, хорошо известно, что сложно индуцировать образование антител с высоким титром к рекомбинантной Der p 1, у которой отсутствует высокая ферментативная активность (и которая, следовательно, ведет себя подобно неспецифическому аллергену). Протеолитическая активность Der p 1 также повышает сенсибилизацию к непептидазным неспецифическим аллергенам HDM и из других источников (Gough et al., 2001).
Доставка аллергена с помощью пептидазных аллергенов может повышаться путем инактивации указанными пептидазными аллергенами системы антипептидазной защиты (Kalsheker et al., 1996). Таким же важным является тот факт, что потеря функционального полиморфизма в генах эндогенных ингибиторов ферментов (например, LETK1 (хромосома 5q32), PAI-I (хромосома 7), ингибитора С1-эстеразы (хромосома 11), кластера серпиновых ингибиторов (хромосома 14), хромосома 18q21) вызывает предрасположенность у субъекта к аллергическому заболеванию. Указанные данные недавних исследований дополняют функциональную связь между аллергией и недостаточностью ингибитора протеазы, которые накапливались в течение последних 25 лет (Rudolph et al., 1978; Hyde et al., 1979; Eden et al., 2003; Sigsgaard et al., 2000).
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Фигура 1 представляет собой гистограмму величины ответа после Сенсибилизации 1 (слева) и Сенсибилизации 2 (справа), выраженной как процент от величины ответа после Сенсибилизации 1. (Представлены медианы; погрешность в виде 25-го/75-го процентилей.)
Фигура 2 представляет собой гистограмму изменения сопротивления дыхательных путей (см H2O L-1 сек-1) после контрольной сенсибилизации аллергеном (слева) и сенсибилизации аллергеном через 120 минут после лечения исследуемым соединением PVA-026. (Представлены медианы. Погрешность в виде 25-го/75-го процентилей. Для (*): Р<0,05, критерий суммы рангов Манна-Уитни по отношению к контрольной сенсибилизации аллергеном.)
Фигура 3 представляет собой гистограмму изменения сопротивления дыхательных путей (см H2O л-1 сек-1) после контрольной сенсибилизации аллергеном (слева) и сенсибилизации аллергеном через 120 минут после лечения тестируемым соединением PVA-038 (в виде соли ТФУ). (Представлены медианы. Погрешность в виде 25-го/75-го процентилей. Для (*): Р<0,05, критерий суммы рангов Манна-Уитни по отношению к контрольной сенсибилизации аллергеном).
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Согласно одному аспекту, изобретение относится к конкретным пирувамидным соединениям (которые для удобства в настоящей заявке вместе называются «PVA соединениями»), описанным в настоящей заявке.
Согласно другому аспекту, изобретение относится к композиции (например, фармацевтической композиции), содержащей PVA соединение, описанное в настоящей заявке, и фармацевтически приемлемый носитель или разбавитель.
Согласно другому аспекту, изобретение относится к способу получения композиции (например, фармацевтической композиций), включающему этап смешения PVA соединения, описанного в настоящей заявке, и фармацевтически приемлемого носителя или разбавителя.
Согласно другому аспекту, настоящее изобретение относится к способу ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу (например, Der p 1, Der f 1, Eur m 1), in vitro или in vivo, включающему приведение в контакт аллергена пылевых клещей 1 группы, представляющего собой пептидазу, с эффективным количеством PVA соединения, описанного в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к способу ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу, в клетке, in vitro или in vivo, включающему приведение клетки в контакт с эффективным количеством PVA соединения, описанного в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к способу лечения, включающему введение субъекту, нуждающемуся в указанном лечении, терапевтически эффективного количества PVA соединения, описанного в настоящей заявке, предпочтительно в форме фармацевтической композиции.
Согласно другому аспекту, настоящее изобретение относится к PVA соединению, описанному в настоящей заявке, для применения в способе лечения человека или животного посредством терапии.
Согласно другому аспекту, настоящее изобретение относится к применению PVA соединения, описанного в настоящей заявке, для получения лекарственного средства для применения в терапии.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение заболевания или состояния, опосредованного аллергеном пылевых клещей 1 группы, представляющим собой пептидазу.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение заболевания или состояния, которое можно облегчить путем ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение: астмы, например, атопической астмы; аллергической астмы; атопической бронхиальной IgE-опосредованной астмы; бронхиальной астмы; экзогенной астмы; вызванной аллергеном астмы; аллергической астмы, обостренной респираторной вирусной инфекцией; инфекционной астмы; инфекционной астмы, вызванной бактериальной инфекцией; инфекционной астмы, вызванной грибковой инфекцией; инфекционной астмы, вызванной протозойной инфекцией; или инфекционной астмы, вызванной вирусной инфекцией.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение бронхиальной гиперреактивности, связанной с астмой; или бронхиальной гиперчувствительности, связанной с астмой.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение ремоделирования дыхательных путей, связанного с аллергическим заболеванием легких, например, ремоделирования дыхательных путей, связанного с астмой.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение астмы, сопровождающейся хроническим обструктивным заболеванием легких, например, астмы, сопровождающейся эмфиземой; или астмы, сопровождающейся хроническим бронхитом.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение ринита, например, аллергического ринита; круглогодичного ринита; персистирующего ринита или IgE-опосредованного ринита.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение аллергического конъюнктивита, включая, например, IgE-опосредованной конъюнктивит.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение атопического дерматита.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение аллергического состояния, которое вызывается пылевыми клещами.
Согласно одному варианту реализации изобретения, лечение представляет собой лечение аллергического состояния, которое вызывается аллергеном пылевых клещей 1 группы, представляющим собой пептидазу (например, Der p 1, Der f 1, Eur m 1).
Согласно одному варианту реализации изобретения, лечение представляет собой лечение атопии у собак.
Согласно одному варианту реализации изобретения, лечение также включает лечение с помощью одного или более дополнительных терапевтических агентов, например, одного или более дополнительных терапевтических агентов, выбранных из агентов, которые применяют или могут применять для лечения респираторного заболевания.
Согласно другому аспекту, настоящее изобретение относится к PVA соединению, описанному в настоящей заявке, для применения в качестве акарицида.
Согласно другому аспекту, настоящее изобретение относится к композиции, содержащей PVA соединение, описанное в настоящей заявке, для применения в качестве акарицида.
Согласно другому аспекту, настоящее изобретение относится к акарицидной композиции, содержащей PVA соединение, описанное в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к применению PVA соединения, описанного в настоящей заявке, в качестве акарицида.
Согласно другому аспекту, настоящее изобретение относится к способу уничтожения клещей (например, пылевых клещей), включающему действие на указанных клещей эффективным количеством PVA соединения, описанного в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к способу регулирования (например, ограничения) популяции клещей (например, пылевых клещей), включающему действие на указанных клещей эффективным количеством PVA соединения, описанного в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к набору, включающему (а) PVA соединение, описанное в настоящей заявке, предпочтительно представленное в виде фармацевтической композиции в подходящем контейнере и/или в подходящей упаковке; и (b) инструкции по применению, например, письменные инструкции по введению соединения.
Согласно другому аспекту, настоящее изобретение относится к PVA соединению, которое может быть получено посредством способа синтеза, описанного в настоящей заявке, или способа, включающего способ синтеза, описанный в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к PVA соединению, полученному посредством способа синтеза, описанного в настоящей заявке, или способа, включающего способ синтеза, описанный в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к новым промежуточным соединениям, описанным в настоящей заявке, которые являются подходящими для применения в способах синтеза, описанных в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к применению указанных новых промежуточных соединений, описанных в настоящей заявке, в способах синтеза, описанных в настоящей заявке.
Специалистам в данной области техники очевидно, что признаки и предпочтительные варианты реализации одного аспекта изобретения также относятся к другим аспектам изобретения.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соединения
Согласно одному варианту реализации, настоящее изобретение относится конкретным пирувамидным соединениям, которые относятся к 3-[2-(2-ациламиноацетиламино)ацетиламино]-2-оксопропионамиду:
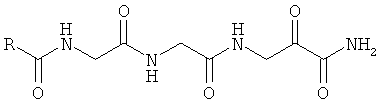
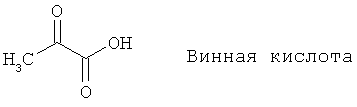
Все соединения согласно настоящему изобретению имеют пирувамидную связь (т.е. -C-C(=O)-C(=O)-N<), которая относится к винной кислоте (также называемой 2-оксопропановой кислотой) и пирувамиду (также называемому 2-оксопропионамидом).
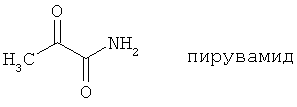
Таким образом, согласно одному аспекту, настоящее изобретение относится к соединениям, выбранным из соединений следующей формулы (которые в настоящей заявке для удобства вместе называются «PVA соединениями») и их солям, гидратам и сольватам (например, к их фармацевтически приемлемым солям, гидратам и сольватам), где R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11 и R12 являются такими, как определено в настоящей заявке:
 .
.
В зависимости от значений -R1 и -R2 атом углерода, к которому они присоединены, может являться хиральным и в указанном случае может независимо находиться в (R)- или (S)-конфигурации. Если иное не указано, предполагается, что включены обе конфигурации. Согласно предпочтительному варианту реализации изобретения, конфигурация представляет собой (S)-конфигурацию.
В зависимости от значений -R4 и -R5, атом углерода, к которому они присоединены, может являться хиральным и в указанном случае может независимо находиться в (R)- или (S)-конфигурации. Если иное не указано, предполагается, что включены обе конфигурации. Согласно предпочтительному варианту реализации изобретения, представляет собой (S)-конфигурацию.
В зависимости от значений -R7 и -R8, атом углерода, к которому они присоединены, может являться хиральным и в указанном случае может независимо находиться в (R)- или (S)-конфигурации. Если иное не указано, предполагается, что включены обе конфигурации.
В зависимости от значений -R1, -R2, -R4, -R5, -R7 и -R8, соединение может содержать один, два или три хиральных центра, что приводит к образованию энантиомеров или диастереоизомеров. Если иное не указано, предполагается, что включены все указанные энантиомеры или диастереоизомеры.
Некоторые варианты реализации изобретения включают следующее:
(1) Соединение, выбранное из соединений следующей формулы и их фармацевтически приемлемых солей, гидратов и сольватов:

где:
-R1 независимо представляет собой -Н или -R1A
-R1A независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным;
-R2 независимо представляет собой -Н или -R2A;
-R2A независимо представляет собой насыщенный алифатический C1-3алкил и является необязательно замещенным;
или -R1 и -R2 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C3-7циклоалкильное кольцо или насыщенное C3-7гетероциклическое кольцо, которое является необязательно замещенным;
-R3 независимо представляет собой -Н или -R3A;
-R3A независимо представляет собой насыщенный алифатический C1-3алкил и является необязательно замещенным;
-R4 независимо представляет собой -Н или -R4A;
-R4A независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным;
-R5 независимо представляет собой -Н или -R5A;
-R5A независимо представляет собой насыщенный алифатический C1-3алкил и является необязательно замещенным;
-R6 независимо представляет собой -Н или -R6A;
-R6A независимо представляет собой насыщенный алифатический C1-3алкил и является необязательно замещенным;
-R7 независимо представляет собой -Н, -R7A или -R7B;
-R7A независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным;
-R7B независимо представляет собой -L7B1-R7BB, -R7BB, -L7B2-O-R7BB или -L7B2-O-L7B1-R7BB;
-L7B1 - независимо представляет собой насыщенный алифатический C1-3алкилен;
-L7B2 - независимо представляет собой насыщенный алифатический C1-3алкилен;
-R7BB независимо представляет собой -R7BB1, -R7BB2, -R7BB3 или -R7BB4;
-R7BB1 независимо представляет собой фенил или нафтил и является необязательно замещенным;
-R7BB2 независимо представляет собой C5-10гетероарил и является необязательно замещенным;
-R7BB3 независимо представляет собой C3-7циклоалкил и является необязательно замещенным или является необязательно конденсированным с бензольным кольцом, которое является необязательно замещенным;
R7BB4 независимо представляет собой насыщенный C5-10циклоалкил с мостиком и является необязательно замещенным;
-R8 независимо представляет собой -Н или -R8A;
-R8A независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным;
или -R7 и -R8, совместно с атомом углерода, к которому они присоединены, образуют насыщенное C3-7циклоалкильное кольцо, насыщенное C5-10циклоалкильное кольцо с мостиком или неароматическое C3-7гетероциклическое кольцо, которое является необязательно замещенным;
-R9 независимо представляет собой -Н или -R9A;
-R9A независимо представляет собой насыщенный алифатический C1-4алкил и является необязательно замещенным;
или -R8 представляет собой -Н, и -R7 и -R9, совместно с атомом углерода и атомом азота, к которым они, соответственно, присоединены, образуют насыщенное C3-7гетероциклическое кольцо, которое является необязательно замещенным или которое является необязательно конденсированным с бензольным кольцом, которое является необязательно замещенным;
-R10 независимо представляет собой -R10A, -R10B, -R10C или -R10D;
-R10A независимо представляет собой фенил или нафтил и является необязательно замещенным;
-R10B независимо представляет собой C5-10гетероарил и является необязательно замещенным;
-R10C независимо представляет собой насыщенный C3-7циклоалкил и является необязательно замещенным;
-R10D независимо представляет собой неароматическое C3-10гетероциклил и является необязательно замещенным;
или -R9 и -R10, совместно с атомом азота и атомом углерода, к которым они, соответственно, присоединены, образуют неароматическое C5-7гетероциклическое лактамное кольцо, которое является необязательно замещенным или которое является необязательно конденсированным с бензольным кольцом, которое является необязательно замещенным;
-R11 независимо представляет собой -Н, -R11A или -R11B;
-R11A независимо представляет собой -RZ1, -RZ2, -RZ3, -RZ4, -RZ5, -LZ-RZ2, -L-RZ3, -LZ-RZ4 или -LZ-RZ5;
-RZ1 независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным;
каждый -RZ2 независимо представляет собой насыщенный C3-7циклоалкил и является необязательно замещенным или является необязательно конденсированным с бензольным кольцом, которое является необязательно замещенным;
каждый -RZ3 независимо представляет собой -RZ3A или -RZ3B;
каждый -RZ3A независимо представляет собой неароматический C3-7гетероциклил и является необязательно замещенным;
каждый -RZ3B независимо представляет собой насыщенный C5-10гетероциклил с мостиком и является необязательно замещенным;
каждый -RZ4 независимо представляет собой фенил или нафтил и является необязательно замещенным;
каждый -RZ5 независимо представляет собой C5-10гетероарил и является необязательно замещенным;
каждый -LZ - независимо представляет собой насыщенный алифатический C1-4алкилен;
-R11B независимо представляет собой -CRJ1RJ2-C(=O)-NRJ3RJ4;
-RJ1 независимо представляет собой -Н или насыщенный алифатический C1-4алкил;
-RJ2 независимо представляет собой -Н или насыщенный алифатический C1-4алкил;
-RJ3 независимо представляет собой -Н, насыщенный алифатический C1-4алкил, фенил или бензил;
-RJ4 независимо представляет собой -Н, насыщенный алифатический C1-4алкил, фенил или бензил;
or -NRJ3RJ4 независимо представляет собой C3-10гетероциклильную группу и является необязательно замещенным;
-R12 независимо представляет собой-Н или -R12A;
-R12A независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным;
или -NR11R12 независимо представляет собой C3-10гетероциклильную группу и является необязательно замещенным.
Во избежание неправильного толкования, обозначение «Cx-y» в таких терминах, как «C5-10гетероарил», «C3-7гетероциклическое кольцо», «C3-7гетероциклил» и т.д., относится к числу атомов в кольце, которые могут представлять собой атомы углерода или гетероатомы (например, N, О, S). Например, пиридил представляет собой пример C6гетероарильной группы, и пиперидино представляет собой пример C6гетероциклильной группы.
Во избежание неправильного толкования, «гетероарил» относится к группе, которая присоединена к остатку молекулы через атом, который является частью ароматического кольца, и которая содержит один или более гетероатомов (например, N, О, S), образующих часть ароматической системы колец. Например, пиридил представляет собой пример C6гетероарильной группы, и хинолил представляет собой пример C10гетероарильной группы. Напротив, «гетероциклил» относится к группе, которая присоединена к остатку молекулы через атом кольца, который не является частью ароматического кольца (т.е., кольцо полностью или частично является насыщенным), и система колец содержит один или более гетероатомов (например, N, О, S). Например, пиперидино представляет собой пример C6гетероциклильной группы.
Группы -R1 и -R2
(2) Соединение согласно (1), где -R1 независимо представляет собой -Н или -R1A.
(3) Соединение согласно (1), где -R1 независимо представляет собой -R1A.
(4) Соединение согласно (1), где -R1 независимо представляет собой -Н.
(5) Соединение согласно любому из (1)-(4), где -R2 независимо представляет собой -Н или -R2A.
(6) Соединение согласно любому из (1)-(4), где -R2 независимо представляет собой -R2A.
(7) Соединение согласно любому из (1)-(4), где -R2 независимо представляет собой -Н.
(8) Соединение согласно (1), где:
-R1 независимо представляет собой -Н или -R1A; и
-R2 независимо представляет собой -Н или -R2A.
(9) Соединение согласно (1), где:
-R1 независимо представляет собой -Н или -R1A; и
-R2 независимо представляет собой -Н.
(10) Соединение согласно (1), где:
-R1 независимо представляет собой -R1A; и
-R2 независимо представляет собой -Н.
(11) Соединение согласно (1), где:
-R1 независимо представляет собой -Н; и
-R2 независимо представляет собой -Н.
Группа -R1A
(12) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(13) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил.
(14) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(15) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
(16) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой -Me, -Et, -nPr, -iPr, -nBu, -iBu, -sBu или -tBu.
(17) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой насыщенный алифатический C3-4алкил.
(18) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой -nPr, -iPr, -nBu, -iBu, -sBu или -tBu.
(19) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой -iPr, -nBu, -iBu или -sBu.
(20) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой -iPr, -nBu, -iBu или -tBu.
(21) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой -iPr или -nBu.
(22) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой -iPr.
(23) Соединение согласно любому из (1)-(11), где -R1A, если присутствует, независимо представляет собой -nBu.
Группа -R2A
(24) Соединение согласно любому из (1)-(23), где -R2A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(25) Соединение согласно любому из (1)-(23), где -R2A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил.
(26) Соединение согласно любому из (1)-(23), где -R2A, если присутствует, независимо представляет собой -Me, -Et, -nPr или -iPr.
(27) Соединение согласно любому из (1)-(23), где -R2A, если присутствует, независимо представляет собой -Me или -Et.
(28) Соединение согласно любому из (1)-(23), где -R2A, если присутствует, независимо представляет собой -Me.
Группа -C(R1)(R2)-
(29) Соединение согласно (1), где -R1 и -R2 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C3-7циклоалкильное кольцо или неароматическое C3-7гетероциклическое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2.
(30) Соединение согласно (1), где -R1 и -R2 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C3-7циклоалкильное кольцо или неароматическое C3-7гетероциклическое кольцо.
(31) Соединение согласно (1), где -R1 и -R2 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C3-7циклоалкильное кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2.
(32) Соединение согласно (1), где -R1 и -R2 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C3-7циклоалкильное кольцо.
(33) Соединение согласно (1), где -R1 и -R2, совместно с атомом углерода, к которому они присоединены, образуют циклопропил, циклобутил, циклопентил или циклогексил, и являются необязательно замещенными, например, содержат один или более заместителей -RX2.
(34) Соединение согласно (1), где -R1 и -R2, совместно с атомом углерода, к которому они присоединены, образуют циклопропил, циклобутил, циклопентил или циклогексил.
(35) Соединение согласно (1), где -R1 и -R2, совместно с атомом углерода, к которому они присоединены, образуют неароматическое C3-7гетероциклическое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2.
(36) Соединение согласно (1), где -R1 и -R2, совместно с атомом углерода, к которому они присоединены, образуют неароматическое C3-7гетероциклическое кольцо.
Группа -R3
(37) Соединение согласно любому из (1)-(36), где -R3 независимо представляет собой -Н.
(38) Соединение согласно любому из (1)-(36), где -R3 независимо представляет собой -R3A.
Группа -R3A
(39) Соединение согласно любому из (1)-(38), где -R3A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(40) Соединение согласно любому из (1)-(38), где -R3A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил.
(41) Соединение согласно любому из (1)-(38), где -R3A, если присутствует, независимо представляет собой -Me, -Et, -nPr или -iPr.
(42) Соединение согласно любому из (1)-(38), где -R3A, если присутствует, независимо представляет собой -Me или -Et.
(43) Соединение согласно любому из (1)-(38), где -R3A, если присутствует, независимо представляет собой -Me.
группы -R4 и -R5
(44) Соединение согласно любому из (1)-(43), где -R4 независимо представляет собой -Н или -R4A.
(45) Соединение согласно любому из (1)-(43), где -R4 независимо представляет собой -R4A.
(46) Соединение согласно любому из (1)-(43), где -R4 независимо представляет собой -Н.
(47) Соединение согласно любому из (1)-(46), где -R5 независимо представляет собой -Н или -R5A.
(48) Соединение согласно любому из (1)-(46), где -R5 независимо представляет собой -R5A.
(49) Соединение согласно любому из (1)-(46), где -R5 независимо представляет собой -Н.
(50) Соединение согласно любому из (1)-(43), где:
-R4 независимо представляет собой -Н или -R4A; и
-R5 независимо представляет собой -Н или -R5A.
(51) Соединение согласно любому из (1)-(43), где:
-R4 независимо представляет собой -Н или -R4A; и
-R5 независимо представляет собой -Н.
(52) Соединение согласно любому из (1)-(43), где:
-R4 независимо представляет собой -R4A и
-R5 независимо представляет собой -Н.
(53) Соединение согласно любому из (1)-(43), где:
-R4 независимо представляет собой -Н; и
-R5 независимо представляет собой -Н.
Группа -R4A
(54) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(55) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил.
(56)Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(57) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
(58) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой -Me, -Et, -nPr, -iPr, -nBu, -iBu, -sBu или -tBu.
(59) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(60) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил.
(61) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой -Me, -Et, -nPr или -iPr.
(62) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой -Me, -nPr или -CH2C(=O)NH2.
(63) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой -Me или -nPr.
(64) Соединение согласно любому из (1)-(53), где -R4A, если присутствует, независимо представляет собой -Me.
Группа -R5A
(65) Соединение согласно любому из (1)-(64), где -R5A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(66) Соединение согласно любому из (1)-(64), где -R5A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил.
(67) Соединение согласно любому из (1)-(64), где -R5A, если присутствует, независимо представляет собой -Me, -Et, -nPr или -iPr.
(68) Соединение согласно любому из (1)-(64), где -R5A, если присутствует, независимо представляет собой -Me или -Et.
(69) Соединение согласно любому из (1)-(64), где -R5A, если присутствует, независимо представляет собой -Me.
Группа -R6
(70) Соединение согласно любому из (1)-(69), где -R6 независимо представляет собой -Н.
(71) Соединение согласно любому из (1)-(69), где -R6 независимо представляет собой -R6A.
Группа -R6A
(72) Соединение согласно любому из (1)-(71), где -R6A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(73) Соединение согласно любому из (1)-(71), где -R6A, если присутствует, независимо представляет собой насыщенный алифатический C1-3алкил.
(74) Соединение согласно любому из (1)-(71), где -R6A, если присутствует, независимо представляет собой -Me, -Et, -nPr или -iPr.
(75) Соединение согласно любому из (1)-(71), где -R6A, если присутствует, независимо представляет собой -Me или -Et.
(76) Соединение согласно любому из (1)-(71), где -R6A, если присутствует, независимо представляет собой -Me.
Группа -R7
(77) Соединение согласно любому из (1)-(76), где -R7 независимо представляет собой -R7A или -R7B.
(78) Соединение согласно любому из (1)-(76), где -R7 независимо представляет собой -R7A.
(79) Соединение согласно любому из (1)-(76), где -R7 независимо представляет собой -R7B.
(80) Соединение согласно любому из (1)-(76), где -R7 независимо представляет собой -Н.
Группа -R7A
(81) Соединение согласно любому из (1)-(80), где -R7A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(82) Соединение согласно любому из (1)-(80), где -R7A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил.
(83) Соединение согласно любому из (1)-(80), где -R7A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(84) Соединение согласно любому из (1)-(80), где -R7A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
(85) Соединение согласно любому из (1)-(80), где -R7A, если присутствует, независимо представляет собой -Me, -Et, -nPr, -iPr, -nBu, -sBu, -iBu или -tBu.
(86) Соединение согласно любому из (1)-(80), где -R7A, если присутствует, независимо представляет собой насыщенный алифатический C3-4алкил.
(87) Соединение согласно любому из (1)-(80), где -R7A, если присутствует, независимо представляет собой -nPr, -iPr, -nBu, -sBu, -iBu или -tBu.
(88) Соединение согласно любому из (1)-(80), где -R7A, если присутствует, независимо представляет собой -tBu.
Группа -R7B
(89) Соединение согласно любому из (1)-(88), где -R7B, если присутствует, независимо представляет собой -L7B1-R7BB, -L7B2-O-R7BB или -L7B2-O-L7B1-R7BB.
(90) Соединение согласно любому из (1)-(88), где -R7B, если присутствует, независимо представляет собой -L7B1-R7BB или -L7B2-O-L7B1-R7BB.
(91) Соединение согласно любому из (1)-(88), где -R7B, если присутствует, независимо представляет собой -L7B1-R7BB или -R7BB.
(92) Соединение согласно любому из (1)-(88), где -R7B, если присутствует, независимо представляет собой -L7B1-R7BB.
(93) Соединение согласно любому из (1)-(88), где -R7B, если присутствует, независимо представляет собой -L7B2-O-L7B1-R7BB.
(94) Соединение согласно любому из (1)-(88), где -R7B, если присутствует, независимо представляет собой -L7B2-O-R7BB.
(95) Соединение согласно любому из (1)-(88), где -R7B, если присутствует, независимо представляет собой -R7BB.
Группа -L7B1-
(96) Соединение согласно любому из (1)-(95), где -L7B1-, если присутствует, независимо представляет собой -CH2-, -CH(Me)-, -С(Me)2-, -CH2CH2- или -CH2CH2CH2-.
(97) Соединение согласно любому из (1)-(95), где -L7B1-, если присутствует, независимо представляет собой -CH2- или -CH2CH2-.
(98) Соединение согласно любому из (1)-(95), где -L7B1-, если присутствует, независимо представляет собой -CH2-.
(99) Соединение согласно любому из (1)-(95), где -L7B1-, если присутствует, независимо представляет собой -С(Me)2-.
Группа -L7B2-
(100) Соединение согласно любому из (1)-(99), где -L7B2-, если присутствует, независимо представляет собой -CH2-, -СН(Me)-, -С(Me)2-, -CH2CH2- или -CH2CH2CH2-.
(101) Соединение согласно любому из (1)-(99), где -L7B2-, если присутствует, независимо представляет собой -CH2- или -CH2CH2-.
(102) Соединение согласно любому из (1)-(99), где -L7B2-, если присутствует, независимо представляет собой -CH2-.
Группа -R7BB
(103) Соединение согласно любому из (1)-(102), где -R7BB, если присутствует, независимо представляет собой -R7BB1, -R7BB2 или -R7BB3.
(104) Соединение согласно любому из (1)-(102), где -R7BB, если присутствует, независимо представляет собой -R7BB1.
(105) Соединение согласно любому из (1)-(102), где -R7BB, если присутствует, независимо представляет собой -R7BB2.
(106) Соединение согласно любому из (1)-(102), где -R7BB, если присутствует, независимо представляет собой -R7BB3.
(107) Соединение согласно любому из (1)-(102), где -R7BB, если присутствует, независимо представляет собой -R7BB4.
Группа -R7BB1
(108) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(109) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me, -CF3, -Ph, -NH2, -NHMe, -NMe2, пирролидино, пиперидино, морфолино, пиперизино и N-(метил)пиперизино.
(110) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me и -Ph.
(111) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой фенил или нафтил.
(112) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(113) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me, -CF3, -Ph, -NH2, -NHMe, -NMe2, пирролидино, пиперидино, морфолино, пиперизино и М-(метил)пиперизино.
(114) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me и -Ph.
(115) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой фенил.
(116) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой нафтил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(117) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой нафтил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me, -CF3, -Ph, -NH2, -NHMe, -NMe2, пирролидино, пиперидино, морфолино, пиперизино и N-(метил)пиперизино.
(118) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой нафтил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me и -Ph.
(119) Соединение согласно любому из (1)-(107), где -R7BB1, если присутствует, независимо представляет собой нафтил.
Группа -R7BB2
(120) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой C5-10гетероарил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(121) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой C5-10гетероарил.
(122) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой C5-6гетероарил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(123) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой C5-6гетероарил.
(124) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, триазолил (например, 1Н-[1,2,3]триазолил, 2Н-[1,2,3]триазолил, 4Н-[1,2,4]триазолил, 1Н-[1,2,4]триазолил), оксадиазолил (например, [1,2,3]оксадиазолил, фуразанил, [1,3,4]оксадиазолил, [1,2,4]оксадиазолил), тиадиазолил (например, [1,2,3]тиадиазолил, [1,2,5]тиадиазолил, [1,3,4]тиадиазолил, [1,2,4]тиадиазолил), пиридил, пиримидинил, пиразинил, пиридазинил или триазинил (например, [1,3,5]-триазинил) и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(125) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, пиразинил или пиридазинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(126) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, пиразинил или пиридазинил.
(127) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой пиридил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(128) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой пиридил.
(129) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой C9-10гетероарил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(130) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой C9-10гетероарил.
(131) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой хинолинил, изохинолинил или индолил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(132) Соединение согласно любому из (1)-(119), где -R7BB2, если присутствует, независимо представляет собой хинолинил, изохинолинил или индолил.
Группа -R7BB3
(133) Соединение согласно любому из (1)-(132), где -R7BB3, если присутствует, независимо представляет собой C3-7циклоалкил и является необязательно замещенным, например, содержит один или более заместителей -RX2, или является необязательно конденсированным с бензольным кольцом, которое необязательно содержит один или более заместителей -RX3.
(134) Соединение согласно любому из (1)-(132), где -R7BB3, если присутствует, независимо представляет собой C3-7циклоалкил и является необязательно замещенным, например, содержит один или более заместителей -RX2 или является необязательно конденсированным с бензольным кольцом.
(135) Соединение согласно любому из (1)-(132), где -R7BB3, если присутствует, независимо представляет собой C3-7циклоалкил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(136) Соединение согласно любому из (1)-(132), где -R7BB3, если присутствует, независимо представляет собой циклопропил, циклобутил, циклопентил, циклогексил или циклогептил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(137) Соединение согласно любому из (1)-(132), где -R7BB3, если присутствует, независимо представляет собой циклопропил, циклобутил, циклопентил, циклогексил или циклогептил.
(138) Соединение согласно любому из (1)-(132), где -R7BB3, если присутствует, независимо представляет собой C3-6циклоалкил и является необязательно конденсированным с бензольным кольцом.
(139) Соединение согласно любому из (1)-(132), где -R7BB3, если присутствует, независимо представляет собой циклопропил, циклобутил, циклопентил, циклогексил или циклогептил и является необязательно конденсированным с бензольным кольцом.
(140) Соединение согласно любому из (1)-(132), где -R7BB3, если присутствует, независимо представляет собой циклопентил, конденсированный с бензольным кольцом; как, например, в индан-2-иле.

Группа -R7BB4
(141) Соединение согласно любому из (1)-(140), где -R7BB4, если присутствует, независимо представляет собой насыщенный C5-10циклоалкил с мостиком и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(142) Соединение согласно любому из (1)-(140), где -R7BB4, если присутствует, независимо представляет собой насыщенный C5-10циклоалкил с мостиком.
(143) Соединение согласно любому из (1)-(140), где -R7BB4, если присутствует, независимо представляет собой бицикло[1.1.1]пентил или адамантил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(144) Соединение согласно любому из (1)-(140), где -R7BB4, если присутствует, независимо представляет собой бицикло[1,1,1]пентил (например, насыщенную C5циклоалкильную группу с мостиком) или адамантил (например, насыщенную C10циклоалкильную группу с мостиком).
(145) Соединение согласно любому из (1)-(140), где -R7BB4, если присутствует, независимо представляет собой адамантил.


Группа -R8
(146) Соединение согласно любому из (1)-(145), где -R8 независимо представляет собой -Н.
(147) Соединение согласно любому из (1)-(145), где -R8 независимо представляет собой -R8A.
Группа -R8A
(148) Соединение согласно любому из (1)-(147), где -R8A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(149) Соединение согласно любому из (1)-(147), где -R8A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил.
(150) Соединение согласно любому из (1)-(147), где -R8A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(151) Соединение согласно любому из (1)-(147), где -R8A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
(152) Соединение согласно любому из (1)-(147), где -R8A, если присутствует, независимо представляет собой -Me, -Et, -nPr, -iPr, -nBu, -sBu, -iBu или -tBu.
(153) Соединение согласно любому из (1)-(147), где -R8A, если присутствует, независимо представляет собой -Me, -Et, -nPr или -iPr.
(154) Соединение согласно любому из (1)-(147), где -R8A, если присутствует, независимо представляет собой -Me.
Группа -C(R7)(R8)-
(155) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C3-7циклоалкильное кольцо, насыщенное C5-10циклоалкильное кольцо с мостиком или неароматическое C3-7гетероциклическое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2.
(156) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C3-7циклоалкильное кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2.
(157) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C3-7циклоалкильное кольцо.
(158) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют циклопропил, циклобутил, циклопентил или циклогексил, и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(159) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют циклопропил, циклобутил, циклопентил или циклогексил.
(160) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют циклогексил.
(161) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C5-10циклоалкильное кольцо с мостиком, которое является необязательно замещенным, например, содержит один или более заместителей -RX2.
(162) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют насыщенное C5-10циклоалкильное кольцо с мостиком.
(163) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют неароматическое C3-7гетероциклическое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2.
(164) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют неароматическое C3-7гетероциклическое кольцо.
(165) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют неароматическое C5-7гетероциклическое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2.
(166) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют неароматическое C5-7гетероциклическое кольцо.
(167) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют неароматическое C6гетероциклическое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2.
(168) Соединение согласно любому из (1)-(76), где -R7 и -R8 совместно с атомом углерода, к которому они присоединены, образуют неароматическое C6гетероциклическое кольцо.
Группа -R9
(169) Соединение согласно любому из (1)-(168), где -R9 независимо представляет собой -Н.
(170) Соединение согласно любому из (1)-(168), где -R9 независимо представляет собой -R9A.
Группа -R9A
(171) Соединение согласно любому из (1)-(170), где -R9A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(172) Соединение согласно любому из (1)-(170), где -R9A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
(173) Соединение согласно любому из (1)-(170), где -R9A, если присутствует, независимо представляет собой -Me, -Et, -nPr, -iPr, -nBu, -sBu, -iBu или -tBu.
(174) Соединение согласно любому из (1)-(170), где -R9A, если присутствует, независимо представляет собой -Me, -Et, -nPr или -iPr.
(175) Соединение согласно любому из (1)-(170), где -R9A, если присутствует, независимо представляет собой -Me.
Группа -NR9-C(R7)(R8)-
(176) Соединение согласно любому из (1)-(76), где -R8 представляет собой -Н; и -R7 и -R9, совместно с атомом углерода и атомом азота, к которым они, соответственно, присоединены, образуют неароматическое C3-7гетероциклическое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2, или которое является необязательно конденсированным с бензольным кольцом, которое необязательно содержит один или более заместителей -RX3.
(177) Соединение согласно любому из (1)-(76), где -R8 представляет собой -Н; и -R7 и -R9, совместно с атомом углерода и атомом азота, к которым они, соответственно, присоединены, образуют неароматическое C3-7гетероциклическое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2, или которое является необязательно конденсированным с бензольным кольцом.
(178) Соединение согласно любому из (1)-(76), где -R8 представляет собой -Н; и -R7 и -R9, совместно с атомом углерода и атомом азота, к которым они, соответственно, присоединены, образуют пирролидиновое кольцо или пиперидиновое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2, или которое является необязательно конденсированным с бензольным кольцом.
(179) Соединение согласно любому из (1)-(76), где -R8 представляет собой -Н; и -R7 и -R9, совместно с атомом углерода и атомом азота, к которым они, соответственно, присоединены, образуют пирролидиновое кольцо или пиперидиновое кольцо, которое является необязательно конденсированным с бензольным кольцом.
(180) Соединение согласно любому из (1)-(76), где -R8 представляет собой -Н; и -R7 и -R9, совместно с атомом углерода и атомом азота, к которым они, соответственно, присоединены, образуют пирролидиновое кольцо; как, например, в следующей формуле:
 .
.
(181) Соединение согласно любому из (1)-(76), где -R8 представляет собой -Н; и -R7 и -R9, совместно с атомом углерода и атомом азота, к которым они, соответственно, присоединены, образуют пиперидиновое кольцо, которое является конденсированным с бензольным кольцом; как, например, в следующей формуле:
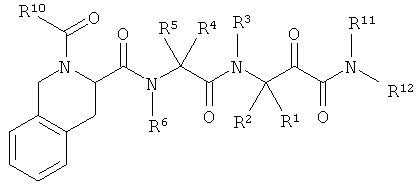 .
.
Группа R10-C(=O)-N(R9)-
(182) Соединение согласно любому из (1)-(168), где -R9 и -R10, совместно с атомом азота и атомом углерода, к которым они, соответственно, присоединены, образуют неароматическое C5-7гетероциклическое лактамное кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2, или которое является необязательно конденсированным с бензольным кольцом, которое является необязательно замещенным, например, содержит один или более заместителей -RX3.
(183) Соединение согласно любому из (1)-(168), где -R9 и -R10, совместно с атомом азота и атомом углерода, к которым они, соответственно, присоединены, образуют пирролидин-2-оновое кольцо или пиперидин-2-оновое кольцо, которое является необязательно замещенным, например, содержит один или более заместителей -RX2, или которое является необязательно конденсированным с бензольным кольцом, которое является необязательно замещенным, например, содержит один или более заместителей -RX3.
(184) Соединение согласно любому из (1)-(168), где -R9 и -R10, совместно с атомом азота и атомом углерода, к которым они, соответственно, присоединены, образуют пирролидин-2-оновое кольцо или пиперидин-2-оновое кольцо, которое является конденсированным с бензольным кольцом.
(185) Соединение согласно любому из (1)-(168), где -R9 и -R10, совместно с атомом азота и атомом углерода, к которым они, соответственно, присоединены, образуют пирролидин-2-оновое кольцо, которое является конденсированным с бензольным кольцом; например, где группа -N(R9)-C(=O)-R10 представляет собой следующую группу:

как, например, в следующей формуле:
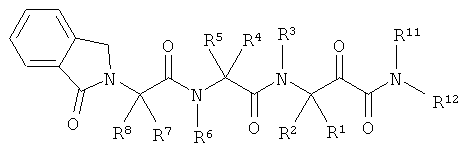 .
.
(186) Соединение согласно любому из (1)-(168), где -R9 и -R10, совместно с атомом углерода и атомом азота, к которым они, соответственно, присоединены, образуют пирролидин-2-оновое кольцо; например, где группа -N(R9)-C(=O)-R10 представляет собой следующую группу:

как, например, в следующей формуле:
 .
.
Некоторые предпочтительные комбинации
(187) Соединение согласно (1), где: -R2 представляет собой -Н; -R3 представляет собой -Н; -R5 представляет собой -Н; -R6 представляет собой -Н; например, как показано далее:

(188) Соединение согласно (187), где атом углерода, к которому -R4 и -R5 присоединены, имеет конфигурацию, как показано в следующей формуле:
 .
.
(189) Соединение согласно (187), где атом углерода, к которому -R4 и -R5 присоединены, и атом углерода, к которому -R1 и -R2 присоединены, имеют конфигурацию, как показано в следующей формуле:
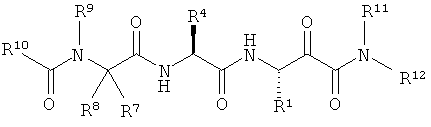
(190) Соединение согласно любому из (187)-(189), где: -R1 представляет собой -iPr, и -R4 представляет собой -Me; например, как показано далее:
 .
.
(191) Соединение согласно (1), где: -R2 представляет собой -Н; -R3 представляет собой -Н; -R5 представляет собой -Н; -R6 представляет собой -Н; -R8 представляет собой -Н и -R9 представляет собой -Н; например, как показано далее:
 .
.
(192) Соединение согласно (191), где атом углерода, к которому -R4 и -R5 присоединены, имеет конфигурацию, как показано в следующей формуле:
 .
.
(193) Соединение согласно (191), где атом углерода, к которому -R4 и -R5 присоединены, и атом углерода, к которому -R1 и -R2 присоединены, имеют конфигурацию, как показано в следующей формуле:
 .
.
(194) Соединение согласно (191), где атом углерода, к которому -R4 и -R5 присоединены, атом углерода, к которому -R1 и -R2 присоединены, и атом углерода, к которому -R7 и -R8 присоединены, имеют конфигурацию, как показано в следующей формуле:
 .
.
(195) Соединение согласно (191), где атом углерода, к которому -R4 и -R5 присоединены, атом углерода, к которому -R1 и -R2 присоединены, и атом углерода, к которому -R7 и -R8 присоединены, имеют конфигурацию, как показано в следующей формуле:
 .
.
(196) Соединение согласно любому из (191)-(195), где: -R1 представляет собой -iPr, и -R4 представляет собой -Me; например, как показано далее:
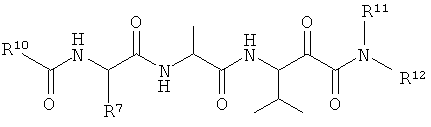 .
.
(197) Соединение согласно любому из (191)-(195), где -R7 представляет собой -CH2-R7BB; например, как показано далее:
 .
.
(198) Соединение согласно любому из (191)-(195), где -R7 представляет собой -CH2-Ph; например, как показано далее:
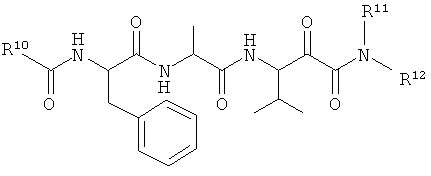 .
.
(199) Соединение согласно любому из (191)-(195), где -R7 представляет собой -R7A; например, как показано далее:
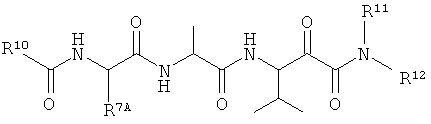 .
.
(200) Соединение согласно любому из (191)-(195), где -R7 представляет собой -tBu; например, как показано далее:
 .
.
(201) Соединение согласно любому из (191)-(195), где -R7 представляет собой -R7BB; например, как показано далее:
 .
.
(202) Соединение согласно любому из (191)-(195), где -R7 представляет собой -tBu; например, как показано далее:
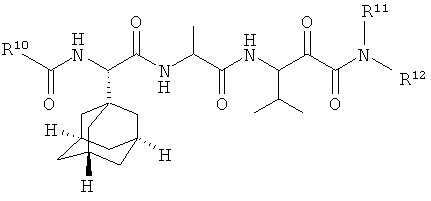 .
.
Группа -R10
(203) Соединение согласно любому из (1)-(181) и (187)-(202), где -R10 независимо представляет собой -R10A, -R10B или -R10C.
(204) Соединение согласно любому из (1)-(181) и (187)-(202), где -R10 независимо представляет собой -R10A, -R10B или -R10D.
(205) Соединение согласно любому из (1)-(181) и (187)-(202), где -R10 независимо представляет собой -R10A или -R10B.
(206) Соединение согласно любому из (1)-(181) и (187)-(202), где -R10 независимо представляет собой -R10A.
(207) Соединение согласно любому из (1)-(181) и (187)-(202), где -R10 независимо представляет собой -R10B.
(208) Соединение согласно любому из (1)-(181) и (187)-(202), где -R10 независимо представляет собой -R10C.
(209) Соединение согласно любому из (1)-(181) и (187)-(202), где -R10 независимо представляет собой -R10D.
Группа -R10A
(210) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(211) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
-F, -Cl, -Br, -I, -CF3,
-С(=O)ОН, -С(=O)O(C1-4алкила),
-S(=O)2(C1-4алкила),
фенила, -O-фенила,
-NH2, -NH(C1-4алкила), -N(C1-4алкила)2,
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино,
-O-CH2CH2-NH2, -O-CH2CH2-NH(C1-4алкила), -O-CH2CH2-N(C1-4алкила)2,
-O-CH2CH2-пирролидино, -O-CH2CH2-пиперидино, -O-CH2CH2-морфолино,
-O-CH2CH2-пиперизино, -O-CH2CH2-{N-(C1-4алкил)-пиперизино},
-O-CH2-имидазол-2-ила и -O-CH2-{N-(C1-4алкил)имидазол-2-ила}.
(212) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
фенила, -O-фенила,
-NH2, -NH(C1-4алкила), -N(C1-4алкила)2,
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино,
-O-CH2CH2-NH2, -O-CH2CH2-NH(C1-4алкила), -O-CH2CH2-N(C1-4алкила)2,
-O-CH2CH2-пирролидино, -O-CH2CH2-пиперидино, -O-CH2CH2-морфолино,
-O-CH2CH2-пиперизино, -O-CH2CH2-{N-(C1-4алкил)-пиперизино},
-O-CH2-имидазол-2-ила и -O-CH2-{N-(C1-4алкил)-имидазол-2-ила}.
(213) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
-F, -Cl, -Br, -I, -CF3,
-С(=O)ОН, -С(=O)O(C1-4алкила),
-S(=O)2(C1-4алкила),
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино,
-O-CH2-имидазол-2-ила и -O-CH2-{N-(C1-4алкил)имидазол-2-ила}.
(214) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(215) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
-F, -Cl, -Br, -I, -CF3,
-С(=O)ОН, -С(=O)O(C1-4алкила),
-S(=O)2(C1-4алкила), фенила, -O-фенила,
-NH2, -NH(C1-4алкила), -N(C1-4алкила)2,
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино,
-O-CH2CH2-NH2, -O-CH2CH2-NH(C1-4алкила), -O-CH2CH2-N(C1-4алкила)2,
-O-CH2CH2-пирролидино, -О-CH2CH2-пиперидино, -O-CH2CH2-морфолино,
-O-CH2CH2-пиперизино, -O-CH2CH2-{N-(C1-4алкил)пиперизино},
-O-CH2-имидазол-2-ила и -O-CH2-{N-(C1-4алкил)имидазол-2-ила}.
(216) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
фенила, -O-фенила,
-NH2, -NH(C1-4алкила), -N(C1-4алкила)2,
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино,
-O-CH2CH2-NH2, -O-CH2CH2-NH(C1-4алкила), -O-CH2CH2-N(C1-4алкила)2,
-O-CH2CH2-пирролидино, -O-CH2CH2-пиперидино, -O-CH2CH2-морфолино,
-О-CH2CH2-пиперизино, -O-CH2CH2-{N(C1-4алкил)пиперизино},
-O-CH2-имидазол-2-ила и -O-CH2-{N-(C1-4алкил)имидазол-2-ила}.
(217) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
-F, -Cl, -Br, -I, -CF3,
-С(=O)ОН, -С(=O)O(C1-4алкила),
-S(=O)2(C1-4алкила),
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино,
-O-CH2-имидазол-2-ила и -O-CH2-{N-(C1-4алкил)имидазол-2-ила}.
(218) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой фенил.
(219) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A,, если присутствует, независимо представляет собой нафтил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(220) Соединение согласно любому из (1)-(181) и (187)-(209), где -R10A, если присутствует, независимо представляет собой нафтил.
Группа -R10B
(221) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой C5-10гетероарил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(222) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, триазолил (например, 1Н-[1,2,3]триазолил, 2Н-[1,2,3]триазолил, 4Н-[1,2,4]триазолил, 1Н-[1,2,4]триазолил), оксадиазолил (например, [1,2,3]оксадиазолил, фуразанил, [1,3,4]оксадиазолил, [1,2,4]оксадиазолил), тиадиазолил (например, [1,2,3]тиадиазолил, [1,2,5]тиадиазолил, [1,3,4]тиадиазолил, [1,2,4]тиадиазолил), пиридил, пиримидинил, пиразинил, пиридазинил, триазинил (например, [1,3,5]-триазинил), индолил, изоиндолил, индазолил, бензофуранил, изобензофуранил, бензотиенил, изобензотиенил, бензимидазолил, бензотиазолил, бензоксазолил, бензоизоксазолил, хинолинил, изохинолинил, циннолинил, хиназолинил, фталазинил или хиноксалинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(223) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой C5-6гетероарил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(224) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой C5-6гетероарил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
насыщенного алифатического C1-4алкила,
-NH2, -NH(C1-4алкила), -N(C1-4алкила)2,
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино,
-NHC(=O)(C1-4алкила), и
-OH.
(225) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой C5-6гетероарил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
-NH2, -NH(C1-4алкила), -N(C1-4алкила)2,
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино,
-NHC(=O)(C1-4алкила), и
-OH.
(226) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, пиразинил или пиридазинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(227) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой пиразолил, пиридил, пиримидинил, пиразинил или пиридазинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(228) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой пиридил, пиримидинил, пиразинил или пиридазинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(229) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой пиридил, пиримидинил или пиразинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(230) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой пиридил, пиримидинил или пиразинил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
-NH2, -NH(C1-4алкила), -N(C1-4алкила)2,
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино,
-NHC(=O)(C1-4алкила), и
-ОН.
(231) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой пиридил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(232) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой пиридил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
-NH2, -NH(C1-4алкила), -N(C1-4алкила)2,
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино,
-NHC(=O)(C1-4алкила), и
-OH.
(233) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой пиразолил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(234) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой пиразолил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из: насыщенного алифатического C1-4алкила.
(235) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой C9-10гетероарил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(236) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой индолил, изоиндолил, индазолил, бензофуранил, изобензофуранил, бензотиенил, изобензотиенил, бензимидазолил, бензотиазолил, бензоксазолил, бензоизоксазолил, хинолинил, изохинолинил, циннолинил, хиназолинил, фталазинил или хиноксалинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(237) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой индазолил, бензимидазолил, бензотиазолил, хинолинил или изохинолинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(238) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой индазолил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(239) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой бензимидазолил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(240) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой бензотиазолил, хинолинил или изохинолинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(241) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой бензотиазолил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(242) Соединение согласно любому из (1)-(181) и (187)-(220), где -R10B, если присутствует, независимо представляет собой хинолинил или изохинолинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
Группа -R10C
(243) Соединение согласно любому из (1)-(181) и (187)-(242), где -R10C, если присутствует, независимо представляет собой насыщенный C3-7циклоалкил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(244) Соединение согласно любому из (1)-(181) и (187)-(242), где -R10C, если присутствует, независимо представляет собой циклопропил, циклобутил, циклопентил или циклогексил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(245) Соединение согласно любому из (1)-(181) и (187)-(242), где -R10C, если присутствует, независимо представляет собой циклопропил, циклобутил, циклопентил или циклогексил.
(246) Соединение согласно любому из (1)-(181) и (187)-(242), где -R10C, если присутствует, независимо представляет собой циклопентил или циклогексил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(247) Соединение согласно любому из (1)-(181) и (187)-(242), где -R10C если присутствует, независимо представляет собой циклопентил или циклогексил.
Группа -R10D
(248) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D, если присутствует, независимо представляет собой неароматический C3-10гетероциклил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(249) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D, если присутствует, независимо представляет собой неароматический C3-10гетероциклил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(250) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D, если присутствует, независимо представляет собой неароматический C3-10гетероциклил.
(251) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D, если присутствует, независимо представляет собой неароматический C5-7гетероциклил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(252) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D, если присутствует, независимо представляет собой неароматический C5-7гетероциклил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(253) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D, если присутствует, независимо представляет собой неароматический C5-7гетероциклил.
(254) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пирролидинил, пиперидинил, морфолинил, пиперизинил, тетрагидрофуранил, тетрагидропиранил, диоксанил, азепанил или диазепанил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(255) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пирролидинил, пиперидинил, морфолинил, пиперизинил, тетрагидрофуранил, тетрагидропиранил, диоксанил, азепанил или диазепанил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(256) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пирролидинил, пиперидинил, морфолинил, пиперизинил, тетрагидрофуранил, тетрагидропиранил, диоксанил, азепанил или диазепанил.
(257) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пирролидинил, пиперидинил, морфолинил, пиперизинил, тетрагидрофуранил, тетрагидропиранил или диоксанил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(258) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пирролидинил, пиперидинил, морфолинил, пиперизинил, тетрагидрофуранил, тетрагидропиранил или диоксанил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(259) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пирролидинил, пиперидинил, морфолинил, пиперизинил, тетрагидрофуранил, тетрагидропиранил или диоксанил.
(260) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперидинил, морфолинил или пиперизинил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(261) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперидинил, морфолинил или пиперизинил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(262) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперидинил, морфолинил или пиперизинил.
(263) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперидинил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(264) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперидинил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(265) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперидин-4-ил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(266) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперидин-4-ил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(267) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой N-(C1-4алкил)пиперидин-4-ил, например, N-(метил)пиперидин-4-ил или N-(изопропил)пиперидин-4-ил, как показано далее:
 и
и  .
.
(268) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой N,N-(ди-C1-4алкил)пиперидин-4-ил, например, N,N-(диметил)пиперидин-4-ил, как показано далее:
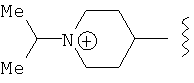 .
.
(269) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперизинил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(270) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперизинил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(271) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперизино и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(272) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой пиперизино и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(273) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой N-(C1-4алкил)пиперизино, например, N-(метил)пиперизино, как показано далее:
 .
.
(274) Соединение согласно любому из (1)-(181) и (187)-(247), где -R10D независимо представляет собой N,N-(ди-C1-4алкил)пиперизино, например, N,N-(диметил)пиперизино, как показано далее:
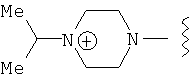 .
.
Во избежание неправильного толкования, предполагается, что катионная группа, например, группа, содержащая четвертичный азот, например, N,N-(диметил)пиперидин-4-ил и N,N-(диметил)пиперизино, показанные выше, сопровождается соответствующим противоионом, например, галогенанионом, например, Cl-.
Группа-R11
(275) Соединение согласно любому из (1)-(274), где -R11 независимо представляет собой -Н или -R11A.
(276) Соединение согласно любому из (1)-(274), где -R11 независимо представляет собой -R11A.
(277) Соединение согласно любому из (1)-(274), где -R11 независимо представляет собой -R11B.
(278) Соединение согласно любому из (1)-(274), где -R11 независимо представляет собой -Н.
Группа -R11A
(279) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -RZ1, -RZ2, -RZ3, -RZ4, -RZ5, -LZ-RZ2, -LZ-RZ3, -LZ-RZ4 или -LZ-RZ5.
(280) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -RZ1, -RZ2, -RZ3, -RZ4, -RZ5, -LZ-RZ4 или -LZ-RZ5.
(281) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -RZ1, -RZ2, -RZ3, -RZ4, -LZ-RZ4 или -LZ-RZ5.
(282) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -RZ1, -RZ2, -LZ-RZ4 или -LZ-RZ5.
(283) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -RZ2 или -LZ-RZ4.
(284) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -RZ1.
(285) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -RZ2.
(286) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -RZ3.
(287) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -RZ24.
(288) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -LZ-RZ2.
(289) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -LZ-RZ3.
(290) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -LZ-RZ4.
(291) Соединение согласно любому из (1)-(278), где -R11A, если присутствует, независимо представляет собой -LZ-RZ5.
Группа -RZ1
(292) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(293) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил.
(294) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(295) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил, -CH2CH2-ОМе, -CH2CH2-пирролидино, -CH2CH2-пиперизино или -CH2CH2-(N-метил)пиперизино.
(296) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил, -CH2CH2-ОМе или -CH2CH2-пирролидино.
(297) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой -Me, -iPr, -CH2CH2-ОМе, -CH2CH2-пирролидино, -CH2CH2-пиперизино или -CH2CH2-(N-метил)пиперизино.
(298) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой -iPr, -CH2CH2-ОМе или -CH2CH2-пирролидино.
(299) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
(300) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой -Me, -Et, -nPr, -iPr, -nBu, -iBu, -sBu или -tBu.
(301) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой -Me.
(302) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой насыщенный алифатический C3-4алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(303) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой насыщенный алифатический C3-4алкил.
(304) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой -nPr, -iPr, -nBu, -iBu, -sBu или -tBu.
(305) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой -iPr, -nBu, -sBu или -tBu.
(306) Соединение согласно любому из (1)-(291), где -RZ1, если присутствует, независимо представляет собой -iPr.
Группа -RZ2
(307) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой насыщенный C3-7циклоалкил и является необязательно замещенным, например, содержит один или более заместителей -RX2, или является необязательно конденсированным с бензольным кольцом, которое необязательно содержит один или более заместителей -RX3.
(308) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой насыщенный C3-7циклоалкил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(309) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой насыщенный C3-7циклоалкил.
(310) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой насыщенный C3-7циклоалкил и является конденсированным с бензольным кольцом.
(311) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклопропил, циклобутил, циклопентил или циклогексил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(312) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклопропил, циклобутил, циклопентил или циклогексил.
(313) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклопентил или циклогексил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(314) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклопентил или циклогексил.
(315) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклопентил или циклогексил и является конденсированным с бензольным кольцом.
(316) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклопентил и является конденсированным с бензольным кольцом, например, следующую группу:
 .
.
(317) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклогексил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(318) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклогексил.
(319) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклопропил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(320) Соединение согласно любому из (1)-(306), где каждый -RZ2, если присутствует, независимо представляет собой циклопропил.
Группа -RZ3
(321) Соединение согласно любому из (1)-(320), где каждый -RZ3, если присутствует, независимо представляет собой -RZ3A.
(322) Соединение согласно любому из (1)-(320), где каждый -RZ3, если присутствует, независимо представляет собой -RZ3B.
Группа -RZ3A
(323) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо представляет собой неароматический C3-7гетероциклил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(324) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо представляет собой неароматический C3-7гетероциклил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(325) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо представляет собой пирролидинил, пиперидинил, пиперизинил, морфолинил, тетрагидрофуранил, тетрагидропиранил, диоксанил, азепанил или диазепанил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(326) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо представляет собой пирролидинил, пиперидинил, пиперизинил, морфолинил, тетрагидрофуранил, тетрагидропиранил, диоксанил, азепанил или диазепанил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(327) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо представляет собой пирролидинил, пиперидинил, пиперизинил или тетрагидропиранил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(328) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо представляет собой пирролидинил, пиперидинил, пиперизинил или тетрагидропиранил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(329) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо выбран из:
 ,
,  ,
,
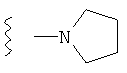 и
и  .
.
(330) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо представляет собой пиперидинил или тетрагидропиранил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(331) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо представляет собой пиперидинил или тетрагидропиранил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(332) Соединение согласно любому из (1)-(322), где каждый -RZ3A, если присутствует, независимо выбран из:
 ,
,  ,
,
Группа -RZ3B
(333) Соединение согласно любому из (1)-(332), где каждый -RZ3B, если присутствует, независимо представляет собой насыщенный C5-10гетероциклил с мостиком и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(334) Соединение согласно любому из (1)-(332), где каждый -RZ3B, если присутствует, независимо представляет собой насыщенный C5-10гетероциклил с мостиком и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(335) Соединение согласно любому из (1)-(332), где каждый -RZ3B, если присутствует, независимо представляет собой:
 .
.
Группа -RZ4
(336) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(337) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me, -Et, -nPr, -iPr, -tBu, -C(=O)OH, -C(=O)OMe, -C(=O)OEt, -C(=O)O(nPr), -C(=O)O(iPr), -C(=O)O(tBu), -OH, -OMe, -OEt, -CF3, -OCF3, -CN, -S(=O)2NH2, -S(=O)2NHMe, -C(=O)NH2, -C(=O)NHMe, пиперизино, N-(метил)пиперизино, -CH2-NMe;, -СН2-пиперидино, -NHC(=O)NH2 и -OCH2O-.
(338) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой фенил или нафтил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me, -Et, -C(=O)OH, -C(=O)OMe, -C(=O)OEt, -ОН, -ОМе, -OEt и -OCH2O-.
(339) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(340) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо выбран из:
 ,
,  и
и  .
.
(341) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me, -Et, -nPr, -iPr, -tBu, -C(=O)OH, -C(=O)OMe, -C(=O)OEt, -C(=O)O(nPr), -C(=O)O(iPr), -C(=O)O(tBu), -ОН, -ОМе, -OEt, -CF3, -OCF3, -CN, -S(=O)2NH2, -S(=O)2NHMe, -C(=O)NH2, -C(=O)NHMe, пиперизино, N-(метил)пиперизино, -CH2-NMe2, -CH2-пиперидино, -NHC(=O)NH2 и -OCH2O-.
(342) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой фенил и необязательно содержит в мета- или пара-положении заместитель, независимо выбранный из -С(=O)ОН, -С(=O)ОМе, -C(=O)OEt, -C(=O)O(nPr), -C(=O)O(iPr), -C(=O)O(tBu), -S(=O)2NH2, -S(=O)2NHMe, -C(=O)NH2, -C(=O)NHMe, пиперизино, N-(метил)-пиперизино, -CH2-NMe2, -CH2-пиперидино или -NHC(=O)NH2.
(343) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой фенил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из -F, -Cl, -Br, -I, -Me, -Et, -C(=O)OH, -C(=O)OMe, -C(=O)OEt, -ОН, -ОМе, -OEt и -OCH2O-.
(344) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой фенил.
(345) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой нафтил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(346) Соединение согласно любому из (1)-(335), где каждый -RZ4, если присутствует, независимо представляет собой нафтил.
Группа -RZ5
(347) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой C5-10гетероарил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(348) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой C5-10гетероарил.
(349) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, триазолил (например, 1Н-[1,2,3]триазолил, 2Н-[1,2,3]триазолил, 4Н-[1,2,4]триазолил, 1Н-[1,2,4]триазолил), оксадиазолил (например, [1,2,3]оксадиазолил, фуразанил, [1,3,4]оксадиазолил, [1,2,4]оксадиазолил), тиадиазолил (например, [1,2,3]тиадиазолил, [1,2,5]тиадиазолил, [1,3,4]тиадиазолил, [1,2,4]тиадиазолил), пиридил, пиримидинил, пиразинил, пиридазинил, триазинил (например, [1,3,5]-триазинил), индолил, изоиндолил, индазолил, бензофуранил, изобензофуранил, бензотиенил, изобензотиенил, бензимидазолил, бензотиазолил, бензоксазолил, бензоизоксазолил, хинолинил, изохинолинил, циннолинил, хиназолинил, фталазинил или хиноксалинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(350) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, пиразинил, пиридазинил, индолил, изоиндолил, индазолил, бензофуранил, изобензофуранил, бензотиенил, изобензотиенил, бензимидазолил, бензотиазолил, бензоксазолил, бензоизоксазолил, хинолинил, изохинолинил, циннолинил, хиназолинил, фталазинил или хиноксалинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(351) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, пиразинил, пиридазинил, индолил, изоиндолил, индазолил, бензофуранил, изобензофуранил, бензотиенил, изобензотиенил, бензимидазолил, бензотиазолил, бензоксазолил, бензоизоксазолил, хинолинил, изохинолинил, циннолинил, хиназолинил, фталазинил или хиноксалинил.
(352) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой C5-6гетероарил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(353) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой C5-6гетероарил.
(354) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, пиразинил или пиридазинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(355) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой фуранил, тиенил, пирролил, имидазолил, пиразолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пиридил, пиримидинил, пиразинил или пиридазинил.
(356) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой пиридил, пиримидинил, пиразинил или пиридазинил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(357) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой пиридил, пиримидинил, пиразинил или пиридазинил.
(358) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой пиридил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(359) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой пиридил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из:
-NH2, -NH(C1-4алкил), -N(C1-4алкила)2,
пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино,
-NHC(=O)(C1-4алкила), и
-OH.
(360) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой пиридил или пиридонил.
(361) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой пиридил.
(362) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой имидазолил, пиразолил, оксазолил, изоксазолил и является необязательно замещенным, например, содержит один или более заместителей -RX3.
(363) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой имидазолил, пиразолил, оксазолил, изоксазолил и является необязательно замещенным, например, содержит один или более заместителей, выбранных из C1-4алкила.
(364) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой пиразолил и является необязательно замещенным, например, содержит один или более заместителей -RX.
(365) Соединение согласно любому из (1)-(346), где каждый -RZ5, если присутствует, независимо представляет собой пиразолил и является необязательно замещенным, например, содержит один или более заместителей, выбранных из C1-4алкила.
Группа -LZ-
(366) Соединение согласно любому из (1)-(365), где каждый -LZ-, если присутствует, независимо представляет собой -CH2-, -CH(Ме)-, -C(Me)2-, -CH2CH2- или -CH2CH2CH2-
(367) Соединение согласно любому из (1)-(365), где каждый -LZ -, если присутствует, независимо представляет собой -CH2-, -CH(Ме)- или -CH2CH2-.
(368) Соединение согласно любому из (1)-(365), где каждый -LZ-, если присутствует, независимо представляет собой -CH2- или -CH(Ме)-.
(369) Соединение согласно любому из (1)-(365), где каждый -L2-, если присутствует, независимо представляет собой -CH2-.
Группа -R11B
(370) Соединение согласно любому из (1)-(369), где -RJ1, если присутствует, независимо представляет собой -Н, -Me, -Et, -nPr или -iPr.
(371) Соединение согласно любому из (1)-(369), где -RJ1, если присутствует, независимо представляет собой -Н, -Me или -Et.
(372) Соединение согласно любому из (1)-(369), где -RJ1, если присутствует, независимо представляет собой -Н.
(373) Соединение согласно любому из (1)-(372), где -RJ2, если присутствует, независимо представляет собой -Н, -Me, -Et, -nPr или -iPr.
(374) Соединение согласно любому из (1)-(372), где -RJ2, если присутствует, независимо представляет собой -Н, -Me или -Et.
(375) Соединение согласно любому из (1)-(372), где -RJ2, если присутствует, независимо представляет собой -Н.
(376) Соединение согласно любому из (1)-(375), где -RJ3, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил, фенил или бензил.
(377) Соединение согласно любому из (1)-(375), где -RJ3, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
(378) Соединение согласно любому из (1)-(377), где -RJ4, если присутствует, независимо представляет собой -Н, насыщенный алифатический C1-4алкил, фенил или бензил.
(379) Соединение согласно любому из (1)-(377), где -RJ4, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил, фенил или бензил.
(380) Соединение согласно любому из (1)-(377), где -RJ4, если присутствует, независимо представляет собой -Н или насыщенный алифатический C1-4алкил.
(381) Соединение согласно любому из (1)-(377), где -RJ4, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
(382) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой C3-10гетероциклильную группу и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(383) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой а C3-10гетероциклильную группу и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(384) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой пирролидино, пиперидино, морфолино, пиперизино, азепино, диазепино, [1,4]-оксазепан-4-ил, 1,2,3,4-тетрагидрохинолин-1-ил, 1,2,3,4-тетрагидроизохинолин-2-ил, 1,2,3,4-тетрагидрохиноксалин-1-ил, 3,4-дигидро-2Н-бензо[1,4]оксазин-4-ил, 2,3-дигидро-1Н-индол-1-ил или 2,3-дигидро-1Н-изоиндол-2-ил и является необязательно замещенным, например, содержит один или более заместителей -RX2.



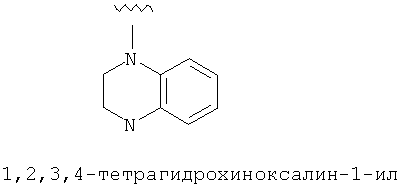



(385) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой 1,2,3,4-тетрагидроизохинолин-2-ил или 2,3-дигидро-1Н-индол-1-ил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(386) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой 1,2,3,4-тетрагидроизохинолин-2-ил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(387) Соединение согласно любому из (1)-(306), где -NRJ3RJ4, если присутствует, независимо представляет собой пирролидино, пиперидино, морфолино, пиперизино, азепино, диазепино, [1,4]-оксазепан-4-ил, 1,2,3,4-тетрагидрохинолин-1-ил, 1,2,3,4-тетрагидроизохинолин-2-ил, 1,2,3,4-тетрагидрохиноксалин-1-ил, 3,4-дигидро-2Н-бензо[1,4]оксазин-4-ил, 2,3-дигидро-1Н-индол-1-ил или 2,3-дигидро-1Н-изоиндол-2-ил и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(388) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой 1,2,3,4-тетрагидроизохинолин-2-ил или 2,3-дигидро-1Н-индол-1-ил и необязательно содержит один или более заместителей, независимо выбранных из C1-4алкила.
(389) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой 1,2,3,4-тетрагидроизохинолин-2-ил и необязательно содержит один или более заместителей, независимо выбранных из C1-4алкила.
(390) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой 1,2,3,4-тетрагидроизохинолин-2-ил или 2,3-дигидро-1Н-индол-1-ил.
(391) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой 1,2,3,4-тетрагидроизохинолин-2-ил.
(392) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой неароматическую Сз-угетероциклильную группу и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(393) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой неароматическую C3-7гетероциклильную группу и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(394) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой пирролидино, пиперидине, морфолино или пиперизино и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(395) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой пирролидино, пиперидино, морфолино или пиперизино и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(396) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо выбран из:
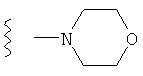 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
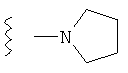 и
и 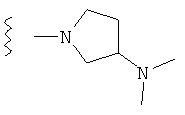 .
.
(397) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой пиперидино, морфолино или пиперизино и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(398) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой пиперидино, морфолино или пиперизино и является необязательно замещенным, например, содержит один или более заместителей, независимо выбранных из C1-4алкила.
(399) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо выбран из:
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
(400) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо выбран из:
 ,
,  ,
,  ,
,
(401) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой:

(402) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой:

Во избежание неправильного толкования, так же предполагается, что катионная группа, например, группа, содержащая четвертичный азот, например, N,N-(диметил)пиперизино, показанный выше, сопровождается соответствующим противоанионом, например, анионом галогена, например, Cl-.
(403) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой:

(404) Соединение согласно любому из (1)-(375), где -NRJ3RJ4, если присутствует, независимо представляет собой пиперидине, морфолино, пиперизино или N-(C1-4алкил)пиперизино.
(405) Соединение согласно любому из (1)-(369), где -R11B, если присутствует, независимо выбран из:
 ,
,  ,
,
 ,
,  ,
,
 ,
, 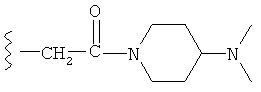 ,
,
 ,
,  .
.
(406) Соединение согласно любому из (1)-(369), где -R11B, если присутствует, независимо выбран из:
 ,
,  ,
,
 ,
,  ,
,
 ,
,  ,
,
(407) Соединение согласно любому из (1)-(369), где -R11B, если присутствует, независимо представляет собой:

(408) Соединение согласно любому из (1)-(369), где -R11B, если присутствует, независимо выбран из:
 ,
,  ,
,
 ,
,  , и
, и

(409) Соединение согласно любому из (1)-(369), где -R11B, если присутствует, независимо выбран из:
 ,
,  ,
,
 ,
,  , и
, и
Группа -R12
(410) Соединение согласно любому из (1)-(409), где -R12 независимо представляет собой -Н или -R12A.
(411) Соединение согласно любому из (1)-(409), где -R12 независимо представляет собой -Н.
(412) Соединение согласно любому из (1)-(409), где -R12 независимо представляет собой -R12A.
Группа -R12A
(413) Соединение согласно любому из (1)-(412), где -R12A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(414) Соединение согласно любому из (1)-(412), где -R12A, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил.
(415) Соединение согласно любому из (1)-(412), где -R12A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил и является необязательно замещенным, например, содержит один или более заместителей -RX1.
(416) Соединение согласно любому из (1)-(412), где -R12A, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
(417) Соединение согласно любому из (1)-(412), где -R12A, если присутствует, независимо представляет собой -Me, -Et, -nPr, -iPr, -nBu, -sBu, -iBu или -tBu.
(418) Соединение согласно любому из (1)-(412), где -R12A если присутствует, независимо представляет собой -Me, -Et, -nPr или -iPr.
(419) Соединение согласно любому из (1)-(412), где -R12A, если присутствует, независимо представляет собой -Me.
Группа -NR11R12
(420) Соединение согласно любому из (1)-(274), где -NR11R12 независимо представляет собой C3-10гетероциклильную группу и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(421) Соединение согласно любому из (1)-(274), где -NR11R12 независимо представляет собой пирролидино, пиперидино, морфолино, пиперизино, азепино, тетрагидрохинолино или тетрагидроизохинолинил и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(422) Соединение согласно любому из (1)-(274), где -NR11R12 независимо представляет собой неароматическую C3-7гетероциклильную группу и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(423) Соединение согласно любому из (1)-(274), где -NR11R12 независимо представляет собой пирролидино, пиперидино, морфолино, пиперизино или азепино и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(424) Соединение согласно любому из (1)-(274), где -NR11R12 независимо представляет собой пирролидино, пиперидино, морфолино или пиперизино и является необязательно замещенным, например, содержит один или более заместителей -RX2.
(425) Соединение согласно любому из (1)-(274), где -NR11R12 независимо выбран из:
 ,
,  ,
,  , и
, и 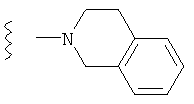 .
.
Необязательные заместители -RX1
(426) Соединение согласно любому из (1)-(425), где каждый -RX1, если присутствует, независимо выбран из:
-F, -Cl, -Br, -I, фенила, -CF3, -ОН, -ORS, -OCF3, -NH2, -NHRS,  , пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RS, -NRSC(=O)RS, -С(=O)RS, -С(=O)ОН, -С(=O)ORS, -С(=O)NH2, -С(=O)NHRS,
, пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RS, -NRSC(=O)RS, -С(=O)RS, -С(=O)ОН, -С(=O)ORS, -С(=O)NH2, -С(=O)NHRS,  , -С(=O)-пирролидино, -С(=O)-пиперидино, -С(=O)-морфол ино, -С(=O)-пиперизино, -С(=O)-{N-(C1-4алкил)пиперизино}-, -SRS, -S(=O)RS и -S(=O)2RS;
, -С(=O)-пирролидино, -С(=O)-пиперидино, -С(=O)-морфол ино, -С(=O)-пиперизино, -С(=O)-{N-(C1-4алкил)пиперизино}-, -SRS, -S(=O)RS и -S(=O)2RS;
где каждый -RS независимо представляет собой насыщенный алифатический C1-6алкил, фенил или -CH2-фенил;
где каждый фенил необязательно содержит в качестве заместителя одну или более групп, выбранных из: -F, -Cl, -Br, -I, -RSS, -CF3, -ОН, -ORSS или -OCF3, где каждый -RSS независимо представляет собой насыщенный алифатический C1-4алкил.
(427) Соединение согласно (426), где каждый -RX1, если присутствует, независимо выбран из:
-F, -Cl, -Br, -I, -ОН, -ORS, -NH2, -NHRS,  , пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RS, -NRSC(=O)RS, -С(=O)NH2, -С(=O)NHRS,
, пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RS, -NRSC(=O)RS, -С(=O)NH2, -С(=O)NHRS,  , -С(=O)-пирролидино, -С(=O)-пиперидино, -С(=O)-морфолино, -С(=O)-пиперизино и -С(=О)-{N-(C1-4алкил)пиперизино}-.
, -С(=O)-пирролидино, -С(=O)-пиперидино, -С(=O)-морфолино, -С(=O)-пиперизино и -С(=О)-{N-(C1-4алкил)пиперизино}-.
(428) Соединение согласно (426), где каждый -RX1, если присутствует, независимо выбран из:
-ОН, -ORS, -NH2, -NHRS,  , пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RS, -NRSC(=O)RS, -C(=O)NH2, -С(=O)NHRS,
, пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RS, -NRSC(=O)RS, -C(=O)NH2, -С(=O)NHRS,  , -С(=O)-пирролидино, -С(=O)-пиперидино, -С(=O)-морфолино, -С(=O)-пиперизино и -С(=O)-{N-(C1-4алкил)пиперизино}-.
, -С(=O)-пирролидино, -С(=O)-пиперидино, -С(=O)-морфолино, -С(=O)-пиперизино и -С(=O)-{N-(C1-4алкил)пиперизино}-.
(429) Соединение согласно любому из (426)-(428), где каждый -RS, если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил.
(430) Соединение согласно любому из (426)-(428), где каждый -RS, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
Необязательные заместители -RX2
(431) Соединение согласно любому из (1)-(430), где каждый -RX2, если присутствует, независимо выбран из:
-F, -Cl, -Br, -I, -RT, фенила, -ОН, -ORT, -C(=O)RT, -NH2, -NHRT,  , пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино, -NHC(=O)RT и -NRTC(=O)RT;
, пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино, -NHC(=O)RT и -NRTC(=O)RT;
где каждый -RT независимо представляет собой насыщенный алифатический C1-6алкил, фенил или -CH2-фенил;
где каждый фенил необязательно содержит в качестве заместителя одну или более групп, выбранных из: -F, -Cl, -Br, -I, -RTT, -CF3, -ОН, -ORTT или -OCF3, где каждый -RTT независимо представляет собой насыщенный алифатический C1-4алкил.
(432) Соединение согласно (431), где каждый -RX2, если присутствует, независимо выбран из:
-RT, -ОН, -ORT, -C(=O)RT, -NH2, -NHRT,  , пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино, -NHC(=O)RT и -NRTC(=O)RT.
, пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)-пиперизино, -NHC(=O)RT и -NRTC(=O)RT.
(433) Соединение согласно (431), где каждый -RX2, если присутствует, независимо выбран из:
-RT, C(=O)RT, -NH2, -NHRT,  , пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RT и -NRTC(=O)RT.
, пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RT и -NRTC(=O)RT.
(434) Соединение согласно (431), где каждый -RX2, если присутствует, независимо выбран из:
-RT, -NH2, -NHRT,  , пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RT и -NRTC(=O)RT.
, пирролидино, пиперидино, морфолино, пиперизино, N-(C1-4алкил)пиперизино, -NHC(=O)RT и -NRTC(=O)RT.
(435) Соединение согласно (431), где каждый -RX2, если присутствует, независимо выбран из:
-R7, -NH2, -NHRT,  , пирролидино, пиперидино, морфолино, пиперизино и N-(C1-4алкил)пиперизино.
, пирролидино, пиперидино, морфолино, пиперизино и N-(C1-4алкил)пиперизино.
(436) Соединение согласно любому из (431)-(435), где каждый -RT, если присутствует, независимо представляет собой насыщенный алифатический C1-6еалкил.
(437) Соединение согласно любому из (431)-(435), где каждый -RT, если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
Необязательные заместители -RX3
(438) Соединение согласно любому из (1)-(437), где каждый -RX3, если присутствует, независимо выбран из:
-F, -Cl, -Br, -I,
-RV,
-CH=CH2, -C≡CH, циклопропила,
-CF3, -CHF2, -OCF3, -OCHF2,
-CN,
-NO2,
-ОН, -ORV
-LV-OH, -LV-ORV,
-O-LV-OH, -O-LV-ORV,
-NH2, -NHRV,  ,
,
пирролидино, пиперидино, морфолино,
пиперизино, N-(C1-4алкил)пиперизино,
-LV-NH2, -LV-NHRV, 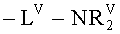 ,
,
-LV-пирролидино, -LV-пиперидино, -LV-морфолино,
-LV-пиперизино, -LV-{N-(С1-4алкил)пиперизино},
-LV-имидазол-2-ила, -LV-{N-(С1-4алкил)имидазол-2-ила},
-O-LV-NH2, -O-LV-NHRV, -O-LV-NRV 2,
-O-LV-пирролидино, -О-LV-пиперидино, -О-LV-морфолино,
-O-LV-пиперизино, -O-LV-{N-(С1-4алкил)пиперизино},
-O-LV-имидазол-2-ила, -O-LV-{N-(С1-4алкил)имидазол-2-ила},
-NHC(=O)RV, -NRVC(=O)RV,
-C(=O)RV,
-С(=O)ОН, -C(=O)ORV,
-C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2,
-С(=O)-пирролидино, -С(=O)-пиперидино, -С(=O)-морфолино,
-С(=O)-пиперизино, -С(=O)-{N-(С1-4алкил)пиперизино}-,
-NHC(=O)NH2, -NHC(=O)NHRV, -NHC(=O)NRV 2,
-NHC(=O)-пирролидино, -NHC(=O)-пиперидино, -NHC(=O)-морфолино,
-NHC(=O)-пиперизино, -NHC(=O)-{N-(С1-4алкил)пиперизино}-,
-S(=O)2RV,
-S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2, и
=O;
где каждый -LV- независимо представляет собой насыщенный алифатический С1-4алкилен;
где каждый -RV независимо представляет собой насыщенный алифатический С1-6алкил, фенил, -СН2-фенил, С5-6гетероарил или -СН2-С5-6гетероарил;
где каждый фенил необязательно содержит в качестве заместителя одну или более групп, выбранных из: -F, -Cl, -Br, -I, -RVV, -CF3, -ОН, -ORVV или -OCF3;
где каждый С5-6гетероарил необязательно содержит в качестве заместителя одну или более групп, выбранных из: -F, -Cl, -Br, -I, -RVV, -CF3, -ОН, -ORVV или -OCF3;
где каждый -RVV независимо представляет собой насыщенный алифатический С1-4алкил;
и дополнительно две соседние группы -RX3 могут совместно образовывать -OCH2O-, -OCH2CH2O-, -СН2ОСН2- или -ОСН2СН2-;
и дополнительно две соседние группы -RX3 совместно с атомами кольца, к которому они присоединены, могут образовывать С5-7карбоциклическое кольцо или С5-7гетероциклическое кольцо.
(439) Соединение согласно (438), где каждый -RX3, если присутствует, независимо выбран из:
-F, -Cl, -Br, -I,
-RV,
-CH=СН2, -С≡СН, циклопропила,
-CF3, -CHF2, -OCF3, -OCHF2,
-CN,
-NO2,
-OH, -ORV,
-LV-OH, -LV-ORV,
-O-LV-OH, -O-LV-ORV,
-NH2, -NHRV, -NRV 2,
пирролидино, пиперидино, морфолино,
пиперизино, N-(С1-4алкил)пиперизино,
-LV-NH2, -LV-NHRV, -LV-NRV 2,
-LV-пирролидино, -LV-пиперидино, -LV-морфолино,
-LV-пиперизино, -LV-{N-(С1-4алкил)пиперизино},
-LV-имидазол-2-ила, -LV-{N-(С1-4алкил)имидазол-2-ила},
-O-LV-NH2, -O-LV-NHRV, -O-LV-NRV 2,
-O-LV-пирролидино, -О-LV-пиперидино, -О-LV-морфолино,
-O-LV-пиперизино, -O-LV-{N-(С1-4алкил)пиперизино},
-O-LV-имидазол-2-ила, -O-LV-{N-(С1-4алкил)имидазол-2-ила},
-NHC(=O)RV, -NRVC(=O)RV,
-C(=O)RV,
-С(=O)ОН, -C(=O)ORV,
-C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2,
-С(=O)-пирролидино, -С(=O)-пиперидино, -С(=O)-морфолино,
-С(=O)-пиперизино, -С(=O)-{N-(С1-4алкил)пиперизино}-,
-NHC(=O)NH2, -NHC(=O)NHRV, -NHC(=O)NRV 2,
-NHC(=O)-пирролидино, -NHC(=O)-пиперидино, -NHC(=O)-морфолино,
-NHC(=O)-пиперизино, -NHC(=O)-{N-(С1-4алкил)пиперизино}-,
-S(=O)2RV,
-S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2, и
=O;
и кроме того, две соседние группы -RX3 могут совместно образовывать -OCH2O-, -OCH2CH2O-, -СН2ОСН2- или -ОСН2СН2-.
(440) Соединение согласно (438), где каждый -RX3, если присутствует, независимо выбран из:
-F, -Cl, -Br, -I,
-RV,
-ОН, -ORV,
-NH2, -NHRV, -NRV 2,
пирролидино, пиперидино, морфолино,
пиперизино и N-(С1-4алкил)пиперизино.
(441) Соединение согласно (438), где каждый -RX3, если присутствует, независимо выбран из:
-F, -Cl, -Br, -I,
-RV,
-ОН, -ORV,
-NH2, -NHRV и -NRV 2.
(442) Соединение согласно любому из (438)-(441), где каждый -LV-, если присутствует, независимо представляет собой -CH2-, -CH2CH2-, -CH2CH2CH2- или -CH2CH2CH2CH2-.
(443) Соединение согласно любому из (438)-(441), где каждый -LV-, если присутствует, независимо представляет собой насыщенный алифатический C2-4алкилен.
(444) Соединение согласно любому из (438)-(441), где каждый -LV-, если присутствует, независимо представляет собой -CH2CH2-, -CH2CH2CH2- или -CH2CH2CH2CH2-.
(445) Соединение согласно любому из (438)-(444), где каждый -RV если присутствует, независимо представляет собой насыщенный алифатический C1-6алкил.
(446) Соединение согласно любому из (438)-(444), где каждый -RV если присутствует, независимо представляет собой насыщенный алифатический C1-4алкил.
Молекулярная масса
(447) Соединение согласно любому из (1)-(446), где молекулярная масса указанного соединения находится в диапазоне от 258 до 1200.
(448) Соединение согласно (447), где нижняя граница указанного диапазона составляет 275, 300, 325, 350, 375, 400 или 500.
(449) Соединение согласно (447) или (448), где верхняя граница указанного диапазона составляет 1100, 1000, 900, 800, 700 или 600.
(450) Соединение согласно любому из (1)-(446), где молекулярная масса указанного соединения находится в диапазоне от 500 до 800.
Конкретные соединения
(451) Соединение согласно (1), выбранное из соединений следующих формул, и его фармацевтически приемлемые соли, гидраты и сольваты:






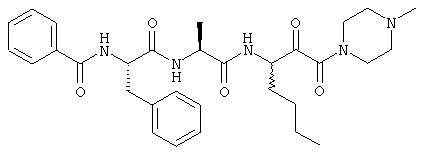
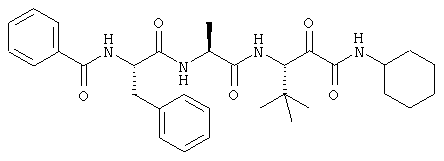









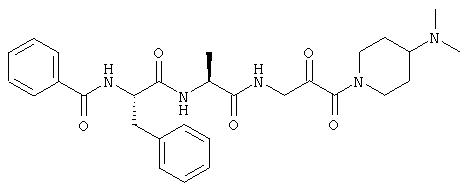

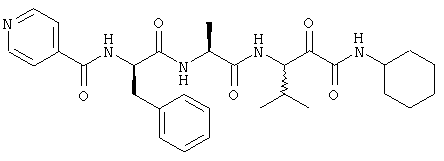






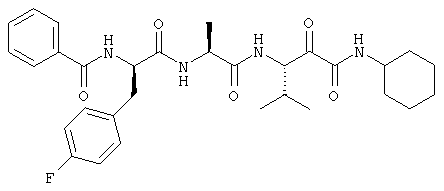

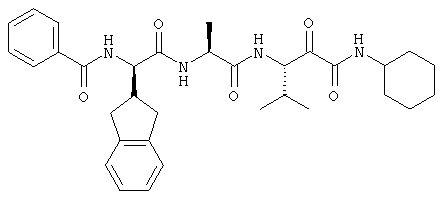



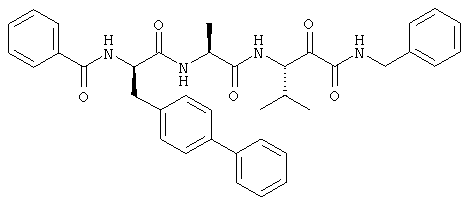































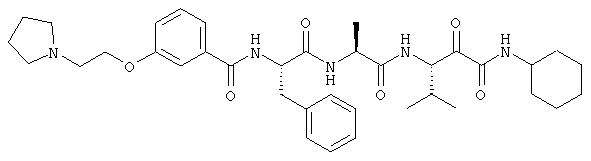





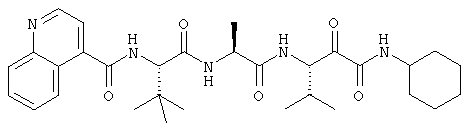



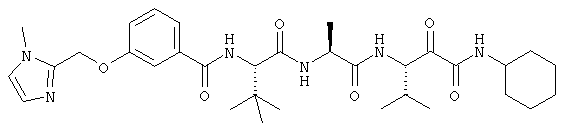



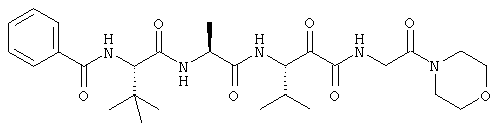




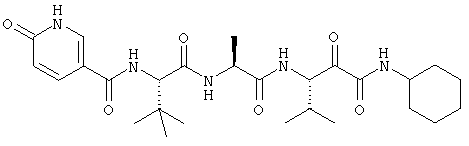
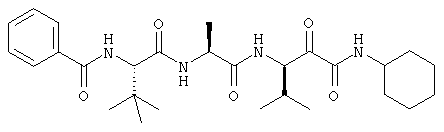

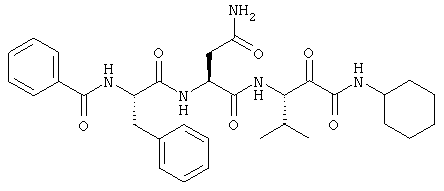
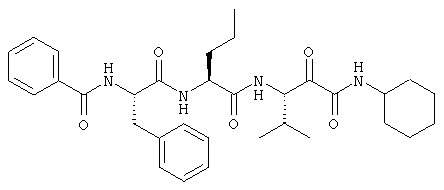



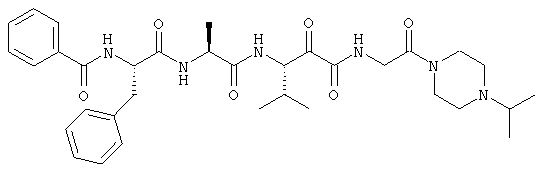


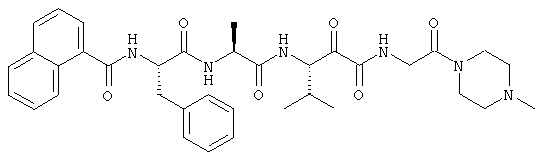










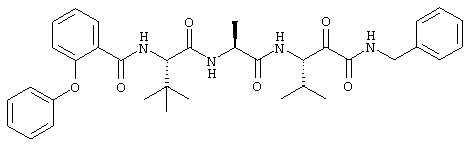




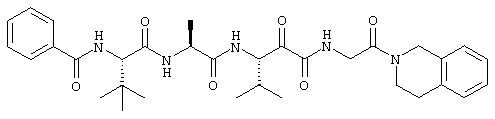

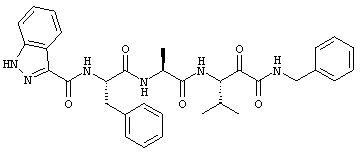





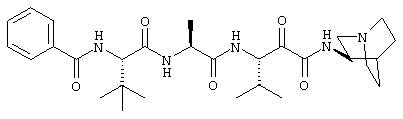







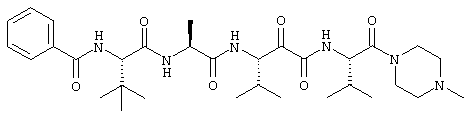

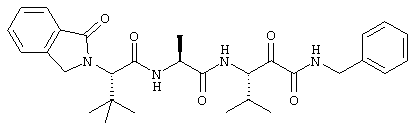
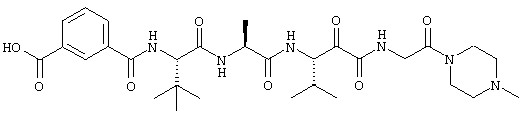

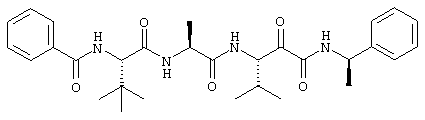
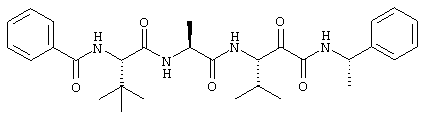



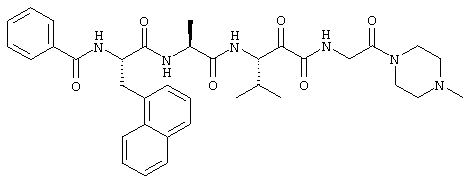

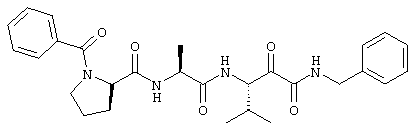
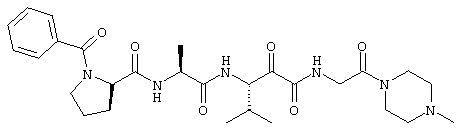


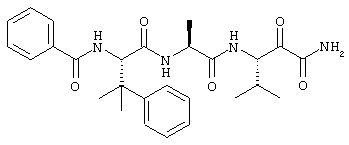
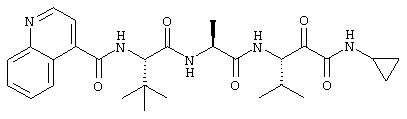





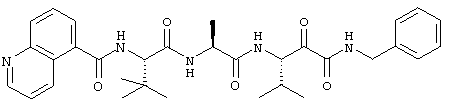






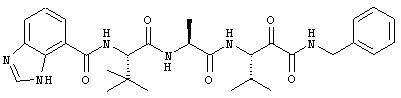




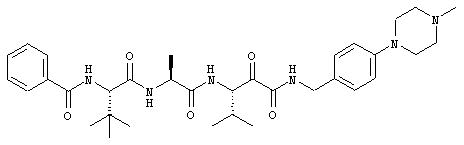




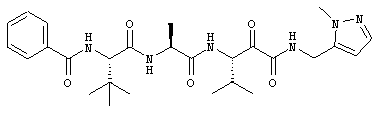
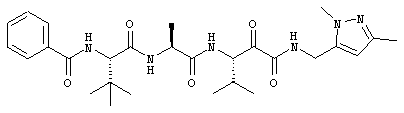

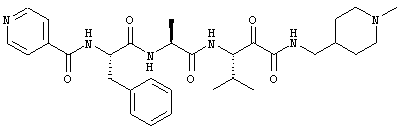
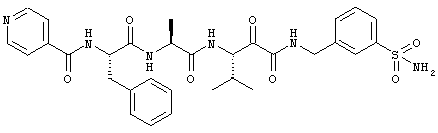


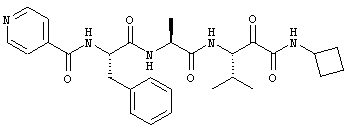
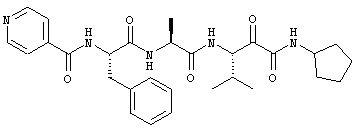


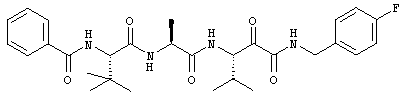
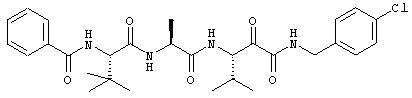
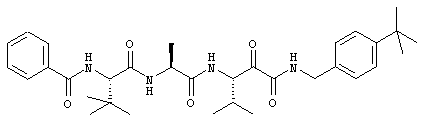




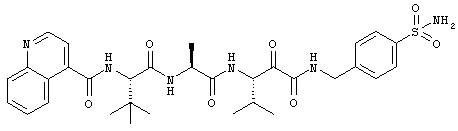

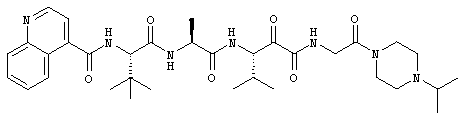



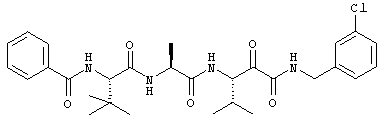

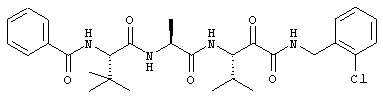


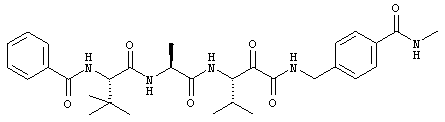

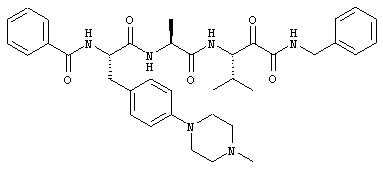
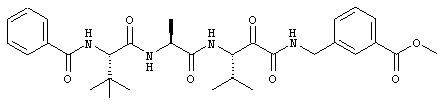



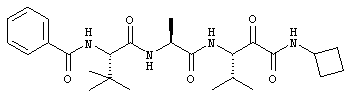


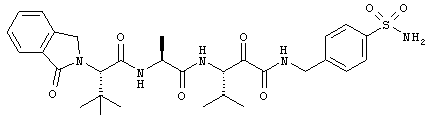
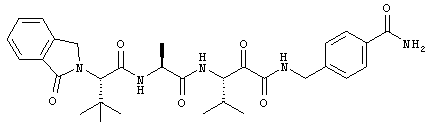







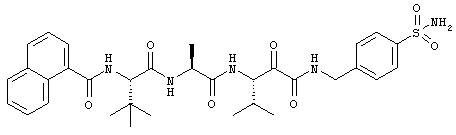

Комбинации
Очевидно, что некоторые признаки изобретения, которые для ясности описаны в контексте конкретных вариантов реализации изобретения, могут также быть предложены в комбинации в пределах одного варианта реализации изобретения. Напротив, различные признаки изобретения, которые для краткости описаны в контексте одного варианта реализации изобретения, могут также быть предложены отдельно или в любых подходящих подкомбинациях. Все комбинации вариантов реализации изобретения, относящиеся к химическим группам, представленным переменными (например, R1, R2, R3, R4, R5, R6, R7, R8, R9, R10, R11, R12, -R1A, -R2A, -R3A, -R4A, -R5A, -R6A, -R7A, -R7B, -R7B1, -R7B2, -R7BB, -R7BB1, -R7BB2, -R7BB3, -R7BB4, -R8A, -R9A, -R10A, -R10B, -R10C, -R10D, -R11A, -R11B, -RZ1, -RZ2, -RZ3, -RZ3A, -RZ3B, -RZ4, -RZ5, -LZ-, -RJ1, -RJ2, -RJ3, -RJ4, -R12A, -RX1, -RX2, -RX3 и т.д.), конкретно включены в настоящее изобретение и раскрыты в настоящей заявке в той же мере, как если бы каждая комбинация была отдельно и подробно раскрыта, при условии, что указанные комбинации включают соединения, которые представляют собой стабильные соединения (т.е., соединения, которые могут быть выделены, охарактеризованы и исследованы на предмет биологической активности). Кроме того, все подкомбинации химических групп, перечисленных в вариантах реализации изобретения, описывающих указанные переменные, также конкретно включены в настоящее изобретение и раскрыты в настоящей заявке в той же мере, как если бы каждая из указанных подкомбинации химических групп была отдельно и подробно раскрыта в настоящей заявке.
По существу очищенные формы
Согласно одному аспекту, настоящее изобретение относится к PVA соединениям, описанным в настоящей заявке, находящимся в по существу очищенной форме и/или в форме, по существу свободной от примесей.
Согласно одному варианту реализации изобретения, по существу очищенная форма составляет по меньшей мере 50% по массе, например, по меньшей мере 60% по массе, например, по меньшей мере 70% по массе, например, по меньшей мере 80% по массе, например, по меньшей мере 90% по массе, например, по меньшей мере 95% по массе, например, по меньшей мере 97% по массе, например, по меньшей мере 98% по массе, например, по меньшей мере 99% по массе.
Если иное не указано, по существу очищенная форма относится к соединению в любой стереоизомерной или энантиомерной форме. Например, согласно одному варианту реализации изобретения, по существу очищенная форма относится к смеси стереоизомеров, т.е., является очищенной с точки зрения содержания других соединений. Согласно одному варианту реализации изобретения, по существу очищенная форма относится к одному стереоизомеру, например, оптически чистому стереоизомеру. Согласно одному варианту реализации изобретения, по существу очищенная форма относится к смеси энантиомеров. Согласно одному варианту реализации изобретения, по существу очищенная форма относится к эквимолярной смеси энантиомеров (т.е., рацемической смеси, рацемату). Согласно одному варианту реализации изобретения, по существу очищенная форма относится к одному энантиомеру, например, оптически чистому энантиомеру.
Согласно одному варианту реализации изобретения, примеси составляют не более 50% по массе, например, не более 40% по массе, например, не более 30% по массе, например, не более 20% по массе, например, не более 10% по массе, например, не более 5% по массе, например, не более 3% по массе, например, не более 2% по массе, например, не более 1% по массе.
Если иное не указано, примеси относятся к другим соединениям, то есть, отличным от стереоизомеров или энантиомеров. Согласно одному варианту реализации изобретения, примеси относятся к другим соединениям и другому стереоизомеру. Согласно одному варианту реализации изобретения, примеси относятся к другим соединениям и другому энантиомеру.
Согласно одному варианту реализации изобретения, по существу очищенная форма является по меньшей мере на 60% оптически чистой (т.е., 60% соединения, на основе молярности, составляет желаемый стереоизомер или энантиомер, и 40% соединения составляет не желаемый стереоизомер или энантиомер), например, по меньшей мере на 70% оптически чистой, например, по меньшей мере на 80% оптически чистой, например, по меньшей мере на 90% оптически чистой, например, по меньшей мере на 95% оптически чистой, например, по меньшей мере на 97% оптически чистой, например, по меньшей мере на 98% оптически чистой, например, по меньшей мере на 99% оптически чистой.
Геминальные диолы. полуацетали и ацетали
Предполагается, что 2-оксагруппа (-С(=O)-) пирувамидного фрагмента PVA соединений может преднамеренно или непреднамеренно превращаться полностью или частично в соответствующий геминальный диол, полуацеталь или ацеталь при контактировании с водой, спиртом или смесью воды и спирта. Такое превращение может происходить, например, в процессе очистки (например, в процессе перекристаллизации из водного или спиртового растворителя), как показано далее, где, например, каждый -RA независимо представляет собой C1-4алкил, например, -Me. Более того, если для получения соответствующего 1,3-диоксолана используется диол, например, этиленгликоль, может образовываться циклический ацеталь.

Предполагается, что в водном растворе любые указанные геминальные диолы, полуацетали и ацетали присутствуют в равновесии с исходным соединением. Во избежание неправильного толкования, предполагается, что, если иное не указано, в настоящей заявке ссылки на PVA соединения также включают указанные формы геминальных диолов, полуацеталей и ацеталей.

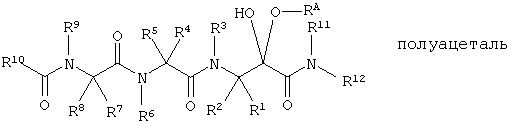

Изомеры
Некоторые соединения могут существовать в одной или более конкретных геометрических, оптических, энантиомерных, диастереоизомерных, эпимерных, атроповых, стереоизомерных, таутомерных, конформационных или аномерных формах, включая, но не ограничиваясь ими, цис- и транс-формы; Е- и Z-формы; с-, t- и r-формы; эндо- и экзо-формы; R-, S- и мезо-формы; D- и L-формы; d- и l-формы; (+) и (-) формы; кето-, енол- и енолат-формы; син- и анти-формы; синклинальные и антиклинальные формы; α- и β-формы; аксиальные и экваториальные формы; форму ванны, кресла, твист-форму, форму конверта и полукресла; и их комбинации, которые здесь и далее совместно называются «изомерами» (или «изомерными формами»).
Ссылка на класс структур может включать структурно изомерные формы, входящие в указанный класс (например, C1-7алкил включает н-пропил и изопропил; бутил включает н-, изо-, втор- и трет-бутил; метоксифенил включает орто-, мета- и пара-метоксифенил). Однако предполагается, что ссылка на конкретную группу или схему замещения не включает другие структурные (или конституционные) изомеры, которые отличаются по связям между атомами, а не по положению атомов в пространстве. Например, не следует рассматривать ссылку на метоксигруппу, -OCH3, как ссылку на ее структурный изомер, гидроксиметильную группу, -CH2OH. Подобным образом, не следует рассматривать ссылку на орто-хлорфенил как ссылку на его структурный изомер, мета-хлорфенил.
Выше указанное исключение не относится к таутомерным формам, например, кето-, енол- и енолат-формам, как, например, в следующих таутомерных парах: кето/енол (показанных ниже), имин/енамин, амид/имино спирт, амидин/амидин, нитрозо/оксим, тиокетон/енетиол, N-нитрозо/гидроксиазо и нитро/ацинитро.

Например, 1Н-пиридин-2-он-5-ил и 2-гидроксил-пиридин-5-ил (показаны ниже) являются таутомерами друг друга. Предполагается, что ссылка в настоящей заявке на один из них включает оба указанных соединения. См., например, PVA-084.
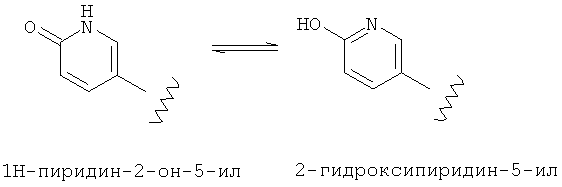
Следует отметить, что соединения с одним или более изотопными замещениями конкретно включены в термин «изомер». Например, Н может быть в любой изотопной форме, включая 1H, 2H (D) и 3Н (Т); С может быть в любой изотопной форме, включая 12С, 13С и 14С; О может быть в любой изотопной форме, включая 16O и 18О; и т.д.
Если иное не указано, ссылка на конкретное соединение включает все такие изомерные формы, включая их смеси (например, рацемические смеси). Способы получения (например, асимметрический синтез) и разделения (например, фракциональная кристаллизция и хроматографические способы) указанных изомерных форм либо известны в данной области техники, либо с легкостью могут быть получены путем внесения известных изменений в способы, описанные в настоящей заявке, или в известные способы.
Соли
Может быть удобным или желательным получать, очищать, и/или обрабатывать соответствующую соль соединения, например, фармацевтически приемлемую соль. Примеры фармацевтически приемлемых солей описаны в источнике Berge et al., 1977, "Pharmaceutically acceptable salts," J. Pharm. Sci., Vol.66, pp.1-19.
Например, если соединение является анионным или имеет функциональную группу, которая может быть анионной (например, -СООН может представлять собой -СОО-), то может образовываться соль с подходящим катионом. Примеры подходящих неорганических катионов включают, но не ограничиваются ими, ионы щелочных металлов, такие как Na+ и K+, катионы щелочно-земельных металлов, такие как Са2+ и Mg2+, и другие катионы, такие как Al+3. Примеры подходящих органических катионов включают, но не ограничиваются ими, ион аммония (т.е.,  ) и ионы замещенного аммония (например, NH3R+,
) и ионы замещенного аммония (например, NH3R+, 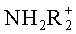 ,
,  ,
,  ). Примеры некоторых подходящих ионов замещенного аммония представляют собой ионы, произошедшие из: этиламина, диэтиламина, дициклогексиламина, триэтиламина, бутиламина, этилендиамина, этаноламина, диэтаноламина, пиперазина, бензиламина, фенилбензиламина, холина, меглумина и трометамина, также как и аминокислот, таких как лизин и аргинин. Пример типичного иона четвертичного аммония представляет собой
). Примеры некоторых подходящих ионов замещенного аммония представляют собой ионы, произошедшие из: этиламина, диэтиламина, дициклогексиламина, триэтиламина, бутиламина, этилендиамина, этаноламина, диэтаноламина, пиперазина, бензиламина, фенилбензиламина, холина, меглумина и трометамина, также как и аминокислот, таких как лизин и аргинин. Пример типичного иона четвертичного аммония представляет собой 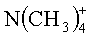 .
.
Если соединение является катионным или содержит функциональную группу, которая при протонировании может становиться катионной (например, -NH2 может становиться  ), то может образовываться соль с подходящим анионом.
), то может образовываться соль с подходящим анионом.
Например, если исходная структура содержит катионную группу (например, 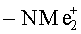 ) или содержит функциональную группу, которая при протонировании может становиться катионной (например, -NH2 может становиться
) или содержит функциональную группу, которая при протонировании может становиться катионной (например, -NH2 может становиться  ), то может образовываться соль с подходящим анионом. В случае четвертичного аммонийного соединения в целом всегда присутствует противоанион для уравновешивания положительного заряда. Если кроме катионной группы (например,
), то может образовываться соль с подходящим анионом. В случае четвертичного аммонийного соединения в целом всегда присутствует противоанион для уравновешивания положительного заряда. Если кроме катионной группы (например, 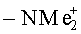 ,
, 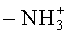 ) соединение также содержит группу, способную образовывать анион (например, -COOH), то может образовываться внутренняя соль (также относящаяся к цвиттериону).
) соединение также содержит группу, способную образовывать анион (например, -COOH), то может образовываться внутренняя соль (также относящаяся к цвиттериону).
Примеры подходящих неорганических анионов включают, но не ограничиваются ими, неорганические анионы, произошедшие из следующих неорганических кислот: соляной, бромистоводородной, йодистоводородной, серной, сернистой, азотной, азотистой, фосфорной и фосфористой.
Примеры подходящих органических анионов включают, но не ограничиваются ими, органические анионы, произошедшие из следующих органических кислот: 2-ацетилоксибензойная, уксусная, трифторуксусная, аскорбиновая, аспарагиновая, бензойная, камфорсульфоновая, коричная, лимонная, этилендиаминтетрауксусная, этандисульфоновая, этансульфоновая, фумаровая, глюкогептоновая, глюконовая, глутаминовая, гликолевая, гидроксималеиновая, гидроксинафталинкарбоновая, изэтиновая, молочная, лактобионовая, лауриновая, малеиновая, яблочная, метансульфоновая, муциновая, олеиновая, оксалиновая, пальмитиновая, памовая, пантотеновая, фенилуксусная, фенилсульфоновая, пропановая, пировиноградная, салициловая, стеариновая, сукциновая, сульфаниловая, винная, толуолсульфоновая и валериановая. Примеры подходящих полимерных органических анионов включают, но не ограничиваются ими, органические анионы, произошедшие из следующих полимерных кислот: дубильная кислота, карбоксиметилцеллюлоза.
Примеры подходящих противоионов, которые, в частности, подходят для четвертичных аммониевых соединений (например, соединений, содержащих группу 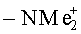 ), включают 1-адамантансульфонат, бензолсульфонат, бисульфат, бромид, хлорид, йодид, метансульфонат, метилсульфат, 1,5-нафталинбиссульфонат, 4-нитробензолсульфонат, формат, тартрат, тозилат, трифторацетат, трифторметилсульфонат, сульфат. Опять же, если соединение также содержит группу, способную образовывать анион (например, -COOH), то может образовываться внутренняя соль.
), включают 1-адамантансульфонат, бензолсульфонат, бисульфат, бромид, хлорид, йодид, метансульфонат, метилсульфат, 1,5-нафталинбиссульфонат, 4-нитробензолсульфонат, формат, тартрат, тозилат, трифторацетат, трифторметилсульфонат, сульфат. Опять же, если соединение также содержит группу, способную образовывать анион (например, -COOH), то может образовываться внутренняя соль.
Если иное не указано, ссылка на конкретное соединение также включает формы его солей.
Сольваты и гидраты
Может быть удобным или желательным получать, очищать и/или обрабатывать соответствующий сольват соединения. Термин «сольват» используется в настоящей заявке в общепринятом смысле для ссылки на комплекс растворенного вещества (например, соединения, соли соединения) и растворителя. Если растворитель представляет собой воду, сольват может для удобства называться гидратом, например, моногидратом, дигидратом, тригидратом и т.д.
Если иное не указано, ссылка на конкретное соединение также включает формы его сольвата и гидрата.
Химически «защищенные» Формы
Может быть удобным или желательным получать, очищать, и/или обрабатывать соединение в химически защищенной форме. Термин «химически защищенная форма» используется в настоящей заявке в общепринятом химическом смысле и относится к соединению, в котором одна или более реактивных функциональных групп являются «защищенными» от нежелательных химических реакций при определенных условиях (например, рН, температуре, облучении, растворителе и т.д.). На практике используются хорошо известные химические способы обратимого превращения при определенных условиях в нереактивную группу функциональной группы, которая в обратном случае была бы реактивной. В химически защищенной форме одна или более реактивных функциональных групп находятся в защищенной форме, или форме, содержащей защитную группу (также называемой маскированной формой или формой, содержащей маскирующую группу, или блокированной формой или формой, содержащей блокирующую группу). С помощью введения защитной группы для реактивной функциональной группы можно проводить реакции, включающие другие незащищенные реактивные функциональные группы, не затрагивая защищенную группу; защитную группу можно удалять, обычно в ходе последующего этапа, по существу не затрагивая остальную часть молекулы. См., например, Protective Groups in Organic Synthesis (Т.Green and P.Wuts; 4th Edition; John Wiley and Sons, 2006).
Большое разнообразие таких способов введения «защитной», «блокирующей» или «маскирующей» группы широко используется и является хорошо известным в области органического синтеза. Например, можно получать производное соединения, имеющего две не эквивалентные реактивные функциональные группы, обе из которых являются реактивными при определенных условиях, содержащее одну из функциональных групп в «защищенной», и следовательно, нереактивной при определенных условиях форме; «защищенные» соединения, например, могут использоваться в качестве реагента, имеющего только одну эффективную реактивную функциональную группу. После завершения желаемой реакции (включающей другую функциональную группу) от защищенной группы можно удалять защитную группу для восстановления ее исходной функциональности.
Например, гидроксигруппа может быть защищена с получением эфира (-OR) или сложного эфира (-OC(=O)R), например: трет-бутилового эфира; бензила, бензгидрильного (дифенилметилового) или тритилового (трифенилметилового) эфира; триметилсилильного или трет-бутилдиметилсилильного эфира; или сложного ацетилового эфира (-ОС(=O)CH3, -OAc).
Например, альдегидная или кетонная группы могут быть защищены с получением ацеталя (R-CH(OR)2) или кеталя (R2C(OR)2), соответственно, в котором карбонильная группа (>С=O) превращается в диэфир (>C(OR)2), с помощью реакции, например, с первичным спиртом. Альдегидная или кетоновая группа легко восстанавливается, например, путем гидролиза с использованием воды в присутствии кислоты.
Например, аминогруппа может быть защищена с получением, например, амида (-NRCO-R) или уретана (-NRCO-OR), например: метиламида (-NHCO-СН3); бензилоксиамида (-NHCO-OCH2C6H5, -NH-Cbz); m-бутоксиамида (-NHCO-ОС(СН3)3, -NH-Boc); 2-бифенил-2-пропоксиамида (-NHCO-ОС(СН3)2С6Н4С6Н5, -NH-Bpoc), 9-флуоренилметоксиамида (-NH-Fmoc), 6-нитровератрилоксиамида (-NH-Nvoc), 2-триметилсилилэтилоксиамида (-NH-Teoc), 2,2,2-трихлорэтилоксиамида (-NH-Troc), аллилоксиамида (-NH-Alloc), 2(-фенилсульфонил)этилоксиамид (-NH-Psec) или, в подходящих случаях (например, в случае циклических аминов), нитроксидного радикала (>N-O•).
Например, для группа карбоновой кислоты может быть защищена с получением сложного эфира, например: сложного C1-7алкилэфира (например, сложного метилового эфира; сложного m-бутилового эфира); сложного C1-7галогеналкилэфира (например, сложного C1-7тригалогеналкилэфира); сложного три-C1-7алкилсилил-C1-7алкилэфира; или сложного C5-20арил-C1-7алкилэфира (например, сложного бензилового эфира; сложного нитробензилового эфира); или амида, например, метиламида.
Например, тиоловая группа может быть защищена с получением тиоэфира (-SR), например: бензилового тиоэфира; ацетамидометилового эфира (-S-CH2NHC(=O)СН3).
Пролекарства
Может быть удобным или желательным получать, очищать и/или обрабатывать соединение в форме Пролекарства. Термин «пролекарство» в настоящей заявке относится к соединению, которое приводит к получению желаемого активного соединения in vivo. Как правило, пролекарство является неактивным или менее активным по сравнению с желаемым активным соединением, но может иметь преимущества с точки зрения обработки, введения или метаболических свойств.
Например, некоторые Пролекарства представляют собой сложные эфиры активного соединения (например, физиологически приемлемый метаболически активный сложный эфир). В ходе метаболизма группа сложного эфира (-C(=O)OR) расщепляется с получением активного лекарственного средства. Указанные сложные эфиры могут быть образованы путем сложной этерификации, например, любой группы карбоновой кислоты (-С(=O)ОН) в исходном соединении, если применимо, с предварительным введением защитных групп для любых других реактивных групп, присутствующих в исходном соединении, при необходимости, с последующим удалением указанных защитных групп.
Другие формы пролекарств PVA соединений могут представлять собой форму, в которой 2-оксагруппа (С=O) PVA соединения защищена, например, в виде ацеталя или полуацеталя, который превращается in vivo в соответствующую 2-оксагруппу.
Также некоторые Пролекарства активируются ферментативным путем с получением активного соединения или соединения, которое в ходе дальнейшей химической реакции приводит к получению активного соединения (например, как в направленной на антитела ферментативно-пролекарственной терапии (ADEPT), направленной на гены ферментативно-пролекарственной терапии (GDEPT), направленной на липиды ферментативно-пролекарственной терапии (LIDEPT) и т.д.). Например, пролекарство может представлять собой производное сахара или другой гликозидный конъюгат или может представлять собой производное сложного эфира аминокислоты.
Химический синтез
Некоторые способы химического синтеза PVA соединений согласно настоящему изобретению описаны в настоящей заявке. Указанные способы и/или другие хорошо известные способы могут быть модифицированы и/или адаптированы по известным путям для облегчения синтеза дополнительных соединений в пределах объема настоящего изобретения.
Соединения формулы (I) могут быть получены, например, путем проведения реакции между α-гидроксиамидом формулы (II) и соответствующим окиконденсированнелем, как показано на следующей схеме. Подходящие окиконденсированнели включают, но не ограничиваются ими, периодинан Десс-Мартина, хлорхромат пиридиния (РСС), перрутинат тетрапропиламмония (ТРАР) и применение условий Сверна или модифицированных условий Сверна, согласно которым используется ДМСО в сочетании с активирующим агентом, таким как оксалилхлорид.
Схема 1

α-Гидроксиамиды формулы (II) могут быть получены несколькими различными способами, которые хорошо известны в данной области техники. Примеры указанных способов описаны в источнике Arasappan et al., 2009; Barrett et al., 2005; и Zhaozhao et al., 1996. Один способ синтеза соединений формулы (II), когда R12 представляет собой Н, включает проведение реакции между соответствующим пептидилальдегидом (III) и изонитрилом с использованием модифицированной реакции Пассерини (см., например, Marcaccini et al., 2005), как показано на следующей схеме.
Схема 2

Изонитрилы могут быть получены с применением способов, известных в данной области техники. Один способ включает дегидрирование соответствующего формамида с использованием реагентов, включающих, но не ограничивающихся ими, п-тозилхлорид, тионилхлорид, фосфорилхлорид и дифосген.
Альтернативно, соединения формулы (II) могут быть получены путем проведения реакции между соединением формулы (А) и соединением формулы (IV) с использованием стандартных условий сочетания кислоты и амина, как показано на следующей схеме.
Указанные условия известны в данной области техники. Возможной побочной реакцией в указанных условиях может являться эпимеризация R4/R5 хирального центра. Для избежания указанной побочной реакции обычно проводят низкотемпературные реакции сочетания с использованием смешанного ангидрида, полученного из Формулы (А). Смешанные ангидриды обычно получают in situ с использованием, например, изобутилхлорформата или этилхлорформата и слабого основания, такого как N-метилморфолин. Указанные способы известны в данной области техники.
Схема 3

Соединения формулы (IV) могут быть получены в несколько этапов из α-аминоальдегида, содержащего соответствующие защитные группы. Последовательность реакций включает образование соответствующего цианогидрина с последующим гидролизом с образованием соответствующих гидроксикислот. Указанные гидроксикислоты могут использоваться для получения ряда амидов с использованием стандартных реакций сочетания кислоты и амина, причем соединение формулы (IV) получают после удаления защитной группы для азота.
Подходящие защитные группы для азота включают, но не ограничиваются ими, бензилоксикарбонил (Cbz), трет-бутоксикарбонил (Boc) и флуоренилметилоксикарбонил (Fmoc). Обзор защитных групп для амина можно найти, например, в источнике Protective Groups in Organic Synthesis. 3rd Ed., (T.Green and P.Wuts; 4th Edition; Wiley-Interscience, 1999). pp.494-653.
Способы получения α-аминоальдегидов включают окисление соответствующего спирта или восстановление соответствующего амида Вейнреба, оба из которых могут быть получены из α-аминокислот, содержащих подходящие защитные группы, с использованием способов, известных в данной области техники.
Альтернативно, соединения формулы (I) могут быть получены путем обработки озоном трифенилфосфинацетонитрильного промежуточного соединения формулы (P) для получения соответствующего ацилцианида in situ с последующим проведением реакции с подходящим аминным нуклеофилом, как показано на следующей схеме. Трифенилфосфинацетонитрильные промежуточные соединения могут быть получены из соответствующего пептида с использованием условий, аналогичных условиям, используемым в реакциях сочетания кислоты и амина. Указанные условия включают применение 1-этил-3-(3-диметиламинопропил)карбодиимида (EDC) с использованием катализатора 4-диметиламинопиридина (DMAP) и известны в данной области техники.
Схема 4
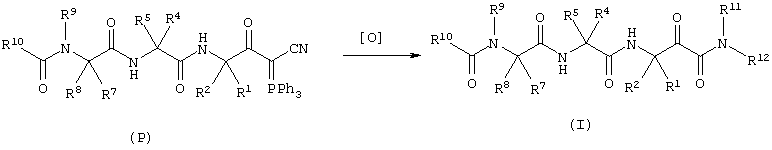
Дипептидные и трипептидные производные можно синтезировать на полимерах (например, полистирольной смоле) с использованием стандартных способов сочетания Fmoc на основе смолы. Первую аминокислоту, содержащую защитную группу Fmoc, в целом сочетали со смолой Ванга или 2-хлортритиловой смолой. Следующие аминокислоты сочетали с использованием стандартных условий сочетания кислоты и амина. Подходящие условия включали применение гидроксибензотриазола (HOBt) с N,N′-диизопропилкарбодиимидом (ДИС) или гексафторфосфата метанаминия 2-(1Н-7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония (HATU), тетрафторбората O-(бензотриазол-1-ил)-N,N,N′,N′-тетраметилурония (TBTU), гексафторфосфата O-бензотриазол-N,N,N′,N′-тетраметилурония (HBTU) или гексафторфосфата бензотриазол-1-ил-окситрипирролидинофосфония (PyBop), с подходящим основанием, таким как DIPEA. Дополнительная информация о синтезе пептида на смоле может быть найдена, например, в источнике: Chan and White, Fmoc Solid Phase Peptide Synthesis: A Practical Approach (Oxford University Press, 2000).
Альтернативно, пептидные производные могут быть получены в результате последовательных реакций с использованием химии растворов с содержащими подходящие защитные группы аминокислотами с использованием способов, известных в данной области техники. Для указанной цели обычно используют подходящие защитные группы для азота, такие как Boc, Cbz или Fmoc, в сочетании с низкотемпературными условиями сочетания смешанного ангидрида.
Композиции
Согласно одному аспекту, настоящее изобретение относится к композиции (например, фармацевтической композиции), содержащей PVA соединение, описанное в настоящей заявке, и фармацевтически приемлемый носитель, разбавитель или наполнитель.
Согласно одному варианту реализации изобретения, композиция представлена в виде сухого порошка, например, подходящего для доставки (например, введения) с использованием ингалятора сухого порошка (DPI). Примеры подходящих DPI хорошо известны в данной области техники. Введение с помощью DPI может использоваться для доставки лекарственного средства в легкие или в нос.
Согласно одному варианту реализации изобретения, композиция представлена в виде суспензии, например, подходящей для доставки (например, введения) с использованием небулайзера. Указанная композиция может использоваться для доставки лекарственного средства в легкие или в нос.
Согласно одному варианту реализации изобретения, композиция представлена в виде раствора или суспензии в жидком пропелленте, например, подходящем для доставки (например, введения) в виде аэрозоля, например, с использованием ингалятора отмеренных доз с распылением сжатым воздухом (pMDI). Примеры подходящих pMDI хорошо известны в данной области техники. Подходящие пропелленты хорошо известны в данной области техники и включают, например, дихлордифторметан (CFC-12), трихлорфторметан, дихлортетрафторэтан, HFA-134a, HFA-227, HCFC-22, HFA-152, изобутен и диоксид углерода. Указанная композиция может использоваться для доставки лекарственного средства в легкие или в нос.
Согласно одному варианту реализации изобретения, композиция представлена в виде водного раствора, например, подходящего для доставки (например, введения) с использованием капельницы, шприца, дозирующего пульверизатора или распылителя. Указанные формы могут применяться для доставки лекарственного средства через нос.
Согласно одному варианту реализации изобретения, композиция также содержит один или более (например, 1, 2, 3, 4) дополнительных терапевтических агентов, описанных в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к способу получения композиции (например, фармацевтической композиции), включающему смешение PVA соединения, описанного в настоящей заявке, и фармацевтически приемлемого носителя, разбавителя или наполнителя.
Согласно другому аспекту, настоящее изобретение относится к способу получения композиции (например, фармацевтической композиции), включающему смешение PVA соединения, описанного в настоящей заявке; одного или более (например, 1, 2, 3, 4) дополнительных терапевтических агентов, описанных в настоящей заявке; и фармацевтически приемлемого носителя, разбавителя или наполнителя.
Применение
Соединения, описанные в настоящей заявке, могут применяться, например, для лечения заболеваний и нарушений, которые можно облегчить с помощью ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу (например, Der p 1, Der f 1, Eur m 1), таких как, например, астма; ринит; аллергический конъюнктивит; атопический дерматит; аллергическое состояние, вызванное пылевыми клещами; аллергическое состояние, вызванное аллергеном пылевых клещей 1 группы, представляющим собой пептидазу; и атопия у собак.
Применение способов ингибирования аллергена пылевых клещей 1 группы. представляющего собой пептидазу
Согласно одному аспекту, настоящее изобретение относится к способу ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу (например, Der p 1, Der f 1, Eur m 1) in vitro или in vivo, включающему приведение в контакт аллергена пылевых клещей 1 группы, представляющего собой пептидазу, с эффективным количеством PVA соединения, описанного в настоящей заявке.
Согласно одному аспекту, настоящее изобретение относится к способу ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу (например, Der p 1, Der f 1, Eur m 1) в клетке in vitro или in vivo, включающему приведение в контакт указанной клетки с эффективным количеством PVA соединения, описанного в настоящей заявке.
Подходящие анализы для выявления ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу, описаны в настоящей заявке и/или известны в данной области техники.
Применение в способах терапевтического лечения
Согласно другому аспекту, настоящее изобретение относится к PVA соединению, описанному в настоящей заявке, для применения согласно способу лечения человека или животного с помощью терапии.
Согласно другому аспекту, настоящее изобретение относится к PVA соединению, описанному в настоящей заявке, в комбинации с одним или более (например, 1, 2, 3, 4) дополнительными терапевтическими агентами, описанными в настоящей заявке, для применения согласно способу лечения человека или животного с помощью терапии.
Применение для получения лекарственных средств
Согласно другому аспекту, настоящее изобретение относится к применению PVA соединения, описанного в настоящей заявке, для получения лекарственного средства для применения в лечении.
Согласно одному варианту реализации изобретения, лекарственное средство содержит PVA соединение.
Согласно другому аспекту, настоящее изобретение относится к применению PVA соединения, описанного в настоящей заявке, и одного или более (например, 1, 2, 3, 4) дополнительных терапевтических агентов, описанных в настоящей заявке, для получения лекарственного средства для применения в лечении.
Согласно одному варианту реализации изобретения, лекарственное средство содержит PVA соединение и один или более (например, 1, 2, 3, 4) дополнительных терапевтических агентов.
Способы лечения
Согласно другому аспекту, настоящее изобретение относится к способу лечения, включающему введение пациенту, нуждающемуся в указанном лечении, терапевтически эффективного количества PVA соединения, описанного в настоящей заявке, предпочтительно в форме фармацевтической композиции.
Согласно другому аспекту, настоящее изобретение относится к способу лечения, включающему введение пациенту, нуждающемуся в указанном лечении, терапевтически эффективного количества PVA соединения, описанного в настоящей заявке, предпочтительно в виде фармацевтической композиции, и одного или более (например, 1, 2, 3, 4) дополнительных терапевтических агентов, описанных в настоящей заявке, предпочтительно в виде фармацевтической композиции.
Подвергаемые лечению состояния: заболевания и нарушения, опосредованные аллергеном пылевых клещей 1 группы, представляющим собой пептидазу
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение заболевания или нарушения, опосредованного аллергеном пылевых клещей 1 группы, представляющим собой пептидазу (например, Der p 1, Der f 1, Eur m 1).
Подвергаемые лечению состояния: заболевания и нарушения, которые можно облегчить путем ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение заболевания или состояния, которое можно облегчить путем ингибирования аллергена пылевых клещей 1 группы, представляюшего собой пептидазу (например, Der p 1, Der f 1, Eur m 1).
Подвергаемые лечению состояния: конкретные заболевания и нарушения
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение астмы, например, атопической астмы; аллергической астмы; атопической бронхиальной IgE-опосредованной астмы; бронхиальной астмы; экзогенной астмы; индуцированной аллергеном астмой; аллергической астмы, обостряемой вирусной респираторной инфекцией; инфекционной астмы; инфекционной астмы, вызванной бактериальной инфекцией; инфекционной астмы, вызванной грибковой инфекцией; инфекционной астмы, вызванной протозойной инфекцией; или инфекционной астмы, вызванной вирусной инфекцией.
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение бронхиальной гиперреактивности, связанной с астмой; или бронхиальной гиперчувствительности, связанной с астмой.
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение ремоделирования дыхательных путей, связанного с аллергическим заболеванием легких, например, ремоделирования дыхательных путей, связанного с астмой.
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение астмы, сопровождающейся хроническим обструктивным заболеванием легких, например, астмы, сопровождающейся эмфиземой; или астмы, сопровождающейся хроническим бронхитом.
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение ринита, например, аллергического ринита; круглогодичного ринита; персистирующего ринита или IgE-опосредованного ринита.
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение аллергического конъюнктивита, например, IgE-опосредованного конъюнктивита.
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение атопического дерматита.
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение аллергического состояния, вызванного пылевыми клещами.
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение аллергического состояния, вызванного аллергеном пылевых клещей 1 группы, представляющим собой пептидазу (например, Der p 1, Der f 1, Eur m 1).
Согласно одному варианту реализации изобретения (например, применению в способах терапии, применению для получения медикаментов, способам лечения), лечение представляет собой лечение атопия у собак.
Лечение
В настоящей заявке термин «лечение» при использовании в контексте лечения состояния в целом относится к лечению и терапии человека или животного (например, в области ветеринарии), где достигается некоторый желаемый терапевтический эффект, например, подавление прогрессирования состояния, и включает снижение скорости прогрессирования состояния, остановка прогрессирования состояния, облегчение симптомов состояния, облегчение состояния и вылечивание состояния. Также включено проведение лечения в качестве профилактической меры (т.е., профилактики). Например, применение у пациентов, у которых еще не развилось состояние, но которые имеют риск развития указанного состояния, включено в термин «лечение».
Например, лечение включает профилактику астмы, уменьшение частоты возникновения астмы, снижение тяжести астмы, облегчение симптомов астмы и т.д..
В настоящей заявке термин «терапевтически эффективное количество» относится к такому количеству соединения или материала, композиции или формы дозирования, содержащей указанное соединение, которое является эффективным для обеспечения некоторого желаемого терапевтического эффекта, в соответствии с благоприятным соотношением польза/риск, при введении в соответствии с желаемой схемой лечения.
Комбинированная терапия
Термин «лечение» включает комбинированное лечение и терапию, в которой комбинируются две или более схемы лечения или терапия, например, последовательно или параллельно. Например, соединения, описанные в настоящей заявке, могут также использоваться в комбинированной терапии, например, в сочетании с другими агентами.
Типичные примеры комбинации для ингаляционного применения в лечении респираторного заболевания представляют собой фиксированные комбинации агонистов глюкокортикоидного рецептора и агонистов бета-2-адренорецептора. Продукт указанной комбинации представляет собой «адваир» (также известный как «серетид»), который представляет собой фиксированную комбинацию пропионата флутиказона и салметерола. Указанные комбинации могут использоваться в устройствах сухого порошка, ингаляторах отмеренных доз с распылением сжатым воздухом и небулайзерах. Многие другие агенты для лечения респираторных заболеваний могут использоваться в фиксированных комбинациях в указанных устройствах. Они также могут вводиться раздельно из различных устройств в различных относительных дозах.
Комбинированный продукт для ингаляции представляет собой фиксированную комбинацию соединения, описанного в настоящей заявке, с одним или более дополнительными агентами (в которой отношения рассчитывают на основании отдельных компонентов и выбирают из подходящего диапазона экспериментальным путем) совместно с подходящими наполнителями.
Например, согласно одному аспекту, настоящее изобретение относится к соединению, описанному в настоящей заявке, в комбинации с одним или более (например, 1, 2, 3, 4) дополнительными терапевтическими агентами.
Таким образом, агенты (т.е., соединение, описанное в настоящей заявке, плюс один или более других агентов) могут вводиться одновременно в фиксированной комбинации или в разное время путем раздельного варьирования режима дозирования из одного или из разных ингаляционных устройств. Точный режим дозирования в комбинированном или последовательном лечении определяется в соответствии со свойствами терапевтического агента (агентов).
Дополнительные терапевтические агенты
PVA соединения, описанные в настоящей заявке, могут применяться в комбинации с одним или более (например, 1, 2, 3, 4) дополнительных терапевтических агентов, например, в комбинированной терапии, как описано в настоящей заявке.
Согласно одному варианту реализации изобретения, один или более дополнительных терапевтических агентов выбраны из агентов, которые используются или могут использоваться для лечения респираторного заболевания.
Согласно одному варианту реализации изобретения, один или более дополнительных терапевтических агентов выбраны из:
противоастматического агента и противоаллергического агента.
Согласно одному варианту реализации изобретения, один или более дополнительных терапевтических агентов выбраны из:
агониста бета2-адренергического рецептора;
антагониста мускаринового рецептора М3;
одновременного агониста бета2-адренорецептора - антагониста мускаринового рецептора М3;
агониста глюкокортикоидного рецептора;
антагониста лейкотриена;
ингибитора 5-липоксигеназы;
кромона;
иммунодепрессанта;
иммуномодулятора, например, агониста одного или более Toll-подобных рецепторов (например, TLR2, TLR4, TLR7, TLR8, TLR9), или вакцины;
производного ксантина;
селективного ингибитора фосфодиэстеразного (PDE) изофермента, например, ингибитора PDE4 и/или PDE5;
ингибитора определенных ферментов с киназной активностью, например, митоген-активируемых протеинкиназ (MAP) p38, I-каппа-В киназы 2 (IKK2), тирозиновой протеинкиназы (Syk) и фосфоинозитид-3-киназы гамма (PI3Kgamma);
антагониста рецептора гистамина типа 1;
агониста альфа-адренорецепторов, вазоконстриктора, симпатомиметика;
ингибитора матриксной металлопротеиназы;
модулятора функции хемокинового рецептора;
цитокина;
модулятора функции цитокинов;
агента, действующего на цитокиновый сигнальный путь;
иммуноглобулина;
иммуноглобулинового состава;
антагониста, модулирующего функцию иммуноглобулина;
антитела, модулирующего функцию иммуноглобулина;
легочного поверхностно-активного белка, в частности, SP-A, SP-D;
ингибитора Der p 3, ингибитора Der p 6 и ингибитора Der p 9.
Применение в качестве акарицида
PVA соединения, описанные в настоящей заявке, могут также использоваться в качестве акарицида, например, для контроля популяции клещей или уничтожения клещей, например, пылевых клещей.
Согласно другому аспекту, настоящее изобретение относится к PVA соединениям, описанного в настоящей заявке, для использования в качестве акарицида.
Согласно другому аспекту, настоящее изобретение относится к композиции, содержащей PVA соединение, описанное в настоящей заявке, для применения в качестве акарицида.
Согласно другому аспекту, настоящее изобретение относится к акарицидной композиции, содержащей PVA соединение, описанное в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к применению PVA соединения, описанного в настоящей заявке, в качестве акарицида.
Согласно другому аспекту, настоящее изобретение относится к способу уничтожения клещей (например, пылевых клещей), включающему действие на указанных клещей эффективным количеством PVA соединения, описанного в настоящей заявке.
Согласно другому аспекту, настоящее изобретение относится к способу регуляции (например, ограничения) популяции клещей (например, пылевых клещей), включающему действие на клещей эффективным количеством PVA соединения, описанного в настоящей заявке.
Другие способы применения
PVA соединения, описанные в настоящей заявке, могут также использоваться в качестве добавок для клеточных культурам для ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу (например, Der p 1, Der f 1, Eur m 1).
PVA соединения, описанные в настоящей заявке, могут также использоваться как часть анализа in vitro, например, для определения возможности получения благоприятного эффекта от лечения интересующим соединением у хозяина, который является кандидатом на указанное лечение.
PVA соединения, описанные в настоящей заявке, могут также использоваться в качестве контроля, например, в анализе, для идентификации других соединений, других ингибиторов аллергена пылевых клещей 1 группы, представляющего собой пептидазу, других противоастматических агентов и т.д.
Наборы
Согласно одному аспекту, изобретение относится к набору, содержащему (а) PVA соединение, описанное в настоящей заявке, или композицию, содержащую PVA соединение, описанное в настоящей заявке, например, предпочтительно представленную в подходящем контейнере и/или в подходящей упаковке; и (b) инструкции по применению, например, письменные инструкции по введению соединения или композиции.
Согласно одному варианту реализации изобретения, набор также содержит один или более (например, 1, 2, 3, 4) дополнительных терапевтических агентов, описанных в настоящей заявке.
Письменные инструкции могут также включать перечень показаний, для которых применение активного ингредиента является подходящим лечением.
Пути введения
PVA соединение или фармацевтическая композиция, содержащая PVA соединение, может вводиться субъекту любым удобным способом введения, системно/периферически или местно (т.е., в место желаемого приложения действия).
Способы введения включают, но не ограничиваются ими, пероральное (например, путем приема внутрь); трансбуккальное; сублингвальное; трансдермальное (включая, например, с помощью наклейки, пластыря и т.д.); трансмукозальное (включая, например, с помощью наклейки, пластыря и т.д.); интраназальное (например, с помощью назального спрея, капель или из распылителя или устройства для доставки сухого порошка); глазное (например, с помощью глазных капель); легочное (например, путем ингаляционной или инсуффляционной терапии с использованием, например, аэрозоля, например, через рот или нос); ректальное (например, с помощью суппозитория или клизмы); вагинальное (например, с помощью пессария); парентеральное введение, например, путем инъекции, включая подкожную, внутрикожную, внутримышечную, внутривенную, внутриартериальную, внутрисердечную, интратекальную, интраспинальную, внутрикапсулярную, подкапсулярную, внутриглазничную, внутрибрюшинную, внутритрахеальную, субкутикулярную, внутрисуставную, субарахноидальную и внутригрудинную; введение путем имплантации депо или резервуара, например, подкожной или внутримышечной.
Субъект/пациент
Субъект/пациент может представлять собой хордовое, позвоночное, млекопитающее, плацентарное млекопитающее, сумчатое (например, кенгуру, вомбата), грызуна (например, морскую свинку, хомячка, крысу, мышь), представителя мышиных (например, мышь), зайцеобразных (например, кролика), птичьих (например, птицу), псовых (например, собаку), кошачьих (например, кошку), лошадиных (например, лошадь), свиньих (например, свинью), овечьих (например, овцу), бычьих (например, корову), примата, человекообразную обезьяну (например, мартышку или обезьяну), обезьяну (например, игрунку, бабуина), мартышку (например, гориллу, шимпанзе, орангутанга, гиббона) или человека.
Более того, субъект/пациент может находиться на любой стадии развития, например, на стадии эмбриона.
Согласно одному варианту реализации изобретения, субъект/пациент представляет собой человека.
Согласно одному варианту реализации изобретения, субъект/пациент представляет собой собаку.
Лекарственные Формы
Несмотря на то, что PVA соединение можно вводить отдельно, предпочтительно, чтобы указанное соединение представлено в виде фармацевтической лекарственной формы (например, композиции, состава, медикамента), содержащей по меньшей мере одно PVA соединение, описанное в настоящей заявке, совместно с одним или более другими фармацевтически приемлемыми ингредиентами, хорошо известными специалистам в данной области техники, включая, но не ограничиваясь ими, фармацевтически приемлемые носители, разбавители, наполнители, адъюванты, основы, буферы, консерванты, антиоксиданты, скользящие вещества, стабилизаторы, солюбилизаторы, поверхностно-активные вещества (например, увлажнители), маскирующие агенты, красящие вещества, ароматизаторы и подсластители. Лекарственная форма может также включать другие активные агенты, например, другие терапевтические или профилактические агенты.
Таким образом, согласно настоящему изобретению, также предложены фармацевтические композиции, определенные выше, и способы получения указанных фармацевтический композиций, включающие смешение по меньшей мере одного PVA соединения, описанного в настоящей заявке, с одним или более другими фармацевтически приемлемыми ингредиентами, хорошо известными специалистам в данной области техники, например, носителями, разбавителями, наполнителями и т.д. Если указанная фармацевтическая композиция представлена в виде дискретных единиц (например, таблеток и т.д.), то каждая указанная единица содержит предварительно определенное количество (дозировку) соединения.
Термин «фармацевтически приемлемый» при использовании в настоящей заявке, относится к соединениям, ингредиентам, материалам, композициям, формам дозирования и т.д., которые, по результатам тщательной медицинской проверки подходят для применения в контакте с тканями интересующего субъекта (например, человека) и не проявляют избыточной токсичности, не вызывают раздражения, аллергического реакции или других проблем или осложнений, в соответствии с благоприятным соотношением польза/риск. Каждый носитель, разбавитель, наполнитель и т.д. также должен являться «приемлемым» с точки зрения совместимости с другими ингредиентами лекарственной формы.
Подходящие носители, разбавители, наполнители и т.д. можно найти в стандартных фармацевтических текстах, например, Remington′s Pharmaceutical Sciences. 18th edition, Mack Publishing Company, Easton, Pa., 1990; и Handbook of Pharmaceutical Excipients. 5th edition, 2005.
Лекарственные формы могут быть получены с помощью любых способов, хорошо известных в области фармации. Указанные способы включают этап приведения соединения во взаимодействие с носителем, который содержит один или более вспомогательных ингредиентов. В целом, лекарственные формы готовят путем равномерного и тщательного приведения соединения во взаимодействие с носителями (например, жидкими носителями, мелкоизмельченным твердым носителем и т.д.) и, при необходимости, последующего придания формы продукту.
Лекарственная форма может быть получена в виде формы с быстрым или медленным высвобождением; немедленным, отсроченным, регулируемым или замедленным высвобождением; или их комбинации.
Лекарственные формы соответствующим образом могут быть представлены в виде жидкости, раствора (например, водного, неводного), суспензии (например, водной, неводной), эмульсии (например, по типу «масло-в-воде», «вода-в-масле»), эликсира, сиропов, электуариев, ополаскивателей для полости рта, капель, таблеток (включая, например, таблетки с покрытием), гранул, порошков, таблеток для рассасывания, пастилок, капсул (включая, например, твердые и мягкие желатиновые капсулы), пакетиков, пилюлей, ампул, болюсов, суппозиториев, пессариев, настоев, гелей, паст, мазей, кремов, лосьонов, масел, пен, спреев, распылителей или аэрозолей.
Лекарственные формы соответствующим образом могут быть представлены в виде наклейки, лейкопластыря, повязки, накладки и т.д., пропитанной одним или более соединениями и необязательно одним или более другими фармацевтически приемлемыми ингредиентами, включая, например, усилители проникновения, проницаемости и абсорбции. Лекарственные формы также соответствующим образом могут быть представлены в виде депо или резервуара.
Соединение может быть растворено, суспендированного или смешено с одним или более другими фармацевтически приемлемыми ингредиентами. Соединение может быть представлено в виде липосомы или другой микрочастицы, созданной для направления соединение, например, к компонентам крови или одному или более органам.
Лекарственные формы, подходящие для введения в легкое (например, путем ингаляции или инсуффляционной терапии с использованием, например, аэрозоля, например, через рот) включают лекарственные формы, представленные в виде раствора или суспензии для доставки из небулайзера; сухого порошка для использования в соответствующем устройстве для ингаляции; и в виде аэрозольного спрея для доставки из упаковки со сжатым воздухом с использованием подходящего пропеллента, такого как дихлордофторметан (CFC-12), трихлорфторметан, дихлортетрафторэтан, HFA-134a, HFA-227, HCFC-22, HFA-152, изобутен, диоксид углерода или Других подходящих газов. Устройства для указанных способов доставки являются доступными. Лекарственные формы, предназначенные для доставки через нос, могут вводиться в виде водных растворов или суспензий, в виде растворов или суспензий в подходящих пропеллентах или в виде сухих порошков. Для доставки через нос доступны капельницы для носа, небулайзеры, распылители, ингаляторы отмеренных доз с распыление сжатым воздухом и ингаляторы сухого порошка.
Для введения путем ингаляции активное соединение предпочтительно представлено в форме микрочастиц. Подходящие микрочастицы могут быть получены с помощью различных методов, включая сушку распылением, лиофильную сушку и микронизацию.
Микрочастицы могут быть представлены совместно с наполнителями, способствующими доставке и высвобождению. Например, в лекарственной форме сухого порошка микрочастицы могут быть представлены совместно с большими частицами носителя, способствующими току, например, из ингалятора сухого порошка (DPI) в легкие. Подходящие частицы носителя хорошо известны в данной области техники и включают лактозные частицы; указанные частицы могут иметь масс-медианный аэродинамический диаметр >90 мкм.
Для доставки с помощью аэрозоля активное соединение может вводиться согласно способу, совместимому с используемой ингаляционной системой. Подходящая аэрозольная лекарственная форма помимо активного соединения сожжет содержать наполнители, такие как, например, пропеллент (например, Frigen в случае аэрозолей отмеренных доз), поверхностно-активные вещества, эмульгаторы, стабилизаторы, консерванты, ароматизаторы, наполнители (например, лактозу в случае порошковых ингаляторов) и, если применимо, один или более дополнительных активных соединений.
Для ингаляции лекарственных форм типа микрочастиц известно большое количество систем, с помощью которых могут создаваться и вводиться аэрозоли с оптимальным размером частиц при использовании способа ингаляции, подходящего для пациента. Помимо применения адаптеров (спейсерных устройств, экспандеров) и грушевидных контейнеров (например, Nebulator™, Volumatic™) и автоматических устройств с аэрозольным распылением (например, Autohaler™), для дозированных аэрозолей, в частности, в случае порошковых ингаляторов, доступен ряд технических растворов (например, Diskhaler™, Rotadisk™, Turbohaler™). Дополнительно активное соединение может доставляться через многокамерное устройство, таким образом, обеспечивая возможность доставки комбинации агентов.
Для введения в нос или легкое может также использоваться активное соединение, представленное в виде водной дисперсии наночастиц или аэрозольной лекарственной формы, содержащей наночастицы сухого порошка, или в виде аэрозольной лекарственной формы на основе пропеллента. Подходящие наночастицы можно получать путем сушки распылением или лиофилизации водных дисперсий наночастиц лекарственных средств. Способы получения дисперсий наночастиц лекарственных средств, получения водных лекарственных форм, лекарственных форм в виде сухого порошка и лекарственных форм на основе пропеллента наночастиц лекарственных средств и их применение в системах доставки аэрозолей являются известными (см., например, Bosch et al., 2009).
Лекарственные формы, подходящие для перорального введения (например, путем приема внутрь), включают жидкости, растворы (например, водные, неводные), суспензии (например, водные, неводные), эмульсии (например, по типу «масло-в-воде», «вода-в-масле»), эликсиры, сиропы, электуарии, таблетки, гранулы, порошки, капсулы, крахмальные капсулы, пилюли, ампулы, болюсы.
Лекарственные формы, подходящие для буккального введения, включают ополаскиватели для полости рта, таблетки для рассасывания, пастилки, а также наклейки, лейкопластыри, депо и резервуары. Таблетки для рассасывания, как правило, содержат соединение в ароматизированной основе, обычно сахарозе и гуммиарабике или траганте. Пастилки, как правило, содержат соединение в инертной матрице, такой как желатин и глицерин или сахароза и гуммиарабик. Ополаскиватели для полости рта, как правило, содержат соединение в подходящем жидком носителе.
Лекарственные формы, подходящие для сублингвального введения, включают таблетки, таблетки для рассасывания, пастилки, капсулы и пилюли.
Лекарственные формы, подходящих для перорального трансмукозального введения, включают жидкости, растворы (например, водные, неводные), суспензии (например, водные, неводные), эмульсии (например, типа «масло-в-воде», типа «вода-в-масле»), ополаскиватели для полости рта, таблетки для рассасывания, пастилки, а также наклейки, лейкопластыри, депо и резервуары.
Лекарственные формы, подходящие для не перорального трансмукозального введения, включают жидкости, растворы (например, водные, неводные), суспензии (например, водные, неводные), эмульсии (например, по типу «масло-в-воде», «вода-в-масле»), суппозитории, пессарии, гели, пасты, мази, крема, лосьоны, масла, а также наклейки, лейкопластыри, депо и резервуары.
Лекарственные формы, подходящие для трансдермального введения, включают гели, пасты, мази, крема, лосьоны и масла, а также наклейки, лейкопластыри, бандажи, повязки, депо и резервуары.
Таблетки могут быть получены с помощью стандартных способов, например, прессования или формования, необязательно с одним или более вспомогательных ингредиентов. Прессованные таблетки могут быть получены путем прессования в подходящем аппарате соединения в легкосыпучей форме, например, в форме порошка или гранул, необязательно смешанных с одним или более связующими веществами (например, повидоном, желатином, гуммиарабиком, сорбитолом, трагантом, гидроксипропилметилцеллюлозой); наполнителями или разбавителями (например, лактозой, микрокристаллической целлюлозой, гиброфосфатом кальция); веществами, обеспечивающими скольжение (например, стеаратом магния, тальком, диокисдом кремния); дезинтегрирующими веществами (например, гликолятом крахмала натрия, поперечно сшитым повидоном, поперечно сшитой карбоксиметилцеллюлозой натрия); поверхностно-активными или диспергирующими или увлажняющими агентами (например, лаурилсульфатом натрия); консервантами (например, метил-п-гидроксибензоатом, пропил-п-гидроксибензоатом, сорбиновой кислотой); отдушками, усилителями вкуса и подсластителями. Формованные таблетки могут быть получены путем формования в подходящем аппарате смеси порошкообразного соединения, смоченной инертной жидкостью. Таблетки могут необязательно иметь покрытие или риску и могут быть представлены в форме, обеспечивающей медленное или контролируемое высвобождение соединения с использованием, например, гидроксипропилметилцеллюлозы в различных пропорциях с получением желаемого профиля высвобождения. Таблетки необязательно могут иметь покрытие, например, для регуляции высвобождения, например энтеросолюбильное покрытие, для обеспечения высвобождения в участках кишечника, а не в желудке.
Мази, как правило, готовят из соединения и парафиновой или водорастворимой основы для мази.
Кремы, как правило, получают из соединения и основы для крема по типу «масло-в-воде». При необходимости водная фаза основы для крема может включать, например, по меньшей мере примерно 30% масс./ масс. многоатомного спирта, т.е., спирта, содержащего две или более гидроксильных групп, такого как пропиленгликоль, бутан-1,3-диол, маннит, сорбитол, глицерин и полиэтиленгликоль и их смеси. Лекарственные формы для наружного применения желательно содержат соединение, которое усиливает абсорбцию или проникновение соединения через кожу или другие пораженные зоны. Примеры указанных усилителей проникновения через кожу включают диметилсульфоксид и родственные ему аналоги.
Эмульсии, как правило, получают из соединения и масляной фазы, которая может необязательно содержать только эмульгирующее вещество (также называемое эмульгатором) смесь по меньшей мере одного эмульгатора с жиром или маслом или жиром и маслом. Предпочтительно гидрофильный эмульгатор содержится совместно с липофильным эмульгатором, который действует в качестве стабилизатора. Также предпочтительно содержится как масло, так и жир. Эмульгатор (эмульгаторы), вместе со стабилизатором (стабилизаторами) или без него, создает так называемый эмульгирующий воск, и воск совместно с маслом и/или жиром создает так называемую эмульгирующую основу для мази, которая формирует масляную дисперсную фазу лекарственных форм типа крема.
Подходящие эмульгаторы и стабилизаторы эмульсии включают твин 60, спан 80, цетостеариловый спирт, миристиловый спирт, глицерилмоностеарат и лацрилсульфат натрия. Выбор подходящих масел или жиров для лекарственной формы основан на достижении желаемых косметических свойств, так как растворимость соединения в большинстве масел, которые могут использоваться в лекарственные формах типа фармацевтических эмульсий может быть очень низкой. Таким образом, крем предпочтительно должен представлять собой не жирный, не оставляющий пятен и смываемый продукт с подходящей консистенцией, предотвращающей вытекание из тюбиков или других контейнеров. Могут использоваться одно- или двухосновные сложные алкиловые эфиры с прямой или разветвленной цепью, такие как диизоадипат, изоцетилстеарат, сложный пропиленгликолиевый диэфир кокосовых жирных кислот, изопропилмиристат, дицилолеат, изопропилпальмитат, бутилстеарат, 2-этилгексилпальмитат или смесь сложных эфиров с разветвленной цепью, известная как Crodamol CAP, причем последние три из указанных являются предпочтительными сложными эфирами. Указанные эфиры могут использоваться отдельно или в комбинации в зависимости от требуемых характеристик. Альтернативно, могут использоваться липиды с высокой температурой плавления, такие как белый мягкий парафин и/или жидкий парафин или другие минеральные масла.
Лекарственные формы, подходящие для интраназального введения, где носитель является жидким, и лекарственное средство может вводиться в виде водного раствора или суспензии в подходящем носителе или пропелленте, включая, например, назальный спрей, капли в нос или аэрозольные формы для введения с помощью небулайзера, с помощью ингалятора отмеренных доз с распылением сжатым воздухом или распылителя, включают водный или масляные составы соединения.
Лекарственные формы, подходящие для интраназального введения, где носитель является твердым, включают, например, лекарственные формы, представленные в виде крупного порошка с размером частиц, например, в диапазоне от примерно 20 до примерно 500 микрон, которые вводятся в соответствии со способом, согласно которому делается вдох через нос, т.е., путем быстрой ингаляции порошка через носовой ход из контейнера, который необходимо держать непосредственно перед носом.
Лекарственные формы, подходящие для глазного введения, включают глазные капли, где соединение растворено или суспендировано в подходящем носителе, в частности, водном растворителе, для соединения.
Лекарственные формы, подходящие для ректального введения, могут быть представлены в виде суппозитория с подходящей основой, включающей, например, природные или гидрогенизированные масла, воска, жиры, полутвердые или жидкие полиолы, например, масло какао или салицилат; или в виде раствора или суспензии для лечения с помощью клизмы.
Лекарственные формы, подходящие для вагинального введения, могут быть представлены в виде лекарственных форм в виде пессариев, тампонов, кремов, гелей, паст, пен или спрея, содержащих помимо соединения такие носители, которые, как известно в данной области техники, являются подходящими.
Лекарственные формы, подходящие для парентерального введения (например, путем инъекции), включают водные или неводные, изотонические, апирогенные стерильные жидкости (например, растворы, суспензии), в которых соединение растворено, суспендировано или включено другим образом (например, в липосоме или других микрочастицах). Указанные жидкости могут дополнительно содержать другие фармацевтически приемлемые ингредиенты, такие как антиоксиданты, буферы, консерванты, стабилизаторы, бактериостатики, суспендирующие агенты, загустители и растворы, которые делают лекарственную форму изотоничной крови (или другой соответствующей жидкости организма) предполагаемого реципиента. Примеры наполнителей включают, например, воду, спирты, полиолы, глицерин, растительные масла и т.д. Примеры подходящих изотонических носителей для использования в указанных лекарственных формах включают инъекции хлорида натрия, инъекции раствора Рингера или раствора Рингера с лактатом. Как правило, концентрация соединения в жидкости составляет от примерно 1 нг/мл до примерно 10 мкг/мл. Лекарственные формы могут быть представлены в однодозовых или многодозовых герметичных контейнерах, например, ампулах и пробирках, и могут храниться в замороженном-высушенном (лиофилизированном) состоянии, требующем только добавления стерильного жидкого носителя, например, воды для инъекций, непосредственно перед применением. Растворы и суспензии для немедленного введения могут быть получены из стерильных порошков, гранул и таблеток.
Дозировка
Специалисту в данной области техники ясно, что соответствующие дозировки PVA соединений и композиций, содержащих PVA соединения, могут варьировать в зависимости от конкретного пациента. Определение оптимальной дозировки в целом включает взвешивание соотношения терапевтической эффективности и любого риска или вредных побочных эффектов. Выбранный уровень дозировки зависит от различных факторов, включая, но не ограничиваясь ими, активность конкретного PVA соединения, способ введения, время введение, скорость выведения PVA соединения, продолжительность лечения, другие лекарственные средства, соединения и/или материалы, используемые в комбинации, тяжесть состояния и вид, пол, возраст, масса тела, состояние, общее состояние здоровья и история болезни пациента. Несмотря на то, что в целом дозировка соединения выбирается на основании достижения локальных концентраций в месте приложения действия, приводящих к достижению желаемого эффекта и не оказывающих значительного вредного воздействия или неблагоприятных побочных эффектов, количество PVA соединения и способ введения в конечном итоге определяется врачом, ветеринаром или клиницистом.
В течение курса лечения может осуществляться введение в виде одной дозы, непрерывное или прерывистое (например, в виде дробной дозы с соответствующими интервалами). Методы определения наиболее эффективных способов и доз введения хорошо известны специалистам в данной области техники и варьируют в зависимости от используемой в терапии лекарственной формы, цели проведения указанной терапии, клетки (клеток)-мишени, на которую направлено лечение, и субъекта, подвергаемого лечению. Может осуществляться однократное или множественное введение в соответствии с уровнем дозы и схемой дозирования, выбранной лечащим врачом, ветеринаром или клиницистом.
В целом, подходящая доза PVA соединения находится в диапазоне от примерно 0,5 мкг до примерно 20 мг на килограмм массы тела субъекта в день. На практике верхняя граница для агента, вводимого в помощью ингалятора, определяется выбранным устройством для доставки. Если соединение представлено в виде соли, сложного эфира, амида, пролекарства и т.д., вводимое количество рассчитывается на основе исходного соединения и, таким образом, используемая в действительности масса пропорционально повышается.
ПРИМЕРЫ
Следующие примеры приведены исключительно для иллюстрации настоящего изобретения и не ограничивают объем изобретения, описанного в настоящей заявке.
Химический синтез
Аббревиатуры
Aq., водный;
Boc, трет-бутоксикарбонил;
Конц., концентрированный;
ДХМ, дихлорметан;
DIC, диизопропилкарбодиимид;
DIPEA, N,N-диизопропилэтиламин;
DMAP, 4-диметиламинопиридин;
ДМФА, диметилформамид;
ДМСО, диметилсульфоксид;
EDC, 1-этил-3-[3-диметиламинопропил]карбодиимид;
ELSD, детекция по светорассеянию испаренного образца;
экв., эквивалент;
Et2O, диэтиловый эфир;
EtOAc, этилацетат;
Fmoc, флуоренилметилоксикарбонил;
ч., часы;
HATU, гексафторфосфат 2-(7-аза-1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония;
HOAt, 1-гидрокси-7-азабензотриазол;
HOBt, N-гидроксибензотриазол;
ВЭЖХ, высоко эффективная жидкостная хроматография;
ЖХ/МС, жидкостная хроматография/масс-спектрометрия;
LDA, диизопропиламид лития;
мин., минуты;
МеОН, метанол;
МТБЭ, метил-трет-бутиловый эфир;
NMM, N-метилморфолин;
ЯМР, ядерно-магнитный резонанс;
Пет. эфир, петролейный эфир;
PS-тозилхлорид, тозилхлорид на полистироле;
Rf, фактор удерживания;
Rt, время удерживания;
Насыщ., насыщенный;
ТФУ, трифторуксусная кислота;
ТГФ, тетрагидрофуран;
TIPS, триизопропилсилан;
TMS, триметилсилан;
TBTU, тетрафторборат O-(бензотриазол-1-ил)-N,N,N′,N′-тетраметилурония;
СЭЖХ, сверхэффективная жидкостная хроматография;
% (по объему), процентное объемное отношение;
% масс./об., процентное отношение массы к объему.
Аналитические способы
Обращенно-фазовая препаративная ЖХ/МС: Препаративная ЖХ/МС с очисткой по массе с использованием препаративной колонки С-18 (Phenomenex Luna C18 (2), 100×21,2 мм, 5 мкм).
Анализ продуктов и промежуточных соединений проводили с использованием обращенно-фазовой аналитической ВЭЖХ/МС или СЭЖХ/МС, с использованием параметров, представленных ниже. Чистоту, как правило, оценивали с помощью диодной матрицы при 210-400 нм.
Аналитические способы ВЭЖХ:
AnalpH2_MeOH: Phenomenex Luna C18 (2), 3 мкм, 50×3,0 мм; А=вода+0,1% муравьиная кислота; В=МеОН; 45°C; % В: 0 мин. 5%, 4,4 мин. 95%, 5,2 мин. 95%, 5,21 мин. 5%, 6,5 мин. 5%; 1,1 мл/мин.
AnalpH2_МеОН_4 мин: Phenomenex Luna C18 (2), 3 мкм, 50×4,6 мм; А=вода+0,1% муравьиная кислота; В=МеОН; 45°C; % В: 0 мин. 5%, 1 мин. 37,5%, 3 мин. 95%, 3,5 мин. 95%, 3,51 мин. 5%, 4,5 мин. 5%; 2,25 мл/мин.
AnalpH9_MeOH: Phenomenex Luna C18 (2), 3 мкм, 50×4,6 мм; А=вода рН9 (вода/бикарбонат аммония 10 мм); В=МеОН; 45°C; % В: 0 мин. 5%, 1 мин. 37,5%, 3 мин. 95%, 3,5 мин. 95%, 3,51 мин. 5%, 4,5 мин. 5%; 2,25 мл/мин.
Aldehyde_QC_1A: Phenomenex Luna C18 (2), 5 мкм, 150×4,6 мм; А=вода+0,1% ТФУ; В=MeCN+0,1% ТФУ; 55°C; % В: 0 мин. 5%, 1 мин. 5%, 7 мин. 95%, 10 мин. 95%, 10,1 мин. 5%, 13 мин. 5%; 1,5 мл/мин.
Aldehyde_QC_1B: Phenomenex Luna C18 (2), 5 мкм, 150×4,6 мм; А=вода+0,1% ТФУ; В=MeCN+0,1% ТФУ; 55°C; % В: 0 мин. 5%, 0,5 мин. 5%, 7,5 мин. 95%, 10 мин. 95%, 10,1 мин. 5%, 13 мин. 5%; 1,5 мл/мин.
Aldehyde_QC_2: Phenomenex Luna C18 (2), 5 мкм, 150×4,6 мм; А=вода+0,1% ТФУ; В=MeCN+0,1% ТФУ; 50°C; % В: 0 мин. 5%, 0,1 мин. 5%, 8 мин. 95%, 10,5 мин. 95%, 10,55 мин. 5%, 13,5 мин. 5%; 1,5 мл/мин.
Aldehyde_QC (Gemini)_1: Phenomenex Gemini C18, 5 мкм, 150×4,6 мм; А=вода+0,1% ТФУ; В=MeCN+0,1% ТФУ; 55°C; % В: 0 мин. 5%, 0,5 мин. 5%, 7,5 мин. 95%, 10 мин. 95%, 10,1 мин. 5%, 13 мин. 5%; 1,5 мл/мин.
Aldehyde_QC (Gemini)_2: Phenomenex Gemini C18, 5 мкм, 150×4,6 мм; А=вода+0,1% ТФУ; В=MeCN+0,1% ТФУ; 50°C; % В: 0 мин. 5%, 0,1 мин. 5%, 8 мин. 95%, 10,5 мин. 95%, 10,55 мин. 5%, 13,5 мин. 5%; 1,5 мл/мин.
AnalpH2_MeOH_QC: Phenomenex Luna C18 (2), 5 мкм, 150×4,6 мм; А=вода+0,1% муравьиная кислоты; В=МеОН; 35°C; % В: 0 мин. 5%, 0,5 мин. 5%, 7,5 мин. 95%, 10 мин. 95%, 10,1 мин. 5%, 13,0 мин. 5%; 1,5 мл/мин.
AnalpH9_MeOH_QC: Phenomenex Luna C18 (2), 5 мкм, 150×4,6 мм; А=водный рН9 (вода/аммония bicarb 10 мм); В=МеОН; 35°C; % В: 0 мин. 5%, 0,5 мин. 5%, 7,5 мин. 95%, 10 мин. 95%, 10,1 мин. 5%, 13 мин. 5%; 1,5 мл/мин.
AnalpH_2QC: Phenomenex Luna C18 (2), 5 мкм, 150×4,6 мм; А=вода+0,1% муравьиная кислоты; В=ацетонитрил+0,1% муравьиная кислоты; 30°C; % В: 0 мин. 5%, 1 мин. 5%, 7 мин. 95%, 10 мин. 95%, 10,1 мин. 5%, 13 мин. 5%; 1,5 мл/мин.
AnalpH2_A1B1_QC: Phenomenex Gemini C18, 5 мкм, 150×4,6 мм; А=вода+0,1% муравьиная кислоты; В=ацетонитрил+0,1% муравьиная кислота; 40°C; %В: 0 мин. 5%, 0,5 мин. 5%, 7,5 мин. 95%, 10 мин. 95%, 10,1 мин. 5%, 13 мин. 5%; 1,5 мл/мин.
Аналитические способы СЭЖХ:
Способ_2_Bic: Acquity UPLC BEH С-8, 1,7 мкм, 100×2,1 мм; 40°C; А=0,005 М раствор бикарбоната аммония (водный); В=ацетонитрил; % В: 0 мин. 30%, 4 мин. 80%, 6 мин. 80%, 6,1 мин. 30%; 0,3 мл/мин.
Способ_2_ТФУ_СЭЖХ_2: Acquity UPLC BEH C18 1,7 мкм, 100×2,1 мм; 25°C; А=вода+0,025% ТФУ; В=ацетонитрил+0,025% ТФУ; % В: 0 мин. 30%, 4 мин. 80%, 6 мин. 80%, 6,1 мин. 30%; 0,4 мл/мин.
Способ_4_ТФУ_СЭЖХ_2: Acquity UPLC BEH C18 1,7 мкм, 100×2,1 мм; 25°C А=вода+0,025% ТФУ; В=ацетонитрил+0,025% ТФУ; % В: 0 мин. 10%, 4 мин. 80%, 6 мин. 80%, 6,1 мин. 10%; 0,3 мл/мин.
Общий подход для синтеза PVA соединений (I)
Некоторые общие способы синтеза PVA соединений согласно настоящему изобретению показаны в следующей схеме.
Схема 5
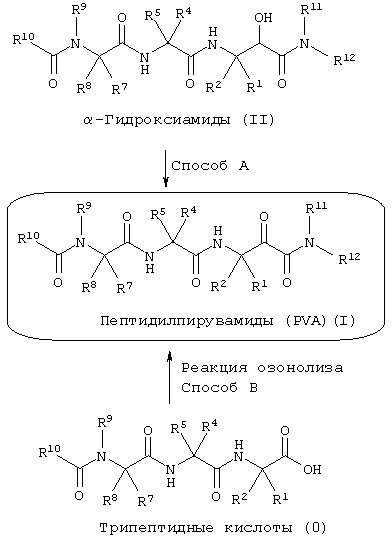
Способ А синтеза PVA соединений путем окисления α-гидроксиамидов (II)
Типичный способ
К перемешанному раствору соответствующего α-гидроксиамида (II) (1 экв.) в сухом ДХМ (1 мл/25-250 мг спирта) и необязательно сухом ДМФА (10-35% об./об. в зависимости от растворимости) при комнатной температуре порциями добавляли периодинан Десса-Мартина (1,6 экв.). Реакционную смесь перемешивали при комнатной температуре и за реакцией следили с помощью ЖХ/МС до полного превращения пирувамидного продукта (как правило, от 1 часа до 1 дня). При необходимости, добавляли дополнительную порцию периодинана Десса-Мартина для завершения окисления. Реакцию гасили путем добавления насыщенного (водного) раствора NaHCO3 (1 объем) и раствора (водного) Na2S2O3 (10% масс./об.). Смесь перемешивали в течение примерно 30 мин., разбавляли EtOAc (10 объемами) и промывали насыщенным (водным) раствором NaHCO3 (2×5 объемами), деионизированной водой (5 объемами) и солевым раствором (5 объемами). Органический слой затем сушили над MgSO4 и выпаривали. В результате очищения с помощью обращенно-фазовой препаративной ВЭЖХ в целом с последующей лиофилизацией получали желаемый пептидилпирувамид (I).
В некоторых примерах, в частности, где PVA соединения являлись растворимыми в воде, реакционную смесь концентрировали без выделения периодинана Десса-Мартина (DMP) после реакции окисления, осадок растворяли в ДМСО и непосредственно подвергали очистке с помощью обращенно-фазовой препаративной ВЭЖХ.
Альтернативно, в некоторых примерах реакция может осуществляться непосредственно в ДМСО.
Некоторые общие способы синтеза α-гидроксиамидов формулы (II) показаны в следующей схеме.
Схема 6

Пути 3 и 4 требуют синтеза дипептидных промежуточных соединений (А). Некоторые пути синтеза указанных соединений и конкретные примеры, полученные по указанным путям, описаны далее.
Синтез дипептидных промежуточных соединений (А)
Путь 1: Дипептидные промежуточные соединения (А) посредством твердофазного пептидного синтеза
Схема 7

Пептиды синтезировали на смоле Ванга с использованием стандартных способов сочетания амида (см., например, Chan, W.С. and White, P.D., Fmoc Solid Phase Peptide Synthesis A Practical Approach, Oxford University Press, 2000). Fmoc-аминокислоты получали от частных поставщиков (например, Advanced Chemtech, Bachem, NovaBiochem или Polypeptide). В реакциях сочетания пептида использовали чистый ДМФА, свободный от примеси диметиламина, для предотвращения любого нежелательного удаления Fmoc-группы. Для подтверждения успешного сочетания Fmoc-аминокислот использовали тесты Кайзера.
Типичный способ
Этап 1 - Сочетание первой аминокислоты со смолой Ванга:
Смолу Ванга вымачивали в подходящем объеме ДМФА, затем сушили в вакууме. Добавляли Fmoc-аминокислоты (6 экв.) с последующим добавлением подходящего объема ДМФА (5 мл/г смолы), достаточного, чтобы покрыть смолу и пептид, и полученную смесь перемешивали в течение 30 мин. После этого добавляли DIC (3 экв.) и DMAP (катализатор) и смесь перемешивали в течение 4-5 часов. Смолу сушили в вакууме, промывали ДХМ и MeOH, затем заново вымачивали в ДХМ. Успешное сочетание подтверждали путем осуществления 2 этапа с использованием небольшой порции смолы и проведения теста Кайзера для обнаружения свободной группы NH2. В целом, не определяли точное количество аминокислоты, связанной со смолой, и последующие реакции проводили на основе максимальной нагрузки, указанной поставщиком. Для аминокислот, которые были получены в предварительно соединенным со смолой Ванга виде, примерная нагрузка была указана поставщиком, и указанные данные использовали для расчета количества реагента для последующих этапов.
Этап 2 - Удаление защитной группы Fmoc:
Смолу перемешивали с соответствующим объемом 20% (по объему) пиперидина в ДМФА (5 мл/г смолы) в течение 1 часа, затем промывали ДМФА, ДХМ, MeOH и заново вымачивали в ДХМ. Положительный тест Кайзера (синий цвет) указывал на присутствие свободной группы NH2.
Этап 3 - Сочетание с получением амида:
Смолу перемешивали в соответствующем объеме ДМФА (~5 мл/г смолы) с подходящей Fmoc-аминокислотой (2 экв.) или кэпирующей группой R10CO2H (2 экв.), TBTU (2 экв.) и DIPEA (4 экв. или 6 экв. если, например, использовали соль HCl) в течение 4-5 часов. После этого смолу сушили в вакууме, промывали ДМФА, ДХМ, MeOH и заново вымачивали в ДХМ. Отрицательный тест Кайзера (отсутствие изменения цвета) указывал на то, что все свободные сайты аминогрупп являлись связанными. Если раствор оставался синим, Этап 3 повторяли.
Этапы 2 и 3 повторяли для сочетания дополнительных аминокислот и, при необходимости, кэпирующих групп.
Этап 4 - Расщепление смолы:
Смолу перемешивали с расщепляющим раствором, состоящим из 95% ТФУ, 2,5% TIPS и 2,5% воды (10 мл/г смолы), в течение 90 мин. и затем сливали в подходящую колбу. Смолу промывали ДХМ при вакуумном фильтровании. Затем растворитель выпаривали в вакууме, получали азеотропную смесь с толуолом для удаления остаточной воды или растирали с изо-гексаном и диэтиловым эфиром или МТБЭ, для получения осадка неочищенного продукта. Полученный пептид (А) либо использовали неочищенным, либо дополнительно очищали посредством растирания с Et2O, колоночной флэш-хроматографии или обращенно-фазовой препаративной ВЭЖХ.
Дипептидные промежуточные соединения (А), полученные по Пути 1

Rt=2,96 мин.;
m/z 341 (MH+);
твердое вещество белого цвета
Rt=3,78 мин.;
m/z 341 (MH+);
твердое вещество белого цвета
Rt=4,54 мин.;
m/z 417 (MH+);
твердое вещество бледно-розового цвета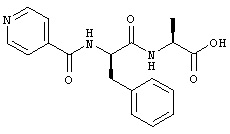
Rt=3,04 мин.;
m/z 342 (MH+);
твердое вещество бледно-оранжевого цвета
Rt=4,54 мин.;
m/z 433 (MH+);
твердое вещество белого цвета

Rt=3,59 мин.;
m/z 307 (MH+);
твердое вещество белого цвета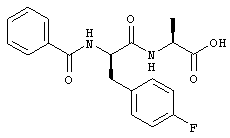
Rt=3,85 мин.;
m/z 359 (MH+);
твердое вещество белого цвета
Rt=3,98 мин.;
m/z 377 (MH+);
твердое вещество белого цвета
Rt=4,12 мин.;
m/z 367 (MH+);
твердое вещество белого цвета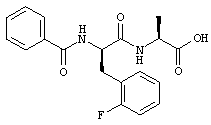
Rt=3,78 мин.;
m/z 359 (MH+);
твердое вещество белого цвета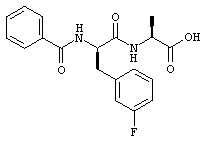
Rt=3,85 мин.;
m/z 359 (MH+);
твердое вещество белого цвета
Rt=4,23 мин.;
m/z 391 (MH+);
твердое вещество белого цвета
Rt=4,49 мин.;
m/z 417 (MH+);
твердое вещество белого цвета

Rt=4,26 мин.;
m/z 391 (MH+);
твердое вещество белого цвета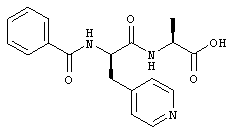
Rt=1,12 мин.;
m/z 342 (MH+);
твердое вещество белого цвета
Rt=1,77 мин.;
m/z 308 (МН+);
белая пена
Rt=1,51 мин.;
m/z 440 (MH+);
твердое вещество белого цвета
Rt=2,16 мин.;
m/z 393 (MH+);
твердое вещество белого цвета
Rt=2,38 мин.;
m/z 384 (MH+);
твердое вещество белого цвета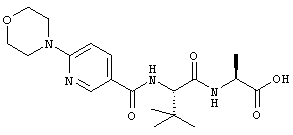
Rt=2,24 мин.;
m/z 393 (MH+);
твердое вещество белого цвета
Rt=2,90 мин.;
m/z 436 (MH+);
твердое вещество белого цвета

Rt=2,53 мин.;
m/z 398 (MH+);
твердое вещество белого цвета
Rt=2,74 мин.;
m/z 357 (МН+);
твердое вещество белого цвета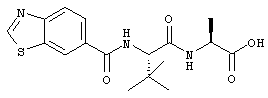
Rt=2,38 мин.;
m/z 364 (МН+);
твердое вещество белого цвета
Rt=2,13 мин.;
m/z 309 (MH+);
твердое вещество белого цвета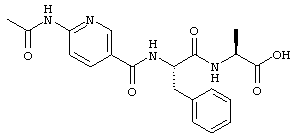
Rt=2,18 мин.;
m/z 399 (МН+);
твердое вещество белого цвета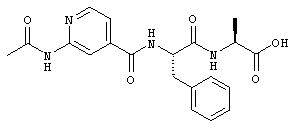
Rt=2,13 мин.;
m/z 399 (MH+);
твердое вещество белого цвета
Rt=2,08 мин.;
m/z 365 (MH+);
твердое вещество белого цвета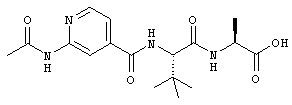
Rt=2,02 мин.;
m/z 365 (MH+);
твердое вещество белого цвета

Rt=1,52 мин.;
m/z 454 (MH+);
твердое вещество кремового цвета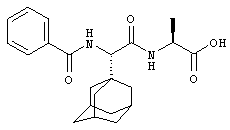
Rt=3,08 мин.;
m/z 385 (МН+);
твердое вещество белого цвета
Rt=2,20 мин.;
m/z 427 (MH+);
твердое вещество белого цвета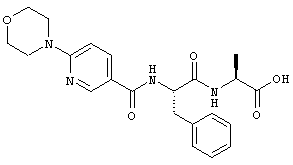
Rt=2,30 мин.;
m/z 427 (МН+);
бесцветное масло
RT 3,08 мин.;
m/z 441 (МН+);
твердое вещество белого цвета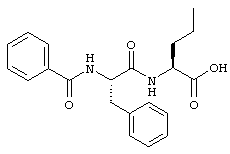
Rt=2,76 мин.;
m/z 369 (MH+);
твердое вещество белого цвета
Rt=0,71/0,84 мин.;
m/z 328 (MH+);
прозрачное твердое вещество
Путь 2: Дипептидные промежуточные соединения (А) посредством жидкофазного синтеза пептида
Схема 8

Типичный способ Этап 1 - Синтез сложных этиловых эфиров Boc-аминодипептида (3):
Раствор соединения (1) (1 экв.) в ТГФ (~ 1 г/10 мл) обрабатывали изобутилхлорформатом (1,05 экв.) при -40°C и NMM (1 экв.) и перемешивали при -40°C в течение 30 мин. К указанной выше реакционной смеси добавляли раствор соединения (2) (1,1 экв.) в смеси ДМФА и ТГФ (-1 г/ 4 мл, 1:1) при -40°C с последующим добавлением NMM (1 экв.). Полученную смесь перемешивали при -40°C в течение 2 часов. Выпавшую в осадок соль фильтровали и промывали EtOAc. Объединенный фильтрат промывали 10% масс./об. раствором лимонной кислоты, 5% масс./об. раствором NaHCO3, солевым раствором, сушили над Na2SO4, фильтровали и концентрировали в вакууме с получением неочищенного осадка. Указанный осадок в целом очищали с помощью флэш-хроматографии на силикагеле или обращенно-фазовой препаративной ВЭЖХ с получением желаемого соединения (3).
Этап 2 - Синтез сложных этиловых эфиров аминодипептида (4):
Раствор соединения (3) (1 экв.) в ДХМ (1 г/10 мл) обрабатывали ТФУ (5 экв.) при 0°C и перемешивали при комнатной температуре в течение 16 часов. Летучие вещества концентрировали и осадок растирали с Et2O (150 мл) с получением желаемого соединения (4).
Альтернативно указанную реакцию можно проводить путем растворения в ДХМ соединения (3), содержащего защитную группу Вое, и перемешивания с ~10 экв. 4 н. HCl в диоксане в течение до 18 часов.
Этап 3 - Синтез сложных этиловых эфиров амидодипептида (5):
Этап 3 может осуществляться с использованием различных условий сочетания амида, хорошо известных специалистам в данной области техники. Указанный этап включают реакцию соответствующей карбоновой кислоты с соединением формулы (4) в присутствии реагентов, таких как HATU, TBTU или EDC/HOBt, и третичного аминного основания, такого как DIPEA, в растворителях, таких как ДХМ или ДМФА. Альтернативно, соответствующий хлорангидрид может использоваться в присутствии третичного аминного основания в растворителях, таких как ДХМ.
Один из типичных способов представлен далее:
Синтез сложного этилового эфира (S)-2-((S)-2-бензоиламино-3-фенилпропиониламино)пропановой кислоты (для А1)
К раствору сложного этилового эфира (S)-2-((S)-2-амино-3-фенилпропиониламино)пропановой кислоты добавляли трифторацетат (10 г, 37,9 ммоль) и DIPEA (19,5 мл, 113,6 ммоль) в ДХМ (100 мл). Добавляли бензоилхлорид (4,0 мл, 34,1 ммоль) при -20°C и перемешивали при -20°C в течение 1 часа. Реакционную смесь фильтровали для удаления солей и фильтрат промывали 10% раствором лимонной кислоты (2×50 мл), 5% раствором NaHCO3 (2×50 мл) и солевым раствором (50 мл), соответственно, сушили над Na2SO4, фильтровали и концентрировали в вакууме с получением осадка, который растворяли в CHCl3 (20 мл) и растирали с н-пентаном. Выпавшее в осадок твердое вещество фильтровали и промывали смесью Et2O и н-пентана (50 мл, 1:1), затем сушили с получением сложного этилового эфира (S)-2-((S)-2-бензоиламино-3-фенилпропиониламино)пропановой кислоты (6,5 г, 47%) в виде твердого вещества белого цвета. Rf: 0,8 (10% MeOH/CHCl3); 1H ЯМР (400 МГц, ДМСО-d6): δ 8,60-8,55 (1Н, m), 7,76 (2H, d, J = 6,8 Гц), 7,52-7,35 (5Н, m), 7,27 (2H, t, J = 7,6 Гц), 7,18 (1Н, t, J = 7,6 Гц), 4,80-4,70 (1Н, m), 4,30-4,22 (1Н, m), 4,07 (2H, q), 3,11 (1Н, dd, J = 4, 14 Гц), 3,01-2,98 (1Н, m), 1,34 (3H, d, J = 7,2 Гц), 1,18 (3Н, t, J = 6,8 Гц); m/z 369 (MH)+.
Этап 4 - Синтез кэпированных дипептидов (А):
К раствору соединения (5) (1 экв.) в ТГФ (6 объемах) и H2O (6 объемах) добавляли LiOH.H2O (4 экв.) при 0°C. Реакционную смесь перемешивали в течение 2 часов. Летучие вещества (ТГФ) удаляли из реакционной смеси и рН водной фазы доводили до ~3 с помощью 10% масс./об. раствора лимонной кислоты или 1М HCl. Если твердое вещество выпадало в осадок, его собирали посредством фильтрования, промывали H2O и н-пентаном и сушили с получением соответствующего промежуточного соединения (А), представляющего собой копированный дипептид. Альтернативно, подкисленный водный слой экстрагировали EtOAc × 3 и объединенные органические слои сушили над MgSO4 и выпаривали с получением неочищенного продукта. В некоторых примерах указанный неочищенный продукт далее очищали с помощью флэш-хроматографии на силикагеле или обращенно-фазовой препаративной ВЭЖХ.
Дипептидные промежуточные соединения (А), полученные по Пути 2

Rt=1,01 мин.;
m/z 339 (M-H)-1;
твердое вещество белого цвета
Rt=1,54 мин.;
m/z 307 (МН+);
твердое вещество белого цвета
Rt=1,78 минут;
m/z 336 (MH+);
твердое вещество не совсем белого цвета
m/z 357 (MH)+;
твердое вещество белого цвета
Rt=3,12 мин.; m/z 385
(MH+);
твердое вещество кремового цвета
Rt=2,40 мин.; m/z 410
(MH+);
твердое вещество белого цвета

Rt=2,40 мин.;
m/z 307 (М-Н)-;
твердое вещество белого цвета
Rt=2,75 мин.; m/z 407
(MH)+;
твердое вещество белого цвета
Rt=1,90 мин.;
m/z 324 (MH+);
твердое вещество белого цвета
Rt=2,25 мин.; m/z 357
(MH+);
твердое вещество белого цвета
Rt=2,20 мин.; m/z 358
(МН+);
твердое вещество белого цвета
Rt=1,49 мин.;
m/z 417 (MH+);
твердое вещество белого цвета
Rt=1,20 мин.;
m/z 420 (MH+);
прозрачное твердое вещество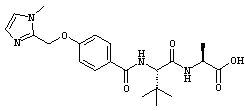
Rt=1,42 мин.;
m/z 417 (MH+);
прозрачное твердое вещество

m/z 279 (MH+);
твердое вещество белого цвета
m/z 319 (MH+);
твердое вещество белого цвета
твердое вещество белого цвета

смолистая жидкость бледно-желтого цвета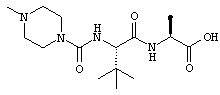
m/z 329 (MH+)
твердое вещество белого цвета

твердое вещество белого цвета
Rt=2,53 мин.;
m/z 353 (MH+);
твердое вещество белого цвета
Rt=1,80 мин.;
m/z 291 (MH+);
твердое вещество белого цвета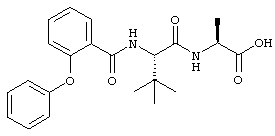
m/z 399 (MH)+;
твердое вещество белого цвета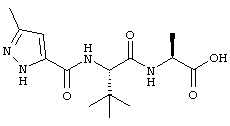
m/z 311 (МН)+;
твердое вещество не совсем белого цвета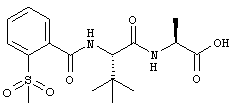
m/z 385 (МН)+;
твердое вещество белого цвета

Rt=2,60 минут;
m/z 379 ((М-Н)-);
твердое вещество бледно-желтого цвета
m/z 324 (МН)+;
твердое вещество не совсем белого цвета
m/z 323 (М-Н)-;
твердое вещество не совсем белого цвета
Rt=2,37 мин.;
m/z 339 (MH+);
твердое вещество белого цвета
m/z 391 (MH)+;
твердое вещество белого цвета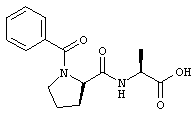
RT=1,91 мин.;
m/z 291 (MH+);
твердое вещество белого цвета
m/z 369 (MH)+;
твердое вещество белого цвета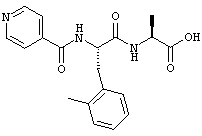
Rt=2,87 мин.;
m/z 355 (МН)+;
твердое вещество белого цвета
Для получения соединений (А46) и (АДУ) α-дизамещенную аминокислоту сначала превращали в соответствующий сложный этиловый эфир (SOCl3, этанол), который в свою очередь, превращали в соответствующий бензамид, который затем сочетали с промежуточными соединениями (2), как показано на Схеме 8, и затем гидролизовали аналогичным образом с получением соответствующей дипептидной кислоты (А).
Для получения соединения (А48) сложный этиловый эфир (S)-2-((S)-2-амино-3,3-диметилбутириламино)пропановой кислоты сочетали с 1-метилпиперидин-4-карбоновой кислотой с использованием изобутилхлорформата и N-метилморфолина в ДМФА с получением сложного этилового эфира (S)-2-{(S)-3,3-диметил-2-[(1-метилпиперидин-4-карбонил)амино]бутириламино}пропановой кислоты, который кватернизировали с помощью Mel в смеси ДХМ-ацетон и затем гидролизовали с помощью гидроксидной смолы, такой как смола Ambersep 900 - ОН.
Для получения соединения (А49) сначала получали соединение формулы (1), как следует далее. Boc-п-бром-Phe-ОН сначала превращали в его сложный метиловый эфир с использованием диазометана в стандартных условиях. Группу брома затем замещали 4-метилпиперазином в условиях реакции Бухвальда-Хартвига (Pd2(dba)3, DavePhos, CsCO3, ТГФ с обратным холодильником, в течение 16 часов). В результате конечного гидролиза сложного метилового эфира с помощью гидроксидной смолы Ambersep 900 ОН в ТГФ в течение 48 часов получали Boc-п-(4-метилпиперазин-1-ил)-Phe-OH (формула (1)), который использовали для синтеза желаемого соединения А49, как показано на Схеме 8.
Для получения соединения (А50) раствор сложного этилового эфира (S)-2-((S)-2-амино-3,3-диметилбутириламино)пропановой кислоты в смеси смесь ДХМ и 5% водного раствора NaHCO3 (1:1) обрабатывали трифосгеном с получением соответствующего изоцианата. Полученный изоцианат затем подвергали реакции с 1-метилпиперазином с получением мочевины, которую затем гидролизовали LiOH в ТГФ/H2O с получением желаемого соединения (А50).
Путь 3: Синтез PVA соединений (I) с использованием химической реакции Пассерини
Схема 9

Типичный способ Этап 1 - Синтез пептидилспиртов (б):
К раствору кислоты (А) (1 экв.) в ТГФ (25-50 мг/мл) и необязательно ДМФА (0,05-0,25 объемах) при -40°C добавляли NMM (3,1 экв.) и изобутилхлорформат (1,1 экв.). Реакционную смесь перемешивали при -40°C в течение примерно 30 мин. (за процессом образования смешанного ангидрида можно следить путем гашения аликвоты реакционный смеси, например, избытком пирролидина и оценки уровня образования амида с помощью ЖХ/МС). Добавляли по каплям раствор аминоспирта (1,1 экв.) в ТГФ или ДМФА (0,1 объемов). Реакционную смесь перемешивали при -40°C в течение примерно 1 часа до полного перемешивания по результатам измерения с помощью ЖХ/МС. При необходимости может быть добавлена дополнительная порция аминоспирта. Реакционной смеси позволяли нагреваться до комнатной температуры. Полученную в результате смесь разбавляли EtOAc (10 объемов) и насыщенным водным NaHCO3 (10 объемами). Слои разделяли и водный слой экстрагировали EtOAc (2×10 объемами). Объединенные органические фазы промывали водой (3×10 объемами) и солевым раствором (10 объемами) и концентрировали в вакууме. Полученный спирт (6) либо использовали непосредственно, либо очищали с помощью колоночной флэш-хроматографии на силикагеле или с помощью обращенно-фазовой препаративной ВЭЖХ.
Этап 2 - Синтез пептидилальдегидов (III):
К перемешанному раствору соответствующего спирта (6) (1 экв.) в сухом ДХМ (1 мл/15-200 мг спирта) и необязательно сухом ДМФА (10-100% (объем к объему) в зависимости от растворимости) при комнатной температуре порциями добавляли периодинан Десса-Мартина (2 экв.). Реакционную смесь перемешивали при комнатной температуре и за реакцией следили с помощью ЖХ/МС до полного превращения альдегидного продукта (как правило, от 1 часа до 1 дня). При необходимости добавляли дополнительную порцию периодинана Десса-Мартина для завершения окисления. Реакцию гасили путем добавления насыщенного раствора (водного) NaHCO3 (1 объем) и раствора (водного) Na2S2O3 (10% масс./об.). Смесь перемешивали в течение примерно 30 мин., разбавляли EtOAc (10 объемами) и промывали насыщенным раствором (водным) NaHCO3 (2×5 объемами), деионизированной водой (5 объемами) и солевым раствором (5 объемами). Органический слой затем сушили над MgSO4 и выпаривали с получением желаемого соединения, которое необязательно использовали в указанном виде или очищали с помощью обращенно-фазовой препаративной ВЭЖХ (для препаративной ВЭЖХ использовали градиент H2O + 0,1% ТФУ:MeCN + 0,1% ТФУ при 50°C) с последующей лиофилизацией с получением желаемого соединения (III).
Этап 3 - Синтез пептидил-α-гидроксиамидов (II):
К перемешанному раствору соответствующего альдегида (III) (1 экв.) в сухом ДХМ (1 мл/10-50 мг альдегида) и необязательно сухом ДМФА (10-35% (по объему) в зависимости от растворимости) при 0°C добавляли соответствующий изоцианид (1,1 экв.), а затем пиридин (4 экв.), с последующим добавлением по каплям трифторуксусной кислоты (2 экв.). Реакционную смесь перемешивали при 0°C в течение 10 мин. и затем позволяли нагреваться до комнатной температуры. За реакцией следили с помощью ЖХ/МС до тех пор, пока не происходило полное превращение в продукт, представляющий собой α-гидроксиамиды и/или сложные эфиры α-гидроксиамидтрифторацетата (как правило, 0,5-1 день). При необходимости добавляли дополнительную порцию изоцианида для завершения реакции. Реакционную смесь выпаривали в вакууме, разбавляли EtOAc (5 объемами) и реакцию гасили путем добавления насыщенного раствора (водного) NaHCO3 (1 объем). Смесь перемешивали в течение примерно 30 мин. и промывали насыщенным раствором (водным) NaHCO3 (2×5 объемами) и солевым раствором (5 объемами). Органический слой затем сушили над MgSO4 и выпаривали и использовали в указанном виде или очищали с помощью препаративной ВЭЖХ с получением желаемого соединения (II).
Этап 4 - Синтез PVA соединений (I)
См. Способ А
PVA соединения, полученные по Пути 3

Rt 7,70 мин.;
m/z 563 (MH+);
твердое вещество белого цвета
(Gemini)_1;
Rt 6,91 мин.;
m/z 585 (MH+);
твердое вещество белого цвета
(Gemini)_1;
Rt 6,82 мин.;
m/z 549 (MH+);
твердое вещество белого цвета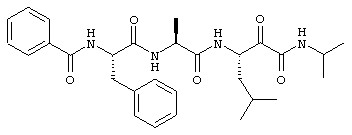
(Gemini)_1;
Rt 6,53 мин.;
m/z 523 (MH+);
твердое вещество белого цвета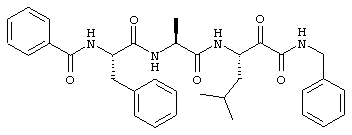
(Gemini)_1;
Rt 6,76 мин.;
m/z 571 (MH+);
твердое вещество белого цвета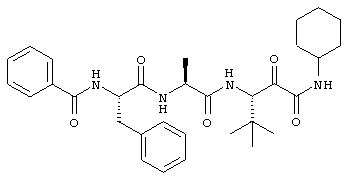
(Gemini)_1;
Rt 6,97 мин.;
m/z 563 (MH+);
твердое вещество белого цвета

(Gemini)_1;
Rt 6,53 мин.;
m/z 557 (MH+);
твердое вещество белого цвета
(Gemini)_1;
Rt 6,65 мин.;
m/z 571 (MH+);
твердое вещество белого цвета
Rt6,65 мин.;
m/z 561 (MH+);
твердое вещество белого цвета
(Gemini)_1;
Rt 6,55 мин.;
m/z 573 (MH+);
твердое вещество бежевого цвета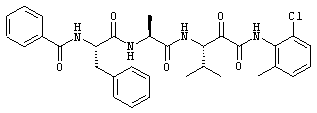
(Gemini)_1;
Rt 6,69 мин.;
m/z 592 (MH+);
твердое вещество бежевого цвета
(Gemini)_1;
Rt 6,31 мин.;
m/z 509 (MH+);
твердое вещество белого цвета

(Gemini)_1;
Rt 6,83 мин.;
m/z 571 (MH+);
твердое вещество белого цвета
Rt 8,28 мин.;
m/z 625 (MH+);
твердое вещество белого цвета
Rt 5,62 мин.;
m/z 550 (MH+);
твердое вещество белого цвета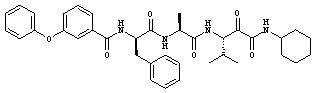
(Gemini)_1;
Rt 7,66 мин.;
m/z 641 (MH+);
твердое вещество белого цвета
Rt 7,38 мин.;
m/z 515 (MH+);
твердое вещество белого цвета
Rt 7,49 мин.;
m/z 567 (МН+);
твердое вещество белого цвета
Rt 7,60 мин.;
m/z 585 (MH+);
твердое вещество белого цвета

Rt 7,80 мин.;
m/z 575 (MH+); твердое вещество белого цвета
Rt 7,48 мин.;
m/z 567 (MH+);
твердое вещество белого цвета
Rt 7,50 мин.;
m/z 567 (MH+);
твердое вещество белого цвета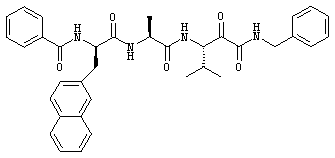
Rt 7,57 мин.;
m/z 607 (MH+);
твердое вещество бледно-желтого цвета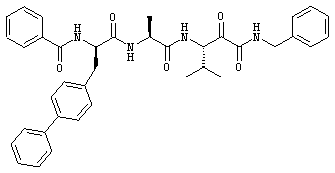
Rt 7,84 мин.;
m/z 633 (MH+);
твердое вещество белого цвета
Rt 7,60 мин.;
m/z 607 (MH+);
твердое вещество белого цвета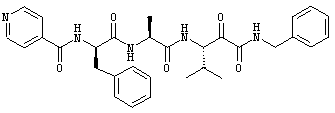
Rt 5,36 мин.;
m/z 558 (MH+);
твердое вещество белого цвета

Rt 5,32 мин.;
m/z 550 (MH+);
твердое вещество белого цвета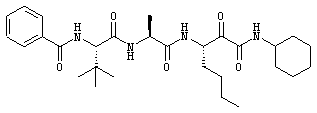
Rt 7,76 мин.;
m/z 529 (MH+);
твердое вещество белого цвета
Rt 5,54 мин.;
m/z 516 (MH+);
твердое вещество белого цвета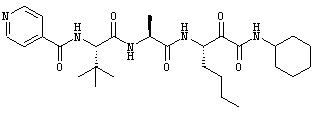
Rt 5,90 мин.;
m/z 530 (MH+);
твердое вещество белого цвета
Rt 6,94 мин.;
m/z 601 (MH+);
твердое вещество кремового цвета
Rt 7,02 мин.;
m/z 587 (MH+);
твердое вещество кремового цвета
Rt 5,81 мин.;
m/z 661 (MH+);
твердое вещество белого цвета
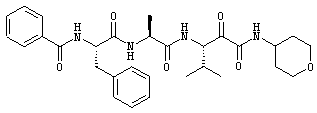
Rt 6,20 мин.;
m/z 551 (MH+);
твердое вещество белого цвета
Rt 7,14 мин.;
m/z 575 (MH+);
твердое вещество белого цвета
Rt 6,18 мин.;
m/z 525 (MH+);
твердое вещество белого цвета
Rt 4,86 мин.;
m/z 607 (MH+);
твердое вещество белого цвета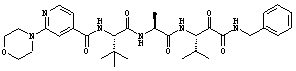
Rt 5,42 мин.;
m/z 609 (MH+);
твердое вещество белого цвета
Rt 5,75 мин.;
m/z 601 (MH+);
твердое вещество белого цвета
Rt 7,06 мин.;
m/z 606 (MH+);
твердое вещество белого цвета

Rt 6,73 мин.;
m/z 614 (MH+);
твердое вещество белого цвета
Rt 7,82 мин.;
m/z 565 (MH+);
твердое вещество белого цвета
Rt 7,06 мин.;
m/z 572 (MH+);
твердое вещество белого цвета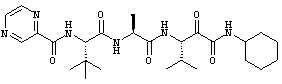
Rt 6,92 мин.;
m/z 517 (MH+);
твердое вещество белого цвета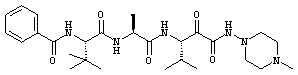
Rt 4,75 мин.;
m/z 573 (MH+);
твердое вещество белого цвета
Rt 7,47 мин.;
m/z 573 (MH+); твердое вещество белого цвета
Rt 6,72 мин.;
m/z 580 (MH+);
твердое вещество белого цвета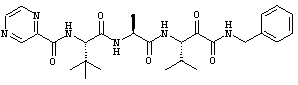
Rt 6,56 мин.;
m/z 525 (MH+);
твердое вещество белого цвета

Rt 6,06 мин.;
m/z 615 (MH+);
твердое вещество белого цвета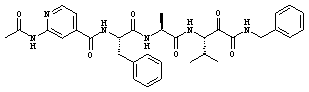
Rt 5,98 мин.;
m/z 615 (MH+);
твердое вещество белого цвета
Rt 6,23 мин.;
m/z 573 (MH+);
твердое вещество белого цвета
Rt 6,13 мин.;
m/z 573 (MH+);
твердое вещество белого цвета
Rt 5,92 мин.;
m/z 581 (MH+);
твердое вещество белого цвета
Rt 5,83 мин.;
m/z 581 (MH+);
твердое вещество белого цвета
Rt 5,85 мин.;
m/z 662 (MH+);
твердое вещество белого цвета

Rt 8,04 мин.;
m/z 601 (MH+),
твердое вещество белого цвета
Rt 6,56 мин.;
m/z 592 (MH+),
твердое вещество кремового цвета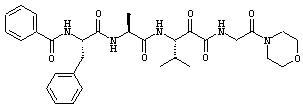
Rt 5,83 мин.;
m/z 594 (MH+),
твердое вещество кремового цвета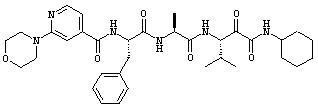
Rt 8,32 мин.;
m/z 635 (MH+),
твердое вещество белого цвета
Rt 8,01 мин.;
m/z 643 (MH+),
твердое вещество белого цвета
m/z 566 (MH+),
твердое вещество белого цвета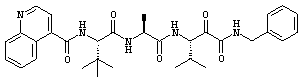
Rt 5,70 мин.;
m/z 574 (MH+),
твердое вещество белого цвета

Rt 5,81 мин.;
m/z 566 (MH+),
твердое вещество белого цвета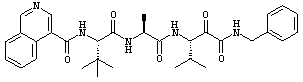
Rt 5,55 мин.;
m/z 575 (MH+),
твердое вещество белого цвета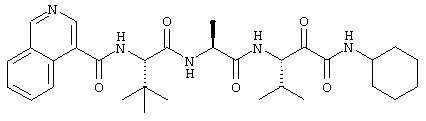
Rt 5,74 мин.;
m/z 625 (MH+),
твердое вещество белого цвета
Rt 5,73 мин.;
m/z 628 (MH+),
твердое вещество белого цвета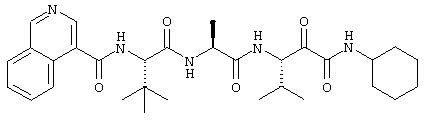
Rt 5,68 мин.;
m/z 625 (MH+),
твердое вещество белого цвета
Rt 6,49 мин.;
m/z 558 (MH+),
твердое вещество белого цвета
Rt 5,72 мин.;
m/z 560 (MH+),
твердое вещество белого цвета

Rt 6,90 мин.;
m/z 517 (MH+),
твердое вещество белого цвета
Rt 5,90 мин.;
m/z 532 (MH+),
твердое вещество белого цвета
Rt 7,42 мин.;
m/z 515 (MH+),
твердое вещество белого цвета
Rt 5,52 мин.;
m/z 516 (MH+),
твердое вещество белого цвета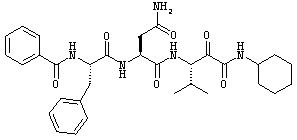
Rt 6,73 мин.;
m/z 592 (MH+),
твердое вещество белого цвета
Rt 7,76 мин.;
m/z 577 (MH+),
твердое вещество белого цвета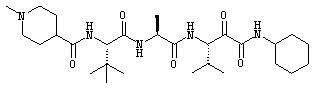
Rt 5,26 мин.;
m/z 536 (MH+),
твердое вещество белого цвета
Rt 6,81 мин.;
m/z 487 (MH+),
твердое вещество белого цвета

Rt 7,50 мин.;
m/z 527 (MH+),
твердое вещество белого цвета
(Gemini)_2;
Rt 6,09 мин.;
m/z 561 (MH+),
твердое вещество белого цвета
Rt 5,31 мин.;
m/z 499 (MH+),
твердое вещество белого цвета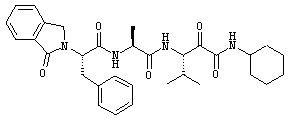
Rt 7,38 мин.;
m/z 561 (MH+),
твердое вещество белого цвета
Rt 3,99 мин.;
m/z 557 (MH+);
твердое вещество желтого цвета
Пути 4, 5 и 6
Для всех соединений, полученных по Пути 4, 5 и 6, использовали общие промежуточные соединения 12А и/или 12В.
Синтез β-амино-α-гидроксиамидных промежуточных соединений (12А и 12В)*
Схема 10

(*) необходимо отметить, что хотя 12А и 12В могли быть выделены в виде отдельных соединений, не пытались однозначно охарактеризовать стереоцентры в альфа-положении карбоновой кислоты, следовательно, указанные структуры приведены только для того, чтобы разъяснить, что они являются двумя диастереомерами. Для удобства, при использовании 12А указанное соединение изображали, как показано выше, с альфа-хиральным центром в (S)-конфигурации.
Синтез сложного бензинового эфира [(S)-1-(метоксиметилкарбамоила)-2-метилпропил]-карбаминовой кислоты (8)
К (S)-2-бензилоксикарбониламино-3-метилмасляной кислоте (7) (50,0 г, 199 ммоль), гидрохлориду N-метоксиметиламина (38,8 г, 398 ммоль) и EDC.HCl (47,7 г, 249 ммоль) в ДХМ (500 мл) добавляли DIPEA (87 мл, 497 ммоль) и реакционную смесь перемешивали при комнатной температуре в течение 20 часов, после чего реакционную смесь разбавляли ДХМ (200 мл), промывали раствором 1М HCl (водным) (3×200 мл), 1М NaOH (водным раствором) (200 мл), насыщенным раствором NaHCO3 (водным) (200 мл) и солевым раствором (300 мл). Органический слой сушили над MgSO4, фильтровали и растворитель удаляли в вакууме с получением желаемого соединения в виде бесцветного масла (51,2 г, 87%); (AnalpH2_МеОН_4 мин.) Rt 2,76 мин.; m/z 295 (МН)+.
Синтез сложного бензинового эфира ((S)-1-формил-2-метилпропил)карбаминовой кислоты (9)
К раствору сложного бензилового эфира [(S)-1-(метоксиметилкарбамоил)-2-метилпропил)карбаминовой кислоты (8) (33 г, 112 ммоль) в сухом ТГФ (300 мл) при от -30 до -40°C добавляли порциями LiAlH4 (4,3 г, 113 ммоль) в течение 45 мин. Реакционную смесь нагревали до 0°C и перемешивали при указанной температуре в течение 2 часов. Реакцию гасили с помощью 1 М KHSO4 (330 мл) при 0°C, затем добавляли 10% масс./об. раствор соли Рошелля (водного) (330 мл) и смесь перемешивали в течение 20 минут, затем экстрагировали EtOAc (2×700 мл). Объединенные органические фазы промывали 10% масс./об. раствором соли Рошелля (водным) (330 мл) и солевым раствором (450 мл), сушили над MgSO4, фильтровали и концентрировали в вакууме с получением желаемого альдегида в виде прозрачного масла (26,3 г) (AnalpH2_МеОН_4 мин) Rt 2,59 мин.; m/z 236 (МН)+. (Указанный альдегид использовали без дополнительной очистки в следующем этапе.)
Синтез сложного бензинового эфира ((S)-2-циано-2-гидрокси-1-изопропилэтил)карбаминовой кислоты (10)
К перемешанному раствору сложного бензинового эфира ((S)-1-формил-2-метил-пропил)карбаминовой кислоты (9) (26,0 г, 110 ммоль) в МеОН (150 мл) при 0°C добавляли раствор NaHSO3 (11,9 г, 114 ммоль) в H2O (230 мл) и смесь перемешивали при 0°C в течение 2,5 часов. Полученную в результате смесь добавляли к раствору NaCN (8,5 г, 174 ммоль) в H2O (150 мл) и EtOAc (450 мл) при 0°C и перемешивали при комнатной температуре в течение 20 часов. Слой EtOAc отделяли и водный слой экстрагировали EtOAc (2×500 мл). Объединенные органические экстракты промывали солевым раствором (400 мл), сушили (MgSO4) и концентрировали с получением желаемого цианогидрина (29,7 г, неочищенного продукта, ~1:1 смеси диастереоизомеров) в виде призрачной смолистой жидкости (AnalpH2_МеОН_4 мин) Rt 2,44 мин., 2,48 мин.; m/z 280 [M+H2O]+. (Указанную смесь использовали без дополнительной очистки в следующем этапе.)
Синтез (S)-3-амино-2-гидрокси-4-метилпентановой кислоты (11)
К раствору сложного бензилового эфира ((S)-2-циано-2-гидрокси-1-изопропилэтил)карбаминовой кислоты (10) (5,1 г, 19,5 ммоль) в 1,4-диоксане (90 мл) добавляли концентрированную HCl (90 мл) и анизол (1,5 экв.) и смесь нагревали до 110°C в течение 18 часов. Реакционную смесь охлаждали до комнатной температуры и концентрировали в вакууме для удаления диоксана. Затем смесь промывали EtOAc и осадок далее концентрировали в вакууме при 40°C для удаления концентрированной HCl. Всю остаточную воду удаляли путем создания азеотропной смеси с толуолом. Осадок промывали Et2O (2×50 мл) с получением гидроксикислоты (11) в виде смолистого твердого вещества (неочищенного, смеси диастереоизомеров). 1H ЯМР (400 МГц, ДМСО-d6): δ 8,20 (1Н, brs), 7,96 (1H, brs), 4,42 (1H, d J = 3,0 Гц), 4,17(1Н, d J = 4,0 Гц), 3,17-3,05 (2Н, m), 1,98-1,86 (2H, m), 0,96-0,86 (6H, m); m/z 148 (MH)+.
Синтез (S)-3-трет-бутоксикарбониламино-2-гидрокси-4-метилпентановой кислоты (12)
К раствору (S)-3-амино-2-гидрокси-4-метилпентановой кислоты (11) (предположительно 19,5 ммоль) в МеОН (100 мл) добавляли триэтиламин (9,0 мл, 64 ммоль). Добавляли порциями ди-трет-бутилдикарбонат (4,7 г, 1,1 экв.) и реакционную смесь перемешивали при комнатной температуре в течение 20 часов. Реакционную смесь концентрировали в вакууме и осадок растворяли в EtOAc (100 мл) и 1 н растворе (водном) NaOH (75 мл). Органическую фазу отделяли и водную фазу далее промывали EtOAc (2×100 мл) для удаления всех неполярных/некислотных примесей. Водный слой затем подкисляли (рН ~2) 2 н раствором HCl и экстрагировали EtOAc (3×100 мл). Объединенные органические фазы сушили (MgSO4) и концентрировали в вакууме с получением воскообразного твердого вещества белого цвета. Указанное вещество могли далее очищать на картридже Biotage Isolate (IST)-NH2 (25 г/150 мл). Указанный картридж сначала заполняли МеОН (75 мл), MeCN (75 мл) и этилацетатом (75 мл). Неочищенную смесь затем наносили на указанный картридж в смеси 5% МеОН/этилацетат (50 мл), далее промывали этилацетатом (2×75 мл) и MeCN (75 мл). Желаемую смесь диастереомерных кислот затем вымывали из картриджа MeCN, содержащим 1% муравьиную кислоту (350 мл). После выпаривания растворителя в вакууме получали смесь (1:1) желаемого соединения в виде твердого вещества белого цвета (1,5 г, 31%).
Альтернативно, единственный диастереомер 12А могли выделять путем растворения неочищенного материала в CHCl3 и растирания с н-пентаном с получением изомера 12А в виде осадка, который можно было собрать посредством фильтрования.
Фильтрат могли концентрировать с получением другого диастереоизомера (12В) в виде смолистого твердого вещества коричневого цвета, которое затем могли очищать с помощью флэш-хроматографии на силикагеле (градиент 1% МеОН/CHCl3 - 10% МеОН/CHCl3). Не пытались однозначно охарактеризовать стереоцентры в альфа-положении карбоновой кислоты.
(12А): 1H ЯМР (400 МГц, ДМСО-d6): δ 12,4 (1Н, s br), 6,46 (1H, d, J = 10 Гц), 5,38 (1Н, br s), 3,83 (1Н, d, J = 6,8 Гц), 3,65-3,59 (1Н, m), 1,99-1,91 (1Н, m), 1,36 (9H, s), 0,81-0,76 (6H, m); m/z: 246 [M-H]-.
(12В): 1H ЯМР (400 МГц, ДМСО-d6): δ 12,44 (1Н, s br), 6,21 (1Н, d, J = 10 Гц), 4,95 (1Н, br s), 4,11 (1Н, d, J = 1,6 Гц), 3,53-3,47 (1Н, m), 1,74 (1Н, m), 1,35 (9H, s), 0,91-0,83 (6H, m); m/z: 246 [M-H]-.
Альтернативно, 12А и 12В можно синтезировали в соответствии со следующим способом:
К раствору гидроксикислоты (11) (2×11,5 г,) в 1 н водном растворе NaOH (100 мл) добавляли раствор ди-трет-бутилдикарбоната (0,8 экв.) в 1,4-диоксане (100 мл) при 0°C и перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь концентрировали в вакууме и осадок растворяли в H2O и промывали Et2O (2×100 мл) для удаления любых неполярных примесей. Водный слой охлаждали до 0°C и подкисляли (рН ~2) с помощью 1 н раствора HCl и экстрагировали 10% МеОН/CHCl3 (2×500 мл). Объединенные органические фазы промывали солевым раствором (200 мл), сушили (Na2SO4) и концентрировали в вакууме с получением неочищенной смеси диастереомерных спиртов (12А) и (12В), которые могли дополнительно очищать, как описано выше.
В некоторых примерах использовали смесь диастереомерных спиртов (12А) и (12В) или, альтернативно, (12А) или (12В) использовали в качестве единственных диастереомеров для облегчения характеристики последующих продуктов.
Синтез PVA соединений (I) по Пути 4
Схема 11

Типичный способ
Этап 1 - Синтез кэпированных пептидил-α-гидроксиамидов (II):
К раствору (А) (375 мг, 1 экв.) в ТГФ (5 мл) добавляли изобутилхлорформат (0,15 мл, 1 экв.), NMM (2,5 экв.) при -40°C. Через 40 мин. добавляли раствор соединения (IV) (1 экв.) в ТГФ (2 мл) и перемешивали при -40°C в течение 3 часов. Реакционную смесь разбавляли EtOAc (20 мл) и фильтровали. Фильтрат промывали раствором (водным) 5% NaHCO3 (10 мл), солевым раствором (10 мл), сушили (Na2SO4) и концентрировали в вакууме. Осадок, как правило, очищали с помощью обращенно-фазовой препаративной ВЭЖХ с получением желаемого соединения (II).
Этап 2 - Синтез PVA соединений (I):
См. способ А
РУА соединения, полученные по Пути 4
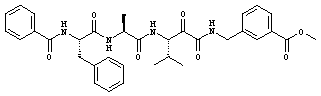
Rt 6,96 мин.;
m/z 615 (MH+);
твердое вещество белого цвета
Rt 6,27 мин.;
m/z 601 (MH+);
твердое вещество белого цвета
Rt 4,98 мин.;
m/z 564 (MH+);
твердое вещество белого цвета
Rt 7,80 мин.;
m/z 651 (MH+);
твердое вещество белого цвета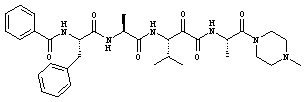
Rt 7,65 мин.;
m/z 621 (MH+);
твердое вещество белого цвета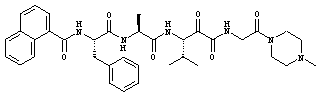
Rt 5,33 мин.;
m/z 657 (MH+);
твердое вещество белого цвета
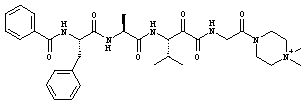
m/z 621 (M+);
твердое вещество белого цвета
Rt 7,07 мин.;
m/z 523 (MH+);
твердое вещество белого цвета
Rt 5,41 мин.;
m/z 558 (MH+);
твердое вещество белого цвета
Rt 8,05 мин.;
m/z 615 (MH+);
твердое вещество белого цвета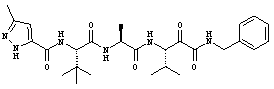
Rt 6,25 мин.;
m/z 527 (MH+);
твердое вещество белого цвета
Rt 6,63 мин.;
m/z 601 (MH+);
твердое вещество белого цвета

Rt 6,96 мин.;
m/z 597 (MH+);
твердое вещество бледно-желтого цвета
Rt 5,56 мин.;
m/z 540 (MH+);
твердое вещество белого цвета
Rt 5,82 мин.;
m/z 541 (MH+);
твердое вещество белого цвета
Rt 6,33 мин.;
m/z 473 (MH+); твердое вещество белого цвета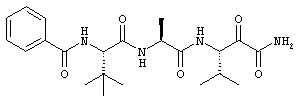
Rt 5,61 мин.;
m/z 433 (MH+);
твердое вещество белого цвета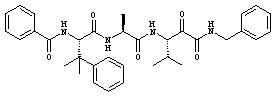
Rt 7,55 мин.;
m/z 585 (MH+);
твердое вещество белого цвета

Rt 4,90 мин.;
m/z 545 (MH+);
твердое вещество белого цвета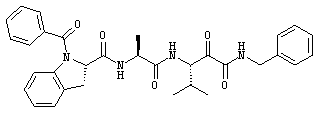
Rt 7,03 мин.;
m/z 555 (MH+);
твердое вещество белого цвета
Rt 5,23 мин.;
m/z 524 (MH+);
твердое вещество белого цвета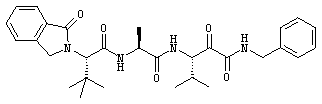
Rt 7,25 мин.;
m/z 535 (MH+);
твердое вещество белого цвета
Rt 5,81 мин.;
m/z 617 (MH+);
твердое вещество белого цвета
Rt 5,33 мин.;
m/z 657 (MH+);
твердое вещество белого цвета

Rt 5,68 мин.;
m/z 707 (MH+);
твердое вещество белого цвета
(Gemini)_2,;
Rt 5,33 мин.;
m/z 507 (MH+);
твердое вещество белого цвета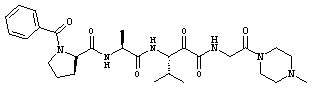
(Gemini)_2;
Rt 3,32 мин.;
m/z 557 (MH+);
твердое вещество бледно-желтого цвета

твердое вещество белого цвета
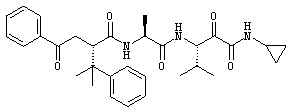
твердое вещество белого цвета
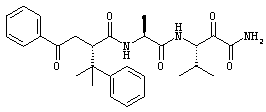
твердое вещество белого цвета
Rt 4,89 мин.;
m/z 524 (MH+);
твердое вещество белого цвета
Rt 5,57 мин.;
m/z 651 (MH+);
твердое вещество белого цвета

Rt 4,58 мин.;
m/z 702 (MH+);
твердое вещество белого цвета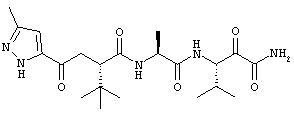
твердое вещество кремового цвета
Rt 5,61 мин.;
m/z 572 ((MH+);
твердое вещество белого цвета
Rt 5,87 мин.;
m/z 626 (MH+);
твердое вещество белого цвета

Rt 5,21 мин.;
m/z 550 (M+);
твердое вещество белого цвета
Rt 4,96 мин.;
m/z 558 (M+);
твердое вещество белого цвета
Rt 4,26 мин.;
m/z 484 (MH+);
твердое вещество белого цвета
Rt 6,75 мин.;
m/z 637 (MH+);
твердое вещество белого цвета
Rt 8,03 мин.;
m/z 485 (MH+);
твердое вещество белого цвета
Rt 3,94 мин.;
m/z 652(MH+);
твердое вещество белого цвета

Rt 5,27 мин.;
m/z 655 (MH+);
твердое вещество бледно-желтого цвета
Rt 7,02 мин.;
m/z 553(MH+);
твердое вещество белого цвета
Rt 6,93 мин.;
m/z 680 (MH+);
твердое вещество белого цвета
Rt 6,43 мин.;
m/z 652(MH+);
твердое вещество белого цвета
(+) Включает дополнительное удаление защитной группы от группы tBu с помощью ТФУ и триизопропилсилана в ДХМ до окисления периодинаном Десса-Мартина.
Кроме дипептидных промежуточных соединений (А) все выше указанные соединения, синтезируемые по Пути 4, были получены с применением α-гидроксиамидных промежуточных соединений формулы (IV).
Синтез α-гидроксиамидов (IV)
Схема 12

Типичные способы
Этап 1 - Синтез Boc-β-амино-α-гидроксиамидов (14):
К раствору (12А) (1,0 экв.) в ДМФА или ДХМ (1 г / 5 мл) добавляли EDC.HCl (1,2 экв.), HOBt (1,1 экв.) и DIPEA (1,5 экв.), затем добавляли амин (13) (1,1-2 экв.) либо в чистом виде, либо растворенным в подходящем растворителе, таком как ДХМ или ДМФА при 0°C, и реакционную смесь перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь концентрировали в вакууме и осадок растворяли в EtOAc (50 мл), промывали раствором (водным) 5% масс./об. NaHCO3 (10 мл), солевым раствором (2×20 мл), сушили (Na2SO4) и концентрировали. Осадок в целом очищали с помощью колоночной флэш-хроматографии на силикагеле или с помощью обращенно-фазовой препаративной ВЭЖХ с получением желаемого соединения (14).
В некоторых примерах EDC и HOBT могли замещать другими реагентами для сочетания амида, такими как HATU. Boc-β-амино-α-гидроксиамиды могли также получать путем реагирования гидроксикислоты (12А) и/или (12В)) с дифосгеном с образованием 1,3-диоксолан-2,4-дионовых промежуточных соединений, кольцо которых могли раскрывать с помощью необходимых аминов с получением гидроксиамидов.
Этап 2 - Синтез β-амино-α-гидроксиамидов (26):
Раствор соединения (14) (1 экв.) в ДХМ (~100 мг/ мл) обрабатывали ТФУ (6 экв.) при 0°C и позволяли перемешиваться при комнатной температуре. Через 3 часа реакционную смесь концентрировали и осадок промывали Et2O и сушили в вакууме с получением соединения (IV), которое использовали в следующем этапе без дополнительной очистки.
Альтернативно, удаление защитной группы проводили путем обработки Boc-содержащих β-амино-α-гидроксиамидов раствором 4М HCl в диоксане после растворения соединения в ДХМ.
Путь 5: Синтез PVA соединений (I) через трипепетидную гидроксикислоту
Схема 13
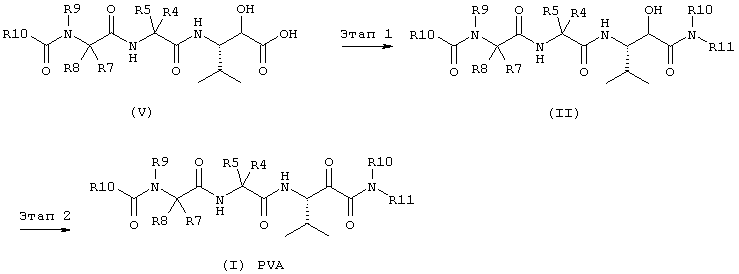
Типичный способ
Этап 1:
Указанный этап, как правило, осуществляли с использованием стандартной реакции сочетания кислоты и амина аналогично Этапу 1 / Пути 4.
Этап 2 - Синтез PVA соединений (I):
См. Способ А.
PVA соединения, полученные по Пути 5

Rt=5,05 мин.;
m/z 635 (MH+);
твердое вещество белого цвета

Rt 4,70 мин.;
m/z 593 (MH+);
твердое вещество белого цвета
(Gemini)_2;
Rt 6,13 мин.;
m/z 583 (MH+); твердое вещество белого цвета
Rt 4,69 мин.;
m/z 587 (MH+);
твердое вещество белого цвета
Rt 7,50 мин.;
m/z 549 (MH+);
твердое вещество белого цвета
Rt 7,50 мин.;
m/z 549 (MH+);
твердое вещество белого цвета
Rt 6,93 мин.;
m/z 606 (MH+);
твердое вещество белого цвета
Rt 7,03 мин.;
m/z 592 (MH+);
твердое вещество белого цвета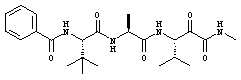
Rt 5,91 мин.;
m/z 447 (MH+);
твердое вещество белого цвета
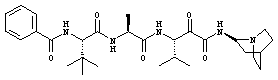
Rt 4,85 мин.;
m/z 542 (MH+);
твердое вещество белого цвета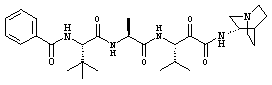
Rt 4,90 мин.;
m/z 542 (MH+);
твердое вещество белого цвета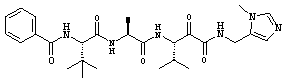
Rt 4,81 мин.;
m/z 527 (MH+);
твердое вещество белого цвета
Rt 4,75 мин.;
m/z 587 (MH+);
твердое вещество белого цвета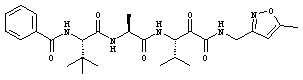
Rt 6,42 мин.;
m/z 528 (MH+);
твердое вещество белого цвета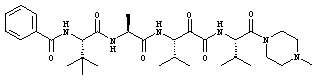
Rt 5,23 мин.;
m/z 615 (MH+);
твердое вещество белого цвета
(Gemini)_2;
Rt 6,04 мин.;
m/z 537 (MH+);
твердое вещество белого цвета

(Gemini)_2, ТФУ;
Rt 6,05 мин.;
m/z 537 (MH+);
твердое вещество белого цвета
(Gemini)_2;
Rt 4,57 мин.;
m/z 540 (MH+);
твердое вещество белого цвета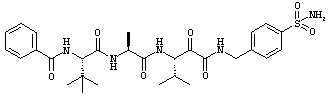
Rt 5,98 мин.;
m/z 601 (MH+);
твердое вещество белого цвета
Rt 5,84 мин.;
m/z 566 (MH+);
твердое вещество белого цвета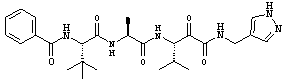
Rt 5,41 мин.;
m/z 513 (MH+);
твердое вещество белого цвета
Rt 5,37 мин.;
m/z 588 (MH+);
твердое вещество белого цвета
Rt 5,42 мин.;
m/z 588 (MH+);
твердое вещество белого цвета

Rt 8,15 мин.;
m/z 621 (MH+);
твердое вещество белого цвета
QC_2;
Rt 8,01 мин.;
m/z 544 (MH+);
твердое вещество белого цвета
QC_2;
Rt 8,24 мин.;
m/z 581 (MH+);
твердое вещество белого цвета
QC_2;
Rt 8,72 мин.;
m/z 620 (MH+);
твердое вещество белого цвета;
QC_2;
Rt 7,66 мин.;
m/z 528 (MH+);
твердое вещество белого цвета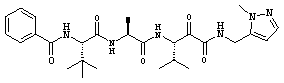
QC_2;
Rt 7,67 мин.;
m/z 527 (MH+);
твердое вещество белого цвета
QC_2;
Rt 7,85 мин.;
m/z 542 (MH+);
твердое вещество белого цвета

Rt 6,93 минут;
m/z 601 (MH+);
твердое вещество белого цвета
Rt 7,39 мин.;
m/z 579 (MH+);
твердое вещество белого цвета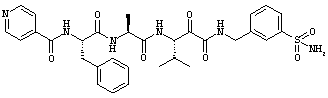
Rt 6,82 мин.;
m/z 637 (MH+);
твердое вещество белого цвета
Rt 5,08 мин.;
m/z 522 (MH+);
твердое вещество белого цвета
Rt 5,33 мин.;
m/z 536 (MH+);
твердое вещество белого цвета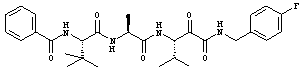
Rt 7,10 мин.;
m/z 541 (MH+);
твердое вещество белого цвета
Rt 7,42 мин.;
m/z 557, 559 (MH+);
твердое вещество белого цвета
Rt 8,13 мин.;
m/z 579 (MH+);
твердое вещество белого цвета
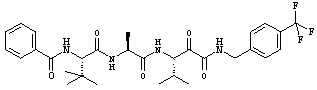
Rt 7,56 мин.;
m/z 591 (MH+);
твердое вещество белого цвета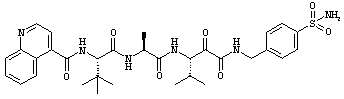
Rt 4,73 мин.;
m/z 653 (MH+);
твердое вещество белого цвета
Rt 5,64 мин.;
m/z 657 (MH+);
твердое вещество белого цвета
Rt 4,55 мин.;
m/z 617 (MH+);
твердое вещество белого цвета
Rt 7,67 мин.;
m/z 607 (MH+);
твердое вещество белого цвета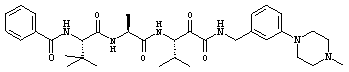
Rt 5,29 мин.;
m/z 621 (MH+);
твердое вещество белого цвета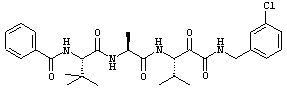
Rt 7,41 мин.;
m/z 557, 559 (MH+);
твердое вещество белого цвета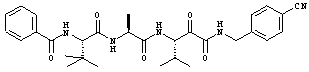
Rt 6,76 мин.;
m/z 548 (MH+);
твердое вещество белого цвета

Rt 7,39 мин.;
m/z 557, 559 (MH+);
твердое вещество белого цвета
QC_2;
Rt 7,57 мин.;
m/z 581 (MH+);
твердое вещество кремового цвета
Rt 4,59 мин.;
m/z 622 (MH+);
твердое вещество белого цвета
Rt 5,96 мин.;
m/z 580 (MH+);
твердое вещество белого цвета
QC_2;
Rt 7,67 мин.;
m/z 616 (MH+);
твердое вещество белого цвета
QC_2;
Rt 8,23 мин.;
m/z 581 (MH+);
твердое вещество белого цвета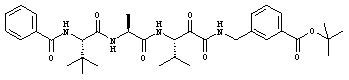
QC_2;
Rt 8,71 мин.;
m/z 623 (MH+);
твердое вещество белого цвета

QC_2;
Rt 7,55 мин.;
m/z 566 (MH+);
твердое вещество белого цвета
QC_2; Rt 8,71 мин.;
m/z 487 (MH+);
твердое вещество белого цвета
QC_2; Rt 8,41 мин.;
m/z 537 (MH+);
твердое вещество кремового цвета
QC_2; Rt 7,63 мин.;
m/z 614 (MH+); твердое вещество белого цвета
Rt 5,88 мин.;
m/z 578 (MH+);
твердое вещество белого цвета
Rt 6,43 мин.;
m/z 628 (MH+);
твердое вещество белого цвета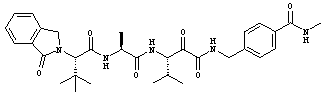
QC_2;
Rt 7,85 мин.;
m/z 592 (MH+);
твердое вещество белого цвета
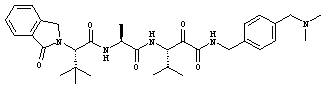
Rt 5,25 мин.;
m/z 592 (MH+);
твердое вещество белого цвета
Rt 5,35 мин.;
m/z 633 (MH+);
твердое вещество белого цвета
Rt 7,09 мин.;
m/z 618 (MH+);
твердое вещество белого цвета
Rt 4,07 мин.;
m/z 634 (MH+);
твердое вещество белого цвета
Синтез указанных выше соединений по Пути 5 требует промежуточного соединения (V).
Синтез промежуточного соединения (V)
Схема 14
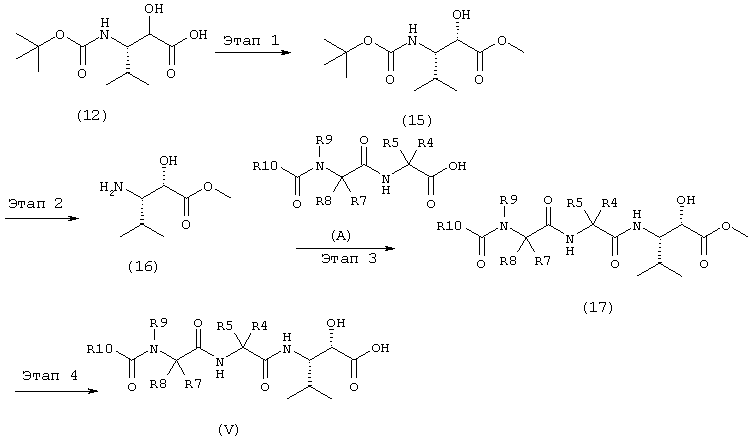
Типичный способ
Этап 1 - Синтез сложного метилового эфира Boc-β-амино-α-гидроксикислоты (15)
К раствору (12А) (2,0 г, 1 экв.) в ДМФА (18 мл) и МеОН (2 мл) при 0°C медленно добавляли по каплям TMS-диазометан (4,9 мл, 1,2 экв.). Реакционную смесь медленно нагревали до комнатной температуры и перемешивали в течение 22 часов. Медленно добавляли по каплям уксусную кислоту (5 экв.) при охлаждении (на ледяной бане) для гашения избытка TMS-диазометана. Реакционную смесь концентрировали в вакууме и осадок растворяли в EtOAc и промывали насыщенным (водным) раствором NaHCO3, H2O и солевым раствором. Затем органический слой сушили над MgSO4 и выпаривали с получением желаемого сложного метилового эфира (15А) (1,7 г, 83%) в виде твердого вещества желтого цвета. 1Н ЯМР (400 МГц, CDCl3) 4,64 (1Н, d, J = 9,3 Гц), 4,15 (1Н, d, J = 4,0 Гц), 3,66 (3H, s), 3,65-3,59 (1Н, m), 1,8-1,72 (1Н, m), 1,31 (9H, s), 0,81 (6H, m).
Этап 2 - Синтез сложного метилового эфира β-амино-α-гидроксикислоты (16)
Раствор (15А) (1,7 г, 1 экв.) в ДХМ (20 мл) обрабатывали раствором HCl в диоксане (4М, 16,8 мл, 10 экв.) при 0°C. Затем реакционную смесь перемешивали при комнатной температуре в течение 18 часов. Реакционную смесь концентрировали в вакууме с получением оранжевого масла, которое очищали с помощью колоночной хроматографии (на силикагеле) при использовании в качестве элюента EtOAc, затем 5% МеОН/EtOAc, с получением желаемого продукта (16А) (1,2 г, 92%). 1Н ЯМР (400 МГц, ДМСО-d6) 7,88 (2Н, s, NH2), 4,34 (1Н, d, J = 3,5 Гц), 3,62 (3H, s), 3,11-3,08 (1Н, m), 3,44-3,42 (1Н, m), 0,86 (3H, d, J = 6,8 Гц), 0,82 (3H, d, J = 6,8 Гц)
Соединение (16) также можно получать с использованием 5-10 экв. ТФУ в ДХМ.
Этап 3 - Синтез сложных метиловых эфиров кэпированной пептидил-α-гидроксикислоты (17)
К раствору кэпированной дипептидной кислоты (А) (1 экв.) в ТГФ (5 мл) добавляли изобутилхлорформат (1 экв.) и NMM (2,5 экв.) при -40°C. Через 40 минут добавляли раствор амина (16) (1 экв.) в ТГФ (2 мл) и перемешивали при -40°C в течение 3 часов. Реакционную смесь разбавляли EtOAc (20 мл) и фильтровали. Фильтрат промывали 5% (водным) NaHCO3 (10 мл), солевым раствором (10 мл), сушили (Na2SO4) и концентрировали в вакууме. Осадок в целом очищали с помощью обращенно-фазовой препаративной ВЭЖХ с получением желаемого соединения (17).
Этап 4 - Синтез кэпированных пептидил-α-гидроксикислот (V)
К раствору сложного метилового эфира кэпированной пептидил-α-гидроксикислоты (17) в ТГФ и H2O добавляли гидроксид лития (2 экв.) при охлаждении (на ледяной бане).
Реакционную смесь медленно нагревали до комнатной температуры и перемешивали в течение 15 часов. Реакционную смесь подкисляли 10% водным раствором уксусной кислоты и водный слой экстрагировали EtOAc (3×5 объемами). Объединенные органические экстракты промывали H2O (5 объемами) и солевым раствором (5 объемами), сушили (MgSO4) и концентрировали в вакууме с получением желаемого соединения.
Путь 6: Синтез PVA соединений (I) через трипептид гидроксиамид
Схема 15

Типичный способ
Этап 1 - Синтез кэпированного пептидил-α-гидроксиамида (II)
Указанный синтез осуществляли аналогично Этапу 3/Пути 2
Этап 2 - Синтез PVA соединений (I)
См. Способ А.
PVA соединения, полученные по Пути 6

Rt 4,28 мин.;
m/z 617 (MH+);
твердое вещество белого цвета

Rt 4,23 мин.;
m/z 617 (MH+);
твердое вещество белого цвета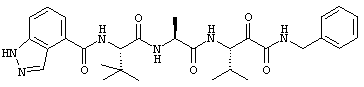
Rt 6,39 мин.;
m/z 563 (MH+);
твердое вещество белого цвета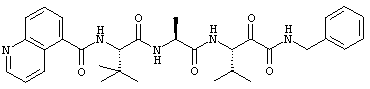
Rt 5,39 мин.;
m/z 574 (MH+);
твердое вещество белого цвета
Rt 5,49 мин.;
m/z 563 (MH+);
твердое вещество белого цвета
QC_2;
Rt 8,16 мин.;
m/z 572 (MH+);
твердое вещество белого цвета
QC;
Rt 8,31 мин.;
m/z 621 (MH+);
твердое вещество белого цвета
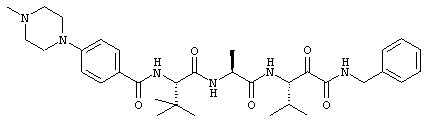
QC;
Rt 8,31 мин.;
m/z 621 (MH+);
твердое вещество белого цвета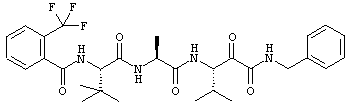
Rt 7,28 мин.;
m/z 591 (MH+);
твердое вещество белого цвета
Rt 7,49 мин.;
m/z 557,559 (MH+);
твердое вещество белого цвета
Rt 7,49 мин.;
m/z 557,559
(MH+);
твердое вещество белого цвета
QC_2; Rt 6,25
мин.; m/z 621
(MH+);
твердое вещество белого цвета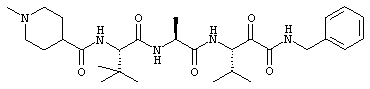
QC_2;
Rt 5,73 мин.;
m/z 544 (MH+);
твердое вещество белого цвета
Схема 16
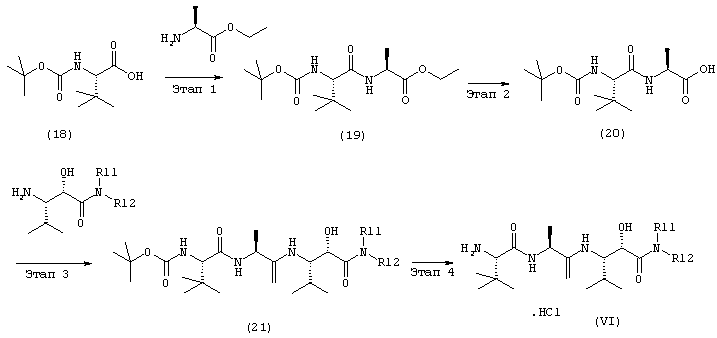
Для синтеза указанных выше соединений по 6 Пути требуются промежуточные соединения (VI). Соединения формулы (VI) получали следующим образом:
Этап 1 - Синтез сложного этилового эфира (S)-2-((S)-2-трет-бутоксикарбониламино-3,3-диметилбутириламино)пропановой кислоты (19)
К раствору (S)-2-(трет-бутоксикарбониламино)-3,3-диметилбутановой кислоты (18) (10 г, 43,3 ммоль) в ТГФ (100 мл) при -40°C добавляли изобутилхлорформат (5,9 мл, 45,5 ммоль) с последующим добавлением NMM (10,45 мл, 95,23 ммоль) и перемешивали при -40°C в течение 1 часа. К указанной выше реакционной смеси добавляли раствор H-Ala-OMe (7,3 г, 47,6 ммоль) в ДМФА (5 мл) и перемешивали при -40°C. Через 2,5 часа к указанной реакционной смеси добавляли EtOAc (500 мл), перемешивали в течение 10 минут и фильтровали для удаления солей. Фильтрат промывали 10% раствором лимонной кислоты (3×100 мл), 5% раствором NaHCO3 (3×100 мл), солевым раствором (100 мл), сушили (Na2SO4) и концентрировали. Полученный осадок перемешивали с петролейным эфиром (100 мл) в течение 30 минут, полученное твердое вещество выделяли посредством фильтрования с получением желаемого соединения (6 г, 43%) в виде твердого вещества белого цвета. Rf: 0,3 (20% EtOAc/петролейный эфир); 1H ЯМР (400 МГц, ДМСО-d6): 8,3 (1Н, d, J = 6 Гц), 6,36 (1Н, d, J = 9,6 Гц), 4,22 (1Н, m), 4,1-4,03 (2H, m), 3,89 (1Н, d, J = 9,6 Гц), 1,38 (9Н, s), 1,27 (3H, d, J = 7,2 Гц), 1,16 (3H, t, J = 6,8 Гц), 0,91 (9Н, s); m/z 331 (MH)+;
Этап 2 - Синтез (S)-2-((S)-2-трет-бутоксикарбониламино-3,3-диметилбутириламино)пропановой кислоты (20)
К раствору (S)-2-(трет-бутоксикарбониламино)-3,3-диметилбутановой кислоты (18) (6,5 г, 19,7 ммоль) в ТГФ (30 мл) добавляли NaOH (1,7 г, 43,8 ммоль) в H2O (60 мл) и реакционную смесь перемешивали при комнатной температуре в течение 16 часов. Затем ТГФ удаляли в вакууме и водную фазу промывали EtOAc (50 мл). Затем рН водной фазы доводили до ~ 2 путем добавления 1М HCl и экстрагировали EtOAc (3×50 мл). Органические слои объединяли, сушили над MgSO4 и выпаривали с получением желаемого соединения (20) в виде твердого вещества белого цвета (5,7 г, 95%); AnalpH2_MeOH; Rt 2,61 мин.; m/z 303 (MH+); твердое вещество белого цвета
Этап 3 - Синтез Boc-пептидил-α-гидроксиамидов (21)
К раствору (20) (1,1 г, 1 экв.) в ТГФ (20 мл) добавляли изобутилхлорформат (496 мкл, 1 экв.), NMM (2,5 экв.) при -40°C. Через 40 минут добавляли раствор соединения (IV) (1 экв.) в ТГФ (20 мл) и перемешивали при -40°C в течение 3 часов. Реакционную смесь разбавляли EtOAc (100 мл) и фильтровали. Фильтрат промывали (водным) 5% раствором NaHCO3 (100 мл), солевым раствором (100 мл), сушили (Na2SO4) и концентрировали в вакууме. Осадок, как правило, очищали с помощью обращенно-фазовой препаративной ВЭЖХ с получением желаемого соединения (21).
Этап 4 - Синтез пептидил-α-гидроксиамидов (VI)
Раствор Boc-пептидил-α-гидроксиамида (21) (1 экв.) в ДХМ (10 объемов) обрабатывали ТФУ (6 экв.) при 0°C и позволяли перемешиваться при комнатной температуре. Через 3 часа реакционную смесь концентрировали и осадок промывали Et2O (2×10 объемами) и сушили в вакууме с получением желаемого соединения (VI), которое использовали в следующем этапе без дополнительной очистки.
В некоторых примерах удаление защитную группу удаляли с помощью раствора 4 М HCl в диоксане после растворения соединения (21), содержащего защитную группу Boc, в ДХМ.
Способ В: Синтез PVA соединений (I) с помощью реакций озонолиза
Схема 17

Типичный способ
Синтез трипептидных промежуточных соединений:
Следующие трипептиды (О) получали с использованием такой же методологии, как описано в способе Пути 1 для синтеза дипептидных промежуточных соединений (А).

Rt=3,15 мин.;
m/z 454 (MH+);
твердое вещество белого цвета
Rt=4,06 мин.;
m/z 440 (MH+);
твердое вещество белого цвета
Rt=3,55 мин.;
m/z 398 (MH+);
твердое вещество белого цвета
Этап 1 - Синтез цианофосфоранильного промежуточного соединения (Р):
К раствору триппетидного промежуточного соединения (О) (1 экв.) в ДХМ (1 г/30 мл) добавляли EDC.HCl (2 экв.), (трифенилфосфоранилиден)ацетонитрил (2 экв.) и DMAP (0,1 экв.). Полученную смесь перемешивали в течение 16 часов при 22°C, после чего растворитель удаляли и полученный неочищенный материал очищали с помощью обращенно-фазовой препаративной ВЭЖХ с получением желаемого соединения (Р).
Следующие соединения формулы (Р) получали с использованием указанного способа.

Rt=4,03 минут;
m/z 737 (MH+);
твердое вещество коричневого цвета

Rt=4,59 минут;
m/z 723 (MH+);
твердое вещество бледного оранжевого-коричневого цвета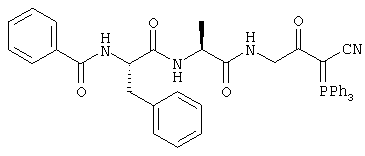
Rt=4,37 минут;
m/z 681 (MH+);
твердое вещество бледно-коричневого цвета
Этап 2 - Синтез PVA соединений (I):
Через раствор промежуточного соединения (Р) (1 экв.) в ДХМ (100 объемов) барботировали газообразный озон при -78°C в течение 5-10 мин. Через указанную смесь барботировали азот в течение 5 мин. с последующим добавлением раствора амина (R11R12NH) (1 экв.) в ДХМ (20 объемов), после чего реакционную смесь перемешивали в течение 30 мин. при -78°C до удаления растворителя. Осадок очищали с помощью обращенно-фазовой препаративной ВЭЖХ с последующей лиофилизацией с получением желаемого соединения (I).
PVA соединения, полученные согласно Способу В

Rt=6,82 мин.;
m/z 535 (MH+); твердое вещество белого цвета
Rt=5,50 мин.;
m/z 564 (MH+);
твердое вещество белого цвета
Rt=7,45 мин.;
m/z 541 (MH+); твердое вещество белого цвета

(Gemini)_1;
Rt=4,18 мин.;
m/z 536 (MH+);
твердое вещество белого цвета
(Gemini)_1;
Rt=5,43 мин.;
m/z 558 (MH+);
твердое вещество белого цвета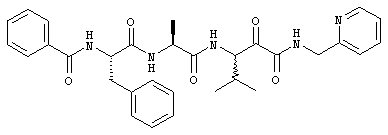
Rt=6,24 мин.;
m/z 558 (MH+);
твердое вещество белого цвета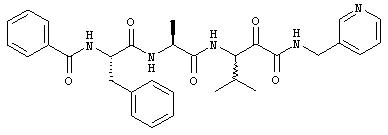
Rt=5,97 мин.;
m/z 558 (MH+);
твердое вещество кремового цвета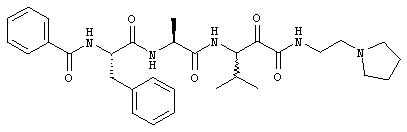
Rt=5,09 мин.;
m/z 664 (MH+); твердое вещество кремового цвета
PVA соединения, синтезированные альтернативными способами
Следующие PVA соединения синтезировали альтернативными способами. Тем не менее, способы, описанные выше, могут в равной степени применяться для синтеза указанных соединений.
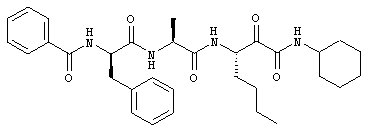
(Gemini)_1;
Rt=7,22 мин.;
m/z 563 (MH+);
твердое вещество белого цвета
Rt=7,28 мин.;
m/z 572 (MH+);
твердое вещество белого цвета
Rt=7,65 мин.;
m/z 515 (MH+);
твердое вещество бежевого цвета
PVA-017 готовили путем синтеза Bz-D-Phe-Ala-OH (A2) на смоле Ванга (Путь 1) и сочетания его с подходящим α-гидрокси-β-аминоциклогексиламидным структурным блоком, который, в свою очередь, был получен с помощью реакции Пассерини на содержащем защитную группу Cbz предшественнике аминокапронового альдегида. Из указанного предшественника удаляли защитную группу (гидрогенолиз), проводили сочетание (в присутствии изобутилхлорформата) и окисляли (периодинан Десс-Мартина) с получением желаемого пирувамида.
PVA-040 готовили из соответствующих пировиноградной кислоты, содержащей в качестве защитной группы дитиолан, и 4-пиколиламина (HOAT, EDC) с последующим гидролизом дитиолановой группы с помощью 1 М HCl (водного раствора) с использованием этилацетата в качестве сорастворителя. Пировиноградную кислоту, содержащую в качестве защитной группы дитиолан, получали путем гидролиза из соответствующего сложного этилового эфира (1М NaOH, MeOH), который, в свою очередь, готовили из соответствующего этилпирувала (24) (этан-1,2-дитиол, BF3.Et2O). Этилпируват (24) готовили в два этапа из BzPheAlaNleOH (01). Сначала проводили реакцию Дейкина-Уэста с этилоксалилхлоридом (22) для получения этилоксалиленолата (23), который затем гидролизовали с помощью этокисда натрия в этаноле с получением желаемого этилпирувата (24).
Схема 18

PVA-102 готовили путем сочетания диметилацеталя (25) с BzPheAlaOH (A1) с использованием стандартных условий в присутствии изобутилхлорформата. В результате гидролиза ацеталя (26) с использованием смеси ТФУ:ацетон:вода получали желаемое конечное соединение PVA-102. Диметилацеталь (25) получали из глицина (27), содержащего защитную группу Cbz, в 10 этапов. Указанный глицин сначала превращали в соответствующую гидроксикислоту (28), содержащею защитную группу Boc, с использованием способа, аналогичного способам, описанным для синтеза 12А и 12 В (Схема 10). 28 затем превращали в желаемый ацеталь (25) в 5 этапов. Первое сочетание с бензиламином проводили в стандартных условиях сочетания кислоты и амина с получением соответствующего бензиламида. Защитную группу Boc затем замещали на F-moc в два этапа (удаление защитной группы Boc с последующим введением защитной группы Fmoc с использованием стандартных условий). Затем спирт окисляли с помощью периодинана Десса-Мартина и далее превращали в ацеталь с использованием метилортоформата и п-толуолсульфоновой кислоты в метаноле. В конечном итоге защитную группу F-moc удаляли с использованием пиперидина в ДХМ с получением соединения 25.
Схема 19

Дополнительные детали синтеза
Ниже описаны процессы синтеза материалов и реагентов, которые не могут быть с легкостью получены или не являются коммерчески доступными, и последовательности реакций синтеза, не входящих в объем представленных выше синтетических реакций.
Синтез промежуточных соединений, представляющих собой связанные с эфиром бензойные кислоты - Общие способы:

Синтез метил-4-(2-пирролидин-1-ил)этоксибензоата (ВВ1):

Суспензию сложного метилового эфира 4-гидроксибензойной кислоты (20 г, 132 ммоль, 1 экв.) и порошкообразного безводного K2CO3 (2,5 экв.) в безводном ДМФА (160 мл) нагревали до 100°C.Добавляли порциями 1-(2-хлорэтил)пирролидин (1,3 экв.) и полученную в результате смесь перемешивали при 100°C в течение 5 часов. Реакционную смесь охлаждали до комнатной температуры и фильтровали. Фильтрат разбавляли H2O (200 мл) и экстрагировали EtOAc (2×250 мл). Объединенные органические экстракты промывали солевым раствором (4×50 мл), сушили (Na2SO4) и концентрировали в вакууме. Полученный неочищенный материал очищали с помощью колоночной хроматографии (100-200 меш на силикагеле, 20% EtOAc-ДХМ) с получением (ВВ1) (17,1 г, 52%) в виде желтой жидкости. Rf: 0,2 (50% EtOAc/петролейный эфир). 1Н ЯМР (400 МГц, CDCl3): δ 7,98 (2Н, d, J = 9,4 Гц), 6,93 (2Н, d, J = 9,4 Гц), 4,16 (2Н, t, J = 6 Гц), 3,88 (3H, s), 2,92 (2Н, t, J = 6 Гц), 2,65-2,61 (4Н, m), 1,85-1,78 (4H, m); m/z 250 (MH)+.
Синтез гидрохлорида метил-4-(2-пирролидин-1-ил)этоксибензойной кислоты (ВВ2):

К раствору соединения (ВВ1) (16,9 г, 68 ммоль) в МеОН (150 мл) добавляли 5 н водный раствор NaOH (40 мл) при комнатной температуре. Реакционную смесь перемешивали в течение 5 часов и концентрировали в вакууме. Полученный осадок растворяли в H2O (25 мл), охлаждали до 0°C (на ледяной бане) и подкисляли 6 н водным раствором HCl (рН ~6). Полученный осадок собирали посредством фильтрования и промывали холодным МеОН (25 мл) и сушили с получением (ВВ2) (8,45 г, 53%) в виде твердого вещества не совсем белого цвета. Rf: 0,2 (84:15:1 МеОН/CHCl3/АсОН). 1H ЯМР (400 МГц, ДМСО-d6): δ 7,92 (2Н, d, J = 8,4 Гц), 7,1 (2Н, d, J = 8,4 Гц), 4,43-4,42 (2Н, m), 3,6-3,55 (2H, m), 3,2-3,1 (4H, br s), 2,0-1,9 (4H, m); m/z 236 (MH)+.
Синтез метил-3-(2-пирролидин-1-ил)этоксибензоата (ВВ3):

Суспензию сложного метилового эфира 3-гидроксибензойной кислоты (20 г, 131,57 ммоль) и порошкообразного безводного K2CO3 (45,3 г, 328,26 ммоль) в сухом ДМФА (160 мл) нагревали до 100°C.Добавляли шестью порциями 1-(2-хлорэтил)пирролидин (29,1 г, 171 ммоль) к реакционной смеси, которую перемешивали в течение 5 часов. Реакционную смесь охлаждали до комнатной температуры и фильтровали. Фильтрат растворяли в H2O (200 мл), экстрагировали EtOAc (2×250 мл), промывали солевым раствором (4×50 мл), сушили (Na2SO4) и концентрировали в вакууме. Полученное неочищенное соединение очищали с помощью колоночной хроматографии (100-200 меш, на силикагеле, 20% EtOAc-ДХМ) с получением соединения (ВВ3) (11,8 г, 36%) в виде жидкости желтого цвета. Rf: 0,2 (50% EtOAc/петролейный эфир). 1H ЯМР (400 МГц, CDCl3): δ 7,63 (1Н, d, J = 8 Гц), 7,58 (1Н, s), 7,32 (1Н, t, J = 4 Гц), 7,13 (1Н, dd, J = 2,4, 8 Гц), 4,15 (2Н, d, J = 6 Гц), 3,91 (3H, s), 2,92 (2Н, t, J = 6 Гц), 2,63-2,60 (4H, m), 1,85-1,77 (4H, m); m/z 250 (MH+).
Синтез гидрохлорида 4-(2-пирролидин-1-ил)этоксибензойной кислоты (ВВ4):

К раствору (ВВ3) (11,7 г, 46,98 ммоль) в МеОН (150 мл) добавляли 5 н водный раствор NaOH (40 мл) при комнатной температуре, перемешивали в течение 5 часов и концентрировали в вакууме. Осадок растворяли в H2O (10 мл), охлаждали на ледяной бане, подкисляли 6 н водным раствором HCl (рН ~6), экстрагировали 10% MeOH-CHCl3 (3×50 мл), объединенные органические слои концентрировали и осадок обрабатывали эфирным раствором HCl (100 мл) с получением твердого осадка, который фильтровали и сушили с получением (ВВ4) (5,5 г, 49%) в виде твердого вещества белого цвета. Rf: 0,2 (15% МеОН/CHCl3). 1H ЯМР (400 МГц, ДМСО-d6): δ 13,01 (1Н, br s), 7,58 (1Н, d, J = 7,6 Гц), 7,51 (1Н, s), 7,46 (1Н, t, J = 8,4 Гц), 7,13 (1Н, d, J = 2,4, 8 Гц), 4,45-4,35 (2Н, m), 3,65-3,50 (4H, m), 3,15-3,05 (2Н, m), 2,05-1,85 (4H, m).
Синтез 1-метил-1Н-имидазол-2-карбальдегида (BBS):

К раствору 1-метилимидазола (57 г, 0,7 ммоль) в ТГФ (250 мл) добавляли LDA (2 М раствор в ТГФ, 348 мл) при -60°C и перемешивали в течение 3 часов. Реакционную смесь охлаждали до -78°C, быстро добавляли ДМФА (75 мл) и реакционной смеси позволяли медленно нагреваться до комнатной температуры и перемешивали при комнатной температуре в течение ночи. Реакционную смесь охлаждали до 0°C, добавляли раствор NaH2PO4 (100 г в 350 мл H2O) и полученную смесь перемешивали в течение 30 мин. Указанную смесь фильтровали для удаления нерастворенного материала и фильтрат экстрагировали ДХМ (4×400 мл). Объединенные органические экстракты концентрировали в вакууме и неочищенный осадок очищали с помощью колоночной хроматографии (на силикагеле, 100-200 меш, 30% EtOAc/петролейный эфир) с получением (ВВ5) (41 г, 53%) в виде твердого вещества желтого цвета. Rf: 0,3 (15% МеОН/CHCl3). 1H ЯМР (400 МГц, CDCl3): δ 9,82 (1Н, s), 7,28 (1Н, арр d), 7,13 (1Н, арр d), 4,04 (3H,s);m/z 111 (MH)+.
Синтез (1-метил-1Н-имидазол-2-ил)метанола (ВВ6):

К раствору соединения (ВВ5) (40,5 г, 368 ммоль) в МеОН (300 мл) при 0°C порциями добавляли NaBH4 (20,89 г, 551 ммоль). Реакционную смесь медленно нагревали до комнатной температуры и перемешивали в течение 5 часов. Реакционную смесь охлаждали до 0°C, добавляли Н2О (150 мл) и смесь перемешивали в течение 30 мин. при комнатной температуре, затем концентрировали в вакууме. Неочищенной осадок растворяли в H2O (150 мл) и экстрагировали CHCl3 (4×200 мл). Объединенные органические слои сушили над Na2SO4 и концентрировали. Осадок перемешивали с Et2O (150 мл) и фильтровали с получением (ВВ6) (36 г, 87%) в виде твердого вещества белого цвета. Rf: 0,4 (15% МеОН/CHCl3). 1H ЯМР (400 МГц, CDCl3): δ 6,89 (1Н, арр d), 6,83 (1Н, арр d), 4,66 (2Н, s), 3,72 (3H, s); m/z 113 (МН)+.
Синтез гидрохлорида 2-(хлорметил)-1-метил-1Н-имидазола (ВВ7):

К раствору (ВВ6) (35,5 г, 316,96 ммоль) в ДХМ (1500 мл) добавляли SOCl2 (330 мл, 4436 ммоль) при 0°C. Реакционную смесь нагревали до комнатной температуры и перемешивали в течение 5 часов. Указанную реакционную смесь концентрировали, осадок промывали ДХМ (2×500 мл) с последующей промывкой Et2O (2×200 мл) с получением (ВВ7) (50 г, 95%) в виде твердого вещества не совсем белого цвета. Rf: 0,4 (EtOAc). 1H ЯМР (400 МГц, ДМСО-d6): δ 7,76 (1Н, арр d), 7,70 (1Н, арр d), 5,17 (2Н, s), 3,87 (3H, s); m/z 131 (MH)+.
Синтез метил-4-((1-метил-1Н-имидазол-2-ил)метокси)бензоата (ВВ8):

Суспензию сложного метилового эфира 4-гидроксибензойной кислоты (18 г, 118,42 ммоль) и порошкообразного безводного K2CO3 (40,85 г, 296 ммоль) в сухом ДМФА (150 мл) нагревали до 100°C.К перемешанной реакционной смеси добавляли (ВВ7) (25,5 г, 153,6 ммоль) шестью порциями. Реакционную смесь перемешивали в течение 6 часов и затем охлаждали до комнатной температуры и фильтровали. Фильтрат растворяли в H2O (200 мл), экстрагировали EtOAc (2×250 мл), объединенные органические слои промывали солевым раствором (3×100 мл), сушили над Na2SO4, концентрировали в вакууме. Полученное неочищенное соединение очищали с помощью колоночной хроматографии (100-200 меш на силикагеле, при элюировании 2% МеОН-CHCl3) с получением (ВВ8) (17,1 г, 52%) в виде твердого вещества не совсем белого цвета. Rf: 0,2 (50% EtOAc/петролейный эфир). 1H ЯМР (400 МГц, CDCl3): δ 8,0 (2Н, d, J = 8,8 Гц), 7,33 (2Н, d, J = 8,8 Гц), 7,02 (1Н, арр d), 6,91 (1Н, арр d), 5,22 (2Н, s), 3,88 (3H, s), 3,73 (3H, s); m/z 247 (MH)+.
Синтез гидрохлорида 4-(1-метил-1Н-имидазол-2-ил)метоксибензойной кислоты (ВВ9):

К раствору (ВВ8) (24,1 г, 97,96 ммоль) в МеОН (180 мл) добавляли водный 5 н раствор NaOH (70 мл) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение 8 часов и концентрировали в вакууме. Осадок растворяли в H2O (100 мл) и промывали Et2O (2×100 мл), водный слой охлаждали на ледяной бане и подкисляли 6 н водным раствором HCl (рН ~6). Выпавшее в осадок твердое вещество собирали посредством фильтрования и промывали петролейным эфиром (200 мл) и сушили с получением (ВВ9) (20,7 г, 76%) в виде твердого вещества белого цвета. Rf: 0,6 (5% МеОН/CHCl3). 1H ЯМР (400 МГц, ДМСО-d6): δ 7,92 (2Н, d, J = 8,8 Гц), 7,42 (1Н, s), 7,21-7,19 (3H, m), 5,36 (2Н, s), 3,76 (3H, s); m/z 233 (MH)+.
Синтез метил-3-(1-метил-1Н-имидазол-2-ил)метоксибензоата (ВВ10):
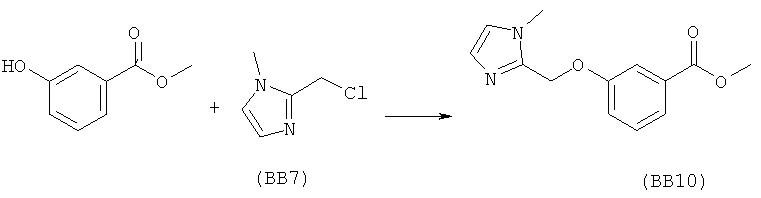
Суспензию сложного метилового эфира 3-гидроксибензойной кислоты (18 г, 118,42 ммоль) и порошкообразного безводного K2CO3 (40,85 г, 296 ммоль) в сухом ДМФА (150 мл) нагревали до 100°C. К реакционной смеси добавляли (ВВ7) (25,5 г, 153,6 ммоль) шестью порциями. Полученную реакционную смесь перемешивали в течение 6 часов и затем охлаждали до комнатной температуры и фильтровали. Фильтрат растворяли в H2O (200 мл), экстрагировали EtOAc (2×250 мл) и объединенные органические слои промывали солевым раствором (3×100 мл), сушили (Na2SO4) и концентрировали в вакууме. Полученное неочищенное соединение очищали с помощью колоночной хроматографии (100-200 меш на силикагеле, 2% МеОН-CHCl3) с получением (ВВ10) (15,3 г, 52%) в виде твердого вещества не совсем белого цвета. Rf: 0,2 (50% EtOAc/петролейный эфир). 1H ЯМР (400 МГц, CDCl3): δ 7,67-7,55 (2Н, m), 7,36 (1Н, t, J = 7,6 Гц), 7,25 (1Н, арр d), 7,02 (1Н, app d), 6,91 (1Н, app d), 5,19 (2Н, s), 3,92 (3H, s), 3,74 (3H, s); m/z 247 (MH+).
Синтез гидрохлорида метил-3-(1-метил-1Н-имидазол-2-ил)метоксибензойной кислоты (ВВ11):

К раствору (ВВ10) (15,1 г, 61,38 ммоль) в МеОН (150 мл) добавляли 5 н водный раствор NaOH (40 мл) при комнатной температуре. Реакционную смесь перемешивали при комнатной температуре в течение 5 часов и концентрировали в вакууме. Осадок растворяли в H2O (150 мл) и промывали Et2O (2×100 мл), водный слой охлаждали на ледяной бане и подкисляли с помощью 6 н водного раствора HCl (рН ~6). Выпавшее в осадок твердое вещество собирали посредством фильтрования, промывали охлажденной H2O (50 мл) и петролейным эфиром (200 мл) и сушили с получением (ВВ11) (7,8 г, 46%) в виде твердого вещества не совсем белого цвета. Rf: 0,6 (15% МеОН/CHCl3). 1H ЯМР (400 МГц, ДМСО-d6): δ 7,65-7,56 (2Н, m), 7,43 (1Н, t, J = 8 Гц), 7,35-7,30 (1Н, m), 7,26-7,20 (m, 1Н), 6,92-6,90 (m, 1Н), 5,21 (2Н, s), 3,7 (3H, s); m/z 233 (MH+).
Синтез пиримидин-4-карбоновой кислоты (ВВ12):

К раствору 4-метилпиримидина (4 г, 46,5 ммоль) в пиридине (20 мл) добавляли SeO2 (8,7 г, 79,06 ммоль) при комнатной температуре. Реакционную смесь затем нагревали до 60°C в течение 2 часов и затем перемешивали при комнатной температуре в течение 16 часов. Реакционную смесь разбавляли ДХМ (50 мл) и фильтровали для удаления отработанного селена. Фильтрат концентрировали с получением осадка, который перемешивали с H2O (20 мл), выпавшее в осадок твердое вещество фильтровали и промывали ацетоном (2×20 мл) и сушили с получением (ВВ12) (3,1 г, 58%) в виде твердого вещества коричневого цвета. Rf: 0,2 (40% МеОН/CHCl3). 1Н ЯМР (400 МГц, ДМСО-d6): δ 13,8 (1Н, br s), 9,37 (1Н, s), 9,07 (1Н, d, J = 5,2 Гц), 8,01 (1Н, d, J = 4 Гц); m/z 123 (M-H)-.
Синтез (S)-2-(трет-бутоксикарбониламино)-3-метил-3-фенилбутановой кислоты (ВВ17):

ВВ17 синтезировали в соответствии со способами, описанными в заявке на патент США 2009/0264487, А1.
Синтез (ВВ19):

Синтез (ВВ18)
Дипептид NH2-Tle-Ala-OEt (1,5 г, 1 экв.) суспендировали в MeCN (30 мл). К перемешанной суспензии добавляли фталдиальдегид (584 мг, 1 экв.) и уксусную кислоту (25 мл, 0,1 экв.). Реакционную смесь перемешивали при комнатной температуре в течение 3,5 часов. Реакционную смесь концентрировали в вакууме и неочищенный осадок растворяли в EtOAc (50 мл). Органическую фазу промывали раствором (водным) HCl (2M, 3×20 мл), насыщенным водным раствором NaHCO3 (2×20 мл) и солевым раствором (20 мл), сушили (MgSO4). Полученный неочищенный материал очищали с помощью колоночной хроматографии (на силикагеле, 0-40% EtOAc/изогексан) с получением желаемого соединения (ВВ18) (1,18 г, 78%) в виде твердого вещества кремового цвета. ЖХ/МС чистота 95%; m/z 347 [MH]+.
Синтез (ВВ19)
К перемешанному раствору (ВВ18) (1,18 г, 1 экв.) в ТГФ/Н2О (1:1; 20 мл) добавляли LiOH.H2O (173 мг, 1,2 экв.) и реакционную смесь перемешивали при комнатной температуре в течение 5,5 часов. ТГФ удаляли в вакууме и водную фазу промывали EtOAc (5 мл) и подкисляли до рН 4-5 (2М HCl, ~1-2 мл). Водную фазу экстрагировали EtOAc (3×20 мл), сушили (Na2SO4) и концентрировали в вакууме с получением желаемого соединения (ВВ19) (669 мг, 62%) в виде пены кремового цвета. ЖХ/МС чистота 98,8%; m/z 319 [МН]+.
Синтез (ВВ20)

ВВ20 синтезировали с использованием химических реакций, аналогичных реакциям, описанным выше для ВВ19.
Этап гидролиза промежуточных соединений в процессе синтеза PVA-081:

К перемешанному раствору сложного эфира (ВВ21) (130 мг) в ТГФ/Н2О (3:1, 8 мл) добавляли LiOH (20 мг). Реакционную смесь нагревали с обратным холодильником в течение ночи и затем позволяли охлаждаться до комнатной температуры. Реакционную смесь концентрировали при пониженном давлении до примерно 1 мл. Доводили значение рН до 2-3 путем добавления HCl (1,0 М водного раствора). Полученный осадок фильтровали и промывали H2O (10 мл) и диэтиловым эфиром (5 мл) и затем сушили в вакуумной печи при 50°C с получением (ВВ22) (90 мг, 71%) в виде твердого вещества белого цвета. ЖХ/МС, Rt=2,81 мин. (AnalpH2_MeOH), m/z 603 (МН+).
Синтез изоиианида - Общий способ:

Синтез формиламидов:
Типичный способ включает:
К раствору амина (1 г, 1 экв.) при 0°C добавляли этилформат (1,2 экв.), после чего реакционную смесь перемешивали при 0°C в течение 2 часов. Добавляли ДХМ (5 мл) и реакционную смесь перемешивали в течение 30 минут при комнатной температуре, после чего неочищенную реакционную смесь растирали с изо-гексаном с получением желаемого соединения.
Синтез изоцианидов:
К раствору формиламида (100 мг, 0,58 ммоль, 1 экв.) в ДХМ (5 мл) добавляли PS-тозилхлорид (3 экв.) и пиридин (1,5 мл), после чего реакционную смесь перемешивали при комнатной температуре в течение 20 минут до удаления PS-тозилхлорида посредством фильтрования. Органический слой промывали раствором (водным) 2 М KHSO4 (3×30 мл), сушили над MgSO4, фильтровали и растворитель удаляли в вакууме с получением желаемого изоцианида, который использовали в указанном виде без дополнительной очистки.
Биологические методы - Ферментативные анализы
Многие соединения содержали достаточно основный центр и были очищены таким образом, что, вероятно, они были получены в виде соответствующей соли трифторуксусной кислоты (ТФУ). Таким образом, считается, что в биологических исследованиях, описанных в настоящей заявке, следующие соединения исследовали в форме соответствующей соли ТФУ:
PVA-007, PVA-018, PVA-020, PVA-022, PVA-023, PVA-024, PVA-025, PVA-035, PVA-036, PVA-038, PVA-039, PVA-040, PVA-043, PVA-047, PVA-048, PVA-049, PVA-055, PVA-059, PVA-060, PVA-061, PVA-062, PVA-063, PVA-064, PVA-065, PVA-069, PVA-070, PVA-071, PVA-072, PVA-073, PVA-074, PVA-083, PVA-086, PVA-089, PVA-092, PVA-093, PVA-099, PVA-105, PVA-119, PVA-120, PVA-124, PVA-125, PVA-127, PVA-128, PVA-130, PVA-131, PVA-136, PVA-137, PVA-138, PVA-140, PVA-145, PVA-146, PVA-147, PVA-150, PVA-159, PVA-160, PVA-172, PVA-173, PVA-174, PVA-175, PVA-176, PVA-185, PVA-186, PVA-187, PVA-188, PVA-195, PVA-210, PVA-211, PVA-216.
Многие соединения содержали достаточно основный центр и были очищены таким образом, что, вероятно, они были получены в виде соответствующей соли муравьиной кислоты. Таким образом, считается, что в биологических исследованиях, описанных в настоящей заявке, следующие соединения исследовали в форме соответствующей соли муравьиной кислоты: PVA-098.
Некоторые их соединений содержат четвертичную аммонийную группу и были очищены с их получением с трифторацетатным противоионом или форматным противоионом. Предполагается, что в биологических исследованиях, описанных в настоящей заявке, следующие соединения исследовали в форме соответствующей соли с трифторацетатным противоионом: PVA-153, PVA-154. Подобным образом, предполагается, что в биологических исследованиях, описанных в настоящей заявке, следующие соединения исследовали в форме соответствующей соли с форматным противоионом: PVA-096.
Анализ Der p 1
Очистка Der p 1:
Клещей домашней пыли вида Dermatophagoides pteronyssinus культивировали, как описано в источнике Zhang et al., 2007. Der p 1 очищали хроматографическим методом и идентифицировали с помощью электрофореза в полиакриламидном геле в присутствии додецилсульфата натрия и масс-спектрометрии MALDI-TOF (время-пролетной ионизации лазерной десорбцией с использованием матрицы) (см. Zhang et al., 2007). Концентрацию Der p 1 в растворе определяли в кварцевой кювете на основании абсорбции при 280 нм с использованием коэффициента экстинкции 47,705 М-1 см-1.
Анализ ферментативной активности Der p 1:
Используемый флуорогенный субстрат для измерения протеолитической активности Der p 1 представлял собой 2-аминобензоилвалилаланилнорлейцилсерил(3-нитро)тирозиниласпартамид.
Флуоресценция указанного соединения тушится внутренним резонансным переносом энергии флуоресценции (FRET), но при расщеплении повышается его излучение на 420 нм, тогда когда субстрат возбуждается при 330 нм (см. Zhang et al., 2007).
Исследуемые соединения растворяли в безводном ДМСО и хранили при 4°C в виде исходных растворов до момента их разведения для использования в скрининговых анализах. Конечная концентрация ДМСО во всех ферментативных анализах составляла 0,5% об./об.
Реакционные смеси наносили в 96-луночные планшеты (Perkin Elmer Optiplate 96F, Perkin Elmer LAS, Seer Green, Бакингемшир, Великобритания) с использованием роботизированной системы Perkin Elmer MultiPROBE II Plus HTS EX с приспособлением Gripper. Планшеты предварительно заполняли серийными разведениями (10 мкл/лунку) тестируемого соединения или соответствующего контроля в реакционном буфере (состав: калиевый фосфатный буфер, рН 8,25, содержащий 1 мМ ЭДТА), к которому добавляли дополнительные 60 мкл реакционного буфера. Затем добавляли дитиотреитол (DTT, 10 мкл/лунку, конечная концентрация 1 мМ) совместно с 10 мкл Der p 1, растворенного в концентрации 2,5 мкг/мл в реакционном буфере, с добавлением 1 мМ DTT. Реакционные смеси затем инкубировали при комнатной температуре в течение 20 минут до инициации реакции путем добавления 10 мкл субстрата (конечная концентрация 12,5 мкМ). Планшет сразу переносили на флуоресцентный планшетный ридер (Perkin Elmer Fusion Alpha-FP или Perkin Elmer Envision), снабженный термостатируемым держателем с установленной температурой 30°C, и за реакцией следили на основании возбуждения/излучения на 330/420 нм.
Анализ данных Ферментативного анализа
Активность ингибирования определяли из кривой процесса реакций в присутствии диапазона концентраций ингибиторов. Изначальные скорости реакции рассчитывали с помощью расчетной нелинейной регрессии и определяли обеспечиваемый соединением уровень ингибирования, на основании которого рассчитывали концентрацию, необходимую для ингибирования реакции на 50% (IC50), в соответствии со схемой ниже:
Изначальную скорость в каждой лунке переводили в относительную активность с помощью Уравнения 1:
Уравнение 1:
Относительная активность = (изначальная скорость при концентрации ингибитора [X] / Изначальная скорость при концентрации ингибитора ноль) * 100
Затем определяли IC50 путем нанесения данных относительной активности и концентрации ингибитора на 4-параметрическую логистическую кривую с использованием Уравнения 2:
Уравнение 2:
V=Vmin+[Vmax-Vmin]/[1+(X/IC50) Наклон]
где:
V представляет собой относительную активность фермента в присутствии ингибитора в концентрации [X];
[X] представляет собой концентрацию ингибитора;
Vmin представляет собой минимальное значение Y, наблюдаемое при высокой концентрации ингибитора;
Vmax представляет собой максимальное значение Y, наблюдаемое при нулевой концентрации ингибитора; и
Наклон представляет собой тангенс угла наклона кривой зависимости доза-эффект (ингибирования).
Биологические данные - Ферментативный анализ Per p 1
Следующие соединения исследовали с помощью анализа Der p 1, описанного выше: PVA-001-PVA-216.
Было обнаружено, что IC50 всех соединений для Der p 1 составляет менее 10 мкМ.
Было обнаружено, что IC50 следующих соединений для Der p 1 составляет менее 2 мкМ:
PVA-001, PVA-002, PVA-003, PVA-004, PVA-005, PVA-006, PVA-007, PVA-009, PVA-010, PVA-011, PVA-012, PVA-015, PVA-016, PVA-017, PVA-018, PVA-019, PVA-020, PVA-021, PVA-022, PVA-023, PVA-024, PVA-025, PVA-026, PVA-027, PVA-028, PVA-029, PVA-030, PVA-031, PVA-032, PVA-033, PVA-034, PVA-035, PVA-036, PVA-037, PVA-038, PVA-039, PVA-040, PVA-041, PVA-042, PVA-043, PVA-044, PVA-045, PVA-046, PVA-047, PVA-048, PVA-049, PVA-050, PVA-051, PVA-052, PVA-053, PVA-054, PVA-055, PVA-056, PVA-057, PVA-058, PVA-059, PVA-060, PVA-061, PVA-062, PVA-063, PVA-064, PVA-065, PVA-066, PVA-067, PVA-068, PVA-069, PVA-070, PVA-071, PVA-072, PVA-073, PVA-074, PVA-075, PVA-076, PVA-077, PVA-078, PVA-079, PVA-080, PVA-081, PVA-082, PVA-083, PVA-084, PVA-085, PVA-086, PVA-088, PVA-089, PVA-090, PVA-091, PVA-092, PVA-093, PVA-094, PVA-095, PVA-096, PVA-097, PVA-098, PVA-099, PVA-100, PVA-101, PVA-102, PVA-103, PVA-104, PVA-105, PVA-106, PVA-107, PVA-108, PVA-109, PVA-110, PVA-111, PVA-112, PVA-113, PVA-114, PVA-115, PVA-116, PVA-117, PVA-118, PVA-119, PVA-120, PVA-121, PVA-122, PVA-123, PVA-124, PVA-125, PVA-126. PVA-127, PVA-128, PVA-129, PVA-130, PVA-131, PVA-132, PVA-133, PVA-134, PVA-135, PVA-136, PVA-137, PVA-138, PVA-140, PVA-141, PVA-142, PVA-143, PVA-144, PVA-145, PVA-146, PVA-147, PVA-148, PVA-149, PVA-150, PVA-151, PVA-152, PVA-153, PVA-154, PVA-155, PVA-156, PVA-157, PVA-158, PVA-159, PVA-160, PVA-161, PVA-162, PVA-163, PVA-164, PVA-165, PVA-166, PVA-167, PVA-168, PVA-169, PVA-170, PVA-171, PVA-172, PVA-173, PVA-174, PVA-175, PVA-176, PVA-177, PVA-178, PVA-179, PVA-180, PVA-181, PVA-182, PVA-183, PVA-184, PVA-185, PVA-186, PVA-187, PVA-188, PVA-189, PVA-190, PVA-191, PVA-192, PVA-193, PVA-194, PVA-195, PVA-196, PVA-197, PVA-198, PVA-199, PVA-200, PVA-201, PVA-202, PVA-203, PVA-204, PVA-205, PVA-206, PVA-207, PVA-208, PVA-209, PVA-210, PVA-211, PVA-212, PVA-213, PVA-214, PVA-215, PVA-216.
Было обнаружено, что IC50 следующих соединений для Der p 1 составляет менее 200 нМ:
PVA-001, PVA-002, PVA-003, PVA-004, PVA-005, PVA-009, PVA-010, PVA-011, PVA-015, PVA-017, PVA-019, PVA-020, PVA-022, PVA-023, PVA-024, PVA-026, PVA-027, PVA-028, PVA-030, PVA-031, PVA-032, PVA-033, PVA-035, PVA-036, PVA-037, PVA-038, PVA-039, PVA-041, PVA-042, PVA-044, PVA-045, PVA-046, PVA-047, PVA-048, PVA-049, PVA-050, PVA-051, PVA-052, PVA-053, PVA-054, PVA-055, PVA-056, PVA-057, PVA-058, PVA-059, PVA-060, PVA-061, PVA-062, PVA-063, PVA-064, PVA-065, PVA-066, PVA-067, PVA-068, PVA-071, PVA-072, PVA-073, PVA-074, PVA-075, PVA-076, PVA-077, PVA-078, PVA-079, PVA-080, PVA-081, PVA-082, PVA-083, PVA-084, PVA-085, PVA-086, PVA-088, PVA-089, PVA-091, PVA-092, PVA-093, PVA-094, PVA-095, PVA-096, PVA-097, PVA-098, PVA-099, PVA-100, PVA-101, PVA-102, PVA-103, PVA-104, PVA-105, PVA-106, PVA-107, PVA-108, PVA-109, PVA-110, PVA-111, PVA-112, PVA-113, PVA-114, PVA-115, PVA-116, PVA-117, PVA-118, PVA-119, PVA-120, PVA-121, PVA-122, PVA-123, PVA-124, PVA-125, PVA-126, PVA-127, PVA-128, PVA-129, PVA-130, PVA-131, PVA-132, PVA-133, PVA-134, PVA-135, PVA-136, PVA-137, PVA-138, PVA-141, PVA-142, PVA-143, PVA-144, PVA-145, PVA-146, PVA-147, PVA-148, PVA-149, PVA-150, PVA-151, PVA-152, PVA-153, PVA-154, PVA-155, PVA-156, PVA-157, PVA-158, PVA-159, PVA-160, PVA-161, PVA-162, PVA-163, PVA-164, PVA-165, PVA-166, PVA-167, PVA-168, PVA-169, PVA-170, PVA-171, PVA-172, PVA-173, PVA-174, PVA-175, PVA-176, PVA-177, PVA-178, PVA-179, PVA-180, PVA-181, PVA-182, PVA-183, PVA-184, PVA-185, PVA-186, PVA-187, PVA-188, PVA-189, PVA-190, PVA-191, PVA-192, PVA-193, PVA-194, PVA-195, PVA-196, PVA-197, PVA-198, PVA-199, PVA-200, PVA-201, PVA-202, PVA-203, PVA-204, PVA-205, PVA-206, PVA-207, PVA-208, PVA-209, PVA-210, PVA-211, PVA-212, PVA-213, PVA-214, PVA-215, PVA-216.
Было обнаружено, что IC50 следующих соединений для Der p 1 составляет менее 20 нМ:
PVA-001, PVA-003, PVA-005, PVA-009, PVA-026, PVA-035, PVA-037, PVA-038, PVA-039, PVA-042, PVA-047, PVA-055, PVA-066, PVA-067, PVA-068, PVA-071, PVA-072, PVA-073, PVA-074, PVA-078, PVA-079, PVA-080, PVA-092, PVA-093, PVA-094, PVA-096, PVA-097, PVA-099, PVA-104, PVA-105, PVA-108, PVA-111, PVA-112, PVA-116, PVA-118, PVA-128, PVA-129, PVA-130, PVA-132. PVA-134, PVA-135, PVA-136, PVA-137, PVA-143, PVA-144, PVA-146, PVA-147, PVA-149, PVA-150, PVA-151, PVA-153, PVA-154, PVA-155, PVA-156, PVA-157, PVA-158, PVA-161, PVA-162, PVA-164, PVA-169, PVA-177, PVA-178, PVA-182, PVA-183, PVA-185, PVA-186, PVA-187, PVA-188, PVA-192, PVA-194, PVA-195, PVA-196, PVA-197, PVA-199, PVA-202, PVA-204, PVA-205, PVA-206, PVA-207, PVA-208, PVA-209, PVA-210, PVA-211, PVA-212, PVA-213, PVA-214, PVA-215, PVA-216.
Данные для четырех PVA соединений показаны в следующей таблице.
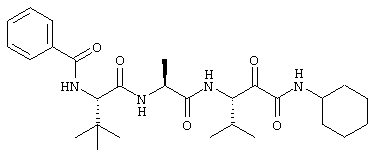
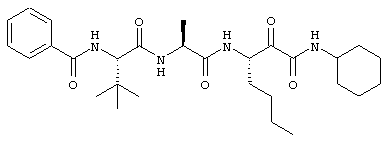

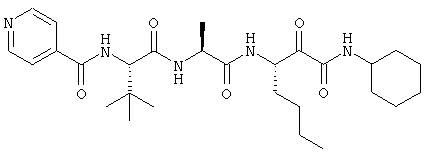
Биологические способы - Исследование сенсибилизации аллергеном in vivo
Идентификация и распределение животных по группам:
Исследования проводили на самцах крыс Brown Norway (массой примерно 350 г на момент сенсибилизации аллергеном), полученных из Harlan UK Ltd. Каждому животному после сенсибилизации присваивали уникальный идентификационный номер с помощью водостойкой пометки на хвосте и случайным образом распределяли по группам. Все исследования проводили в соответствии с «Актом о животных» (Animals (Scientific Procedures) Act) 1986 года согласно руководству по реализации указанного Акта Министерства внутренних дел (Home Office) Великобритании и в соответствии со всеми применимыми нормами и правилами по уходу и содержанию лабораторных животных.
Содержание и условия окружающей среды:
Сначала животных содержали с проветриваемой жилой комнате в помещении для животных, затем перемещали в процедурную комнату. Животных помещали в клетки в группах до 5 животных. Во время проведения исследования комнаты и клетки регулярно чистили для поддержания гигиены. Комнаты освещали люминесцентными лампами с установленным 12-часовым светотемновым циклом (лампы включали в 07:00 и выключали в 19:00) в соответствии с рекомендациями по реализации «Акта о животных» (Animals (Scientific Procedures) Act 1986) Министерства внутренних дел (Home Office) Великобритании. Температуру воздуха (требуемая температура 21°C±2°C) и относительную влажность (не контролировали) измеряли во время фазы акклиматизации и натурализации. Животные имели неограниченный доступ к пище (RM-1, Special Diets Services, Битам, Великобритания) и водопроводной воде.
Способ сенсибилизации аллергеном клещей домашней пыли (HDM):
Смесь аллергенов HDM отбирали из лабораторной культуры Dermatophagoides pteronyssinus. Дозу аллергена стандартизировали в соответствии с содержанием в смеси Der p 1, которое определяли с помощью ИФА с использованием в качестве контроля стандарта IUIS (International Union of Immunological Societies, Международного союза иммунологических обществ) для Der p 1. Ежедневная доза аллергена для сенсибилизации для каждого животного содержала 10 мкг Der p 1. Лиофилизированные исходные растворы смеси аллергена HDM, которые хранили при -20°C, восстанавливали до исходного объема с помощью стерилизованной посредством фильтрования через 0,22 мкм фильтр деионизированной воды, содержащей 5 мМ L-цистеин и 0,05% (по объему) твин 20, и разводили до рабочей концентрации стерильным фосфатно-солевым буфером Дульбекко, содержащим 5 мМ L-цистеин и 0,05% (по объему) твин 20. Животных сенсибилизировали к смеси всех аллергенов HDM на 0, 7 и 14 день путем внутрибрюшинной инъекции (0,5 мл) указанной смеси, представленной в описанной выше форме.
Регистрация физиологических показателей:
На 21 день протокола сенсибилизации и провокации аллергеном, крыс анестезировали пентобарбитоном (100 мг/кг, внутрибрюшинно) и вентилировали с помощью трахеальной канюли (примерно 7 мл/кг, 1 Гц) смесью воздуха и кислорода (50:50). Анестезированных вентилируемых животных парализовали с помощью норкурона (4 мг/кг, внутримышечно). За вентиляций следили с помощью датчика тока (Fleisch, тип 0000), последовательно соединенным с респираторным насосом. За соответствующими изменениями давления в грудной клетке следили непосредственно с помощью внутригрудной канюли таким образом, что могли измерять и регистрировать разницу давлений между трахеей и грудной клеткой. На основании указанных измерений тока и разности давлений рассчитывали сопротивление дыхательных путей (RL) и динамической податливости легких (Cdyn) для каждого дыхательного цикла на цифровом электронном респираторном анализаторе (PMS, Mumed Ltd, Великобритания). Кровяное давление и частоту сердечных сокращений регистрировали с помощью датчика на сонной артерии.
Доставка лекарственных средств и сенсибилизация аллергеном:
Лекарственные средства растворяли в ДМСО с получением 10 мМ исходных растворов и затем разводили в стерильном соляном растворе (Baxter Healthcare, Беркшир, Великобритания) для применения в лечении. Растворы лекарственных средств (100 мкл 40 мкМ раствора) вводили интратрахеальным (ИТ) путем с использованием распыляющего устройства Perm Century IA-1C с сапфировым наконечником, соединенного со шприцом высокого давления FMJ-250 (Penn Century, Филадельфия, Пенсильвания, США). Для указанных исследований наконечник распыляющего устройства IA-1C вводили в трахеальную канюлю и доставляли объем лекарственного средства, регулируя введение с помощью волюметрических фиксаторов поршня шприца. Указанная комбинация распыляющего устройства и шприца обеспечивала распыление капель жидкости, имеющих масс-медианный аэродинамический диаметр 16-22 мкм.
Сенсибилизацию аллергеном проводили с использованием смеси аллергенов HDM, содержащей Der p 1 в дозе 10 мкг. Лиофилизированные исходные растворы смеси аллергенов HDM, которые хранили при -20°C, восстанавливали до их исходного объема с помощью стерилизованной посредством фильтрования через 0,22 мкм фильтр деионизированной воды, содержащей 5 мМ L-цистеин и 0,05% об./об. твин 20, и разводили до рабочей концентрации стерильным фосфатно-солевым буфером Дульбекко, содержащим 5 мМ L-цистеин и 0,05% (по объему) твин 20. Сенсибилизацию аллергеном (100 мкл) проводили интратрахеальным (ИТ) путем с использованием распыляющего устройства Penn Century, как описано выше.
План исследования:
План исследования включал группы из 12 животных, которых активно сенсибилизировали к аллергенам HDM, как описано выше. На 21 день исследования группы подвергали двум отдельным сенсибилизациям к аллергенам HDM интратрахеальным (ИТ) путем. Во всех случаях эффект сенсибилизации 1 полностью устранялся до проведения второй сенсибилизации. За два 2 часа до второй сенсибилизации аллергеном животные получали дозу исследуемого соединения.
Анализ данных:
Для оценки эффекта сенсибилизации аллергеном и его модификации исследуемыми соединениями измеряли параметры легочной функции до момента доставки аллергена (исходный уровень) и во время максимального ответа. Количественную разницу в параметре легочной функции (например, изменении сопротивления дыхательных путей) записывали как интенсивность сенсибилизации аллергеном. Описанный процесс повторяли после дозирования животных исследуемым соединением. Статистический анализ ответов до и после введения исследуемого соединения использовали для определения того, оказывало ли указанное соединение значимый эффект. Экспериментальным путем было обнаружено, что указанные статистические сравнения можно проводить как путем сравнения самого изменения параметра легочной функции до и после лечения исследуемым соединением, так и путем выражения величины второй сенсибилизации аллергеном в виде процента от первой сенсибилизации и проведения статистической оценки с использованием трансформированных данных, с одинаковой достоверностью.
Биологические данные - Исследования сенсибилизации аллергеном in vivo
Обоснование плана исследования
Фигура 1 представляет собой гистограмму величины ответа после Сенсибилизации 1 (слева) и Сенсибилизации 2 (справа), выраженной как процент от величины ответа после Сенсибилизации 1.
На Фигуре 1 показаны результаты, полученные после подвержения группы крыс, сенсибилизированных к HDM аллергенам, двум последовательным сенсибилизациям одной и той же смесью аллергенов интратрахеальным (ИТ) путем на 21 день после начала сенсибилизации. Средний ответ (медиану) на сенсибилизацию 1 определяли и выражали как 100%. Затем определяли величину второго ответа для каждой крысы и выражали как процент от ответа на сенсибилизацию 1. Для иллюстрации ответа на вторую сенсибилизацию данные представлены в виде медианы и межквартильного размаха, определенного у 12 животных.
Приведенные данные указывают на то, что величина второй сенсибилизации подобна величине первой сенсибилизации, что дает возможность определения модулирующего эффекта вводимого между двумя обработками лекарственного средства.
Влияние соединений на острый аллергический бронхоспазм:
Два соединения (PVA-026 и PVA-038) исследовали с помощью способов сенсибилизации аллергеном in vivo, описанных выше. (PVA-038 использовали в форме соответствующей соли трифторуксусной кислоты (ТФУ)).


Фигура 2 представляет собой гистограмму изменения сопротивления дыхательных путей (см H2O л-1 сек-1) после контрольной сенсибилизации аллергеном (слева) и сенсибилизации аллергеном через 120 минут после лечения исследуемым соединением PVA-026. (Представлены медианы. Погрешность в виде 25-го/75-го перцентилей. Для (*): Р<0,05, критерий суммы рангов Манна-Уитни по отношению к контрольной сенсибилизации аллергеном.)
Данные на Фигуре 2 показывают изменение сопротивления дыхательных путей при контрольной сенсибилизации аллергеном и изменение после следующей сенсибилизации, проведенной через 2 часа после интратрахеального (ИТ) дозирования животных исследуемым соединением PVA-026. Данные представлены в виде медиан с погрешностями, представляющими собой межквартильный размах. Интенсивность второй сенсибилизации аллергеном была значительно ниже по сравнению с первой сенсибилизацией (Р<0,05, критерий суммы рангов Манна-Уитни). Специалистам в данной области техники известно, что подавление острого бронхоспазма после провокации аллергеном в подобных описанной экспериментальных моделях является показателем клинически благоприятного эффекта при астме.
Фигура 3 представляет собой гистограмму изменения сопротивления дыхательных путей (см H2O л-1 сек-1) после контрольной сенсибилизации аллергеном (слева) и сенсибилизации аллергеном через 120 минут после лечения исследуемым соединением PVA-038 (в виде соли ТФУ). (Представлены медианы. Погрешность в виде 25-го/75-го процентилей. Для (*): Р<0,05, критерий суммы рангов Манна-Уитни по отношению к контрольной сенсибилизации аллергеном.)
Данные на Фигуре 3 показывают изменение сопротивления дыхательных путей при контрольной сенсибилизации аллергеном и изменение, наблюдаемое при последующей сенсибилизации, проведенной через 2 часа после интратрахеального (ИТ) дозирования животных исследуемым соединением PVA-038 (в виде соли ТФУ). Данные представлены в виде медиан с погрешностями, представленными межквартильным размахом. Величина второй сенсибилизации аллергеном была значительно ниже по сравнению с первой сенсибилизацией (Р<0,05, критерий суммы рангов Манна-Уитни). Специалистам в данной области техники известно, что подавление острого бронхоспазма после провокации аллергеном в подобных описанной экспериментальных моделях является показателем клинического благоприятного эффекта при астме.
***
Выше описаны принципы, предпочтительные варианты реализации и способы реализации настоящего изобретения. Однако изобретение не ограничивается конкретными обсуждаемыми вариантами реализации. Напротив, описанные выше варианты реализации изобретения следует считать иллюстративными, а не ограничивающими, и следует понимать, что специалисты в данной области техники могут вносить изменения в указанные варианты реализации изобретения, не выходя за рамки объема настоящего изобретения.
Ссылки
Для более полного описания и раскрытия изобретения и уровня техники, к которому относится изобретение, в настоящее заявке цитируется ряд патентов и публикаций. Полные ссылки на указанные цитаты представлены ниже. Каждая из указанных цитат в настоящей заявке полностью включена посредством ссылки в настоящее описание в той же мере, как если бы было особо и отдельно указано, что каждая отдельная ссылка включена посредством ссылки.
Arasappan et al., 2009, "Toward second generation hepatitis С virus NS3 serine protease inhibitors: Discovery of novel P4 modified analogues with improved potency and pharmacokinetic profile", J. Med. Chem.. pp.2806-2897.
Arruda et al., 1991, "Exposure and sensitization to dust mite allergens among asthmatic children in Sao Paulo, Brazil", Clin. Exp. Allergy. Vol.21, pp.433-439.
Asokananthan et al., 2002, "House dust mite allergens induce proinflammatory cytokines from respiratory epithelial cells: the cysteine protease allergen, Der p 1, activates protease-activated receptor (PAR)-2 and inactivates PAR-1", J. Immunol., Vol.169, pp.4572-4578.
Barrett et al., 2005, "P2-P3 conformationally constrained ketoamide-based inhibitors of cathepsin K", Biorg. Med. Chem. Lett., Vol.15, pp.3540-3546.
Bodini et al., 2004, "Exhaled breath condensate eicosanoids and sputum eosinophils in asthmatic children: a pilot study", Pediatr. Allergy Immunol., Vol.15, pp.26-31.
Bosch et al., 2009, "Dry powder aerosols of nanoparticulate drugs", US Patent No. 7,521,068, granted 21 April 2009.
Broide et al., 1992, "Cytokines in symptomatic asthma airways", J. Allergy Clin. Immunol., Vol.89, pp.958-967.
Charpin et al., 1991, "Altitude and allergy to house-dust mites. A paradigm of the influence of environmental exposure on allergic sensitization", Am. Rev. Respir. Dis., Vol.143, pp.983-986.
Comoy et al., 1998, "The house dust mite allergen, Dermatophagoides pteronyssinus, promotes type 2 responses by modulating the balance between IL-4 and IFN-gamma", J. Immunol., Vol.160, pp.2456-2462.
Deb et al., 2007, "Major house dust mite allergens Dermatophagoides pteronyssinus 1 and Dermatophagoides farinae 1 degrade and inactivate lung surfactant proteins A and D", J. Biol. Chem., Vol.282, pp.36808-36819.
Dowse et al., 1985, "The association between Dermatophagoides mites and the increasing prevalence of asthma in village communities within the Papua New Guinea highlands", J. Allergy Clin. Immunol., Vol.75, pp.75-83.
Eden et al., 2003, "Asthma features in severe alpha1-antitrypsin deficiency: experience of the National Heart, Lung, and Blood Institute Registry", Chest. Vol.123, pp.765-771.
Fahy et al., 1995, "Comparison of samples collected by sputum induction and bronchoscopy from asthmatic and healthy subjects", Am. J. Respir. Crit. Care Med., Vol.152, pp.53-58.
Gelber et al., 1993, "Sensitization and exposure to indoor allergens as risk factors for asthma among patients presenting to hospital", Am. Rev. Respir. Dis., Vol.147, pp.573-578.
Ghaemmaghami et al., 2002, "The proteolytic activity of the major dust mite allergen Der p 1 conditions dendritic cells to produce less interleukin-12: allergen-induced Th2 bias determined at the dendritic cell level", Clin. Exp. Allergy. Vol.32, pp.1468-1475.
Gough et al., 2001. "The proteolytic activity of the major dust mite allergen Der p 1 enhances the IgE antibody response to a bystander antigen", Clin. Exp. Allergy. Vol.31, pp.1594 1598.
Gourgoulianis et al., 2001, "The influence of altitude in bronchial asthma", Arch. Med. Res., Vol.32, pp.429-431.
Grootendorst et al., 2001, "Benefits of high altitude allergen avoidance in atopic adolescents with moderate to severe asthma, over and above treatment with high dose inhaled steroids", Clin. Exp. Allergy. Vol.31, pp.400-408.
Hellings et al., 2001, "Eosinophilic rhinitis accompanies the development of lower airway inflammation and hyper-reactivity in sensitized mice exposed to aerosolized allergen", Clin. Exp. Allergy. Vol.31, pp.782-790.
Holt et al., 1990, "A contiguous network of dendritic antigen-presenting cells within the respiratory epithelium", Int. Arch. Allergy Appl. Immunol., Vol.91, pp.155-159.
Holt, 2002, "The role of airway dendritic cell populations in regulation of T-cell responses to inhaled antigens: atopic asthma as a paradigm", J. Aerosol Med., Vol.15, pp.161-168.
Huh et al., 2003, "Bidirectional interactions between antigen-bearing respiratory tract dendritic cells (DCs) and Т cells precede the late phase reaction in experimental asthma: DC activation occurs in the airway mucosa but not in the lung parenchyma", J. Exp. Med., Vol.198, pp.19-30.
Hyde et al., 1979, "Protease inhibitor variants in children and young adults with chronic asthma", Ann. Allergy. Vol.43, pp.8-13.
Jaakkola et al., 2006, "Are atopy and specific IgE to mites and molds important for adult asthma?", J. Allergy Clin. Immunol., Vol.117, pp.642-648.
Marcaccini et al., "2. Post Condensation Modifications of the Passerini and Ugi Reactions", in Multicomponent Reactions. 1st Edition (Ed., Jieping et al., Wiley-VCH, 2005), Chapter 2, pp.33-75, and especially pp.41-47.
Kalsheker et al., 1996, "The house dust mite allergen Der p1 catalytically inactivates alpha 1-antitrypsin by specific reactive centre loop cleavage: a mechanism that promotes airway inflammation and asthma", Biochem. Biophys. Res. Commun., Vol.221, pp.59-61.
King et al., 1998, "Dust mite proteolytic allergens induce cytokine release from cultured airway epithelium", J. Immunol., Vol.161, pp.3645-3651.
Lambrecht et al., 2002, "Myeloid dendritic cells make it to the top", Clin. Exp. Allergy. Vol.32, pp.805-810.
Lambrecht et al., 2003a, "Taking our breath away: dendritic cells in the pathogenesis of asthma", Nat. Rev. Immunol., Vol.3, pp.994-1003.
Lambrecht et al., 2003b, "The other cells in asthma: dendritic cell and epithelial cell crosstalk", Current Opinion in Pulmonary Medicine. Vol.9, pp.34-41.
McCusker et al., 2002, "Site-specific sensitization in a murine model of allergic rhinitis: role of the upper airway in lower airways disease", J. Allergy Clin. Immunol., Vol.110, pp.891-898.
McMillan et al., 2004, "Prolonged allergen challenge in mice leads to persistent airway remodelling", Clin. Exp. Allergy. Vol.34, pp.497-507.
Miyamoto et al., 1968, "Allergenic identity between the common floor mite (Dermatophagoides farinae Hughes, 1961) and house dust as a causative antigen in bronchial asthma", J. Allergy. Vol.42, pp.14-28.
Muraguchi et al., 1988, "The essential role of В cell stimulatory factor 2 (BSF-2/IL-6) for the terminal differentiation of В cells", J. Exp. Med. Vol.167, pp.332-344.
Peat et al., 1991, "Sensitivity to common allergens: relation to respiratory symptoms and bronchial hyper-responsiveness in children from three different climatic areas of Australia", Clin. Exp. Allergy. Vol.21, pp.573-581.
Peat et al., 1996, "House dust mite allergens. A major risk factor for childhood asthma in Australia", Am. J. Respir. Crit. Care Med., Vol.153, pp.141-146.
Peroni et al., 1994, "Effective allergen avoidance at high altitude reduces allergen-induced bronchial hyperresponsiveness", Am. J. Respir. Crit. Care Med., Vol.149, pp.1442-1446.
Piacentini et al., 1998, "Mite-antigen avoidance can reduce bronchial epithelial shedding in allergic asthmatic children", Clin. Exp. Allergy. Vol.28, pp.561-567.
Piacentini et al., 1999, "Allergen avoidance at high altitude and urinary eosinophil protein X", J. Allergy Clin. Immunol. Vol.104, pp.243-244.
Platts-Mills et al., 1987, "Seasonal variation in dust mite and grass-pollen allergens in dust from the houses of patients with asthma", J. Allergy Clin. Immunol., Vol.79, pp.781-791.
Platts-Mills et al., 1997, "Indoor allergens and asthma: report of the Third International Workshop", J. Allergy Clin. Immunol., Vol.100, pp.S2-24.
Platts-Mills et al., 2000, "The role of intervention in established allergy: avoidance of indoor allergens in the treatment of chronic allergic disease", J. Allergy Clin. Immunol.. Vol.106, pp.787-804.
Pollart et al., 1989, "Epidemiology of acute asthma: IgE antibodies to common inhalant allergens as a risk factor for emergency room visits", J. Allergy Clin. Immunol., Vol 83, pp.875-882.
Rudolph et al., 1978, "The significance of nasal protease inhibitor concentrations in house dust allergy", Allergy. Vol.33, pp.310-315.
Schultze-Werninghaus, 2006, "Should asthma management include sojourns at high altitude?", Chem. Immunol. Allergy. Vol.91, pp.16-29.
Seymour et al., 1998, "Aerosol-induced immunoglobulin (Ig)-E unresponsiveness to ovalbumin does not require CD8+ or Т cell receptor (TCR)-gamma/delta+ Т cells or interferon (IFN)-gamma in a murine model of allergen sensitization", J. Exp. Med., Vol.187, pp.721-731.
Sigsgaard et al., 2000, "S and Z alphal-antitrypsin alleles are risk factors for bronchial hyperresponsiveness in young farmers: an example of gene/environment interaction", Eur. Respir. J. Vol.16, pp.50-55.
Smith et al., 1969, "Clinical significance of skin reactions to mite extracts in children with asthma", Br. Med. J. Vol.1, pp.723-726.
Sporik et al., 1990, "Exposure to house-dust mite allergen (Der p 1) and the development of asthma in childhood. A prospective study", N. Engl. J. Med., Vol.323, pp.502-507.
Stewart et al., 2003, "Allergen structure and function", in: Middleton′s Allergy. Principles and Practice. (Eds. Adkinson et al.; Publisher: Mosby, Philadelphia), pp.585-609.
Stick et al., 2003, "The airway epithelium as immune modulator: the LARC ascending", Am. J. Respir. Cell Mol. Biol. Vol.28, pp.641-644.
Sture et al., 1995, "Canine atopic dermatitis: the prevalence of psoitive intradermal skin tests at two sites in the north and south of Great Britain", Vet. Immunol. Immunopathol., Vol.44, pp.293-308.
van Halteren et al., 1997, "Regulation of antigen-specific IgE, lgG1, and mast cell responses to ingested allergen by mucosal tolerance induction", J. Immunol., Vol.159, pp.3009-3015.
van Velzen et al., 1996., "Effect of allergen avoidance at high altitude on direct and indirect bronchial hyperresponsiveness and markers of inflammation in children with allergic asthma", Thorax. Vol.51, pp.582-584.
Vercelli., 1989, "Endogenous interleukin 6 plays an obligatory role in interleukin 4-dependent human IgE synthesis", Eur. J. Immunol., Vol.19, pp.1419-1424.
Vervloet et al., 1982, "Altitude and house dust mites", J. Allergy Clin. Immunol., Vol.69, pp.290-296.
Wan et al., 1999, "Der p 1 facilitates transepithelial allergen delivery by disruption of tight junctions". J. Clin. Invest., Vol.104, pp.123-133.
Wan et al., 2000, "Tight junction properties of the immortalized human bronchial epithelial cell lines Calu-3 and 16HB", Eur. Respir. J., Vol.15, pp.1058-1068.
Winton et al., 1998, "Cell lines of pulmonary and non-pulmonary origin as tools to study the effects of house dust mite proteinases on the regulation of epithelial permeability", Clin. Exp. Allergy. Vol.28, pp.1273-1285.
Zhang et al., 2007, "Interactions between mature Der p 1 and its free prodomain indicate membership of a new family of C1 peptidases," Allergy. Vol.62, pp.1302-1309.
Zhang et al., 2009, "Novel Der p 1 inhibitors attenuate HDM sensitization in mice", Amer. J. Respir. Crit. Care Med., Vol.179, p.A4249.
Zhaozhao et al., 1996, "Novel peptidyl α-keto amide inhibitors of Calpains and Other Cysteine Proteases", J. Med. Chem., pp.4089-4098.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПИРРОЛИДИН-2-ОНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ФАКТОРА ХА | 2002 |
|
RU2318807C2 |
| ИМИДАЗОПИРАЗИНЫ В КАЧЕСТВЕ ИНГИБИТОРОВ ТИРОЗИНКИНАЗ | 2004 |
|
RU2405784C2 |
| НОВЫЕ ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ АЗАИНДОЛИНА В КАЧЕСТВЕ ИНГИБИТОРОВ NIK | 2018 |
|
RU2780577C2 |
| аЭКЗО-АЗАСПИРО-ИНГИБИТОРЫ ВЗАИМОДЕЙСТВИЯ МЕНИН-MLL | 2018 |
|
RU2795096C2 |
| МАКРОГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ | 2001 |
|
RU2275373C2 |
| НОВЫЕ ХИНОЛИНОВЫЕ СОЕДИНЕНИЯ | 2018 |
|
RU2810113C2 |
| N-СОДЕРЖАЩИЕ ГЕТЕРОАРИЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ JAK3 КИНАЗЫ | 2010 |
|
RU2553681C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, ИСПОЛЬЗУЕМЫЕ В КАЧЕСТВЕ ИНГИБИТОРОВ PDK1 | 2010 |
|
RU2615130C2 |
| БИЦИКЛИЧЕСКИЕ ГЕТЕРОАРИЛЬНЫЕ ПРОИЗВОДНЫЕ В КАЧЕСТВЕ СТИМУЛЯТОРОВ CFTR | 2017 |
|
RU2753056C2 |
| 3-АРИЛ-5-ЗАМЕЩЕННЫЕ СОЕДИНЕНИЯ ИЗОХИНОЛИН-1-ОНА И ИХ ТЕРАПЕВТИЧЕСКОЕ ПРИМЕНЕНИЕ | 2013 |
|
RU2696572C2 |



Изобретение относится к области лекарственных соединений. Предложены пирувамидные соединения формулы (X), которые ингибируют аллерген пылевых клещей 1 группы, представляющий собой пептидазу, например, Der p 1, Der f 1, Eur m 1. Также предложены фармацевтические композиции, содержащие указанные соединения, и применение указанных соединений и композиций для ингибирования аллергена 1 группы, представляющего собой пептидазу пылевых клещей, и для лечения заболеваний и нарушений, опосредованных аллергеном пылевых клещей 1 группы, в частности астмы, ринита, аллергического конъюнктивита, атопического дерматита, аллергического состояния, вызванного пылевыми клещами, аллергического состояния, вызванного аллергеном пылевых клещей 1 группы, и атопии у собак. 10 н. и 41 з.п. ф-лы, 3 ил., 1 табл., 1 пр.

1. Соединение, выбранное из соединений следующей формулы и их фармацевтически приемлемых солей:
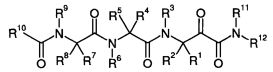
где:
-R1 независимо представляет собой -H или -R1A;
-R1A представляет собой насыщенный алифатический С1-6алкил;
-R2 представляет собой -H;
-R3 независимо представляет собой -H или -R3A;
-R3A представляет собой насыщенный алифатический С1-3алкил;
-R4 представляет собой -R4A;
-R4A представляет собой -Me;
-R5 представляет собой -H;
-R6 представляет собой -H или -R6A;
-R6A представляет собой насыщенный алифатический С1-3алкил;
-R7 представляет собой -H, -R7A или -R7B;
-R7A представляет собой насыщенный алифатический С1-6алкил;
-R7B независимо представляет собой -L7B1-R7BB или -R7BB;
-L7B1- представляет собой насыщенный алифатический С1-3алкилен;
-R7BB независимо представляет собой -R7BB1, -R7BB2, -R7BB3 или -R7BB4;
-R7BB1 независимо представляет собой фенил или нафтил и необязательно содержит один или более заместителей -RX3;
-R7BB2 представляет собой С5-10гетероарил и необязательно содержит один или более заместителей -RX3;
-R7BB3 представляет собой С3-7циклоалкил и необязательно содержит один или более заместителей -RX2 или является необязательно конденсированным с бензольным кольцом, которое необязательно содержит один или более заместителей -RX3;
-R7BB4 представляет собой насыщенный С5-10циклоалкил с мостиком и необязательно содержит один или более заместителей -RX2;
-R8 представляет собой -Н;
-R9 независимо представляет собой -Н или -R9A;
-R9A представляет собой насыщенный алифатический С1-4алкил;
-R10 независимо представляет собой -R10A, -R10B, -R10C или -R10D;
-R10A независимо представляет собой фенил или нафтил и необязательно содержит один или более заместителей -RX3;
-R10B представляет собой С5-10гетероарил и необязательно содержит один или более заместителей -RX3;
-R10C представляет собой насыщенный С3-7циклоалкил и необязательно содержит один или более заместителей -RX2;
-R10D представляет собой неароматический С3-10гетероциклил и необязательно содержит один или более заместителей -RX2;
или -R9 и -R10, совместно с атомом азота и атомом углерода, к которым они, соответственно, присоединены, образуют неароматическое С5-7гетероциклическое лактамное кольцо, которое необязательно содержит один или более заместителей -RX2, или которое является необязательно конденсированным с бензольным кольцом, которое необязательно содержит один или более заместителей -RX3;
-R11 независимо представляет собой -Н, -R11A или -R11B;
-R11A независимо представляет собой -RZ1, -RZ2, -RZ3, -RZ4, -RZ5, -LZ-RZ2, -LZ-RZ3, -LZ-RZ4 или -LZ-RZ5;
-RZ1 представляет собой насыщенный алифатический С1-6алкил и необязательно содержит один или более заместителей -RX1;
каждый -RZ2 представляет собой насыщенный С3-7циклоалкил и необязательно содержит один или более заместителей -RX2;
каждый -RZ3 независимо представляет собой -RZ3A или -RZ3B;
каждый -RZ3A представляет собой неароматический С3-7гетероциклил и необязательно содержит один или более заместителей -RX2;
каждый -RZ3B представляет собой насыщенный С5-10гетероциклил с мостиком и необязательно содержит один или более заместителей -RX2;
каждый -RZ4 независимо представляет собой фенил или нафтил и необязательно содержит один или более заместителей -RX3;
каждый -RZ5 представляет собой С5-10гетероарил и необязательно содержит один или более заместителей -RX3;
каждый -LZ- представляет собой насыщенный алифатический С1-4алкилен;
-R11B представляет собой -CRJ1RJ2-C(=O)-NRJ3RJ4;
-RJ1 независимо представляет собой -Н или насыщенный алифатический С1-4алкил;
-RJ2 независимо представляет собой -Н или насыщенный алифатический С1-4алкил;
-RJ3 независимо представляет собой -Н или насыщенный алифатический С1-4алкил;
-RJ4 независимо представляет собой -Н или насыщенный алифатический С1-4алкил;
или -NRJ3RJ4 представляет собой С3-10гетероциклильную группу и необязательно содержит один или более заместителей -RX2;
-R12 независимо представляет собой -Н или -R12A;
-R12A представляет собой насыщенный алифатический С1-4алкил;
где каждый -RX1 независимо выбран из:
-OH и -ORS;
где каждый -RS независимо представляет собой насыщенный алифатический С1-6алкил;
и где каждый -RX2 независимо выбран из:
-RT, -NH2, -NHRT, -NRT 2, пирролидино, пиперидино, морфолино, пиперизино и N-(С1-4алкил)пиперизино;
где каждый -RT независимо представляет собой насыщенный алифатический С1-6алкил;
и где каждый -RX3 независимо выбран из:
-F, -Cl, -Br, -I,
-RV,
-CF3, -CHF2, -OCF3, -OCHF2,
-CN,
-OH, -ORV,
-NH2, -NHRV, -NRV 2,
пирролидино, пиперидино, морфолино,
пиперизино, N-(С1-4алкил)пиперизино,
-LV-NH2, -LV-NHRV, -LV-NRV 2,
-LV-пирролидино, -LV-пиперидино, -LV-морфолино,
-LV-пиперизино, -LV-{N-(С1-4алкил)пиперизино},
-LV-имидазол-2-ила, -LV-{N-(С1-4алкил)имидазол-2-ила},
-O-LV-NH2, -O-LV-NHRV, -O-LV-NRV 2,
-O-LV-пирролидино, -О-LV-пиперидино, -О-LV-морфолино,
-O-LV-пиперизино, -O-LV-{N-(С1-4алкил)пиперизино},
-O-LV-имидазол-2-ила, -O-LV-{N-(С1-4алкил)имидазол-2-ила},
-NHC(=O)RV, -NRVC(=O)RV,
-С(=O)ОН, -C(=O)ORV,
-C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2,
-С(=O)-пирролидино, -С(=O)-пиперидино, -С(=O)-морфолино,
-С(=O)-пиперизино, -С(=O)-{N-(С1-4алкил)пиперизино}-,
-NHC(=O)NH2, -NHC(=O)NHRV, -NHC(=O)NRV 2,
-NHC(=O)-пирролидино, -NHC(=O)-пиперидино, -NHC(=O)-морфолино,
-NHC(=O)-пиперизино, -NHC(=O)-{N-(С1-4алкил)пиперизино}-,
-S(=O)2RV,
-S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2, и
=O;
где каждый -LV- представляет собой насыщенный алифатический С1-4алкилен;
где каждый -RV независимо представляет собой насыщенный алифатический С1-6алкил или фенил;
и, дополнительно, две соседние группы -RX3 могут совместно образовывать -OCH2O-, -OCH2CH2O-, -СН2ОСН2- или -ОСН2СН2-;
где:
«гетероарил» относится к группе, которая присоединена к остальной части молекулы через атом, являющийся частью ароматического кольца, и которая содержит один или два гетероатома, выбранных из N, О или S, образующих часть ароматической системы колец; и
«гетероциклил» относится к группе, которая присоединена к остальной части молекулы через атом кольца, не являющийся частью ароматического кольца, и указанная кольцевая система содержит один или два гетероатома, выбранных из N, О и S.
2. Соединение по п. 1, где -R1 независимо представляет собой -R1A, a -R1A представляет собой -iPr.
3. Соединение по п. 1, где -R3 представляет собой -H и R6 представляет собой H.
4. Соединение по п. 2, где R3 представляет собой -H и -R6 представляет собой -H.
5. Соединение по п. 1, где -R7 независимо представляет собой -R7A или -R7B; -R7A представляет собой -tBu, R7B представляет собой -L7B1-R7BB, -L7B1- представляет собой -СН2-; -R7BB представляет собой -R7BB1; и -R7BB1 представляет собой фенил.
6. Соединение по п. 4, где -R7 независимо представляет собой -R7A или R7B; -R7A представляет собой -tBu, R7B представляет собой -L7B1-R7BB, -L7B1- представляет собой -СН2-; -R7BB представляет собой -R7BB1 и -R7BB1 представляет собой фенил.
7. Соединение по п. 1, где -R9 представляет собой -H; -R10 представляет собой -R10A; a -R10A представляет собой фенил и необязательно содержит один или более заместителей -RX3.
8. Соединение по п. 6, где -R9 представляет собой -H; -R10 представляет собой -R10A; a -R10A представляет собой фенил и необязательно содержит один или более заместителей -RX3.
9. Соединение по п. 1, где -R9 представляет собой -Н; -R10 представляет собой -R10B; a -R10B представляет собой пиридил и необязательно содержит один или более заместителей -RX3.
10. Соединение по п. 6, где -R9 представляет собой -Н; -R10 представляет собой -R10B; a -R108 представляет собой пиридил и необязательно содержит один или более заместителей -RX3.
11. Соединение по п. 1, где -R9 представляет собой -Н; -R10 представляет собой -R10B; a -R10B представляет собой индазолил, бензимидазолил, бензотиазолил,
хинолинил или изохинолинил и необязательно содержит один или более заместителей -RX3.
12. Соединение по п. 6, где -R9 представляет собой -Н; -R10 представляет собой -R10B; a -R10B представляет собой индазолил, бензимидазолил, бензотиазолил, хинолинил или изохинолинил и необязательно содержит один или более заместителей -RX3.
13. Соединение по п. 1, где -R9 представляет собой -H; -R10 представляет собой -R10D; a -R10D независимо представляет собой:

14. Соединение по п. 6, где -R9 представляет собой -Н; -R10 представляет собой -R10D; a -R10D независимо представляет собой:
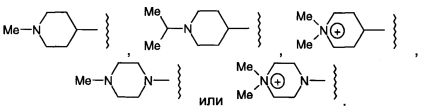
15. Соединение по п. 1, где группа -N(R9)-C(=O)-R10 представляет собой следующую группу:
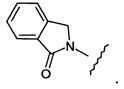
16. Соединение по п. 6, где группа -N(R9)-C(=O)-R10 представляет собой следующую группу:

17. Соединение по п. 1, где:
-R11 представляет собой -R11A;
-R11A представляет собой -LZ-RZ4;
-LZ- представляет собой -СН2- или -СН(Ме)-; и
-RZ4 независимо выбран из:
 ,
, 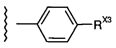 и
и  ; и
; и
-R12 представляет собой -Н.
18. Соединение по п. 8, где:
-R11 представляет собой -R11A;
-R11A представляет собой -LZ-RZ4;
-LZ- представляет собой -СН2- или -СН(Me)-; и
-RZ4 независимо выбран из:
 ,
,  и
и  ; и
; и
-R12 представляет собой -Н.
19. Соединение по п. 10, где:
-R11 представляет собой -R11A;
-R11A представляет собой -LZ-RZ4;
-LZ- представляет собой -СН2- или -СН(Ме)-; и
-RZ4 независимо выбран из:
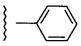 ,
,  и
и  ; и
; и
-R12 представляет собой -Н.
20. Соединение по п. 12, где:
-R11 представляет собой -R11A;
-R11A представляет собой -LZ-RZ4;
-LZ- представляет собой -СН2- или -СН(Ме)-; и
-RZ4 независимо выбран из:
 ,
,  и
и  ; и
; и
-R12 представляет собой -Н.
21. Соединение по п. 14, где:
-R11 представляет собой -R11A;
-R11A представляет собой -LZ-RZ4;
-LZ- представляет собой -СН2- или -СН(Ме)-; и
-RZ4 независимо выбран из:
 ,
,  и
и  ; и
; и
-R12 представляет собой -Н.
22. Соединение по п. 16, где:
-R11 представляет собой -R11A;
-R11A представляет собой -LZ-RZ4;
-LZ- представляет собой -СН2- или -СН(Ме)-; и
-RZ4 независимо выбран из:
 ,
,  и
и  ; и
; и
-R12 представляет собой -Н.
23. Соединение по п. 1, где:
-R11 представляет собой -R11B;
-RJ1 независимо представляет собой -Н, -Me, -Et, -nPr или -iPr;
-RJ2 представляет собой -Н;
-NRJ3RJ4 независимо выбран из:

-R12 представляет собой -Н.
24. Соединение по п. 8, где:
-R11 представляет собой -R11B;
-RJ1 независимо представляет собой -Н, -Me, -Et, -nPr или -iPr;
-RJ2 представляет собой -Н;
-NRJ3RJ4 независимо выбран из:

-R12 представляет собой -Н.
25. Соединение по п. 10, где:
-R11 представляет собой -R11B;
-RJ1 независимо представляет собой -Н, -Me, -Et, -nPr или -iPr;
-RJ2 представляет собой -Н;
-NRJ3RJ4 независимо выбран из:
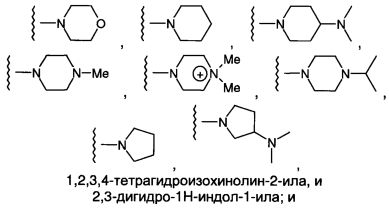
-R12 представляет собой -Н.
26. Соединение по п. 12, где:
-R11 представляет собой -R11B;
-RJ1 независимо представляет собой -Н, -Me, -Et, -nPr или -iPr;
-RJ2 представляет собой -Н;
-NRJ3RJ4 независимо выбран из:

-R12 представляет собой -Н.
27. Соединение по п. 14, где:
-R11 представляет собой -R11B;
-RJ1 независимо представляет собой -Н, -Me, -Et, -nPr или -iPr;
-RJ2 представляет собой -Н;
-NRJ3RJ4 независимо выбран из:

-R12 представляет собой -H.
28. Соединение по п. 16, где:
-R11 представляет собой -R11B;
-RJ1 независимо представляет собой -Н, -Me, -Et, -nPr или -iPr;
-RJ2 представляет собой -Н;
-NRJ3RJ4 независимо выбран из:

-R12 представляет собой -Н.
29. Соединение по п. 1, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(C1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
30. Соединение по п. 18, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2 и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(С1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
31. Соединение по п. 19, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(С1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
32. Соединение по п. 20, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(С1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
33. Соединение по п. 21, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(С1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
34. Соединение по п. 22, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(С1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
35. Соединение по п. 24, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(C1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
36. Соединение по п. 25, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(С1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
37. Соединение по п. 26, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(С1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
38. Соединение по п. 27, где:
каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, независимо выбран из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(С1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
39. Соединение по п. 28, где: каждый -RX1, если присутствует, представляет собой -ORS;
каждый -RX2, если присутствует, независимо выбран из: -RT, -NH2, -NHRT и -NRT 2; и
каждый -RX3, если присутствует, если присутствует из: -F, -Cl, -RV, -CN, -ОН, -ORV, морфолино, пиперизино, N-(С1-4алкил)-пиперизино, -LV-NH2, -LV-NHRV, -LV-NRV 2, -LV-пирролидино, -LV-пиперидино, -LV-морфолино, -LV-пиперизино, -LV-{N-(С1-4алкил)-пиперизино}, -С(=O)ОН, -C(=O)ORV, -C(=O)NH2, -C(=O)NHRV, -C(=O)NRV 2, -NHC(=O)NH2, -S(=O)2NH2, -S(=O)2NHRV, -S(=O)2NRV 2 и =O.
40. Соединение по п. 1, выбранное из следующих соединений и их фармацевтически приемлемых солей:



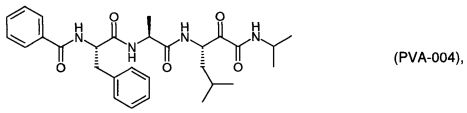



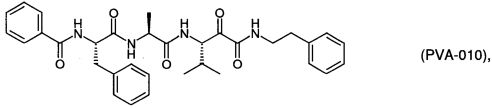



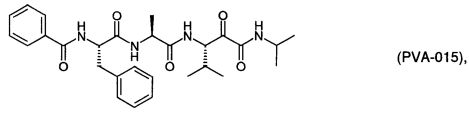
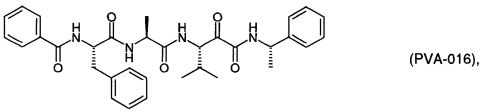








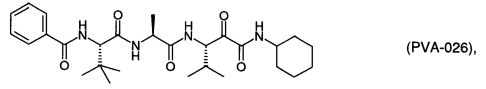



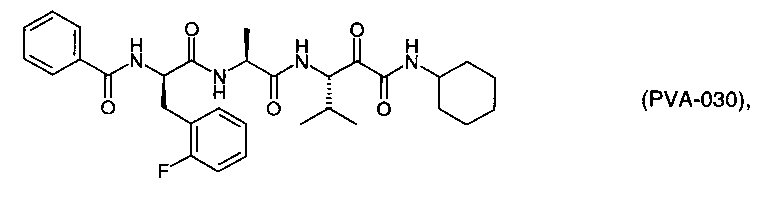


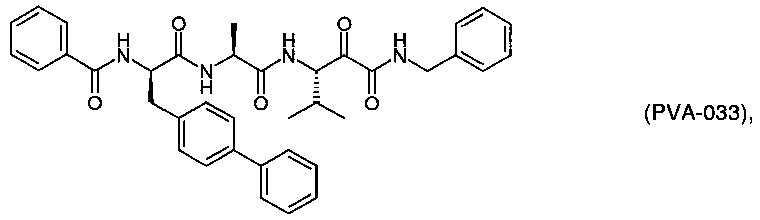

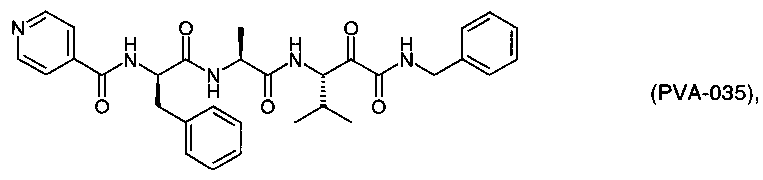

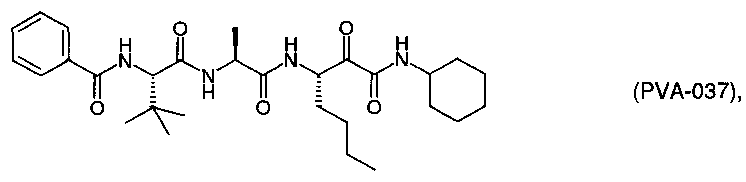

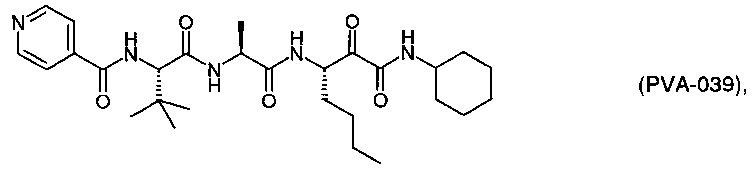
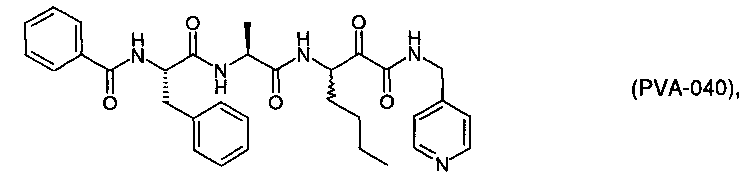
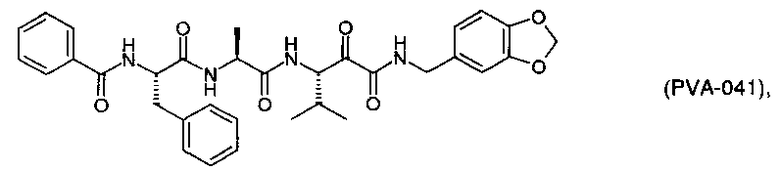
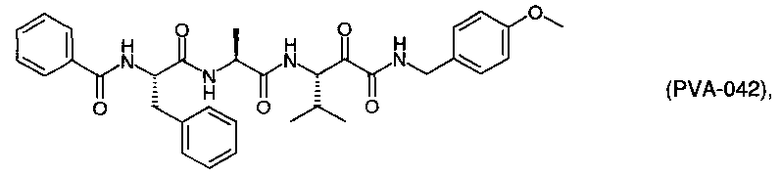
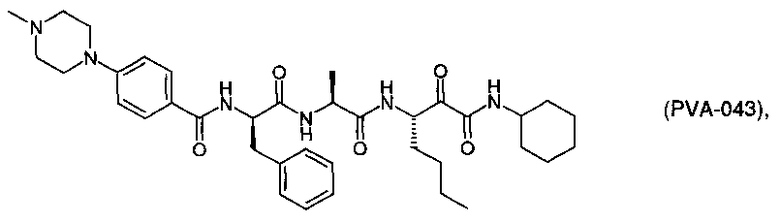
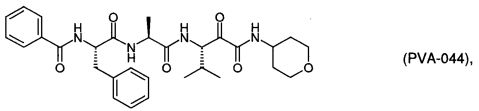
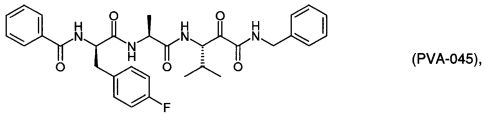






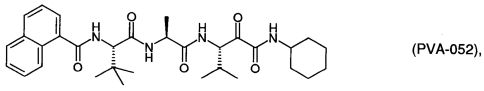



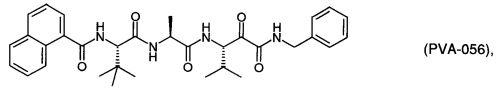












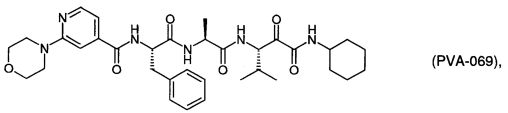










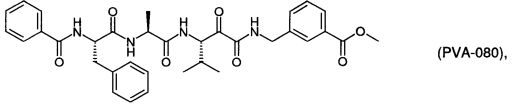









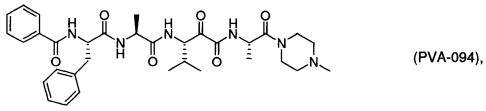


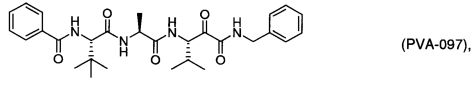


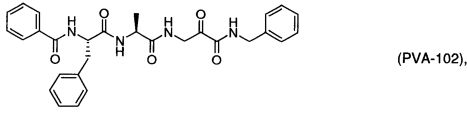





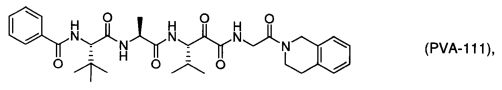









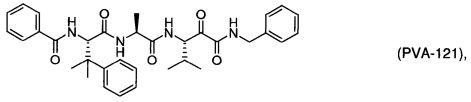

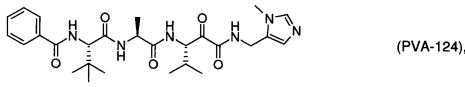

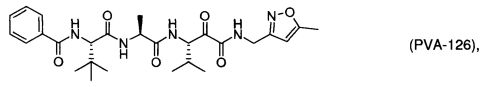
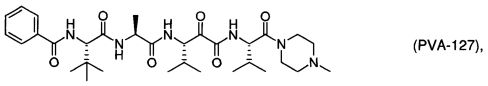
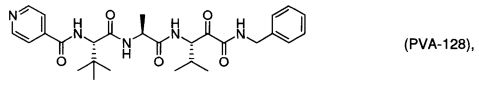
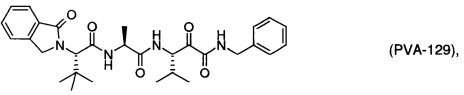

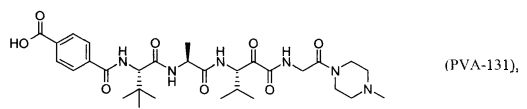
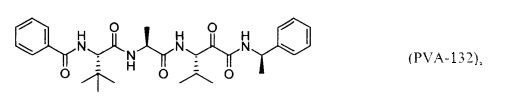



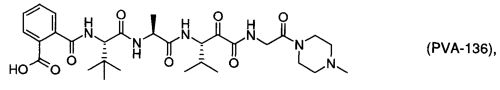

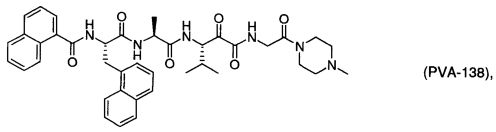

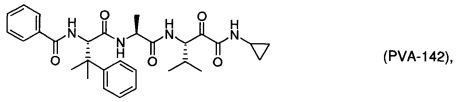


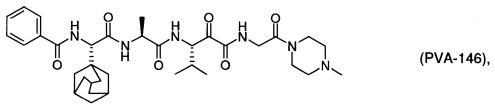



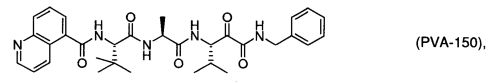

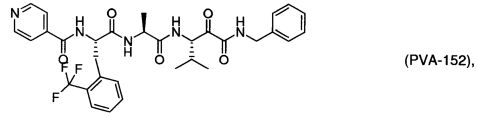





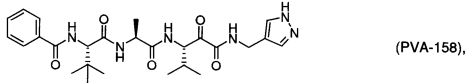


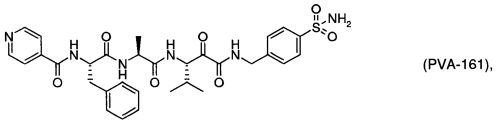

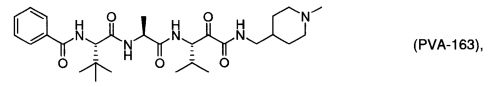
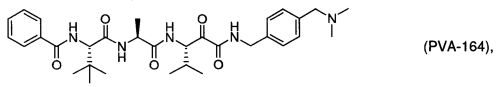
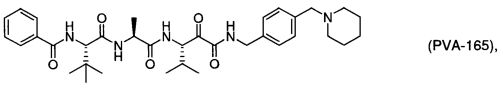

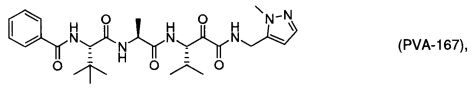



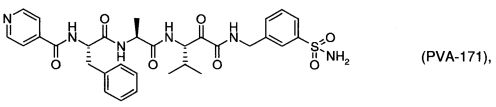
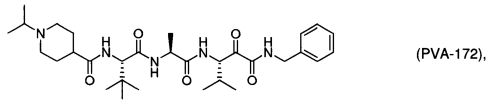
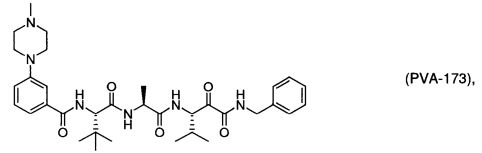







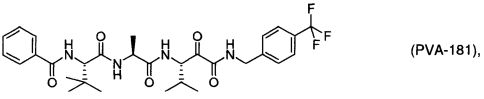

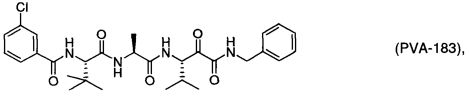



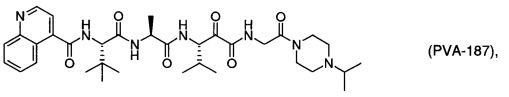
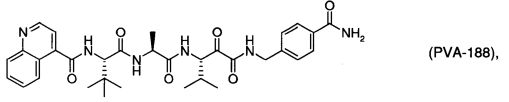


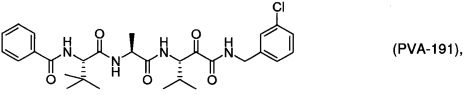
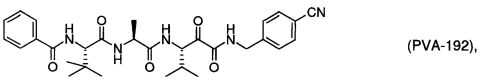




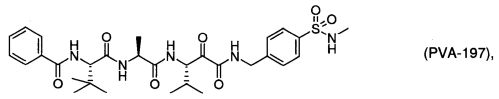

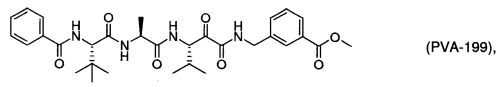


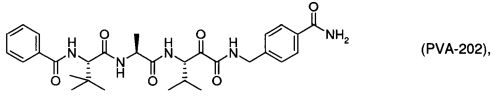


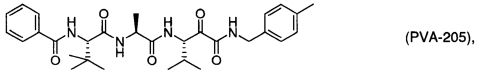
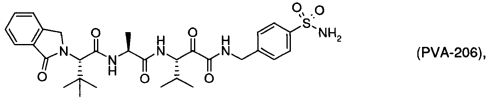
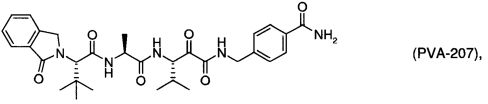
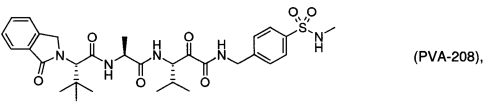





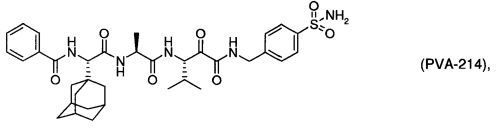
 и
и

41. Композиция для ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу, содержащая эффективное количество соединения по любому из пп. 1-40 и фармацевтически приемлемый носитель, разбавитель или наполнитель.
42. Способ получения композиции, включающий смешение соединения по любому из пп. 1-40 с фармацевтически приемлемым носителем, разбавителем или наполнителем.
43. Соединение по любому из пп. 1-40 для применения в способе лечения заболевания или нарушения, которое опосредовано аллергеном пылевых клещей 1 группы, представляющим собой пептидазу.
44. Соединение по любому из пп. 1-40 для применения в способе лечения:
астмы, например атопической астмы; аллергической астмы; атопической бронхиальной IgE-опосредованной астмы; бронхиальной астмы; экзогенной астмы; индуцированной аллергеном астмы; аллергической астмы, обостренной респираторной вирусной инфекцией; инфекционной астмы; инфекционной астмы, вызванной бактериальной инфекцией; инфекционной астмы, вызванной грибковой инфекцией; инфекционной астмы, вызванной протозойной инфекцией; или инфекционной астмы, вызванной вирусной инфекцией;
бронхиальной гиперреактивности, связанной с астмой; или бронхиальной гиперчувствительности, связанной с астмой;
ремоделирования дыхательных путей, связанного с аллергическим заболеванием легких, например ремоделирования дыхательных путей, связанного с астмой;
астмы, сопровождающейся хроническим обструктивным заболеванием легких, например астмы, сопровождающейся эмфиземой; или астмы, сопровождающейся хроническим бронхитом;
ринита, например аллергического ринита; круглогодичного ринита; персистирующего ринита или IgE-опосредованного ринита;
аллегического конъюнктивита, например IgE-опосредованного конъюнктивита;
атопического дерматита;
аллергического состояния, вызванного пылевыми клещами;
аллергического состояния, вызванного аллергеном пылевых клещей 1 группы, представляющим собой пептидазу; или
атопии у собак.
45. Применение соединения по любому из пп. 1-40 для получения лекарственного средства для лечения:
астмы, например атопической астмы; аллергической астмы; атопической бронхиальной IgE-опосредованной астмы; бронхиальной астмы; экзогенной астмы; индуцированной аллергеном астмы; аллергической астмы, обостренной респираторной вирусной инфекцией; инфекционной астмы; инфекционной астмы, вызванной бактериальной инфекцией; инфекционной астмы, вызванной грибковой инфекцией; инфекционной астмы, вызванной протозойной инфекцией; или инфекционной астмы, вызванной вирусной инфекцией;
бронхиальной гиперреактивности, связанной с астмой; или бронхиальной гиперчувствительности, связанной с астмой;
ремоделирования дыхательных путей, связанного с аллергическим заболеванием легких, например ремоделирования дыхательных путей, связанного с астмой;
астмы, сопровождающейся хроническим обструктивным заболеванием легких, например астмы, сопровождающейся эмфиземой; или астмы, сопровождающейся хроническим бронхитом;
ринита, например аллергического ринита; круглогодичного ринита; персистентного ринита или IgE-опосредованного ринита;
аллергического конъюнктивита, например IgE-опосредованного конъюнктивита;
атопического дерматита;
аллергического состояния, вызванного пылевыми клещами;
аллергического состояния, вызванного аллергеном пылевых клещей 1 группы, представляющим собой пептидазу; или
атопии у собак.
46. Способ лечения, включающий введение субъекту, нуждающемуся в указанном введении, терапевтически эффективного количества соединения по любому из пп. 1-40, где лечение представляет собой лечение:
астмы, например атопической астмы; аллергической астмы; атопической бронхиальной IgE-опосредованной астмы; бронхиальной астмы; экзогенной астмы; индуцированной аллергеном астмы; аллергической астмы, обостренной респираторным вирусной инфекцией; инфекционной астмы; инфекционной астмы, вызванной бактериальной инфекцией; инфекционной астмы, вызванной грибковой инфекцией; инфекционной астмы, вызванной протозойной инфекцией; или инфекционной астмы, вызванной вирусной инфекцией;
бронхиальной гиперреактивности, связанной с астмой; или бронхиальной гиперчувствительности, связанной с астмой;
ремоделирования дыхательных путей, связанного с аллергическим заболеванием легких, например ремоделирования дыхательных путей, связанного с астмой;
астмы, сопровождающейся хроническим обструктивным заболеванием легких, например астмы, сопровождающейся эмфиземой; или астмы, сопровождающейся хроническим бронхитом;
ринита, например аллергического ринита; круглогодичного ринита; персистирующего ринита или IgE-опосредованного ринита;
аллергического конъюнктивита, например IgE-опосредованного конъюнктивита;
атопического дерматита;
аллергического состояния, вызванного пылевыми клещами;
аллергического состояния, вызванного аллергеном пылевых клещей 1 группы, представляющим собой пептидазу; или
атопии у собак.
47. Способ ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу, in vitro или in vivo, включающий приведение указанного аллергена пылевых клещей 1 группы, представляющего собой пептидазу, в контакт с эффективным количеством соединения по любому из пп. 1-40.
48. Способ ингибирования аллергена пылевых клещей 1 группы, представляющего собой пептидазу, в клетке in vitro или in vivo, включающий приведение клетки в контакт с эффективным количеством соединения по любому из пп. 1-40.
49. Акарицидная композиция, содержащая эффективное количество соединения по любому из пп. 1-40.
50. Способ уничтожения клещей, включающий воздействие на указанных клещей эффективным количеством соединения по любому из пп. 1-40.
51. Способ регулирования популяции клещей, включающий воздействие на указанных клещей эффективным количеством соединения по любому из пп. 1-40.
| US 6235929 B1, 22.05.2001 | |||
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
| RU 2003105221 A, 20.09.2004 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Стрелочный контрольный замок | 1924 |
|
SU421A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
2016-06-10—Публикация
2011-01-21—Подача