Изобретение относится к органической химии, конкретно к способу получения имидов малеопимаровой кислоты на основе метилового эфира малеопимаровой кислоты (МЭМПК).
Малеопимаровая кислота и ее производные проявляют высокую биологическую активность (противовоспалительную, нематоцидную, фунгицидную) [О.Б. Казакова, Е.В. Третьякова, О.С. Куковинец, Г.А. Толстиков, Т.И. Назыров, И.В. Чудов, А.Ф. Исмагилова// Биоорганическая химия, 36, 832-840 (2010); Gui-yang Yao, Man-yi Ye, Ri-zhen Huang, Ya-jun Li, Yong-tao Zhu, Ying-ming Pan, Zhi-Xin Liao, Heng-shan Wang. // Bioorg. Med. Chem. Lett. 23 (2013) 6755-6758].
Известные способы получения имидов МЭМПК делятся на две группы. Первый способ получения соответствующих имидов заключается в прямом сплавлении аминов и МЭМПК. Как показано в работе [М.П. Бей, А.П. Ювченко // Журнал общей химии. - 2010. - Т. 80, вып. 2. - С. 228-232.], эквимольное количество алкиламинов и МЭМПК медленно нагревали на песчаной бане (чтобы избежать сильного вспенивания). После образования жидкой фазы при перемешивании выдерживали 12 ч при 160°С. По окончании реакции продукт выдерживали в вакууме (1 мм рт.ст.) при температуре 80°С в течение 1 ч. Выход целевых продуктов составляет 96-98%%.
Другой метод получения соответствующих имидов заключается в конденсации аминов и МЭМПК в различных высококипящих растворителях [Jinxing Yu, Na Xu, Zhengping Liu, and Liyuan // WangACS Appl. Mater. Interfaces 2012, 4, 2591-2596; Lisheng Zhang, Yanhua Jiang, Zhu Xiong, Xiaoqing Liu, Haining Na, Ruoyu Zhang and Jin ZhuJ. // Mater. Chem. A, 2013, 1, 3263-3267]. Так, в соответствии с [Huani С, Manyi Y., Guiyang Y. // Chemical journal of Chinese universities- Chinese - 2014. - T. 35. - №. 4. - C. 839-846] раствор двухкратного мольного избытка малеопимаровой кислоты и тетрогидронафталинамина кипятили в уксусной кислоте в течение 10 ч. Смесь упарили, полученный остаток хроматографировали на двуокиси кремния (3:1, гексан-этилацетат в качестве элюента). Выход имида МЭМПК составил 40%.
Основными недостатками рассмотренных способов являются длительность процесса и ограничения по природе аминосоединения. Образование целевых продуктов происходит лишь в случае, когда аддукты и образующиеся продукты плавятся в данных интервалах температуры, при этом не подвержены возгонке и термическому разложению и в случае конденсации исходные амины обладают способностью растворяться.
Наиболее близким к предлагаемому изобретению является способ получения имидов МЭМПК [CN 102329309 А, 2012.01.25], согласно которому смесь γ-аминомасляной кислоты и двухкратного мольного избытка МЭМПК выдерживали в ДМФА при комнатной температуре 8 ч, затем температуру доводили до 150°С и выдерживали еще 4 ч. В остывшую реакционную массу добавляли 150 мл воды. Выпавший желтый осадок отфильтровали, промывали водой и сушили в вакууме 5 ч, затем многократно перекристаллизовывали в системе ДМФА : вода, поместили в вакуумную печь при 90°С и сушили 10 ч. Полученный имид МЭМПК представлял собой белый порошок с выходом 53%.
Задача, на решение которой направлено заявленное техническое решение, заключается в разработке способа получения имидов МЭМПК, существенно сокращающего длительность процесса и приводящего к увеличению выхода потенциально биологически активных целевых продуктов.
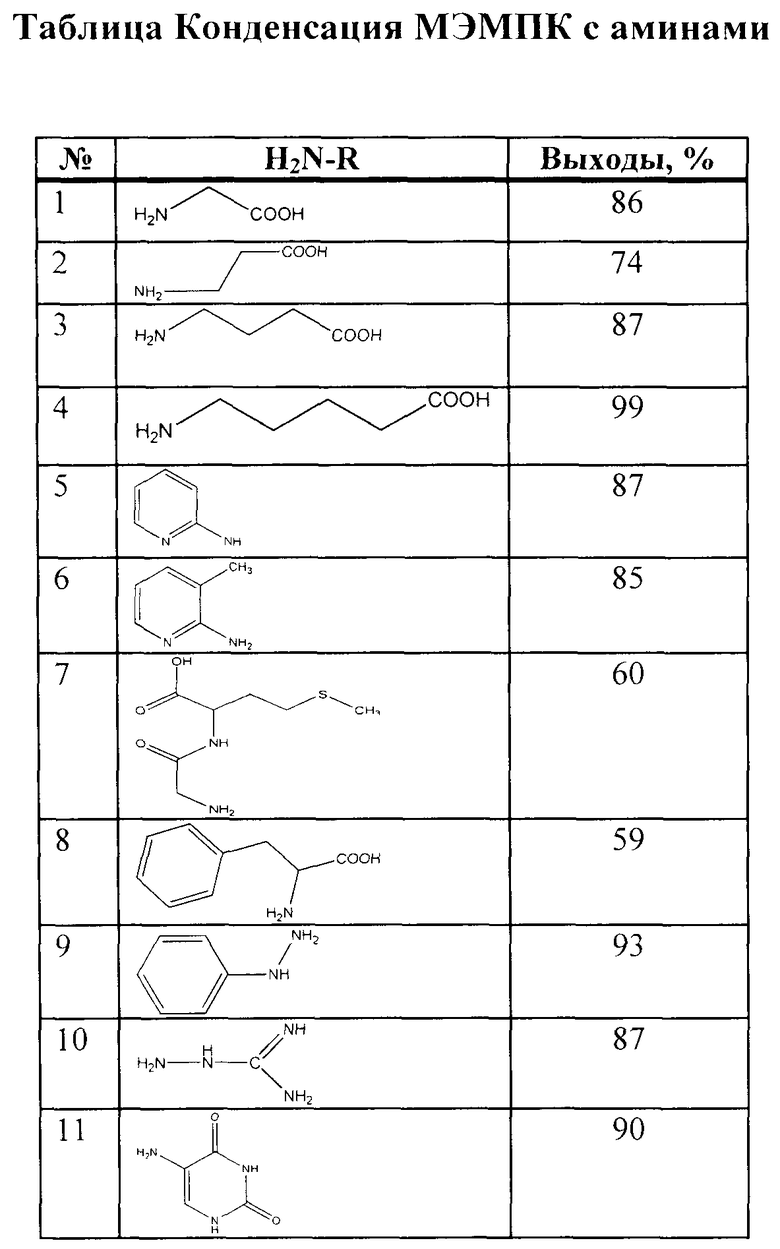
Поставленная задача решается предлагаемым способом получения имидов МЭМПК путем конденсации метилового эфира малеопимаровой кислоты с аминами в диметилсульфоксиде (ДМСО) при мольном соотношении МЭМПК : амин, равном 1:2, при температуре 120-160°С в условиях ультразвукового воздействия в течение 30-40 минут. Затем реакционную массу охлаждают до комнатной температуры, добавляют воду и очищают выпавший осадок целевого продукта колоночной хроматографией. В качестве различных по структуре аминов используют 5-аминоурацил, аминогуанидин, 2-аминопиридин, ε-аминокапроновую кислоту, глицин, β-аланин, 2-амино-3-метилпиридин, глицил-метионин, β-фенил-α-аланин, γ-аминомасляную кислоту и фенилгидразин. Время ультразвукового воздействия контролируют по исчезновению МЭМПК в реакционной массе методом тонкослойной хроматографии. Выход целевых продуктов составляет 59-99% (см. табл.).

Непрореагировавшие аминосоединения регенерируются в зависимости от природы реагента. После высаживания водой целевого продукта водорастворимые амины выделяются путем выпаривания воды с последующим растиранием смесью растворителей петролейный эфир : этилацетат в соотношении 9:1. Труднорастворимые в органических растворителях амины выделяются путем фильтрации из хлористого метилена, в котором растворяются все полученные по предлагаемому способу упомянутые выше имиды МЭМПК.
Таким образом, предложен способ получения имидов МЭМПК с использованием ультразвукового воздействия, позволивший повысить выход целевых продуктов, существенно сократить время протекания процесса и получать малеопимаримиды даже в случае малорастворимых аминов за счет диспергирования аддуктов под влиянием ультразвукового воздействия.
Сущность изобретения подтверждается следующими примерами.
Пример 1. Метил (9aR)-2-(2′,4′-диоксо-1′,2′,3′,4′-тетрагидропиримидин-5′-ил)-6,9a-диметил-1,3-диоксо-12-(пропан-14-ил)гексадекагидро-3b,11-этенонафто[2,1-e]изоиндол-6-карбоксилат. Смесь 0,5 г (1.2 ммоль) метилового эфира малеопимаровой кислоты и 0,31 г (2.4 ммоль) 5-аминоурацила в 6 мл ДМСО подвергается ультразвуковому воздействию в течение 30 минут, при этом реакционную массу нагревают до температуры 120°С. После того как МЭМПК израсходовался, реакционную массу охлаждают до комнатной температуры, добавляют 2-3 мл дистиллированной воды и выпавший осадок отфильтровывают. Твердый осадок промывают дистиллированной водой, растворяют в хлористом метилене и сушат над сульфатом магния. Продукт хроматографируют, элюент хлороформ : ацетон = 9:1. Выход 90%.
ЯМР Н1; 0.56 д. (3Н, С17Н3), 0.89 и 1.41 гем. м. (2Н, С9Н2), 0.92 м. (6Н, 3 С15,16Н3), 1.13 с. (3Н, С18Н3), 1.19 и 1.42 гем. м. (2Н, С8Н2), 1,18 и 1.45 м. (2Н, С5Н2), 1.22 и 1.66 гем. м. (2Н, С10Н2), 1.32 м. (Н, C9bH), 1.51-1.68 м. (2Н, С7Н2), 1.68 и 2.43 гем. м. (2Н, С4Н2), 1-72 м. (Н, С5аН), 2.12 м. (Н, С14Н), 2.51 м. (Н, С3аН), 2.85 м. (Н, С11аН), 3.16 м. (Н, С11Н), 3.68 с. (3Н, С20Н3), 5.45 с. (Н, С13Н), 7.11 с. (Н, С4′Н), 10.23 (Н, NH), 10.36 д. (H, NH). ЯМР С13; 15.62 (С17Н3), 16.63 (C18H3), 16.91 (C8H2), 19.36 (2C15,16H3), 21.64 (С5Н2), 27.36 (С10Н2), 32.59 (С14Н), 34.94 (С4Н2), 35.74 (С11Н), 36,54 (С7Н2), 37, 58 (С9а), 37,94 (С9Н2), 40.75 (C3b), 45.13 (С11аН), 47.01 (С6), 49.27 (С5аН), 51.89 (С20Н3), 52.50 (С3аН), 53.77 (C9bH), 107.2 (С5′), 124.46 (С13Н), 141.34 (С4′Н), 147.21 (С12Н), 151.56 (С2′), 159.70 (С6′=O), 176, 15 (С1=O), 177.41 (С3=O), 179.11 (МеООС19).
Пример 2. Метил (3aR,6R,9aR,11aR)-6,9а-диметил-2-(3′-метилпиридин-2′-ил)-1,3-диоксо-12-(пропан-14-ил)гексадекагидро-3b,11-этенонафто[2,1-e]изоиндол-6-карбоксилат. Смесь 0,5 г (1.2 ммоль) метилового эфира малеопимаровой кислоты и 0,23 г (2.4 ммоль) 2-аминопиридина в 6 мл ДМСО подвергается ультразвуковому воздействию при нагревании до 160°С в течение 30 минут. Реакционную массу охлаждают до комнатной температуры, добавляют 2-3 мл дистиллированной воды и выпавший осадок отфильтровывают. Твердый осадок промывают дистиллированной водой, растворяют в хлористом метилене и сушат над сульфатом магния. Продукт хроматографируют, элюент петролейный эфир : этилацетат = 7:3. Выход 87%.
ЯМР Н1; 0.62 с. (3Н, С17Н3), 0.98 и 1.42 гем. м. (2Н, С9Н2), 1.02 м. (6Н, 3 С15-16Н3), 1.09 и 1.46 гем. м. (2Н, С8Н2), 1.16 с. (3Н, С18Н3), 1.21 и 1.48 гем. м. (2Н, С5Н2), 1.28 и 1.73 гем. м. (2Н, С10Н2), 1.41 м. (Н, C9bH), 1.54 и 1.69 гем. м. (2Н, С7Н2), 1.7 и 2.61 гем. м. (2Н, С4Н2), 1.78 м. (Н, С5аН), 2.29 м. (Н, С14Н), 2.68 м. (Н, С3аН), 2.99 м. (Н, С11аН), 3.16 м. (Н, С11Н), 3.68 с. (3Н, С20Н3), 5.56 м. (Н, =С13Н), 7.09 м. (Н, С5′Н), 7.28 д. (Н, С3′Н), 7.78 м. (Н, С4′Н), 8.61 м. (Н, С2′Н). ЯМР С13; 14.62 (С17Н3), 15.74 (С18Н3), 16.01 (С8Н2), 19.12 и 20.81 (2С15-16Н3), 20.74 (С5Н2), 26.56 (С10Н2), 31.84 (С14Н), 34.18 (С4Н2), 34.95 (С11Н), 35,66 (С7Н2), 36.69 (С9а), 37,08 (С9Н2), 39.96 (C3b), 44.31 (С11аН), 46.09 (С6), 48.45(С5аН), 50.96 (С20Н3), 51.68 (С3аН), 52.93 (C9bH), 121.04 (С5Н), 122.74 (С3Н), 123.61 (=С13Н), 137.17 (С4′Н), 145.30 (С12), 146.33 (С6′), 148.72 (С2′), 174.92 (С1=O), 176,14 (С3=O), 178.14 (МеООС19).
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННЫЕ ПОКРЫТИЯ НА ОСНОВЕ БИОЛОГИЧЕСКИ АКТИВНЫХ RGD-ФУНКЦИОНАЛИЗИРОВАННЫХ БИФОСФОНАТОВ АМИНОКИСЛОТ И ПЭО-ПОДСЛОЯ ДЛЯ ТИТАНА | 2019 |
|
RU2735649C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСОВ 1-ХЛОР-2-АЛКИЛ(ФЕНИЛ)БОРИРЕНОВ с SMe | 2016 |
|
RU2654806C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ НЕПРИРОДНЫХ АМИНОКИСЛОТ | 2020 |
|
RU2758455C1 |
| Способ получения бис-аддукта имидо-амина метилового эфира малеопимаровой кислоты с диметил-гексаазапергидропиреновым спейсером и его применение в качестве средства с цитотоксической активностью | 2023 |
|
RU2794743C1 |
| Бис-аддукты имидо-амина метилового эфира малеопимаровой кислоты с азаполициклическими спейсерами и способ их получения | 2022 |
|
RU2792569C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСОВ 1-ХЛОР-2-АЛКИЛ(ФЕНИЛ)БОРИРАНОВ с SMe | 2016 |
|
RU2640209C2 |
| Способ получения терпеноидного димера с пергидротетраценовым спейсером и его применение в качестве средства с цитотоксической активностью | 2023 |
|
RU2794745C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,9-БИС-ЗАМЕЩЕННЫХ ТРАНС-2,3a,7b,9,10a,14b-ГЕКСААЗАПЕРГИДРОДИБЕНЗОТЕТРАЦЕНОВ НА ОСНОВЕ АМИНОПРОИЗВОДНЫХ МЕТИЛОВОГО ЭФИРА МАЛЕОПИМАРОВОЙ КИСЛОТЫ | 2019 |
|
RU2730493C1 |
| СПОСОБ ПОЛУЧЕНИЯ ТРЕТИЧНЫХ СПИРТОВ РЕАКЦИЕЙ АРИЛОЛЕФИНОВ С AlCl3 И КЕТОНАМИ ПОД ДЕЙСТВИЕМ КАТАЛИЗАТОРА Cp2ZrCl2 | 2023 |
|
RU2813640C1 |
| Способ получения калиевых солей производных смоляных кислот | 2022 |
|
RU2811798C1 |
Изобретение относится к области органической химии, конкретно к способу получения имидов малеопимаровой кислоты. Способ заключается в конденсации метилового эфира малеопимаровой кислоты с аминами в органическом растворителе при повышенной температуре с последующим охлаждением реакционной массы до комнатной температуры и добавлением воды для выделения целевого продукта. Способ характеризуется тем, что мольное соотношение метиловый эфир малеопимаровой кислоты:амин равно 1:2, в качестве органического растворителя используют диметилсульфоксид, а процесс протекает при температуре 120-160°C в условиях ультразвукового воздействия в течение 30-40 мин. Способ позволяет повысить выход целевых продуктов и сократить продолжительность синтеза. 2 з.п. ф-лы, 1 табл., 2 пр.
1. Способ получения имидов малеопимаровой кислоты путем конденсации метилового эфира малеопимаровой кислоты с аминами в органическом растворителе при повышенной температуре с последующим охлаждением реакционной массы до комнатной температуры и добавлением воды для выделения целевого продукта, отличающийся тем, что мольное соотношение метиловый эфир малеопимаровой кислоты:амин равно 1:2, в качестве органического растворителя используют диметилсульфоксид, процесс протекает при температуре 120-160°C в условиях ультразвукового воздействия в течение 30-40 мин.
2. Способ по п.1, отличающийся тем, что в качестве аминов используют 5-аминоурацил, аминогуанидин, 2-аминопиридин, ε-аминокапроновую кислоту, глицин, β-аланин, 2-амино-3-метилпиридин, глицил-метионин, β-фенил-α-аланин, γ-аминомасляную кислоту и фенилгидразин.
3. Способ по п.1, отличающийся тем, что время ультразвукового воздействия контролируют по исчезновению метилового эфира малеопимаровой кислоты в реакционной массе методом тонкослойной хроматографии.
| CN 102329309 A, 25.01.2012 | |||
| М.П | |||
| БЕЙ И ДР., Синтез и свойства N-н-алкилимидов малеопимаровой кислоты, ЖУРН | |||
| ОБЩ | |||
| ХИМИИ, 2010, Т | |||
| Капельная масленка с постоянным уровнем масла | 0 |
|
SU80A1 |
| СОЛИ ИЛИ ЭФИРЫ N-ЗАМЕЩЕННЫХ ИМИДОВ МАЛЕОПИМАРОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩИЕ ФУНГИЦИДНУЮ АКТИВНОСТЬ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1975 |
|
SU584722A1 |
| Поизводные -замещенных имидов малеопимаровой кислоты, проявляющие фунгицидную активность и способ их получения | 1974 |
|
SU543252A1 |
Авторы
Даты
2016-07-10—Публикация
2015-05-21—Подача