По предлагаемому способу используют следующие вторичные амины: алифатические, карбоциклические, гетероциклические и ациклические насыщенные оксиам и- ы. Применение вторичных аминов исключает образование смесей продукта и упрощает их очистку.
Избыток амина существенно повышает выход реакции, поэтому рекомендуется брать молярное соотношение Ы-(оксиметил)имида малеопи1У1аровой кислоты н аминов в пределах 1 : 1,5- 1 : 10,0. Реакцию можно вести как с растворителем, так и без него, без существенного влияния на выход и качество продукта. Однако работа без растворителя упрощает очистку продукта, снижает степень пожароопасиости и удешевляет процесс.
Биологическую активность предлагаемых соедипений сравнивают с препаратом фундазол, действующее начало которого представляет собой метиловый эфир 1-бутилкарбамил-2-бензимидазолкарбаминовой кислоты. Препарат изготовляется на заводе фармацевтических и химических продуктов ХИНОИН, Будапещт.
N-замещенные имиды малеоиимаровой кислоты, взятые в концентрации 0,5-0,7%, оказывают более продолжительное действие на мучнистую росу, чем фундазол, взятый в концентрации 0,15%. Эффективность фундазола увеличить нельзя, поскольку 0,15%-пая концентрация растворов фундазола предельна, так как повышение коицентрации растворов фундазола вызывает нарушения в физиологии растения - хозяина, т. е. изменяет осмотическую концентрацию (ожоги) и вызывает хлороз. Растворы предлагаемых соединений даже в копцептрации 1% подобных явлений не вызывают.
Испытуемые соединения стимулируют рост молодых побегов. Таким образом, эти соединения выгодно отличаются от фундазола, применение которого вызывает тормозящее действие на рост растения-хозяина.
В отличие от фундазола предлагаемые N-замещенпые пмидн малеопимг.розой кислоты не раздражают глаза и кожу экспериментатора и их можно применять также и в тепличиых условиях.
Синтезированные N-замещенные имиды малеопимаровой кислоты можно использовать , в качестве фунгицидов против мучнистой росы на культуре роз, как это следует из данных табл. 2.
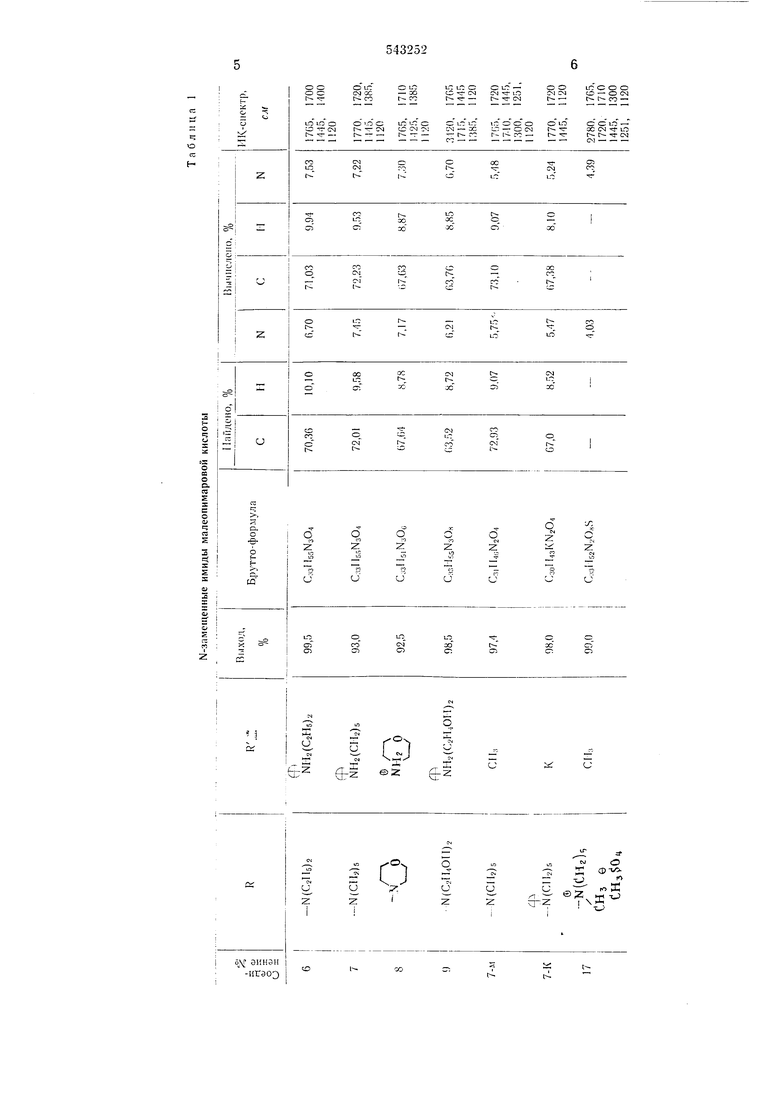
Пример 1. Диэтиламиновая соль N-(диэтиламинометил)имида малеопимаровой кислоты (соединение 6).
5 г Ы-(оксиметил)имида малеопимаровой кислоты (C25H35N05, Т. пл. 215° С) и 3,42 г
диэтиламина кипятят при 56° С в течение 10 i и затем отгоняют избыток диэтиламина. Остаток сушат в вакууме при 60° С в течение 15 ч. Получают 6,47 г (99,5%) соединения 6, которое очищают на силикагеле марки КСК с помощью хроматографии.
Аналогично получают и очищают соединения 7 и 8 табл. 1.
П р и м ер 2. Диэтаноламиновая соль N- (диэтаноламинометил)имида .малеопимаровой кислоты (соединение 9).
5 г М-(оксиметил)имида малеоппмаровой кислоты и 4,96 г диэтаноламина кипятят прн
180° С в течение 10 ч. После охлаждения полученную темно-коричневую массу растворяют в смеси этанол-ацетон 1:1, вынаривают и сущат в вакууме при 80° С в течение 5 ч. Получают 7,15 г (98,5%) соединения 9, которое очищают па катионите КУ 2-20.
Пример 3. Метиловый эфир -(пиперидилметил) имида малеопимаровой кислоты (7-М).
5 г Ы-(оксиметил) имида малеопимаровой
кислоты растворяют в 50 мл метанола, раствор охлаждают ниже 10° С и медленно, в течение 2 ; добавляют эфирный раствор диазомстана до получения постоянной желтой окраски. Затем отгоняют растворители. 0статок сушат в вакууме при 60° С в течение 5 ч. Получают 5,01 г (97,1%) метилового эфира М-(оксиметил)имида малеопимаровой кислоты, из которого по методике при.мера 1 получают 5,72 г (97,4%) соединения 7-М.
Очищают на катионите КУ 2-20.
Пример 4. Калиевая соль Ы-(иинеридилметил)имида малеопимаровой кислоты
(7-К).
5 г М-(оксиметил)имида малеопимаровой
кислоты в виде 10%-ного спиртового раствора нейтрализуют 0,65 г КОН в виде 5 п. спиртового раствора. Растворитель отгоняют, сухой остаток кристаллизуют из горячего ацетона, отфильтровывают и сущат в вакууме
при 60° С в течение 5 ч. Получают 5,4 г (00%) калиевой соли N-(oкcимeтил)имида малеопимаровой кислоты, из которой по методике примера 1 получают 6,14 г (99,5%) соедипения 7-К.
Пример 5. Метилсульфат метилового эфира N- (N-метил)пиперидинометил имида малеопимаровой кислоты (17).
3 г метилового эфира 1-(пиперидилметил) имида малеопимаровой кислоты и 0,25 мл
диметилсульфата кипятят при 125° С в течение 1 ч. Получают 3,62 г (99,5%) соединения 17. Очищают на ионообменной смоле ЭДЭ-Шп. Биологическая активность N-(aлкилaминoмeтил)и.чидoв Таблица 2 малеопимарсвой кислоты на мучнистую росу роз



Формула изобретения
О
Чоон
где R - диэтиламино-, диоксиэтиламиногруипа, морфолил или пиперидил, R - низший алкил, ион щелочного металла, или нон амФ
мония формулы H2R , где R имеет указанные значения,
нроявляющие фунгицидную активность.
Источники информации, принятые во внимание при экспертизе:
2- Tawney Р. О. с соавторами, J. Org. Chem., 26, 15, 1961 (прототип).
Авторы
Даты
1977-06-25—Публикация
1974-12-13—Подача