Изобретение относится к области медицины и фармакологии и представляет собой композиции на основе высокомолекулярного гепарина с аминокислотами (аргинином, пролином, глицином) и 3-d металлами (Mn(II), Fe(III), Co(II), Ni(II), Cu(II), Zn(II)), обладающие способностью доставлять в организм необходимые и важные аминокислоты (аргинин, пролин, глицин) и микроэлементы (Mn(II), Fe(III), Co(II), Ni(II), Cu(II), Zn(II)) и отличающиеся от обычных поливитаминных комплексов совмещением с гепаринотерапией.
Высокомолекулярный гепарин применяют при профилактике и терапии (гепаринотерапии) различных тромбоэмболических заболеваний и их осложнений, например для предотвращения или ограничения тромбообразования при остром инфаркте миокарда, тромбозах и эмболиях магистральных вен и артерий, сосудов мозга и глаз.
Мономерное звено гепарина представляет собой дисахарид уроновая кислота-(1→4)-0-глюкозамин.
Структурная формула мономерного дисахаридного звена гепарина состава 4-L-IdoA2S-α-4-D-GlcNS, 6S-α-l

Моносахарид уроновой кислоты может быть или α-L-идуроновой кислотой (IdoA) или β-D-глюкуроновой кислотой (GlcA), каждая из которых может быть 2-О-сульфатирована (Ido(2S) и GlcA(2S)). Моносахарид β-D-глюкозамина может быть незамещен (GlcN), сульфатирован (GlcNS) или ацетилирован (GlcNAc) по аминогруппе. Аминосульфатированный глюкозамин допускает 3-O- и 6-O- сульфатацию (GlcNS(3S), GlcNS(6S), GlcNS(3,6S)). Аминоацетилированный глюкозамин может быть 6-О-сульфатирован (GlcNAc(6S)).
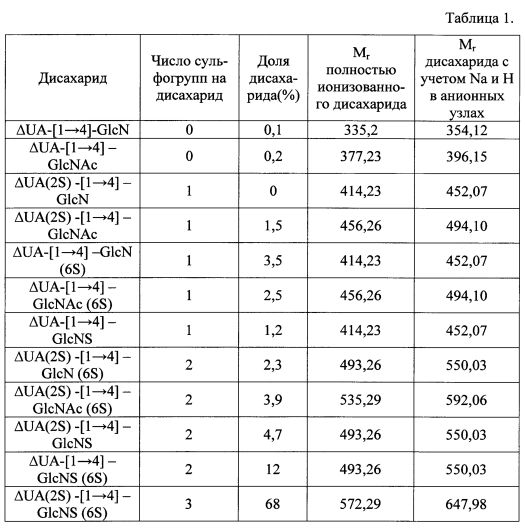
Из таблицы 1 видно, какие виды дисахаридов были экспериментально обнаружены в гепарине. На основании изложенного можно рассчитать средние параметры мономерного звена нефракционированного гепарина (таблица 2). Кольцо уроновой кислоты обозначено как AUA для несульфатированного моносахарида и как ΔUA(2S) для 2-О-сульфатированного.
В таблице 2 представлены усредненные параметры дисахаридного звена высокомолекулярного мукозного гепарина.
Из всего вышеперечисленного становится ясно, что все расчеты и структурные предположения имеет смысл выполнять в предположении, что полимерная цепь построена из усредненных мономерных звеньев [Nikos К. Karamanos. Ion-pair high-performance liquid chromatography for determining di-saccharide composition in heparin and heparan sulphate / Nikos K. Karamanos // J. of Chromatography A. - 1997, Vol. 765, No. 6, p. 169-179].
Хотя гепарин и применяется для лечения сердечно-сосудистых заболеваний, но он имеет несколько типов донорных групп: карбоксильная, сульфогруппы, гидроксогруппы, гликозидный и эфирный кислород, карбонильный кислород и амидный азот. Попадая в кровь, гепарин способен образовывать химические связи с металлами и аминокислотами, находящимися в крови, тем самым провоцируя их дефицит.
Структурная формула аминокислоты аргинин
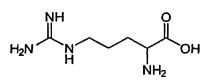
Аргинин (L-Arginine) - относится к условно незаменимым аминокислотам, оказывает стимулирующее действие на выработку инсулина поджелудочной железой в качестве компонента вазопрессина (гормона гипофиза) и помогает (стимулирует) синтез гормона роста, который, в свою очередь, улучшает сопротивляемость заболеваниям. Расширяет сосуды и усиливает их кровенаполнение. Снижает кровяное давление, улучшает реологию крови, способствует снижению уровня холестерина в крови и препятствует тромбообразованию. Способствует восстановлению соединительной ткани, усиливает синтез белка для роста мышц.
Структурная формула аминокислоты глицин
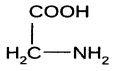
Глицин (Glycine) - укрепляет функции печени, стимулирует в обмене алкоголя. Снижает содержания сахара в крови и уменьшает содержания холестерина в крови.
Структурная формула молекулы пролина

Пролин (L-Proline) - заменимая аминокислота выполняет вспомогательные ГАМК функции торможения ЦНС, содержится в большинстве белков. Является источником энергии для печени и мышц. Является важнейшим элементом при образовании коллагена. Поддерживает нормальное состояния сухожилий суставов.
Цинк является катализатором многих реакций, входит в состав инсулина, входит в состав крови и мышечной ткани, участвует в белковом обмене, способствует всасыванию витамина Е и поддержанию нормальной концентрации этого витамина в крови, необходим для стабилизации структуры ДНК, РНК, рибосом, играет важную роль в процессе трансляции и незаменим на многих ключевых этапах экспрессии гена, обнаружен в составе более 300 ферментов.
Медь является жизненно важным элементом, который входит в состав многих витаминов, гормонов, ферментов, дыхательных пигментов, участвует в процессах обмена веществ, в тканевом дыхании. Медь имеет большое значение для поддержания нормальной структуры костей, хрящей, сухожилий, эластичности стенок кровеносных сосудов, легочных альвеол, кожи. Медь входит в состав миелиновых оболочек нервов.
Железо находится в составе гемоглобина, каждая молекула которого обладает четырьмя его атомами. С помощью гемоглобина связывается кислород, который проходит кровеносные сосуды легких, и доставляется в ткани, забирается углекислый. Также железо требуется многим ферментам и белкам, контролирующим: обмен холестерина; разрушение ядовитых веществ печенью; процесс кроветворения; производство ДНК; ответ иммунной системы на бактериальную или вирусную инфекцию; окислительно-восстановительные реакции; энергетический метаболизм.
Кобальт, один из микроэлементов, жизненно важных организму. Он входит в состав витамина B12 (кобаламин). Кобальт задействован при кроветворении, функциях нервной системы и печени, ферментативных реакциях. Соли Со2+ способствуют накоплению некоторых других витаминов: пиридоксина, никотинамида, которые положительно влияют на все виды обмена веществ: белковый, минеральный и углеводный.
Марганец входит в состав активного центра многих ферментов: пиру-ваткарбоксилаза, аргиназа, холинэстераза, фосфоглюкомутаза, перокисдаза, аминофенолоксидаза. В составе ферментов аргиназы и холинэстеразы марганец участвует в свертывании крови; в составе пероксидазы и аминофенолоксидазы регулирует превращение молекулярного кислорода; в составе пируваткарбоксилазы и фосфоглюкодисмутазы влияет на углеводный обмен. Марганец участвует в синтезе витаминов группы В и влияет на синтез гемоглобина.
Никель входит в активный центр фермента уреазы, ответственной за гидролиз мочевины, а также вместе с кофактором F-430 «помогает» бактериям-метаногенам восстанавливать группы - СН3СО до метана. Никель также участвует в процессах кроветворения в обмене жиров, обеспечении клеток кислородом. В определенных дозах никель активизирует действие инсулина.
Из уровня техники известна композиция на основе высокомолекулярного гепарина с антикоагулянтными, антитромбоцитарными, фибринолитическими и фибриндеполимеризационными свойствами (RU №02454237, опубл. 27.06.2012), содержащая лейцин при следующих количествах компонентов в расчете на 90-120 ME активности гепарина: лейцин - 0,56-0,58 мг, эйконол - 113-115 мг.
Недостатками данного технического решения является то, что композиция представляет собой узконаправленный препарат, который не учитывает химической активности основного вещества, способ его получения требует значительных количеств веществ, входящих в его состав.
Из уровня техники также известен способ получения низкомолекулярного гепарина (RU №2512768, опубл. 10.04.14), который включает получение бензетониевой соли нефракционированного гепарина в 0,05-0,5 М водном растворе натрия хлорида при температуре 50-60°С, рН=8,2-8,8 и массовом соотношении гепарин/бензетоний хлорид 1/(2,35-2,70), бензилирование бензетониевой соли гепарина, проводя в течение 2-3 часов в среде биполярного апротонного растворителя бензилхлоридом в соотношении гепари-нат/бензилхлорид 1/(0,2-1,0), который предварительно подвергают активированию в апротонном растворителе в течение 15-20 мин, осаждение бензило-вого эфира гепарина методом Спиро этиловым спиртом, предварительно насыщенным безводным натрия ацетатом, с последующим снятием защиты с сульфогрупп, проведение β - элиминирования бензилового эфира со степенью этерификации гепарина 9-13% 1±0,5 N щелочью NaOH при температуре 55±5°С, длительности процесса 40-60 мин и массовым соотношением реагентов бензиловый эфир/щелочь 1/(0,5-2).
Недостатками вышеописанного способа является применение бензил-хлорида, который является ядовитой высокоопасной летучей жидкостью, выделяющей слезоточивые пары. Бесцветная, с резким запахом. В присутствии влаги коррозионна для большинства металлов, что будет затруднять промышленное применение. Также большое количество химических взаимодействий (бензилирование, снятие защиты с сульфогрупп, β - элиминирование) увеличивает трудоемкость процесса и уменьшает предсказуемость результатов.
Наиболее близким к заявленному техническому решению является способ получения антикоагулянтно-фибринолитического средства на основе гепарина (RU №02448717, опубл. 27.04.2012), который заключается в смешивании водных растворов гепарина и лейцина в молярном соотношении 1:3-4, после чего образовавшийся продукт замораживают при температуре не выше -10°С и лиофильно высушивают. Обычно перемешивание ведут в течение 25-30 мин. Преимущественно используют 0,8-1,0% водный раствор гепарина и 0,3-1,0% раствор лейцина.
Недостатками данного способа являются: использование достаточно больших количеств веществ, необходимых для получения средства; необходимость поддержания низкой температуры для хранения и получения средства; отрицательное воздействие на организм основного действующего вещества - гепарина, входящего в состав средства.
Задачей, на решение которой направлено заявляемое изобретение, является создание способа получения композиций на основе гепарина, способствующих уменьшению дефицита микроэлементов и аминокислот в крови при гепаринотерапии.
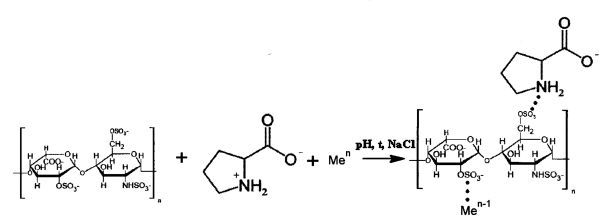
Данная задача решается за счет того, что способ получения композиций на основе высокомолекулярного гепарина с аминокислотами и 3-d металлами, включает смешивание водных растворов гепарина, аминокислоты и соли 3-d металла, их осаждение, декантацию и осушение. При этом смешивание производят в молярном соотношении 1:1:1 при температуре 37°С, рассчетных рН, ионной силе 0.15М NaCl, затем осаждают композицию с помощью полярного апротонного растворителя - ацетона в соотношении композиция/ацетон: 1/1,25, выдерживают в термостате при температуре 0°С 180 минут, центрифугируют при 8000-1000 об/мин и осушают осадок в сушильном шкафу при t=60°С в течение 60 минут.
Схема взаимодействия гепарина с аргинином и солью 3-d металла
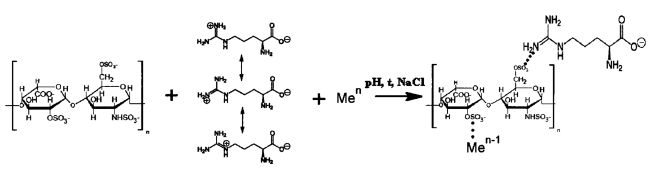
Схема взаимодействия с глицином и солью 3-d металла
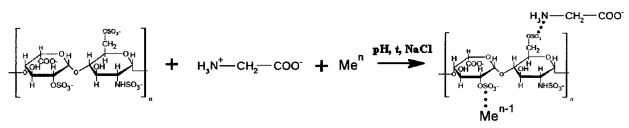
Схема взаимодействия гепарина с пролином и солью 3-d металла
Техническим результатом, обеспечиваемым приведенной совокупностью признаков, является получение лекарственных композиций, которые позволят уменьшить риск возникновения дефицита различных металлов и аминокислот в крови человека при лечении тромбоэмболических заболеваний, при операциях на сердце и кровеносных сосудах, при поддержании жидкого состояния крови в аппаратах искусственного кровообращения и гемодиализа, а также варьировать дозу лекарственных препаратов в направлении ее уменьшения, что в конечном итоге приведет к снижению экономических затрат на приобретение этих веществ, на лечение последствий от их воздействия и к уменьшению вреда здоровью.
Сущность изобретения поясняется сведениями, приведенными в таблицах.
В таблице 1 представлен дисахаридный состав мукозного гепарина.
В таблице 2 представлены усредненные параметры дисахаридного звена высокомолекулярного мукозного гепарина.
Для получения композиций используются глицин, L-аргинин и L-пролин, которые имеют квалификацию ч.д.а. и стандартный фармакологический раствор гепарина (12000 Да) в форме тетранатриевой соли производства «Московский эндокринный завод» - каждый миллилитр такого раствора содерит 5000 ЕД (1 ЕД=0,0077 мг гепарина) или 38.5 мг соли. А также применяются реактивы: L-аргинин (1,2*10-2 М), глицин (1,2*10-2 М), L-пролин (1,2*10-2 М), CuCl2 (1,04*10-2М), NiCl2 (3,73*10-2 М), CoCl2 (1,07*10-2М), MnCl2 (1,09*10-2М), FeCl3 (1,16*10-2 М), ZnCl2 (1,16*10-2 М), NaOH (конц.), HCl (конц.), гепарин (0,058 М).
Композиции создаются при смешивании в емкости с магнитной мешалкой водных растворов гепарина, одной из аминокислот (аргинин, пролин, глицин) и соли одного 3-d металла (Mn(II), Fe(III), Co(II), Ni(II), Cu(II), Zn(II)) в молярном соотношении 1:1:1 при температуре 37°С, определенных рН, ионной силе 0.15М NaCl.
Для определения рН полученного раствора используют откалиброванный рН-метр (1,65; 9,18). Для измерения рН были использованы стеклянный (индикаторный) и хлорсеребряный (электрод сравнения) электроды. Доводим рН с помощью NaOH (концентрированная) или НС1 (концентрированная) до значений, рассчитанных по уравнению материального баланса и закона действующих масс для функции рН по базисным компонентам. Для всех имеющихся систем была составлена математическая модель. Нужные рН среды были рассчитаны методами рН-метрии и математического моделирования химических равновесий. Расчеты моделей химических равновесий и определение соответствующих констант выполнены с помощью комплекса вычислительных программ New DALSFEK. При полученных рассчетным путем значений рН для каждой композиции наблюдается наибольший выхода продукта.
Опытные значения рН для каждой композиции, при которых наблюдается наибольший выход продукта.
Затем композиции осаждают с помощью полярного апротонного растворителя - ацетона («хч») в соотношении композиция/ацетон: 1/1 и помещают в термостат с температурой 0°С на 180 минут. После чего, в течение 30 минут раствор центрифугируют при 8000-1000 об/мин, проводят декантацию и осушают осадок в сушильном шкафу при t=60°С в течение 60 минут.
Для различных видов композиций определен объем реагентов в молярном соотношении 1:1:1 на 100 мл дистиллированной воды.
Пример 1. Приготовление аминокислот.
Растворы аминокислот аргинина, пролина, глицина готовятся в трех колбах каждая на 100 мл по навеске так, чтобы в 10 мл каждого из растворов содержалось 1.16*10-4 моль аминокислоты (соблюдаем эквимолярное соотношение). Для этого взвешивается на листочке алюминиевой фольги 0.087 г глицина (М=75.07 г/моль), 0.1337 г L-пролина (М=115.3 г/моль), 0.2021 г L-аргинина (М=174.2 г/моль). Насыпаем в каждую колбу соответсвующую аминокислоту по навеске и добавляем дистиллированной воды до риски 100 мл.
Полученные растворы содержат заданные количества аминокислот.
Пример 2. Приготовление раствора соли 3-d металла MeCln (Men+: Mn(II), Fe(III), Co(II), Ni(II), Cu(II), Zn(II)).
Соблюдая эквимолярное соотношение компонентов в композиции 1:1:1, приготавливаются растворы MeCln в колбе на 100 мл, путем растворения их солей (m(CuCl2)=0,015602 г, m(NiCl2)=0,01508 г, m(CoCl2)=0,01508 г, m(MnCl2)=0,014616 г, m(FeCl3)=0,01885 г), кроме ZnCl2. Хлористый цинк получили путем растворения металлического цинка (m=0,00754 г) в концентрированной (39%) соляной кислоте (при плотности соляной кислоты 1.19 г/см3). Кислоту осторожно вливают в посуду с кусочками цинка так, чтобы уровень не превышал 3/4 глубины посуды. При окончательном растворении цинка выделение пузырьков водорода прекращается. Полученному раствор хлористого цинка отстаивается до прозрачности, что свидетельствует о полном растворении цинка в растворе соляной кислоты, и сливается в колбу.
Пример 3. Приготовление растворов NaCl, HCl, NaOH.
Раствор соляной кислоты приготовливается из фиксанала, концентрация кислоты 0.1н.
1.54 М раствор NaCl приготовлен из ч.д.а его соли по навеске (m(NaCl)=9.009 г) путем растворения в 100 мл дистиллированной воды.
Титрант - бескарбонатный раствор гидроксида натрия готовится растворением 0,2 г NaOH в предварительно прокипяченной дистиллированной воде(0,5 л).
Последующей стандартизацией путем титрования навески сульфаминовой кислоты, предварительно очищенной перекристаллизацией. Данным способом было подтверждено процентное содержание щелочи.
Пример 4. Приготовление рабочего раствора.
Для приготовления основного раствора в колбу на 100 мл было добавлено: 10 мл 1.16*10-3 М аминокислоты (глицин - Gly-, аргинин - Arg", пролин -Pro-), 10 мл 1.16*10-3М раствора соли 3-d металла MeCln, 2 мл гепарина, 10 мл 1.54 М NaCl. Далее доводили дистиллированной водой до метки и опускали в ультратермостат UTU-2/77 на 15 минут.
Пример 5. Проведение рН-метрии.
Измерения значений рН проводили с помощью И-135, укомплектованного измерительным стеклянным электродом ЭСЛ 63-07 и насыщенным хлоридсеребряным электродом сравнения. Перед началом титрования была проведена калибровка рН-метра с помощью стандартных буферных растворов с величинами рН равными 1.65 и 9.18, с учетом поправки на температуру 37°С и ионную силу 0.15 М хлорида натрия.
Пример 6. Математическое моделирование.
Исследования взаимодействия в системе Men+-L1-L2 (Men+: Mn(II), Fe(III), Co(II), Ni(II), Cu(II), Zn(II); L1: Hep4-; L2: Gly-, Arg-, Pro-) проводилось по экспериментальным данным рН-метрического титрования водных растворов при соотношении 1:1:1 исходных концентраций составляющих компонентов системы.
Благодаря высокой плотности отрицательного заряда макромолекула гепарина в растворе находится в вытянутом, палочкообразном состоянии, поэтому анионные узлы должны оставаться доступными для взаимодействия с противоионами; макромолекула гепарина представляется нами как совокупность отдельных мономерных звеньев - дисахаридов, концентрация которых в растворе и принимается за концентрацию самого гепарина, а монозвено - за базисный термодинамический компонент раствора.
По уравнению материального баланса и закона действующих масс для функции рН по базисным компонентам для всех имеющихся систем была составлена математическая модель. Расчеты моделей химических равновесий и определение соответствующих констант выполнены с помощью комплекса вычислительных программ New DALSFEK.
Пример 7. Центрифугирование, декантация и осушение.
После получасовой выдержки полученной смеси с ацетоном (50 мл) в термостате с температурой 0°С в течение 180 минут центрифугировали при 8000-10000 об/мин в течение 30 мин. По истечении указанного времени с осадка геля сливали маточный раствор, а оставшийся в микростакане гель высушивали в токе теплого воздуха. Во всех случаях наблюдали образование хрупких стеклообразных веществ легко растворимых в воде. Наибольший выход достигнут в случае выделения металлокомплексов ионов микроэлементов с гепарином и аргинином. Осадки высушиваем в сушильном шкафу при t=60°C 1 час.
Полученные предлагаемым способом композиции содержат в своем составе наиболее важные аминокислоты и микроэлементы, которые при попадании в кровеносную систему разлагаются из-за отличия рН среды (7.3) от рН устойчивости этих композиций с выделением гепарина, аминокислот и микроэлементов, тем самым играя компенсационную роль при гепаринотерапии.

| название | год | авторы | номер документа |
|---|---|---|---|
| АНТИТРОМБОТИЧЕСКИЙ КОМПЛЕКС НА ОСНОВЕ ГЕПАРИНА, СПОСОБ ЕГО ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2015 |
|
RU2600817C2 |
| ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ПРОГРЕССИРУЮЩЕЙ БЛИЗОРУКОСТИ | 2013 |
|
RU2635185C2 |
| ЭМУЛЬСИЯ ПЕРФТОРОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С УВЕЛИЧЕННОЙ КИСЛОРОДНОЙ ЁМКОСТЬЮ | 2022 |
|
RU2803466C2 |
| КОМПОЗИЦИИ ДЛЯ УСИЛЕНИЯ АНТИБАКТЕРИАЛЬНОЙ АКТИВНОСТИ МИЕЛОПЕРОКСИДАЗЫ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2009 |
|
RU2529799C2 |
| Водная композиция инсулина аспарта и инъецируемый инсулиновый препарат | 2022 |
|
RU2832344C2 |
| ПЕПТИДИЛЬНЫЕ ГЕТЕРОЦИКЛЫ, ИСПОЛЬЗУЕМЫЕ ПРИ ЛЕЧЕНИИ ТРОМБИНАССОЦИИРОВАННЫХ ЗАБОЛЕВАНИЙ | 1996 |
|
RU2181125C2 |
| ПЕПТИДИЛАРГИНАЛИ И СПОСОБЫ ЛЕЧЕНИЯ СИНДРОМА ДИССЕМИНИРОВАННОГО ВНУТРИСОСУДИСТОГО СВЕРТЫВАНИЯ | 2002 |
|
RU2312856C2 |
| Кормовая добавка на основе этилендиаминтетраацетата цинка и комплекса аминокислот для птиц и сельскохозяйственных животных и способ ее изготовления | 2023 |
|
RU2823608C1 |
| НОВЫЕ АНАЛОГИ ГЛЮКАГОН-ПОДОБНОГО ПЕПТИДА, КОМПОЗИЦИЯ И СПОСОБ ПРИМЕНЕНИЯ | 2010 |
|
RU2557301C2 |
| СПОСОБ КОНТРОЛЯ РЕАКЦИИ МОДИФИКАЦИИ ПОЛИПЕПТИДА | 2009 |
|
RU2532850C2 |
Изобретение относится к области медицины и фармакологии и представляет собой способ получения композиции на основе высокомолекулярного гепарина с аминокислотами и 3-d металлами. Способ получения включает смешивание водных растворов гепарина, аминокислоты и соли 3-d металла. При этом смешивание производят в молярном соотношении 1:1:1 при температуре 37°С, определенных рН, ионной силе 0.15М NaCl, затем осаждают композицию с помощью полярного апротонного растворителя - ацетона в соотношении композиция/ацетон: 1/1,25, выдерживают в термостате при температуре 0°С 180 минут, декантируют, центрифугируют при 8000-1000 об/мин и осушают осадок в сушильном шкафу при t=60°С в течение 60 минут. Полученные предлагаемым способом композиции содержат в своем составе важные аминокислоты и микроэлементы, которые при попадании в кровеносную систему разлагаются из-за отличия рН среды (7.3) от рН устойчивости этих композиций с выделением гепарина, аминокислот и микроэлементов, тем самым играя компенсационную роль при гепаринотерапии. 2 табл., 7 пр.
Способ получения композиций на основе высокомолекулярного гепарина с аминокислотами и 3-d металлами, включающий смешивание водных растворов гепарина, аминокислоты и соли 3-d металла, их осаждение, декантацию и осушение, отличающийся тем, что смешивание производят в молярном соотношении 1:1:1 при температуре 37°C, рассчетных pH, ионной силе 0.15М NaCl, затем осаждают композицию с помощью полярного апротонного растворителя - ацетона в соотношении композиция/ацетон: 1/1,25, выдерживают в термостате при температуре 0°C 180 минут, центрифугируют при 8000-1000 об/мин и осушают осадок в сушильном шкафу при t=60°C в течение 60 минут.
| СПОСОБ ПОЛУЧЕНИЯ АНТИКОАГУЛЯНТНО-ФИБРИНОЛИТИЧЕСКОГО СРЕДСТВА НА ОСНОВЕ ГЕПАРИНА | 2011 |
|
RU2448717C1 |
| КОМПОЗИЦИЯ НА ОСНОВЕ ВЫСОКОМОЛЕКУЛЯРНОГО ГЕПАРИНА С АНТИКОАГУЛЯНТНЫМИ, АНТИТРОМБОЦИТАРНЫМИ, ФИБРИНОЛИТИЧЕСКИМИ И ФИБРИНДЕПОЛИМЕРИЗАЦИОННЫМИ СВОЙСТВАМИ | 2011 |
|
RU2454237C1 |
| US3577534 A, 04.05.1971 | |||
| ЛЯПИНА Л.Α?., ЗИАДЕТДИНОВА Г.А | |||
| "Комплексное соединение гепарина с глутаминовой кислотой: получение и его влияние на показатели гемостаза in vitro и in vivo" | |||
| Известия РАН | |||
| Серия биологическая | |||
| Перекатываемый затвор для водоемов | 1922 |
|
SU2001A1 |
| Машина для разделения сыпучих материалов и размещения их в приемники | 0 |
|
SU82A1 |
| ФРАНЦЕВА Ю.В | |||
| Физико-химическое исследование систем, | |||
Авторы
Даты
2016-07-27—Публикация
2015-06-30—Подача