Изобретение относится к области медицинской микробиологии и биотехнологии и представляет собой оригинальный штамм Helicobacter pylori, обладающий комплексом детерминант факторов патогенности (ureC, ureI, cagA, vacA) и используемый как тест-штамм для индикации и идентификации Helicobacter pylori в биологическом материале (образцах биоптатов слизистой оболочки желудка или двенадцатиперстной кишки) при эпидемиологических и микробиологических исследованиях. Данный штамм также может быть использован при создании диагностических тест-систем.
Как известно, Helicobacter pylori ассоциируется с такими заболеваниями, как гастрит, язвенная болезнь, рак желудка и некоторыми другими (Malfertheiner P., Megraud F., O′Morain С.А., Atherton J. et al., 2012). Среди инфицированных лиц имеются различия в ответе на наличие Н. pylori, обусловленные особенностями как микроба, так и организма человека. Особенно важен полиморфизм бактериальных факторов патогенности (Furuta Т., Delchier J.C., 2007). Штаммы Н. pylori условно разделяют на две группы - с высоким и низким уровнем вирулентности. Эти различия чаще всего связывают со статусом cagA и vacA генов, которые известны своей неоднородностью (Jafari F., Shokrzadeh L., Dabiri H. et al., 2008). Показано, что CagA является онкогенным белком, способным вызывать гиперплазию желудочного эпителия, развитие полипов желудка и аденокарциномы желудка (Ohnishi N., Yuasa Н., Tanaka S. et al., 2008). CagA принимает участие в модуляции экспрессии генов эпителиальных клеток, кодирующих мутагенактивные протеинкиназы и транскрипцию гена интерлейкина 8, который способствует образованию противовоспалительных цитокинов. В связи с этим в слизистой оболочке желудка больных, инфицированных CagA+ штаммами Н. pylori, воспалительная реакция в слизистой выражена в большей степени (Мироджов Г.К., Мансурова Ф.Х., Ишанкулова Д.М., 2008). Ген vacA кодирует белок, являющийся цитотоксином, который повреждает эпителиальные клетки слизистой. Он вызывает образование пор в цитоплазматической мембране, увеличивает ее проницаемость, в результате чего в цитоплазме возникают вакуоли. Известно, что ген vacA имеется у всех штаммов Н. pylori, поэтому он может быть использован, как достоверный критерий наличия генома данного микроорганизма (Megraud F., Lehours P., 2007). Ген cagA Н. pylori присутствует не всегда.
Удельный вес заболеваний, обусловленных Н. pylori, в общей популяции населения отличатся, что связано с географическими, этническими, возрастными, социально-экономическими особенностями регионов. Проведенный нами анализ показывает, что на территории Санкт-Петербурга преобладают штаммы Н. pylori, имеющие ген токсигенности cagA (до 80% выделенных штаммов). Доля CagA-позитивных штаммов у больных в Санкт-Петербурге максимальна при раке желудка (90,8%), тогда как при язвенной болезни и гастритах она равна 64,7% и 72,2% соответственно. Полученные данные о возрастании доли CagA-позитивных штаммов в циркуляции среди населения определяют важность проведения мониторинга за возбудителем на разных территориях, при различных формах патологии желудочно-кишечного тракта и проведении эрадикации при наличии заболеваний, ассоциированных с Н. pylori с последующим контролем ее эффективности.
Наиболее близким по сущности к заявленному штамму является штамм микроорганизма Helicobacter pylori GB1 (В-0573), используемый при разработке методов диагностики хеликобактер-ассоциированных заболеваний (Казахстан, инновационный патент 26385, опубл. 15.11.2012). Штамм Helicobacter pylori пополняет коллекцию микроорганизмов Национального референтного центра по ветеренарии. Штамм Helicobacter pylori генотипирован по 16S рРНК, охарактеризован на гены факторов вирулентности, такие как cagA, cagE, vacA, iceA, BаBА, hopQ.
Недостатком указанного штамма является отсутствие данных по фенотипическим и генотипическим характеристикам его антибиотикорезистентности.
Изобретение направлено на получение тест-штамма Н. pylori, обладающего комплексом детерминант факторов патогенности (ureC; ureI; cagA, vacA).
Технический результат - индикация и идентификация бактерий Helicobacter pylori в биологическом материале (образцах биоптатов слизистой оболочки желудка или двенадцатиперстной кишки) по наличию генов вирулентности cagA и vacA, что позволит установить факт инфицированности данным микробом и определить его патогенетический потенциал, а также проводить мониторинг за циркуляцией штаммов на различных территориях.
Авторский штамм Helicobacter pylori депонирован в государственной коллекции патогенных микроорганизмов и клеточных культур «ГКПМ-Оболенск» под номером В-7215 26.09.2012.
Штамм Helicobacter pylori №782, депонированный в государственной коллекции патогенных микроорганизмов и клеточных культур «ГКПМ-Оболенск» под номером В-7215 26.09.2012, выделен в НИИЭМ имени Пастера в 2007 году от больного хроническим гастродуоденитом.
Штамм характеризуется следующими признаками.
Морфологические признаки: грамотрицательная аспорогенная бескапсульная палочка слегка изогнутой формы длиной 1-3 мкм.
Культуральные особенности: на селективной кровяной среде, содержащей основу Колумбийского агара, дефибринированную кровь и ростовые и антибиотические добавки, образует мелкие, круглые, гладкие, прозрачные, влажные колонии диаметром около 1 мм.
Биохимические свойства: оксидаза (+), каталаза (+), щелочная фосфатаза (+), уреаза (+), подвижность в бульоне (+), подвижность в агаре (-), толерантность к 1% желчи (-), рост в микроаэрофильных условиях при 30-37°С (+), рост в микроаэрофильных условиях при 42°С (-). рН оптимум штамма 6,0-7,0. При рН выше 8,5 и ниже 3,5 бактерии погибают.
Серологические свойства: не определялись.
Продукция антигенов, ферментов, токсинов: обладает ферментом уреаза, цитотоксическим токсином (CagA), вакуолизирующим токсином (VacA).
Устойчивость к антибактериальным препаратам: штамм устойчив к: метронидазолу, кларитромицину; чувствителен к: амоксициллину, тетрациклину.
Генетические характеристики: штамм Helicobacter pylori обладает комплексом детерминант факторов патогенности (ureC; ureI; cagA, сасА), имеет мутацию в гене 23 S rRNA Т2182С, определяющую устойчивость к кларитромицину.
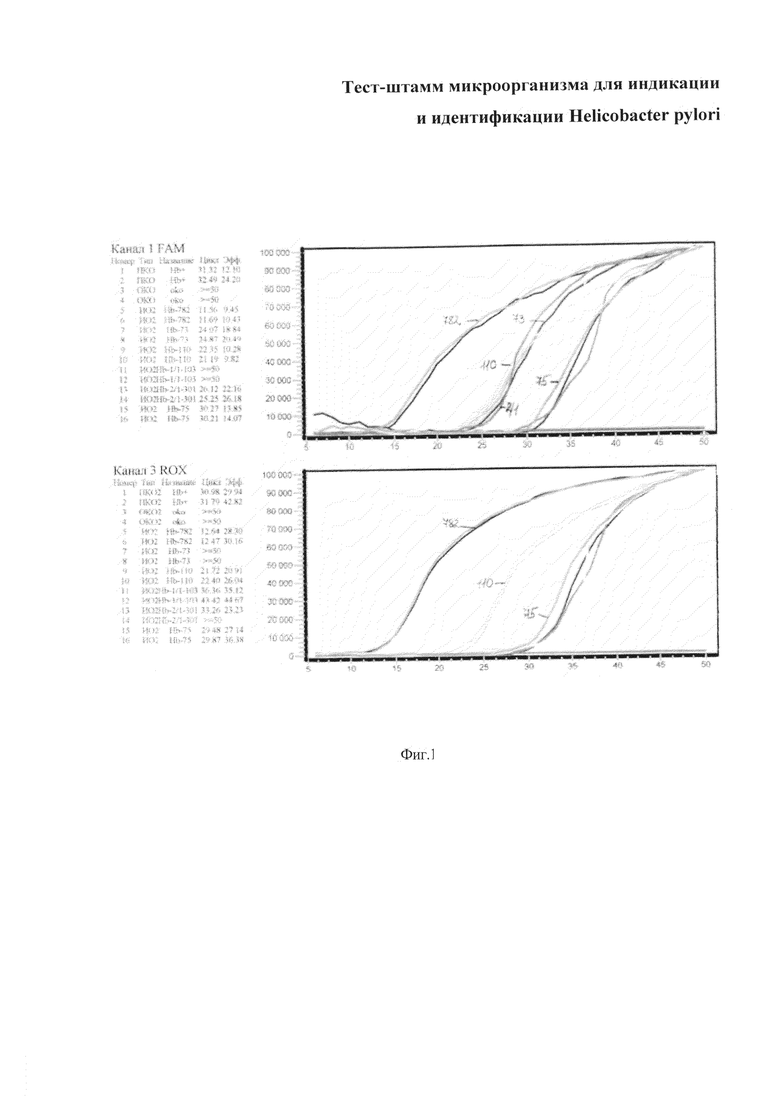
Сущность изобретения подтверждается фиг. 1, где представлены результаты определения наличия генов vacA и cagA Н. pylori методом ПЦР в режиме реального времени в образцах биоптатов слизистой оболочки желудка или двенадцатиперстной кишки.
Штамм получен с помощью бактериологического метода. Материалом для исследования послужил образец биопсии слизистой оболочки желудка. В качестве основы питательной среды для выделения и культивирования H. pylori использовали основу колумбийского агара (Columbia Agar Base, Becton Dickinson, USA). Перед использованием в нее добавляли 5-7% дефибринированной лошадиной крови и раствор IsoVitalex до концентрации 1%. Для подавления роста сопутствующей флоры использовали различные антибиотические добавки: ванкомицин в концентрации 6 мкг/мл для подавления кокковой флоры, триметоприм в концентрации 2 мкг/мл для ингибиции грамотрицательных палочек, амфотерицин B в концентрации 2 мкг/мл для ингибирования грибов. рН оптимум агара 7,3±0,2. Н. pylori является микроаэрофильной бактерией, поэтому для успешного его культивирования необходим особый состав газовой среды. Оптимальным составом газовой среды является: содержание кислорода - 5%, углекислого газа - 7-10%, азота - 80-85%, водорода - 8-10%, относительная влажность газовой среды - 98-100%. Для инкубации посевов использовались анаэростаты системы GasPac100. Для создания в анаэростате микроаэрофильных условий используются газогенерирующие пакеты типа GasPak (BBL CampyPak Plus Microaerophilic System envelopes with Palladium Catalyst). После загрузки анаэростаты размещали в термостате при температуре 37°С, оптимальной для роста H. pylori. Сроки формирования колоний - 5-7 суток. Решение вопроса о принадлежности выделенной культуры к роду Helicobacter выносили на основании характерной морфологии выделенных колоний (мелкие, круглые, гладкие, прозрачные, влажные колонии диаметром около 1 мм), а также следующих тестов: морфология культуры в мазке, окрашенном по граму (грамотрицательная палочка слегка изогнутой формы длиной 1-3 мкм), и наличия характерных биохимических свойств (способность к продукции уреазы, каталазы и оксидазы).
Штамм Н. pylori хранится в криопробирках с добавлением равного количества стерильного глицерина и сыворотки крупного рогатого скота при температуре -70°С.
Изобретение реализуется следующим образом.
Пример 1. Определение наличия cagA Н. pylori методом ПЦР
Штамм Н. pylori высевается на чашки Петри, содержащие основу Колумбийского агара с добавлением 5-7% дефибринированной лошадиной крови и 1% IsoVitalex. Для инкубации посевов используются анаэростаты системы GasPac100. Для создания в анаэростате микроаэрофильных условий используются газогенерирующие пакеты типа GasPak (BBL CampyPak Plus Microaerophilic System envelopes with Palladium Catalyst). После загрузки анаэростаты размещают в термостате при температуре 37°С, оптимальной для роста H. pylori. Через 5-7 суток с каждой чашки Петри проводится смыв бактериальной массы с помощью 1 мл стерильного физиологического раствора. Затем проводится выделение ДНК с помощью набора реагентов для экстракции ДНК. Для этого ресуспендируют сорбент универсальный to, вносят в каждую пробирку по 20 мкл сорбента универсального и 300 мкл лизирующего раствора. Вносят в каждую пробирку по 100 мкл суспензии бактерий. В пробирку отрицательного контроля экстракции вносят 100 мкл ОКО. Пробирки плотно закрывают, перемешивают на вортексе и инкубируют 5 мин при 65°С в термостате. Содержимое пробирок перемешивают на вортексе и оставляют при комнатной температуре на 2 мин. Центрифугируют пробирки при 10 тыс. оборотов/мин в течение 30 секунд. Удаляют надосадочную жидкость. Добавляют в пробы по 1 мл отмывочного раствора, перемешивают на вортексе до полного ресуспендирования сорбента. Центрифугируют пробирки при 10 тыс. оборотов/мин в течение 30 секунд. Удаляют надосадочную жидкость. Помещают пробирки в термостат при 65°С на 5-10 мин для подсушивания сорбента. В пробирки добавляют ТЕ-буфер для элюции ДНК. Перемешивают на вортексе до полного ресуспендирования сорбента. Помещают в термостат с температурой 65°С на 5 мин. Центрифугируют пробирки при 12 тыс. об/мин в течение 1 минуты. Надосадочная жидкость содержит очищенную ДНК Н. pylori и может быть использована для дальнейших постановок ПЦР.
Бактерии исследуют методом полимеразной цепной реакции с праймерами к участкам генов, кодирующими факторы патогенности Н. pylori производства ООО «Синтол» (Москва) (таблица 1).

Реакционную смесь готовят из расчета на одну пробу: 17,5 мкл дистиллированной воды, 3,0 мкл буфера для Taq ДНК-полимеразы, 2 мМ/ мкл MgCl2, 4,8 мкл dNTP (дезоксинуклеотидтрифосфат), 1,0 мкл праймера прямого и 1,0 праймера обратного, 0,3 мкл Taq-полимеразы. После этого пробирки центрифугируют для перемешивания компонентов смеси и в каждую пробирку добавляют 5 мкл ДНК из пробы. Добавляют во все пробирки по 20 мкл минерального масла. ПЦР проводят по программе: 1 цикл 95°С - 2 мин; 45 циклов 95°С - 60 сек, 58°С - 40 сек, 74°С - 60 сек; 1 цикл - 74°С 120 сек. Для учета результатов ПЦР проводят электрофорез в 1,5% агарозном геле (1,5 г агарозы, 100 мл 1% ТВЕ-буфера, 7 мкл бромистого этидия) при постоянном напряжении 100 В.
Пример 2. Определение наличия генов vacA и cagA Н. pylori методом ПЦР в режиме реального времени в образцах биоптатов слизистой оболочки желудка или двенадцатиперстной кишки.
Были исследованы пять образцов биопсийного материала слизистой оболочки желудка, полученные от пациентов с различной патологией желудка и двенадцатиперстной кишки. Биопсийный материал из слизистой оболочки желудка помещали в пробирку типа «эппендорф» с транспортной средой и хранили до отправки в лабораторию в условиях холодильника при +4°С, при полном погружении биоптата в раствор. Биопсийный материал подлежал обработке и посеву немедленно после доставки в лабораторию. Выделение из биоптата ДНК осуществлялось с помощью набора реагентов «АмплиПрайм ДНК-сорб-В» (ООО «НекстБио»). Полученную ДНК исследовали методом ПЦР-РВ с помощью набора «Helicobacter pylori-РВ». Набор содержит реакционную смесь, положительный контрольный образец, содержащий фрагменты ДНК генов cagA и vacA Н. pylori, отрицательный контрольный образец, фрагмент Taq ДНК-полимераза 5 Е/мл. Исследование проводится на приборе АНК-32. Рекомендуемые условия проведения ПЦР: 1 цикл 95°С - 900 сек; 50 циклов 62°С - 50 сек; 50 циклов 95°С - 20 сек. Реакции и цветовые каналы прибора: Helicobacter pylori vacA ген - канал FAM; Helicobacter pylori cagA ген - канал ROX. Результаты исследования представлены в таблице 2 и на фиг. 1.

По полученным данным видно, что штамм Н. pylori №782 (В-7215) имеет в своем наличии vacA и cagA гены, также как и образцы биопсии №110 и №75, тогда как образцы биопсийного материала из слизистой оболочки желудка №1/1 данных генов не содержали. Только ген vacA содержит образцы №2/1 и №73.
Таким образом, заявленный штамм пригоден для индикации и идентификации Helicobacter pylori в биологическом материале (образцах биоптатов слизистой оболочки желудка или двенадцатиперстной кишки) по содержанию генов патогенности, что позволит установить факт инфицированности данным микробом и определить его патогенетический потенциал, а также проводить мониторинг за циркуляцией штаммов на различных территориях.
Изобретение относится к области медицинской биотехнологии и может быть использовано для эпидемиологических и микробиологических исследований. Штамм микроорганизма Helicobacter pylori №782, предназначенный для создания диагностических тест-систем, депонирован в Государственной коллекции патогенных микроорганизмов и клеточных культур «ГКПМ-Оболенск» под номером ГКПМ - Оболенск В-7215. Тест-штамм обладает комплексом детерминант факторов патогенности (UreC; UreI; CagA, VacA), имеет мутацию в гене 23 S rRNA - Т2182С. Изобретение обеспечивает использование тест-штамма при идентификации Н. pylori в образцах биоптатов слизистой оболочки желудка или двенадцатиперстной кишки, определении его генотипа и устойчивости к антибиотикам. 1 ил., 2 табл., 2 пр.
Тест-штамм микроорганизма Helicobacter pylori ГКПМ - Оболенск В-7215 для индикации и идентификации Helicobacter pylori в образцах биоптатов слизистой оболочки желудка или двенадцатиперстной кишки.
| Станок для намотки проволоки или ленты | 1931 |
|
SU26385A1 |
| СИМАНЕНКОВ В.И | |||
| и др | |||
| Резистентность Helicobacter pylori к антимикробным препаратам по результатам бактериологического тестирования.//Лечащий врач, 2015, 4, с.91-95 | |||
| СПОСОБ БАКТЕРИОЛОГИЧЕСКОЙ ДИАГНОСТИКИ Helicobacter pylori В СЛИЗИСТОЙ ОБОЛОЧКЕ ЖЕЛУДКА У ПАЦИЕНТОВ С ГАСТРОДУОДЕНАЛЬНОЙ ПАТОЛОГИЕЙ | 2011 |
|
RU2478957C2 |
| САБЛИН О.А | |||
| и др | |||
| Первичная резистентность Helicobacter pylori к антибиотикам в Санкт-Петербурге.//Экспериментальная и клиническая | |||
Авторы
Даты
2016-08-27—Публикация
2015-10-06—Подача