ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к способу функционализации поверхностей для выявления аналитов. Указанный способ функционализации поверхностей, в частности, основан на устройстве для выявления аналитов, которое можно применять для осуществления различных химических, биологических и диагностических анализов. В изобретении также предлагаются специальные полимеры, которые подходят для осуществления указанного способа функционализации поверхностей.
УРОВЕНЬ ТЕХНИКИ
Эталонным анализом в диагностике является так называемый анализ «ELISA». С использованием такого анализа можно выявлять или определять аналит в биологической жидкости. В общем, лунки планшета для микротитрования покрывают (главным образом, за счет гидрофобного взаимодействия) улавливающим элементом (например, антителом), способным специфично связываться с искомым аналитом (в частности, с антигеном). Затем в лунки микропланшета помещают раствор для тестирования, и если искомая молекула присутствует, она специфично связывается с улавливающим элементом.
Индикаторный элемент также способный связываться с искомой молекулой, добавляют в лунки. Таким индикаторным элементом может быть, например, фермент, который катализирует образование окрашенного продукта, так что такой индикаторный элемент можно оценивать количественно, используя колориметрию.
Анализ ELISA хорошо подходит для автоматизации. Однако поверхности, обычно используемые для такого анализа (из полистирола) не могут легко иммобилизовать гидрофильные молекулы, такие как отрицательно заряженные полисахариды или молекулы с низкой молекулярной массой. Также было предложено, например, конъюгировать полисахарид с полилизином, для того чтобы можно было фиксировать его на поверхности полистирола, используя способность полилизина к адсорбции (Leinonen and Frasch, Infect. Immun., 38(3): 1203-7, 1982).
Анализ ELISA также имеет ограничения, связанные с зарядом поверхности, поскольку взаимодействия обычно являются более специфичными с отрицательно заряженными поверхностями (Graves, J. Immunol. Methods, 111(2): 157-66, 1988), тогда как поверхности пластмассы являются гидрофобными.
Кроме того, стандартный анализ ELISA ограничен однопараметрическими анализами, что означает, что доступна одна часть информации в одном месте и для одного образца. В том случае, когда требуется проведение нескольких анализов на одном и том же образце, необходимо выполнять несколько анализов типа ELISA, предпочтительно в параллели, либо в обычном масштабе, либо в уменьшенном масштабе в устройстве, известном как «биочип». В настоящее время на ранке продается очень небольшое количество биочипов, и в устройства, имеющихся в настоящее время в продаже, главным образом, используют предметные стекла для микроскопии в качестве подложек. Такая подложка плохо подходит для массового применения.
С другой стороны, пластиковые подложки плохо подходят для изготовления биочипов. Обычно получают неудовлетворительное соотношение сигнал/шум при прямой адсорбции на подложке вследствие значительной неспецифичной адсорбции аналитов. Гидрофобные пластиковые поверхности также имеют недостаток, который заключается в том, что они денатурируют белки и поэтому не могут быть использованы без модификации.
Однако возможности для функционализации пластмассы за счет химической модификации полимеров, о которых идет речь, очень ограничены, так как можно вводить немногие химические группы. Кроме того, небольшое изменение в составе полимеров или даже вариации состава от партии к партии могут приводить к различиям в свойствах функционализированных подложек.
Кроме того, серьезные ограничения встречаются во время литографического изготовления биочипа, так как на такие подложки трудно наносить нанокапли воспроизводимым образом (так чтобы получить нанесения, которые были бы четко очерченными и регулярными). Наиболее часто используемый на практике способ нанесения капель, контактная литография иглами, в данном контексте является технической проблемой, так что обычно используют бесконтактный способ нанесения пьезоэлектрического типа. Однако ввиду того, что последний способ является медленным, он не очень подходит для промышленного производства.
Были предложены некоторые примеры функционализации 96-луночных пластиковых планшетов. Так плазменный способ предложен в публикации Marson, Robinson с соавторами, Glycobiology 19(2): 1537-46 (2009), для получения основанных на сахарах чипов. Такой способ связан с трудностями сохранения функциональности сахара после иммобилизации. Другой пример основа на использовании стрептавидина для покрытия пластиковых поверхностей (Gehring, Albin с соавторами, Anal. Bioanal. Chem., 5 April 2008).
В документе EP 1953555 описано устройство, содержащее пластиковую подложку, покрытую металлической пленкой, на которой иммобилизуют физиологически активное вещество и соединение для создания водородных связей.
В документе EP 2030677 описан биосенсор, содержащий подложку, покрытую металлической пленкой, с помощью которой фиксируют анионный полимер.
В таких документах не раскрыто прямое взаимодействие между полимером и пластиковой подложкой.
Поэтому все еще существует необходимость в получении устройств для выявления аналитов, которые легки в производстве, устойчивы, легки в применении и/или которые позволяют параллельно выявлять большие количества аналитов.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Изобретение, во-первых, относится к устройству для выявления аналитов, включающему в себя пластиковую подложку, покрытую, по меньшей мере, частично связывающими полимерами, фиксированными на подложке нековалентно, при этом указанные связывающие полимеры содержат полисахаридный остов, снабженный ароматическими группами и группами карбоновой кислоты.
Согласно одному варианту полисахаридный остов представляет собой остов из декстрана, молекулярная масса которого предпочтительно составляет от 15000 до 100000 и, в частности, более предпочтительно от 30000 до 60000.
Согласно одному варианту полисахаридный остов дополнительно снабжен реакционно-способными группами, при этом указанные реакционно-способные группы предпочтительно имеют форму -X-CONH-Z', где X означает неразветвленную или разветвленную, замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, в частности, X более предпочтительно означает CH2 и Z' означает группу, которая способна связываться с другой молекулой.
Согласно одному варианту группы карбоновой кислоты имеют форму -X-COOH, где X означает неразветвленную или разветвленную, замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, при этом X предпочтительно означает CH2.
Согласно одному варианту ароматические группы имеют форму -X-CONH-Z, где X означает неразветвленную или разветвленную, замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, при этом X предпочтительно означает CH2, и Z означает арильную функцию, предпочтительно содержащую от 6 до 30 атомов углерода, при этом Z предпочтительно означает необязательно замещенную бензильную функцию, такую как -CH2-Ph или -CH2-Ph-пара-OH.
Согласно одному варианту связывающие полимеры содержат:
- от 0,4 до 0,8 ароматических групп, предпочтительно от 0,4 до 0,6 ароматических групп, предпочтительно от 0,45 до 0,6 ароматических групп на единицу сахарида полисахаридного остова; и/или
- от 0 до 0,8 реакционно-способных групп, предпочтительно от 0 до 0,6 реакционно-способных групп на единицу сахарида полисахаридного остова; и/или
- от 0,5 до 1,5 ароматических групп, групп карбоновой кислоты и реакционно-способных групп в совокупности, предпочтительно от 0,9 до 1,3 ароматических групп, групп карбоновой кислоты и реакционно-способных групп в совокупности на единицу сахарида полисахаридного остова.
Согласно одному варианту подложкой является подложка из полистирола, поликарбоната, поли(метилметакрилата) или полипропилена, и предпочтительно из полистирола.
Согласно одному варианту устройство содержит улавливающие элементы, иммобилизованные на связывающих полимерах, при этом указанные улавливающие элементы предпочтительно выбраны из полипептидов, необязательно модифицированных и/или конъюгированных, сахаридов, олигосахаридов или липополисахаридов, вирусов или вирусных фрагментов и клеток, при этом улавливающие элементы предпочтительно иммобилизованы на связывающих полимерам посредством адсорбции или ковалентного связывания с реакционно-способными группами F.
Согласно одному варианту устройство содержит множество зон для выявления, при этом зоны для выявления предпочтительно содержат разные улавливающие элементы.
Согласно одному варианту подложка представляет собой непрозрачное или прозрачное предметные пластины, планшет для микротитрования, набор шариков, чашку для культуры, полоску или палочку.
Изобретение также относится к полимеру, содержащему полисахаридный остов, снабженный ароматическими группами, группами карбоновой кислоты, а также реакционно-способными группами формулы (V):
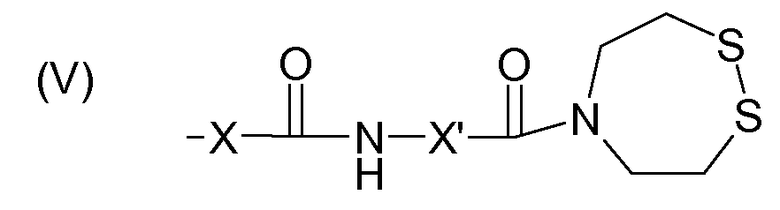 ,
,
при этом каждый из X и X' означает замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода.
Изобретение также относится к полимеру, содержащему полисахаридный остов, снабженный ароматическими группами, группами карбоновой кислоты, а также реакционно-способными группами формулы (V'):
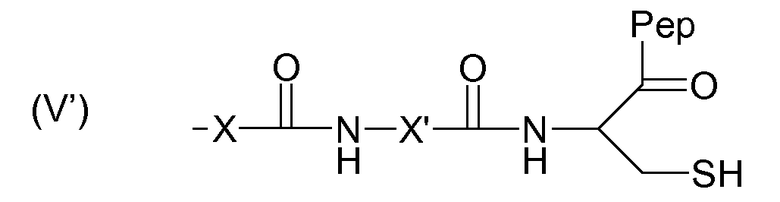 ,
,
при этом каждый и X и X' означает замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, и Pep означает пептидный фрагмент.
Согласно одному варианту в двух вышеупомянутых полимерах X означает CH2 и/или X' означает (CH2)2.
Изобретение также относится к способу производства указанного выше полимера, снабженного реакционно-способными группами формулы (V), включающему в себя:
- получение полисахарида;
- прививку групп карбоновой кислоты на полисахарид; затем
- модификацию части привитых групп карбоновой кислоты, чтобы получить ароматические группы; с последующей или предшествующей
- модификацией другой части привитых групп карбоновой кислоты, чтобы получить реакционно-способные группы формулы (V), при этом указанная модификация включает в себя взаимодействие полисахарида с соединением формулы (VII):
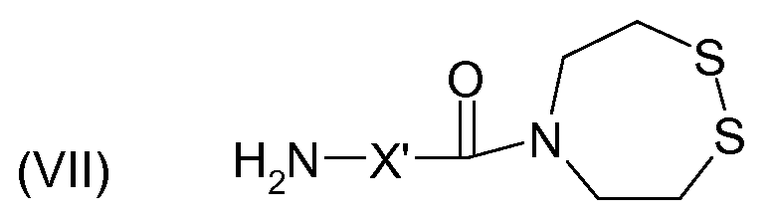 ,
,
в котором X' означает замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода.
Изобретение также относится к способу производства указанного выше полимера, снабженного реакционно-способными группами формулы (V'), включающему в себя:
- получение полимера формулы (V), указанного выше; и
- взаимодействие такого полимера с полипептидом H-Cys-Pep, где Pep означает пептидный фрагмент, и Cys означает остаток цистеина.
Согласно одному варианту описанного выше устройства связывающие полимеры представляют собой вышеупомянутые полимеры (снабженные реакционно-способными группами формулы (V) или (V')).
Изобретение также относится к применению устройства для выявления аналитов, которое описано выше, для выявления и необязательно количественного определения химических молекул, биологических молекул, клеток или живых организмов.
Изобретение также относится к способу производства устройства для выявления аналитов, которое описано выше, включающему в себя:
- получение пластиковой подложки;
- осуществление контакта подложки, по меньшей мере, с одним раствором, содержащим связывающие полимеры.
Согласно одному варианту, такой способ дополнительно включает в себя осуществление контакта подложки с одним или несколькими растворами, содержащими улавливающие элементы.
Изобретение также относится к способу производства устройства для выявления аналитов, которое описано выше, включающему в себя:
- получение пластиковой подложки;
- осуществление контакта подложки с одним или несколькими растворами, содержащими связывающие полимеры, связанные с улавливающими элементами.
Настоящее изобретение позволяет преодолеть недостатки предшествующего уровня техники. Более конкретно, изобретение относится к устройствам для выявления аналитов, которые легки в производстве, устойчивы и легки в применении. Согласно одному варианту такие устройства позволяют выявлять большое количество аналитов параллельно. В частности, изобретение позволяет иммобилизовать гидрофильные и/или небольшие молекулы (а также антитела или белки).
Такой результат достигается за счет функционализации поверхности с использованием связывающих полимеров, имеющих полисахаридный остов. Связывающие полимеры содержат ароматические группы, которые способствуют нековалентной фиксации связывающих полимеров с относительно гидрофобными поверхностями, а также группы карбоновой кислоты для отрицательного заряда связывающих полимеров, с тем, чтобы ограничить явление неспецифичной адсорбции между связывающими полимерами и выявляемыми аналитами (которые само по себе часто являются отрицательно заряженными).
Применение пластиковых и, в частности, полистироловых поверхностей в устройствах согласно изобретению позволяет избежать проблем, связанных со стеклом: риска разбить стекло и связанной с этим опасности для персонала, затрат, связанных с утилизацией отходов, гетерогенности функционализации, связанной с химической природой стекла, высокой стоимости подложки и характеризации, трудности распределения на подложке.
Согласно некоторым конкретным вариантам изобретение также обладает одним или предпочтительно несколькими преимущественными признаками, перечисленными ниже.
- Связывающие полимеры легко синтезировать в больших количествах, и они могут быть охарактеризованы обычными аналитическими способами (ЯМР, измерение pH, микроанализ), что позволяет строго контролировать производство.
- Связывающие полимеры фиксируют на поверхностях благодаря простой адсорбции (нековалентному связыванию), в частности, посредством ароматических групп связывающих полимеров. Адсорбция является способом фиксации, который особенно прост для осуществления, надежен и не очень чувствителен к умеренному варьированию физико-химических свойств поверхностей. В любом случае также можно корректировать плотность ароматических групп в связывающих полимерах в зависимости от природы поверхностей.
- Изобретение может быть осуществлено, исходя из подложек, которые в настоящее время широко доступны и стоят недорого: планшеты для микротитрования, изготовленные из полистирола, чашки Петри и т.д..
- Изобретение также может быть использовано для изготовления биочипов, т.е. миниатюрных устройств для выявления аналитов для параллельного выявления большого количества аналитов на основе пластиковых и, в частности, полистироловых подложек.
- Функционализацию поверхности согласно изобретению осуществляют благодаря фиксации улавливающих элементов (или зондов) на связывающих полимерах, либо ковалентно (посредством реакционно-способных групп, присутствующих на связывающих полимерах), в частности, когда улавливающие элементы представляют собой небольшие молекулы, либо нековалентно (посредством адсорбции). Таким образом, изобретение обеспечивает большую гибкость в применении.
- Функциональные группы преимущественно стабильны (сохраняют свои свойства) в присутствии влаги или на воздухе.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг.1 показана взаимосвязь между степенью замещения ароматическими группами (по оси y) в полимере PsAcAr1 из примера 3 и количеством эквивалентов бензиламина (по оси x). Фигура будет описана в примере 4.
На фиг.2 показана взаимосвязь между степенью замещения азидными группами (на оси y) в полимере PsAcF1 из примера 7 и количеством эквивалентов азида амина (на оси x). Фигура будет описана в примере 8.
На фиг.3 приведена гистограмма, показывающая измерения углов контактов (в градусах) на функционализированных или не функционализированных полистироловых планшетах. Фигура будет описана в примере 22.
Фиг.4, 5 и 6 иллюстрируют специфичность фиксации конканавалина A (по сравнению с другими лектинами) на полимере согласно изобретению. Фигуры будут описаны в примерах 23 и 24.
Фиг.7 представляет собой гистограмму, иллюстрирующую влияние степени ароматического замещения на угол контакта (в градусах) на функционализированных планшетах из полистирола. Фигура будет описана в примере 25.
Фиг.8 представляет собой гистограмму, иллюстрирующую хемоселективное связывание альдегида пептида с поверхностью, функционализированной полимером согласно изобретению. Фигура будет описана в примере 26.
Фиг.9 и 10 представляют собой гистограммы, показывающие функционализацию поверхностей пептидами и выявление с использованием подходящих антител (инкубация с анти-HA-антителом или анти-FLAG-антителом). Фигуры будут описаны в примере 27.
Фиг.11 представляет собой гистограмму, иллюстрирующую хемоселективное связывание пептида, несущего N-концевой цистеин, с поверхностью, функционализированной полимером согласно изобретению. Фигура будет описана в примере 33.
Фиг.12 и 13 представляют собой диаграммы, иллюстрирующие колориметрическое выявление на биочипе с антителом на дне 96-луночных планшетов из полистирола. Фигуры будут описаны в примере 34.
ОПИСАНИЕ ВАРИАНТОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Изобретение описано боле подробно в следующем далее описании, которое не является ограничивающим.
Связывающие полимеры и их производство
Связывающие полимеры, используемые в контексте изобретения, содержат полисахаридный остов (далее сокращенно «Ps»), снабженный группами карбоновой кислоты (далее сокращенно «Ac») и ароматическими группами (далее сокращенно «Ar»). Согласно одному варианту полисахаридный остов также может быть снабжен реакционно-способными группами, отличающимися от вышеупомянутых групп карбоновой кислоты (далее сокращенно «F»).
Под «полисахаридным остовом» подразумевают структуру, образованную совокупностью сахаров (или сахаридных единиц), связанных вместе O-гликозидными связями. Такая структура может быть линейной или разветвленной. Предпочтительно она содержит от 80 до 600 сахаридных единиц и, в частности, более предпочтительно от 150 до 350 сахаридных единиц.
Сахаридные единицы предпочтительно являются циклическими. Они могут быть триозами, тетрозами, пентозами, гексозами или гептозами и предпочтительно они являются гексозами.
«Уровень замещения» или «степень замещения» означает среднее количество заместителей (Ac, Ar или F) на сахаридную единицу. Способы определения степени замещения приведены в разделе «Примеры».
Все группы Ac, Ar и F предпочтительно привиты на некоторых или на всех гидроксильных функциях сахаридных единиц.
Молекулярная масса полисахаридного остова предпочтительно составляет от 15000 до 100000 и, в частности, более предпочтительно от 30000 до 60000.
Полисахаридный остов может быть гомополисахаридного типа (идентичные сахаридные единицы) или гетерополисахаридного типа (разные сахаридные единицы).
В качестве примеров гомополисахаридов можно указать: глюкозаны или глюканы (альфа-глюканы или бета-глюканы), такие как крахмал, гликоген, целлюлоза, декстран, пуллулан, гиалуроновая кислота, хитин или хитозан (деацетилированные формы хитина); арабинаны, ксиланы и пектины. В качестве примеров гетерополисахаридов можно упомянуть камеди, которые представляют собой разветвленные структуры, содержащие D-галактозу, L-арабинозу, L-рамнозу и D-глюкуроновую кислоту, а также гемицеллюлозы.
Согласно предпочтительному варианту сахаридные единицы являются единицами глюкозы (или декстрозы). Предпочтительно полисахаридный остов представляет собой молекулу декстрана, т.е. она имеет основную цепь из молекул глюкозы, связанных вместе α-1,6-гликозидными связями, необязательно с ответвлениями, связанными с главной цепью α-1,2- и/или α-1,3- и/или α-1,4-связями. Декстран доступен в больших количествах, недорого стоит и имеет хорошую растворимость в воде.
В остальной части описания будет упоминаться полисахаридный остов типа декстрана, при этом следует понимать, что такое описание аналогично применимо к другим типам полисахаридных остовов.
Связывающие полимеры согласно изобретению, которые не снабжены реакционно-способными группами F (полимеры типа «PsAcAr»), могут быть получены посредством:
- получения полисахарида Ps (незамещенный полисахаридный остов);
- прививки групп Ac на такой полисахарид так, чтобы получить полимер типа «PsAc»;
- модификации части групп Ac полимера PsAc, чтобы получить полимер PsAcAr.
Таким образом, что касается общей формулы (I), приведенной ниже:
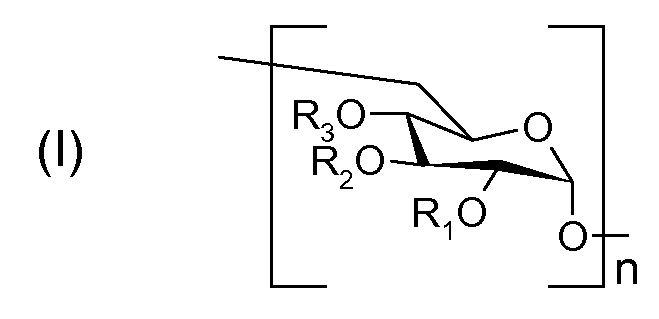
то исходный полимер Ps представляет собой полимер формулы (I), в котором все группы R1, R2 и R3 представляют собой атом водорода; промежуточный полимер PsAc представляет собой полимер формулы (I), в котором некоторые группы R1, R2 и R3 представляют собой атом водорода, а другие группы R1, R2 и R3 представляют собой группу, несущую функцию карбоновой кислоты; и связывающий полимер PsAcAr представляет собой полимер формулы (I), в котором некоторые группы R1, R2 и R3 представляют собой атом водорода, другие группы R1, R2 и R3 представляют собой группу, несущую функцию карбоновой кислоты и третья и последняя часть групп R1, R2 и R3 представляют собой группу, несущую ароматическое ядро.
Группы карбоновой кислоты Ac группы имеют форму -X-COOH, где X означает неразветвленную или разветвленную алкильную цепь, содержащую от 1 до 6 атомов углерода, необязательно снабженную одним или несколькими заместителями, выбранными из хлора, брома, кетонной группы, фтора, спиртовой группы, группы карбоновой кислоты и ароматической группы (в частности, фенила). Предпочтительно, такая цепь является линейной и незамещенной и/или содержит не более 5 атомов углерода, не более 4 атомов углерода, не более 3 атомов углерода или не более 2 атомов углерода. Согласно предпочтительному варианту, в котором исключены возможные проблемы, связанные с избыточной реакционной способностью, группы Ac имеют форму -CH2-COOH (группы метилкарбоновой кислоты).
Понятно, что группы Ac могут быть в ионизованной форме (COOH заменена на COO-, ассоциированную с противоионом) или в форме соли (COOH заменена, например, на COONa) в зависимости от контекста.
Предпочтительно все группы Ac идентичны, но также можно предусмотреть прививку разных групп Ac.
Ароматические группы Ar имеют форму -Y-Z, где Y означает связывающую группу, и Z означает арильную функцию, предпочтительно, содержащую от 6 до 30 атомов углерода, предпочтительно от 6 до 24 атомов углерода, более предпочтительно от 6 до 12 атомов углерода, и один или несколько заместителей, выбранных из галогенов, -OH, -NH2, -NO2, -OR', -COOR', -CONHR', где R' означает алкильную группу, имеющую от 1 до 6 атомов углерода. Z может быть моноциклическим или полициклическим и необязательно гетероциклическим. Z предпочтительно означает производное бензола и, в частности, фенильную, бензильную и фенольную группу.
Y предпочтительно означает амидную группу формы -X-CONH-, где X имеет такое же значение, которое указано выше в отношении групп Ac.
Согласно предпочтительному варианту группы Ar представляют собой группы -CH2-CONH-CH2-Ph (где Ph означает фенильную группу) или группы -CH2-CONH-CH2-Ph-пара-OH.
Предпочтительно все группы Ar являются идентичными, но также можно предусмотреть прививку разных групп Ar.
Стадию прививки групп Ac на полисахарид Ps, чтобы получить полимер PsAc, можно осуществлять посредством взаимодействия полисахарида Ps с соединением карбоновой кислоты, несущим функцию галогена, и предпочтительно функцию хлора.
Например, прививку предпочтительных групп Ac в форме -CH2-COOH можно получить в результате взаимодействия полисахарида Ps с монохлоруксусной кислотой. Предпочтительно, реакцию осуществляют в присутствии изопропанола.
Стадию модификации части групп Ac полимера PsAc для получения полимера PsAcAr можно осуществить в результате взаимодействия полимера PsAc с соединением типа R-Z, где Z имеете такое же значение, которое указано выше, и R означает функцию, которая способны взаимодействовать с карбоксильной функцией. Предпочтительно R означает аминную функцию, способную образовывать амидную связь с группами Ac.
Например, предпочтительные группы Ar типа -CH2-CONH-CH2-Ph могут быть получены в результате взаимодействия полисахарида PsAc с бензиламином. В качестве следующего примера, предпочтительные группы Ar типа -CH2-CONH-CH2-Ph-пара-OH могут быть получены в результате взаимодействия полисахарида PsAc с пара-гидроксибензиламином. Предпочтительно реакцию осуществляют в присутствии 1-циклогексил-3-(2-морфолиноэтил)карбодиимида.
Связывающие полимеры согласно изобретению, которые снабжены реакционно-способными группами F (полимеры типа «PsAcArF») могут быть получены, исходя из полимеров типа PsAc (таких как полученные выше), в результате модификации части групп Ac с одной стороны до групп F, и с другой стороны до групп Ar. Указанные две стадии модификации могут быть осуществлены в любом порядке.
Другими словами, первый полимер типа PsAcAr может быть получен из полимера PsAc (который описан выше), затем такой полимер типа PsAcAr может быть модифицирован, чтобы получить полимер типа PsAcArF. Также можно получить полимер типа «PsAcF» сначала из полимера PsAc и затем модифицировать такой полимер типа PsAcF, чтобы получить полимер типа PsAcArF (способ, применяемый для такой второй модификации, такой же, как способ, используемый для модификации полимера типа PsAc в полимер типа PsAcAr).
Преимущество таких различных методик заключается в том, что они позволяют модулировать степени замещения в соответствии с тем, требуется ли более высокий уровень групп Ar или более высокий уровень группы F.
Что касается общей формулы (I), приведенной ниже:
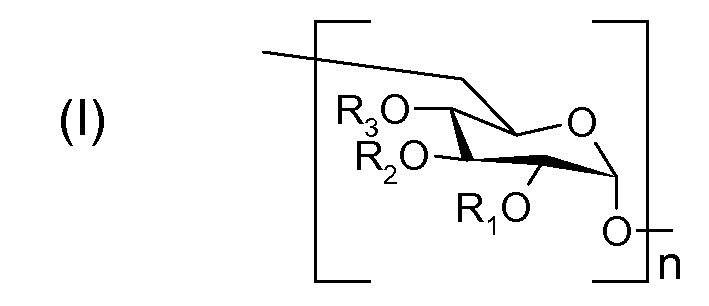
то полимер PsAcF представляет собой полимер формулы (I), в котором некоторые группы R1, R2 и R3 представляют собой атом водорода, другие группы R1, R2 и R3 представляют собой группу карбоновой кислоты, и третья и последняя часть групп R1, R2 и R3 представляют собой реакционно-способную группу (отличную от группы карбоновой кислоты); и полимер PsAcArF представляет собой полимер формулы (I), в котором некоторые группы R1, R2 и R3 представляют собой атом водорода, другие группы R1, R2 и R3 представляют собой группу карбоновой кислоты, другие группы R1, R2 и R3 представляют собой ароматическую группу, и четвертая и последняя часть групп R1, R2 и R3 представляют собой реакционно-способную группу (отличную от группы карбоновой кислоты).
Реакционно-способные группы F имеют форму -Y-Z', где Y означает связывающую группу (имеющую такое же значение, которое указано выше), и Z' означает группу, которая способна связываться, в частности, ковалентно, с улавливающим элементом, который более подробно описан ниже. Согласно предпочтительному варианту группа Z' способна образовывать ковалентную связь с полипептидом.
Y предпочтительно представляет собой амидную группу формы -X-CONH-, где X имеет такое же значение, которое указано выше в отношении групп Ac (и X предпочтительно означает CH2).
Согласно первому предпочтительному варианту группы Z' являются азидными группами (и, в частности, алкилазидами), и группы F предпочтительно являются группами формы -X-CONH-X'-N3, где каждый из X и X' означает замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, следовательно группы F могут представлять собой, например, группы -CH2-CONH-(CH2)3-N3. Такие группы особенно применимы в качестве промежуточных групп, позволяющих получать, например, группы типа триазола (смотри третий вариант ниже). Они также могут связываться с некоторыми улавливающими элементами.
Согласно второму предпочтительному варианту группы Z' представляют собой группы гидразида, и группы F предпочтительно являются группами формы -X-CONH-NH2, где X означает замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, следовательно, группы F могут представлять собой, например, группы -CH2-CONH-NH2. Такие группы F способны связываться, например, с альдегидной функцией пептидов. Они также могут способствовать адсорбции полипептидов (нековалентной иммобилизации).
Согласно третьему предпочтительному варианту группы Z' представляют собой группы триазола, предпочтительно замещенные одним или несколькими неразветвленными или разветвленными, замещенными или незамещенными алкильными цепями, содержащими от 1 до 6 атомов углерода, и, следовательно, группы F могут представлять собой, например, группы формулы (II):
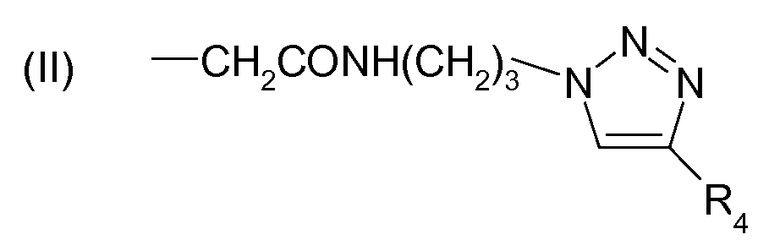 ,
,
в которой R4 означает группу формулы (III):
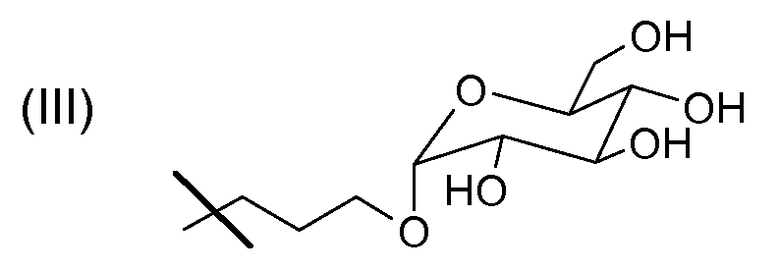
Группы F такого типа могут связывать некоторые конкретные улавливающие элементы. Группы F группы формулы (II), указанной выше, где R4 означает -(CH2)3OH, используют в качестве негативных контролей в примерах.
Согласно четвертому предпочтительному варианту группы Z' имеют следующую формулу (IV):
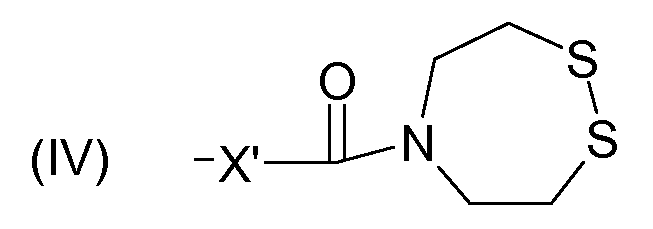 ,
,
в которой X' означает неразветвленную или разветвленную алкильную цепь, содержащую от 1 до 6 атомов углерода, необязательно снабженную заместителями типа галогена (в частности Cl или Br). Предпочтительно X' означает (CH2)2. Следовательно, согласно указанному четвертому варианту группы F предпочтительно имеют следующую формулу (V):
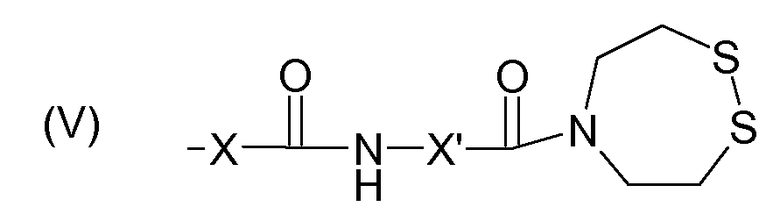 ,
,
в которой X и X' имеют значение, указанное выше. Согласно особенно предпочтительному варианту X означает CH2 и X' означает (CH2)2.
Группы F, соответствующие указанному четвертому варианту, могут взаимодействовать с молекулами, несущими бета-аминотиольную или гамма-аминотиольную функцию, например, полипептидами, имеющими цистеин или гомоцистеин в N-концевом положении, с образованием амидной связи. Таким образом, связывающие полимеры, соответствующие указанному четвертому варианту, могут связываться с улавливающими элементами, образованными полипептидами, имеющими цистеин или гомоцистеин в N-концевом положении.
Таким образом, в случае цистеина получают связывающий полимер, в котором группы F связывающиеся с улавливающими элементами, имеют формулу (V'):
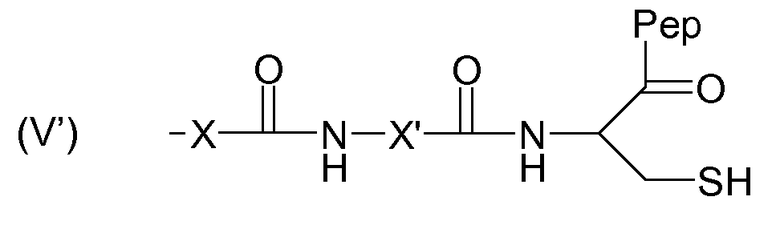 ,
,
при этом X и X' имеют указанное выше значение, и Pep означает фрагмент пептида, т.е. часть полипептида, содержащую, по меньшей мере, один аминокислотный остаток (предпочтительно последовательность нескольких аминокислотных остатков), с C-концевой функцией (например, COOH или CONH2).
Все группы F группы могут быт идентичными, или в ином случае может быть предусмотрена прививка разных групп F.
Стадию модификации части групп Ac полимера PsAc (соответственно и полимера PsAcAr) для получения полимера PsAcF (соответственно и полимера PsAcArF) можно осуществлять за счет взаимодействия полимера PsAc (соответственно полимера PsAcAr) с соединением типа R-Z', где Z' имеет такое же значение, которое указано выше, и R означает функцию, которая взаимодействует с карбоксильной функцией. Предпочтительно R означает аминную функцию, способную образовывать амидную связь с группами Ac.
Некоторые группы F могут быть привиты в результате прививки сначала промежуточных реакционно-способных групп F', а затем химической модификации групп F' с получение групп F после осуществления отдельной стадии взаимодействия.
Например, группы F типа -CH2-CONH-NH2 могут быть получены в результате взаимодействия полисахарида PsAc (или полимера PsAcAr) с гидразином (предпочтительно в присутствии 1-циклогексил-3-(2-морфолиноэтил)карбодиимида.
Группы F типа -CH2-CONH-(CH2)3-N3 могут быть получены в результате взаимодействия полисахарида PsAc (или полимера PsAcAr) с гидрохлоридом 3-азидопропиламмония (предпочтительно в присутствии 1-циклогексил-3-(2-морфолиноэтил)карбодиимида).
Группы F формулы (II), указанной выше, могут быть получены в результате взаимодействия полимера PsAcF (или полимера PsAcArF), снабженного реакционно-способными группам типа -CH2-CONH-(CH2)3-N3, с соединением формулы (VI):
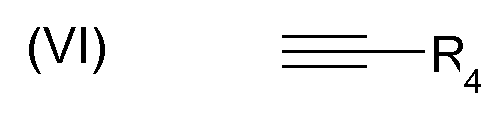
(предпочтительно в присутствии ионов меди(II) и аскорбата натрия).
В таком случае получают полимер PsAcF (или полимер PsAcArF), в котором либо все группы F имеют формулу (II), приведенную выше, либо часть групп F имеют формулу (II), приведенную выше, а часть групп F являются группами типа -CH2-CONH-(CH2)3-N3 (в случае неполного замещения соединениями формулы (VI)).
Группы F формулы (V), приведенной выше, могут быть получены в результате взаимодействия полисахарида PsAc (или полимера PsAcAr) с соединением формулы (VII):
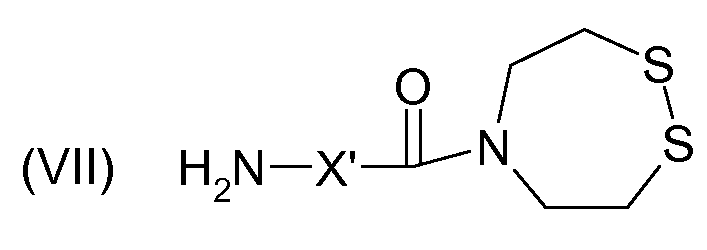
(предпочтительно в присутствии 1-циклогексил-3-(2-морфолиноэтил)карбодиимида), в которой X' имеет значение, указанное выше. Соединение формулы (VII) может быть получено, как указано в примерах ниже.
В общем, степень замещения группами Ac, Ar и F можно корректировать в зависимости, с одной стороны, от порядка, в котором осуществляют прививку групп (Ac, затем Ar, затем F или в другом случае Ac, затем F, затем Ar), и с другой стороны, от подбора условий прививки и, в частности, от молярного соотношения между полисахаридом и реагентом, ответственным за прививку соответствующей группы.
Полимеры, полученные из декстранов и соответствующие общей формуле связывающих полимеров, приведенной выше, с сульфатными и сульфонатными группами в качестве реакционно-способных групп F, а также применение таких полимеров для терапевтических целей, описаны в документах WO 99/29734, WO 00/76452, WO 00/76562, WO 01/91742 и FR 2891149.
Предпочтительно связывающие полимеры согласно изобретению не имеют сульфатных или сульфонатных функций. Действительно, такие функции могут взаимодействовать с большим количеством белков, которые вредны для оптимального выявления. Кроме того, отсутствие сульфатных или сульфонатных функций особенно полезно, когда улавливающие элементы сами являются сульфатированными (в частности, олигосахариды).
Функционализация поверхностей
Связывающие полимеры согласно изобретению (типа PsAcAr или PsAcArF) могут быть нанесены на подложку, чтобы функционализировать поверхность указанной подложки. Подложка состоит из пластика (твердого материала полимерной природы, которому обычно придают форму в горячем виде и под давлением), который предпочтительно выбран из полистирола, поликарбоната, поли(метилметакрилата) и полипропилена.
Таким образом, изобретение позволяет, например, функционализировать поверхность прозрачных или непрозрачных пластиковых пластин или в ином случае полистироловых планшетов для микротитрования (например, 96-луночных), шариков (магнитных или немагнитных), планшетов для культивирования из полистирола (например, 96-луночных), полосок или палочек ил полистирола.
Функционализация обычно включает в себя две стадии: первую стадию фиксации связывающих полимеров на поверхности подложки и вторую стадию фиксации улавливающих элементов на связывающих полимерах. Альтернативно связывающие полимеры могут быть связаны с улавливающими элементами перед фиксацией связывающих полимеров на поверхности подложки (особенно, когда связь между связывающими полимерами и улавливающими элементами является связью ковалентного типа).
Фиксацию связывающих полимеров на поверхности подложки осуществляют, в частности, в случае плоских поверхностей, погружением поверхности, которую необходимо обработать, в раствор, содержащий полимер PsAcAr или PsAcArF. В случае формованных поверхностей, которые могут содержать жидкость (например, 96-луночных планшетов для титрования), функционализация может быть осуществлена простым заполнением. Обычно предусмотрена последующая промывка и сушка. В общем, раствор полимера имеет концентрацию от 0,1 до 50 мкг/мл, и предпочтительно от 1 до 10 мкг/мл.
Не имея намерения быть связанными с какой-либо теорией, авторы изобретения полагают, что связывающие полимеры фиксируются нековалентно на поверхности подложки (адсорбция), в частности, посредством групп Ar.
Улавливающие элементы, фиксированные на связывающих полимерах, могут представлять собой полипептиды, необязательно модифицированные и/или конъюгированные, сахариды, олигосахариды или липополисахариды, вирусы или вирусные фрагменты или даже клетки. Например, улавливающими элементами могут быть антитела.
Термин «полипептид» в контексте настоящей заявки охватывает любую цепь из аминокислотных остатков (в количестве больше или равном двум), связанных пептидными связями. Следовательно, «полипептидами» в используемом в настоящее описании смысле могут быть, например, олигопептиды, пептиды или белки согласно общепринятым значениям таких терминов. Аминокислотные остатки, присутствующие в полипептидах согласно изобретению, могут быть выбраны из протеиногенных или непротеиногенных аминокислотных остатков. Предпочтительно, они выбраны из двадцати протеиногенных аминокислотных остатков.
Фиксация улавливающих элементов на связывающих полимерах может происходить за счет адсорбции, если используют связывающие полимеры без реакционно-способных групп F. Фиксация также происходит за счет образования ковалентных связей с реакционно-способными группами F. Фиксация также может быть осуществлена за счет адсорбции, которой способствуют реакционно-способные группы F. Такая фиксация происходит, например, в случае адсорбции антител, которой способствуют группы типа гидразида.
Также могут быть предусмотрены улавливающие элементы, содержащие несколько частей. Например, можно использовать промежуточный улавливающий элемент (например, полипептид или соединение сахарида или гликопептид), который может быть фиксирован на связывающих полимерах, и конечный улавливающий элемент (например, вирус или вирусный фрагмент или клетку), который может связываться с промежуточным улавливающим элементом.
Когда устройство для выявления аналитов предназначено только для выявления одного аналита (или аналитов одного типа), достаточно нанести связывающие полимеры (и улавливающий элемент или элементы) на всю используемую поверхность подложки.
Когда устройство для выявления аналитов предназначено для выявления нескольких аналитов с разными улавливающими элементами, необходимо обеспечить несколько отдельных зон для выявления. 96-луночный планшет для микротитрования является примером подложки, которая особенно применима для такой цели.
В данном случае либо связывающие полимеры могут быть нанесены на всю используемую поверхность подложки, и затем различные улавливающие элементы могут быть нанесены на ограниченные зоны подложки (например, посредством нанесения небольших капелек различных растворов, содержащих улавливающие элементы, на определенные участки подложки); либо различные растворы связывающих полимеров, связанных с улавливающими элементами, могут быть нанесены непосредственно на ограниченные зоны подложки (например, в лунки планшета для микротитрования); либо один или несколько растворов связывающих полимеров могут быть нанесены непосредственно на ограниченные зоны подложки (например, в лунки планшета для микротитрования) и затем различные растворы, содержащие улавливающие элементы, могут быть нанесены на те же самые ограниченные зоны подложки.
Зоны на поверхности подложки, покрытые связывающими полимерами, предпочтительно являются гидрофильными, характеризуемыми углом контакта воды меньше или равным 70°, предпочтительно меньше или равным 65° и оптимально меньше или равным 60°. Гидрофильность поверхности подложки, покрытой связывающими полимерами позволяет минимизировать неспецифичные взаимодействия большого количества аналитов (в частности, белков) с подложкой. Она также позволяет наносить нанокапли для получения биочипов, в то время как такой тип нанесения является сложным и плохо воспроизводимым, когда его осуществляют непосредственно на необработанные пластиковые подложки.
Аналиты, которые можно выявлять с применением изобретения, могут представлять собой все виды химических и биологических материалов: минеральные частицы, органические молекулы (в частности, пестициды или другие загрязняющие вещества), биомолекулы (в частности, соединения сахаридов, полипептиды, модифицированные или не модифицированные, конъюгированные или не конъюгированные), вирусы или фрагменты вирусов, клетки или организмы (одноклеточные или многоклеточные).
В частности, изобретение позволяет производить чипы с полипептидами, применимые для серотипирования, скрининга эпитопов, количественной оценки белков в биологических средах или других анализов соотношений между пептидными молекулами типа лиганд-рецептор.
В общем, применение детекторных устройств согласно изобретению заключается в осуществлении контакта поверхности подложки, покрытой связывающими полимерами и улавливающими элементами, с одним или несколькими растворами или суспензиями, которые могут содержать представляющие интерес аналиты (например, образцом воды из окружающей среды, образцом продукта питания, биологическим образцом, таким как моча, кровь или полученный из крови продукт и т.д.).
Выявление аналитов, которые вероятно специфично фиксированы на улавливающих элементах, можно осуществлять с помощью индикаторных элементов, которые могут быть, например, флуоресцентными, радиоактивными или химически мечеными и могут связываться с аналитами, удерживаемыми на устройстве согласно изобретению, или могут взаимодействовать с ними другим образом. Затем, индикаторные элементы, удерживаемые на устройстве согласно изобретению, могут быть идентифицированы и необязательно подвергнуты количественной оценке с применением устройства для регистрации флуоресценции, колориметрической детекции или регистрации радиоактивности.
Также возможно регистрация, основанная на изменении среды (например, окраски, видимой невооруженным глазом) благодаря химической реакции между индикаторным элементом и аналитом или в ином случае между индикаторным элементом (фиксированном на аналите) и дополнительным реагентом.
В качестве иллюстрации индикаторный элемент может содержать фермент, который катализирует образование окрашенного продукта. Он также может содержать шарики, покрытые молекулами, которые могут связываться с удерживаемыми аналитами. Также можно использовать меченые антитела (флуоресцирующие или радиоактивные), которые могут связываться с антигенами, присутствующими на аналитах.
Выявление и необязательно количественная оценка аналитов, которые возможны благодаря изобретению, в частности, применимы для медицинской диагностики (в медицине или ветеринарии).
ПРИМЕРЫ
Следующие примеры иллюстрируют, но не ограничивают изобретение. В примерах, приведенных ниже получают различные полимеры с полисахаридным остовом из декстрана:
- полимер PsAc1, который содержит группы Ac типа -CH2COONa;
- полимер PsAcAr1, который содержит группы Ac типа -CH2COONa и группы Ar типа -CH2CONHCH2Ph;
- полимер PsAcF1, который содержит Ac группы типа -CH2COONa и группы F типа -CH2CONH(CH2)3N3;
- полимер PsAcArF1 который содержит группы Ac типа -CH2COONa, группы Ar типа -CH2CONHCH2Ph и группы F типа -CH2CONHNH2;
- полимер PsAcArF2, который содержит группы Ac типа -CH2COONa, группы Ar типа -CH2CONHCH2Ph и группы F типа -CH2CONH(CH2)3N3;
- полимер PsAcF2, который содержит группы Ac типа -CH2COONa и группы F формулы (II), приведенной выше, где R4 означает -(CH2)3OH;
- полимер PsAcF3, который содержит группы Ac типа -CH2COONa и группы F формулы (II), приведенной выше, где R4 имеет формулу (III), приведенную выше;
- полимер PsAcArF3, который содержит группы Ac типа -CH2COONa, группы Ar типа -CH2CONHCH2Ph и группы F группы формулы (II), приведенной выше, где R4 означает -(CH2)3OH;
- полимер PsAcArF4, который содержит группы Ac типа -CH2COONa, группы Ar типа -CH2CONHCH2Ph и группы F формулы (II), приведенной выше, где R4 имеет формулу (III), приведенную выше;
- полимер PsAcArF5, который содержит группы Ac типа -CH2COONa, группы Ar типа -CH2CONHCH2Ph и группы F формулы (V), приведенной выше, где X означает CH2 и X' означает (CH2)2.
Форма PsAc (x) означает полимер, имеющий степень замещения группами Ac, равную x.
Форма PsAcAr (x; y) означает полимер, имеющий общую степень замещения группами Ac и Ar, равную x, и степень замещения группами Ar, равную y.
Форма PsAcF (x; z) означает полимер, имеющий общую степень замещения группами Ac и F, равную x, и степень замещения группами F, равную z.
Форма PsAcArF (x; y; z) означает полимер, имеющий общую степень замещения группами Ac, Ar и F, равную x, степень замещения группами Ar, равную y, и степень замещения группами F, равную z.
Пример 1 - Получение полимера PsAc1 (общий протокол)
Декстран T40 (2 г, 11,1 ммоль, 1 эквивалент) растворяют в 6,4 мл деионизованной воды. К полученному раствору медленно добавляют изопропанол (36 мл) при очень энергичном перемешивании, затем карбонат натрия (2,4 г, 60 ммоль, 5,4 эквивалента), и реакционную смесь перемешивают в течение 1 часа при 60°C. Наконец добавляют монохлоруксусную кислоту (3 г, 31,7 ммоль), затем перемешивают в течение ночи при 60°C. Полученную белую пасту извлекают и три раза осаждают из метанола и центрифугируют. Полученное твердое вещество растворяют в деионизованной воде и подвергают лиофилизации, получая полимер PsAc1. Обычно такой протокол дает степень замещения группами Ac от 1,2 до 1,4.
Пример 2 - Измерение степени замещения группами карбоновой кислоты
Определение степени замещения метилкарбоксилатными группами осуществляют, используя 1H-ЯМР после гидролиза.
С этой целью продукт гидролизуют следующим образом:
Полимер PsAc1 (200 мг) растворяют в 2 мл D2O, затем медленно добавляют 666 мкл D2SO4. Реакционную смесь нагревают при 90°C в течение 4 часов. Смесь анализируют, используя 1H-ЯМР, 300 МГц.
Степень замещения (СЗ) вычисляют из следующего уравнения: СЗ = A/B, где A: (1/2) × интегральная интенсивность сигналов протонов CH2CO2H при 4 - 4,5 м.д.; и B: интегральная интенсивность протонов при атомах углерода C1 единиц глюкозы, или (1/6) × интегральная интенсивность протонов при атомах углерода C2-6 при 3 - 4 м.д.
Пример 3 - Получение полимера PsAcAr1
100 мг PsAc1 (1,1) растворяют в 2 мл деионизованной воды, затем pH доводят до 4,74, используя 1н раствор HCl. Добавляют 1-циклогексил-3-(2-морфолиноэтил)карбодиимид (CMC) (233 мг, 0,55 ммоль, 1,1 эквивалента), затем pH снова доводят до 4,74, используя 1н раствор HCl. Добавляют бензиламин и реакционную смесь перемешивают в течение ночи при температуре окружающей среды. Затем образцы диализуют в течение 70 часов в 2M растворе NaCl и затем в течение 100 часов в деионизованной воде, получая полимер PsAcAr1.
Пример 4 - Измерение степени замещения ароматическими группами
Степень замещения ароматическими группами вычисляют на основании спектра 1H-ЯМР, 300 МГц, используя следующее уравнение: СЗ=(B/A)/5, где A: интегральная интенсивность сигнала протонов при C1; B: интегральная интенсивность сигнала ароматических протонов фенильной группы.
Фиг.1 иллюстрирует взаимосвязь между степенью замещения (y) группой CH2CONHCH2Ph и количеством эквивалентов (экв.) бензиламина, используемого в реакции (0,3 экв., 0,6 экв., 1 экв., 2 экв., 5 экв. и 15 экв. относительно степени замещения доступными карбоксильными группами).
Пример 5 - Синтез 2-(3-азидопропил)изоиндол-1,3-диона
N-(3-бромпропил)фталимид (15 г, 56,02 ммоль) растворяют в 200 мл диметилформамида, затем добавляют нитрид натрия (7,25 г, 112,05 ммоль, 2 эквивалента). Перемешивание осуществляют в течение 2 часов при 70°C. Затем реакционную смесь упаривают досуха и затем упаривают совместно с толуолом, чтобы удалить следы диметилформамида. Полученный остаток растворяют в диэтиловом эфире (150 мл), и органическую фазу промывают водой (2×150 мл). Органическую фазу сушат над безводным сульфатом магния. Растворитель выпаривают, получая 2-(3-азидопропил)изоиндол-1,3-дион в форме белого порошка (12,44 г, 54,1 ммоль, 97%).
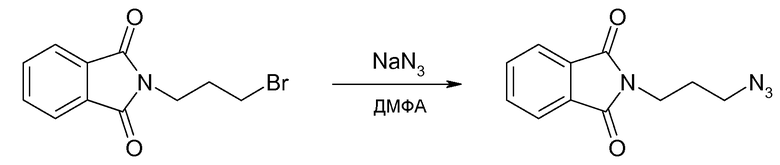
1H ЯМР (CDCl3, 300 МГц): δ м.д. 7,78 (м, 2H), 7,65 (м, 2H), 3,72 (т, 2H, J=6,9 Гц), 3,31 (т, 2H, J=6,9 Гц), 1,90 (тт, 2H, J=6,9 Гц).
13C ЯМР (75 МГц CDCl3): δ м.д. 168,28, 134,04, 131,96, 123,31, 49,0, 35,35, 28,0; MALDI-TOF: Mвычисленная=230,08 (C11H10N4O2), найдено (m/z) 231,1 [M+H]+, 253,1 [M+Na]+.
Пример 6 - Синтез 3-азидопропиламина
2-(3-азидопропил)изоиндол-1,3-дион (3 г, 12 ммоль) растворяют в 10 мл дихлорметана, затем добавляют гидразин (9,6 мл, 32 ммоль, 2,6 эквивалента). Реакционную смесь кипятят с обратным холодильником в течение ночи при перемешивании. Затем добавляют 1н водный раствор хлористоводородной кислоты (100 мл). Органическую фазу декантируют и затем водную фазу промывают дихлорметаном (3×50 мл). pH водной фазы доводят до 14, используя насыщенный раствор карбоната натрия. Затем водную фазу экстрагируют дихлорметаном (3×40 мл). Фазы в дихлорметане объединяют и экстрагируют 1н водным раствором хлористоводородной кислоты (3×50 мл). Наконец кислый водный раствор замораживают и подвергают лиофилизации. Гидрохлорид 3-азидопропиламмония получают в форме белого порошка (1,49 г, 10,97 ммоль, 84%).
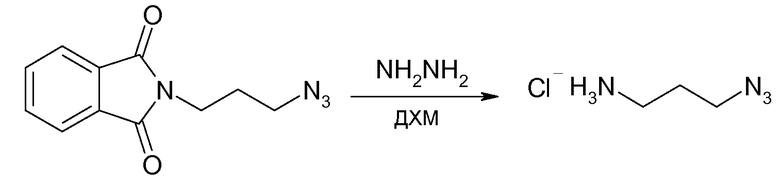
1H ЯМР (D2O, 300 МГц): δ м.д. 3,52 (т, 2H, J=6,6 Гц), 3,11 (т, 2H, J=7,2 Гц), 1,96 (тт, 2H, J=6,6 Гц).
13C ЯМР (D2O, 75 МГц): δ м.д. 39,02, 26,48, 15,67.
MALDI-TOF: Mвычисленная=100,07 (C3H8N4): найдено m/z 101,0 [M+H]+, 123,0 [M+Na]+, 139,0 [M+K]+, 107,1 [M+Li]+.
Пример 7 - Получение полимера PsAcF1
100 мг PsAc1 (1,4) растворяют в 2 мл деионизованной воды, затем pH доводят до 4,74, используя 1н раствор HCl. Затем добавляют 1-циклогексил-3-(2-морфолиноэтил)карбодиимид (CMC) (296,5 мг, 0,7 ммоль, 1,1 эквивалента) и pH снова доводят до 4,74, используя 1н раствор HCl. Добавляют 3-азидопропиламин в форме гидрохлорида, затем pH доводят до 8,4. Реакционную смесь перемешивают в течение ночи при температуре окружающей среды. Затем образцы диализуют в течение 70 часов в 2M растворе NaCl и затем в течение 100 часов в деионизованной воде. Наконец, продукт PsAcF1, полученный таким образом, замораживают и подвергают лиофилизации.
Пример 8 - Измерение степени замещения реакционно-способными группами
Степень замещения азидными группами вычисляют, используя следующее уравнение: СЗ=(B/A)/2, где A: интегральная интенсивность сигналов протонов при атомах углерода C1; B: интегральная интенсивность сигналов протонов в сильном поле (вследствие сигналов протонов 3-азидопропиламина).
Фиг.2 иллюстрирует взаимосвязь между степенью замещения азидными группами (y) и количеством эквивалентов (экв.) 3-азидопропиламина, используемого в реакции, относительно степени замещения доступными карбоксильными группами.
Пример 9 - Получение полимера PsAc1 (1,15)
90 мл изопропанола добавляют по каплям при энергичном перемешивании к раствору 5 г (27,7 ммоль, 1 эквивалента) декстрана T40, растворенного в 16 мл воды. Добавляют 6 г (150 ммоль, 5,4 эквивалента) карбоната натрия к реакционной смеси, которую затем перемешивают при 60°C в течение 1 часа.
Затем к полученной смеси добавляют 7,5 г (79,36 ммоль, 2,8 эквивалента) монохлоруксусной кислоты. Затем смесь перемешивают при 60°C в течение ночи. Получают беловатую пасту, которую растворяют в 50 мл воды. Затем продукт преципитируют из 500 мл MeOH, охлажденного до 0°C, при энергичном перемешивании. Осадки, полученные после центрифугирования (2500 об./мин, 10 минут, 4°C), растворяют в минимальном количестве воды и продукт преципитируют второй раз из 500 мл MeOH. Осадки, полученные после второй преципитации, дважды промывают MeOH и затем растворяют в минимальном количестве воды и подвергают лиофилизации. Получают 3 г (15,7 ммоль) PsAc1 со степенью замещения 1,15, т.е. PsAc1 (1,15).
Пример 10 - Получение полимера PsAcAr1 (1,15; 0,64)
Значение pH раствора, содержащего 468 мг (2,44 ммоль, 1 эквивалент) PsAc1 (1,15), растворенного в 9,4 мл воды, доводят до 4,74 добавлением 1н и 0,1н HCl. К полученному раствору добавляют 1,187 г (2,806 ммоль) CMC, pH снова доводят до 4,74. Затем к реакционной смеси добавляют 266 мкл (2,44 ммоль, 1 эквивалент относительно x) бензиламина, и смесь перемешивают, используя магнитную мешалку, в течение ночи при температуре окружающей среды. Конечное значение pH раствора составляет 10,2.
Затем реакционную смесь помещают в диализную трубку (3500 г/моль; 1 мл/см), которую погружают в 3,5 л 2M раствора NaCl, где ее оставляют на 5 суток, и затем в 3,5 л воды, в которой она остается также на 5 суток.
Затем содержимое мешка помещают в чашу для заморозки и затем подвергают лиофилизации. Получают 477 мг (1,67 ммоль) PsAcAr1 (1,15; 0,64) (степень замещения бензиламиногруппами 0,64).
Пример 11 - Получение полимера PsAcArF1 (1,15; 0,64; 0,26)
Значение pH раствора, содержащего 256 мг (0,895 ммоль, 1 эквивалент) PsAcAr1 (1,15; 0,64), растворенного в 2 мл воды, доводят до 4,74 добавлением 1н и 0,1н HCl. К полученному раствору добавляют 212,5 мг (0,502 ммоль) CMC, pH снова доводят до 4,74. Затем к реакционной смеси добавляют 870 мкл (4,56 ммоль) раствора гидразина в концентрации 24-26% в воде, и смесь перемешивают, используя магнитную мешалку, в течение ночи при температуре окружающей среды. Конечное значение pH раствора составляет 10,28.
Затем реакционную смесь помещают в диализную трубку (3500 г/моль; 1 мл/см), которую погружают в 3,5 л 2M раствора NaCl, где ее оставляют на 5 суток, и затем в 3,5 л воды, где ее оставляют также на 5 суток.
Содержимое мешка затем помешают в чашу для заморозки и затем подвергают лиофилизации. Таким образом получают 235 мг (0,81 ммоль) PsAcArF1 (1,15; 0,64; 0,26) (степень замещения гидразидом 0,26).
Пример 12 - Получение полимера PsAcAr1 (1,2; 0,49)
Значение pH раствора, содержащего 513,3 мг PsAc1 (1,2), растворенного в 10 мл деионизованной воды, доводят до 4,74, используя 1н раствор хлористоводородной кислоты. Добавляют метилсульфонат N-циклогексил-N'-(2-морфолиноэтил)карбодиимида (931,85 мг, 2,2 ммоль, 1,1 эквивалента) при температуре окружающей среды, затем pH раствора доводят до 4,74 таким же образом. Затем по каплям добавляют бензиламин (428,6 мг, 4,0 ммоль, 2 экв.) и раствор перемешивают при температуре окружающей среды в течение 16 часов. Реакционную смесь очищают диализом в 2M растворе NaCl в течение 3 суток, затем в деионизованной воде в течение 3 суток. После лиофилизации получают PsAcAr1 (1,2; 0,49) в форме аморфного белого порошка (степень замещения бензиламиногруппами 0,49).
1H ЯМР (D2O, 300 МГц): δ (м.д.): 7,21 (с, ls, Har), 5,09 (с, ls, Hano), 4,89 (с, ls, Hano), 4,53-3,39 (м, ls).
Пример 13 - Получение полимера PsAcF1 (1,2; 0,38)
513,3 мг PsAc1 (1,2) растворяют в 10 мл деионизованной воды. Значение pH раствора доводят до 4,74, используя 1н раствор HCl. К раствору добавляют метилсульфонат N-циклогексил-N'-(2-морфолиноэтил)карбодиимида (931,85 мг, 2,2 ммоль, 1,1 экв.) и pH сова доводят до 4,74. К реакционной смеси добавляют гидрохлорид 3-азидопропиламмония (819,5 мг, 6 ммоль, 3 экв.), затем pH доводят до 8,4 1н раствором Na2CO3. Реакционную смесь перемешивают при температуре окружающей среды в течение 16 часов. Сырой продукт диализуют в течение 3 суток в 2M растворе NaCl и затем в течение 3 суток в деионизованной воде. Лиофилизация дает PsAcF1 (1,2; 0,38) в форме аморфного белого порошка (степень замещения азидогруппами 0,38).
1H ЯМР (D2O, 300 MHz): δ (м.д.): 5,07 (с, ls, Hano), 4,88 (с, ls, Hano), 4,28-3,26 (м, ls), 1,77 (с, ls, CH2).
Пример 14 - Получение полимера PsAcArF2 (1,2; 0,34; 0,38)
Раствор, содержащий 272,2 мг PsAcF1 (1,2; 0,38), растворенного в 5 мл деионизованной воды, доводят до pH 4,74 с 1н раствором HCl. Добавляют метилсульфонат N-циклогексил-N'-(2-морфолиноэтил)карбодиимида (372,8 мг, 0,88 ммоль, 1,1 экв.) и pH реакционной смеси сова доводят до 4,74, используя 1н раствор HCl. Добавляют бензиламин (171,4 мг, 4,6 ммоль, 2 экв.) и раствор перемешивают при температуре окружающей среды в течение 18 часов. Диализ в 2н NaCl в течение 3 суток, затем в деионизованной воде в течение 3 суток с последующей лиофилизацией дает соединение PsAcArF2 (1,2; 0,34; 0,38) (степень замещения бензиламиногруппами 0,34).
1H ЯМР (D2O, 300 МГц): δ (м.д.): 7,23 (с, ls, Har), 5,05 (с, ls, Hano), 4,84 (с, ls, Hano), 4,33-3,26 (м, ls), 1,68 (с, ls, CH2).
Пример 15 - Получение полимера PsAcArF2 (1,2; 0,49; 0,62)
Метилсульфонат N-циклогексил-N'-(2-морфолиноэтил)карбодиимида (372,7 мг, 0,88 ммоль, 1,1 экв.) добавляют к раствору, содержащему 224,2 мг PsAcAr1 (1,2; 0,49) в 5 мл деионизованной воды при pH4,74. Значение pH раствора доводят до 4,74 1н раствором HCl и затем добавляют гидрохлорид 3-азидопропиламмония (327,8 мг, 2,4 ммоль, 3 экв.). Значение pH доводят до 8,4, затем раствор перемешивают при температуре окружающей среды в течение 17 часов. Диализ в 2н NaCl в течение 3 суток, затем в деионизованной воде в течение 3 суток и наконец лиофилизация дают полимер PsAcArF2 (1,2; 0,49; 0,62) (степень замещения азидными группами 0,62).
1H ЯМР (D2O, 300 МГц): δ (м.д.): 7,23 (с, ls, Har), 5,05 (с, ls, Hano), 4,84 (с, ls, Hano), 4,33-3,26 (м, ls), 1,68 (с, ls, CH2).
Пример 16 - Синтез пент-4-инил-α-D-глюкопиранозида
Продукт формулы (VIII) синтезируют как описано ниже:
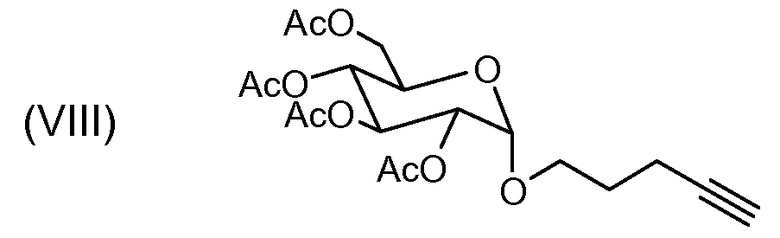
D-(+)-глюкозу (360,3 мг, 2,0 ммоль) растворяют в 4-пентин-1-оле (1,01 г, 12,0 ммоль, 6,0 экв.) и раствор нагревают до 65°C. Добавляют 120 мг H2SO4-SiO2 и раствор перемешивают при 65°C в течение 10 часов. Раствор охлаждают до температуры окружающей среды и затем соединение очищают хроматографией на силикагеле, используя градиент от CH2Cl2 до CH2Cl2-MeOH, 9:1, в качестве смеси элюентов. Требуемый продукт получают в форме бесцветного масла с выходом 79% и соотношением аномеров α/β 1,6/1. Остаток (405,0 мг, 1,63 ммоль) растворяют в пиридине (5 мл) и уксусном ангидриде (1,33 г, 13,0 ммоль, 8 экв.) при температуре окружающей среды.
Затем добавляют DMAP (20 мг) при 0°C и реакционную смесь перемешивают при температуре окружающей среды в течение 5 часов. Реакционную смесь нейтрализуют, добавляя по каплям 5 мл MeOH при 0°C. Растворители удаляют при пониженном давлении на роторном испарителе и остаточные растворители 3 раза выпаривают совместно с толуолом. Очитка хроматографией на силикагеле с использованием смеси элюентов пентан-EtOAc (8/2) дает 190 мг белых кристаллов требуемого тетрацетилированного продукта в α-конформации, а также 450 мг смеси двух аномеров, что соответствует общему выходу 98%:
1H ЯМР (D2O, 300 МГц): δ (м.д.): 5,47 (дд, 1H, J=10,0, 9,6 Гц), 5,06 (м, 2H), 4,87 (дд, 1H, J=10,2, 3,7 Гц), 4,27 (дд, 1H, J=12,3, 4,3 Гц), 4,07 (м, 2H), 3,85 (дт, 1H, J=9,9, 5,9 Гц), 3,54 (дт, 1H, J=9,9, 6,1 Гц), 2,34 (дт, 2H, 1H, J=6,8, 2,7 Гц), 2,10 (с, 3H), 2,07 (с, 3H), 2,03 (с, 3H), 2,02 (с, 3H), 1,97 (т, 1H, J=2,6 Гц), 1,82 (кв, 2H, J=6,5 Гц),
13C ЯМР (D2O, 75 МГц): δ (м.д.): 170,9, 170,4, 170,3, 169,8, 96,1, 83,3, 71,0, 70,4, 69,4, 68,9, 68,7, 67,4, 66,9, 62,1, 28,4, 20,9, 20,9, 20,8, 20,8, 15,2. HRMS вычислено для C19H26O10 [M+Na]+: 437,5; найдено m/z: 437,1.
Пример 17 - Синтез пент-4-инил-α-D-глюкопиранозида
Продукт формулы (IX) синтезировали как описано ниже:
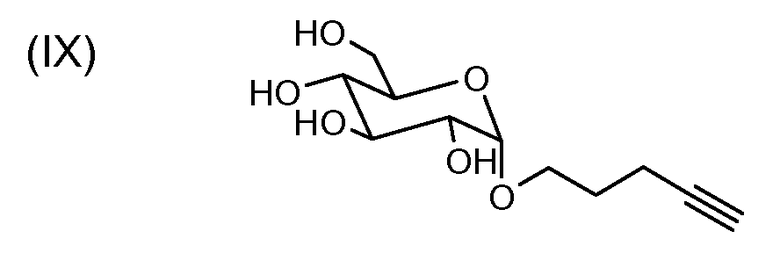
4 мл NaOMe в концентрации 0,1М в MeOH добавляют при 0°C к раствору тетраацетилированного соединения, полученного в примере 16 (180 мг, 0,434 ммоль), растворенного в 3 мл MeOH, и реакционную смесь перемешивают при температуре окружающей среды в течение 4 часов. Затем реакционную смесь нейтрализуют до pH7, используя смолу Dowex-50W. Затем реакционную смесь фильтруют, упаривают досуха при пониженном давлении и очищают хроматографией на колонке с силикагелем, используя CH2Cl2-MeOH, 9:1, в качестве элюента, получая производное α-глюкозы с количественным выходом в форме бесцветного масла.
1H ЯМР (D2O, 300 МГц): δ (м.д.): 5,12 (д, 1H, J=3,9 Гц), 4,08 (м, 2H), 4,00 (м, 1H), 3,92 (м, 2H), 3,82 (м, 1H), 3,76 (м, 1H), 3,62 (м, 1H), 2,55 (м, 3H), 2,03 (м, 2H). 13C ЯМР (D2O, 75 МГц): δ (м.д.): 100,0, 87,0, 75,1, 73,6, 73,3, 71,6, 71,4, 68,2, 62,4, 29,3, 16,5, HRMS вычислено для C11H18O6 [M+Na]+: 269,1; найдено m/z: 269,0
Пример 18 - Получение полимера PsAcF2 (1,2; 0,4)
Полимер PsAcF1 (1,2; 0,4) (24,8 мг) и 4-пентин-1-ол (200 мкл раствора в концентрации 92,5 мг/мл в воде, 0,22 ммоль, 2,2 экв.) перемешивают в 150 мкл деионизованной воды при температуре окружающей среды. Затем к реакционной смеси добавляют аскорбат натрия (50 мкл свежеприготовленного раствора в воде в концентрации 200 мг/мл, 0,05 ммоль, 0,5 экв.) и пентагидрат сульфата меди(II) (50 мкл раствора в концентрации 25 мг/мл в воде, 0,005 ммоль, 0,05 экв.), смесь перемешивают при температуре окружающей среды в течение 20 часов. Очистка диализом в 2M растворе NaCl в течение 3 суток, затем в деионизованной воде в течение 3 суток с последующей лиофилизацией дают полимер PsAcF2 (1,2; 0,4) в форме аморфного белого порошка. Степень замещения триазолом 0,4 (т.е., по существу все реакционно-способные группы Ar были подвергнуты превращению).
1H ЯМР (D2O, 300 МГц): δ (м.д.): 7,65 (s, ls, Hтриазол), 5,03 (с, ls, Hano), 4,85 (с, ls, Hano), 4,30-3,30 (м, ls), 3,13 (с, ls, CH2), 2,61 (с, ls, CH2), 2,01 (с, ls, CH2), 1,75 (с, ls, CH2).
Пример 19 - Получение полимера PsAcF3 (1,2; 0,34)
Аскорбат натрия (50 мкл свежеприготовленного раствора в воде в концентрации 200 мг/мл, 0,05 ммоль, 0,5 экв.) и затем пентагидрат сульфата меди(II) (50 мкл раствора в концентрации 25 мг/мл в воде, 0,005 ммоль, 0,05 экв.) последовательно добавляют к смеси PsAcF1 (1,2; 0,34) (24,8 мг) и пент-4-инил-α-D-глюкопиранозида (49,3 мг, 0,2 ммоль, 2,0 экв.) в 900 мкл деионизованной воды при температуре окружающей среды. Через 20 часов реакционную смесь очищают диализом в 2M растворе NaCl в течение 3 суток, затем в деионизованной воде в течение 2 суток. Полимер PsAcF3 (1,2; 0,34) получают после лиофилизации в форме аморфного белого порошка. Степень замещения триазолом составляет 0,26, т.е., только некоторые реакционно-способные группы F были подвергнуты превращению.
1H ЯМР (D2O, 300 МГц): δ (м.д.): 7,74 (с, ls, Hтриазол), 5,06 (с, ls, Hano), 4,88 (с, ls, Hano), 4,78 (с, ls, Hano), 4,34-3,16 (м, ls), 2,71 (с, ls, CH2), 2,05 (с, ls, CH2), 1,89 (с, ls, CH2).
Пример 20 - Получение полимера PsAcArF3 (1,2; 0,42; 0,38)
Аскорбат натрия (50 мкл свежеприготовленного раствора в воде в концентрации 200 мг/мл, 0,05 ммоль, 0,5 экв.) и затем пентагидрат сульфата меди(II) (50 мкл раствора в концентрации 25 мг/мл в воде, 0,005 ммоль, 0,05 экв.) последовательно добавляют к смеси PsAcArF2 (1,2; 0,42; 0,38) (28,7 мг) и 4-пентин-1-ола (200 мкл раствора в концентрации 92,5 мг/мл в воде, 0,22 ммоль, 2,2 экв.) в 700 мкл деионизованной воды при температуре окружающей среды. Через 20 часов реакционную смесь очищают диализом в 2M растворе NaCl в течение 3 суток, затем в деионизованной воде в течение 2 суток. Полимер PsAcArF3 (1,2; 0,42; 0,38) получают после лиофилизации в форме аморфного белого порошка. Степень замещения триазолом 0,28 (степень превращения 74% реакционно-способных групп F).
1H ЯМР (300 МГц, D2O) δ (м.д.): 7,62 (с, ls, Hтриазол), 7,21 (с, ls, Har), 5,04 (с, ls, Hano), 4,89 (с, ls, Hano), 4,29-3,50 (м, ls), 3,13 (с, ls, CH2), 2,58 (с, ls, CH2), 1,96 (с, ls, CH2), 1,73 (с, ls, CH2).
Пример 21 - Получение полимера PsAcArF4 (1,2; 0,42; 0,38)
Аскорбат натрия (100 мкл в концентрации 200 мг/мл в PBS, 0,05 ммоль, 1 экв.) добавляют к раствору PsAcArF2 (1,2; 0,42; 0,38) (28,7 мг) и пент-4-инил-α-D-глюкопиранозида (43,8 мг, 0,178 ммоль, 1,8 экв.) в 500 мкл деионизованной воды и 400 мкл PBS в концентрации 0,1M. Добавляют пентагидрат сульфата меди(II) (100 мкл, 25 мг/мл в PBS, 0,005 ммоль, 0,1 экв.) и реакционную смесь перемешивают при температуре окружающей среды в течение 20 часов. Декстран собирают в водном растворе EDTA-2Na в концентрации 0,5M (2 мл) перед очисткой диализом в 2M растворе NaCl в течение 3 суток, затем в деионизованной воде в течение 2 суток. Лиофилизация дает PsAcArF4 (1,2; 0,42; 0,38) в форме аморфного белого порошка. Степень замещения триазолом составляет 0,34 (степень превращения 89% реакционно-способных групп F).
1H ЯМР (300 MHz, D2O) δ (м.д.): 7,63 (с, ls, Hтриазол), 7,21 (с, ls, Har), 5,00 (с, ls, Hano), 4,90 (с, ls, Hano), 4,85 (с, ls, Hano), 4,23-3,22 (м, ls), 3,09 (с, ls, CH2), 2,64 (с, ls, CH2), 1,22 (с, ls, CH2), 1,19 (с, ls, CH2).
Пример 22 - Функционализация планшетов из полистирола и измерение угла контакта
Планшет из полистирола (планшет Goodfellow, 10 см × 10 см), предварительно промытый водой и этанолом, наполовину погружают в раствор полимера в буфере PBS в концентрации 10 мкг/мл или только в PBS (контроль) в течение ночи при температуре окружающей среды (один планшет на один тип полимера). Полимеры, подвергаемые проверке, представляют собой полимеры, описанные выше, и более конкретно PsAc1 (1,2), PsAcAr1 (1,2; 0,42), PsAcArF2 (1,2; 0,42; 0,38) и PsAcArF4 (1,2; 0,42; 0,27) (при этом значение 0,27 означает здесь только степень замещения триазолом).
Полистироловую поверхность в контакте с раствором затем дважды погружают на 5 минут в водяную баню. Затем сушат в атмосфере азота в течение 10 минут.
Затем такие поверхности используют для измерений угла контакта. Зону подложки, которая была в контакте с раствором, используют в качестве контроля.
Десять капель воды по 1 мкл наносят в середину обработанной и необработанной (контрольной) поверхности. Результаты (медиана угла и межквартильный размах) показаны на фиг.3.
Можно видеть, что обработка полистироловой поверхности полисахаридами PsAcAr1, PsAcArF2 и PsAcArF4 приводит к значимому снижению угла контакта воды по сравнению с необработанным полистиролом. Следовательно, такие полимеры позволяют осуществлять функционализацию полистирола.
Пример 23 - Функционализация 96-луночных полистироловых планшетов лигандами
В данном примере дно полистироловых лунок полностью покрывают слоем PsAc, PsAcAr или PsAcArF и затем инкубируют с лигандами (лектинами). Затем белок инкубируют с функционализированной лигандами поверхностью. Наконец, система регистрации флуоресценции позволяет идентифицировать лунки, в которых произошло улавливание белка-мишени.
Используемые 96-луночные планшеты представляли собой планшеты типа MaxiSorp Immunoplate от производителя Nunc.
1) 100 мкл раствора полимера в PBS (pH7,4) (от 50 мкг/мл до 0,1 мкг/мл) инкубируют в лунках планшета в течение 16 часов при температуре окружающей среды.
2) Затем лунки промывают 3×300 мкл PBS (pH7,4), содержащим 0,1% твин 20 в течение 3×5 минут.
3) Затем лунки инкубируют с 300 мкл раствора PBS (pH7,4) с твином 20 (0,1%), содержащего БСА (3%, 1% или 0,1%) или казеин (0,1%) в течение 1 часа при температуре окружающей среды.
4) Лунки промывают 3×300 мкл PBS (pH7,4) с твином 20 (0,1%) в течение 3×5 минут.
5) Затем лунки инкубируют с 200 мкл раствора биотинилированного лектина (например 10 мкг/мл, 5 мкг/мл или 1 мкг/мл) в PBS (pH7,4) с твином 20 (0,1%), содержащем MnCl2 и CaCl2 в конечной концентрации 1 мМ. Инкубация занимает 1 час при температуре окружающей среды при перемешивании.
Использовали следующие лектины (коммерчески доступные): конканавалин A (ConA), агглютинин из проростков пшеницы (WGA) и лектин Erythrina cristagalli (ECL).
ConA взаимодействует с концевыми остатками альфа-D-глюкозы или альфа-D-маннозы. WGA узнает N-ацетил-D-глюкозамины. ECL узнает концевые остатки альфа-D-галактозы.
6) Лунки промывают 3×300 мкл PBS (pH7,4) с твином 20 (0,1%) в течение 3×5 минут.
7) Затем лунки инкубируют с 200 мкл раствора меченого тетраметилродамином стрептавидина (5 мкг/мл или 1 мкг/мл) в PBS (pH7,4) с твином 20 (0,1%) в течение 2 часов при температуре окружающей среды.
8) Лунки промывают, используя 3×300 мкл PBS (pH7,4) с твином 20 (0,1%), в течение 3×5 минут.
9) Лунки промывают 3×300 мкл деионизованной воды в течение 3×5 минут.
10) Планшет сушат в центрифуге в течение 10 минут и затем сушат в атмосфере азота в течение 5 минут.
11) Флуоресценцию на дне лунок измеряют при 532 нм, используя конфокальный флуоресцентный сканнер.
Результаты показаны на фиг.4 и 5.
Фиг.4 представляет собой гистограмму, показывающую интенсивность флуоресценции, получаемой при использовании полимера PsAcArF4 (1,2; 0,42, 0,34) (степень замещения 0,34 только в отношении триазола в качестве группы F) и трех лектинов, указанных выше. Отношения, показанные на оси x, представляют собой отношения лектин/стрептавидин.
Можно видеть, что PsAcArF4, как и ожидалось, избирательно распознается конканавалином A (ConA), что свидетельствует о качестве функционализации полистиролового планшета и доступности лиганда в отношении белка-мишени.
Фиг.5 представляет собой гистограмму, показывающую интенсивность флуоресценции, получаемой с использованием того же самого полимера PsAcArF4 (1,2; 0,42, 0,34) и ConA. Отношения, показанные на оси x, представляют собой отношения лектин/стрептавидин. Последний результат (T) является контролем без полисахарида.
Данный эксперимент иллюстрирует взаимосвязь между интенсивностью сигнала флуоресценции и концентрацией ConA, используемого в лунках. Флуоресценция, ассоциированная с лунками, в которые не вносили ConA, стрептавидин или PsAcArF4, была очень низкой.
Пример 24 - Образование микроточек на дне лунок 96-луночного планшета при нанесении полисахаридов посредством печати, взаимодействие с лектинами
В данном эксперименте различные полимеры наносят посредством микропечати на дно необработанного 96-луночного планшета.
Полученные таким образом биочипы затем инкубируют с белками (лектинами).
Используемые 96-луночные планшеты представляют собой иммунологические планшеты типа MaxiSorp от производителя Nunc. 300 пл раствора полимера (в концентрациях 10 мкг/мл, 7,5 мкг/мл, 5 мкг/мл и 1 мкг/мл в PBS) наносят на планшет, используя устройство Packard BioChipArrayer BCA-1, в следующем порядке:
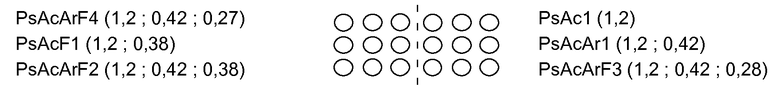
В случае полимера PsAcArF4 степень замещения 0,27 соответствует только группам триазола. В случае полимера PsAcArF3 степень замещения 0,28 соответствует только группам триазола.
1) Затем лунки инкубируют со 100 мкл раствора PBS (pH7,4) с твином 20 (0,1%), содержащего БСА (3%), в течение 15 минут при температуре окружающей среды.
2) Затем лунки промывают 3×100 мкл PBS (pH7,4), содержащего 0,1% твин 20, в течение 3×5 минут.
3) Затем лунки инкубируют со 100 мкл раствора биотинилированного лектина (например, 20 мкг/мл, 10 мкг/мл или 5 мкг/мл) в PBS (pH7,4), твин 20 (0,1%) в течение 1 часа при температуре окружающей среды и орбитальном перемешивании. В случае лектинов (ConA, ECL и WGA) добавляют соли MnCl2 и CaCl2 в конечной концентрации 1 мМ.
4) Лунки промывают 3×100 мкл PBS (pH7,4), содержащего твин 20 (0,1%), в течение 3×5 минут.
5) Затем лунки инкубируют со 100 мкл раствора стрептавидина, меченого тетраметилродамином (5 мкг/мл), в PBS (pH7,4), твин 20 (0,1%) в течение 2 часов при температуре окружающей среды.
6) Лунки промывают 3×100 мкл PBS (pH7,4), содержащего твин 20 (0,1%), в течение 3×5 минут.
7) Лунки промывают 3×100 мкл деионизованной воды в течение 3×5 минут.
8) Планшет сушат в центрифуге в течение 10 минут и затем сушат в атмосфере азота в течение 5 минут.
9) Регистрацию осуществляют, используя сканнер, при 532 нм.
На фиг.6 суммированы полученные результаты. Можно видеть, что ConA избирательно фиксирован на полимере PsAcArF4, при этом ни один из двух других лектинов не фиксирован.
Пример 25 - Функционализация полистироловых планшетов и измерение угла контакта, влияние степени ароматического замещения
В данном эксперименте использовали полимеры PsAc1 (1,27), PsAcAr1 (1,27; 0,03), PsAcAr1 (1,27; 0,39) и PsAcAr1 (1,27; 0,54).
Пять полистироловых планшетов (планшеты Goodfellow, 10 см × 10 см), предварительно промытых водой и этанолом, наполовину погружают в растворы PsAc1 или PsAcAr1, растворенных в буфере PBS в концентрации 10 мкг/мл, или только в PBS в течение ночи при температуре окружающей среды.
Затем полистироловую поверхность в контакте с раствором дважды погружают на 5 минут в водяную баню. Затем сушат в атмосфере азота в течение 10 минут.
Затем такие поверхности используют для измерений угла контакта. Зону подложки, которая не была в контакте с раствором, используют в качестве контроля.
Десять капель воды по 1 мкл наносили в середине обработанной и необработанной (контроль) поверхности.
Результаты (медиана угла и межквартильный размах) показаны на фиг.7. Первый столбик представляет результат немедленного измерения, и второй столбик представляет результат после хранения в течение 24 часов в условиях частичного вакуума (эксикатор).
Можно видеть, что PsAcAr1 (1,27; 0,54) позволяет достигать значимого уменьшения угла контакта, при этом имеет место уменьшение от 86° для необработанного полистирола до 56° для обработанного полистирола. Функции, привитые на полистироловую поверхность с помощью PsAcAr1 (1,27; 0,54), делают поверхность более гидрофильной, что отражается в уменьшении угла контакта воды на таких поверхностях по сравнению с необработанным полистиролом. Таким образом, полимер PsAcAr1 (1,27; 0,54) позволяет осуществлять химическую функционализацию полистирола.
Пример 26 - Функционализация 96-луночных полистироловых планшетов и связывание посредством гидразоновой связи с флуоресцирующими пептидами
В данном эксперименте использованы полимеры PsAcArF1 (1,1; 0,75; 0,03) и PsAcAr 1 (1,1; 0,75). Полимер PsAcArF 1 (1,1; 0,75; 0,03) позволяет функционализировать дно лунок функцией гидразида. Полимер PsAcAr1 (1,1; 0,75), который не несет такой функции, служит в качестве контроля. Известно, что функция гидразида взаимодействует с молекулами, несущими альдегидную функцию. Образованная связь является гидразоновой. Принцип реакции заключается в следующем:
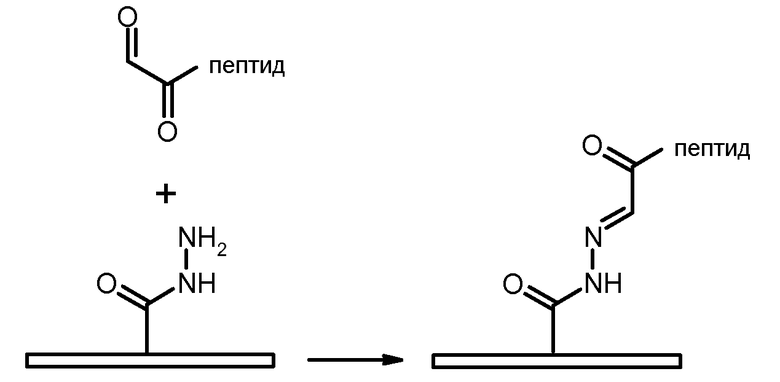
Использованы два пептида: пептид 1 (SEQ ID NO: 1) формулы Rho-KR-NH(CH2)3-NH-CHOCO (функционализированный тетраметилродамином и функцией CHOCO) и пептид 2 (SEQ ID NO: 2) формулы Rho-KR-NH2 (функционализированный тетраметилродамином и амидной функцией). Синтез таких пептидов описан Ollivier с соавторами, Alpha-oxo semicarbazone peptide or oligodeoxynucleotide microarrays, Bioconjug. Chem. 14, 430-9 (2003).
Протокол:
Лунки 96-луночного полистиролового микропланшета (Maxisorp, Nunc) обрабатывают 100 мкл раствора PsAcArF1 (1,1; 0,75; 0,03) или PsAcAr1 (1,1; 0,75) в концентрации 5 мкг/мл в PBS. Обработку проводят при температуре окружающей среды при перемешивании в течение ночи.
Затем планшет промывают PBS/твин 20, 0,05%, используя устройство для промывки планшетов (300 мкл/лунку, 6 промывок).
Две серии растворов пептидов 1 и 2 готовят в концентрациях 10-6, 5×10-7, 2,5×10-7, 1,25×10-7 и 6,25×10-8М в ацетатном буфере, pH 5,5/0,1% БСА. По 60 мкл каждого раствора наносят на дно лунок, обработанных PsAcArF1 (1,1; 0,75; 0,03) или PsAcAr1 (1,1; 0,75) (2 лунки/условие). Реакцию лигирования проводят с перемешиванием в течение 2 часов при температуре окружающей среды.
Планшет промывают PBS/твин 20 (0,05%) (300 мкл/лунку, 6 промывок) и затем деионизованной водой (300 мкл/лунку, 3 промывки). Затем осуществляют сушку в центрифуге (2500 об./мин, 5 минут, 20°C). Планшет считывают, используя сканер флуоресценции Técan.
Результат показан на фиг.8. Серые столбики соответствуют пептиду 1, а белые столбики соответствуют пептиду 2. Cn соответствует разным концентрациям PsAcArF1 (1,1; 0,75; 0,03) и C'n соответствует разным концентрациям PsAcAr1 (1,1; 0,75), при этом 1 = 10-6М; 2 = 5×10-7М; 3 = 2,5×10-7М; 4 = 1,25×10-7М; 5 = 6,25×10-8М.
Интенсивность сигналов (на оси y), которые ассоциированы с лунками, обработанными PsAcArF1 (1,1; 0,75; 0,03) и затем инкубированы с альдегидом пептида 1, является высокой (Cn, пептид 1). В сравнении интенсивность сигналов, ассоциированных с лунками, обработанными PsAcAr1 (1,1; 0,75) (контрольные лунки, не имеющие функции гидразида, которая является реакционно-способной в отношении альдегидной функции пептида 1) является очень низкой (C'n, пептид 1).
Во всех случаях интенсивность сигналов, ассоциированных с лунками, инкубированными с контрольным пептидом 2, не имеющим альдегидной функции, является очень низкой (Cn или C'n, пептид 2).
Настоящий пример демонстрирует хемоселективное связывание несущего альдегид пептида 1 с лунками, обработанными PsAcArF1 (1,1; 0,75; 0,03) и имеющими доступные функции гидразида.
Дополнительные эксперименты осуществляли, варьируя pH реакционной смеси для лигирования. Предпочтительное значение pH для реакции составляет 5, как и ожидалось для такого типа химической реакции.
Пример 27 - Функционализация 96-луночных полистироловых планшетов, получение биочипов с использованием печати пептидов и реакции in situ
В настоящем эксперименте лунки функционализируют полисахаридным полимером. Пептиды наносят посредством печати, образуя биочип, при этом пептиды связываются с поверхностью за счет образования ковалентной связи гидразона.
Синтез пептидов, используемых в данном эксперименте, описан в публикации Carion с соавторами, Chemical Micropatterning of Polycarbonate for Site-Specific Peptide Immobilization and Biomolecular Interactions. Chembiochem. 8, 315-322 (2007).
Использовали следующие пептиды:

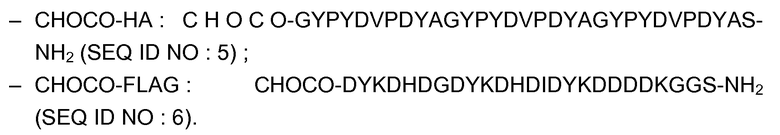
Протокол:
Нанесение посредством печати пептидов Ser-HA, CHOCO-HA, Ser-FLAG и CHOCO-FLAG в концентрации 10-4М в PBS-буфере или ацетатном буфере при pH 5,5 на планшеты 96-луночного типа, функционализированные полимером PsAcArF1 (10 мкг/мл), полимером PsAcAr1 (10 мкг/мл), буфером PBS или необработанный.
Насыщение лунок осуществляют, используя 300 мкл PBS+1% БСА, в течение 30 минут при перемешивании.
Лунки промывают вручную PBS/0,1% твин 20.
Инкубацию анти-HA- и анти-FLAG-антител осуществляют в концентрации 1 мкг/мл в PBS/0,1% БСА в течение 1,5 часа при перемешивании (100 мкл/лунку). Лунки промывают вручную PBS/0,1% твин 20.
Инкубацию меченых тетраметилродамином антител против IgG мыши осуществляют в концентрации 2 мкг/мл в PBS/0,1% БСА в течение 1 часа при перемешивании (100 мкл/лунку).
Лунки промывают вручную PBS/0,1% твин 20, 3 раза водой и сушат центрифугированием (2500 об./мин, 5 минут, 20°C).
Планшеты считывают, используя сканнер Técan (фокусное расстояние: -1000/MTP-усиление: 90/разрешение: 4 мкм).
Результаты инкубации c анти-HA-антителом показаны на фиг.9, и результаты инкубации с анти-FLAG-антителом показаны на фиг.10 (интенсивность флуоресценции на оси y).
Пример 28 - Получение бис({2-[трифенилметил)сульфанил]этил})амина
1,50 г бис(2-хлорэтил)амина (8,4 ммоль) и 4,65 г трифенилметантиола (2 эквивалента, 16,80 ммоль) вносят в колбу и помещают в инертную атмосферу. Добавляют 25 мл безводного диметилформамида (ДМФА) при перемешивании на магнитной мешалке и реакционную смесь охлаждают на бане со льдом. К смеси по каплям добавляют 4 эквивалента 1,8-диазабицикло[5,4,0]ундец-7-ена (DBU). Смесь перемешивают при температуре окружающей среды в течение 3 часов и реакцию контролируют с помощью тонкослойной хроматографии (ТСХ) (элюент: циклогексан/этилацетат/триэтиламин: 8/2/0,1). После указанного периода времени растворитель выпаривают на роторном испарителе. Затем полученное белое твердое вещество растворяют в 50 мл дихлорметана (ДХМ) и продукт экстрагируют три раза 5% водным раствором KH2PO4. Затем продукт очищают хроматографией на колонке с силикагелем (элюент: циклогексан/EtOAc/триэтиламин (TEA): 8/2/0,1), получая 1,46 г аморфного белого твердого вещества (выход 28%).
Получены следующие результаты анализа продукта.
Rf=0,37 (силикагель, циклогексан/EtOAc/TEA: 8/2/0,1).
1H ЯМР (300 МГц, CDCl3) δ 7,41-7,37 (м, 12H, Trt), 7,15-7,29 (м, 18H, Trt), 2,23-2,36 (м, 8H, CH2), 1,26 (с, 1H, NH).
13C (75 МГц, CDCl3) 154,1; 129,8; 128,1; 126,9; 47,9; 32,6; MALDI-TOF: 243,1 [Trt+], 622,3 [M+H+]+, 644,3 [M++Na+].
Пример 29 - Синтез Boc-βAla-N(CH2CH2STrt)2
Boc-β-аланин (1,908 г, 10,1 ммоль) растворяют в 50 мл дихлорметана, затем раствор охлаждают до 0°C и добавляют N,N-дициклогексилкарбодиимид (5 ммоль). Перемешивание продолжают в течение 30 минут при температуре окружающей среды. После фильтрования добавляют бис({2-(трифенилметил)сульфанил]этил})амин (2,5 г, 4 ммоль). Реакционную смесь перемешивают в течение 2 часов при температуре окружающей среды. Реакционную смесь упаривают досуха. К полученному остатку добавляют 100 мл водного раствора карбоната натрия (1н) и экстрагируют дихлорметаном (3×100 мл). Органическую фазу сушат над безводным сульфатом магния и упаривают. Сырой продукт очищают хроматографией на силикагеле (циклогексан/этилацетат/триэтиламин, 80/20/0,1, об./об./об.). Продукт Boc-βAla-N(CH2CH2STrt)2 получают в форме белого порошка (3,1 г, 3,9 ммоль, 97%).
Диаграмма реакции приведена ниже:
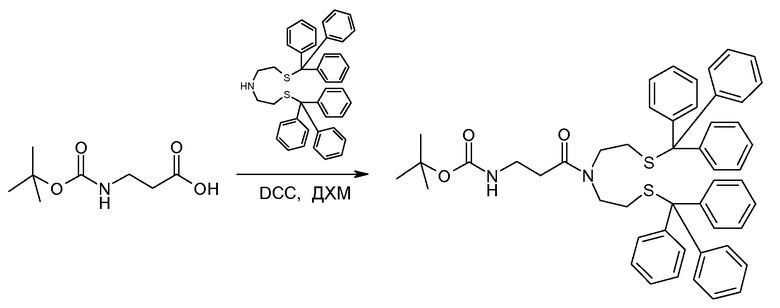
Точка плавления: 53°C.
1H ЯМР (300 МГц, CDCl3): δ м.д. 1,43 (9H, с, CH3); 1,94 (2H, т, J=4 Гц, CH2S); 2,14 (2H, т, J=4 Гц, CH2S); 2,31 (2H, т, J=4 Гц, CH2CON); 2,73 (4H, м, CONCH2); 3,23 (2H, м, OCONCH2); 5,23 (H, м, CONH); 7,10-7,50 (30 HAr, м).
13C ЯМР (75 МГц, CDCl3): δ м.д. 28,50 (CH3); 29,50 (CH2); 30,0 (CH2); 33,0 (CH2); 36,0 (CH2); 45,0 (CH2); 47,0 (CH2); 126,7 (CH); 127,0 (CH); 128,0 (CH); 129,5 (CH); 130,0 (CH); 143,0 (Cчетв.); 144,5 (Cчетв.); 145,0 (Cчетв.); 156,0 (Cчетв.); 171,0 (Cчетв.),
MALDI-TOF (DHB матрица): Mвычисленная=792,3 (C50H52N2O3S2); m/z=815,4 [M+Na]+; m/z=831,3 [M+K]+.
Пример 30 - Синтез Boc-βAla-дитиазепана
Продукт Boc-βAla-дитиазепан (3 г, 3,78 ммоль) растворяют в дихлорметане (50 мл) и добавляют иод (2,87 г, 11,3 ммоль). Перемешивают в течение 30 минут при температуре окружающей среды. Избыток иода нейтрализуют водным раствором тиосульфата натрия (3M, 100 мл). Экстракцию осуществляют дихлорметаном (4×100 мл). Органическую фазу сушат над безводным сульфатом магния и упаривают. Сырой продукт очищают хроматографией на силикагеле (гексан/этилацетат/триэтиламин, 40/60/0,1, об./об./об). Продукт Boc-βAla-дитиазепан получают в форме белой пасты (1,1 г, 3,6 ммоль, 95%).
Диаграмма реакции приведена ниже:
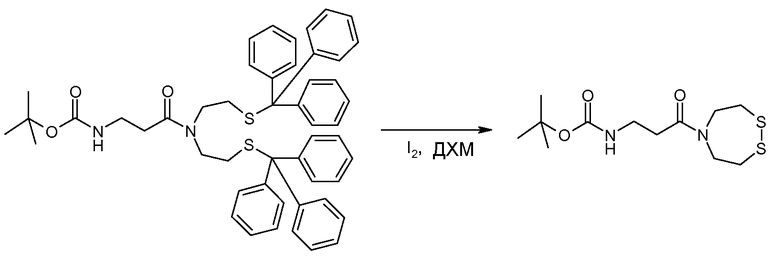
1H ЯМР (300 МГц, CDCl3): δ м.д. 1,39 (9H, с, CH3); 2,48 (2H, т, J=4 Гц, CH2CON); 2,87 (2H, т, J=4 Гц, CH2S); 3,04 (2H, т, J=4 Гц, CH2S); 3,39 (2H, м, OCONCH2); 3,76 (2H, т, J=4 Гц, CONCH2); 3,86 (2H, т, J=4 Гц, CONCH2); 5,25 (H, м, NH),
13C ЯМР (75 МГц, CDCl3): δ м.д. 28,5 (CH3); 33,0 (CH2); 36,0 (CH2); 37,0 (CH2); 39,5 (CH2); 50,0 (CH2); 53,0 (CH2); 143,0 (Cчетв.); 156,0 (Cчетв.); 172,0 (Cчетв.),
MALDI-TOF (DHB матрица): Mвычисленная=306,1 (C12H22N2OS2); m/z=307,1 [M+H]+; m/z=329,1 [M+Na]+; m/z=345,1 [M+K]+.
Пример 31 - Синтез NH2-βAla-дитиазепана
Продукт Boc-βAla-дитиазепан (1 г, 3,26 ммоль) растворяют в дихлорметане (5 мл) и добавляют трифторуксусную кислоту (5 мл). Перемешивают в течение 30 минут при температуре окружающей среды. Реакционную смесь упаривают досуха. К полученному остатку добавляют водный раствор карбоната натрия (1н) и экстрагируют дихлорметаном (3×100 мл). Органическую фазу сушат над безводным сульфатом магния и упаривают. Продукт NH2-βAla-дитиазепан получают в форме прозрачного масла (628 мг, 3,04 ммоль, 94%).
Диаграмма реакции приведена ниже:

1H ЯМР (300 МГц, CDCl3): δ м.д. 2,44 (2H, т, J=4 Гц, CH2CON); 2,60 (H, м, NH2); 2,90 (2H, т, J=4 Гц, NH2CH2); 3,0 (4 H, м, CH2S); 3,77 (2H, т, J=4 Гц, CONCH2); 3,84 (2H, т, J=4 Гц, CONCH2).
13C ЯМР (75 МГц, CDCl3): δ м.д. 35,0 (CH2); 35,5 (CH2); 37,5 (CH2); 39,0 (CH2); 50,0 (CH2); 52,0 (CH2); 172,0 (Cчетв.).
MALDI-TOF (DHB матрица): Mвычисленная=206,05 (C7H14N2OS2); m/z=207,0 [M+H]+; m/z=229,0 [M+Na]+.
Пример 32 - Синтез полимера PsAcArF5
50 мг полимера PsAcAr1 (1,1; 0,49) (0,20 ммоль) растворяют в 1 мл деионизованной воды в колбе, затем pH доводят до 4,74, используя 1н раствор HCl. Добавляют 1-циклогексил-3-(2-морфолиноэтил)карбодиимид (CMC) (100 мг, 0,22 ммоль, 1,1 эквивалента), затем pH доводят до 4,74. Добавляют амин H2N(CH2)2CON(CH2CH2S-)2 (75 мг, 0,36 ммоль, 1,8 эквивалента). Реакционную смесь перемешивают в течение ночи при температуре окружающей среды.
Затем реакционную смесь помещают в диализную трубку (3500 г/моль; 1 мл/см), затем погружают в 2,5 л 2M раствора NaCl, оставляя в нем на 5 суток, затем в 2,5 л воды, где также оставляют на 5 суток.
Содержимое мешка затем помещают в чашу, подвергают лиофилизации, получая 47 мг PsAcArF5. Диаграмма реакции приведена ниже:
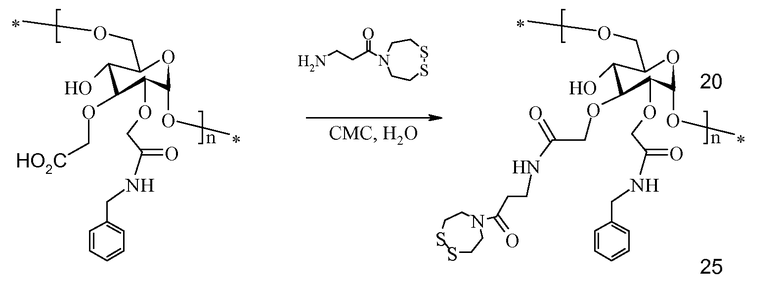
Пример 33 - Химическая функционализация 96-луночных полистироловых планшетов, амидное связывание с флуоресцирующими пептидами
В настоящем примере использовали полимеры PsAcAr1 и PsAcArF5.
Полимер PsAcArF5 позволяет функционализировать дно лунок функцией CON(CH2CH2S-)2. Полимер PsAcAr1, который не несет такой функции, служит в качестве контроля. Функция CON(CH2CH2S-)2 может взаимодействовать с молекулами, несущими бета-аминотиольную функцию, такими как, например, цистеин, присутствующий в N-концевом положении пептидов. Образуемая связь является амидной связью.
Химия иммобилизации полимером PsAcArF5 описана на следующей диаграмме:
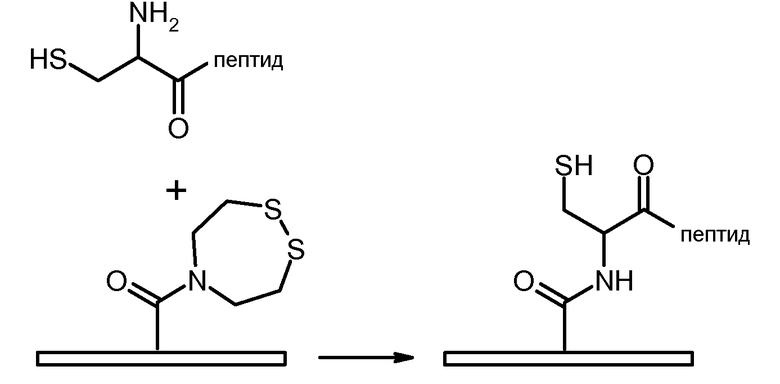
В настоящем примере использованы два пептида:
1) H-CILK(родамин)EPVHGV-NH2 (SEQ ID NO: 7);
2) H-SILK(родамин)EPVHGV-NH2 (SEQ ID NO: 8).
Два указанных пептида синтезированы согласно следующему протоколу:
Пептид H-ILK(Mtt)E(tBu)PVH(Trt)GV-NH2 (SEQ ID NO: 9) собирают на смоле Novasyn TGR® (Novabiochem, 0,25 ммоль, 0,23 ммоль/г), используя микроволновой синтезатор пептидов (CEM) и методику на основе Fmoc/трет-бутила. Удаление защитной группы Mtt осуществляют с использованием 1% раствора ТФУ в CH2Cl2 (17×15 мл). Смолу нейтрализуют 5% раствором DIEA в CH2Cl2 (5×2 мин) и затем промывают CH2Cl2 (3×2 мин), затем ДМФА (3×2 мин). Затем смолу подвергают взаимодействию в течение 2 часов с 5(6)-карбокситетраметилродамином (150,6 мг, 0,35 ммоль), HOBT (47 мг, 0,35 ммоль), HBTU (132,7 мг, 0,35 ммоль) и DIEA (217,8 мкл, 1,75 ммоль, 5 эквивалент) в ДМФА. Затем смолу промывают ДМФА (4×2 мин). Защитную концевую группу Fmoc удаляют, используя 20% раствор пиперидина в ДМФА (5 и 15 мин). Смолу промывают ДМФА (4×2 мин). Смолу делят на две части и подвергают взаимодействию с Fmoc-Cys(Trt)-OH или Fmoc-Ser(tBu)-OH, соответственно. Связывание осуществляют вручную, используя 4 эквивалента защищенной аминокислоты, 4 эквивалента HBTU и HOBT и 12 эквивалентов DIEA. Смолу промывают ДМФА (4×2 мин). Защитную концевую группу Fmoc удаляют, используя 20% раствор пиперидина в ДМФА (5 и 15 мин). Затем смолу промывают ДМФА (4×2 мин), CH2Cl2 (6×2 мин), этиловым эфиром и затем сушат при пониженном давлении. Затем осуществляют снятие защиту и отщепление пептидов, используя раствор ТФУ/H2O/EDT/TIS: 94/2,5/2,5/1 по объему в случае пептида 1) и ТФУ/H2O/TIS: 95/2,5/2,5 по объему в случае пептида 2), в течение 1 часа. Затем пептиды осаждают из раствора Et2O/н-гептана: 1/1 по объему, растворяют в воде и подвергают лиофилизации. Очистку осуществляют, используя ОФ-ВЭЖХ, и получают 41 мг (20%) и 28 мг (14%) в случае пептидов 1) и 2), соответственно.
MALDI-TOF (DHB матрица) пептид 1): Mвычисленная=1505,7 (C74H104N16O16S); m/z=1506,8 [M+H]+; m/z=1528,8 [M+Na]+.
MALDI-TOF (DHB матрица) пептид 2): Mвычисленная=1488,7 (C75H105N15O17); m/z=1489,7 [M+H]+; m/z=1511,7 [M+Na]+.
Полимеры PsAcAr1 и PsAcArF5 инкубируют в 96-луночном полистироловом планшете в концентрации 10 мкг/мл в PBS в течение ночи при температуре окружающей среды и перемешивании (100 мкл/лунку).
Затем лунки 6 раз промывают раствором PBS/0,1% твин 20. Планшет сушат в центрифуге.
Пептиды 1) и 2) растворяют в концентрации 10-4М в 200 мМ фосфатном буфере в присутствии 200 мМ меркаптофенилуксусной кислоты (MPAA) и 80 мМ трис(карбоксиэтил)фосфина при pH 7,6. Такие растворы инкубируют в течение 10 минут с перемешиванием при 37°C (60 мкл/лунку) в функционализированных лунках.
Затем лунки 6 раз промывают раствором PBS/0,1% твин 20 и 3 раза деионизованной водой. Планшет сушат в центрифуге (2500 об./мин, 5 минут, 20°C). Планшет анализируют в сканере флуоресценции Técan.
Результаты показаны на фиг.11 (интенсивность флуоресценции по оси y). Настоящий пример демонстрирует, что лунки полистиролового планшета, функционализированные с помощью полимера PsAcArF5, позволяют связывать содержащий цистеин пептид 1), но не контрольный, содержащий серин пептид 2). Очень слабый сигнал, полученный при использовании контрольного полимера PsAcAr1 для двух пептидов, показывает важность наличия функции 2,5-дитиазепана на полистироловой поверхности для связывания содержащего цистеин пептида 1).
Пример 34 - Получение биочипа с антителами на дне 96-луночных полистироловых планшетов
В настоящем примере лунки функционализируют, используя полисахарид, затем наносят антитела, получая биочип. Такие белки связываются с поверхностью за счет образования нековалентных связей. Затем биочипы инкубируют с белками-мишенями.
8 лунок 96-луночного полистиролового микропланшета (планшет Maxisorp, Nunc-Immuno) обрабатывают 100 мкл PsAcArF1 (1,15; 0,64; 0,26) в концентрации 10 мкг/мл в буфере (условия A). 8 лунок обрабатывают только буфером (условия B). Обработку осуществляют при температуре окружающей среды в течение ночи с перемешиванием.
Затем планшет промывают буфером, используя устройство для промывки планшетов (200 мкл/лунку, 3 промывки, перемешивание), затем деионизованной водой, используя устройство для промывки планшетов (200 мкл/лунку, 3 промывки, перемешивание).
Антитело против стрептавидина (кроличье поликлональное антитело против стрептавидина, Antibodies-on line, ссылка ABIN107091) затем наносят на дно лунки в растворенном в буфере виде (3 пятна на лунку, 8 лунок, всего 24 пятна).
Насыщение лунок осуществляют, используя 200 мкл буфера с 2% БСА, в течение 2 часов.
Лунки промывают, используя автоматическое устройство для промывки (3 цикла, перемешивание), буфером с добавлением 0,05% твина 20.
Затем инкубируют стрептавидин-HRP (стрептавидин-HRP, ссылка Thermo-Pierce 21130), используя разведение 1:10 000 в буфере с добавлением твина 20 в концентрации 0,05% и БСА в концентрации 0,2%, в течение 1 часа (100 мкл/лунку).
Дополнительный эксперимент проводили с использованием контрольного белка: конъюгата антитела козы против IgG мыши с HRP, Southern Biotech, ссылка 103105, в разбавлении 1:6000 в таком же растворе.
Лунки промывают, используя автоматическое устройство для промывки (3 цикла), буфером, содержащим 0,05% твин 20. Затем инкубируют с раствором TMB (3,3',5,5"-тетраметилбензидина) в течение 12 минут при температуре окружающей среды. Лунки промывают 200 мкл деионизованной воды.
Изображение дна каждой лунки получают, используя ПЗС-камеру (разрешение: 3 мкм), которая позволяет создавать изображения в серых тонах. Затем пятна количественно оценивают с помощью стандартной компьютерной программы для количественной оценки микроматриц.
Результаты определения интенсивностей всех пятен после инкубации со стрептавидином-HRP показаны на фиг.12 (интенсивность в условных единицах по сои y; A: лунки, обработанные PsAcArF1 (1,15; 0,64; 0,26); B: необработанные контрольные лунки). Инкубация с контрольным белком, конъюгатом антитела козы против IgG мыши с HRP, не давала регистрируемого сигнала.
На данной фигуре показано, что медианная интенсивность, получаемая в случае пятен антитела против стрептавидина в лунках A, значимо выше, чем в лунках B.
Результаты в отношении стандартного отклонения пикселей для каждого пятна (не заштрихованные кружки), с медианой и межквартильным размахом для всех пятен показаны на фигуре 13. Стандартное отклонение среди пятен, которое характеризует в качестве нанесения пятен, намного меньше в случае условия A по сравнению с условием B.
В общем, полученные результаты показывают превосходство обработки A для получения биочипов.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБЫ И НАБОРЫ ДЛЯ ПРОГНОЗИРОВАНИЯ РИСКА ДЫХАТЕЛЬНОЙ НЕДОСТАТОЧНОСТИ, ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ ИЛИ ТРОМБОПЕНИИ У ПАЦИЕНТА, СТРАДАЮЩЕГО СЕПСИСОМ, ПУТЕМ ИЗМЕРЕНИЯ УРОВНЕЙ ЭНДОКАНА В КРОВИ | 2012 |
|
RU2589903C2 |
| АНТАГОНИСТЫ РЕЦЕПТОРА FLT3 | 2015 |
|
RU2710928C2 |
| СОЛИ СУЛЬФАТЫ N-(3-(4-(3-(ДИИЗОБУТИЛАМИНО)ПРОПИЛ)ПИПЕРАЗИН-1ИЛ)ПРОПИЛ)-1Н-БЕНЗО[D]ИМИДАЗОЛ-2-АМИНА, ИХ ПОЛУЧЕНИЕ И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2655454C2 |
| ПЕПТИДОМИМЕТИКИ | 2013 |
|
RU2662973C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ 2-ГИДРОКСИТЕТРАГИДРОФУРАНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2004 |
|
RU2360920C2 |
| НОВЫЕ АНТИИНВАЗИВНЫЕ СОЕДИНЕНИЯ | 2013 |
|
RU2641650C2 |
| ФЕРМЕНТАТИВНОЕ ОБРАЗОВАНИЕ ПЕРКИСЛОТЫ ДЛЯ ПРИМЕНЕНИЯ В ПРОДУКТАХ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА | 2011 |
|
RU2660373C2 |
| НОВЫЕ АМФИФИЛЬНЫЕ ПРОИЗВОДНЫЕ AЛЬФА-C-ФЕНИЛ-N-ТРЕТ-БУТИЛНИТРОНА | 2003 |
|
RU2364602C2 |
| НОВЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2000 |
|
RU2260009C2 |
| ФЕРМЕНТАТИВНОЕ ОБРАЗОВАНИЕ ПЕРКИСЛОТЫ ДЛЯ ПРИМЕНЕНИЯ В ПРОДУКТАХ ДЛЯ УХОДА ЗА ПОЛОСТЬЮ РТА | 2011 |
|
RU2793140C2 |
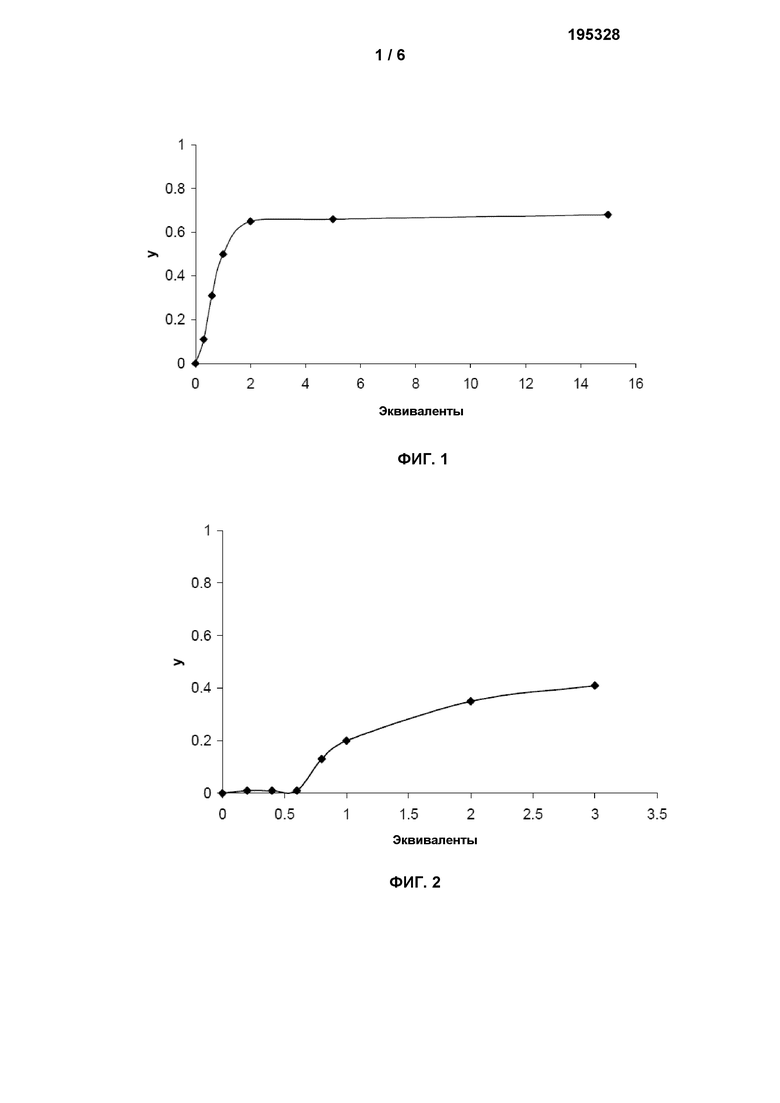
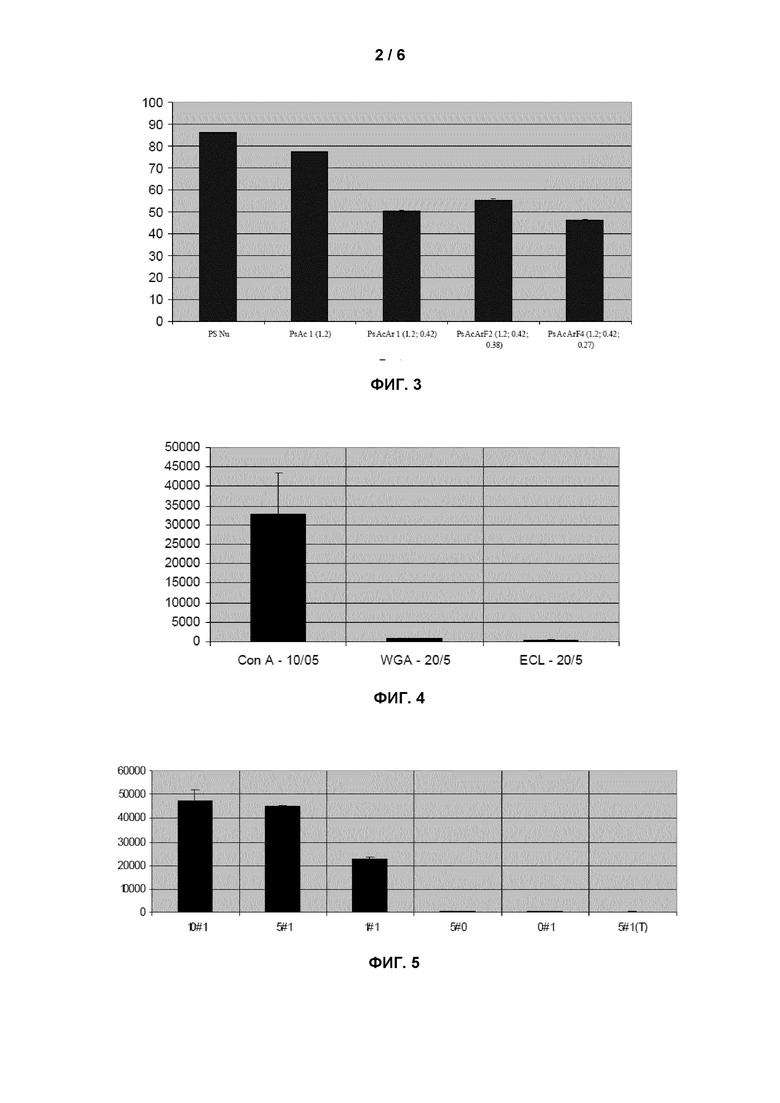
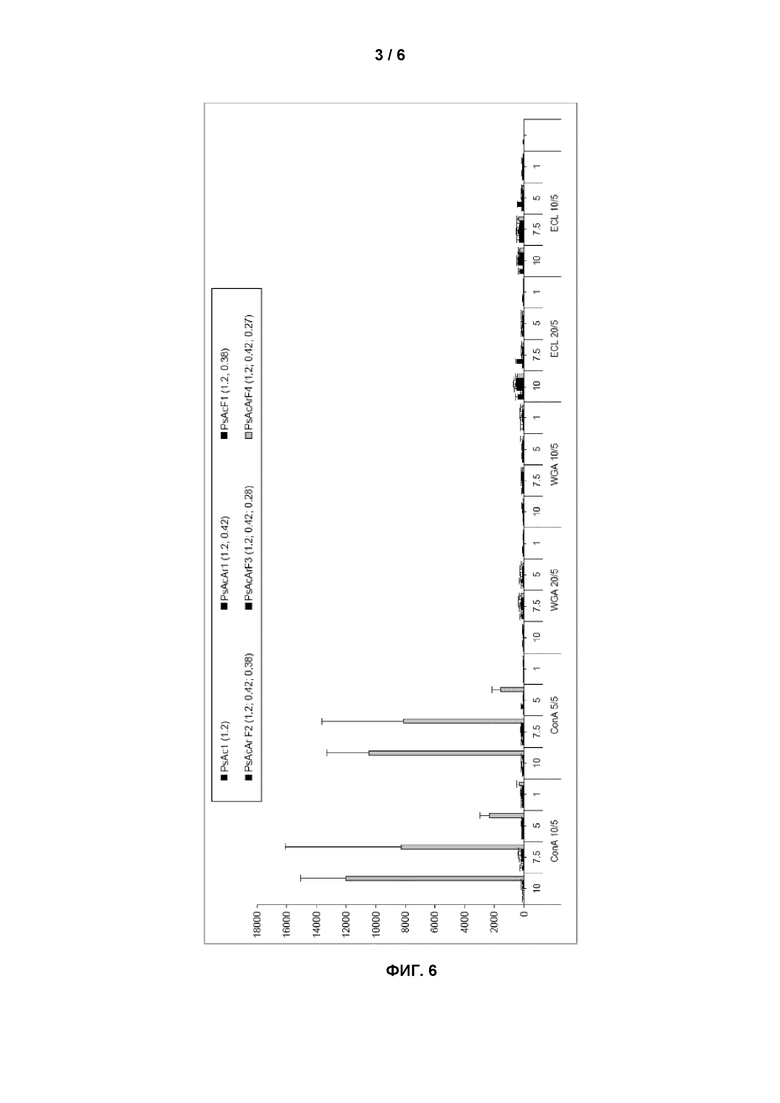
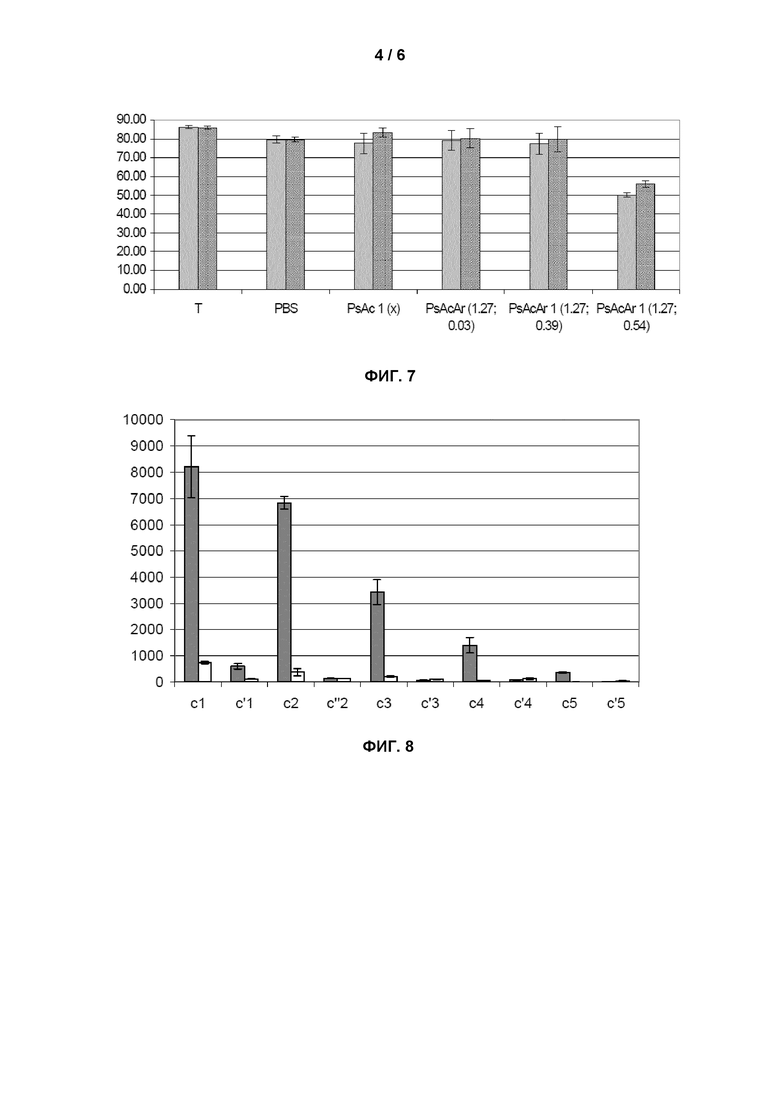
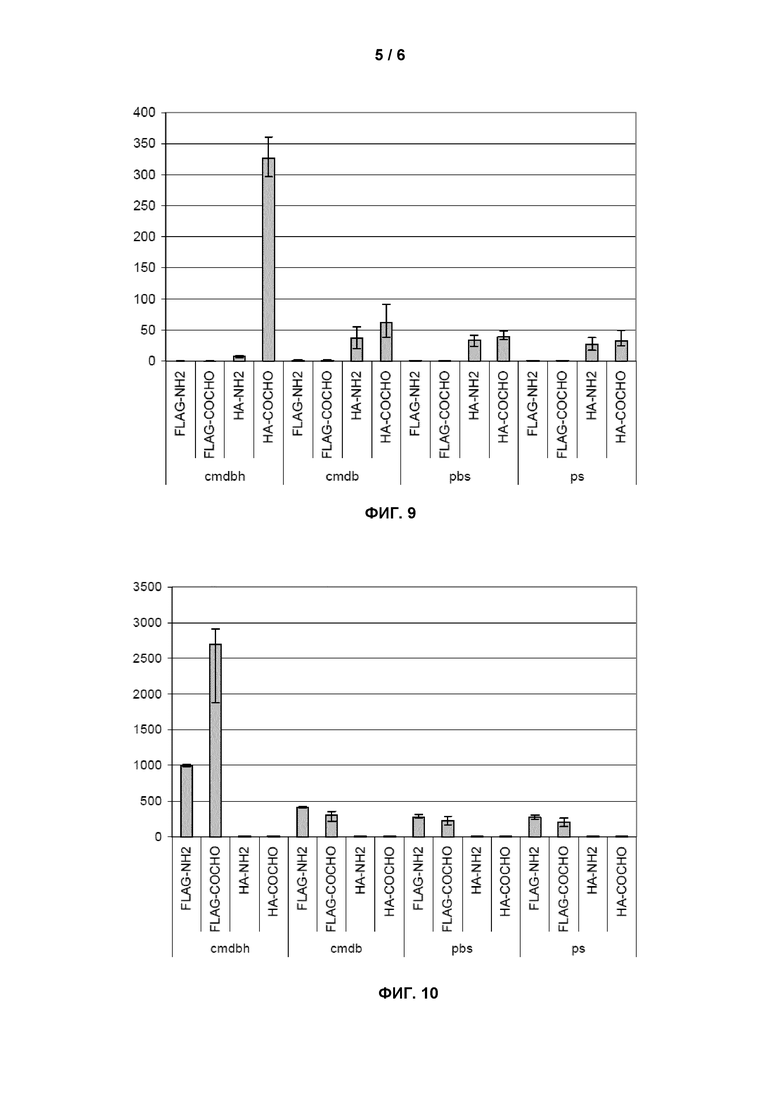
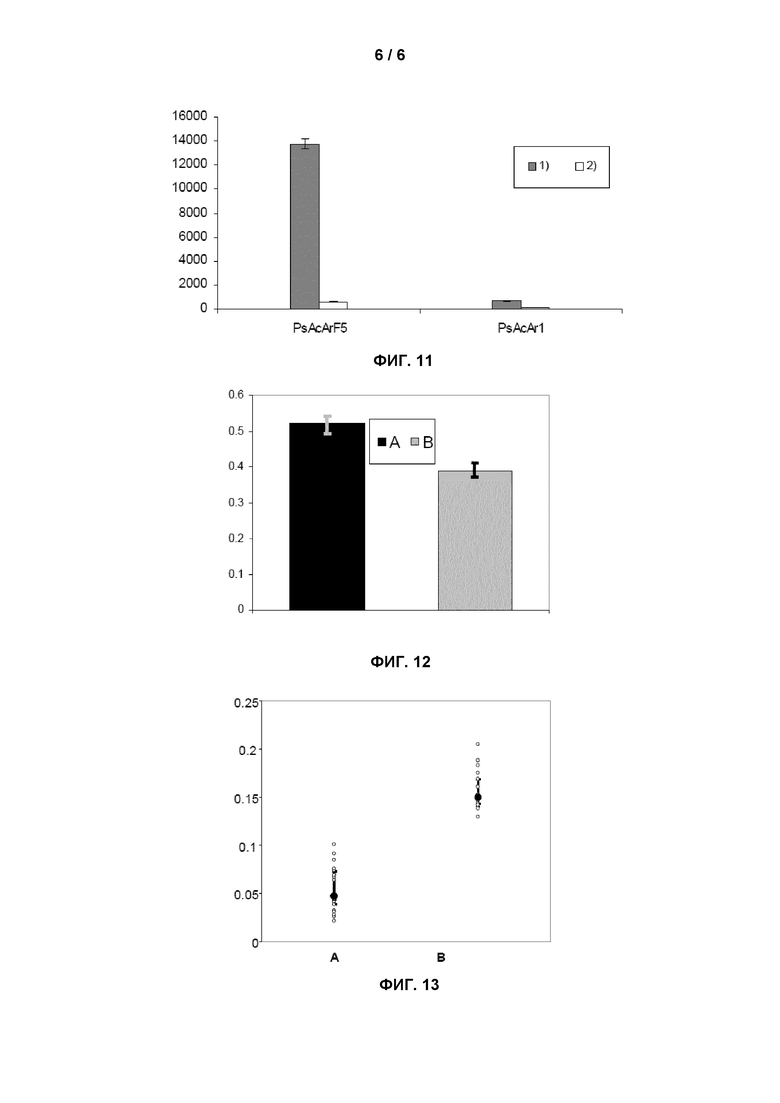





Группа изобретений относится к области диагностики, а именно к устройству для выявления аналитов, включающему пластиковую подложку, частично или полностью непосредственно покрытую связывающими полимерами, фиксированными на подложке нековалентно, при этом указанные связывающие полимеры содержат полисахаридный остов, снабженный: ароматическими группами формы -X-CONH-Z, группами карбоновой кислоты формы -Х-СООН и реакционно-способными группами F, имеющими форму -X-CONH-Z′, где X означает неразветвленную или разветвленную, замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, Z означает арильную функцию, Z′ означает группу, которая способна связываться с другой молекулой, а также к способам производства указанного устройства, кроме того, к связывающему полимеру и к способу его получения. Группа изобретений обеспечивает получение устройства для выявления различных аналитов. 6 н. и 14 з.п. ф-лы, 13 ил., 34 пр.
1. Устройство для выявления аналитов, включающее пластиковую подложку, частично или полностью непосредственно покрытую связывающими полимерами, фиксированными на подложке нековалентно, при этом указанные связывающие полимеры содержат полисахаридный остов, снабженный:
- ароматическими группами формы -X-CONH-Z, где X означает неразветвленную или разветвленную, замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, и Z означает арильную функцию;
- группами карбоновой кислоты формы -Х-СООН, где X означает неразветвленную или разветвленную, замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода; и
- реакционно-способными группами F, имеющими форму -X-CONH-Z′, где X означает неразветвленную или разветвленную, замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, и Z′ означает группу, которая способна связываться с другой молекулой.
2. Устройство по п. 1, в котором полисахаридный остов представляет собой остов из декстрана, молекулярная масса которого предпочтительно составляет от 15000 до 100000 Да, и, в частности, более предпочтительно от 30000 до 60000 Да.
3. Устройство по п. 1, в котором реакционно-способные группы F выбраны из:
- групп формы -X-CONH-X′-N3;
- групп формы -X-CONH-NH2;
- групп формулы (V):
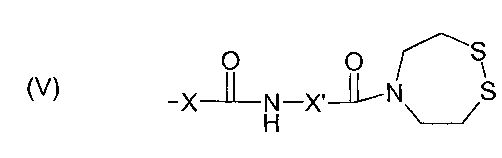
- групп формулы (V):
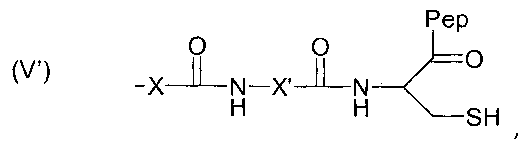
где каждый из X и X′ означает замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, и Pep означает фрагмент пептида.
4. Устройство по любому из пп. 1-2, в котором:
- X означает СН2; и/или
- Z означает -CH2-Ph или -CH2-Ph-пара-OH.
5. Устройство по любому из пп. 1-2, в котором связывающие полимеры содержат:
- от 0,4 до 0,8 ароматических групп, предпочтительно от 0,4 до 0,6 ароматических групп, предпочтительно от 0,45 до 0,6 ароматических групп на единицу сахарида полисахаридного остова; и/или
- от 0 до 0,8 реакционно-способных групп, предпочтительно от 0 до 0,6 реакционно-способных групп на единицу сахарида полисахаридного остова; и/или
- от 0,5 до 1,5 ароматических групп, групп карбоновой кислоты и реакционно-способных групп в совокупности, предпочтительно от 0,9 до 1,3 ароматических групп, групп карбоновой кислоты и реакционно-способных групп в совокупности на единицу сахарида полисахаридного остова.
6. Устройство по любому из пп. 1-2, в котором подложка представляет собой подложку из полистирола, поликарбоната, поли(метилметакрилата) или полипропилена и предпочтительно из полистирола.
7. Устройство по любому из пп. 1-2, содержащее улавливающие элементы, иммобилизованные на связывающих полимерах, при этом указанные улавливающие элементы предпочтительно иммобилизованы на связывающих полимерах посредством адсорбции или ковалентного связывания с реакционно-способными группами F.
8. Устройство по п. 7, в котором улавливающие элементы выбраны из:
- полипептидов, необязательно модифицированных и/или конъюгированных;
- сахаридов, олигосахаридов и липополисахаридов;
- вирусов или фрагментов вирусов и клеток.
9. Устройство по любому из пп. 1-2, содержащее множество зон для выявления, при этом зоны для выявления предпочтительно содержат разные улавливающие элементы.
10. Устройство по любому из пп. 1-2, в котором подложка представляет собой непрозрачные или прозрачные пластины, планшет для микротитрования, набор шариков, чашку для культивирования, полоску или палочку.
11. Применение устройства для выявления аналитов по любому из пп. 1-10 для выявления химических молекул, биологических молекул, клеток или живых организмов.
12. Применение по п. 11 для выявления и количественной оценки химических молекул, биологических молекул, клеток или живых организмов.
13. Способ производства устройства для выявления аналитов по любому из пп. 1-10, включающий:
- получение пластиковой подложки;
- осуществление контакта подложки по меньшей мере с одним раствором, содержащим связывающие полимеры.
14. Способ по п. 13, дополнительно включающий осуществление контакта подложки с одним или несколькими растворами, содержащими улавливающие элементы.
15. Способ производства устройства для выявления аналитов по любому из пп. 1-10, включающий:
- получение пластиковой подложки;
- осуществление контакта подложки с одним или несколькими растворами, содержащими связывающие полимеры, связанные с улавливающими элементами.
16. Связывающий полимер, который можно применять в устройстве по любому из пп. 1-10, содержащий полисахаридный остов, имеющий:
- от 0,4 до 0,8 ароматических групп на единицу сахарида формы -X-CONH-Z, где X означает неразветвленную или разветвленную, замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, и Z означает арильную функцию;
- группы карбоновой кислоты формы -Х-СООН, где X означает неразветвленную или разветвленную алкильную цепь, содержащую от 1 до 6 атомов углерода, и
- реакционно-способные группы F выбраны из:
- групп формы -X-CONH-X′-N3;
- групп формы -X-CONH-NH2;
- групп формулы (V):
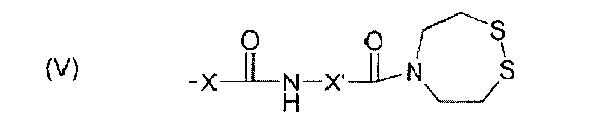
- групп формулы (V′):
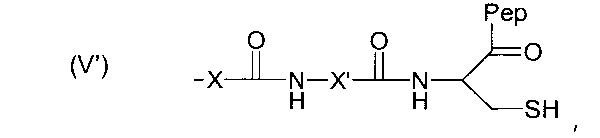
где каждый из X и X′ означает замещенную или незамещенную алкильную цепь, содержащую от 1 до 6 атомов углерода, и Pep означает фрагмент пептида.
17. Связывающий полимер по любому из предшествующих пунктов, в котором полисахаридный остов представляет собой остов из декстрана, молекулярная масса которого предпочтительно составляет от 15000 до 100000 Да, и, в частности, более предпочтительно от 30000 до 60000 Да.
18. Связывающий полимер по одному из пп. 16-17, в котором:
- X означает СН2; и/или
- X и X′ означают (СН2)2; и/или
- Z означает -CH2-Ph или -CH2-Ph-пара-OH.
19. Связывающий полимер по любому из пп. 16-17, содержащий:
- от 0,4 до 0,6 ароматических групп, предпочтительно от 0,45 до 0,6 ароматических групп на единицу сахарида полисахаридного остова; и/или
- от 0 до 0,8 реакционно-способных групп, предпочтительно от 0 до 0,6 реакционно-способных групп на единицу сахарида полисахаридного остова; и/или
- от 0,5 до 1,5 ароматических групп, групп карбоновой кислоты и реакционно-способных групп в совокупности, предпочтительно от 0,9 до 1,3 ароматических групп, групп карбоновой кислоты и реакционно-способных групп в совокупности на единицу сахарида полисахаридного остова.
20. Способ производства связывающего полимера по любому из пп. 16-19, включающий:
- получение декстранового полисахарида;
- прививку групп карбоновой кислоты на полисахарид;
- модификацию части привитых групп карбоновой кислоты, чтобы получить ароматические группы;
- модификацию части групп карбоновой кислоты, чтобы получить реакционно-способные группы F.
| US 20020169120 A1, 14.11.2002 | |||
| US 4740594 A, 26.04.1988. |
Авторы
Даты
2016-09-20—Публикация
2011-10-11—Подача