Изобретение относится к области медицины, в частности к способам получения пористого материала на основе титана с биоактивным покрытием, который в дальнейшем может быть использован для изготовления костного имплантата.
Известен способ получения имплантатов, в котором в качестве основы используется титановая лента, из которой просекают сетку с квадратными или ромбовидными ячейками с величиной сторон 0,8-2,5 мм и шагом 0,05-0,1 мм. На поверхность сетки методом плазменного напыления наносят слой титана толщиной 50-100 мкм из порошка дисперсностью 60-150 мкм, который затем покрывают слоем биокерамики толщиной 30-50 мкм из порошка дисперсностью 40-60 мкм. Напыление может быть однослойным (титан) или двухслойным (титан + биокерамика), односторонним или двусторонним (патент RU №2157245; МПК A61L 27/06, A61F 2/28; 1999 год).
Известный способ является сложным, трудоемким, а биологическая активность гидроксиапатита (ГАП) теряется при высокотемпературной обработке в процессе плазменного напыления.
Известен также способ получения биомедицинского материала для создания костных имплантатов на основе пористого сплава титан-кобальт в режиме СВС, включающий приготовление экзотермической смеси исходных реагентов из порошка титана и кобальта, добавление в смесь не более 4 мас. % гидрида титана, не более 15 мас. % аморфного нанодисперсного порошка ГАП или аморфного нанокомпозита ГАП с биополимером природного происхождения, прессование из смеси порошков заготовки, размещение ее в реакторе СВС, предварительный нагрев заготовки до 350-580°C, инициирование процесса горения в инертной атмосфере с последующим выделением целевого продукта (патент RU №2341293; МПК A61L27/04, A61L27/06, A61L27/24, A61F2/28; 2007 год)(прототип).
Известный способ является многостадийным, высокотемпературная обработка приводит к разложению биоактивного гидроксиапатита и поровое пространство сплава покрывается соединениями кальция, фосфора и кислорода, представляющими собой продукты его распада, биоактивность которых значительно ниже, чем у гидроксиапатита. Необходимо отметить, что любая высокотемпературная обработка переводит гидроксиапатит в кристаллическую структуру, менее растворимую по сравнению с минеральной составляющей кости (Е.А. Богданова. Диссерт. на соискание уч. степ. канд. хим. наук. Физико-химические свойства биоактивных композиционных материалов на основе фосфатов кальция и кремнийорганических соединений. Екатеринбург, 2012).
Таким образом, перед авторами была поставлена задача - разработать простой способ получения биомедицинского материала, обеспечивающий сохранение минерального состава биоактивного компонента - гидроксиапатита (ГАП) наряду с хорошей адгезией нанесенного покрытия.
Поставленная задача решена в предлагаемом способе получения биомедицинского материала, включающем нанесение на пористую основу, содержащую титан, покрытия из гидроксиапатита, в котором нанесение осуществляют путем импрегнирования водной суспензией гидроксиапатита, при этом окунают пористый титан в 12-14%-ную водную суспензию гидроксиапатита на 2-3 сек, а затем помещают в 2-3%-ную водную суспензию гидроксиапатита и осуществляют в вакууме 2·10-10÷9·10-10 мм рт. ст. 3-5-кратный пульсационный режим с соотношением между длительностью импульса и паузы 3÷5:10÷5.
В настоящее время из патентной и научно-технической литературы не известен способ получения биомедицинского материала путем импрегнирования суспензией гидроксиапатита разной концентрации и осуществлением в вакууме 2·10-10÷9·10-10 мм рт. ст. 3-5-кратного пульсационного режима с определенным соотношением между длительностью импульса и паузы.
В качестве биосовместимой высокопористой основы авторы предлагают использовать пористый титан, обладающий такими свойствами, как: биосовместимость, коррозионная стойкость, достаточно низкий модуль упругости (С.М. Баринов, B.C. Комлев. Биокерамика на основе фосфатов кальция. М.: Наука, 2005. 205 с.). Роль биоактивного материала, усиливающего остеоинтеграцию имплантата с костью, выполняет покрытие гидроксиапатита (ГАП), которое получают из суспензии, полученной в соответствии с патентом RU 2406693. Проведенные авторами исследования позволили разработать способ получения биоактивного покрытия на пористом титане, позволяющий сохранить минеральный состав биоактивного компонента - гидроксиапатита (ГАП) наряду с хорошей адгезией нанесенного покрытия. Для достижения необходимого результата авторами предлагается способ пульсационного вакуумного импрегнирования, в ходе которого осуществляют осаждение частиц ГАП из суспензии, получая покрытие не только пор поверхности высокопористого титана равномерным слоем биоактивного материала, но и пор во всем его объеме. Перед обработкой в вакууме образцы титана окунают в 12-14%-ную суспензию ГАП для снижения пористости и исключения проскока суспензии при вакуумировании. При использовании суспензии с концентрацией менее 12% возможен проскок суспензии при дальнейшем вакуумировании. Использование суспензии с концентрацией выше 14% ведет к значительному снижению пористости, что затрудняет получение покрытия в порах по всему объему. Обработку суспензией ГАП в вакууме осуществляют в интервале определенных технологических параметров. Так повышение давления выше 9·10-10 мм рт. ст. не позволяет прокачать водную суспензию через весь объем образца, поэтому происходит излишнее увеличение толщины покрытия на его поверхности, способствующее в дальнейшем растрескиванию последнего, при одновременном слабом покрытии пор в объеме. При снижении давления меньше 2·10-10 мм рт. ст. наблюдается неконтролируемый проскок водной суспензии через пористый образец, что приводит к нарушению равномерности покрытия. Пульсационный режим импрегнирования включает в себя чередующиеся стадии подвода вакуума и паузы. Длительность импульса составляет 3-5 сек, длительность паузы -10-15 сек. Пролонгирование первой стадии ведет к утоньшению покрытия, а второй - к замедлению технологического процесса. 3-5-кратная пропитка ГАП позволяет достичь его максимального содержания от массы титана в зависимости от исходной пористости основы. Увеличение количества пропиток приводит к зарастанию и снижению остеоинтеграционных свойств материала, а уменьшение мешает возможности создания сплошного биоактивного покрытия.
Предлагаемый способ может быть осуществлен следующим образом.
Пористый титан (пористость 40-45%) окунают в емкость с сетчатым дном с водной суспензией ГАП состава Ca10(PO4)6(ОН)2 с концентрацией 12-14% в течение 2-3 сек, затем заполняют емкость 2-3% водной суспензией ГАП состава Ca10(PO4)6(OH)2 с размером частиц 3-4 мкм и осуществляют в вакууме 2·10-10÷9·10-10 мм рт. ст. 3-5-кратный пульсационный режим с соотношением между длительностью импульса и паузы 3÷5:10÷5. После чего образцы сушат на воздухе при комнатной температуре в течение 10 часов и получают пористый материал на основе титана с покрытием ГАП, при этом содержание ГАП составляет 6,0-13,5 мас. % от массы титана.
Содержание ГАП от массы титана определяют путем взвешивания образцов до и после обработки. Морфологию образующегося в процессе вакуумного импрегнирования покрытия пор исследовали методом Брунауэра, Эммета и Тейлера (БЭТ) низкотемпературной адсорбцией азота на приборе Gemini VII 2390 VI.03 (V1.03 t) и установили, что в результате пропитки ГАП формируется новая развитая поверхность, о чем свидетельствует изменение величины площади удельной поверхности в случае образцов с начальной пористостью 45% с 0,3256±0,0453 до 11,4029±0,0831 м2/г, а с начальной пористостью 40% с 0,3943±0,0120 до 8,7330±0,0585.
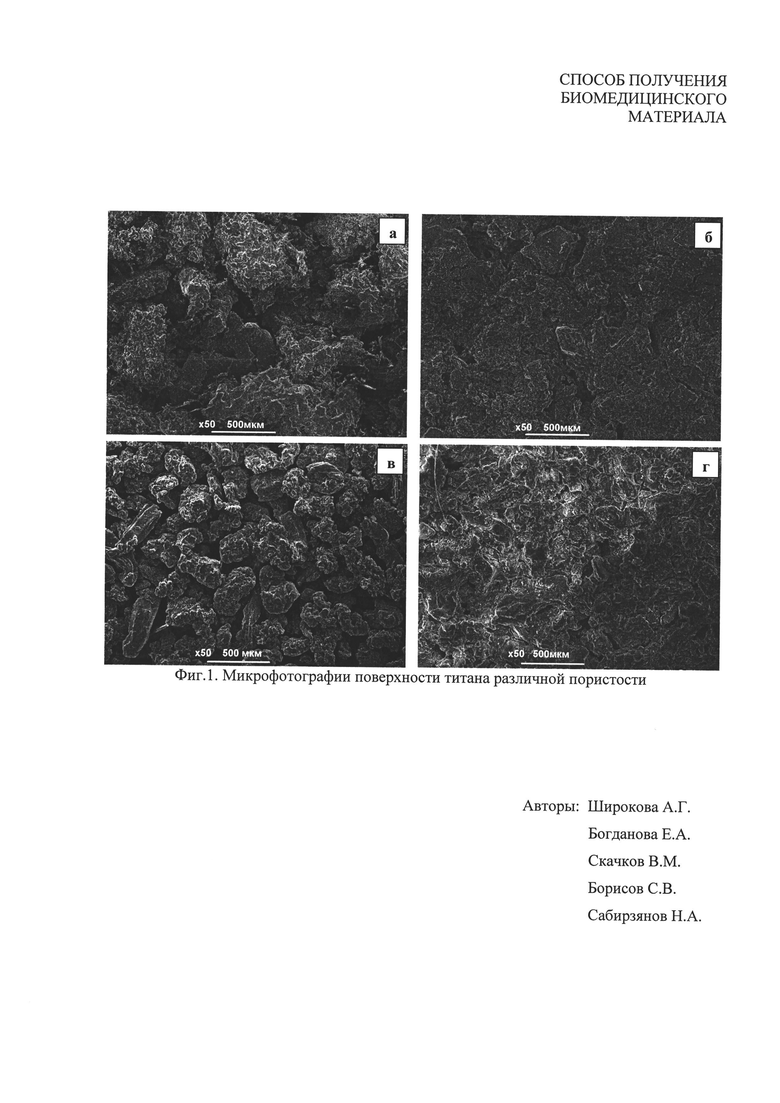
Микрофотографии образцов пористого титана до и после покрытия (см. фиг.1) получали на анализирующем сканирующем электронном микроскопе JSM 6390 LA (JEOL-Япония).
Прочность сцепления биоактивного покрытия с титановой основой определяли методом ультразвукового воздействия в ультразвуковой ванне «САПФИР 1,3 ТТЦ» при мощности 35 кГц. Потеря массы образца с покрытием ГАП по предлагаемому способу после обработки ультразвуком в течение 1 часа при температуре 25°C составляет 0,16 мас. %, что позволяет оценить прочность адгезии как достаточно высокую.
Предлагаемый способ иллюстрируется следующими примерами.
Пример 1. Образец пористого титана размером 10×10×4 мм (пористость 40%) окунают в емкость с сетчатым дном с водной суспензией ГАП состава Ca10(PO4)6(ОН)2 с концентрацией 12% в течение 2 сек, затем заполняют емкость 2% водной суспензией ГАП состава Ca10(PO4)6(ОН)2 с размером частиц 3-4 мкм и осуществляют в вакууме 2·10-10 мм рт. ст. 3-кратный пульсационный режим с соотношением между длительностью импульса и паузы 3:15 (длительность импульса 3 сек; длительность паузы 15 сек). После чего образцы сушат на воздухе при комнатной температуре в течение 10 часов и получают пористый материал на основе титана с покрытием ГАП, при этом содержание ГАП составляет 6,0 мас. % от массы титана. На фиг.1 изображена микрофотография поверхности титана пористости 40%: а) исходный образец титана; б) образец титана с покрытием ГАП.
Пример 2. Образец пористого титана размером 10×10×4 мм (пористость 40%) окунают в емкость с сетчатым дном с водной суспензией ГАП состава Ca10(PO4)6(ОН)2 с концентрацией 12% в течение 3 сек, затем заполняют емкость 2% водной суспензией ГАП состава Ca10(PO4)6(ОН)2 с размером частиц 3-4 мкм и осуществляют в вакууме 9·10-10 мм рт. ст. 5-кратный пульсационный режим с соотношением между длительностью импульса и паузы 5:10 (длительность импульса 5 сек; длительность паузы 10 сек). После чего образцы сушат на воздухе при комнатной температуре в течение 10 часов и получают пористый материал на основе титана с покрытием ГАП, при этом содержание ГАП составляет 8,1 мас. % от массы титана.
Пример 3. Образец пористого титана размером 10×10×4 мм (пористость 45%) окунают в емкость с сетчатым дном с водной суспензией ГАП состава Ca10(PO4)6(ОН)2 с концентрацией 14% в течение 2 сек, затем заполняют емкость 3% водной суспензией ГАП состава Ca10(PO4)6(ОН)2 с размером частиц 3-4 мкм и осуществляют в вакууме 2·10-10 мм рт. ст. 3-кратный пульсационный режим с соотношением между длительностью импульса и паузы 3:15 (длительность импульса 3 сек; длительность паузы 15 сек). После чего образцы сушат на воздухе при комнатной температуре в течение 10 часов и получают пористый материал на основе титана с покрытием ГАП, при этом содержание ГАП составляет 11,4 мас. % от массы титана. На фиг. 1 изображена микрофотография поверхности титана пористости 45%: в) исходный образец титана; г) образец титана с покрытием ГАП.
Пример 4. Образец пористого титана размером 10×10×4 мм (пористость 45%) окунают в емкость с сетчатым дном с водной суспензией ГАП состава Ca10(PO4)6(ОН)2 с концентрацией 14% в течение 3 сек, затем заполняют емкость 3% водной суспензией ГАП состава Ca10(PO4)6(ОН)2 с размером частиц 3-4 мкм и осуществляют в вакууме 9·10-10 мм рт. ст. 5-кратный пульсационный режим с соотношением между длительностью импульса и паузы 5:10 (длительность импульса 5 сек; длительность паузы 10 сек). После чего образцы сушат на воздухе при комнатной температуре в течение 10 часов и получают пористый материал на основе титана с покрытием ГАП, при этом содержание ГАП составляет 13,5 мас. % от массы титана.
Таким образом, авторами предлагается технологически простой способ получения биомедицинского материала на основе пористого титана, позволяющий сохранить биологическую активность ГАП за счет исключения высоких температур при обработке и достичь равномерного и прочного покрытия не только поверхности, но и пор во всем объеме.
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения биомедицинского материала | 2018 |
|
RU2687737C1 |
| Биоактивное покрытие для восстановления костной ткани | 2019 |
|
RU2717676C1 |
| Биоактивный композиционный материал | 2020 |
|
RU2724611C1 |
| Биомедицинский материал на основе гидроксиапатита и способ его получения | 2022 |
|
RU2782925C1 |
| Биорезорбируемый материал и способ его получения | 2017 |
|
RU2652429C1 |
| Композиционный биоматериал на основе гидроксиапатита и способ его получения | 2023 |
|
RU2816008C1 |
| Биоактивное покрытие на основе гидроксиапатита для восстановления костной ткани | 2024 |
|
RU2829755C1 |
| СПОСОБ МОДИФИЦИРОВАНИЯ ПОВЕРХНОСТИ ИМПЛАНТАТОВ ИЗ ТИТАНА И ЕГО СПЛАВОВ | 2008 |
|
RU2394601C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОРИСТЫХ МАТЕРИАЛОВ НА ОСНОВЕ НИКЕЛИДА ТИТАНА | 2006 |
|
RU2310548C1 |
| Способ получения модифицированного биопокрытия на имплантате из титана (варианты) | 2019 |
|
RU2693468C1 |
Изобретение относится к области медицины, в частности к способам получения костных имплантов на основе титана с биоактивным покрытием. Для этого на пористую основу, содержащую титан, наносят 12-14% водную суспензию гидроксиапатита (ГАП) в течение 2-3 сек. Затем материал помещают в 2-3%-ную водную суспензию ГАП и импрегнируют в вакууме при 2·10-10÷9·10-10 мм рт. ст. в трех-пятикратном пульсационном режиме. Соотношение между длительностью импульса и паузы составляет от 3-5 до 10-15. Изобретение обеспечивает технологически простой способ получения биомедицинского материала на основе пористого титана, позволяющий достичь равномерного и прочного покрытия во всем объеме пор материала и сохранить биологическую активность ГАП. 1 ил., 4 пр.
Способ получения биомедицинского материала, включающий нанесение на пористую основу, содержащую титан, покрытия из гидроксиапатита, отличающийся тем, что нанесение осуществляют путем импрегнирования водной суспензией гидроксиапатита, при этом окунают пористый титан в 12-14%-ную водную суспензию гидроксиапатита на 2-3 сек, а затем помещают в 2-3%-ную водную суспензию гидроксиапатита и осуществляют в вакууме 2·10-10÷9·10-10 мм рт. ст. 3-5-кратный пульсационный режим с соотношением между длительностью импульса и паузы 3÷5:10÷15.
| СПОСОБ ПОЛУЧЕНИЯ БИОМЕДИЦИНСКОГО МАТЕРИАЛА И МАТЕРИАЛ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 2007 |
|
RU2341293C1 |
| ПОКРЫТИЕ НА ИМПЛАНТАТ ИЗ ТИТАНА И ЕГО СПЛАВОВ И СПОСОБ ЕГО НАНЕСЕНИЯ | 1999 |
|
RU2154463C1 |
| RU 2157245 C1, 10.10.2000 | |||
| СПОСОБ ИЗГОТОВЛЕНИЯ ВНУТРИКОСТНОГО СТОМАТОЛОГИЧЕСКОГО ИМПЛАНТАТА С ПЛАЗМОНАПЫЛЕННЫМ МНОГОСЛОЙНЫМ БИОАКТИВНЫМ ПОКРЫТИЕМ | 1998 |
|
RU2146535C1 |
| СПОСОБ НАНЕСЕНИЯ ПОКРЫТИЙ НА ИЗДЕЛИЯ ИЗ ТИТАНА | 2011 |
|
RU2453630C1 |
| ЛЯСНИКОВ В.Н | |||
| и др., Ионно-лучевая технология наноструктурирования гидроксиапатитовых плазмонапыленных покрытий, Вестник СПГУ, 2012, 2 (66), стр | |||
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
Авторы
Даты
2016-10-10—Публикация
2015-04-27—Подача