Данное изобретение относится к новым соединениям для применения в лечении воспалительного заболевания кишечника.
Введение
Воспалительное заболевание кишечника (IBD) включает в себя два идиопатических воспалительных заболевания: неспецифический язвенный колит (UC) и болезнь Крона (CD). Главным различием между UC и CD является область воспаленной ткани кишечника. Воспаление при CD представляет собой прерывисто сегментированное воспаление, известное как регионарный энтерит, в то время как UC представляет собой поверхностное воспаление, распространяющееся проксимально и непрерывно от прямой кишки. В настоящее время точная причина IBD неизвестна. Как полагают, заболевание связано с чрезмерным иммунным ответом слизистой оболочки на инфекцию кишечного эпителия вследствие дисбаланса между провоспалительными и иммунорегуляторными молекулами. Модели наследования IBD указывают на сложный генетический компонент патогенеза, который может состоять из ряда комбинированных генетических мутаций. В настоящее время не существует конкретных диагностических тестов для IBD, но как только понимание патогенеза будет улучшено, будут улучшены и способы диагностики. Лечение IBD заключается в индуцировании и поддержании ремиссии. Ремиссия у пациентов с IBD может поддерживаться при использовании 5-аминосалицилата. Однако, в то время как использование аминосалицилатов при UC обеспечивает положительный результат как в индуцировании ремиссии на стадии болезни от легкой до средней, так и в предотвращении рецидива, эффективность этих препаратов для поддержания ремиссии при CD находится под вопросом и более не рекомендуется. Основным препаратом при лечении настоящего заболевания является кортикостероид, обычно используемый в течение ограниченного периода времени для возвращения пациентов с UC и CD в состояние ремиссии, однако, будесонид, предназначенный для местного введения с ограниченной системной абсорбцией, не обладает преимуществами в поддержании ремиссии. Альтернативные препараты, такие как иммунодепрессанты азатиоприн и меркаптопурин, вместе с метотрексатом и циклоспорином обладают ограниченной эффективностью и способны вызывать серьезные побочные эффекты. Антитела анти-TNFα (фактор некроза опухоли-альфа), такие как инфликсимаб и адалимубаб, могут применяться пациентами, нечувствительными к стандартной иммунодепрессивной терапии. Однако многие пациенты не в состоянии реагировать на анти-TNFα терапию, либо вследствие их конкретного фенотипа, либо в результат выработки аутоантител.
Описание изобретения
Согласно настоящему изобретению предложены соединения для применения в лечении воспалительного заболевания кишечника, включающей болезнь Крона и неспецифический язвенный колит.
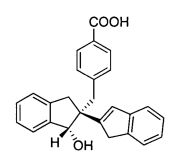
В частности, в настоящем изобретении предложены соединения структурной формулы I:
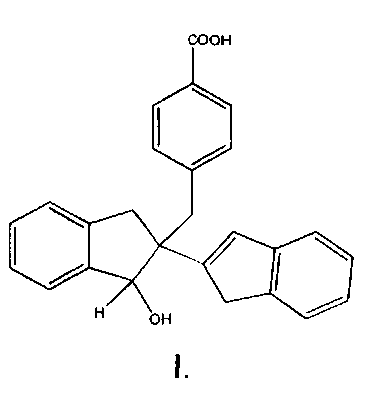
Также предложены фармацевтически приемлемые изомеры и соли соединения формулы (I) - соединение 1.
В частности, в настоящем изобретении предложены соединения, имеющие относительную стереохимию, как показано в структурной формуле II:
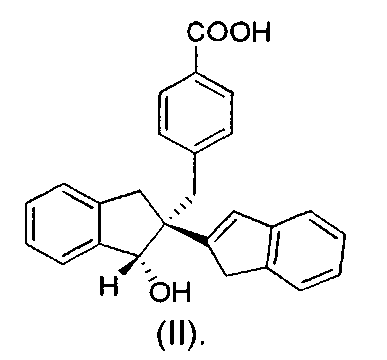
Также предложены фармацевтически приемлемые соли соединения формулы (II) - соединение 2.
Активные энантиомеры были охарактеризованы спектроскопически по их физическим и химическим свойствам и по данным об удерживании, полученным с помощью нормальной и хиральной HPLC.
Было обнаружено, что конкретная энантиомерная форма является особенно полезной для лечения IBD.
В изобретении также предложена N-метил-(D)-глюкаминная соль соединения, имеющая формулу III:
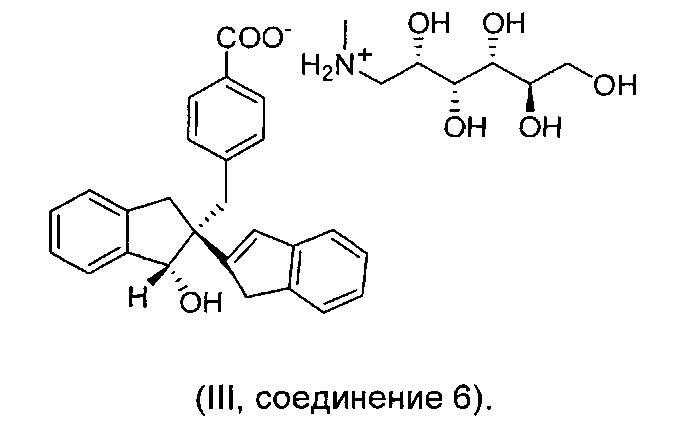
Соединения по изобретению могут кристаллизовываться более чем в одной форме. Эту особенность называют полиморфизмом, и такие полиморфные формы ("полиморфы") находятся в пределах объема настоящего изобретения. Обычно полиморфизм может возникать в ответ на изменения температуры, давления или обоих показателей. Полиморфизм также может возникать в результате изменений в процессе кристаллизации. Полиморфы можно различать по различным физическим характеристикам, известным в области техники, таким как дифракционные рентгенограммы, растворимость и температура плавления.
Некоторые из соединений, описанных в данной заявке, могут существовать в виде стереоизомеров. Объем настоящего изобретения включает смеси стереоизомеров, а также очищенные или обогащенные смеси. Также в объем изобретения включены индивидуальные изомеры соединений по изобретению, а также любые их полностью или частично уравновешенные смеси. Некоторые соединения по изобретению содержат один или более хиральных центров. Следовательно, настоящее изобретение включает рацематы, очищенные энантиомеры и энантиомерно обогащенные смеси соединений по изобретению. Соединения по настоящему изобретению включают рацемические и хиральные индановые димеры.
Соли, включенные в термин "фармацевтически приемлемые соли", относятся к нетоксичным солям соединений по данному изобретению. Соли соединений по настоящему изобретению могут включать соли добавления кислоты.
Изобретение включает сольват любого соединения по изобретению. Термин "сольват" относится к комплексу переменной стехиометрии, образованному растворенным соединением (в данном изобретении соединением по изобретению, или его солью, или его физиологически функциональным производным) и растворителем. Такие растворители, для реализации назначения изобретения, не должны препятствовать биологической активности растворенного соединения. Неограничивающие примеры подходящих растворителей включают, но не ограничены этим, воду, метанол, этанол и уксусную кислоту. Предпочтительно используемый растворитель представляет собой фармацевтически приемлемый растворитель. Неограничивающие примеры фармацевтически приемлемых растворителей включают воду, этанол и уксусную кислоту. Наиболее предпочтительным используемым растворителем является вода.
Изобретение включает пролекарство любого из соединений по изобретению. Термин "пролекарство" относится к любому фармацевтически приемлемому производному соединения по настоящему изобретению, которое при введении млекопитающему способно обеспечивать (прямо или непрямо) соединение по настоящему изобретению или его активный метаболит. Такие производные, например, сложные эфиры и амиды, будут очевидны специалистам в данной области.
В изобретении также предложена фармацевтическая композиция, содержащая любое из соединений, описанных выше.
Активное соединение может присутствовать в лекарственном средстве для применения человеком в подходящих дозах с целью достижения требуемого эффекта. Например, конечная доза может лежать в диапазоне от 0,1 до 10 мг/кг.
Возможно введение соединений по изобретению самих по себе. Однако предпочтительно, чтобы соединения вводили в форме фармацевтического препарата или композиции. Такие композиции могут содержать один или более чем один фармацевтически приемлемый эксципиент, носитель или разбавитель.
Соединения по изобретению могут быть введены множеством различных способов. Соединения могут быть введены перорально. Предпочтительные фармацевтические композиции для перорального введения включают таблетки, капсулы, каплеты, растворы, суспензии или сиропы.
Фармацевтические композиции могут быть предложены в форме с модифицированным высвобождением, такой как капсула или таблетка с длительным высвобождением.
Лекарственное средство может быть введено перорально, парентерально, интраназально, чрескожно или путем ингаляции.
Фармацевтические композиции могут быть приспособлены для введения любым подходящим путем, например, пероральным (включая трансбуккальный или подъязычный), ректальным, назальным, местным (включая трансбуккальный, подъязычный или чрескожный), вагинальным или парентеральным (включая подкожный, внутримускульный, внутривенный или внутрикожный) путем. Такие препараты могут быть получены путем ассоциации активного ингредиента с носителем(ями) или эксципиентом(ами).
Фармацевтические композиции, приспособленные для перорального введения, могут быть представлены в виде дискретных единиц, таких как капсулы или таблетки; порошков или гранул; растворов или суспензий, каждый из которых вместе с водными или неводными жидкостями; пригодных в пищу пенок или спреев; или жидких эмульсий типа «масло в воде» или жидких эмульсий типа «вода в масле». Для перорального введения в виде таблетки или капсулы активный лекарственный компонент может быть объединен с пероральным, нетоксичным фармацевтически приемлемым инертным носителем, таким как этанол, глицерин, вода и им подобные. Порошки могут быть получены путем измельчения соединения до подходящего малого размера и смешивания с соответствующим фармацевтическим носителем, таким как пищевой углеводный крахмал или маннит. Также в состав могут быть включены ароматизаторы, консерванты, диспергирующие агенты, красители и тому подобное.
Капсулы могут быть изготовлены путем приготовления порошка, жидкости или суспензии, и их инкапсуляции в желатин или другой подходящий для оболочки материал. К смеси могут быть добавлены смазывающие вещества, такие как коллоидный кремнезем, тальк, стеарат магния, стеарат кальция или твердый полиэтилен гликоль. Также может быть добавлен дезинтегрирующий или солюбилизирующий агент, такой как карбонат кальция или карбонат натрия для улучшения доступности лекарственного средства после заглатывания капсулы. Также в смесь могут быть включены другие агенты, такие как связующие вещества, смазывающие вещества, дезинтегрирующие агенты, красители. Примеры подходящих связующих веществ включают крахмал, желатин, природные сахара, кукурузные подсластители, природные и синтетические смолы, трагакант, или альгинат натрия, карбоксиметилцеллюлозу, полиэтиленгликоль и тому подобное. Подходящие смазывающие вещества для этих лекарственных форм включают, например, олеат натрия, стеарат натрия, стеарат магния, бензоат натрия, ацетат натрия, хлорид натрия и тому подобное. Подходящие дезинтеграторы включают, не ограничиваясь этим, крахмал, метилцеллюлозу, агар, бентонит, ксантановую смолу и тому подобное.
Таблетки могут быть изготовлены путем получения порошковой смеси, гранулирования этой смеси, добавления смазывающего вещества и разрыхлителя, и прессования в таблетки. Порошковая смесь может быть получена путем смешивания подходящим образом измельченного соединения с разбавителем или основой, как описано выше. Дополнительные ингредиенты включают связующие, такие как карбоксиметилцеллюлоза, альгинаты, желатины или поливинилпирролидон, ингибиторы растворения, такие как парафин, ускорители резорбции, такие как четвертичные соли и/или агенты абсорбции, такие как бентонит, каолин или тому подобное. Порошковая смесь может быть гранулирована во влажном состоянии со связующим, таким как патока, крахмальный клейстер или растворы целлюлозных или полимерных материалов, и прессования через сито.
Соединения по настоящему изобретению также могут быть объединены со свободно сыпучим инертным носителем и спрессованы в таблетки непосредственно без прохождения через другие шаги, такие как гранулирование. Может быть предложено прозрачное или непрозрачное защитное покрытие, состоящее из герметичного покрытия подходящего вещества, такого как шеллак, сахар или полимерное вещество, и лаковое покрытие, например, из воска. При необходимости в эти покрытия могут быть добавлены красители для различения различных стандартных лекарственных форм.
Пероральные жидкости, такие как растворы, сиропы, и эликсиры могут быть приготовлены в виде стандартной лекарственной формы, содержащей заранее определенное количество соединения. Сиропы могут быть получены, например, путем растворения соединения в водном растворе, ароматизированном соответствующим образом, в то время как эликсиры получают с использованием нетоксичного спиртового разбавителя. Суспензии могут быть приготовлены путем диспергирования соединения в нетоксичном разбавителе. Также могут быть добавлены солюбилизаторы и эмульгаторы, такие как этоксилированные изостеариловые спирты и простые эфиры полиоксиэтиленсорбита, консерванты; вкусовые добавки, такие как масло перечной мяты, или натуральные подсластители, сахарин, или другие искусственные подсластители и тому подобное.
В случае необходимости, стандартные лекарственные формы для перорального введения могут быть помещены в микрокапсулы. Также может быть получен препарат с пролонгированным или замедленным высвобождением, как, например, путем покрытия или включения измельченного вещества в подходящие полимеры, воск или тому подобное.
Описанные здесь соединения и их соли, сольваты, и физиологические функциональные производные, можно также вводить в форме липосомных систем доставки, таких как небольшие однослойные везикулы, большие однослойные везикулы, и многослойные везикулы. Липосомы могут быть образованы из различных фосфолипидов, таких как холестерин, стеариламин или фосфатидилхолины.
Соединения по изобретению и их соли, сольваты, и физиологически функциональные производные также могут быть доставлены с использованием моноклональных антител в качестве индивидуальных носителей, с которыми соединены молекулы соединения.
Соединения также могут быть сопряжены с растворимыми полимерами в качестве носителей лекарственных средств. Такие полимеры могут включать, например, поливинилпирролидон (ПВП). Соединения также могут быть сопряжены с биодеградируемым полимером, обеспечивающим контролируемое высвобождение лекарственного средства. Такие полимеры включают полимолочную кислоту, полицианоакрилаты и блок-сополимеры гидрогелей.
Фармацевтические композиции, приспособленные для чрескожного введения, могут быть представлены в виде отдельных пластырей, предназначенных для того, чтобы оставаться в тесном контакте с эпидермисом/кожей пациента в течение длительного периода времени. Например, активный ингредиент может быть доставлен из пластыря путем ионтофореза.
Фармацевтические композиции, приспособленные для местного введения, могут быть приготовлены в виде мазей, кремов, суспензий, лосьонов, порошков, растворов, паст, гелей, спреев, аэрозолей или масел. Для лечения наружных тканей композиции могут быть применены в качестве мази или крема для местного применения.
Для местного введения во рту препарат может использоваться в виде таблеток для рассасывания, пастилок и жидкости для полоскания рта.
Для интраназального введения может быть использован порошок, имеющий размер частиц в диапазоне от 20 до 500 мкм. Порошок можно вводить с помощью быстрой ингаляции через носовой проход из емкости с порошком, поднесенной близко к носу. Подходящие препараты, в которых носителем является жидкость, для введения в виде назального спрея или назальных капель, включают водные или масляные растворы активного ингредиента.
Фармацевтические композиции, приспособленные для введения путем ингаляции, включают мелкодисперсные порошки или аэрозоли, которые могут быть получены посредством дозированных аэрозолей под давлением, небулайзеров или инсуфляторов и тому подобного.
Для ректального введения композиция может быть представлена в виде суппозиториев или в виде клизмы.
Для вагинального введения композиция может быть представлена в виде пессариев, тампонов, кремов, гелей, спреев или тому подобного.
Для парентерального введения композиция может быть представлена в виде водных и неводных стерильных растворов для инъекций, которые могут содержать различные добавки, такие как антиоксиданты, буферы, бактериостатические и растворенные вещества, которые делают препарат изотоничным крови предполагаемого реципиента; водных и неводных стерильных суспензий, которые могут включать суспендирующие агенты и загустители. Композиции могут быть представлены в контейнерах единичной или многократной дозы, например, в герметичных ампулах и флаконах, и могут храниться в сублимированном (лиофилизированном) состоянии, требующем добавления только стерильного жидкого носителя, например, воды для инъекций, непосредственно перед использованием. Приготовленные для немедленного применения растворы и суспензии для инъекций могут быть приготовлены из стерильных порошков, гранул и тому подобного.
Соединения по настоящему изобретению и их соли, сольваты, и физиологически функциональные производные, могут применяться отдельно или в комбинации с другими терапевтическими агентами. Соединение по изобретению и другое(ие) фармацевтически активное вещество(а) может(гут) быть введено(ы) вместе или по отдельности. При раздельном введении, введение может осуществляться одновременно или последовательно в любом порядке. Количество соединения по изобретению и другого(их) фармацевтически активного(ых) вещества (веществ) и соответствующие временные периоды введения могут быть выбраны с целью достижения необходимого комбинированного терапевтического эффекта. Введение соединения по изобретению, его солей, сольватов или физиологически функциональных производных в сочетании с другими терапевтическими агентами может осуществляться в комбинации путем одновременного введения либо в одной фармацевтической композиции, содержащей об а соединения, либо в отдельных фармацевтических композициях, каждая из которых содержит одно из соединений. В некоторых случаях комбинация лекарственных средств может вводиться по отдельности в последовательном порядке, когда один агент вводят первым, а второй агент вводят вторым или наоборот. Такое введение может производиться примерно в один и тот же период времени или в течение более длительного времени.
Краткое описание фигур
Изобретение будет более ясным для понимания из следующего описания, приведенного исключительно в качестве примера, где:
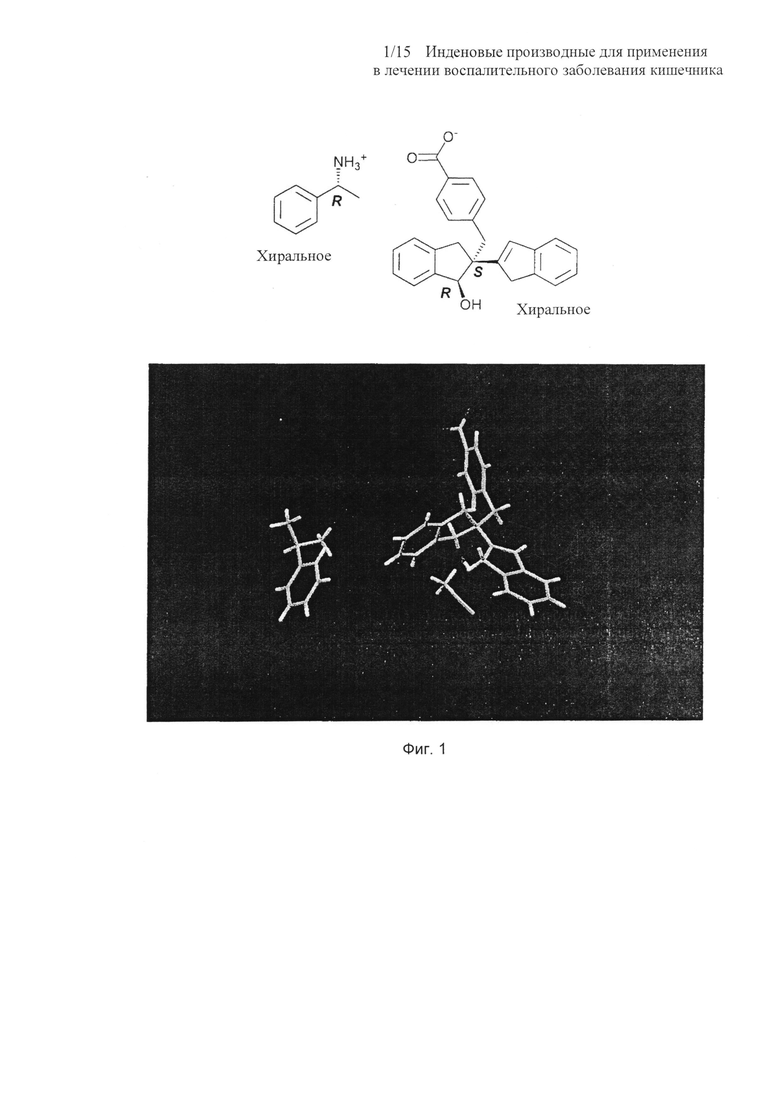
На Фиг. 1 представлена рентгеновская кристаллическая структура, показывающая абсолютную стереохимию энантиомерного соединения 4-(R)-(+)-метилбензиламинной соли (соединение 9);
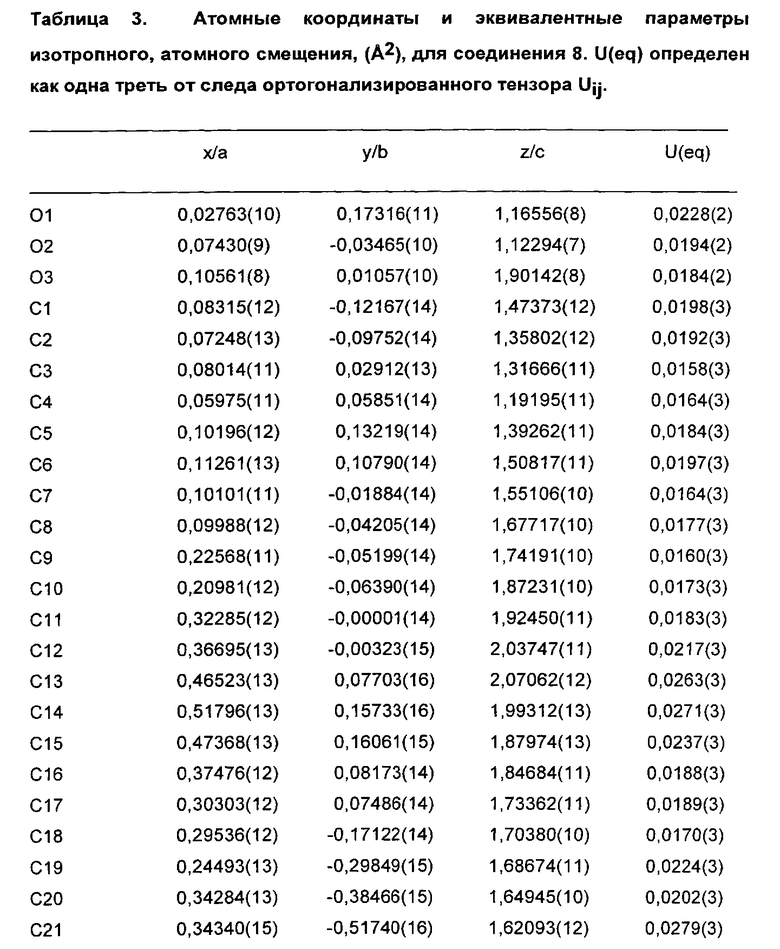
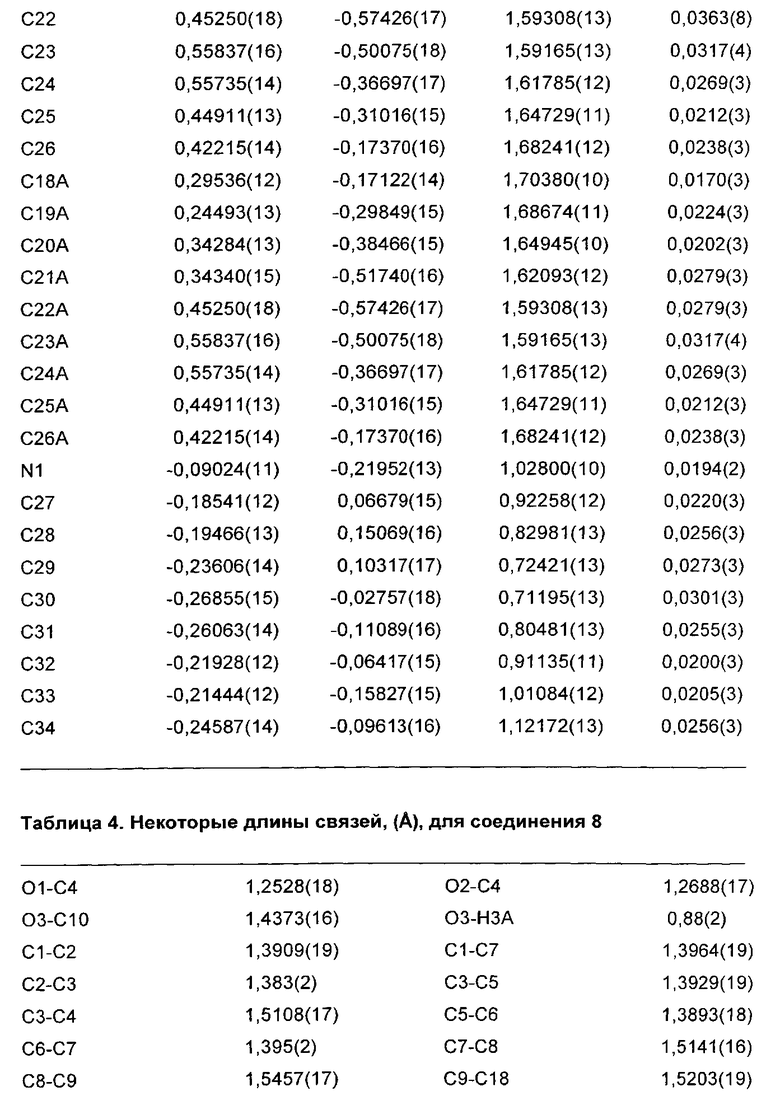
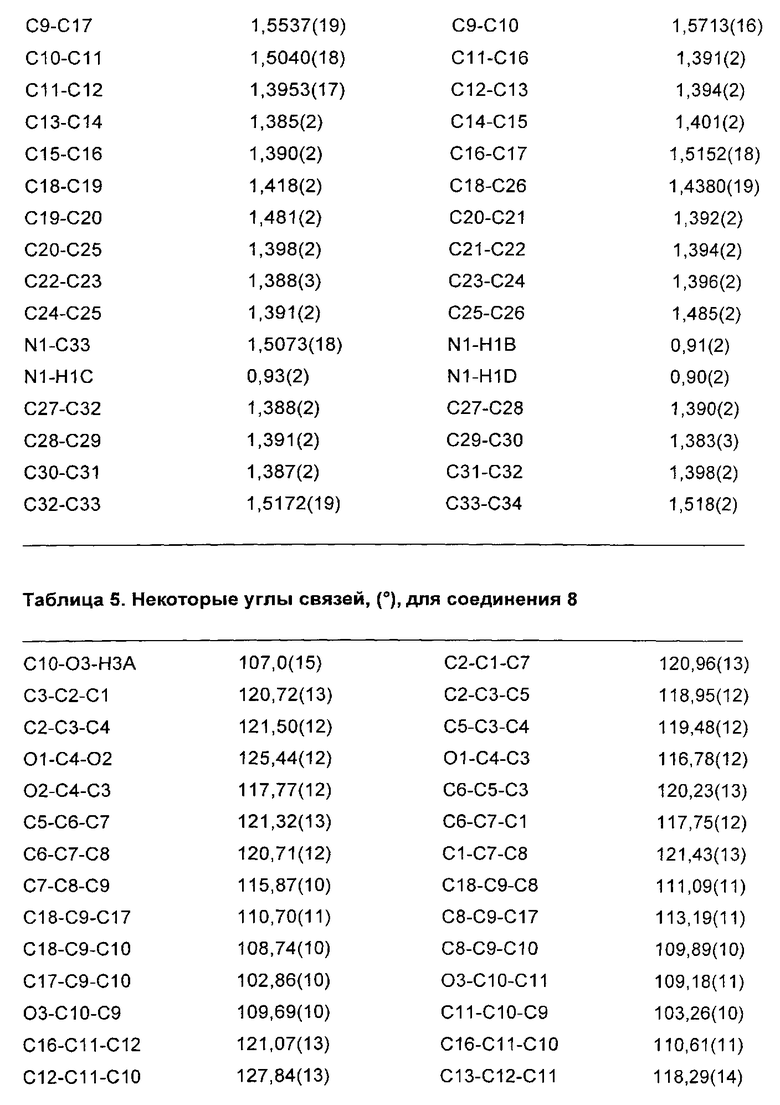
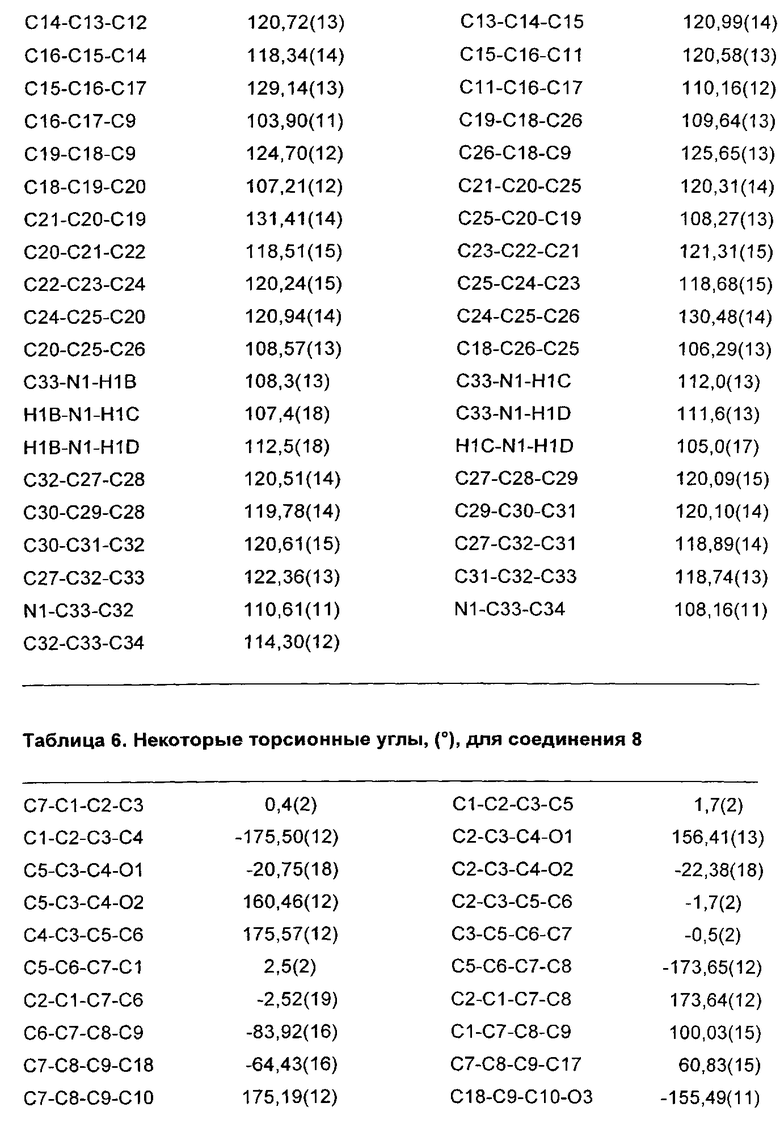
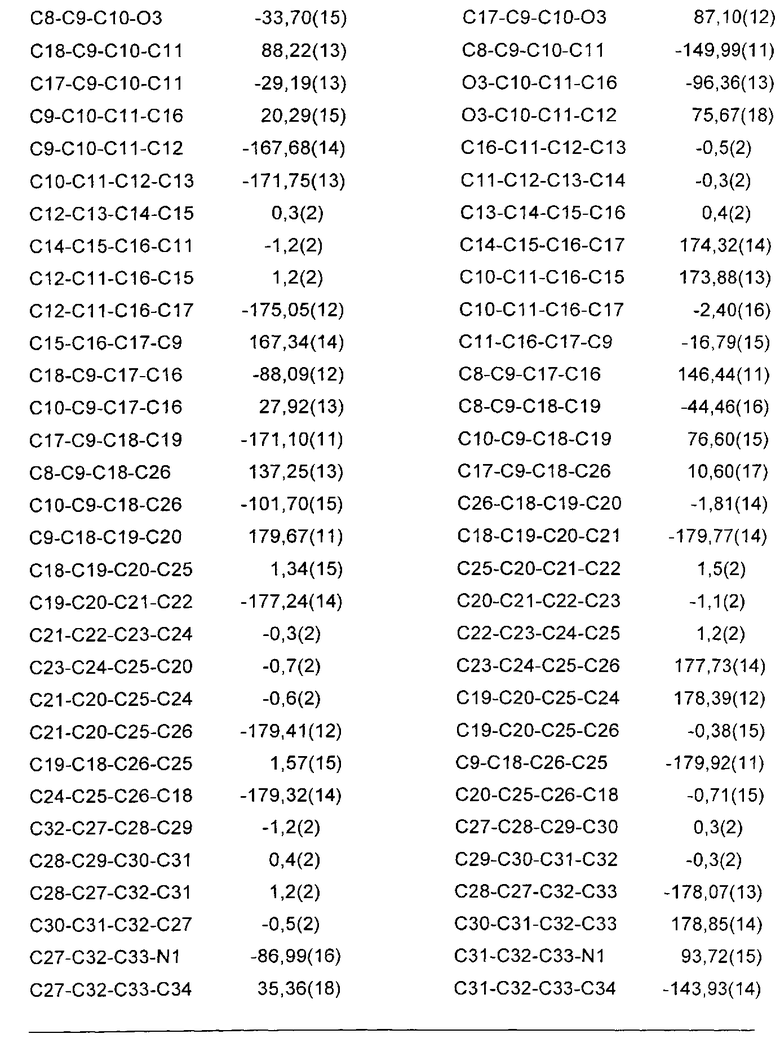
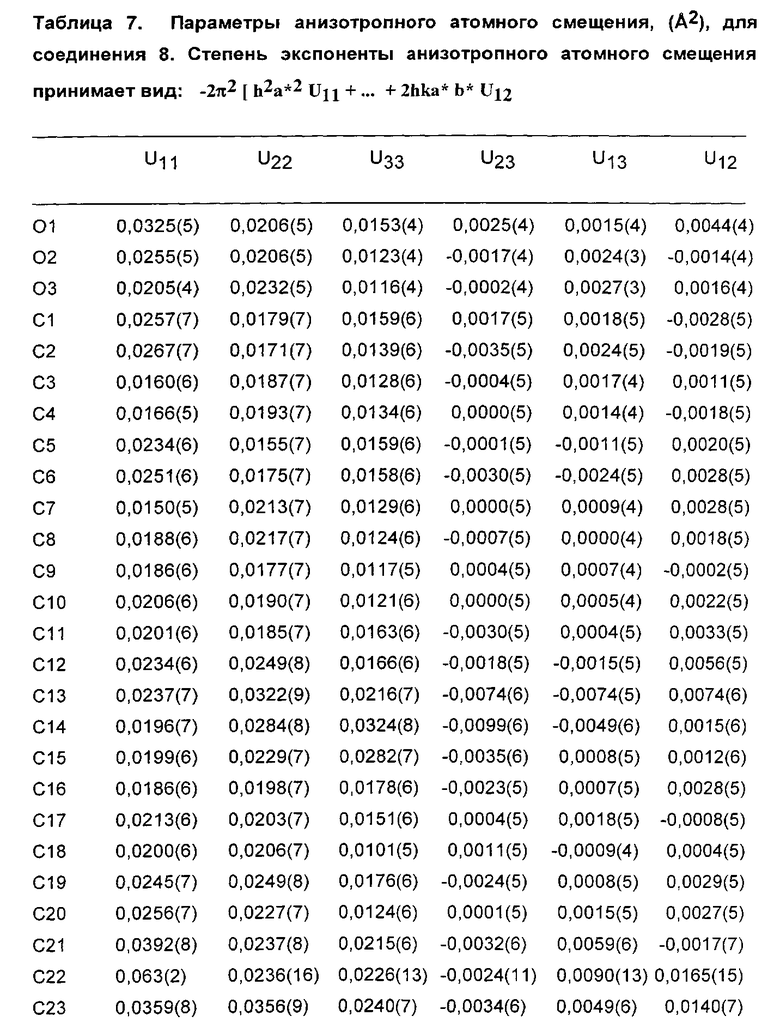
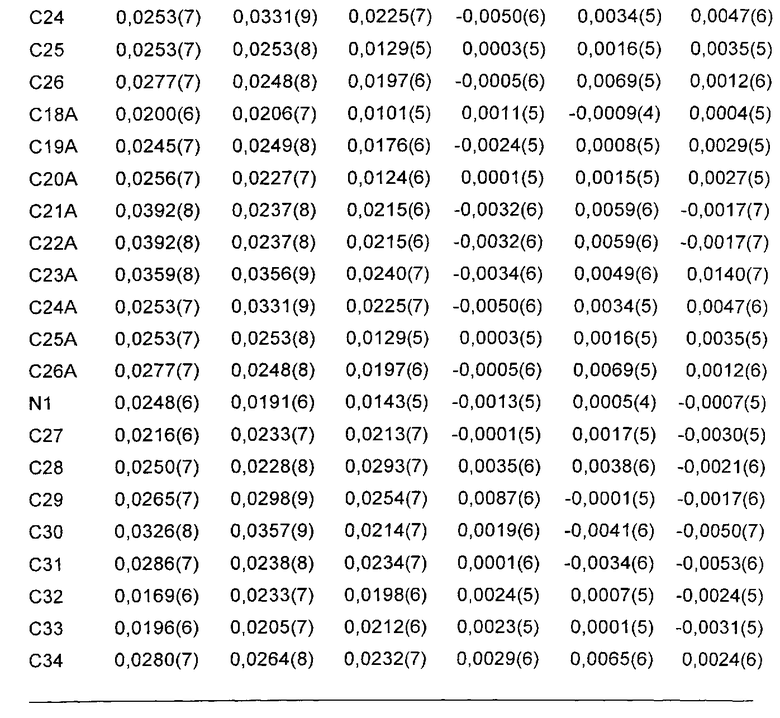
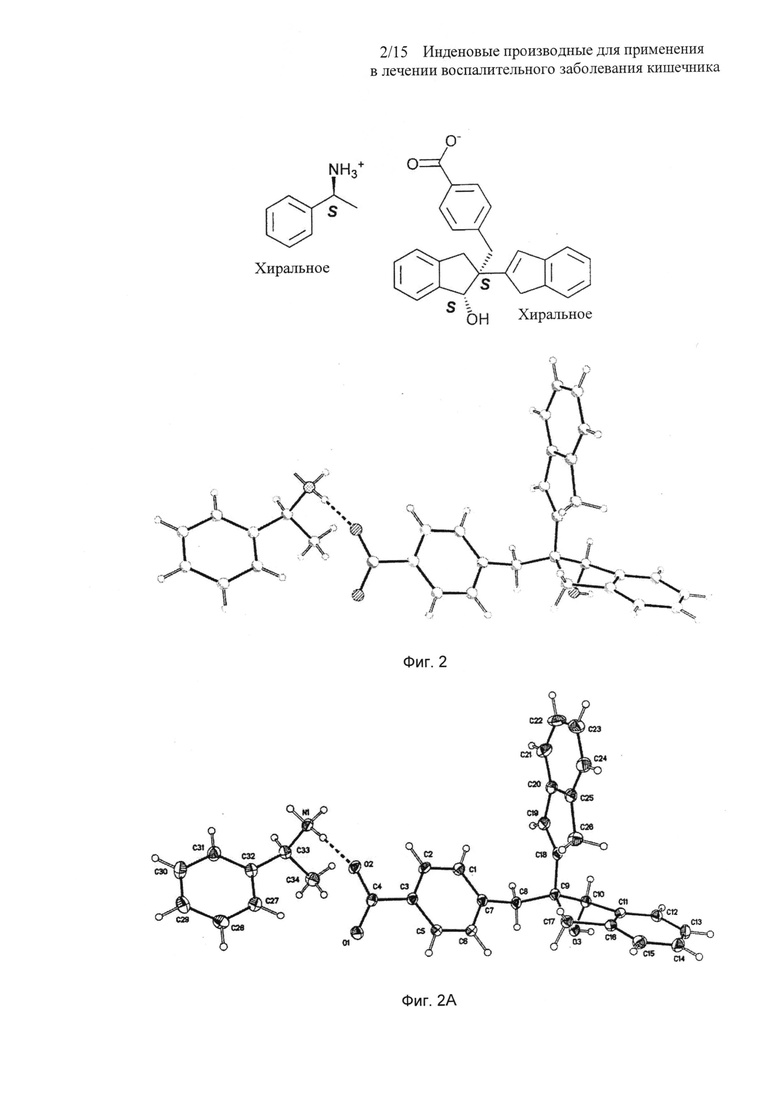
На Фиг. 2 представлена рентгеновская кристаллическая структура, показывающая абсолютную стереохимию энантиомерного соединения 2-(S)-(-)-метилбензиламинной соли (соединение 8);
На Фиг. 2A представлен вид молекулы соединения 8 из кристаллической структуры, показывающий использованный алгоритм нумерации. Эллипсоиды анизотропного атомного смещения неводородных атомов показаны на уровне 50%-ной вероятности. Атомы водорода показаны с условным малым радиусом. Показан только главный компонент разупорядочения;
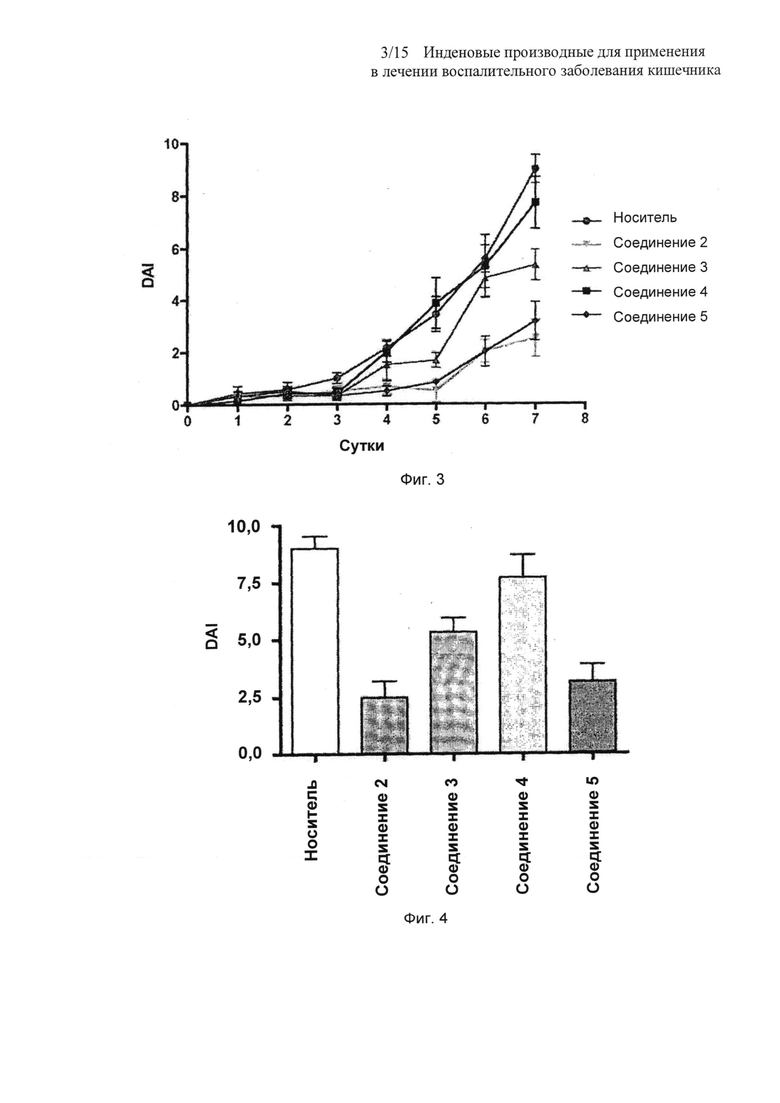
На Фиг. 3 представлен график влияния соединений 2, 3, 4 и 5 при дозировке 30 мг/кг на индекс активности заболевания (DAI) в течение 7 суток при колите, индуцированном 5% DSS (декстран сульфата натрия);
На Фиг. 4 представлена столбчатая диаграмма влияния соединений 2, 3, 4 и 5 при дозировке 30 мг/кг на индекс активности заболевания (DAI) на 7 сутки при колите, индуцированном 5% DSS;
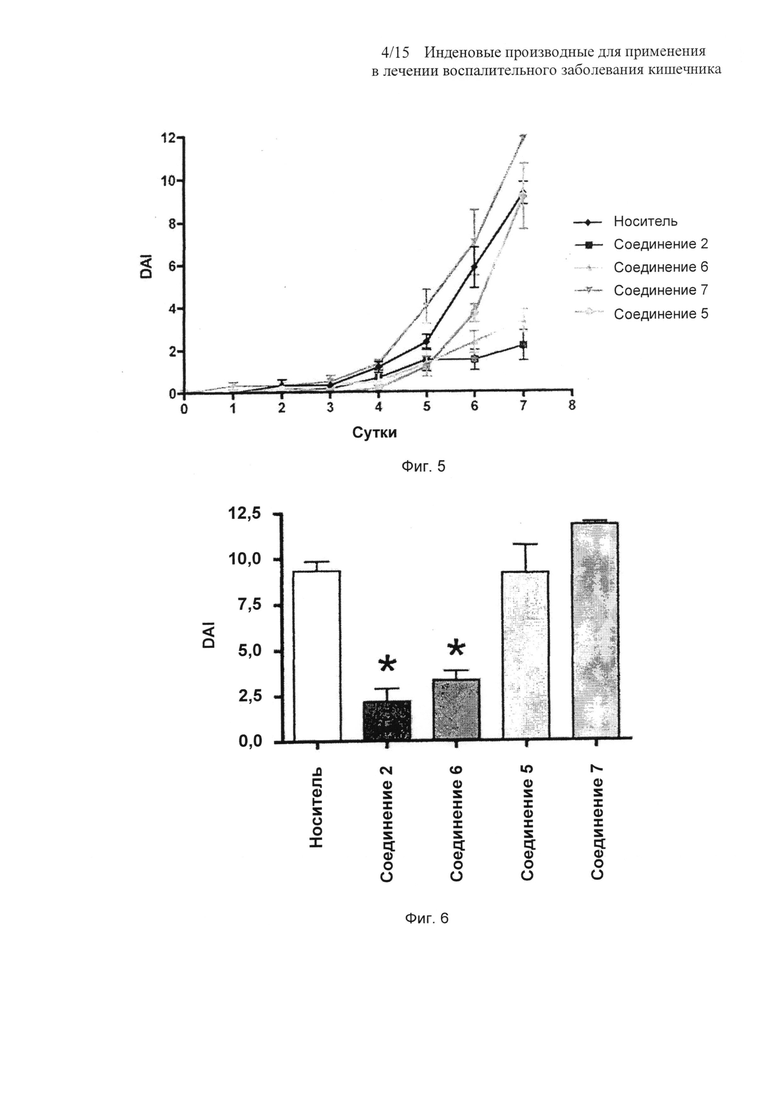
На Фиг. 5 представлен график влияния соединений 5, 7, 2 и 6 при дозировке 10 мг/кг на индекс активности заболевания (DAI) в течение 7 суток при колите, индуцированном 5% DSS;
На Фиг. 6 представлена столбчатая диаграмма влияния соединений 5, 7, 2 и 6 при дозировке 10 мг/кг на индекс активности заболевания (DAI) на 7 сутки при колите, индуцированном 5% DSS. Звездочками отмечены значимые (P<0.05) отличия (однофакторный дисперсионный анализ (ANOVA)) от контрольной группы с носителем.
На Фиг. 7 представлен график, показывающий влияние соединения 6 на потерю веса у мышей, обрабатываемых 5% DSS. Данные представляют собой среднее ± SEM (стандартная ошибка среднего) от 6-7 мышей на группу;
На Фиг. 8 представлен график, показывающий влияние соединения 6 на DAI у мышей, обрабатываемых 5% DSS. Данные представляют собой среднее ± SEM (стандартная ошибка среднего) от 6-7 мышей на группу;
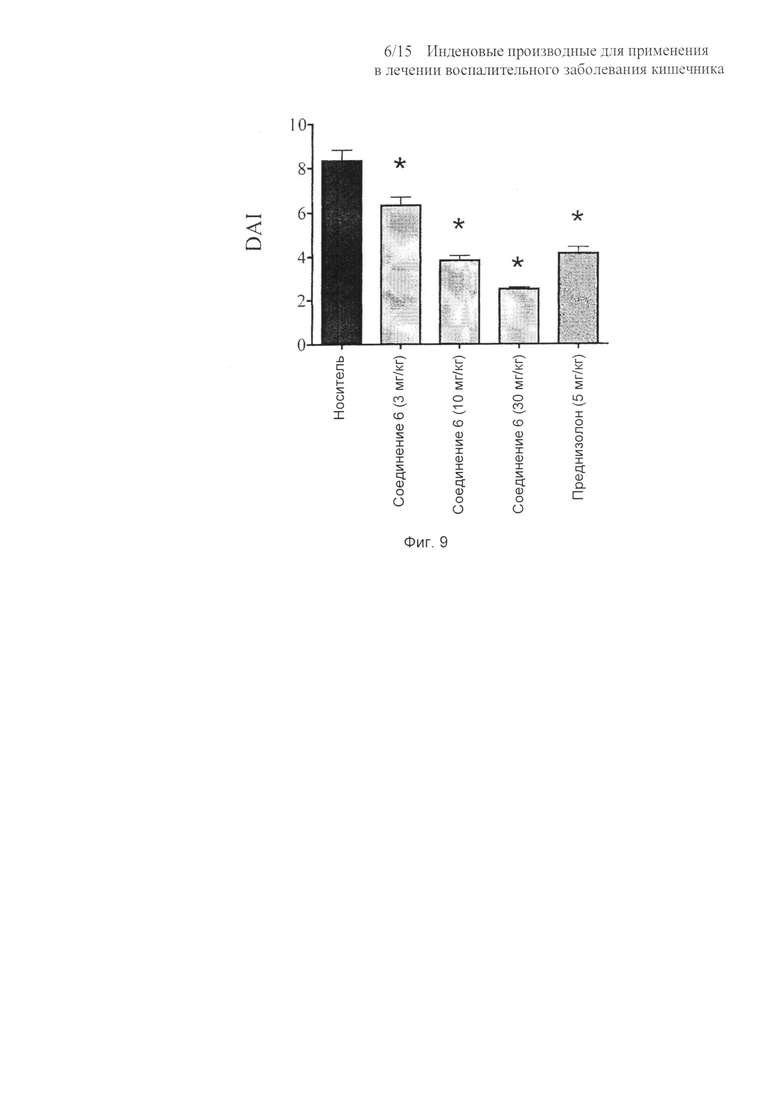
На Фиг. 9 представлена столбчатая диаграмма, показывающая влияние соединения 6 на DAI у мышей, обрабатываемых 5% DSS, на 7 сутки. Данные представляют собой среднее ± SEM. Звездочками отмечены значимые (P<0,05) отличия (однофакторный ANOVA) от контрольной группы с носителем;
На Фиг. 10 представлена столбчатая диаграмма, показывающая влияние соединения 6 на длину толстой кишки у мышей, обрабатываемых 5% DSS, на 7 сутки. Звездочками отмечены значимые (P<0,05) отличия (однофакторный ANOVA) от контрольной группы с носителем;
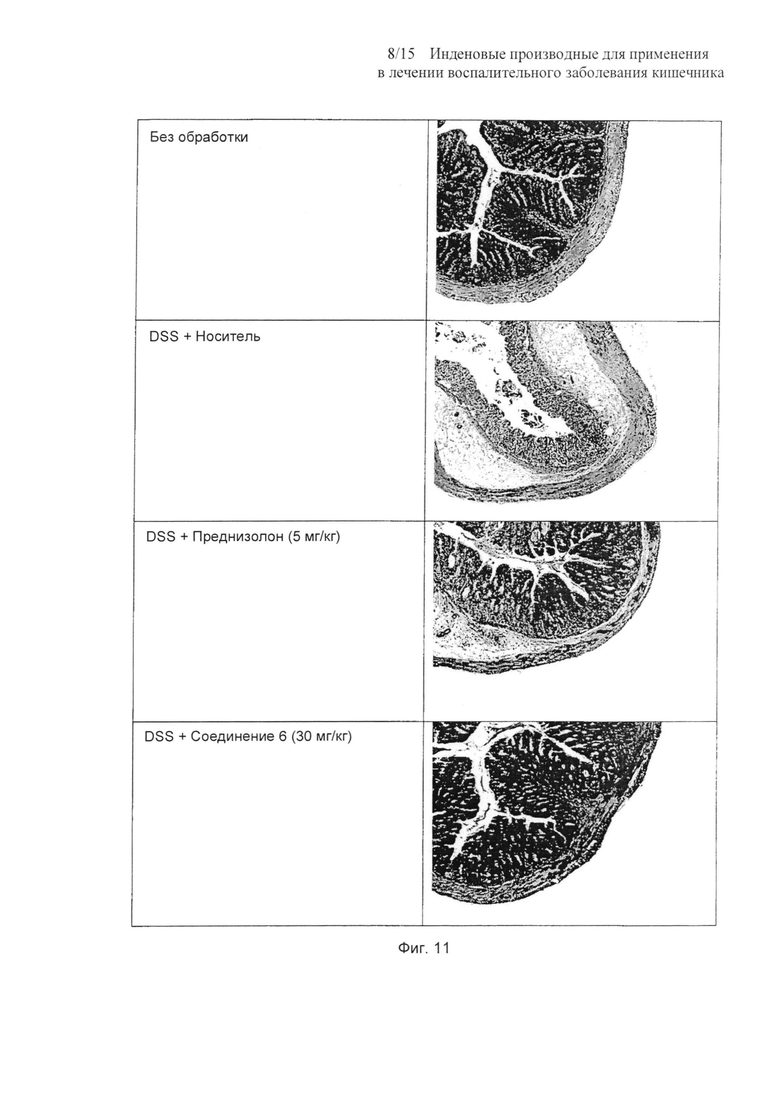
На Фиг. 11 представлены репрезентативные гематоксилин- и эозинокрашенные срезы дистальных отделов толстой кишки мышей. Показаны большие увеличения (X10);
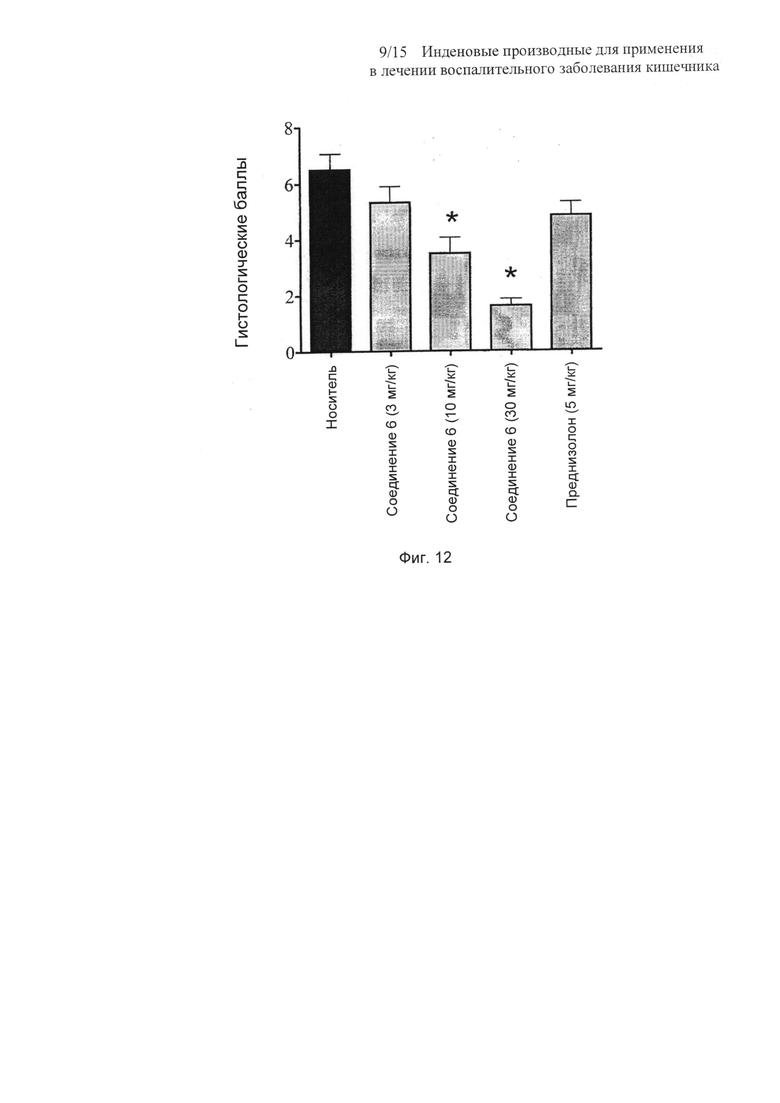
На Фиг. 12 представлена столбчатая диаграмма, показывающая влияние соединения 6 на гистологические баллы толстых кишок у мышей, обрабатываемых DSS. Данные представляют собой среднее ± SEM от 5-6 мышей. Звездочками отмечены значимые (P<0,05) отличия (однофакторный ANOVA) от контрольной группы с носителем. Внимание, максимальное количество баллов - 10;
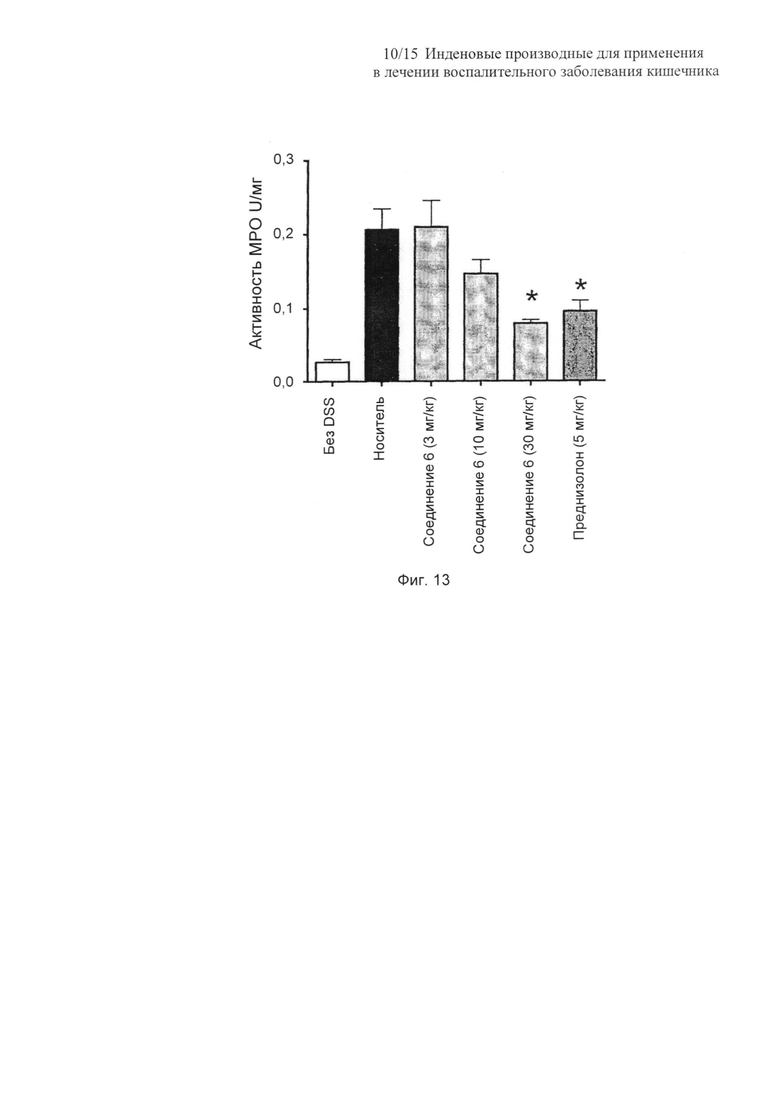
На Фиг. 13 представлена столбчатая диаграмма, показывающая активность миелопероксидазы (МРО) в толстых кишках необрабатываемых или обрабатываемых носителем, а также обрабатываемых преднизолоном и соединением 6 мышей, которых подвергали воздействию 5% DSS. Данные представляют собой среднее ± SEM от 5-6 мышей. Звездочками отмечены значимые (P<0,05) отличия (однофакторный ANOVA) от контрольной группы с носителем;
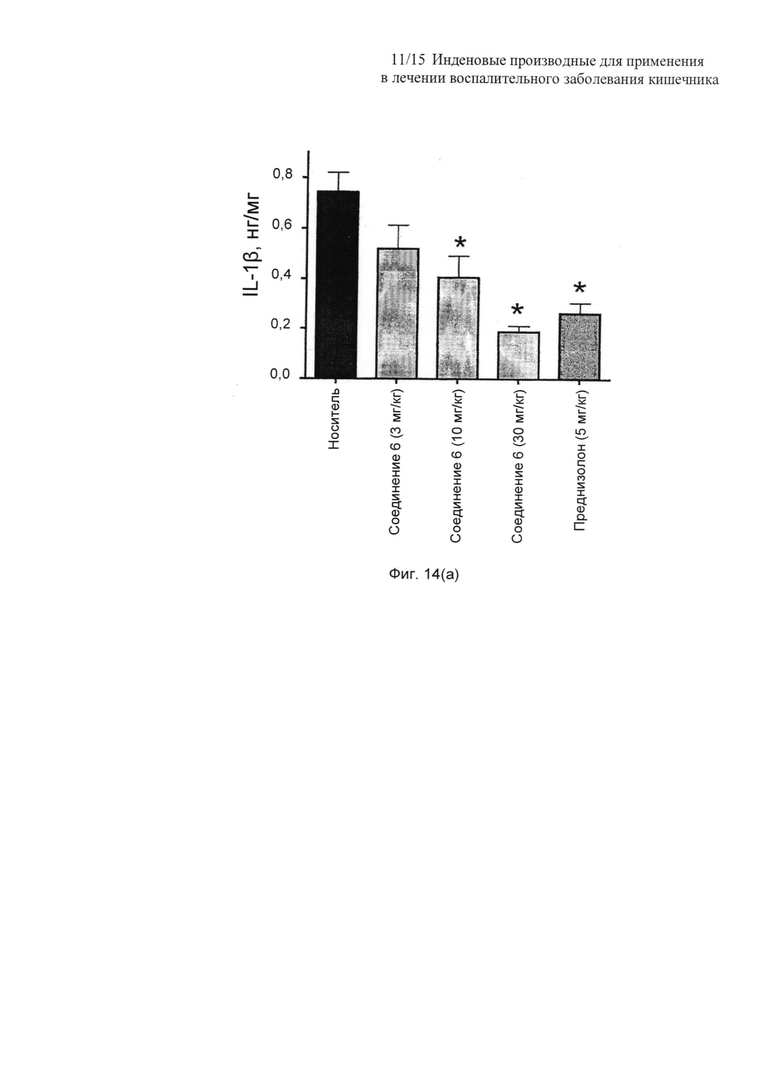
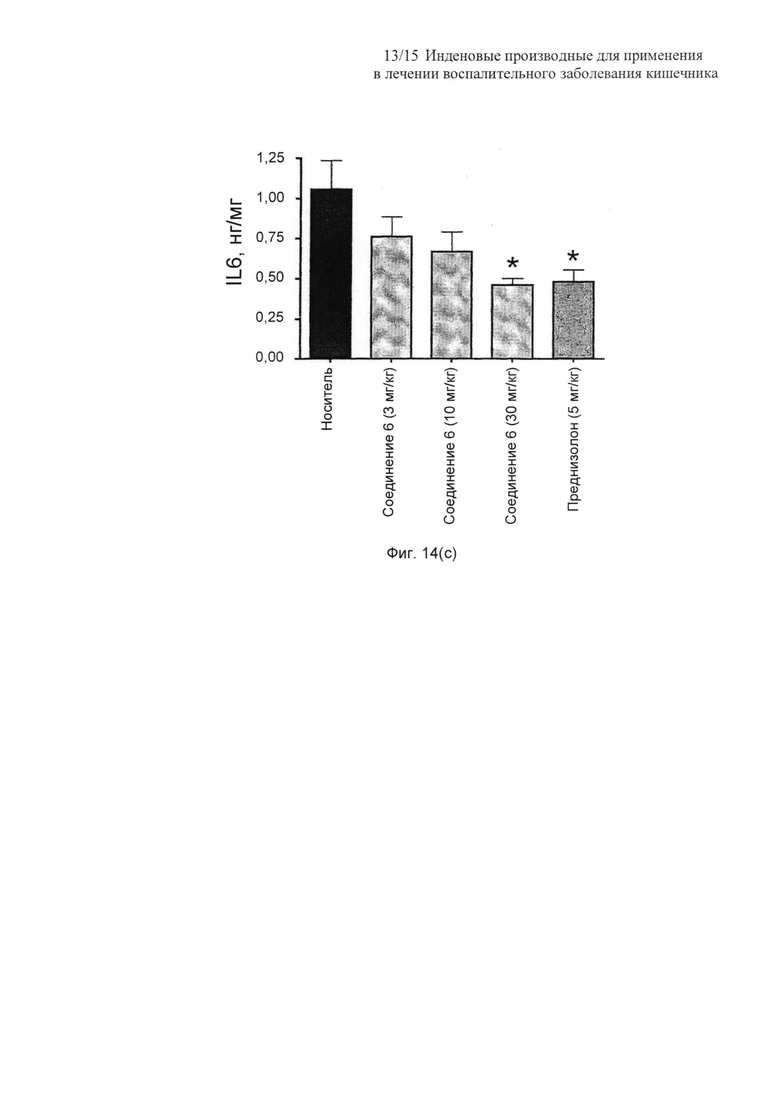
На Фиг. 14 (a)-(c) представлены столбчатые диаграммы, показывающие влияние соединения 6 на уровни цитокинов (IL1β, TNFα и IL6) у мышей, обрабатываемых DSS. Данные представляют собой среднее ± SEM от 5-6 мышей. Звездочками отмечены значимые (P<0,05) отличия (однофакторный ANOVA) от контрольной группы с носителем;
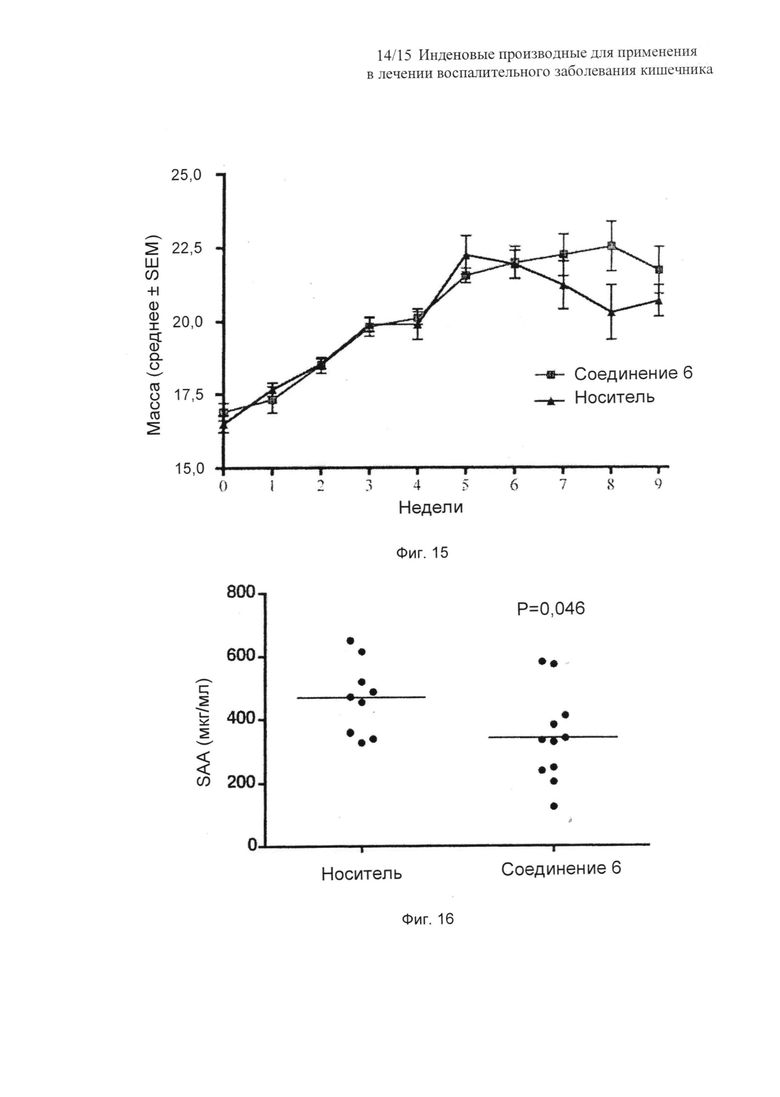
На Фиг. 15 представлен график, показывающий потерю массы у IL10--/-- мышей, обрабатываемых носителем или соединением 6. Мышам вводили соединение 6 (300 мг/кг/неделя) или носитель перорально по расписанию дозировки понедельник/среда/пятница (MWF). Возраст мышей составлял около 4 недель в начале эксперимента, и мышей обрабатывали в течение 9 недель. Мышей взвешивали еженедельно, и данные представляют собой среднее ± SEM от 9-12 мышей на группу. Мышей контролировали на наличие заболевания с явной клинической картиной, ректальный пролапс, и агонизирующих животных гуманно умерщвляли;
На Фиг. 16 представлен график разброса, показывающий уровни сывороточного амилоида A (SAA) индивидуальных мышей, и среднее (полоса), от выживших животных на неделе 9 (11 и 9 мышей в группах обработки соединением 6 и носителем, соответственно). Для теста на статистические различия между группами использовали t-критерий Стьюдента;
На Фиг. 17 представлены репрезентативные гематоксилин- и эозин-окрашенные срезы дистальных отделов толстой кишки IL10--/-- мышей, обрабатываемых в течение 9 недель носителем или соединением 6; и
На Фиг. 18 представлен график разброса, показывающий гистологические баллы дистальных отделов толстой IL10--/-- мышей, обрабатываемых носителем или соединением 6, где график разброса показывает гистологические баллы индивидуальных мышей, и среднее (полоса), от выживших животных на 9 неделе (11 и 9 мышей в группах обрабатывания соединением 6 и носителем, соответственно). Для теста на статистические различия между группами использовали t-критерий Стьюдента.
Подробное описание изобретения
Соединение 1 представляет собой пару диастереомеров, которые получены в результате восстановления и деметилирования кетонного соединения A, которое имеет хиральный центр по C-2, и вследствие этого представляет собой пару энантиомеров.
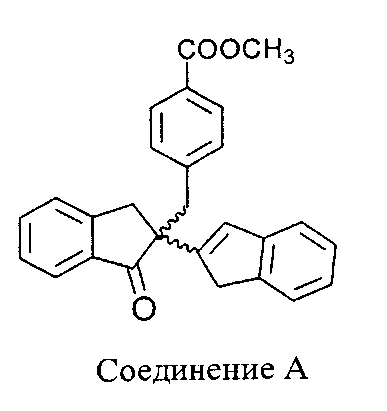
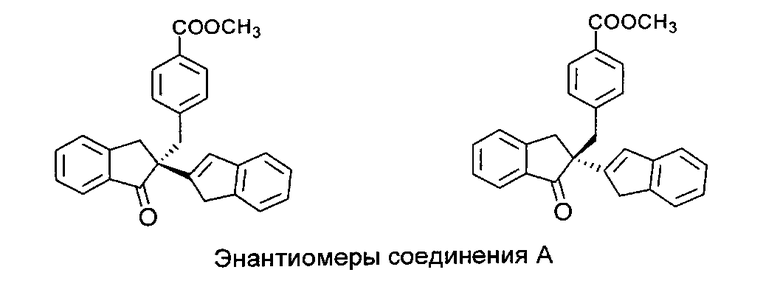
Восстановление этого соединения с помощью LiAlH4 дает соединение формулы
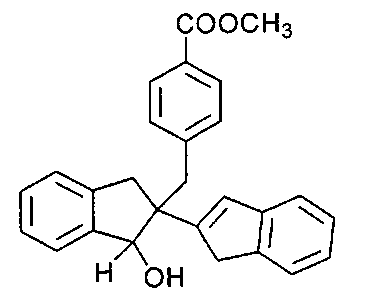
Это соединение включает два диастереомера:
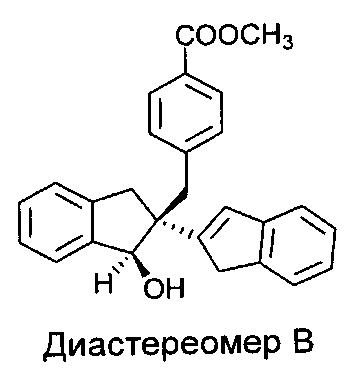
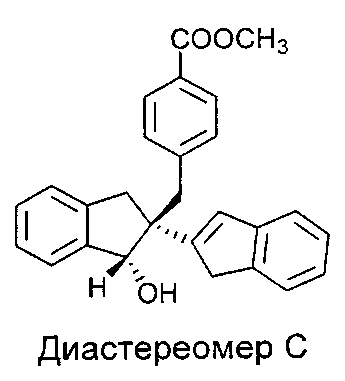
Гидролиз Диастереомера B дает соединения 2 и 3
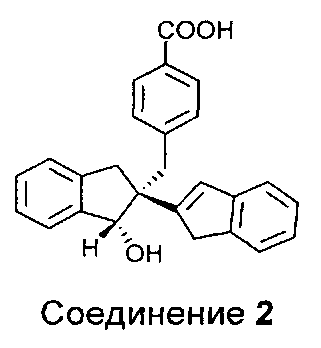
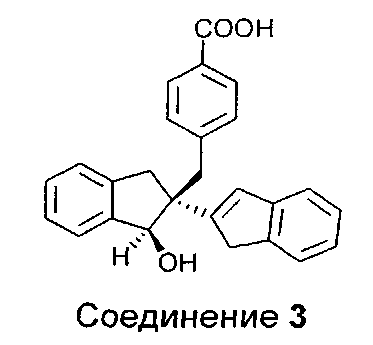
Гидролиз Диастереомера C дает соединения 4 и 5.
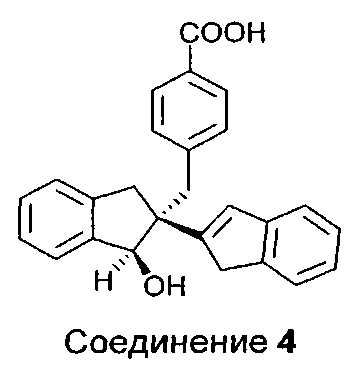
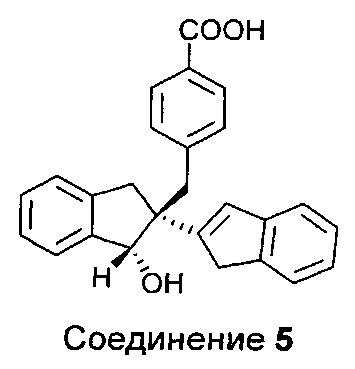
Диастереомеры могут быть разделены химически или хроматографически на составляющие их энантиомеры.
Абсолютная стереохимия соединения 4 была установлена посредством монокристаллической рентгеновской дифракции (R)-(+)-метилбензиламинной соли соединения 4 (соединение 9) (Фиг. 1).
Абсолютная стереохимия соединения 2 была подтверждена посредством монокристаллической рентгеновской дифракции (S)-(-)-метилбензиламинной соли соединения 2 (соединение 8) (Фиг. 2 и 2A).
Общие реакционные процедуры
Общие синтетические процедуры сочетания энантиомерных смесей, как проиллюстрировано ниже, описаны в WO9720806A, полное содержание которой включено в данную заявку посредством ссылки.
Общее получение кислотного производного соединения A
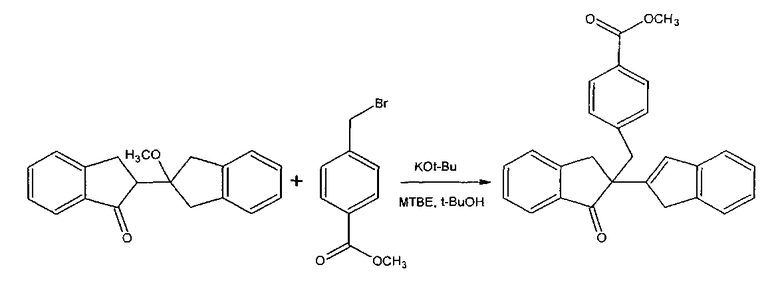
К перемешиваемому раствору продукта сочетания (4 ммоль, 1,00 г) в трет-бутаноле (5 мл) и диэтиловом эфире (30 мл) в атмосфере азота добавляли метил-(4-бромметил)бензоат (6 ммоль, 1,41 г). К нему медленно по каплям добавляли раствор трет-бутоксида калия в трет-бутаноле (30 мл) и диэтиловый эфир (5 мл). С каждой каплей раствор становился желтого цвета, и затем возвращался к первоначальному серому цвету. Смесь перемешивали в течение последующих 3 часов до тех пор, пока посредством TLC (тонкослойная хроматография) (80:20 гексан:этилацетат) не показывали отсутствие исходного вещества. Реакционную смесь гасили путем добавления насыщенного раствора NH4Cl. Слои разделяли, и водный слой экстрагировали диэтиловым эфиром (2×120 мл). Объединенные органические слои промывали водой, рассолом, сушили над MgSO4 и упаривали. Твердый продукт осаждали из неочищенного материала после удаления большей части растворителя. Его отфильтровывали и промывали холодным диэтиловым эфиром с получением 0,98 г (62%) кремового твердого вещества.
Восстановление метилбензоатного соединения
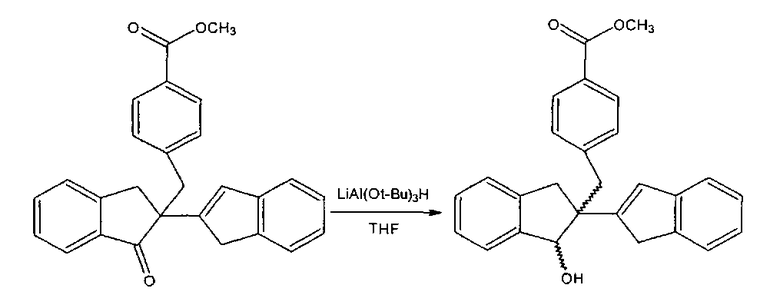
К перемешиваемому раствору метилбензоатного соединения (1,27 ммоль, 0,50 г) в THF (тетрагидрофуран) (15 мл) медленно порциями добавляли лития три-трет-бутоксиалюминогидрид (1,9 ммоль, 0,48 г). Реакцию контролировали посредствоми TLC (80:20, гексан:этилацетат), и по прошествии 3 ч. все исходное вещество было израсходовано.
Реакционную смесь гасили путем ее переноса на лед, и неочищенный продукт экстрагировали этилацетатом путем перемешивания водной смеси в течение 10-15 мин с этилацетатом, последующего переноса в делительную воронку, и затем оставляли до разделения. Объединенные органические слои промывали водой, рассолом, сушили над MgSO4 и упаривали с получением 0,34 г (68%) кремово-золотистого твердого вещества. Продукт выделяли в виде смеси двух диастереомеров в приблизительном соотношении 2:1.
Результаты анализов смеси двух диастереомеров
Там где это возможно, значение для побочного диастереомера дано в квадратных скобках.
Гидролиз метилбензоатной группировки
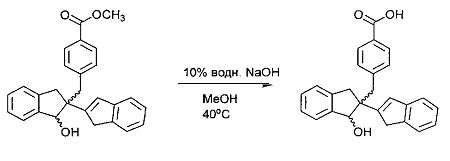
Сложный эфир помещали в круглодонную колюу и добавляли 10% водный NaOH (1 мл), затем добавляли достаточное количество метанола для получения раствора (6 мл). Раствор нагревали до 40°C и контролировали посредством TLC (80:20, гексан:этилацетат). По прошествии приблизитель 4 ч., более не наблюдали сложного эфира.
Смесь охлаждали и добавляли насыщенный NH4Cl (раствор при pH 12). Добавляли разбавленный HCl до кислого pH (pH 2). Продукт экстрагировали из мутного раствора этилацетатом (3×10 мл). Объединенные экстракты сушили над MgSO4 и упаривали в вакууме с получением 0,15 г (количественно) кремового твердого вещества. Продукт выделяли в виде смеси двух диастереомеров в соотношении приблизительно 2:1.
Результаты анализов смеси двух диастереомеров
Там где это возможно, значение для побочного диастереомера дано в квадратных скобках.
Химическое разделение энантиомеров
Получение N-BOC (N-трет-бутоксикарбонил) D-фенилаланиновое производного метилбензоатного диастереомера и/или разделение последующих диастереомеров α1 и α2 (или β1 и β2)
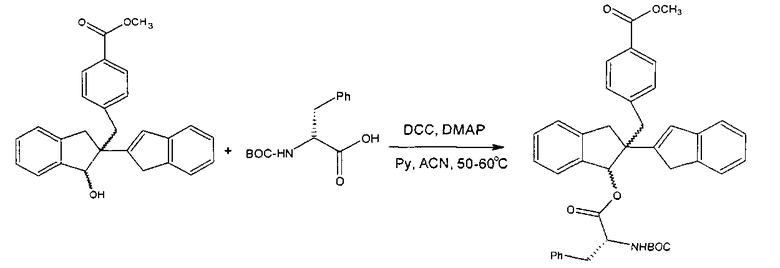
Внимание: процедура применима к обоим диастереомерам, но пример приведен для первого диастереомера.
Диастереомер A (2,5 ммоль, 1,0 г) и N-BOC D-фенилаланин (3,1 ммоль, 0,8 г) помещали в круглодонную колбу, снабженную обратным холодильником и суспендировали в CH3CN (25 мл) в атмосфере азота. К этой суспензии добавляли пиридин (3,1 ммоль, 0,3 мл), затем добавляли раствор DCC (N, N′-дициклогексилкардобиимид) (3,1 ммоль, 0,7 г) и DMAP (4-диметиламинопиридин) (10 мол. %, 0,25 ммоль, 0,05 г) в CH3CN (2 мл). Смесь перемешивали в течение 20 ч. при 50°C, и затем оставляли до достижения комнатной температуры.
Белое твердое вещество отфильтровывали и растворитель удаляли в вакууме. Добавляли этилацетат и полученный раствор промывали 10% H2SO4, насыщенным NaHCO3, сушили над MgSO4 и упаривали с получением 2,1 г желтого масла (83% чистоты согласно HPLC, выход: количественный).
Диастереомеры α1 и α2 разделяли посредством флэш-хроматографии (90 г диоксида кремния/г продукта), используя градиент гексан/МТВЕ (метил-трет-бутиловый простой эфир) 90:10. Из 4,17 г смеси получали 1,3 г производного α2 (а также 1,71 г производного α1 и 0,3 г в виде смеси обоих).
Гидролиз N-BOC D-фенилаланинового производного метилбензоатного соединения (α1, α2, β1 или β2)
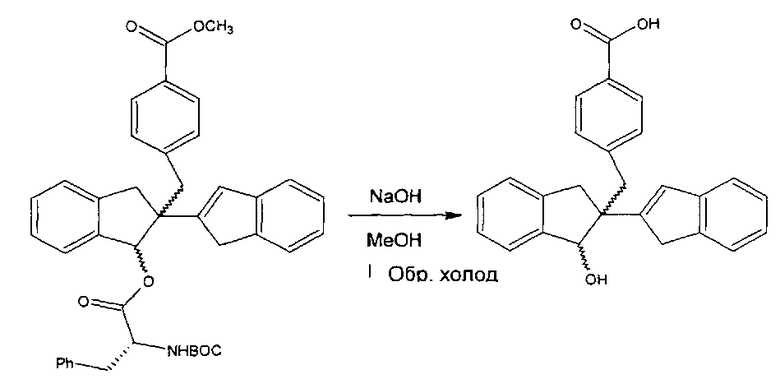
Диастереомер α2 (2,3 ммоль, 1,45 г) растворяли в метаноле (25 мл), добавляли NaOH (11,5 ммоль, 0,45 г) и смесь перемешивали при температуре флегмообразования и контролировали посредством TLC. По прошествии 20 ч. исходное вещество было израсходовано.
Реакционную смесь охлаждали до комнатной температуры и гасили путем добавления насыщенного NH4Cl. Метанол удаляли в вакууме и водный раствор подкисляли с помощью концентророванной HCl до pH 1. Продукт экстрагировали этилацетатом, сушили над MgSO4 и упаривали с получением 1,6 г желтой смолы, которую очищали на короткой колонке с диоксидом кремния, используя гексан:МТВЕ 80:20 в качестве элюента. Получали 0,44 г кислотного производного соединения 5 (50%-ный выход), которое было 97,2%-ной чистоты, согласно HPLC.
Внимание: Также осуществляли альтернативный гидролиз с использованием 10%-ного водного NaOH в метаноле при 40-50°C. Эта процедура занимала практически 5 суток до завершения.
Результаты анализова энантиомеров α1, α2, β1, β2
Энантиомер β1 из диастереомера B - соединение 3

Энантиомер β2 из диастереомера B - соединение 2

Энантиомер α1 из диастереомера C - соединение 4
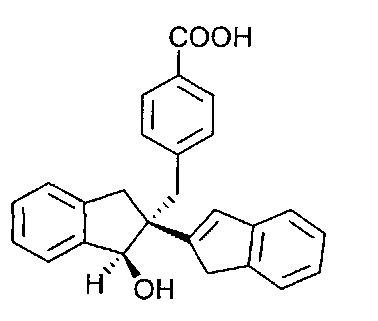
Энантиомер α2 из диастереомера C - соединение 5
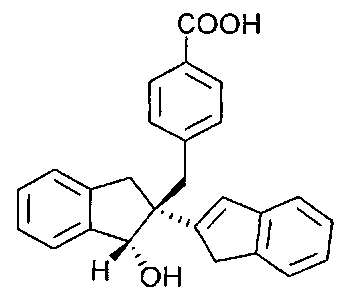
Метод HPLC
Осуществляли ахиральные и хиральные методы HPLC для качественного и количественного разделения энантиомерных соединений 2, 3, 4, 5.
Разделение энантиомеров посредством HPLC
Получение соли
Соли получали путем растворения свободных кислотных соединений 2, 3, 4 и 5 в водной или водном органическом растворителе в присутствии подходящего основания и выделения соли путем упаривания растворителя.
Соединение 6: N-Метил-(D)-глюкаминная соль (NMDG) соединения 2.

Физико-химические свойства соединения 6:
Рентгеновские исследования
Абсолютную стереохимию соединения 2 определяли посредством анализа монокристаллической рентгеновской дифракции его (S)-(-)-метилбензиламинной соли (соединение 8). Результаты приведены в Приложении 2. Результаты сходились со стереохимией, показанной на Фиг.2. Абсолютную стереохимию соединений 4 и 5 определяли путем превращения спиртов (соединения 2-5) в их кетены и путем корреляции их оптических вращений.
Воспалительное заболевание кишечника (IBD)
Воспалительное заболевание кишечника (IBD) включает в себя два идиопатических воспалительных заболевания: неспецифический язвенный колит (UC) и болезнь Крона (CD). Главным различием между UC и CD является область воспаленной ткани кишечника. Воспаление при CD представляет собой прерывисто сегментированное воспаление, известное как регионарный энтерит, в то время как UC представляет собой поверхностное воспаление, распространяющееся проксимально и непрерывно от прямой кишки. В настоящее время точная причина IBD неизвестна. Как полагают, заболевание связано с чрезмерным иммунным ответом слизистой оболочки на инфекцию кишечного эпителия вследствие дисбаланса между провоспалительными и иммунорегуляторными молекулами. Модели наследования IBD указывают на сложный генетический компонент патогенеза, который может состоять из ряда комбинированных генетических мутаций. В настоящее время не существует конкретных диагностических тестов для IBD, но как только понимание патогенеза будет улучшено, будут улучшены и способы диагностики. Лечение IBD заключается в индуцировании и поддержании ремиссии. Ремиссия у пациентов с IBD может поддерживаться при использовании 5-аминосалицилата. Однако, в то время как использование аминосалицилатов при UC обеспечивает положительный результат как в индуцировании ремиссии на стадии болезни от легкой до средней, так и в предотвращении рецидива, эффективность этих препаратов для поддержания ремиссии при CD находится под вопросом и более не рекомендуется. Основным препаратом при лечении настоящего заболевания является кортикостероид, обычно используемый в течение ограниченного периода времени для возвращения пациентов с UC и CD в состояние ремиссии, однако, будесонид, предназначенный для местного введения с ограниченной системной абсорбцией, не обладает преимуществами в поддержании ремиссии. Альтернативные препараты, такие как иммунодепрессанты азатиоприн и меркаптопурин, вместе с метотрексатом и циклоспорином обладают ограниченной эффективностью и способны вызывать серьезные побочные эффекты. Антитела анти-TNFα (фактор некроза опухоли-альфа), такие как инфликсимаб и адалимубаб, могут применяться пациентами, нечувствительными к стандартной иммунодепрессивной терапии. Однако многие пациенты не в состоянии реагировать на анти-TNFα терапию, либо вследствие их конкретного фенотипа, либо в результат выработки аутоантител.
Острая мышиная модель колита, индуцированного DSS
Модель декстрана сульфата натрия (DSS) является экспериментальной мышиной моделью, которая выказывает многие из симптомов, наблюдаемых при человеческом UC, такие как диарея, кровяные фекалии, изъязвление слизистой, укорачивание толстой кишки, потеря веся и изменения в некоторых цитокинах толстой кишки. Это исследование широко используется в качестве модели изучения патогенеза UC, а также для поиска новых терапевтических процедур для лечения UC.
В этих исследованиях использовали модель острого колита, где 5% DSS вводили в составе питьевой воды мышам BALB/c. Этот режим дозировки индуцирует тяжелый острый колит, к 7-8 суткам у мышей наблюдали ректальное кровотечение и значительную потерю массы; при отсутствии заблаговременного умерщвления все мыши умирали бы на 10-12 сутки.
Мыши
Специальных свободных от патогенов мышей BALB/c, возраст 6-8 недель, получали от коммерческого поставщика (Harlan UK). Мыши находились на диете облученного корма в индивидуально вентилируемых клетках (Tecniplast UK) под положительным давлением.
Обработка DSS
DSS (5%) растворяли в питьевой воде. Соединения вводили перорально при дозе 10 мг/кг или 30 мг/кг на сутки 0-7, и мышей отбраковывали на сутки 8 или 9 в зависимости от тяжести заболевания. Мышей ежедневно проверяли на клинические проявления, и регистрировали массу каждой мыши. Индуцирование колита определяли по результатам вскрытия, длины толстой кишки и гистологического анализа. Толстые кишки выделяли и хранили при -20°C для иммунологического анализа. Все из соединений и экспериментальных групп случайным образом наименовали по алфавиту. На протяжении экспериментов вся регистрация данных осуществлялась слепым образом. Коды на коробках/группах не были нарушены до тех пор, пока данные не были проанализированы, т.е., коробки, именованные A, B, C и т.д. идентифицировались как необработанные, обработанные DSS или обработанные DSS + соединением.
Для количественного выражения степени колита определяли индекс активности болезни (DAI) в зависимости от потери массы, фекальной крови и консистенции стула. По каждому параметру присваивали баллы, сумма которых использовалась как DAI. Для каждой группы лечения n=8.
Введение соединений
Все соединения приготавливали для перорального кормления (0,1 мл внутрь (перорально) на 10 г массы тела) в виде суспензии в смеси 0,5% карбоксиметилцеллюлозы/2% Tween 80, при дозе 3-30 мг/кг. Соединения в виде свободной кислоты сначала растворяли в абсолютном спирте и разбавляли 14+1 смесью 0,5% карбоксиметилцеллолозы/2% Tween 80; результатом этого являлся мелкий осадок в суспензии, в то время как N-метил-(D)-глюкаминные соли были растворимы только в носителе.
Действие энантиомеров соединений 2, 3, 4 и 5 на колит, индуцированный 5% DSS, у мышей
Мышам BALB/c, получавшим 5% DSS вместе с питьевой водой, вводили соединения 2, 3, 4 и 5 в дозировке 30 мг/кг перорально в виде суспензии в смеси 0,5% карбоксиметилцеллюлоза/ 2% Tween 80 ежедневно в течение 7 суток. Измерение DAI показывает степень заболевания в этой модели. Соединение 4 не оказывало действия на эту переменную величину, не наблюдали значимых (P>0,05) различий в значениях DAI в любой момент времени (Фиг. 3). На 7 сутки, как соединение 2, так и соединение 5 значимо (P<0,5) уменьшали DAI на значительную величину, от 9,0±0,53 для контроля с носителем до 3,2±0,73 для соединения 5 и 2,5±0,71 для соединения 2, причем не было значимых различий между этими двумя соединениями (Фиг. 4). В сравнении, соединение 3 уменьшало DAI лишь до значений 5,3±0,6. Оно являлось значимо (P>0,05) менее эффективным, чем соединение 2 и соединение 5. Кроме того, в то время как DAI у мышей, обрабатываемых соединением 3, был статистически (P<0,05) меньше, чем у контроля с носителем на 7 сутки (Фиг. 4), на 6 сутки не было статистического (P>0.05) различия между соединением 3 и носителем (Фиг. 3). В заключение, из четырех энантиомеров соединений 2, 3, 4 и 5, соединение 2 и соединение 5 являются высоко активными в этой модели при дозировке 30 мг/кг. Соединение 3 имеет минимальную активность, которая является значимо (P<0,05) меньшей, чем у соединения 2 и соединения 5. Соединение 4 практически лишено активности в этой мышиной модели колита, индуцированного 5% DSS.
Выбор соли соединений 2 и 5
Вследствие ограниченной растворимости в воде энантиомерного соединения 2 и соединения 5, авторы изобретения осуществили синтез пяти солей соединения 5. Были синтезированы натриевая соль, калиевая соль, кальциевая соль, α-метилбензиламинная соль и N-метил-(D)-глюкаминная соль. Натриевая и кальциевая соли были неудачными. Три соли соединения 5, а именно калиевую соль, α-метилбензиламинную соль и N-метил-(D)-глюкаминную соль использовали для изучения растворимости и коэффициента распределения (logP).
Определяли растворимость четырех соединений:
С удивлением обнаружили, что N-метил-(D)-глюкаминная соль соединения 5 (соединение 7) является наиболее растворимым соединением из этой группы аналогичных соединений со значительным отрывом, имея растворимость >60,000 мкг/мл в воде Milli-RO, 0,14 мкг/мл в буфере с pH4, >60,000 мкг/мл в буфере с pH7,0 и >3,000 мкг/мл в буфере с pH 9,0. Почти идентичные значения были получены для N-метил-(D)-глюкаминной соли соединения 2 (соединение 6) с растворимостью >60,000 мкг/мл в воде Milli-RO, 0,5 мкг/мл в буфере с pH4, >60,000 мкг/мл в буфере с pH 7,0 и >3,000 мкг/мл в буфере с pH 9,0.
Коэффициент распределения соединения 5 и родственных аналогичных соединений исследовали с помощью метода HPLC (обращено-фазная колонка C18 HPLC) при нейтральной, кислом и щелочном pH.
Определяли коэффициент распределения для четырех соединений:
Обнаружили, что коэффициенты распределения для каждой соли соединение 5 был схожи. Предполагают, что это происходит в результате того, что соль в растворе соединения диссоциирует на родительское соединение 5 и связанный солевой ион. В результате этого измеренный коэффициент распределения был обусловлен скорее родительским ионом, а не молекулами соли.
Коэффициент распределения (Log10 POW) N-метил-D-глюкаминной соли соединения 2 (соединение 6) успешно определили в нейтральных, щелочных и кислых условиях со значениями 3,5, 4,3 и 2,6, соответственно.
N-Метил-(D)-глюкамин был выбран в качестве соли-кандидата как для соединения 2, так и для соединения 5.
Действие энантиомеров соединения 2 и соединения 5 и их N-метил-(D)-глюкаминных солей (соединения 6 и 7) при дозировке 10 мг/кг на колит, индуцированный 5% DSS, у мышей
Учитывая тот факт, что оба из соединений 2 и 5 показывают значительную активность в модели 5% DSS при дозировке 30 мг/кг, авторы повторно протестировали их активность вместе с их N-метил-(D)-глюкаминными солями при более низкой дозе 10 мг/кг, обрабатывая ежедневно в течение 7 дней суспензией или раствором в смеси 0,5% карбоксиметилцеллюлоза/2% Tween 80. В дозировках солей не делали корректировок для компенсации их возросшей молекулярной массы. Оба соединения 5 и 7 при дозировке 10 мг/кг не оказывали значимого (P>0,05) влияния на DAI модели колита, индуцированного 5% DSS, у мышей по сравнению с контрольным носителем (см. Фиг. 5). Напротив, на 7 сутки N- метил-(D)-глюкаминной соли обоих соединений 2 и 6, при дозировке 10 мг/кг значимо (P<0,05) и сильно уменьшали DAI с 9,3±0,51 (носитель) до 2,1±0,7 и 3,3±0,52, соответственно (Фиг. 6).
В заключение, соединение 2 (и его N-метил-(D)-глюкаминная соль, соединение 6) является самым эффективным из четырех энантиомеров, значительно превосходя их, и является единственным энантиомером, который сохраняет активность при низкой дозе 10 мг/кг.
Действие соединения 6 в различных дозировках и его сравнение с преднизолоном на мышином колите, индуцированном 5% DSS
Соединение 6 выбирали как наиболее предпочтительный энантиомер. Тестировали активность соединения 6 в модели мышиного колита, индуцированного 5% DSS, при различных дозах для оценки наличия зависимости доза/ответ и сравнения с эффективным пероральным стероидом преднизолоном, широко используемым для возвращения пациентов, страдающих от острого приступа IBD, к ремиссии.
Мышам вводили соединение соединение 6 в дозировках 3, 10 и 30 мг/кг (эквивалентно 6,6-20 мг/кг соединения 2). Группу обрабатываемых DSS мышей также обрабатывали преднизолоном, 5 мг/кг. Преднизолон представляет собой кортикостероид, применяемый в клинике для лечения IBD у человека, и количество, используемое в этом тесте, является оптимальной дозой для этой модели. По истечении 3 суток обработки мышей BALB/c 5% DSS в питьевой воде признаки колита были выражены. Это проявлялось в потере массы (Фиг. 7) и увеличении DAI заболевания (Фиг. 8). Однако, при пероральном ежедневном введении в течение 7 суток соединения 6 в трех дозах (3, 10 и 30 мг/кг), у мышей не вызывались выраженные реакции. Соединение 6 облегчало тяжесть колита после ощутимой обработки DSS по многим параметрам изучаемой болезни. Способность соединения 6 облегчать заболевание в модели DSS являлась дозозависимой. Соединение 6 при дозировке 30 мг/кг являлось терапевтическим в модели DSS при сравнимой или лучшей эффективности по сравнению с преднизолоном при дозировке 5 мг/кг.
Тяжесть этих симптомов является прогрессирующей; к 7 суткам обрабатываемые DSS мыши потеряли до 15% своей массы тела, и все мыши имели перфузирующее ректальное кровотечение. Значения DAI на день вскрытия показывали, что мыши, которых обрабатывали соединением 6 при дозировке 3-30 мг/кг, имели при каждом уровне дозировки значимо (P<0,05 - P<0,01) меньший DAI, чем контроль с носителем. Преднизолон (5 мг/кг) также значимо (P<0,01; ANOVA; тест множественного сравнения Даннетта) уменьшал суммарный балл DAI (Фиг. 9).
При вскрытии на 7 сутки наблюдалось значимое укорачивание прямой кишки (P<0,05 - P<0,01; ANOVA; Тест множественного сравнения Даннетта) во всех обрабатываемых DSS группах по сравнению с прямыми кишками мышей, которых не обрабатывали DSS (Фиг. 10). Наименьшая доза 3 мг/кг соединения 6 не оказывала значимого влияния на ингибирование укорачивания прямой кишки по сравнению с контрольным носителем, в то время как группы доз 10 и 30 мг/кг и группа преднизолона оказывали значимое влияние. Соединение 6 при дозировке 30 мг/кг действовало значимо лучше, чем преднизолон (P<0,05; ANOVA; Тест множественного сравнения Даннетта) (Фиг. 10).
После обработки DSS гистологические срезы дистального отдела прямой кишки показывали значительное повреждение крипт и инфильтрацию клеток (Фиг. 11).
Степень повреждения толстой кишки количественно выражали с использованием условной системы баллов. Соединение 6 при дозировках как 10, так и 30 мг/кг, вызывало дозозависимое и в высокой степени статистически значимое уменьшение (P<0,01; дисперсионный анализ Краскела-Уоллиса; Тест множественного сравнения Даннетта) патологии толстой кишки по сравнению с группой носителя. Напротив, не было значимого улучшения по гистологических баллам у группы, обрабатываемой преднизолоном (5 мг/кг), по сравнению с мышами, обрабатываемым носителем (Фиг. 12).
Согласуясь с гистологическими результатами, показывающими воспаление в толстых кишках мышей, наблюдалось значимое (P<0,001; дисперсионный анализ Краскела-Уоллиса; Тест множественного сравнения Даннетта) увеличение активности миелопероксидазы толстой кишки (MPO) у мышей, обрабатываемых DSS, которым вводили только носитель. Активность миелопероксидазы толстой кишки (MPO), представляющая уровень воспалительной инфильтрации нейтрофилов в стенку кишки, которая увеличилась практически в 8 раз после обработки DSS, была значимо (P<0,05) уменьшена как соединением 6 при дозировке 30 мг/кг, так и преднизолоном, на 63% и 54% к 7 суткам, соответственно (Фиг. 13).
Количественное определение уровней цитокинов толстой кишки показало, что обработка DSS индуцирует увеличение уровня IL1β (Фиг. 14(a)), TNFα (Фиг. 14(b)) и IL6 (Фиг. 14(c)), до 0,744±0,076 нг/мг, 1,478±0,378 нг/мг и 1,057±0,1784 нг/мг, соответственно. В каждом случае соединение 6 вызывало значимое (P<0,05, 30 мг/кг) и дозозависимое уменьшение уровней цитокинов. Преднизолон (5 мг/кг) также снижал (p<0,05) эти увеличения уровней цитокинов; для каждого цитокина не было значимого различия между действием преднизолона в дозе 5 мг/кг и соединения 6 при более высоком уровне дозировки 30 мг/кг на 7 сутки.
В заключение, после перорального ежедневного введения в течение 7 суток соединение 6 при трех дозировках (3, 10 и 30 мг/кг) не вызывало явных реакций у мышей. Соединение 6 облегчало тяжесть колита после ощутимой обработки 5% DSS по многим параметрам изучаемой болезни, и способность облегчать заболевание является дозозависимой. Также, соединение 6 при дозировке 30 мг/кг являлось терапевтически эффективным в модели DSS со сравнимой или лучшей эффективностью, по сравнению с преднизолоном (5 мг/кг).
Модель хронического IL10--/--
У мышей с удаленным геном IL10--/-- спонтанно развивается хронический колит, где возраст начала и тяжесть болезни зависят от предыстории линии мышей и условий, в которых животные выращивались. Начало колита у мышей IL10--/--, выращиваемых в условиях, используемых в этом исследовании, также являлось зависимым от линии, где более раннее начало и большая тяжесть, с точки зрения смертности, наблюдалась у мышей линии BALB/c, по отношению к мышам линии C57BL/6. В этом эксперименте животные получали пероральное лечение по режиму MWF в течение 9 недель. Изначально, обе группы мышей последовательно набирали массу (Фиг. 15). Мыши, обрабатываемые носителем, прекращали набирать массу, начиная с 5 недели обработки, в то время как мыши, обрабатываемые соединением 6, продолжали набирать массу вплоть до недели 8. К 9 неделе животные имели выраженную потерю массы, где по одному агонизирующему животному гуманно умерщвляли на 60 сутки в каждой группе. Поскольку другие мыши теряли вес и выказывали клинические симптомы болезни, обе группы отбраковывали на 9 неделе (63 сутки) и анализировали. В то время как наблюдалась большая смертность в группе, обрабатываемой носителем (25%) по сравнению с мышами, обрабатываемыми соединением 6 (9,2%) согласно анализу Каплана-Мейера, не было статистической разницы в выживаемости мышей IL10-/- на протяжении 9 недель.
Из мышей выделяли сыворотку и анализировали сывороточный амилоид A (SAA) в качестве маркера тяжести колита. Наблюдали значимо (P<0,05; t-тест Стьюдента) сниженные уровни SAA у мышей, обрабатываемых соединением 6 по сравнению с мышами IL10--/-- обрабатываемыми носителем (Фиг. 16).
Гистологические срезы прямых кишок мышей IL10--/--, обрабатываемых носителем или соединением 6, показаны на Фиг. 17.
Производили оценку гистологических срезов прямых кишок мышей IL10--/--, обрабатываемых носителем или соединением 6. Степень патологии прямой кишки была значимо снижена (P<0,05; t-тест Стьюдента) у мышей IL10--/--, получавших соединение, по сравнению с мышами, обрабатываемыми носителем (Фиг. 18).
Подводя итог, пероральное лечение соединением 6 (300 мг/кг/неделя) мышей линий IL10--/-- BALB/c с использованием режима MWF в течение 9 недель, задерживало потерю массы и снижало смертность от колита по сравнению с мышами, обрабатываемыми носителем. В этой модели хронического колита соединение 6 значимо снижало показатели болезни, а именно сывороточный маркер воспаления прямой кишки и повреждения прямой кишки. Это особо примечательно ввиду того факта, что период полувыведения соединения 6 из плазмы крови (t1/2) составляет 3 часа у крысы. При стандартном расписании дозировки MWF мыши не были подвержены действию соединению 6 в течение существенных периодов в ходе эксперимента.
Изобретение не ограничено воплощениями, описанными в данной заявке, которые могут отличаться в деталях.
Приложение 1
Список использованных сокращений
Приложение 2
Рентгеновские исследования
Анализ монокристаллической рентгеновской дифракции (S)-(-)-метилбензиламинной соли соединении 2 (соединение 8) осуществляли с использованием SuperNova, Dual, Си at zero, Atlas Diffractometer и параметров, приведенных в Таблице 1.

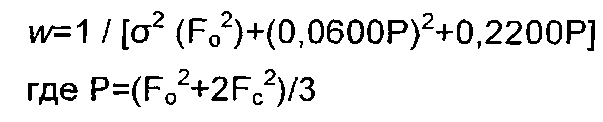
| название | год | авторы | номер документа |
|---|---|---|---|
| НОВЫЕ ЗАМЕЩЕННЫЕ ХИНОЛИНОВЫЕ СОЕДИНЕНИЯ КАК ИНГИБИТОРЫ S-НИТРОЗОГЛУТАТИОН-РЕДУКТАЗЫ | 2011 |
|
RU2599144C2 |
| ЛЕКАРСТВЕННЫЕ СРЕДСТВА НА ОСНОВЕ ЛАНТИОНИНСИНТЕТАЗА C-ПОДОБНОГО БЕЛКА 2 | 2020 |
|
RU2768888C1 |
| ТЕРАПЕВТИЧЕСКИЕ СОЕДИНЕНИЯ И СПОСОБЫ | 2018 |
|
RU2837261C2 |
| ЛЕКАРСТВЕННЫЕ СРЕДСТВА НА ОСНОВЕ ЛАНТИОНИНСИНТЕТАЗА C-ПОДОБНОГО БЕЛКА 2 | 2015 |
|
RU2741576C2 |
| БИ-АРИЛ-МЕТА-ПИРИМИДИНОВЫЕ ИНГИБИТОРЫ КИНАЗ | 2006 |
|
RU2597364C2 |
| Производные пиримидина - ингибиторы репродукции вирусов, относящихся к роду Orthoflavivirus | 2023 |
|
RU2831118C1 |
| Фармацевтическая композиция, содержащая никотиновую кислоту и/или никотинамид, и/или триптофан, для положительного воздействия на кишечную микробиоту | 2013 |
|
RU2657797C2 |
| НОВЫЙ АГОНИСТ ЕР4 | 2011 |
|
RU2564414C2 |
| БИ-АРИЛ-МЕТА-ПИРИМИДИНОВЫЕ ИНГИБИТОРЫ КИНАЗ | 2006 |
|
RU2589878C2 |
| Спиросоединения в качестве ингибиторов ERK и их применение | 2020 |
|
RU2800042C1 |




Изобретение относится к соединению формулы:
или к его фармацевтически приемлемой соли; либо к N-Метил-(D)-глюкаминной соли формулы:
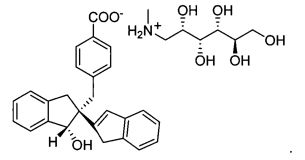
Соединения являются полезными в лечении воспалительного заболевания кишечника. 6 н.п. ф-лы, 21 ил., 7 табл.
1. Соединение формулы:

или его фармацевтически приемлемая соль.
2. N-Метил-(D)-глюкаминная соль соединения формулы:

3. Фармацевтическая композиция для профилактики или лечения воспалительного заболевания кишечника, содержащая эффективное количество соединения или его фармацевтически приемлемой соли п. 1 или 2 и фармацевтически приемлемый носитель.
4. Лекарственное средство для профилактики или лечения воспалительного заболевания кишечника, содержащее соединение или его фармацевтически приемлемую соль по п. 1 или 2.
5. Лекарственное средство для профилактики или лечения неспецифического язвенного колита, содержащее соединение или его фармацевтически приемлемую соль по п. 1 или п. 2.
6. Лекарственное средство для профилактики или лечения болезни Крона, содержащее соединение или его фармацевтически приемлемую соль по п. 1 или 2.
| US 6300376 B1, 09.10.2001;US 2002/128256 A1, 12.09.2002;EA 7983 B1, 27.02.2007 | |||
| US 6297399 B1, 02.10.2001. |
Авторы
Даты
2016-11-10—Публикация
2012-07-20—Подача