ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
[0001] Настоящее изобретение в целом относится к соединениям, применимым для модуляции митохондриальной активности. Настоящее изобретение также относится к применению этих соединений для лечения заболеваний и нарушений, связанных с митохондриальной дисфункцией.
УРОВЕНЬ ТЕХНИКИ
[0002] Ссылки на публикации, сделанные автором в настоящей заявке, приведены в алфавитном порядке в конце описания.
[0003] В настоящем описании ссылка на любую предшествующую публикацию (или полученную из нее информацию) не является и не должна приниматься за признание или допущение выраженного в любой форме предположения о том, что предшествующая публикация (или полученная из нее информация) или известный объект образует часть известного уровня техники в области техники, к которой относится настоящая заявка.
[0004] Митохондрии являются цитоплазматическими органеллами, которые выполняют целый ряд клеточных метаболических функций. Первичной функцией митохондрий является выработка энергии в форме аденозинтрифосфата (ATP) путем окислительного фосфорилирования. ATP действует, как запас энергии или носитель энергии в клетке и эукариотные клетки получают большую часть своего ATP из биохимических процессов, проводимых митохондриями. Митохондрии также играют первичную роль в передаче сигналов, дифференциации клеток и регулировании гибели клеток. Биохимические процессы, проводимые митохондриями, включают цикл лимонной кислоты (также известный, как цикл Кребса), который генерирует восстановленный никотинамидадениновый динуклеотид (NADH+H+) из окисленного никотинамидаденинового динуклеотида (NAD+), и окислительное фосфорилирование, во время которого NADH+H+ окисляется обратно в NAD+. Все в большей степени признается, что митохондрии участвуют в целом ряде заболеваний и нарушений.
[0005] Митохондриальная дисфункция, т. е. ослабление или нарушение типичной митохондриальной функции, может быть обусловлена генетическими или экологическими факторами или их комбинациями. Считается, что митохондриальная дисфункция вносит вклад в разные патологические состояния и является признаком целого ряда врожденных нарушений. По оценкам до 1 из 100 новорожденных поражены митохондриальной болезнью во время своей жизни. Кроме того, считается, что митохондриальная дисфункция может образовывать часть лежащей в основе патофизиологии при многих обычных заболеваниях и патологических состояниях, включая, но не ограничиваясь только ими, нейродегенеративные нарушения, диабет, рак, слепоту, глухоту, заболевание сердца, заболевание печени, заболевание почек, желудочно–кишечные нарушения, удар, припадок, болезнь Альцгеймера, болезнь Паркинсона, аутизм, биполярную шизофрению, депрессию, астму, хроническую усталость, миоклонический эпилептический припадок с разорванными красными волокнами (MERRF); хромосомную миопатию, энцефалопатию, лактоцидоз; наследственную оптическую нейропатию Лебера (LHON); доминантную оптическую атрофию (DOA); синдром Ли; синдром Кирнса–Сейра (KSS); наследственную атаксию Фридрейха (FRDA); кардиомиопатию; энцефаломиопатию; почечноканальцевый ацидоз; боковой амиотрофический склероз (ALS); болезнь Гентингтона и глубокие нарушения развития.
[0006] Идентифицирующие терапии, которые могут восстановить или усилить митохондриальную функцию, перспективны для широкого ряда применение. В настоящее время терапевтические подходы при указанных выше показаниях обычно были направлены на облегчение симптомов и/или лечение вторичных или сопутствующих патологических состояний, а не лежащей в основе митохондриальной дисфункции. Бензохинон, идебенон, был утвержден Европейским медицинским агентством в 2015 г. для лечения формы вызванной митохондриальной дисфункцией потери зрения у юношей (наследственная оптическая нейропатия Лебера, LHON). Однако идебенон обладает очень плохой биодоступностью и после введения характеризуется чрезмерным пресистемным метаболизмом в печени.
[0007] Необходимы улучшенные и специфические средства лечения заболеваний и нарушений, связанных с митохондриальной дисфункцией.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0008] Настоящее изобретение относится к соединениям формулы (I) и содержащим их фармацевтическим композициям. В одном варианте осуществления соединения формулы (I) применимы для модулирования митохондриальной активности. В другом варианте осуществления соединения формулы (I) применимы для усиления митохондриальной функции. В еще одном варианте осуществления соединения формулы (I) применимы для восстановления митохондриальной функции. В еще одном варианте осуществления соединения формулы (I) применимы для защиты от митохондриальной дисфункции.
[0009] Предполагается, что соединения формулы (I) и содержащие их фармацевтические композиции, предложенные в настоящем изобретении, применимы для профилактики и/или лечения заболеваний и нарушений, связанных с митохондриальной дисфункцией.
[0010] Одним или большим количеством объектов являются соединения формулы (I):
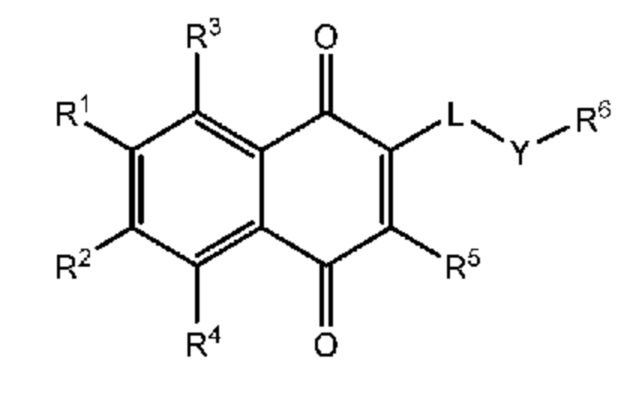
Формула (I)
или их фармацевтически приемлемая соль, в которой
R1, R2, R3 и R4 все независимо выбраны из группы, включающей H, необязательно замещенный C1–C6 алкил, необязательно замещенный C2–C6 алкенил, необязательно замещенный C2–C6 алкинил, необязательно замещенную C1–C6 алкоксигруппу, галоген, необязательно замещенный C1–C6 алкилгалоген; необязательно замещенный C1–C6 тиоалкил, –SR, –NRR’, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил,
R5 выбран из группы, включающей H, необязательно замещенный C1–C6 алкил, необязательно замещенный C2–C6 алкенил, необязательно замещенный C2–C6 алкинил, необязательно замещенную C1–C6 алкоксигруппу, галоген, необязательно замещенный C1–C6 алкилгалоген; необязательно замещенный C1–C6 тиоалкил, –SR, –NRR’, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил,
L означает двухвалентный мостик, выбранный из группы, включающей связь, необязательно замещенный C1–C20 алкилен, необязательно замещенный C1–C20 алкенилен, необязательно замещенный C1–C20 алкинилен;
Y отсутствует или означает двухвалентный мостик, выбранный из группы, включающей необязательно замещенный C3–C6 циклоалкилен, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арилен, необязательно замещенный C2–C12 гетероарилен, –C(O)–NR–, –C(O)–NR–(CH2)y–, –C(O)–O–, –C(O)–OR–, –C(O)–O–(CH2)y–, –C(O)–, –C(CX3)–NR–, –CRR’X–NR–, –NR–C(O)–NR’–, –O–C(O)O–, –C=N–O–, –SO2–NR–, –(CH2)x–NR–, –(CH2)y–S–(CH2)z–, –(CH2)y–O–(CH2)z–, где y и z оба означают целые числа, независимо выбранные из группы, включающей 0, 1, 2, 3 и 4;
R6 выбран из группы, включающей H, –COOR, –OR, –NRR’, –SR, необязательно замещенный C1–C20 алкил, необязательно замещенный C2–C20 алкенил, необязательно замещенный C2–C20 алкинил; необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C5–C12 арил, необязательно замещенный C2–C12 гетероарил или необязательно замещенный C2–C12 гетероциклил, необязательно замещенную C1–C6 алканоламиногруппу, необязательно замещенный аминокислотный остаток, необязательно замещенный дипептид, необязательно замещенный трипептид и необязательно замещенный полипептид,
или Y и R6 вместе образуют группу, выбранную из группы, включающей
–C(O)–[NR7–C(R8)(R9)–C(O)]w–OR10;
–C(O)–[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10;
–[NR7–C(R8)(R9)–C(O)]w–OR10; и
–[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10,
где R7, R8, R10, R11 и R12 в каждом случае означают H или необязательно замещенный C1–C6–алкил; R9 в каждом случае независимо выбран из группы, включающей H и боковую цепь аминокислоты или ее производное; и w означает целое число, равное от 0 до 20,
R и R’ независимо означают H, необязательно замещенный C1–C6 алкил, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил, и
X означает галоген.
[0011] Другими объектами являются соединения формулы (Ia):
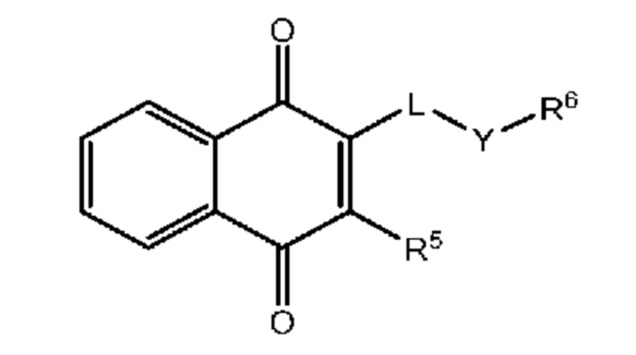
Формула (Ia)
или их фармацевтически приемлемая соль, в которой:
R5 выбран из группы, включающей H и необязательно замещенный C1–C6 алкил,
L означает необязательно замещенный C1–C20 алкилен,
Y означает двухвалентный мостик, выбранный из группы, включающей необязательно замещенный –C(O)–NR–, –C(O)–NR–(CH2)y–, –C(O)–O–, –C(O)–, –(CH2)y–S–(CH2)z–, –(CH2)y–O–(CH2)z–, где y и z оба означают целые числа, независимо выбранные из группы, включающей 0, 1, 2, 3 и 4;
R6 выбран из группы, включающей H, –COOR; необязательно замещенный C5–C12 арил, необязательно замещенный C2–C12 гетероарил, необязательно замещенную C1–C6 алканоламиногруппу, необязательно замещенный аминокислотный остаток,
или Y и R6 вместе образуют группу, выбранную из группы, включающей
–C(O)–[NR7–C(R8)(R9)–C(O)]w–OR10;
–C(O)–[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10;
где R7, R8, R10, R11 и R12 в каждом случае означают H или необязательно замещенный C1–C6–алкил; R9 в каждом случае независимо выбран из группы, включающей H и боковую цепь аминокислоты или ее производное; и w означает целое число, равное от 0 до 20;
R и R’ независимо означают H, необязательно замещенный C1–C6 алкил.
[0012] Другим объектом являются соединения формулы (Ib):
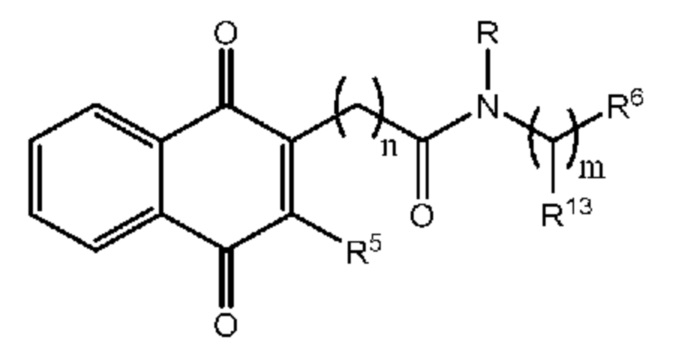
Формула (Ib)
или их фармацевтически приемлемая соль, в которой:
R5 выбран из группы, включающей H и метил,
R6 выбран из группы, включающей H, –COOR, –OH, необязательно замещенный C5–C12 арил, необязательно замещенный C2–C12 гетероарил,
R означает H или необязательно замещенный C1–C6 алкил;
R13 в каждом случае независимо выбран из группы, включающей H, необязательно замещенный фенил и необязательно замещенный бензил,
n означает целое число, выбранное из группы, включающей 1, 2, 3, 4 и 5, и
m означает целое число, выбранное из группы, включающей 0, 1, 2 и 3.
[0013] В настоящем изобретении также предложены способы получения соединений формулы (I), формулы (Ia) и формулы (Ib). Эти способы эффективно обеспечивают быстрое получение соединений формулы (I), формулы (Ia) и формулы (Ib) за относительно небольшое количество химических стадий и/или с высокой чистотой.
[0014] Настоящее изобретение также включает способ лечения млекопитающего, включающий введение соединения формулы (I), определенного в настоящем изобретении, или его фармацевтически приемлемой соли. Как отмечено выше, считается, что соединения формулы (I) и содержащие их фармацевтические композиции, предлагаемые в настоящем изобретении, применимы для профилактики и/или лечения заболеваний и нарушений, связанных с митохондриальной дисфункцией.
[0015] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, являются первичными митохондриальными заболеваниями включая, но не ограничиваясь только ими, наследственную оптическую нейропатию Лебера (LHON), доминантную оптическую невропатию (DOA), синдром Ли, наследственную атаксию Фридрейха, хромосомную миопатию, энцефаломиопатию, лактоцидоз, симптомы типа удара (MELAS), миоклонический эпилептический припадок с разорванными красными волокнами (MERRF), мионейрогенную гастроинтестинальную энцефаломиопатию (MNGIE), синдром Кирнса–Сейра, дефицит CoQ.10, или дефицит митохондриального комплекса, невропатию, атаксию, пигментную дегенерацию сетчатки и птоз (NARP).
[0016] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, представляют собой нейродегенеративные или нейромышечные нарушения, связанные с митохондриальной дисфункцией, включая, но не ограничиваясь только ими, спинально–церебеллярные атаксии, атаксию–телеангиэктазию, атаксию с окуломоторной апраксией 1 и 2 (AOA1 и 2), эпилептические припадки, боковой амиотрофический склероз (ALS), заболевание двигательных нейронов (MND), болезнь Паркинсона, болезнь Альцгеймера, болезнь Гентингтона, удар/реперфузионное поражение, или слабоумие, мышечную дистрофию Дюшенна (DMD), мышечную дистрофию Беккера (BMD), конечностно–поясную мышечную дистрофию (LGMD), сцепленную с Х–хромосомой дилатационную кардиомиопатию (XLDCM), пантотенаткиназа–ассоциированную нейродегенерацию (PKAN), спинальную мышечную атрофию (SMA), рассеянный склероз и первичный прогрессирующий рассеянный склероз (PP–MS), болезнь Кугельберга–Веландера и болезнь Верднига–Хоффмана , сахарный диабет и глухоту (DAD).
[0017] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, представляют собой метаболические нарушения, связанные с митохондриальной дисфункцией, включая, но не ограничиваясь только ими, синдром Вольфрама, неалкогольное заболевание печени (т. е. NAFLD, NASH, цирроз), возрастное ухудшение физического состояния, ожирение, избыточную массу тела, сахарный диабет, диабет типа II, диабетическую ретинопатию и метаболический синдром.
[0018] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, представляют собой психические нарушения, связанные с митохондриальной дисфункцией, включая, но не ограничиваясь только ими, шизофрению, большую депрессию, биполярное расстройство, эпилепсию, посттравматическое стрессовое нарушение (PTSD) и нарушения суточного ритма.
[0019] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, представляют собой воспалительные нарушения, связанные с митохондриальной дисфункцией, включая, но не ограничиваясь только ими, язвенный колит (UC), болезнь Крона (CD), артрит, псориаз или ревматоидный артрит, мигрень, сухой кератит, увеит, аллергический конъюнктивит, послеоперационное воспаление и острое повреждение почек. Настоящее изобретение также выполняет роль средства ослабления эффектов старения. Следовательно, имеются терапевтические и косметические аспекты лечения митохондриальной дисфункции.
[0020] В одном варианте осуществления заболевание и нарушение обусловлено вызванной лекарственным средством или вызванной окружающей средой митохондриальной дисфункцией. Например, факторы, оказывающих негативное влияние на митохондриальную активность или функцию, включают вызванную лекарственным средством или окружающей средой митохондриальную дисфункцию, обусловленную противовирусным средством; противораковым средством; антибиотиком; CNS лекарственным средством; гипотензивным лекарственным средством; антрациклинами; нестероидным противовоспалительным лекарственным средством (NSAID); анестетиком; бета–блокатором; противоаритмическим; противодиабетическим; противовоспалительным или другим средством.
[0021] Примеры противовирусных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают абакавир, диданозин, эмтрицитабин, энтекавир, эмтрицитабин, ламивудин, невирапин, телбивудин, тенофовир, типранавир, ставудин, залцитабин и зидовудин. Примеры противораковых средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают триоксид мышьяка, цетуксимаб, дакарбазин, денилейкин, дифтитокс, флутамид, гемтузумаб, метотрексат, митоксантрон, пентостатин и тамоксифен. Примеры антибиотиков, оказывающих негативное влияние на митохондриальную активность или функцию, включают антимицин A, изониазид, хлорамфеникол, этамбутол, гентамицин, кетоконазол, линезолид, стрептозоцин, стрептомицин, тобрамицин, тетрациклины и тровафлоксацин. Примеры of CNS drugs, оказывающих негативное влияние на митохондриальную активность или функцию, включают амитриптилин, амфетамины, атомоксетин, хлорпромазин, кокаин, дантролен, дезипрамин, дивалпроекс, дроперидол, фелбамат, флуфеназин, имипрамин, метамфетамин, налтрексон, нефазодон, перголид и вальпроевую кислоту. Примеры гипотензивных лекарственных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают босентан. Примеры антрациклинов, оказывающих негативное влияние на митохондриальную активность или функцию, включают даунорубицин, доксорубицин, эпирубицин и идарубицин. Примеры нестероидных противовоспалительных лекарственных средств (NSAIDs), оказывающих негативное влияние на митохондриальную активность или функцию, включают аспирин, целекоксиб, диклофенак, дифлунизал, этодолак, фенопрофен, ибупрофен, индометацин, кетопрофен, мефенаминовая кислота, мелоксикам, напроксен, набуметон, оксапрозин, пироксикам, салсалат, сулиндак, тиоридазин и толметин. Примеры анестетиков, оказывающих негативное влияние на митохондриальную активность или функцию, включают бупивакаин и изофлуран. Примеры бета–блокаторов, оказывающих негативное влияние на митохондриальную активность или функцию, включают атенолол. Примеры противоаритмических средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают амиодарон, дизопирамид, дофетилид и ибутилид. Примеры противодиабетических средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают пиоглитазон и росиглитазон. Примеры противовоспалительных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают преднизолон, дексаметазон, гидрокортизон и триамцилон. Примеры других средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают клиохинол, цианид, гексахлорофен, ротенон и статины.
[0022] В одном варианте осуществления млекопитающим является человек.
[0023] Кроме того, настоящее изобретение относится к фармацевтической композиции, включающей соединение формулы (I), определенное в настоящем изобретении и один или большее количество фармацевтически приемлемых носителей, разбавителей и/или инертных наполнителей. Настоящее изобретение также включает косметическую композицию, включающую соединение формулы (I), определенное в настоящем изобретении и один или большее количество косметически приемлемых носителей, разбавителей и/или инертных наполнителей.
[0024] Кроме того, в настоящем изобретении описано применение соединения формулы (I), определенного в настоящем изобретении, или его фармацевтически приемлемой соли для приготовления лекарственного средства для лечения млекопитающего, нуждающегося в лечении. Родственным вариантом осуществления настоящего изобретения является соединение формулы (I), определенное в настоящем изобретении или его фармацевтически приемлемая соль для применения для лечения млекопитающего, нуждающегося в лечении. Другим вариантом осуществления настоящего изобретения является соединение формулы (I), определенное в настоящем изобретении или его фармацевтически приемлемая соль для применения для косметического лечения млекопитающего для ослабления эффектов старения. В одном варианте осуществления млекопитающим является человек.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0025] Фиг. 1: Цитопротекторные эффекты соединений формулы (I) (10 мкМ) in vitro по отношению к токсичности ротенона при 10 мкМ. Типичные примеры формулы (I) UTA23, UTA37, UTA62, UTA74, UTA77; контрольными веществами были производные, в которых бензохиноновый или пластохиноновый фрагмент заменен нафтохиноновым фрагментом.
[0026] Фиг. 2: Цитопротекторные эффекты соединений формулы (I) (10 мкМ) in vitro по отношению к токсичности ротенона. 23 Соединения(белые кружки) обладали значительно улучшенной цитопротекторной активностью по сравнению с идебеноном (пунктирная линия, ~65% жизнеспособность). У клеток, обработанных только ротеноном, жизнеспособность снижалась от составляющей 100% (черная пунктирная линия, 100% жизнеспособность) до составляющей менее 30% (пунктирная линия, ˂30% жизнеспособность).
[0027] Фиг. 3: Сравнительные содержания ATP in vitro после обработки соединениями формулы (I) (10 мкМ) против токсичности ротенона. 7 Соединений (белые кружки) значительно увеличивали содержание ATP в клетках по сравнению с идебеноном (пунктирная линия, ~80% жизнеспособность) в присутствии ротенона. У клеток, обработанных только ротеноном, жизнеспособность снижалась от составляющей 100% (черная пунктирная линия, 100% жизнеспособность) до составляющей менее 30% (пунктирная линия, ˂30% жизнеспособность). Все соединения исследовали при 10 мкМ.
[0028] Фиг. 4: Токсичность in vitro типичных соединений формулы (I) (10 мкМ) по сравнению с идебеноном в клетках печени. Длительную токсичность оценивали с помощью анализа колониеобразующих единиц в клетках HepG2 в течение 14 дней для типичных соединений. Типичные соединения обладали токсичностью in vitro, сходной с данными для идебенона.
[0029] Фиг. 5: Эффективность типичных соединений формулы (I) с помощью модели наследственной оптической нейропатии Лебера (LHON) на мышах. LHON вызывали инъекцией ротенона в левый глаз (5 мкМ) в модели на мышах C57BL/6 (см. Heitz, F. D et al. (2012). PLoS One., 7(9), e45182). Лечение типичными соединениями приводило к усиленной защите зрения по сравнению с контролем, идебеноном. Типичные соединения (UTA 37 и UTA 77) и идебенон вводили по 200 мг/кг в течение периода наблюдения. Статистически значимую защиту остроты зрения наблюдали для типичных соединений UTA 37 и UTA 77, но не для идебенона (отмечен значком R на фиг. 5) при этой концентрации.
[0030] Фиг. 6: Изменение содержания глюкозы в крови в модели диабетической ретинопатии на крысах после лечения типичными соединениями формулы (I). Крысам Long Evans имплантировали осмотические насосы со стрептозотоцином (STZ) (125 мг/кг) в неделю 4, после чего содержания глюкозы в крови быстро увеличивались во времени. В неделю 14 один раз в день вводили глазные капли с типичными соединениями формулы (I) (UTA37 4,6 мг/мл; UTA77 7,36 мг/мл), идебеноном (маркирован #1; 10 мг/мл) или разбавителем в качестве контроля. n=23 глаза/группа для глаз без лечения (недели 1–14), n=10 глаз/группа (недели 14–18) и n=7 глаз/группа (недели 18–20) для #01 подвергнутых лечению глаз, n=4 глаза/группа и 7 глаз/группа для UTA37 и UTA77 соответственно (недели 14–20), n=2 глаза/группа для введения разбавителя.
[0031] Фиг. 7: Острота зрения в модели диабетической ретинопатии на крысах после лечения типичными соединениями формулы (I). Остроту зрения определяли с помощью оптокинетического ответа для левых и правых глаз крыс Long Evans в течение 19 недель. Введение стрептозотоцина (STZ) (неделя 4) значительно ухудшало непроизвольное движение головы к неделе 9. В неделю 14 один раз в день вводили глазные капли с типичными соединениями формулы (I) (UTA37 4,6 мг/мл; UTA77 7,36 мг/мл), идебенон (#1; 10 мг/мл) или разбавитель в качестве контроля. n=23 глаза/группа для глаз без лечения (недели 1–14), n=10 глаз/группа (недели 14–18) и n=7 глаз/группа (недели 18–19) для идебенона (#1) подвергнутых лечению глаз, n=4 глаза/группа и 7 глаз/группа для UTA37 и UTA77 соответственно (недели 14–19). При n=2 глаза/группа лечили разбавителем в качестве контроля. Величина ошибки=SEM.
[0032] Фиг. 8–11: Модель язвенного колита на мышах после лечения типичным соединением формулы (I) (UTA77); Фиг. 8: Потеря массы тела; Фиг. 9: Консистенция кала; Фиг. 10: Кровь в кале; Фиг. 11: Показатель активности заболевания. Колит вызывали у мышей химически путем введения 2,5% декстрансульфата натрия (DSS) в течение 7 дней. UTA77 готовили с порошкообразным кормом (200 мг/кг массы тела), который перорально вводили один раз в день в течение 7 дней.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0033] В настоящей заявке, если из контекста не следует иное, термин "включает" и его варианты, такие как "включают" или "включающий", следует считать включением указанного элемента или целого числа, или стадии способа, или группы элементов или стадий способа, но не исключение любого другого элемента или целого числа, или стадий способа, или группы элементов, или целых чисел, или стадий способа.
[0034] При использовании в настоящей заявке единственные формы терминов включают множественные формы, если из контекста явно не следует иное. Так, например, указание на "биологический регулятор" включает указание на один биологический регулятор, а также два или большее количество биологических регуляторов; указание на "средство" включает указание на одно средство, а также два или большее количество средств; указание на "раскрытие" включает указание на один или множество признаков, приведенных в раскрытии; и т. п. Объекты, приведенные и предлагаемые в настоящем изобретении, входят в термин "изобретение". Все такие объекты входят в объем настоящего изобретения. Любые варианты и производные, указанные в настоящем изобретении, входят в "формы" настоящего изобретения.
[0035] Настоящее изобретение в целом относится к соединениям формулы (I), формулы (Ia) и формулы (Ib), которые модулируют митохондриальную активность. В одном варианте осуществления соединения формулы (I) применимы для усиления митохондриальной функции. В другом варианте осуществления соединения формулы (I), формулы (Ia) и формулы (Ib) применимы для восстановления митохондриальной дисфункции.
[0036] Кроме того, настоящее изобретение относится к способам получения соединений формулы (I), формулы (Ia) и формулы (Ib) за относительно небольшое количество химических стадий и/или с высокой чистотой.
[0037] При использовании в настоящем изобретении термины "митохондрион" и "митохондрии" означают цитоплазматические органеллы, которые выполняют целый ряд клеточных метаболических функций. Первичной функцией митохондрий является выработка энергии в форме аденозинтрифосфата (ATP) путем окислительного фосфорилирования. Митохондрии также играют важную роль в процессе апоптоза или запрограммированной гибели клеток. Кроме того, митохондрии содействуют поддержанию подходящих концентраций ионов кальция в клетке. В некоторых типах клеток, таких как клетки печени, митохондрии способствуют детоксификации аммиака. В других контекстах митохондрии способствуют выработке компонентов крови, а также гормонов, таких как тестостерон и эстроген.
[0038] При использовании в настоящем изобретении термин "митохондриальная дисфункция" означает ослабление или нарушение типичной митохондриальной функции в здоровых клетках, тканях и органах. Митохондриальная дисфункция участвует в широком диапазоне заболеваний и нарушений. В некоторых случаях митохондриальная дисфункция и связанные с ней нарушения могут быть вызваны приобретенными или врожденными мутациями в митохондриальной DNA или в ядерных генах, которые кодируют митохондриальные компоненты. В других случаях митохондриальная дисфункция может быть обусловлена факторами окружающей среды, такими как применение лекарственного средства или инфекция. Следует понимать, что при использовании в настоящем изобретении термины "митохондриальное заболевание" и "митохондриальное нарушение" и родственные термины можно использовать взаимозаменяемым образом и они включают приобретенные или врожденные нарушения, связанные с митохондриальной дисфункцией, а также заболевания или нарушения, связанные с митохондриальной дисфункцией, вследствие неблагоприятных факторов окружающей среды, если не указано иное.
[0039] В настоящем изобретении указание на "модулирование" или "модуляцию" относится к ингибированию и/или стимулированию взаимодействия и включает его. Модуляция может включать, но не ограничивается только ими, нормализацию и усиление.
[0040] В настоящем изобретении указание на "нормализацию" или "нормализирование" биомаркера означает изменение содержания биомаркера от соответствующего патологии к нормальному содержанию, где нормальное содержание энергетического биомаркера может представлять собой i) содержание биомаркера у здорового лица или субъекта или ii) содержание энергетического биомаркера, которое облегчает один или большее количество нежелательных симптомов у лица или субъекта. Таким образом, нормализация биомаркера, который подавлен в патологическом состоянии, означает увеличение содержания биомаркера по направлению к нормальному (соответствующему здоровому состоянию) значению или по направлению к значению, при котором облегчается нежелательный симптом; нормализация энергетического биомаркера, содержание которого увеличено в патологическом состоянии, означает уменьшение содержания энергетического биомаркера по направлению к нормальному (соответствующему здоровому состоянию) значению или по направлению к значению, при котором облегчается нежелательный симптом.
[0041] В настоящем изобретении указание на "усиленный" или "усиление" биомаркера означает изменение содержания одного или большего количества биомаркеров от нормального значения или значения до усиления для обеспечения благоприятного или желательного эффекта. Например, в случае, когда субъекту необходимо значительное количество энергии, может быть желательно увеличить содержание ATP у этого субъекта до значения, превышающего нормальное содержание ATP у этого субъекта. Усиление также может оказать благоприятное воздействие субъекта, страдающего от заболевания или патологии, такой как митохондриальное заболевание, при котором нормализация биомаркера может не обеспечить оптимальный результат для субъекта; в таких случаях может быть благоприятным усиление одного или большего количества биомаркеров, например, превышающие нормальное содержания ATP или меньшие, чем нормальные содержания молочной кислоты (лактата) может быть благоприятным для такого субъекта.
[0042] Термин "аминокислота" используется в настоящем изобретении в самом широком смысле и может означать соединения, содержание аминогруппу и карбоксигруппу. Аминокислоты, включенные в пептиды, использующиеся в настоящем изобретении, могут представлять собой D– или L–формы протеогенных или природных аминокислот, или могут представлять собой D– или L–формы аминокислот. Как указано в настоящем изобретении, термин распространяется на синтетические аминокислоты и их аналоги, включая соли, изомеры, таутомеры, сложные эфиры и N–метилированные аминокислоты.
[0043] Термин "боковая цепь аминокислоты" при использовании в настоящем изобретении означает группу, присоединенную к α–атому углерода, например, приведенную ниже, как группа R:
 .
.
[0044] Природные протеогенные аминокислоты приведены в таблице 1 вместе с их трехбуквенными и однобуквенными кодами. L–Аминокислоты обозначены прописными буквами или начальными прописными буквами, а D–аминокислоты обозначены строчными буквами.
Таблица 1: Коды стандартных аминокислот
[0045] Примеры неприродных или непротеогенных аминокислот включают, но не ограничиваются только ими, орнитин, норлейцин, 4–аминомасляную кислоту, 4–амино–3–гидрокси–5–фенилпентановую кислоту, 6–аминогексановую кислоту, трет–бутилглицин, норвалин, фенилглицин, саркозин, 4–амино–3–гидрокси–6–метилпентановую кислоту и 2–тиенилаланин. Примеры подходящих непротеогенных или неприродных аминокислот, использующихся в настоящем изобретении, приведены в таблице 2.
Таблица 2: Нестандартные аминокислоты
[0046] Термины "дипептид" и "трипептид" при использовании в настоящем изобретении означают пептид, включающий 2 и 3 аминокислотных остатка или их производных соответственно.
[0047] Термины "полипептид" и "пептид" используются в настоящем изобретении взаимозаменяемым образом и означают полимер из аминокислотных остатков. Термины относятся к полимерам аминокислот, в которых один или большее количество аминокислотных остатков являются искусственными химическими аналогами соответствующей природной аминокислоты, а также к полимерам природной аминокислоты.
[0048] Термин "алкил" при использовании по отдельности или в комбинации в настоящем изобретении означает обладающую линейной или разветвленной цепью насыщенную углеводородную группу. Термин "C1–12 алкил" означает такую группу, содержащую от 1 до 12 атомов углерода и "низший алкил" означает C1–6 алкильные группы, содержащие от 1 до 6 атомов углерода, такие как метил ("Me"), этил ("Et"), н–пропил, изопропил, н–бутил, изобутил, втор–бутил, трет–бутил и т. п.
[0049] Термин "циклоалкил" означает неароматические, насыщенные неароматические карбоциклы. Термин "C4–9 циклоалкил", например, означает такую группу, содержащую от 4 до 9 атомов углерода. Примеры включают циклобутил, циклопентил и циклогексил.
[0050] Термин "алкенил" означает линейный или разветвленный углеводород, содержащий одну или большее количество двойных связей. Термин "C2–12 алкенил", например, означает такую группу, содержащую от 2 до 12 атомов углерода. Примеры алкенила включают аллил, пренил, геранил, 1–метилвинил, бутенил, изобутенил, 1,3–бутадиенил, 3–метил–2–бутенил, 1,3–бутадиенил, 1,4–пентадиенил, 1–пентенил, 1–гексенил, 3–гексенил, 1,3–гексадиенил, 1,4–гексадиенил и 1,3,5–гексатриенил.
[0051] Термин "циклоалкенил" означает циклические алкенильные группы, включающие одно циклическое кольцо или несколько конденсированных колец и по меньшей мере одну внутреннюю двойную связь, предпочтительно содержащие от 4 до 11 атомов углерода. Примеры подходящих циклоалкенильных групп включают, например, циклобут–2–енил, циклопент–3–енил, циклогекс–4–енил, циклоокт–3–енил, инденил и т. п.
[0052] Термин "алкинил" означает линейный или разветвленный углеводород, содержащий одну или большее количество тройных связей, предпочтительно 1 или 2 тройных связи. Термин "C2–12 алкинил", например, означает такую группу, содержащую от 2 до 12 атомов углерода. Примеры включают 2–пропинил и 2– или 3–бутинил.
[0053] Термин "алкоксигруппа" при использовании по отдельности или в комбинации означает обладающую линейной или разветвленной цепью алкильную группу, ковалентно присоединенную через кислородный мостик (–O–) и термины "C1–6 алкоксигруппа" и "низшая алкоксигруппа" означает такие группы, содержащие от 1 до 6 атомов углерода, такие как метоксигруппу, этоксигруппу, пропоксигруппу, изопропоксигруппу, бутоксигруппу, трет–бутоксигруппу и т. п.
[0054] Термины "алканоламиногруппа" и "аминоспирт" используют взаимозаменяемым образом в широком смысле и означают соединения, содержащие аминогруппу (–NH2, –NHR и –NR2) и спиртовую или гидроксигруппу (–OH). В предпочтительном варианте осуществления соединения формулы (I), формулы (Ia) и формулы (Ib) или в вариантах осуществления, указанных выше в настоящем изобретении, могут содержать один или большее количество β–аминоспиртовых групп. β–Аминоспирты в соответствии с настоящим изобретением можно получить из природных и/или неприродных аминокислот и поэтому могут содержать "боковую цепь аминокислоты", например, приведенную ниже, как группа R:
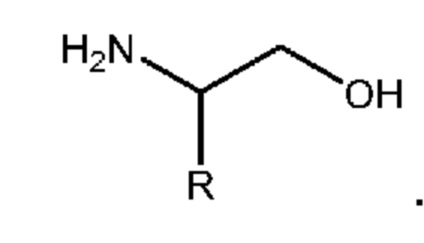 .
.
[0055] Термин "арил" означает карбоциклические (негетероциклические) ароматические кольца или кольцевые системы. Ароматические кольца могут представлять собой моно– или бициклические кольцевые системы. Ароматические кольца или кольцевые системы обычно содержат от 5 до 10 атомов углерода. Примеры подходящих арильных групп включают, но не ограничиваются только ими, фенил, бифенил, нафтил, тетрагидронафтил и т. п.
[0056] Арильные группы включают фенил, нафтил, инденил, азуленил, флуоренил или антраценил.
[0057] Термин "гетероарил" означает одновалентную ароматическую карбоциклическую группу, предпочтительно содержащую в кольце от 2 до 10 атомов углерода и от 1 до 4 гетероатомов, выбранных из группы, включающей кислород, азот и серу. Предпочтительно, если гетероатомом является азот. Такие гетероарильные группы могут содержать одно кольцо (например, пиридил, пирролил или фурил) или несколько конденсированных колец (например, индолизинил, бензотиенил или бензофуранил).
[0058] Термин "гетероциклил" означает одновалентную насыщенную или ненасыщенную группу, содержащую одно кольцо или несколько конденсированных колец, предпочтительно содержащую в кольце от 1 до 8 атомов углерода и от 1 до 4 гетероатомов, выбранных из группы, включающей азот, серу, кислород, селен или фосфор.
[0059] Примеры 5–членных моноциклических гетероциклильных и гетероарильных групп включают фурил, тиенил, пирролил, H–пирролил, пирролинил, пирролидинил, оксазолил, оксадиазолил (включая 1,2,3 и 1,2,4–оксадиазолилы) тиазолил, изоксазолил, фуразанил, изотиазолил, пиразолил, пиразолинил, пиразолидинил, имидазолил, имидазолинил, триазолил (включая 1,2,3– и 1,3,4–триазолилы), тетразолил, тиадиазолил (включая 1,2,3– и 1,3,4–тиадиазолилы).
[0060] Примеры 6–членных моноциклических гетероциклильных и гетероарильных групп включают пиридил, пиримидинил, пиридазинил, пиранил, пиразинил, пиперидинил, 1,4–диоксанил, морфолинил, 1,4–дитианил, тиоморфолинил, пиперазинил, 1,3,5–тритианил и триазинил.
[0061] Примеры 8–, 9– и 10–членных бициклических гетероциклильных и гетероарильных групп включают 1H–тиено[2,3–c]пиразолил, тиено[2,3–b]фурил, индолил, изоиндолил, бензофуранил, бензотиенил, бензоксазолил, бензотиазолил, бензизоксазолил, бензизотиазолил, бензимидазолил, индазолил, изохинолинил, хинолинил, хиноксалинил, уридинил, пуринил, циннолинил, фталазинил, хиназолинил, хиноксалинил, бензотриазинил, нафтиридинил, птеридинил и т. п.
[0062] Термин "галоген" означает фтор, хлор, бром и йод.
[0063] Термин "галогеналкильная" группа озанчает, что один или большее количество из атомов водорода алкильной группы заменены галогенами. Примечательными примерами являются –CF3 или –CF2H.
[0064] Термин "арилоксигруппа" означает арильную группу, определенную выше, связанную с исходной структурой кислородным мостиком (–O–). Примечательным примером является феноксигруппа. Аналогичным образом, термин "гетероарилоксигруппа" означает гетероарильную группу, описанную выше, связанную с исходной структурой кислородным мостиком. Примечательным примером является 4–, 6– или 7–бензо[b]фуранилоксигруппа.
[0065] Термин "ацил" означает группы H–C(O)–, алкил–C(O)–, циклоалкил–C(O)–, арил–C(O)–, гетероарил–C(O)– и гетероциклил–C(O)–, где алкил, циклоалкил, арил, гетероарил и гетероциклил описаны в настоящем изобретении.
[0066] Термин "оксиацил" означает группы HOC(O)–, алкил–OC(O)–, циклоалкил–OC(O)–, арил–OC(O)–, гетероарил–OC(O)– и гетероциклил–OC(O)–, где алкил, циклоалкил, арил, гетероарил и гетероциклил являются такими, как описано в настоящем изобретении.
[0067] Термин "ациламиногруппа" означает группу –NR"C(O)R", в которой каждый R" независимо означает водород, алкил, циклоалкил, арил, гетероарил и гетероциклил и в которой каждый алкил, циклоалкил, арил, гетероарил и гетероциклил является таким, как описано в настоящем изобретении.
[0068] Термин "алкилен" означает линейные или разветвленные двухвалентные алкильные группы предпочтительно содержащие от 1 до 20 атомов углерода и более предпочтительно от 1 до 6 атомов углерода. Примеры таких алкиленовых групп включают метилен (–CH2–), этилен (–CH2CH2–) и изомеры пропилена (например, –CH2CH2CH2– и –CH(CH3)CH2–) и т. п.
[0069] Термин "алкенилен" означает линейную или разветвленную двухвалентную алкенильную группу, содержащую одну или большее количество двойных связей и предпочтительно содержащую от 2 до 20 атомов углерода. Примеры таких алкениленовых групп включают этенилен (–CH=CH–), пропенилен, прененилен, гераненилен и их изомеры.
[0070] Термин "сульфамоил" означает группу –S(O)2NR"R", в которой each R" независимо означает водород, алкил, циклоалкил, арил, гетероарил и гетероциклил и в которой каждый алкил, циклоалкил, арил, гетероарил и гетероциклил являются такими, как описано в настоящем изобретении.
[0071] Термин "необязательно замещенный" означает, что группа может включать один или большее количество заместителей. Один или большее количество атомов водорода группы могут быть заменены замещающими группами, независимо выбранными из группы, включающей галогены (например, галогеналкил, такой как –CF3 или –CF2H), C1–6 алкил, C2–6 алкенил, C2–6 алкинил, –(CH2)vC3–7 циклоалкил, –(CH2)vC4–7 циклоалкенил, –(CH2)v арил, –(CH2)v гетероциклил, –(CH2)v гетероарил, –C6H4S(O)qC1–6 алкил, –C(Ph)3, –CN, –OR, –O–(CH2)1–6–R, –O–(CH2)1–6–OR, –OC(O)R, –C(O)R, –C(O)OR, –OC(O)NR'R", –NR'R", –NO2, –NRC(O)R', –NRC(O)NR'R", –NRC(S)NR'R", –NRS(O)2R', –NRC(O)OR', –C(NR)NR'R", –C(=NOR')R, –C(=NOH)NR'R", –C(O)NR'R", –C(=NCN)–NR'R", –C(=NR)NR'R", –C(=NR')SR", –NR'C(=NCN)SR", –CONRSO2R', –C(S)NR'R", –S(O)qR, –SO2NR'R", –SO2NRC(O)R', –OS(O)2R, –PO(OR)2 и –NO2;
где v равно 0–6, q равно 0–2 и каждый R, R' и R" независимо выбран из группы, включающей H, C1–6 алкил, C2–6 алкенил, C2–6 алкинил, C3–7 циклоалкил, C4–7 циклоалкенил, арил, гетероциклил, гетероарил, C1–6 алкиларил, C1–6 алкилгетероарил и C1–6 алкилгетероциклил, где алкил, алкенил, алкинил, циклоалкил, циклоалкенил, арил, гетероциклил, гетероарил, C1–6 алкиларил, C1–6 алкилгетероарил или C1–6 алкилгетероциклил, необязательно могут быть замещены с помощью от 1 до 6 одинаковых или разных групп, выбранных из группы, включающей галоген, гидроксигруппу, низший алкил, низшую алкоксигруппу, –CO2H, CF3, CN, фенил, NH2 и –NO2; или если R' и R" присоединены к одному атому азота, то вместе с атомом, в которому они присоединены они могут образовани 5– – 7членное азотсодержащее гетероциклическое кольцо.
[0072] В одном варианте осуществления необязательные заместители могут быть выбраны из группы, включающей: галоген (в частности, Cl, Br или F), C1–6 алкил, C1–6 алкоксигруппу, C2–6 алкенил, C2–6 алкинил, C1–6 галогеналкил (in particular –CF3), C1–6 галогеналкоксигруппу (такую как –OCF3), –OH, фенил, бензил, феноксигруппу, бензилоксигруппу, бензоил, силил, –NH2, –NHC1–4 алкил, –N(C1–4 алкил)2, –CN, –NO2, меркаптогруппу, –P=O(OH)(NH2), –S(O)2NH2, –S(O)2NHC1–4 алкил, –S(O)2N(C1–4 алкил)2, C1–6 алкилкарбонил, C1–6 алкоксикарбонил, CO2H, –S(O)R"' (где R"' означает низший алкил или циклоалкил) и –S(O)2R"' (где R"' означает низший алкил, циклоалкил или OH).
[0073] Если не приведено другое определение и только для кольцевых атомов неароматические карбоциклических или гетероциклических соединений, кольцевые атомы таких соединений также могут быть необязательно замещены одной или двумя группами =O, вместо или в дополнение к описанным выше необязательным заместителям.
[0074] Если необязательный заместитель представляет собой или содержит алкильную, алкенильную, алкинильную, циклоалкильную, арильную, гетероарильную или гетероциклильную группу, то сама группа необязательно может быть замещенной с помощью от 1 до 6 одинаковых или разных заместителей, выбранных из группы, включающей галоген, C1–6 алкил, C1–6 алкоксигруппу, C2–6 алкенил, C2–6 алкинил, C1–6 галогеналкил (in particular –CF3), C1–6 галогеналкоксигруппу (такую как –OCF3), –OH, фенил, бензил, феноксигруппу, бензилоксигруппу, бензоил, –NH2, –NHC1–4 алкил, –N(C1–4 алкил)2, –CN, –NO2, меркаптогруппу, –P=O(OH)(NH2), –S(O)2NH2, –S(O)2NHC1–4 алкил, –S(O)2N(C1–4 алкил)2, C1–6 алкилкарбонил, C1–6 алкоксикарбонил, CO2H, –S(O)R"' (где R"' означает низший алкил или циклоалкил) и –S(O)2R"' (где R"' означает низший алкил, циклоалкил или OH).
[0075] Как указано выше, одним объектом является соединения формулы (I):

Формула (I)
или их фармацевтически приемлемая соль, в которой
R1, R2, R3 и R4 все независимо выбраны из группы, включающей H, необязательно замещенный C1–C6 алкил, необязательно замещенный C2–C6 алкенил, необязательно замещенный C2–C6 алкинил, необязательно замещенную C1–C6 алкоксигруппу, галоген, необязательно замещенный C1–C6 алкилгалоген; необязательно замещенный C1–C6 тиоалкил, –SR, –NRR’, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил,
R5 выбран из группы, включающей H, необязательно замещенный C1–C6 алкил, необязательно замещенный C2–C6 алкенил, необязательно замещенный C2–C6 алкинил, необязательно замещенную C1–C6 алкоксигруппу, галоген, необязательно замещенный C1–C6 алкилгалоген; необязательно замещенный C1–C6 тиоалкил, –SR, –NRR’, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил,
L означает двухвалентный мостик, выбранный из группы, включающей связь, необязательно замещенный C1–C20 алкилен, необязательно замещенный C1–C20 алкенилен, необязательно замещенный C1–C20 алкинилен;
Y отсутствует или означает двухвалентный мостик, выбранный из группы, включающей необязательно замещенный C3–C6 циклоалкилен, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арилен, необязательно замещенный C2–C12 гетероарилен, –C(O)–NR–, –C(O)–NR–(CH2)y–, –C(O)–O–, –C(O)–OR–, –C(O)–O–(CH2)y–, –C(O)–, –C(CX3)–NR–, –CRR’X–NR–, –NR–C(O)–NR’–, –O–C(O)O–, –C=N–O–, –SO2–NR–, –(CH2)x–NR–, –(CH2)y–S–(CH2)z–, –(CH2)y–O–(CH2)z–, где y и z оба означают целые числа, независимо выбранные из группы, включающей 0, 1, 2, 3 и 4;
R6 выбран из группы, включающей H, –COOR, –OR, –NRR’, –SR, необязательно замещенный C1–C20 алкил, необязательно замещенный C2–C20 алкенил, необязательно замещенный C2–C20 алкинил; необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C5–C12 арил, необязательно замещенный C2–C12 гетероарил или необязательно замещенный C2–C12 гетероциклил, необязательно замещенную C1–C6 алканоламиногруппу, необязательно замещенный аминокислотный остаток, необязательно замещенный дипептид, необязательно замещенный трипептид и необязательно замещенный полипептид,
или Y и R6 вместе образуют группу, выбранную из группы, включающей
–C(O)–[NR7–C(R8)(R9)–C(O)]w–OR10;
–C(O)–[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10;
–[NR7–C(R8)(R9)–C(O)]w–OR10; и
–[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10,
где R7, R8, R10, R11 и R12 в каждом случае означают H или необязательно замещенный C1–C6–алкил; R9 в каждом случае независимо выбран из группы, включающей H и боковую цепь аминокислоты или ее производное; и w означает целое число, равное от 0 до 20;
R и R’ независимо означают H, необязательно замещенный C1–C6 алкил, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил, и
X означает галоген.
[0076] Другим объектом являются соединения формулы (Ia):

Формула (Ia)
или их фармацевтически приемлемая соль, в которой:
R5 выбран из группы, включающей H и необязательно замещенный C1–C6 алкил
L означает необязательно замещенный C1–C20 алкилен,
Y означает двухвалентный мостик, выбранный из группы, включающей необязательно замещенный –C(O)–NR–, –C(O)–NR–(CH2)y–, –C(O)–O–, –C(O)–, –(CH2)y–S–(CH2)z–, –(CH2)y–O–(CH2)z–, где y и z оба означают целые числа, независимо выбранные из группы, включающей 0, 1, 2, 3 и 4;
R6 выбран из группы, включающей H, –COOR; необязательно замещенный C5–C12 арил, необязательно замещенный C2–C12 гетероарил, необязательно замещенную C1–C6 алканоламиногруппу, необязательно замещенный аминокислотный остаток,
или Y и R6 вместе образуют группу, выбранную из группы, включающей
–C(O)–[NR7–C(R8)(R9)–C(O)]w–OR10;
–C(O)–[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10;
где R7, R8, R10, R11 и R12 в каждом случае означают H или необязательно замещенный C1–C6–алкил; R9 в каждом случае независимо выбран из группы, включающей H и боковую цепь аминокислоты или ее производное; и w означает целое число, равное от 0 до 20;
R и R’ независимо означают H, необязательно замещенный C1–C6 алкил.
[0077] Другим объектом являются соединения формулы (Ib):

Формула (Ib)
или их фармацевтически приемлемая соль, в которой:
R5 выбран из группы, включающей H и метил,
R6 выбран из группы, включающей H, –COOR, –OH, необязательно замещенный C5–C12 арил, необязательно замещенный C2–C12 гетероарил,
R означает H или необязательно замещенный C1–C6 алкил;
R13 в каждом случае независимо выбран из группы, включающей H, необязательно замещенный фенил и необязательно замещенный бензил,
n означает целое число, выбранное из группы, включающей 1, 2, 3, 4 и 5, и
m означает целое число, выбранное из группы, включающей 0, 1, 2 и 3.
[0078] В одном варианте осуществления L означает любую подходящую мостиковую группу. В одном варианте осуществления L означает связь. В других вариантах осуществления L означает двухвалентную мостиковую группу, выбранную из группы, включающей необязательно замещенный C1–C20 алкилен, необязательно замещенный C1–C20 алкенилен, необязательно замещенный C1–C20 алкинилен. В одном предпочтительном варианте осуществления L означает C2 алкилен. В другом предпочтительном варианте осуществления L означает C3 алкилен. В другом предпочтительном варианте осуществления L означает C4 алкилен. В другом предпочтительном варианте осуществления L означает C5 алкилен. В другом предпочтительном варианте осуществления L означает C10 алкилен.
[0079] В одном варианте осуществления Y отсутствует или означает любую подходящую мостиковую группу. В одном варианте осуществления Y отсутствует. В другом варианте осуществления Y означает двухвалентную мостиковую группу, выбранную из группы, включающей необязательно замещенный C3–C6 циклоалкилен, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арилен, необязательно замещенный C2–C12 гетероарилен, –C(O)–NR–, –C(O)–NR–(CH2)y–, –C(O)–O–, –C(O)–OR–, –C(O)–O–(CH2)y–, –C(O)–, –C(CX3)–NR–, –CRR’X–NR–, –NR–C(O)–NR’–, –O–C(O)O–, –C=N–O–, –SO2–NR–, –(CH2)x–NR–, –(CH2)y–S–(CH2)z–, –(CH2)y–O–(CH2)z–, где y и z оба означают целые числа, независимо выбранные из группы, включающей 0, 1, 2, 3 и 4; R и R’ независимо означают H, необязательно замещенный C1–C6 алкил, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил, и X означает галоген. В другом предпочтительном варианте осуществления Y означает –C(O)–NH–. В другом предпочтительном варианте осуществления Y означает –C(O)–. В другом предпочтительном варианте осуществления Y означает –S–. В другом предпочтительном варианте осуществления Y означает –S–(CH2)2–. В другом предпочтительном варианте осуществления Y означает –O–. В другом предпочтительном варианте осуществления Y означает –C(O)–NR–(CH2)y–. В другом предпочтительном варианте осуществления Y означает –C(O)–NH–(CH2)2–.
[0080] В одном варианте осуществления R1, R2, R3 и R4 независимо означают выбраны из группы, включающей H, необязательно замещенный C1–C6 алкил, необязательно замещенный C2–C6 алкенил, необязательно замещенный C2–C6 алкинил, необязательно замещенную C1–C6 алкоксигруппу, галоген, необязательно замещенный C1–C6 алкилгалоген; необязательно замещенный C1–C6 тиоалкил, –SR, –NRR’, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил; где R и R’ независимо означают H, необязательно замещенный C1–C6 алкил, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил. В предпочтительном варианте осуществления один или большее количество из R1, R2, R3 и R4 означают H. В другом предпочтительном варианте осуществления R1 означает H. В другом предпочтительном варианте осуществления R2 означает H. В другом предпочтительном варианте осуществления R3 означает H. В другом предпочтительном варианте осуществления R4 означает H.
[0081] В одном варианте осуществления R5 выбран из группы, включающей H, необязательно замещенный C1–C6 алкил, необязательно замещенный C2–C6 алкенил, необязательно замещенный C2–C6 алкинил, необязательно замещенную C1–C6 алкоксигруппу, галоген, необязательно замещенный C1–C6 алкилгалоген; необязательно замещенный C1–C6 тиоалкил, –SR, –NRR’, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил, где R и R’ независимо означают H, необязательно замещенный C1–C6 алкил, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил. В предпочтительном варианте осуществления R5 означает H. В другом предпочтительном варианте осуществления R5 означает метил.
[0082] В одном варианте осуществления R6 выбран из группы, включающей H, –OR, –C(O)OR, C(O)NR, –NRR’, –SR, необязательно замещенный C1–C20 алкил, необязательно замещенный C2–C20 алкенил, необязательно замещенный C2–C20 алкинил; необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C5–C12 арил, необязательно замещенный C2–C12 гетероарил или необязательно замещенный C2–C12 гетероциклил, необязательно замещенную C1–C6 алканоламиногруппу, необязательно замещенный аминокислотный остаток, необязательно замещенный дипептид, необязательно замещенный трипептид и необязательно замещенный полипептид, где R и R’ независимо означают H, необязательно замещенный C1–C6 алкил, необязательно замещенный C3–C7 циклоалкил, необязательно замещенный C2–C12 гетероциклил, необязательно замещенный C5–C12 арил и необязательно замещенный C2–C12 гетероарил. В предпочтительном варианте осуществления R6 означает H. В других предпочтительных вариантах осуществления R6 означает необязательно замещенный C5–C12 арил. В других предпочтительных вариантах осуществления R6 означает необязательно замещенный C6 арил. В других предпочтительных вариантах осуществления, R6 означает C5–C12 арил, замещенный одной или большим количеством алкоксигрупп. В других предпочтительных вариантах осуществления R6 означает C5–C12 арил, замещенный одной или большим количеством метоксигрупп. В других предпочтительных вариантах осуществления, R6 означает C6 арил, замещенный двумя метоксигруппами. В других предпочтительных вариантах осуществления, R6 означает 3,4–диметоксифенил. В других предпочтительных вариантах осуществления R6 означает группу, образованную из аминокислоты. В других предпочтительных вариантах осуществления R6 означает группу, образованную из аминоспирта. В других предпочтительных вариантах осуществления, R6 означает группу, образованную из фенилаланина.
[0083] В других вариантах осуществления Y и R6 вместе могут образовать группу
a) –C(O)–[NR7–C(R8)(R9)–C(O)]w–OR10
b) –C(O)–[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10;
c) –[NR7–C(R8)(R9)–C(O)]w–OR10; или
d) –[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10;
в которой R7, R8, R10, R11 и R12 в каждом случае означают H или необязательно замещенный C1–C6–алкил; R9 в каждом случае независимо выбран из группы, включающей H и боковую цепь аминокислоты или ее производное; и w означает целое число, равное от 0 до 20. В некоторых вариантах осуществления R7 означает H. В некоторых вариантах осуществления R8 означает H. В некоторых вариантах осуществления R11 означает H. В некоторых вариантах осуществления R12 означает H. В некоторых вариантах осуществления R10 выбран из группы, включающей H, метил, этил, пропил и трет–бутил. В некоторых вариантах осуществления w означает целое число, равное от 0 до 10. В некоторых вариантах осуществления w равно 1. В некоторых вариантах осуществления w равно 2. В некоторых вариантах осуществления w равно 3. В некоторых вариантах осуществления R9 означает H или боковую цепь аминокислоты или ее производное, выбранное из группы, включающей 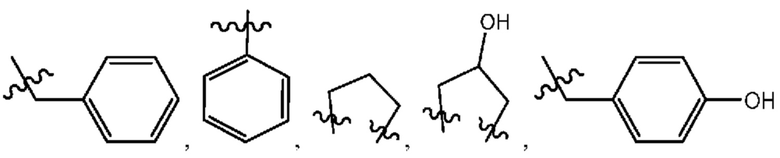 , и
, и  . В некоторых вариантах осуществления Y и R6 вместе образуют группу формулы –C(O)–[NR7–C(R8)(R9)–C(O)]w–OR10, где R7, R8 и R10 означают H, R9 означает
. В некоторых вариантах осуществления Y и R6 вместе образуют группу формулы –C(O)–[NR7–C(R8)(R9)–C(O)]w–OR10, где R7, R8 и R10 означают H, R9 означает  и w равно 1.
и w равно 1.
[0084] Для соединений формулы (I), раскрытых в настоящем изобретении, возможны следующие комбинации любых одного или большего количества (i) – (viii):
(i) R1 означает H;
(ii) R2 означает H;
(iii) R3 означает H;
(iv) R4 означает H;
(v) R5 означает H; или
R5 означает метил;
(vi) L означает связь; или
L означает C2 алкилен; или
L означает C3 алкилен; или
L означает C4 алкилен; или
L означает C5 алкилен; или
L означает C10 алкилен;
(vii) Y отсутствует; или
Y означает –C(O) –NH–; или
Y означает –C(O)–NH–(CH2)y–; или
Y означает –C(O)–NH–(CH2)2–; или
Y означает –C(O)–O–; или
Y означает –C(O)–; или
Y означает –S–; или
Y означает –S–(CH2)2–; или
Y –O–;
(viii) R6 означает H; или
R6 означает –COOH; или
R6 означает –фенил; или
R6 означает –3,4–диметоксифенил; или
R6 означает гетероарил; или
R6 означает аминокислотный остаток или его производное; или
R6 означает остаток аминоспирта или его производное; или
Y и R6 вместе образуют группу формулы
a) –C(O)–[NR7–C(R8)(R9)–C(O)]w–OR10
b) –C(O)–[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10;
c) –[NR7–C(R8)(R9)–C(O)]w–OR10; или
d) –[NR7–C(R8)(R9)–C(R11)(R12)]w–OR10,
где R7, R8, R9, R10, R11 и R12 и w являются такими, как определено выше.
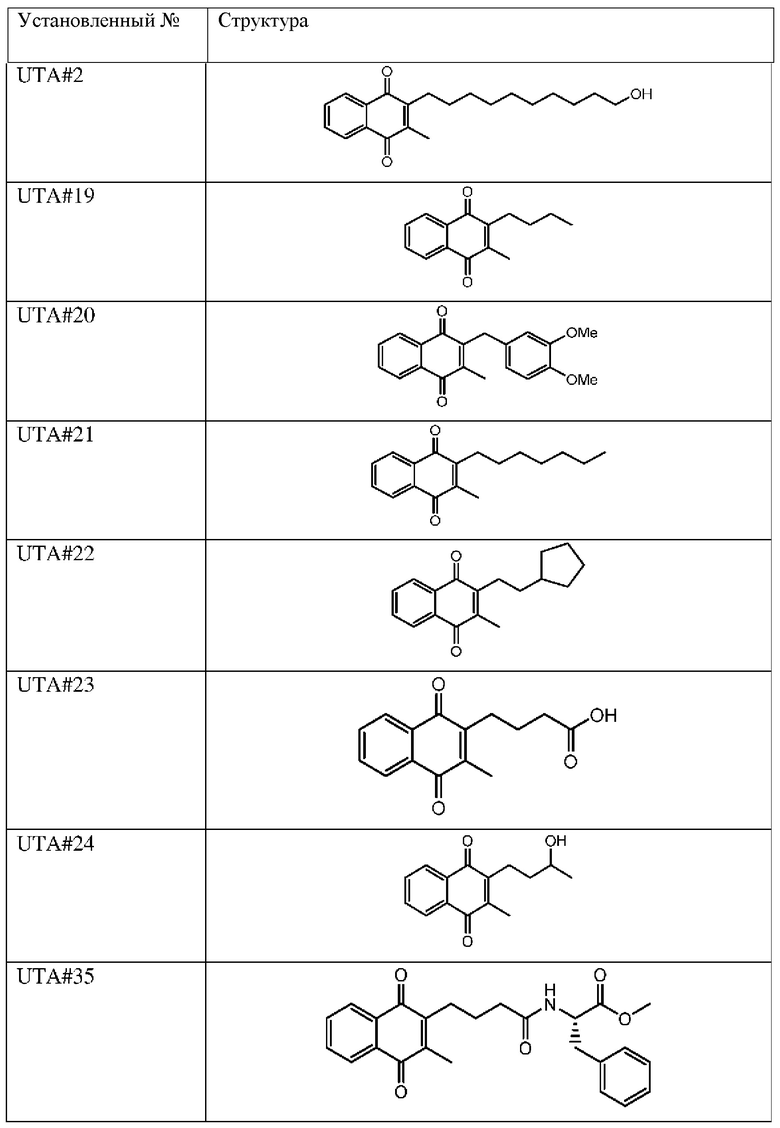
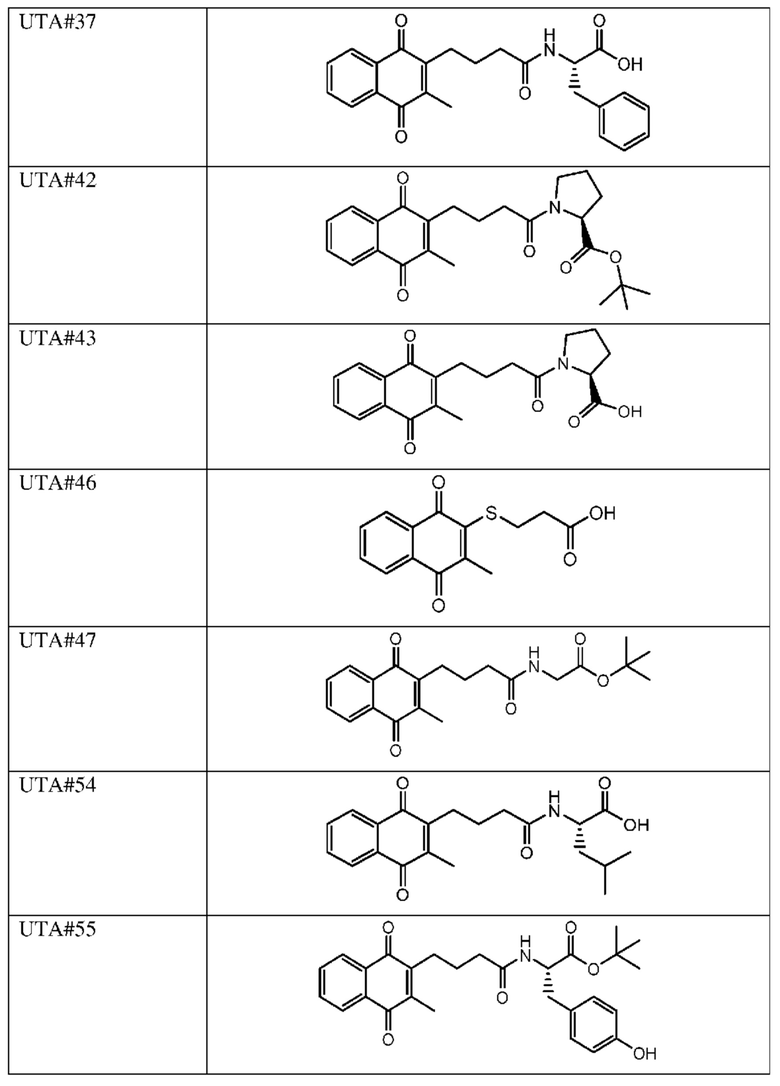
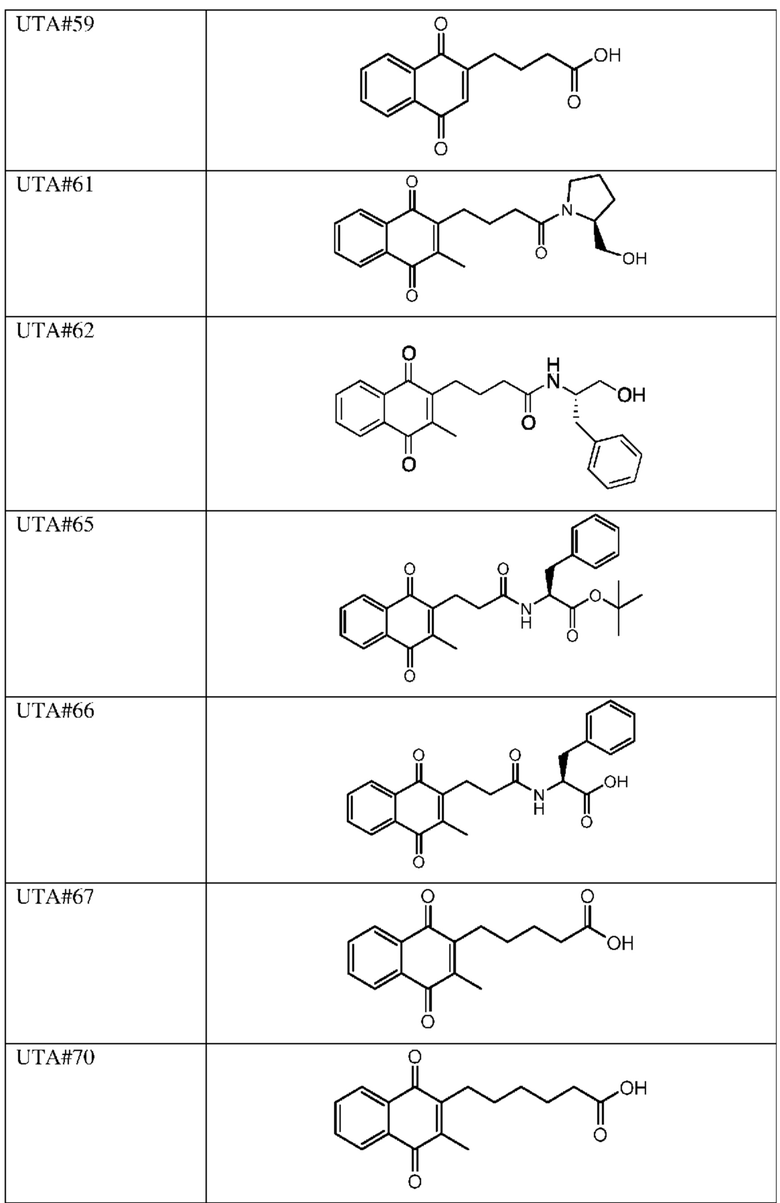
[0085] Типичные соединения формулы (I) включают:
Таблица 3: Типичные соединения формулы (I)
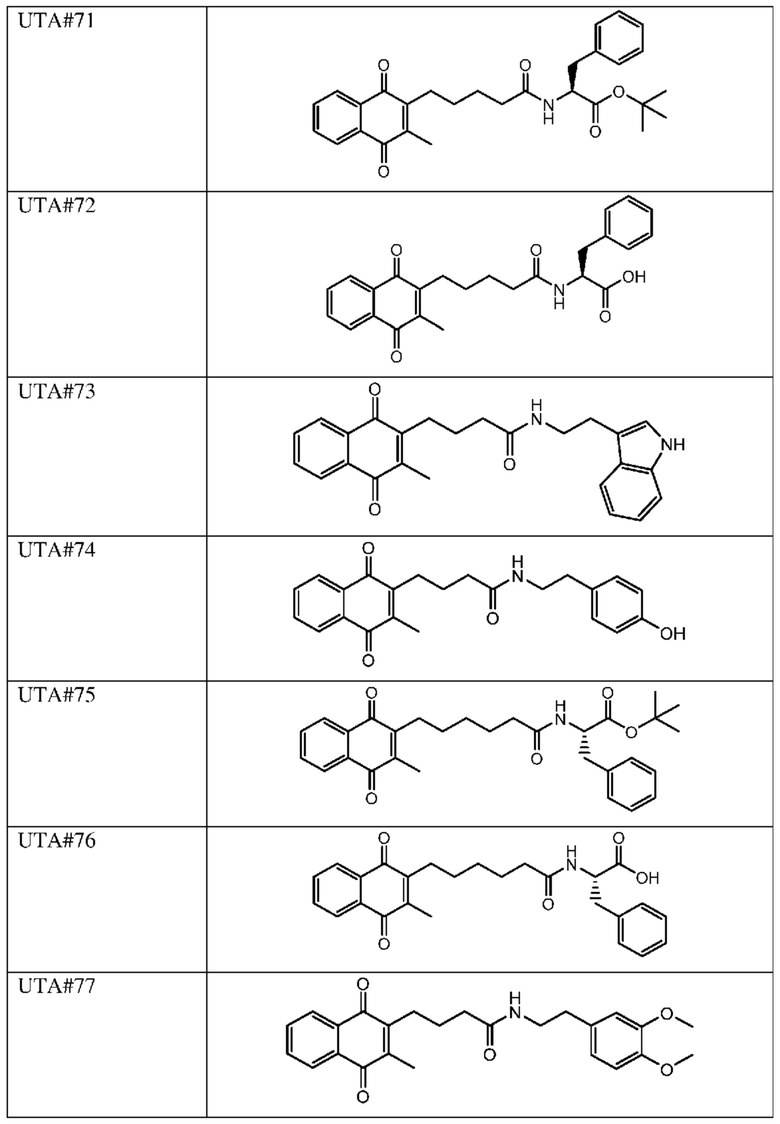
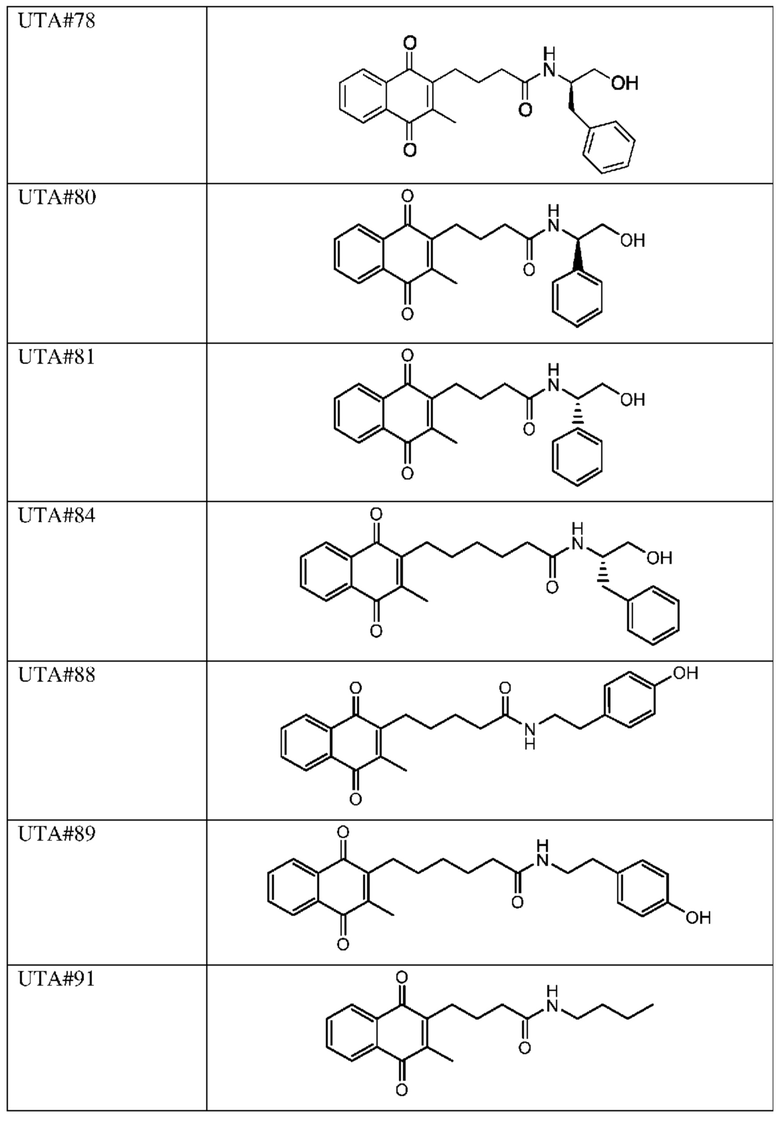
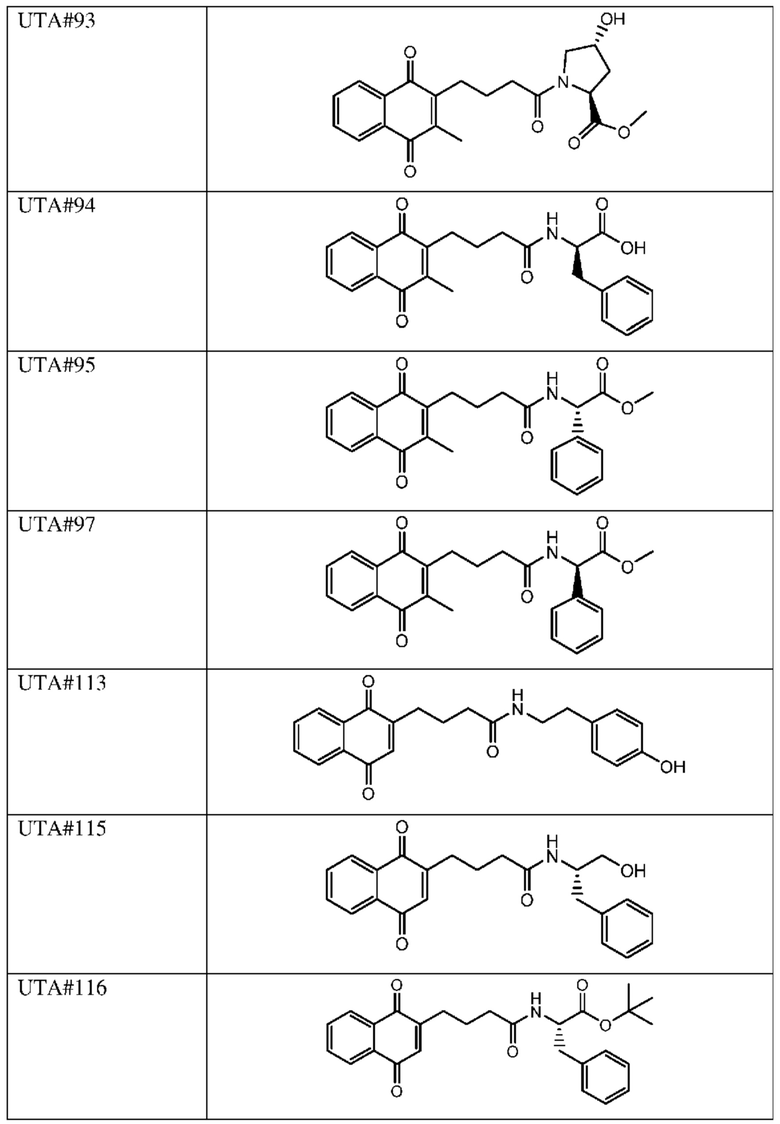
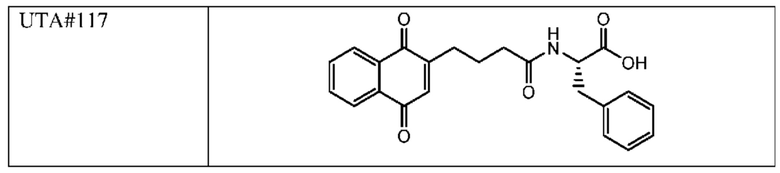
[0086] Соли соединений формулы (I), формулы (Ia) и формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, предпочтительно являются фармацевтически приемлемыми, но следует понимать, что фармацевтически неприемлемые соли также входят в объем настоящего изобретения, поскольку они применимы в качестве промежуточных продуктов для получения фармацевтически приемлемых солей. Соли также могут быть косметически приемлемыми, если соединения используют для замедления старения.
[0087] Следует понимать, что соединения формулы (I), формулы (Ia) и формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, и их соли, могут содержаться в форме фармацевтически приемлемых производных. Термин "фармацевтически приемлемое производное" включает фармацевтически приемлемые сложные эфиры, пролекарства, сольваты и гидраты соединений формулы (I), формулы (Ia) или формулы (Ib) или их соли. Фармацевтически приемлемые производные могут включать любой фармацевтически приемлемый гидрат или любое другое соединение или пролекарство, которое после введения субъекту способно образовать (прямо или косвенно) соединение формулы (I) или его активный метаболит или остаток.
[0088] Фармацевтически приемлемые соли включают соли присоединения с кислотами, соли присоединения с основаниями и соли четвертичных аминов и пиридиниевых соединений. Соли присоединения с кислотами образуются из соединения, предлагаемого в настоящем изобретении, и фармацевтически приемлемой неорганической или органической кислоты включая, но не ограничиваясь только ими, хлористоводородную, бромистоводородную, серную, фосфорную, метансульфоновую, толуолсульфоновую, бензолсульфоновую, уксусную, пропионовую, аскорбиновую, лимонную, малоновую, фумаровую, малеиновую, молочную, салициловую, сульфаминовую или винную кислоты. Противоионы четвертичных аминов и пиридиниевых соединений включают хлорид, бромид, йодид, сульфат, фосфат, метансульфонат, цитрат, ацетат, малонат, фумарат, сульфамат и тартрат. Соли присоединения с основаниями включают, но не ограничиваются только ими, такие соли, как соли натрия, калия, кальция, лития, магния, аммония и алкиламмония. Кроме того, основные азотсодержащие группы можно кватернизовать такими реагентами, как низшие алкилгалогениды, такие как метил–, этил–, пропил– и бутилхлориды, –бромиды и –йодиды; диалкилсульфаты, такие как диметил– и диэтилсульфат; и др. Соли можно получить обычным образом, например, путем обработки соединения подходящей кислотой или основанием в присутствии подходящего растворителя.
[0089] Соединения формулы (I), формулы (Ia) и формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении могут находиться в кристаллическом виде и/или в виде сольватов (например, гидратов) и следует понимать, что обе формы входят в объем настоящего изобретения. Термин "сольват" означает комплекс переменной стехиометрии, образованный растворенным веществом и растворителем. Такие растворители не должны мешать биологической активности растворенного вещества. Растворителями могут быть, например, вода, этанол или уксусная кислота. Методики сольватации обычно известны в данной области техники.
[0090] Термин "пролекарство" используется в самом широком смысле и включает такие производные, которые in vivo превращаются в соединения, предлагаемые в настоящем изобретении. Такие производные известны специалистам в данной области техники и включают, например, соединения, в которых свободную гидроксигруппу превращают в сложноэфирное производное или кольцевой атом азота превращают в N–оксид. Примеры сложноэфирных производных включают алкиловые сложные эфиры, фосфаты и образованные из аминокислот, предпочтительно валина. Любое соединение, которое является пролекарством соединения формулы (I), формулы (Ia) и формулы (Ib) или вариантов осуществления, указанных выше в настоящем изобретении, входит в объем и сущность настоящего изобретения.
[0091] Термин "фармацевтически приемлемый сложный эфир" включает биологически приемлемые сложные эфиры соединения формулы (I), формулы (Ia) и формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, такие как производные сульфоновой, фосфоновой и карбоновой кислоты.
[0092] Таким образом, другим объектом настоящего изобретения является пролекарство или фармацевтически приемлемый сложный эфир соединения, предлагаемого в настоящем изобретении, или его соль.
[0093] Следует понимать, что соединения, предлагаемые в настоящем изобретении, содержат по меньшей мере один асимметрический центр и поэтому могут находиться более, чем в одной стереоизомерной форме. Настоящее изобретение включает все эти формы по отдельности и в смесях, включая рацематы. Изомеры обычно можно разделить по хроматографическим методикам или с использованием разделяющего реагента. Альтернативно, отдельные изомеры можно получить асимметрическим синтезом с использованием хиральных промежуточных продуктов. Если соединение содержит по меньшей мере одну двойную углерод–углеродную связь, то оно может находиться в Z– и E–формах и все изомерные формы соединений формулы (I), формулы (Ia) и формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, включены в настоящее изобретение.
[0094] Настоящее изобретение также включает, если это возможно, соль или фармацевтически приемлемое производное, такое как фармацевтически приемлемый сложный эфир, сольват и/или пролекарство указанных выше вариантов осуществления настоящего изобретения.
[0095] Другим объектом настоящего изобретения является фармацевтическая композиция, которая включает терапевтически эффективное количество одного или большего количества указанных выше соединений или их фармацевтически приемлемых солей, включая их фармацевтически приемлемые производные и необязательно фармацевтически приемлемый носитель или разбавитель. Еще одним объектом настоящего изобретения является косметическая композиция, которая включает косметически эффективное количество одного или большего количества указанных выше соединений или фармацевтически или косметически приемлемых их солей, включая их фармацевтически приемлемые производные и необязательно фармацевтически приемлемый носитель или разбавитель. Косметический препарат применим для ослабления эффектов старения и его можно назвать препаратом от старения.
[0096] Термин "композиция" включает препарат активного ингредиента с капсулирующим материалом в качестве носителя и представляет собой капсулу, в которой активный ингредиент (с носителем или без него) окружен носителями.
[0097] Фармацевтические композиции или препараты включают подходящие для перорального, ректального, назального, местного (включая трансбуккальное и сублингвальное), глазного, вагинального или парентерального (включая внутримышечное, подкожное и внутривенное) введения или в форме, подходящей для введения путем ингаляции или вдувания.
[0098] Соединения формулы (I), формулы (Ia) или формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, вместе с обычным вспомогательным веществом, носителем или разбавителем, можно ввести в форму фармацевтических композиций и их разовых дозированных форм и в такой форме можно использовать в виде твердых веществ, таких как таблетки или заполненные капсулы, или жидкостей, таких как растворы, суспензии, эмульсии, эликсиры, или заполненных ими капсул, все для перорального применения, в форме суппозиториев для ректального введения; или в форме стерильных растворов для инъекций для парентерального (включая подкожное) применения.
[0099] Такие фармацевтические композиции и их разовые дозированные формы могут содержать обычные ингредиенты в стандартных соотношениях с добавлением или без добавления активных соединений или действующих веществ и такие разовые дозированные формы могут содержать любое подходящее эффективное количество активного ингредиента, соответствующее назначенному суточному диапазону доз. Препараты, содержащие десять (10) мг активного ингредиента или, шире от 0,1 до ста (100) мг на таблетку соответственно, являются подходящими типичными разовыми дозированными формами.
[00100] Соединения формулы (I), формулы (Ia) и формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, можно вводить в широком диапазоне пероральных, местных, глазных и парентеральных дозированных форм. Специалисты в данной области техники должны понимать, что указанные ниже дозированные формы могут содержать в качестве активного компонента, соединение формулы (I), формулы (Ia) и формулы (Ib) или его фармацевтически приемлемую соль.
[00101] Для приготовления фармацевтических композиций из соединений формулы (I), формулы (Ia) или формулы (Ib) или вариантов осуществления, указанных выше в настоящем изобретении, фармацевтически приемлемые носители могут быть твердыми или жидкими. Твердые формы препаратов включают порошки, таблетки, пилюли, капсулы, каше, суппозитории, диспергирующиеся гранулы. Твердым носителем может быть одно или большее количество веществ, которые также могут действовать, как разбавители, вкусовые агенты, солюбилизаторы, смазывающие вещества, суспендирующие агенты, связующие, консерванты, разрыхляющие агенты для таблеток или капсулирующий материал.
[00102] В порошках носителем является тонкоизмельченное твердое вещество, которое находится в смеси с тонкоизмельченным активным компонентом.
[00103] В таблетках активный компонент смешан с носителем, обладающим необходимой связующей способностью, в подходящих соотношениях и уплотнен в приданием необходимой формы и размера.
[00104] Порошки и таблетки предпочтительно содержат от 5 или 10 примерно до 70% активного соединения. Подходящими носителями являются карбонат магния, стеарат магния, тальк, сахар, лактоза, пектин, декстрин, крахмал, желатин, трагакантовая камедь, метилцеллюлоза, натриевая соль карбоксиметилцеллюлозы, низкоплавкий воск, масло какао и т. п. Термин "препарат" включает препарат активного соединения с капсулирующим материалом в качестве носителя с образованием капсулы, в которой активный компонент с носителями или без них окружен носителем, который таким образом с ним совмещен. Аналогичным образом, включены саше и облатки. Таблетки, порошки, капсулы, пилюли, саше и облатки можно использовать в виде твердых форм, подходящих для перорального введения.
[00105] Для приготовления суппозиториев низкоплавкий воск, такой как смесь глицеридов жирных кислот или масло какао, сначала расплавляют и активный компонент равномерно диспергируют в нем, например, путем перемешивания. Затем расплавленную однородную смесь выливают в формы подходящего размера, дают охладиться и тем самым затвердеть.
[00106] Препараты, подходящие для вагинального введения, могут находиться в форме пессариев, тампонов, кремов, гелей, паст, пенок или спреев, в дополнение к активному ингредиенту содержащих такие носители, которые известны в данной области техники, как подходящие.
[00107] Жидкие формы препаратов включают растворы, суспензии и эмульсии, например, растворы в воде или смеси или вода–пропиленгликоль. Например, парентеральные жидкие препараты для инъекции можно приготовить в виде растворов в водном растворе полиэтиленгликоля.
[00108] Стерильные жидкие формы композиций включают стерильные растворы, суспензии, эмульсии, сиропы, эликсиры или стерильные глазные растворы. Активный ингредиент можно растворить или суспендировать в фармацевтически приемлемом носителе, таком как стерильная вода, стерильный органический растворитель или их смесь.
[00109] Соединения формулы (I), формулы (Ia) и формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, можно приготовить для парентерального введения (например, путем инъекции, например, болюсной инъекции или непрерывного вливания) и можно приготовить в разовой дозированной форме в ампулах, заполненных шприцах, для малообъемного вливания или в многодозовых контейнерах с добавлением консерванта. Композиции могут быть в таких формах, как суспензии, растворы, или эмульсии в маслообразных или водных разбавителях и могут содержать агенты для приготовления препаратов, такие как суспендирующие, стабилизирующие и/или диспергирующие агенты. Альтернативно, активный ингредиент может находиться в форме порошка, полученного с помощью асептического выделения стерильного твердого вещества или с помощью лиофилизации из растворов для восстановления перед использованием подходящим разбавителем, например, стерильной апирогенной водой.
[00110] Водные растворы, подходящие для перорального применения, можно получить путем растворения активного компонента в воде и при желании добавления подходящих окрашивающих, вкусовых, стабилизирующих и загущающих агентов.
[00111] Водные суспензии, подходящие для перорального применения, можно получить путем диспергирования тонкоизмельченного активного компонента в воде вместе с вязким материалом, таким как натуральные или синтетические камеди, смолы, метилцеллюлоза, натриевая соль карбоксиметилцеллюлозы или другие хорошо известные суспендирующие агенты.
[00112] Также включены твердые формы препаратов, которые предназначены для проводимого незадолго до использования превращения в жидкие формы препаратов для перорального введения. Такие жидкие формы включают растворы, суспензии и эмульсии. Эти препараты в дополнение к активному компоненту могут содержать красители, вкусовые вещества, стабилизаторы, буферы, искусственные и натуральные подсластители, диспергирующие средства, загустители, солюбилизирующие агенты и т. п.
[0100] Для местного введения в эпидермис соединения, предлагаемые в настоящем изобретении, можно приготовить в виде мазей, кремов или примочек или в виде чрескожного пластыря. Мази и кремы можно, например, приготовить с водной или масляной основой путем добавления подходящих загущающих и/или гелеобразующих агентов. Примочки можно приготовить с водной или масляной основой и обычно они также содержат один или большее количество эмульгирующих агентов, стабилизирующих агентов, диспергирующих агентов, суспендирующих агентов, загущающих агентов или окрашивающих агентов.
[0101] Препараты, подходящие для местного введения в полость рта, включают лепешки, включающие активное средство в придающей вкус основе, обычно такой как сахароза и камедь акации или трагакантовая камедь; пастилки, включающие активный ингредиент в инертной основе, такой как желатин и глицерин или сахароза и камедь акации; и полоскания для рта, включающие активный ингредиент в подходящем жидком носителе.
[0102] Растворы или суспензии вводят непосредственно в полость носа обычными средствами, например, капельницей, пипеткой или распылительным устройством. Препараты могут находиться в однодозовой или многодозовой форме. В последнем случае при использовании капельницы или пипетки это может обеспечить введение пациенту заданного объема раствора или суспензии. В случае распыления это можно обеспечить, например, с помощью дозирующего атомизирующего распылительного насоса. Для улучшения назальной доставки и удерживания соединения формулы (I), формулы (Ia) или формулы (Ib) можно капсулировать циклодекстринами или готовить с другими средствами, которые могут улучшить доставку и удерживание в слизистой оболочке носа.
[0103] Введение в дыхательные пути также можно провести с помощью аэрозольного препарата, в котором активный ингредиент находится в упаковке под давлением с подходящим пропеллентом, таким как хлорфторуглерод (CFC), например, дихлордифторметан, трихлорфторметан или дихлортетрафторэтан, диоксид углерода или другой подходящий газ. Аэрозоль также может содержать поверхностно–активное вещество, такое как лецитин. Дозу лекарственного средства можно регулировать с помощью дозирующего клапана.
[0104] Альтернативно, активные ингредиенты могут находиться в форме порошка, например, смеси порошка соединения с подходящей порошкообразной основой, такой как лактоза, крахмал, производные крахмала, такие как гидроксипропилметилцеллюлоза и поливинилпирролидон (PVP). Затем порошкообразный носитель образует гель в полости носа. Порошкообразная композиция может находиться в форме разовой дозы, например, в капсулах или картриджах, например, из желатина, или в блистерных упаковках, из которых порошок можно вводить с помощью ингалятора.
[0105] В препаратах, предназначенных для введения в дыхательные пути, включая назальные препараты, соединение обычно обладает частицами небольшого размера, например, порядка от 5 до 10 мкм или менее. Частицы такого размера можно получить по методикам, известным в данной области техники, например, путем микронизации.
[0106] Для глазного введения, соединения, предлагаемые в настоящем изобретении, можно приготовить в виде стерильного глазного раствора или в виде глазного устройства доставки (такого как контактная линза и т. п., облегчающего немедленное высвобождение, последовательное высвобождение или пролонгированное высвобождение). Для глазного введения, композиция предпочтительно находится в форме офтальмологической композиции. Офтальмологические композиции предпочтительно готовят в виде препаратов глазных капель и помещают в подходящие контейнеры для облегчения введения в глаза, например, в капельницу, снабженную подходящей пипеткой. Предпочтительно, если композиции являются стерильными и изготовлены на водной основе с использованием очищенной воды. В дополнение к соединению, предлагаемому в настоящем изобретении, офтальмологическая композиция может содержать один или большее количество из следующих: поверхностно–активное вещество; загущающие агенты; антиоксидант; этанол и другие инертные наполнители, такие как изотонический агент, буфер, консервант и/или регулирующий pH агент. Желательное значение pH офтальмологической композиции находится в диапазоне от 4 до 8.
[0107] При желании можно использовать препараты, приспособленные для замедленного высвобождения активного ингредиента. Кроме того, препараты могут быть в форме, подходящей для использования в косметике с целью ослабления эффектов старения.
[0108] Фармацевтические препараты предпочтительно находятся в виде разовых дозированных форм. В такой форме препарат разделен на разовые дозы, содержащие соответствующие количества активного компонента. Разовая дозированная форма может представлять собой упакованный препарат, упаковка содержит дискретные количества препарата, такие как упакованные таблетки, капсулы и порошки во флаконах или ампулах. Кроме того, разовая дозированная форма может представлять собой капсулу, таблетку, саше или лепешку, или она может содержать соответствующее количество этих упакованных форм.
[0109] Настоящее изобретение также включает соединения формулы (I), формулы (Ia) и формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, при отсутствии носителя, где соединения находятся в разовой дозированной форме.
[0110] Количество вводимого соединения формулы (I), формулы (Ia) и формулы (Ib) или вариантов осуществления, указанных выше в настоящем изобретении, может находиться в диапазоне примерно от 10 мг до 2000 мг/сутки в зависимости от активности соединения и подвергающегося лечению заболевания.
[0111] Жидкости или порошки для назального введения, таблетки или капсулы для перорального введения и жидкости для внутривенного введения являются предпочтительными композициями.
[0112] Фармацевтические препараты соединений формулы (I), формулы (Ia) и формулы (Ib) или вариантов осуществления, указанных выше в настоящем изобретении, можно вводить совместно с одним или большим количеством других активных средств в комбинированной терапии. Например, фармацевтические препараты активного соединения можно вводить совместно (например, по отдельности, одновременно или последовательно) с одним или большим количеством других средств, использующихся для лечения заболеваний или нарушений, связанных с митохондриальной дисфункцией. Например, фармацевтические препараты соединений, предлагаемых в настоящем изобретении, можно вводить совместно с другими митохондриальными защитными средствами или антиоксидантами, или компонентом, который модулирует метаболизм энергии, таким как предшественники или продукты дыхания клеток. Некоторые варианты осуществления относятся к фармацевтической композиции, дополнительно включающей противодиабетическое средство в качестве дополнительного активного средства.
[00113] Кроме того, фармацевтические препараты активных соединений можно вводить совместно (например, по отдельности, одновременно или последовательно) для лечения, предупреждения, облегчения протекания или уменьшения вызванной лекарственным средством или вызванной окружающей средой митохондриальной дисфункции. Например, фармацевтические препараты активных соединений можно вводить совместно с другими активными средствами, оказывающими негативное влияние на митохондриальную активность или функцию, для лечения, предупреждения, облегчения протекания или уменьшения вызванной лекарственным средством или окружающей средой митохондриальной дисфункции. Примеры других активных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают противовирусное средство; противораковое средство; антибиотик; CNS лекарственное средство; гипотензивное лекарственное средство; антрациклины; нестероидное противовоспалительное лекарственное средство (NSAID); анестетик; бета–блокатор; противоаритмическое; противодиабетическое; противовоспалительное; или другое средство. Соответственно, предполагается, что фармацевтические препараты соединений формулы (I) можно вводить совместно для лечения, предупреждения, облегчения протекания или уменьшения негативного влияния на митохондриальную активность или функцию, связанную с введением других активных средств.
[00114] Примеры противовирусных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают абакавир, диданозин, эмтрицитабин, энтекавир, эмтрицитабин, ламивудин, невирапин, телбивудин, тенофовир, типранавир, ставудин, залцитабин и зидовудин. Примеры противораковых средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают триоксид мышьяка, цетуксимаб, дакарбазин, денилейкин, дифтитокс, флутамид, гемтузумаб, метотрексат, митоксантрон, пентостатин и тамоксифен. Примеры антибиотиков, оказывающих негативное влияние на митохондриальную активность или функцию, включают антимицин A, изониазид, хлорамфеникол, этамбутол, гентамицин, кетоконазол, линезолид, стрептозоцин, стрептомицин, тобрамицин, тетрациклины и тровафлоксацин. Примеры of CNS drugs, оказывающих негативное влияние на митохондриальную активность или функцию, включают амитриптилин, амфетамины, атомоксетин, хлорпромазин, кокаин, дантролен, дезипрамин, дивалпроекс, дроперидол, фелбамат, флуфеназин, имипрамин, метамфетамин, налтрексон, нефазодон, перголид и вальпроевую кислоту. Примеры гипотензивных лекарственных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают босентан. Примеры антрациклинов, оказывающих негативное влияние на митохондриальную активность или функцию, включают даунорубицин, доксорубицин, эпирубицин и идарубицин. Примеры нестероидных противовоспалительных лекарственных средств (NSAIDs), оказывающих негативное влияние на митохондриальную активность или функцию, включают аспирин, целекоксиб, диклофенак, дифлунизал, этодолак, фенопрофен, ибупрофен, индометацин, кетопрофен, мефенаминовая кислота, мелоксикам, напроксен, набуметон, оксапрозин, пироксикам, салсалат, сулиндак, тиоридазин и толметин. Примеры анестетиков, оказывающих негативное влияние на митохондриальную активность или функцию, включают бупивакаин и изофлуран. Примеры бета–блокаторов, оказывающих негативное влияние на митохондриальную активность или функцию, включают атенолол. Примеры противоаритмических средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают амиодарон, дизопирамид, дофетилид и ибутилид. Примеры противодиабетических средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают пиоглитазон и росиглитазон. Примеры противовоспалительных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают преднизолон, дексаметазон, гидрокортизон и триамцилон. Примеры других средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают клиохинол, цианид, гексахлорофен, ротенон и статины. Например, предполагается, что фармацевтические препараты соединений формулы (I) можно вводить совместно для лечения, предупреждения, облегчения протекания или уменьшения негативного влияния влияние на митохондриальную активность или функцию, связанную с введением других активных средств.
[0113] Термин "терапевтически эффективное количество" означает количество, которое достаточно для проведения лечения, определенного выше, при введении субъекту, такому как млекопитающее, включая человека, нуждающемуся в таком лечении. Терапевтически эффективное количество меняется в зависимости от субъекта и подвергающегося лечению патологического состояния, тяжести поражения и пути введения и специалист с общей подготовкой в данной области техники может его определить стандартным образом.
[0114] Термин "лечение" при использовании в настоящем изобретении включает любое лечение патологического состояния или заболевания у животного, предпочтительно млекопитающего, более предпочтительно человека, и включает: (i) предупреждение возникновения заболевания или патологического состояния у субъекта, который может быть предрасположен к заболеванию, но у которого оно пока не диагностировано; (ii) подавление заболевания или патологического состояния, т. е. остановку его развития; (iii) облегчение протекания заболевания или патологического состояния, т. е. обеспечение его регрессии путем "лечения" и также включает косметическое лечение, которое включает нетерапевтическое косметическое лечение для ослабления эффектов старения.
[0115] Настоящее изобретение включает способ лечения млекопитающего, включающий введение соединения формулы (I), формулы (Ia) и формулы (Ib), определенного в настоящем изобретении или его фармацевтически приемлемой соли или содержащих их композиций. Считается, что соединения формулы (I) и содержащие их фармацевтические композиции, предлагаемые в настоящем изобретении применимы для профилактики и/или лечения заболеваний и нарушений, связанных с митохондриальной дисфункцией.
[0116] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, являются первичными митохондриальными заболеваниями включая, но не ограничиваясь только ими, наследственную оптическую нейропатию Лебера (LHON), доминантную оптическую невропатию (DOA), синдром Ли, наследственную атаксию Фридрейха, хромосомную миопатию, энцефаломиопатию, лактоцидоз, симптомы типа удара (MELAS), миоклонический эпилептический припадок с разорванными красными волокнами (MERRF), мионейрогенную гастроинтестинальную энцефаломиопатию (MNGIE), синдром Кирнса–Сейра, дефицит CoQ.10, или дефицит митохондриального комплекса, невропатию, атаксию, пигментную дегенерацию сетчатки и птоз (NARP).
[0117] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, представляют собой нейродегенеративные или нейромышечные нарушения, связанные с митохондриальной дисфункцией, включая, но не ограничиваясь только ими, спинально–церебеллярные атаксии, атаксию–телеангиэктазию, атаксию с окуломоторной апраксией 1 и 2 (AOA1 и 2), эпилептические припадки, боковой амиотрофический склероз (ALS), заболевание двигательных нейронов (MND), болезнь Паркинсона, болезнь Альцгеймера, болезнь Гентингтона, удар/реперфузионное поражение, или слабоумие, мышечную дистрофию Дюшенна (DMD), мышечную дистрофию Беккера (BMD), конечностно–поясную мышечную дистрофию (LGMD), сцепленную с Х–хромосомой дилатационную кардиомиопатию (XLDCM), пантотенаткиназа–ассоциированную нейродегенерацию (PKAN,), спинальную мышечную атрофию (SMA), рассеянный склероз и первичный прогрессирующий рассеянный склероз (PP–MS), болезнь Кугельберга–Веландера и болезнь Верднига–Хоффмана , сахарный диабет и глухоту (DAD).
[0118] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, представляют собой метаболические нарушения, связанные с митохондриальной дисфункцией, включая, но не ограничиваясь только ими, синдром Вольфрама, неалкогольное заболевание печени (т. е. NAFLD, NASH, цирроз), возрастное ухудшение физического состояния, ожирение, избыточную массу тела, сахарный диабет, диабет типа II, диабетическую ретинопатию и метаболический синдром.
[0119] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, представляют собой психические нарушения, связанные с митохондриальной дисфункцией, включая, но не ограничиваясь только ими, шизофрению, большую депрессию, биполярное расстройство, эпилепсию, посттравматическое стрессовое нарушение (PTSD) и нарушения суточного ритма.
[0120] В одном варианте осуществления заболевания и нарушения, связанные с митохондриальной дисфункцией, представляют собой воспалительные нарушения, связанные с митохондриальной дисфункцией, включая, но не ограничиваясь только ими, язвенный колит (UC), болезнь Крона (CD), артрит, псориаз или ревматоидный артрит, мигрень, сухой кератит, увеит, аллергический конъюнктивит, послеоперационное воспаление и острое повреждение почек. В одном варианте осуществления заболевание или нарушение, связанное с митохондриальной дисфункцией, является следствием старения. Hence, соединения, описанные в настоящем изобретении, предложены для ослабления старения путем уменьшения митохондриальной дисфункции.
[00115] В одном варианте осуществления заболевание и нарушение является вызванной лекарственным средством или вызванной окружающей средой митохондриальной дисфункцией. Например, факторы, оказывающие негативное влияние на митохондриальную активность или функцию, включают вызванную лекарственным средством или окружающей средой митохондриальную дисфункцию, обусловленную противовирусным средством; противораковым средством; антибиотиком; CNS лекарственным средством; гипотензивным лекарственным средством; антрациклинами; нестероидным противовоспалительным лекарственным средством (NSAID); анестетиком; бета–блокатором; противоаритмическим; противодиабетическим; противовоспалительным; или другим средством.
[00116] Примеры противовирусных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают абакавир, диданозин, эмтрицитабин, энтекавир, эмтрицитабин, ламивудин, невирапин, телбивудин, тенофовир, типранавир, ставудин, залцитабин и зидовудин. Примеры противораковых средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают триоксид мышьяка, цетуксимаб, дакарбазин, денилейкин, дифтитокс, флутамид, гемтузумаб, метотрексат, митоксантрон, пентостатин и тамоксифен. Примеры антибиотиков, оказывающих негативное влияние на митохондриальную активность или функцию, включают антимицин A, изониазид, хлорамфеникол, этамбутол, гентамицин, кетоконазол, линезолид, стрептозоцин, стрептомицин, тобрамицин, тетрациклины и тровафлоксацин. Примеры лекарственных средств CNS, оказывающих негативное влияние на митохондриальную активность или функцию, включают амитриптилин, амфетамины, атомоксетин, хлорпромазин, кокаин, дантролен, дезипрамин, дивалпроекс, дроперидол, фелбамат, флуфеназин, имипрамин, метамфетамин, налтрексон, нефазодон, перголид и вальпроевую кислоту. Примеры гипотензивных лекарственных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают босентан. Примеры антрациклинов, оказывающих негативное влияние на митохондриальную активность или функцию, включают даунорубицин, доксорубицин, эпирубицин и идарубицин. Примеры нестероидных противовоспалительных лекарственных средств (NSAIDs), оказывающих негативное влияние на митохондриальную активность или функцию, включают аспирин, целекоксиб, диклофенак, дифлунизал, этодолак, фенопрофен, ибупрофен, индометацин, кетопрофен, мефенаминовую кислоту, мелоксикам, напроксен, набуметон, оксапрозин, пироксикам, салсалат, сулиндак, тиоридазин и толметин. Примеры анестетиков, оказывающих негативное влияние на митохондриальную активность или функцию, включают бупивакаин и изофлуран. Примеры бета–блокаторов, оказывающих негативное влияние на митохондриальную активность или функцию, включают атенолол. Пример противоаритмических средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают амиодарон, дизопирамид, дофетилид и ибутилид. Примеры противодиабетических средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают пиоглитазон и росиглитазон. Примеры противовоспалительных средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают преднизолон, дексаметазон, гидрокортизон и триамцилон. Примеры других средств, оказывающих негативное влияние на митохондриальную активность или функцию, включают клиохинол, цианид, гексахлорофен, ротенон и статины.
[0121] В одном варианте осуществления млекопитающим является человек.
[0122] Термины "предупреждение" и "профилактика" при использовании в настоящем изобретении означают проводимое заранее введение лекарственного средства для предупреждения или предотвращения появления одного или большего количества симптомов заболевания или нарушения. Специалист с общей подготовкой в медицине понимает, что термин "предупреждение" не является абсолютным. В области медицины это означает профилактическое введение лекарственного средства для существенного уменьшения вероятности или тяжести патологического состояния или симптома патологического состояния и этот смысл подразумевается в настоящем раскрытии. В соответствии со стандартным руководством в этой области техники, the Physician’s Desk Reference, термины "предупреждать", "предупреждение" и "предупредить" применительно к нарушению или заболеванию, означают предупреждение причины, проявлений, симптомов или прогрессирования заболевания или нарушения до полного проявления самого заболевания или нарушения. Это также относится к ослаблению эффектов старения с целью непосредственного влияния на старения.
[0123] Термины "вводить", "вводят" или "введение" применительно к соединению, композиции или препарату формулы (I), формулы (Ia) или формулы (Ib) или вариантам осуществления, указанным выше в настоящем изобретении, означают введение соединения в систему животного, нуждающегося в лечении. Если соединение, предлагаемое в настоящем изобретении, вводят в комбинации с одним или большим количеством других активных средств, "введение" и его варианты все включают одновременное и/или последовательное введение соединения и других активных средств.
[0124] Соединения формулы (I), формулы (Ia) или формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, также можно использовать для исследований, таких как эксперименты in vitro, in vivo или ex vivo для модулирования одного или большего количества биомаркеров в экспериментальной системе. Такими экспериментальными системами могут быть образцы клеток, образцы тканей, компоненты клеток или смеси компонентов клеток, части органов, цельные органы или организмы. Такие применения в исследованиях могут включать, но не ограничиваются только ими, применение в качестве реагентов для анализа, для изучения биохимических путей или для изучения воздействия других средств на метаболическое состояний экспериментальной системы в присутствии/при отсутствии одного или большего количества соединений, предлагаемых в настоящем изобретении.
[0125] Кроме того, соединения формулы (I), формулы (Ia) и формулы (Ib) или варианты осуществления, указанные выше в настоящем изобретении, можно использовать в биохимических исследованиях или анализах. Такие исследования могут включать инкубацию одного или большего количества соединений формулы (I), формулы (Ia) и формулы (Ib) или вариантов осуществления, указанных выше в настоящем изобретении, с образцом ткани или клеток субъекта для изучения потенциального ответа субъекта (или ответа конкретной подгруппы субъектов) на введение указанного одного или большего количества соединений, или для определения того, какое соединение формулы (I) или формулы (Ia) или вариантов осуществления, указанных выше в настоящем изобретении, приводит к оптимальному эффекту для конкретного субъекта подгруппы субъектов. Соответственно, настоящее изобретение включает анализ или скрининг для выявления соединения формулы (I), формулы (Ia) и формулы (Ib) или варианта осуществления, указанных выше в настоящем изобретении, которое модулирует активность одного или большего количества биомаркеров, анализ включает стадии i) взятия образца клеток или образца ткани у субъекта или группы субъектов, у которых можно изучить модуляцию одного или большего количества биомаркеров; ii) введения одного или большего количества соединений, предлагаемых в настоящем изобретении, в образец (образцы) клеток или образец (образцы) ткани; и iii) количественную оценку влияния соединений на модуляцию одного или большего количества биомаркеров после введения одного или большего количества соединений, по сравнению со статусом биомаркера до введения одного или большего количества соединений.
[0126] Кроме того, настоящее изобретение включает анализ или скрининг для выявления соединения формулы (I), формулы (Ia) и формулы (Ib) или варианта осуществления, указанных выше в настоящем изобретении, которые модулируют активность одного или большего количества биомаркеров, анализ включает стадии i) взятия образца клеток или образца ткани у субъекта или группы субъектов, у которых можно изучить модуляцию одного или большего количества биомаркеров; ii) введения по меньшей мере двух соединений, предлагаемых в настоящем изобретении, в образец (образцы) клеток или образец (образцы) ткани; и iii) количественную оценку влияния соединений на модуляцию одного или большего количества биомаркеров после введения по меньшей мере двух соединений, по сравнению со статусом биомаркера до введения по меньшей мере двух соединений, и iv) выбор соединения для применения для лечения, подавления или модуляции на основе степени модуляции, определенной на стадии iii).
[0127] В одном варианте осуществления биомаркером является хемокин, цитокин, фактор роста или хемотаксическое средство. В методике идентификации соединения формулы (I), формулы (Ia) и формулы (Ib) или варианта осуществления, указанных выше в настоящем изобретении, которое модулирует активность одного или большего количества биомаркеров, соединения можно выбрать на основании одной или большего количества физико–химических, фармакокинетических, биологических и/или физиологических характеристик. Примеры таких характеристик включают, но не ограничиваются только ими, сродство связывания, селективность, токсичность, эффективность, стабильность, липофильность и/или активность, такую как агонизм, антагонизм и/или ингибирование.
[0128] Взаимодействие с биомаркером можно зарегистрировать любыми обычными средствами, такими как ядерный магнитный резонанс (NMR), масс–спектрометрия (MS), изотермическая титрационная калориметрия (ITC), динамическое рассеяние света (DLS), поверхностный плазмонный резонанс(SPR), двойная поляризационная интерферометрия (DPI), микроскопический термофорез (MST), задержка в геле, задержка на фильтре, аффинный совместный электрофорез, анализы с помощью резонансного переноса энергии биолюминесценции (BRET), анализы с помощью резонансного переноса энергии флуоресценции (FRET) assays, поляризация флуоресценции (FP), проксимальные сцинтилляционные анализы или иммобилизация на биочипах или других поверхностях, включая связанные с масс–спектрометрическим детектированием.
[0129] Последнее можно провести с помощью проводимой сначала иммобилизации соединения на чипе с последующим добавлением образца. Альтернативно, данный биомаркер можно иммобилизировать на чипе и использовать для скрининга способности связывать соединение.
[0130] Разумеется, имеется много других методик анализа, которые можно использовать для скрининга взаимодействия между соединением формулы (I), формулы (Ia) или формулы (Ib) и биомаркером. Другой методикой является анализ связывания с фильтром. В этой методике одно из соединений или биомаркер метят репортерной молекулой, способной вырабатывать идентифицирующий сигнал, такой как флуоресцентный краситель, и молекулам дают взаимодействовать в растворе. Затем полученную смесь пропускают через фильтр, способный удерживать один из компонентов, такой как соединение или биомаркер.
[0131] Разные соединения взаимодействуют с разными биологическими регуляторами или разные регуляторы взаимодействуют с разными соединениями или происходит и то, и другое. Кроме того, разные соединения могут взаимодействовать с разными цепями рецептора биологического регулятора. таким образом, другой анализ включает использование афинных колонок, содержащих иммобилизованные хемокины. Затем соединения пропускают через колонку и определяют замедление прохождения соединений. Для элюирования связанных соединений обычно используют градиент соли.
[0132] Другие примеры анализов, входящих в настоящее изобретение, включают функциональные анализы, такие как анализы цельных клеток. Такие функциональные анализы могут дать более полезную информацию о влиянии исследуемого соединения, чем анализы связывания.
[0133] При использовании в настоящем изобретении выражение "фармацевтически приемлемая соль" означает соль данного соединения, где соль является подходящей для введения в качестве фармацевтического средства. Например, такие соли можно получить по реакции кислоты или основания с аминогруппой или карбоксигруппой соответственно.
[0134] Фармацевтически приемлемые соли присоединения с основаниями можно получить из неорганических и органических оснований. Соли, полученные из неорганических оснований включают, но не ограничиваются только ими, соли натрия, калия, лития, аммония, кальция и магния. Соли, полученные из органических оснований включают, но не ограничиваются только ими, соли первичных, вторичных и третичных аминов, замещенных аминов, включая природные замещенные амины и циклические амины, включая изопропиламин, триметиламин, диэтиламин, триэтиламин, трипропиламин, этаноламин, 2–диметиламиноэтанол, трометамин, лизин, аргинин, гистидин, кофеин, прокаин, гидрабамин, холин, бетаин, этилендиамин, глюкозамин, N–алкилглюкамины, теобромин, пурины, пиперазин, пиперидин и N–этилпиперидин. Также следует понимать, что применимы другие производные карбоновой кислоты, например, амиды карбоновой кислоты, включая карбоксамиды, низшие алкилкарбоксамиды, ди(низший алкил)карбоксамиды и т. п.
[0135] Фармацевтически приемлемые соли присоединения с кислотами можно получить из неорганических и органических кислот. Соли, полученные из неорганических кислот, включают соли хлористоводородной кислоты, бромистоводородной кислоты, серной кислоты, азотной кислоты, фосфорной кислоты и т. п. Соли, полученные из органических кислот включают соли уксусной кислоты, пропионовой кислоты, гликолевой кислоты, пировиноградной кислоты, щавелевой кислоты, яблочной кислоты, малоновой кислоты, янтарной кислоты, малеиновой кислоты, фумаровой кислоты, винной кислоты, лимонной кислоты, бензойной кислоты, коричной кислоты, миндальной кислоты, метансульфоновой кислоты, этансульфоновой кислоты, п–толуолсульфоновой кислоты, салициловой кислоты и т. п.
[0136] Термин "защитная группа" означает любую группу, которая после связывания с одной или большим количеством гидроксигрупп, тиогрупп, аминогрупп или карбоксигрупп соединений предупреждает протекание реакций этих групп и эту защитную группу можно удалить с помощью обычных химических или ферментативных стадий с восстановлением гидроксигруппы, тиогруппы, аминогруппы или карбоксигруппы. То, какая конкретная удаляемая блокирующая группа используется, не является критически важным и предпочтительная удаляемая блокирующая группа гидроксигруппы включают обычные заместители, такие как аллил, бензил, ацетил, хлорацетил, тиобензил, бензилидин, фенацил, трет–бутилдифенилсилил и любую другую группу, которую можно химически присоединить к гидроксигруппе и затем селективно удалить с помощью химических или ферментативных методик в мягких условиях, сопоставимых с природой продукта. Защитные группы подробнее описаны в Greene и Wuts (1991), "Protective Groups in Organic Synthesis" 2nd Ed, John Wiley и Sons, N.Y.
[0137] Примеры удаляемых блокирующих групп аминогруппы включают обычные заместители, такие как трет–бутоксикарбонил (t–BOC), бензилоксикарбонил (CBZ), флуоренилметоксикарбонил (FMOC), аллилоксикарбонил (ALOC) и т. п., которые можно удалить в обычных условиях, сопоставимых с природой продукта.
[0138] Примеры удаляемых блокирующих групп гидроксигруппы включают обычные заместители, такие как простые эфирные группы, включая метоксигруппу, трет–бутоксигруппу, силилоксигруппу; метоксиметилоксигруппу (MOM), аллилоксигруппу, бензилоксигруппу и сложноэфирные группы, такие как ацетоксигруппа (AcO–) и бензилоксигруппа, которые можно удалить в обычных условиях, сопоставимых с природой продукта.
[0139] Примеры удаляемых блокирующих групп карбонильной или карбоксигруппы групп включают обычные заместители, такие как сложноэфирные группы, включая метоксигруппу, трет–бутоксигруппу, бензилоксигруппу, которые можно удалить в обычных условиях, сопоставимых с природой продукта.
[0140] "Селективность" или "специфичность" в общем случае является мерой предпочтительности связывания лиганда с разными рецепторами и/или мерой предпочтительности связывания разных лигандов рецептором. Селективность лиганда по отношению к целевому рецептору по сравнению с другим рецептором задается отношением соответствующих значений Kd (т. е. констант диссоциации каждого комплекса лиганд–рецептор) или в случаях, когда биологический эффект наблюдается при значениях, меньших Kd, селективность задается отношением соответствующих значений EC50 (т. е. концентраций, которые обеспечивают 50% максимального ответа на лиганд, взаимодействующий с этими двумя разными рецепторами.
ПРИМЕРЫ
ОБЩИЕ СХЕМЫ СИНТЕЗА И ОПИСАНИЕ
[0141] Для удобства многие химические фрагменты обозначены с помощью хорошо известных аббревиатур, включая, но не ограничиваясь только ими, метил (Me), этил (Et), н–пропил (nPr), изопропил (iPr), н–бутил (nBu), трет–бутил (tBu), н–гексил (nHex), циклогексил (cHex), фенил (Ph), метоксигруппа (MeO), этоксигруппа (EtO), триметилсилил (TMS), трет–бутилоксикарбонил (Boc) и ацетил (Ac).
[0142] Для удобства многие химические соединения обозначены с помощью хорошо известных аббревиатур, включая, но не ограничиваясь только ими, следующие: метанол (MeOH), этанол (EtOH), диэтиловый эфир (Et2O), этилацетат (EtOAc), триэтиламин (TEA), дихлорметан (метиленхлорид, DCM), трифторуксусная кислота (TFA), трифторэтанол (TFE), диметилформамид (DMF), сульфат натрия (Na2SO4), тетрагидрофуран (THF), мета–хлорпероксибензойная кислота (mCPBA), натриевая соль гексаметилдисилазана (NaHMDS), O–(7–азабензотриазол–1–ил)–N, N,N′,N′–тетраметилуронийгексафторфосфат (HATU), диметилсульфоксид (DMSO), сульфат магния (MgSO4), гидрокарбонат натрия (NaHCO3), трет–бутанол (t–BuOH), 1–этил–3–(3–диметиламинопропил)карбодиимидгидрохлорид (EDCl.HCl), тетра–н–бутилфторид аммония (TBAF), тетра–н–бутилбромид аммония (TBAB), N, N–диизопропилэтиламин (DIPEA), трет–бутилдиметилсилил (TBDMS), 1–гидроксибензотриазол (HOBt), транс–дихлорбис(трифенилфосфин)палладий(II) (PdCl2(PPh3)2), тетракис(трифенилфосфин)палладий(0) (Pd(PPh3)4) трис(дибензилиденацетон)дипалладий(0) (Pd2(dba)3), три–трет–бутилфосфонийтетрафторборат (t–Bu3PH.BF4), 4,5–бис(дифенилфосфино)–9,9–диметилксантен (Xantphos), трифенилфосфин (PPh3), диизопропилазодикарбоксилат (DIAD), пиридинийхлорхромат (PCC), диметилсульфид борана (BMS), изопропоксид титана (TiOiPr4), триацетоксиборогидрид натрия (NaBH(OAc)3), цианоборогидрид натрия (NaBH3(CN)), борогидрид натрия (NaBH4), хлорид аммония (NH4Cl), хлороформ (CHCl3), диоксид марганца (MnO2), карбонат калия (K2CO3), 1,2–дихлорэтан (DCE), азид натрия (NaN3), нитрит натрия (NaNO2) и ди–трет–бутилдикарбонат (Boc2O).
Общая методика A: Синтез хиноновой кислоты; катализируемое серебром радикальное декарбоксилирование
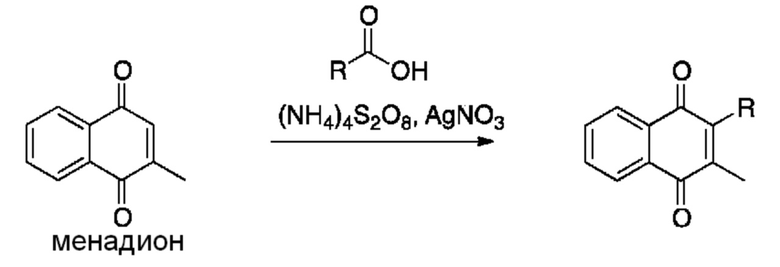
[0143] Карбоновую кислоту (2 экв.) добавляли к раствору менадиона (1 экв.) в CH3CN/H2O (3:1) и смесь нагревали при 75°C. К этому раствору в течение 10 мин медленно добавляли AgNO3 (0,1 экв.) (NH4)2S2O8 (2,5 экв.) в H2O (5 мл). Полученную смесь перемешивали в течение еще 2 ч. Смесь охлаждали до комнатной температуры, экстрагировали дихлорметаном и органический экстракт промывали с помощью H2O. Органический слой сушили над MgSO4, фильтровали и растворитель удаляли при пониженном давлении и получали неочищенный продукт, который очищали с помощью флэш–хроматографии (силикагель).
Общая методика B: Сочетание хинона с образованием амида

[0144] Хиноновую кислоту (1 экв.) добавляли к безводному дихлорметану (5–10 мл) в атмосфере N2 и охлаждали до 0°C. Последовательно амин добавляли (1 экв.), диметиламинопиридин (DMAP, 0,1 экв.), триэтиламин (Et3N, 2,5 экв.) и реагент сочетания (1,4 экв.) и реакционную смесь медленно нагревали до комнатной температуры и оставляли на ночь. Реакцию останавливали с помощью H2O (20 мл) и органический слой промывали насыщенным раствором KHSO4, насыщенным раствором NaHCO3 и H2O. Органический слой сушили над MgSO4, фильтровали и растворитель удаляли при пониженном давлении и получали неочищенный продукт, который очищали с помощью флэш–хроматографии (силикагель) и получали чистый аналог.
Общая методика C: Удаление защитной трет–бутильной группы
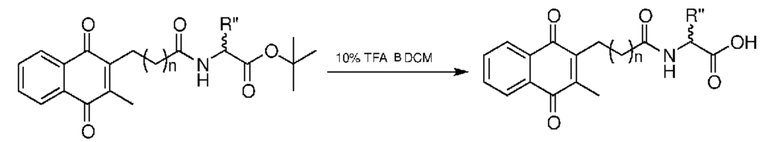
[0145] Трет–бутиловые эфиры добавляли к 10% TFA в дихлорметане (5,0 мл) и реакционную смесь перемешивали при комнатной температуре в течение ночи, затем растворитель удаляли при пониженном давлении. Неочищенный продукт получали и очищали с помощью флэш–хроматографии (силикагель) и получали чистый аналог.
Типичные примеры
[0146] Типичные примеры соединений формулы (I) получали, как описано в общих методиках A, B и/или C.
Пример 1: 2–(10–Гидроксидецил)–3 метил–1,4–нафтохинон (UTA#2)

[0147] UTA#2 получали по общей методике A из менадиона (201 мг, 1,17 ммоля) и 11–гидроксиундекановой кислоты (467 мг, 2,30 ммоля) и продукт очищали с помощью флэш–хроматографии (40% этилацетат/гексаны) и получали UTA#2 в виде бледно–желтого твердого вещества с выходом 19% (168 мг, 0,511 ммоля) с температурой плавления, равной 74–75°C.
[0148] 1H NMR δ (CDCl3, 300 MHz): 1,24–1,57 (m, 16H), 2,17 (s, 3H), 2,61 (t, J=7,0 Hz, 2H), 3,62 (t, J=6,6 Hz, 2H), 7,65–7,69 (m, 2H), 8,04–8,07 (m, 2H) ; 13C NMR δ (CDCl3, 75 MHz): 12,8, 25,8, 27,2, 28,9, 29,5, 29,6, 29,7, 30,1, 32,9, 63,2, 126,3, 126,4 132,3, 132,4, 133,4, 133,5, 143,3, 147,7, 184,9, 185,5 (перекрывание с одним атомом углерода) ; HRMS: Для C21H28O3, предсказано 328,20384, найдено 328,20383; MS m/z (EI+): 328 (M+, 62), 310 (5), 211 (10), 187 (100), 174 (12) 158 (18); IR Vmax: 3525, 2917, 2848, 1658, 1618, 1593, 1459, 1738, 1327, 1297, 717
Пример 2: 4–(3–Метил–1,4–нафталин–2–ил)–бутановая кислота (UTA#23)
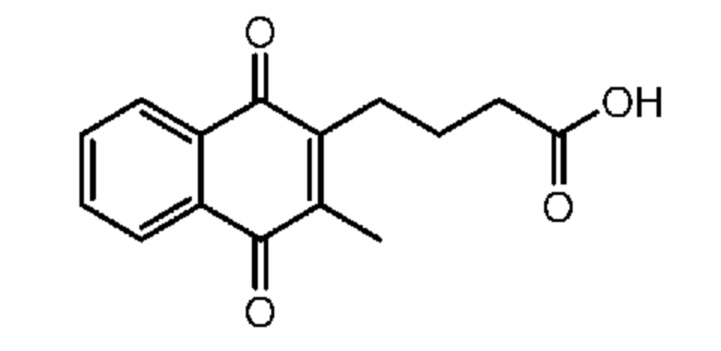
[0149] UTA#23 получали по общей методике A из менадиона (1,953 г, 11,34 ммоля) и глутаровой кислоты (3,041 г, 23,01 ммоля) и очищали с помощью флэш–хроматографии (силикагель, 100% CH2Cl2 затем 100% этилацетат) и получали UTA#23 в виде желтого твердого вещества с выходом 40% (1,169 г, 4,525 ммоля) с температурой плавления, равной 74–78°C.
[0150] 1H NMR δ (CDCl3, 400 MHz): 1,82 (квинтет, J =7,6 Hz, 2H), 2,20 (s, 3H), 2,46 (t, J =7,2 Hz, 2H), 2,69 (t, J=7,9 Hz, 2H), 7,66–7,69 (m, 2H), 8,04–8,06 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 12,84, 23,57, 26,41, 33,89, 126,43, 126,50, 132,24, 132,28, 133,61, 133,62, 144,15, 146,27, 179,39, 184,77, 185,36; IR Vmax: 3064, 2938, 2359, 2340, 1706, 1699, 1695, 1658, 1616, 1595, 1412, 1379, 1325, 1295, 1260, 717, 692, 66.
Пример 3: 25–(3–Метил–1,4–нафтохинон–2–ил)пентановая кислота (UTA#67)
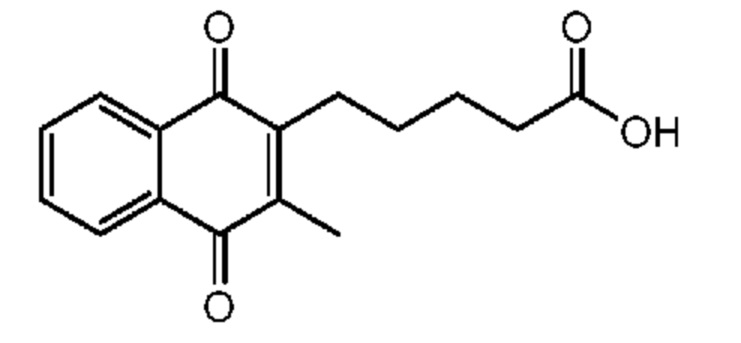
[0151] UTA#67 получали по общей методике A из менадиона (2,1636 г, 12,566 ммоля) и адипиновой кислоты (3,7242 г, 25,484 ммоля) и продукт очищали с помощью флэш–хроматографии (100% дихлорметан затем 100% этилацетат) и получали UTA#67 в виде кристаллического желтого твердого вещества с выходом 78% (2,6528 г, 9,7422 ммоля) с температурой плавления, равной 66–70°C.
[0152] 1H NMR δ (CDCl3, 400 MHz): 1,49–1,57 (m, 2H), 1,70–1,77 (m, 2H), 2,17 (s, 3H), 2,40 (t, J=7,4 Hz, 2H), 2,64 (t, J=7,9 Hz, 2H), 7,66–7,68 (m, 2H), 8,03–8,05 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 12,7, 24,9, 26,7, 28,1, 33,8, 126,3, 126,4, 132,20, 132,21, 133,4, 133,5, 143,5, 146,8, 179,6, 184,7, 185,3; IR Vmax: 2939, 1705, 1658, 1618, 1595, 1379, 1327, 1294, 1261, 715.
Пример 4: 4–(1,4–Нафтохинон–2–ил)бутановая кислота (UTA#59)
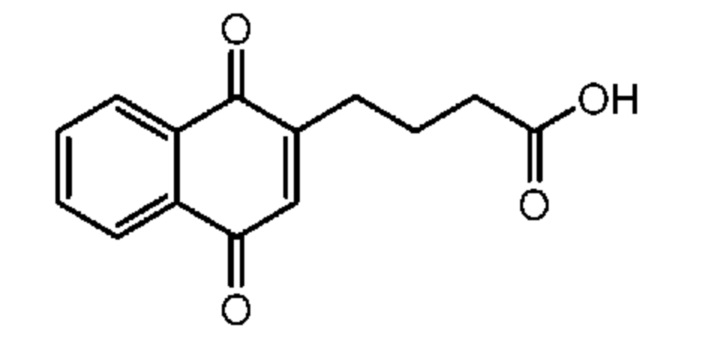
[0153] UTA#59 получали по общей методике A из нафтохинона (1,9989 г, 12,64 ммоля) и глутаровой кислоты (0,8354 мг, 6,323 ммоля) и продукт очищали с помощью автоматической системы флэш–хроматографии Reveleris (зарегистрированная торговая марка) X2 (Элюент: градиентный режим 0–80% этилацетат в гексане, Колонка: Reveleris (зарегистрированная торговая марка) диоксид кремния 24 г, Скорость потока: 18 мл/мин) и получали UTA#59 в виде коричневого твердого вещества с выходом 42% (0,6546 г, 2,680 ммоля) с температурой плавления, равной 120–122°C.
[0154] 1H NMR δ (CD3OD, 400 MHz): 1,90 (квинтет, J=7,6 Hz, 2H), 2,39 (t, J=7,2 Hz, 2H), 2,62 (td, J=7,6, 1,1 Hz, 2H), 6,85 (t, J=1,2 Hz, 1H), 7,78–7,80 (m, 2H), 8,02–8,04 (m, 1H), 8,07–8,10 (m, 1H); 13C NMR δ (CD3OD, 100 MHz): 24,4, 30,0, 34,3, 126,8, 127,4, 133,4, 133,7, 134,8, 134,9, 136,0, 152,4, 186,1, 186,3 (один атом углерода отсутствует или перекрывается) ; IR Vmax: 2956, 1699, 1660, 1620, 1953, 1417, 1327, 1303, 1265, 1143, 783, 661.
Пример 5: (R)–Метил–2(4–(3–метил–1,4–нафтохинон–2–ил)бутамидо)–3–фенилпропаноат (UTA#35)
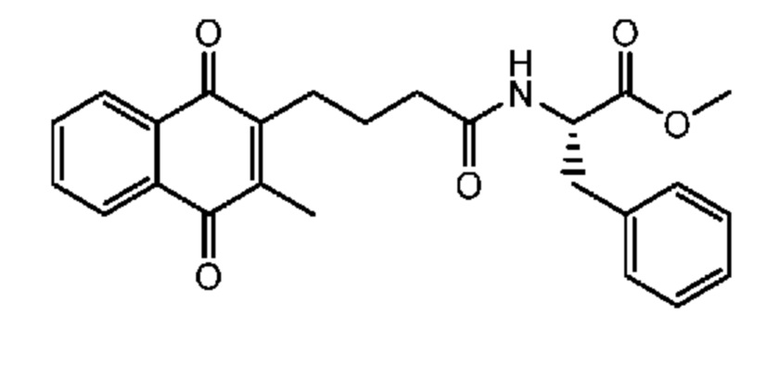
[0155] UTA#35 получали по общей методике B из UTA#23 (107,7 мг, 0,4170 ммоля) и метилового эфира (R)–фенилаланина (90,4 мг, 0,4193 ммоля). Продукт очищали с помощью автоматической системы флэш–хроматографии Reveleris (зарегистрированная торговая марка) X2 (Элюент: градиентный режим 100% гексаны – 100% этилацетат, Колонка: Reveleris (зарегистрированная торговая марка) диоксид кремния 4 г, Скорость потока: 18 мл/мин) и получали UTA#35 в виде желтого масла с выходом 29% (51,3 мг, 0,1223 ммоля).
[0156] 1H NMR δ (CDCl3, 400 MHz): 1,80 (квинтет, J=8,2 Hz, 2H), 2,20 (s, 3H), 2,29 (t, J=7,2 Hz, 2H), 2,65 (t, J=7,9, 2H), 3,15 (qd, J=14,0, 6,0 Hz, 2H), 3,74 (s, 3H), 6,11 (d, J=7,8, 1H), 4,92 (q, J=6,1 Hz, 1H), 7,12–7,14 (m, 2H), 7,24–7,31 (m, 3H), 7,70–7,72 (m, 2H), 8,07–8,10 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 12,9, 24,3, 26,4, 23,9, 38,1, 52,5, 53,2, 126,4, 126,5, 127,3 128,7 (два атома углерода), 129,4 (два атома углерода), 132,2, 132,3, 133,5, 133,6, 136,1, 144,2, 146,4, 172,0, 172,3, 184,9, 185,3; HRMS: Для C25H25N1O5, предсказано 419,17327, найдено 419,17403; MS m/z (EI+): 419 (M+, 45), 241 (100), 197 (50), 162 (100), 120 (45); IR Vmax : 3371, 3293, 2951, 1745, 1652, 1596, 1538, 1436, 1378, 1329, 1295, 1215, 717.
Пример 6: (S)–трет–Бутил–2–(4–(3–метил–1,4–нафтохинон–2–ил)бутанамидо)–3–фенилпропаноат (UTA#36)
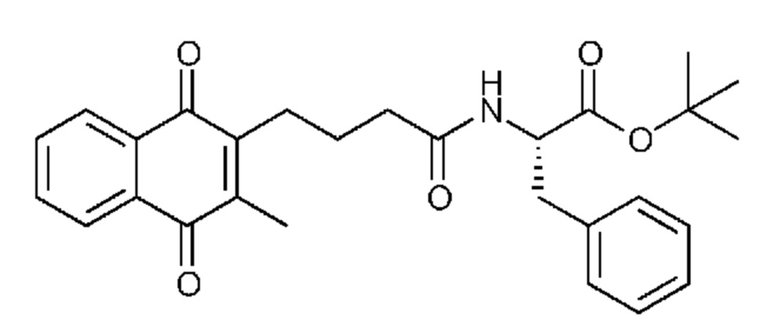
[0157] UTA#36 получали по общей методике B из UTA#23 (504,2 мг, 1,9522 ммоля) и трет–бутилового эфира L–фенилаланина.HCl (489,4 мг, 1,9023 ммоля) и продукт очищали с помощью флэш–хроматографии (40% этилацетат/гексаны) и получали UTA#36 в виде желтого масла с выходом 36% (317,3 мг, 0,6875 ммоля).
[0158] 1H NMR δ (CDCl3, 400 MHz): 1,40 (s, 9H), 1,78 (квинтет, J=7,8 Hz, 2H), 2,17 (s, 3H), 2,27 (t, J=7,4 Hz, 2H), 2,62 (t, J=8,0 Hz, 2H), 3,04–3,13 (m, 2H), 4,77 (q, J=6,2 Hz, 1H), 6,09 (d, J=7,8 Hz, 1H), 7,14–7,27 (m, 5H), 7,66–7,69 (m, 2H), 8,04–8,07 (m, 2H)
13C NMR δ (CDCl3, 100 MHz): 12,8, 24,3, 26,3, 28,0 (три атома углерода), 36,1, 38,2, 53,5, 82,4, 126,3, 126,4, 127,0, 128,4 (два атома углерода), 129,5 (два атома углерода), 132,21, 132,26, 133,4, 133,5, 136,3, 144,0, 146,4, 170,9, 171,8, 184,8, 185,3; [α]D20: +36,24° (c 0,91, CHCl3); IR Vmax: 3420, 2978, 1732, 1658, 1595, 1525, 1367, 1329, 1294, 1257, 1226, 1155, 700.
Пример 7: (S)–трет–Бутил–1–(4–(3–метил–1,4–нафтохинон–2–ил)бутаноил)пирролидин–2–карбоксилат (UTA#42)

[0159] UTA#42 получали по общей методике B из UTA#23 (196,9 мг, 0,7623 ммоля) и трет–бутилового эфира L–пролина.HCl (139,5 мг, 0,6716 ммоля) и продукт очищали с помощью флэш–хроматографии (60% этилацетат/гексаны) и получали UTA#42 в виде желтого масла с выходом 53% (145,8 мг, 0,3543 ммоля).
[0160] 1H NMR δ (CDCl3, 400 MHz): 1,44 (s, 9H), 1,82–1,88 (m, 2H), 1,90–1,96 (m, 2H), 2,04–2,13 (m, 2H), 2,21 (s, 3H), 2,36–2,48 (m, 2H), 2,67–2,71 (m, 2H), 3,47–3,52 (m, 1H), 3,59–3,64 (m, 1H), 4,37 (dd, J=8,5, 3,9 Hz, 1H), 7,66–7,68 (m, 2H), 8,03–8,07 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 12,8, 23,7, 24,7, 26,5, 28,0 (три атома углерода), 29,3, 34,1, 47,1, 59,5, 81,2, 126,2 (два атома углерода), 132,23, 132,26, 133,3 (два атома углерода),144,0, 146,7, 171,0, 171,6, 184,7, 185,3 ; [α]D20: +48,70° (c 0,97, CHCl3); IR Vmax: 2976, 2935, 1735, 1654, 1618, 1595, 1456, 1425, 1367, 1294, 1153, 719.
Пример 8: N–(2–(1H–Индол–3–ил)этил)–4–(3–метил–1,4–нафтохинон–2–ил)бутанамид (UTA#73)
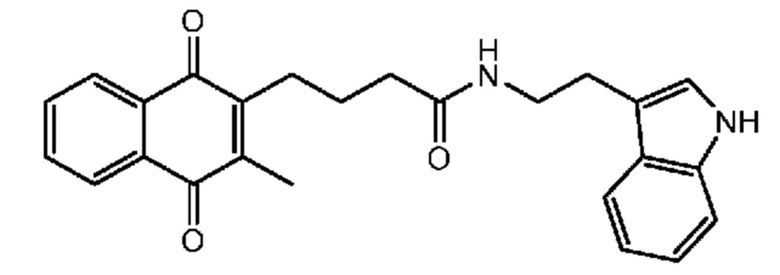
[0161] UTA#73 получали по общей методике B из UTA#23 (193,9 мг, 0,7507 ммоля) и триптамина (123,5 мг, 0,7708 ммоля) и продукт очищали с помощью флэш–хроматографии (80% этилацетат/гексаны) и получали UTA#73 в виде коричневого вязкого масла с выходом 42% (127,3 мг, 0,3178 ммоля).
[0162] 1H NMR δ (CDCl3, 400 MHz): 1,77 (квинтет, J=7,6 Hz, 2H), 2,14 (s, 3H), 2,22 (t, J=7,3 Hz, 2H), 2,59 (t, J=7,9 Hz, 2H), 2,97 (t, J=6,8 Hz, 2H), 3,61 (q, J=6,2 Hz, 2H), 6,13 (t, J=5,2 Hz, 1H), 7,01 (bs, 1H), 7,04–7,08 (m, 1H), 7,11–7,15 (m, 1H), 7,32 (d, J=8,1 Hz, 1H), 7,56 (d, J=7,9 Hz, 1H), 7,64–7,67 (m, 2H), 7,99–8,04 (m, 2H), 8,69 (bs, 1H); 13C NMR δ (CDCl3, 100 MHz): 12,7, 24,3, 25,2, 26,3, 36,1, 39,9, 111,4, 112,7, 118,6, 119,3, 122,0, 122,2, 126,2 (два атома углерода), 127,3, 132,02, 132,09, 133,42, 133,47, 136,4, 143,9, 146,2, 172,6, 184,8, 185,1; IR Vmax: 3392, 3294, 2935, 1705, 1653, 1595, 1527, 1458, 1332, 1296, 740, 715.
Пример 9: N–(4–Гидроксифенетил)–4–(3–метил–1,4–нафтохинон–2–ил)бутанамид (UTA#74)
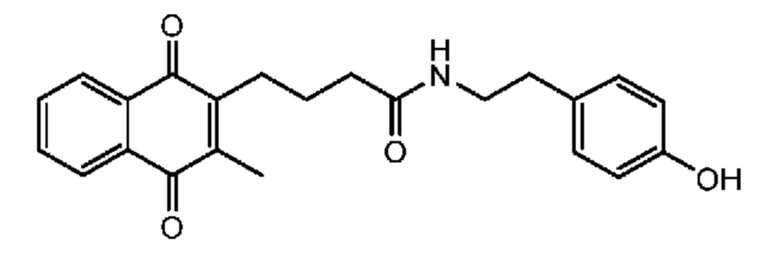
[0163] UTA#74 получали по общей методике B из UTA#23 (235,6 мг, 0,9122 ммоля) и тирамина (119,0 мг, 0,8675 ммоля) и продукт очищали с помощью флэш–хроматографии (80% этилацетат/гексаны) и получали UTA#74 в виде желтого твердого вещества с выходом 33% (108,9 мг, 0,2885 ммоля) с температурой плавления, равной 116–118°C.
[0164] 1H NMR δ (CDCl3, 400 MHz): 1,76 (квинтет, J=7,5 Hz, 2H), 2,12 (s, 3H), 2,24 (t, J=7,2 Hz, 2H), 2,56–2,60 (m, 2H), 2,71 (t, J=7,0 Hz, 2H), 3,47 (q, J=6,4 Hz, 2H), 6,22 (t, J=5,5 Hz, 1H), 6,75 (d, J=8,4 Hz, 2H), 6,96 (d, J=8,4 Hz, 2H), 7,62–7,65 (m, 2H), 7,97–8,00 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 12,7, 24,4, 16,3, 34,7, 36,1, 41,1, 115,7 (два атома углерода), 126,3 (два атома углерода), 129,8 (два атома углерода), 129,9, 132,0, 132,1, 133,53, 133,59, 144,2, 146,2, 155,3, 173,1, 185,0, 185,2; IR Vmax: 3365, 3306, 2935, 1654, 1616, 1595, 1541, 1516, 1375, 1330, 1296, 715.
Пример 10: N–(3,4–Диметоксифенетил)–4–(3–метил–1,4–нафтохинон–2–ил)бутанамид (UTA#77)
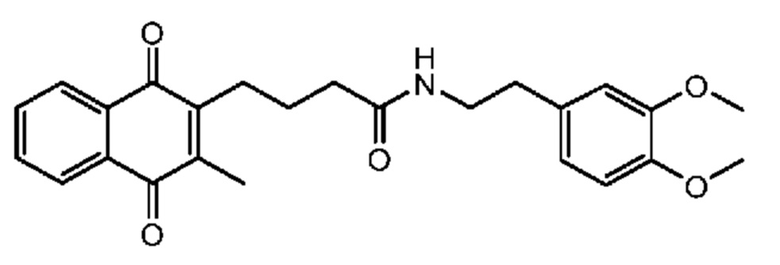
[0165] UTA#77 получали по общей методике B из UTA#23 (187,5 мг, 0,7260 ммоля) и 3,4–диметоксифенилэтиламина (146,6 мг, 0,8088 ммоля) и продукт очищали с помощью флэш–хроматографии (90% этилацетат/гексаны) и получали UTA#77 в виде бледно–оранжевого кристаллического твердого вещества с выходом 38% (117,0 мг, 0,2776 ммоля) с температурой плавления, равной 105–108°C.
[0166] 1H NMR δ (CDCl3, 400 MHz): 1,77 (квинтет, J=7,7 Hz, 2H), 2,16 (S, 3H), 2,22 (t, J=7,2 Hz, 2H), 2,60 (t, J=8,0 Hz, 2H), 2,74 (t, J=7,2 Hz, 2H), 3,48 (q, J=6,5 Hz, 2H), 3,79 (s, 3H), 3,81 (s, 3H), 5,94 (t, J=5,6 Hz, 1H), 6,68–6,76 (m, 3H), 7,63–7,66 (m, 2H), 7,98–8,02 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 12,7, 24,3, 26,3, 35,2, 36,1, 40,7, 55,8, 55,9, 111,4, 111,9, 120,7, 126,25, 126,29, 131,4, 132,0, 132,1, 133,4, 133,5, 144,0, 146,2, 147,7, 149,0, 172,3, 184,8, 185,1.; IR Vmax: 3377, 3296, 2935, 2656, 1595, 1516, 1462, 1329, 1294, 1261,1236, 1157, 1141, 1028, 717.
Пример 12: (S)–N–(1–Гидрокси–3–фенилпропан–2–ил)–4–(3–метил–1,4–нафтохинон–2–ил)бутанамид (UTA#62)
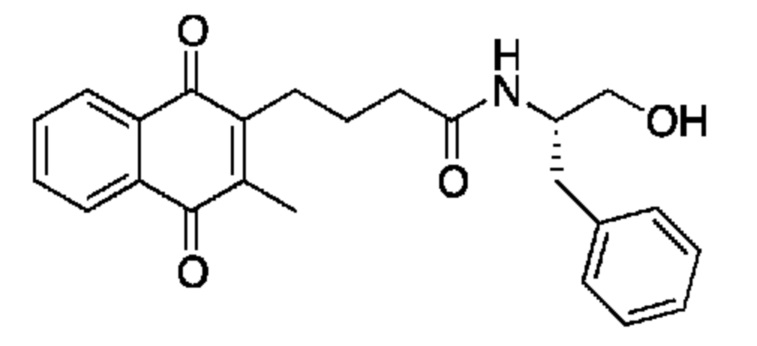
[0167] UTA#62 получали по общей методике B из UTA#23 (133,5 мг, 5169 ммоля) и L–фенилаланинола (76,4 мг, 0,5053 ммоля) и продукт очищали с помощью флэш–хроматографии (100% этилацетат) и получали UTA#62 в виде желто–апельсинового масла с выходом 49% (97,7 мг, 0,2496 ммоля).
[0168] 1H NMR δ (CDCl3, 400 MHz): 1,70–1,78 (m, 2H), 2,15 (s, 3H), 2,25 (t, J=7,2 Hz, 2H), 2,55 (t, J=8,0 Hz, 2H), 2,83–2,94 (m, 2H), 3,03 (bs, 1H), 3,59 (dd, J=11,2, 5,4 Hz, 1H), 3,71 (dd, J=11,2, 3,8 Hz, 1H), 4,21–4,29 (m, 1H), 6,31 (d, J=8,0 Hz, 1H), 7,15–7,27 (m, 5H), 7,64–7,69 (m, 2H), 8,00–8,05 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 12,7, 24,3, 26,2, 36,2, 37,0, 52,9, 64,1, 126,35, 126,36, 126,6, 128,6 (два атома углерода), 129,2 (два атома углерода), 132,0, 132,1, 133,5, 133,6, 137,9, 144,2, 146,2, 173,1, 185,12, 185,13; [α]D20: –21,33° (c 1,57, CHCl3); IR Vmax: 3369, 3296, 2933, 1658, 1595, 1539, 1456, 1377, 1330, 1296, 1043, 717, 702.
Пример 13: (S)–2–(4–(2–(Гидроксиметил)пирролидин–1–ил)–4–оксобутил)–3–метил–1,4–нафтохинон (UTA#61)
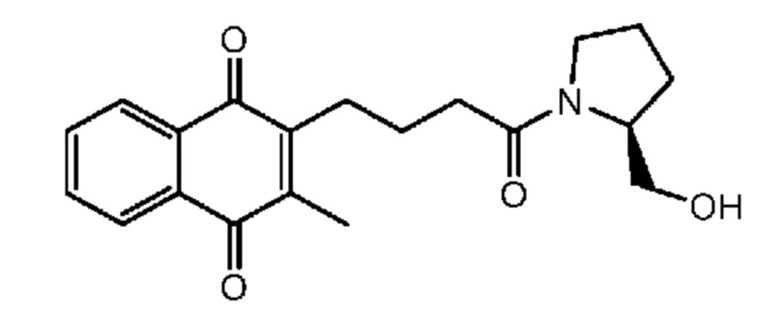
[0169] UTA#61 получали по общей методике B из UTA#23 (116,8 мг, 0,4522 ммоля) и L–пролинола (159,1 мг, 0,7587 ммоля) и продукт очищали с помощью флэш–хроматографии (100% этилацетат) и получали UTA#61 в виде желтого масла с выходом 36% (49,8 мг, 1459 ммоля).
[0170] 1H NMR δ (CDCl3, 400 MHz): 1,60 (квинтет, J=6,2 Hz, 2H), 1,82–2,02 (m, 6H), 2,21 (s, 3H), 2,39 (t, J=7,2 Hz, 2H), 2,67–2,72 (m, 2H), 3,50–3,55 (m, 1H), 3,66 (dd, J=11,3, 2,8 Hz, 1H), 4,15–4,22 (m, 1H), 7,66–7,68 (m, 2H), 8,03–8,07 (m, 2H). ; 13C NMR δ (CDCl3, 100 MHz): 12,8, 23,6, 24,5, 26,4, 28,3, 34,6, 48,1, 61,2, 67,3, 126,33, 126,37, 132,1, 132,2, 133,4, 133,5, 144,1, 146,6, 173,6, 184,9, 185,3; [α]D20: –35,12° (c 0,41, CHCl3); IR Vmax: 3367, 2953, 2877, 1695, 1654, 1616, 1595, 1454, 1329, 1296, 1047, 732, 719.
Пример 14: (S)–трет–Бутил 2–(4–(1,4–нафтохинон–2–ил)бутанамидо)–3–фенилпропаноат (UTA#116)

[0171] UTA# 116 получали по общей методике B из UTA#59 (29,5 мг, 0,1208 ммоля) и трет–бутилового эфира L–фенилаланина.HCl (34,8 мг, 0,1353 ммоля) и продукт очищали с помощью автоматической системы флэш–хроматографии Reveleris (зарегистрированная торговая марка) X2 (Элюент: градиентный режим 100% гексаны – 80% этилацетат, Колонка: Reveleris ® диоксид кремния 4 г, Скорость потока: 18 мл/мин) и получали UTA#116 в виде коричневого масла с выходом 20% (10,9 мг, 0,0243 ммоля).
[0172] 1H NMR δ (CDCl3, 400 MHz): 1,43 (s, 9H), 1,91 (квинтет, J=7,6 Hz, 2H), 2,29 (td, J=7,5, 2,9 Hz, 2H), 2,56–2,60 (m, 2H), 3,10–3,14 (M, 2H), 4,76–4,81 (M, 1H), 6,03 (d, J=7,3 Hz, 1H), 7,16 –6 7,31 (m, 5H), 7,74–7,76 (m, 2H), 8,07–8,12 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 23,9, 28,1 (три атома углерода), 29,1, 35,8, 38,2, 53,5, 82,5, 126,2, 126,7, 127,1, 128,5 (два атома углерода), 129,6 (два атома углерода), 132,2, 132,3, 133,7, 133,8, 135,3, 136,3, 150,9, 170,9, 172,5, 185,1, 185,2; [α]D20: +38,46° (c 0,39, CHCl3); IR Vmax: 3309,2978, 2931, 1732, 1662, 1595, 1525, 1367, 1301, 1259, 1153, 700. UTA#116 необязательно может быть метилирован в положении 3 (R5).
Пример 15: (S)–2–(4–(3–Метил–1,4–нафтохинон–2–ил)бутанамидо)–3–фенилпропановая кислота (UTA#37)
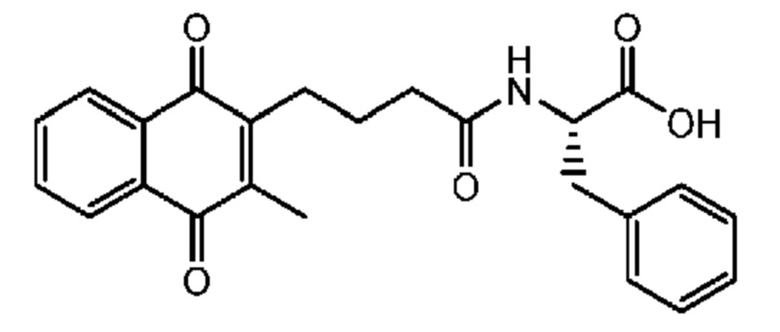
[0173] UTA#37 получали из продукта удаления защитной группы из UTA#36 (317,3 мг, 0,6875 ммоля) по общей методике C. Продукт очищали с помощью флэш–хроматографии (5% метанол/этилацетат) и получали UTA#37 в виде коричневого вязкого масла с выходом 79% (219,6 мг, 0,5416 ммоля).
[0174] 1H NMR δ (CDCl3, 400 MHz): 1,72–1,79 (m, 2H), 2,14 (s, 3H), 2,29 (t, J=7,2 Hz, 2H), 2,58 (t, J=7,8 Hz, 2H), 3,12 (dd, J=14,0, 7,0 Hz, 1H), 3,26 (dd, J=14,1, 5,4 Hz, 1H), 4,90 (m, 1H), 6,54 (d, J=7,7 Hz, 1H), 7,17–7,28 (m, 5H), 7,66–7,69 (m, 2H), 8,02–8,05 (m, 2H), 8,92 (bs, 1H); 13C NMR δ (CDCl3, 100 MHz): 12,8, 24,2, 26,2, 35,8, 37,3, 53,4, 126,4 (два атома углерода), 127,2, 128,7 (два атома углерода), 129,4 (два атома углерода), 132,0, 132,2, 133,5, 133,6, 135,9, 144,3, 146,2, 173,5, 174,7, 185,1, 185,2; [α]D20: +35,83° (c 0,24, CHCl3); IR Vmax: 3491, 2931, 1716, 1660, 1616, 1595, 1521, 1456, 1332, 1296, 1267, 1217, 702.
Пример 16: (S)–1–(4–(3–Метил–1,4–нафтохинон–2–ил)бутаноил)пирролидин–2–карбоновая кислота (UTA#43)
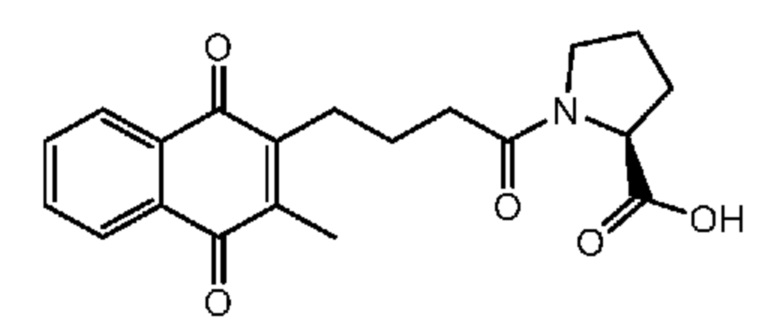
[0175] UTA#43 получали из продукта удаления защитной группы из UTA#42 (113,8 мг, 0,2766 ммоля) по общей методике C. Продукт очищали с помощью флэш–хроматографии (3% метанол/этилацетат) и получали UTA#43 в виде коричневого вязкого масла с выходом 65% (63,9 мг, 0,1798 ммоля).
[0176] 1H NMR δ (CDCl3, 400 MHz): 1,82–1,90 (m, 2H), 2,02–2,08 (m, 2H), 2,21 (s, 3H), 2,13–2,33 (m, 2H), 2,45–2,50 (m, 2H), ,68–2,72 (m, 2H), 3,49–3,53 (m, 1H), 3,60–3,63 (m, 1H), 4,55–4,58 (m, 1H), 7,53 bs, 1H), 7,68–7,07 (m, 2H), 8,04–8,08 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 12,8, 23,3, 24,8, 26,4, 28,0, 34,1, 47,8, 59,7, 126,34, 126,38, 132,1, 132,2, 133,51, 133,56, 144,2, 146,3, 173,4, 173,9, 184,8, 185,3; [α]D20: –65,80° (c 1,69, CHCl3); IR Vmax: 2976, 2956, 1732, 1658, 1616, 1595, 1456, 1329, 1294, 1188, 717.
Пример 17: 3–((3–Метил–1,4–нафтохинон–2–ил)тио)пропановая кислота (UTA#46)
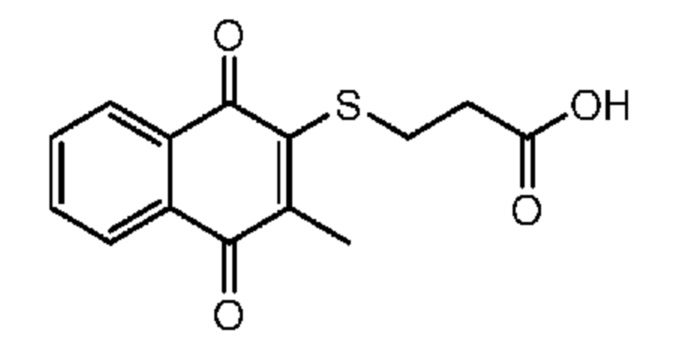
[0177] 3–Меркаптопропановую кислоту (1,4 мл, 10,829 ммоля) добавляли к раствору менадиона (535,8 мг, 3,1119 ммоля) в метаноле (50 мл) и 2–пропаноле (40 мл) и реакционную смесь перемешивали при комнатной температуре в течение 24 ч. Растворитель удаляли при пониженном давлении и продукт повторно растворяли в дихлорметане и промывали 10% раствором сульфата меди (2×25 мл) и H2O (3×25 мл) Органический слой сушили над MgSO4, фильтровали и растворитель удаляли при пониженном давлении и получали неочищенный продукт, который очищали с помощью флэш–хроматографии (30% этилацетат/гексаны) и получали UTA#46 в виде красного маслообразного твердого вещества с выходом 48% (387,4 мг, 1,4021 ммоля). Спектральные данные согласовались с приведенными в литературе [9]. 1H NMR δ (CDCl3, 400 MHz): 2,34 (s, 3H), 2,75 (t, J=7,0 Hz, 2H), 3,42 (t, J=7,0 Hz, 2H), 7,69–7,71 (m, 2H), 8,06–8,09 (m, 2H); 13C NMR δ (CDCl3, 100 MHz): 15,4, 28,9, 35,4, 126,7, 126,9, 132,1, 132,9, 133,5, 133,8, 145,8, 147,6, 176,2, 181,3, 182,2.
Фармакокинетика/биологические примеры
Пример 18: Исследование резкого восстановления содержания ATP (при условиях нарушенной митохондриальной функции)
[0178] Митохондриальные нарушения характеризуются нарушенной митохондриальной функцией, что обычно проявляется, как уменьшение митохондриального синтеза ATP. Это резкое уменьшение количества энергии является основным вкладом в поражение клеток и в конечном счете в их гибель. Таким образом, для нормализации функций клеток и тканей необходимо улучшение нарушенного энергетического статуса, который связан с нарушенной митохондриальной функцией.
[0179] Клетки HepG2 высевали при плотности 5000 клеток/лунка в 96–луночный планшет и инкубировали в течение 24 ч в DMEM с добавлением 0,3 г/л глюкозы, 10% FBS и смеси пенициллин–стрептомицин–глутамин. Клетки обрабатывали с помощью 1 мкМ хинонов в присутствии или при отсутствии ротенона (10 мкМ) в течение 60 мин в не содержащей глюкозы DMEM. Содержания ATP количественно определяли по люминесценции с использованием зависимого от ATP ферментативного окисления люциферина люциферазой. Клетки лизировали в объеме 40 мкл (4 мМ EDTA, 0,2% Triton X–100) в течение 5 мин при комнатной температуре (RT) на орбитальном встряхивающем устройстве при 200 об/мин. Для инициирования реакции в 96–луночных планшетах 100 мкл буфера для определения содержания ATP (25 мМ HEPES pH 7,25, 300 мкМ D–люциферин, 5 мкг/мл люциферазы светляка, 75 мкМ DTT, 6,25 мМ MgCL2, 625 мкМ EDTA и 1 мг/мл BSA) объединяли с 10 мкл лизата. Сразу количественно определяли интенсивность люминесценции с использованием многорежимного устройства для считывания планшетов (Fluoroscan Ascent, Thermo Scientific). Содержания ATP стандартизировали на содержания белка с использованием имеющегося в продаже набора для анализа BCA (Protein DC; BioRad) и изменения рассчитывали в процентах по сравнению со значениями для контрольных клеток, обработанных с помощью DMSO. Данные представляли, как содержание ATP в % по сравнению с необработанным контролем (без ротенона). Данные характеризуют среднее значение ± S.D. для 3 независимых экспериментов с использованием по 6 лунок (n=6) в каждом.
[0180] Степени восстановления содержания ATP для типичных соединений формулы (I) приведены ниже в таблице 4. Витамин K, менадион и идебенон использовали в качестве сравнительных контролей. DMSO использовали в качестве контроля.
Таблица 4: Исследование восстановления содержания ATP
[0181] Измененная митохондриальная функция, например, при митохондриальных нарушениях, может привести к уменьшению содержания ATP в клетках. Как показано в таблице 4, типичные соединения формулы (I) в значительной степени восстанавливают содержания ATP при условиях нарушенной митохондриальной функции, тогда как сравнительные соединения витамин K и менадион не оказывают влияние или оказывают небольшое влияние.
Пример 19: Восстановление жизнеспособности клеток в присутствии митохондриального ингибитора
[0182] Митохондриальная дисфункция вследствие уменьшения выработки ATP и увеличения выработки реакционноспособных кислородсодержащих частиц приводит к значительному уменьшению выживаемости клеток. Таким образом, улучшенное поступление энергии, которое наблюдается при использовании соединений формулы (I) или формулы (Ia) или вариантов осуществления, указанных выше в настоящем изобретении, должно защитить жизнеспособность клеток от митохондриальной дисфункции.
[0183] Цитопротекцию клеток HepG2 нафтохинонами количественно определяли в присутствии митохондриального токсина, ротенона. Вкратце, методика заключалась в следующем: клетки HepG2 высевали в 96–луночные планшеты по 5000 клеток/лунка в DMEM с добавлением 0,3 г/л глюкозы, 10% FBS и смеси пенициллин–стрептомицин–глутамин. После инкубации в течение ночи при стандартных условиях клетки обрабатывали исследуемыми соединениями (10 мкМ) в течение 2 дней, затем клетки обрабатывали 1 мкМ ротеноном в присутствии 10 мкМ исследуемых соединений в сбалансированном солевом растворе Хэнка (HBSS) в течение 6 ч. Затем дополнительно инкубировали в течение еще 18 ч с использованием только 10 мкМ исследуемых соединений в HBSS. Для исследования жизнеспособности клеток их дважды промывали с помощью 100 мкл PBS и затем лизировали с помощью 40 мкл литического раствора (4 мМ EDTA, 0,2% Triton X–100) в течение 5 мин при комнатной температуре (RT) на орбитальном встряхивающем устройстве при 200 об/мин. Затем 10 мкл лизата смешивали с 90 мкл смеси фермент–субстрат (описанной выше) в белом 96–луночном планшете и сразу определяли интенсивность люминесценции с использованием устройства для считывания планшетов (Fluoroscan Ascent, Thermo Scientific). Данные представляли в виде жизнеспособности в % по сравнению с необработанным (без ротенона) контролем. Данные характеризуют среднее значение ± S.D. для 3 независимых экспериментов с использованием по 6 лунок (n=6) в каждом.
[0184] Степени защиты жизнеспособности клеток от воздействия ротенона типичными соединениями формулы (I) приведены ниже в таблице 5. Витамин K, менадион и идебенон использовали в качестве сравнительных контролей. DMSO использовали в качестве контроля.
Таблица 5: Исследование жизнеспособности клеток
[0185] Как показано в таблице 5, при условиях нарушенной митохондриальной функции типичные соединения формулы (I) значительно улучшают защиту жизнеспособности клеток, в особенности по сравнению со сравнительными соединениями менадионом и идебеноном. Сравнительное соединение витамин K не оказывало защитного действия.
Пример 20: Жизнеспособность клеток в присутствии митохондриального ингибитора
[0186] Цитопротекторные эффекты типичных соединений формулы (I) дополнительно исследовали in vitro в ответ на токсическое воздействие ротенона (10 мкМ). Типичные соединения исследовали на клетках HepG2 в присутствии митохондриального токсина, ротенона, при условиях, аналогичных использованным в примере 19. Клетки обрабатывали типичными соединениями формулы (I) (10 мкМ) в течение 2 дней и затем клетки обрабатывали с помощью 10 мкМ ротенона.
[0187] Как показано на фиг. 1, при условиях нарушенной митохондриальной функции типичные соединения формулы (I) значительно улучшали жизнеспособность клеток. Типичные нафтохиноны формулы (I) (отмечены символом N) сопоставляли с соответствующими производными бензохинона (B) или пластохинона (C). Несмотря на наличие таких же заместителей у L, Y, R5, R6, эквивалентные производные бензохинона (B) или пластохинона (P) обладали в целом меньшей цитопротекторной активностью, чем соответствующий нафтохинон формулы (I).
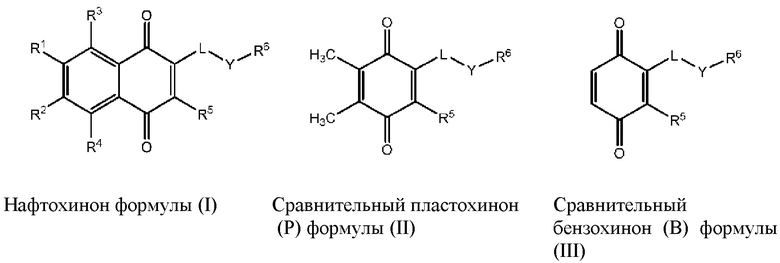
[0188] Как показано на фиг. 2, 23 соединения (белые кружки) обладали значительно улучшенной цитопротекторной активностью по сравнению с идебеноном (пунктирная линия, ~65% жизнеспособность). У клеток, обработанных только ротеноном, жизнеспособность снижалась от составляющей 100% (черная пунктирная линия, 100% жизнеспособность) до составляющей менее 30% (пунктирная линия, ˂30% жизнеспособность).
[0189] Жизнеспособности клеток в ответ на воздействие ротенона для типичных соединений формулы (I) приведены ниже в таблице 6, они соответствуют данным на фиг. 2. Витамин K, менадион и идебенон использовали в качестве сравнительных контролей.
Таблица 6: Жизнеспособность клеток [%] [10 мкМ] HepG2
Пример 21: Восстановление содержания ATP в присутствии митохондриального ингибитора
[0190] Степень восстановления содержания ATP при использовании типичных соединений формулы (I) дополнительно исследовали in vitro в ответ на токсическое воздействие ротенона (10 мкМ). Типичные соединения исследовали на клетках HepG2 в присутствии митохондриального токсина, ротенона, при условиях, аналогичных использованным в примере 18. Клетки обрабатывали типичными соединениями формулы (I) (10 мкМ) в течение 2 дней и затем клетки обрабатывали с помощью 10 мкМ ротенона.
[0191] Как показано на фиг. 3, 7 соединений (белые кружки) значительно увеличивали содержание ATP в клетках по сравнению с идебеноном (фиолетовая пунктирная линия) в присутствии ротенона. У клеток, обработанных только ротеноном, жизнеспособность снижалась от составляющей 100% (черная пунктирная линия, 100% жизнеспособность) до составляющей менее 30% (пунктирная линия, ˂30% жизнеспособность). Все соединения исследовали при 10 мкМ.
[0192] Характеристики восстановления содержания ATP в ответ на воздействие ротенона типичных соединений формулы (I) приведены ниже в таблице 7, они соответствуют данным на фиг. 2. Витамин K, менадион и идебенон использовали в качестве сравнительных контролей.
Таблица 7:% Восстановление содержания ATP [10 мкМ] HepG2
Пример 22: Влияние на внеклеточное содержание лактата
[0193] Митохондриальная дисфункция и последующее уменьшение выработки ATP обычно компенсируется клеткой путем увеличенного гликолиза для поддержания содержания ATP. Однако это обычно также связано с увеличением содержания побочного продукта гликолиза, лактата. Лактат при более высоких концентрациях подкисляет среды и становится токсичным in vitro и in vivo (это называется лактоцидозом). Поэтому уменьшение содержания лактата исследуемыми соединениями указывает на улучшение митохондриальной функции.
[0194] Концентрации лактата в культуральной среде определяли с помощью ферментативного колориметрического анализа. Вкратце, методика заключалась в следующем: 150000 клеток HepG2 высевали в обычные среды для выращивания (DMEM, 10% FCS, Pen/Strep) в каждую 6–луночного планшета (Life Science, USA) и инкубировали в течение 24 ч. Среды заменяли средами для выращивания, содержащими (25 мМ глюкозы) с использованием и без использования исследуемых соединений. Необработанные лунки, содержащие только клетки, считали экспериментальными исходными контролями и все соединения исследовали в трех разных лунках одновременно. Надосадочные жидкости собирали через 48 ч и переносили в 96–луночный планшет. После добавления 90 мкл реакционного буфера (10 мМ KH2PO4 pH 7,8, 1 мг/мл BSA, 0,5 мМ PMS, 2 мМ EDTA, 0,6 мМ DCPIP, 0,8 мМ NAD+, 5 Ед/мл глутаматпируваттрансаминазы, 1,5 мМ глутамата, 12,5 Ед/мл лактатдегидрогеназы) планшет инкубировали при 30°C внутри устройства для считывания планшетов (Multiscan Go, Thermo Scientific) и поглощение измеряли при 600 нм в течение 100 мин. Калибровочную кривую получали с использованием сред с добавкой лактата в известных концентрациях. В заключение количественно определяли содержания белка и концентрации лактата в каждой лунке стандартизировали на содержания в ней белка и затем выражали в % от контроля.
[0195] Степени уменьшения концентраций лактата в клеточной культуральной среде под действием исследуемых соединений, предлагаемых в настоящем изобретении, и сравнительных соединений витамина K, менадиона и идебенона приведены ниже в таблице 6.
Таблица 8: Влияние на содержания лактата
[0196] Как показано в таблице 6, типичные соединения формулы (I) значительно уменьшали выработку лактата, что указывает на улучшение митохондриальной функции. В то же время установлено, что сравнительные соединения менадион и идебенон увеличивают концентрацию лактата. Сравнительные соединение, витамин K, проявляло лишь небольшой, но незначительный эффект.
Пример 23: Токсичность in vivo
[0197] Токсичность типичных соединений формулы (I) in vivo проявлялась в клетках печени. В частности, длительную токсичность, оцениваемую с помощью анализа колониеобразующих единиц в клетках HepG2, определяли в течение 14 дней для типичных соединений формулы (I) при 10 мкМ. Идебенон использовали в качестве сравнительного контроля (10 мкМ). Как показано на фиг. 5; типичные соединения, предлагаемые в настоящем изобретении, обладали токсичностью in vitro, сходной с данными для идебенона.
Пример 24: Активность в модели наследственной оптической нейропатии Лебера (LHON)
[0198] Эффективность типичных соединений формулы (I) оценивали с помощью модели наследственной оптической нейропатии Лебера (LHON) на мышах. LHON представляет собой редкое наследственное митохондриальное нарушение, отличающееся быстрой потерей остроты зрения и чувствительности к цветовому контрасту, приводящее к слепоте. LHON вызвано мутациями митохондриальной DNA (mtDNA), три из которых являются так называемыми первичными мутациями mtDNA, приводящими к более 95% всех случаев LHON.
[0199] Модель LHON включает введение ротенона в стекловидное тело левого глаза мышей C57BL/6 и она описана в публикации Heitz et al. 2012. Типичные соединения (UTA 37 и UTA 77) и идебенон вводили по 200 мг/кг в течение периода наблюдения. Потерю зрения оценивали путем определения количества поворотов головы.
[0200] Мышей C57BL/6 (самцы в возрасте 8–11 недель, средняя масса тела ≈ 25 г) использовали в соответствии с законом Австралии по использованию животных для научных целей и в соответствии с этикой обращения с животными, утвержденной Комитетом по этике обращения с животными университета Тасмании (UTAS) Animal Ethics Committee (Approval number A0016080). Животным в течение по меньшей мере 7 дней до исследования поведения давали акклиматизироваться в помещении для животных с целью уменьшения стресса, вызванного транспортировкой. Всем мышам перорально вводили исследуемые соединения путем смешивания исследуемых соединений с индивидуальными суточными порциями корма, как это описано ранее (Heitz, F. D. et al. (2012). PLoS One., 7(9), e45182). Для контроля поступления лекарственного средства мышей помещали в отдельные клетки и им обеспечивали улучшенные условия, включая помещение и подстилку, небольшие игрушки, туалет с откачкой, небольшие кусочки дерева для обгладывания и стеклянные шарики, что обеспечивало возможность естественного поведения. Всем мышам (n=10–11 на группу) предварительно давали исследуемые соединения по 200 мг/кг массы тела в течение 7 дней до внутриглазной инъекции митохондриального токсина, ротенона, и затем в течение оставшегося периода исследования. Исследуемые соединения готовили с порошкообразным кормом с получением индивидуальных порций, которые помещали в клетку один раз в сутки. Вкратце, методика заключалась в следующем: исследуемые соединения (20 мг/мл) перемешивали в течение ночи при 4°C с 500 мл 0,5% раствора карбоксиметилцеллюлозы (CMC). С 37,5 мл раствора CMC смешивали 41,25 г сахарозы, 371,25 г порошкообразного корма и 0,5% раствор CMC для приготовления кормовой мешанки, которую делили на порции (по 5,5 г) во взвешивающих лотках и по отдельности хранили при –20°C. В течение исследования неограниченно предоставляли дополнительные пеллеты корма и воду. Для инициирования вызванной митохондриальной дисфункцией потери зрения мышей анестезировали с помощью 5% изофлурана (600 мл/мин кислорода), который разводили до 2% изофлурана (300 мл/мин кислорода) и использовали во время операции. До и после внутриглазной инъекции для очистки участков вокруг глаз использовали ватные палочки, смоченные стерильным физиологическим раствором. При инъекции в стекловидное тело иглу 31 калибра использовали для прокалывания склеры и глаз осторожно массировали для удаления небольшого количества стекловидного тела для предупреждения последующего повышения внутриглазного давления. Затем иглу 33 калибра, приспособленную к шприцу Hamilton на 10 мкл (набор для внутриглазной инъекции, World Precision Instruments, USA) использовали для инъекции 1 мкл ротенона (5 мМ в диметилсульфоксиде) в стекловидную камеру левого глазного яблока. Правый глаз выступал в качестве внутреннего контроля. Кончик иглы вводили в верхнюю полусферу глаза на уровне плоской части радужной оболочки и под углом 45° через склеру в стекловидное тело. Этот путь введения исключает отделение сетчатки или повреждение структур глаза, включая хрусталик и радужную оболочку. Затем мышам представляли возможность восстановиться на нагретом коврике и затем их возвращали в свои клетки. Глаз, в который проводили инъекцию, для выявления признаков воспаления осматривали один раз в день в течение 7 дней после операции. Остроту зрения мышей повторно исследовали раз в неделю с использованием оптомоторного ответа, как описано ранее (Heitz et al. 2012). Мышей помещали на небольшую платформу, окруженную барабаном с электроприводом (диаметр 30 см) с вертикальными черными и белыми полосками (шириной 1 см). После периода адаптации к системе длительностью 10 мин исследование остроты зрения проводили путем вращения полосок по часовой стрелке и против часовой стрелки со скоростью 2 об/мин в течение 2 мин в каждом направлении и с промежутком в 30 с между вращениями. Поведение мышей регистрировали цифровой видеокамерой для последующей оценки поворотов головы. Весь анализ видеоматериала проводил исследователь по слепой схеме. В конце периода наблюдения всех мышей умерщвляли путем внутрибрюшинной инъекции пентобарбитала натрия (110 мг/кг массы тела).
[0201] Лечение типичными соединениями формулы (I) приводило к усиленной защите зрения по сравнению с контролем, идебеноном. Как показано на фиг. 5 значительная защита остроты зрения наблюдалась для типичных соединений UTA 37 и UTA 77, но не для идебенона (отмечен значком R на фиг. 5) при этой концентрации.
Пример 25: Активность в модели диабетической ретинопатии
[0202] Диабетическая ретинопатия (DR) представляет собой осложнение, связанное с хронической гипергликемией у пациентов с сахарным диабетом. Активность соединений, предлагаемых в настоящем изобретении, оценивали в модели химически вызванной диабетической ретинопатии на крысах, в которой введение стрептозотоцина (STZ) вызывает развитие заболевания у крыс Long Evans. Изменение содержания глюкозы в крови и остроту зрения оценивали после лечения типичными соединениями формулы (I).
[0203] Использовали самцов крыс Long–Evans в возрасте 30 недель; со средней массой тела ≈ 400 г. Крыс делили на группы по 3 и держали при 21±2°C с циклом освещение–затемнение 12 ч–12 ч. В течение исследования корм и воду давали без ограничений. Диабет типа 2 вызывали, как описано выше (Premilovac D, et al. (2017) Sci Rep. 7(1) pp. 14158), с объединением жирного кормового рациона (HFD; вызывает ожирение, связанное с резистентностью к инсулину) с доставкой стрептозотоцина (STZ) с помощью осмотического мини–насоса для уменьшения количества продуцирующих инсулин бета–клеток. Эта комбинация обеспечивает контроль обеспечиваемой степени гипергликемии при сохранении подвергнутого ожирению резистентного к инсулину фенотипа, типичного для людей с диабетом типа 2.
[0204] В течение первых 4 недель проводили мониторинг массы тела, содержания глюкозы в крови, потребления воды и остроты зрения, затем хирургически имплантировали осмотический мини–насос. После установления содержания глюкозы в крови, равного 20 мМ, насос удаляли. За 5 недель после начальной операции регистрировали значительную потерю остроты зрения. Для изучения остроты зрения определяли оптокинетический ответ (OKR). Крыс помещали на небольшую платформу, окруженную барабаном с электроприводом (диаметр 70 см) с вертикальными черными и белыми полосками (шириной 6,11 см). После периода адаптации к системе длительностью 10 мин исследование остроты зрения проводили путем вращения полосок по часовой стрелке и против часовой стрелки со скоростью 2,61 об/мин в течение 2 мин в каждом направлении и с промежутком в 30 с между вращениями, так что оценивали остроту зрения левого и правого глаза. Поведение крыс регистрировали цифровой видеокамерой для последующей оценки поворотов головы. Весь анализ видеоматериала проводил исследователь по слепой схеме.
[0205] Крыс с диабетом (n=3–10) разделяли случайным образом на 4 разные группы для исследования
1. без лекарственных средств;
2. лечение идебеноном;
3. лечение с помощью UTA 37,
4. лечение с помощью UTA 77.
[0206] Исследуемые соединения растворяли в растворе глазных капель (5% тилоксапола, 5% минерального масла в 66 мМ цитратном буфере, pH 7,4) по 10 мг/мл для идебенона, 4,6 мг/мл для UTA 37 и 7,36 мг/мл для UTA 77. С недели 14 правые глаза крыс с диабетом лечили содержащим исследуемое соединение раствором глазных капель один раз в день (вводимый объем составлял примерно 50 мкл). Левый (не подвергнутый лечению) глаз выступал в качестве внутреннего контроля. В конце периода наблюдения (неделя 21) всех животных умерщвляли и собирали ткани.
[0207] Как показано на фиг. 6, имплантация осмотического насоса со стрептозотоцином (STZ) (125 мг/кг) после недели 4 быстро приводила к увеличению содержания глюкозы в крови у крыс Long Evans. Проводимое один раз в день введение глазных капель, включающих идебенон, UTA37 или UTA 77, не приводило к значительному изменению содержания глюкозы в крови по сравнению с контрольными крысами.
[0208] Как показано на фиг. 7, остроту зрения определяли с помощью оптокинетического ответа для левых и правых глаз крыс Long Evans в течение 19 недель. Введение стрептозотоцина (STZ) на неделе 4 значительно ухудшало непроизвольное движение головы к неделе 9. В неделю 14 один раз в день вводили глазные капли с типичными соединениями формулы (I). Соединения формулы (I) были эффективными в модели диабетической ретинопатии. В частности, проводимое один раз в день введение типичных соединений формулы (I) частично восстанавливало остроту зрения после ухудшения под действием STZ, о чем свидетельствовал оптокинетический ответ, и это показывало, что такие соединения могут быть эффективным для лечения вторичных осложнений, связанных с диабетом, включая офтальмологические осложнения, связанные с диабетом.
Пример 26: Активность в модели колита
[0209] Язвенный колит (UC) представляет собой форму хронического воспаления желудочно–кишечного тракта, обычно ободочной и прямой кишки. Симптомы включают развитие геморрагического поноса со слизью или без слизи, неотложный позыв на испражнение или мочеиспускание, болезненный позыв на испражнение или мочеиспускание, боль в животе, потерю массы, усталость и внекишечные проявления. Модель колита, вызванного декстрансульфатом натрия (DSS) принята в качестве подходящей модели на мышах для язвенного колита у людей.
[0210] Колит вызывали у мышей химически путем введения 2,5% декстрансульфата натрия (DSS). Во время лечения типичным соединением формулы (I), UTA77, определяли массу тела (см. фиг. 8), консистенцию кала (см. фиг. 9), содержание крови в кале (см. фиг. 10) и общий показатель активности заболевания (см. фиг. 11).
[0211] Использовали самок мышей C57BL/6 в возрасте 7–8 недель со средней массой тела ≈ 17 г. Мышей разделяли случайным образом на 3 разные группы:
1. здоровые, контрольная группа без использования DSS,
2. контрольная группа с использованием DSS,
3. группа мышей, которых лечили с помощью DSS и исследуемым соединением (n=5 на группу).
[0212] Массы тела мышей определяли ежедневно в начальный период акклиматизации в течение одной недели (фиг. 8). Все мыши не голодали и им был предоставлен неограниченный доступ к корму и питьевой воде (стерилизованная в автоклаве водопроводная вода). Типичные соединения формулы (I) готовили с порошкообразным кормом (200 мг/кг массы тела) с получением индивидуальных порций, которые помещали в клетку один раз в сутки. Типичные соединения формулы (I) (20 мг/мл) перемешивали в течение ночи при 4°C с 500 мл 0,5% раствора карбоксиметилцеллюлозы (CMC). С 37,5 мл раствора CMC смешивали 41,25 г сахарозы, 371,25 г порошкообразного корма и 0,5% раствор CMC для приготовления кормовой мешанки, которую делили на порции (по 2,2 г) во взвешивающих лотках и по отдельности хранили при –20°C. Колит инициировали путем добавления 2,5% мас./об. декстрансульфата натрия (DSS, MW=36000–50000, марки для инициирования колита, MP Biomedicals, USA) в питьевую воду мышей от дня 0 до дня 7 (день завершения). В день 0 всех мышей взвешивали и определяли консистенцию кала и скрытую кровь и затем вводили DSS и исследуемые соединения. Контрольные животные получали стерилизованную в автоклаве водопроводную воду без DSS и обычные кормовые пеллеты, а мышам групп, которым давали DSS от дня 0 до дня 7, вводили 2,5% DSS в водопроводную воду. Мышам всех контрольных групп также давали 2,2 г кормовой мешанки без исследуемых соединений. Животные, которым давали лекарственное средство, получали 200 мг/кг исследуемых соединений в кормовой мешанке с 2,5% DSS в воде от дня 0 до дня 7. Ежедневно регистрировали массу тела (см. фиг. 8), консистенцию кала (см. фиг. 9), содержание крови в кале (см. фиг. 10). Показатель активности заболевания (DAI) (фиг. 11) рассчитывали в соответствии со шкалой, приведенной ниже в таблице 9. Каждый параметр оценивали независимо и все три параметра использовали для расчета DAI.
Таблица 9: Шкала параметров для расчета показателя активности заболевания (DAI)
[0213] У мышей, которых лечили с помощью UTA77, обнаружена уменьшенная активность заболевания, улучшенный кал и уменьшенное количество крови в кале по сравнению с мышами контрольных групп, получавших DSS. Кроме того, у мышей, которых лечили с помощью UTA77, обнаружена меньшая потеря массы, чем у мышей контрольных групп, получавших DSS в период лечения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ИНГИБИТОРЫ α-АМИНО-β-КАРБОКСИМУКОНАТ-ε-СЕМИАЛЬДЕГИД-ДЕКАРБОКСИЛАЗЫ | 2015 |
|
RU2746405C2 |
| ИНГИБИТОРЫ ДЕКАРБОКСИЛАЗЫ ПОЛУАЛЬДЕГИДА α-АМИНО-β-КАРБОКСИМУКОНОВОЙ КИСЛОТЫ | 2019 |
|
RU2841136C2 |
| ПРОИЗВОДНЫЕ БИСФЕНОЛА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ МОДУЛЯТОРОВ АКТИВНОСТИ РЕЦЕПТОРА АНДРОГЕНА | 2017 |
|
RU2767257C2 |
| ПРОИЗВОДНАЯ ИМИДАЗОПИРИДИНА И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ ЕЕ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2020 |
|
RU2810973C2 |
| СОЕДИНЕНИЯ ПУРИНОНА В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗ | 2013 |
|
RU2655388C2 |
| ИНГИБИТОРЫ БЕЛКА АКТИВАЦИИ ФИБРОБЛАСТОВ | 2020 |
|
RU2802426C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ СУЛЬФОНАМИДА, ОБЛАДАЮЩИЕ СЕЛЕКТИВНОЙ NOX-ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ | 2019 |
|
RU2809030C2 |
| ПРОИЗВОДНЫЕ 1,3,4-ОКСАДИАЗОЛА, КАК ИНГИБИТОР ГИСТОНДЕЗАЦЕТИЛАЗЫ 6 И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2019 |
|
RU2763936C1 |
| СОЕДИНЕНИЯ, ПРИМЕНИМЫЕ ДЛЯ ЛЕЧЕНИЯ РЕСПИРАТОРНОГО ЗАБОЛЕВАНИЯ КРУПНОГО РОГАТОГО СКОТА ИЛИ СВИНЕЙ | 2017 |
|
RU2775529C2 |
| МОДУЛЯТОРЫ АНДРОГЕНОВОГО РЕЦЕПТОРА И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2019 |
|
RU2797622C2 |


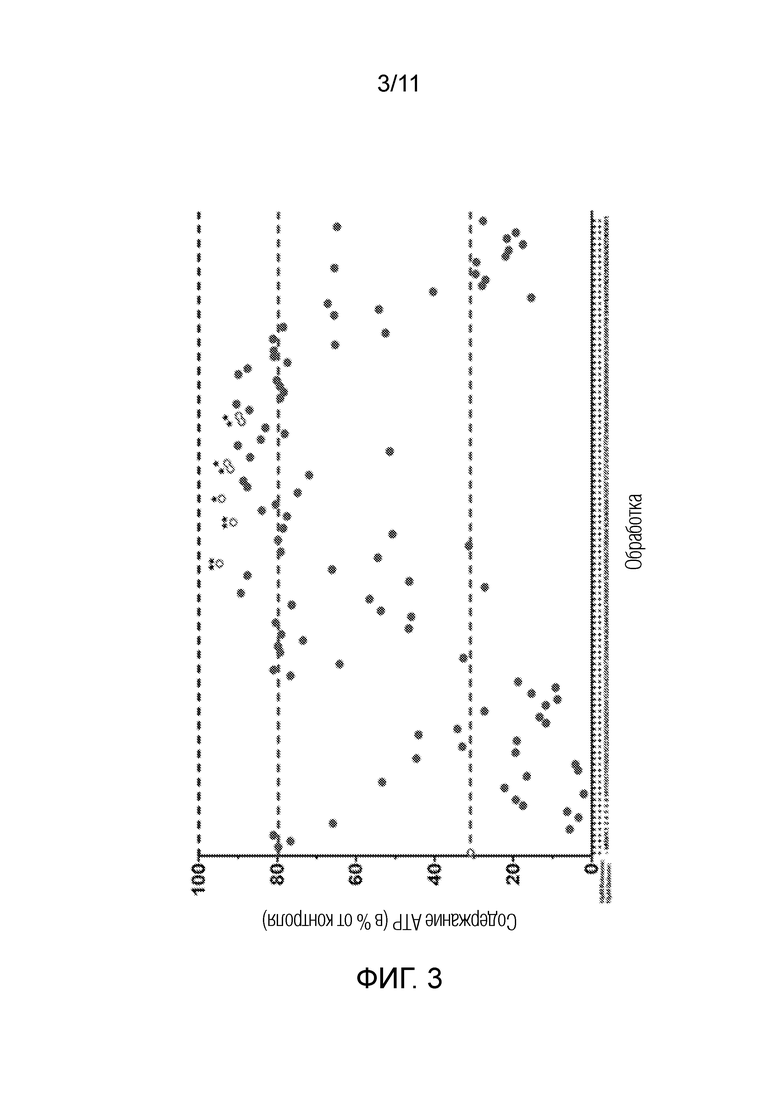
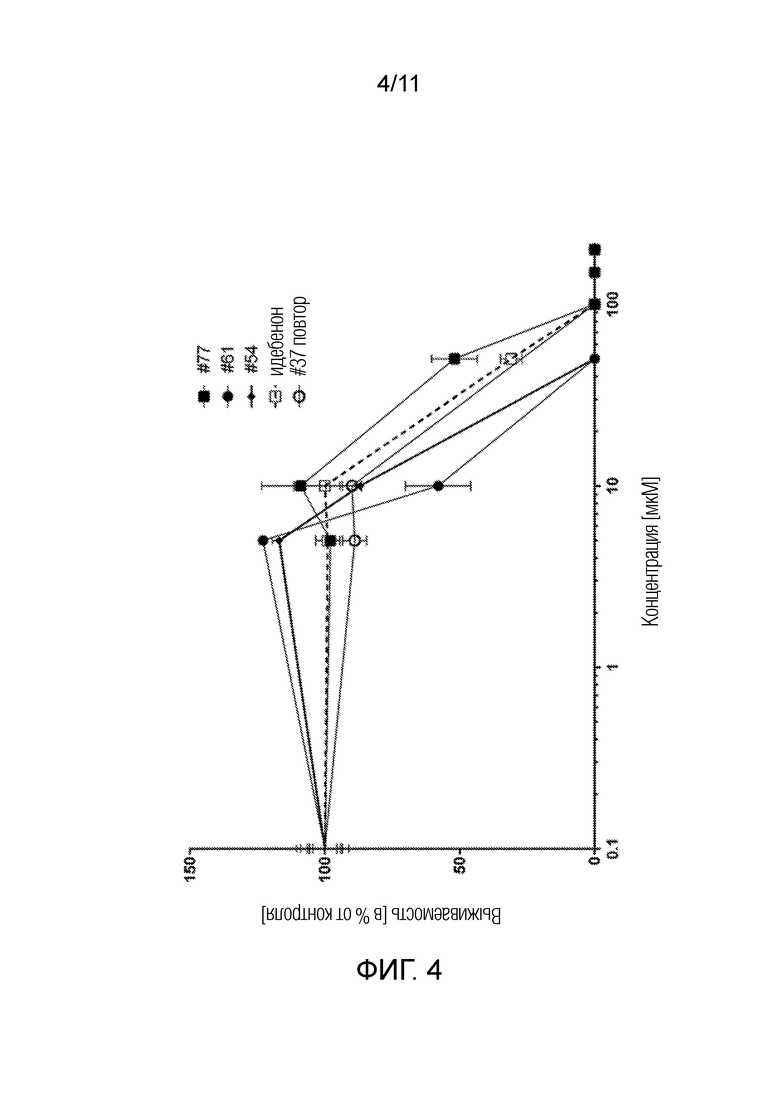

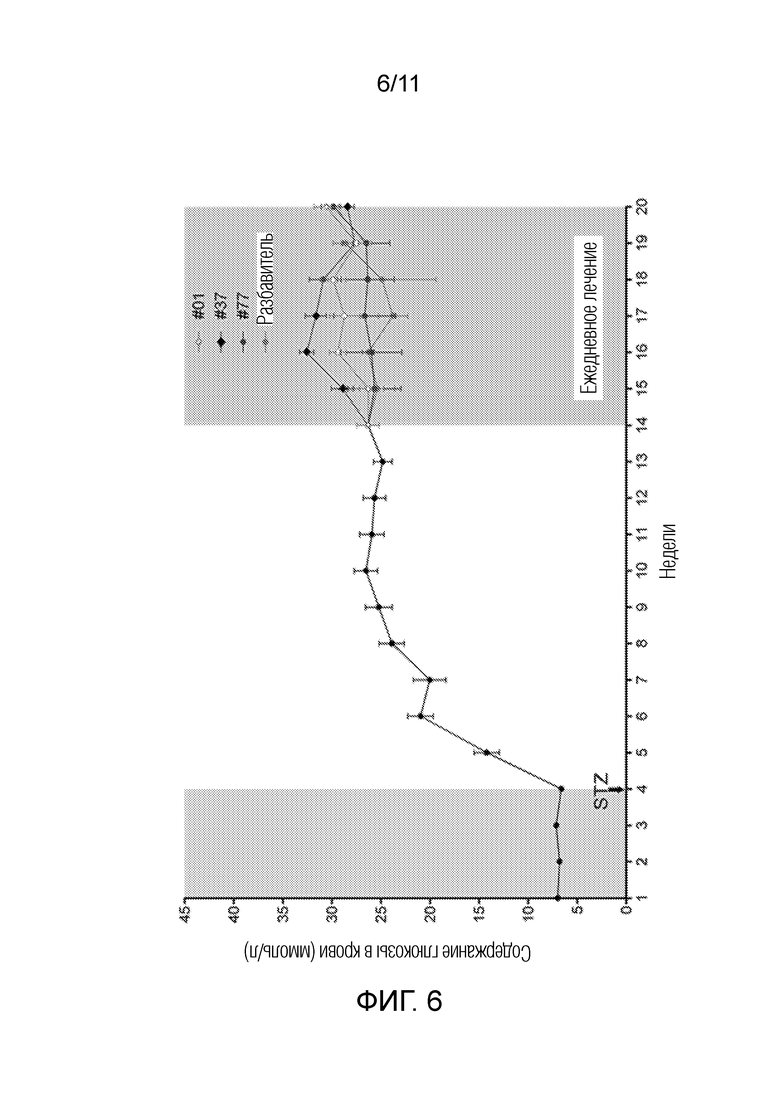
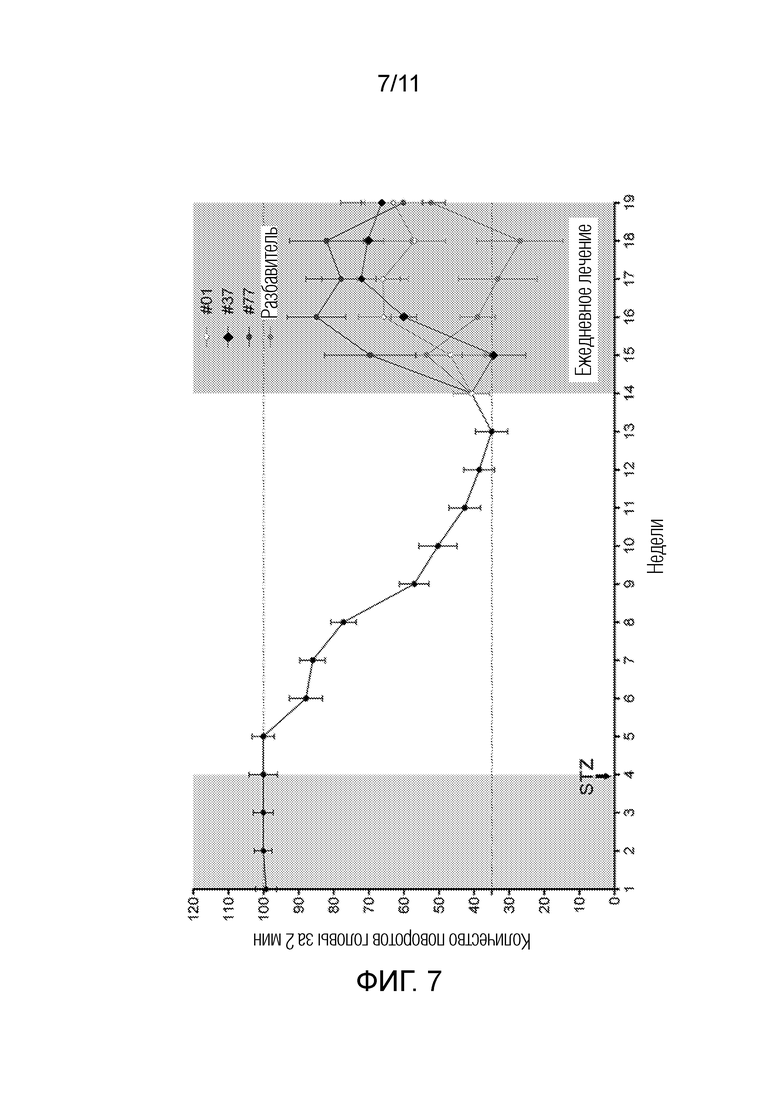
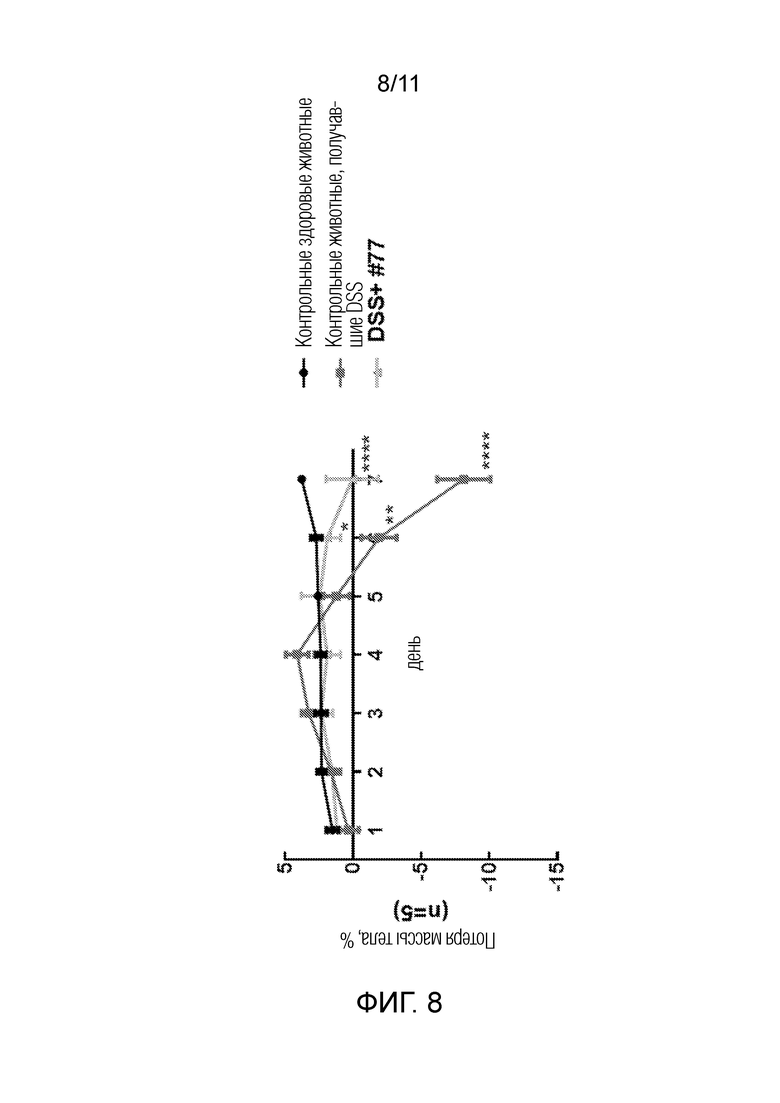
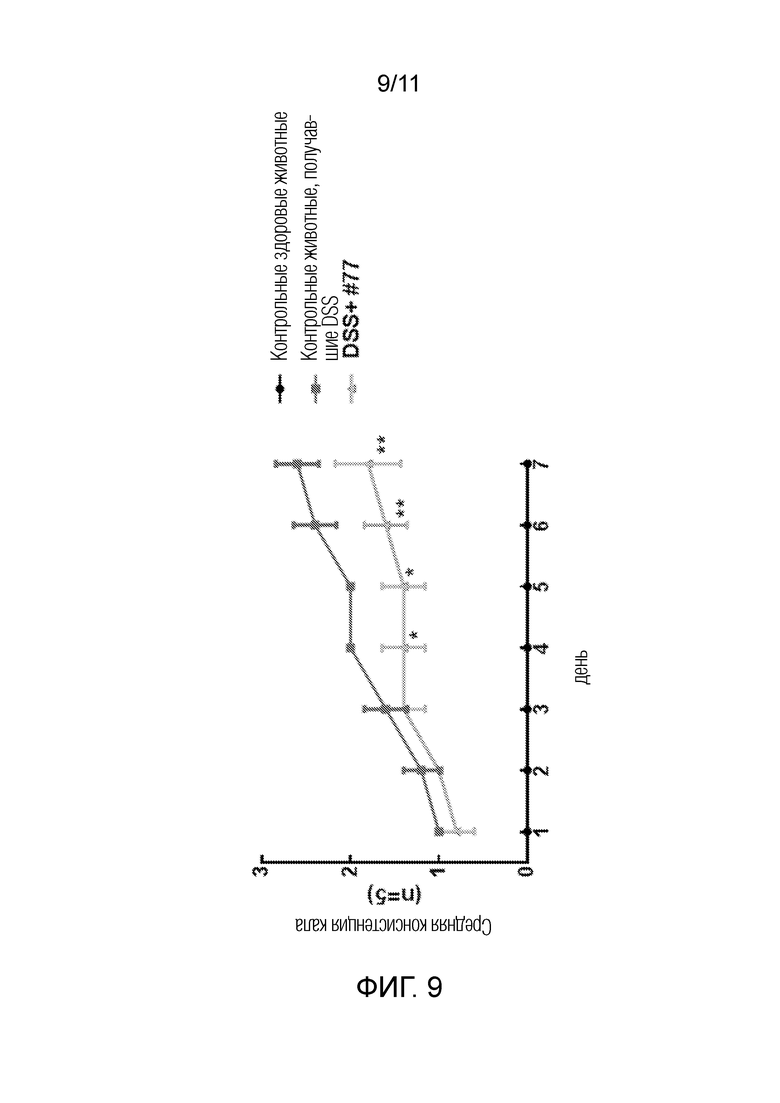
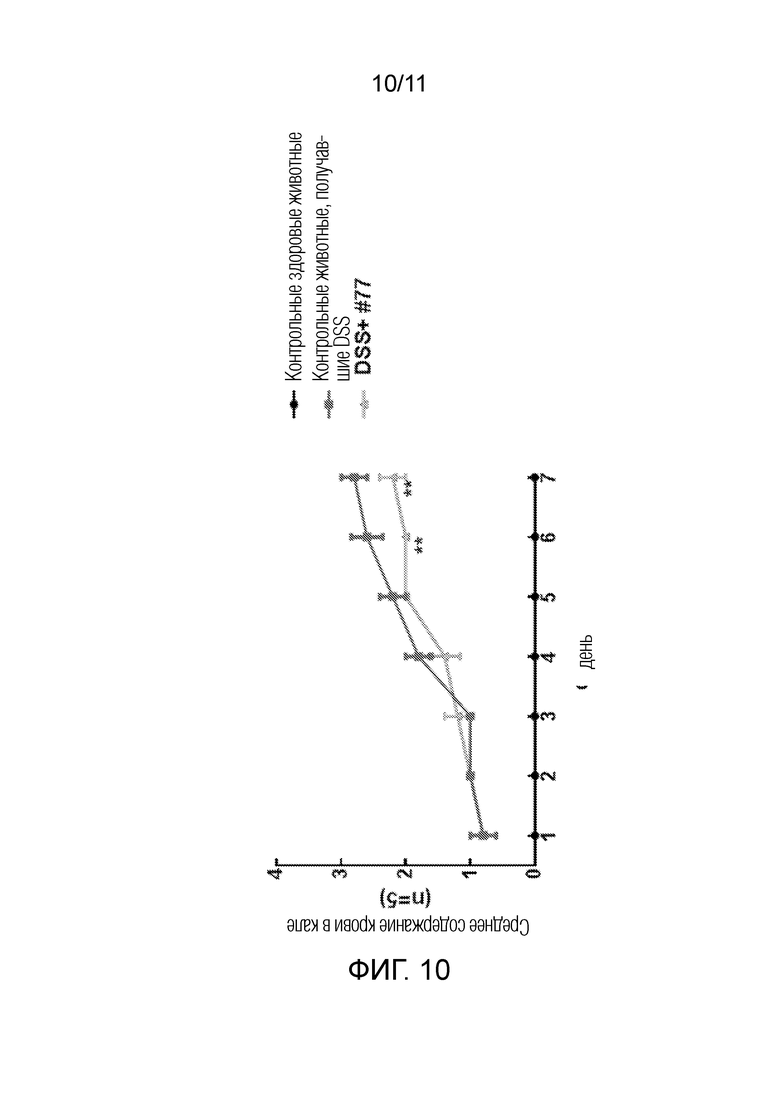
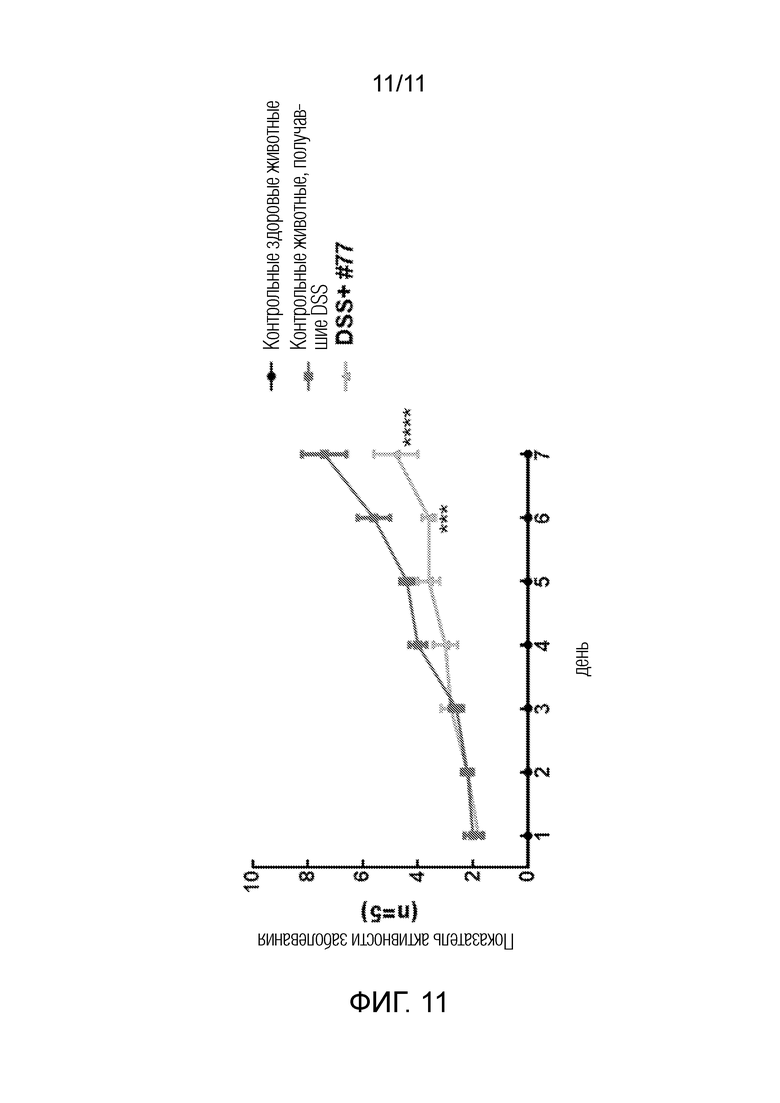
Изобретение относится к соединению формулы (Ib) или его фармацевтически приемлемой соли, в которой R5 выбран из группы, включающей H и метил, R6 означает необязательно замещенный C6–C12 арил, R означает H или необязательно замещенный C1–C6 алкил; R13 в каждом случае независимо выбран из группы, включающей H, необязательно замещенный фенил и необязательно замещенный бензил, n означает целое число, выбранное из группы, включающей 1, 2, 3, 4 и 5, и m означает целое число, выбранное из группы, включающей 0, 1, 2 и 3, где необязательные заместители выбраны из группы, состоящей из галогена, C1-6 алкила, C1-6 алкокси, C2-6 алкенила, C2-6 алкинила, C1-6 галогеналкила, C1-6 галогеналкокси, -ОН, фенила, бензила, фенокси, бензилокси, бензоила, силила, -NH2, -NHC1-4 алкил, -N(C1-4 алкил)2, -CN, -NO2, меркапто, P=O(OH)(NH2), -S(O)2NH2, -S(O)2NHC1-4 алкила, -S(O)2N(C1-4 алкил)2, C1-6 алкилкарбонила, C1-6 алкоксикарбонила, CO2H, -S(O)R-, где R представляет собой низший алкил или циклоалкил, и -S(O)2R-, где R представляет собой низший алкил, циклоалкил или ОН, где термин «низший алкил» относится к алкильным группам, содержащим от одного до шести атомов углерода. Изобретение относится к конкретным соединениям, которые приведены в формуле изобретения. Также изобретение относится к фармацевтической композиции для лечения или предупреждения заболевания или нарушения, связанного с митохондриальной дисфункцией, включающей терапевтически эффективное количество соединения по изобретению. Соединения по изобретению применяют для лечения или предупреждения заболевания или нарушения, связанного с митохондриальной дисфункцией, которое выбрано из группы, включающей наследственную оптическую нейропатию Лебера (LHON), диабетическую ретинопатию, язвенный колит (UC). Технический результат - соединения, применимые для профилактики и/или лечения заболеваний и нарушений, связанных с митохондриальной дисфункцией. 7 н. и 4 з.п. ф-лы, 9 табл., 11 ил., 26 пр.
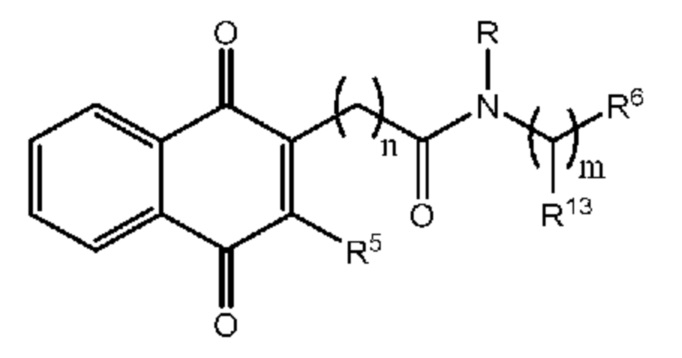 (Ib)
(Ib)
1. Соединение формулы (Ib)

Формула (Ib)
или его фармацевтически приемлемая соль, в которой:
R5 выбран из группы, включающей H и метил,
R6 означает необязательно замещенный C6–C12 арил,
R означает H или необязательно замещенный C1–C6 алкил,
R13 в каждом случае независимо выбран из группы, включающей H, необязательно замещенный фенил и необязательно замещенный бензил,
n означает целое число, выбранное из группы, включающей 1, 2, 3, 4 и 5, и
m означает целое число, выбранное из группы, включающей 0, 1, 2 и 3, где необязательные заместители выбраны из группы, состоящей из галогена, C1-6 алкила, C1-6 алкокси, C2-6 алкенила, C2-6 алкинила, C1-6 галогеналкила, C1-6 галогеналкокси, -ОН, фенила, бензила, фенокси, бензилокси, бензоила, силила, -NH2, -NHC1-4 алкил, -N(C1-4 алкил)2, -CN, -NO2, меркапто, P=O(OH)(NH2), -S(O)2NH2, -S(O)2NHC1-4 алкила, -S(O)2N(C1-4алкил)2, C1-6алкилкарбонила, C1-6 алкоксикарбонила, CO2H, -S(O)R-, где R представляет собой низший алкил или циклоалкил, и -S(O)2R-, где R представляет собой низший алкил, циклоалкил или ОН, где термин «низший алкил» относится к алкильным группам, содержащим от одного до шести атомов углерода.
2. Соединение по п. 1, в котором R6 означает необязательно замещенный C6 арил.
3. Соединение по п. 1 или 2, в котором R6 означает диметоксифенил, предпочтительно 3,4–диметоксифенил.
4. Соединение по п. 1, в котором R5 означает H.
5. Соединение по п. 1, в котором R5 означает метил.
6. Соединение, выбранное из группы, включающей:
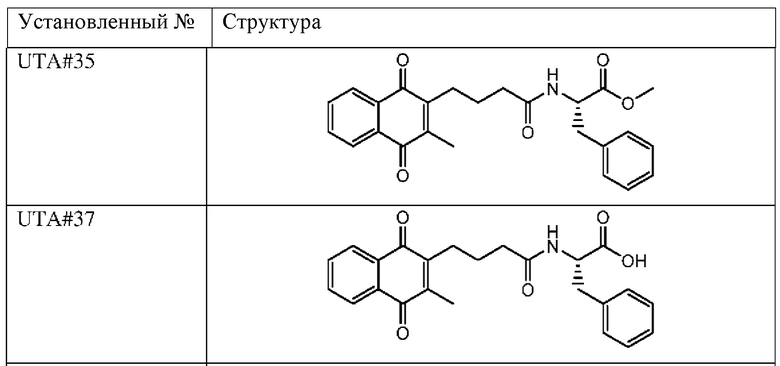
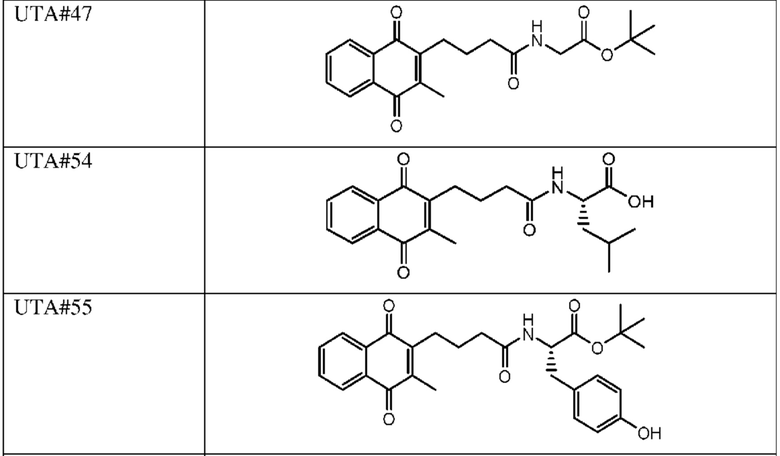
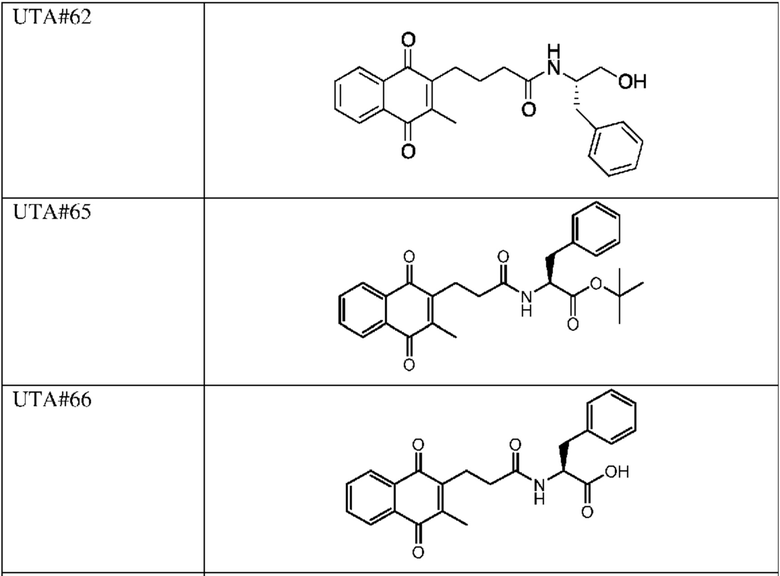
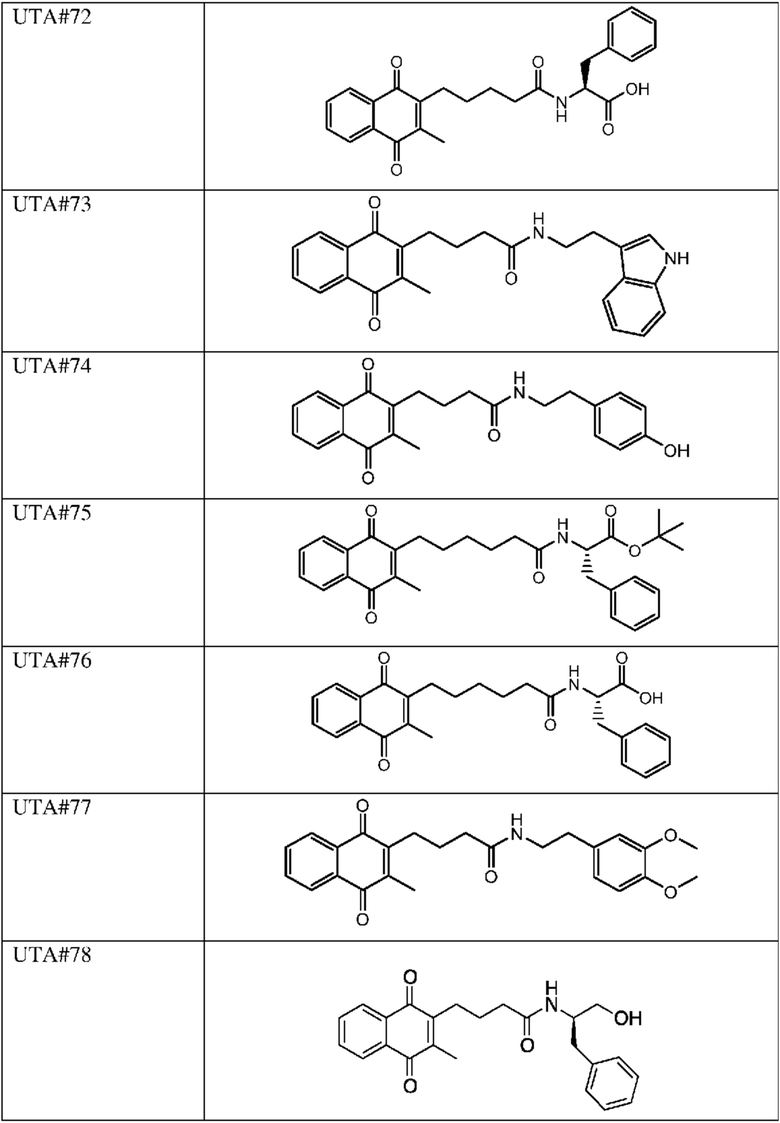
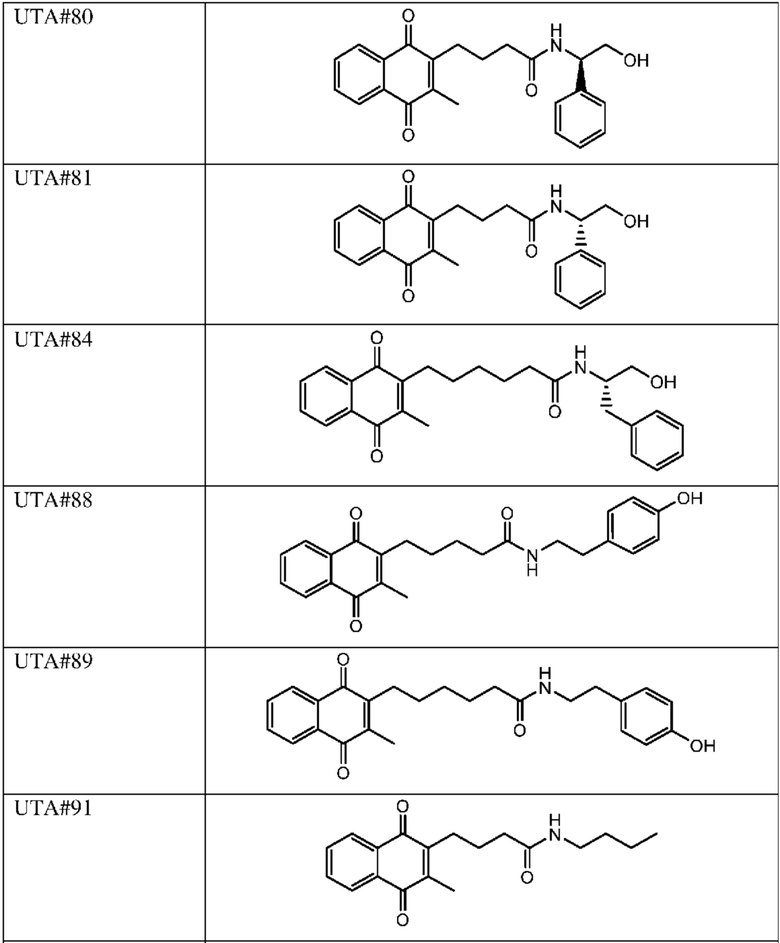
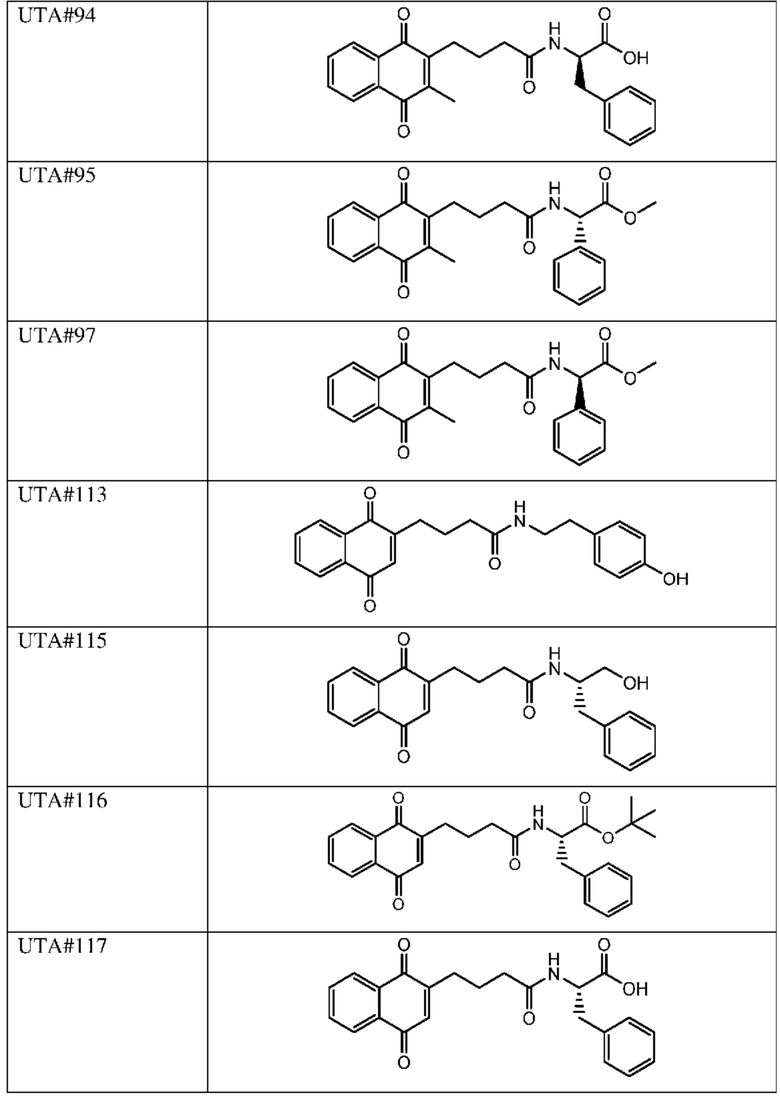
7. Фармацевтическая композиция для лечения или предупреждения заболевания или нарушения, связанного с митохондриальной дисфункцией, включающая терапевтически эффективное количество соединения по любому из предыдущих пунктов.
8. Способ лечения или предупреждения заболевания или нарушения, связанного с митохондриальной дисфункцией, включающий введение нуждающемуся в нем лицу терапевтически эффективного количества соединения по любому из пп. 1–6 или фармацевтической композиции по п. 7,
в котором заболевание или нарушение, связанное с митохондриальной дисфункцией, выбрано из группы, включающей наследственную оптическую нейропатию Лебера (LHON), диабетическую ретинопатию, язвенный колит (UC).
9. Способ лечения или предупреждения вызванной лекарственным средством или вызванной окружающей средой митохондриальной дисфункции, включающий введение нуждающемуся в нем лицу терапевтически эффективного количества соединения по любому из пп. 1–6 или фармацевтической композиции по п. 7,
в котором митохондриальная дисфункция представляет собой вызванную лекарственным средством митохондриальную дисфункцию, обусловленную применением противовирусного средства; противоракового средства; антибиотика; CNS лекарственного средства; гипотензивного лекарственного средства; антрациклинов; нестероидного противовоспалительного лекарственного средства (NSAID); анестетика; бета–блокатора; противоаритмического; противодиабетического; противовоспалительного; или другого средства.
10. Применение соединения по любому из пп. 1–6 для приготовления косметического средства для ослабления эффектов старения.
11. Применение соединения по любому из пп. 1–6 для приготовления лекарственного средства для лечения или предупреждения вызванной лекарственным средством или вызванной окружающей средой митохондриальной дисфункции,
в котором митохондриальная дисфункция представляет собой вызванную лекарственным средством митохондриальную дисфункцию, обусловленную применением противовирусного средства; противоракового средства; антибиотика; CNS лекарственного средства; гипотензивного лекарственного средства; антрациклинов; нестероидного противовоспалительного лекарственного средства (NSAID); анестетика; бета–блокатора; противоаритмического; противодиабетического; противовоспалительного; или другого средства.
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Изложница с суживающимся книзу сечением и с вертикально перемещающимся днищем | 1924 |
|
SU2012A1 |
| Способ защиты переносных электрических установок от опасностей, связанных с заземлением одной из фаз | 1924 |
|
SU2014A1 |
| Колосоуборка | 1923 |
|
SU2009A1 |
| ХИНОНОВЫЕ ПРОИЗВОДНЫЕ | 1992 |
|
RU2054412C1 |
| ФТОРИРОВАННЫЕ ПРОИЗВОДНЫЕ 1,4-НАФТОХИНОНА, ОБЛАДАЮЩИЕ ЦИТОТОКСИЧЕСКОЙ АКТИВНОСТЬЮ ПО ОТНОШЕНИЮ К РАКОВЫМ КЛЕТКАМ ЧЕЛОВЕКА В КУЛЬТУРЕ | 2010 |
|
RU2443678C1 |
| Louis F | |||
| Fieser, Richard B | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2025-03-28—Публикация
2018-04-20—Подача