6-(1,3-бензимидазол-2-ил)-7-гидрокси-замещенные спиро[бензопиран-индолины], обладающие флуоресценцией.
Изобретение относится к новым соединениям в ряду спиро[бензопиран-индолинов], а именно к 6-(1,3-бензимидазол-2-ил)-7-гидрокси-замещенным спиро[бензопиран-индолинам] общей формулы
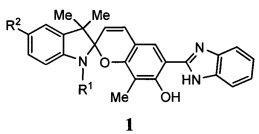
где R1 - C1-C6 алкил, R2 - H, галоген.
Соединения 1 проявляют фотохромные свойства и в спироциклической форме обладают интенсивной флуоресценцией с аномально высоким стоксовым сдвигом. Флуоресценция с аномальным стоксовым сдвигом не поглощается исходной спироциклической формой, что обеспечивает высокий флуоресцентный контраст при фотопереключении. В связи с этим соединения могут быть использованы в качестве флуоресцирующих фотохромов, например, как фотоуправляемые молекулярные переключатели с флуоресцентным откликом.
В ряду спиро[бензопиран-индолинов] известны производные спиропиранов, содержащие 4,4-дифтор-4-бора-3а,4а-диаза-s-индацен (2, 3) и 1',4'-бис-(пиренилэтинил)-производные спиропиранов (4).
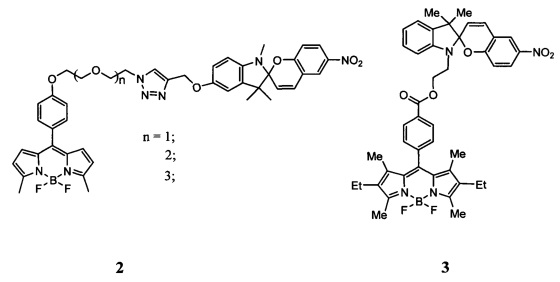
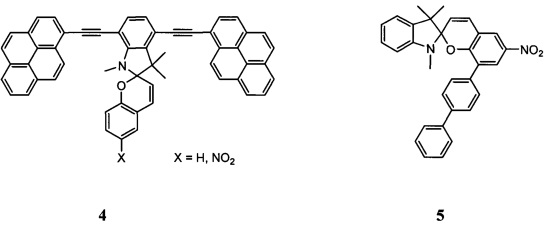
Дизайн соединений 2-4 основан на ковалентном связывании известного флуорофорного остатка с фотохромным спиропираном, что обеспечивает флуоресцентные свойства спироциклической форме. Соединения 2-4 проявляют фотохромные свойства, а также обладают флуоресценцией с незначительным стоксовым сдвигом ввиду применения тривиальных флуорофоров. (L. Kong, Hok-Lai Wong, A. Yiu-Yan Tam, Wai Han Lam, Lixin Wu, Vivian Wing-Wah Yam. // ACS Appl. Mater. Interfaces 2014, 6, 1550-1562. M. Tomasulo, E. Deniz, R.J. Alvarado, F.M. Raymo. // J. Phys. Chem. С 2008, 112, 8038-8045. A.C. Benniston, A. Harriman, S.L. Howell, P. Li, D.P. Lydon // J. Org. Chem. 2007, 72, 888-897).
Наиболее близким по выполнению и достигаемому результату является 2-(4-бифенил)-2',3'-дигидро-6-нитро-1',3',3'-триметилспиро[2H-1-бензопиран-2,2'-индол] (5) (N.P. Manjrekar, R.V. Roshi, N.S. Bahulekar, S.D. Sahasrabudhe // WO 2009/141236 A1).
Соединение также проявляет фотохромные свойства и также обладает флуоресценцией с незначительным стоксовым сдвигом ввиду применения тривиальных флуорофоров.
Техническим результатом изобретения являются соединения в ряду спиро[бензопиран-индолинов], проявляющие фотохромные свойства и флуоресценцию с высоким стоксовым сдвигом.
Технический результат достигается соединениями общей формулы 1.
Изобретение удовлетворяет критерию изобретательского уровня, так как не известны соединения ряда спиро[бензопиран-индолинов], обладающие интенсивной флуоресценцией с аномально высоким стоксовым сдвигом.
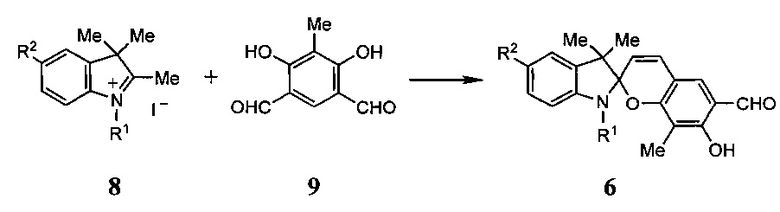
Способ получения соединений 1 заключается во взаимодействии 7-гидрокси-6-формилзамещенного спиропирана 6, о-фенилендиамина (7) и метабисульфита натрия (Na2S2O5):

7-Гидрокси-6-формилзамещенные спиропираны 6 (R1 - C1-C6 алкил, R2 - Н, галоген), получены взаимодействием йодида тетраметил-3H-индолия 8 и изофталевого альдегида 9 в присутствии триэтиламина в качестве основания.
Ниже приведены примеры получения соединений. Пример 1.6-(1H-бензо[d]имидазол-2-ил)-1',1',3',8-тетраметилспиро[2H-1-бензопиран-2,2'-индолин]-7-ол (1, R1 - СН3, R2 - Н).
Смесь 0.34 г (1 ммоль) спиропирана 6, 0.11 г (1 ммоль) о-фенилендиамина 7 и 0.03 г Na2S2O5 в 5 мл диметилформамида перемешивали при 80°C в течение 2 ч, затем смесь вылили в 50 мл воды и экстрагировали 80 мл CHCl3. Экстракт сушили безводным Na2SO4, остаток очищали колоночной хроматографией на Al2O3 (элюент - CHCl3) и перекристаллизовывали из смеси толуол-изооктан (1:1). Выход 24%, т.пл. 270-271°C. Спектр ЯМР 1Н (δ, м.д., J/Гц): 1.19 (3Н, с, 3'-СН3); 1.31 (3Н, с, 3'-СН3); 1.97 (3Н, с, 8-СН3); 2.73 (3Н, с, 1'-СН3); 5.63 (1Н, д, J=10.2, 3-Н); 6.54 (1H, д, J=7.7, 7'-Н); 6.84 (1Н, д, J=10.2, 4-Н); 6.85 (1Н, д.т, J=7.3 и 0.9, 5'-Н); 7.08 (1H, д.д, J=7.3 и 1.3, 4'-Н); 7.14 (1Н, с, 5-Н); 7.18 (1Н, д.т, J=7.6 и 1.2, 6'-Н); 7.27-7.29 (2Н, m, H-im); 7.44-7.47 (1Н, m, H-im); 7.68-7.72 (1Н, m, H-im); 9.17 (1H, s, NH-im); 13.48 (1Н, с, 7-ОН). Масс-спектр, m/z (Iотн, %): 423 [М]+ (97), 408 [М-СН3]+ (49). Найдено (%): С, 76.45; Н, 5.79; N, 9.97. C27H25N3O2. Вычислено (%): С, 76.57; Н, 5.95; N, 9.92.
Пример 2. 6-(1H-бензо[d]имидазол-2-ил)-1',3',3',8-тетраметил-5'-хлорспиро[2H-1-бензопиран-2,2'-индолин]-7-ол (1, R1 - СН3, R2 - Cl).
Соединение получено аналогично примеру 1 из 0.37 г (1 ммоль) спиропирана 6 (R1 - СН3, R2 - Cl).
Выход 22%, т.пл. 290-291°C (толуол-изооктан, 3:1). Спектр ЯМР 1Н (δ, м.д., J/Гц): 1.18 (3Н, с, 3'-СН3); 1.28 (3Н, с, 3'-СН3); 1.98 (3Н, с, 8-СН3); 2.70 (3Н, с, 1'-СН3); 5.60 (1H, д, J=10.2, 3-Н); 6.44 (1H, д, J=8.2, 7'-Н); 6.84 (1Н, д, J=10.2, 4-Н); 7.02 (1H, д, J=2.1, 4'-Н); 7.12 (1Н, д.д, J=8.2 и 2.1, 6'-Н); 7.14 (1Н, с, 5-Н); 7.27-7.29 (2Н, m, H-im); 7.441-7.472 (1H, m, H-im); 7.688-7.718 (1Н, m, H-im); 9.17 (1Н, s, NH-im); 13.51 (1Н, s 7-ОН). Найдено (%): С, 70.64; Н, 5.39; N, 9.27. C27H24ClN3O2. Вычислено (%): С, 70.81; Н, 5.28; N, 9.18.
Пример 3. 6-(1H-бензо[d]имидазол-2-ил)-5'-бром-1',3',3',8-тетраметилспиро[2H-1-бензопиран-2,2'-индолин]-7-ол (1, R1 - Me, R2 - Br).
Соединение получено аналогично примеру 1.
Выход 26%, т.пл. 272-273°C (толуол-изооктан, 3:1). Спектр ЯМР 1Н (δ, м.д., J/Гц): 1.18 (3Н, с, 3'-СН3); 1.28 (3Н, с, 3'-СН3); 1.98 (3Н, с, 8-СН3); 2.69 (3Н, с, 1'-СН3); 5.60 (1Н, д, J=10.2, 3-Н); 6.40 (1Н, д, J=8.2, 7'-Н); 6.84 (1Н, д, J=10.2, 4-Н); 7.11 (1H, д, J=2.0, 4'-Н); 7.14 (1Н, с, 5-Н); 7.26 (1Н, д.д, J=8.2 и 2.0, 6'-Н); 7.27-7.29 (2Н, м, H-im); 7.43-7.47 (1H, м, H-im); 7.69-7.72 (1Н, м, H-im); 9.17 (1Н, с, NH-im); 13.43 (1Н, с, 7-ОН). Найдено (%): С, 64.43; Н, 4.88; N, 8.30. C27H24BrN3O2. Вычислено (%): С, 64.55; Н, 4.81; N, 8.36.
У полученных соединений по стандартным методикам определены спектрально-абсорбционные и спектрально-флуоресцентные характеристики изомерных форм при 293 К.
Электронные спектры поглощения исследуемых соединений регистрировали на спектрофотометре "Agilent 8453" с приставкой для термостатирования образцов. Спектры испускания и возбуждения флуоресценции регистрировали на спектрофлуориметре Varian Cary Eclipse.
Облучение растворов фильтрованным светом ртутной лампы высокого давления осуществлялось на установке «Newport 66902». Для выделения монохроматического излучения использовался интерференционный светофильтр (λ=365 нм).
Методика определения квантовых выходов флуоресценции изложена в: Паркер С. Фотолюминесценция растворов. - М.: Мир, - 1972 - 511 с. В качестве стандартного люминофора использовали 1,8-нафтален-1',2'-бензимидазол (квантовый выход 0,55 в толуоле при длине волны возбуждения 365 нм, Красовицкий Б.М., Болотин Б.М. Органические люминофоры. - 2-е изд. перераб. - М.: Химия, 1984. - 336 с., ил.)
Исследуемое соединение 1а в этаноле присутствует практически полностью в виде спироциклического изомера, что проявляется в отсутствии поглощения в видимой области спектра. Спироциклическая форма обладает интенсивной флуоресценцией с аномальным стоксовым сдвигом с максимумом при 460 нм и квантовым выходом 0,594. Облучение бесцветного раствора УФ светом (интенсивность ~4⋅1013 фотон/с) приводит к образованию мероцианиновой формы соединения, сопровождающееся окрашиванием раствора. В спектрах поглощения при этом наблюдается образование полосы поглощения мероцианинового изомера с максимумом при 574 нм. Процесс фотоокрашивания термически полностью обратим.
В таблице приведены результаты исследований соединений по примерам 1, 2 и 3 (соединения 1а, б, в). Для сравнения в таблице приведены также результаты для аналогов: спиропиран, содержащий 4,4-дифтор-4-бора-3а,4а-диаза-s-индацен в хроменовой части молекулы (2) (соединение 2) данные взяты из статьи L. Kong, Hok-Lai Wong, A. Yiu-Yan Tam, Wai Han Lam, Lixin Wu, Vivian Wing-Wah Yam. // ACS Appl. Mater. Interfaces 2014, 6, 1550-1562; спиропиран, содержащий 4,4-дифтор-4-бора-3а,4а-диаза-s-индацен в индолиновой части молекулы (3) (соединение 3) данные взяты из статьи М. Tomasulo, Е. Deniz, R.J. Alvarado, F.M. Raymo. // J. Phys. Chem. С 2008, 112, 8038-8045; 1',4'-бис-(пиренилэтинил)-производные спиропирана (4) (соединение 4) данные взяты из статьи А.С. Benniston, A. Harriman, S.L. Howell, P. Li, D.P. Lydon // J. Org. Chem. 2007, 72, 888-897; 2-(4-,бифенил)-2',3'-дигидро-6-нитро-1',3',3'-триметилспиро[2H-1-бензопиран-2,2'-индол] (5) (соединение 5) данные взяты из патента N.P. Manjrekar, R.V. Roshi, N.S. Bahulekar, S.D. Sahasrabudhe // WO 2009/141236 A1.
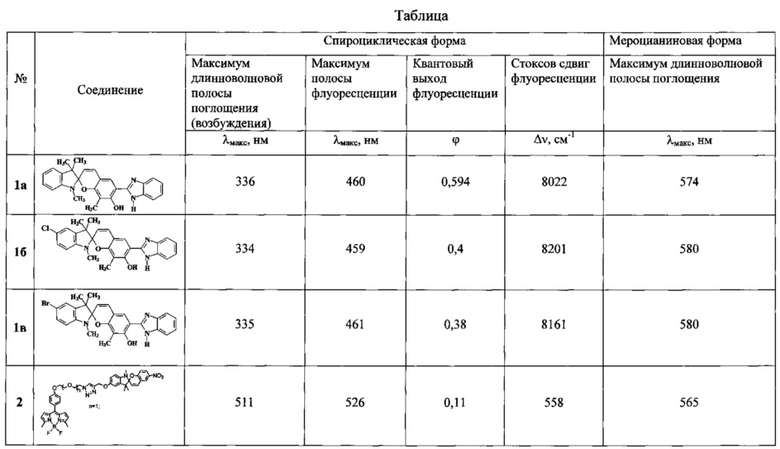
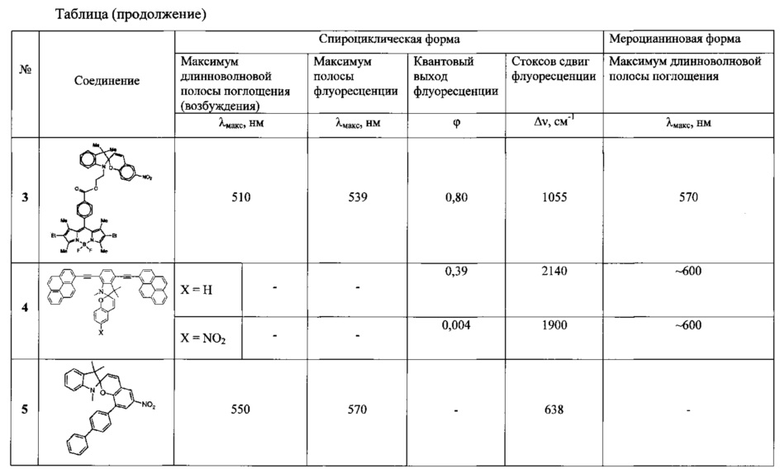
Как видно из таблицы, соединения 1, подобно аналогам (2-5), демонстрируют интенсивную флуоресценцию в спироциклической форме (λмакс=460 нм, ϕ=0,38-0,6) с величиной стоксового сдвига порядка 8000 см-1, что в несколько раз превышает соответствующие значения для аналогов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Фотохромные производные 5'-гидроксиметил-6-нитро-1',3',3'-триметилспиро[2Н-1-бензопиран-2,2'-индолина] | 2019 |
|
RU2694904C1 |
| ФОТОХРОМНЫЕ ПРОИЗВОДНЫЕ 5'-ВИНИЛ-6-НИТРО-СПИРОБЕНЗОПИРАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2458927C1 |
| 5-ФОРМИЛ-ЗАМЕЩЕННЫЕ ИНДОЛИНОВЫЕ СПИРОБЕНЗОПИРАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2358977C1 |
| Перхлораты 1,3,3-триметилспиро[хромен-2,2'-индолина], обладающие фотохромными свойствами | 2016 |
|
RU2627358C1 |
| 1,3,3-триметил-5-метокси-6´-бром-8´-[(Е)-2-(1´´,3´´,3´´-триметил-5-метокси-3Н-индолий-2´´-ил)винил]-спиро[индолин-2,2´-2Н-хромен] йодид, обладающий фотохромными свойствами | 2022 |
|
RU2786996C1 |
| Способ получения спиропиранов бензтиазольного ряда | 1988 |
|
SU1608189A1 |
| 5'-(1,3-БЕНЗОТИАЗОЛ-2-ИЛ)-ЗАМЕЩЕННЫЕ СПИРО[ИНДОЛИН-НАФТОПИРАНЫ] И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФОТООБРАТИМЫХ КОМПЛЕКСООБРАЗОВАТЕЛЕЙ | 2011 |
|
RU2458926C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНОГО ИНДОЛИНОСПИРОПИРАНА | 2001 |
|
RU2293738C2 |
| 1-ЗАМЕЩЕННЫЕ-3-[(1Е)-1-АЛКЕНИЛ]-4-(5-АЛКОКСИ-1,2-ДИМЕТИЛ-1Н-ИНДОЛ-3-ИЛ)-1Н-ПИРРОЛ-2,5-ДИОНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФЛУОРЕСЦИРУЮЩИХ ФОТОХРОМОВ | 2008 |
|
RU2397979C2 |
| 4-ЗАМЕЩЕННЫЕ-3-(1-АЛКИЛ-2-ХЛОР-1Н-ИНДОЛ-3-ИЛ)ФУРАН-2,5-ДИОНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ДЛЯ ФОТОХИМИЧЕСКОГО ГЕНЕРИРОВАНИЯ СТАБИЛЬНЫХ ФЛУОРЕСЦИРУЮЩИХ СОЕДИНЕНИЙ И (4,5-ЗАМЕЩЕННЫЕ-6-АЛКИЛ-1Н-ФУРО[3,4-c]КАРБАЗОЛ-1,3(6Н)-ДИОНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФЛУОРОФОРОВ | 2009 |
|
RU2396267C1 |
Изобретение относится к новым соединениям в ряду спиро[бензопиран-индолинов]. Описан 6-(1,3-бензимидазол-2-ил)-7-гидрокси-замещенный спиро[бензопиран-индолин] общей формулы

где R1 - C1-C6 алкил, R2 - H, галоген. Технический результат - получение нового соединения, содержащего спироциклический фрагмент, обладающего интенсивной флуоресценцией с аномально высоким стоксовым сдвигом и проявляющего фотохромные свойства. 1 табл., 2 пр.
6-(1,3-бензимидазол-2-ил)-7-гидрокси-замещенные спиро[бензопиран-индолины] общей формулы
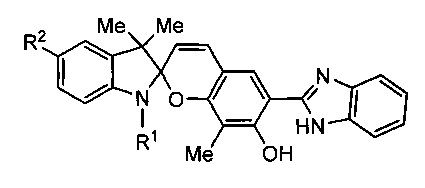
где R1 - C1-C6 алкил, R2 - H, галоген.
| WO 2009141236 A1, 26.11.2009 | |||
| US 5942532 A, 24.08.1999 | |||
| Photophysical and redox properties of dinuclear Ru and Os polypyridyl complexes with incorporated photostable spiropyran bridge | |||
| Jukes, Ron T | |||
| F., et al., Inorganic Chemistry, 2009 48(4) 1711-1721 | |||
| Спиропираны 2-оксаинданового ряда, проявляющие фотохромные свойства, и способ их получения | 1974 |
|
SU518491A1 |
Авторы
Даты
2017-01-10—Публикация
2015-11-16—Подача