Изобретение относится к новому производному в ряду индолиновых спиропиранов, а именно к неописанному ранее 1,3,3-триметил-5-метокси-6'-бром-8'-[(Е)-2-(1'',3'',3''-триметил-5-метокси-3Н-индолий-2''-ил)винил]-спиро[индолин-2,2'-2Н-хромен] йодиду формулы 1:
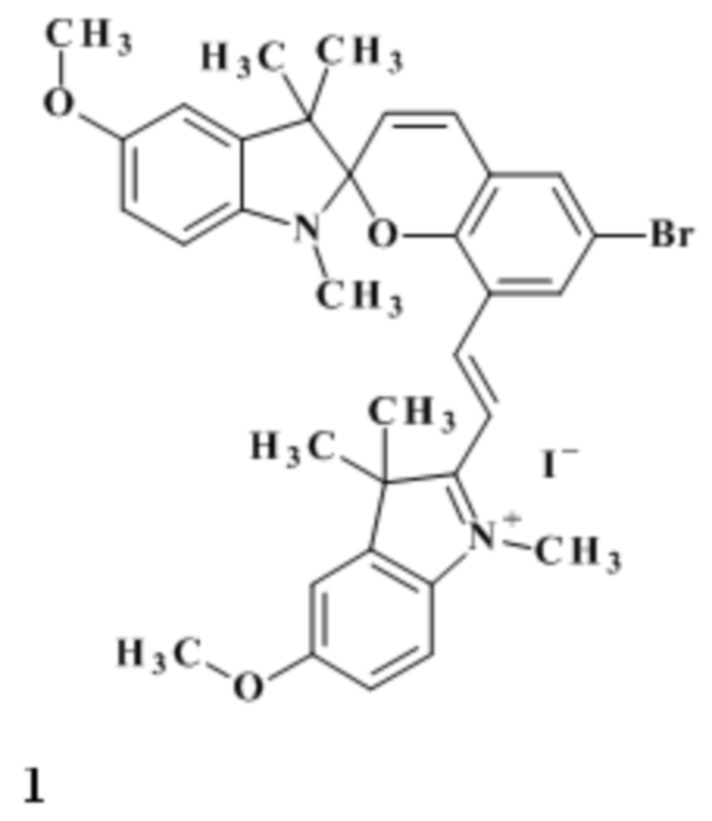
Соединение обладает фотохромными свойствами и может быть использовано при создании органических магнитов с управляемыми характеристиками в качестве катионной функциональной составляющей со сложными металло-оксалатными анионами, а также в системах записи-чтения информации.
Спиропираны являются одним из наиболее перспективных классов органических фотохромных соединений. Это связано с высокими квантовыми выходами фотоизомеризации, сравнительной легкостью синтеза и модификации структуры молекулы спиропиранов, позволяющей осуществлять тонкую настройку фотодинамических характеристик, а также существенным различием в физико-химических, прежде всего спектральных свойствах исходной и фотоиндуцированной формы. Фотохромные превращения спиропиранов представляют собой большой интерес, так как материалы на их основе могут быть использованы для записи и хранения информации. Фотохромные превращения нейтральных спиропиранов, связанны с разрывом связи Сспиро-О и последующей изомеризацией молекулы, что требуют достаточного свободного пространства и поэтому в кристаллах затруднены в силу плотной упаковки молекул в решётке. Как правило, нейтральные спиропираны в монокристаллах и кристаллических порошках не проявляют фотоокрашивания, обусловленного образованием открытых мероцианиновых структур.
В солевых спироциклических системах, содержащих объемные анионы, рыхлая упаковка кристаллической решетки не создает стерических затруднений для фотоизомеризации закрытой формы спиропирана в соответствующие фотоиндуцированные мероцианиновые изомеры. Таким образом, переход к катионным производным спиропиранов позволит инкорпорировать их в солевые структуры, кристаллы которых, за счет наличия противоионов, предоставляют больше пространства для успешного протекания фотоизомеризации.
Получение таких солевых систем со сложным плоскими двумерными метало-оксалатными анионами является эффективной методологией создания перспективных органических магнитов с управляемыми характеристиками. В настоящее время актуальным направлением в химии «умных» материалов, обладающих переключаемыми свойствами, является разработка новых гибридных полифункциональных материалов для молекулярной электроники. Кристаллы молекулярных магнетиков должны объединять в себе две функциональные подрешетки, одна из которых представлена анионами моно- и биметаллических оксалатных комплексов, являющихся эффективными мостиковыми лигандами для переноса магнитных взаимодействий между ионами металлов и используются в качестве магнитной подрешетки. В качестве катионной функциональной составляющей в молекулярный магнетик могут быть инкорпорированы катионные формы спиропиранов. В подобной системе спиросоединение действует как фотохимический молекулярный переключатель, возмущающий магнитную подрешетку.
Все современные системы записи/чтения/хранения информации работают в ближнем ИК-диапазоне.
Для возможного использования в таких системах фотохромных спиропиранов необходимо, чтобы максимумы поглощения открытой формы находился в области работы лазера. Так, например, распространенный гелий-неоновый лазер, используемый для считывания штрих-кодов, имеет рабочую длину волны 632,8 нм.
Актуальной проблемой современной химии функциональных материалов является синтез новых солевых производных спиропиранов и изучение их свойств, что позволит отработать подходы к получению новых магнитных материалов, потенциально обладающих способностью к фотопереключению в твердой фазе.
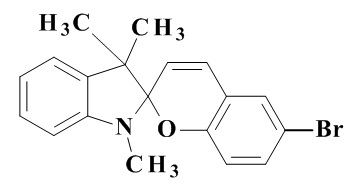
Известен 8'-метокси-1,3,3-триметил-спиро-индолино-2,2'-2Н-хромен 2, проявляющий фотохромные свойства (S. Torres R., A. L. Vazquez S., and E. A. Gonzdez S. Synthetic Communications. 1995, Vol. 25, № 1, 105 - 110).
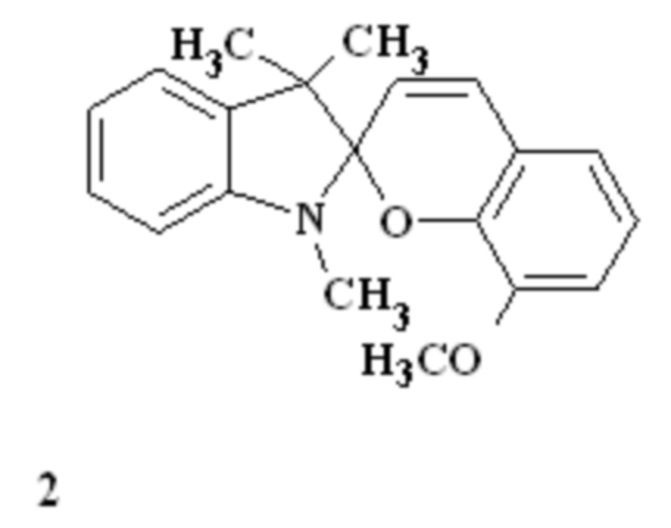
Однако максимум поглощения его открытой формы находится в недостаточно длинноволновой области, не позволяющей использовать его в системах для записи/чтения/хранения информации.
Известен 6'-бром-1,3,3,-триметил-спиро индолино-2,2'-2Н-хромен формулы 3, проявляющий фотохромные свойства с максимумом длинноволновой полосы поглощения при 408 нм, что недостаточно для целей практического применения (Silvia Torres R. , Ana L. VAzquez S., and Eduardo A. Gonzdez S. Novel syntheses of spiropyran photochromatic compounds using ultrasound Synthetic communications, 25(1), 105-1 10 (1995).
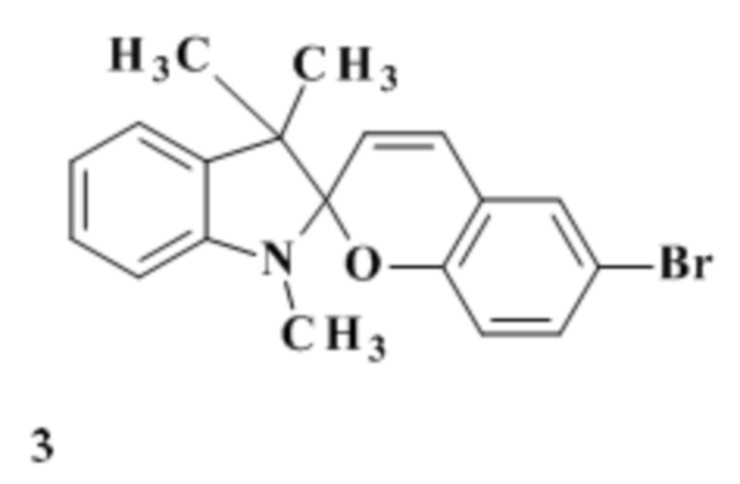
Известен 1,3,3,6'-тетраметил-8' [(Е)-2-(1'',3'',3''-триметилиндолий-2''- ил)винил]спиро [индолин-2,2' 2H-хромен] перхлорат 4
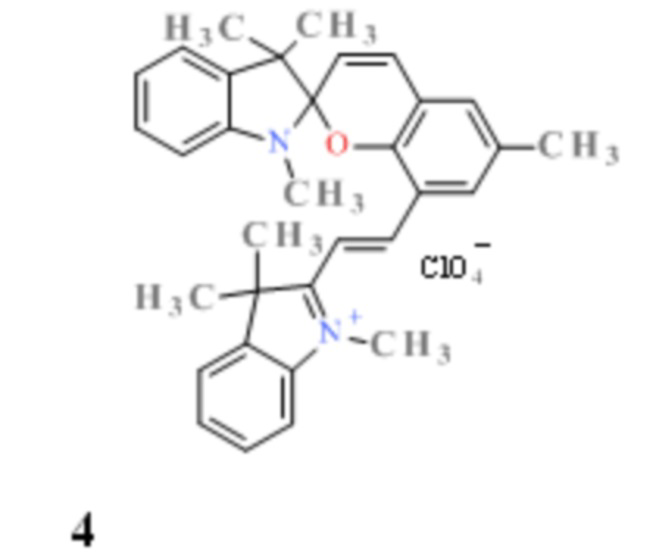 (Pugachev, A.D., Ozhogin, I.V., Lukyanova, M.B., Lukyanov, B.S., Kozlenko, A.S., Rostovtseva, I.A., Makarova, N.I., Tkachev, V.V., Aldoshin, S.M., Metelitsa, A.V. Synthesis, structure and photochromic properties of indoline spiropyrans with electron-withdrawing substituents) Journal of Molecular Structure, 2021 V. 1229, Article 129615). Фотоиндуцированная форма его находится в том же спектральном диапазоне (708 нм для соединения 1 и 730 для соединений 4), однако он обладает низким временем жизни фотоокрашенной формы (8.4 сек).
(Pugachev, A.D., Ozhogin, I.V., Lukyanova, M.B., Lukyanov, B.S., Kozlenko, A.S., Rostovtseva, I.A., Makarova, N.I., Tkachev, V.V., Aldoshin, S.M., Metelitsa, A.V. Synthesis, structure and photochromic properties of indoline spiropyrans with electron-withdrawing substituents) Journal of Molecular Structure, 2021 V. 1229, Article 129615). Фотоиндуцированная форма его находится в том же спектральном диапазоне (708 нм для соединения 1 и 730 для соединений 4), однако он обладает низким временем жизни фотоокрашенной формы (8.4 сек).
Наиболее близким по структуре и достигаемому результату является 1,3,3-триметил-6'-бром-8' [(Е)-2-(1'',3'',3''-триметилиндолий-2''- ил)винил]спиро [индолин-2,2' 2H-хромен] перхлорат 5
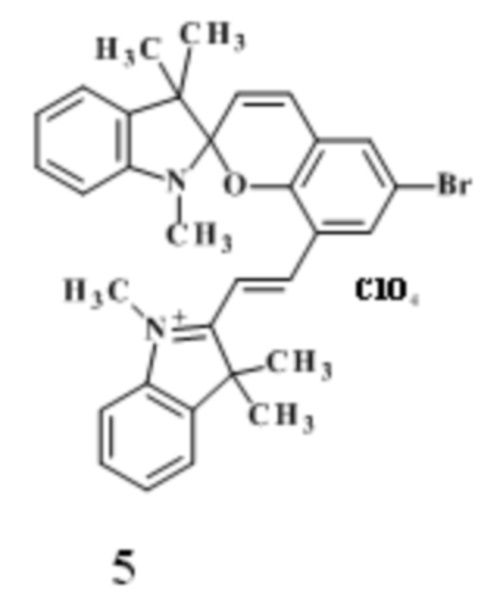
(Artem D. Pugachev, Ilya V. Ozhogin, Maria B. Lukyanova, Boris S. Lukyanov, Irina A. Rostovtseva, Igor V. Dorogan, Nadezhda I. Makarova, Valery V. Tkachev, Anatoly V. Metelitsa, Sergey M. Aldoshin Visible to near-IR molecular switches based on photochromic indoline spiropyrans with a conjugated cationic fragment. Spectrochimica Acta Part A. Molecular and Biomolecular Spectroscopy. 2020. V. 230. Article 118041). Фотоиндуцированная форма его находятся в том же спектральном диапазоне (708 нм для соединения 1 и для соединений 5), однако он обладают низким временем жизни фотоокрашенной формы (238.7 сек).
Задачей изобретения является получение нового фотохромного катиона, который может быть инкорпорирован в анионную магнитную подрешетку в качестве фотохимического молекулярного переключателя.
Техническим результатом изобретения является увеличение времени жизни открытой формы спиропирана в ряду 1,3,3-триметилспиро-индолино-2,2'-[2Н]хроменов с заместителями в бензопирановом фрагменте.
Технический результат достигается соединением 1.
Изобретение удовлетворяет критерию изобретательского уровня, так как среди спиропиранов индолинового ряда не известна взаимосвязь между строением сложного заместителя в бензоядре 2Н-хроменового фрагмента молекулы и их фотохромными свойствами.
Соединение 1 получают исходя из иодида 1,2,3,3-тетраметил-5-метокси-индолилия и 4-бром-2,6-диформил-фенола.
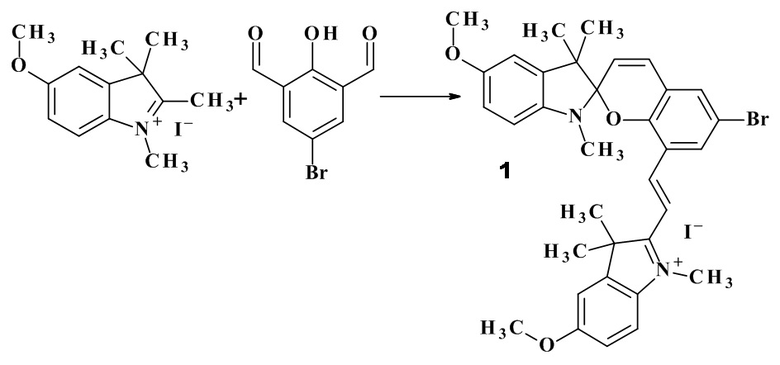
Ниже приведён пример получения соединения 1.
Пример 1. 1,3,3-триметил-5-метокси-6'-бром-8'-[(Е)-2-(1'',3'',3''-триметил-5-метокси-3Н-индолий-2''-ил)винил]-спиро[индолин-2,2'-2Н-хромен] йодид.
В 10 мл изопропилового спирта растворяют 0.229 г (0.001 моль) 2,6-диформил-4-бромфенола и 0.662 г (0.002 моль) 1,2,3,3-тетраметил-5-метокси-индолия, по каплям добавляют 0.1 мл триэтиламина. Кипятят с обратным холодильником 3 часа. Осадок перекристаллизовывают из этанола, промывают водой и холодным этанолом. Получают темно бордовый порошок (0.275 г), выход 37.8 %, Т пл. 242-243°С.
ИК-спектр, см-1:1651, 1604 (νС=С), 1309 (νСар-N), 1074 (?Cl=O в ClO4-), 928 (νСспиро-O).
Спектр ЯМР 1H (CDCl3) δ, м.д.: 7.96 (d, J = 2.3 Hz, 1H, H-7′), 7.86 (d, J = 16.5 Hz, 1H, H-10′′), 7.63 (d, J = 8.8 Hz, 1H, H-7′′), 7.38 (d, J = 16.5 Hz, 1H, H-9′′), 7.32 (d, J = 2.2 Hz, 1H, H-5′), 7.01 (dd, J = 8.8, 2.4 Hz, 1H, H-6′′), 6.93 (d, J = 2.4 Hz, 1H, H-4′′), 6.85 (d, J = 10.3 Hz, 1H, H-4′), 6.79 (dd, J = 8.3, 2.5 Hz, 1H, H-6), 6.73 (d, J = 2.5 Hz, 1H, H-4), 6.52 (d, J = 8.4 Hz, 1H, H-7), 5.86 (d, J = 10.3 Hz, 1H, H-3′), 3.90 (s, 3H, N+-CH3), 3.87 (s, 3H, O-CH3), 3.82 (s, 3H, O-CH3), 2.69 (s, 3H, N-CH3), 1.42 (s, 3H, гем-С-CH3), 1.39 (s, 3H, гем-С-CH3), 1.25 (s, 3H гем-С-CH3), 1.19 (s, 3H, гем-С-CH3).
Спектр ЯМР 13C (CDCl3) δ, м.д.: 179.93 (С-2′′), 161.71 (С-8′′а), 154.52 (С-5), 154.24 (С-9′), 145.45 (С-5′′), 145.20 (C-10′′), 141.92 (С-8), 137.87 (С-8), 134.85 (С-8′′), 134.04 (C-5′), 133.33 (C-7′), 128.52 (C-4′), 122.10 (С-6′), 121.71 (С-8′), 121.21 (C-3′), 116.77 (C-7′′), 114.63 (С-9′а), 113.95 (C-6′′), 113.11 (C-9′′), 112.07 (C-6), 109.66 (C-4), 108.87 (C-4′′), 108.04 (C-2,2′), 107.97 (C-7), 56.35 (O-CH3), 56.32 (O-CH3), 52.56 (C-3′′), 52.06 (C-3), 36.47 (N+-CH3), 29.67 (N-CH3), 26.79 (гем-С-CH3), 26.64 (гем-С-CH3), 25.38 (гем-С-CH3), 20.06 (гем-С-CH3).
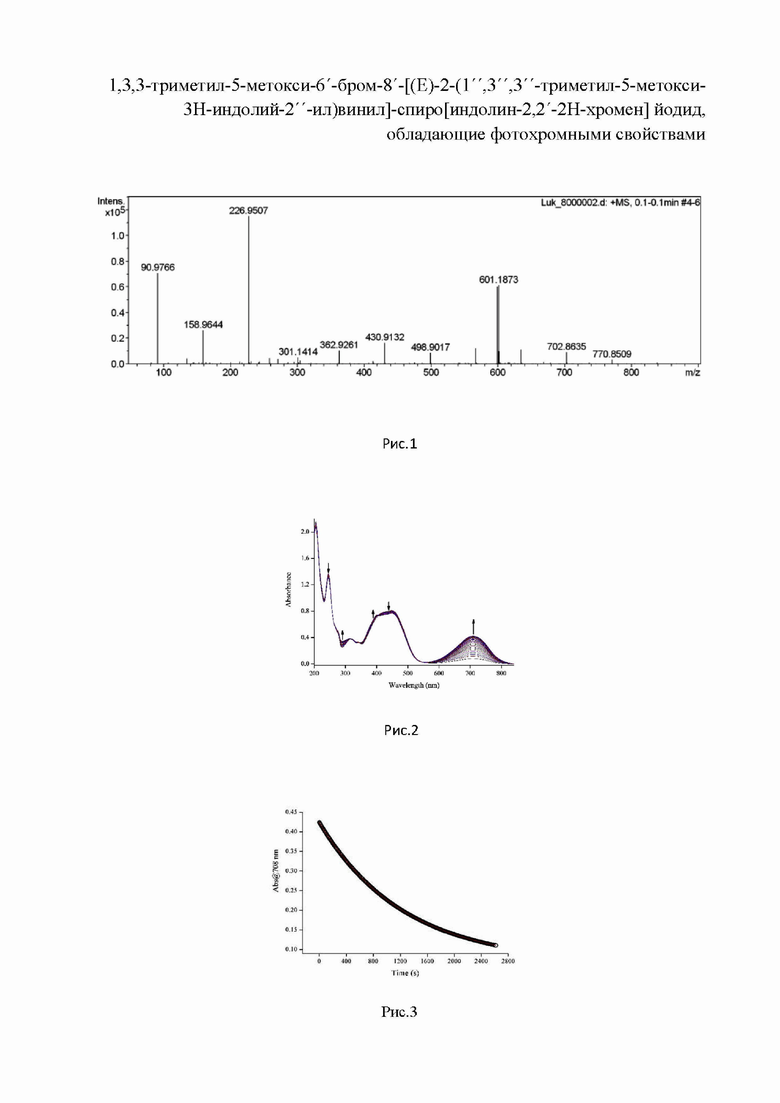
На рис. 1 приведён масс-спектр соединения 1. Масс-спектр: HRMS (ESI): m/z [M] + calcd для C34H36BrN2O3 : 599.1904; найдено 599.1888
Электронные спектры поглощения растворов исследуемого соединения до и после облучения регистрировались на спектрофотометре Cary 100 Scan. Для приготовления раствора использовали ацетонитрил («Aldrich») спектральной степени чистоты. На рис. 2 приведены изменения в спектрах поглощения спиропирана 1 при облучении УФ-светом (λобл = 365 нм, Δt = 30 c) в ацетонитриле, C = 3.3⋅10-5 M, Т = 293 K. На рис. 3 приведена кинетическая кривая термического процесса рециклизации в максимуме мероцианинового изомера спиропирана 1 в ацетонитриле, Т = 293 K. Точки - экспериментальные данные, линия - результат аппроксимации моно-экспоненциальной функции
Спектральные и кинетические характеристики соединения 1 приведены в таблице 1. Там же приведены результаты исследований для ближайших аналогов.
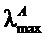 , нм
, нм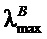 , нм
, нм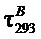 , с
, с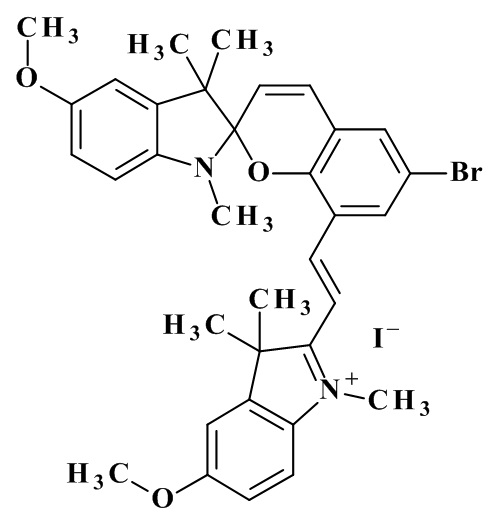
1
318
321пл
426пл
450 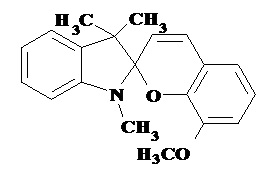
2
3
256
314пл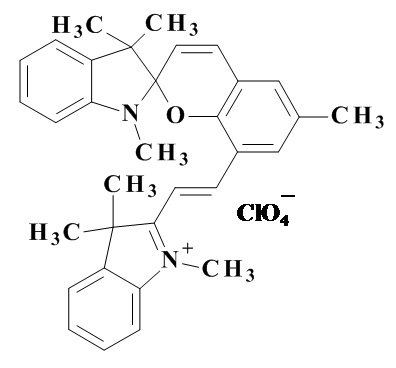
4
273пл
289пл
388
451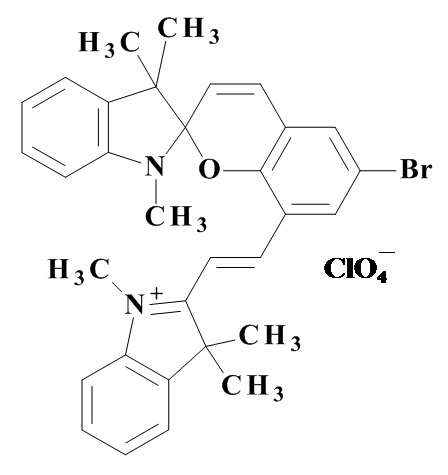
5
245
276пл
296
379
444пл
Как видно, время жизни соединения 1 существенно превышает этот показатель аналогов.
| название | год | авторы | номер документа |
|---|---|---|---|
| Перхлораты 1,3,3-триметилспиро[хромен-2,2'-индолина], обладающие фотохромными свойствами | 2016 |
|
RU2627358C1 |
| 5-ФОРМИЛ-ЗАМЕЩЕННЫЕ ИНДОЛИНОВЫЕ СПИРОБЕНЗОПИРАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2358977C1 |
| 6-(1,3-бензимидазол-2-ил)-7-гидрокси-замещенные спиро[бензопиран-индолины], обладающие флуоресценцией | 2015 |
|
RU2605984C1 |
| ФОТОХРОМНЫЕ ПРОИЗВОДНЫЕ 5'-ВИНИЛ-6-НИТРО-СПИРОБЕНЗОПИРАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2458927C1 |
| Фотохромные производные 5'-гидроксиметил-6-нитро-1',3',3'-триметилспиро[2Н-1-бензопиран-2,2'-индолина] | 2019 |
|
RU2694904C1 |
| Фотосенсибилизатор | 2023 |
|
RU2809967C1 |
| (E)-N'-((замещённые-3',3'-диметил-3'H-спиро[хромен-2,1'-изобензофуран]-8-ил)метилен)изоникотиногидразиды,обладающие противотуберкулезной активностью, и способ их получения | 2024 |
|
RU2824628C1 |
| СВЕТОЧУВСТВИТЕЛЬНАЯ КОМПОЗИЦИЯ ДЛЯ СВЕТОФИЛЬТРОВ ЗАЩИТНО-ПРОФИЛАКТИЧЕСКОГО НАЗНАЧЕНИЯ | 2011 |
|
RU2466173C1 |
| Способ получения 3 @ ,3 @ -диметил-6,8-динитро-1 @ -пропилспиро [2Н-1-бензопиран-2,2 @ -индолина] | 1988 |
|
SU1608188A1 |
| Способ получения 1,3,3-триметил5,6 , -динитроспиро-(2 , н,1 , -бензопиран) -2,2 , -индолина | 1973 |
|
SU455955A1 |
Изобретение относится к области органической химии, а именно к новому производному в ряду индолиновых спиропиранов. Представлен 1,3,3-триметил-5-метокси-6'-бром-8'-[(Е)-2-(1'',3'',3''-триметил-5-метокси-3Н-индолий-2''-ил)винил]-спиро[индолин-2,2'-2Н-хромен] йодид формулы 1. Изобретение обеспечивает увеличение времени жизни открытой формы спиропирана в ряду 1,3,3-триметилспиро-индолино-2,2'-[2Н]хроменов с заместителями в бензопирановом фрагменте и может быть инкорпорировано в анионную магнитную подрешетку в качестве фотохимического молекулярного переключателя. 1 з.п. ф-лы, 3 ил., 1 табл., 1 пр.
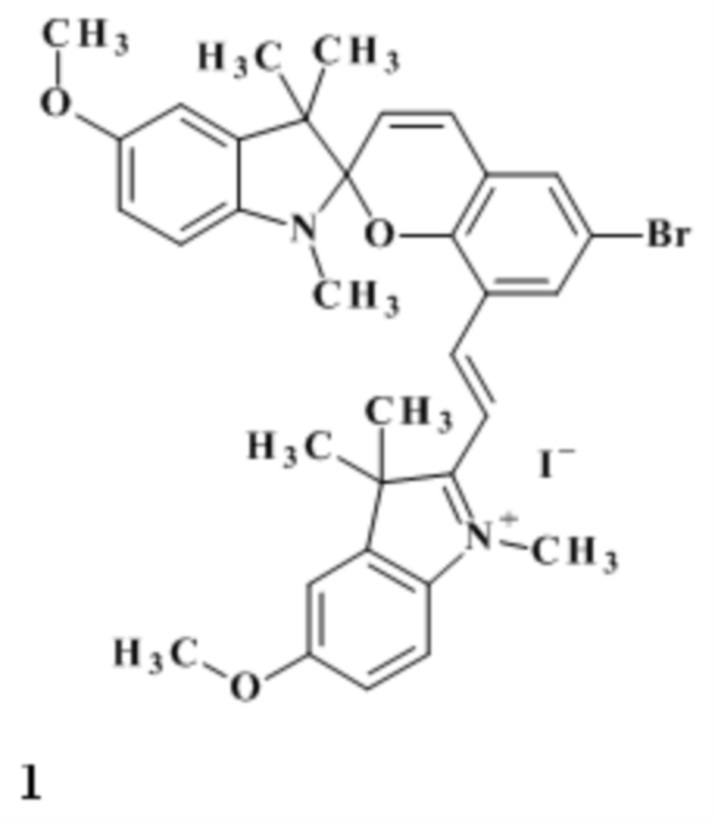
1. 1,3,3-триметил-5-метокси-6´-бром-8´-[(Е)-2-(1´´,3´´,3´´-триметил-5-метокси-3Н-индолий-2´´-ил)винил]-спиро[индолин-2,2´-2Н-хромен]йодид формулы 1
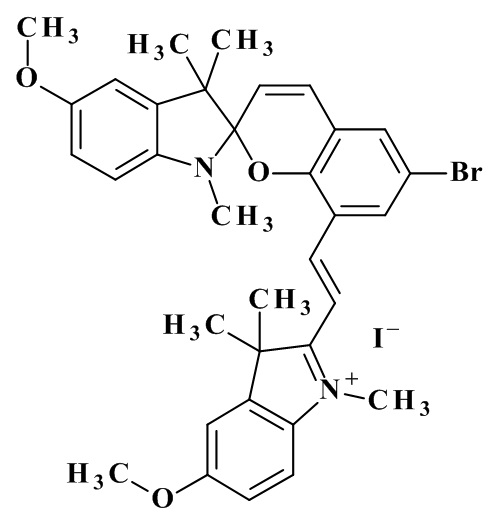 .
.
2. 1,3,3-триметил-5-метокси-6´-бром-8´-[(Е)-2-(1´´,3´´,3´´-триметил-5-метокси-3Н-индолий-2´´-ил)винил]-спиро[индолин-2,2´-2Н-хромен] йодид по п. 1, обладающий фотохромными свойствами.
| Перхлораты 1,3,3-триметилспиро[хромен-2,2'-индолина], обладающие фотохромными свойствами | 2016 |
|
RU2627358C1 |
| ФОТОХРОМНЫЕ ПРОИЗВОДНЫЕ 5'-ВИНИЛ-6-НИТРО-СПИРОБЕНЗОПИРАНА И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2011 |
|
RU2458927C1 |
| 5-ФОРМИЛ-ЗАМЕЩЕННЫЕ ИНДОЛИНОВЫЕ СПИРОБЕНЗОПИРАНЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2008 |
|
RU2358977C1 |
| PUGACHEV A.D et al | |||
| Visible to near-IR molecular switches based on photochromic indoline spiropyrans with a conjugated cationic fragment | |||
| Spectrochimica Acta Part A | |||
| Molecular and Biomolecular Spectroscopy, 2020, vol | |||
| Канальная печь-сушильня | 1920 |
|
SU230A1 |
| Приспособление для отделения листов от стопки | 1924 |
|
SU1386A1 |
| YONGKANG YUE et al | |||
| A Dual | |||
Авторы
Даты
2022-12-27—Публикация
2022-04-08—Подача