ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится к связанным со стрептавидином магнитным частицам и к способу их изготовления, к связанным с белком магнитным частицам, изготовленным с использованием связанных со стрептавидином магнитных частиц, и к способу их изготовления; к способу измерения измеряемого компонента и к реагенту для измерения измеряемого компонента.
УРОВЕНЬ ТЕХНИКИ
В диагностических материалах магнитные частицы часто используют как твердофазные носители для обнаружения измеряемых веществ, таких как гормоны, онкомаркеры и маркеры инфекций. В таких измерительных системах антитела, антигены и т.п. (первичные зонды) присоединены к магнитным частицам, и они связаны с измеряемыми веществами в образце, и, кроме того, измеряемые вещества дополнительно связаны с вторичными зондами, маркированными флуоресцентными веществами, хемилюминесцентными субстратами, ферментами и т.п., и измеряемые вещества определяются качественно или количественно.
В последнее время существует необходимость повышения чувствительности анализов для раннего обнаружения заболеваний, увеличения точности анализов, применения высокочувствительных маркеров в следовых количествах и т.п. Существует также необходимость повышения скорости анализов вследствие высокой производительности обслуживающих учреждений аналитических центров, скорого получения результатов анализов, предназначенных для оказания услуг пациентам, и т.п.
В качестве средства обеспечения повышенной чувствительности и скорости измерительных систем с использованием таких магнитных частиц часто используют способ реакции первичного зонда и вторичного зонда в жидкой фазе и последующего присоединения их к магнитным частицам. Представительным примером является способ, в котором маркированный биотином первичный зонд, изготовленный присоединением биотина к первичному зонду, реагирует с измеряемым компонентом в образце и вторичным зондом, образуя комплекс, включающий маркированный биотином первичный зонд, измеряемый компонент и вторичный зонд, и после этого связанные с авидином магнитные частицы могут воздействовать на комплекс, присоединяя комплекс к магнитной частице посредством взаимодействия авидина и биотина.
Что касается таких связанных с авидином магнитных частиц, более полезными являются связанные со стрептавидином магнитные частицы с использованием стрептавидина, который имеет такие же свойства, как авидин. Как и авидин, стрептавидин очень прочно соединяется с биотином и обладает свойством более высокой устойчивости к денатурации, чем авидин. Кроме того, авидин имеет изоэлектрическую точку в основной области, в то время как изоэлектрическая точка стрептавидина находится в слабокислой или нейтральной области; таким образом, известно, что стрептавидин обладает преимуществом проявления очень слабого неспецифического связывания с другими белками. Связанные со стрептавидином магнитные частицы с использованием этого стрептавидина применяются для многих целей.
Однако существует ограничение количества стрептавидина, которое можно присоединять к магнитным частицам, и, таким образом, необходимо использовать большое число связанных со стрептавидином магнитных частиц, чтобы обеспечивать способность связывания биотина, требуемую для реагента в каждом анализе, что приводит к проблемам, таким как высокая стоимость изготовления. Кроме того, существуют следующие проблемы при измерениях, в которых используют связанные со стрептавидином магнитные частицы:
(1) поскольку магнитные частицы осаждаются в статических условиях, их необходимо диспергировать в процессе использования, и для их диспергирования требуются затраты времени и сил в случае высокого содержания частиц;
(2) когда присутствует высокое содержание частиц, эти частицы занимают большой объем, когда их переносят на одну сторону контейнера, используя магнит, и это приводит к снижению эффективности вымывания реакционного раствора, задержанного внутри них в процессе разделения связанных и свободных частиц и промывания; и
(3) мутность, вызванная цветом самих магнитных частиц, увеличивается, когда существует большое количество магнитных частиц в процессе обнаружения измеряемого компонента, и, например, при обнаружении посредством хемилюминесценции и флуоресценции чувствительность уменьшается вследствие оптического экранирования.
В условиях, где количество связанных со стрептавидином магнитных частиц ограничено созданием минимально требуемой способности связывания биотина, существует возможность, что конкуренция с биотином (витамином H), который присутствует в образце, ингибирует реакцию для измерения, и можно не получить точные значения анализов. Биотин можно принимать в качестве добавки или вводить в качестве лекарственного средства, и такие проблемы часто отмечаются.
До настоящего времени было предложено несколько способов в качестве средства решения данной проблемы. Один из них представляет собой способ уменьшения размера магнитных частиц для увеличения удельной поверхности этих частиц. Однако уменьшение размера частиц также имеет свои проблемы. Например, время, расходуемое на сбор частиц с помощью магнита, может значительно увеличиваться, и большее число частиц может уноситься в процессе осуществления подачи и удаления промывочного раствора на стадии промывания. Патентный документ 1 описывает, в качестве способа отделения вещества, подлежащего обнаружению в образце, способ сбора магнитных частиц из водного раствора путем использования магнитных частиц, модифицированных на поверхности чувствительными к температуре полимерами, причем даже магнитные частицы, у которых средний размер составляет от 50 нм до 1000 нм, можно собирать посредством агрегации частиц на чувствительных к температуре полимерах. Хотя такие частицы обладают преимуществами в реакции вследствие уменьшения размера магнитных частиц, они проявляют неспецифическую адсорбцию вследствие покрытия поверхности частиц чувствительными к температуре полимерами, и для них требуется предпринимать меры по изменению условий на особые условия для агрегации.
Кроме того, предложены также способы изготовления пористых нерастворимых носителей для увеличения их удельной поверхности. Например, патентный документ 2 описывает способ химического образования пористого слоя на внешнем слое магнитных частиц. Согласно данному способу, хотя связующая способность в расчете на единичную площадь поверхности увеличивается в иммунологических реакциях между антигенами и антителами, а также в гибридизации между ДНК или между ДНК и РНК, эффективность реакций в порах является неудовлетворительной, и таким образом оказывается затруднительным достижение предполагаемой производительности.
ДОКУМЕНТЫ ПРЕДШЕСТВУЮЩЕГО УРОВНЯ ТЕХНИКИ
Патентные документы
Патентный документ 1 - публикация японской патентной заявки Kokai № (JP-A) 2009-28711 (нерассмотренная опубликованная японская патентная заявка)
Патентный документ 2 - публикация японской патентной заявки Kokai № (JP-A) 2006-307126
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Проблемы, решаемые изобретением
Задача настоящего изобретения заключается в том, чтобы предложить связанные со стрептавидином магнитные частицы, имеющие высокую способность связывания биотина, и способ их изготовления. Кроме того, еще одна задача настоящего изобретения заключается в том, чтобы предложить связанные с белком магнитные частицы, изготовленные с использованием связанных со стрептавидином магнитных частиц, которые имеют высокую способность связывания биотина, и способ их изготовления, а также способ измерения измеряемого компонента и реагент для измерения измеряемого компонента.
Средства решения проблем
Авторы настоящего изобретения осуществили назначенные исследования, чтобы решить данные проблемы, и обнаружили, что связанные со стрептавидином магнитные частицы, имеющие высокую способность связывания биотина, можно получать в реакции магнитных частиц со стрептавидином и глутаральдегидом посредством введения глутаральдегида в присутствии стрептавидина в суспензию, содержащую магнитные частицы, на поверхности которых находятся аминогруппы; и авторы настоящего изобретения выполнили настоящее изобретение. Более конкретно, настоящее изобретение относится к представленным ниже пп. [1]-[12]:
[1] связанные со стрептавидином магнитные частицы, имеющие структуру, в которой молекулы стрептавидина сшиты друг с другом на магнитной частице;
[2] связанные со стрептавидином магнитные частицы по п. [1], которые изготавливают способом, включающим следующие стадии:
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы; и
(2) реакция магнитных частиц со стрептавидином и глутаральдегидом путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1);
[3] связанные со стрептавидином магнитные частицы по п. [2], которые изготавливают способом, дополнительно включающим следующую стадию (3):
(3) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (2), с восстановителем;
[4] связанные с белком магнитные частицы, которые изготавливают, используя связанные со стрептавидином магнитные частицы по любому из пп. [1]-[3] и биотинилированный белок;
[5] способ измерения измеряемого компонента в образце, в котором используют связанные с белком магнитные частицы по п. [4];
[6] способ измерения измеряемого компонента в образце, в котором используют связанные со стрептавидином магнитные частицы по любому из пп. [1]-[3] и биотинилированный белок;
[7] реагент для измерения измеряемого компонента в образце, который включает связанные с белком магнитные частицы по п. [4];
[8] реагент для измерения измеряемого компонента в образце, который включает связанные со стрептавидином магнитные частицы по любому из пп. [1]-[3] и биотинилированный белок;
[9] способ изготовления связанные со стрептавидином магнитные частицы, который включает следующие стадии:
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы; и
(2) реакция магнитных частиц со стрептавидином и глутаральдегидом путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1);
[10] способ изготовления по п. [9], дополнительно включающий следующую стадию (3):
(3) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (2), с восстановителем;
[11] способ изготовления связанных с белком магнитных частиц, который включает следующие стадии:
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы;
(2) изготовление связанных со стрептавидином магнитных частиц путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1); и
(3) реакция связанных со стрептавидином частиц, изготовленных на стадии (2), с биотинилированным белком; и
[12] способ изготовления связанных с белком магнитных частиц, который включает следующие стадии:
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы;
(2) изготовление связанных со стрептавидином магнитных частиц путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1);
(3) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (2), с восстановителем (1); и
(4) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (3), с биотинилированным белком.
ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
Настоящее изобретение предлагает связанные со стрептавидином магнитные частицы, имеющие высокую способность связывания биотина, и способ их изготовления, связанные с белком магнитные частицы, изготовленные с использованием связанных со стрептавидином магнитных частиц, и способ их изготовления, способ измерения измеряемого компонента и реагент для измерения измеряемого компонента. Связанные со стрептавидином магнитные частицы и связанные с белком магнитные частицы, изготовленные способом изготовления согласно настоящему изобретению, а также способ измерения измеряемого компонента и реагент для измерения измеряемого компонента согласно настоящему изобретению можно использовать в клинической диагностике.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг.1 представляет электрофоретический профиль SDS-PAGE, показывающий структуры молекул стрептавидина на магнитных частицах связанных со стрептавидином магнитных частиц согласно настоящему изобретению и имеющихся в продаже связанных со стрептавидином магнитных частиц. Дорожки представляют собой следующие: дорожка 1 - молекулярные маркеры; дорожка 2 - стрептавидин; дорожка 3 - связанные со стрептавидином магнитные частицы, имеющие способность связывания биотина на уровне 2,61 пмоль/мм2; дорожка 4 - связанные со стрептавидином магнитные частицы, имеющие способность связывания биотина на уровне 4,95 пмоль/мм2; дорожка 5 - связанные со стрептавидином магнитные частицы, имеющие способность связывания биотина на уровне 6,76 пмоль/мм2; дорожка 6 - имеющиеся в продаже связанные со стрептавидином магнитные частицы Dynabeads T1 (производитель Dynal); и дорожка 7 - имеющиеся в продаже связанные со стрептавидином магнитные частицы BE-M08/10 (производитель Merck). Полоска A представляет мономеры, полоска B представляет димеры, полоска C представляет тримеры, полоска D представляет тетрамеры, и полоска E представляет сшитые структуры более высокого порядка.
Фиг.2 представляет фотографии, показывающие диспергируемость связанных со стрептавидином магнитных частиц согласно настоящему изобретению. Верхняя фотография представляет статическое состояние связанных со стрептавидином магнитных частиц, и нижняя фотография представляет диспергированное состояние связанных со стрептавидином магнитных частиц после перемешивания посредством 25-кратного переворачивания.
СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
1. Связанные со стрептавидином магнитные частицы
Связанные со стрептавидином магнитные частицы согласно настоящему изобретению имеют структуру, в которой молекулы стрептавидина сшиты друг с другом на магнитных частицах. Молекулы стрептавидина образуют тетрамерную структуру, в которой мономеры соединены друг с другом посредством нековалентных связей. В связанных со стрептавидином магнитных частицах согласно настоящему изобретению эти молекулы стрептавидина, имеющие тетрамерную структуру, ковалентно соединены друг с другом посредством глутаральдегида, образуя сшитую структуру на магнитных частицах. Молекулы стрептавидина присоединены к аминогруппам магнитных частиц посредством глутаральдегида. Более конкретно, часть молекул стрептавидина, имеющих тетрамерную структуру, присоединена к аминогруппам магнитных частиц посредством глутаральдегида. Сшитую структуру стрептавидина можно подтвердить способом электрофореза в полиакриламидном геле с додецилсульфатом натрия (SDS-PAGE), гельпроникающей жидкостной хроматографии высокого разрешения (HPLC), например, помещая связанные со стрептавидином магнитные частицы в раствор 1% SDS и подвергая их нагреванию при 60°C в течение одного часа для разрушения связей между фрагментами молекул стрептавидина, которые присоединены к магнитным частицам. Способ SDS-PAGE представляет собой способ разделения белков в зависимости от их размера посредством электрофореза и является способом разделения и идентификации белков на основании полученного электрофоретического профиля путем денатурации образца с использованием SDS и последующего воздействия электрофореза в полиакриламидном геле на денатурированный белок. Способ SDS-PAGE не ограничивается определенным образом при том условии, что он представляет собой способ, которым можно подтверждать сшитые структуры стрептавидина, и его примером является способ, описанный в работе «Baio Jikken Irasutoreiteddo (Bio-experiment Illustrated, Иллюстрированные биологические эксперименты) 5» (Cell Engineering Supplement, Приложение клеточной инженерии, Shujunsha).
В процессе SDS-PAGE молекулы стрептавидина, имеющие тетрамерную структуру, теряют свою тетрамерную структуру посредством денатурирующей обработки в присутствии SDS. Если молекулы стрептавидина на магнитных частицах не присутствуют в форме сшитых структур, продукт разложения, который можно получать посредством денатурирующей обработки в присутствии SDS, будет представлять собой исключительно образующиеся из стрептавидина мономеры. С другой стороны, если молекулы стрептавидина на магнитных частицах присутствуют в форме сшитых структур, денатурирующая обработка в присутствии SDS должна производить, помимо образующихся из стрептавидина мономеров, также димеры, тримеры и олигомеры более высокого порядка, которые присутствуют в сшитых структурах молекул стрептавидина. Таким образом, в том случае, если в процессе SDS-PAGE наблюдаются полоски, которые создают образующиеся из стрептавидина мономеры, димеры, тримеры и олигомеры более высокого порядка, это означает, что сшитые структуры молекул стрептавидина образуются на магнитных частицах.
Связанные со стрептавидином магнитные частицы согласно настоящему изобретению имеют высокую способность связывания биотина, потому что они имеют структуру, в которой молекулы стрептавидина сшиты друг с другом на магнитных частицах. Способность связывания биотина в расчете на одну частицу из связанных со стрептавидином магнитных частиц согласно настоящему изобретению составляет, как правило, от 0,5 до 10 пмоль/мм2, предпочтительно от 2 до 9 пмоль/мм2 и особенно предпочтительно от 4 до 8 пмоль/мм2. Связанные со стрептавидином магнитные частицы согласно настоящему изобретению также имеют хорошую диспергируемость, которая представляет собой превосходное свойство. Диспергируемость связанных со стрептавидином магнитных частиц можно определять, например, помещая частицы в кювету, перемешивая осажденные связанные со стрептавидином магнитные частицы путем переворачивания и подтверждая состояние внутри кюветы посредством визуального наблюдения.
Способность связывания биотина в расчете на одну частицу из связанных со стрептавидином магнитных частиц согласно настоящему изобретению можно измерять любым способом при том условии, что он представляет собой способ, которым можно измерять способность связывания биотина. Например, способность связывания можно вычислять, вводя в реакцию данное количество флуоресцентного маркированного биотина и данное количество связанных со стрептавидином магнитных частиц, собирая связанные со стрептавидином магнитные частицы с помощью магнита, затем собирая данное количество надосадочной жидкости, измеряя интенсивность флуоресценции собранной надосадочной жидкости и сопоставляя полученные при измерениях значения с построенной заблаговременно калибровочной кривой, которая показывает соотношение между интенсивностью флуоресценции и концентрацией биотина.
В связанных со стрептавидином магнитных частицах согласно настоящему изобретению стрептавидин может представлять собой естественно произведенный или генетически модифицированный стрептавидин, причем генетически модифицированный стрептавидин является предпочтительным.
В связанных со стрептавидином магнитных частицах согласно настоящему изобретению магнитные частицы, с которыми связан стрептавидин, представляют собой частицы, на поверхности которых находятся аминогруппы. Магнитные частицы, на поверхности которых находятся аминогруппы согласно настоящему изобретению, не ограничиваются определенным образом, при том условии, что из них можно производить связанные со стрептавидином магнитные частицы согласно настоящему изобретению. Примеры структуры частицы из магнитных частиц, на поверхности которых находятся аминогруппы согласно настоящему изобретению, включают магнитные частицы с содержащей ядро и оболочку структурой, в которой внутренняя область частиц содержит магнитное вещество, и внешний слой состоит из органического полимера; магнитные частицы, имеющие структуру, которая не включает внешний слой и содержит магнитные вещества, неоднородно диспергированные в органическом полимере; и магнитные частицы в кластерном состоянии, состоящие исключительно из магнитных веществ.
Конкретные примеры магнитных частиц, на поверхности которых находятся аминогруппы (имеющиеся в продаже продукты), включают содержащие аминогруппы магнитные частицы Estapor (производитель Merck).
Магнитные вещества, содержащиеся в магнитных частицах, предпочтительно представляют собой суперпарамагнитные микрочастицы с небольшой остаточной намагниченностью, в качестве которых используют, например, разнообразные ферриты, такие как оксид железа(II, III) (Fe3O4) и γ-оксид железа(III) (γ-Fe2O3), металлы, такие как железо, марганец, кобальт и хром, сплавы этих металлов и т.п.
Содержание магнитных веществ в магнитных частицах, состоящих из органических полимеров и магнитных веществ, составляет предпочтительно 10 мас.% или более и предпочтительнее 30-60 мас.% по отношению к суммарной массе магнитных частиц.
Примеры формы магнитных частиц включают сферические и игольчатые формы, причем предпочтительными являются сферические формы. Размер магнитных частиц составляет, например, от 0,1 до 5 мкм и предпочтительно от 0,5 до 3 мкм.
2. Способы изготовления связанных со стрептавидином магнитных частиц
Способ изготовления связанные со стрептавидином магнитные частицы согласно настоящему изобретению представляет собой способ изготовления, включающий следующие стадии:
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы; и
(2) реакция магнитных частиц со стрептавидином и глутаральдегидом путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1).
Связанные со стрептавидином магнитные частицы согласно настоящему изобретению можно изготавливать путем использования способов изготовления согласно настоящему изобретению.
(1) Стадия изготовления суспензии, содержащей магнитные частицы
Суспензию, содержащую магнитные частицы, на поверхности которых находятся аминогруппы, можно изготавливать введением магнитных частиц, на поверхности которых находятся аминогруппы, в водную среду или добавлением водной среды к магнитным частицам, на поверхности которых находятся аминогруппы. Примеры магнитных частиц, на поверхности которых находятся аминогруппы, включают вышеупомянутые магнитные частицы, на поверхности которых находятся аминогруппы. Водная среда не ограничивается определенным образом при том условии, что она представляет собой водную среду, которая способна суспендировать магнитные частицы, на поверхности которых находятся аминогруппы, и соответствующие примеры включают дистиллированную воду, очищенную воду и буферный раствор. Значение pH водной среды составляет обычно от 4,5 до 7 и предпочтительно от 5 до 6. Когда используют буферный раствор в качестве водной среды, оказывается желательным использование буферного раствора, соответствующего устанавливаемому значению pH. Примеры буферных растворов, используемых в соответствующем качестве, включают ацетатный буферный раствор, цитратный буферный раствор, сукцинатный буферный раствор, фосфатный буферный раствор и буферные растворы Гуда (Good).
К числу примеров буферных растворов Гуда относятся 2-морфолиноэтансульфоновая кислота (MES), бис(2-гидроксиэтил)иминотрис(гидроксиметил)метан (Bis-Tris), пиперазин-N,N’-бис(2-этансульфоновая кислота) (PIPES), N-(2-ацетамидо)-2-аминоэтансульфоновая кислота (ACES), 3-морфолино-2-гидроксипропансульфоновая кислота (MOPSO), N,N-бис(2-гидроксиэтил)-2-аминоэтансульфоновая кислота (BES), 3-морфолинопропансульфоновая кислота (MOPS), N-[трис(гидроксиметил)метил]-2-аминоэтансульфоновая кислота (TES), 2-[4-(2-гидроксиэтил)-1-пиперазинил]этансульфоновая кислота (HEPES), 3-[N,N-бис(2-гидроксиэтил)амино]-2-гидроксипропансульфоновая кислота (DIPSO) и N-[трис(гидроксиметил)метил]-2-гидрокси-3-аминопропансульфоновая кислота (TAPSO).
Магнитные частицы, на поверхности которых находятся аминогруппы и которые подлежат суспендированию в водной среде, можно предварительно промывать. Магнитные частицы, на поверхности которых находятся аминогруппы, можно промывать, например, вводя магнитные частицы, на поверхности которых находятся аминогруппы, в диспергирующую жидкость в контейнере, диспргируя магнитные частицы, на поверхности которых находятся аминогруппы, затем собирая магнитные частицы, на поверхности которых находятся аминогруппы, с помощью магнита, и удаляя диспергирующую жидкость, оставшуюся в контейнере, путем всасывания. Примеры диспергирующих жидкостей включают водные растворы, содержащие поверхностно-активные вещества.
Значение pH диспергирующей жидкости составляет, как правило, от 4,5 до 7 и предпочтительно от 5 до 6. Примеры водной среды, используемой в качестве водного раствора, включают вышеупомянутые водные среды. Поверхностно-активное вещество не ограничивается определенным образом при том условии, что оно обеспечивает диспергирование магнитных частиц, и соответствующие примеры включают анионные поверхностно-активные вещества, катионные поверхностно-активные вещества, амфотерные поверхностно-активные вещества и неионные поверхностно-активные вещества. Концентрация поверхностно-активного вещества в диспергирующем растворе не ограничивается определенным образом при том условии, что она представляет собой концентрацию, при которой возможно диспергирование магнитных частиц, и она составляет, например, от 0,01% до 5,0%.
(2) Стадия реакции магнитных частиц с глутаральдегидом и стрептавидином
Стадия (2) представляет собой стадию образования структуры, в которой молекулы стрептавидина сшиты на магнитных частицах посредством реакции магнитных частиц со стрептавидином и глутаральдегидом путем введения глутаральдегида, в присутствии стрептавидина, в суспензию, содержащую магнитные частицы, на поверхности которых находятся аминогруппы, которые были изготовлены на стадии (1). Структура сшитых молекул стрептавидина образуется за счет ковалентных связей между молекулами стрептавидина посредством глутаральдегида. В настоящем документе введение глутаральдегида в присутствии стрептавидина означает, что стрептавидин уже присутствует, когда вводят глутаральдегид, и включает случаи, в которых стрептавидин вводят в суспензию магнитных частиц, и затем к нему последовательно добавляют глутаральдегид, а также случаи, в которых глутаральдегид и стрептавидин вводят одновременно в суспензию магнитных частиц.
Количество вводимого глутаральдегида не ограничивается определенным образом при том условии, что оно представляет собой количество, которое способно производить связанные со стрептавидином магнитные частицы согласно настоящему изобретению, и оно составляет, как правило, от 0,1 мг до 1,0 мг и предпочтительно от 0,35 мг до 0,6 мг по отношению к 100 мг магнитных частиц.
Количество вводимого стрептавидина не ограничивается определенным образом при том условии, что оно представляет собой количество, которое способно производить связанные со стрептавидином магнитные частицы согласно настоящему изобретению, и оно составляет, как правило, от 0,2 мг до 25 мг и предпочтительно от 10 мг до 15 мг по отношению к 100 мг магнитных частиц.
Концентрация магнитных частиц в реакционном растворе не ограничивается определенным образом при том условии, что она представляет собой концентрацию, которая способна производить связанные со стрептавидином магнитные частицы согласно настоящему изобретению, и она составляет, как правило, от 20 мг/мл до 80 мг/мл и предпочтительно от 40 мг/мл до 60 мг/мл.
Температура реакции составляет, как правило, от 0°C до 40°C, предпочтительно от 27,5°C до 37,5°C и особенно предпочтительно 35°C. Продолжительность реакции составляет, как правило, от 4 до 24 часов, предпочтительно от 8 до 20 часов и особенно предпочтительно 18 часов.
Хотя саму по себе реакционную смесь, полученную на стадии (2), можно использовать в качестве связанных со стрептавидином магнитных частиц согласно настоящему изобретению, магнитные частицы, которые получают, собирая с помощью магнита магнитные частицы в реакционной смеси, полученной на стадии (2), удаляя раствор, но не магнитные частицы, и затем, промывая частицы с использованием промывочного раствора, можно также использовать в качестве связанных со стрептавидином магнитных частиц согласно настоящему изобретению. Промывочный раствор не ограничивается определенным образом при том условии, что он представляет собой промывочный раствор, который способен вымывать вещества, отличные от связанных со стрептавидином магнитных частиц согласно настоящему изобретению, и соответствующие примеры включают вышеупомянутые водные среды. Кроме того, водные среды, содержащие белки и/или антисептики, можно также использовать в качестве промывочного раствора. Белки включают, например, бычий сывороточный альбумин (BSA). Антисептики включают, например, азид натрия. Кроме того, промытые магнитные частицы, можно хранить после их суспендирования в растворе для хранения. Раствор для хранения не ограничивается определенным образом при том условии, что он представляет собой раствор, который обеспечивает устойчивое хранение связанных со стрептавидином магнитных частиц согласно настоящему изобретению, и соответствующие примеры включают водные нейтральные и слабокислые буферные растворы, содержащие белки, такие как бычий сывороточный альбумин (BSA).
Способы изготовления связанных со стрептавидином магнитных частиц согласно настоящему изобретению могут дополнительно включают стадия восстановления после стадии (2). Стадия восстановления представляет собой стадию реакции связанных со стрептавидином магнитных частиц, изготовленных на стадии (2), с восстановителем. В процессе стадии (2) на магнитных частицах образуются молекулы стрептавидина со сшитыми структурами, и поскольку сшитые молекулы стрептавидина содержат основания Шиффа (Schiff), то есть имины, восстановление оснований Шиффа (иминов) с использованием восстановителя позволяет сшитым структурам становиться более устойчивыми.
После стадии (2) реакционную смесь саму по себе или промытые магнитные частицы можно использовать в качестве связанных со стрептавидином магнитных частиц на стадии восстановления. Растворитель, используемый в реакции между связанными со стрептавидином магнитными частицами и восстановителем, не ограничивается определенным образом при том условии, что он представляет собой растворитель, который способен обеспечивать протекание реакции восстановления, и соответствующие примеры включают вышеупомянутые диспергирующие жидкости. Кроме того, диспергирующую жидкость, содержащую органический растворитель, можно также использовать в качестве растворителя в реакции восстановления. Органический растворитель не ограничивается определенным образом при том условии, что он представляет собой органический растворитель, который является растворимым в воде и способен обеспечивать протекание реакции восстановления, и соответствующие примеры включают метанол, этанол и тетрагидрофуран. Восстановитель не ограничивается определенным образом при том условии, что он представляет собой восстановитель, который способен восстанавливать основания Шиффа (имины) и поддерживать сшитую структуру, и соответствующие примеры включают восстановители на основе боранов. Примеры восстановителей на основе боранов включают 2-пиколинборан и борогидрид натрия. Количество вводимого восстановителя составляет, как правило, от 0,0001 до 0,1 мас.%, предпочтительно от 0,0005 до 0,05 мас.% и особенно предпочтительно от 0,001 мас.% магнитных частиц.
Температура реакции в случае реакции восстановления составляет, как правило, от 30°C до 50°C, предпочтительно от 35°C до 45°C и особенно предпочтительно 40°C. Продолжительность реакции в случае реакции восстановления составляет, как правило, от двух до десяти суток, предпочтительно от пяти до восьми суток и особенно предпочтительно шесть суток.
После реакции восстановления магнитные частицы можно отделять с помощью магнита от компонентов раствора, отличных от магнитных частиц. Например, отделенные магнитные частицы можно промывать, используя вышеупомянутую диспергирующую жидкость или разбавленный раствор для хранения, и их можно хранить в форме суспензии в растворе для хранения. Раствор для хранения не ограничивается определенным образом при том условии, что он представляет собой раствор, который обеспечивает устойчивое хранение связанных со стрептавидином магнитных частиц согласно настоящему изобретению, и соответствующие примеры включают вышеупомянутый раствор для хранения.
3. Способы изготовления связанных с белком магнитных частиц
Связанные с белком магнитные частицы согласно настоящему изобретению изготавливают, используя связанные со стрептавидином магнитные частицы согласно настоящему изобретению и биотинилированный белок. Белки присоединяются к магнитным частицам посредством взаимодействия между стрептавидином на магнитных частицах и биотином, связанным с белком.
Например, связанные с белком магнитные частицы согласно настоящему изобретению можно изготавливать способом, который включает стадии, описанные ниже. Далее представлены конкретные варианты осуществления способа изготовления связанных с белком магнитных частиц согласно настоящему изобретению.
- Способ 1 изготовления связанных с белком магнитных частиц
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы;
(2) изготовление связанных со стрептавидином магнитных частиц путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1); и
(3) реакция связанных со стрептавидином частиц, изготовленных на стадии (2), с биотинилированным белком.
- Способ 2 изготовления связанных с белком магнитных частиц
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы;
(2) изготовление связанных со стрептавидином магнитных частиц путем введения глутаральдегида, в присутствии стрептавидина, в суспензию, изготовленную на стадии (1);
(3) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (2) с восстановителем; и
(4) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (3), с биотинилированным белком.
Реакцию между связанными со стрептавидином магнитными частицами и биотинилированными белками можно осуществлять в любых условиях при соблюдении того, что они представляют собой условия, в которых белок присоединяется к магнитным частицам. Температура реакции составляет, как правило, от 25°C до 50°C и предпочтительно от 30°C до 40°C. Продолжительность реакции составляет, как правило, от 30 минут до 24 часов, и предпочтительно от 2 до 18 часов.
Примеры белков включают антитела, которые присоединяются к измеряемому компоненту, и конкурентные вещества, которые конкурируют с измеряемым компонентом в реакции антигена и антитела. Примеры конкурентных веществ включают измеряемый компонент, а также вещество, содержащее эпитоп, распознаваемый антителом, которое присоединяется к измеряемому компоненту. Конкретные примеры белков включают иммуноглобулин IgG, антитело анти-IgG, IgM, антитело анти-IgM, IgA, антитело анти-IgA, IgE, антитело анти-IgE, апопротеин AI, антитело анти-апопротеина AI, апопротеин AII, антитело антиапопротеина AII, апопротеин B, антитело анти-апопротеина B, апопротеин E, антитело анти-апопротеина E, ревматоидный фактор, антитело анти-ревматоидного фактора, D-димер, антитело анти-D-димера, окисленный липопротеин низкой плотности (LDL), антитело антиокисленного LDL, гликозилированный LDL, антитело антигликозилированного LDL, гликоальбумин, антитело антигликоальбумина, трийодтиронин (T3), антитело анти-T3, суммарный тироксин (T4), антитело анти-T4, лекарственные средства (например, противоэпилептические лекарственные средства), антитела, которые присоединяются к лекарственным средствам, C-реактивный белок (CRP), антитело анти-CRP, цитокины, антитела, которые присоединяются к цитокинам, α-фетопротеин (AFP), антитело анти-AFP, карциноэмбриональный антиген (CEA), антитело анти-CEA, раковый антиген CA19-9, антитело анти-CA19-9, CA15-3, антитело анти-CA15-3, CA-125, антитело анти-CA-125, обусловленный отсутствием витамина К белок PIVKA-II, антитело анти-PIVKA-II, паратиреоидный гормон (PTH), антитело анти-PTH, хорионический гонадотропный гормон человека (hCG), антитело анти-hCG, тиреостимулирующий гормон (TSH), антитело анти-TSH, инсулин, антиинсулиновое антитело, С-пептид, антитело анти-С-пептида, эстроген, антиэстрогеновое антитело, фактор роста фибробластов-23 (FGF-23), антитело анти-FGF-23, глутаматдекарбоксилаза (GAD), антитело анти-GAD, пепсиноген, антипепсиногеновое антитело, антиген вируса гепатита B (HBV), антитело анти-HBV, антиген вируса гепатита C (HCV), антитело анти-HCV, антиген вируса Т-клеточного лейкоза человека типа 1 (HTLV-I), антитело анти-HTLV-I, антиген вируса иммунодефицита человека (HIV), антитело анти-HIV, антиген вируса гриппа, антитело антивируса гриппа, антиген туберкулезных микобактерий (туберкулезный гликолипид) (TBGL), антитело анти-TBGL, антиген микоплазмы, антитело антимикоплазмы, гемоглобин A1e, антитело антигемоглобина A1e, предсердный натрийуретический пептид (ANP), антитело анти-ANP, натрийуретический пептид головного мозга (BNP), антитело анти-BNP, тропонин T, антитело антитропонина T, тропонин I, антитело антитропонина I, креатинкиназа-MB (CK-MB), антитело анти-CK-MB, миоглобин, антимиоглобиновое антитело, связывающий жирные кислоты белок L-FABP, антитело анти-L-FABP, H-FABP, антитело анти-H-FABP, антиген циклического цитрулинового пептида (CCP), антитело анти-CCP, поверхностно-активный белок D (SP-D), антитело анти-SP-D, антитела, которые присоединяются к микотоксинам [таким как деоксиниваленол (DON), ниваленол (NIV) и токсин T-2 (T2)], антитела, которые присоединяются к эндокринным разрушителям [таким как бисфенол A, нонилфенол, дибутилфталат, полихлорированные бифенилы (PCB), диоксины, п,п’-дихлордифенилтрихлорэтан и трибутилолово], антитела, которые присоединяются к стероидным гормонам (таким как альдостерон и тестостерон), грибы, такие как кишечная палочка (Escherichia coli), антитела, которые присоединяются к белкам грибкового происхождения, пищевые аллергены, другие аллергены, такие как клещи, и антиаллергеновые антитела.
При добавлении к биотинилированным белкам можно использовать биотинилированные углеводородные соединения и биотинилированный нуклеиновые кислоты. Связанные с углеводородными соединениями магнитные частицы можно изготавливать посредством реакции связанных со стрептавидином магнитных частиц согласно настоящему изобретению с биотинилированным углеводородным соединением. Кроме того, связанные с нуклеиновыми кислотами магнитные частицы можно изготавливать посредством реакции связанных со стрептавидином магнитных частиц согласно настоящему изобретению с биотинилированной нуклеиновой кислотой.
В число примеров углеводородных соединений в биотинилированных углеводородных соединениях включены микотоксины [такие как деоксиниваленол (DON), ниваленол (NIV) и токсин T-2 (T2)], эндокринные разрушители [такие как бисфенол A, нонилфенол, дибутилфталат, полихлорированные бифенилы (PCB), диоксины, п,п’-дихлордифенилтрихлорэтан и трибутилолово], а также стероидные гормоны (такие как альдостерон и тестостерон).
Примеры нуклеиновых кислот в биотинилированных нуклеиновых кислотах включают ДНК, РНК, аптамер и их производные.
4. Способы измерения измеряемого компонента
Вариант осуществления способ измерения измеряемого компонента согласно настоящему изобретению представляет собой способ измерения измеряемого компонента в образце с использованием связанных со стрептавидином магнитных частиц согласно настоящему изобретению и биотинилированного белка. Еще один вариант осуществления способа измерения измеряемого компонента согласно настоящему изобретению представляет собой способ измерения измеряемого компонента в образце с использованием связанных с белком магнитных частиц согласно настоящему изобретению. В качестве способа измерения согласно настоящему изобретению можно использовать любой способ при том условии, что он представляет собой способ, используемый в обычных иммунологических анализах, и соответствующие примеры включают способ двойных антител и способ конкуренции.
Примеры белков в биотинилированных белках и связанных с белком магнитных частицах включают антитела, которые присоединяются к измеряемому компоненту и конкурентным веществам, конкурирующим с измеряемым компонентом в реакции антигена и антитела. Примеры конкурентных веществ включают измеряемые компоненты и вещества, содержащие эпитоп, который распознает антитело, присоединяющееся к измеряемому компоненту. Конкретные примеры белков включают вышеупомянутые белки.
Образец в настоящем изобретении не ограничивается определенным образом при том условии, что он представляет собой образец, который обеспечивает измерение измеряемого компонента согласно настоящему изобретению. В число примеров включены цельная кровь, плазма, сыворотка, спинномозговая жидкость, слюна, амниотическая жидкость, моча, пот и поджелудочный сок, причем предпочтительными являются плазма и сыворотка.
Измеряемый компонент не ограничивается определенным образом, при том условии, что его можно измерять, используя способ измерения согласно настоящему изобретению, и соответствующие примеры включают иммуноглобулины IgG, IgM, IgA, IgE, апопротеин AI, апопротеин AII, апопротеин B, апопротеин E, ревматоидный фактор, D-димер, окисленный LDL, гликозилированный LDL, гликоальбумин, трийодтиронин (T3), суммарный тироксин (T4), лекарственные средства (например, противоэпилептические лекарственные средства), C-реактивный белок (CRP), цитокины, α-фетопротеин (AFP), карциноэмбриональный антиген (CEA), CA19-9, CA15-3, CA-125, PIVKA-II, паратиреоидный гормон (PTH), хорионический гонадотропный гормон человека (hCG), тиреостимулирующий гормон (TSH), инсулин, С-пептид, эстроген, фактор роста фибробластов-23 (FGF-23), антитело антиглутаматдекарбоксилазы (GAD), пепсиноген, антиген вируса гепатита B (HBV), антитело анти-HBV, антиген вируса гепатита C (HCV), антитело анти-HCV, антиген вируса Т-клеточного лейкоза человека типа 1 (HTLV-I), антитело анти-HTLV-I, антитело антивируса иммунодефицита человека (HIV), антиген вируса гриппа, антитело антивируса гриппа, антиген туберкулезных микобактерий (туберкулезный гликолипид) (TBGL), антитело анти-TBGL, антитело антимикоплазмы, гемоглобин A1e, предсердный натрийуретический пептид (ANP), натрийуретический пептид головного мозга (BNP), тропонин T, тропонин I, креатинкиназа-MB (CK-MB), миоглобин, L-FABP, H-FABP, антитело анти-CCP, SP-D, микотоксины [такие как деоксиниваленол (DON), ниваленол (NIV) и токсин T-2 (T2)], эндокринные разрушители [такие как бисфенол A, нонилфенол, дибутилфталат, полихлорированные бифенилы (PCB), диоксины, п,п’-дихлордифенилтрихлорэтан и трибутилолово], стероидные гормоны (такие как альдостерон и тестостерон), грибы, такие как кишечная палочка (Escherichia coli), антитела, которые присоединяются к белкам грибкового происхождения, пищевые аллергены, другие аллергены, такие как клещи, и антиаллергеновые антитела.
(I) Способы измерения измеряемого компонента с использованием связанных со стрептавидином магнитных частиц согласно настоящему изобретению и биотинилированного белка
(I-1) Способ двойных антител
Примеры способа измерения измеряемого компонента в образце с использованием двойных антител представляют собой способы, включающие следующие стадии:
(1) образование на магнитных частицах иммунокомплексов, включающих первое антитело, которое присоединяется к измеряемому компоненту, измеряемый компонент и второе антитело, которое присоединяется к измеряемому компоненту, посредством реакции в водной среде измеряемого компонента в образце со связанными со стрептавидином магнитными частицами согласно настоящему изобретению, биотинилированного первого антитела, в котором биотин присоединен к первому антителу, которое присоединяется к измеряемому компоненту, и второго антитела, которое присоединяется к измеряемому компоненту;
(2) сбор магнитных частиц в реакционной смеси после стадии (1) с помощью магнитной силы и отделение магнитных частиц, собранных с помощью магнитной силы, от других компонентов; и
(3) измерение иммунокомплексов на магнитных частицах, отделенных на стадии (2).
Вместо первого и второго антител можно использовать фрагмент первого антитела и фрагмент второго антитела. Примеры фрагмента антитело включают Fab, F(ab’)2, и Fab’.
Водная среда не ограничивается определенным образом, при том условии, что она представляет собой водную среду, которая обеспечивает реакцию антигена и антитела, и соответствующие примеры включают вышеупомянутые водные среды.
На стадии (1) измеряемый компонент в образце реагирует в водной среде со связанными со стрептавидином магнитными частицами, биотинилированным первым антителом и вторым антителом, образуя на магнитных частицах иммунокомплекс, включающий первое антитело, измеряемый компонент и второе антитело.
В настоящем документе реакция измеряемого компонента в образце со связанными со стрептавидином магнитными частицами, биотинилированного первого антитела и второго антитела может представлять собой любую реакцию при том условии, что она является реакцией, которая образует на магнитных частицах иммунокомплекс, включающий первое антитело, измеряемый компонент и второе антитело. Например, измеряемый компонент в образце может реагировать со связанными со стрептавидином магнитными частицами и биотинилированным первым антителом, образуя на магнитных частицах иммунокомплекс первого антитела и измеряемого компонента, затем этот комплекс может реагировать со вторым антителом; или, в качестве альтернативы, измеряемый компонент в образце может реагировать одновременно со связанными со стрептавидином магнитными частицами, биотинилированным первым антителом и вторым антителом. В том случае, когда после образования иммунокомплекса первого антитела и измеряемого компонента на магнитных частицах следует реакция иммунокомплекса со вторым антителом, стадию промывания можно осуществлять после образования иммунокомплекса. Промывание магнитных частиц после образование иммунокомплекса первого антитела и измеряемого компонента не ограничивается определенным образом при том условии, что оно представляет собой промывание, которое способно сохранять иммунокомплекс на магнитных частицах. Примеры включают способы промывания магнитных частиц посредством удаления компонентов, отличных от магнитных частиц, из реакционной смеси после образования иммунокомплекса первого антитела и измеряемого компонента на магнитных частицах, а также введение промывочного раствора в реакционный резервуар, содержащий оставшиеся магнитные частицы; и способы промывания магнитных частиц посредством введения промывочного раствора в реакционную смесь после реакции и одновременного удаления компонентов, отличных от магнитных частиц. Удаление компонентов, отличных от магнитных частиц, можно осуществлять, например, собирая магнитные частицы посредством магнитной силы и затем всасывая оставшиеся компоненты. Примеры промывочного раствора включают вышеупомянутые водные среды, а также водные среды, изготовленные введением поверхностно-активного вещества в вышеупомянутые водные среды. Примеры поверхностно-активного вещества включают неионные поверхностно-активные вещества, такие как Tween 20.
Температура реакции в случае реакции антигена и антитела на стадии (1) не ограничивается определенным образом при том условии, что она представляет собой температуру, которая обеспечивает измерение измеряемого компонента согласно настоящему изобретению, и она составляет, как правило, от 0°C до 50°C, предпочтительно от 4°C до 45°C и особенно предпочтительно от 20°C до 40°C. Продолжительность реакции не ограничивается определенным образом при том условии, что она представляет собой продолжительность, которая обеспечивает измерение измеряемого компонента согласно настоящему изобретению, и она составляет, как правило, от пяти минут до одного часа и предпочтительно от пяти минут до 20 минут.
На стадии (2) магнитные частицы после стадии (1) или, конкретно, магнитные частицы, к которым присоединены иммунокомплексы, включающие первое антитело, измеряемый компонент и второе антитело, собирают посредством магнитной силы, и собранные магнитные частицы отделяют от других компонентов. Магнитная сила для сбора магнитных частиц не ограничивается определенным образом при том условии, что она представляет собой магнитную силу, которая обеспечивает измерение измеряемого компонента согласно настоящему изобретению. Отделение магнитных частиц, собранных посредством магнитной силы, от других компонентов не ограничивается определенным образом, при том условии, что оно представляет собой отделение, которое обеспечивает измерение измеряемого компонента согласно настоящему изобретению.
После стадии (2) или одновременно со стадией (2) можно осуществлять стадию промывания магнитных частиц, к которым присоединены иммунокомплексы, включающие первое антитело, измеряемый компонент и второе антитело. Магнитные частицы можно промывать, используя, например, вышеупомянутые способы.
На стадии (3) измеряемый компонент в образце можно измерять посредством измерения иммунокомплексов на магнитных частицах, отделенных на стадии (2). Примеры способа измерения иммунокомплексов включают следующие способы.
(1) Случай немаркированного второго антитела
Иммунокомплексы на отделенных магнитных частицах можно измерять посредством реакции маркированного третьего антитела, в которой метку присоединяют к третьему антителу, которое присоединяется ко второму антителу, с магнитными частицами, к которым присоединены иммунокомплексы, включающие первое антитело, измеряемый компонент и второе антитело, образуя на магнитных частицах иммунокомплексы, включающие первое антитело, измеряемый компонент, второе антитело и третье антитело, и затем измеряя метку в иммунокомплексах. Фрагмент третьего антитела можно использовать вместо третьего антитела.
Примеры третьего антитела, которое присоединяется ко второму антителу, включают антитела или их фрагменты, которые присоединяются к области Fc второго антитела. Способ измерения метки не ограничивается определенным образом при том условии, что он представляет собой способ, который обеспечивает измерение иммунокомплекса на отделенных магнитных частицах. Примеры включают измерение хемилюминесценции, измерение флуоресценции и измерение поглощения. Примеры фрагмента антитела включают Fab, F(ab’)2, и Fab’.
(2) Случай маркированного второго антитела, которое присоединяется к измеряемому компоненту
Иммунокомплексы на отделенных магнитных частицах можно измерять посредством измерения метки в иммунокомплексах, образованных на магнитных частицах и включающих первое антитело, измеряемый компонент и маркированное второе антитело. Способ измерения метки не ограничивается определенным образом при том условии, что он представляет собой способ, который обеспечивает измерение иммунокомплекса на отделенных магнитных частицах. Примеры включают измерение хемилюминесценции, измерение флуоресценции и измерение поглощения.
(A) Измерение хемилюминесценции
Измерение хемилюминесценции можно осуществлять представленными ниже способами.
(A-1) Случай метки, представляющей собой фермент
В случае метки, представляющей собой фермент, измерение можно осуществлять, например, заставляя субстрат, который производит свет в реакции с ферментом, воздействовать на маркированное антитело или его фрагмент, и измеряя интенсивность произведенного света (hν), используя измеритель интенсивности люминесценции или аналогичный прибор. Фермент не ограничивается определенным образом, при том условии, что он способен реагировать с субстратом фермента и производить свет, и в число соответствующих примеров включены щелочная фосфатаза, пероксидаза, β-D-галактозидаза, и люцифераза.
В случае использования щелочной фосфатазы в качестве фермента примеры субстрата щелочной фосфатазы, который реагирует со щелочной фосфатазой и производит свет, включают динатриевую соль 3-(2’-спироадамантан)-4-метокси-4-(3’-фосфорилокси)фенил-1,2-диоксетана (AMPPD), динатриевую соль 2-хлор-5-4-метоксиспиро[1,2-диоксетан-3,2’-(5’-хлор)трицикло[3,3,1,13,7]декан]-4-ил}фенилфосфата (CDP-Star™), динатриевую соль 3-{4-метоксиспиро[1,2-диоксетан-3,2’-(5’-хлор)трицикло[3,3,1,13,7]декан]-4-ил}фенилфосфата (CSPD™), динатриевую соль [10-метил-9(10H)-акридинилиден]феноксиметилфосфата (Lumigen™ APS-5) и динатриевую соль 9-(4-хлорфенилтиофосфорилоксиметилиден)-10-метилакридана.
В случае использования пероксидазы в качестве фермента примеры субстрата пероксидазы, который реагирует с пероксидазой и производит свет, включают сочетания пероксида водорода с люминесцентным соединением (например, соединением люминола или соединением люцигенина).
В случае использования β-D-галактозидазы в качестве фермента примеры субстрата β-D-галактозидазы, который реагирует с β-D-галактозидазой и производит свет, включают Galacton-Plus (производитель Applied Biosystems).
В случае использования люциферазы в качестве фермента примеры субстрата люциферазы, который реагирует с люциферазой и производит свет, включают люциферин и целентеразин.
(A-2) Случай метки, представляющей собой люминесцентное вещество
В случае метки, представляющей собой люминесцентное вещество, измерение можно осуществлять, например, посредством измерения интенсивности света, происходящего из люминесцентного вещества в образованных иммунокомплексах, используя измеритель интенсивности люминесценции или подобное устройство. Люминесцентное вещество не ограничивается определенным образом при том условии, что оно представляет собой люминесцентное вещество, которое обеспечивает измерение настоящего изобретения, и соответствующие примеры включают акридиний и его производные, комплексные соединения рутения и 2,4,5-трифенилимидазол.
(B) Измерение флуоресценции
Флуоресценцию можно измерять представленными ниже способами.
(B-1) Случай метки, представляющей собой фермент
В случае метки, представляющей собой фермент, измерение можно осуществлять, например, заставляя субстрат, который производит флуоресценцию в реакции с ферментом, воздействовать на маркированное антитело или его фрагмент, и измеряя интенсивность производимой флуоресценции с использованием измерителя интенсивность флуоресценции или подобного устройства. Фермент не ограничивается определенным образом при том условии, что он способен реагировать с субстратом фермента, производя флуоресценцию, и соответствующие примеры включают пероксидазу, β-D-галактозидазу и β-глюкуронидазу.
В случае использования пероксидазы в качестве фермента, примеры субстрата пероксидазы, который реагирует с пероксидазой и производит флуоресценцию, включают сочетания пероксида водорода и флуоресцентного соединения (например, 4-гидроксифенилуксусная кислота, 3-(4-гидроксифенил)пропионовая кислота или кумарин).
В случае использования β-D-галактозидазы в качестве фермента, примеры субстрата β-D-галактозидазы, который реагирует с β-D-галактозидазой и производит флуоресценцию, включают 4-метилумбелиферил-β-D-галактопиранозид или его аналог.
В случае использования β-глюкуронидазы в качестве фермента, примеры субстрата β-глюкуронидазы, который реагирует с β-глюкуронидазой и производит флуоресценцию, включают TokyoGreen™-PGluU (производитель Sekisui Medical Co. Ltd.).
(B-2) Случай метки, представляющей собой флуоресцентное вещество
В случае метки, представляющей собой флуоресцентное вещество, измерение можно осуществлять, например, посредством измерения интенсивности флуоресценции, происходящей из флуоресцентного вещества в образованных иммунокомплексах, с использованием измерителя интенсивность флуоресценции или подобного устройства. Флуоресцентное вещество не ограничивается определенным образом при том условии, что оно представляет собой флуоресцентное вещество, которое обеспечивает измерение настоящего изобретения, и в число примеров включены флуоресцинизотиоцианат (FITC), родамин- B-изотиоцианат (RITC), квантовая точка (Science, 1998 г., т. 281, с. 2016-2018), фикобилипротеины, такие как фикоэритин, зеленый флуоресцентный белок (GFP), красный флуоресцентный белок (RFP), желтый флуоресцентный белок (YFP) и синий флуоресцентный белок (BFP).
(C) Измерение поглощения
Поглощение можно измерять представленными ниже способами.
(C-1) Случай метки, представляющей собой фермент
В случае метки, представляющей собой фермент, измерение можно осуществлять, например, заставляя субстрат, который образует краситель в реакции с ферментом, воздействовать на маркированное антитело или его фрагмент, и измеряя поглощение образованного красителя, используя спектрофотометр, считывающее многолуночные планшеты устройство или подобное устройство. Фермент не ограничивается определенным образом при том условии, что он способен реагировать с субстратом фермента, образуя краситель, и соответствующие примеры включают пероксидазу.
В том случае, где пероксидазу используют в качестве фермента, примеры субстрата пероксидазы, который реагирует с пероксидазой, образуя краситель, включают сочетания пероксида водорода и хромогена окислительного окрашиваемого типа. Примеры хромогена окислительного окрашиваемого типа включают хромогены бесцветного типа и хромогены типа окислительного окрашиваемого сочетания.
Хромоген бесцветного типа представляет собой вещество, которое превращается в краситель само по себе в присутствии пероксида водорода и катализирующего пероксид вещества, такого как пероксидаза. Конкретные примеры включают тетраметилбензидин, о-фенилендиамин, 10-N-карбоксиметилкарбамоил-3,7-бис(диметиламино)-10H-фенотиазин (CCAP), 10-N-метилкарбамоил-3,7-бис(диметиламино)-10H-фенотиазин (MCDP), натриевая соль 10-N-(карбоксиметиламинокарбонил)-3,7-бис(диметиламино)-10H-фенотиазина (DA-67), N,N,N’,N’,N”,N”-гекса(3-сульфопропил)-4,4’,4”-триаминотрифенилметан (TPM-PS), натриевая соль N-(карбоксиметиламинокарбонил)-4,4’-бис(диметиламино)дифениламина (DA-64), 4,4’-бис(диметиламино)дифениламин и бис[3-бис(4-хлорфенил)метил-4-диметиламинофенил]амин(BCMA).
Хромоген типа окислительного окрашиваемого сочетания представляет собой вещество, которое образует краситель путем окислительного сочетания двух соединений в присутствии пероксида водорода и катализирующего пероксид вещества, такого как пероксидаза. Примеры сочетания двух соединений включают сочетание связующих реагентов и анилинов (реагент Триндера (Trinder)), и сочетание связующих реагентов и фенолов. Примеры связующих реагентов включают 4-аминоантипирин (4-AA) и 3-метил-2-бензотиазолинонгидразин.
Примеры анилинов включают N-(3-сульфопропил)анилин,
N-этил-N-(2-гидрокси-3-сульфопропил)-3-метиланилин (TOOS),
N-этил-N-(2-гидрокси-3-сульфопропил)-3,5-диметиланилин (MAOS), N-этил-N-(2-гидрокси-3-сульфопропил)-3,5-диметоксианилин (DAOS), N-этил-N-(3-сульфопропил)-3-метиланилин (TOPS),
N-(2-гидрокси-3-сульфопропил)-3,5-диметоксианилин (HDAOS),
N,N-диметил-3-метиланилин,
N,N-бис(3-сульфопропил)-3,5-диметоксианилин,
N-этил-N-(3-сульфопропил)-3-метоксианилин,
N-этил-N-(3-сульфопропил)анилин,
N-этил-N-(3-сульфопропил)-3,5-диметоксианилин,
N-(3-сульфопропил)-3,5-диметоксианилин,
N-этил-N-(3-сульфопропил)-3,5-диметиланилин,
N-этил-N-(2-гидрокси-3-сульфопропил)-3-метоксианилин,
N-этил-N-(2-гидрокси-3-сульфопропил)анилин,
N-этил-N-(3-метилфенил)-N’-сукцинилэтилендиамин (EMSE),
N-этил-N-(3-метилфенил)-N’-ацетилэтилендиамин, и
N-этил-N-(2-гидрокси-3-сульфопропил)-4-фтор-3,5-диметоксианилин (F-DAOS). Примеры фенолов включают фенол, 4-хлорфенол, 3-метилфенол и 3-гидрокси-2,4,6-трийодбензойную кислоту (HTIB).
Концентрацию измеряемого компонента в образце, на основании измеренных значений, полученных в результате измерений иммунокомплексов, образующихся на магнитных частицах, можно определять такими способами, как описано ниже.
Концентрацию измеряемого компонента в измеряемом образце определяют, осуществляя вышеупомянутые стадии (1)-(3) с использованием измеряемого компонента в известной концентрации, строя калибровочную кривую, представляющую соотношение между концентрацией измеряемого компонента и измеренным значением (объемом информации, полученной из метки), и затем осуществляя измерения с использованием измеряемого образца и сопоставляя измеренные значения с построенной калибровочной кривой.
(I-2) Способ конкуренции 1
Примеры способов измерения измеряемого компонента в образце с использованием способа конкуренции представляют собой способы, включающие следующие стадии:
(1) реакция в водной среде измеряемого компонента в образце со связанными со стрептавидином магнитными частицами согласно настоящему изобретению биотинилированного антитела, где биотин присоединен к антителу, которое одновременно присоединено к измеряемому компоненту и конкурентному веществу, и маркированного конкурентного вещества, где метка присоединена к конкурентному веществу; и
(2) измерение метки в иммунокомплексе маркированного конкурентного вещества и антитела, которое присоединяется к измеряемому компоненту, который образовался на стадии (1).
После стадии (1) можно осуществлять стадию промывания магнитных частиц, которые были использованы для реакции антигена и антитела. Магнитные частицы можно промывать, используя например, вышеупомянутые способы промывания.
Измерение метки на стадии (2) можно осуществлять, используя, например, вышеупомянутые способы.
Концентрацию измеряемого компонента в образце на основании измеренных значений, полученных в результате измерений иммунокомплексов, образовавшихся на магнитных частицах, можно определять представленными ниже способами.
Концентрацию измеряемого компонента в измеряемом образце определяют, осуществляя вышеупомянутые стадии (1) и (2) с использованием измеряемого компонента в известной концентрации, строя калибровочную кривую, представляющую соотношение между концентрацией измеряемого компонента и измеренным значением (объемом информации, полученной из метки), и затем осуществляя измерения с использованием измеряемого образца и сопоставляя измеренные значения с построенной калибровочной кривой.
(I-3) Способ конкуренции 2
Примеры способов измерения измеряемого компонента в образце с использованием способа конкуренции представляют собой способы, включающие следующие стадии:
(1) реакция, в водной среде, измеряемый компонент в образце со связанными со стрептавидином магнитными частицами согласно настоящему изобретению, биотинилированное конкурентное вещество, в котором биотин присоединен к конкурентное вещество, и маркированное антитело, в котором метка присоединена к антителу, которое одновременно присоединено к измеряемому компоненту и конкурентному веществу; и
(2) измерение метки в иммунокомплексе конкурентного вещества и маркированного антитела, которая образовалась на стадии (1).
После стадии (1) можно осуществлять стадию промывания магнитных частиц, которые были использованы для реакции антигена и антитела. Магнитные частицы можно промывать, используя, например, вышеупомянутые способы промывания.
Измерение метки на стадии (2) можно осуществлять, используя, например, вышеупомянутые способы.
Концентрацию измеряемого компонента в образце на основании измеренных значений, полученных в результате измерений иммунокомплексов, образовавшихся на магнитных частицах, можно определять представленными ниже способами.
Концентрацию измеряемого компонента в измеряемом образце определяют, осуществляя вышеупомянутые стадии (1) и (2) с использованием измеряемого компонента в известной концентрации, строя калибровочную кривую, представляющую соотношение между концентрацией измеряемого компонента и измеренным значением (объемом информации, полученной из метки), и затем осуществляя измерения с использованием измеряемого образца и сопоставляя измеренные значения с построенной калибровочной кривой.
(II) Способы измерения измеряемого компонента, использующие связанные с белком магнитные частицы согласно настоящему изобретению
(II-1) Способ двойных антител
Примеры способов измерения измеряемого компонента в образце с использованием способа двойных антител включают способы, использующие антитело, которое присоединяется к измеряемому компоненту как белок в связанных с белком магнитных частицах согласно настоящему изобретению, и включают следующие стадии:
(1) образование на магнитных частицах иммунокомплексов, включающих первое антитело, которое присоединяется к измеряемому компоненту, измеряемый компонент и второе антитело, которое присоединяется к измеряемому компоненту посредством реакции в водной среде измеряемого компонента в образце с магнитными частицами, к которому присоединяется первое антитело, и второго антитела, которое присоединяется к измеряемому компоненту;
(2) сбор магнитных частиц в реакционной смеси после стадии (1) с помощью магнитной силы и отделение магнитных частиц, собранных посредством магнитной силы, от других компонентов; и
(3) измерение иммунокомплексов на магнитных частицах, отделенных на стадии (2).
Вместо первого и второго антител можно использовать фрагмент первого антитела и фрагмент второго антитела. Водная среда не ограничивается определенным образом при том условии, что она представляет собой водную среду, которая обеспечивает реакцию антигена и антитела, и соответствующие примеры включают вышеупомянутые водные среды.
На стадии (1) измеряемый компонент в образце реагирует в водной среде с первым антителом на магнитных частицах и вторым антителом, образуя на магнитных частицах иммунокомплекс, включающий первое антитело, измеряемый компонент и второе антитело.
В настоящем документе реакция измеряемого компонента в образце с первым антителом на магнитных частицах и второе антитело может представлять собой любую реакцию при том условии, что она представляет собой реакцию, которая образует на магнитных частицах иммунокомплекс, включающий первое антитело, измеряемый компонент и второе антитело. Например, измеряемый компонент в образце может реагировать с первым антителом на магнитных частицах, образуя на магнитных частицах иммунокомплекс первого антитела и измеряемого компонента, затем этот иммунокомплекс может реагировать со вторым антителом; или, в качестве альтернативы, измеряемый компонент в образце может реагировать одновременно с первым антителом на магнитных частицах и вторым антителом. В том случае, когда после образования иммунокомплекса первого антитела и измеряемого компонента на магнитных частицах следует реакция иммунокомплекса со вторым антителом, стадию промывания можно осуществлять после образования иммунокомплекса. Промывание магнитных частиц после образования иммунокомплекса первого антитела и измеряемого компонента не ограничивается определенным образом при том условии, что оно представляет собой промывание, которое способно сохранять иммунокомплекс на магнитных частицах, и соответствующие примеры включают вышеупомянутые способы промывания.
Температура реакции в случае реакции антигена и антитела на стадии (1) не ограничивается определенным образом при том условии, что она представляет собой температуру, которая обеспечивает измерение измеряемого компонента согласно настоящему изобретению, и она составляет, как правило, от 0°C до 50°C, предпочтительно от 4°C до 45°C и особенно предпочтительно от 20°C до 40°C. Продолжительность реакции не ограничивается определенным образом при том условии, что она представляет собой продолжительность, которая обеспечивает измерение измеряемого компонента согласно настоящему изобретению, и она составляет, как правило, от пяти минут до одного часа и предпочтительно от пяти до 20 минут.
Стадия (2) и стадия (3) являются такими же, как вышеупомянутые стадия (2) и стадия (3) способа (I-1). Концентрацию измеряемого компонента в образце на основании измеренных значений, полученных в результате измерений иммунокомплексов, образовавшихся на магнитных частицах, можно определять, используя, например, способы, аналогичные вышеупомянутому случаю способа (I-1).
(II-2) Способ конкуренции 1
Примеры способов измерения измеряемого компонента в образце с использованием способа конкуренции представляют собой способы с использованием антитела, которое одновременно присоединено к измеряемому компоненту и конкурентному веществу, как белок в связанных с белком магнитных частицах согласно настоящему изобретению, и включают следующие стадии:
(1) реакция в водной среде измеряемого компонента в образце с магнитными частицами, к которым присоединено антитело, которое одновременно присоединено к измеряемому компоненту и конкурентному веществу, и маркированного конкурентного вещества, где метка присоединена к конкурентному веществу; и
(2) измерение метки в иммунокомплексе маркированного конкурентного вещества и антитела, которое присоединяется к измеряемому компоненту, который образовался на стадии (1).
После стадии (1) можно осуществлять стадию промывания магнитных частиц, которые были использованы для реакции антигена и антитела. Магнитные частицы можно промывать, используя, например, вышеупомянутые способы промывания.
Измерение метки на стадии (2) можно осуществлять, используя, например, вышеупомянутые способы.
Концентрацию измеряемого компонента в образце на основании измеренных значений, полученных в результате измерений иммунокомплексов, образовавшихся на магнитных частицах, можно определять, используя, например, способы, аналогичные вышеупомянутому случаю способа (I-2).
(II-3) Способ конкуренции 2
Примеры способов измерения измеряемого компонента в образце с использованием способа конкуренции представляют собой способы с использованием конкурентного вещества, которое конкурирует с измеряемым компонентом в реакции антигена и антитела, как белок в связанных с белком магнитных частицах согласно настоящему изобретению, и включают следующие стадии:
(1) реакция в водной среде измеряемого компонента в образце с магнитными частицами, к которым присоединено конкурентное вещество, и маркированным антителом, в которой метка присоединена к антителу, которое одновременно присоединено к измеряемому компоненту и конкурентному веществу; и
(2) измерение метки в иммунокомплексе маркированного антитела и конкурентного вещества, который образовался на стадии (1).
После стадии (1) можно осуществлять стадию промывания магнитных частиц, которые были использованы для реакции антигена и антитела. Магнитные частицы можно промывать, используя, например, вышеупомянутые способы промывания.
Измерение метки на стадии (2) можно осуществлять, используя, например, вышеупомянутые способы.
Концентрацию измеряемого компонента в образце на основании измеренных значений, полученных в результате измерений иммунокомплексов, образовавшихся на магнитных частицах, можно определять способами, аналогичными описанному выше случаю (I-3).
Вместо биотинилированного белка можно использовать биотинилированное углеводородное соединение, чтобы измерять измеряемый компонент в образце. Примеры измеряемого компонента включают углеводородное соединение, которое составляет биотинилированное углеводородное соединение, и антитело, которое присоединяется к углеводородному соединению. Примеры углеводородного соединения включают вышеупомянутые углеводородные соединения. Измерение измеряемого компонента в образце с использованием биотинилированного углеводородного соединения можно осуществлять, применяя способы, такие как вышеупомянутый способ двойных антител (I-1) или (II-1) и способ конкуренции (I-3) или (II-3). В этом случае углеводородное соединение используют вместо первого антитела в способе двойных антител (I-1) и (II-1), и углеводородное соединение используют в качестве конкурентного вещества в способе конкуренции (I-3) или (II-3).
Кроме того, измеряемый компонент в образце можно измерять, используя биотинилированную нуклеиновую кислоту вместо биотинилированного белка. Примеры измеряемого компонента включают нуклеиновую кислоту, которая присоединяется к нуклеиновой кислоте, составляющей биотинилированную нуклеиновую кислоту, и белок, который присоединяется к нуклеиновой кислоте, составляющей биотинилированную нуклеиновую кислоту. Примеры белков включают вышеупомянутые белки. Измерения измеряемого компонента в образце с использованием биотинилированной нуклеиновой кислоты можно осуществлять, применяя обычные способы измерения нуклеиновых кислот, вышеупомянутые способы измерения и т.п.
5. Реагенты для измерения измеряемого компонента
Вариант осуществления реагента для измерения измеряемого компонента согласно настоящему изобретению представляет собой реагент, включающий связанные со стрептавидином магнитные частицы согласно настоящему изобретению и биотинилированный белок. Еще один вариант осуществления реагента для измерения измеряемого компонента согласно настоящему изобретению представляет собой реагент, включающий связанные с белком магнитные частицы согласно настоящему изобретению. Реагент для измерения измеряемого компонента согласно настоящему изобретению используют в способе измерения измеряемого компонента согласно настоящему изобретению. Примеры белков в биотинилированном белке и связанных с белком магнитных частицы включают вышеупомянутый белки.
Кроме того, измеряемый компонент в образце можно измерять, используя реагент, включающий связанные со стрептавидином магнитные частицы согласно настоящему изобретению и биотинилированное углеводородное соединение, или реагент, включающий связанные с углеводородными соединениями магнитные частицы, изготовленные из связанных со стрептавидином магнитных частиц согласно настоящему изобретению и биотинилированного углеводородного соединения. Примеры измеряемого компонента включают углеводородное соединение, составляющее биотинилированное углеводородное соединение, и антитело, которое присоединяется к углеводородному соединению. Примеры углеводородных соединений включают вышеупомянутые углеводородные соединения.
Кроме того, измеряемый компонент в образце можно измерять, используя реагент, включающий связанные со стрептавидином магнитные частицы согласно настоящему изобретению и биотинилированную нуклеиновую кислоту, или реагент, включающий связанные с нуклеиновыми кислотами магнитные частицы, изготовленные из связанных со стрептавидином магнитных частиц согласно настоящему изобретению, и биотинилированную нуклеиновую кислоту. Примеры измеряемого компонента включают нуклеиновую кислоту, которая присоединяется к нуклеиновой кислоте, составляющей биотинилированную нуклеиновую кислоту, и белок, который присоединяется к нуклеиновой кислоте, составляющей биотинилированную нуклеиновую кислоту. Примеры белков включают вышеупомянутые белки.
Реагент для измерения согласно настоящему изобретению может включать в качестве обязательного компонент, включенный в реагент для иммунологических измерений, который используют в обычных иммунологических анализах. Примеры компонента включают водную среду, соль, ионы металла, сахар, антисептическое вещество, вещество для подавления неспецифической реакции, поверхностно-активное вещество и стабилизатор фермента. Примеры водной среды включают вышеупомянутые водные среды. Примеры соли включают хлорид лития, хлорид натрия, хлорид калия, хлорид кальция, хлорид магния, хлорид аммония, бромид лития, бромид натрия, бромид калия, бромид кальция, бромид магния и бромид аммония. Примеры ионов металлов включают ионы магния, ионы марганца и ионы цинка. Примеры сахара включают маннит и сорбит. Примеры антисептического вещества включают азид натрия, антибиотики (стрептомицин, пенициллин, гентамицин и т.д.), BioAce и Proclin 300. Примеры вещества для подавления неспецифической реакции включают бычий сывороточный альбумин (BSA), эмбриональную бычью сыворотку (FBS), казеин и BlockAce (производитель Dainippon Pharmaceutical Co., Ltd.). Примеры поверхностно-активного вещества включают катионное поверхностно-активное вещество, анионное поверхностно-активное вещество, амфотерное поверхностно-активное вещество и неионное поверхностно-активное вещество. Примеры стабилизатора фермента включают стабилизирующий пероксидазу буферный раствор и стабилизирующий щелочную фосфатазу буферный раствор.
В представленной ниже части настоящего документа настоящее изобретение будет конкретно описано со ссылкой на примеры, которые не следует истолковывать как ограничивающие объем настоящего изобретения.
Пример 1
(1) Изготовление связанных со стрептавидином магнитных частиц
В качестве магнитных частиц использовали содержащие аминогруппы магнитные частицы типа Estapor EM2-100/40 (производитель Merck). Эти магнитные частицы имеют состоящую из ядра и оболочки структуру, размер этих частиц составляет 1,62 мкм, и они представляют собой частицы, в которой внутреннее ядро содержит магнитный материал, который составляет 41,2% суммарной массы, и в которой оболочечная часть содержит полистирол, химически модифицированный и содержащий 97 мкэкв/г аминогрупп. Собирали 2 мг магнитных частиц, и для диспергирования добавляли 4 мл 10 ммоль/л ацетатного буферного раствора при pH 5,5, содержащего 1,0% хлорида триметилстеариламмония (производитель Tokyo Chemical Industry Co., Ltd.) (далее называется «диспергирующая жидкость A»). После этого магнитные частицы собирали, помещая мощный магнит сбоку от контейнера, и диспергирующую жидкость удаляли путем всасывания (далее последовательность операций, включающих введение диспергирующей жидкости, сбор магнитных частиц и удаление путем всасывания для краткости называется «промывание»). После четырехкратного последовательного промывания частицы суспендировали в 10 ммоль/л ацетатном буферном растворе при pH 5,5, получая 30 мг/мл суспензию магнитных частиц в растворе. Растворы, содержащие 0,038%, 0,063%, 0,088% и 0,113% глутаральдегида, изготавливали, разбавляя 25% водный раствор глутаральдегида (производитель Nacalai Tesque) 10 ммоль/л ацетатным буферным раствором, имеющим pH 5,5. В качестве стрептавидина использовали рекомбинантный стрептавидин (производитель Roche), и раствор стрептавидина изготавливали, растворяя его в количестве 24,5 мг/мл в 10 ммоль/л ацетатном буферном растворе, имеющем pH 5,5. Раствор выдерживали при охлаждении до температуры льда в течение одного часа или более.
После этого 30 мкл раствора стрептавидина вводили в 66,7 мкл жидкости с диспергированными частицами, затем добавляли 30 мкл 0,038% раствора глутаральдегида и полученную смесь перемешивали, используя волновой ротор, при 35°C в течение 20 часов. Аналогичные операции осуществляли для растворов глутаральдегида, у которых концентрации составляли 0,063%, 0,088%, и 0,113%.
Полученные частицы десятикратно промывали, используя 50 ммоль/л буферный раствор MES (pH 6,5), содержащий 1,0% BS и 0,09% азида натрия, чтобы получать связанные со стрептавидином магнитные частицы.
(2) Измерение способности связывания биотина связанных со стрептавидином магнитных частиц
Способность связывания биотина определяли для вышеупомянутых связанных со стрептавидином магнитных частиц, полученных на стадии (1), и для имеющихся в продаже связанных со стрептавидином магнитных частиц, используя следующий способ.
Связанные со стрептавидином магнитные частицы диспергировали в количестве 1 мг/мл, используя 0,1% BSA-PBS [PBS представляет собой 10 ммоль/л фосфатный буферный раствор (pH 7,2), содержащий 0,15 моль/л хлорида натрия], и дисперсию разбавляли путем последовательного двукратного разбавления вплоть до шести ступеней (64-кратное разбавление), получая концентрацию 0,0156 мг/мл. Каждый из шести образцов и холостой раствор (0,1% BSA-PBS) помещали в виде аликвот по 50 мкл в 96-луночный планшет. После этого биотин-флуоресцеин (производитель Thermo Scientific) разбавляли до 1 мкг/мл, используя 0,1% BSA-PBS, и этот раствор помещали в виде аликвот по 50 мкл в лунки, содержащие распределенные образцы. Планшет, содержащий распределенные образцы, инкубировали при 37°C в течение десяти минут в процессе встряхивания, используя встряхиватель-инкубатор (производитель Amalyte), и интенсивности флуоресценции диспергированных частиц измеряли, используя считывающее планшеты флуоресцентное устройство Plate Chameleon V (производитель HIDEX).
Когда на данной стадии флуоресцентный маркированный биотин присоединяется к стрептавидину на магнитных частицах, молекулы флуоресцентного маркированного биотина, присоединенные к молекулам стрептавидина, будут находиться близко друг к другу, и происходит гашение флуоресценции. Гашение флуоресценции увеличивается по мере того, как увеличивается в расчете на единицу площади количество флуоресцентного маркированного биотина, присоединенного к стрептавидину, связанному с магнитными частицами. Используя данное свойство, заблаговременно определяли скорость уменьшения флуоресценции, используя в качестве стандарта имеющиеся в продаже магнитные частицы с известной способностью связывания биотина и вычисляя способность связывания биотина связанных со стрептавидином магнитных частиц согласно настоящему изобретению. В данном примере концентрацию связанных со стрептавидином магнитных частиц при уменьшении интенсивности флуоресценции на 50% вычисляли посредством прямолинейной аппроксимации, используя разбавление образцов связанных со стрептавидином магнитных частиц, и способность связывания биотина (пмоль/мм2) вычисляли путем сравнения со способностью связывания стандартных связанных со стрептавидином магнитных частиц.
Результаты измерений представлены в таблице 1.
(производитель Merck)
Как ясно следует из Таблицы 1, оказалось, что вышеупомянутые связанные со стрептавидином магнитные частицы, полученные на стадии (1), имеют высокую способность связывания биотина по сравнению с имеющимися в продаже связанными со стрептавидином магнитными частицами Dynabeads T1 (производитель Dynal) и BE-M08/10 (производитель Merck).
Пример 2
Анализ сшитой структуры стрептавидина на магнитных частицах
Использовали связанные со стрептавидином магнитные частицы, у которых способность связывания биотина составляла 2,61 пмоль/мм2, 4,95 пмоль/мм2 и 6,76 пмоль/мм2 и которые получали способом, аналогичным способу примера 1. Соответствующие связанные со стрептавидином магнитные частицы десятикратно промывали, используя по 4 мл PBS, и после замены PBS раствором 1% SDS/PBS осуществляли инкубацию при 60°C в течение одного часа. После этого магнитные частицы собирали с помощью магнита и после сбора надосадочного раствора белка надосадочный раствор подвергали анализу посредством SDS-PAGE. Аналогичную операцию осуществляли, используя имеющиеся в продаже связанные со стрептавидином магнитные частицы. Результаты анализа SDS-PAGE представлены на Фиг.1.
Как четко представляет Фиг.1, в то время как только мономеры, составляющие стрептавидин, наблюдали в случае стрептавидина и имеющихся в продаже связанных со стрептавидином магнитных частиц, наблюдали полоски димеров, тримеров, тетрамеров и олигомеров более высокого порядка при введении в полоску мономеров связанных со стрептавидином магнитных частиц согласно настоящему изобретению. Это показывает, что в имеющихся в продаже связанных со стрептавидином магнитных частицах из молекул стрептавидина не образуется сшитая структура, в то время как в связанных со стрептавидином магнитных частицах согласно настоящему изобретению молекулы стрептавидина образуют сшитую структуру.
Пример исследования 1. Исследование диспергируемости связанных со стрептавидином магнитных частиц
Связанные со стрептавидином магнитные частицы, имеющие способность связывания биотина 4,54 пмоль/мм2, которые были изготовлены способом, аналогичным примеру 1, диспергировали при содержании 0,1 мг/мл в PBS, содержащем 0,1% BSA, и дисперсию выдерживали в прохладном темном месте в течение 24 часов. После перемешивания посредством 25-кратного переворачивания сравнивали степени дисперсии. Результаты представлены на Фиг.2. На Фиг.2 верхняя фотография представляет статическое состояние связанных со стрептавидином магнитных частиц, и нижняя фотография представляет диспергированное состояние связанных со стрептавидином магнитных частиц после перемешивания посредством 25-кратного переворачивания.
Как четко показывает Фиг.2, оказалось, что связанные со стрептавидином магнитные частицы согласно настоящему изобретению имеют очень хорошие дисперсионные свойства.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Настоящее изобретение предлагает связанные со стрептавидином магнитные частицы, имеющие высокую способность связывания биотина, и способ их изготовления, связанные с белком магнитные частицы, изготовленные с использованием связанных со стрептавидином магнитных частиц, и способ их изготовления, способ измерения измеряемого компонента и реагент для измерения измеряемого компонента. Связанные со стрептавидином магнитные частицы и связанные с белком магнитные частицы, изготовленные способом изготовления согласно настоящему изобретению, а также способ измерения измеряемого компонента и реагент для измерения измеряемого компонента согласно настоящему изобретению можно использовать в клинической диагностике.
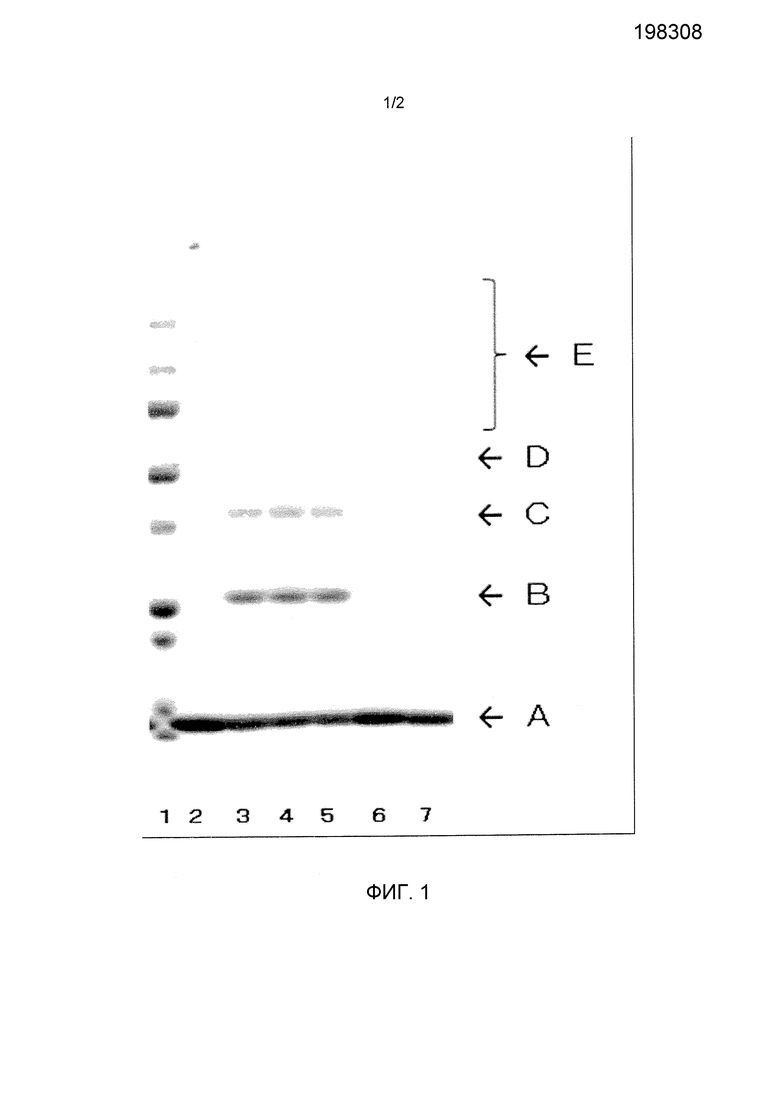
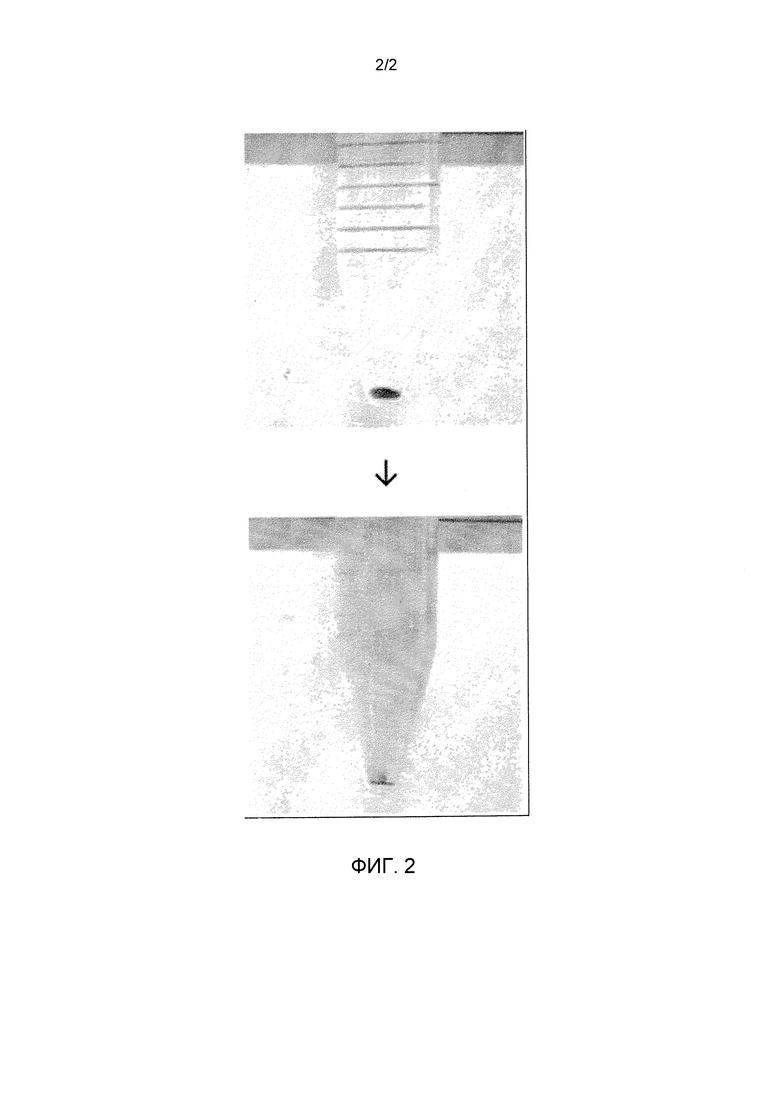
Группа изобретений предлагает связанные со стрептавидином магнитные частицы, имеющие высокую способность связывания биотина, и способ их изготовления. Связанная со стрептавидином магнитная частица имеет структуру, в которой молекулы стрептавидина сшиты друг с другом на магнитной частице, где связанную со стрептавидином магнитную частицу изготавливают способом, включающим следующие стадии: (1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы; и (2) реакция магнитных частиц со стрептавидином и глутаральдегидом путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1). Настоящая группа изобретений может быть эффективно использована в клинической диагностике. 9 н. и 2 з.п. ф-лы, 2 ил., 1 табл., 2 пр.
1. Связанная со стрептавидином магнитная частица, имеющая структуру, в которой молекулы стрептавидина сшиты друг с другом на магнитной частице, где связанную со стрептавидином магнитную частицу изготавливают способом, включающим следующие стадии:
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы; и
(2) реакция магнитных частиц со стрептавидином и глутаральдегидом путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1).
2. Связанная со стрептавидином магнитная частица по п. 1, которую изготавливают способом, дополнительно включающим следующую стадию (3):
(3) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (2), с восстановителем.
3. Связанная с белком магнитная частица, которую изготавливают с использованием связанной со стрептавидином магнитной частицы по п. 1 или 2, и биотинилированный белок, где белок связан с магнитной частицей посредством взаимодействия стрептавидина на магнитной частице и биотина, связанного с белком.
4. Способ измерения измеряемого компонента в образце, в котором используют связанную с белком магнитную частицу по п. 3, где образец выбран из группы, состоящей из цельной крови, плазмы, сыворотки, спинномозговой жидкости, слюны, амниотической жидкости, мочи, пота и поджелудочного сока.
5. Способ измерения измеряемого компонента в образце, в котором используют связанную со стрептавидином магнитную частицу по п. 1 или 2 и биотинилированный белок, где образец выбран из группы, состоящей из цельной крови, плазмы, сыворотки, спинномозговой жидкости, слюны, амниотической жидкости, мочи, пота и поджелудочного сока.
6. Реагент для измерения измеряемого компонента в образце, который включает связанную с белком магнитную частицу по п. 3, где образец выбран из группы, состоящей из цельной крови, плазмы, сыворотки, спинномозговой жидкости, слюны, амниотической жидкости, мочи, пота и поджелудочного сока.
7. Реагент для измерения измеряемого компонента в образце, который включает связанную со стрептавидином магнитную частицу по п. 1 или 2 и биотинилированный белок, где образец выбран из группы, состоящей из цельной крови, плазмы, сыворотки, спинномозговой жидкости, слюны, амниотической жидкости, мочи, пота и поджелудочного сока.
8. Способ изготовления связанных со стрептавидином магнитных частиц, который включает следующие стадии:
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы; и
(2) реакция магнитных частиц со стрептавидином и глутаральдегидом путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1).
9. Способ изготовления по п. 8, дополнительно включающий следующую стадию (3):
(3) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (2), с восстановителем.
10. Способ изготовления связанных с белком магнитных частиц по п. 3, который включает следующие стадии:
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы;
(2) изготовление связанных со стрептавидином магнитных частиц путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1); и
(3) реакция связанных со стрептавидином частиц, изготовленных на стадии (2), с биотинилированным белком.
11. Способ изготовления связанных с белком магнитных частиц, который включает следующие стадии:
(1) изготовление суспензии, содержащей магнитные частицы, на поверхности которых находятся аминогруппы;
(2) изготовление связанных со стрептавидином магнитных частиц путем введения глутаральдегида в присутствии стрептавидина в суспензию, изготовленную на стадии (1);
(3) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (2), с восстановителем; и
(4) реакция связанных со стрептавидином магнитных частиц, изготовленных на стадии (3), с биотинилированным белком.
| WO03089906, 30.10.2003 | |||
| WO9704862 А1, 13.02.1997 | |||
| WO2005118870, 15.12.2005 | |||
| US20070059763, 15.03.2007 | |||
| SAI N | |||
| et al | |||
| A sensitive immunoassay based on direct hapten coated format and biotin-streptavidin system for the detection of chloramphenicol | |||
| Talanta | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| ПИШУЩАЯ МАШИНА ДЛЯ ШИФРОВАННОЙ КОРРЕСПОНДЕНЦИИ | 1922 |
|
SU1113A1 |
| SIMA V.H | |||
| et al | |||
| Tyrosinase immobilized magnetic nanobeads for the amperometric assay of enzyme inhibitors: application to the skin whitening agents | |||
| Talanta | |||
| Способ приготовления лака | 1924 |
|
SU2011A1 |
| Устройство для избирательного управления с одного конца линии несколькими реле | 1918 |
|
SU980A1 |
| SKOTTRUP P.D | |||
| et al | |||
| Superparamagnetic bead interactions with functionalized surfaces characterized by an immunomicroarray | |||
| Acta Biomater | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Машина для изготовления проволочных скрепок для бумаг | 1924 |
|
SU3936A1 |
| AL-HAKIM AH, HULL R | |||
| Studies towards the development of chemically synthesized non-radioactive biotinylated nucleic acid hybridization probes | |||
| Nucleic Acids Res | |||
| Пневматический водоподъемный аппарат-двигатель | 1917 |
|
SU1986A1 |
| Способ получения асфальтового битума из содержащих таковой песчаников | 1927 |
|
SU9965A1 |
Авторы
Даты
2017-01-23—Публикация
2012-02-15—Подача