Изобретение касается нового медицинского применения 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида, улучшенной фармацевтически приемлемой соли 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида и их композиций.
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид является ингибитором потенциалзависимого натриевого канала (NaV), особенно более ингибитором NaV1.7, и описан как Пример 788 в Международной патентной заявке с номером публикации WO 2010/079443, полное содержание которой включено сюда посредством ссылки. Как ингибитор NaV1.7, упомянутое соединение потенциально полезно при лечении широкого спектра расстройств, особенно боли, включая: острую боль; хроническую боль; невропатическую боль; воспалительную боль; висцеральную боль; ноцицептивную боль, включая послеоперационную боль; и смешанные типы боли, включающие боль внутренних органов, желудочно-кишечного тракта, черепных структур, костно-мышечной системы, позвоночника, мочеполовой системы, сердечнососудистой системы и ЦНС, включая раковую боль, боль в пояснице и орофациальную боль.
Мочевая кислота является конечным продуктом метаболизма пурина у людей. У людей, в отличие от других животных, мочевая кислота далее не разрушается, а преимущественно (70%) выводится с мочой, оставшаяся часть 30% выводится с калом. Гиперурикемия определяется как чрезмерное продуцирование или уменьшенное выведение мочевой кислоты и может иметь место как чрезмерное продуцирование или недостаточное выведение сывороточной мочевой кислоты (sUA), или комбинация обеих. Проблемы с почечным выведением мочевой кислоты являются первичной причиной гиперурикемии в приблизительно 90% случаях, в то время как чрезмерное продуцирование является причиной в меньше, чем 10%. Повышение концентрации sUA выше чем 6,8 мг/дл приводит к кристаллизации мочевой кислоты в форме солей, таких как мононатрий урат, и осаждению этих кристаллов в суставах, на сухожилиях и в окружающих тканях. Эти кристаллы (известны как тофус) запускают локальную имунноопосредованную воспалительную реакцию, приводя к подагре. Риск подагры увеличивается с увеличением уровней sUA.
Проблемы с почечным выведением мочевой кислоты являются первичной причиной гиперурикемии в приблизительно 90% случаях, в то время как чрезмерное продуцирование является причиной в меньше, чем 10%. Риск подагры увеличивается с увеличением уровней мочевой кислоты.
Подагра является болезненным состоянием, которое может проявляться несколькими симптомами, хотя наиболее обычными являются повторяющиеся приступы острого воспалительного артрита (красный, чувствительный, горячий, опухший сустав), часто встречающегося на больших пальцах ног, пятках, коленях, запястьях и пальцах.
Подагра лечится с помощью агентов, уменьшающих причину и воспалительное и болевое действие кристаллов мочевой кислоты.
Боль, связанная с подагрой, обычно лечится с помощью противоболевых и противовоспалительных лекарственных средств, таких как нестероидные противовоспалительные лекарственные средства (NSAID), колхицин и стероиды. Агенты, уменьшающие уровни sUA, могут быть использованы для лечения причины подагры. Ими являются следующие агенты: ингибиторы ферментов, способствующих образованию мочевой кислоты, такие как ингибиторы ксантиноксидазы (например, аллопуринол, фебуксостат или тисопурин) или ингибитор пуриннуклеозидфосфорилазы (PNP) (например, улодезин); агенты, метаболизирующие мочевую кислоту, такие как уратоксидаза - также известна как уриказа (например, пеглотиказа); или средство, способствующее выведению мочевой кислоты с мочой (урикозурики). Урикозурики включают агенты, ингибирующие транспортеры, отвечающие за почечную реабсорбцию мочевой кислоты в кровь, такие как бензиодарон, изоброминдион, пробенецид и сульфинпиразон, или ингибиторы URAT-1 (например, бензбромарон).
URAT-1 также известен как транспортер растворенных веществ семейства 22 (транспортер органического аниона/катиона), член 12, и кодируемый геном SLC22A12. Анализ генома человека показал, что полиморфизм в SLC22A12 гене, непосредственно связан с изменениями сывороточной мочевой кислоты. Кроме того, ингибиторы транспорта мочевой кислоты, такого как URAT-1, являются эффективными при лечении подагры.
Все еще существует потребность в новых подходах к лечению подагры, которые являются более эффективными и/или более толерантными.
Неожиданно, было установлено, что 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид уменьшает уровни мочевой кислоты в крови. Как тут показано, 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид является ингибитором URAT-1. Эта способность снижать уровни мочевой кислоты обговаривается более детально тут далее со ссылкой на данные в Таблицах 5 - 9 и Фиг. 7 и 8. Эти данные были получены при использовании оральных дисперсий, полученных из 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида и его тозилатной соли.
Кроме того, 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид полезен при лечении заболеваний, связанных с высокими уровнями мочевой кислоты в крови, таких как гиперурикемия, включая почечные расстройства, связанные с гиперурикемией (например, мочевой конкремент); и подагра, включая подагрический тофус и подагрический артрит. Также следует, что 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид полезен при лечении заболеваний, при которых показан ингибитор URAT-1.
В первом аспекте изобретения обеспечивается 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемая соль для лечения заболевания, связанного с повышенными уровнями мочевой кислоты в крови.
В одном из воплощений заболеванием, связанным с повышенными уровнями мочевой кислоты в крови, является гиперурикемия.
В другом воплощении заболеванием, связанным с повышенными уровнями мочевой кислоты в крови, является подагра.
В другом аспекте изобретения обеспечивается 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемая соль для лечения заболевания, при котором показан ингибитор URAT-1.
В другом аспекте изобретения обеспечивается применение 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида или его фармацевтически приемлемой соли при изготовлении медикамента для лечения заболевания, связанного с повышенными уровнями мочевой кислоты в крови.
В другом аспекте изобретения обеспечивается применение 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида или его фармацевтически приемлемой соли при изготовлении медикамента для лечения заболевания, при котором показан ингибитор URAT-1.
В другом аспекте изобретения обеспечивается способ лечения заболевания, связанного с повышенными уровнями мочевой кислоты в крови, который включает назначение эффективного количества 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида или его фармацевтически приемлемой соли.
В другом аспекте изобретения обеспечивается способ лечения заболевания, при котором показан ингибитор URAT-1, который включает назначение эффективного количества 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида или его фармацевтически приемлемой соли.
Неожиданно было найдено, что тозилатная соль 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида имеет ряд неожиданных свойств, что делает ее особенно пригодной для получения фармацевтически приемлемых рецептур. Тозилатная соль проявляет лучшую химическую стабильность по сравнению со свободным основанием, в частности касательно формулирования и хранения. Она также может быть получена в кристаллической форме, обеспечивающей лучшую стабильность твердой формы, нежели свободное основание. Неожиданно тозилатная соль проявляет лучшую стабильность касательно диссоциации, нежели другие соли, а также демонстрирует хорошую растворимость в воде.
Соответственно в другом аспекте изобретения обеспечивается тозилатная соль 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида.
В одном из воплощений тозилатная соль 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида является кристаллическим веществом.
В другом воплощении кристаллическое вещество характеризуется порошковой рентгенограммой (PXRD), которая имеет любые три, четыре, пять или шесть характеристических два тета (2θ) пиков, которые выбирают из группы пиков, определенных в Таблицах 4 и 4a, приведенных ниже, при использовании рентгеновского излучения CuKalpha1 (длина волны =1,5406 Å).
В дополнительном воплощении кристаллическое вещество характеризуется PXRD, которая имеет любые три, четыре, пять или шесть характеристических 28 пиков, которые выбирают из группы, включающей: 9,0, 9,3, 10,0, 10,7, 11,6, 12,5, 12,9, 13,2, 13,8, 14,4, 16,0, 16,6, 17,5, 17,8, 18,1, 21,4 и 23,4θ (±0,2° 2θ), более предпочтительно из группы, включающей: 9,0, 9,3, 10,0, 10,7, 11,6, 12,9, 13,2, 16,0, 16,6, 17,5, 17,8, 18,1, 21,4 и 23,4° (±0,2° 2θ), наиболее предпочтительно из группы, включающей: 11,6, 12,9, 16,0, 17,5, 17,8, 18,1° (±0,2° 2θ) при использовании рентгеновского излучения CuKalpha1 (длина волны =1.5406 Å).
В другом воплощении кристаллическое вещество характеризуется порошковой рентгенограммой (PXRD), которая имеет основные два тета (28) пики при 9,0, 10,7, 16,0, 21,4 и 23,4° (±0,1° 2θ) при использовании рентгеновского излучения CuKalphal (длина волны=1,540562 Å).
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемая соль, такая как тозилатная соль, обычно вводят как рецептуры в комбинации с одним или более фармацевтически приемлемыми эксципиентами. Термин 'эксципиент' используется здесь для описания любого ингредиента, отличного от упомянутого выше бензолсульфонамида. Выбор эксципиента будет в большей степени зависеть от факторов, таких как определенный путь введения, влияние эксципиента на растворимость и стабильность и природа дозированной формы.
В другом аспекте изобретения обеспечивается фармацевтическая композиция, которая содержит тозилатную соль 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида вместе с одним или более фармацевтически приемлемыми эксципиентами.
Фармацевтические композиции, пригодные для высвобождения 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида или его фармацевтически приемлемой соли, такой как тозилатная соль, и способы их получения будет очевидны среднему специалисту в этой области техники. Такие композиции и способы можно найти, например, в "Remington's Pharmaceutical Sciences", 19th Edition (Mack Publishing Company, 1995). Пригодными путями введения является оральное, парентеральное, местное, ингаляционное/интраназальное, ректальное/интравагинальное и окулярное/ауральное введение.
Рецептуры, пригодные для упомянутых выше способов введения, можно сформулировать для немедленного и/или модифицированного высвобождения. Рецептуры модифицированного высвобождения включают отсроченное-, длительное-, пульсирующее-, контролированное-, нацеленное и программируемое высвобождение.
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемую соль, такую как тозилатная соль, можно вводить перорально. Пероральное введение может включать заглатывание, так что соединение попадает в желудочно-кишечный тракт, или букальное, или сублингвальное введения, при которых соединение попадает в кровоток непосредственно из ротовой полости. Композиции, пригодные для перорального введения, включают твердые композиции, такие как таблетки, капсулы, которые содержат частицы, жидкости или порошки; лозенги (включая наполненные жидкостью), жвачки, мульти- или наночастицы, гели, твердые растворы, липосомы, пленки, овулы, спреи, жидкие рецептуры и букальные/мукоадгезивные пластыри.
Жидкие композиции охватывают суспензии, растворы, сиропы и эликсиры. Такие композиции можно применять как наполнители мягких или твердых капсул и обычно они содержат носитель, например воду, этанол, полиэтиленгликоль, пропиленгликоль, метилцеллюлозу или пригодное масло, и один или более эмульгаторов и/или суспендирующих агентов. Жидкие композиции также можно получить восстановлением твердого вещества, например саше.
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемую соль, такую как тозилатная соль, также можно применять в форме быстрорастворимых, быстрораспадаемых форм, таких, как описано в Expert Opinion in Therapeutic Patents, 11 (6), 981-986, by Liang and Chen (2001).
Для таблетированных дозированных форм в зависимости от дозы 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемая соль, такая как тозилатная соль, лекарственное средство может составлять от 1 мас.% до 80 мас.% дозированной формы, более типично от 5 мас.% до 60 мас.% дозированной формы. Дополнительно к лекарственному средству таблетки обычно содержат дезинтегрант. Примерами дезинтегрантов являются натрий крахмалгликолят, натрий карбоксиметилцеллюлоза, кальций карбоксиметилцеллюлоза, натрий кроскармеллоза, кросповидон, поливинилпирролидон, метилцеллюлоза, микрокристаллическая целлюлоза, замещенная низшим алкилом гидроксипропилцеллюлоза, крахмал, предварительно желатинизированный крахмал и альгинат натрия. Вообще, дезинтегрант будет составлять от 1 мас.% до 25 мас.%, преимущественно от 5 мас.% до 20 мас.% дозированной формы.
Связывающие агенты обычно используются для придания качества композиции таблетки. Пригодными связывающими агентами являются микрокристаллическая целлюлоза, желатин, сахара, полиэтиленгликоль, природные и синтетические смолы, поливинилпирролидон, предварительно желатинизированный крахмал, гидроксипропилцеллюлоза и гидроксипропилметилцеллюлоза. Таблетки также могут содержать разбавители, такие как лактоза (моногидрат, высушенный распылением моногидрат, безводную и т.д.), маннит, ксилит, декстрозу, цукрозу, сорбит, микрокристаллическую целлюлозу, крахмал и дигидрат дигидрофосфата кальция.
Таблетки необязательно также могут содержать поверхностно-активные агенты, такие как лаурилсульфат натрия и полисорбат 80, и глиданты, такие как диоксид кремния и тальк. Когда присутствуют, поверхностно-активные агенты могут составлять от 0,2 мас.% до 5 мас.% таблетки, и глиданты могут составлять от 0,2 мас.% до 1 мас.% таблетки.
Таблетки также, вообще, содержат смазывающие агенты, такие как стеарат магния, стеарат кальция, стеарат цинка, стеарилфумарат натрия и смеси, стеарата магния с лаурилсульфатом натрия. Смазывающие агенты обычно составляют от 0,25 мас.% до 10 мас.%, преимущественно от 0,5 мас.% до 3 мас.% таблетки. Другими возможными ингредиентами являются антиоксиданты, красители, ароматизаторы, консерванты и агенты, маскирующие вкус.
Типичные таблетки содержат приблизительно до 80% лекарственного средства, от приблизительно 10 мас.% до приблизительно 90 мас.% связывающего агента, от приблизительно 0 мас.% до приблизительно 85 мас.% разбавителя, от приблизительно 2 мас.% до приблизительно 10 мас.% дезинтегрантов и от приблизительно 0,25 мас.% до приблизительно 10 мас.% лубриканта. Таблеточные смеси можно прессовать непосредственно или роликом для формирования таблеток. Таблеточные смеси или порции смесей альтернативно могут быть подвергнуты влажному, сухому гранулированию или гранулированию расплава, замораживанию расплава или экструдированию перед таблетированием. Конечные композиции могут содержать один или более слоев и могут иметь покрытие или не иметь покрытия; они даже могут быть инкапсулированы. Составы таблеток рассмотрены в Pharmaceutical Dosage Forms: Таблица ts, Vol. 1, by H. Lieberman and L. Lachman (Marcel Dekker, New York, 1980).
Композиции пригодного модифицированного высвобождения для целей изобретения описаны в патенте US 6106864. Подробности технологий другого приемлемого высвобождение, такого как высокоэнергетические дисперсии, осмотические и покрытые частицы, можно найти в Pharmaceutical Technology On-line, 25(2), 1-14, by Verma et al. (2001). Применение жвачек для обеспечения контролируемого высвобождения описано в WO 00/35298.
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемая соль, такая как тозилатная соль, также могут быть введены непосредственно в кровоток, в мышцу или во внутренний орган. Пригодные способы парентерального введения включают внутривенное, внутриартериальное, интраперитонеальное, интратекальное, интравентрикулярное, интрауретральное, интрастернальное, интракраниальное, внутримышечное и подкожное введение. Пригодными устройствами для парентерального введения являются иголочные (включая микроиголочные) инжекторы, безиголочные инжекторы и техники вливания.
Парентеральные композиции типично являются водными растворами, которые могут содержать наполнители, такие как соли, углеводы и буферирующие агенты (предпочтительно до pH 3-9), но, для некоторых применений, они могут быть более пригодно сформулированы как стерильный неводный раствор или как сухая форма для применения в сочетании с пригодным наполнителем, таким как стерильная свободная от пирогена вода.
Получение парентеральных композиций в стерильных условиях, например лиофилизацией, можно легко осуществить, применяя обычные фармацевтические способы, хорошо известные специалистам в этой области техники.
Растворимость 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида или его фармацевтически приемлемой соли, такой как тозилатная соль, используемых при получении парентеральных растворов, можно повысить путем использования пригодных способов получения композиции, таких как введение средств, которые повышают растворимость. Композиции для парентерального применения можно компоновать для непосредственного и/или модифицированного высвобождения. Модифицированное высвобождение композиции охватывают отсроченное, длительное, пульсирующее, контролируемое, целевое и программируемое высвобождение.
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемую соль, такую как тозилатная соль, также можно наносить местно на кожу или слизистую оболочку, то есть дермально или трансдермально. Типичные композиции для этой цели включают гели, гидрогели, лосьоны, растворы, кремы, мази, присыпки, повязки, пены, пленки, пластыри на кожу, облатки, имплантаты, тампоны, волокна, бандажи и микроэмульсии. Также можно применять липосомы. Типичные носители включают спирт, воду, минеральное масло, жидкий вазелин, белый вазелин, глицерин, полиэтиленгликоль и пропиленгликоль. Можно вводить промоторы проникновение, см., например, J Pharm Sci, 88 (10), 955-958, by Finnin and Morgan (October, 1999).
Другие способы местного применения включают введение с помощью электропорации, ионтофореза, фонофореза, сонофореза и микроиголочной или безиголочной инъекции (например, Powderject™, Bioject™ и т.д.).
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемую соль, такую как тозилатная соль, также можно вводить интраназально или с помощью ингаляции, типично в форме сухого порошка (как таковые или как смесь, например, в форме сухой смеси с лактозой, или форме частицы из смешанных составляющих, например, смешанных с фосфолипидами, такими как фосфатидилхолин) из ингалятора с сухим порошком, как аэрозольный спрей из контейнера под давлением, насоса, спрея, пульверизатора (предпочтительно пульверизатора с применением электрогидродинамики для получения тонкого тумана) или распылителя, с применением или без применения пригодного пропелланта, такого как 1,1,1,2-тетрафторэтан или 1,1,1,2,3,3,3-гептафторпропан. Порошок для интраназального применения может содержать биоадгезивное средство, например хитозан или циклодекстрин.
Контейнер с повышенным давлением, насос, спрей, пульверизатор или распылитель содержат раствор или суспензию соединения(соединений) изобретения, которые содержат как растворитель, например, этанол, водный этанол или пригодное альтернативное средство, для диспергирования, солюбилизации или увеличения времени высвобождения активного агента, пропеллант(ы) как растворитель, и необязательно поверхностно-активное вещество, такое как триолеатсорбита, олеиновая кислота или олигомолочная кислота.
Перед применением в форме композиции сухого порошка или суспензии лекарственный продукт тонко измельчают до размера, пригодного для высвобождения ингаляцией (типично меньше чем 5 микрон). Это можно осуществить любым пригодным способом измельчение, таким как винтовая струйная мельница, измельчение в потоковой мельнице с псевдосжиженным слоем, обработка сверхкритической жидкостью с образованием наночастиц, гомогенизация при условиях высокого давления или сушка распылением.
Капсулы (изготовленные, например, из желатина или гидроксипропилметилцелюлозы), блистеры и картриджи для применения в ингаляторе или инсуффляторе можно формулировать для включения порошковой смеси соединения изобретения, пригодного порошкового основания, такого как лактоза или крахмал, и модификатора распыления, такого как I-лейцин, маннит или стеарат магния. Лактоза может быть безводной или в форме моногидрата, преимущественно последней. Другие пригодные наполнители включают декстран, глюкозу, мальтозу, сорбит, ксилит, фруктозу, цукрозу и трехалозу.
Пригодные ароматизаторы, такие как ментол и левоментол, или подсластители, такие как сахарин или натрий сахарин, можно добавлять к этой композиции изобретения, предназначенной для ингаляционного/интраназального введения.
В случае сухих порошковых ингаляторов и аэрозолей единичная доза определяется типом клапана, который высвобождает определенное количество. Единицы согласно изобретению, конечно, являются отрегулированными для введения отмеренной дозы или "пшика", который содержит от 1 мкг до 100 мг соединения формулы (I). Общую суточную дозу типично в интервале от 1 мкг до 200 мг можно вводить как единичную дозу или, более конечно, как разделенные дозы на протяжении суток.
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемая соль, такая как тозилатная соль, также можно вводить непосредственно в глаз или ухо, типично в форме капель, тонкоизмельченной суспензии или раствора в изотоническом, pH-корригированном стерильном физрастворе. Другие композиции, пригодные для глазного и ушного введения, включают мази, биоразлагаемые (например, абсорбируемые гелевые губки, коллаген) и бионеразлагаемые (например, силиконовые) имплантаты, тампоны, линзы и дольковые и пузырчатые системы, такие как ниосомы или липосомы. Полимер, такой как поперечносшитая полиакриловая кислота, поливиниловый спирт, гиалуроновая кислота, целлюлозный полимер, например гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза или метилцеллюлоза, или гетерополисахаридный полимер, например гелановая смола, можно вводить вместе с консервантом, таким как бензалконий хлорид. Такие композиции также можно вводить ионтофорезом.
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемая соль, такая как тозилатная соль, можно комбинировать с растворимыми макромолекулярными веществами, такими как циклодекстрин и его пригодные производные или полиэтиленгликольсодержащие полимеры, для того чтобы улучшить их растворимость, скорость растворения, улучшить вкус, биоусваивание и/или стабильность для использования в любых вышеупомянутых способах применения.
Например, найдено, что комплексы лекарственное средство - циклодекстрин вообще являются полезными для большинства форм дозирования и путей введения. Можно использовать комплексы включения и невключения. Как альтернативу прямому комплексообразованию с лекарственным средством можно использовать циклодекстрин как вспомогательную добавку, то есть как носитель, разбавитель или солюбилизатор. С этой целью в большинстве случаев используют альфа-, бета- гамма-циклодекстрины, например, которые можно найти в Международных патентных заявках № WO 91/11172, WO 94/02518 и WO 98/55148.
Для введения людям общая суточная доза 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида или его фармацевтически приемлемой соли, такой как тозилатная соль, типично находится в интервале от 1 мг до 10 г, например от 10 мг до 1 г, например от 25 мг до 500 мг, конечно, в зависимости от пути введения и эффективности. Общая суточная доза может вводиться в единичной или разделенной дозах и может, по решению врача, быть уменьшена ниже предоставленного здесь диапазона, в зависимости от возраста, массы и ответа определенного пациента.
4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемую соль, такую как тозилатная соль, может быть полезно объединять с другими фармакологически активными соединениями или с двумя или большим количеством других фармакологически активных соединений, особенно для лечения подагры. Такие комбинации часто имеют значительные преимущества, включая восприятие пациентами, легкость дозирования и синергическую активность.
В комбинациях, которые приведены дальше, соединение изобретения может вводиться одновременно, последовательно или раздельно в комбинации с другим терапевтическим агентом или агентами.
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид или его фармацевтически приемлемую соль, такую как тозилатная соль, можно вводить в комбинации с одним или большим количеством агентов, которые выбирают из:
- противовоспалительного лекарственного средства, такого как NSAID (например, целекоксиб), колхицин или стероид;
- ингибитора ксантиноксидазы (например, аллопуринол, фебуксостат или тисопурин) или ингибитора пуриннуклеозидфосфорилазы (PNP) (например, улодезин);
- уриказы (например, пеглотиказа или расбуриказа); или
- средства, способствующего выведению мочевой кислоты, такого как агент, ингибирующий транспортеры, отвечающие за почечную реабсорбцию мочевой кислоты в кровь, такой как бензиодарон, изоброминдион, пробенецид и сульфинпиразон, или ингибитор URAT-1 (например, бензбромарон).
Должно быть понятно, что все ссылки тут на лечение включают исцеляющее, смягчающее и профилактическое лечение.
4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид можно получить с помощью любого способа, известного в этой области для получения соединений аналогичной структуры, и, в частности, используя способы описанные в WO 2010/079443, такой как, показанный в Примере 788.
Изобретение иллюстрируется следующими неограничивающими примерами.
Пример 1
Получение тозилата 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида
К 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамиду (пример 788 WO 2010/079443, 36,75 г, 73,45 ммоль) в этилацетате (20 мг/г, 735 мл) прибавляли метанол (3 мл/г, 110,25 мл) и смесь нагревали до 50°C. К реакционной смеси на протяжении 6 минут из капельной воронки прибавляли раствор моногидрата п-толуолсульфоновой кислоты (13,27 г, 69,77 ммоль) в метаноле (2 мл/г, 73,50 мл), после чего прибавляли еще метанол (1 мл/г, 36,75 мл). Реакционную смесь охлаждали до комнатной температуры, фильтровали в вакууме и твердое вещество промывали этилацетат:метанол (9:1, 2×37 мл). Твердое вещество сушили в вакууме при 50°С на протяжении ночи, получая указанное в заголовке соединение как свободно текучее почти белое твердое вещество (43,99 г, 65,41 ммоль, 89%).
Далее приведены детали спектроскопического анализа тозилатной соли 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида:
Инфракрасная (ИК) спектроскопия
Снимали спектр инфракрасной абсорбции, используя однократное отражение Нарушенного Полного Отражения (ATR). Спектр получали при разрешении 4 см-1, используя ИК спектрометр ThermoNicolet Avatar 360 FT и добавочный Smart Golden Gate™. Этот подход не требует получения образца. Спектр показан на Фиг. 1.
Масс-спектрометрия (МС)
Полные сканированные масс-спектры показаны на Фиг. 2 и Фиг. 3 и были получены с помощью позитивной (ЭС+) и негативной (ЭС-) электроспрей ионизации. Данные снимали, используя масс-спектрометр Bruker MaXis Quadrupole Time of Flight, снабженный источником электрораспыления. Проводили внутреннюю калибровку, используя раствор формиата натрия, который давал наблюдаемое максимальное отклонение массы 0,2 мДа (ЭС+) и 0,3 мДа (ЭС-) в интервале масс от m/z 113 до m/z 997.
Точная измеренные масса, теоретическая моноизотопная масса и молекулярная формула наблюдаемого аддукта и фрагментарных ионов для ЭС+ и ЭС- данных показаны в Таблицах 1 и 2 соответственно. Соответствующие масс-спектры показаны на Фиг. 2 и 3 соответственно.


Спектроскопия Ядерного Магнитного Резонанса (ЯМР)
Спектр ядерного (1H) ЯМР снимали в растворе в ДМСО d6. Данные получали при 30°С на ЯМР спектрометре Bruker AVANCE III 600 МГц, снабженном криогенным зондом тройного резонанса, настроенном на протоны при 599,77 МГц. Спектр снимали относительно ДМСО d5 (2,50 м.д.).
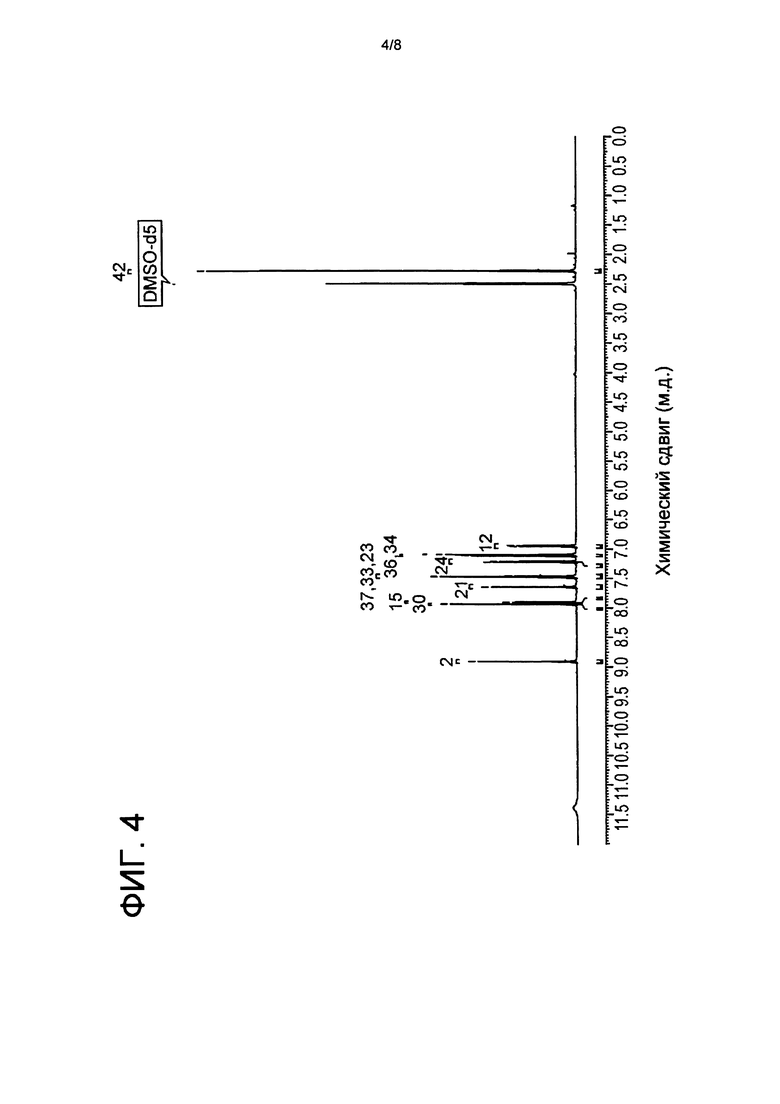
1H ЯМР спектр, показанный на Фиг. 4 и соответствующий приведенной ниже структуре, имеет 12 ароматических и три алифатических (одна CH3 группа) протонов. Соотнесенные 1H химические сдвиги сведены в Таблице 3.

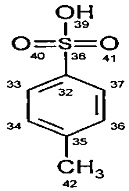

Ультрафиолетовая/Видимая (УФ/Вид) спектрофотомерия
Снимали спектр УФ/Видимый, используя спектрофотометр Hitachi U-3000 в метаноле при концентрации 1,09 мг/100 мл,и он показан на Фиг. 5. Наблюдали два λmax при 281 и 240 нм.
Характеризование 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата с помощью порошковой рентгенограммы
Спектр порошковой рентгенограммы 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата снимали на порошковом рентгенодифрактометре Bruker-AXS Ltd. D4 ENDEAVOR, оснащенном автоматическим сменщиком образцов, тета-тета гониометром геометрии, автоматической щелью расходимости луча и детектором PSD Vantec-1. Получали образец для анализа путем расположения на слабофонящей кремниевой пластине для образца, имеющей 0,5 мм углубление. Образец вращали с одновременным рентгеновским облучением меди Kα1 (длина волны =1,5406 Å) с параметрами рентгеновской трубки 35 кВ/40 мА.
Анализ проводили в непрерывном режиме сбора данных с шагом 0,018° через каждые 0,2 секунды в интервале два тета от 2° до 55° при комнатной температуре. Проводили поиск пиков, используя параметры порога и ширины 1 и 0,3 соответственно, в рамках программного продукта Eva, выпускаемого Bruker-AXS. Проверяли калибровку инструмента, используя корундовый стандарт (стандарт интенсивности NIST: SRM 1976 XRD flat palate).
Вследствие отличий инструментов, образцов и получения образца значения пиков приведены здесь с приблизительной вариабельностью значений пиков. Это общеизвестная практика в области твердых тел, поскольку свойственны вариации в значениях пиков. Типичная вариабельность 2θ значения x-оси для порошковой рентгенограммы составляет приблизительно плюс или минус 0,2° 2θ.
Вариабельность интенсивности пика является результатом ориентации отдельных кристаллов в контейнере образца относительно внешнего источника рентгеновского излучения (известна как "предпочтительная ориентация"). Этот ориентационный эффект не обеспечивает информации о структуре кристалла.
Кроме того, специалист в этой области также должен понимать, что интенсивности характеристических пиков, описанных выше, будут изменяться, когда кристаллический материал представленного изобретения смешивают или разводят дополнительными компонентами, такими как фармацевтические эксципиенты. По этой причине специалист в этой области должен понимать, что способ рентгеноструктурного анализа, описанный выше, может быть слегка оптимизирован для возможности детектирования характеристических пиков в рамках смеси компонентов. Эта оптимизация может включать применение более интенсивного источника рентгеновского излучения (длина волны =1,5406 Å), немного измененный размер шага или немного измененное время шага.
Специалист в этой области также должен понимать, что измерения с использованием разных длин волн будут давать разные сдвиги согласно закону Брегга - nλ=2d sinθ. Такие дополнительные рентгенограммы, полученные с применением альтернативных длин волн, считаются альтернативными видами рентгенограмм кристаллических материалов представленного изобретения и как таковые попадают в рамки представленного изобретения.
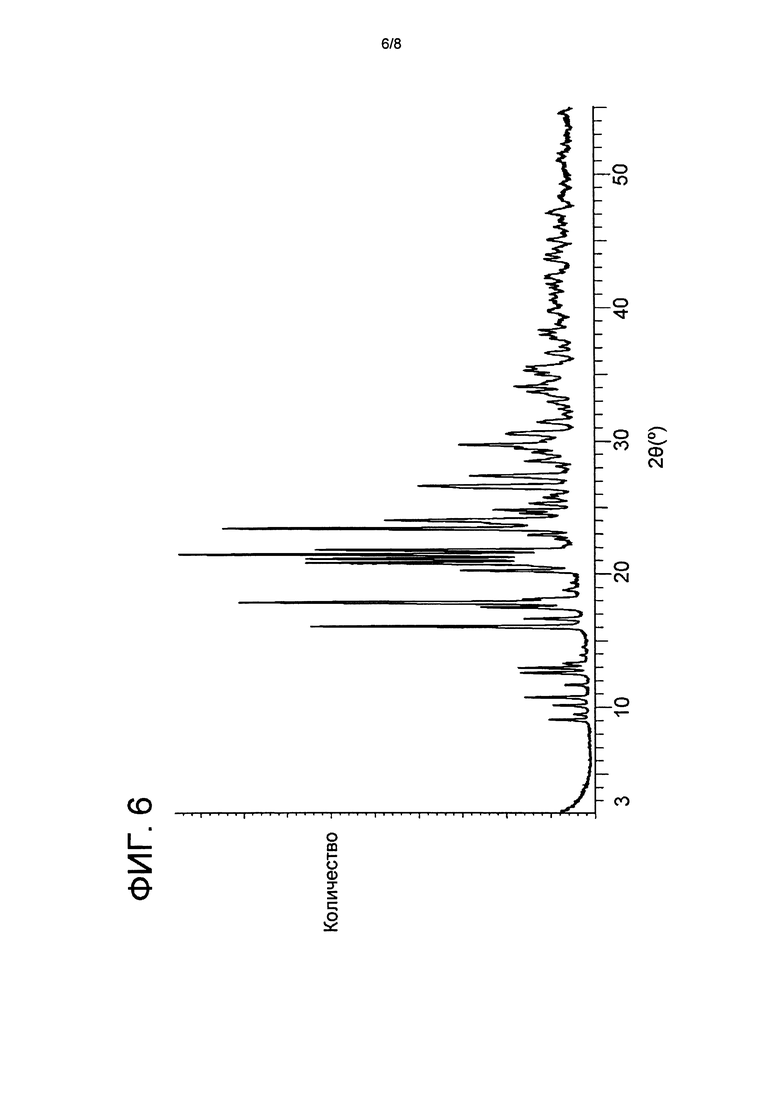
Рентгенограмма показана на Фиг. 6. Положения и относительные интенсивности основных 2θ пиков приведены в Таблицах 4 и 4a.
Таблица 4: Характеристические дифракционные пики 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата (±0,2° 2θ) с относительными интенсивностями ≥10%

Пример 2
Получение дисперсии высушенной распылением (SDD) 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида
Тетрагидрофуран (нестабилизированный, 14,5 кг) и воду (0,76 кг) загружали в танк из нержавеющей стали, оснащенный верхней мешалкой. Потом к раствору добавляли 4-[2-(5-Амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид (742,4 г) и перемешивали по крайней мере, 1 час до полного растворения всех твердых веществ. К раствору добавляли ацетат сукцинат гидроксипропилметилцеллюлозы (гранулят среднего размера, 1338,4 г) и перемешивали до полного растворения. Раствор затем сушили распылением в потоке азота, используя условия, приведенные в таблице ниже.


NB: 95:5 (мас/мас%) тетрагидрофуран (нестабилизированный):вода использовали для системы начало/окончание.
Полученный SDD 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида потом сушили в лотке в конвекционной лотковой сушке при 40°С/50% относительной влажности (ОВ) минимум 6 часов, после чего поднимали до 40°С/75% ОВ еще на протяжении минимум 25 часов.
SDD хранили при 2-8°С до использования.
Пример 3
Получение дисперсий для перорального введения:
(а) Использование тозилатной соли 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида
Метилцеллюлозный растворитель (0,5% мас/об) получали следующим образом. Воду для промывания (600 мл) нагревали в стакане при температуре от 80°С до 90°С. При перемешивании добавляли метилцеллюлозный (5 г) порошок до полного диспергирования порошка. Дисперсию потом переносили на баню с льдом и быстро охлаждали и в это время прибавляли охлажденную воду для промывания (400 мл), получая прозрачный раствор.
Получали дисперсию для перорального введения путем взвешивания необходимого количества 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата (от 10 мг до 2400 мг) в дозированной бутылке приемлемого размера из янтарного стекла (0,5% (мас/об) метилцеллюлозы). Прибавляли растворитель в количестве в зависимости от дозы: 15 мл для доз лекарственного средства в интервале от 10 мг до <30 мг; и 50 мл для доз лекарственного средства в интервале от 30 мг до 2400 мг, так чтобы концентрация лекарственного средства была в интервале от 0,6 до 50 мг/мл.
Дисперсию хранили при 2-8°С и вводили на протяжении 72 часов непосредственно из дозированных контейнеров. После введени, стеклянную дозированную бутылку промывали двумя приблизительно эквивалентными аликвотами питьевой воды, так что общий введенный объем, включая дозированный объем, был 240 мл.
(b) Использование SDD 4-[2-(5-мино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида
Метилцеллюлозный растворитель 0,5% (мас/об) получали, используя методику, приведенную в Примере 3(a), выше.
Получали дисперсию для перорального введения путем взвешивания необходимого количества 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида SDD] в дозированной бутылке приемлемого размера из янтарного стекла (0,5% (мас/об) метилцеллюлозы) и прибавляли растворитель в количестве в зависимости от дозы: 20 мл-100 мл для дозы в интервале от 10 мг до 2400 мг, так чтобы концентрация лекарственного средства была в интервале от 0,6 до 50 мг/мл.
Дисперсию хранили при 2-8°С и вводили на протяжении 72 часов непосредственно из дозированных контейнеров. После введения стеклянную дозированную бутылку промывали двумя приблизительно эквивалентными аликвотами питьевой воды, так что общий введенный объем, включая дозированный объем, был 240 мл.
Биологическая активность
Способность 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида и его фармацевтически приемлемых солей, таких как тозилатная соль, снижать уровни мочевой кислоты в крови показана в следующих экспериментах. Измерение мочевой кислоты проводили, используя коммерчески доступный набор для колориметрического исследования (Beckman Coulter).
Пример 4
Исследование с единичной дозой: дважды слепое, рандомизированное, плацебоконтролируемое, перекрестное исследование в шести группах здоровых субъектов.
Исследовали единичные дозы дисперсии 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида SDD ('SDD') для перорального введения, в интервале от 10 мг до 2400 мг. Кроме того, также исследовали единичные дозы дисперсии 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата ('TS') для перорального введения, в интервале от 200 мг до 1000 мг.
Исследовали следующие дозы и все дозы назначали натощак, за исключением 200 мг и 1000 мг SDD дисперсий, которые назначали натощак и после высокожирной диеты ('еда').
Группа 1: 10 мг SDD, 100 мг SDD, 300 мг SDD, 200 мгТЭ, плацебо
Группа 2: 30 мг SDD, 300 мг SDD, 200 мг SDD (еда), плацебо
Группа 3: 100 мг SDD, 200 мг SDD, 300 мг SDD, плацебо
Группа 4: 450 мг SDD, 600 мг SDD, 800 мг SDD, 1000 мг SDD, плацебо
Группа 5: 600 MrTS, 1000 мгТЭ, 1000 мг SDD (еда)
Группа 6: 1250 мг SDD, 1600 мг SDD, 2000 мг SDD, 2400 мг SSD, плацебо
В общем, участвовал 61 субъект (все мужчины) и все получали по крайней мер, одну дозу дисперсии SDD или TS для орального введения.
Далее приведены средние данные уровней мочевой кислоты на группу дозирования:
Отмечали дозозависимое уменьшение мочевой кислоты в крови на протяжении 48 часов после лечения. Хотя значения обычно остаются в рамках нормального интервала (3,5-7,2 мг/дл) при дозах 10-1000 мг, при дозах 1250-2400 мг уровни мочевой кислоты снижаются более значительно, по крайней мере, половина субъектов имеет значения ниже нижней нормальной границы (LLN) на протяжении 48 часов после лечения. Все значения до лечения и после были выше LLN. Все субъекты, получавшие плацебо (n=42), имели значения мочевой кислоты в рамках нормального интервала, за исключением того, что только один субъект имел значение ниже LLN на протяжении 48 часов после лечения.
Пример 5
Исследование с использованием нескольких доз: дважды слепое, рандомизированное, плацебоконтролируемое, исследование здоровых субъектов.
На протяжении 14 дней исследовали пероральное мультидозированное лечение, в котором дважды в день (BID) назначали 100 мг, 300 мг BID и 600 мг BID 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида SDD дисперсии для орального применения и плацебо. Субъекты голодали на протяжении ночи перед утренним назначением и по крайней мере 2 часа до вечернего назначения. Воздерживались от еды по крайней мере 2 часа после лечения.
В исследовании суммарно зарегистрировали 30 субъектов (все мужчины) и 27 субъектов завершили исследование (три субъекта отказались вследствие побочных эффектов при употреблении 600 мг BID 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида).
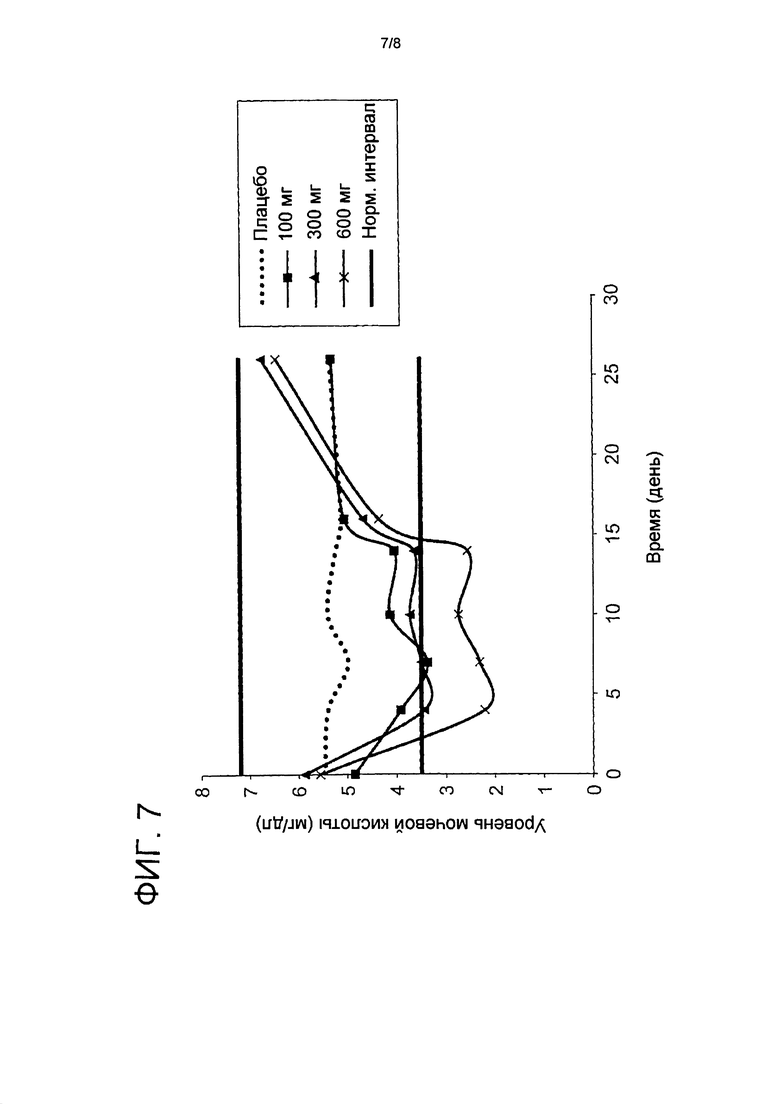
Средние данные уровней мочевой кислоты на группу дозирования приведены в Таблице 8 и Фиг. 7.
Наблюдали дозозависимое уменьшение мочевой кислоты в крови на День 4 (первая оценка после начала лечения) с наименьшими средними значениями в День 4 или 7. Пять из 8 субъектов имели значения мочевой кислоты ниже LLN на День 7 при 100 мг BID (фактический диапазон для субъектов с низкой мочевой кислоты был 2,6-3,4 мг/дл; один субъект имел значение ниже базового значения; фактическое значение 2,7 мг/дл) и при 300 мг (фактический диапазон для субъектов с низкой мочевой кислоты был 2,2-3,4 мг/дл). Все субъекты имели значения мочевой кислоты ниже LLN на День 4 и 7 при лечении 600 мг BID (фактический диапазон был <1,5-3,0 мг/дл). Значения обычно увеличивались на День 10 и 14, несмотря на продолжающееся лечение, хотя все, за исключением 1 субъекта, возвращались к нормальному интервалу на День 16 (2 дня после последнего назначения). Этот оставшийся субъект имел значение мочевой кислоты ниже базового (4,7 мг/дл) и последующие значения 2,2 мг/дл (День 4), <1,5 мг/дл (День 7), 1,6 мг/дл (День 10), 3,1 мг/дл (День 14) и 4,9 мг/дл после. Все субъекты, получавшие плацебо (n=6), имели концентрации мочевой кислоты в рамках нормального интервала на протяжении всего времени.
Пример 6
Исследование с использованием нескольких доз: дважды слепое, рандомизированное, плацебоконтролируемое, исследование здоровых субъектов и пожилых субъектов.
На протяжении 14 дней исследовали пероральное мультидозированное лечение TS дисперсией 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида и плацебо, следующим образом:
- здоровые субъекты, 300 мг дважды в день (BID,)
- здоровые субъекты, 450 мг BID, и
- пожилые субъекты, 300 мг BID.
Субъекты голодали на протяжении ночи перед утренним назначением и по крайней мере 2 часа до вечернего назначения. Воздерживались от еды по крайней мере 2 часа после лечения.
В исследовании суммарно регистрировали 49 субъектов, из которых 39 получали 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамид TS и 10 получали плацебо.
Средние данные уровней мочевой кислоты и данные экскреции мочи на группу дозирования приведены в Таблице 9. Фиг. 8 показывает процент выделенной мочевой кислоты в моче.

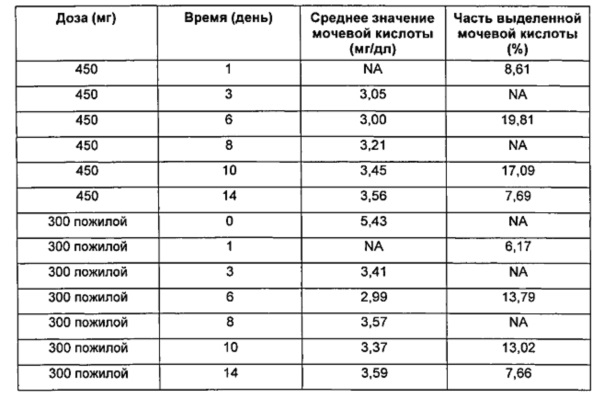
Концентрации мочевой кислоты в крови уменьшались после введения 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида. Все субъекты имели значения мочевой кислоты в крови выше LLN в День 1. Субъекты, получавшие плацебо, имели концентрации мочевой кислоты в крови выше LLN на протяжении исследования. Средние концентрации мочевой кислоты в крови опускались ниже LLN на День 3 у субъектов, получавших 450 мг BID 4, и средние значения были ниже LLN для всех групп (300 мг и 450 мг BID) на День 6. Концентрации мочевой кислоты в крови возвращались выше LLN у всех субъектов на протяжении 2 дней после прекращения введения 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида (то есть на День 16).
Также измеряли мочевую кислоту в моче, собранной за 24 часа до начала лечения в День 1, и потом в День 6, 14 и 16. Рассчитывали и анализировали процент выделенной мочевой кислоты в моче, используя модель эффекта линейного перемешивания. Эти данные показаны на Фиг. 8. Данные показывают, что выделенная фракция мочевой кислоты в моче увеличивается при введении 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида и возвращается к базовому уровню на День 16.
Пример 7
Активность ингибирования URAT-1
Эффективность 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида как ингибитора транспортера URAT-1 определяли следующим образом.
Выращивали НЕК293 клетки в среде, содержащей среду Игла, модифицированную Дульбекко (DMEM) с L-GlutaMax (4,5 г глюкозы на литр), дополненной инактивированной нагреванием сывороткой эмбриона теленка (10% об/об), 100 Е/мл пенициллина и 100 мкг/мл стрептомицина. НЕК клетки обычно выращивали в колбах культуры ткани 75 см2 в влажном инкубаторе приблизительно при 37°С в приблизительно 95% воздуха/5% CO2. Собирали почти слившиеся культуры клеток НЕК путем трипсинизации, повторного суспендирования в культуральной среде и процесс повторяли еще одну или две недели для получения достаточного количества клеток для использования.
Для проведения экспериментов высевали НЕК293 клетки на 24-луночные планшеты, покрытые поли-D-лизином с густотой 4×105 клеток на лунку. Клетки выращивали 1 день приблизительно при 37°С во влажном инкубаторе, содержащем приблизительно 5% CO2 в воздухе. После этого клетки трансфицировали или pcDNA3.1/hygro/URAT1 (HEK-URAT1 клетки), или pcDNA3.1/hygro (HEK-control клетки), используя реагент Lipofectamine 2000. Через приблизительно 24 часа приблизительно при 37°С во влажном инкубаторе, содержащем приблизительно 5% CO2 в воздухе, клетки использовали для экспериментов.
Через один день после трансфекции культуральную среду удаляли из лунок и клетки предварительно инкубировали с 0,2 мл инкубационной среды, свободной от хлора (125 мМ Na-клюконата, 4,8 мМ K-глюконата, 1,3 мМ Ca-глюконата, 1,2 мМ KH2PO4, 1,2 мМ MgSO4, 5,6 мМ D-глюкозы, 25 мМ HEPES, pH 7,4), в отсутствие и присутствии 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида (0-30 мкМ), на протяжении 15 минут приблизительно при 37°С. После этого инкубационную среду удаляли и добавляли 0,2 мл инкубационной среды, свободной от хлора, содержащей [14C]-мочевую кислоту (20 мкМ), трижды, в отсутствии и присутствии 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида (0-30 мкМ). Клетки инкубировали 2 минуты приблизительно при 37°С. В конце инкубации, среду отсасывали и монослои дважды быстро промывали 1 мл охлажденной льдом инкубационной среды. Впоследствии клетки солюбилизировали в 0,5 мл 0,5 н. NaOH и аликвоты образцов клеточного лизата из каждой лунки собирали в сцинтилляционных бутылочках. Определяли концентрации [14C]-мочевой кислоты ,используя сцинтилляционный счетчик (LSC). Также определяли ингибирование транспорта [14С]-мочевой кислоты в присутствии известного ингибитора бензбромарона (30 мкМ). Конечная концентрация органического растворителя была меньше чем 1% (об/об).
Определяли содержание протеина солюбилизированных НЕК клеток с помощью способа Бредфорда, используя реагент Bio-Rad Bradford Reagent с бычьим сывороточным альбумином (BSA) в качестве протеина стандарта (концентрация в интервале 0-1 мг/мл). Смешивали раствор BSA или солюбилизированные клетки с разведенным концентратом красителя (Bio-Rad). Измеряли абсорбцию при 595 нм после инкубации при комнатной температуре на протяжении 10 минут.
Определяли количество радиоактивности, присутствующей в образцах клеточного лизата с помощью сцинтилляционного счетчика (LSC). Ко всем образцам прибавляли жидкий сцинтиллянт (Hionic Fluor™) и определяли радиоактивность с помощью LSC на жидкостном сцинтилляционном счетчике Tri-Carb 3100TR, используя программное обеспечение QuantaSmart™, где все значения переводили в DPM, используя tSIE/AEC (трансформированный Спектральный Индекс внешних стандартов, связанных с Автокоррекцией Эффективности). Методики калибровки инструментов установлены на испытательной аппаратуре. Все образцы считывали по крайней мере 2 минуты. Измеряли фоновые значения, используя каждый образец последовательности с помощью жидкого сцинтиллянта в отсутствие образца. Рассчитывали накопление (пмоль/мг протеина) [14С]-мочевой кислоты в НЕК клетках и рассчитывали значения IC50, определенные как концентрацию ингибитора, необходимую для 50% ингибирования транспорта, используя GraphPad Prism версия 4.00 с помощью уравнения Хилла.
Данные
Измеренное ингибирование поглощения мочевой кислоты 4-[2-(5-амино-1H-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамидом с помощью методики, описанной выше, нормализированное к соединению стандарту бензбромарону, составляло 3,54 мкМ.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПРИМЕНЕНИЯ ИНГИБИТОРОВ ЦИКЛООКСИГЕНАЗЫ-2 ДЛЯ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ НЕОПЛАЗИИ | 1997 |
|
RU2239429C2 |
| СПОСОБ ЛЕЧЕНИЯ ВОСПАЛЕНИЯ ИЛИ СВЯЗАННОГО С ВОСПАЛЕНИЕМ ЗАБОЛЕВАНИЯ У СОБАК | 1996 |
|
RU2253456C2 |
| ПИРАЗОЛПИРИМИДИНЫ | 2005 |
|
RU2412186C2 |
| ПИРАЗОЛИЛЗАМЕЩЕННЫЙ БЕНЗОЛСУЛЬФОНАМИД ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ЛЕЧЕНИЯ ОТ ВОСПАЛЕНИЯ ИЛИ СВЯЗАННОГО С ВОСПАЛЕНИЕМ ЗАБОЛЕВАНИЯ | 1994 |
|
RU2139281C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ПРИМЕНЕНИЯ В ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ, ВКЛЮЧАЮЩАЯ КОМБИНАЦИЮ БИФОСФОНАТА, ИНГИБИТОРА СОХ-2 И ТАКСОЛА | 2002 |
|
RU2317819C2 |
| НОВЫЕ 1,2-БИС-СУЛЬФОНАМИДНЫЕ ПРОИЗВОДНЫЕ КАК МОДУЛЯТОРЫ ХЕМОКИНОВОГО РЕЦЕПТОРА | 2011 |
|
RU2654213C9 |
| МОДУЛЯТОРЫ НАТРИЕВОГО КАНАЛА ДЛЯ ЛЕЧЕНИЯ БОЛИ | 2014 |
|
RU2669367C2 |
| СПОСОБ ПРИМЕНЕНИЯ ИНГИБИТОРОВ ЦИКЛООКСИГЕНАЗЫ-2 В КАЧЕСТВЕ АНТИАНГИОГЕННЫХ СРЕДСТВ | 1997 |
|
RU2268716C2 |
| АНТАГОНИСТ РЕЦЕПТОРА CRF1, ЕГО ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ И ТВЕРДЫЕ ФОРМЫ ДЛЯ ЛЕЧЕНИЯ ВРОЖДЕННОЙ ГИПЕРПЛАЗИИ НАДПОЧЕЧНИКОВ | 2019 |
|
RU2824490C2 |
| ПРИМЕНЕНИЕ РЕЦЕПТОРА АНТАГОНИСТА ЕР4 ДЛЯ ЛЕЧЕНИЯ ХРЯЩЕВОЙ БОЛЕЗНИ | 2014 |
|
RU2663620C2 |





Изобретение относится к тозилату 4-[2-(5-Амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида. Данное соединение является кристаллическим веществом и характеризуется порошковой рентгенограммой (PXRD), которая имеет любые три, четыре, пять или шесть характеристических два тета (2θ) пиков, которые выбирают из группы, включающей 9,0, 9,3, 10,0, 10,7, 11,6, 12,5, 12,9, 13,2, 13,8, 14,4, 16,0, 16,6, 17,5, 17,8, 18,1, 21,4 и 23,4° (±0,2° 2θ), при использовании рентгеновского излучения CuKalpha1 (длина волны = 1,5406  ). Изобретение также относится к применению 4-[2-(5-амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата для изготовления медикамента для лечения боли, предпочтительно невропатической, ноцицептивной, или воспалительной боли, или для лечения заболевания, связанного с повышенными уровнями мочевой кислоты в крови. Технический результат - 4-[2-(5-амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилат, обладающий лучшей химической стабильностью и хорошей растворимостью в воде. 5 н. и 5 з.п. ф-лы, 8 ил., 9 табл., 7 пр.
). Изобретение также относится к применению 4-[2-(5-амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата для изготовления медикамента для лечения боли, предпочтительно невропатической, ноцицептивной, или воспалительной боли, или для лечения заболевания, связанного с повышенными уровнями мочевой кислоты в крови. Технический результат - 4-[2-(5-амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилат, обладающий лучшей химической стабильностью и хорошей растворимостью в воде. 5 н. и 5 з.п. ф-лы, 8 ил., 9 табл., 7 пр.
1. 4-[2-(5-Амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилат.
2. 4-[2-(5-Амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилат по п. 1, являющийся кристаллическим веществом.
3. Кристаллическое вещество по п. 2, характеризующееся порошковой рентгенограммой (PXRD), которая имеет любые три, четыре, пять или шесть характеристических два тета (2θ) пиков, которые выбирают из группы, включающей 9,0, 9,3, 10,0, 10,7, 11,6, 12,5, 12,9, 13,2, 13,8, 14,4, 16,0, 16,6, 17,5, 17,8, 18,1, 21,4 и 23,4° (±0,2° 2θ), при использовании рентгеновского излучения CuKalpha1 (длина волны = 1,5406  ).
).
4. 4-[2-(5-Амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилат по какому-либо одному из пп. 1-3 для применения в лечении расстройства, для которого показан ингибитор Nav1.7.
5. 4-[2-(5-Амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилат по п. 4, где расстройством, для которого показан ингибитор Nav1.7, является боль, предпочтительно невропатическая, ноцицептивная или воспалительная боль.
6. 4-[2-(5-Амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилат по какому-либо одному из пп 1-3 для применения в лечении заболевания, связанного с повышенными уровнями мочевой кислоты в крови.
7. Применение 4-[2-(5-амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата по какому-либо одному из пп. 1-3 для изготовления медикамента для лечения боли, предпочтительно невропатической, ноцицептивной или воспалительной боли.
8. Применение 4-[2-(5-амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата по какому-либо одному из пп. 1-3 для изготовления медикамента для лечения заболевания, связанного с повышенными уровнями мочевой кислоты в крови.
9. Способ лечения боли, предпочтительно невропатической, ноцицептивной или воспалительной боли, в котором субъекту, нуждающемуся в таком лечении, назначают терапевтически эффективное количество 4-[2-(5-амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата по какому-либо одному из пп. 1-3.
10. Способ лечения заболевания, связанного с повышенными уровнями мочевой кислоты в крови, в котором субъекту, нуждающемуся в таком лечении, назначают терапевтически эффективное количество 4-[2-(5-амино-1Н-пиразол-4-ил)-4-хлорфенокси]-5-хлор-2-фтор-N-(1,3-тиазол-4-ил)бензолсульфонамида тозилата по какому-либо одному из пп. 1-3.
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Устройство для компаундирования синхронных генераторов | 1955 |
|
SU104483A1 |
| N-ФЕНИЛАРИЛСУЛЬФОНАМИД, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ УКАЗАННОЕ СОЕДИНЕНИЕ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА, СОЕДИНЕНИЕ, ЯВЛЯЮЩЕЕСЯ ПРОМЕЖУТОЧНЫМ В СИНТЕЗЕ УКАЗАННОГО СОЕДИНЕНИЯ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2002 |
|
RU2299202C2 |
Авторы
Даты
2017-01-30—Публикация
2012-10-19—Подача