Изобретение относится к медицине и фармацевтической химии, в частности к способу получения лекарственного препарата на основе наночастиц фталоцианинов, который может быть использован при лечении злокачественных новообразований методом импульсной лазерной абляции наночастиц (ИЛАН).
Суть метода ИЛАН состоит в следующем: в организм больного инъекционно вводят лекарственный препарат, содержащий наночастицы, обладающие интенсивным светопоглощением в так называемом «терапевтическом окне прозрачности биоткани» (диапазон длин волн 600-1200 нм). Через некоторое время лекарственный препарат с кровотоком попадает в опухоль, затем опухоль облучают импульсным лазером с длиной волны, соответствующей области светопоглощения наночастиц. Под действием импульса лазерного излучения наночастицы резко нагреваются, в результате чего происходит их разрушение в виде «микровзрывов» - абляции наночастиц, приводящее к повреждению окружающих наночастицы биологических структур и, прежде всего, кровеносных сосудов опухоли, что вызывает гибель опухолевых клеток.
Известно применение наночастиц (НЧ) золота в способе индукции гибели злокачественных клеток in vitro путем введения НЧ в культуру клеток опухоли с последующим облучением лазерными импульсами [Biophysical Journal, 84, 4023-4032, 2003]; [Biophysical Journal, 90, 619-627, 2006]. Однако эксперименты по эффективности наночастиц золота in vitro не были подтверждены в экспериментах in vivo, которые ближе к клиническому применению.
Кроме того, способ получения нанодисперсий золота [Российские нанотехнологии. 2007. Т. 2. №3-4. с. 69-86] достаточно сложен и длителен, а эффективность их в качестве термосенсибилизаторов недостаточно высока.
В работе [NSTI Nanotech 2006, Boston, 2006, Vol. 2, Chapter 1, p. 71-74] описано применение НЧ углерода в способе подавления роста опухолей в эксперименте in vivo на мышах путем внутривенного введения НЧ углерода в дозе 30 мг/кг с последующим облучением опухоли лазерными импульсами в спектральной области поглощения НЧ с плотностью энергии в импульсе 3 Дж/см2 и суммарной плотностью энергии 180 Дж/см2.
Максимальные значения торможения роста опухоли (ТРО) для карциномы С-26 и саркомы S-37 достигали 70-75%.
Недостатком применения этих НЧ является невысокая эффективность, т.к. способы с их применением при довольно высокой плотности энергии в импульсе (3 Дж/см2) и суммарной плотности энергии (180 Дж/см2) обеспечивают ТРО лишь 70-75%.
Наиболее близким аналогом к предлагаемому решению является термосенсибилизатор, описанный в Патенте РФ 2339414. Лекарственный препарат представляет собой водную суспензию наночастиц фталоцианинов алюминия, цинка или безметального фталоцианина. Его вводили внутривенно подопытным животным с привитыми опухолями, а затем облучали опухоль импульсным лазером с длиной волны, попадающей в спектральную полосу поглощения наночастиц фталоцианинов, что приводило к подавлению роста опухолей.
Недостатком данного термосенсибилизатора является то, что высокая противоопухолевая эффективность лечения (ТРО на 80%-90%) была достижима только при использовании достаточно высоких доз термосенсибилизатора - не менее 30 мг/кг веса, что возможно связано с низкой стабильностью суспензии.
В данном патенте нет описания метода получения термосенсибилизатора и лишь отмечено, что в качестве активного компонента термосенсибилизатора использовались наночастицы фталоцианина цинка, фталоцианина алюминия или безметального фталоцианина.
Задачей настоящего изобретения является разработка способа получения лекарственного препарата на основе наночастиц фталоцианина, обеспечивающего получение лекарственного препарата, характеризующегося высокой противоопухолевой эффективностью при использовании в методе ИЛАН при низких дозах, и стабильностью при хранении.
Для решения этой задачи предложен способ получения лекарственного препарата на основе наночастиц фталоцианина, состоящий из следующих стадий:
- на первой стадии производят диспергирование грубодисперсного (с размером частиц 100-1000 мкм) фталоцианина методом пластического размола в смесителе тяжелого типа с использованием в качестве мелющих тел смеси двух неорганических солей и пластификатора - диэтиленгликоля при температуре 20-30°С, в результате чего исходный фталоцианин превращается в наночастицы с распределением размеров от 70 до 250 нм и со средним размером частиц 100-150 нм;
- на второй стадии производят выделение наночастиц из солевой пасты, полученной на первой стадии, и отмывку водой наночастиц фталоцианина от солей и пластификатора, используемых при диспергировании, в результате получают водную суспензию/пасту с содержанием фталоцианина 2-30%, и средним размером частиц 100-150 нм;
- на третьей стадии к водной суспензии/пасте добавляют раствор хлорида натрия и ПАВ, а затем повторно диспергируют и получают лекарственный препарат на основе наночастиц фталоцианинов следующего состава (мас.%):
Нижеприведенные примеры иллюстрируют предлагаемое изобретение.
Пример 1.
Способ получения лекарственного препарата на основе наночастиц фталоцианина цинка
В смеситель загружают 200,0 г сульфата натрия и 70,0 г карбоната натрия, смесь солей перемешивают до получения однородной сыпучей массы. Затем в смеситель добавляют 30,0 г порошкообразного фталоцианина цинка с размером частиц 100-1500 мкм. Полученную смесь перемешивают до получения равномерно окрашенной голубой массы.
Затем постепенно добавляют 25,6 г диэтиленгликоля, доводя массу до однородной консистенции.
После достижения тестообразного пластичного состояния массы ведут пластический размол фталоцианина цинка при температуре 25-30°С. Полученную солевую пасту растворяют в воде и полученный раствор обессоливают, получая суспензию НЧ фталоцианина цинка в воде.
К обессоленной водной суспензии объемом 1 л, содержащей 30 г фталоцианина цинка, добавляют 30 г ПАВ - блок-сополимера окиси этилена и окиси пропилена и диспергируют в течение 1 часа. Затем полученную суспензию разбавляют при перемешивании 14 л 0,9% раствором хлорида натрия до рабочей концентрации - 0,2% по фталоцианину цинка. Средний размер частиц полученного препарата составляет 155 нм, а через 3 года хранения - 165 нм.
Пример 2.
Лекарственный препарат получают по примеру 1, но в качестве действующего вещества берут 30 г безметального фталоцианина с размером частиц 100-1500 мкм, а при диспергировании вводят 30 г блок-сополимера окиси этилена и окиси пропилена. Затем полученную суспензию разбавляют при перемешивании 29 л 0,9% раствора хлорида натрия до рабочей концентрации - 0,1%. Состав полученного препарата в мас.%:
Средний размер частиц полученного препарата составляет 167 нм, а через 3 года хранения - 185 нм.
Пример 3.
Лекарственный препарат получают по примеру 1, но в качестве действующего вещества используют фталоцианин алюминия с размером частиц 100-1500 мкм в количестве 35 г. Затем полученную суспензию разбавляют при перемешивании 5 л 0,9% раствора хлорида натрия до рабочей концентрации - 0,5%.
Состав полученного препарата в мас.%:
Средний размер частиц полученного препарата составляет 160 нм, а через 3 года - 178 нм.
Пример 4.
Лекарственный препарат получают, используя по 10 мл обессоленных суспензий, полученных по примерам 1, 2, 3, и содержащих по 0,3 г фталоцианина цинка, алюминия и безметального, смешивают, добавляют 15 мл 10% раствора ПАВ и диспергируют, затем постепенно добавляют раствор 1,5 г хлорида натрия в 52,6 мл воды и перемешивают в течение 15 минут. Состав полученного препарата в мас.%:
Средний размер частиц полученного препарата составляет 168 нм, а через 3 года - 185 нм.
Пример 5.
Лекарственный препарат получают по примеру 1, но в смеситель загружают 100 г сульфата калия, 120 г карбоната натрия, 20 г хлорида калия и 30 г фталоцианина цинка с размером частиц 100-1500 мкм. Состав полученного препарата в мас.%:
Средний размер частиц полученного препарата составляет 166 нм, а через 3 года - 187 нм.
Пример 6.
Проводят исследования на противоопухолевую эффективность ИЛАН с использованием препаратов, полученных по примерам 1-5 на мышах с саркомой S-37.
Исследования проводят на мышах с перевиваемыми солидными опухолями саркомы S-37. Препараты, полученные по примерам 1-5, вводят однократно внутривенно в дозе, равной 7 мг/кг в расчете на действующее вещество. Контрольная группа - мыши, которым вводили физиологический раствор в объеме, равном вводимому препарату.
Мыши F1, самки. Лечение начинали на 6 день после инокуляции опухолевого материала. Облучение опухолевого узла проводили через 2-5 минут после внутривенного введения. В качестве источника излучения использовали импульсный лазер на рубине с длиной волны генерации, равной 694 нм. Плотность энергии в импульсе была не ниже 0,1 Дж/см2, суммарная плотность энергии - не ниже 10 Дж/см2.
Оценку противоопухолевого эффекта осуществляли по торможению роста опухоли (ТРО, %), которое рассчитывали по формуле:
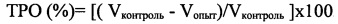 ,
,
где, Vконтроль - объем опухоли в контрольной группе;
Vопыт - объем опухоли в опытной группе.
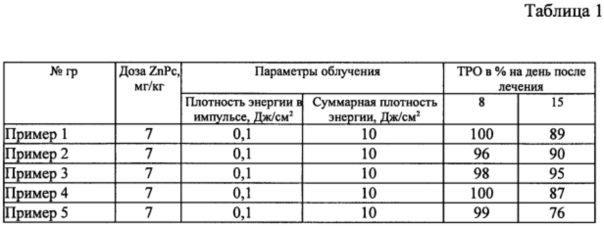
Результаты приведены в таблице 1
Пример 7.
Проводят исследование на противоопухолевую эффективность ИЛАН с использованием препаратов, полученных по примерам 1-5 на мышах с привитой карциномой С-26. Исследования проводятся аналогично примеру 6.
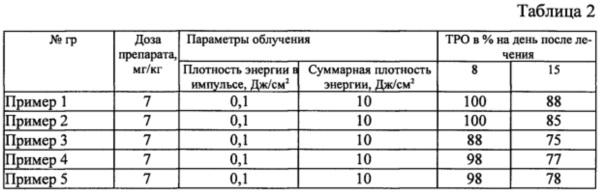
Результаты приведены в таблице 2
Таким образом, предлагаемый способ получения обеспечивает получение препарата, обладающего высокой эффективностью при доклинических испытаниях при использовании в методе ИЛАН (ТРО до 100%), и, кроме того, этот препарат обладает хорошей стабильностью: средний размер наночастиц после трехлетнего хранения снижается незначительно.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОДАВЛЕНИЯ РОСТА ОПУХОЛЕЙ | 2007 |
|
RU2339414C1 |
| СПОСОБ ПОДАВЛЕНИЯ РОСТА ОПУХОЛЕЙ | 2008 |
|
RU2383370C1 |
| АЛКИЛТИОЗАМЕЩЕННЫЕ ФТАЛОЦИАНИНЫ, ИХ ЛЕКАРСТВЕННЫЕ ФОРМЫ И СПОСОБ ПРОВЕДЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2007 |
|
RU2340615C1 |
| ФОТОСЕНСИБИЛИЗАТОР, ЛИПОСОМАЛЬНАЯ ФОРМА ФОТОСЕНСИБИЛИЗАТОРА И СПОСОБ ПРОВЕДЕНИЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 2004 |
|
RU2257898C1 |
| ПЛАЗМОЗАМЕЩАЮЩИЙ ПРЕПАРАТ С РЕОЛОГИЧЕСКИМИ И ГЕМОДИНАМИЧЕСКИМИ СВОЙСТВАМИ: СОСТАВ И СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ | 2010 |
|
RU2461383C2 |
| ТЕРМОСЕНСИБИЛИЗАТОР ДЛЯ ЛАЗЕРНОЙ ГИПЕРТЕРМИИ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2474443C1 |
| ВЫСОКОЭФФЕКТИВНЫЙ СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОЙ ФОРМЫ АДРЕСНОГО ДЕЙСТВИЯ ДЛЯ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 2019 |
|
RU2727924C1 |
| ПРОТИВООПУХОЛЕВЫЙ ПРЕПАРАТ | 2011 |
|
RU2451509C1 |
| Терапевтические полимерные наночастицы и способы их получения и применения | 2014 |
|
RU2682332C2 |
| ПРОТИВОВОСПАЛИТЕЛЬНЫЙ ПРЕПАРАТ НА ОСНОВЕ КЕТОПРОФЕНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2018 |
|
RU2694221C1 |
Изобретение относится к медицине и фармацевтической химии, в частности оно касается лекарственного препарата на основе наночастиц фталоцианина, который может быть использован при лечении злокачественных новообразований методом импульсной лазерной абляции наночастиц. Описан трехстадийный способ получения лекарственного препарата и полученный этим способом препарат, имеющий следующий состав в мас.%: фталоцианин в виде наночастиц 0,1-1,0; ПАВ 0,1-1,5; хлорид натрия 0,1-1,5; вода - остальное. Лекарственный препарат, полученный предлагаемым способом, показал высокую эффективность - обеспечивает торможение роста опухоли (ТРО) до 100%, а также стабильность при хранении - после 3-х лет хранения размер наночастиц фталоцианина изменился незначительно. 2 н. и 1 з.п. ф-лы, 2 табл., 7 пр.
1. Способ получения лекарственного препарата для лечения злокачественных новообразований на основе наночастиц фталоцианина, фталоцианина цинка, фталоцианина алюминия или их смеси, включающий следующие стадии:
первая стадия - получение наночастиц фталоцианинов методом пластического размола с использованием в качестве мелющих тел смеси водорастворимых неорганических солей и диэтиленгликоля при температуре 20-30°С;
вторая стадия - выделение наночастиц фталоцианинов из солевой пасты и отмывка их от солей и диэтиленгликоля водой, получение водной суспензии нанодисперсных фталоцианинов;
третья стадия - получение лекарственного препарата диспергированием нанодисперсных фталоцианинов в водном растворе хлорида натрия в присутствии поверхностно-активного вещества - стабилизатора блок-сополимера окиси этилена и окиси пропилена - и доведение до рабочей концентрации.
2. Лекарственный препарат для лечения злокачественных новообразований, полученный по способу п. 1, следующего состава, мас.%:
3. Лекарственный препарат по п. 2, отличающийся тем, что в качестве действующего вещества содержит безметальный фталоцианин, фталоцианин цинка, фталоцианин алюминия или их смесь.
| СПОСОБ ПОДАВЛЕНИЯ РОСТА ОПУХОЛЕЙ | 2007 |
|
RU2339414C1 |
| СУЛЬФОЗАМЕЩЕННЫЕ ФТАЛОЦИАНИНЫ КАК ФОТОСЕНСИБИЛИЗАТОРЫ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ | 1999 |
|
RU2183635C2 |
| ПРЕПАРАТ ДЛЯ ФОТОДИНАМИЧЕСКОЙ ТЕРАПИИ ЗЛОКАЧЕСТВЕННЫХ НОВООБРАЗОВАНИЙ | 1996 |
|
RU2145221C1 |
Авторы
Даты
2017-03-15—Публикация
2015-07-17—Подача