Изобретение относится к биологии, экологии, токсикологической и санитарной химии, а именно к способам определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в биологическом материале, и может быть использовано в практике санэпидстанций, химико-токсикологических, клинических, ветеринарных и экологических лабораторий. Способ относится к числу массовых.
Известен способ определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в биологическом материале (клубнях картофеля) путем измельчения биологического объекта, трехкратной обработки в режиме встряхивания порциями гексана, масса каждой из которых в два раза превышает массу биоматериала, отделения извлечений, их объединения, обезвоживания безводным сульфатом натрия, упаривания до незначительного объема, определения методом ТСХ в тонком слое широкопористого силикагеля на пластинах «Силуфол» с использованием подвижной фазы гексан-ацетон (3:2) (Методы определения микроколичеств пестицидов в продуктах питания, кормах и внешней среде. Т. 1 / М.А. Клисенко, А.А. Калинина, К.Ф. Новикова, Г.А. Хохолькова. - М.: Колос, 1992. - С. 190-192).
Способ отличается относительно низкой чувствительностью и недостаточно высокой точностью определения.
Известен способ определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в биологическом материале, заключающийся в том, что анализируемое вещество изолируют из биологической пробы хлороформом, получаемое извлечение подвергают очистке в колонке силикагеля L 40/100μ, используя элюент гексан-ацетон (9:1) и проводят определение методом ТСХ в тонком слое широкопористого силикагеля, применяя подвижную фазу гексан-диоксан-пропанол-2 (80:30:6) (Шорманов В.К., Баранов Ю.Н. Применение метода ТСХ для определения банкола в извлечениях из биологического материала // Научно-практическая конференция с международным участием «Состояние, перспективы судебно-токсикологической службы и научных исследований» (Харьков. 9-10 ноября 2005 г). - Харьков, 2005. - С. 43).
Способ характеризуется недостаточно высокими чувствительностью и точностью определения.
Наиболее близким является способ определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в биологическом материале, который заключается в том, что биологический объект измельчают, двукратно по 45 минут обрабатывают порциями органического изолирующего агента, которым является толуол, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта, полученные органические извлечения объединяют, обезвоживают безводным сульфатом натрия, растворитель из объединенного извлечения испаряют, остаток растворяют в хлороформе, хроматографируют в колонке с силикагелем L 40/100 μ, вначале пропуская через нее гексан, а затем элюируя смесью растворителей гексан-диоксан-пропанол-2 в соотношении 8:3:0,6 по объему, фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, остаток растворяют в смеси растворителей гексан-диоксан-пропанол-2 в соотношении 15:5:1 по объему и проводят определение методом ВЭЖХ в колонке размерами 64×2 мм, заполненной сорбентом «Силасорб 600», с применением подвижной фазы гексан-диоксан-пропанол-2 в соотношении 15:5:1 по объему и УФ-детектора.
Способ характеризуется недостаточно высокой чувствительностью определения.
Техническим результатом настоящего изобретения является повышение чувствительности определения.
Технический результат достигается тем, что биологический объект измельчают, двукратно по 45 минут обрабатывают порциями органического изолирующего агента, которым является смесь толуол-этилацетат в соотношении 7:3 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта, полученные органические извлечения объединяют, обезвоживают безводным сульфатом натрия, растворитель из объединенного извлечения испаряют, остаток растворяют в ацетоне, хроматографируют в колонке с силикагелем L 40/100 μ, вначале пропуская через нее гексан, а затем элюируя смесью растворителей этилацетат-гексан в соотношении 6:4 по объему, фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, остаток растворяют в смеси растворителей ацетонитрил-вода в соотношении 6:4 по объему и проводят определение методом ВЭЖХ в колонке размерами 150×3,9 мм, заполненной сорбентом «Nova Pack» С-18, с применением подвижной фазы ацетонитрил-вода в соотношении 6:4 по объему и УФ-детектора на основе диодной матрицы.
Способ осуществляется следующим образом: биологический объект, содержащий 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропан, измельчают, двукратно по 45 минут обрабатывают порциями органического изолирующего агента, которым является смесь толуол-этилацетат в соотношении 7:3 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта, полученные органические извлечения объединяют, обезвоживают безводным сульфатом натрия, растворитель из объединенного извлечения испаряют, остаток растворяют в ацетоне, хроматографируют в колонке с силикагелем L 40/100 μ, вначале пропуская через нее гексан, а затем элюируя смесью растворителей этилацетат-гексан в соотношении 6:4 по объему, фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, остаток растворяют в смеси растворителей ацетонитрил-вода в соотношении 6:4 по объему и проводят определение методом ВЭЖХ в колонке размерами 150×3,9 мм, заполненной сорбентом «Nova Pack» С-18, с применением подвижной фазы ацетонитрил-вода в соотношении 6:4 по объему и УФ-детектора на основе диодной матрицы.
Способ иллюстрируется следующими примерами.
Пример 1
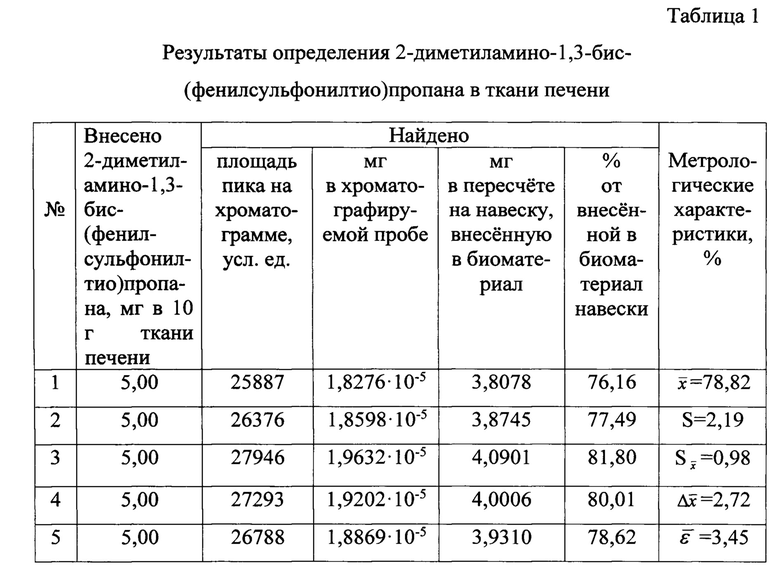
Определение 2-диметиламино-1,3-бис-(фенил-сульфонилтио)пропана в ткани печени
К 10 г мелкоизмельченной ткани печени прибавляют 5 мг 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана, тщательно перемешивают биологическую ткань с веществом и оставляют на полтора часа при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, обрабатывают порциями органического изолирующего агента, которым является смесь толуол-этилацетат в соотношении 7:3 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта. При этом биологический объект заливают 20 г смеси толуол-этилацетат в соотношении 7:3 по объему и выдерживают 45 минут при периодическом перемешивании. Извлечение отделяют от твердых частиц биоматериала, операцию настаивания повторяют в указанных условиях. Полученные органические извлечения объединяют, обезвоживают безводным сульфатом натрия путем фильтрования через стеклянный фильтр диаметром 4 см со слоем безводного сульфата натрия высотой 1-1,5 см. Фильтр дополнительно промывают 10 г смеси толуол-этилацетат в соотношении 7:3 по объему. Фильтрат и промывную жидкость объединяют, растворитель из объединенного извлечения испаряют в токе воздуха при комнатной температуре. Остаток растворяют в 8 мл ацетона, 2 мл полученного раствора смешивают с 1 г силикагеля L 40/100μ и испаряют остатки ацетона из сорбента в токе воздуха.
В колонку размером 490×10 мм вносят вначале 9 г силикагеля типа L 40/100μ, а затем, поверх образующегося слоя, - 1 г силикагеля L 40/100μ, содержащего анализируемое вещество, предварительно введенное в виде ацетонового раствора. Хроматографируют в колонке силикагеля L 40/100μ, вначале пропуская через колонку гексан. После истечения из колонки 20 мл элюата растворитель, находящийся над поверхностью столба сорбента, удаляют и начинают элюировать смесью растворителей этилацетат-гексан в соотношении 6:4 по объему. С момента начала подачи системы растворителей этилацетат-гексан в соотношении 6:4 по объему выходящий из колонки элюат собирают отдельными фракциями по 2 мл каждая. Фракции элюата с 48 по 56 включительно, содержащие анализируемое вещество, объединяют в выпарительной чашке, элюент испаряют в токе воздуха при комнатной температуре. Остаток растворяют в смеси растворителей ацетонитрил-вода в соотношении 6:4 по объему. Для этого вначале остаток обрабатывают 6-8 мл ацетонитрила, полученный раствор количественно переносят в мерную колбу вместимостью 10 мл и доводят содержимое колбы до метки ацетонитрилом (раствор А). 4,8 мл раствора А вносят в мерную колбу вместимостью 10 мл, прибавляют 1,2 мл ацетонитрила и доводят до метки водой. 4 мкл полученного раствора вводят в хроматограф типа «Alliance» фирмы «Waters».
Хроматографируют методом ВЭЖХ. Процесс хроматографирования осуществляют в колонке размерами 150×3,9 мм, заполненной обращеннофазовым сорбентом «Nova Pack» С-18, с применением подвижной фазы ацетонитрил-вода в соотношении 6:4 по объему и УФ-детектора на основе диодной матрицы.
Скорость подачи элюента составляет 1000 мкл/мин. Температура термостата колонки составляет 20°С. Оптическую плотность регистрируют при длине волны 224 нм.
Пик на хроматограмме с временем удерживания 2,25 мин (объемом удерживания 2250 мкл) соответствует 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропану.
Количественное содержание 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана определяют, исходя из площади хроматографического пика, по уравнению градуировочного графика и пересчитывают на навеску вещества, внесенную в ткань печени.
Построение градуировочного графика
В ряд мерных колб вместимостью 25 мл вносят 0,5; 1,0, 2,0; 4,0, 8,0 мл 0,005% раствора, 2,0, 4,0, 8,0 мл 0,05% раствора 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в ацетонитриле, соответственно 14,5, 14,0, 13,0, 11,0, 7,0, 13,0, 11,0, 7,0 мл ацетонитрила и доводят содержимое каждой колбы до метки водой. 4 мкл каждого из полученных растворов вводят в хроматограф «Alliance» фирмы «Waters».
Хроматографирование осуществляют в колонке размером 150×3,9 мл, заполненной сорбентом «Nova Раck», используя подвижную фазу ацетонитрил-вода в соотношении 6:4 по объему и диодно-матричный УФ-детектор. Скорость подачи элюента составляет 1000 мкл/мин. Температура термостата колонки составляет 20°С. Оптическую плотность регистрируют при длине волны 224 нм.
Пик на хроматограмме с временем удерживанием 2,25 мин (объемом удерживания 2250 мкл) соответствует 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропану.
По результатам измерений на хроматографе строят график зависимости площади хроматографического пика от концентрации определяемого вещества. График линеен в интервале концентраций 0,004-0,48 мкг 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в хроматографируемой пробе.
Методом наименьших квадратов рассчитывают уравнение градуировочного графика, которое в данном случае имеет вид:
S=151823⋅C-186,
где S - площадь хроматографического пика, С - концентрация определяемого вещества в хроматографируемой пробе, мкг.
Результаты количественного определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в ткани печени представлены в таблице 1.
Пример 2
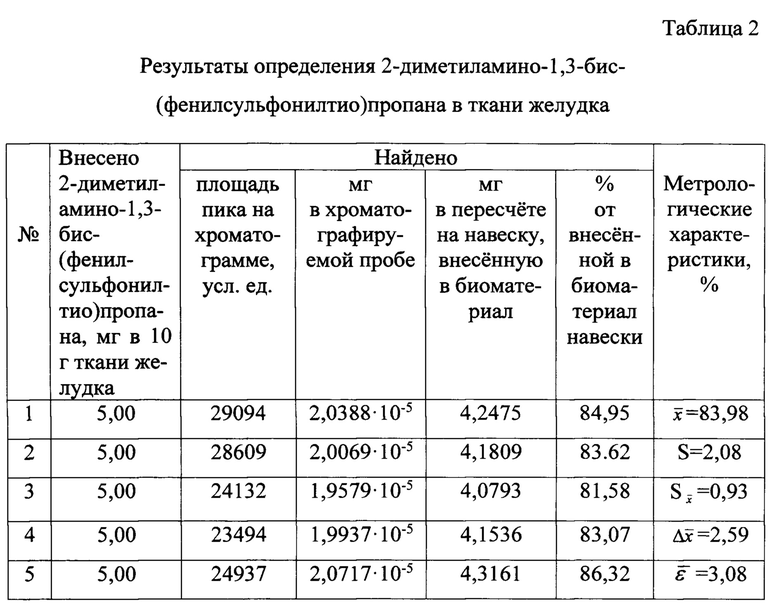
Определение 2-диметиламино-1,3-бис-(фенил-сульфонилтио)пропана в ткани желудка
К 10 г мелкоизмельченной ткани желудка прибавляют 5 мг 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана, тщательно перемешивают биологическую ткань с веществом и оставляют на полтора часа при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, обрабатывают порциями органического изолирующего агента, которым является смесь толуол-этилацетат в соотношении 7:3 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта. При этом биологический объект заливают 20 г смеси толуол-этилацетат в соотношении 7:3 по объему и выдерживают 45 минут при периодическом перемешивании. Извлечение отделяют от твердых частиц биоматериала, операцию настаивания повторяют в указанных условиях. Полученные органические извлечения объединяют, обезвоживают безводным сульфатом натрия путем фильтрования через стеклянный фильтр диаметром 4 см со слоем безводного сульфата натрия высотой 1-1,5 см. Фильтр дополнительно промывают 10 г смеси толуол-этилацетат в соотношении 7:3 по объему. Фильтрат и промывную жидкость объединяют, растворитель из объединенного извлечения испаряют в токе воздуха при комнатной температуре. Остаток растворяют в 8 мл ацетона, 2 мл полученного раствора смешивают с 1 г силикагеля L 40/100μ и испаряют остатки ацетона из сорбента в токе воздуха.
В колонку размером 490×10 мм вносят вначале 9 г силикагеля типа L 40/100μ, а затем, поверх образующегося слоя, - 1 г силикагеля L 40/100μ, содержащего анализируемое вещество, предварительно введенное в виде ацетонового раствора. Хроматографируют в колонке силикагеля L 40/100μ, вначале пропуская через колонку гексан. После истечения из колонки 20 мл элюата растворитель, находящийся над поверхностью столба сорбента, удаляют и начинают элюировать смесью растворителей этилацетат-гексан в соотношении 6:4 по объему. С момента начала подачи системы растворителей этилацетат-гексан в соотношении 6:4 по объему выходящий из колонки элюат собирают отдельными фракциями по 2 мл каждая. Фракции элюата с 48 по 56 включительно, содержащие анализируемое вещество, объединяют в выпарительной чашке, элюент испаряют в токе воздуха при комнатной температуре. Остаток растворяют в смеси растворителей ацетонитрил-вода в соотношении 6:4 по объему. Для этого вначале остаток обрабатывают 6-8 мл ацетонитрила, полученный раствор количественно переносят в мерную колбу вместимостью 10 мл и доводят содержимое колбы до метки ацетонитрилом (раствор А). 4,8 мл раствора А вносят в мерную колбу вместимостью 10 мл, прибавляют 1,2 мл ацетонитрила и доводят до метки водой. 4 мкл полученного раствора вводят в хроматограф типа «Alliance» фирмы «Waters».
Хроматографируют методом ВЭЖХ. Процесс хроматографирования осуществляют в колонке размерами 150×3,9 мм, заполненной обращеннофазовым сорбентом «Nova Pack» С-18, с применением подвижной фазы ацетонитрил-вода в соотношении 6:4 по объему и УФ-детектора на основе диодной матрицы.
Скорость подачи элюента составляет 1000 мкл/мин. Температура термостата колонки составляет 20°С. Оптическую плотность регистрируют при длине волны 224 нм.
Пик на хроматограмме с временем удерживания 2,25 мин (объемом удерживания 2250 мкл) соответствует 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропану.
Количественное содержание 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана определяют, исходя из площади хроматографического пика, по уравнению градуировочного графика и пересчитывают на навеску вещества, внесенную в ткань желудка.
Построение градуировочного графика и его уравнение приводятся выше в примере 1.
Результаты количественного определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в ткани желудка представлены в таблице 2.
Пример 3
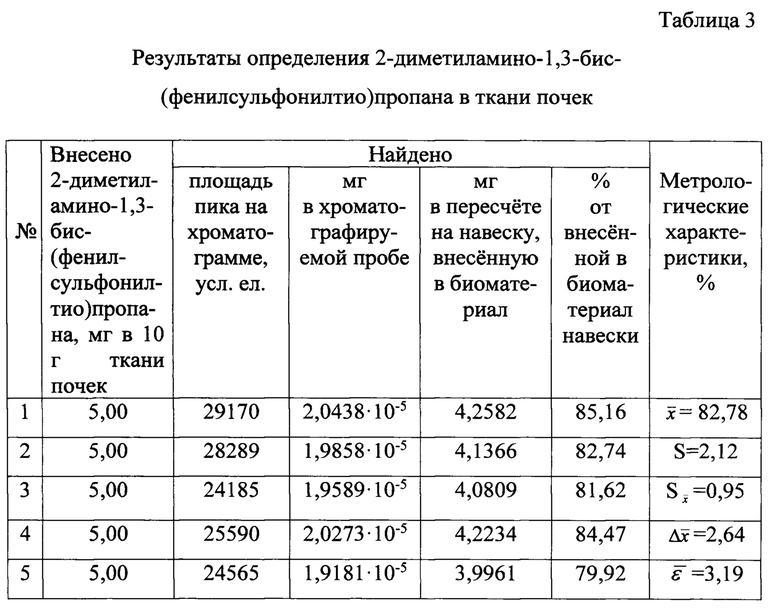
Определение 2-диметиламино-1,3-бис-(фенил-сульфонилтио)пропана вткани почек
К 10 г мелкоизмельченной ткани почек прибавляют 5 мг 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана, тщательно перемешивают биологическую ткань с веществом и оставляют на полтора часа при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, обрабатывают порциями органического изолирующего агента, которым является смесь толуол-этилацетат в соотношении 7:3 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта. При этом биологический объект заливают 20 г смеси толуол-этилацетат в соотношении 7:3 по объему и выдерживают 45 минут при периодическом перемешивании. Извлечение отделяют от твердых частиц биоматериала, операцию настаивания повторяют в указанных условиях. Полученные органические извлечения объединяют, обезвоживают безводным сульфатом натрия путем фильтрования через стеклянный фильтр диаметром 4 см со слоем безводного сульфата натрия высотой 1-1,5 см. Фильтр дополнительно промывают 10 г смеси толуол-этилацетат в соотношении 7:3 по объему. Фильтрат и промывную жидкость объединяют, растворитель из объединенного извлечения испаряют в токе воздуха при комнатной температуре. Остаток растворяют в 8 мл ацетона, 2 мл полученного раствора смешивают с 1 г силикагеля L 40/100μ и испаряют остатки ацетона из сорбента в токе воздуха.
В колонку размером 490×10 мм вносят вначале 9 г силикагеля типа L 40/100μ, а затем, поверх образующегося слоя, - 1 г силикагеля L 40/100μ, содержащего анализируемое вещество, предварительно введенное в виде ацетонового раствора. Хроматографируют в колонке силикагеля L 40/100μ, вначале пропуская через колонку гексан. После истечения из колонки 20 мл элюата растворитель, находящийся над поверхностью столба сорбента, удаляют и начинают элюировать смесью растворителей этилацетат-гексан в соотношении 6:4 по объему. С момента начала подачи системы растворителей этилацетат-гексан в соотношении 6:4 по объему выходящий из колонки элюат собирают отдельными фракциями по 2 мл каждая. Фракции элюата с 48 по 56 включительно, содержащие анализируемое вещество, объединяют в выпарительной чашке, элюент испаряют в токе воздуха при комнатной температуре. Остаток растворяют в смеси растворителей ацетонитрил-вода в соотношении 6:4 по объему. Для этого вначале остаток обрабатывают 6-8 мл ацетонитрила, полученный раствор количественно переносят в мерную колбу вместимостью 10 мл и доводят содержимое колбы до метки ацетонитрилом (раствор А). 4,8 мл раствора А вносят в мерную колбу вместимостью 10 мл, прибавляют 1,2 мл ацетонитрила и доводят до метки водой. 4 мкл полученного раствора вводят в хроматограф типа «Alliance» фирмы «Waters».
Хроматографируют методом ВЭЖХ. Процесс хроматографирования осуществляют в колонке размерами колонке размерами 150×3,9 мм, заполненной обращеннофазовым сорбентом «Nova Pack» С-18, с применением подвижной фазы ацетонитрил-вода в соотношении 6:4 по объему и УФ-детектора на основе диодной матрицы.
Скорость подачи элюента составляет 1000 мкл/мин. Температура термостата колонки составляет 20°С. Оптическую плотность регистрируют при длине волны 224 нм.
Пик на хроматограмме с временем удерживания 2,25 мин (объемом удерживания 2250 мкл) соответствует 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропану.
Количественное содержание 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана определяют, исходя из площади хроматографического пика, по уравнению градуировочного графика и пересчитывают на навеску вещества, внесенную в ткань почек.
Построение градуировочного графика и его уравнение приводятся выше в примере 1.
Результаты количественного определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в ткани почек представлены в таблице 3.
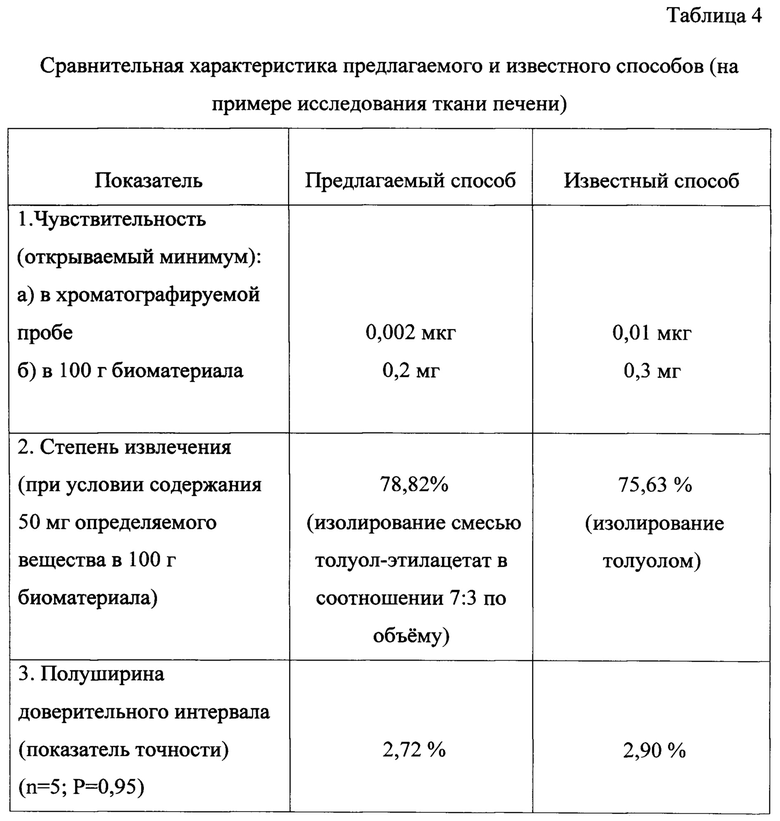
Предлагаемый способ по сравнению с прототипом в 1,5 раза повышает чувствительность определения в биологическом материале и в 5 раз в хроматографируемой пробе. Сравнительная характеристика предлагаемого и известного способов представлена в таблице 4.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ 2-ДИМЕТИЛАМИНО-1,3-БИС-(ФЕНИЛСУЛЬФОНИЛТИО)ПРОПАНА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2010 |
|
RU2426726C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 2,4,6-ТРИНИТРОМЕТИЛБЕНЗОЛА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2006 |
|
RU2319142C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ 2,4-ДИХЛОРФЕНОКСИУКСУСНОЙ КИСЛОТЫ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2011 |
|
RU2453848C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СЛОЖНОГО НИТРОФЕНОЛЬНОГО ПРЕПАРАТА "НИТРАФЕН" В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 1999 |
|
RU2153169C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДЕЛЬТАМЕТРИНА И ЛЯМБДА-ЦИГАЛОТРИНА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2009 |
|
RU2413225C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ O-(2,3-ДИГИДРО-2,2-ДИМЕТИЛ-7-БЕНЗОФУРАНИЛ)-N-МЕТИЛКАРБАМАТА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2004 |
|
RU2269780C1 |
| Способ определения 2,6-бис-[бис-(бета-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале | 2016 |
|
RU2617176C1 |
| Способ определения N-(бензимидазолил-2)-О-метилкарбамата в биологическом материале | 2018 |
|
RU2692127C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ N-(4-НИТРО-2-ФЕНОКСИФЕНИЛ)-МЕТАНСУЛЬФОНАМИДА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2013 |
|
RU2537121C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ТЕТРАМЕТИЛТИУРАМДИСУЛЬФИДА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2009 |
|
RU2415425C1 |
Изобретение относится к биологии, экологии, токсикологической и санитарной химии, а именно к способам определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в биологическом материале. Способ определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в биологическом материале заключается в том, что биологический материал измельчают, двукратно по 45 минут обрабатывают порциями органического изолирующего агента, которым является смесь толуол-этилацетат в соотношении 7:3 по объему, при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта, полученные органические извлечения объединяют, обезвоживают безводным сульфатом натрия, растворитель из объединенного извлечения испаряют, остаток растворяют в ацетоне, хроматографируют в колонке с силикагелем L 40/100 μ, вначале пропуская через нее гексан, а затем элюируя смесью растворителей этилацетат-гексан в соотношении 6:4 по объему, фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, остаток растворяют в смеси растворителей ацетонитрил-вода в соотношении 6:4 по объему и проводят определение методом ВЭЖХ. 4 табл., 3 пр.
Способ определения 2-диметиламино-1,3-бис-(фенилсульфонилтио)пропана в биологическом материале, заключающийся в том, что биологический объект измельчают, двукратно по 45 минут обрабатывают порциями органического изолирующего агента при условии, что масса каждой порции изолирующего агента в 2 раза превышает массу биологического объекта, полученные органические извлечения объединяют, обезвоживают безводным сульфатом натрия, растворитель из объединенного извлечения испаряют, остаток растворяют, хроматографируют в колонке с силикагелем L 40/100 μ, вначале пропуская через нее гексан, а затем элюируя смесью растворителей, фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, остаток растворяют в смеси растворителей и проводят определение методом ВЭЖХ в колонке, заполненной сорбентом, с применением подвижной фазы и УФ-детектора, отличающийся тем, что органическим изолирующим агентом является смесь толуол-этилацетат в соотношении 7:3 по объему, остаток, полученный после испарения растворителя из объединенного извлечения, растворяют в ацетоне, для элюирования из колонки с силикагелем L 40/100 μ применяют смесь растворителей этилацетат-гексан в соотношении 6:4 по объему, остаток, полученный после испарения элюента, растворяют в смеси растворителей ацетонитрил-вода в соотношении 6:4 по объему, определение методом ВЭЖХ проводят в колонке размерами 150×3,9 мм, заполненной сорбентом «Nova Pack» С-18, с применением подвижной фазы ацетонитрил-вода в соотношении 6:4 по объему и УФ-детектора на основе диодной матрицы.
| СПОСОБ ОПРЕДЕЛЕНИЯ 2-ДИМЕТИЛАМИНО-1,3-БИС-(ФЕНИЛСУЛЬФОНИЛТИО)ПРОПАНА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ | 2010 |
|
RU2426726C1 |
| В | |||
| К | |||
| Шорманов и др | |||
| Особенности распределения банкола в организме теплокровных животных / Судебно-медицинская экспертиза, 2013;56(5), стр | |||
| Нивелир для отсчетов без перемещения наблюдателя при нивелировании из средины | 1921 |
|
SU34A1 |
| В.Н | |||
| Кавецким и др | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
| Автоматические весы для сыпучих тел | 1925 |
|
SU2795A1 |
Авторы
Даты
2018-03-15—Публикация
2017-05-23—Подача