Изобретение относится к химической промышленности, а именно, к получению комплексов индия, европия, гадолиния, гольмия, эрбия, иттербия и лютеция с 5, 15-дифенилтетрабензопорфином.
За прототип принят способ получения комплексов трехвалентных металлов, в том числе индия и гадолиния, с 5,15-дифенилтетрабензопорфином. Он включает синтез исходного дибензопиррометена, темплатный синтез на его основе комплекса с цинка с 5,15-дифенйлтетрабензопорфином, его деметаллирование соляной кислотой и взаимодействие основания 5,15-дифенилтетрабензопорфина с хлоридом металла в растворителе. [Н.Е. Галанин // Дисс. докт. хим. наук. 2010. Иваново. Ивановский гос. хим.-технол. университет. 300 с.].
Способ реализуется в четыре стадии:
I стадия. Темплатный синтез 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она путем конденсации фталимида с ацетатом цинка.
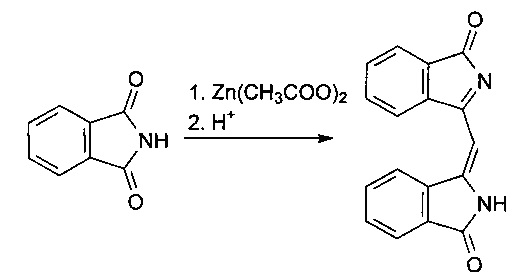
Реакцию вели при температуре 230-240°C в течение 20-30 минут. Полученную реакционную массу измельчали, кипятили 10 минут в 200 мл 10%-ной соляной кислоты, осадок отфильтровывали, промывали водой и очищали колоночной хроматографией, используя в качестве элюента ацетон. Получен 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-он. Выход - 40%.
II стадия. Темплатный синтез комплекса цинка с 5,15-дифенилтетрабензопорфином путем конденсации 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она с фенилуксусной кислотой и оксидом цинка.
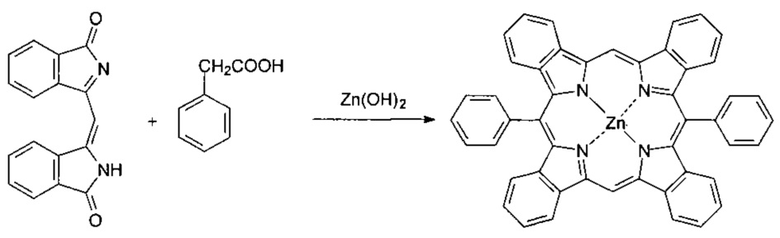
Реакцию вели при температуре 340°C в течение 1 часа. Реакционную массу измельчали, комплекс цинка экстрагировали бензолом и очищали колоночной хроматографией, используя в качестве элюента бензол. Получен 5,15-дифенилтетрабензопорфиринат цинка. Выход - 32%.
III стадия. Деметаллирование комплекса цинка с 5,15-дифенилтетрабензопорфирином путем обработки соляной кислотой.
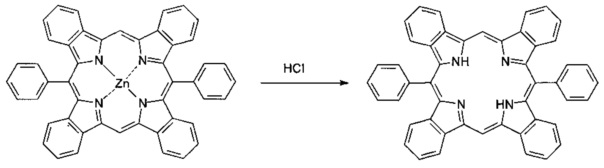
Комплекс цинка растворяли хлороформе, добавляли соляную кислоту, перемешивали 2 часа, разбавляли водой, органический слой отделяли, промывали водой, разбавленным раствором аммиака, растворитель отгоняли. Порфирин очищали колоночной хроматографией, используя в. качестве элюента бензол. Получен 5,15-дифенилтетрабензопорфирин. Выход - 75%.
IV стадия. Синтез комплексов индия или гадолиния с 5,15-дифенилтетрабензопорфирином путем взаимодействия основания порфирина с хлоридами металлов в кипящем ДМФА.
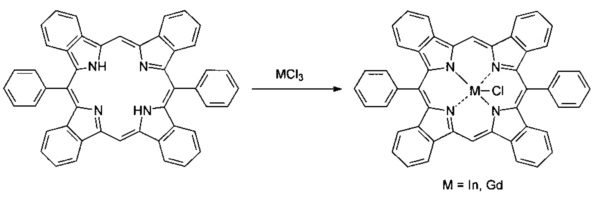
0.1 мМоля 5,15-дифенилтетрабензопорфирина растворяли в 20 мл ДМФА, добавляли 2 ммоля хлорида соответствующего металла и выдерживали полученную смесь при кипении в течение 3 часов. По завершении выдержки реакционную массу разбавляли водой, выпавший осадок отфильтровывали, промывали 200 мл воды и сушили на воздухе при 80°C. Полученные металлокомплексы очищали колоночной хроматографией, используя в качестве элюента бензол. Получены комплексы индия и гадолиния с 5,15-дифенилтетрабензопорфирином. Выход по стадии комплекса индия - 47%, комплекса гадолиния - 27%. В пересчете на исходный фталимид выход комплекса индия - 4.5%, комплекса гадолиния - 2.6%
Недостатками этого способа являются:
- Большое число химических стадий.
- Малый выход целевых продуктов;
Техническим результатом изобретения является поиск способа получения комплексов лантаноидов, в том числе индия, европия, гадолиния, гольмия, эрбия, иттербия и лютеция с 5,15-дифенилтетрабензопорфирином, который состоял бы из меньшего числа химических стадий и позволял бы получать целевые соединения с более высокими выходами.
Указанный результат достигается тем, что в способе получения комплексов лантаноидов с 5, 15-дифенилтетрабензопорфином, заключающемся во взаимодействии фталимида с ацетатом цинка при температуре 230-240°C в течение 20-30 мин, выделении и очистке целевых продуктов методом хроматографии, согласно изобретению, полученный 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-он сплавляют с фенилуксусной кислотой и солью лантаноида при температуре 320-330°C в течение 50-60 мин, а при очистке хроматографией в качестве элюента используют смесь толуола, ацетона и этанола в соотношении 1:1:1.
Изобретение позволяет:
1. Провести процесс в две химические стадии вместо четырех.
2. Повысить выход комплексов в расчете на фталимид до 7-12%, т.е. более чем в 2.5 раза.
Проведение синтеза целевых продуктов в несколько стадий с выделением промежуточных продуктов каждой стадии сопровождается их потерями. Сокращение числа стадий с четырех до двух позволило повысить общий выход целевых продуктов.
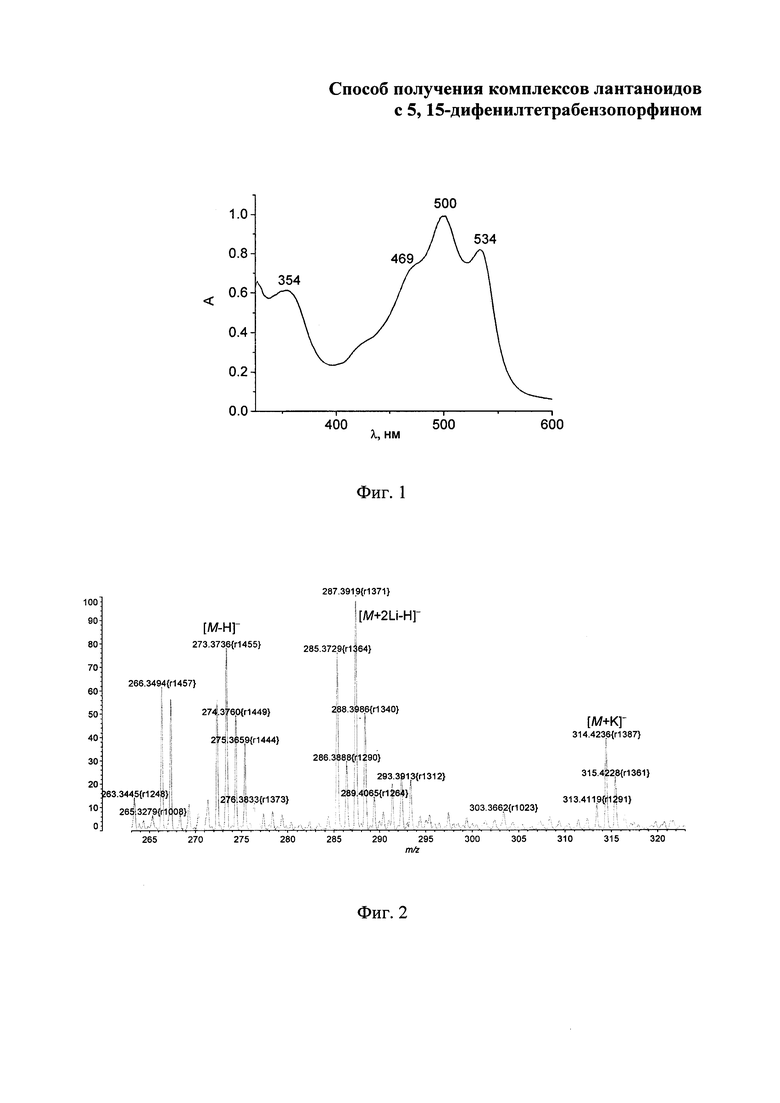
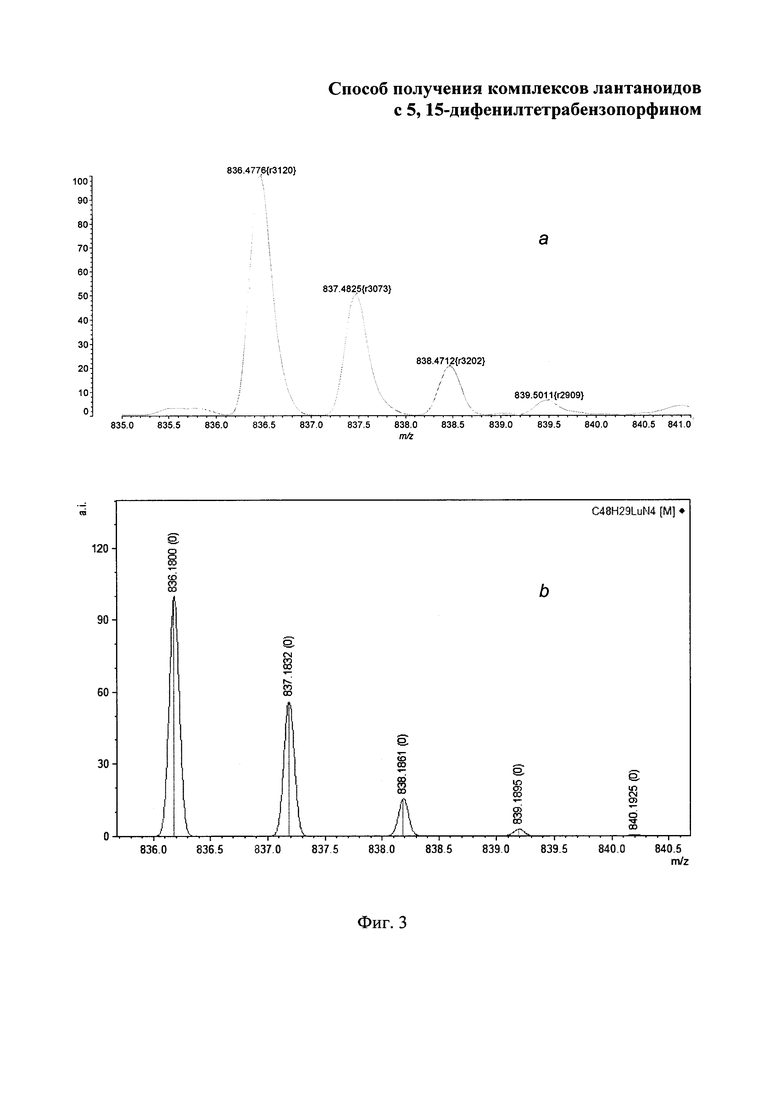
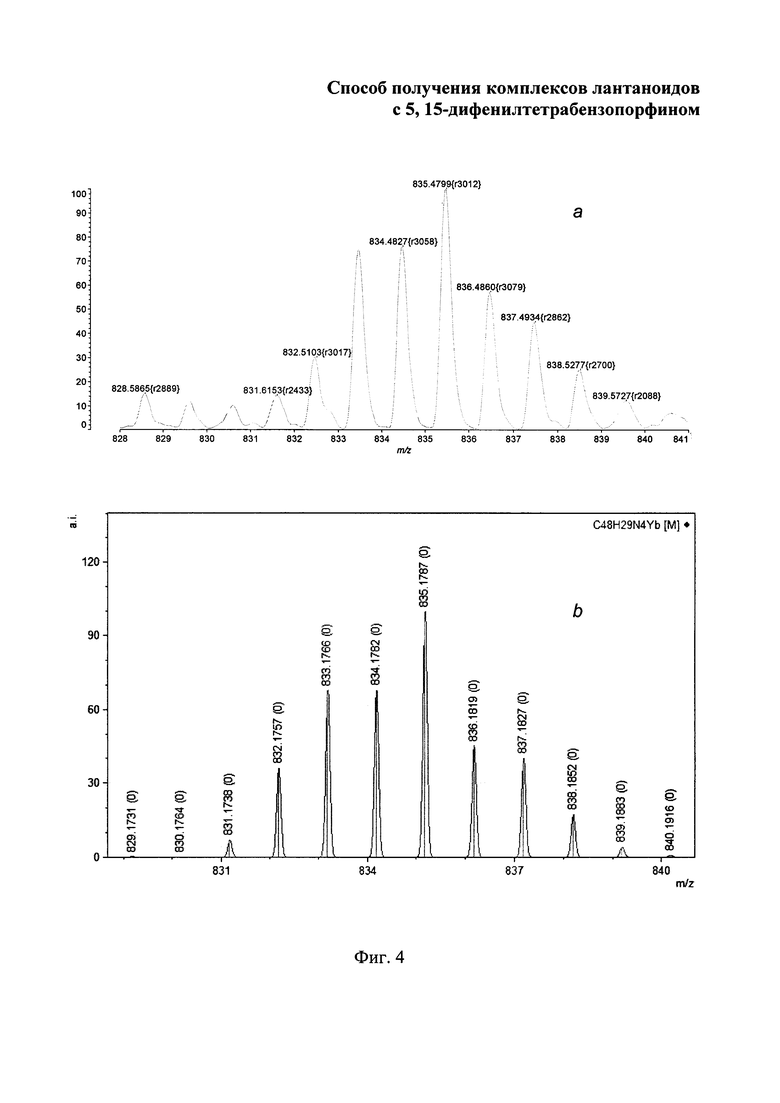
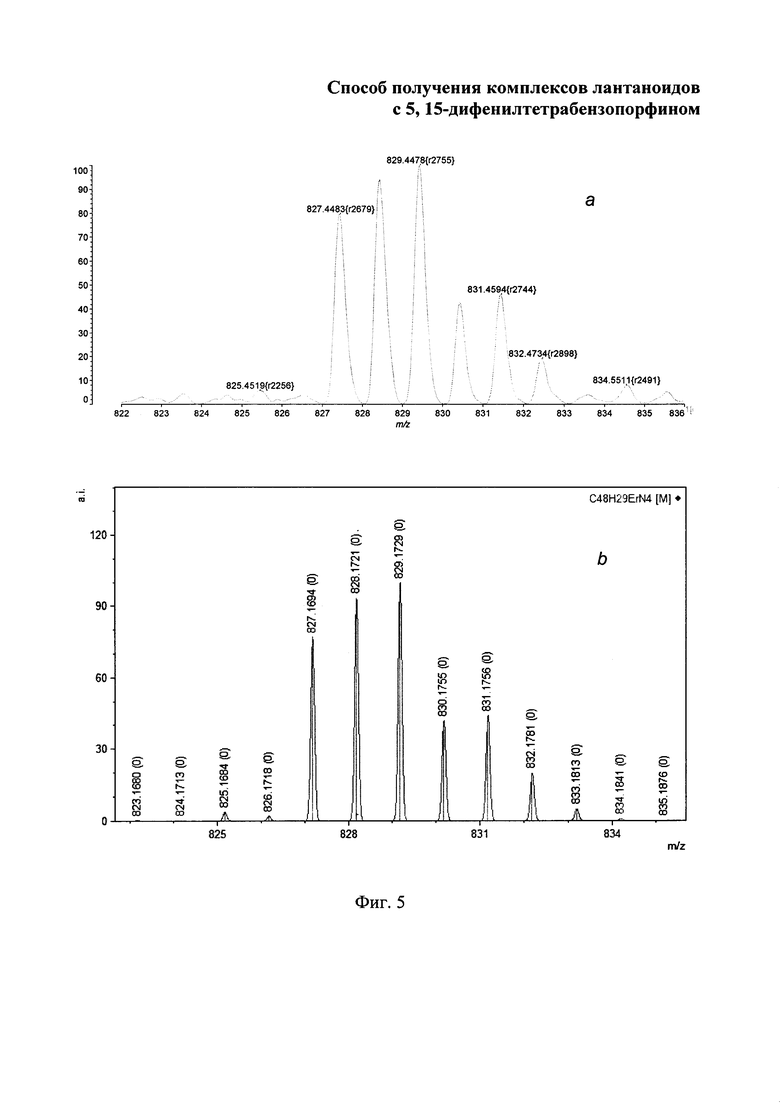
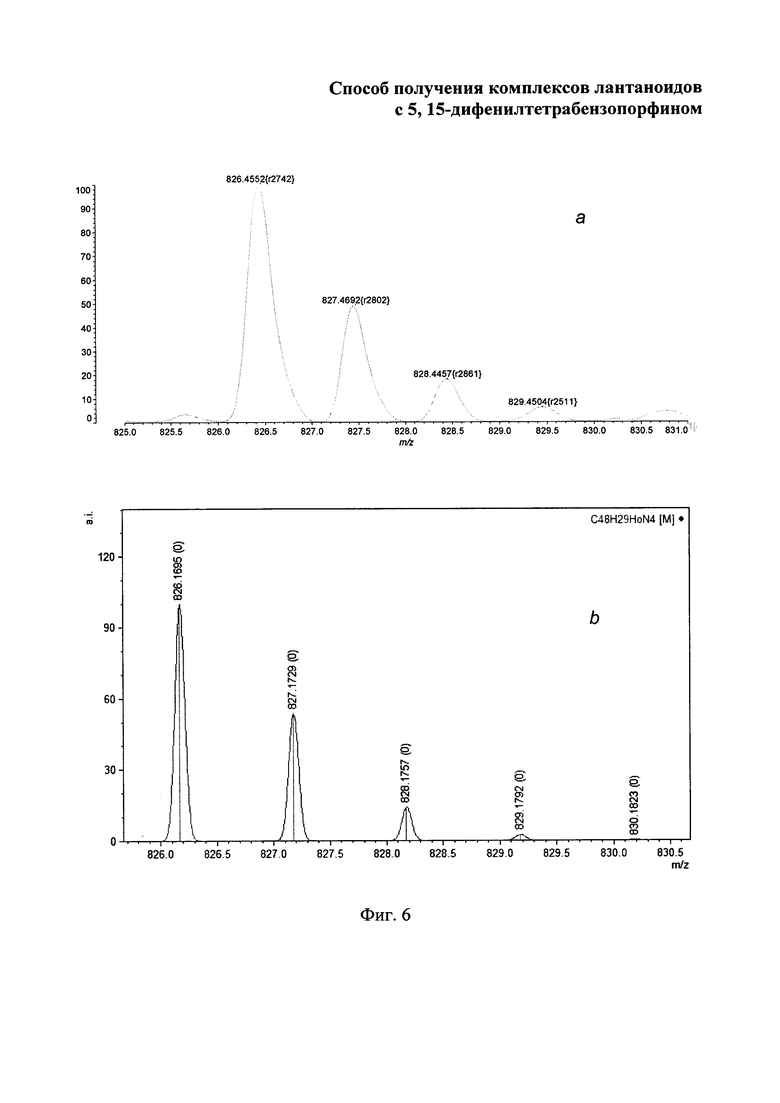
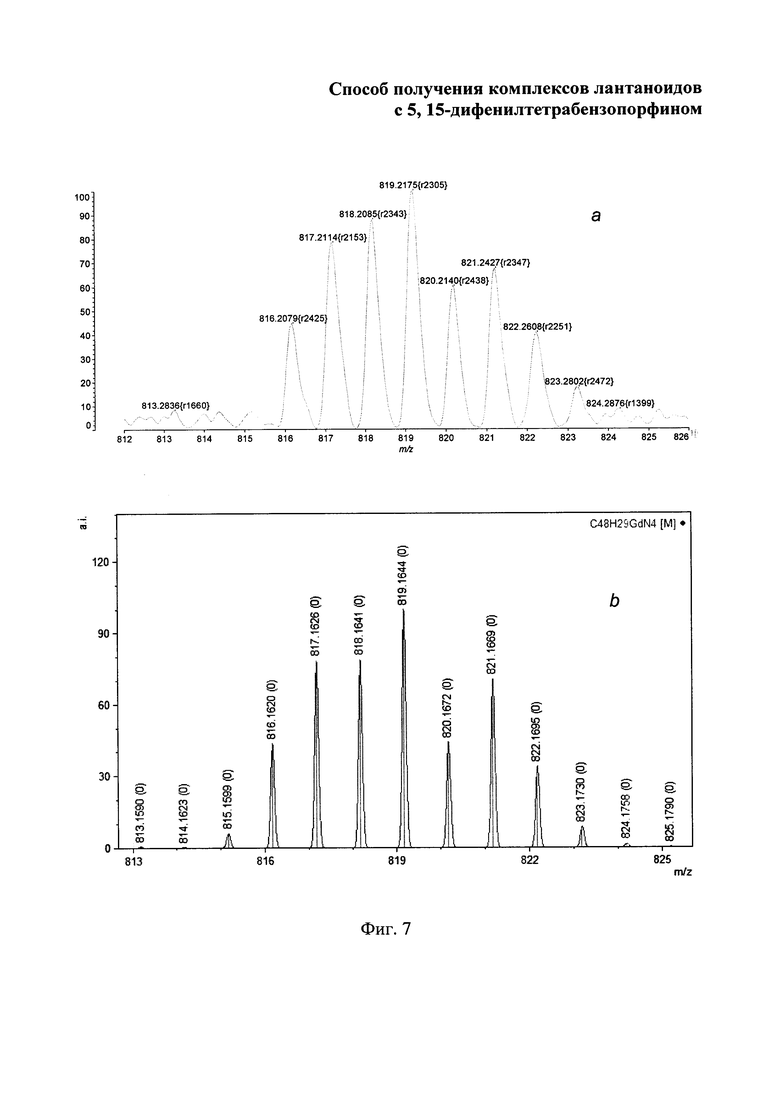
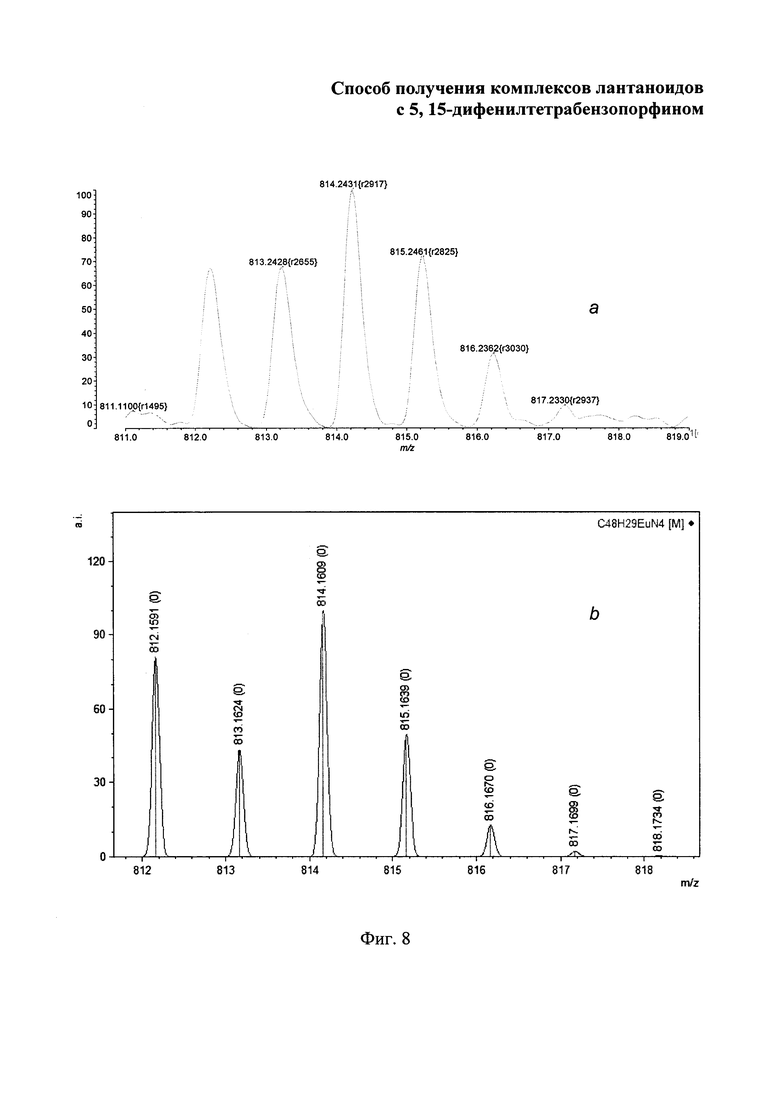
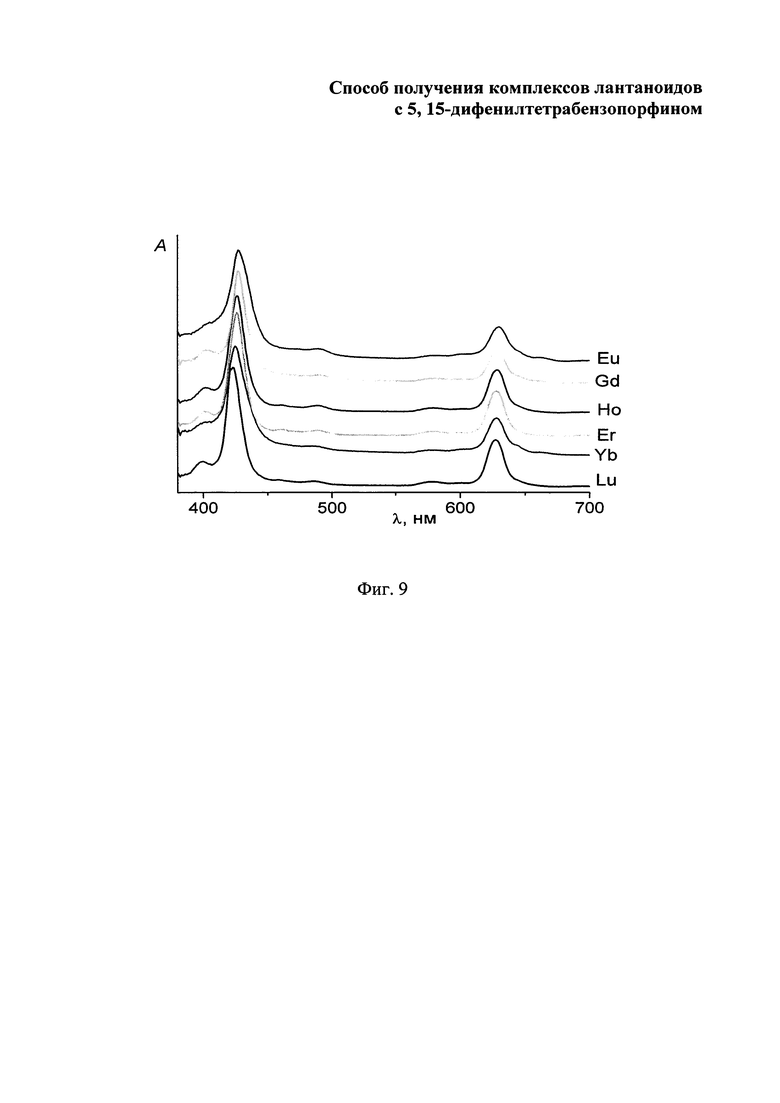
Изобретение поясняется чертежами, где на фиг. 1 приведен электронный спектр поглощения 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-он в ацетоне; на фиг. 2 - масс-спектр (LDI-TOF) 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-он; на фиг. 3 - изотопное расщепление иона [М-Cl+Н]+ в масс-спектре комплекса лютеция с 5,15-дифенилтетрабензопорфирином: где а - найдено, b - вычислено; на фиг. 4 - изотопное расщепление иона [М-Cl+Н]+ в масс-спектре комплекса иттербия с 5,15-дифенилтетрабензопорфирином, где а - найдено, b - вычислено; на фиг. 5 - изотопное расщепление иона [М-Cl+Н]+ в масс-спектре комплекса, эрбия с 5,15-дифенилтетрабензопорфирином, где а - найдено, b - вычислено; на фиг. 6 - изотопное расщепление иона [М-Cl+Н]+ в масс-спектре комплекса гольмия с 5,15-дифенилтетрабензопорфирином, где а - найдено, b - вычислено; на фиг. 7 - изотопное расщепление иона [М-Cl+Н]+ в масс-спектре комплекса гадолиния с 5,15-дифенилтетрабензопорфирином, где а - найдено, b -вычислено; на фиг. 8 - изотопное расщепление иона [М-Cl+Н]+в масс-спектре комплекса европия) с 5,15-дифенилтетрабензопорфирином, где а - найдено, b - вычислено; на фиг. 9 - электронные спектры поглощения комплексов лютеция, иттербия, эрбия, гольмия, гадолиния и европия с 5,15-дифенилтетрабензопорфирином в ДМФА.
Для реализации способа используются следующие вещества:
Фталимид - ТУ 6-09-3635-75;
Ацетат цинка дигидрат - ГОСТ 5823-78;
Фенилуксусная кислота, импортная, CAS №103-82-2;
Индий треххлористый, импортный, CAS №10025-82-8;
Европий треххлористый 6-водный, импортный, CAS №10025-76-0;
Гадолиний треххлористый 6-водный, импортный, CAS №13450-84-5;
Гольмий треххлористый 6-водный, импортный, CAS №10138-62-2;
Эрбий треххлористый 6-водный, импортный, CAS №10025-75-9;
Иттербий треххлористый 6-водный, импортный CAS №10361-91-8;
Лютеций хлористый 6-водный, импортный, CAS №15230-79-2;
Способ реализуют следующим образом.
Пример 1.
I стадия. Взаимодействие фталимида с ацетатом цинка, по схеме:
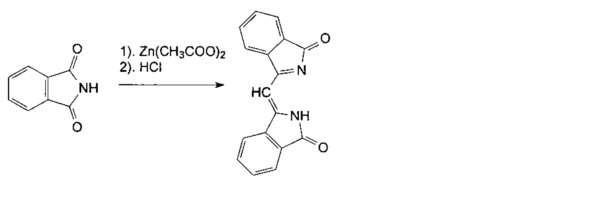
Смесь 16 г фталимида и 25 г дигидрата ацетата цинка нагревают до 230-240°C и выдерживают при этой температуре 20-30 мин. После охлаждения плав извлекают, измельчают и промывают последовательно 10% раствором едкого натра, водой, 10% раствором соляной кислоты, водой до нейтральной реакции промывных вод и высушивают.
Получен 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-он.
Выход 6.04 г (40%), порошок красного цвета, растворим в ацетоне, пиридине, ДМФА, уксусной кислоте, не растворим в воде. Тпл. 231-232°C.
Электронный спектр поглощения (ДМФА), λмакс., нм (А/Амакс): 354 (0.62), 469 пл., 500 (1.00), 534 (0.76).
1Н ЯМР, δН, м.д.: 9.73 с (1H, NH), 8.09-7.75 м (8Н, Ar-H), 5.82 с (1Н, мезо-H).
Масс-спектр (LDI-TOF, режим отрицательных ионов), m/z: 273.37 [М-H]-.
Найдено: С 74.40, Н 3.70, N 10.19. C17H10N2O2
Вычислено: С 74.45 Н 3.67, N 10.21.
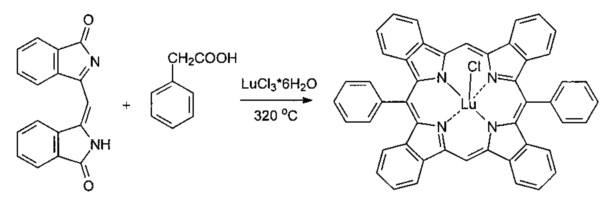
II стадия. Взаимодействие 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она с фенилуксусной кислотой и треххлористым индием, по схеме:
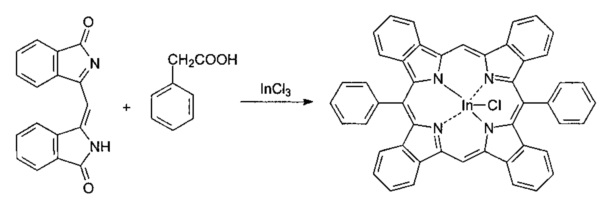
Смесь 0.2 г (0.72 ммоль) 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она, 0.3 г (2.2 ммоль) фенилуксусной кислоты и 0.16 г (0.72 ммоль) треххлористого индия сплавляли при температуре 320°C в течение 1 ч, охлаждали, измельчали и экстрагировали ДМФА в аппарате Сокслета. Экстракт разбавляли водой, экстрагировали хлороформом, органический слой промывали водой, растворитель отгоняли, остаток растворяли в минимальном количестве ДМФА и хроматографировали на колонке, заполненной силикагелем Kieselgel 60, используя в качестве элюента смесь толуол - ацетон - этанол (1:1:1), собирая основную зеленую зону.
Получен комплекс индия с 5, 15-дифенилтетрабензопорфином.
Выход 0.1 г (32%). В прототипе выход комплекса составил 0.014 г (4,5%). Порошок зеленого цвета, не растворим в воде, хорошо растворим в ДМФА, ДМСО, хлороформе, ТГФ.
Электронный спектр поглощения в ДМФА, λмакс., нм (lg ε): 636 (4.88), 434 (5.22).
Масс-спектр (MALDI), m/z: 775.28 [M-Cl]+.
Найдено, %: С 71.22; Н 3.51; N 6.14. C48H28ClInN4.
Вычислено, %: С 71.08; Н 3.48; N 6.91.
Результаты проведенной серии опытов приведены в таблице 1:
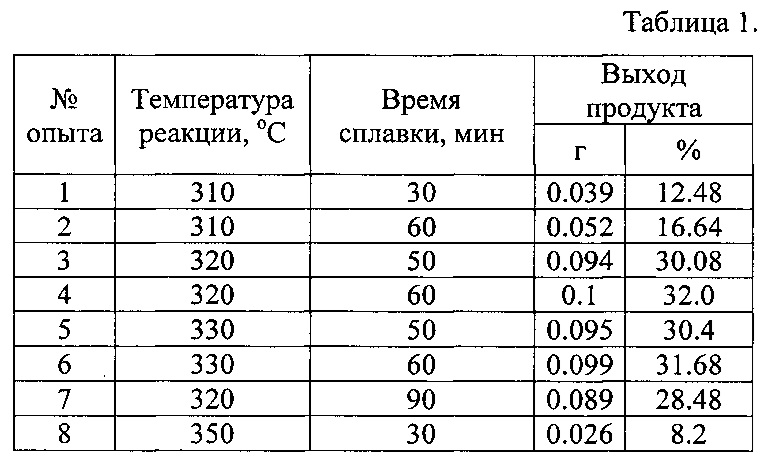
При температуре реакции ниже 320°C скорость реакции становится ниже, требуется большее время сплавки. Увеличение времени сплавки более 60 минут и (или) температуры более 330°C может привести к отщеплению заместителей и понижает выход целевого продукта.
Пример 2.
I стадия. Осуществляют по примеру 1.
II стадия. Осуществляют по примеру 1, с использованием гексагидрата хлорида европия.
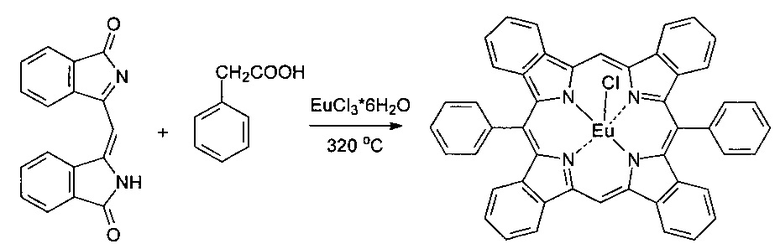
Смесь 0.2 г (0.72 ммоль) 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она, 0.3 г (2.2 ммоль) фенилуксусной кислоты и 0.19 г (0.72 ммоль) треххлористого европия нагревали при температуре 320°C в течение 1 ч, охлаждали, измельчали и экстрагировали ДМФА в аппарате Сокслета. Экстракт разбавляли водой, экстрагировали хлороформом, органический слой промывали водой, растворитель отгоняли, остаток растворяли в минимальном количестве ДМФА и хроматографировали на колонке, заполненной силикагелем Kieselgel 60, используя в качестве элюента смесь толуол-ацетон-этанол (1:1:1), собирая основную зеленую зону.
Получен комплекс европия с 5, 15-дифенилтетрабензопорфином. Выход 0.056 г (18%).
Порошок зеленого цвета, не растворим в воде, хорошо растворим в ДМФА, ДМСО, хлороформе, ТГФ.
Электронный спектр поглощения в ДМФА, λмакс., нм (lg ε): 630 (4.60), 427 (5.03).
Масс-спектр (MALDI), m/z: 814.24 [М-Cl]+.
Найдено, %: С 65.34; Н 3.58; N 6.10. C48H28ClEuN4⋅2H2O.
Вычислено, %: С 65.20; Н 3.65; N 6.34.
Результаты проведенной серии опытов приведены в таблице 2:
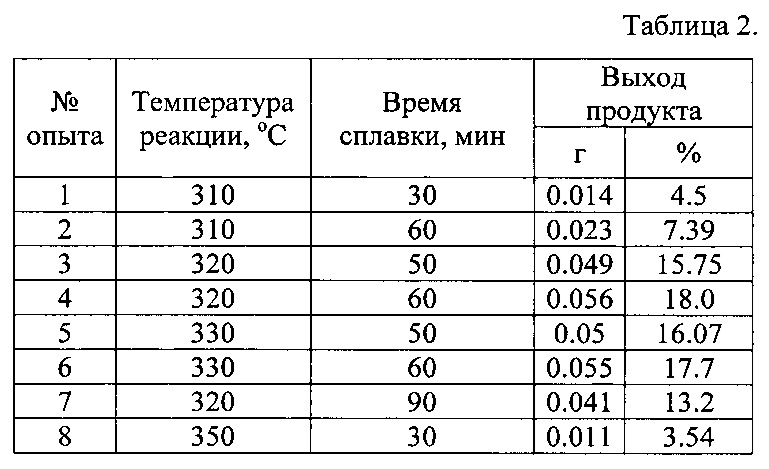
Выводы по результатам опытов аналогичны примеру 1.
Пример 3.
I стадия. Осуществляют по примеру 1.
II стадия. Осуществляют по примеру 1, с использованием гексагидрата хлорида гадолиния.
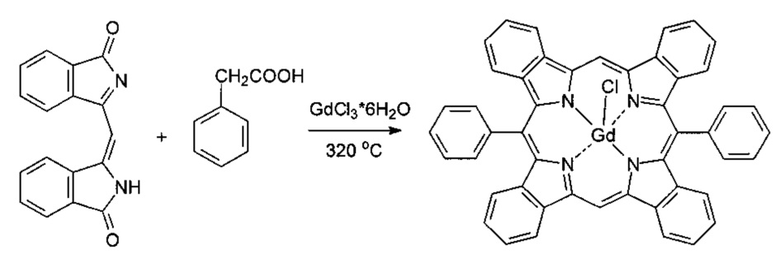
Смесь 0.2 г (0.72 ммоль) 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она, 0.3 г (2.2 ммоль) фенилуксусной кислоты и 0.19 г (0.72 ммоль) треххлористого гадолиния нагревали при температуре 320°C в течение 1 ч, охлаждали, измельчали и экстрагировали ДМФА в аппарате Сокслета. Экстракт разбавляли водой, экстрагировали хлороформом, органический слой промывали водой, растворитель отгоняли, остаток растворяли в минимальном количестве ДМФА и хроматографировали на колонке, заполненной силикагелем Kieselgel 60, используя в качестве элюента смесь толуол-ацетон-этанол (1:1:1), собирая основную зеленую зону.
Получен комплекс гадолиния с 5, 15-дифенилтетрабензопорфином.
Выход 0.07 г (23%).
Порошок зеленого цвета, не растворим в воде, хорошо растворим в ДМФА, ДМСО, хлороформе, ТГФ.
Электронный спектр поглощения в ДМФА, λмакс. нм (lg ε): 629 (4.62), 427 (5.06).
Масс-спектр (MALDI), m/z: 819.22 [М-Cl]+.
Найдено, %: С 64.14; Н 3.60; N 6.01. C48H28ClGdN4⋅2H2O.
Вычислено, %: С 64.81; Н 3.63; N 6.30.
Результаты проведенной серии опытов приведены в таблице 3:
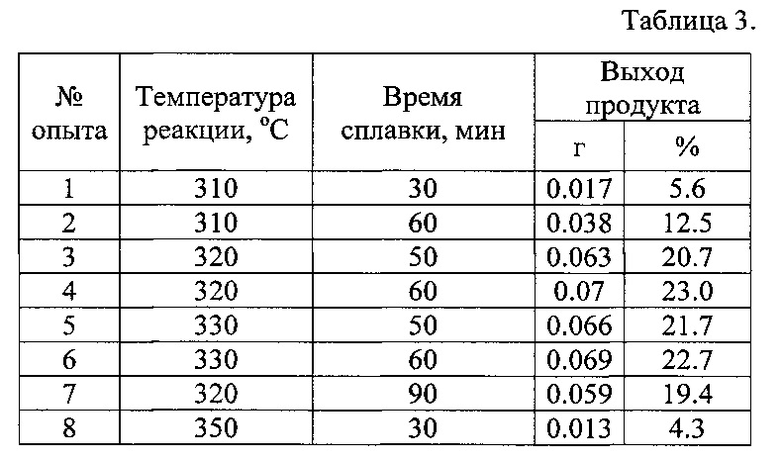
Выводы по результатам опытов аналогичны примеру 1.
Пример 4.
I стадия. Осуществляют по примеру 1.
II стадия. Осуществляют по примеру 1, с использованием гексагидрата хлорида гольмия.
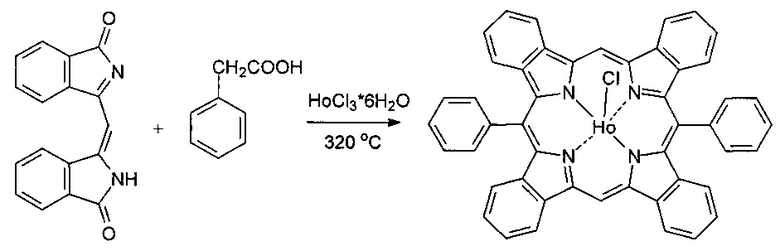
Смесь 0.2 г (0.72 ммоль) 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она, 0.3 г (2.2 ммоль) фенилуксусной кислоты и 0.195 г (0.72 ммоль) треххлористого гольмия нагревали при температуре 320°C в течение 1 ч, охлаждали, измельчали и экстрагировали ДМФА в аппарате Сокслета. Экстракт разбавляли водой, экстрагировали хлороформом, органический слой промывали водой, растворитель отгоняли, остаток растворяли в минимальном количестве ДМФА и хроматографировали на колонке, заполненной силикагелем Kieselgel 60, используя в качестве элюента смесь толуол-ацетон-этанол (1:1:1), собирая основную зеленую зону.
Получен комплекс гольмия с 5, 15-дифенилтетрабензопорфином.
Выход 0.08 г (26%).
Порошок зеленого цвета, не растворим в воде, хорошо растворим в ДМФА, ДМСО, хлороформе, ТГФ.
Электронный спектр поглощения в ДМФА, λмакс., нм (lg ε): 628 (4.64), 427 (5.05).
Масс-спектр (MALDI), m/z: 826.46 [М-Cl]+.
Найдено, %: С 64.33; Н 3.56; N 5.98. C48H28ClHoN4⋅2H2O.
Вычислено, %: С 64.26; Н 3.60; N 6.24.
Результаты проведенной серии опытов приведены в таблице 4:
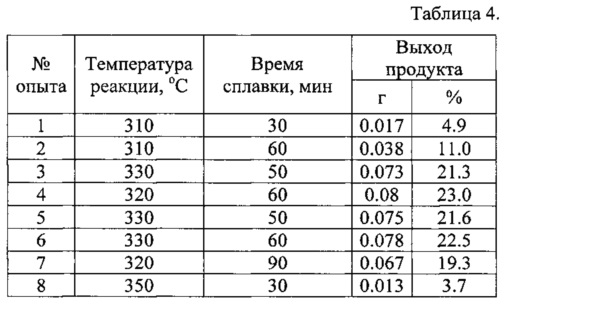
Выводы по результатам опытов аналогичны примеру 1.
Пример 5.
I стадия. Осуществляют по примеру 1.
II стадия. Осуществляют по примеру 1, с использованием гексагидрата хлорида эрбия.
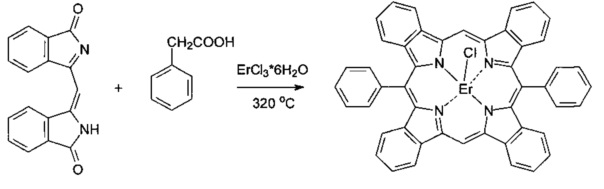
Смесь 0.2 г (0.72 ммоль) 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она, 0.3 г (2.2 ммоль) фенилуксусной кислоты и 0.197 г (0.72 ммоль) треххлористого эрбия нагревали при температуре 320°C в течение 1 ч, охлаждали, измельчали и экстрагировали ДМФА в аппарате Сокслета. Экстракт разбавляли водой, экстрагировали хлороформом, органический слой промывали водой, растворитель отгоняли, остаток растворяли в минимальном количестве ДМФА и хроматографировали на колонке, заполненной силикагелем Kieselgel 60, используя в качестве элюента смесь толуол - ацетон - этанол (1:1:1), собирая основную зеленую зону.
Получен комплекс эрбия с 5, 15-дифенилтетрабензопорфином.
Выход 0.093 г (30%).
Порошок зеленого цвета, не растворим в воде, хорошо растворим в ДМФА, ДМСО, хлороформе, ТГФ.
Электронный спектр поглощения в ДМФА, λмакс., нм (lg ε): 628 (4.71), 426 (5.11).
Масс-спектр (MALDI), m/z: 829.45 [М-Cl]+.
Найдено, %: С 65.11; Н 3.44; N 6.22. C48H28ClErN4H2O.
Вычислено, %: С 65.40; Н 3.43; N 6.36.
Результаты проведенной серии опытов приведены в таблице 5:
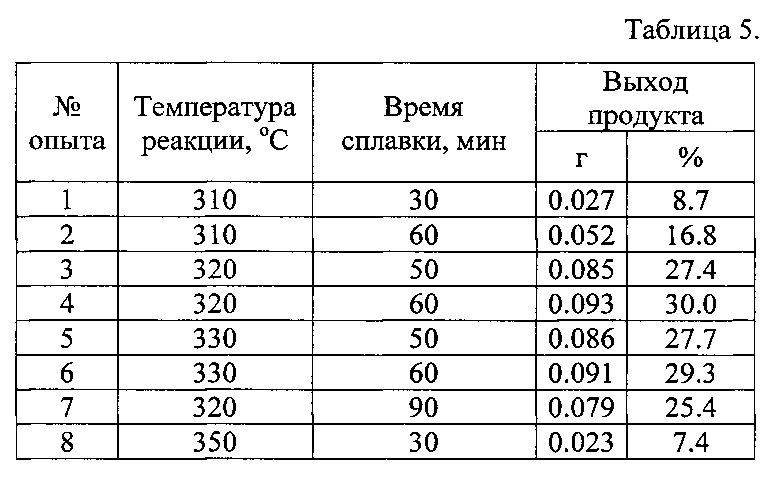
Выводы по результатам опытов аналогичны примеру 1.
Пример 6.
I стадия. Осуществляют по примеру 1.
II стадия. Осуществляют по примеру 1, с использованием гексагидрата хлорида иттербия.
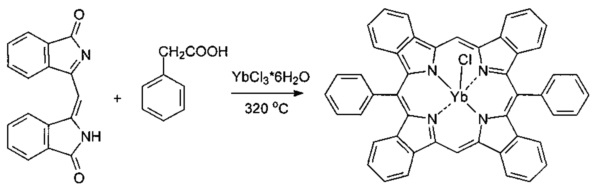
Смесь 0.2 г (0.72 ммоль) 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она, 0.3 г (2.2 ммоль) фенилуксусной кислоты и 0.2 г (0.72 ммоль) треххлористого иттербия нагревали при температуре 320°C в течение 1 ч, охлаждали, измельчали и экстрагировали ДМФА в аппарате Сокслета. Экстракт разбавляли водой, экстрагировали хлороформом, органический слой промывали водой, растворитель отгоняли, остаток растворяли в минимальном количестве ДМФА и хроматографировали на колонке, заполненной силикагелем Kieselgel 60, используя в качестве элюента смесь толуол - ацетон - этанол (1:1:1), собирая основную зеленую зону.
Получен комплекс иттербия с 5, 15-дифенилтетрабензопорфином.
Выход 0.085 г (27%).
Порошок зеленого цвета, не растворим в воде, хорошо растворим в ДМФА, ДМСО, хлороформе, ТГФ.
Электронный спектр поглощения в ДМФА, λмакс, нм (lg ε): 628 (4.62), 425 (5.07).
Масс-спектр (MALDI), m/z: 835.48 [М-Cl]+.
Найдено, %: С 64.69; Н 3.52; N 6.13. C48H28ClYbN4⋅2H2O.
Вычислено, %: С 63.68; Н 3.56; N 6.19.
Результаты проведенной серии опытов приведены в таблице 6.
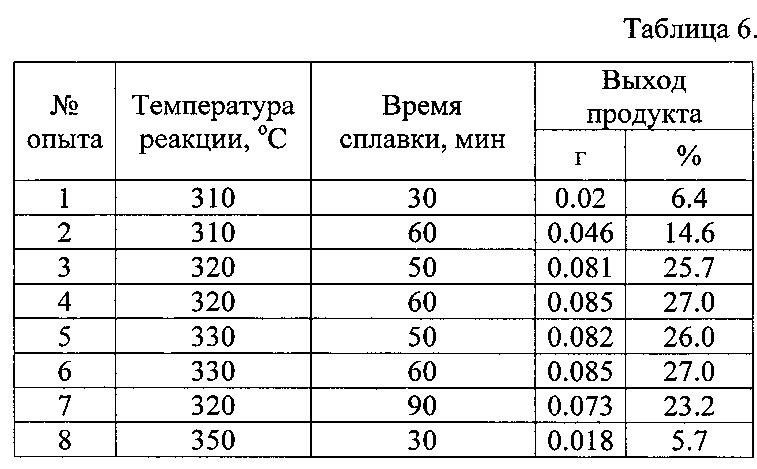
Выводы по результатам опытов аналогичны примеру 1.
Пример 7.
I стадия. Осуществляют по примеру 1.
II стадия. Осуществляют по примеру 1, с использованием гексагидрата хлорида лютеция.
Смесь 0.2 г (0.72 ммоль) 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-она, 0.3 г (2.2 ммоль) фенилуксусной кислоты и 0.2 г (0.72 ммоль) треххлористого лютеция нагревали при температуре 320°C в течение 1 ч, охлаждали, измельчали и экстрагировали ДМФА в аппарате Сокслета. Экстракт разбавляли водой, экстрагировали хлороформом, органический слой промывали водой, растворитель отгоняли, остаток растворяли в минимальном количестве ДМФА и хроматографировали на колонке, заполненной силикагелем Kieselgel 60, используя в качестве элюента смесь толуол - ацетон - этанол (1:1:1), собирая основную зеленую зону.
Получен комплекс лютеция с 5, 15-дифенилтетрабензопорфином.
Выход 0.09 г (29%).
Порошок зеленого цвета, не растворим в воде, хорошо растворим в ДМФА, ДМСО, хлороформе, ТГФ.
Электронный спектр поглощения в ДМФА, λмакс., нм (lg ε): 627 (4.73), 423 (5.10).
Масс-спектр (MALDI), m/z: 836.48 [М-Cl]+.
Найдено, %: С 64.23; Н 3.41; N 6.21. C48H28ClLuN4⋅H2O.
Вычислено, %: С 64.84; Н 3.40; N 6.30.
Результаты проведенной серии опытов приведены в таблице 7.
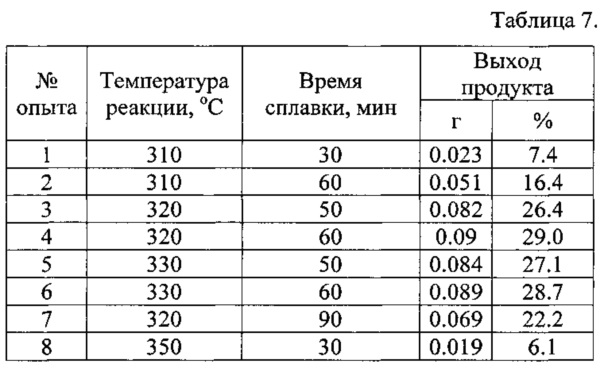
Выводы по результатам опытов аналогичны примеру 1.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ДВУХПАЛУБНОГО КОМПЛЕКСА ГАДОЛИНИЯ С ТЕТРАБЕНЗОПОРФИРИНОМ | 2017 |
|
RU2649402C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСОВ ЛЮТЕЦИЯ И ГАДОЛИНИЯ С ТЕТРАБЕНЗОПОРФИРИНОМ | 2015 |
|
RU2579149C1 |
| 5,15-ДИАМИНОТЕТРАБЕНЗОПОРФИРИНАТ ЦИНКА | 2011 |
|
RU2454417C1 |
| ПРОЛЕКАРСТВА 3-АЦИЛ-2-ОКСИНДОЛ-1-КАРБОКСАМИДОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2124514C1 |
| МЕЗО-ТРАНС-ДИГЕКСАДЕЦИЛТЕТРАБЕНЗОПОРФИРИНАТ ЦИНКА | 2006 |
|
RU2326883C1 |
| ПРОИЗВОДНЫЕ БЕНЗОДИАЗЕПИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2139282C1 |
| ИЗОИНДОЛИНОНОВЫЕ ИНГИБИТОРЫ ВЗАИМОДЕЙСТВИЯ MDM2-P53, ОБЛАДАЮЩИЕ ПРОТИВОРАКОВОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2797295C1 |
| ИЗОИНДОЛИНОНОВЫЕ ИНГИБИТОРЫ ВЗАИМОДЕЙСТВИЯ MDM2-P53, ОБЛАДАЮЩИЕ ПРОТИВОРАКОВОЙ АКТИВНОСТЬЮ | 2016 |
|
RU2794333C1 |
| КОМПЛЕКСЫ 1-МЕТИЛТЕТРАБЕНЗООКТАДЕГИДРОКОРРИНА С ЦИНКОМ, МЕДЬЮ И ГИДРОКСИЛАНТАНОМ | 2007 |
|
RU2360915C1 |
| 5-ЗАМЕЩЕННЫЕ ИЗОИНДОЛИНОВЫЕ СОЕДИНЕНИЯ | 2007 |
|
RU2448101C2 |
Изобретение относится к способу получения комплексов лантаноидов с 5,15-дифенилтетрабензопорфином. Способ включает взаимодействие фталимида с ацетатом цинка при температуре 230-240°C в течение 20-30 мин, сплавление полученного 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-он с фенилуксусной кислотой и солью лантаноида при температуре 320-330°C в течение 50-60 мин, выделение и очистку целевых продуктов методом хроматографии. Техническим результатом изобретения являются более высокие выходы целевых соединений при меньшем числе химических стадий. 1 з.п. ф-лы, 9 ил, 7 табл., 7 пр.
1. Способ получения комплексов лантаноидов с 5,15-дифенилтетрабензопорфином, заключающийся во взаимодействии фталимида с ацетатом цинка при температуре 230-240°C в течение 20-30 мин, выделении и очистке целевых продуктов методом хроматографии, отличающийся тем, что полученный 3-[(1-оксо-1H-изоиндол-3-ил)метилен]-2,3-дигидро-1H-изоиндол-1-он сплавляют с фенилуксусной кислотой и солью лантаноида при температуре 320-330°C в течение 50-60 мин.
2. Способ по п. 1, отличающийся тем, что при очистке целевых продуктов методом хроматографии в качестве элюента используют смесь толуола, ацетона и этанола в соотношении 1:1:1.
| ГАЛАНИН Н.Е., Синтез и свойства мезо-замещенных тетрабензопорфиринов и их структурных аналогов, Автореферат дисс | |||
| докт | |||
| хим | |||
| наук, Иваново, 2010, 32 c | |||
| КУДРИК Е.В | |||
| и др., Комплексы "сэндвичевого" типа тетрабензопорфирин-фталоцианин с лютецием и гадолинием, Синтез и спектральные свойства, Журнал общей химии, 2000, т | |||
| Деревянный торцевой шкив | 1922 |
|
SU70A1 |
| Кипятильник для воды | 1921 |
|
SU5A1 |
| Ручной ткацкий станок | 1923 |
|
SU821A1 |
| VINOGRADOV S.A | |||
| et al, Metallotetrabenzoporphyrins | |||
| New phosphorescent probes for oxygen measurement, J | |||
| Chem | |||
| Soc., Perkin Transaction 2, 1995, p | |||
| Клапанный регулятор для паровозов | 1919 |
|
SU103A1 |
| US 5830138 A1, 03.11.1998. | |||
Авторы
Даты
2017-06-14—Публикация
2016-06-21—Подача