Способ относится к химии высокомолекулярных соединений, а именно к способу получения биологически активных полимеров, и касается получения полимерных комплексов антибиотика рифампицина. Антибиотик рифампицин (I) является одним из основных эффективных средств, используемых в настоящее время в комбинированной терапии туберкулезных заболеваний.
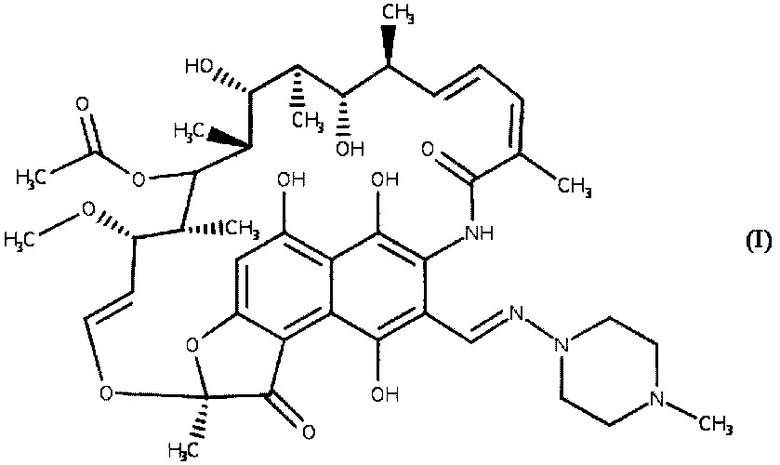
Однако рифампицин токсичен, в частности обладает выраженной гепатотоксичностью. Поскольку рифампицин незаменим при лечении туберкулеза, занимающего первое место в структуре смертности от инфекционных заболеваний, модификация его свойств является актуальной задачей. При этом важно добиться не только снижения токсичности этого антибиотика, но и полного сохранения его биоспецефической активности. Как известно [Г.Е. Афиногенов, Е.Ф. Панарин. Антимикробные полимеры. СПб.: Гиппократ, 1993, 261 с.], одним из распространенных, технологичных способов снижения токсичности лекарственных веществ (ЛВ) является их комплексообразование с синтетическими полиэлектролитами в водных растворах.
Ближайшим аналогом заявляемого способа являются водорастворимые комплексы рифампицина (II) на основе сополимеров N-винил-2-пирролидона (ВП) с 3-бутеновой кислотой общей формулы:
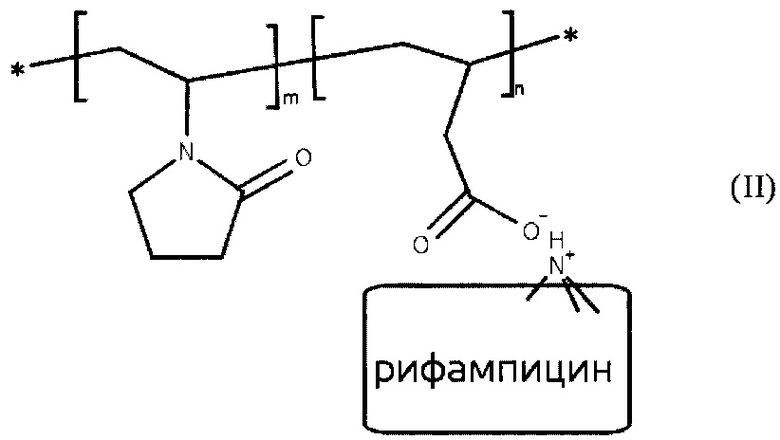
Комплексообразование проводят в гетерофазных условиях при добавлении к водному раствору полиэлектролита нерастворимого в воде рифампицина при массовом соотношении полиэлектролит : антибиотик, равном 2,3:1. Полимерные комплексы содержат 20,6-25,2 мас. % антибиотика. По показателю цитотоксичности они в 2,2-2,6 раза менее токсичны, чем рифампицин [М.С. Борисенко, Н.В. Захарова, Е.Б. Тарабукина, М.В. Соловский// ЖПХ, 2015. Т. 88. Вып. 11. С. 1579-1585]. Однако известные полимерные комплексы рифампицина ингибируют рост микобактерий туберкулеза при достаточно высокой концентрации (МИК), равной 50 мкг/мл. В то же время МИК рифампицина в отношении Micobacterium tuberculosis H37Rv составляет 3,1 мкг/мл.
Технической задачей изобретения является разработка способа снижения токсичности рифампицина при полном сохранении его противотуберкулезной активности путем комплексообразования рифампицина с анионным полиэлектролитом.
Поставленная задача и результат достигаются способом получения полимерных комплексов рифампицина с пониженной токсичностью и высокой противотуберкулезной активностью путем комплексообразования рифампицина с анионным полиэлектролитом в его водном растворе, при этом для получения полимерных комплексов рифампицина в качестве анионного полиэлектролита используют поли-2-акриламидо-2-метилпропансульфокислоту (поли-ААМПСК) с молекулярной массой (ММ) 20000-40000, а комплексообразование проводят при массовом соотношении полимер: антибиотик, равном 1,9-4,0, при этом полученный полимерный комплекс рифампицина (III) имеет структурную формулу:
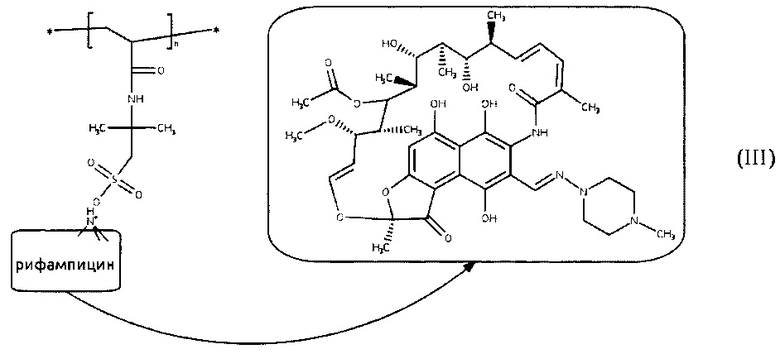
Для большего понимания сущности предлагаемого способа приводим конкретные примеры его выполнения.
Пример 1. Синтез анионного полиэлектролита - поли-ААМПСК.
В стеклянную ампулу сначала загружают 0,06 г инициатора (азо-бис-изобутиронитрила), а затем раствор, содержащий 6 г мономерной ААМПСК в 30 мл этанола. Через ампулу в течение 10 мин пропускают аргон. Ампулу запаивают и помещают в термостат, в котором поддерживается температура (70±0,1)°С. Через 48 ч ампулу охлаждают, вскрывают и вязкий полимеризат по каплям выливают в 400 мл серного эфира. Высадившийся полимер собирают на фильтре Шотта, сушат в вакууме и подвергают диализу против воды в течение 24 ч. После диализа водный раствор полимера лиофилизуют. Получают 3,98 г (66,3%) поли-ААМПСК.
Найдено: %S=15,23; 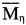 (Средневязкостная ММ) равна 29000.
(Средневязкостная ММ) равна 29000.
Вычислено: %S=15,46.
Пример 2. Получение полимерного комплекса рифампицина III-1.
0,4 г поли-ААМПСК, полученной по примеру 1, растворяют в 20 мл дистиллированной воды, затем при перемешивании, при комнатной температуре добавляют 0,215 г рифампицина (массовое соотношение полимер: антибиотик равно 1,9: 1). Реакционный раствор перемешивают в течение 3-х часов, затем фильтруют через воронку с бумажным фильтром. Фильтрат подвергают лиофильной сушке. Выход: 0,385 г (62,6%). Содержание рифампицина в полученном комплексе III-1, определенное методом УФ-спектроскопии, составляет 35,2 мас %. Биологические характеристики полимерного комплекса III -1 приведены в таблице.
Пример 3. В условиях примера 2 из 0,2 г поли-ААМПСК и 0,086 г рифампицина (массовое соотношение полимер: антибиотик равно 2,3: 1) получают 0,215 г (75,3%) полимерного комплекса рифампицина III-2, содержащего 30,7 мас. % антибиотика. Биологические характеристики полимерного комплекса III-2 приведены в таблице.
Пример 4. В условиях примера 2 из 0,3 г поли-ААМПСК и 0,075 г рифампицина (массовое соотношение полимер: антибиотик равно 4,0:1) получают 0,247 г (65,9%) полимерного комплекса III-3, содержащего 16,9 мас % антибиотика. Биологические характеристики комплекса III-3 приведены в таблице.
Полученные полимерные комплексы рифампицина имеют структурную формулу:
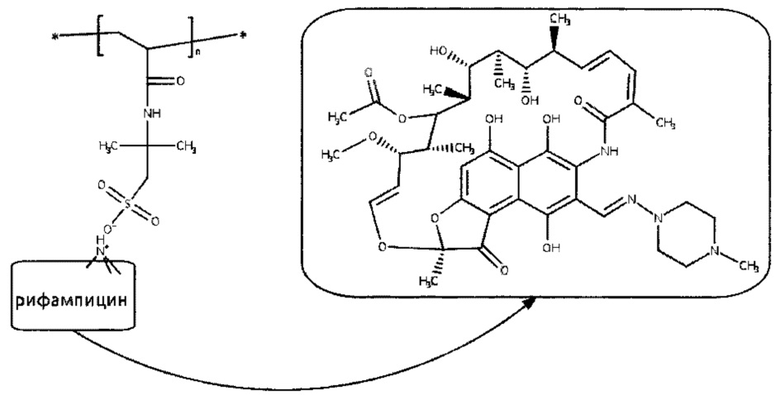
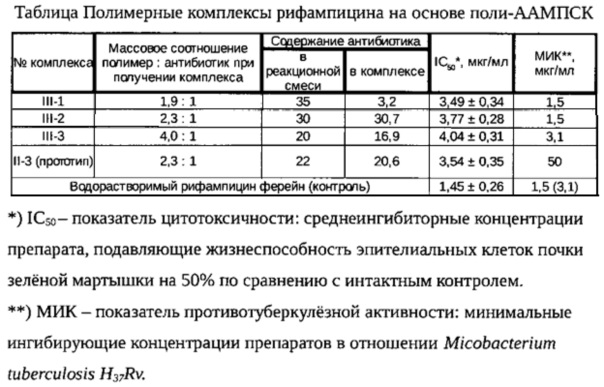
Как следует из данных таблицы, заявляемые полимерные комплексы рифампицина в 2,4-2,8 раза менее токсичны, чем немодифицированный полимером рифампицин. По показателям токсичности они сопоставимы с известными комплексами рифампицина, например с комплексом II-3.
Однако по значениям минимальных ингибирующих концентраций заявляемые полимерные комплексы в 16,6-33,3 раза более активны в отношении микобактерий туберкулеза человеческого типа, чем известные полимерные комплексы II-1 - II-3. По уровню противотуберкулезной активности заявляемые полимерные комплексы рифампицина сопоставимы с активностью исходного антибиотика.
Наблюдаемое явление повышения антимикробной активности при использовании в качестве носителя в комплексе поли-ААМПСК с высокой плотностью заряженных -SO3- групп на макромолекуле обусловлено эффектом высоких локальных концентраций, выражающимся в присоединении к одной макромолекуле значительного числа молекул низкомолекулярного ЛВ. Это благоприятствует интенсивному переходу молекул рифампицина с макромолекул полимера-носителя в микробную клетку. Напротив, в случае сополимера ВП с 3-бутеновой кислотой (прототип), где задержанные -СОО- группы разделены микроблоками из звеньев ВП и локальная плотность их понижена, такой переход происходит менее интенсивно.
Заявляемый интервал ММ полимерного носителя (20000 - 40000) обусловлен тем, что синтетические водорастворимые карбоцепные полимеры с ММ>40000 не выводятся из организма путем почечной фильтрации и накапливаются в клетках ретикулоэндотелиальной системы, оказывая неблагоприятное воздействие на живой организм [Е.Ф. Панарин, Н.А. Лавров, М.В. Соловский, Л.И. Шальнова. Полимеры-носители биологически активных веществ. СПб.: Профессия, 2014, 299 с.]. С другой стороны, эти полимеры с ММ<20000 быстро элиминируется из организма, не успев обеспечить в полной мере биологическое действие связанного ЛВ.
Заявляемый интервал массового соотношения полимер: антибиотик (1,9-4,0:1) связан с тем, что увеличение этого значения > 4,0: 1 может привести к снижению антимикробной активности полимерного комплекса рифампицина. Уменьшение этого показателя <1,9:1 может отразиться на увеличении его цитотоксичности.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ МОДИФИКАЦИИ ГЕНТАМИЦИНА СОПОЛИМЕРОМ ВИНИЛПИРРОЛИДОНА С ДИАЦЕТАЛЕМ АКРОЛЕИНА | 2017 |
|
RU2659032C1 |
| ВОДОРАСТВОРИМЫЕ ПОЛИМЕРНЫЕ КОМПЛЕКСЫ АРБИДОЛА | 2008 |
|
RU2394618C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ПОЛИМЕРНЫХ КОМПЛЕКСОВ | 2024 |
|
RU2839245C1 |
| ПОЛИДИАЛЛИЛАММОНИЕВЫЕ СОЛИ В КАЧЕСТВЕ МИКОБАКТЕРИЦИДНОГО И ТУБЕРКУЛОЦИДНОГО ДЕЗИНФИЦИРУЮЩЕГО СРЕДСТВА | 2009 |
|
RU2415679C1 |
| ВОДОРАСТВОРИМЫЕ ПОЛИМЕРНЫЕ КОМПЛЕКСЫ АНТИБИОТИКОВ-АМИНОГЛИКОЗИДОВ | 2006 |
|
RU2335510C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ И ПРЕДУПРЕЖДЕНИЯ ВОЗНИКНОВЕНИЯ ОСЛОЖНЕНИЙ, СВЯЗАННЫХ С ХИМИОТЕРАПИЕЙ И РЕНТГЕНОТЕРАПИЕЙ, А ТАКЖЕ СОСТОЯНИЙ, СВЯЗАННЫХ С ПОВЫШЕННОЙ ПРОНИЦАЕМОСТЬЮ КИШКИ | 2018 |
|
RU2692469C1 |
| ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОТУБЕРКУЛЕЗНОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2469711C1 |
| ПРОТИВОТУБЕРКУЛЕЗНОЕ СРЕДСТВО В ВИДЕ РАСТВОРА ДЛЯ ИНЪЕКЦИИ | 2007 |
|
RU2358742C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО КОМПЛЕКСА | 2010 |
|
RU2435611C1 |
| БИОЛОГИЧЕСКИ АКТИВНАЯ ПОЛИМЕРНАЯ МЕДИЦИНСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ) | 2010 |
|
RU2447902C2 |
Изобретение относится к медицине и заключается в способе получения полимерных комплексов рифампицина с пониженной токсичностью и высокой противотуберкулезной активностью путем комплексообразования рифампицина с анионным полиэлектролитом в его водном растворе. В качестве анионного полиэлектролита используют поли-2-акриламидо-2-метилпропансульфокислоту с молекулярной массой 20000-40000, комплексообразование проводят при массовом соотношении полимер : антибиотик, равном 1,9-4,0. Технический результат – снижение токсичности рифампицина при полном сохранении высокого уровня противотуберкулезной активности. 1 табл., 4 пр.
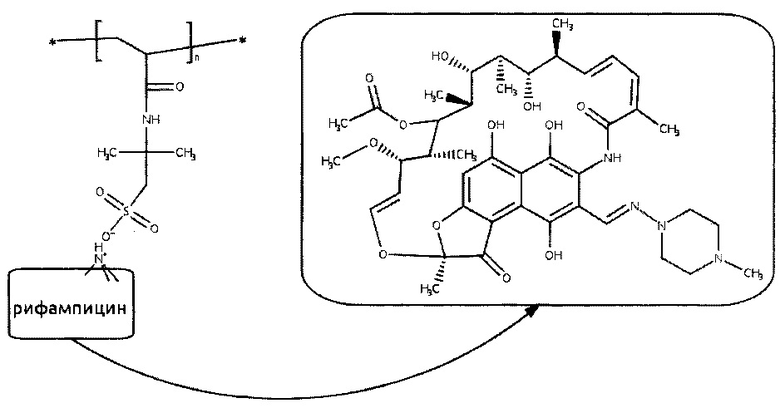
Способ получения полимерных комплексов рифампицина с пониженной токсичностью и высокой противотуберкулезной активностью путем комплексообразования рифампицина с анионным полиэлектролитом в его водном растворе, отличающийся тем, что для получения полимерных комплексов рифампицина в качестве анионного полиэлектролита используют поли-2-акриламидо-2-метилпропансульфокислоту с молекулярной массой 20000-40000, а комплексообразование проводят при массовом соотношении полимер : антибиотик, равном 1,9-4,0, при этом полученный полимерный комплекс рифампицина имеет структурную формулу:
| М.С | |||
| БОРИСЕНКО и др., Синтез сополимера N-винил-2-пирролидона с 3-бутеновой кислотой - носителей лекарственных веществ, Журнал прикладной химии, 2015, Т.88, вып | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Выдвижная подножка для трамваев | 1924 |
|
SU1579A1 |
| КОСМЕТИЧЕСКАЯ И/ИЛИ ДЕРМАТОЛОГИЧЕСКАЯ КОМПОЗИЦИЯ С КИСЛЫМ ЗНАЧЕНИЕМ РH, СПОСОБ НЕТЕРАПЕВТИЧЕСКОЙ ОБРАБОТКИ КОЖИ, СПОСОБ НЕТЕРАПЕВТИЧЕСКОЙ ДЕПИГМЕНТАЦИИ КОЖИ И ПРИМЕНЕНИЕ СШИТОЙ И НЕЙТРАЛИЗОВАННОЙ, ПО КРАЙНЕЙ МЕРЕ, НА 90% ПОЛИ(2-АКРИЛАМИДО-2-МЕТИЛПРОПАНСУЛЬФОКИСЛОТЫ) | 1997 |
|
RU2167642C2 |
| WO 2004041284 A1, 21.05.2004 | |||
| US 20110020252 A1, 27.01.2011. | |||
Авторы
Даты
2017-06-29—Публикация
2016-08-04—Подача