Изобретение относится к области химии полимеров, в частности катализа получения алифатических сложных полиэфиров способом поликонденсации α-замещенных оксикислот, преимущественно молочной кислоты. Получаемые полимеры обладают способностью к полному биоразложению в живом организме или естественных природных условиях и могут быть использованы для создания изделий широкого ассортимента как медицинского, так и бытового применения.
Известно, что наиболее распространенным и промышленно освоенным способом получения алифатических сложных полиэфиров является полимеризация циклических сложных эфиров - моно- или дилактонов, осуществляемая в расплаве мономеров и катализируемая преимущественно оловосодержащими соединениями (J. Macromol. Sci. part C, Polym. Rev. 45, 325-349, 2005). Однако существует и альтернативный способ получения тех же полиэфиров методом поликонденсации α-замещенных оксикислот, также катализируемой аналогичными оловосодержащими соединениями (Biotechnology Advancts 30, 2012, 321-328). Сопоставление этих двух методов показывает, что оба они хотя и приводят к совершенно идентичным по строению полимерам (при условии одинакового исходного сырья), тем не менее имеют свои отличительные преимущества и недостатки.
Полимеризационный способ характеризуется возможностью более легкого достижения высоких молекулярных масс, необходимых для реализации оптимальных физико-механических свойств конечных полимеров, однако требует для этого промежуточной (дополнительной) стадии синтеза лактонов и высокой степени их очистки.
Поликонденсационный способ позволяет получать полиэфиры прямой конденсацией α-замещенных оксикислот, минуя стадию синтеза мономера, однако для достижения требуемых молекулярных масс необходимо применение достаточно активных катализаторов и вакуума с целью тщательного удаления продуктов конденсации. Оба способа основаны на идентичном исходном, возобновляемом, природном сырье (преимущественно молочной кислоте) и катализируются одними и теми же катализаторами.
Тенденция, наметившаяся в научной и патентной литературе, однозначно показывает, что, несмотря на промышленную реализацию полимеризационного способа в ряде стран (США, Япония, Великобритания, Германия, Китай), предпочтение все больше оказывается поликонденсационному способу, который хотя и не освоен в промышленном масштабе, но при соответствующей технической доработке, несомненно, будет вытеснять полимеризационный способ, т.к. обладает более высокой экономической эффективностью.
Оба обсуждаемых способа имеют один и тот же недостаток, заключающийся в необходимости удаления (или, по крайней мере, понижения концентрации) каталитических остатков в готовом полимере, которые заметно ухудшают его эксплуатационные свойства (катализ обратной реакции разложения полимера, токсичность тяжелых металлов, содержащихся в катализаторе). Указанное требование особенно актуально при использовании биоразлагаемых полиэфиров в медицине, которая требует высокой чистоты конечных полимеров. Известный прямой способ очистки растворением полимера и последующим его осаждением хотя и приводит к приемлемым результатам, однако характеризуется большими отходами и значительным удорожанием продукта.
Две альтернативы известному способу очистки готовых полиэфиров могут быть выявлены при анализе литературы. Первый основан на применении гетерогенных катализаторов полимеризации или поликонденсации, которые характеризуются отсутствием растворения (или уноса) в течение синтеза и возможностью полного (количественного) отделения их по окончании процесса. Второй заключается в повышении активности гомогенных катализаторов, которая позволяет существенно снизить их концентрацию при синтезе полимера и получить приемлемые для данного применения значения остаточных концентраций без дополнительной очистки. Обе альтернативы равноценны и интенсивно разрабатываются.
Из наиболее применяемых гетерогенных катализаторов можно выделить металлсодержащие: металлическое олово, его окислы, окислы других металлов, в частности титана, цинка, сурьмы и т.д. Все указанные металлсодержащие катализаторы характеризуются достаточно высокой каталитической активностью, которая достигается преимущественно за счет применения их в высокодисперсном состоянии, что, однако, создает известные трудности при их выделении из высоковязких конечных полимерных расплавов (в том числе и по причине образования прививок между органической и неорганической составляющими).
В качестве других гетерогенных катализаторов весьма перспективно использование кислых, не содержащих металлов катализаторов, в частности сернокислотных, в которых серная кислота нанесена на подходящий органический носитель, отделяемый от полимера вместе с отработанным катализатором по окончании поликонденсации. Иммобилизованные сернокислотные катализаторы обладают высокой каталитической активностью и позволяют получать полимеры с высокой молекулярной массой, характеризуются малой окрашивающей способностью по сравнению с металлсодержащими, однако трудности по выделению полимера, свободного от каталитических остатков, содержащихся на носителе, при этом сохраняются.
Известно также комбинирование сульфониевых и оловосодержащих компонент, например, в виде сульфониевых солей олова, которое в условиях полимеризации активирует катализатор в целом. В условиях конденсации (и при наличии воды в системе) указанные соли диссоциируют на отдельные (и, возможно, индивидуальные) компоненты, самостоятельно ведущие процесс, что приводит к отсутствию активирующего действия.
Повышение активности гомогенных оловосодержащих катализаторов осуществляется преимущественно как за счет выбора их оптимального для данного типа реакции строения (валентность металла, строение органического радикала, связанного с ним, стерические затруднения, создаваемые около металла и т.д.), так и за счет подбора соответствующего лигандного окружения вокруг металла (например, с помощью азотсодержащих оснований).
Известны приемы конструирования каталитических систем поликонденсации на основе олова, добавлением других различных катионов (например, в синтезе ароматических полиэфиров на основе терефталевой кислоты).
В качестве примеров можно привести следующие патенты аналоги.
Индивидуальное металлическое олово в качестве катализатора получения ароматического полиэфира на основе терефталевой кислоты предложено достаточно давно в качестве замены классической p-толуолсульфокислоты (например, пат. США №3055867 от 1962 г.). Такая замена позволила ликвидировать окраску полиэфира, резко снизить его кислотное число (с 10 до 2-3) и необходимую концентрацию катализатора (вплоть до 0,001%), а также гидролитическую стабильность полимера. Этерификация проводилась в интервале температур 220-240°C, в течение 4-5 часов, по достижении кислотного числа 2,5.
Дальнейшим развитием "металлического" катализа явился переход от монометалла (олово) к полиметаллическим системам, содержащим наряду с оловом в разных сочетаниях сурьму, медь, цинк, кадмий, висмут, свинец и даже ртуть. Наиболее удобным способом комбинирования металлов явилось применение в качестве катализаторов металлических сплавов, в которых основным компонентом фигурировало все то же олово.
Известно, что применение сплавов вместо чистого металла впервые стало применяться при получении полиэтилентерефталата способом сополиконденсации терефталевой кислоты с диэтиленгликолем. В качестве примеров можно привести следующие работы.
В патенте СССР №343451 для катализа синтеза полиэтилентерефталата предложен многокомпонентный сплав, содержащий, помимо олова, сурьму, свинец и кадмий (который в другом варианте заменялся на добавку марганца). Предложенный катализатор позволял проводить одновременно переэтерификацию эфира терефталевой кислоты (взятого в качестве исходного продукта) и получение собственно полиэтилентерефталата. Температурный интервал реакции 250-275°C, при котором наиболее вероятным состоянием катализатора является жидкий расплав.
В патенте СССР №346877 предложен модифицированный, также многокомпонентный катализатор синтеза полиэтилентерефталата. В качестве модифицирующих добавок предложены щелочные или щелочноземельные металлы, вводимые в виде предварительно синтезированных гликолятных производных. Модификация катализатора позволила существенно улучшить качество полиэфира. В обоих приведенных примерах остатки катализатора растворялись в полимере и в дальнейшем из него не извлекались, что составляло по современным меркам не менее 300-500 ppm.
В пат. США №3651016 предложен 3-компонентный катализатор, состоящий из 35-50% сурьмы, 35-50% свинца и 5-30% цинка и позволяющий получать полиэтилентерефталат из диметилового эфира терефталевой кислоты и этиленгликоля в две стадии: первой при 250°C и полной отгонке метанола за 2,5 часа, второй при 260°C и остаточном давлении 0,5 торр за 3 часа. Предложенный катализатор не нарушал термостабильность полимера и не вызывал его распада при температуре 280°C в течение как минимум 2 часов.
Приведенные примеры применения полиметаллических катализаторов в синтезе полиэтилентерефталата несомненно доказывают их преимущества перед монометаллами, и их перечень можно продолжить, однако аналогичных примеров на получение алифатических сложных полиэфиров и, в частности, полимолочной кислоты из молочной кислоты в патентной литературе нами не обнаружено.
Следует также отметить, что полиэтилентерефталат хотя и является полиэфиром, однако вследствие высокой кристалличности полимера удовлетворительной биоразлагаемостью ни в естественных природных условиях, ни тем более в живом организме не обладает и применяется преимущественно в качестве упаковок для пищевых продуктов (бутылки, изделия одноразового использования). Тем не менее, опыт, накопленный в синтезе этого полимера, вполне может использоваться для получения полиэфиров алифатического типа.
Наиболее употребительными катализаторами полимеризации лактонов и поликонденсации оксикислот был (до недавнего времени) дигидрат двуххлористого олова, который впоследствии был вытеснен 2-этилгексоатом также двухвалентного олова. Двуххлористое олово характеризовалось достаточно высокой активностью в обоих типах процессов, однако содержащаяся в нем кристаллизационная вода создавала трудности как в катализе, так и при хранении продукта вследствие возможности его гидролиза и появления хлористого водорода, вызывающего неустойчивость процесса и коррозию аппаратуры.
2-этилгексоат олова в значительной мере ликвидировал недостатки двуххлористого олова, стабилизировав катализ, однако как соль слабой кислоты и слабого основания также обладает неустойчивостью к гидролизу.
Первое промышленное применение 2-этилгексоата (октоата) олова в качестве катализатора зафиксировано в 1994 г. (Пат. США №5357035). Далее это соединение стало преобладающим в катализе получения полилактида и полимолочной кислоты (J. Polym. Environ, 2002, 9, 63-84. J. Macromol. Sci. part C, Polym. Rev. 45, 325-349, 2005). Синтез высокомолекулярной полимолочной кислоты прямой ее катализированной конденсацией впервые представлен в Macrom. Chem. Phys. 2002, 203, 2245-2250.
В качестве примеров, в которых предложены другие способы, позволяющие активировать соединения олова, и в частности 2-этилгексоат, можно привести следующие. В патенте США №2013197186 A1 заявлен процесс получения полимолочной кислоты и преполимера на ее основе с помощью катализатора, комбинированного из диацетата 2-валентного олова, взятого в количестве 120 ppm (в расчете на атом олова и 100%-ную молочную кислоту), а также метансульфоновой кислоты, взятой в количестве 1100 ppm (в расчете на атом серы). Процесс получения форполимера проводят при 155°C, давлении 700 Ра, в течение 3,5 час. Получают форполимер с молекулярной массой 14700, с которым далее проводят доводочные операции при той же концентрации катализатора. Конечное содержание олова в готовом полимере не указывается, но оно, несомненно, превышает первоначальное (120 ppm), вследствие удаления воды из кислоты и превращения ее в полимер (ориентировочное превышение составляет не менее 20-25%). Как видно из данного патента, все операции проводятся при однократном введении катализатора, без предварительного получения его концентрата в преполимере с дальнейшим разбавлением в основной операции.
В более раннем патенте США №5310865 конденсация молочной кислоты производилась с использованием метода азеотропной отгонки воды (компоненты азеотропа мета-ксилол, анизол, орто-дихлорбензол и т.д.) в присутствии трифторметансульфоната 2-валентного олова (570 ppm в расчете на металл) или металлического олова (2700-13000 ppm) с четким разделением процесса на две стадии. Первая - 2 час, 138°C, вторая - 40 час, 138°C (с применением вакуума температуру можно снижать до 130°C). Содержание олова в конечном полимере не сообщается, но можно полагать, что в случае трифторметансульфоната оно составляет 570+20% ppm, а с применением в качестве катализатора металлического олова оно может достигать не менее 500-1000 ppm вследствие частичного растворения металла в молочной кислоте на первой стадии конденсации. Достоинство патента состоит в применении высокоактивного катализатора, который позволил снизить температуру конденсации до 130°C, при которой рацемизация L-молочной кислоты практически отсутствует, однако содержание каталитических остатков в полимере остается достаточно высоким.
Значительного снижения концентрации оловосодержащего катализатора при полимеризации лактида удалось реализовать при введении соответствующего (например, азотсодержащего) лигандного окружения олова, а с использованием биологически активных азотсодержащих соединений получать катализатор конденсации молочной кислоты, вообще не содержащий металл. Так, например, заявлен катализатор полимеризации лактида - металлоорганический комплекс Sn-октоата с различными замещенными и незамещенными карбодиимидами. Отличительной особенностью примененного катализатора - высокая активность и возможность полимеризации при очень малых его дозировках (5-15 ppm), что в итоге позволяет получать высокие молекулярные массы полимера в диапазоне 100000-1000000 (EP 2395009 A2 - 2011-12-14).
Заявлен также биоразлагаемый полимер для медицинского применения, содержащий креатинин (N-метилированное производное гуанидина и гликолевой кислоты) в количестве 100-10000 ppm и получаемый конденсацией молочной кислоты с его участием. Катализатор не содержит олова, однако, по-видимому, может иметь только узко специфическое применение.
В последнее время разрабатываются высокоактивные комплексные катализаторы полимеризации лактида на основе редкоземельных элементов, содержащие в качестве активирующей компоненты биядерные амиды. Указанная комбинация (предложенная в работе Synthesis and Reactivity in Inorganic, Mttal-Organic and Nano-Metal Chemistry, 44, 611-615, 2014) позволила проводить растворную полимеризацию L-лактида в толуоле при 50°C. Несмотря на наличие 2 каталитических центров в каталитическом комплексе, молекулярно-массовое распределение получаемых полимеров оказалось достаточно узким (коэффициент полидисперсности в пределах 1,43-1,48).
Аналогичные данные получены в работе J. Organomet. Chem. 758, (2014), 65-72, при использовании в качестве катализаторов полимеризации рацемического лактида органолантанидных комплексов, содержащих в качестве лиганд совместное азот-кислородное окружение. Полимеризация в толуоле при температуре 20°C приводила к чередующемуся гетеротактическому полимеру с молекулярно-массовым распределением 1,21-1,38.
Более ранние работы китайских авторов, также связанные с применением редкоземельных элементов в комплексных каталитических системах со сложным азотсодержащим лигандным окружением, также свидетельствовали о возможности повышения активности катализатора и его стереоизбирательности при полимеризации рацемической смеси лактида (Polyhedron, 27, (2008), 1665-1672. J, Organomet, Chem, 694, (2009), 691-696. Inorg. Chem. Communication, 13, (2010), 445-448.
В работе J. Organomet. Chem. 754, (2014), 51-58 предложена серия биядерных азотсодержащих алюминиевых комплексов, позволяющая получать в растворе из рацемической смеси лактида гетеротактический (чередующийся) полимер с узким молекулярно-массовым распределением (1,13-1,25) при температуре 70°C, что свидетельствует о высокой активности каталитического комплекса также в случае "легкого" металла, его образующего.
Полимеризация ε-капролактона в растворе исследована в работе J. Organom. Chem. 738, (2013), 1-9, которая продемонстрировала отказ от оловосодержащих катализаторов и в которой получено, что высокоактивные катализаторы можно получать на основе "легких" металлов - магния или цинка с помощью специально подобранного комбинированного азот-кислородного лигандного окружения. Всего за несколько минут в толуоле при температуре 25°C получены образцы поликапролактона с высоким выходом и чрезвычайно узким молекулярно-массовым распределением (1,06-1,25).
Подводя итог вышеприведенным ссылкам, можно утверждать, что совершенствование каталитических систем идет преимущественно в области катализа полимеризации лактонов и в гораздо меньшей степени для процессов конденсации оксикислот (молочной). Такое положение, по-видимому, обусловлено тем обстоятельством, что в последнем случае необходимы водоустойчивые катализаторы, не подверженные гидролизу, что в условиях непрерывно выделяющейся в ходе конденсации воды создает дополнительные трудности их конструирования. В связи с этим тезис о полной взаимозаменяемости катализаторов полимеризации и поликонденсации может применяться с известными ограничениями. Особенно это касается систем повышенной сложности, содержащих "весомое" лигандное окружение, обладающее относительно высокой основностью (амины, гуанидины и их производные).
В качестве более эффективного, чем 2-этилгексоат, двухвалентного олова, катализатора поликонденсации оксикислот, недавно предложена молочнокислая соль Sn (2+), которая более устойчива к гидролизу и является начальным звеном, как в поликонденсации, так и полимеризации, вследствие чего отпадает стадия предварительного инициирования этих процессов (EP WO 2012103170 (A2) от 2012.08.02). Данный патент принят в качестве прототипа, согласно которому получение 2-гидроксикарбоксилата Sn (2+) включает следующие операции:
1. Получение водного раствора соли Sn 2+.
2. Добавление к полученному раствору 2-гидроксикарбоксильной кислоты, или ее соли, или их раствора.
3. Введение основания и регулирование pH раствора для осаждения 2-гидроксикарбоксилата Sn 2+.
4. Фильтрация осадка.
5. Сушка осадка.
Катализ реакции конденсации проводится в присутствии 0,001-5,0 вес. % катализатора, предпочтительно 0,001-2,0 вес. %, что в ppm составляет 10-50000 или 10-10000 соответственно. Режим конденсации 60-120°C, время конденсации 1-12 час. О достигаемых при этом молекулярных массах полимера не сообщается, однако, учитывая существующий уровень техники, можно утверждать, что они в указанных условиях реакции не превышают 1000-2000.
Недостатки прототипа заключаются в многостадийности способа синтеза катализатора, технологических трудностях отдельных стадий, наличии сливов и отходов производства, а также в неизбежных потерях катализатора, обусловленных стадиями осаждения и отмывки (стадии 3 и 4 прототипа).
Задача предлагаемого изобретения состоит в повышении каталитической активности катализатора, в устранении многостадийности процесса его синтеза и обеспечении возможности хранения катализатора в течение длительного времени.
Для этого предложен способ получения катализатора синтеза биоразлагаемых алифатических сложных полиэфиров на основе α-замещенных гидроксилсодержащих карбоновых кислот и оловосодержащих соединений, взаимодействие которых осуществляют в водных растворах, при этом взаимодействие компонент проводят в концентрированном водном растворе молочной кислоты при температуре 100-180°С, при исходной концентрации оловосодержащих солей 5,0-0,01 вес. %, причем оловосодержащие соли выбирают из группы, в которой анион обладает летучестью в выбранном температурном интервале, а реакцию формирования катализатора проводят в течение 1-5 часов с непрерывным удалением воды. Кроме того, в оловосодержащих солях 60-80% составляют катионы металлов, выбранные из ряда: Mg (4-13%), Zn (25-35%), Al (5-11%), Sb (20-25%), Mn (1-4%), Co (2%), Cu (1%), Mo (2%), Ni (2%), Bi (50-4%), B (1-2%).
Основные отличия предлагаемого изобретения от прототипа состоят в следующем.
1. Получение катализатора конденсации проводится в одну стадию с использованием солей 2-валентного олова, растворимых в концентрированном водном растворе молочной кислоты (90%-ной).
2. Получаемый катализатор представляет собой оловосодержащий олигомер молочной кислоты и при проведении основной реакции конденсации с его участием не требует растворителя для гомогенного распределения в реакционной среде. Гомогенное распределение катализатора осуществляется за счет достаточно длинных полимерных "хвостов" каталитического олигомера.
3. Удаление постороннего аниона, связанного с оловом, в соответствии с прототипом осуществляется осаждением дилактата в водной среде с последующей индивидуализацией его с помощью фильтрации. По предлагаемому техническому решению для получения катализатора выбираются соли олова, имеющие летучий (при температуре конденсации) анион, что предоставляет возможность удалять его вместе с продуктами конденсации, не выделяя этот процесс в отдельную стадию (анионы галоидного, карбонатного, гидроксильного, ацетатного типов).
4. Формирование катализатора в соответствии с предлагаемым способом проводится только при высоких концентрациях олова (1000-50000 ppm, концентрат катализатора), что позволяет, при соответствующем последующем его разведении, для проведения основной реакции получать катализатор в активированном состоянии.
5. Активация катализатора достигается также заменой части олова на другие катионы, не снижающие его активность в конденсации молочной кислоты и выполняющих в качестве микроэлементов полезную функцию в живом организме при введении в него биоразлагаемого полимера, рассасывающегося далее в нем с выделением каталитических остатков.
Повышение каталитической активности основано на следующих допущениях и достигается с помощью следующих приемов.
1. Известно, что при полимеризации лактида под действием оловосодержащих катализаторов константа скорости процесса существенно возрастает при переходе от активных центров, представляющих собой ионные пары к свободным ионам. Такому переходу способствует как создание соответствующего лигандного окружения вокруг активного металлического центра, так и понижение концентрации самого катализатора. Известно также, что и полимеризация лактида, и поликонденсация молочной кислоты являются типично ионными процессами, в связи с чем уместно допустить аналогию в поведении активных центров в обоих этих процессах.
Итак, мы допускаем, что при разбавлении концентрированного катализатора в процессе конденсации молочной кислоты его активность может не только падать пропорционально степени разведения, но даже в какой-то степени возрастать. Такое поведение будет обусловлено переходом ассоциатов активных центров (преимущественное состояние металлических солей при концентрациях 30-40 тыс. ppm) к индивидуальным ионным парам, ионным тройникам и далее к свободным ионам. Таким образом, разбавление катализаторов перед их основным применением, в том числе известных и наиболее часто применяемых (октоат олова), является одним из приемов, принятых в данном техническом решении.
2. Известно, что разбавление катализатора может осуществляться различным образом. Наиболее простой и наиболее часто применяемый способ - введение сразу малых количеств не подвергавшегося никакой обработке катализатора (порядка 10-15 ppm или 0,001-0,0015%) в виде раствора в подходящем растворителе. Такой прием, однако, не приводит к удовлетворительным результатам, т.к. сопряжен с потерей (или дезактивацией) части катализатора, а также представляет известные технологические трудности (наличие растворителя и необходимость его удаления после введения катализатора).
Более предпочтителен вариант, который состоит в предварительном получении олигомерного форполимера при достаточно высокой концентрации металлсодержащего катализатора (1000-10000 ppm по металлу) с последующим синтезом полимолочной кислоты под действием полученного каталитического концентрата. Необходимое для этого разбавление катализатора может быть выбрано в широких пределах (от 1 до 2-3 порядков в зависимости от выбранной первоначальной и конечной концентрации катализатора), т.к. каталитический центр защищен собственным полимером от внешнего воздействия.
Указанное разбавление может быть осуществлено одно-, 2-х или более кратно, а также непрерывно, в режиме подпитки процесса исходной кислотой. При непрерывной подаче кислоты в процессе конденсации влияние приема на степень диссоциации катализатора снижается, однако он становится полезным для расширения молекулярно-массового распределения получаемого полимера, вследствие появления низкомолекулярной фракции, оказывающей на него пластифицирующее действие. Указанный прием может быть также полезен при создании непрерывного поликонденсационного процесса.
3. Повышение степени диссоциации оловосодержащих каталитических систем может достигаться также добавлением других катионов, способных не только самостоятельно принимать участие в процессе катализа конденсации молочной кислоты, но и влиять на состояние основной оловосодержащей составляющей. Таким образом, создается поликатионная каталитическая система, в которой содержание олова понижено (по-крайней мере в 2-3 раза) по сравнению с монокатионной, содержащей только олово.
Известно, что электропроводность неводных систем, содержащих набор катионов, как правило, выше, чем для монокатионных, при их одинаковой концентрации. Это означает, что при прочих равных условиях суммарная степень диссоциации поликатионной системы выше, чем монокатионной, а в приложении к процессу конденсации молочной кислоты то, что активность поликатионов в данном случае выше, чем монокатионов.
Из этого заключения вытекает ряд положений, важных для катализа процесса конденсации и последующей судьбы каталитических остатков в биоразлагаемом изделии, введенных в живой организм:
- по крайней мере часть нежелательного олова (а возможно и целиком) может быть изъята и заменена другими катионами, также обладающими активностью в конденсационных процессах, но проявляющими меньшую токсичность;
- более того, подбор "вспомогательных" катионов может производиться по принципу родственности, а возможно, даже и полезности живому организму. При достаточно малой общей концентрации каталитических остатков в биоразлагаемом изделии они могут усваиваться и играть роль активных микроэлементов, например в составе ферментов, выполняя те или иные важные процессы в организме. В качестве таких микроэлементов можно перечислить следующие: медь, кобальт, цинк, магний, никель, железо, молибден.
По данным Российского Центра судебно-медицинской экспертизы Минздрава РФ микроэлементная составляющая костной ткани (общее содержание 1,5-2,0%), определяемая методом эмиссионного спектрального анализа, может содержать как минимум 10 основных элементов с достаточно ощутимым содержанием (5-400 ppm): Mg, Fe, Si, Cu, Al, Pb, Mn, Ti, F. Исходя из этого и были выбраны значения и количества предлагаемых для реализации способа элементов;
- подбор анионов, вводимых в многокомпонентную каталитическую систему совместно с катионами, должен осуществляться по принципу легкости их удаляемости (летучести) при последующей конденсации молочной кислоты. Такими анионами могут быть гидроксилы (или окисные анионы), дающие при взаимодействии с молочной кислотой воду, карбонаты, освобождающиеся от аниона в виде CO2, галоиды, частично гидролизующиеся с выделением галоидных кислот, удаляемых из системы в виде азеотропа с водой и т.д. В любом случае в результате конденсации в конденсате должны оставаться только лактатные анионы.
Таким образом, суммируя вышесказанное, можно утверждать, что состав поликатионных каталитических систем поликонденсации молочной кислоты должен выбираться, как минимум, в соответствии с двумя вышеназванными принципами:
- активностью в конденсации, не уступающей олову, и полезностью живому организму при введениии биоразлагаемого изделия в живой организм, который "усваивает" не только полимерную составляющую, но и полиметаллические каталитические остатки, содержащиеся в ней. Только тогда биоразлагаемое изделие можно считать сбалансированным для медицинского применения без дополнительной очистки полимера, из которого оно сформировано. Для соблюдения максимальной анионной чистоты формируемой каталитической системы ее анионный состав должен содержать только легко удаляемые в процессе конденсации (и заменяемые на лактатные) анионы.
Способ осуществляется следующим образом. Сначала при комнатной температуре приготавливается каталитический концентрат растворением индивидуальной оловосодержащей соли или смеси оловосодержащих солей с другими солями, содержащими катионы Mg (4-13%), Zn (25-35%), Al (5-11%), Sb (20-25%), Mn (1-4%), Co (2%), Cu (1%), Mo (2%), Ni (2%), Bi (50-4%), B (1-2%) в молочной кислоте (водный раствор молочной кислоты концентрацией 90%). Получают гомогенный раствор с концентрацией индивидуальной оловосодержащей соли или смеси указанных солей в интервале 0,01-5,0%. Полученный раствор подвергают конденсации при температуре 120-160°C. Длительность конденсации выбирают в зависимости от желаемого физического состояния получаемого каталитического олигомера и удобства его дозировки для последующего проведения основной реакции конденсации. Оно может быть вязкотекучим при комнатной температуре или иметь температуру стеклования 30-40°C для последующей дозировки в твердом состоянии. Тест-поликонденсацию молочной кислоты с получением готового полимера проводят при разбавлении каталитического олигомера в 100-10000 раз.
Олигомерное или полимерное состояние катализатора повышает устойчивость его к атмосферному воздействию, что допускает возможность длительного хранения продукта без специальных защитных мер. Устойчивость зависит в первую очередь от физического состояния катализатора, концентрации металла (или металлов) и гидрофильности других каталитических компонент. Установлено, что жидкие, но достаточно вязкие оловосодержащие олигомеры сохраняют свою активность при хранении на воздухе в течение нескольких дней, а твердые олигомеры с температурой стеклования 40-45°C даже в течение года. Этим они выгодно отличаются от 2-этилоктоата олова, который при контакте с воздухом немедленно подвергается гидролизу.
Для оценки сравнительной активности катализаторов, предлагаемых в данном изобретении, принят метод сравнительной фиксации во времени выделяющейся в процессе конденсации молочной кислоты воды. Принятый метод основывается на следующих допущениях и осуществляется в следующих условиях:
1. Количество воды, выделяющейся в ходе реакции конденсации, зависит от скорости ее возникновения, которая в свою очередь определяется, при прочих равных условиях, активностью катализатора. Это основной оценочный параметр активности, принятый в данном техническом решении.
2. Скорость удаления воды определяется также условиями ее испарения. С целью стандартизации по этому параметру конденсация проводилась при одинаковой поверхности испарения, при одинаковой высоте налитой кислоты, без принудительного перемешивания, которое осуществлялось только за счет конвективных токов, возникающих при подогреве сосуда снизу и испарения воды с поверхности. Такие стандартные условия были осуществлены при проведении процесса в стеклянных стаканчиках емкостью 100 мл, поверхности испарения 8±0,2 см2 и высоте налитой кислоты 2±0,2 см (обычно это соответствовало 20±3 г 90%-ной молочной кислоты).
3. Принятая температура конденсации составляла 135±5°C и позволяла фиксировать достаточно большой разлет в активности предлагаемых катализаторов. Температурный интервал ±5°C обусловлен необходимостью взвешивания образцов, продолжительность которого не превышала 15 сек. Интервал фиксации веса составлял 5 мин, а стандартное время реакции, после которого производилось сравнение, составляло 60 мин. Следует подчеркнуть, что при выходе получаемых кинетических кривых на пологий участок даже небольшая разница в количествах удаляемой воды "откликалась" далее значительной разницей во времени необходимого для получения одинаковых молекулярных масс полимеров, получаемых под действием выбранных катализаторов.
4. Из теории органической химии известно, что равновесная реакция образования сложно-эфирной связи из спиртов и карбоновых кислот останавливается при наличии в системе 32% воды (Краткая химическая энциклопедия, Москва, 1967, т. 5, стр. 1027). Это позволило нам применять для реакции 90%-ную молочную кислоту, изначально содержащую 10% воды, которая не исключала начала и протекания реакции в этих условиях.
Таким образом, формирование оловосодержащих каталитических систем и оценка их относительной активности производится, в соответствии с данным изобретением, получением предварительного низкомолекулярного концентрата оловосодержащих (или комбинированных с другими катионами) солей, превращением его в олигомерный концентрат путем конденсации молочной кислоты с его участием и соответствующим разбавлением олигомерного концентрата для проведения основной реакции поликонденсации.
Полученные указанным методом катализаторы активны и в полимеризации лактонов. Так, в частности, лактид, полимеризуется в расплаве с высоким выходом полимера (92-95%) при концентрации по металлу (металлам) 100-200 ppm, а с применением ускорителей аминного типа резко снижается продолжительность индукционного периода и концентрация оловосодержащего катализатора (при прочих равных условиях) может быть снижена до 10-15 ppm. Это делает полученный полимер приемлемым для медицинских целей без каких-либо дополнительных очисток.
Техническая сущность предлагаемого изобретения иллюстрируется следующими примерами.
Пример 1
Пример иллюстрирует возможность повышения активности индивидуального октоата олова путем проведения предварительной олигомеризации молочной кислоты в присутствии его концентрированного раствора.
Приготовление солевого концентрата октоата олова в молочной кислоте.
0,333 г октоата олова растворяют в 3 мл гептана, получают раствор с концентрацией соли 12,5 вес. %. Добавляют 0,8265 г молочной кислоты (90%-ной концентрации). Выпадает желеобразный осадок, который гомогенизуют 1 час при комнатной температуре и количественно переносят в стеклянный стакан емкостью 100 мл. Туда же дополнительно порционно вводят 0,24 г октоата олова и молочную кислоту до суммарного ее содержания 23,05 г. При нагреве до 40°C и непрерывном перемешивании гептан удаляют и получают гомогенный раствор октоата олова в молочной кислоте с содержанием 24800 ppm по соли или 7286 ppm по олову.
Получение олигомерного каталитического концентрата
Раствор, сформированный на первой стадии, подвергают конденсации со свободным (без перемешивания) удалением воды в температурном интервале 135±5°C. Каждые 5 мин быстро (в течение не более 15 сек) фиксируют снижение веса в процентах от первоначальной загрузки молочной кислоты. По прошествии 1 часа убыль в весе на полученной кинетической кривой фиксируют как стандартную, принятую для сравнения с другими каталитическими системами. В данном примере общее время конденсации составило 2 часа, в результате чего получен совершенно прозрачный, бесцветный, твердый (при комнатной температуре) олигомер с содержанием по олову 11649 ppm.
Тест-поликонденсация молочной кислоты в присутствии малых количеств олигомерного катализатора
В стеклянный стакан емкостью 100 мл вносят 0, 035 г полученного каталитического олигомера и 20,3 г 90%-ной молочной кислоты, разбавление катализатора при этом составило 580 раз. Олигомер растворяют в кислоте при перемешивании и температуре 40°C, после чего проводят конденсацию молочной кислоты при температуре 135±5°C с фиксацией убыли веса во времени. Начальная концентрация по олову - 20 ppm. Сравнение убыли летучих продуктов за 1 час показало, что при концентрации 20 ppm она составила 34,63%, в то время как при концентрации 7286 ppm 27,45%, демонстрируя тем самым увеличенную активность высоко разбавленного катализатора по сравнению с концентрированным.
Проведена сравнительная оценка активности катализатора после хранения его в течение месяца без применения специальных защитных мер, которая показала полную идентичность с ранее синтезированным образцом.
Сравнительная конденсация молочной кислоты в отсутствие катализатора ведет к резкому замедлению процесса конденсации, что находит свое отражение в выделении образующихся летучих продуктов (за час не более 10%).
Аналогичным образом, если процесс предварительной конденсации с высокой концентрацией катализатора не проводится, исходное оловоорганическое соединение (в данном примере октоат олова), взятое сразу в достаточно малых количествах, показывает сниженную активность (22,8% убыли летучих при 17 ppm октоата олова) по сравнению с аналогичным количеством катализатора, прошедшего предварительное формирование в процессе конденсации.
Пример 2
Пример иллюстрирует возможность повышения активности октоата олова путем проведения предварительной олигомеризации молочной кислоты в присутствии его дозировок, обычно применяемых при полимеризации (по олову 100-200 ppm).
В стеклянный стакан емкостью 10 мл под защитой аргона дозируют 26,7 г 90%-ной молочной кислоты. Туда же вводят 0,0171 г октоата олова. Выпавший осадок усредняют перемешиванием и смесь подвергают конденсации при температуре 135±°C с фиксацией убыли веса содержимого через каждые 5 мин. Осадок быстро растворяется на 3-й минуте нагрева, и раствор становится совершенно гомогенным (начальное содержание олова 188 ppm). Через час удаление летучих составило 24,43% от первоначального веса молочной кислоты.
Конденсацию повторяют, используя полученный конденсат в качестве разбавленного катализатора (начальное содержание олова 17,9 ppm). Убыль летучих за час составила 30,95%, демонстрируя тем самым повышенную активность катализатора, несмотря на снижение его концентрации более чем на порядок.
Суммарные сравнительные результаты по октоату олова:

Пример 3
Пример иллюстрирует возможность повышения активности оловосодержащей соли (дигидрат двуххлористого олова) в конденсации молочной кислоты с помощью проведения предварительной конденсационной стадии при высокой начальной концентрации соли.
В стеклянный стакан емкостью 100 мл загружают 1,1194 г дигидрата двуххлористого олова и 28,6 г 90%-ной молочной кислоты. Соль полностью растворяют при комнатной температуре и получают гомогенный раствор с концентрацией 3,77 вес. % (37700 ppm). Конденсацию молочной кислоты проводят при температуре 135±5°C, отмечая убыль в весе, которая составила через час 25,5%, а через 2,5 часа 34,55%. Полученный конденсат разбавляют в 833 раза (0,0241 г на 20,08 г молочной кислоты) и конденсацию продолжают при той же температуре. Убыль воды за час при этом составила 28,28%, а за 3 час 49,0%, демонстрируя тем самым повышенную активность каталитического олигомера. Водная вытяжка из порошкообразного полимера не показала наличия хлора (проба на азотнокислое серебро).
Пример 4
Пример демонстрирует каталитическую активность многокомпонентного каталитического комплекса, содержащего, наряду с оловом, набор других катионов, который также формируется путем предварительной конденсации компонент в молочной кислоте.
Составляется смесь из навесок следующих компонент:
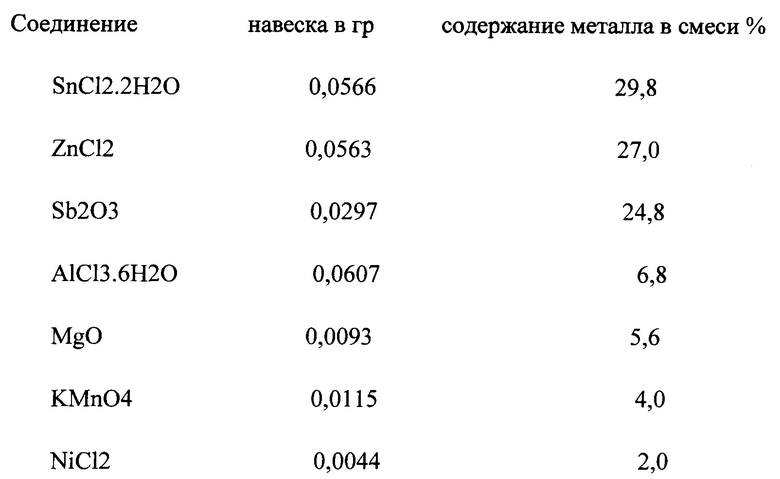
Составленную смесь растворяют в 18,6 г 90%-ной молочной кислоты, в результате чего получают 1,228%-ный солевой раствор (содержание по сумме индивидуальных металлов 5376 ppm). Конденсацию молочной кислоты проводят при температуре 135±5°C в течение 3 часов. Убыль в весе за час составила 22,2%, за 3 часа 45,0%.
Полученный твердый олигомер в количестве 0,12 г заливают 24 г молочной кислоты (начальная концентрация по олову 49,0 ppm) и диспергируют при комнатной температуре в течение часа, после чего проводят ее конденсацию при температуре 135±5°C. Убыль летучих за час составила 31,8%, т.е. больше, несмотря на 200-кратное разбавление первоначального каталитического олигомера.
Последовательную конденсацию продолжают с применением полимера (1,3711 г на 22,4 г молочной кислоты), полученного на предыдущей стадии. Начальная концентрация по сумме взятых поликатионов при этом составила 5,0 ppm. Убыль летучих за контрольный час показала 25,0%, т.е. больше, чем при высокой концентрации поликатионов (22,24%), и выше, чем при 17 ppm индивидуального олова (октоата, см. пример 2).
Пример 5
Данный пример демонстрирует поликатионную каталитическую систему поликонденсации молочной кислоты, комбинированную только из солей металлов, показавших высокую каталитическую активность в индивидуальном состоянии.
Составляют смесь из следующих солей, заливают ее 20,8 г молочной кислоты, содержимое растворяют и нагревают до 135±5°C. Через час конденсации унос летучих продуктов составил 32,04%.

Данная каталитическая система отличается от предыдущих тем, что высокая скорость конденсации осуществляется при высокой начальной концентрации солей, которая составляет на начало процесса 4800 ppm (по сумме металлов). Дальнейшее разбавление конденсата до уровня 18 ppm (в 266 раз) и проведение повторной поликонденсации в тех же условиях показывает 23,82% выноса летучих.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ПОЛИМЕРИЗАЦИИ ЛАКТОНОВ ИЛИ ПОЛИКОНДЕНСАЦИИ АЛЬФА-ОКСИКИСЛОТ | 2013 |
|
RU2525235C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОРАЗЛАГАЕМОГО КОМПОЗИТА НА ОСНОВЕ АЛИФАТИЧЕСКИХ СЛОЖНЫХ ПОЛИЭФИРОВ И ГИДРОКСИАПАТИТА | 2016 |
|
RU2664432C1 |
| СЛОЖНЫЙ ПОЛИЭФИР И КОНЪЮГАТ НА ЕГО ОСНОВЕ | 1994 |
|
RU2185393C2 |
| ИОННЫЙ КОНЪЮГАТ С ДЛИТЕЛЬНЫМ ПЕРИОДОМ ВЫСВОБОЖДЕНИЯ ПЕПТИДА, СПОСОБ СИНТЕЗИРОВАНИЯ ИОННОГО КОНЪЮГАТА, СПОСОБ СИНТЕЗИРОВАНИЯ МИКРОЧАСТИЦ | 1994 |
|
RU2146128C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИЛАКТИДОВ | 2019 |
|
RU2726362C1 |
| РЕАКТОР ПЕРИОДИЧЕСКОГО ДЕЙСТВИЯ И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ ДЛЯ ПОЛИМЕРИЗАЦИИ ЛАКТОНОВ | 2013 |
|
RU2570904C2 |
| ИОННЫЕ МОЛЕКУЛЯРНЫЕ КОНЬЮГАТЫ БИОДЕГРАДИРУЕМЫХ СЛОЖНЫХ ПОЛИЭФИРОВ И БИОАКТИВНЫХ ПОЛИПЕПТИДОВ | 2000 |
|
RU2237681C2 |
| СПОСОБ ПОЛУЧЕНИЯ СОПОЛИМЕРОВ СТИРОЛА С МОЛОЧНОЙ КИСЛОТОЙ | 2008 |
|
RU2404198C2 |
| СПОСОБ НЕПРЕРЫВНОГО ПОЛУЧЕНИЯ СЛОЖНЫХ ПОЛИЭФИРОВ | 2009 |
|
RU2510990C2 |
| СПОСОБ КАТАЛИТИЧЕСКОГО СИНТЕЗА ЛАКТИДА В ПРИСУТСТВИИ НЕОРГАНИЧЕСКИХ ДОБАВОК | 2018 |
|
RU2695998C1 |
Изобретение относится к получению катализатора синтеза биоразлагаемых алифатических сложных полиэфиров поликонденсацией α-замещенных оксикислот, преимущественно молочной кислоты. Полимеры обладают способностью к полному биоразложению в живом организме или естественных природных условиях и могут быть использованы для создания изделий широкого ассортимента как медицинского, так и бытового применения. Способ получения катализатора синтеза биоразлагаемых алифатических сложных полиэфиров на основе α-замещенных гидроксилсодержащих карбоновых кислот и оловосодержащих солей осуществляют взаимодействием компонентов в концентрированном водном растворе молочной кислоты в температурном интервале 100-180°C при исходной концентрации оловосодержащих солей 5,0-0,01 вес. %, реакцию формирования катализатора осуществляют в течение 1-5 часов с непрерывным удалением воды. Способ отличается тем, что оловосодержащие соли выбирают из группы, в которой анион обладает летучестью в выбранном температурном интервале, при этом в оловосодержащих солях 60-80% составляют катионы металлов, выбранные из ряда: Mg (4-13%), Zn (25-35%), Al (5-11%), Sb (20-25%), Mn (1-4%), Co (2%), Cu (1%), Мо (2%), Ni (2%), Bi (50-4%), B (1-2%). Технический результат – получение катализатора, обладающего повышенной каталитической активностью в способе получения биоразлагаемых алифатических сложных полиэфиров. 5 пр.
Способ получения катализатора синтеза биоразлагаемых алифатических сложных полиэфиров на основе α-замещенных гидроксилсодержащих карбоновых кислот и оловосодержащих солей, взаимодействие которых проводят в концентрированном водном растворе молочной кислоты в температурном интервале 100-180°C при исходной концентрации оловосодержащих солей 5,0-0,01 вес. %, а реакцию формирования катализатора осуществляют в течение 1-5 часов с непрерывным удалением воды, отличающийся тем, что оловосодержащие соли выбирают из группы, в которой анион обладает летучестью в выбранном температурном интервале, при этом в оловосодержащих солях 60-80% составляют катионы металлов, выбранные из ряда: Mg (4-13%), Zn (25-35%), Al (5-11%), Sb (20-25%), Mn (1-4%), Co (2%), Cu (1%), Мо (2%), Ni (2%), Bi (50-4%), B (1-2%).
| СПОСОБ ПОЛУЧЕНИЯ КАТАЛИЗАТОРА ПОЛИМЕРИЗАЦИИ ЛАКТОНОВ ИЛИ ПОЛИКОНДЕНСАЦИИ АЛЬФА-ОКСИКИСЛОТ | 2013 |
|
RU2525235C1 |
| US 5446123 A, 29.08.1995 | |||
| ЭЛЕКТРОННО-СЧЕТНЫЙ ДВУХКЛНАЛЬНЫЙ ЧАСТОТОМЕР | 0 |
|
SU261572A1 |
| WO 2012103170 A2, 02.08.2012 | |||
| СПОСОБ ПОЛУЧЕНИЯ БИОРАЗЛАГАЕМОГО СОПОЛИМЕРА | 2009 |
|
RU2426749C1 |
| US 2012245321 A1, 27.09.2012. | |||
Авторы
Даты
2017-07-10—Публикация
2015-12-21—Подача