Изобретение относится к области аналитической химии и может быть использовано для определения интегральной антиоксидантной активности (АОА) растительного сырья и продуктов питания на его основе.
Известен способ определения суммарной АОА в пищевых экстрактах и биологических образцах с использованием оптического сенсора, изготовленного на основе нафиона с иммобилизованным реагентом Cu(II) – неокупроин (Bener M., Özyürek M., Cüclü K., Apak R. Novel optical fiber reflectometric CUPRAC sensor for total antioxidant capacity measurement of food extracts and biological samples // J. Agricultural and Food Chemistry. 2013. № 61. Р. 8381-8388). Определение основано на образовании в мембране окрашенного комплекса Cu(I)-неокупроин в результате ее контакта с аналитом, с последующим измерением отражения мембраны при 530 нм с использованием миниатюрного отражательного спектрометра.
Известен способ определения суммарной АОА в пищевых экстрактах с использованием оптического сенсора на основе нафиона (Bener M., Özyürek M., Cüclü K., Apak R. Development of low-cost optical sensor for cupric reducing antioxidant capacity measurement of food extracts // Analytical Chemistry. 2010. Vol. 82. №10. P. 4252-4258). Как и в способе, описанном выше, для определения АОА использована система Cu(II) – неокупроин, иммобилизованная в нафионовую мембрану. В результате реакции с веществами, обладающими антиоксидантными свойствами, Cu(II) восстанавливается до Cu(I) и в мембране формируется комплекс Cu(I)-неокупроин желтого цвета. В качестве аналитического сигнала в представленной работе измеряли светопоглощение нафионовой мембраны с полученным комплексным соединением при 450 нм.
Недостатком предложенных способов определения АОА является низкая оперативность, которая заключается как в длительности процесса подготовки нафионовой мембраны к анализу, так и в длительности самой методики определения АОА. Кроме того, детектирование аналитического сигнала с помощью миниатюрного отражательного спектрометра необходимо проводить в темном помещении, чтобы свести к минимуму помехи от окружающего света.
Наиболее близким аналогом к заявляемому изобретению является способ оценки интегральной АОА растительного сырья и продуктов питания на его основе с использованием полиметакрилатной матрицы (Патент РФ 2391660, опубл. 10.06.2010, МПК G01N 33/00). Способ основан на взаимодействии восстановителей органической природы с индикаторной системой железо(III) – о-фенантролин, иммобилизованной в полиметакрилатную матрицу, при этом железо(III) восстанавливается до железа(II), которое образует в матрице прочный окрашенный в оранжевый цвет комплекс с о-фенантролином. В качестве аналитического сигнала измеряли светопоглощение образующегося в матрице комплекса при 510 нм.
Существенным недостатком данного способа можно считать длительность методики анализа (45 мин), а также невысокую чувствительность.
Задачей настоящего изобретения является разработка оперативного чувствительного способа определения интегральной АОА с использованием иммобилизованной в полиметакрилатную матрицу индикаторной системы.
Решение указанной задачи достигается тем, что в способе определения интегральной АОА, включающем взаимодействие реагента, иммобилизованного в оптическую мембрану, с аналитом, последующее ее отделение от раствора, измерение аналитического сигнала и оценку величины антиоксидантной активности, отличающемся тем, что в качестве индикаторной системы, иммобилизованной в оптическую мембрану, применяют медь(II)-неокупроин, аналитический сигнал представляют в виде светопоглощения при 450 нм, или визуальной оценки интенсивности окраски оптической мембраны, количественную и/или качественную оценку интегральной антиоксидантной активности проводят по градуировочному графику и /или цветовой шкале, построенным для аскорбиновой кислоты, используемой в качестве вещества-стандарта.
Сущность изобретения поясняется чертежами:
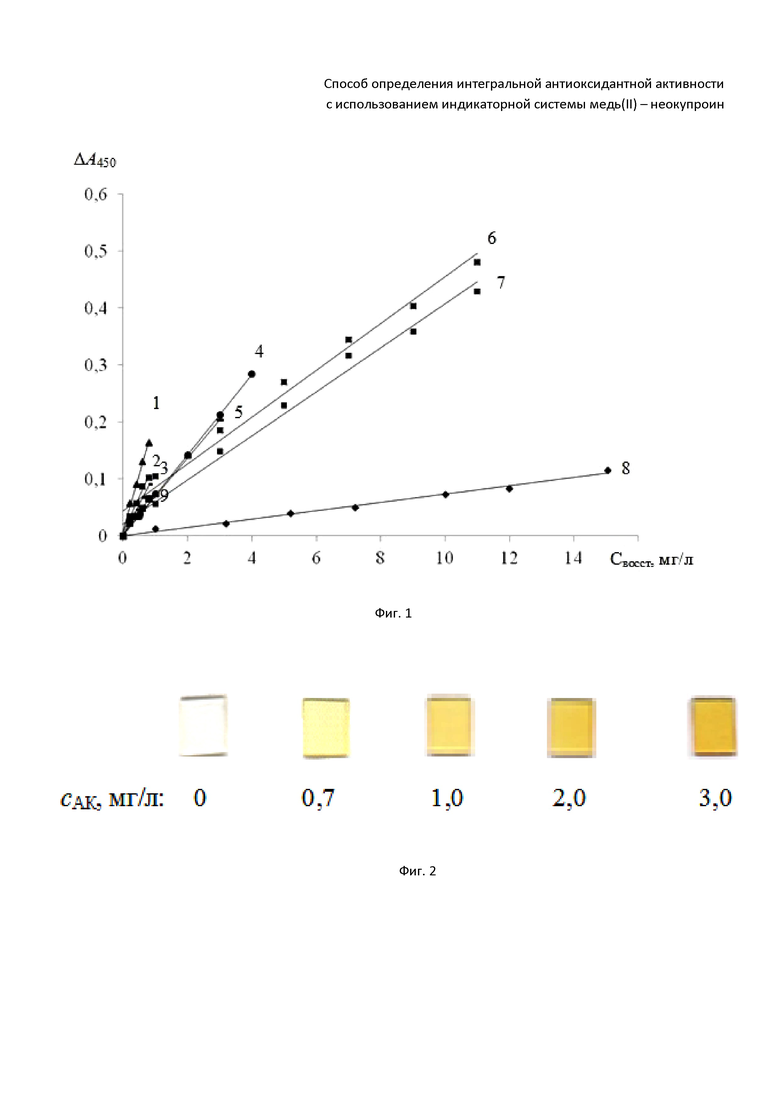
На фиг. 1 представлена зависимость изменения аналитического сигнала от количества восстановителя, где цифрами обозначено:
1 – кверцетин,
2 – лютеолин,
3 – дигидрокверцетин,
4 – галловая кислота,
5 – аскорбиновая кислота,
6 – цистеин,
7 – гидрат катехина,
8 – рутин,
9 – танин.
На фиг. 2 показано сканированное изображение образцов полиметакрилатной матрицы с иммобилизованной индикаторной системой Cu(II) – неокупроин после контакта с растворами АК.
Сущность заявляемого способа заключается в воздействии восстановителей органической природы на индикаторную систему Cu(II) – неокупроин, иммобилизованную в полиметакрилатную матрицу. При этом Cu(II) восстанавливается до Cu(I) и образует с неокупроином комплекс, окрашенный в желтый цвет, имеющий в спектре поглощения максимум при λ=450 нм.
Иммобилизацию индикаторной системы Cu(II) – неокупроин в полиметакрилатную матрицу проводили ее сорбцией из раствора в статическом режиме в одну стадию. Для этого полиметакрилатную матрицу перемешивали в растворе, содержащем 8 мл 0,05% водно-спиртового раствора неокупроина и 2 мл раствора Cu (II) 1 мг/мл в объеме 25 мл в течение 5 мин.
В исследуемый раствор с pH 4, содержащий антиоксиданты, вносили полиметакрилатную матрицу с индикаторной системой Cu(II) – неокупроин, тщательно перемешивали в течение 20 мин, вынимали, подсушивали фильтровальной бумагой, измеряли поглощение при 450 нм. За аналитический сигнал при построении градуировочных зависимостей принимали величину ΔA450 (ΔA450 = А и А0 – оптическая плотность полиметакрилатной матрицы при 450 нм после контакта с раствором в присутствии и отсутствие определяемого компонента соответственно).
Для исследования влияния восстановителей органической природы на индикаторную систему Cu(II) – неокупроин, иммобилизованную в полиметакрилатную матрицу, выбраны широко распространенные в растительных материалах и используемые в пищевой промышленности антиоксиданты фенольной и нефенольной природы. Зависимости аналитического сигнала от содержания восстановителя в растворе и их параметры представлены на фиг. 1 и в таблице 1.
Таблица 1. Зависимость ΔA450 от концентрации восстановителя
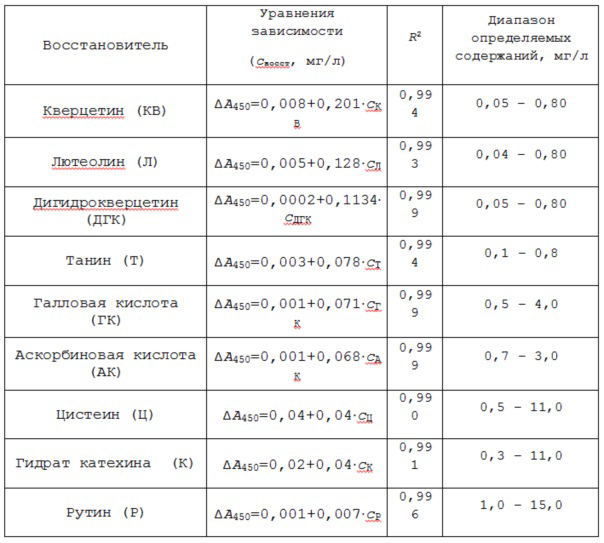
Для доказательства суммирующего характера определяемой величины интегральной АОА изучено влияние модельных смесей, в состав которых входили восстановители кверцетин, галловая кислота и аскорбиновая кислота в различных соотношениях, на индикаторную систему Cu(II) – неокупроин, иммобилизованную в полиметакрилатную матрицу. Расчет теоретической величины интегральной АОА проводили по уравнениям количественного соответствия, характеризующим антиоксидантную способность исследуемого восстановителя по отношению к аскорбиновой кислоте, как вещества-стандарта (таблица 2). Экспериментальные значения АОА рассчитывали по усредненному уравнению регрессии для зависимости ΔA450 от количества аскорбиновой кислоты. Из результатов, представленных в таблице 3, видно, что экспериментально полученные величины АОА удовлетворительно согласуются с теоретически рассчитанными. Полученные данные показывают, что определяемая величина АОА является результатом совместного действия всех присутствующих в модельной смеси восстановителей. Таким образом, определяемый показатель является интегральным и оптическая мембрана на основе полиметакрилатной матрицы с иммобилизованной системой Cu(II) – неокупроин может быть использована для оценки интегральной АОА.
Таблица 2. Уравнения количественного соответствия для восстановителей
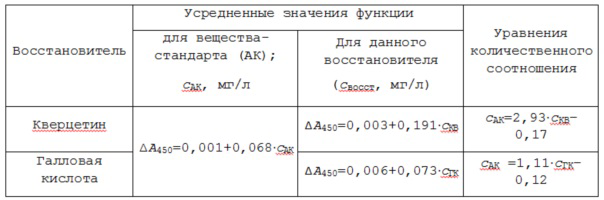
Таблица 3. Результаты анализа модельных смесей
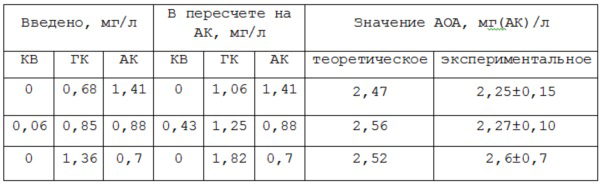
Пример 1. Измерение поглощения полиметакрилатной матрицы и определение интегральной АОА по градуировочному графику
В 25 мл анализируемого раствора с суммарным содержанием антиоксидантов не более 0,075 мг с рН 4 (цитратный буфер, контроль рН-метром) помещали пластинку полиметакрилатной матрицы с иммобилизованной индикаторной системой Cu(II) – неокупроин и перемешивали в течение 20 минут, затем вынимали, подсушивали фильтровальной бумагой, измеряли поглощение при 450 нм и рассчитывали ΔА450. Содержание суммарной АОА находили по градуировочной зависимости, построенной для АК в аналогичных условиях, с последующим расчетом величины суммарной АОА в виде количества вещества-стандарта (аскорбиновой кислоты), производящего антиоксидантный эффект, эквивалентный действию суммы восстановителей в аналите. Уравнение градуировочной зависимости имеет вид: ∆А450=0,001+67,828сАК, где сАК – концентрация АК, г/л. Диапазон линейности градуировочной зависимости составляет 0-0,003 г/л.
Пример 2. Визуально-тестовое определение интегральной АОА
Для визуально-тестового определения АОА получены цветовые шкалы путем сканирования образцов, полученных при построении градуировочных зависимостей для АК. Визуальное тест-определение выполняли аналогично методике, описанной в примере 1, с тем отличием, что после контакта с аналитом поглощение полиметакрилатных матриц не измеряли, а проводили сравнение их окраски с цветовой шкалой (фиг. 2) и полуколичественно определяли концентрацию восстановителей.
Пример 3. Определение интегральной АОА лекарственных настоек, соковой продукции, чая
По предлагаемому способу были проанализированы лекарственные настойки, соковая продукция, зеленые и черные чаи.
Образцы настоек и соковой продукции не требовали предварительной пробоподготовки, приготовление экстрактов чая проводили по ГОСТу (ГОСТ 19885-74 Чай. Методы определения содержания танина и кофеина. – Введ. 1975-06-30. - М.: Стандартинформ, 2009. – 5 с.), далее поступали, как указано в примере 1.
Результаты определения АОА представлены в таблицах 4-6.
Таблица 4. Результаты определения интегральной антиоксидантной активности соковой продукции (n=3, P=0,95)
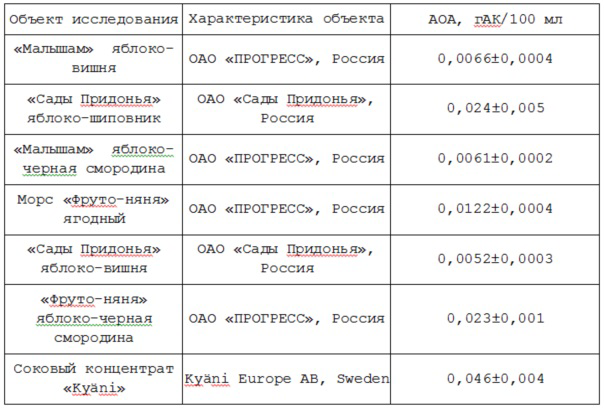
Таблица 5. Результаты определения интегральной антиоксидантной активности лекарственных настоек (n=3, P=0,95)
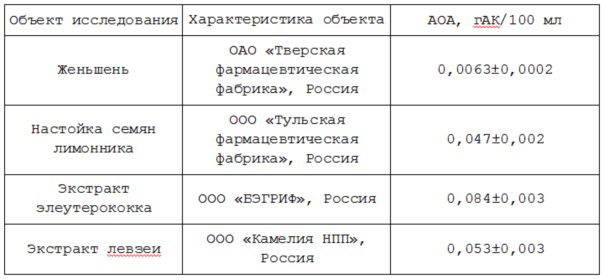
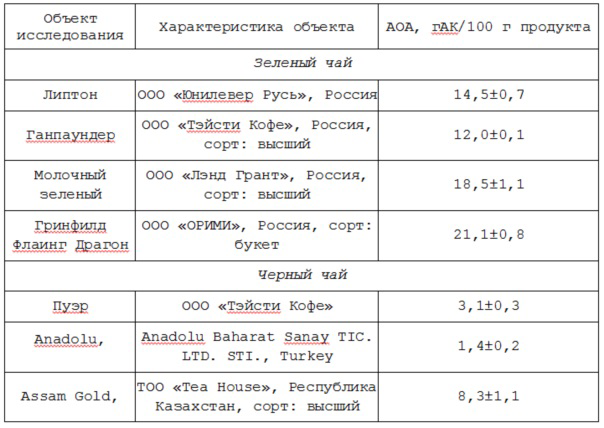
Таблица 6. Результаты определения интегральной антиоксидантной активности чая (n=3, P=0,95)
Как видно из представленных данных, значения антиоксидантной активности исследованной продукции варьируются в широком диапазоне.
Для подтверждения правильности предлагаемого способа определения АОА использовали метод разбавления анализируемой пробы. Показатели прецизионности – повторяемости (σr), правильности (σс), точности (σ) – предлагаемого метода определения АОА продуктов питания определяли в соответствии с требованиями РМГ 61 – 2003. В таблице 7 приведены результаты определения АОА методом разбавления и основные метрологические характеристики предлагаемого способа определения АОА ряда продуктов питания.
Показатели повторяемости по исследованным продуктам составили в относительных единицах в основном не более 5 %, а границы относительной систематической погрешности – не более 8,5 %.
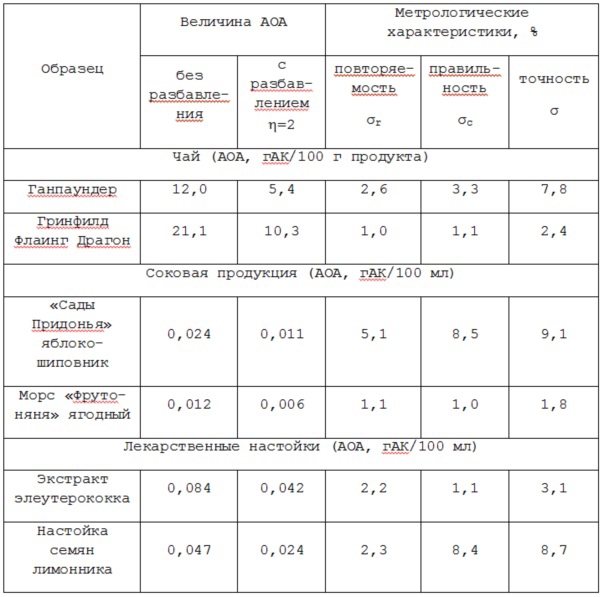
Таблица 7. Результаты определения АОА методом разбавления в продуктах питания и основные метрологические характеристики твердофазно-спектрофотометрической методики определения АОА (n=3, P=0,95)
Преимуществом заявленного изобретения является сокращение в 2 раза времени анализа и увеличение в 3,5 раза чувствительности определения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНТЕГРАЛЬНОЙ АНТИОКСИДАНТНОЙ АКТИВНОСТИ С ИСПОЛЬЗОВАНИЕМ ПОЛИМЕТАКРИЛАТНОЙ МАТРИЦЫ | 2009 |
|
RU2391660C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МЕДИ | 2015 |
|
RU2599517C1 |
| Способ определения меди в воде | 2022 |
|
RU2792612C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СУММЫ МЕТАЛЛОВ С ИСПОЛЬЗОВАНИЕМ ПОЛИМЕТАКРИЛАТНОЙ МАТРИЦЫ | 2015 |
|
RU2613762C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СЕЛЕНА(IV) | 2014 |
|
RU2567844C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НИТРИТОВ | 2015 |
|
RU2578024C1 |
| СПОСОБ ТВЕРДОФАЗНОЙ ЭКСТРАКЦИИ КРАСИТЕЛЯ МАЛАХИТОВОГО ЗЕЛЕНОГО | 2015 |
|
RU2603161C2 |
| СПОСОБ ТВЕРДОФАЗНОЙ ЭКСТРАКЦИИ КРАСИТЕЛЯ ТОЛУИДИНОВОГО СИНЕГО | 2015 |
|
RU2605965C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПАЛЛАДИЯ (II) | 2011 |
|
RU2461822C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ХРОМА (VI) | 2012 |
|
RU2498294C1 |
Изобретение относится к области аналитической химии и может быть использовано для определения интегральной антиоксидантной активности (АОА) растительного сырья и продуктов питания на его основе. Способ включает взаимодействие реагента, иммобилизованного в оптическую полиметакрилатную мембрану, с аналитом, последующее ее отделение от раствора и оценку величины антиоксидантной активности. В качестве реагента применяют индикаторную систему медь(II) – неокупроин, иммобилизованную в полиметакрилатную матрицу, аналитический сигнал представляют в виде светопоглощения при 450 нм, или визуальной оценки интенсивности окраски оптической мембраны, количественную и/или качественную оценку интегральной антиоксидантной активности проводят по градуировочному графику и/или цветовой шкале, построенным для аскорбиновой кислоты, используемой в качестве вещества-стандарта. 2 ил., 7 табл., 3 пр.
Способ определения интегральной антиоксидантной активности, включающий взаимодействие реагента, иммобилизованного в оптическую полиметакрилатную мембрану, с аналитом, последующее ее отделение от раствора и оценку величины антиоксидантной активности, отличающийся тем, что в качестве реагента применяют индикаторную систему медь(II) – неокупроин, иммобилизованную в полиметакрилатную матрицу, аналитический сигнал представляют в виде светопоглощения при 450 нм, или визуальной оценки интенсивности окраски оптической мембраны, количественную и/или качественную оценку интегральной антиоксидантной активности проводят по градуировочному графику и/или цветовой шкале, построенным для аскорбиновой кислоты, используемой в качестве вещества-стандарта.
| СПОСОБ ОПРЕДЕЛЕНИЯ ИНТЕГРАЛЬНОЙ АНТИОКСИДАНТНОЙ АКТИВНОСТИ С ИСПОЛЬЗОВАНИЕМ ПОЛИМЕТАКРИЛАТНОЙ МАТРИЦЫ | 2009 |
|
RU2391660C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СЕРЕБРА С ИСПОЛЬЗОВАНИЕМ ПОЛИМЕТАКРИЛАТНОЙ МАТРИЦЫ | 2009 |
|
RU2391659C1 |
| REŞAT APAK et al | |||
| Comparative Evaluation of Various Total Antioxidant Capacity Assays Applied to Phenolic Compounds with the CUPRAC Assay | |||
| Пресс для выдавливания из деревянных дисков заготовок для ниточных катушек | 1923 |
|
SU2007A1 |
| Темердашев З | |||
| А | |||
| и др | |||
| ОПРЕДЕЛЕНИЕ АНТИОКСИДАНТНОЙ АКТИВНОСТИ ПИЩЕВЫХ ПРОДУКТОВ С ИСПОЛЬЗОВАНИЕМ ИНДИКАТОРНОЙ СИСТЕМЫ Fe (III)/Fe (II) — ОРГАНИЧЕСКИЙ РЕАГЕНТ | |||
| "Заводская лаборатория | |||
| Диагностика материалов" | |||
| Походная разборная печь для варки пищи и печения хлеба | 1920 |
|
SU11A1 |
| Пломбировальные щипцы | 1923 |
|
SU2006A1 |
| Термосно-паровая кухня | 1921 |
|
SU72A1 |
| С | |||
| Прибор для нагревания перетягиваемых бандажей подвижного состава | 1917 |
|
SU15A1 |
Авторы
Даты
2017-07-11—Публикация
2016-08-02—Подача