Область изобретения относится к 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамиду, фармацевтическим композициям на его основе их использование для лечения и профилактики гриппа.
Соответственно, настоящее изобретение связано с соединением формулы (I):
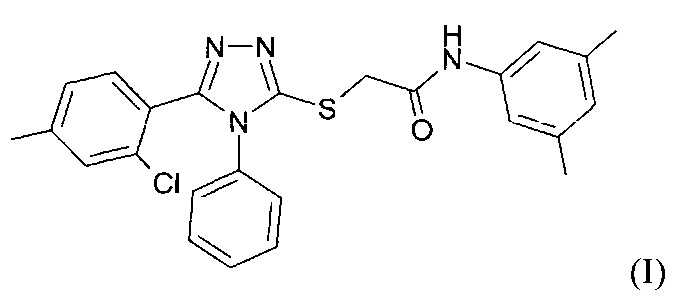
к композициям, в том числе фармацевтическим, средству для лечения и применению 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида (I) в качестве антимикробного, антибактериального и противогрибкового, а также вирулицидного агента.
Вирус гриппа на сегодня является самым распространенным инфекционным заболеванием, приносящим огромный экономический ущерб. По данным Всемирной организации здравоохранения (ВОЗ), ежегодно в мире болеют гриппом около миллиарда человек. Грипп - это острое вирусное заболевание, которое может поражать верхние и нижние дыхательные пути, сопровождается выраженной интоксикацией и может приводить к серьезным осложнениям и летальным исходам - в основном у пожилых больных и детей. Поэтому неудивительно, что о тяжести эпидемии гриппа судят не только по числу заболевших людей, но и по показателю «избыточной смертности» в течение осенне-зимнего периода, который составляет в странах Европы 35-45 тысяч человек в год. При гриппе происходит обострение многих хронических заболеваний, которые также «вносят вклад» в показатель избыточной смертности.
Взрослые от эпидемий страдают в меньшей степени, поскольку уже неоднократно «встречались с вирусами», а вот дети наиболее восприимчивы к гриппу, начиная со второго полугодия жизни (в первом полугодии они защищены материнскими антителами). Восприимчивость повышается также после 60 лет, так как с возрастом теряются накопленные антитела к вирусам гриппа разной антигенной структуры. Часто болеют гриппом медицинские работники, работники транспорта, торговли, педагоги, имеющие широкий круг профессиональных контактов.
В настоящее время вирусные инфекции составляют преобладающую часть инфекционной патологии человека. Самыми распространенными среди них остаются острые респираторные (ОРВИ) и другие вирусные инфекции, передаваемые воздушно-капельным путем, возбудители которых относятся к абсолютно различным семействам, чаще всего это РНК-содержащие вирусы (вирус гриппа A, B, C, вирус эпидемического паротита, вирусы парагриппа, вирус кори, риновирусы и другие).
Эти инфекции способствуют формированию хронических заболеваний дыхательных путей, являются одной из причин возникновения пневмонии, отягощают течение других болезней, способствуя их неблагоприятному исходу Даже в межэпидемическое время грипп и ОРВИ составляют до 40% всех заболеваний, зарегистрированных в медицинских учреждениях Российской Федерации, среди взрослого населения и более 60% среди детей. Вместе с тем для предупреждения этих заболеваний нет гарантированных специфических вакцин, а в их лечении используются, в основном, патогенетические и симптоматические средства, так как арсенал этиотропных противовирусных препаратов невелик.
Для терапии гриппа в медицинской практике широко используют препараты Амантадин и Ремантадин, в качестве противовирусных профилактических и лечебных средств, которые обладают противовирусной активностью в отношении штаммов вируса гриппа [Am. J. Med. - 1997. - V. 102(ЗА) - N 17. - P. 55-60], [Watts J. «Asiannations step up action to curb spread of avian influenza» // Lancet. - 2004. - V. 363 - N 9406. - P. 373]. В Российской Федерации получил распространение противовирусный препарат Ремантадин. Его применяют для лечения и профилактики инфекции, вызванной вирусами гриппа типа A. Выраженный терапевтический эффект, данный препарат показал и в отношении вируса гриппа подтипа H3N2. Механизм воздействия на вирус связан с блокировкой функции вирусного белка внутри мембраны. Ингибирование вирусной активности наступает на этапах рецептор-опосредованного эндоцитоза, декапсидации в фаголизосоме, а также сборки и почкования вирусных частиц [Вестник РАМН // 1993. - N 3. - Р. 10-15]. Однако у Ремантадина, как представителя группы адамантанов, имеются ограничения в применении. При высоких дозах, возникают побочные эффекты со стороны центральной нервной системы (ЦНС), в частности он может вызывать судорожные явления, а также оказывать неблагоприятное влияние на печень, почки, что делает маловероятным его применение у людей с заболеваниями данных органов.
Широко в настоящее время используют ингибиторы нейраминидазы вирусов гриппа A и B - Озельтамивир (Тамифлю) и Занамивир (Реленза), которые действуют на этапе выхода вновь синтезированных вирионов вируса гриппа из оболочки клетки, путем блокирования отцепления вирусных частиц от поверхности клеток. Однако в настоящее время в результате широкого использования данных препаратов значительно утрачены их противовирусные свойства в отношении вирусов гриппа A и B [Menno D. De Jong, Tran Tan Thanh, Truong Huu Khanhetal. Oseltamivir Resistance during Treatment of Influenza A (H5N1) Infection // N. Engi. J. Med. - 2005. - №353. - P. 2667-2572], [Smee D.F., Wong M.H., Bailey K.W., et al. Activities of oseltamivir and ribavirin used alone and in combination against infections in mice with recent isolates of influenza A (H1N1) and В viruses // Antivir. Chem. Chemother. - 2006. - V. 17. - N 4. - P. 185-192]. Потерю активности в основном связывают с мутациями в гене, кодирующем белок М2, которые делают вирус устойчивым к этому классу соединений [Li K.S., Guan Y., Wang J., et al., Genesis of a highly pathogenic and potentially pandemic H5N1 influenza virus in eastern Asia // Nature - 2004. - Vol - 430. - №6996. - P. 209-213]. Мутации, как правило, возникают примерно в 30% случаев. К числу нежелательных явлений, сопровождающих прием ингибиторов нейроминидазы, относят головокружение, головную боль, нарушение сна, слабость; у пациентов (в основном у детей и подростков), принимавших препарат с целью лечения гриппа, были зарегистрированы судороги и делирий (включая такие симптомы, как нарушение сознания, дезориентация во времени и пространстве, анормальное поведение, бред, галлюцинации, возбуждение, тревога и кошмары).
Работа над созданием новых препаратов для лечения и, тем более, профилактики респираторных заболеваний вирусной этиологии проводится постоянно. В частности, ведутся разработки препаратов, способных разрушать оболочку вируса и конкретно тот фермент, который отвечает за размножение конкретного вируса, предотвращая его распространение по дыхательным путям. Примером может быть Плеконарил в отношении риновирусов.
В настоящее время учеными апробирован большой набор средств и проводится разработка оптимальных сочетаний и схем лечения и профилактики ОРВИ. Вероятно, скоро в арсенале практических врачей появятся противовирусные препараты, эффективность которых повышается при комбинированном применении. Разумная комбинация препаратов позволит суммировать достоинства и минимизировать недостатки, свойственные каждому из препаратов, и соответственно повышать их эффективность, а также создавать условия, при которых невозможно, что особенно важно, формирование резистентности вирусов.
Поставленная задача достигается синтезом 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-]-N-(3,5-диметилфенил)ацетамида, имеющего структурную формулу (I),
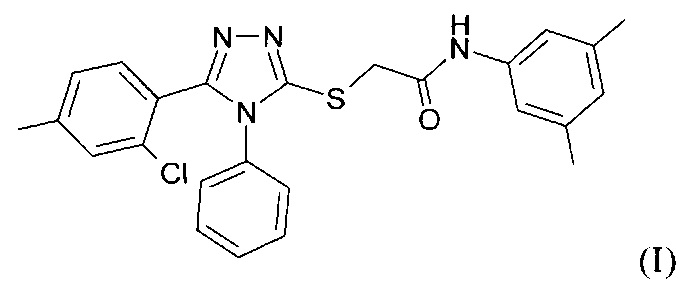
и его фармацевтически приемлемых солей; созданием на его основе противовирусного лекарственного средства, обладающего активностью против вирусов гриппа типа A и B, композиций, в том числе фармацевтических и их применением в терапии и профилактике, в том числе, но не ограничиваясь, - в лечении и профилактики гриппа. Промышленная применимость настоящего изобретения выражается, помимо всего прочего, в применении соединений и веществ по настоящему изобретению для лечения и профилактики гриппа, для производства лекарственных средств для людей и животных.
Информация о ближайших аналогах изобретения содержится в опубликованной статье: Fedichev, P.; Timakhov, R.; Pyrkov, Т.; Getmantsev, Е.; Vinnik, A., (Structure-based drug design of a new chemical class of small molecules active against influenza A nucleoprotein in vitro and in vivo", PLoS Curr. 2011, 3, RRN1253. и патентных заявках российской заявки 201110468 и РСТ заявке на ее основе с аналогичным содержанием WO/2012/108794. Соединения, представляющие собой бензилиденовые производные гидразида 1,2,4-триазол-3-илтиогликолевой кислоты общей формулы:

или его фармацевтически приемлемую соль, солевой аддукт или сольват, для лечения и профилактики гриппа.
Несмотря на опубликованные данные, ближайшие аналоги соединения по настоящему изобретению, например:
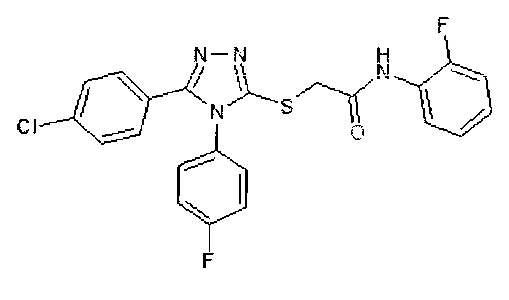

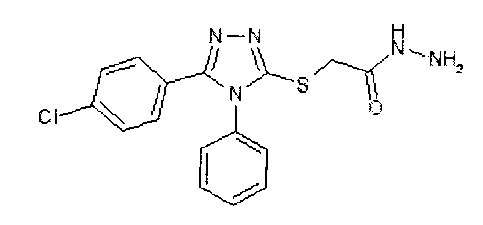
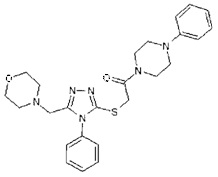
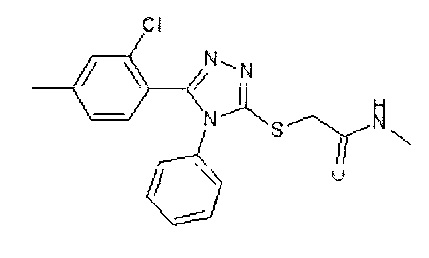
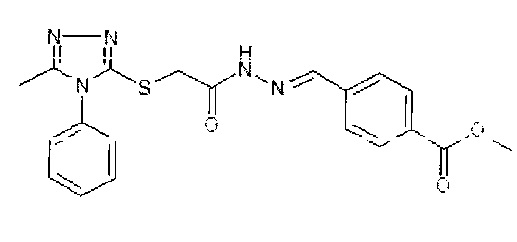
не обладают активностью против гриппа, кроме того, соединение по настоящему изобретению обладает лучшим профилем ADME-свойств (растворимость, стабильность, фармакокинетика, биодоступность и др.) чем ближайшие аналоги с противогрипповым действием.
Противовирусное активное соединение, по настоящему изобретению, может быть использовано (но не обязательно) в виде соли, приемлемой с фармацевтической точки зрения. Кислый аддукт, полученный из приемлемой с фармацевтической точки зрения свободной кислоты, является предпочтительным. Соединение, представленное вышеупомянутой формулой I, можно перевести в приемлемый с фармацевтической точки зрения кислый аддукт при помощи технических приемов, общеупотребительных в вышеупомянутой технической области. Свободная кислота может представлять собой органическую или неорганическую кислоту. Неограничивающими объем защиты примерами соответствующей неорганической кислоты являются соляная кислота, бромноватая кислота, серная кислота, метафосфорная кислота и др., и неограничивающими примерами соответствующей органической кислоты являются (метилтио)уксусная кислота, 1-аминоциклопропан-1-карбоновая кислота, 1-метилциклопропен-1-карбоновая кислота, 2-амино-2-метилбутановая кислота, 2-аминоизобутановая кислота, 2-бутиновая кислота, 2-этилбутановая кислота, фуран-2-карбоновая кислота, 2-гидроксиэтансульфоновая кислота, 2-гидроксипропановая кислота, 2-кетобутановая кислота, 2-метилбутановая кислота, 2-метилциклопропанкарбоновая кислота, 2-метилвалерьяновая кислота, 2-оксоглутаровая кислота, 2-оксопентановая кислота, 2-пентановая кислота, 2-тетрагидрофуранкарбоновая кислота, 2,2-дихлоруксусная кислота, 3-аминогексановая кислота, 3-аминопентановая кислота, 3-аминоизобутановая кислота, 3-фуранкарбоновая кислота, 3-гуанидинопропионовая кислота, 3-метоксипропионовая кислота, 3-метилбутановая кислота, 3-морфолинкарбоновая кислота, 3,3-диметилакриловая кислота, 4-ацетамидобензойная кислота, 4-аминобутановая кислота, 4-аминосалициловая кислота, 4-пентиновая кислота, 5-аминовалерьяновая кислота, 6-аминокапроновая кислота, уксусная кислота, ацетоуксусная кислота, акриловая кислота, адипиновая кислота, ангеликовая кислота, аскорбиновая кислота, аспарагиновая кислота, азетидин-2-карбоновая кислота, азетидин-3-карбоновая кислота, бензолсульфоновая кислота, бензойная кислота, бутановая кислота, камфора-10-сульфоновая (камзиловая) кислота, ванилиновая кислота, каприновая (декановая) кислота, капроновая кислота, каприловая кислота, угольная кислота, коричная кислота, цитраконовая кислота, лимонная кислота, циклобутанкарбоновая кислота, циклопропанкарбоновая кислота, циклопропилуксусная кислота, диэтиламиноуксусная кислота, дигидроксималоновая кислота, додецилсерная кислота, этан-1,2-дисульфоновая кислота, этансульфоновая кислота, этоксиуксусная кислота, муравьиная кислота, фумаровая кислота, галактаровая кислота монометиловый эфир, гентизиновая кислота, глюконовая кислота, глютаконовая кислота, глютаминовая кислота, глутаровая кислота, глицериновая кислота, глицерофосфорная кислота, гликоливая кислота, глиоксаливая кислота, гиппуровая кислота, гидантоиновая кислота, бромводородная кислота, хлорводородная кислота, хлорная кислота, изоникотиновая кислота, изонипекотовая кислота, изовалерьяновая кислота, итаконовая кислота, 1-азетидин-2-карбоновая кислота, молочная кислота, лактобионовая кислота, лауриновая кислота, лейциновая кислота, левулеиновая кислота, малеиновая кислота, яблочная кислота, малоновая кислота, миндальная кислота, мезаконовая кислота, метансульфонофая кислота, метоксиуксусная кислота, метилсукциновая кислота, никотиновая кислота, нипекотовая кислота, азотная кислота, олеиновая кислота, оксамовая кислота, пара-толуолсульфоновая кислота, пальмитиновая кислота, памовая кислота, фосфорная кислота, пипеколиновая кислота, триметилуксусная кислота, пропиоловая (пропаргиловая) кислота, пироглютаминовая кислота, пируватная кислота, салициловая кислота, себациновая кислота, сорбовая кислота, стеариновая кислота, янтарная кислота, сукцинаминовая кислота, серная кислота, винная кислота, тартроновая (гидроксималоновая) кислота, тетрагидро-3-фурановая кислота, тиглиновая кислота, трифторуксусная кислота, триметилпируватная кислота, ундециленовая кислота, валерьяновая (пентановая) кислота и пр. Каждая из этих солей может быть получена из 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида известными из уровня техники способами, например, но не ограничиваясь, путем взаимодействия соединения I с одной из перечисленных выше кислот. Образование фармацевтически приемлемой соли может быть осуществлено в подходящем для этой цели растворителе, например этаноле, ацетонитриле, ацетоне, при нагревании или без него.
Некоторые реализации настоящего изобретения также относятся к фармацевтической композиции, содержащей соединение, представленное формулой (I), или его приемлемую с фармацевтической точки зрения соль в качестве активного ингредиента.
Некоторые реализации настоящего изобретения также относятся к противовирусной композиции, содержащей соединение, представленное формулой (I), или его приемлемую с фармацевтической точки зрения соль в качестве активного ингредиента.
Некоторые реализации настоящего изобретения также относятся к применению 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида, в качестве лекарственного средства,
Некоторые реализации настоящего изобретения также относятся к применению 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида, в качестве лекарственного средства, в лечении болезней, в которых его применение приводит к терапевтическому или профилактическому эффекту.
Некоторые реализации настоящего изобретения относятся к нижеследующему:
1. 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид, имеющий структурную формулу (I):

2. Применение 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида, имеющего структурную формулу (I), для профилактики или лечения гриппа.
3. Фармацевтическая композиция, содержащая в качестве терапевтически активного агента 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид или его пролекарство.
4. Фармацевтическая композиция по п. 2 для профилактики или лечения гриппа.
5. Лекарственная форма для профилактики и/или лечения гриппа, полученная на основе фармацевтической композиции по любому из пп. 3-4.
6. Лекарственная форма по любому из пп. 3 и 5 в виде таблеток, пластинок, капсул, порошка, свечей, (суппозиториев) или инъекционных растворов.
7. Комбинированное лекарственное средство или терапевтический коктейль для профилактики и/или лечения гриппа, полученный на основе фармацевтической композиции по п.п. 3-6.
8. Применение 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида, имеющего структурную формулу (I), для профилактики или лечения заболеваний, связанных РНК-вирусной инфекцией. Другой вариант - заболеваний вызванных вирусом гриппа типа A (в том числе A/H3N2 и A/H5N1 swl, A/H3N2 и A/H5N1), вирусом гриппа типа В и парагриппа, аденовируса, а также вирусом, вызывающих респираторно-синцитиальную инфекцию.
9. Способ профилактики или лечения гриппа, при котором человек или иной субъект, который нуждается в лечении принимает 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-[-(3,5-диметилфенил)ацетамид или его фармацевтически приемлемую соль или его кислоту, или фармацевтическую композицию, содержащую в себе, как минимум, одно из нижеследующего: 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид или его фармацевтически приемлемую соль или его кислоту таким образом, чтобы при одном приеме в организм такого человека или иного субъекта попадало 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида или его фармацевтически приемлемой соли или его кислоты в количестве от менее 0.01 мг/кг массы тела и/или от около 0.01 мг/кг до около 100 мг/кг массы тела или от около 0.01 мг/кг до около 0.05 мг/кг массы тела и/или от около 0.05 мг/кг до около 0.1 мг/кг массы тела и/или или от около 0.1 мг/кг до около 0.5 мг/кг массы тела или от около 0.5 мг/кг до около 1 мг/кг массы тела и/или от около 1 мг до около 5 мг/кг массы тела и/или от около 5 мг до около 10 мг/кг массы тела и/или от около 10 мг/кг до около 50 мг/кг массы тела и/или от около 50 мг/кг до около 100 мг/кг массы или и/или от около 100 мг/кг до около 300 мг/кг массы тела в зависимости от целесообразности и выбранного режима лечения, причем в указанных выше дозах человек или иной субъект, нуждающийся в приеме этого лекарственного средства принимает такое лекарственное средство внутрь один, два, три или четыре раза в день отдельно или совместно с другими лекарствами, применяемыми при лечении соответствующего заболевания, в течение 1 дня, 2 дней, около 1 недели, около 1 месяца, около 6 месяцев, около 1 года или в течение всего срока заболевания или в течение срока, определяемого исходя из состояния пациента постоянно и (или) с перерывами или в профилактическом режиме за 1 день или 2 дня или несколько часов до или в иное время до возможного контакта с источником заражения.
10. Применение соединения по п. 1 для производства лекарственного средства.
11. Применение соединения по п. 1 в качестве сырья для производства лекарственного средства.
Поскольку фармацевтическая композиция содержит соединение, представленное формулой (I) или его фармацевтически приемлемую соль в качестве активного ингредиента и поскольку композиция подавляет размножение вирусов гриппа, ее можно применять при лечении или профилактики гриппа или простуды или инфекции, вызванной другими РНК-содержащими вирусами.
Для клинических и терапевтических целей фармацевтическую композицию по настоящему изобретению, можно вводить перорально или способом, отличным от перорального, например, но не ограничиваясь: внутривенно, подкожно, внутрибрюшинно или локально, интерназально и иными способами принятыми для лекарственных средств.
Типичные формы фармацевтической композиции для перорального введения, по настоящему изобретению, включают, (но не ограничиваются): таблетки, пастилки, суспензии на водной и масляной основе, эмульсии, твердые или мягкие капсулы, спреи, и т.п. Для приготовления в форме таблеток, капсул и др. включают связующее вещество, такое как лактоза, сахароза, сорбитол, маннитол, крахмал, амилопектин, целлюлоза или желатин; формообразующий наполнитель, такой как дикальцийфосфат; дезинтегратор, такой как крахмал; и скользящее вещество, такое как стеарат магния, стеарат кальция, стеарилфумарат натрия или полиоксиэтиленгликолевый воск. Для приготовления в виде капсул дополнительно включают жидкий носитель, такой как жирное масло.
Фармацевтическую композицию, по настоящему изобретению, можно вводить отличными от перорального способа путем подкожного введения, внутривенного введения, внутримышечного введения. Для приготовления в виде формы для введения отличным от перорального способом соединение, представленное формулой (I), смешивают со стабилизатором или буфером в воде для получения раствора или суспензии, который помещают в ампулы или флаконы.
В большинстве случаев эффективная доза соединения, представленного формулой (I), для взрослых составляет 1-200 мг/кг в день, предпочтительно 5-100 мг/кг в день. Следуя указаниям врача или фармацевта, соединение можно вводить несколько раз в день с соответствующими интервалами времени, предпочтительно 2-3 раза в день.
Используемый в настоящем изобретении термин "пролекарство", если не указано иначе, означает производное соединения, которое можно подвергать гидролизу, окислению или иной реакции в биологических условиях в биологических условиях (in vitro или in vivo) для получения указанного соединения. Примеры пролекарств включают, без ограничения, соединения, которые содержат биогидролизуемые функциональные группы, такие как биогидролизуемые амиды, биогидролизуемые сложные эфиры, биогидролизуемые карбаматы, биогидролизуемые карбонаты, биогидролизуемые уреиды и биогидролизуемые фосфатные аналоги. Другие примеры пролекарств включают соединения, которые содержат гемисукцинат, диметиламиноацетат или фосфорилоксиметилоксикарбонильную группу и другие см., например, следующие публикации: Fleisher, D. et al., (1996); Design of Prodrugs, edited by H. Bundgaard, (Elsevier, 1985); Methods in Enzymology, Vol. 42, p. 309-396, edited by K. Widder, et al (Academic Press, 1985); A Textbook of Drug Design and Development, edited by Krogsgaard-Larsen and H. Bundgaard, Chapter 5 "Design and Application of Prodrugs," by H. Bundgaard p. 113-191 (1991); H. Bundgaard, Advanced Drug Delivery Reviews, 8: 1-38 (1992); J. Med. Chem., (1996), 39:10. Обычно пролекарства можно изготавливать, используя общеизвестные способы, такие как описанны в изданиях Burger's Medicinal Chemistry and Drug Discovery, 172-178, 949-982 (Manfred E. Wolff ed., 5th ed., 1995) и Design of Prodrugs (H. Bundgaarded., Elselvier, New York, 1985).
Используемый в настоящем изобретении «метаболит» означает любое вещество, полученное из другого вещества посредством метаболизма или метаболического процесса. Такие продукты могут быть получены в результате окисления, восстановления, гидролиза, амидирования, деамидирования, этерификации, деэтерификации, ферментативного расщепления и тому подобного, вводимого соединения.
Некоторые соединения по настоящему изобретению могут существовать в сольватированных формах, включая гидратированные формы. Обычно сольватированные формы эквивалентны несольватированным формам и также включены в объем настоящего изобретения.
Некоторые соединения по настоящему изобретению могут существовать в различных кристаллических или аморфных формах. Как правило, все физические формы эквивалентны для применений, предусматриваемых настоящим изобретением, и входят в объем настоящего изобретения.
Некоторые воплощения настоящего изобретения включают в себя соединения, меченные изотопами, имеющие один или более атомов, которые заменены на атомы, имеющие атомную массу или массовое число, отличное от числа атомной массы или массового числа обычно находящегося в природе. Примеры изотопов, которые могут быть включены в соединения по настоящему изобретению, включают изотопы водорода, углерода, азота, кислорода, серы, фтора и хлора, такие как 2H, 3H, 13C, 14C, 15N, 18O, 17O, 35S, 18F и 36Cl, соответственно. Соединения по настоящему изобретению, их пролекарства и фармацевтически приемлемые соли указанных соединений и указанных пролекарств, которые содержат вышеупомянутые изотопы и/или другие изотопы других атомов, входят в объем настоящего изобретения.
Некоторые меченные изотопами соединения по настоящему изобретению, например, те, в которые включены радиоактивные изотопы, такие как 3H и 14C, полезны в структуре лекарственного средства и/или субстрата для фармакокинетических исследований по распределению в тканях и органах. Тритий, 3H и углерод-14, 14C изотопы особенно предпочтительны из-за легкости их получения и обнаружения. Кроме того, замещение более тяжелыми изотопами, такими как дейтерий, 2Н, может предоставить некоторые терапевтические преимущества в результате более высокой метаболической стабильности, например увеличение периода полураспада или уменьшение потребностей лекарственных и, следовательно, может быть предпочтительным в некоторых обстоятельствах.
Меченные изотопами соединения по настоящему изобретению и их пролекарства и их фармацевтически приемлемые соли могут быть получены путем проведения известных синтетических процедур, использующих метод замещения атомов с помощью легкодоступных меченных изотопных реагентов.
Термин "терапевтически эффективное количество" подразумевает количество соединения по настоящему изобретению, которое (i) оказывает лечебное или профилактическое действие на конкретное заболевание, состояние или расстройство, (ii) уменьшает, смягчает или устраняет один или несколько симптомов конкретного заболевания, состояния или расстройства, или (iii) предотвращает или замедляет проявление одного или нескольких симптомов конкретного заболевания, состояния или расстройства, описанного в настоящем документе.
Используемый в настоящем документе термин "вспомогательное средство" относится к использованию активных соединений в сочетании с известными терапевтическими средствами. Такие средства включают противовирусные, противовоспалительные, иммуномодулирующие, жаропонижающие и другие средства, но не ограничиваются ими. Примеры вспомогательных лекарственных средств, которые могут сочетаться с 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)-ацетамидом, включают, но не ограничиваются эти списком:
противогриппозные лекарственные средства с другим механизмом действия: ингибиторы нейроаминидазы вируса гриппа - занамивир, озельтамивир; блокаторы М2-каналов - амантадин, римантадин; интерферониндуцирующие и иммуномодулирующие - арбидол, ингавирин и другие, например, рибаверин селективно ингибирующий синтез вирусных РНК.
противогистаминные лекарственные средства: хлорфенамин, тавегил, кетотифен, дифенгидрамин, супрастин, димебон, димедрол и другие;
анальгетические, обезболивающие и жаропонижающие лекарственные средства - ацетилсалициловая кислота, парацетамол, фенацетин, ибупрофен, флурбипрофен, диклофенак натрия и другие;
витамины: аскорбиновая кислота, никотиновая кислота и другие;
«Терапевтический коктейль и комбинированное лекарственное средство» представляет собой комбинацию двух и более лекарственных средств, обладающих различными механизмами фармакологического действия человека или животного и направленных на различные биологические мишени, участвующие в патогенезе заболевания.
«Фармацевтическая композиция» обозначает композицию, включающую в себя 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид и, по крайней мере, один из компонентов, выбранный из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих и воспринимающих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, измельчители, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от природы и способа назначения и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ.
Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие, как оливковое масло) и инъекционные органические сложные эфиры (такие, как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами измельчителей и распределяющих средств являются крахмал, алгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала одного или в комбинации с другим терапевтически активным агентом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения. Фармацевтические композиции, как правило, получают с помощью стандартных процедур, предусматривающих смешение активного соединения с жидким или тонко измельченным твердым носителем. В некоторых воплощениях настоящего изобретения, настоящее изобретение состоит в способе профилактики гриппа или способе лечения гриппа, при котором человек или иной субъект, который нуждается в лечении принимает 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид или его фармацевтически приемлемую соль или его кислоту, или фармацевтическую композицию, содержащую в себе, как минимум, одно из нижеследующего: 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид или его фармацевтически приемлемую соль или его кислоту таким образом, чтобы при одном приеме в организм такого человека или иного субъекта попадало 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида или его фармацевтически приемлемой соли или его кислоты в количестве от менее 0.01 мг/кг массы тела и/или от около 0.01 мг/кг до около 100 мг/кг массы тела или от около 0.01 мг/кг до около 0.05 мг/кг массы тела и/или от около 0.05 мг/кг до около 0.1 мг/кг массы тела и/или или от около 0.1 мг/кг до около 0.5 мг/кг массы тела или от около 0.5 мг/кг до около 1 мг/кг массы тела и/или от около 1 мг до около 5 мг/кг массы тела и/или от около 5 мг до около 10 мг/кг массы тела и/или от около 10 мг/кг до около 50 мг/кг массы тела и/или от около 50 мг/кг до около 100 мг/кг массы или и/или от около 100 мг/кг до около 300 мг/кг массы тела в зависимости от целесообразности и выбранного режима лечения, причем в указанных выше дозах человек или иной субъект, нуждающийся в приеме этого лекарственного средства принимает такое лекарственное средство внутрь один, два, три или четыре раза в день отдельно или совместно с другими лекарствами, применяемыми при лечении соответствующего заболевания, в течение 1 дня, 2 дней, около 1 недели, около 1 месяца, около 6 месяцев, около 1 года или в течение всего срока заболевания или в течение срока, определяемого исходя из состояния пациента постоянно и (или) с перерывами или в профилактическом режиме за 1 день или 2 дня или несколько часов до или в иное время до возможного контакта с источником заражения. Как один из возможных вариантов, вещества и соединения по настоящему изобретению могут применяться постоянно или с перерывами во время эпидемий гриппа здоровыми людьми. В некоторых воплощениях настоящего изобретения, настоящее изобретение состоит в применении 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида или его фармацевтически приемлемой соли или его кислоты, или фармацевтической композиции, содержащей в себе, как минимум, одно из нижеследующего: 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид или его фармацевтически приемлемую соль или его кислоту для производства лекарственного средства, в том числе, но не ограничиваясь, противовирусного лекарственного средства, в том числе, но не ограничиваясь лекарственного средства для лечения и/или профилактики гриппа, причем в некоторых воплощениях настоящего изобретения, настоящее изобретение состоит в применении перечисленных в настоящем предложении веществ и соединений в качестве сырья для производства по крайней мере одного из упомянутых в настоящем предложении лекарственных средств.
Одним из вариантом реализации настоящего изобретения является применение 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида, имеющего структурную формулу (I) или его фармацевтически приемлемой соли или его кислоты, в качестве лекарственного средства.
Сущность некоторых воплощений изобретения иллюстрируется следующим схемами и примерами:
Пример способа синтеза соединения по настоящему изобретению:
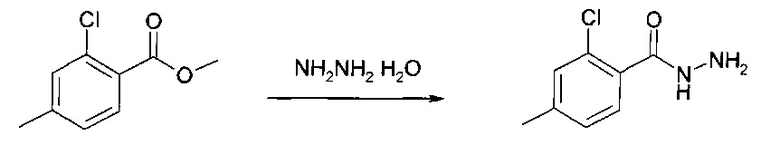



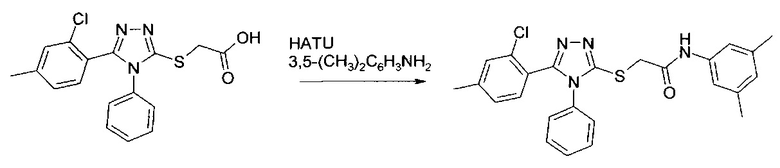

Пример 1. 2-хлор-4-метилбензойной кислоты гидразид
К раствору метилового эфира 2-хлор-4-метилбензойной кислоты (6.8 г, 0.037 моль) в этаноле (100 мл) добавляется (9.25 г, 0.185 моль) гидразин гидрата, затем смесь перемешивается в течение 16 часов при комнатной температуре, выпавший осадок отфильтровывают, промывают водой и высушивают. При упоминании в тексте воды по умолчанию имеется в виду дистиллированная вода. Выход: 2-хлор-4-метилбензойной кислоты гидразида (около 6.8 г, 100%)
Пример 2. 5-(2-хлор-4-метилфенил)-4-фенил-2,4-дигидро-[1,2,4]триазол-3-тион К суспензии 2-хлор-4-метилбензойной кислоты гидразида (6.8 г, 0.037 моль) в этаноле (100 мл) добавляют фенилизотиоцианат (5.9 г, 0.044 моль), кипятят в течение 5 часов, затем в смесь добавляют этанол (100 мл) и раствор NaOH (100 мл). Смесь перемешивают при 80°C 5 часов (контроль по ТСХ). Реакционную смесь, охлаждают до 25°C и подкисляют (pH 3-4) добавлением 37% HCl, выпавший осадок отфильтровывают, промывают водой и высушивают.
Выход: 5-(2-хлор-4-метилфенил)-4-фенил-2,4-дигидро-[1,2,4]триазол-3-тиона (около 9.2 г, 82.7%).
Пример 3. Получение 5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-уксусной кислоты этилового эфира
К суспензии 5-(2-хлор-4-метилфенил)-4-фенил-2,4-дигидро-[1,2,4]триазол-3-тион (9.2 г, 0.031 мол) в этаноле (100 мл) добавляют K2CO3 (12.8 г, 0.093 мол) этилбромацетат (4.7 г, 0.031 мол), перемешивают при кипении в течение 3 часов, затем отфильтровывают осадок, промывают этанолом (50 мл), фильтрат концентрируют в вакууме.
Выход: [5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-уксусной кислоты этиловый эфир (около 12 г, 100%).
Пример 4
Получение [5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]уксусная кислоты
К раствору этилового эфира [5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]уксусной кислоты (12 г, 0.031 мол) в этаноле (100 мл) добавляют NaOH (2.48 г, 0.062 мол) и воду (20 мл). Смесь перемешивают в течение 3 часов при температуре 25°C, затем реакционную смесь нейтрализуют (pH=5-6) лимонной кислотой (12.5 г, 0.065 моль) до pH=5, выпавший осадок отфильтровали, промывают водой, сушат на воздухе.
Выход: [5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]уксусную кислоту (около 10 г, 89.8%).
Пример 5
Получение 2-[5-(2-Хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N(3,5-ди-метилфенил)ацетамида
Способ 1
В реакционный сосуд загружают раствор[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]уксусной кислоты (10.0 г, 0.028 мол) в ДМФА (100 мл), диизопропиламин (5.7 г, 0.056 мол), 3,5-диметиланилин (4.06 г, 0.033 мол) и HATU (1-[бис-(диметиламино)метилен]-1H-1,2,3-триазоло[4,5-b]пиридиниум 3-оксид гексафторфосфонат) (12.76 г, 0.335 моль) и перемешивают в течение 16 часов при комнатной температуре, затем выливают в воду, отфильтровывают технический продукт, который очищают хроматографически ("Biotag", элюент смесь петролейного эфира: AcOEt=10:90).
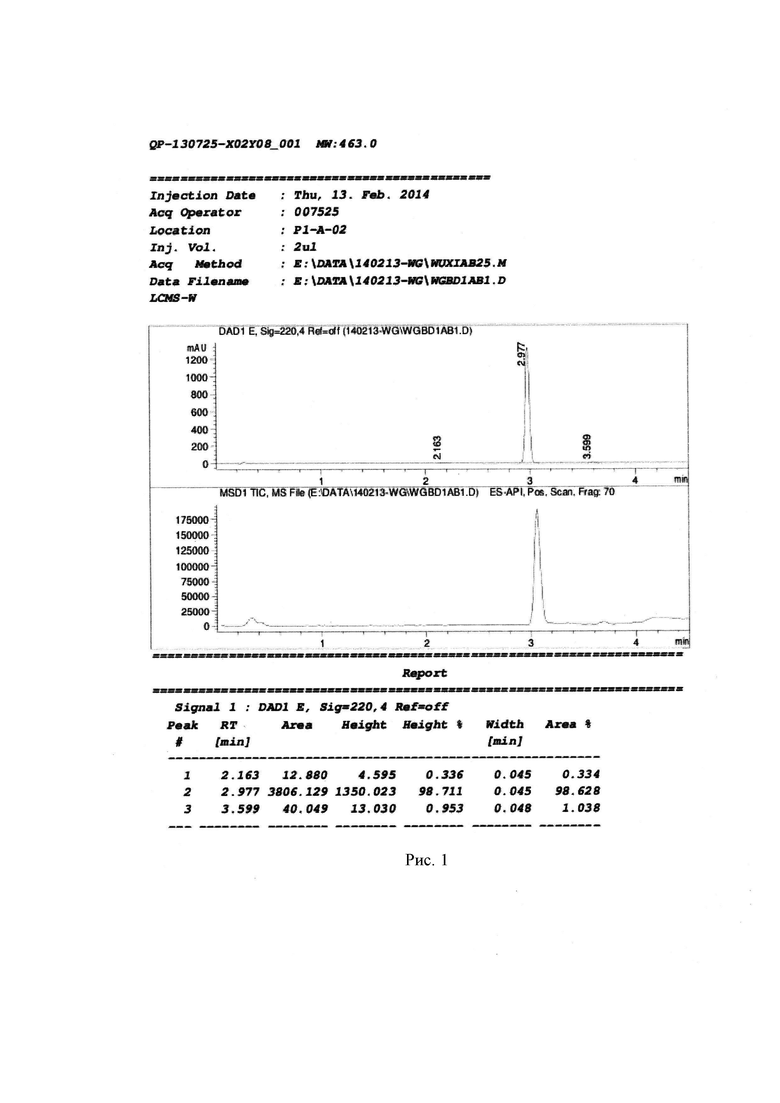
Выход: 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид (около 8 г, 62%), бесцветные кристаллы LC-MS [M+1]=463. (см. Рисунок 1)
Способ 2
Пример 6
Получение гидрохлорида 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметил-фенил)ацетамида
2[5-(2-Хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметил-фенил)ацетамид в количестве 100 ммоль прибавляют к уксусной кислоте (1 мл) и нагревают до кипения. В полученный раствор пропускают ток сухого хлористого водорода в течении 10 минут. Реакционную массу охлаждают до комнатной температуры, выпавший осадок гидрохлорида отфильтровывают.
Пример 7. Исследование противовирусной активности и цитотоксичности 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметил-фенил)ацетамида
Изучение противовирусной активности и цитотоксичности 2-[5-(2-хлор-4-метилфенил)-4-фенил-4H-[1,2,4]триазол-3-илмеркапто]-N-(3,5-диметилфенил)-ацетамида проводили на модели гриппозной инфекции в клеточной культуре в отношении вируса гриппа.
Условия и порядок проведения испытаний:
Вирусы. Для исследования использовали A/FM/1/47 H1N1, приобретенный у American Type Culture Collection (АТСС). Маточный раствор вирусов получали при сборе надосадочной жидкости в среде с зараженными клетками. Клетки разрушали, после чего обломки осаждали при центрифугировании (2000 об/мин при 4°C). Маточный раствор с высоким титром вируса хранили при -80°C до дня проведения эксперимента. В день исследования отбирали аликвоту маточного раствора, оттаивали и использовали в эксперименте.
Клетки. Клетки для исследования были получены из оригинальной коллекции АТСС. Культуры хранили и использовали в виде монослоев в имеющейся в наличии культуральной лабораторной посуде. Перед исследованием проверяли целостность клеток.
Измерение противовирусной активности.
Клетки помещали в 96-ти луночный планшет и оставляли на ночь при 37°C и 5% CO2, после чего вереду каждой из лунок добавляли аликвоту вируса (в количестве, необходимом для 80-95% гибели клеток) и свежую среду с исследуемым соединением. Контрольное соединение исследовалось аналогично. Полученную культуру клеток хранили 3-4 дня при 37°C и 5% CO2, пока вирусная инфекция в контроле с ДМСО не достигнет значительного уровня цитопатогенного эффекта. Далее число выживших клеток оценивали при помощи красителя Alamar Blue.
Измерение цитотоксичности
Цитотоксичность измерялась параллельно противовирусной активности. Порядок проведения эксперимента аналогичен методике исследования противовирусной активности за исключением этапа добавления вируса к клеткам. Материалы. Культура клеток MDCK (АТСС CCL-34), вирус гриппа A/FM/1/47 H1N1 (АТСС VR-97), Alamar Blue.
Эффективность и цитотоксичность выражали в процентах цитопатогенного эффекта и жизнеспособности клеток и рассчитывали следующим образом:
% ингибирования цитопатогенного эффекта = (ODT-ODV)/(ODC-ODV)×100%
% цитотоксичности = (1-ODT/ODC)×100%
% выживших клеток = (ODT/ODC)×100%
ODT, ODV и ODC - оптическая плотность исследуемого образца, вирусного контроля и клеточного контроля.
Значение концентрации вещества, при которой наблюдается ингибирование вируса гриппа на 50% в клеточной культуре (ЕС 50) и концентрации вещества, которая вызывает гибель половины клеток в культуре (СС50) рассчитывали по экспериментальным графикам доза-эффект при помощи программного обеспечения XLfit. Терапевтический индекс (ТИ) рассчитывали как отношение СС50 к ЕС50.
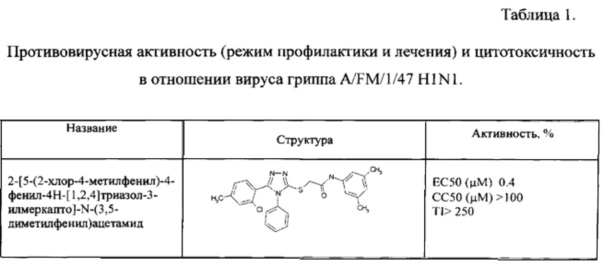
Противовирусная активность соединения по формуле I в отношении различных штаммов вируса гриппа.
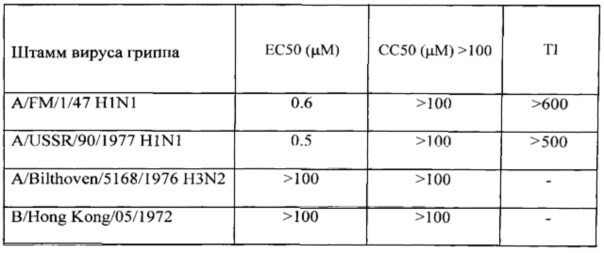
Исследование фармакологической активности in vivo
Цель испытаний: оценка эффективности субстанций I в отношении вируса гриппа in vivo.
Объем испытаний: изучение эффективности I в отношении вируса гриппа A(H3N2). Условия и порядок проведения испытаний:
Оценка биологических свойств возбудителя гриппа A. Биологическую активность оценивали титрованием вируссодержащей суспензии в РКЭ (lg ЭИД50/мл), реакции гемагглютинации и на белых мышах массой 10 г при интраназальном инфицировании (lg ЛД50).
Оценка противовирусной эффективности. Изучение противовирусной активности ряда производных в отношении вируса гриппа А проводили на белых мышах. Основным критерием оценки эффективности препаратов in vivo являются защита инфицированных лабораторных животных от гибели и показатель среднего времени жизни (КЗ, процент и Δ, дни).
Приготовление и паспортизация инфицирующих препаратов вируса гриппа A (H3N2)
Культуру вируса гриппа, штамм A/Aichi/02/68(H3N2) разводили на физиологическом растворе, содержащем по 100 ед./мл антибиотиков (пенициллина и стрептомицина), до рабочих концентраций инфицирующих препаратов. Над воздушной камерой пробивали отверстие и вводили по 0.1 мл рабочего разведения культуры возбудителя в аллантоисную жидкость. Отверстие заклеивали парафином и инкубировали РКЭ при (37.0±0,5)°C в течение 48 ч. По окончании инкубации стерильно отбирали аллантоисную жидкость. Уровень накопления вируса оценивали титрованием на РКЭ (по накоплению гемагглютинина), в культуре клеток MDCK по ЦПД. Наличие посторонней микрофлоры в приготовленных препаратах оценивали посевом 10-кратного разведения на универсальную селективную среду - тиогликолевую.
Посторонняя микрофлора в инфицирующем препарате не выявлена. Препарат удовлетворял регламентирующим требованиям для проведения научно-исследовательских работ.
Схема лечения
Изучение эффективности исследуемых препаратов проводили в отношении экспериментальной гриппозной инфекции A/H3N2 на белых мышах, интраназально инфицированных вирусом гриппа, штамм A/Aichi/02/68, в дозе 10ЛД50. Соединение вводили перорально через 1-2 часа после инфицирования и далее ежедневно в течение 6 суток, изучение эффективности профилактического действия препаратов. При исследовании действия препаратов по схеме лечения соединения вводятся через 24 часа после заражения и далее в течение 5 суток. В качестве препаратов сравнения были использованы лекарственные средства, эффективные в отношении гриппа A/H3N2. Лабораторные животные.
Для моделирования экспериментальной формы гриппа A использовали белых мышей массой 10-12 г.
Вирус
В работе использовали штамм вирус гриппа A/Aichi/02/68(H3N2).
В ходе исследования эффективности действия в модели гриппозной пневмонии на белых мышах в отношении вируса гриппа A/Aichi/02/68 H3N2 оценивали защиту от гибели, среднее время продолжительности жизни (СВЖ) и увеличение СВЖ (Д). Результаты исследования представлены в таблице.
Изучение эффективности химиопрепаратов в отношении экспериментальной гриппозной инфекции у белых мышей, интраназально инфицированных вирусом гриппа, штамм A/Aichi/02/68 H3N2 в дозе 10 ЛД50 при применении по схеме экстренной профилактики.

Пример 8
Композиции настоящего изобретения могут быть использованы в виде фармацевтических препаратов (например, в твердой, полутвердой или жидкой формах), содержащих предлагаемые в настоящем изобретении соединения в качестве активных ингредиентов в смеси с органическим или неорганическим носителем или наполнителем, приемлемым для внутримышечного, внутривенного, перорального и сублингвального введения. Активный ингредиент может быть включен в композицию вместе с обычно используемыми нетоксичными, фармацевтически приемлемыми носителями, пригодными для изготовления растворов, таблеток, пилюль, капсул, суппозиториев, капель и любых других лекарственных форм. В качестве носителей могут быть использованы вода, глюкоза, лактоза, аравийская камедь, желатин, крахмал, триксилит магния, тальк, кукурузный крахмал, мочевина, полиэтиленгликоль и другие носители, пригодные для изготовления твердых, мягких или жидких препаратов. При этом в качестве добавок могут быть использованы стабилизаторы, загустители, красители и отдушки.
Активное действующее соединение общей формулы I вводят в композицию в количестве, достаточном для получения нужного вирулицидного эффекта. При изготовлении разовой лекарственной формы количество активного ингредиента, используемого в комбинации с носителем, может варьировать в зависимости от реципиента, подвергающегося лечению, от конкретного способа введения лекарственного средства.
Так, например, при использовании соединений настоящего изобретения в виде растворов для инъекций содержание действующего начала в них может составлять 0.001-1%. В качестве разбавителя вещества могут быть использованы 0.9% раствор натрия хлорида, дистиллированная вода, раствор новокаина для инъекций, раствор Рингера, раствор глюкозы и другие разбавители. При использовании соединения общей формулы (I) в виде таблеток и суппозиториев количество вещества может составлять 1.0-300 мг на единичную дозированную форму. Для таблеток и суппозиториев в качестве фармацевтического наполнителя используют любую фармацевтически пригодную основу.
Ниже приведены неограничивающие примеры лекарственных форм.
1. Таблетированная форма
Таблетированную форму получают, используя приведенные ниже ингредиенты:
Компоненты смешивают и прессуют для образования таблеток весом 300-1000 мг каждая. В виде конкретного примера приведена рецептура, использованная для получения таблетки, весом 150 мг, содержащей 50 мг активного инградиента: соединение формулы I - 50 мг, крахмал 80 мг, лактоза 10 мг, тальк 10 мг.
2. Желатиновые капсулы Состав вводимого в капсулу порошка:
Указанные выше ингредиенты смешивают и смесь вводят в твердые желатиновые капсулы в количестве 300-500 мг. В виде конкретного примера приведена рецептура, использованная для получения желатиновой капсулы весом 60 мг, содержащей 50 мг активного инградиента: соединение формулы 1-50 мг, лактоза 10 мг.
3. Раствор для инъекций
В качестве растворителя для инъекций могут быть использованы 0.9% раствор натрия хлорида, дистиллированная вода, раствор новокаина. Форма выпуска - ампулы, флаконы, шприц-тюбики. Примеры состава раствора для инъекций:
Возможно изготовление различных лекарственных форм для инъекций - стерильных растворов, стерильных порошков, таблеток. В виде конкретного примера приведена рецептура, использованная для получения инъекции, содержащей 50 мг активного инградиента: соединение формулы I - 50 мг, пропиленгликоль 100 мг, вода дистиллированная до 1 мл.
4. Суппозитории
В качестве суппозиторной основы могут быть использован:
- основы, нерастворимые в воде, - масло какао;
- основы, растворимые в воде или смешиваемые с водой, желатино-глицериновые или полиэтиленоксидные;
- комбинированные основы - мыльно-глицериновые.
Пример состава суппозитория:
Смесь тщательно перемешивают и формируют суппозитории. В виде конкретного примера приведена рецептура, использованная для получения суппозитория, содержащей 50 мг активного инградиента: соединение формулы I - 50 мг, аэросил 100 мг, ланолин 100 мг, масляная фаза 300 мг, пропиловый спирт 100 мг, масло какао 150 мг.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ ТРИАЗОЛА | 2006 |
|
RU2416605C2 |
| СОЕДИНЕНИЯ С ЛИЗОСОМОТРОПНОЙ И ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2021 |
|
RU2817947C2 |
| ПРОИЗВОДНЫЕ 1,3-ДИОКСОИНДЕНА, ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМАЯ СОЛЬ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ АНТИВИРУСНАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ИХ В КАЧЕСТВЕ АКТИВНОГО ИНГРЕДИЕНТА | 2012 |
|
RU2566761C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ РАКА И ВИРУСНЫХ ЗАБОЛЕВАНИЙ, СПОСОБ ЛЕЧЕНИЯ РАКА, СПОСОБ ЛЕЧЕНИЯ ВИРУСНЫХ ИНФЕКЦИЙ НА ЕЕ ОСНОВЕ | 1996 |
|
RU2177316C2 |
| ЗАМЕЩЕННЫЕ АРИЛСУЛЬФОНАМИДЫ КАК ПРОТИВОВИРУСНЫЕ СРЕДСТВА | 2007 |
|
RU2423352C2 |
| ВЕТЕРИНАРНЫЙ ПРОТИВОВИРУСНЫЙ ПРЕПАРАТ | 2014 |
|
RU2561674C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ (ВАРИАНТЫ), ПРОИЗВОДНЫЕ 3,5-ДИФЕНИЛ-1,2,4-ТРИАЗОЛОВ, В НЕЕ ВХОДЯЩИЕ | 1997 |
|
RU2208010C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТИВОВИРУСНОГО ПРЕПАТАТА | 2017 |
|
RU2747082C2 |
| АЦИЛИРОВАННЫЕ ГЕТЕРОАРИЛКОНДЕНСИРОВАННЫЕ ЦИКЛОАЛКЕНИЛАМИНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФАРМАЦЕВТИЧЕСКИХ СРЕДСТВ | 2003 |
|
RU2338743C2 |
| АМИДНОЕ ПРОИЗВОДНОЕ | 2004 |
|
RU2336273C2 |
Изобретение относится к 2-[5-(2-хлор-4-метилфенил)-4-фенил-4Н-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамиду, имеющему структурную формулу (I):
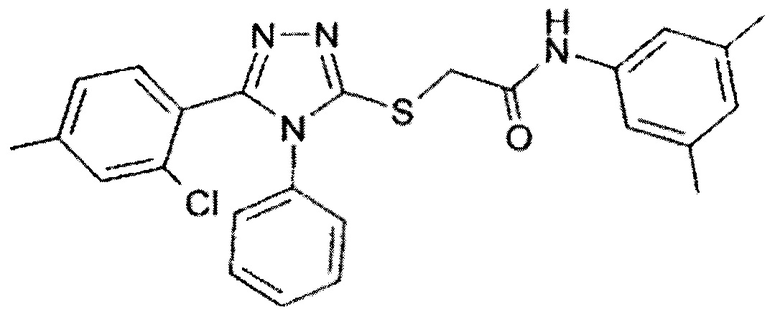 .
.
Изобретение также относится к применениям соединения, к фармацевтической композиции, к лекарственной форме, к способу профилактики или лечения гриппа. Технический результат: получено новое соединение, обладающее избирательной противовирусной активностью в отношении штаммов гриппа A. 9 н. и 1 з.п. ф-лы, 1 ил., 1 табл., 8 пр.
1. 2-[5-(2-хлор-4-метилфенил)-4-фенил-4Н-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид, имеющий структурную формулу (I):
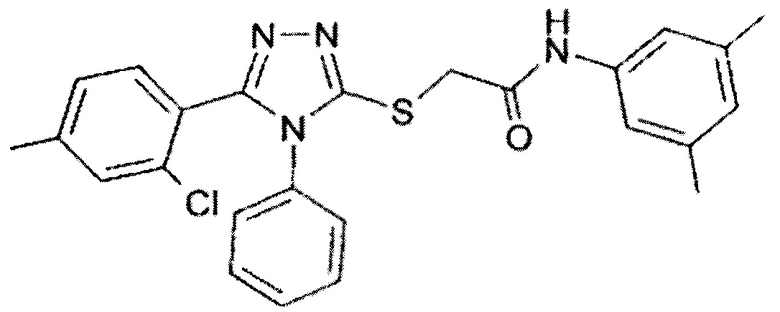
2. Применение 2-[5-(2-хлор-4-метилфенил)-4-фенил-4Н-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида, имеющего структурную формулу (I), для профилактики или лечения гриппа.
3. Фармацевтическая композиция для лечения или профилактики гриппа, содержащая в качестве терапевтически активного агента 2-[5-(2-хлор-4-метилфенил)-4-фенил-4Н-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамид или его пролекарство.
4. Фармацевтическая композиция по п. 3 для профилактики или лечения гриппа.
5. Лекарственная форма для профилактики и/или лечения гриппа, полученная на основе фармацевтической композиции по любому из пп. 3-4.
6. Лекарственная форма по любому из пп. 3 и 5 в виде таблеток, пластинок, капсул, порошка, свечей, (суппозиториев) или инъекционных растворов.
7. Применение 2-[5-(2-хлор-4-метилфенил)-4-фенил-4Н-[1,2,4]тризол-3-илмеркапто]-N-(3,5-диметилфенил)ацетамида, имеющего структурную формулу (I), для профилактики или лечения заболеваний, вызванных вирусом гриппа типа А, в том числе A/H1N1, A/H3N2.
8. Способ профилактики или лечения гриппа, при котором человек или иной субъект, который нуждается в лечении, принимает 2-[5-(2-хлор-4-метилфенил)-4-фенил-4Н-[1,2,4]триазол-3-илмеркапто]-]N-(3,5-диметилфенил)ацетамид, или его фармацевтически приемлемую соль, или фармацевтическую композицию, содержащую 2-[5-(2-хлор-4-метилфенил)-4-фенил-4Н-[1,2,4]триазол-3-илмеркапто]-]N-(3,5-диметилфенил)ацетамид или его фармацевтически приемлемую соль в эффективном количестве.
9. Применение соединения по п. 1 для производства лекарственного средства для лечения и/или профилактики гриппа.
10. Применение соединения по п. 1 в качестве сырья для производства лекарственного средства для лечения и/или профилактики гриппа.
| Fedichev P | |||
| et al | |||
| "Structure-based drug design of a new chemical class of small molecules active against influenza A nucleoprotein in vitro and in vivo" PLOS Currents Influenza, vol.3 | |||
| Цеповая молотилка | 1927 |
|
SU9478A1 |
| WO 2012108794 A2, 16.08.2012 | |||
| WO 2005097758 A1, 20.10.2005 | |||
| WO 2013142346 A1, 26.09.2013. | |||
Авторы
Даты
2017-07-21—Публикация
2014-04-28—Подача