Изобретение относится к области органической химии, а именно к способу получения новых индивидуальных соединений класса пирроло[1,2-а]пиразинов, которые могут быть использованы в качестве исходных продуктов для синтеза новых гетероциклических систем и в фармакологии.
Известен способ синтеза структурных аналогов заявленных соединений - (E)-8а-алкокси-2-арил-8-[арил(гидрокси)метилен]тетрагидропирроло[1,2-а]пиразин-1,6,7(2H)-трионы, являющихся продуктами взаимодействия 2-арил-8-ароил-3,4-дигидропирроло[1,2-a]пиразин-1,6,7(2H)-трионов со спиртами, образующиеся в условиях solvent free (в отсутствие растворителя) по следующей схеме (Червяков А.В., Масливец А.Н. ЖОрХ. 2013, 49, 1259):
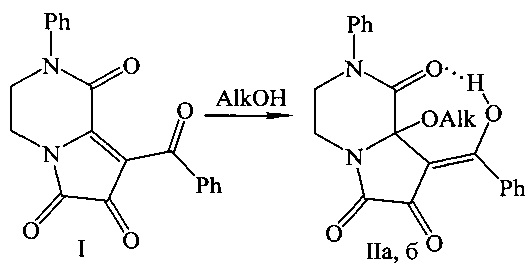
I, II Alk=Me (a), Et (б).
К недостаткам данного способа относится невозможность получения (E)-2-арил-8-[арил(гидрокси)метилен]-8а-гидрокситетрагидропирроло[1,2-а]пиразин-1,6,7(2H)-трионов в отсутствии органического растворителя.
Задачей изобретения является разработка простого способа синтеза неописанных в литературе (E)-2-арил-8-[арил(гидрокси)метилен]-8а-гидрокситетрагидропирроло[1,2-a]пиразин-1,6,7(2H)-трионов и расширение арсенала средств воздействия на живой организм.
Поставленная задача осуществляется путем взаимодействия 2-арил-8-ароил-3,4-дигидропирроло[1,2-а]пиразин-1,6,7(2H)-трионов (Ia-в) с водой в соотношении 1:1 в среде растворителя с последующим выделением целевых продуктов, по следующей схеме:
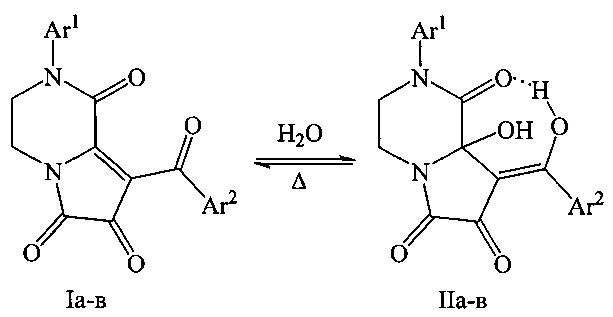
I, II: Ar1=Ar2=Ph (а); Ar1=С6Н4Ме-4, Ar2=Ph (б); Ar1=Ph, Ar2=C6H4Cl-4 (в).
Процесс ведут при температуре 20-25°С, а в качестве растворителя используют толуол либо другие инертные апротонные растворители.
Из патентной и технической литературы не были выявлены способы получения (E)-2-арил-8-[арил(гидрокси)метилен]-8а-гидрокситетрагидропирроло[1,2-а]пиразин-1,6,7(2H)-трионов, имеющие сходные признаки с заявляемым способом, а именно не использовались растворители, в которых проходит реакция, и интервал температур, на основании чего можно сделать вывод о соответствии заявленного технического решения критерию «новизна» и «изобретательский уровень».
Изобретение иллюстрируется следующими примерами.
Пример 1. (Е)-8а-Гидрокси-8-(гидрокси(фенил)метилен)-2-фенилтетрагидропирроло[1,2-а]пиразин-1,6,7(2H)-трион (IIa).
В вакуумный эксикатор поместили стакан с раствором 0,5 г (1.4 ммоль) пирролопиразинтриона (Iа) в 20 мл толуола и стакан с 50 мл нагретой до кипения воды. Воздух из вакуумного эксикатора откачивали, через 12 часов сухой остаток извлекали, высушивали под вакуумом. Выход 95%, т.пл. 147-149°С (разл., толуол). Соединение (IIa) C20H16N2O5
Найдено, %: С 65.80; Н 4.38; N 7.80.
Вычислено, %: С 65.93; Н 4.43; N 7.69.
Соединение (IIa) - светло-желтое кристаллическое вещество, плавящееся с разложением, легкорастворимое в ДМФА, ДМСО, труднорастворимое в хлороформе, бензоле, толуоле, нерастворимое в воде и алканах, дает положительную реакцию (вишневое окрашивание) на наличие енольного гидроксила со спиртовым раствором хлорида железа (III). Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIa), записанном в виде пасты в перфторированном вазелиновом масле, присутствуют полосы валентных колебаний спиртовой группы С8а-ОН в виде узкого пика при 3290 см-1, енольной группы С8=С(Ar)-ОН, участвующей в образовании ВВС, в виде широкого пика при 3078 см-1, карбонильных групп С6=O, С7=O пирролдионового цикла при 1723 см-1 и при 1698 см-1 соответственно и лактамной карбонильной группы С1=O (1603 см-1), участвующей в образовании ВВС.
В спектре ЯМР 1Н соединения (IIa), записанном в растворе в ДМСО-d6, кроме сигналов ароматических протонов присутствуют два дуплета дуплетов четырех протонов двух метиленовых групп при 3.90 м.д. и 4.11 м.д., уширенный синглет протона спиртовой группы C8a-OH при 7.35 м.д. Сигнал енольной группы C8=C(Ar)-OH, участвующей в образовании ВВС, сильно уширен (9-13 м.д.) и в спектре не наблюдается.
Пример 2. (Е)-8а-Гидрокси-8-(гидрокси(фенил)метилен)-2-(п-толил)тетрагидропирроло[1,2-а]пиразин-1,6,7(2H)-трион (IIб).
В вакуумный эксикатор поместили стакан с раствором 0,5 г (1.3 ммоль) пирролопиразинтриона (Iб) в 25 мл толуола и стакан с 50 мл нагретой до кипения воды. Воздух из вакуумного эксикатора откачивали, через 12 часов сухой остаток извлекали, высушивали под вакуумом. Выход 93%, т.пл. 149-151°С (разл., толуол). Соединение (IIб) C21H18N2O5⋅2H2O
Найдено, %: С 60.88; Н 5.39; N 6.61.
Вычислено, %: С 60.86; Н 5.35; N 6.76.
Соединение (IIб) - светло-желтое кристаллическое, вещество, плавящееся с разложением, легкорастворимое в ДМФА, ДМСО, труднорастворимое в хлороформе, бензоле, толуоле, нерастворимое в воде и алканах, дает положительную реакцию (вишневое окрашивание) на наличие енольного гидроксила со спиртовым раствором хлорида железа (III). Устойчиво при хранении в обычных условиях.
В ИК спектре соединения (IIб), записанном в виде пасты в перфторированном вазелиновом масле, присутствуют полосы валентных колебаний спиртовой группы С8а-ОН, енольной группы С8=С(Ar)-ОН, участвующей в образовании ВВС и сольватной воды в виде ряда пиков в области 3450-3050 см-1, карбонильных групп С6=O, С7=O пирролдионового цикла при 1720 см-1 и при 1698 см-1 соответственно, и лактамной карбонильной группы С1=O (1585 см-1), участвующей в образовании ВВС.
В спектре ЯМР 1Н соединения (IIб), записанном в растворе в CDCl3, кроме сигналов ароматических протонов присутствуют синглет трех протонов метальной группы при 2.33 м.д., два дуплета дуплетов четырех протонов двух метиленовых групп при 4.02 м.д. и 4.10 м.д., уширенный синглет протона спиртовой группы С8а-ОН при 7.31 м.д. Сигнал енольной группы С8=С(Ar)-ОН, участвующей в образовании ВВС, сильно уширен (9-13 м.д.) и в спектре не наблюдается.
Пример 3. Фармакологическое исследование соединений (IIa-в) на наличие анальгетической активности.
Оценку анальгетических свойств соединений (IIa-в) изучали на беспородных мышах (самках) массой 18-22 грамм методом термического раздражения «горячая пластинка» по Эдди и Леймбах (Eddy N.B., Leimbarh D.J- Pharmacol and Exper. Gher., 1953, 385-393). В качестве препарата сравнения использовали анальгин (М.Д. Машковский, «Лекарственные средства», т. 1, стр. 184, М., Медицина, 1978).
Проведенные исследования показали (см. табл.), что соединения (IIa-в) обладает анальгетической активностью. Данные о фармакологической активности аналогов заявляемых соединений в доступной литературе отсутствуют.
Предлагаемый способ прост в осуществлении, одностадиен и позволяет получить неописанные в литературе (Е)-2-арил-8-[арил(гидрокси)метилен]-8а-гидрокситетрагидропирроло[1,2-а]пиразин-1,6,7(2Н)-трионы (IIa-в) с хорошими выходами, которые могут найти применение в качестве исходных продуктов для синтеза гетероциклических систем и в фармакологии в качестве потенциальных лекарственных средств.
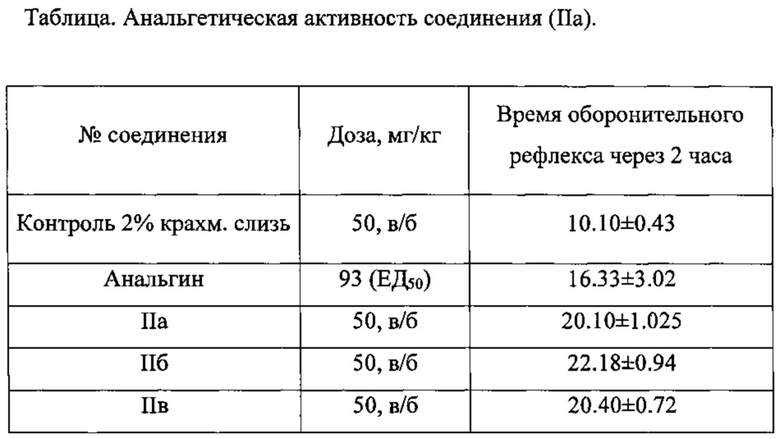
Изобретение относится к области органической химии, а именно к способу получения (E)-2-арил-8-[арил(гидрокси)метилен]-8а-гидрокситетрагидропирроло[1,2-a]пиразин-1,6,7(2H)-трионов указанной ниже формулы, где Ar1=Ph, С6Н5Ме-4; Ar2=Ph, C6H5Cl-4, отличающийся тем, что 2-арил-8-ароил-3,4-дигидропирроло[1,2-a]пиразин-1,6,7(2H)-трионы подвергают взаимодействию с водой в соотношении 1:1 в среде инертного апротонного растворителя с последующим выделением целевых продуктов. Технический результат: разработан способ получения соединений, которые могут быть использованы в качестве исходных продуктов для синтеза гетероциклических систем и в фармакологии как обладающие анальгетической активностью. 2 з.п. ф-лы, 1 табл., 3 пр.
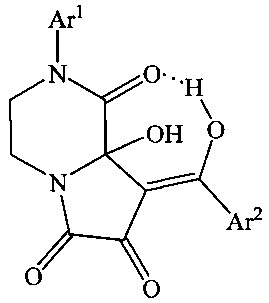
1. Способ получения (E)-2-арил-8-[арил(гидрокси)метилен]-8а-гидрокситетрагидропирроло[1,2-a]пиразин-1,6,7(2H)-трионов общей формулы
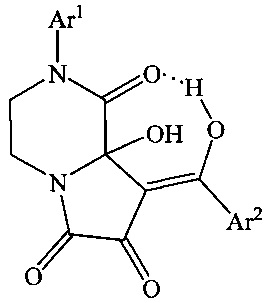
где Ar1=Ph, С6Н5Ме-4; Ar2=Ph, C6H5Cl-4, отличающийся тем, что 2-арил-8-ароил-3,4-дигидропирроло[1,2-a]пиразин-1,6,7(2H)-трионы подвергают взаимодействию с водой в соотношении 1:1 в среде инертного апротонного растворителя с последующим выделением целевых продуктов.
2. Способ по п.1, отличающийся тем, что процесс ведут при температуре 20-25°C.
3. Способ по п.1 или 2, отличающийся тем, что в качестве растворителя используют абсолютный толуол.
| Chervyakov, A | |||
| V | |||
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
Авторы
Даты
2017-08-04—Публикация
2016-05-25—Подача