Область техники, к которой относится изобретение
Изобретение относится к области химико-фармацевтической промышленности и касается фармацевтической композиции, обладающей противотуберкулезной активностью, выполненной в виде твердой пероральной лекарственной формы, которая содержит в качестве действующего начала тиоацетазон в терапевтически эффективном и безопасном количестве и по меньшей мере один фармацевтически приемлемый наполнитель, относящийся к классу углеводов. Фармацевтическая композиция характеризуется высокой терапевтической эффективностью и биодоступностью.
Уровень техники
Эпидемиологические показатели по туберкулезу в мире, несмотря на значительные успехи, достигнутые в последние десятилетия, неоднородны, в некоторых странах показатели заболеваемости и смертности туберкулезом остаются на достаточно высоком уровне. Наряду с этим серьезной проблемой является лекарственная устойчивость микобактерий туберкулеза (далее по тексту МБТ) к противотуберкулезным препаратам.
Высокая частота встречаемости штаммов МБТ с лекарственной устойчивостью в первую очередь связана с тем, что в мире существует достаточно немного противотуберкулезных препаратов, причем практически все они начали применяться более 40 лет назад. Лечение больных, у которых выявлены МБТ с широкой лекарственной устойчивостью, крайне сложный, а порой и безнадежный процесс и включает в себя использование разнообразных схем лекарственной комбинированной терапии, включающей прием по 5-6 препаратов.
Революцией в лечении туберкулеза с широкой лекарственной устойчивостью явилось выведение на фармацевтический рынок компанией ОАО «Фармасинтез» нового лекарственного препарата «Перхлозон®» (RU 2423977), который в качестве активного вещества содержит 4-тиоуреидоиминометилпиридиния перхлорат (см. структурную формулу ниже).
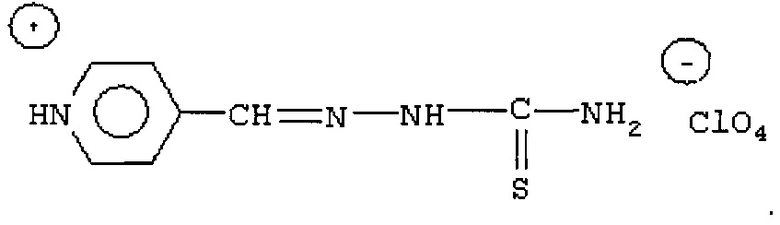
Перхлозон позволил снизить смертность больных туберкулезом, у которых выявлены МБТ с широкой лекарственной устойчивостью.
Однако по прежнему существует необходимость в разработке лекарственных препаратов от туберкулеза с различными видами лекарственной устойчивости.
Тиоацетазон (N-[4-[[(Аминотиоксометил)гидразино]метил]фенил]ацетамид) - противотуберкулезный препарат (см. структурную формулу ниже), полученный в середине 40-х годов 20 века (Domagk et. al., Naturwiss 33, 315 (1946)). Активен в отношении микобактерий туберкулеза и возбудителя лепры.
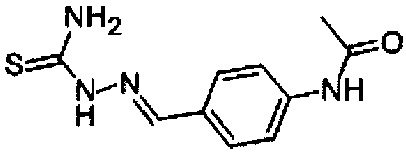
Тиоацетазон показал большую эффективность при лечении больных туберкулезом, у которых появилась устойчивость МБТ к препарату изониазид, являющегося препаратом первой линии лечения туберкулеза и используемого практически всеми больными туберкулеза (Tuberculosis, 1963, 44, 4, 393-416).
Также тиоацетазон in vitro очень эффективен против туберкулеза, в том числе туберкулеза с лекарственной устойчивостью, в сочетании с изониазидом, фтивазидом, стрептомицином, ПАСКом и многими другими противотуберкулезными препаратами.
В недавно завершившемся исследовании, тиоацетазон показал схожий спектр активности и механизм действия, что и перхлозон (International Journal of Antimicrobial Agents, 2015, 45, 4, 430-433). Таким образом, тиоацетазон является очень перспективным лекарственным средством для лечения туберкулеза, особенно туберкулеза с различной лекарственной устойчивостью.
Однако основными препятствиями для широкого применения тиоацетазона являются его крайне низкая растворимость в воде и многих органических растворителях.
Низкая растворимость тиоацетазона обуславливает его крайне низкую биодоступность при приеме, в том числе при пероральном приеме, например в виде водной суспензии порошка тиоацетазона. Водная суспензия тиоацетазона готовится непосредственно перед приемом посредством смешения порошка тиоацетазона с водой. Для улучшения стабильности водной суспензии тиоацетазона могут использовать добавки 2,5% аравийской камеди и 0,1% Твин 80 (Antimicrob Agent Chemother 2003, 47, 8, p.p. 2685-2687) - прототип изобретения.
Ввиду низкой биодоступности тиоацетазона, для достижения положительного терапевтического эффекта больным туберкулезом приходилось принимать тиоацетазон перорально в виде водной суспензии в высоких дозах по 300-400 мг в день. Но действие таких высоких доз достаточно токсичного препарата негативно сказывалось на больных и приводило к быстрому развитию тяжелых побочных эффектов, таких как анорексия, гепатит, эксфолиативный дерматит. По настоящий момент на российском рынке не представлено каких-либо лекарственных форм тиоацетазона, также неизвестны какие-либо твердые пероральные формы тиоацетазона.
В то же время известна композиция изониазида, в которой дополнительным активным веществом является тиоацетазон (National Formulary in India, 4th edition, 2011). Известные композиции изониазида и тиоацетазона имеют следующие составы:
- тиоацетазон 37,5 мг, изониазид 750 мг, крахмал картофельный 20 мг, магния стеарат 4,5 мг, стеариновая кислота 4 мг, диоксид кремния 4 мг;
- тиоацетазон 150 мг, изониазид 300 мг, крахмал картофельный 40 мг, магния стеарат 9 мг, стеариновая кислота 7 мг, диоксид кремния 9 мг.
В вышеприведенных составах изониазида и тиоацетазона не решается проблема с плохой биодоступностью тиоацетазона. Как определили авторы настоящего изобретения, при дозе тиоацетазона 150 мг Cmax тиоацетазона в крови составляет для данных составов около 1,8-2,0 мкг/мл, Tmax составляет около 5-5,5 часов.
Предпринимались попытки перевода тиоацетазона в растворимую форму. Так был получен тиоацетазон растворимый - бензальтиосемикарбазон пара-аминометиленсульфоната натрия моногидрат (см. структурную формулу ниже), известный под торговым наименованием «Солютизон» (Машковский М.Д., Лекарственные средства, 1964 г., с. 186).

Солютизон не нашел применения при пероральном применении, поскольку в условиях человеческого организма при пероральном приеме мгновенно переходил в малорастворимый тиоацетазон. Поэтому солютизон используют только в виде водного раствора при ингаляциях и посредством интратрахеального и внутрибронхиального введения. Однако неудобная форма для приема, а также сильные побочные эффекты со стороны органов дыхательной системы (Машковский М.Д., Лекарственные средства, 1964 г., с. 186), привели к снятию данного препарата с производства.
По вышеописанным причинам необходимо признать, что потенциал тиоацетазона, как противотуберкулезного препарата, остался нереализован, поскольку не удалось получить приемлемую лекарственную форму для его использования, которая характеризовалась бы хорошей эффективностью, биодоступностью и безопасностью.
Поскольку каждое биологически активное лекарственное вещество при создании его лекарственной формы требует индивидуальных вспомогательных веществ с определенным содержанием, то для создания лекарственной формы, которая обеспечит быстрое высвобождение и сохранение высокой активности действующего вещества и снижение побочных действий, оказываемых лекарственным препаратом и содержащимися в нем примесями, то в данном изобретении авторами была поставлена следующая задача: разработка новых и более эффективных композиций тиоацетазона для лечения туберкулеза, которые обладают высокой растворимостью, биодоступностью, а также высоким клиническим эффектом (в сравнении с прототипом).
Достигаемый технический результат предлагаемого изобретения соответствует поставленным задачам и заключается в расширении арсенала качественных доступных отечественных лекарственных средств для лечения туберкулеза, обладающих улучшенной кинетикой растворения, повышенной биологической доступностью, а также несколько большим клиническим эффектом по сравнению с лекарственным препаратом по прототипу. Полученные технические результаты не являются очевидными, и их нельзя было предвидеть специалисту на основании имеющегося уровня техники.
Раскрытие изобретения
Поставленные задачи решаются тем, что предлагаемая фармацевтическая композиция с противотуберкулезным действием включает тиоацетазон и по меньшей мере один фармацевтически приемлемый наполнитель, относящийся к классу углеводов, при следующем массовом соотношении, % от массы композиции:
Тиоацетазон - 12,0-60,0;
По меньшей мере один фармацевтически приемлемый наполнитель, относящийся к классу углеводов - 40,0-88,0.
В одном из вариантов осуществления изобретения фармацевтическая композиция с противотуберкулезным действием включает тиоацетазон и по меньшей мере один фармацевтически приемлемый наполнитель, относящийся к классу углеводов, при следующем массовом соотношении, % от массы композиции:
Тиоацетазон - 20,0-35,0;
По меньшей мере один фармацевтически приемлемый наполнитель, относящийся к классу углеводов - 65,0-80,0.
В предпочтительном варианте осуществления изобретения фармацевтическая композиция с противотуберкулезным действием включает тиоацетазон и по меньшей мере один фармацевтически приемлемый наполнитель, относящийся к классу углеводов, при следующем массовом соотношении, % от массы композиции:
Тиоацетазон - 24,0-28,0;
По меньшей мере один фармацевтически приемлемый наполнитель, относящийся к классу углеводов - 72,0-76,0.
Под термином «фармацевтически приемлемый наполнитель, относящийся к классу углеводов» понимаются известные фармацевтически приемлемые наполнители, в том числе раскрытые в "Handbook of Pharmaceutical Excipients" 7th edition, London: Pharmaceutical Press 2012, которые относятся к моносахарам (например, глюкоза, фруктоза), олигосахарам (например, лактоза, сахароза, циклодектрины), полисахарам (например, крахмал, камеди, микрокристаллическая целлюлоза), а также к их производным (например, натрия карбоксиметилцеллюлоза, этилцеллюлоза, альгинат кальция, сорбит, маннит, пектин).
В предпочтительном варианте осуществления изобретения в качестве по меньшей мере одного фармацевтически приемлемого наполнителя, относящегося к классу углеводов, могут использоваться лактоза, крахмал, глюкоза, сахароза, β-циклодекстрин, микрокристаллическая целлюлоза, метилцеллюлоза, натрия карбоксиметилцеллюлоза.
В одном из вариантов осуществления изобретения фармацевтическая композиция с противотуберкулезным действием наряду с тиоацетазоном и по меньшей мере одним фармацевтически приемлемым наполнителем, относящимся к классу углеводов, может дополнительно содержать обычные фармацевтически приемлемые вспомогательные вещества, принятые в технологии приготовления лекарственных средств, такие как связующие, наполнители, консерванты, регуляторы текучести, смягчители, смачиватели, диспергаторы, эмульгаторы, растворители, антиокислители и/или пропелленты, пролонгаторы действия [Sucker et al.: Pharmazeutische Technologie, Thieme-Verlag, Stuttgard, 1991 г.].
В качестве предпочтительных фармацевтически приемлемых вспомогательных веществ могут быть использованы стеариновая кислота и ее соли, тальк, кросповидон, повидон, диоксид кремния, твины (например, твин-80), оксид магния, карбонат кальция, основный карбонат магния, фосфат кальция, желатин, каолин.
Наиболее предпочтительными вспомогательными веществами являются стеариновая кислота и ее соли, тальк и диоксид кремния.
Предпочтительно фармацевтическую композицию с противотуберкулезным действием по настоящему изобретению выполняют в форме таблетки, которая может дополнительно покрываться пленочной оболочкой. Наличие последней улучшает внешний вид и органолептические свойства лекарственной формы, защищает ее от механических повреждений.
Массовое содержание оболочки композиции обычно составляет от 0,1 до 20% от массы покрытой оболочкой композиции.
В состав оболочки могут входить различные подходящие фармацевтически приемлемые вспомогательные вещества, которые можно условно разделить на следующие группы:
1) адгезивы - сахарный сироп, ПЭГ (Макрогол), поливинилпирролидон, гидроксипропилметилцеллюлоза (гипромеллоза) и др.
2) структурные вещества - сахар, оксид магния, оксид кальция, тальк, основной карбонат магния и др.
3) пластификаторы - растительные масла, карбоксиметилцеллюлоза, твины и др.
4) гидрофобизаторы - аэросил, шеллак, полиакриловые смолы, зеин и др.
5) красители - тропеолин, тартразин, кислотный красный, индигокармин, оксиды железа и др.
6) корригенты - сахар, лимонная кислота, какао, ванилин и др.
Предпочтительно в состав оболочки фармацевтической композиции входят гипромеллоза, макрогол, тальк, железа оксид желтый, титана диоксид.
Наиболее предпочтительно, чтобы в состав оболочки входили гипромелоза и титана диоксид.
При добавлении вспомогательных веществ и/или нанесении оболочки необходимо учитывать, что массовое содержание тиоацетазона от массы композиции не должно быть менее 12%, а массовое содержание по меньшей мере одного фармацевтически приемлемого наполнителя, относящегося к классу углеводов, от массы композиции не должно быть менее 40%.
Наиболее распространенными способами получения таблеток из композиции по настоящему изобретению являются три технологические схемы: с влажным гранулированием, сухим гранулированием и прямым прессованием.
В одном из наиболее предпочтительных вариантов осуществления изобретения фармацевтическая композиция с противотуберкулезным действием включает тиоацетазон, лактозу, крахмал, тальк, кислоту стеариновую и/или ее соль при следующем массовом соотношении, % от массы композиции:
В еще одном из наиболее предпочтительных вариантов осуществления изобретения фармацевтическая композиция с противотуберкулезным действием включает тиоацетазон, крахмал, натрия карбоксиметилцеллюлозу, диоксид кремния, кислоту стеариновую и/или ее соль при следующем массовом соотношении, % от массы композиции:
Авторами настоящего изобретения установлено, что композиции по настоящему изобретению характеризуются приемлемым сроком годности (2 года).
Композиции по настоящему изобретению показали большую эффективность против МБТ в условиях in vitro, чем композиция по прототипу.
Как показали результаты токсикологического исследования, проведенного на мышах, композиции по настоящему изобретению обладают высокой безопасностью. Заявленные композиции даже с большими дозами тиоацетазона не влияют на биохимический состав крови изучаемых мышей.
Кроме того, авторами настоящего изобретения установлено, что в патентуемых композициях сохраняется высокая растворимость таблеток, при этом растворение действующего начала происходит с большей скоростью (около 80% тиоацетазона растворяется примерно за 30-40 мин, в прототипе около 70-80 мин; около 99% тиоацетазона растворяется примерно за 65-70 мин, в прототипе примерно за 100-120 мин).
Композиции по настоящему изобретению также продемонстрировали более высокие параметры биодоступности, чем композиция по прототипу.
Представленные ниже примеры иллюстрируют (без ограничения объема притязаний) наиболее предпочтительные варианты осуществления изобретения, а также подтверждают возможность получения заявляемой фармацевтической композиции и достижения указанных технических результатов.
Пример 1.
Методика получения композиций по настоящему изобретения, которые необязательно могут быть покрыты пленочной оболочкой.
Композиции по настоящему изобретению получают преимущественно влажной грануляцией. Тиоацетазон, фармацевтически приемлемые наполнители, относящиеся к классу углеводов, а также необходимые фармацевтически приемлемые вспомогательные вещества просеивают и смешивают в грануляторе. Полученную смесь увлажняют водой, перемешивают и гранулируют. Полученный гранулят сушат до остаточной влаги не более 2% при температуре 45-50°C. Сухое гранулирование ведут через сетку с диаметром отверстий 1-1,5 мм. Полученную массу таблетируют на ротационном таблеточном прессе.
Таблетки, полученные согласно вышеприведенной методике, могут быть покрыты пленочной оболочкой в установке для покрытия путем распыления водной дисперсии для пленочного покрытия при температуре 50°C до необходимого веса таблетки.
Пример 2.
Примеры композиций по настоящему изобретению.
В соответствии с методикой из примера 1 получения композиций по настоящему изобретению, были получены следующие композиции.
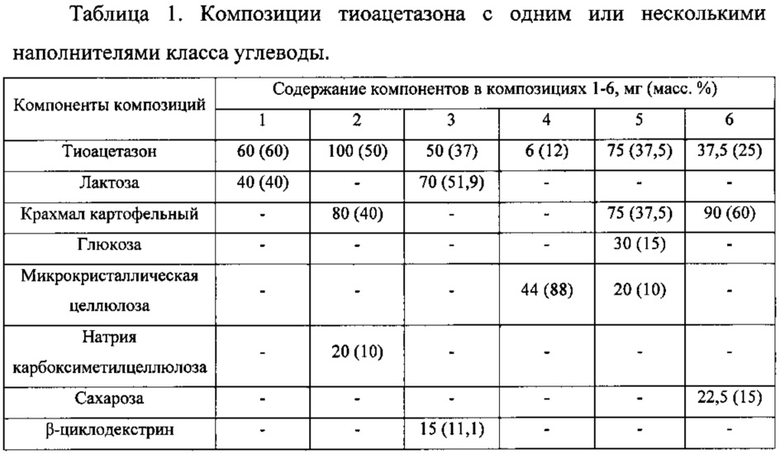
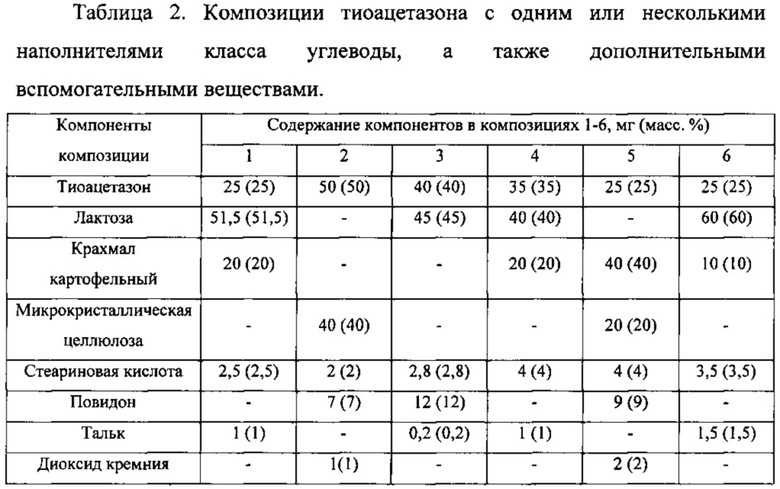
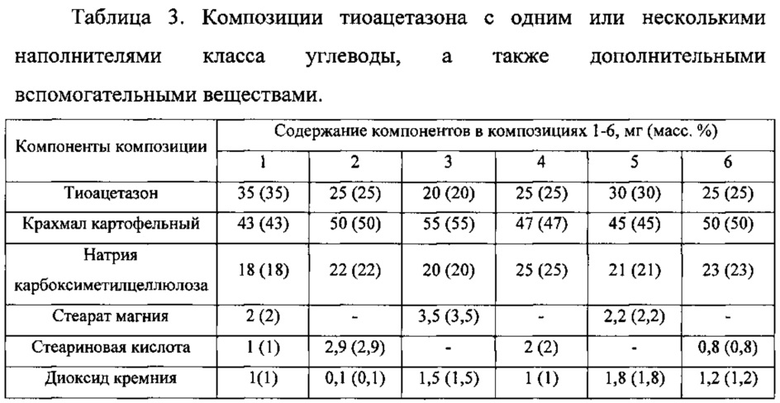
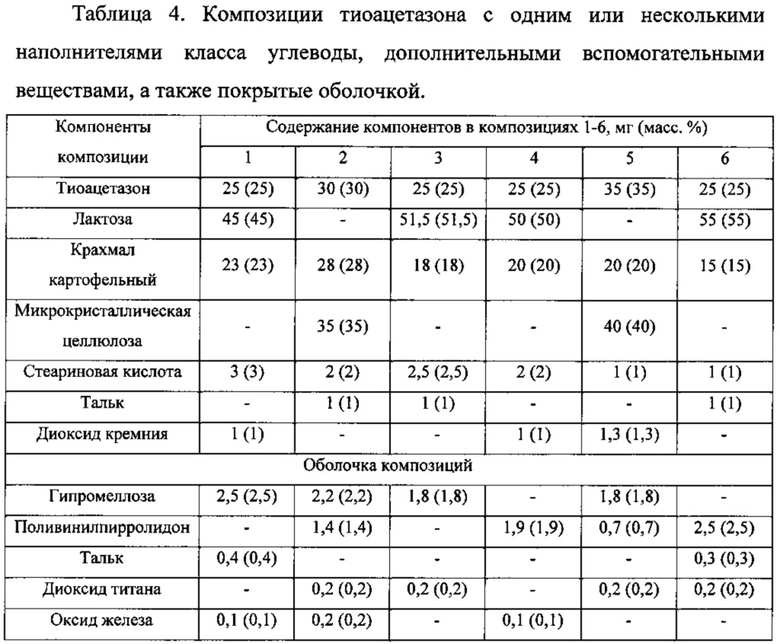
Пример 3.
Установление сроков годности композиций по настоящему изобретению.
Установление сроков годности композиций проводили методом «ускоренного старения» в двух температурных режимах при 40±2°C и 60±2°C и (ОВ) относительной влажности 75±5% в течение 6 мес., а также в естественных условиях (25±2°C и 60±5% ОВ)) («Инструкция по проведению работ с целью определения сроков годности лекарственных средств на основе метода «ускоренного старения» при повышенной температуре И 42-2-82»). В качестве опытных образцов использовали 3 серии композиций тиоацетазона, с аравийской камедью и твином 80 для приготовления суспензии (прототип) и композиций 1-6 из таблицы 1 по примеру 2, полученных в соответствии с настоящим изобретением.
О стабильности ингредиентов заявляемого фармацевтического состава и прототипов судили по содержанию посторонних примесей и количественному содержанию лекарственных веществ в испытуемых образцах. Контроль качества проводили через равные промежутки времени, эквивалентные 6 месяцам хранения. Для композиций по прототипу срок хранения составил 1,5-2 года, для таблеток в соответствии с настоящим изобретением - 3 года.
Пример 4.
Сравнение активности препарата тиоацетазон в виде порошка для приготовления суспензии (прототип) и композиции по настоящему изобретению in vitro.
Влияние препаратов тиоацетазона на рост микобактерий определялось стандартным методом двукратных серийных разведений в жидкой синтетической среде Сотона с 10% нормальной лошадиной сывороткой. Сравнивались препарат тиоацетазона для приготовления суспензии и композиции 1-6 из таблицы 1 по примеру 2. Концентрация сравниваемых препаратов составляла 1 мкг/мл. В качестве тест-штаммов in vitro были использованы лабораторные культуры МБТ, чувствительные к противотуберкулезным препаратам: М. tuberculosis H37RV и «Academia», М. bovis-bovinus 8.

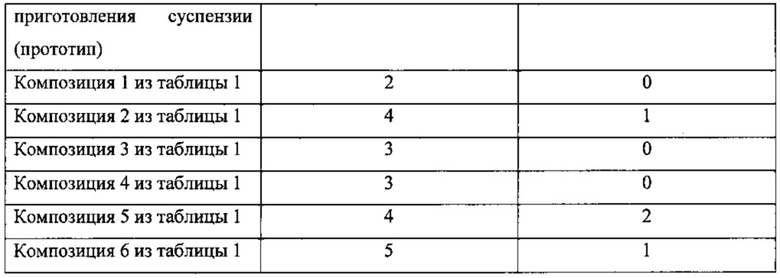
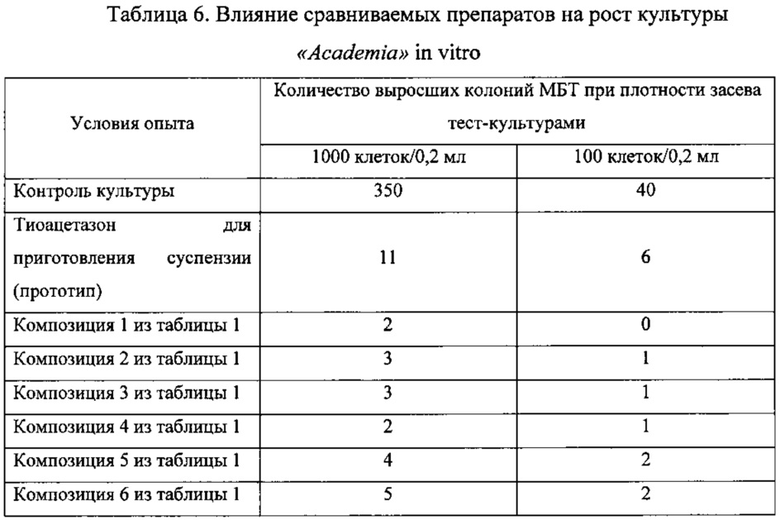

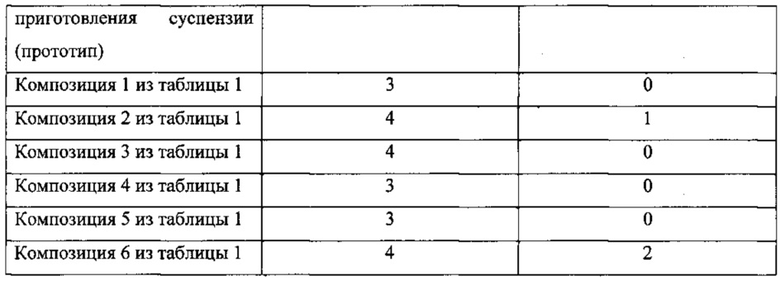
Было выявлено, что при инкубации с композицией по настоящему изобретению практически не наблюдалось роста колоний МБТ, тогда как при инкубации с препаратом по прототипу наблюдался единичный рост МБТ. Данный тест свидетельствует о большей эффективности композиции по данному изобретению в ингибировании роста МБТ, сравнению с прототипом.
Пример 5.
Исследование сравнительной кинетики растворения композиций 1-6 из таблицы 1 по примеру 2 по настоящему изобретению и тиоацетазон для приготовления суспензии (по прототипу).
Исследование проводили согласно ОФС 42-0003-04 «Растворение» на аппарате «лопастная мешалка» при скорости вращения 50 об/мин при температуре 37±0,5°C. Среда растворения - 1% раствор натрия додецилсульфата. Объем среды растворения - 600 мл. Временные точки отбора проб: 15 мин, 30 мин, 40 мин, 50 мин, 60 мин, 70 мин, 80 мин, 90 мин, 120 мин. Количественное определение высвободившегося тиоацетазона проводили методом ВЭЖХ.
Среднее количество тиоацетазона, высвободившегося из композиций по настоящему времени, составило 77,9%-81,2% через 30-40 минут и 97,1%-99,6% через 60-70 минут, 100% через 70-80 минут. Среднее количество тиоацетазона, высвободившегося из композиции для приготовления суспензии по прототипу, составило 51,03% через 30 минут, 71,05% через 60 минут, 89,6% через 90 минут, 100% через 120 минут.
Таким образом, исходя из полученных результатов видно, что фармацевтические композиции в соответствии с настоящим изобретением обладают улучшенным по сравнению с прототипом профилем высвобождения, что и позволяет достигнуть увеличения биодоступности заявленных фармацевтических композиций.
Пример 6.
Сравнение параметров биодоступности препарата тиоацетазона для приготовления суспензии (прототип) и композиций по настоящему изобретению.
Исследование параметров биологической доступности проводили на собаках самцах и самках массой примерно 11,5 кг. Все животные при проведении эксперимента получали сбалансированный кормовой рацион, содержащий 27% жира, и воду в неограниченном количестве. Каждой собаке (примерно за 30 мин до введения исследуемого средства) перорально вводили 100 мкг/кг гистамина. Каждой собаке вводили перорально тиоацетазон (композиции 1-6 из таблицы 1 по примеру 2 по настоящему изобретению, прототип - композицию тиоацетазона с аравийской камедью и твином 80 для приготовления суспензии, а также сравнительную композицию, содержащую 65% мас. тиоацетазона и 35% мас. лактозы) в дозе 50 мг (около 4,3 мг/кг). Затем вводили примерно 10 мл воды. У каждого животного до введения и через 0,25, 0,5, 1,0, 1,5, 2, 3, 3,5, 4, 4,5, 5, 5,5 6, 7 и 8 ч после введения лекарственного средства брали пробы крови.
Плазму отделяли от эритроцитов с помощью центрифугирования и до проведения анализа замораживали (-30°C). Концентрацию тиоацетазона определяли с помощью высокоэффективной жидкостной хроматографии с обращенной фазой с детектированием в коротковолновом УФ-диапазоне, а затем образцы плазмы подвергали жидкостной экстракции. Для изучения каждой дозированной формы использовали группу, содержащую 11-13 собак; приведенные значения являются средними для каждой группы собак. Дозозависимые параметры Cmax tmax для каждой дозированной формы представлены в таблице ниже.

Результаты этого исследования показали, что параметры биологической доступности фармацевтической композиции в соответствии с изобретением была выше, чем у лекарственного препарата по прототипу и композиции сравнения.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОМБИНИРОВАННОЕ ПРОТИВОТУБЕРКУЛЕЗНОЕ СРЕДСТВО И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2001 |
|
RU2182483C1 |
| ФАРМАЦЕВТИЧЕСКАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ КОМБИНИРОВАННАЯ КОМПОЗИЦИЯ | 2011 |
|
RU2478389C2 |
| СИНЕРГИЧЕСКАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ЦИКЛОСЕРИН И ЦИНКОСОДЕРЖАЩЕЕ СОЕДИНЕНИЕ | 2016 |
|
RU2620857C1 |
| КОМБИНИРОВАННЫЙ ПРОТИВОТУБЕРКУЛЕЗНЫЙ ПРЕПАРАТ | 2009 |
|
RU2430724C2 |
| КОМБИНИРОВАННАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2468802C2 |
| КОМБИНИРОВАННАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2009 |
|
RU2422145C2 |
| КОМБИНИРОВАННАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ КОМПОЗИЦИЯ | 2009 |
|
RU2413517C1 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ПРОТИВОТУБЕРКУЛЕЗНЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ И СПОСОБ ИХ ИЗГОТОВЛЕНИЯ | 2001 |
|
RU2240795C9 |
| КОМБИНИРОВАННЫЙ СОСТАВ С ПРОТИВОТУБЕРКУЛЁЗНЫМ ДЕЙСТВИЕМ | 2003 |
|
RU2247560C1 |
| КОМБИНИРОВАННАЯ ПРОТИВОТУБЕРКУЛЕЗНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2008 |
|
RU2417087C2 |
Изобретение относится к медицине, в частности к фармацевтической композиции для лечения туберкулеза, которая включает в качестве активного вещества тиоацетазон, а также лактозу, крахмал, тальк и стеариновую кислоту и/или ее соль, при определенном количественном соотношении. Осуществление изобретения позволяет получить композицию, характеризующуюся высокой растворимостью, биодоступностью и эффективностью. 8 табл., 6 пр.
Противотуберкулезная фармацевтическая композиция, включающая тиоацетазон, лактозу, крахмал, тальк, кислоту стеариновую и/или ее соль при следующем массовом соотношении, % от массы композиции:
| ТЕПЛОГЕНЕРАТОРНАЯ УСТАНОВКА | 2002 |
|
RU2234643C2 |
| WO 2007043542 A1, 19.04.2007 | |||
| US 5104875 A, 14.04.1992 | |||
| СПОСОБ ПОЛУЧЕНИЯ СОРБЕНТА ДЛЯ ОЧИСТКИ СРЕДЫ | 2007 |
|
RU2340022C1 |
Авторы
Даты
2017-08-09—Публикация
2015-10-30—Подача