УРОВЕНЬ ТЕХНИКИ
[0001] Нарушения свертываемости крови такие, как болезнь Виллебранда (БВ) и гемофилия, обычно возникают из-за нарушений в системе свертывания. "Болезнь Виллебранда" относится к группе заболеваний, вызываемых дефицитом фактора Виллебранда. Фактор Виллебранда способствует накоплению и прикреплению тромбоцитов к стенкам кровеносных сосудов, что необходимо для нормального свертывания крови. Гемофилия A обусловлена недостаточной активностью фактора VIII, в то время как гемофилия B обусловлена дефицитом фактора IX. Современное лечение данных коагулопатий включает заместительную терапию с применением фармацевтических препаратов, содержащих нормальный фактор свертывания крови.
[0002] Заместительная терапия у больных БВ и гемофилией включает многократное введение препаратов, которые содержат нормальные факторы свертывания крови, путем внутривенной инфузии, что может оказаться большой нагрузкой для жизни этих больных, в особенности, когда доступ к венам затруднен. Было бы желательно, чтобы частоту инфузий можно было уменьшить. Одной из потенциально осуществимых методик является стабилизация фактора VIII путем его ассоциации со второй молекулой такой, как фактор Виллебранда (ФВ), в результате чего увеличивается время полужизни фактора VIII в плазме крови.
[0003] ФВ является гликопротеином, циркулирующим в плазме крови в виде групп мультимеров, имеющих размеры от 500 до 20000 кДа. Была клонирована полноразмерная кДНК ФВ; полипептид соответствует аминокислотным остаткам в количестве от 23-х до 764-х полноразмерного пре-про-ФВ (Eikenboom et al (1995) Haemophilia 1, 77 90). Мультимерные формы ФВ состоят из полипептидных субъединиц размером 250 кДа, соединенных между собой дисульфидными связями. ФВ опосредует первичную адгезию тромбоцитов к субэндотелию стенки поврежденного сосуда, при этом большие мультимеры проявляют усиленную гемостатическую активность. Мультимеризированный ФВ связывает гликопротеин Gplbα с тромбоцитарной поверхностью через взаимодействие в A1 домене ФВ, обеспечивая адгезию тромбоцитов. Другие сайты ФВ опосредуют прикрепление к стенке кровеносного сосуда. Таким образом, ФВ формирует мост между тромбоцитом и стенкой сосуда, что является существенным для тромбоцитарной адгезии и первичного гемостазиса в условиях сильного гемодинамического удара. Обычно эндотелиальные клетки секретируют крупные полимерные формы ФВ, а формы ФВ, имеющие более низкий молекулярный вес, возникают при протеолитическом расщеплении. Мультимеры с исключительно высокими молекулярными массами накапливаются в тельцах Вейбеля-Палада эндотелиальных клеток и высвобождаются при стимуляции агонистами такими, как тромбин и гистамин.
[0004] То, что фармакокинетика ФVIII является функцией уровней ФВ, подтверждается несколькими предыдущими наблюдениями. Снижение связывающей активности ФVIII при болезни Виллебранда (БВ) вследствие как пониженного уровня протеинов ФВ, так и пониженной связывающей способности ФVIII, приводит к снижению уровня стационарных состояний эндогенного ФVIII (кратко изложено в Castaman et al., Disorders of Hemostasis 88(1):94-108 (2003)), а увеличение продолжительности существования ФВ было предложено в качестве практически осуществимой стратегии по увеличению стабильности ФVIII (Denis et al., Thromb Haemost. 2008 Feb; 99(2):271-8; Turecek et al., Blood, 2006, 108(11): Abstract 1002). Корреляция между доинфузионным уровнем ФВ и временем полужизни инфузионного ФVIII у тяжелых больных гемофилией A была продемонстрирована Финвандраатом и коллегами (Fijnvandraat, et al., Br J Haematol. 1995 Oct; 91(2):474-6). В этом исследовании у пациентов с уровнем ФВ, который составлял 200-300% от обычного, наблюдали 15-29-часовое время полужизни ФVIII по сравнению со средним временем в 12,5 часов у пациентов с нормальным уровнем ФВ. В другом исследовании было продемонстрировано, что у пациентов с 1-й группой крови уровень ФВ значительно ниже, а времена полужизни ФVIII короче (15,3 часов) по сравнению с теми, кто имеет II-ю группу крови (19,7 часов) (Vlot, et al. Thromb Haemost. 2000 Jan; 83(1):65-9). Было показано, что химически модифицированный ФВ продлевает время существования рФVIII (Turecek et al., J. Thromb. Haemost. 2007 Jul 9; 5(2) abstract available at: http/www.blackwellpublishing.com/isth2007/abstract.asp?id=64898). В таком случае, совместное введение рФВ и рФVIII является практически осуществимой стратегией при лечении нарушений свертываемости крови таких, как болезнь Виллебранда и гемофилия А.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0005] Соответственно, в настоящем изобретении предложены способы и комбинации для лечения нарушений свертываемости крови путем введения нуждающемуся в лечении пациенту рекомбинантного фактора Виллебранда (рФВ) как отдельно, так и в сочетании с рекомбинантным фактором VIII (рФVIII), что приводит in-vivo к возрастанию времени полужизни фактора VIII.
[0006] В одном из вариантов осуществления, в настоящем изобретении предложен способ лечения болезни Виллебранда и гемофилии A у нуждающегося в лечении пациента, и этот способ включает: введение испытуемому рекомбинантного фактора Виллебранда (рФВ) таким образом, что время полужизни фактора VIII продлевается по сравнению с испытуемым, которому вводили фактор Виллебранда, полученный из плазмы крови, при этом рФВ является композицией из высокомолекулярных мультимеров рФВ, которая содержит как минимум 20% декамеров ФВ либо мультимеров высших порядков, и рФВ обладает более высокой специфической активностью, чем полученный из плазмы крови фактор Виллебранда.
[0007] В дополнительных осуществлениях изобретения и согласно предыдущему пункту, способы изобретения включают совместное введение рекомбинантного фактора Виллебранда (рФВ) и рекомбинантного фактора VIII (pФVIII).
[0008] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ и pФVIII вводятся совместно в одном составе.
[0009] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, испытуемому вводят от 1.0 МЕ/кг ФВ:РКо до 150 МЕ/кг ФВ:РКо на дозу.
[0010] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, испытуемому вводят от 2 МЕ/кг ФВ:РКо до 50 МЕ/кг ФВ:РКо на дозу.
[0011] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, испытуемому вводят от 5 МЕ/кг ФВ:РКо до 40 МЕ/кг ФВ:РКо на дозу.
[0012] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, испытуемому вводят от 10 МЕ/кг ФВ:РКо до 20 МЕ/кг ФВ:РКо на дозу.
[0013] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ, который применяют в описанных в изобретении способах, созревает in vitro при обработке фурином.
[0014] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ образуется путем экспрессии в яичниках китайского хомячка (клеточная культура СНО).
[0015] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, pФVIII и рФВ образуются путем экспрессии в одной клеточной культуре.
[0016] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ вводят испытуемому не чаще, чем раз в два дня.
[0017] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ вводят испытуемому не чаще, чем дважды в неделю.
[0018] В других вариантах осуществления и согласно любому из предыдущих пунктов, в композиции из высокомолекулярных мультимеров ФВ сохраняется как минимум 20% декамеров ФВ либо мультимеров высших порядков на протяжении, по крайней мере, 3-х часов после введения.
[0019] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, время полужизни фактора VIII продлевается как минимум на 5 часов.
[0020] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, время полужизни фактора VIII продлевается как минимум на 12 часов.
[0021] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, время полужизни фактора VIII продлевается как минимум на 24 часа.
[0022] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, время полужизни фактора VIII продлевается как минимум на 36 часов.
[0023] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, время полужизни фактора VIII продлевается как минимум на 48 часов.
[0024] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, время полужизни фактора VIII продлевается как минимум на 72 часа.
[0025] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, отношение прокоагулирующей активности ФVIII (ME ФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо), который вводят испытуемому, составляет от 2:1 до 1:4.
[0026] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, отношение прокоагулирующей активности ФVIII (ME ФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо), который вводят испытуемому, составляет от 3:2 до 1:3.
[0027] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, отношение прокоагулирующей активности ФVIII (ME ФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо), который вводят испытуемому, составляет от 1:1 до 1:2.
[0028] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, 23 отношение прокоагулирующей активности ФVIII (ME ФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо), который вводят испытуемому, составляет примерно 3:4.
[0029] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ обладает специфической активностью приблизительно в 20-150 мЕ/мкг.
[0030] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, композиция из высокомолекулярных мультимеров ФВ содержит как минимум 30% декамеров ФВ либо мультимеров высших порядков.
[0031] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, композиция из высокомолекулярных мультимеров ФВ содержит как минимум 40% декамеров ФВ либо мультимеров высших порядков.
[0032] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, композиция из высокомолекулярных мультимеров ФВ содержит как минимум 50% декамеров ФВ либо мультимеров высших порядков.
[0033] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, композиция из высокомолекулярных мультимеров ФВ содержит как минимум 60% декамеров ФВ либо мультимеров высших порядков.
[0034] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, композиция из высокомолекулярных мультимеров ФВ содержит как минимум 70% декамеров ФВ либо мультимеров высших порядков.
[0035] В дополнительных вариантах осуществления и согласно любому из предыдущих пунктов, в настоящем изобретении предложен способ лечения болезни Виллебранда и гемофилии A у нуждающегося в лечении пациента, и этот способ включает: введение испытуемому рекомбинантного фактора Виллебранда (рФВ) таким образом, что время полужизни фактора VIII продлевается по сравнению с испытуемым, которому вводили фактор Виллебранда, полученный из плазмы крови, при этом: (а) рФВ обладает более высокой специфической активностью, чем полученный из плазмы крови фактор Виллебранда, а специфическая активность рФВ составляет приблизительно 20-150 мЕ/мкг; и (б) время полужизни ФVIII как минимум в 1.5 раз выше, чем время полужизни ФVIII у испытуемого, которому вводили фактор Виллебранда, полученный из плазмы крови.
[0036] В дополнительных вариантах осуществления и согласно любому из предыдущих пунктов, в настоящем изобретении предложен способ лечения болезни Виллебранда и гемофилии A у нуждающегося в лечении пациента, и этот способ включает: введение испытуемому рекомбинантного фактора Виллебранда (рФВ) таким образом, что время полужизни фактора VIII продлевается по сравнению с испытуемым, которому вводили фактор Виллебранда, полученный из плазмы крови, при этом: (а) рФВ является композицией из высокомолекулярных мультимеров ФВ, которая содержит как минимум 20% декамеров ФВ либо мультимеров высших порядков, (б) рФВ обладает более высокой специфической активностью, чем полученный из плазмы крови фактор Виллебранда, а специфическая активность рФВ составляет как минимум 20-150 мЕ/мкг; и (в) время полужизни ФVIII как минимум в 1.5 раз выше, чем время полужизни ФVIII у испытуемого, которому вводили фактор Виллебранда, полученный из плазмы крови.
[0037] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, уровень прокоагулирующей активности фактора VIII (ФVIII:K) в плазме крови испытуемого через 24 часа после введения рФВ составляет как минимум 90% от уровня активности ФVIII:K, который присутствует в плазме крови через 1 час после введения.
[0038] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, уровень прокоагулирующей активности фактора VIII (ФVIII:K) в плазме крови испытуемого через 24 часа после введения составляет как минимум 100% от уровня активности ФVIII:K, который присутствует в плазме крови через 1 час после введения.
[0039] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, уровень прокоагулирующей активности фактора VIII (ФVIII:K) в плазме крови испытуемого через 36 часов после введения составляет как минимум 80% от уровня активности ФVIII:K, который присутствует в плазме крови через 1 час после введения.
[0040] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, уровень прокоагулирующей активности фактора VIII (ФVIII:K) в плазме крови испытуемого через 48 часов после введения составляет как минимум 50% от уровня активности ФVIII:K, который присутствует в плазме крови через 1 час после введения.
[0041] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны на протяжении как минимум 6 часов после введения.
[0042] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны на протяжении как минимум 12 часов после введения.
[0043] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны на протяжении как минимум 18 часов после введения.
[0044] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны на протяжении как минимум 24 часов после введения.
[0045] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны на протяжении как минимум 36 часов после введения.
[0046] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны на протяжении как минимум 48 часов после введения.
[0047] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны на протяжении как минимум 72 часов после введения.
[0048] В дополнительных вариантах осуществления и согласно любому из предыдущих пунктов, в настоящем изобретении предложен способ лечения гемофилии A или болезни Виллебранда у нуждающегося в лечении пациента, и этот способ включает: введение испытуемому рекомбинантного фактора Виллебранда (рФВ).
[0049] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, заявленный способ включают совместное введение испытуемому рекомбинантного фактора VIII (pФVIII) и рекомбинантного фактора Виллебранда (рФВ).
[0050] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, pФVIII и рФВ вводят совместно в одном составе.
[0051] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, отношение прокоагулирующей активности pФVIII (ME pФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо), который вводят испытуемому, составляет от 2:1 до 1:4.
[0052] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, отношение прокоагулирующей активности pФVIII (ME pФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо), который вводят испытуемому, составляет от 3:2 до 1:3.
[0053] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, отношение прокоагулирующей активности pФVIII (ME pФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо), который вводят испытуемому, составляет от 1:1 до 1:2.
[0054] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, отношение прокоагулирующей активности pФVIII (ME pФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо), который вводят испытуемому, составляет примерно 3:4.
[0055] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ созревает in vitro при обработке фурином.
[0056] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ экспрессируется в клеточной культуре млекопитающего.
[0057] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, pФVIII экспрессируется в клеточной культуре млекопитающего.
[0058] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, культура млекопитающего содержит клетки СНО.
[0059] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФVIII и рФВ экспрессируются совместно в одной культуре.
[0060] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФVIII и рФВ очищают совместно.
[0061] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФVIII и рФВ очищают раздельно.
[0062] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, комплекс рФVIII/рФВ перерастворяют перед введением.
[0063] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ обрабатывают фурином перед перерастворением комплекса рФVIII/рФВ.
[0064] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, перерастворенный комплекс рФVIII/рФВ обрабатывают фурином.
[0065] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, фурин является рекомбинантным фурином.
[0066] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ вводят испытуемому не чаще, чем один раз в день.
[0067] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ вводят испытуемому не чаще, чем раз в два дня.
[0068] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ вводят испытуемому не чаще, чем раз в три дня.
[0069] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, рФВ вводят испытуемому не чаще, чем раз в четыре дня.
[0070] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, испытуемому вводят от 1.5 МЕ/кг ФVIII:К до 150 МЕ/кг ФVIII:К на дозу.
[0071] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, испытуемому вводят от 10 МЕ/кг ФVIII:К до 100 МЕ/кг ФVIII:К на дозу.
[0072] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, испытуемому вводят от 25 МЕ/кг ФVIII:К до 75 МЕ/кг ФVIII:К на дозу.
[0073] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, испытуемому вводят от 40 МЕ/кг ФVIII:К до 60 МЕ/кг ФVIII:К на дозу.
[0074] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, уровень прокоагулирующей активности фактора VIII (ФVIII:К) в плазме крови испытуемого через 24 часа после введения составляет как минимум 90% от уровня активности ФVIII:К, который присутствует в плазме крови через 1 час после введения.
[0075] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, уровень прокоагулирующей активности фактора VIII (ФVIII:К) в плазме крови испытуемого через 24 часа после введения составляет как минимум 100% от уровня активности ФVIII:K, который присутствует в плазме крови через 1 час после введения.
[0076] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, уровень прокоагулирующей активности фактора VIII (ФVIII:K) в плазме крови испытуемого через 36 часов после введения составляет как минимум 80% от уровня активности ФVIII:К, который присутствует в плазме крови через 1 час после введения.
[0077] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, уровень прокоагулирующей активности фактора VIII (ФVIII:K) в плазме крови испытуемого через 48 часов после введения составляет как минимум 50% от уровня активности ФVIII:K, который присутствует в плазме крови через 1 час после введения.
[0078] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, вводимый испытуемому рФВ содержит композицию из высокомолекулярных мультимеров ФВ, которая содержит как минимум 10% декамеров ФВ либо мультимеров высших порядков.
[0079] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, вводимый испытуемому рФВ содержит композицию из высокомолекулярных мультимеров ФВ, которая содержит как минимум 20% декамеров ФВ либо мультимеров высших порядков.
[0080] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, вводимый испытуемому рФВ содержит композицию из высокомолекулярных мультимеров ФВ, которая содержит как минимум 30% декамеров ФВ либо мультимеров высших порядков.
[0081] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, вводимый испытуемому рФВ содержит композицию из высокомолекулярных мультимеров ФВ, которая содержит как минимум 40% декамеров ФВ либо мультимеров высших порядков.
[0082] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, вводимый испытуемому рФВ содержит композицию из высокомолекулярных мультимеров ФВ, которая содержит как минимум 50% декамеров ФВ либо мультимеров высших порядков.
[0083] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны in vitro на протяжении как минимум 3 часов после введения.
[0084] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны in vitro на протяжении как минимум 6 часов после введения.
[0085] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, при этом мультимеры рФВ высших порядков стабильны in vitro на протяжении как минимум 12 часов после введения.
[0086] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, при этом мультимеры рФВ высших порядков стабильны in vitro на протяжении как минимум 18 часов после введения.
[0087] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны in vitro на протяжении как минимум 24 часов после введения.
[0088] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны in vitro на протяжении как минимум 36 часов после введения.
[0089] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, при этом мультимеры рФВ высших порядков стабильны in vitro на протяжении как минимум 48 часов после введения.
[0090] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, мультимеры рФВ высших порядков стабильны in vitro на протяжении как минимум 72 часов после введения.
[0091] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, эндогенная активность ФVIII стабилизируется на протяжении как минимум 12 часов.
[0092] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, эндогенная активность ФVIII стабилизируется на протяжении как минимум 24 часов.
[0093] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, эндогенная активность ФVIII стабилизируется на протяжении как минимум 36 часов.
[0094] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, эндогенная активность ФVIII стабилизируется на протяжении как минимум 48 часов.
[0095] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, эндогенная активность ФVIII стабилизируется на протяжении как минимум 72 часов.
[0096] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, активность вводимого совместно рФVIII стабилизируется на протяжении как минимум 12 часов.
[0097] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, активность вводимого совместно рФVIII стабилизируется на протяжении как минимум 24 часов.
[0098] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, активность вводимого совместно pФVIII стабилизируется на протяжении как минимум 36 часов.
[0099] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, активность вводимого совместно pФVIII стабилизируется на протяжении как минимум 48 часов.
[00100] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, активность вводимого совместно pФVIII стабилизируется на протяжении как минимум 72 часов.
[00101] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, активность вводимого совместно pФVIII стабилизируется путем продления времени полужизни pФVIII in vivo.
[00102] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, время полужизни ФVIII продлевается приблизительно на пять часов по сравнению с пациентами, которым вводили пФVIII.
[00103] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, по крайней мере, 1% активности совместно вводимого pФVIII сохраняется на протяжении как минимум 36 часов у пациента, которому вводили указанный pФVIII.
[00104] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, по крайней мере, 1% активности совместно вводимого pФVIII сохраняется на протяжении как минимум 48 часов у пациента, которому вводили указанный pФVIII.
[00105] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, по крайней мере, 1% активности совместно вводимого pФVIII сохраняется на протяжении как минимум 72 часов у пациента, которому вводили указанный pФVIII.
[00106] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, по крайней мере, 1% активности совместно вводимого pФVIII сохраняется на протяжении как минимум 90 часов у пациента, которому вводили указанный pФVIII.
[00107] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, по крайней мере, 1% активности совместно вводимого pФVIII сохраняется на протяжении как минимум 120 часов у пациента, которому вводили указанный pФVIII.
[00108] В дополнительных осуществлениях и согласно любому из предыдущих пунктов, по крайней мере, 1% активности совместно вводимого pФVIII сохраняется на протяжении как минимум 168 часов у пациента, которому вводили указанный pФVIII.
КРАТКОЕ ОПИСАНИЕ ФИГУР
[00109] Фигура 1. Схематическое изображение дизайна клинического исследования, в котором оценивается переносимость и безопасность после введения единичной дозы рФВ:рФVIII.
[00110] Фигура 2. Фармакокинетические данные. На (А) приведены ФК данные по рФВ/рФVIII и пФВ/пФVIII. На (Б) приведены данные по прогрессирующей потере высокомолекулярного рФВ при воздействии металлопротеиназы ADAMTS13.
[00111] Фигура 3. Фармакокинетические данные, иллюстрирующие ФК ФVIII для рФВ/рФVIII и пФВ/пФVIII.
[00112] Фигура 4. Обобщающая таблица персональных данных пациентов данного исследования.
[00113] Фигура 5. Фармакокинетические данные терапии рФВ/рФVIII и пФВ/пФVIII по группе 4А.
[00114] Фигура 6. Данные ДСН-ПААГ-электрофореза по расщеплению мультимеров ФВ металлопротеиназой ADAMTS13.
[00115] Фигура 7. Фармакокинетические данные терапии рФВ/рФVIII и пФВ/пФVIII по группе 4А.
[00116] Фигура 8. Обобщенные данные по побочным эффектам в данном исследовании.
[00117] Фигура 9. Данные по ФК параметрам рФВ в данном исследовании.
[00118] Фигура 10. Данные по ФК рФВ Пациента 1.
[00119] Фигура 11. Данные по ФК рФВ Пациента 2.
[00120] Фигура 12. Данные по ФК рФВ Пациента 3.
[00121] Фигура 13. Сравнение ФК рФВ Пациентов 1, 2 и 3 - сравнение параметров рФВ и активности ФVIII.
[00122] Фигура 14. Активность ФVIII среди всех групп данного исследования.
[00123] Фигура 15. ФК рФВ пациентов группы 2 - сравнение параметров ФВ и активности ФVIII.
[00124] Фигура 16. Обобщенные результаты фармакокинетических параметров прокоагулирующей активности фактора VIII (ФVIII:К) у пациентов группы 2.
[00125] Фигура 17. ФК рФВ всех пациентов группы 3 - сравнение параметров плазмы крови для ФВ и ФVIII.
[00126] Фигура 18. Обобщенные результаты фармакокинетических параметров прокоагулирующей активности фактора VIII (ФVIII:K) у пациентов группы 3.
[00127] Фигура 19. Данные по пациентам группы 4.
[00128] Фигура 20. Обобщенные результаты фармакокинетических
параметров прокоагулирующей активности фактора VIII (ФVIII:K) у пациентов группы 4А.
[00129] Фигура 21. Фармакокинетические данные по ФVIII:К, в которых сравниваются совместно применяемые рФВ и рФVIII по отношению к Advate Pivotal.
[00130] Фигура 22. Обобщенные результаты по наличию антител у испытуемого, который получал совместно пФВ/пФVIII или рФВ/рФVIII.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Обзор
[00131] В настоящем изобретении предложены составы и способы для лечения нарушений свертываемости крови у пациента путем введения рекомбинантного фактора Виллебранда (рФВ) как отдельно, так и в сочетании с фактором VIII (который может быть рекомбинантным или полученным из плазмы крови). В некоторых вариантах осуществления составы и способы настоящего изобретения применяют для лечения нарушений свертываемости крови, таких как болезнь Виллебранда (БВ) или гемофилия А.
[00132] Согласно одному варианту осуществления, вводимый испытуемому рФВ обеспечивает повышенную стабильность активности in vivo фактора VIII (ФVIII) по сравнению со стабильностью ФVIII, обусловленной полученным из плазмы крови ФВ, что позволяет применять более низкие дозы и/или периодичность лечения, чем при традиционном лечении нарушений свертываемости крови. Повышенная стабильность активности ФVIII и уровней ФVIII могут быть определены с помощью известных в данной области техники и описанных здесь методов, которые включают стандартную аналитику такую, как одностадийный анализ коагулирующей активности, хромогенный анализ и иммуноанализ (смотрите, например, статьи Lippi et al., Blood Coagulation & Fibrinolysis, 2009, 20(1):1-3 и Chandler et al., Am J. Clin. Pathol., 2003, 120:34-39, каждая из которых в полном объеме включена в настоящую заявку посредством ссылки для всестороннего изучения, в особенности того, что касается методов анализа уровня и активности ФVIII). Как показано на Фиг. 20, среднее время полужизни ФVIII было увеличено с помощью рФВ на 5.2 часа по сравнению со временем полужизни у пациентов, которые получали пФВ. Фиг. 2 и 7 также иллюстрируют возрастание активности ФVIII у пациентов, которым вводили рФВ по сравнению с теми, которым вводили пФВ. Фиг. 2 иллюстрирует, что среднее время полужизни ФVIII у пациентов, которым вводили рФВ, было увеличено на 4.7 часа по сравнению пациентами, которым вводили пФВ, а данные по Группе 4А на Фиг. 7 показывают возрастание времени полужизни ФVIII на 5.3 часа у пациентов, которым вводили рФВ, по сравнению пациентами, которым вводили пФВ. Вдобавок, как показано на Фиг. 21, время полужизни плазменного ФVIII у больных БВ, которые получали рФВ в комбинации с рФVIII, возрастает на 12.27 часов по сравнению с пациентами, которые получали только ФVIII (то есть Advate).
[00133] В дополнительном варианте осуществления, введение рФВ стабилизирует эндогенную активность и/или активность совместно вводимого ФVIII, что приводит в возрастанию in vivo времени полужизни и/или активности ФVIII. В тех осуществлениях изобретения, в которых рФВ и ФVIII вводили совместно, рФВ и ФVIII можно вводить испытуемому в одном составе. В дополнительных осуществлениях, ни рФВ, ни ФVIII не являются модифицированными с помощью водорастворимого полимера. В других осуществлениях, либо рФВ, либо ФVIII, либо оба являются модифицированными с помощью водорастворимого полимера. Следует принимать во внимание, что в осуществлениях, в которых рФВ вводили совместно с ФVIII, ФVIII может быть рекомбинантным или полученным из плазмы.
[00134] В дополнительных вариантах осуществления и согласно с предыдущими пунктами, вводимый испытуемому рФВ является составом из высокомолекулярных мультимеров, который содержит декам еры либо высшие мультимеры рФВ. Как обсуждалось выше, применение заявленных в изобретении составов рФВ обеспечивает вариативность терапевтической дозировки (или повторной дозировки) с или без ФVIII (рекомбинантным либо полученным из плазмы крови). В дополнительных осуществлениях изобретения вводимый испытуемому рФВ является составом из высокомолекулярных мультимеров ФВ, который содержит как минимум 20% декамеров либо высших мультимеров ФВ. В отдельных осуществлениях вводимый испытуемому рФВ не модифицирован с помощью водорастворимого полимера.
[00135] В других дополнительных вариантах осуществления вводимый испытуемому рФВ обладает более высокой специфической активностью, чем пФВ.
[00136] В других дополнительных вариантах осуществления рФВ как в отдельности, так и в комбинации с пФVIII или рФVIII, вводят испытуемому не чаще, чем дважды в неделю.
[00137] В других дополнительных вариантах осуществления перед введением испытуемому рФВ обрабатывают фурином. В отдельных осуществлениях рФВ обрабатывают рекомбинантным фурином.
[00138] В дополнительных вариантах осуществления применяемый в настоящем изобретении рФВ получен в соответствии со способами, известными в данной области техники и описанным, например, в US 2012/0035110, зарегистрированном 8 июля 2011 г., и US Patent No. 8,173,597, опубликованном 8 мая 2012 г., каждый из которых в полном объеме включен в настоящую заявку посредством ссылки для всестороннего изучения, в особенности того, что касается рФВ-составов и способов получения данных составов.
[00139] Согласно любому из предыдущих пунктов рФВ как в отдельности, так и в комбинации с ФVIII, применяют для лечения нарушений свертываемости крови, таких как болезнь БВ или гемофилия А. У больных БВ существует определенный уровень ФVIII, но стабильность ФVIII в общем случае снижена, так как у этих пациентов наблюдается недостаток ФВ. Лечение больных БВ в некоторых осуществлениях включает предварительную терапию рФВ и рФVIII, за которой следует повторное введение только рФВ. В других осуществлениях предварительная терапия может осуществляться с помощью одного рФВ, в то время как последующие повторные введения включают рФВ и рФVIII, либо и предварительное и последующие повторные введения могут включать рФВ и рФVIII. Аналогично, больные гемофилией А (страдающие недостатком ФVIII) могут проходить предварительную терапию рФВ и рФVIII, а последующее повторное лечение может включать введение только pФVIII или только рФВ. В других осуществлениях предварительная терапия может осуществляться с помощью одного рФVIII, в то время как последующее повторное лечение включает совместное введение рФВ и рФVIII.
Определения
[00140] Используемый здесь термин "рФВ" обозначает рекомбинантный ФВ.
[00141] Используемый здесь термин "рФVIII" обозначает рекомбинантный ФVIII.
[00142] Термин "рекомбинантный" при применении к чему-либо, например, к клетке или нуклеиновой кислоте, протеину или вектору, указывает на то, что клетка, нуклеиновая кислота, протеин или вектор были модифицированы путем введения гетерологичной нуклеиновой кислоты либо протеина, или путем изменения нативной нуклеиновой кислоты либо протеина, или на то, что клетки получены из клеток, модифицированных подобным образом. Таким образом, к примеру, рекомбинантные клетки экспрессируют гены, которых нет у нативной (нерекомбинантной) формы клеток, или экспрессируют нативные гены, которые в иных случаях экспрессируются чрезмерно, экспрессируются мало или вообще не экспрессируются.
[00143] Используемый здесь термин "рекомбинантный ФВ" включает в себя ФВ, полученный путем рекомбинантной ДНК-технологии. В отдельных осуществлениях протеины ФВ, заявленные в данном изобретении, могут содержать компонент, например, приготовленный как в WO 1986/06096, опубликованном 23 октября 1986 г. и U.S. patent application Ser. No. 07/559,509, зарегистрированном 23 июля 1990 г. на имя Ginsburg et al., которые включены в настоящую заявку посредством ссылок относительно способов получения рекомбинантного ФВ. Заявленный в настоящем изобретении ФВ может содержать все возможные формы, включая мономерные и мультимерные формы. Также следует понимать, что настоящее изобретение охватывает разные формы ФВ для применения их в комбинации. Например, заявленный в настоящем изобретении ФВ может содержать различные мультимеры, различные производные и, как биологически активные, так и не являющиеся биологически активными производные.
[00144] В контексте настоящего изобретения термин рекомбинантный ФВ объединяет любые ФВ, полученные, например, от млекопитающих, таких как приматы, человек, обезьяны, кролики, свиньи, грызуны, мыши, крысы, хомяки, песчанки, собачьи, кошачьи, а также их биологически активные производные. Включены также мутантные и вариантные протеины, обладающие активностью, такие, какими являются функциональные фрагменты и гибридные белки протеинов ФВ. Более того, в контексте настоящего изобретения ФВ может дополнительно содержать маркеры, которые способствуют очищению, детекции либо и тому и другому. Описанный здесь ФВ может быть дополнительно модифицирован с помощью терапевтического препарата или подходящего радиоактивного препарата in vitro или in vivo.
[00145] Используемый здесь термин "полученный из плазмы крови ФВ (пФВ)" включает все протеиновые формы, которые могут быть обнаружены в крови, включая зрелый ФВ, полученный из крови млекопитающего и обладающий свойством стабилизации in vivo, то есть связывания, как минимум одной молекулы ФVIII.
[00146] Термин "высокомультимерный ФВ" или "высокомолекулярный ФВ" обозначает ФВ, который содержит как минимум 10 субъединиц или 12, 14 или 16 субъединиц, и до 20, 22, 24 или 26 единиц и более. Термин "субъединица" обозначает мономерный ФВ. Как известно в данной области техники, в общем случае происходит полимеризация димеров ФВ и образование мультимеров высших порядков, (смотрите Turecek et al., Semin. Thromb. Hemost. 2010, 36(5): 510-521, которая в полном объеме включена в настоящую заявку посредством ссылки для всестороннего изучения, в особенности того, что касается мультимерного анализа ФВ).
[00147] Используемый здесь термин "фактор VIII" или "ФVIII" обозначает любую из форм молекулы фактора VIII, обладающую типичными характеристиками фактора свертывания крови VIII, как являющуюся эндогенной для пациента, так и полученную из плазмы крови или путем применения рекомбинантной ДНК-технологии, и включающую все модифицированные формы фактора VIII. Фактор VIII (ФVIII) в естественных условиях и в терапевтических препаратах существует в виде гетерогенного распределения полипептидов, которые происходят от одного генного продукта {смотрите, например, Andersson et al., Proc. Natl. Acad. Sci. USA, 83:2979-2983 (1986)). Примеры серийно выпускаемых терапевтических препаратов, содержащих фактор VIII, включают те, которые продаются под торговыми наименованиями HEMOFIL М, ADVATE и RECOMBINATE (и предоставляются Baxter Healthcare Corporation, Дирфилд, Иллинойс, США).
[00148] Используемые здесь термины "плазменная активность ФVIII" и "активность ФVIII in vivo" являются взаимозаменяемыми. Измеренная с применением стандартной аналитики активность ФVIII in vivo может быть эндогенной активностью ФVIII, активностью терапевтически применяемого ФVIII (рекомбинантного или полученного из плазмы крови), либо одновременно эндогенной активностью и активностью применяемого ФVIII. Аналогично, "плазменный OVIH" обозначает эндогенный ФVIII либо применяемый рекомбинантный или полученный из плазмы крови ФVIII.
[00149] Используемый здесь термин "болезнь Виллебранда" обозначает группу заболеваний, вызванных дефицитом фактора Виллебранда. Фактор Виллебранда способствует накоплению и прикреплению тромбоцитов к стенкам кровеносных сосудов, что необходимо для нормального свертывания крови. Как будет далее детально описано, существует несколько типов болезни Виллебранда.
[00150] Используемый здесь термин "гемофилия" обозначает группу заболеваний, которая в широком смысле характеризуется сниженным свертыванием крови или сниженной коагуляцией. Гемофилия может относиться к типу A, типу B или типу C, либо к комбинации всех трех типов болезни. Гемофилия типа A (гемофилия A) обусловлена снижением либо утратой активности фактора VIII (ФVIII) и является наиболее известным из подтипов гемофилии. Гемофилия типа B (гемофилия B) вызвана снижением либо утратой функции свертывания фактора IX (OIX. Гемофилия типа C (гемофилия С) является последствием снижения либо утраты свертывающей активности фактора XI (ФXI). Гемофилия A и B являются Х-сцепленными заболеваниями, в то время как гемофилия C аутосомна. Обычные способы лечения гемофилии включают как профилактическое введение, так и введение по необходимости свертывающих факторов таких, как ФVIII, ФXI, включая Бебулин®-VH, и ФXI, а также ФЕЙБА-VH, десмопрессин и вливание плазмы крови.
[00151] Термины "изолированный", "очищенный" или "биологически чистый" обозначают материал, который практически или фактически не содержит компонентов, которые обычно присутствуют вместе с ним в его естественном состоянии. Чистота и гомогенность обычно определяются с помощью методов аналитической химии, таких как электрофорез в полиакриламидном геле или жидкостная хроматография высокого разрешения. ФВ является преобладающей компонентой, которая присутствует в практически очищенном препарате. Термин "очищенный" в некоторых осуществлениях изобретения указывает на то, что нуклеиновая кислота либо протеин имеет одну окрашенную полосу в электрофорезном геле. В других осуществлениях это означает, что нуклеиновая кислота либо протеин являются чистыми как минимум на 50%, предпочтительно на 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% или еще более чистыми. В других осуществлениях термины "очищать" или "очистка" означают удаление как минимум одного постороннего вещества из подлежащего очистке состава. В этом смысле очистка не подразумевает того, что очищенное вещество должно быть гомогенным, то есть чистым на 100%.
[00152] Используемый здесь термин "введение" (и все его грамматические эквиваленты) включает внутривенное введение, внутримышечное введение, подкожное введение, пероральное введение, введение в качестве суппозитория, местное введение, внутрибрюшинное, внутриочаговое или интраназальное введение, либо вживление испытуемому устройства замедленного действия, такого как осмотический мини-насос. Введение осуществляется любым путем, включая парентеральный и трансмукозальный (например, пероральный, назальный, вагинальный, ректальный или трансдермальный). Парентеральное введение включает, например, внутривенное, внутримышечное, внутриартериальное, внутрикожное, подкожное, внутрибрюшинное, интравентрикулярное и внутричерепное. Другие методы доставки включают (но не ограничиваются этим) использование липосомальных технологий, внутривенных инфузий, трансдермального пластыря и т.д.
[00153] Термины "терапевтически эффективная дозировка или доза" либо "терапевтически достаточная дозировка или доза", либо "эффективная или достаточная дозировка или доза" обозначают такую дозировку, которая оказывает терапевтический эффект, для достижения которого она вводилась. Например, терапевтически эффективная доза лекарства для лечения гемофилии может соответствовать дозировке, которая способна предотвратить или снять один или более симптомов, связанных с гемофилией. Точная доза будет зависеть от цели лечения, и будет определяться специалистом в данной области техники с применением известных методов (смотрите, например, Lieberman, Pharmaceutical Dosage Forms (vols. 1-3, 1992); Lloyd, The Art, Science and Technology of Pharmaceutical Compounding (1999); Pickar, Dosage Calculations (1999); и Remington: The Science and Practice of Pharmacy, 20th Edition, 2003, Gennaro, Ed., Lippincott, Williams & Wilkins).
[00154] Используемые здесь термины "пациент" и "испытуемый" являются взаимозаменяемыми и обозначают млекопитающее (обычно человека), у которого присутствует данное заболевание или существует риск заражения.
[00155] Используемый здесь термин "приблизительно" указывает на приблизительный диапазон некоторой величины плюс-минус 10%. К примеру, фраза "приблизительно 20%" охватывает диапазон в 18-22%).
[00156] Используемый здесь термин "время полужизни" обозначает период времени, за который количество вещества, которое разрушается (или выводится из образца или организма пациента) уменьшается наполовину.
Составы, которые применяются в изобретении
[00157] В настоящем изобретении применяются составы, содержащие рекомбинантный фактор Виллебранда (рФВ) для лечения нарушений свертываемости крови, таких как БВ и гемофилия А. В некоторых осуществлениях настоящего изобретения рФР применяется в комбинации с фактором VIII (ФVIII). Вводимый совместно ФVIII может быть как рекомбинантным (pФVIII), так и полученным из плазмы крови (пФVIII). В предпочтительном варианте осуществления составы настоящего изобретения стабилизируют in vivo активность фактора VIII (которая также именуется здесь активностью плазменного фактора VIII) таким образом, что время полужизни фактора VIII in vivo продлевается по сравнению с соответствующим временем у испытуемого, которому не вводили рФВ или вводили пФВ. Определение степени стабилизации рФВ активности ФVIII (включая увеличение времени полужизни ФVIII) может проводится путем применения методов, известных в данной области техники. Уровень активности ФVIII может быть определен с помощью, например, одностадийного анализа коагулирующей активности, хромогенного анализа и иммуноанализа (смотрите, например, статьи Lippi et al., Blood Coagulation & Fibrinolysis, 2009, 20(1): 1-3, European Pharmacopoeia (Ph. Eur., 3.sup.rd Ed. 1997: 2.7.4) и Chandler et al., Am J. Clin. Pathol., 2003, 120:34-39, каждая из которых в полном объеме включена в настоящую заявку посредством ссылки для всестороннего изучения, в особенности того, что касается методов анализа уровня и активности ФVIII).
[00158] В отдельных осуществлениях протеины ФВ, заявленные в данном изобретении, могут содержать компонент, например, приготовленный как в WO 1986/06096, опубликованном 23 октября 1986 г. и U.S. patent application Ser. No. 07/559,509, зарегистрированном 23 июля 1990 г. на имя Ginsburg et al., которые включены в настоящую заявку посредством ссылок относительно способов получения рекомбинантного ФВ. Заявленный в настоящем изобретении ФВ содержит все возможные формы, включая мономерные и мультимерные формы. Одной из особенно используемых форм ФВ являются гомо-мультимеры, состоящие как минимум из двух ФВ. Протеины ФВ также могут являться биологически активными производными или, при применении исключительно в качестве стабилизатора для ФVIII, ФВ может присутствовать в форме, не являющейся биологически активной. Также следует понимать, что настоящее изобретение включает разные формы ФВ для применения в комбинации. Например, состав, заявленный в настоящем изобретении, может содержать различные мультимеры, различные производные и, как биологически активные, так и не являющиеся биологически активными производные.
[00159] При первичном гемостазе ФВ служит мостиком между тромбоцитами и специфическими компонентами внеклеточного матрикса, такими как коллаген. Биологическая активность ФВ при этом процессе может быть измерена с помощью различных in vitro аналитических методов (Turecek et al., Semin. Thromb. Hemost. 28: 149-160, 2002). Ристоцетин-кофакторный метод анализа основан на агглютинации зафиксированных в формалине тромбоцитов, индуцированной антибиотическим ристоцитином в присутствии ФВ. Степень агглютинации тромбоцитов зависит от концентрации ФВ и может быть определена с помощью турбидиметрического метода, то есть при применении агрегометра (Weiss et al., J. Clin. Invest. 52: 2708-2716, 1973; Macfarlane et al., Thromb. Diath. Haemorrh. 34: 306-308, 1975). Второй метод - это анализ связывания коллагена, основанный на технологии ИФА (Brown et Bosak, Thromb. Res. 43: 303-311, 1986; Favaloro, Thromb. Haemost. 83: 127-135, 2000). На титрационный микропланшет наносится коллаген типа I или III. Далее ФВ связывается с поверхностью коллагена и впоследствии распознается меченым ферментом поликлональным антителом. Последний шаг - реакция субстрата, которая может отслеживаться фотометрически с помощью ИФА ридера. Специфическая ристоцетин-кофакторная активность ФВ (ФВ:РКо), которая приводится в настоящем изобретении, при измерении с помощью аналитических in vitro методов в общем случае описывается в единицах мЕ/мкг ФВ.
[00160] Преимуществом ФВ-составов, заявленных в настоящем изобретении, перед пФВ является то, что рФВ проявляет более высокую специфическую активность, чем пФВ. В некоторых осуществлениях заявленный в настоящем изобретении рФВ обладает специфической активностью в, как минимум, 20, 22.5, 25, 27.5, 30, 32.5, 35, 37.5, 40, 42.5, 45, 47.5, 50, 52.5, 55, 57.5, 60, 62.5, 65, 67.5, 70, 72.5, 75, 77.5, 80, 82.5, 85, 87.5, 90, 92.5, 95, 97.5, 100, 105, 110, 115, 120, 125, 130, 135, 140, 145, 150 мЕ/мкг и более. В одном из осуществлений рФВ, который применяли согласно способам, описанным в настоящем изобретении, обладает специфической активностью от 20 мЕ/мкг до 150 мЕ/мкг. В другом осуществлении ФВ обладает специфической активностью от 30 мЕ/мкг до 120 мЕ/мкг. В другом осуществлении рФВ обладает специфической активностью от 40 мЕ/мкг до 90 мЕ/мкг. В еще одном осуществлении рФВ обладает специфической активностью, соответствующей вариантам от 1 до 133, перечисленным в Таблице 1.
[00161] Заявленный в настоящем изобретении рФВ является высокомультимерным и содержит приблизительно от 10 до 40 субъединиц. В дополнительных осуществлениях изобретения мультимерный рФВ, получаемый согласно описанным в данном изобретении способам, содержит приблизительно 10-30, 12-28, 14-26, 16-24, 18-22, 20-21 субъединиц. В дополнительных осуществлениях присутствующий в мультимерах рФВ варьируется по размеру от димеров до мультимеров из более чем 40 субъединиц (>10 миллионов Дальтонов). Наибольшие мультимеры обеспечивают множественные центры связывания, которые могут взаимодействовать как с рецепторами тромбоцитов, так и с субэндотелиальными матриксными сайтами повреждения, и являются наиболее гемостатически активной формой ФВ. Как показано в анализе мультимеров, приведенном на Фиг. 2 (нижняя панель), применение металлопротеиназы ADAMTS13 со временем расщепляет мультимеры, но заявленные в настоящем изобретении рФВ-составы при получении (в общем случае путем экспрессии в клеточной культуре) не подвергаются действию ADAMTS13 и сохраняют высокомультимерную структуру.
[00162] В одном из осуществлений рФВ-состав, применяемый согласно способам, описанным в настоящем изобретении, характеризуется таким распределением олигомеров рФВ, в котором 95% олигомеров содержат от 6 до 20 субъединиц. В других осуществлениях рФВ-состав характеризуется таким распределением олигомеров рФВ, в котором 95% олигомеров содержат такой интервал количества субъединиц, который соответствует вариантам от 458 до 641, перечисленным в Таблице 2.
[00163] В одном из осуществлений рФВ-состав может быть охарактеризован в соответствии с процентным содержанием молекул рФВ, которые входят в состав отдельных мультимеров ФВ высших порядков или больших мультимеров. Например, в одном из осуществлений как минимум 20% молекул рФВ в рФВ-составе, который применяется согласно способам, описанным в настоящем изобретении, входят в состав комплекса олигомеров из, как минимум, 10 субъединиц. В другом осуществлении как минимум 20% молекул рФВ в рФВ-составе, который применяется согласно способам, описанным в настоящем изобретении, входят в состав комплекса олигомеров из, как минимум, 12 субъединиц. В других осуществлениях рФВ-состав, который применяется согласно способам, заявленным в настоящем изобретении, характеризуется минимальным процентным содержанием (например, минимум X%) молекул рФВ, входящих в состав отдельного мультимера высшего порядка или большего мультимера (например, мультимера из как минимум Y субъединиц), соответствующим любому из вариантов от 134 до 457, перечисленным в Таблицах 3-5.
[00164] В соответствии с вышесказанным, рФВ-состав, который вводят испытуемому (с или без ФVIII) в общем случае характеризуется значительным процентным содержанием высокомолекулярных (ВМ) мультимеров рФВ. В других осуществлениях ВМ составы мультимеров рФВ содержат как минимум 10%-80% декамеров рФВ или мультимеров высших порядков. В дополнительных осуществлениях составы содержат приблизительно 10-95%, 20-90%, 30-85%, 40-80%, 50-75%, 60-70% декамеров рФВ или мультимеров высших порядков. В дополнительных осуществлениях ВМ состав мультимеров рФВ содержит как минимум 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% декамеров рФВ или мультимеров высших порядков.
[00165] Оценка количества и процентного содержания мультимеров рФВ может проводиться с применением методов, известных в данной области техники, включая, в частности, методы, использующие электрофорез и эксклюзионную хроматографию для сортировки мультимеров по размеру, например, так, как это обсуждается в статье Cumming et al, (J Clin Pathol. 1993 May; 46(5): 470-473, которая в полном объеме включена в настоящую заявку посредством ссылки для всестороннего изучения, в особенности того, что касается методов оценки мультимеров ФВ). Подобные методы могут дополнительно включать методы иммуноблоттинга (такие, как вестерн-блоттинг), в которых иммуноблоттинг геля проводится с использованием радиоактивно меченого антитела к ФВ с последующей хемолюминисцентной детекцией (смотрите, например, Wen et al., (1993), J. Clin. Lab. Anal., 7: 317-323, которая в полном объеме включена в настоящую заявку посредством ссылки для всестороннего изучения, в особенности того, что касается методов оценки мультимеров ФВ). Дополнительные методы, применяемые для ФВ, включают анализ ФВ:антиген (ФВ:Аг), ФВ:ристоцетин-кофактор (ФВ:РКоф) и ФВ:коллаген-связывающей активности (ФВ:КСА), которые часто применяются для диагностики и классификации болезни Виллебранда. (смотрите, например, Favaloro et al., Pathology, 1997, 29(4): 341-456, которая в полном объеме включена в настоящую заявку посредством ссылки для всестороннего изучения, в особенности того, что касается методов анализа ФВ).
[00166] В дополнительных осуществлениях, заявленные в изобретении мультимеры рФВ высших порядков являются стабильными на протяжении от 1 до 90 часов после введения. В других дополнительных осуществлениях мультимеры рФВ высших порядков являются стабильными на протяжении 5-80, 10-70, 15-60, 20-50, 25-40, 30-35 часов после введения. В других дополнительных осуществлениях мультимеры рФВ высших порядков являются стабильными на протяжении как минимум 3, 6, 12, 18, 24, 36, 48, 72 часов после введения. В определенных осуществлениях стабильность мультимеров рФВ оценивали in vitro.
[00167] В одном из осуществлений мультимеры рФВ высших порядков, которые применяются в составах и согласно способам, описанным в настоящем изобретении, характеризуются временем полужизни в, как минимум, 12 часов после введения. В другом осуществлении мультимеры рФВ высших порядков характеризуются временем полужизни в, как минимум, 24 часа после применения. В других дополнительных осуществлениях мультимеры рФВ высших порядков характеризуются временем полужизни, которое соответствует вариантам от 642 до 1045, перечисленным в Таблице 6.
[00168] В дополнительных вариантах осуществления рФВ, заявленный в настоящем изобретении, повышает стабильность плазменного ФVIII, который, как следует принимать во внимание, может содержать пФVIII или рФVIII, введенные пациенту, либо может содержать эндогенный для пациента ФVIII, либо любую их комбинацию. Например, как показано на Фиг. 22, время полужизни плазменного ФVIII у больных БВ, которые получают рФВ в комбинации в рФVIII, увеличено по сравнению с теми пациентами, которые получают только ФVIII (то есть Advate). В дополнительных осуществлениях рФВ увеличивает время полужизни ФVIII приблизительно в 1.5-5 раз по сравнению со временем полужизни, которое наблюдается у пациентов, получающих только ФVIII. В других дополнительных осуществлениях рФВ увеличивает время полужизни ФVIII приблизительно в 1.0-4.5, 1.5-4.0, 2.0-3.5, 2.5-3.0 раза. В одном из осуществлений введение рФВ увеличивает стабильность плазменного ФVIII по сравнению с введением ФВ, полученного из плазмы крови, кратно величинам, соответствующим вариантам от 1046 до 1089, перечисленным в Таблице 7. В отдельном осуществлении введение комплекса рФВ/ФVIII увеличивает стабильность плазменного ФVIII по сравнению с введением ФВ, полученного из плазмы крови, кратно величинам, соответствующим вариантам от 1046 до 1089, перечисленным в Таблице 7.
[00169] В других дополнительных осуществлениях увеличение времени полужизни ФVIII сохраняется на протяжении как минимум 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 часов после введения рФВ. В других дополнительных осуществлениях увеличение времени полужизни ФVIII сохраняется на протяжении как минимум 5-125, 10-115, 15-105, 20-95, 25-85, 30-75, 35-65, 40-55 часов после введения рФВ.
[00170] В одном из осуществлений увеличение среднего времени удержания (СВУ) плазменного ФVIII сохраняется после введения рФВ на протяжении времени, соответствующего вариантам от 1090 до 1299, перечисленным в Таблице 8. В отдельном осуществлении увеличение времени полужизни плазменного ФVIII сохраняется после введения комплекса рФВ/ФVIII на протяжении времени, соответствующего вариантам от 1090 до 1299, перечисленным в Таблице 8.
[00171] В дополнительных вариантах осуществления рФВ, заявленный в настоящем изобретении, оказывает усиленное действие на стабильность ФVIII по сравнению с действием пФВ. Например, как показано на Фиг. 20, среднее время полужизни ФVIII было увеличено рФВ на 5.2 часа по сравнению со временем полужизни у пациентов, получавших пФВ. В других дополнительных осуществлениях рФВ увеличивает среднее время полужизни ФVIII приблизительно на 1-15, 2-14, 3-13, 4-12, 5-11, 6-10, 5-9, 6-8 часов. В других дополнительных осуществлениях рФВ увеличивает время полужизни ФVIII приблизительно на 10%-75% по сравнению с пФВ. В других дополнительных осуществлениях рФВ увеличивает время полужизни ФVIII приблизительно на 10-80%, 15-65%, 20-60%, 25-55%, 30-50%, 35-45% по сравнению с пФВ. В определенных осуществлениях введение рФВ увеличивает время полужизни ФVIII на величину, соответствующую вариантам от 1300 до 1643, перечисленным в Таблице 9, по сравнению с введением ФВ, полученного из плазмы крови. В других дополнительных осуществлениях среднее или процентное увеличение времени полужизни ФVIII сохраняется на протяжении как минимум 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 часов после введения рФВ. В других дополнительных осуществлениях увеличение времени полужизни ФVIII сохраняется на протяжении как минимум 5-125, 10-115, 15-105, 20-95, 25-85, 30-75, 35-65, 40-55 часов после введения рФВ.
[00172] В других дополнительных вариантах осуществления и в соответствии с вышесказанным стабилизация активности ФVIII с помощью рФВ по сравнению с пФВ может быть оценена по показателям, дополнительным ко времени полужизни ФVIII, и включающим среднее время удержания (СВУ) и площадь под кривой (ППК). В примерах осуществлений рФВ увеличивает СВУ приблизительно на 1-15 часов по сравнению с пФВ. В дополнительных осуществлениях рФВ увеличивает СВУ приблизительно на 1-25, 2-20, 3-15, 4-10, 5-9, 6-8 часов по сравнению с пФВ. В других дополнительных осуществлениях рФВ увеличивает СВУ ФVIII приблизительно на 10-80%, 15-65%, 20-60%, 25-55%), 30-50%, 35-45% по сравнению с пФВ. В других дополнительных осуществлениях среднее или процентное увеличение времени полужизни ФVIII сохраняется на протяжении как минимум 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 часов после введения рФВ. В определенных осуществлениях введение рФВ увеличивает СВУ ФVIII на величину, соответствующую вариантам от 1644 до 1987, перечисленным в Таблице 10, по сравнению с введением ФВ, полученного из плазмы крови.
[00173] В других дополнительных осуществлениях увеличение СВУ сохраняется на протяжении как минимум 5-125, 10-115, 15-105, 20-95, 25-85, 30-75, 35-65, 40-55 часов после введения рФВ. В определенных осуществлениях увеличение СВУ, вызванное введением рФВ, сохраняется на протяжении времени, соответствующего вариантам от 1090 до 1299, перечисленным в Таблице 8.
[00174] Дополнительные примеры различий между пФВ и рФВ приведены в следующей таблице:
[00175] В некоторых осуществлениях отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) составляет от 3:1 до 1:5. В дополнительных осуществлениях данное отношение составляет от 2:1 до 1:4. В других дополнительных осуществлениях данное отношение составляет от 5:2 до 1:4. В дополнительных осуществлениях данное отношение составляет от 3:2 до 1:3. В других дополнительных осуществлениях данное отношение составляет приблизительно 1:1, 1:2, 1:3, 1:4, 1:5, 2.Т, 2:3, 2:4, 2:5, 3:1, 3:2, 3:4, или 3:5. В других дополнительных осуществлениях данное отношение составляет 1.1:1, 1.2:1, 1.3:1, 1.4:1, 1.5:1, 1.6:1, 1.7:1, 1.8:1, 1.9:1, или 2:1. В определенных осуществлениях отношение прокоагулирующей активности рФVIII (ME рФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе, который применяется в описанном настоящим изобретением способе, составляет величину соответствующую вариантам от 1988 до 2140, перечисленным в Таблице 11,
[00176] В определенных вариантах осуществления рФВ и/или ФVIII (рекомбинантный или полученный из плазмы крови), применяемые в соответствии с настоящим изобретением, не являются модифицированными какими-либо сопряжениями, посттрансляционными или ковалентными модификациями. В определенных осуществлениях рФВ и/или ФVIII, заявленные в настоящем изобретении, не являются модифицированными водорастворимым полимером, включая, в частности, полиэтиленгликоль (ПЭГ), полипропиленгликоль, полиоксиалкилен, полисиаловую кислоту, гидроксиэтил углеводы, полиуглеводные и тому подобные вещества.
[00177] В других вариантах осуществления рФВ и/или ФVIII (рекомбинантный или полученный из плазмы крови), применяемые в соответствии с настоящим изобретением, являются модифицированными путем сопряжения, посттрансляционной модификации или ковалентной модификации, включая модификации N- или C-терминальных остатков, а также модификации некоторых боковых цепей, например, свободных сульфгидрильных групп, первичных аминов и гидроксильных групп. В одном из осуществлений водорастворимый полимер связан с протеином (прямо или через линкер) через лизиновую группу или другой первичный амин. В одном из осуществлений протеины заявленных в настоящем изобретении рФВ и/или ФVIII могут быть модифицированы путем сопряжения с водорастворимым полимером, включая, в частности, полиэтиленгликоль (ПЭГ), полипропиленгликоль, полиоксиалкилен, полисиаловую кислоту, гидроксиэтил углеводы, полиуглеводные и тому подобные вещества.
[00178] Водорастворимые полимеры, которые могут быть применены для модификации рФВ и/или ФVIII, включают нормальные и разветвленные структуры. Сопряженные полимеры могут быть присоединены прямо к коагулирующим протеинам, заявленным в данном изобретении, или, наоборот, могут быть присоединены через связывающее вещество. Неограничивающие примеры сопряжения протеина с водорастворимыми полимерами можно найти в U.S. Patent Nos. 4,640,835; 4,496,689; 4,301,144; 4,670,417; 4,791,192 и 4,179,337, а также в Abuchowski and Davis "Enzymes as Drugs," Holcenberg and Roberts, Eds., pp.367 383, John Wiley and Sons, New York (1981), and Hermanson G., Bioconjugate Techniques 2nd Ed., Academic Press, Inc. 2008.
[00179] Сопряжение протеина может быть осуществлено многочисленными методами, известными в данной области техники, например, смотрите Hermanson G., Bioconjugate Techniques 2nd Ed., Academic Press, Inc. 2008. Примеры включают соединение через пептидную связь между карбоксильной группой либо коагулирующего протеина, либо фрагмента водорастворимого полимера и аминогруппой противоположной молекулы или эфирную связь между карбоксильной группой одной молекулы и гидроксильной группой другой. Еще одна связь, с помощью которой коагулирующий протеин, заявленный в настоящем изобретении, может быть сопряжен с молекулой водорастворимого полимера, осуществляется через основание Шиффа; это связь между свободной аминогруппой фрагмента полимера, с которой реагирует альдегидная группа нередуцирующего окончания полимера, которая образуется при окислении периодатом (Jennings and Lugowski, J. Immunol. 1981; 127: 1011-8; Femandes and Gregonradis, Biochim Biophys Acta. 1997; 1341; 26-34). Образовавшееся основание Шиффа может быть стабилизировано путем специфического восстановления с NaCNBH3 с образованием вторичного амина. Альтернативный подход включает генерацию бестерминальных аминогрупп полимера путем восстановительного аминирования с NaCNBH3 после первичного окисления. Для связывания двух амино- или двух гидроксильных групп могут применяться бифункциональные реагенты. Например, полимер, содержащий аминогруппу, может быть привязан к аминогруппе коагулирующего протеина с помощью реагентов типа БСЗ (Бис(сульфосукцинимидил)суберат/Pierce, Рокфорд, Иллинойс). Помимо этого, гетеробифункциональные перекрестносвязывающие реагенты такие, как Сульфо-EMCS (N-ε-малеимидкапролокси) сульфосукцинимидин эфир/Pierce), могут, к примеру, применяться, чтобы связать амино- и тиоловую группы. В других осуществлениях альдегидная функциональная группа, такая как ПЭГ алкоксид плюс диэтил ацеталь бромацетальдегид; ПЭГ плюс диметилсульфоксид и ангидрид уксусной кислоты и ПЭГ хлорид плюс фенолят 4-гидроксибензальдегида, сукцинимидил активные эфиры, активированный дитиокарбонат ПЭГ, 2,4,5-трихлорфенилхлорформат и активированный Р-нитрофенилхлорформатом ПЭГ могут применяться в сопряжении коагулирующего протеина.
[00180] В некоторых вариантах осуществления рФВ, применяемый согласно способам, заявленным в настоящем изобретении, созревал in vitro в присутствии фурина. В дополнительных осуществлениях фурин является рекомбинантным фурином.
[00181] В дополнительных вариантах осуществления рФВ и/или рФVIII, применяемые согласно способам, заявленным в настоящем изобретении, получали путем экспрессии в клеточной культуре млекопитающего с применением способов, известных в данной области техники. В отдельных осуществлениях клеточная культура млекопитающего содержит клетки СНО. В дополнительных осуществлениях рФВ и рФVIII экспрессируются совместно в одной клеточной культуре. В таких осуществлениях рФВ и рФVIII очищают совместно или раздельно с применением способов, известных в данной области техники. В других осуществлениях рФВ и рФVIII экспрессируются в разных культурах.
[00182] В примере осуществления заявленный в изобретении рФВ содержит протеин рФВ, который изолирован от клеточной экспрессирующей системы СНО. В дополнительном осуществлении выведение пропептида опосредовано in vitro воздействием на про-ФВ рекомбинантного фурина - в другом дополнительном осуществлении фурин, который применяется для выведения пропептида, является рекомбинантным фурином. В другом дополнительном осуществлении отсутствуют полностью гликозилированные гликаны/гликаны групп крови АВО.
[00183] В других дополнительных осуществлениях рФВ, применяемый согласно способам и составам, заявленным в настоящем изобретении, получали путем экспрессии в подходящей эукариотической системе- хозяине. Примеры эукариотических клеток включают, в частности, клетки млекопитающих такие, как СНО, COS, НЕК 293, ВНК, SK-Нер и HepG2; клетки насекомых, например, клетки SF9, клетки SF21, клетки S2 и клетки High Five; а также дрожжевые клетки, например, клетки Saccharomyces или Schizosaccharomycess. В одном из осуществлений ФВ может экспрессироваться в дрожжевых клетках, клетках насекомых, клетках птиц, клетках млекопитающих и т.д. Например, в клеточной линии человека, клеточной линии хомяка или клеточной линии мыши. В одном отдельном осуществлении клеточная линия является клеточной линией СНО, ВНК или НЕК. Как правило, для экспрессии ФВ, заявленного в настоящем изобретении, могут использоваться клетки млекопитающих, например, клетки СНО из стабильной клеточной линии.
[00184] В определенных осуществлениях последовательность нуклеиновых кислот, которая содержит последовательность, кодирующую ФВ, может быть вектором. Вектор может доставляться вирусом или являться плазмидой. Последовательность нуклеиновых кислот, кодирующая протеин, может являться специфическим геном или его функциональной частью. В одном из осуществлений этот протеин является как минимум биологически активной частью ФВ.
[00185] Для экспрессии ФВ может использоваться широкий спектр векторов, принадлежащих к эукариотическим экспрессионным векторам. Примеры векторов эукариотической экспрессии включают: (i) для экспрессии в дрожжах такие векторы, как pAO, pPIC, pYES, рМЕТ, использующие такие промоторы, как АОX1, GAP, GAL1, AUG1 и т.д.; (ii) для экспрессии в клетках насекомых такие векторы, как рМТ, рАс5, pIB, pMIB, рВАС и т.д., использующие такие промоторы, как РН, p10, МТ, Ас5, OpIE2, gp64, polh и т.д., и (iii) для экспрессии в клетках млекопитающих такие векторы, как pSVL, pCMV, pRc/RSV, pcDNA3, pBPV и т.д. и векторы, полученные из вирусных систем таких, как вирус осповакцины, адено-ассоциированные вирусы, вирусы герпеса, ретровирусы и т.д. использующие такие промоторы, как CMV, SV40, EF-1, UbC, RSV, ADV, BPV, и β-актин.
[00186] В некоторых осуществлениях настоящего изобретения последовательность нуклеиновых кислот дополнительно содержит другие последовательности, подходящие для контролируемой экспрессии протеина, такие, как последовательность промотера, энхансеры, ТАТА-боксы, сайты инициации транскрипции, полилинкеры, сайты рестрикции, поли-А последовательности, последовательности процессирования протеина, маркеры отбора и тому подобные, которые в целом известны специалисту в данной области техники.
[00187] В определенных осуществлениях способы клеточного культивирования, применяемые в настоящем изобретении, могут включать использование микроносителя. В некоторых осуществлениях клеточное культивирование согласно этим осуществлениям может производиться в большом биореакторе при условиях, которые обеспечивают высокий удельный объем площади поверхности клеточной культуры для достижения высокой клеточной плотности и экспрессии протеина. Одним из способов обеспечения таких условий роста является применение в биореакторах с механическим перемешиванием микроносителей для клеточного культивирования. Схема выращивания клеток на микроносителях впервые была описана ван Везелем (van Wezel, A.L., Nature 216: 64-5 (1967)) и включает присоединение клеток к поверхности небольших твердых частиц, распределенных в питательной среде. Такие методы обеспечивают высокое отношение площади поверхности к объему и, таким образом, создают возможность эффективного использования питательных веществ. Более того, при экспрессии секретируемых протеинов в эукариотической клеточной линии повышенное отношение площади поверхности к объему создает возможность для более высоких уровней секреции и, таким образом, для большего выхода протеина в надосадочную жидкость клеточной культуры. Наконец, эти методы дают возможность легко увеличить эукариотеческие экспрессируемые культуры.
[00188] Клетки, которые экспрессируют ФВ, во время роста клеточной культуры могут быть связаны со сферическим или пористым микроносителем. Микроноситель может принадлежать группе микроносителей на основе декстрана, коллагена, пластика, желатина, целлюлозы и других веществ, описанных в Butler (1988. In: Spier & Griffiths, Animal Cell Biotechnology 3: 283-303). Также возможно вырастить клетки до биомассы на сферических микроносителях и пересеять эти клетки на пористый микроноситель, когда они достигнут конечной биомассы ферментера и перед образованием экспрессируемого протеина либо наоборот. Подходящие сферические микроносители могут включать микроносители с гладкой поверхностью такие, как Цитодекс™ 1, Цитодекс™ 2, and Цитодекс™ 3 (GE Healthcare) и макропористые микроносители такие, как Цитопор™ 1, Цитопор™ 2, Цитолайн™ 1 и Цитолайн™ 2 (GE Healthcare).
[00189] В отдельных осуществлениях рФВ экспрессируется в клетках, которые были культивированы в питательных средах для выращивания культур клеток и которые вырабатывают выкомолекулярный рФВ. Термины "раствор для культивирования клеток", "среда для культивирования клеток" и "надосадочная жидкость клеточной культуры" относятся к аспектам процесса культивирования клеток, которые в целом хорошо известны в данной области техники. В контексте настоящего изобретения раствор для культивирования клеток может включать в себя среду для культивирования клеток и надосадочную жидкость клеточных культур. Среды для культивирования клеток добавляются извне в раствор для культивирования клеток, в некоторых случаях совместно с добавками, чтобы обеспечить наличие питательных веществ и других компонент для культивирования клеток, экспрессирующих ФВ. Надосадочная жидкость клеточной культуры обозначает раствор для культивирования клеток, который содержит питательные вещества и другие компоненты среды для культивирования клеток, а также продукты вырабатываемые, метаболизируемые и/или выделяемые из клеток в процессе культивирования. В дополнительных осуществлениях эти среды могут быть животными безбелковыми и химически определенными. Способы приготовления животных безбелковых и химически определенных сред для культивирования известны в данной области техники и приведены, например, в US 2008/0009040 и US 2007/0212770, которые в полном объеме включены в настоящую заявку посредством ссылок для всестороннего изучения, в особенности того, что касается сред для культивирования клеток. "Безбелковый" и связанные с ним термины относятся к протеину, который является экзогенным или отличным от клеток в культуре, которые в норме выделяют протеины во время роста. В другом осуществлении среда для культивирования является свободной от полипептидов. В другом осуществлении среда для культивирования является бессывороточной. В другом осуществлении среда для культивирования является свободной от животных протеинов. В другом осуществлении среда для культивирования является свободной от животных компонент. В другом осуществлении среда для культивирования содержит протеин, например, животный протеин из сыворотки, такой как фетальная телячья сыворотка. В другом осуществлении культура содержит рекомбинантные протеины, которые были добавлены экзогенно. В другом осуществлении протеины взяты от сертифицированного беспатогенного животного. Термин "химически определенный", при использовании в настоящем описании, обозначает, что среда не содержит никаких неопределенных добавок, таких как, например, экстракты животных компонент, органов, желез, растений или дрожжей. Соответственно, каждая компонента химически определенной среды точно определена. В предпочтительном варианте осуществления среды не содержат животных компонент и протеинов.
[00190] В отдельных осуществлениях культура клеток, которые экспрессируют ФВ, может сохраняться как минимум около 7 дней или как минимум около 14 дней, 21 дня, 28 дней, или как минимум около 5 недель, 6 недель, 7 недель, или как минимум около 2 месяцев, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18 месяцев и дольше. Клеточная плотность, при которой клеточная культура поддерживается и продуцирует рекомбинантный протеин ФВ, зависит от условий культивирования и среды, используемой для экспрессии протеина. Специалист в данной области техники сможет определить оптимальную клеточную плотность для клеточной культуры, продуцирующей ФВ. В одном из осуществлений культура поддерживается при значении клеточной плотности приблизительно в 0.5×106 и 4×107 клеток/мл на протяжении длительного периода времени. В другом осуществлении клеточная плотность поддерживается при концентрации приблизительно от 1.0×106 и до 1.0×107 клеток/мл на протяжении длительного периода времени. В других осуществлениях клеточная плотность поддерживается при концентрации приблизительно от 1.0×106 и до 4.0×106 клеток/мл на протяжении длительного периода времени. В других осуществлениях клеточная плотность поддерживается при концентрации приблизительно от 1.0×106 и до 4.0×106 клеток/мл на протяжении длительного периода времени. В других осуществлениях клеточная плотность может поддерживается при концентрации приблизительно от 2.0×106 и до 4.0×106, или от 1.0×106 и до 2.5×106, или от 1.5×106 и до 3.5×106, или в любом другом схожем диапазоне на протяжении длительного периода времени. После установленного времени нахождения в клеточной культуре рФВ может быть удален из экспрессирующей системы способами, известными в данной области техники.
[00191] В одном отдельном осуществлении клеточная плотность непрерывной клеточной культуры для продуцирования рФВ поддерживается при концентрации не большей, чем 2.5×106 клеток/мЛ на протяжении длительного периода. В другом отдельном осуществлении поддерживается клеточная плотность не большая, чем 2.0×106 клеток/мЛ, 1.5×106 клеток/мЛ, 1.0×106 клеток/мЛ, 0.5×106 клеток/мЛ или меньше. В одном из осуществлений клеточная плотность поддерживается в диапазоне от 1.5×106 клеток/мЛ до 2.5×106 клеток/мЛ.
[00192] В одном отдельном осуществлении вышеописанного выращивания клеточных культур раствор для культивирования клеток содержит среду с добавками, которая содержит медь. Подобные растворы для культивирования клеток описаны, например, в US 2012/0035110, зарегистрированном 8 июля 2011 г., который в полном объеме включен в настоящую заявку посредством ссылки для всестороннего изучения, в особенности того, что касается методов культивирования клеток и составов для продуцирования рекомбинантного ФВ.
[00193] В дополнительных осуществлениях после очистки (отдельно либо совместно) от клеточной культуры млекопитающего комплекс рФVIII/рФВ перерастворяли перед введением. В других дополнительных осуществлениях рФВ обрабатывали фурином до или после перерастворения комплекса рФVIII/рФВ. В дополнительных осуществлениях фурин является рекомбинантным фурином.
[00194] В других дополнительных осуществлениях рФВ, заявленный в настоящем изобретении, не подвергается воздействию металлопротеиназы ADAMTS13, что приводит к наличию ультра-больших частиц (то есть содержащих 10 или более субъединиц) в рФВ составах, заявленных в изобретении.
[00195] В определенных вариантах осуществления рФВ и/или рФVIII, применяемые в способах, заявленных в настоящем изобретении, находятся в составах, содержащих буфер, сахар и/или сахарные спирты (включая, в частности, трегалозу и маннитол), стабилизатор (такой, как глицин) и поверхностно-активное соединение (такое, как полисорбат 80). В дополнительных осуществлениях составы, содержащие рФVIII, могут также содержать натрий, гистидин, кальций и глутатион.
[00196] В одном из вариантов осуществления составы, содержащие рФВ и/или рФVIII лиофилизируют перед введением. Лиофилизация проводится с помощью методов, известных в данной области техники, и должна оптимизироваться для разрабатываемых составов [Tang et al., Pharm Res. 21: 191-200, (2004) and Chang et al., Pharm Res. 13: 243-9 (1996)].
[00197] Способы приготовления фармацевтических составов могут включать одно или более из следующих действий: добавление стабилизирующего вещества, как описано в настоящей заявке, в указанную смесь перед лиофилизированием, добавление как минимум одного вещества из ряда объемообразующих веществ, вещества, регулирующего осмолярность и поверхностно-активного соединения, как описано в настоящей заявке, в указанную смесь перед лиофилизированием. Лиофилизированный состав в одном варианте осуществления состоит из одного или более следующих веществ: буфера, объемообразующего вещества и стабилизатора. В этом варианте осуществления оценивается польза поверхностно-активного соединения, и оно применяется в случаях, когда агрегация во время лиофилизации или перерастворения становится проблематичной. Чтобы поддерживать состав в границах стабильных значений pH во время лиофилизации добавляют соответствующее буферное вещество.
[00198] Стандартная практика перерастворения лиофилизированного вещества состоит в восполнении объема чистой водой или стерильной водой для инъекций (ВДИ) (обычно в количестве, эквивалентном объему, который был удален во время лиофилизации), хотя слабые растворы антибактериальных веществ иногда используются при получении фармацевтических препаратов для парентерального введения [Chen, Drug Development and Industrial Pharmacy, 18: 1311-1354 (1992)]. Соответственно, предлагаются способы приготовления перерастворенных композиций рекомбинантного ФВ (с или без рекомбинантного фактора VIII), которые включают этап добавления растворителя в лифофилизированную композицию рекомбинантного ФВ, заявленного в настоящем изобретении.
[00199] Лиофилизированное вещество может быть перерастворено в виде водного раствора. Существует множество водных носителей, например, стерильная вода для инъекций, вода с антисептиками для многоразового использования или вода с необходимым количеством поверхностно-активных соединений (например, водная суспензия, которая содержит активное соединение с добавлением вспомогательных веществ, подходящих для изготовления водных суспензий). В разных вариантах осуществления такими вспомогательными веществами являются суспендирующие вещества, например и в частности, натриевая соль карбоксиметилцеллюлозы, метилцеллюлоза, гидроксипропилметилцеллюлоза, альгинат натрия, поливинилпирролидон, трагант и сенегальская камедь; диспергирующими или смачивающими веществами являются природные фосфатиды, например и в частности, лецитин, или продукты конденсации окиси алкилена с жирными кислотами, например и в частности, стеарат полиоксиэтилена, или продукты конденсации окиси этилена с длинноцепочечными алифатическими спиртами, например и в частности, гептадекаэтил-энеоксицетанол, или продукты конденсации окиси этилена с неполными эфирами, полученными из жирных кислот, и гекситов, таких как сорбит моноолеат полиоксиэтилена, или продукты конденсации окиси этилена с неполными эфирами, полученными из жирных кислот и гексит ангидридов, например и в частности, сорбитан моноолеат полиоксиэтилена. В различных вариантах осуществления водные суспензии также содержат один или более антисептиков, например и в частности, этил или п-пропил, р-гидроксибензоат.
[00200] В отдельных осуществлениях составы, заявленные в настоящем изобретении, являются жидкими составами для введения с помощью шприца или другой емкости для хранения. В дополнительных осуществлениях данные жидкие составы получают из лиофилизированного вещества, описанного в настоящем изобретении и перерастворенного в виде водного раствора.
[00201] В другом варианте осуществления составы, заявленные в настоящем изобретении, добавочно содержат один или более фармацевтически приемлемых носителей. Выражения "фармацевтически" или "фармакологически" приемлемый относятся к молекулярным частицам или составам, которые являются стабильными, препятствуют разрушению протеина, такому как процессы агрегации и расщепления, и в дополнение не вызывают аллергических или других нежелательных реакций при введении способами, хорошо известными в данной области техники и описанными ниже. "Фармацевтически приемлимые носители" включают любые клинически применяемые растворители, диспергирующие среды, оболочки, антибактериальные и антигрибковые вещества, изотонические и замедляющие абсорбцию вещества и т.п., включая вещества, упомянутые выше.
Применение заявленных в изобретении составов в способах лечения болезни
[00202] Одним из преимуществ введения пациентам рФВ для лечения нарушений свертываемости крови является то, что более высокая специфическая активность рФВ по сравнению с пФВ позволяет варьировать количество вводимого рФВ и количество повторных введений рФВ (с или без совместно вводимого ФVIII). К тому же, рФВ-составы обеспечивают дальнейшую вариативность повторных введений одного лишь рФВ после первого совместного применения рФВ и ФVIII без потребности добавочного введения ФVIII. Следует принимать во внимание, и как дополнительно и детально описано в настоящей заявке, совместно вводимый ФVIII может быть как рекомбинантным, так и полученным из плазмы крови.
[00203] В одном варианте осуществления введение рФВ согласно настоящему изобретению приводит к повышенному уровню плазменного ФVIII и/или его активности у испытуемого, чем те, что наблюдаются у испытуемых, которым вводили пФВ. Как обсуждалось выше, увеличение уровней ФVIII и его активности может быть измерено с использованием методов, являющихся стандартными в данной области техники, и, таким образом, становится возможным определение необходимых дозировок рФВ с или без ФVIII.
[00204] Уровень дозировки и график приема при разовом или многоразовом введении рФВ (с или без ФVIII) назначается лечащим врачом. При профилактике или лечении заболевания необходимая дозировка зависит от типа болезни, которая лечится (например, болезнь Виллебранда), тяжести и течения болезни, от того, применяется лекарство в профилактических или терапевтических целях, предварительного лечения, истории болезни пациента и его реакции на лекарство, и выбора штатного врача.
[00205] В дополнительных осуществлениях изобретения и согласно вышесказанному, лечение нарушений свертываемости крови, таких как БВ или гемофилия A, может включать первичную терапию либо одним рФВ, либо в комбинации с ФVIII, за которой следует одно или более повторных введений только рФВ, рФВ совместно с ФVIII или только ФVIII. Выбор первичного, а затем и повторных введений, будет частично зависеть от болезни, которая лечится. Например, у пациентов с БВ существует определенный уровень ФVIII, но стабильность этого ФVIII в общем случае нарушена, так как у этих пациентов наблюдается недостаточность ФВ. Таким образом, лечение пациентов с БВ в некоторых осуществлениях изобретения может включать первичную терапию рФВ и pФVIII, за которой следуют повторные введения только рФВ. В других осуществлениях первичная терапия может проводиться одним рФВ, а последующие повторные введения включать как рФВ, так и pФVIII. В других осуществлениях первичное и последующие повторные введения могут включать совместное введение рФВ и pФVIII. Аналогично, больные гемофилией A (у которых наблюдается недостаточность ФVIII) могут проходить первичную терапию рФВ и pФVIII, а последующее повторное лечение может включать введение только pФVIII или только рФВ. В других осуществлениях первичная терапия может проводиться одним pФVIII, а последующее повторное лечение включать совместное введение рФВ и pФVIII.
[00206] В дополнительных вариантах осуществления рФВ вводят испытуемым в диапазоне дозировок 0.5 МЕ/кг-200 МЕ/кг. В некоторых осуществлениях рФВ вводят в диапазоне дозировок 1-190, 5-180, 10-170, 15-160, 20-150, 25-140, 30-130, 35-120, 40-110, 45-100, 50-90, 55-80, или 60-70 МЕ/кг. В других осуществлениях и согласно вышесказанному рФВ (с или без ФVIII) вводят испытуемым в дозировках в приблизительном диапазоне от 1 МЕ/кг до 150 МЕ/кг рФВ. В других осуществлениях рФВ и pФVIII вводят в дозировках в приблизительном диапазоне от 1.5 МЕ/кг до 150 МЕ/кг, от 2 МЕ/кг до 50 МЕ/кг, от 5 МЕ/кг до 40 МЕ/кг, от 10 МЕ/кг до 20 МЕ/кг, от 10 МЕ/кг до 100 МЕ/кг, от 25 МЕ/кг до 75 МЕ/кг и от 40 МЕ/кг до 75 МЕ/кг. В других осуществлениях рФВ вводят в дозировках 2, 5, 7.5, 10, 15, 20, 25, 30, 35, 40, 45 или 50 МЕ/кг. Следует принимать во внимание, и как дополнительно описано в настоящей заявке, что необходимые дозировки рФВ (или рФВ совместно с ФVIII) могут быть уточнены с помощью аналитических методов определения уровней крови в сочетании с соответствующими показателями доза-ответ. В одном из осуществлений рФВ вводят испытуемым в дозировках, соответствующим вариантам от 2141 до 2338, перечисленным в Таблице 12.
[00207] В других дополнительных осуществлениях рФВ вводят в таких дозировках, которые приводят к увеличению времени полужизни плазменного ФVIII приблизительно в 1.0-4.5, 1.5-4.0, 2.0-3.5, 2.5-3.0 раз. В других дополнительных осуществлениях дозировка и/или частота введения рФВ является такой, что увеличение времени полужизни ФVIII сохраняется на протяжении как минимум 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 часов после введения рФВ. В других дополнительных осуществлениях дозировка и/или частота введения рФВ является такой, что увеличение времени полужизни ФVIII сохраняется на протяжении как минимум 5-125, 10-115, 15-105, 20-95, 25-85, 30-75, 35-65, 40-55 часов после введения рФВ. В одном из осуществлений рФВ вводят в таких дозировках, которые приводят к увеличению времени полужизни плазменного ФVIII в количество раз, соответствующее вариантам от 1046 до 1089, перечисленным в Таблице 7.
[00208] Как обсуждалось выше, заявленный в настоящем изобретении рФВ оказывает усиленное действие на стабильность ФVIII по сравнению с действием пФВ. В определенных вариантах осуществления рФВ вводят в таких дозировках и/или с такой частотой, которые приводят к увеличению среднего времени полужизни ФVIII приблизительно на 1-15, 2-14, 3-13, 4-12, 5-11, 6-10, 5-9, 6-8 часов. В других дополнительных осуществлениях рФВ вводят в таких дозировках и/или с такой частотой, которые приводят к увеличению времени полужизни ФVIII приблизительно на 10%-75% по сравнению с пФВ. В других дополнительных осуществлениях рФВ увеличивает время полужизни ФVIII приблизительно на 10-80%, 15-65%, 20-60%, 25-55%, 30-50%, 35-45% по сравнению с пФВ. В других дополнительных осуществлениях среднее или процентное увеличение времени полужизни ФVIII сохраняется на протяжении как минимум 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 часов после введения рФВ. В других дополнительных осуществлениях увеличение времени полужизни ФVIII сохраняется как минимум 5-125, 10-115, 15-105, 20-95, 25-85, 30-75, 35-65, 40-55 часов после введения рФВ. Следует принимать во внимание, что увеличение стабильности ФVIII, его времени полужизни и/или активности может быть достигнуто способами, известными в данной области техники, включая, в частности, анализ коагулирующей активности. В других осуществлениях введение рФВ увеличивает время полужизни ФVIII на величину, соответствующую вариантам от 1300 до 1643, перечисленным в Таблице 9, по сравнению с ФВ, полученным из плазмы крови.
[00209] Как обсуждается в настоящей заявке, стабилизация активности ФVIII рФВ по сравнению с пФВ может быть оценена по показателям, дополнительным ко времени полужизни ФVIII, и включающим среднее время удержания (СВУ) и площадь под кривой (ППК). В примерах осуществлений изобретения рФВ вводят в таких дозировках и/или с такой частотой, которые приводят к увеличению СВУ на 1-15 часов по сравнению с пФВ. В дополнительных осуществлениях рФВ увеличивает СВУ приблизительно на 1-25, 2-20, 3-15, 4-10, 5-9, 6-8 часов по сравнению с пФВ. В других дополнительных осуществлениях рФВ увеличивает СВУ ФVIII приблизительно на 10-80%, 15-65%, 20-60%, 25-55%, 30-50%, 35-45% по сравнению с пФВ. В других дополнительных осуществлениях среднее или процентное увеличение времени полужизни ФVIII сохраняется на протяжении как минимум 10, 20, 30, 40, 50, 60, 70, 80, 90, 100 часов после введения рФВ. В других дополнительных осуществлениях увеличение СВУ сохраняется как минимум 5-125, 10-115, 15-105, 20-95, 25-85, 30-75, 35-65, 40-55 часов после введения рФВ. В других осуществлениях введение рФВ увеличивает СВУ ФVIII на величину, соответствующую вариантам от 1300 до 1643, перечисленным в Таблице 9, по сравнению с введением ФВ, полученным из плазмы крови.
[00210] В дополнительных вариантах осуществления вводимые пациентам дозы рФВ сопоставимы с дозами, которые применяют при введении пФВ/пФVIII.
[00211] рФВ-составы с или без ФVIII могут содержаться в фармацевтических препаратах, как описано в настоящей заявке. Подобные препараты могут вводиться перорально, местно, трансдермально, парентерально, с помощью спрея для ингаляций, вагинально, ректально или с помощью внутричерепной инъекции. Используемый в настоящей заявке термин парентеральный включает подкожные инъекции, внутривенные, внутримышечные, интрацистернальные инъекции или инфузионные методы. Рассматривается также введение путем внутривенных, внутрикожных, внутримышечных, интрамаммарных, внутрибрюшинных, интратекальных, ретробульбарных, внутрилегочных инъекций или хирургической имплантации в отдельном месте. В общем случае составы не содержат пирогенные вещества, так же, как и другие примеси, которые могут быть вредными для реципиента.
[00212] В одном из вариантов осуществления препараты, заявленные в настоящем изобретении, применяют в виде первичного болюсного введения, за которым следует непрерывная инфузия для поддержания терапевтического уровня циркулирующего в крови лекарственного препарата. В другом примере заявленное вещество вводят в виде одноразовой дозы. Специалисты в данной области техники легко смогут оптимизировать эффективные дозировки и график применения в соответствии со своей врачебной практикой и клиническим состоянием отдельно взятого пациента. Способ применения может, не ограничиваясь этим, заключаться во внутривенном, внутрибрюшинном, подкожном или внутримышечном введении. Частота применения зависит от фармакокинетических параметров веществ и способа применения. Оптимальный фармацевтический состав определяется специалистом в данной области техники в зависимости от способа применения и желаемой дозировки. Смотрите, например, Remington's Pharmaceutical Sciences, 18th Ed., 1990, Mack Publishing Co., Easton, Pa. 18042 pages 1435-1712, раскрытие которой в полном объеме включено в настоящую заявку посредством ссылки для всестороннего изучения, в особенности того, что касается приготовления составов, способов применения и дозировок фармацевтических препаратов. Подобные препараты влияют на физическое состояние, стабильность, степень выделения in vivo и степень расщепления in vivo вводимых веществ. В зависимости от способа применения рассчитывается необходимая доза в соответствии с массой тела, площадью поверхности тела или размерами органов. Необходимые дозировки могут быть уточнены с помощью общепринятых аналитических методов определения уровней крови в сочетании с соответствующими показателями доза-ответ. Окончательная схема приема лекарственного средства определяется штатным врачом и учитывает различные факторы, которые изменяют действие препарата, например, специфическую активность препарата, степень повреждения и ответную реакцию пациента, возраст, состояние, массу тела, пол и образ питания пациента, опасность инфекции, время применения и другие клинические факторы. В качестве примера можно привести стандартную дозу рекомбинантного ФВ, заявленного в настоящем изобретении, которая составляет приблизительно 50 Е/кг, что эквивалентно 500 мкг/кг. Так как исследования продолжаются, будет появляться дополнительная информация относительно необходимых уровней дозировок и продолжительности лечения различных заболеваний и состояний.
[00213] В некоторых осуществлениях испытуемым вводят только рФВ. В некоторых осуществлениях рФВ вводят испытуемым в комбинации с одним или более факторами свертывания крови. В дополнительных осуществлениях фактором свертывания крови, который вводят совместно с рФВ, является ФVIII. В других дополнительных осуществлениях рФВ вводят перед, после либо одновременно с таким фактором свертывания крови, как ФVIII. В определенных осуществлениях рФВ и ФVIII вводят совместно в одном составе. Следует принимать во внимание, что ФVIII, который вводят совместно с рФВ, может быть как рекомбинантным, так и полученным из плазмы крови.
[00214] В дополнительных осуществлениях рФВ (с или без ФVIII) вводят испытуемым не чаще, чем раз в день. В дополнительных осуществлениях рФВ (с или без ФVIII) вводят испытуемым: не чаще, чем через день, не чаще, чем раз в три дня, не чаще, чем раз в четыре дня, не чаще, чем раз в пять дней, не чаще, чем раз в неделю, не чаще, чем раз в месяц. В других дополнительных осуществлениях рФВ (с или без ФVIII) вводят испытуемым не чаще, чем дважды в день.
[00215] В дополнительных осуществлениях рФВ и ФVIII вводят испытуемым совместно в качестве первичной дозы, а далее последующее повторное применение проводят с одним только рФВ. В других осуществлениях повторное применение проводят с рФВ и ФVIII.
[00216] В других дополнительных осуществлениях рФВ (с или без ФVIII) вводят в такой дозировке, при которой активность плазменного ФVIII стабилизируется на приблизительный период от 10 до 90 часов. В дополнительных осуществлениях активность плазменного ФVIII стабилизируется как минимум на 12, 24, 36, 48 или 72 часа. Следует принимать во внимание, что стабилизированная активность плазменного ФVIII может являться активностью эндогенного ФVIII, совместно вводимого ФVIII (полученного из плазмы крови или рекомбинантного) или комбинацией эндогенного и совместно вводимого ФVIII.
[00217] В некоторых осуществлениях рФВ и ФVIII вводят совместно в такой дозировке, при которой продление in vivo активности плазменного ФVIII стабилизируется на протяжении как минимум 12, 24, 36, 48 или 72 часов. В дополнительных осуществлениях активность плазменного ФVIII стабилизируется приблизительно на период от 10 до 90 часов. В других дополнительных осуществлениях увеличение времени полужизни плазменного ФVIII у пациентов сохраняется на протяжении как минимум 24, 36, 48, 72, 90, 120 или 168 часов. Совместно вводимый ФVIII может являться как рФVIII, так и пФVIII. В некоторых осуществлениях активность плазменного ФVIII после совместного введения рФВ и ФVIII стабилизируется на период времени, соответствующий вариантам от 1090 до 1299, перечисленным в Таблице 8.
[00218] В предпочтительных вариантах осуществления настоящего изобретения предложены способы лечения нарушений свертываемости крови, включающих гемофилию и болезнь Виллебранда (БВ).
[00219] Используемый здесь термин "гемофилия" обозначает группу заболеваний, которая в широком смысле характеризуется сниженным свертыванием крови или сниженной коагуляцией. Гемофилия может относиться к типу A, типу B или типу C, либо к комбинации всех трех типов болезни. Гемофилия типа A (гемофилия А) обусловлена снижением либо утратой активности фактора VIII (ФVIII) и является наиболее известной из подтипов гемофилии. Гемофилия типа B (гемофилия B) вызвана снижением либо утратой функции свертывания фактора XI (ФХI). Гемофилия типа C (гемофилия C) является последствием снижения либо утраты свертывающей активности фактора XI (ФХI). Гемофилии A и B являются Х-сцепленными заболеваниями, в то время как гемофилия C аутосомна. Обычные способы лечения гемофилии включают как профилактическое введение, так и введение по необходимости свертывающих факторов таких, как ФVIII, ФXI, включая Бебулин®-УН, и ФXI, а также ОЕЙБА-VH, десмопрессин и вливание плазмы крови.
[00220] Используемый здесь термин "болезнь Виллебранда" обозначает группу заболеваний, вызванных дефицитом фактора Виллебранда. Фактор Виллебранда способствует накоплению и прикреплению тромбоцитов к стенкам кровеносных сосудов, что необходимо для нормального свертывания крови. Существуют несколько типов болезни Виллебранда. В следующей таблице кратко изложены характеристики различных типов БВ:
[00221] Способы лечения нарушений свертываемости крови включают введение рФВ или комбинации рФВ и pФVIII нуждающимся в лечении пациентам в соответствии с любыми способами введения, описанными в настоящем изобретении и известными в данной области техники. Такие пациенты могут страдать любыми нарушениями свертываемости крови, включая, в частности, болезнь Виллебранда и гемофилию. Следует принимать во внимание, что любой тип болезни Виллебранда, включая любой из описанных в предыдущей таблице типов, может лечиться в согласно способов и с применением составов, описанных в настоящем изобретении.
[00222] В некоторых осуществлениях рФВ (с или без ФVIII) вводят испытуемым таким образом, что уровень прокоагулирующей активности фактора VIII (ФVIII:К) в плазме крови испытуемого через 24, 36, 48 или более часов после введения составляет как минимум 90% от уровня активности ФVIII:К, которая наблюдалась в плазме крови через 1 час после введения. В дополнительных осуществлениях уровень ФVIII:К в плазме крови испытуемого через 24, 36, 48 или более часов после введения составляет как минимум от 50% до 100% от уровня активности ФVIII:К, которая наблюдалась в плазме крови через 1 час после введения. В других дополнительных осуществлениях уровень ФVIII:K в плазме крови испытуемого через 24, 36, 48 или более часов после введения составляет как минимум 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99%, 100% от уровня активности ФVIII:K, которая наблюдалась в плазме крови через 1 час после введения.
Применение рФВ
[00223] В одном из вариантов в раскрытии сущности настоящего изобретения предлагаются способы лечения болезни Виллебранда (БВ) или гемофилии A у нуждающихся в лечении пациентов, которые включают введение состава, содержащего рекомбинантный фактор Виллебранда (рФВ), таким образом, что повышается стабильность фактора VIII (ФVIII) по сравнению со временем полужизни ФVIII у испытуемых, которым вводили составы, содержащие фактор Виллебранда, полученный из плазмы крови (пФВ). В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В другом осуществлении рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ и обладающим более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00224] В одном из осуществлений заявленный способ включает введение рФВ-состава таким образом, что стабильность фактора ФVIII увеличивается как минимум на 10%, 20%, 30%, 2 ч, 4 ч, 6 ч или на величину, соответствующую вариантам от 1300 до 1643, перечисленным в Таблице 9, по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В другом осуществлении рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ и обладающим более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00225] В одном из осуществлений заявленный способ включает введение рФВ-состава таким образом, что стабильность фактора ФVIII увеличивается как минимум на 10% по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00226] В одном из осуществлений заявленный способ включает введение рФВ-состава таким образом, что стабильность фактора ФVIII увеличивается как минимум на 20% по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00227] В одном из осуществлений заявленный способ включает введение рФВ-состава таким образом, что стабильность фактора ФVIII увеличивается как минимум на 30% по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00228] В одном из осуществлений заявленный способ включает введение рФВ-состава, при чем комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00229] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 30% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00230] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 50% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00231] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 70% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00232] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00233] В одном из осуществлений заявленный способ включает введение дозы рФВ-состава, который содержит от 10 МЕ/кг до 40 МЕ/кг рФВ:РКо активности, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В отдельном осуществлении состав содержит от 20 МЕ/кг до 30 МЕ/кг рФВ:РКо активности. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00234] В одном из осуществлений заявленный способ включает введение дозы рФВ-состава, который содержит от 25 МЕ/кг до 75 МЕ/кг рФВ:РКо активности, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В отдельном осуществлении состав содержит от 40 МЕ/кг до 60 МЕ/кг рФВ:РКо активности. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00235] В одном из осуществлений заявленный способ включает введение дозы рФВ-состава, который содержит от 75 МЕ/кг до 125 МЕ/кг рФВ:РКо активности, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В отдельном осуществлении состав содержит от 75 МЕ/кг до 100 МЕ/кг рФВ:РКо активности. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00236] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором испытуемым вводят дозу рФВ, соответствующую вариантам от 2141 до 2338, перечисленным в Таблице 12, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00237] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В другом осуществлении рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ и обладающим более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3
[00238] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 30% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00239] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 50% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00240] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 70% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00241] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00242] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором рФВ в составе обладает специфической активностью от 40 мЕ/мкг до 60 мЕ/мкг, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00243] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором рФВ в составе обладает специфической активностью в, как минимум, 60 мЕ/мкг, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00244] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором рФВ в составе обладает специфической активностью в, как минимум, 80 мЕ/мкг, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00245] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором рФВ в составе обладает специфической активностью, соответствующей вариантам от 1 до 133, перечисленным в Таблице 1, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00246] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В другом осуществлении рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ и обладающим более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00247] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 30% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00248] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 50% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00249] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 70% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00250] В одном из осуществлений заявленный способ включает введение рФВ-состава, при этом рФВ-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00251] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором у испытуемых стабилизируется ФVIII на протяжении как минимум 18 часов после введения, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00252] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором у испытуемых стабилизируется ФVIII на протяжении как минимум 24 часов после введения, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00253] В одном из осуществлений заявленный способ включает введение рФВ-состава, при котором у испытуемых стабилизируется ФVIII на протяжении как минимум 30 часов после введения, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
Применение рФВ/рФVIII
[00254] В одном из вариантов в раскрытии сущности настоящего изобретения предлагаются способы лечения болезни Виллебранда (БВ) или гемофилии A у нуждающихся в лечении пациентов, которые включают введение состава, содержащего рекомбинантный фактор Виллебранда (рФВ) и рекомбинантный ФVIII (рФVIII), таким образом, что повышается стабильность фактора УШ (ФVIII) по сравнению со временем полужизни ФVIII у испытуемых, которым вводили составы, содержащие фактор Виллебранда, полученный из плазмы крови (пФВ). В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В другом осуществлении рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ и обладающим более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00255] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава таким образом, что стабильность фактора ФVIII увеличивается как минимум на 10%, 20%, 30%, 2 ч, 4 ч, 6 ч или на величину, соответствующую вариантам от 1300 до 1643, перечисленным в Таблице 9, по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В другом осуществлении рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ и обладающим более высокой специфической активностью, чем состав, содержащий пФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00256] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава таким образом, что стабильность фактора ФVIII увеличивается как минимум на 10% по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00257] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава таким образом, что стабильность фактора ФVIII увеличивается как минимум на 20% по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00258] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава таким образом, что стабильность фактора ФVIII увеличивается как минимум на 30% по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00259] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при чем комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00260] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 30% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00261] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 50% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00262] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 70% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00263] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00264] В одном из осуществлений заявленный способ включает введение дозы рФВ/рФVIII-состава, который содержит от 10 МЕ/кг до 40 МЕ/кг рФВ:РКо активности, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В отдельном осуществлении состав содержит от 20 МЕ/кг до 30 МЕ/кг рФВ:РКо активности. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00265] В одном из осуществлений заявленный способ включает введение дозы рФВ/рФVIII-состава, который содержит от 25 МЕ/кг до 75 МЕ/кг рФВ:РКо активности, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В отдельном осуществлении состав содержит от 40 МЕ/кг до 60 МЕ/кг рФВ:РКо активности. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00266] В одном из осуществлений заявленный способ включает введение дозы рФВ/рФVIII-состава, который содержит от 75 МЕ/кг до 125 МЕ/кг рФВ:РКо активности, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В отдельном осуществлении состав содержит от 75 МЕ/кг до 100 МЕ/кг рФВ:РКо активности. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00267] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором испытуемым вводят дозу рФВ, соответствующую вариантам от 2141 до 2338. перечисленным в Таблице 12, а комбинации специфической активности пФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00268] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ. В другом осуществлении рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ и обладающим более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00269] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 30% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00270] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 50% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00271] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 70% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00272] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00273] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором рФВ в составе обладает специфической активностью от 40 мЕ/мкг до 60 мЕ/мкг, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00274] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором рФВ в составе обладает специфической активностью в, как минимум, 60 мЕ/мкг, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00275] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором рФВ в составе обладает специфической активностью в, как минимум, 80 мЕ/мкг, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00276] В одном из осуществлений заявленный способ включает введение рФВ/pФVIII-состава, при котором рФВ в составе обладает специфической активностью, соответствующей вариантам от 1 до 133, перечисленным в Таблице 1, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФB/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/pФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00277] В одном из осуществлений заявленный способ включает введение рФВ/pФVIII-состава, при котором доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ/pФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений рФВ/pФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В другом осуществлении рФВ/pФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ и обладающим более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00278] В одном из осуществлений заявленный способ включает введение рФВ/pФVIII-состава, при этом рФВ/pФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 30% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00279] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 50% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00280] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, в которых как минимум 70% молекул рФВ находятся в мультимерах из как минимум 10 субъединиц, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00281] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при этом рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00282] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором у испытуемых стабилизируется ФVIII на протяжении как минимум 18 часов после введения, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00283] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором у испытуемых стабилизируется ФVIII на протяжении как минимум 24 часов после введения, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00284] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором у испытуемых стабилизируется ФVIII на протяжении как минимум 30 часов после введения, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00285] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 4:1-3:2, а рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 3:1-3:2. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00286] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:1-1:2, а рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 3:2-2:3. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00287] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:3-1:6, а рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:3-1:5. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00288] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе соответствует вариантам от 1988 до 2140, перечисленным в Таблице 11, а рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ, которые имеют минимальное процентное содержание молекул рФВ, находящихся в отдельном мультимере высшего порядка или большем мультимере, согласно вариантам от 134 до 457, перечисленным в Таблицах 3-5. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00289] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе соответствует вариантам от 1988 до 2140, перечисленным в Таблице 11. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00290] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 4:1-3:2, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 3:1-3:2. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00291] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:1-1:2, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 3:2-2:3. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00292] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:3-1:6, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:3-1:5. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00293] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе соответствует вариантам от 1988 до 2140, перечисленным в Таблице 11, а комбинации специфической активности рФВ в составе и увеличения стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которьм вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 2339 до 4868, перечисленным в Таблицах 13-19. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, является составом, содержащим высокомолекулярные мультимеры рФВ. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00294] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 4:1-3:2, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 3:1-3:2. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00295] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:1-1:2, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 3:2-2:3. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00296] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:3-1:6, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:3-1:5. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00297] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе соответствует вариантам от 1988 до 2140, перечисленным в Таблице 11, а доза рФВ и увеличение стабильности ФVIII по сравнению со стабильностью ФVIII у испытуемых, которым вводили состав, содержащий пФВ/ФVIII, соответствуют вариантам от 4869 до 8003, перечисленным в Таблицах 20-27. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00298] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 4:1-3:2, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 3:1-3:2. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00299] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:1-1:2, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:K) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 3:2-2:3. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00300] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:3-1:6, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В отдельном осуществлении отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе составляет 2:3-1:5. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00301] В одном из осуществлений заявленный способ включает введение рФВ/рФVIII-состава, при котором отношение прокоагулирующей активности рФVIII (ME рФVIII:К) к ристоцетин-кофакторной активности рФВ (ME рФВ:РКо) в составе соответствует вариантам от 1988 до 2140, перечисленным в Таблице 11, а доза рФВ и специфическая активность рФВ в составе соответствуют вариантам от 8004 до 10625, перечисленным в Таблицах 28-34. В одном из осуществлений рФВ/рФVIII-состав, который вводят испытуемым, обладает более высокой специфической активностью, чем состав, содержащий пФВ/ФVIII. В одном из осуществлений стабильность ФVIII характеризуется временем полужизни ФVIII. В другом осуществлении стабильность ФVIII характеризуется средним временем удержания (СВУ) ФVIII. В дополнительном осуществлении предлагается способ лечения БВ любого типа. В отдельном осуществлении это способ лечения БВ типа 3.
[00302] В практическом осуществлении настоящего изобретения могут применяться, если не указано иное, стандартные методы и технические описания органической химии, технологии производства полимеров, молекулярной биологии (включая рекомбинантные технологии), цитобиологии, биохимии и иммунологии, которые относятся к данной области техники. Подобные стандартные методы включают матричный синтез полимеров, гибридизацию, лигирование и выявление гибридизации с помощью меток. Со специальными примерами соответствующих методов можно ознакомиться с учетом примеров, приведенных ниже. Помимо того, могут применяться любые другие эквивалентные стандартные процедуры. Подобные стандартные методы и технические описания можно найти в стандартных лабораторных руководствах, таких как Genome Analysis: A Laboratory Manual Series (Vols. I-IV), Using Antibodies: A Laboratory Manual, Cells: A Laboratory Manual, PCR Primer: A Laboratory Manual, and Molecular Cloning: A Laboratory Manual (all from Cold Spring Harbor Laboratory Press), Stryer, L. (1995) Biochemistry (4th Ed.) Freeman, Highly stabilized York, Gait, "Oligonucleotide Synthesis: A Practical Approach" 1984, IRL Press, London, Nelson and Cox (2000), Lehninger, Principles of Biochemistry 3rd Ed., W. H. Freeman Pub., Highly stabilized York, N.Y. and Berg et al. (2002) Biochemistry, 5th Ed., W.H. Freeman Pub., Highly stabilized York, N.Y., которые в полном объеме включены в настоящую заявку посредством ссылок для всестороннего изучения.
[00303] Следует обратить внимание на то, что, при применении в настоящей заявке и прилагаемой формуле изобретения, формы единственного числа соответствуют формам множественного числа, если иное четко не предусмотрено контекстом. Таким образом, к примеру, использование термина "полимераза" подразумевает одно вещество или смесь таких веществ, а использование термина "способ" включает отсылку к аналогичным действиям и способам, известным специалистам в данной области техники, и т.д.
[00304] Если не указано иное, все технические и научные термины, которые используются в настоящей заявке, имеют те же значения, что и общепринятые и понятные специалистам в данной области техники, которые являются авторами настоящего изобретения. Все упомянутые в данном тексте публикации включены в настоящую заявку посредством ссылок с целью описания и раскрытия устройств, составов, препаратов и методологий, которые описаны в публикациях и которые могут быть использованы в связи с настоящим изобретением.
[00305] Там, где приводится диапазон величин, если иное четко не предусмотрено контекстом, понятно, что любая промежуточная величина с точностью до десятых от нижнего предела, находящаяся между верхним и нижним пределом этого диапазона, а также любая другая установленная либо промежуточная величина, принадлежащая этому установленному диапазону, охватывается настоящим изобретением. Верхний и нижний пределы этих меньших диапазонов могут быть независимо включены в меньшие диапазоны и, соответственно, в настоящее изобретение, включая любой исключенный предел в установленном диапазоне. Там, где установленный диапазон включает один или оба предела, диапазоны, исключающие оба включенных предела, также охватываются настоящим изобретением.
[00306] В описании, приведенном выше, излагаются многочисленные специфические детали для того, чтобы обеспечить более полное понимание настоящего изобретения. Как бы то ни было, для специалиста в данной области техники является очевидным то, что настоящее изобретение может быть осуществлено без одной или более из этих специфических деталей. В других случаях общеизвестные факты и методы, хорошо известные специалистам в данной области техники, не приводились с целью избежать путаницы в описании изобретении.
[00307] Хотя настоящее изобретение описано, в первую очередь, с отсылкой на определенные варианты осуществления, предусматривается и то, что при прочтении раскрытия сущности настоящего изобретения другие осуществления станут очевидными для специалиста в данной области техники, при этом предполагается, что подобные осуществления могут проводиться способами, заявленными в настоящем изобретении.
ПРИМЕРЫ
ПРИМЕР 1
[00308] Исследование совместного применения рФВ:рФVIII. Основной целью исследования были непосредственная переносимость и безопасность после применения единичной дозы рФВ:рФVIII, которая составляла 2 МЕ/кг, 7.5 МЕ/кг, 20 МЕ/кг и 50 МЕ/кг ФВ:РКо. Второстепенные цели включали ФК ФВ:РКо, ФВ:КС, ФВ:Аг, ФVIII и мультимерных ФВ-составов. Дополнительной второстепенной целью было сравнение ФК с пФВ/пФVIII [Группа 4 (50 МЕ/кг ФВ:РКо)]. Смотрите Фиг. 1, на которой приведен дизайн клинического исследования.
[00309] Рекомбинантный человеческий фактор Виллебранда (рФВ) экспрессировали в клетках СНО. Выведение пропептида было опосредовано in vitro путем обработки про-ФВ рекомбинантным фурином. Полностью гликозилированные гликаны/гликаны групп крови АВО отсутствовали. Рекомбинантный ФВ обладает более высокой специфической активностью, чем ФВ, полученный из плазмы крови (пФВ), и обеспечивает фармацевтическую вариативность дозировок с или без рФVIII. Применяемый в данном исследовании рФВ не подвергали действию металлопротеиназы ADAMTS13, что привело к наличию ультра-больших мультимеров ФВ и неповрежденных субъединиц ФВ. Применение ADAMTS13 приводит к расщеплению субъединичной связи TYR1605-MET1606.
[00310] Наблюдаемые ФК ФВ:РКо/кинетика мультимеров ФВ очень сходны с ФК ФВ:РКо (активности ФВ) между рФВ и гуматом Р (Фиг. 2А). Гумат P является средней чистоты концентратом человеческого фактора VIII, образующим комплекс с ФВ. Для достижения эффективности и определения дозировки использовали суррогатный маркер. Данные Фиг. 2А показывают, что рФА проявляет активность, аналогичную активности ФВ, полученного из плазмы крови. Прогрессирующее уменьшение количества высокомолекулярного рФВ наблюдали при воздействии ADAMTS13 (Фиг. 2Б), что показало, что рФВ находится в высокомолекулярных мультимерах до воздействия ADAMTS13.
[00311] У пациентов, которые получали рФВ, наблюдали более высокий уровень ФVIII по сравнению с теми, кто получал Гумат P (Фиг. 3). Эти данные показывают, что рФВ стабилизирует эндогенный ФVIII in vivo. Существовали различия в эффектах, которые проявлялись при разных соотношениях ФВ:ФVIII (1.3:1 и ~2.1 ФВ:ФVIII). Разные соотношения предполагают, что для стабилизации ФVIII может применяться меньшее количество рФВ, чем то, которое необходимо при применении ФВ, полученного из плазмы крови. Дизайн клинического исследования обеспечивает вариативность повторных применений одного рФВ (без ФVIII) после первичной дозы.
[00312] Ультра-большие высокомолекулярные мультимеры присутствуют вместе с рФВ - эти ультра-большие высокомолекулярные мультимеры быстро исчезают вследствие инфузии. У всех испытуемых наблюдали ADAMTS13 - опосредованные фрагменты расщепления. Фармакокинетический профиль ФВ:РКо был аналогичным таковому у пФВ. Наблюдали длительную стабилизацию эндогенного ФVIII, сравнимую с той, что наблюдали при применении пФВ. Профиль нежелательной реакции на действие препарата, содержащего рФВ, был аналогичным тому, что наблюдали при применении пФВ/пФVIII, а все связанные нежелательные явления (НЯ) были легкими.
[00313] Общая безопасность и фармакокинетический профиль свидетельствуют о том, что рФВ может применяться для лечения и профилактики приступов кровотечений в дозах, сравнимых с дозами пФВ/пФVIII, в то время как уровни ФVIII увеличены по сравнению с эффектом от применения пФВ. Не ограничиваясь теорией, можно предположить, что высокая доля ультра-больших мультимеров (декамеров и больше) среди рФВ приводит к повышенной стабилизации ФVIII, наблюдаемой с рФВ, по сравнению с той, которую обуславливает ФВ, полученный из плазмы крови.
ПРИМЕР 2
[00314] Исследования, проводимые на людях, которые оценивают фармакокинетику и наглядно показывают безопасность и переносимость в тяжелом случае болезни Виллебранда (БВ). В этом исследовании сравнивается действие пФВ и рФВ у пациентов с БВ типа 3 или тяжелыми случаями БВ типа 1.
[00315] В этом исследовании применяли пФВ, который был синтезирован в эндотелиальных клетках и мегакариоцитах. Посттрансляционная модификация выведения пропептида происходила внутриклеточно во время переноса протеина к аппарату Гольджи и последующим компартментам. Наблюдали гликозилирование / гликаны групп крови АВО. пФВ состоял из субъединиц ФВ, которые были подвержены действию плазменной металлопротеиназы ADAMTS13. Ультра-большие мультимеры ФВ отсутствовали в составе пФВ, субъединичная связь TYR1605-MET1606 была расщеплена. Концентраты пФВ содержали другие протеины, включая ADAMTS13 и гемагглютинины.
[00316] рФВ, который применяли в данном исследовании, был экспрессирован в клетках СНО. Выведение пропептида было опосредовано in vitro путем воздействия на про-ФВ рекомбинантного фурина. Полностью гликозилированные гликаны / гликаны групп крови АВО не наблюдали. рФВ не был подвержен действию плазменной металлопротеиназы ADAMTS13. Субъединицы рФВ были неповреждены, присутствовали ультра-большие мультимеры ФВ. Расщепление субъединиц происходило при воздействии ADAMTS13. рФВ проявлял более высокую специфическую активность, чем пФВ.
[00317] Критериями включения в этом исследовании были:
- БВ типа 3 (ФВ:Аг≤3 МЕ/дЛ)
- Тяжелые случаи БВ типа 1 (ФВ:РКо≤10 МЕ/дЛ и ФVIII:К≤20 МЕ/дЛ)
- Возраст от 18 до 60 лет
- Предшествующая заместительная терапия фактора свертывания крови (≥25 ЭД)
- Состояния без кровотечений
[00318] Критериями исключения в этом исследовании были:
- Другие нарушения свертываемости крови
- Наличие в анамнезе ингибиторов ФВ и/или ФVIII
- Наличие сердечно-сосудистых заболеваний
- Наличие в анамнезе тромбоэмболических осложнений
- Наличие в анамнезе других иммунологических нарушений
[00319] В качестве основной цели данного исследования были достигнуты непосредственная переносимость и безопасность после применения единичных доз рФВ: pФVIII, которые составляли 2 МЕ/кг, 7.5 IU/kg, 20 МЕ/кг и 50 МЕ/кг. Второстепенные цели включали ФК ФВ:РКо, ФВ:КС, ФВ:Аг, ФVIII и мультимерных ФВ-составов. Дополнительной второстепенной целью было сравнение ФК с пФВ/пФVIII [Группа 4 (50 МЕ/кг ФВ:РКо)]. Персональные данные пациентов этого исследования приведены на Фиг. 4. Анализ фармакокинетики ФВ:РКо/ФВ:Аг по Группе 4А (БВ типа 3) приведен на Фиг. 5. Эти данные показывают, что общая активность рФВ была сравнима с таковой у пФВ. Прогрессирующее уменьшение количества высокомолекулярного рФВ наблюдали при воздействии ADAMTS13 (Фиг. 6). Дополнительный анализ фармакокинетики ФУПЕК в Группе 4А (БВ типа 3) приведен на Фиг. 7. Данные Фиг. 7 свидетельствуют о том, что рФВ был более эффективным для стабилизации in vivo активности ФVIII, чем пФВ, что привело к увеличению прокоагулирующей активности ФVIII после применения рФВ/рФVIII по сравнению с применением пФВ/пФVIII.
[00320] Ультра-большие высокомолекулярные мультимеры присутствовали в составе рФВ и быстро исчезали вследствие инфузии. У всех испытуемых наблюдали ADAMTS13-опосредованные фрагменты расщепления. Фармакокинетический профиль ФВ:РКо был аналогичным таковому у пФВ. Наблюдали длительную стабилизацию эндогенного ФVIII, сравнимую с той, что наблюдали при применении пФВ. Профиль нежелательной реакции на действие препарата был аналогичным тому, что наблюдали при применении пФВ/пФVIII, а все связанные нежелательные явления (НЯ) были легкими.
[00321] Общая безопасность и фармакокинетический профиль свидетельствуют о том, что рФВ может применяться для лечения и профилактики приступов кровотечений в дозах, сравнимых с дозами пФВ/пФVIII.
ПРИМЕР 3
[00322] Клиническое исследование комплекса рФВ/рФVIII. В данном исследовании изучали фармакокинетику, непосредственную безопасность и переносимость при врожденной БВ типа 3. Фиг. 9 иллюстрирует параметры ФК рФВ для трех пациентов, которые принимали участие в исследовании.
[00323] На Фиг. 10 приведены данные по ФК у Пациента 1. Наблюдали хорошую корреляцию между ФВ:РКо и ФВ:КСА. Активности были измеряемы вплоть до 12 часов (обе были ниже уровня определенности через 24 часа). ФВ:Аг была измеряема и через 96 часов. Эндогенная активность ФVIII возросла до максимального значения в 0.13 МЕ/мЛ.
[00324] На Фиг. 11 приведены данные по ФК у Пациента 2. Как и в случае Пациента 1, наблюдали хорошую корреляцию между ФВ:РКо и ФВ:КСА. Обе активности были измеряемы (хотя и находились на уровне определенности) вплоть до 12 часов. ФВ:Аг была измеряема и через 72 часа (через 96 часов образец не исследовали). Эндогенная активность ФVIII этого пациента возросла до максимального значения в 0.18 МЕ/мЛ.
[00325] На Фиг. 12 приведены данные по ФК у Пациента 3. Активность ФВ:РКо была измеряема вплоть до 24 часов (хотя и находилась на уровне определенности), в то время как ФВ:КСА была ниже уровня определенности через 24 часа. ФВ:Аг была измеряема и через 48 часов. Эндогенная активность ФVIII этого пациента возросла до максимального значения в 0.13 МЕ/мЛ.
[00326] На Фиг. 13 приведены сравнительные данные параметров ФВ и активности ФVIII по трем пациентам. Для всех трех пациентов наблюдали хорошую корреляцию исследуемых параметров (ФВ:РКо, ФВ:КСА, ФВ:Аг и активности ФVIII:Кр).
[00327] рФВ привел к ~100% восстановлению всех пациентов. У трех пациентов наблюдали немного различную ФК рФВ. Через 30 минут после применения 2 ME ФВ:РКо/кг для антигена ФВ наблюдали максимальное значение в 0.06 МЕ/мл, за которым следовало устойчивое снижение. Через 15 минут после применения рФВ+рФVIII базовая активность ФVIII возросла приблизительно до 0.1 МЕ/мл. Впоследствии активность дополнительно возросла до 0.16 МЕ/мл, вышла на плато через 3-6 часов, сохраняя этот уровень вплоть до 28 часов, за чем следовало устойчивое снижение. Отсроченное увеличение активности ФVIII указывает на то, что второе возростание было индуцировано рФВ.
ПРИМЕР 4
[00328] Исследование рФВ - оценка ФК FVII и оценка ТА. На Фиг. 14 приведены данные активности ФVIII по всем группам. На Фиг. 15 приведены данные по Группе 1 (2 МЕ/кг ФВ:РКо/1.5 МЕ/кг ФVIII). Для всех трех пациентов этой группы наблюдали хорошую корреляцию всех исследуемых параметров.
[00329] На Фиг. 15 приведены данные по Группе 2 (7.5 МЕ/кг ФВ:РКо/5.8 МЕ/кг ФVIII). На Фиг. 16 приведены фармакокинетические данные ФVIII:К по этой группе. [00330] На Фиг. 17 приведены данные по Группе 3 (20 МЕ/кг ФВ:РКо/15.4 МЕ/кг ФVIII). Эти данные показывают сравнение плазменных параметров для ФВ и ФVIII. На Фиг. 18 приведены фармакокинетические данные ФVIII:К по этой группе.
[00331] На Фиг. 19 приведены данные по Группе 4 (50 МЕ/кг ФВ:РКо). Доза ФVIII составляла 38.5 МЕ/кг рФVIII или 25 МЕ/кг пФVIII. Эти данные показывают, что параметры для рФВ аналогичны таковым для пФВ (Гемате), но рФВ более эффективен для стабилизации активности ФVIII, что проявляется в увеличении наблюдаемой активности ФVIII по сравнению с наблюдаемой при воздействии пФВ. На Фиг. 20 приведены обобщенные фармакокинетические данные ФVIII:К по этой группе. Как видно из этих данных, медиана и среднее значение времени полужизни Т1/2 возросло при применении рФВ/рФVIII по сравнению с пФВ/пФVIII, что свидетельствует о том, что рФВ более эффективен, чем пФВ, для стабилизации in vivo ФVIII, что приводит к возрастанию времени полужизни.
ПРИМЕР 5
[00332] Клиническое исследование воздействия рФВ на ФVIII при лечении гемофилии А. В данном исследовании оценивали непосредственную переносимость и безопасность рФВ после единичных доз в 50 МЕ/кг одного рФVIII (Advate) или в комбинации с рФВ при значении величины фактор Виллебранда:ристоцетин кофакторная активность (ФВ:РКо) в10 или 50 МЕ/кг. В данном исследовании также оценивали фармакокинетику после единичных доз в 50 МЕ/кг одного рФVIII (Advate) или в комбинации с рФВ при 10 или 50 МЕ/кг (ФВ:РКо).
[00333] Объекты для данного исследования выбирали, используя следующие критерии:
[00334] Критерии включения:
- Тяжелые случаи гемофилии A (ФVIII:К<1 МЕ/дЛ)
- Возраст от 18 до 60 лет
- Предшествующая заместительная терапия фактора свертывания крови (>150 ЭД)
- Состояния без кровотечений
[00335] Критерии исключения:
- Другие нарушения свертываемости крови
- Наличие в анамнезе ингибиторов ФВ и/или ФVIII
- Наличие сердечно-сосудистых заболеваний
- Наличие в анамнезе тромбоэмболических осложнений
- Наличие в анамнезе других иммунологических нарушений (исключения)
[00336] Привлечение к участию испытуемых на протяжении 16 недель при полной длительности исследования в 7 месяцев.
[00337] Дизайн исследования представляет собой многоцентровое, неконтролируемое, нерандомизированное, открытое клиническое исследование с целью оценки безопасности, непосредственной переносимости и фармакокинетики рФВ:рФVIII у испытуемых с тяжелыми случаями наследственной гемофилии A (ФVIII:К<1%).
[00338] Каждый испытуемый (N=14), участвующий в трехкратном анализе ФК, рандомизированно получает по 50 МЕ/кг рФVIII (Advate) без, с 10 МЕ/кг ФВ:РКо или 50 МЕ/кг ФВ:РКо рФВ, и, по расчетам, будет участвовать в исследовании на протяжении приблизительно 16 недель.
[00339] Внутрииндивидуальную фармакокинетику исследуют с интервалом в 5-14 дней, чтобы обеспечить период вымывания, составляющий минимум 5 дней, и своевременное завершение исследования. Анализ безопасности проводят раздельно, после введения 6 испытуемым дозы в10 МЕ/кг ФВ:РКо рФВ и после введения 6 испытуемым дозы в 50 МЕ/кг ФВ:РКо рФВ.
[00340] Испытуемые не должны получать криопреципитат, свежезамороженную плазму крови или другие препараты, которые взаимодействуют с ФВ или ФVIII ФК, как минимум за пять дней до любой из инфузий.
[00341] Дозировку рФВ увеличивают, когда как минимум 6 испытуемых демонстрируют непосредственную переносимость и безопасность после применения 10 МЕ/кг ФВ:РКо рФВ. Действие исследуемого продукта на основные физиологические показатели, гематологию и параметры клинической химии определяет краткосрочную безопасность.
[00342] Образцы для определения уровней активности ФVIII (ФVIII:К), ФВ-антиген (ФВ:Аг), активности ФВ (ФВ:РКо), ФВ:КС (а также распределения мультимеров ФВ) берут перед инфузией (за 30 минут до начала инфузий) и после окончания инфузий через 15 минут (±5 минут), 30 минут (±5 минут), 1 час (±5 минут), 3 часа (±10 минут), 6 часов (±10 минут), 9 часов (±15 минут), 24 часа (±2 часа) и 48 часов (±2 часа), 72 часа (±2 часа), 96 часов (±2 часа), и 120 часов (±2 часа) (или, как минимум, через каждые 24 часа до тех пор, пока уровень ФVIII не упадет ниже <1%). Активность ФVIII определяют, используя как хромогенный, так и одностадийный, основанный на АЧТВ, методы анализа, которые проводят в местной и центральной лабораториях.
[00343] Действие каждой инфузий на основные физиологические показатели и другие симптомы, указывающие на наличие побочных эффектов (ПЭ), гематологию и параметры клинической химии используют как индикаторы краткосрочной безопасности. Основные физиологические показатели, гематологию и параметры клинической химии оценивают до инфузий и на протяжении 120 часов после инфузий. Появление ПЯ непрерывно отслеживают вплоть до 2 часов после инфузий (у испытуемых, к которым применяют рФВ) и в различные моменты времени в период последующего наблюдения.
[00344] Наличие ингибиторов ФVIII и ФВ оценивают перед инфузией исследуемого продукта и при визите после окончания исследования.
[00345] При возникновении серьезных НЯ, связанных с исследуемым продуктом, независимый комитет по мониторингу данных (НКМД) дает рекомендации относительно продолжения исследования.
[00346] Основные цели изучения фармакокинетики в данном исследовании включают: ППК0-∞/доза (площадь под кривой "концентрация плазмы крови/время" от момента времени 0 до бесконечности); ППК0-96ч/доза (площадь под кривой "концентрация плазмы крови/время" от момента времени 0 до 96 часов); среднее время удержания (СВУ); клиренс (КЛ); Т1/2 (элиминационный период полувыведения); объем распределения в равновесном состоянии (Орс) ФВ:РКо, ФВ:Аг, ФВ:КС и ФVIII.
[00347] Основные цели анализа фармакокинетики включают ППК0-96ч/доза, ППК0-∞/доза, СВУ, КЛ, T1/2 и Орс обобщенные по лечебной группе (50 МЕ/кг только рФVIII (Advate), 50 МЕ/кг рФVIII (Advate), предварительно смешанного с рФВ при 10 МЕ/кг ФВ:РКо, 50 МЕ/кг рФVIII (Advate), предварительно смешанного с рФВ при 50 МЕ/кг ФВ:РКо) в среднем и двухстороннем 95-% доверительных интервалах для медианы, среднего значения, средней квадратической погрешности, коэффициента вариации и среднего геометрического. Описательную статистику (медианы и диапазоны) используют для обобщения уровней ФВ:РКо, ФВ:Аг, ФВ:КС и ФVIII в динамике.
[00348] Основная цель безопасности включает: появление НЯ, связанных с лечением. Анализ основной цели безопасности включает количество и процентное отношение испытуемых, у которых проявились НЯ, связанные с лечением. Количество и интенсивность связанных с лечением НЯ заносят в таблицы.
[00349] Второстепенные цели изучения фармакокинетики включают: восстановление in vivo (BIV) и постепенное восстановление (ПВ) ФVIII, ФВ:РКо, ФВ:Аг и ФВ:КС. Анализ второстепенных целей изучения фармакокинетики включает определение BIV И ПВ ФVIII, ФВ:РКо, ФВ:Аг и ФВ:КС для каждого испытуемого и обобщение через медианы и диапазоны.
[00350] Второстепенная цель безопасности включает: образование ингибирующих анти-ФВ антител и антител общего связывания, образование ингибирующих антител к ФVIII, образование антител к протеинам яичников китайского хомячка (СНО), мышиному иммуноглобулину G (ИгG) и p-фурину, появление тромботических осложнений.
[00351] Второстепенные цели безопасности анализируют путем внесения в таблицы количества испытуемых, у которых проявились СНЯ, и количество СНЯ. Дополнительно, количество испытуемых, у которых проявились ПЯ, связанные с лечением, а также количество и интенсивность связанных с лечением НЯ субкатегоризируются по появлениям тромботических осложнений, ингибирующим анти-ФВ антителам и антителам общего связывания, ингибирующим антителам к ФVIII, антителам к протеинам яичников китайского хомячка (СНО), антителам к мышиному иммуноглобулину G (ИгG) и антителам к p-фурину.
[00352] Идентификатор испытуемого содержит перечень всех НЯ, а также возраст, пол, термин предпочтительного употребления и заявленный термин НЯ, продолжительность, степень тяжести, серьезность, предпринятые действия, исход, оценку достоверности причинно-следственной связи, дату начала, дату окончания и медикаментозную либо безмедикаментозную терапия НЯ. Приведенные обзорные таблицы содержат число НЯ, количество испытуемых с НЯ и соответствующий процент таких испытуемых относительно общего числа, а также относительно тяжести и взаимосвязи с лечением. Дополнительная обобщающая таблица содержит полное количество (легких, средних, тяжелых) НЯ в соответствии с классом по поражению органов и систем органов и термином предпочтительного употребления в связи с лечением.
[00353] Для данного исследования не проводили официальной оценки объема выборки.
[00354] Понятно, что приведенные в настоящей заявке примеры и варианты осуществления предназначены только для пояснительных целей, а их многочисленные небольшие модификации или изменения рекомендованы специалистам в данной области техники и включены в сущность и компетенцию настоящей заявки в рамках прилагаемой формулы изобретения. Все публикации, патенты и патентные заявки, перечисленные здесь, включены в настоящую заявку посредством ссылок для всестороннего изучения.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕЧЕНИЕ НАРУШЕНИЙ СВЕРТЫВАЕМОСТИ КРОВИ ПУТЕМ ВВЕДЕНИЯ РЕКОМБИНАНТНОГО ФВ | 2012 |
|
RU2680402C2 |
| ЛЕЧЕНИЕ НАРУШЕНИЙ СВЕРТЫВАЕМОСТИ КРОВИ ПУТЕМ ВВЕДЕНИЯ РЕКОМБИНАНТНОГО ФАКТОРА ВИЛЛЕБРАНДА | 2019 |
|
RU2787855C2 |
| КОНЪЮГАТЫ БЕЛКОВ СВЕРТЫВАНИЯ КРОВИ | 2010 |
|
RU2595442C2 |
| КОНЪЮГАТЫ БЕЛКОВ СВЕРТЫВАНИЯ КРОВИ | 2010 |
|
RU2744370C2 |
| ЛЕЧЕНИЕ ПАЦИЕНТОВ С ТЯЖЕЛОЙ ФОРМОЙ БОЛЕЗНИ ФОН ВИЛЛЕБРАНДА, ПОДВЕРГАЮЩИХСЯ ПЛАНОВОМУ ХИРУРГИЧЕСКОМУ ВМЕШАТЕЛЬСТВУ, ПУТЕМ ВВЕДЕНИЯ РЕКОМБИНАНТНОГО ФФВ | 2018 |
|
RU2766118C2 |
| СОСТАВЫ РЕКОМБИНАНТНОГО ФУРИНА | 2012 |
|
RU2610436C2 |
| ГЛИКОПОЛИСИАЛИРОВАНИЕ БЕЛКОВ, НЕ ЯВЛЯЮЩИХСЯ БЕЛКАМИ СВЕРТЫВАНИЯ КРОВИ | 2014 |
|
RU2662807C2 |
| СПОСОБ ПОЛУЧЕНИЯ СТАНДАРТИЗИРОВАННОГО КОНЦЕНТРАТА ЧЕЛОВЕЧЕСКОГО ФАКТОРА ВИЛЛЕБРАНДА И КОНЦЕНТРАТ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ | 1992 |
|
RU2088590C1 |
| ВОДНАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ АНТИТЕЛА К PD-1 ПРОЛГОЛИМАБА И ЕЕ ПРИМЕНЕНИЕ | 2019 |
|
RU2806320C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ С МГНОВЕННЫМ ВЫСВОБОЖДЕНИЕМ, СОДЕРЖАЩИЕ ОКСИКОДОН И НАЛОКСОН | 2010 |
|
RU2522212C2 |
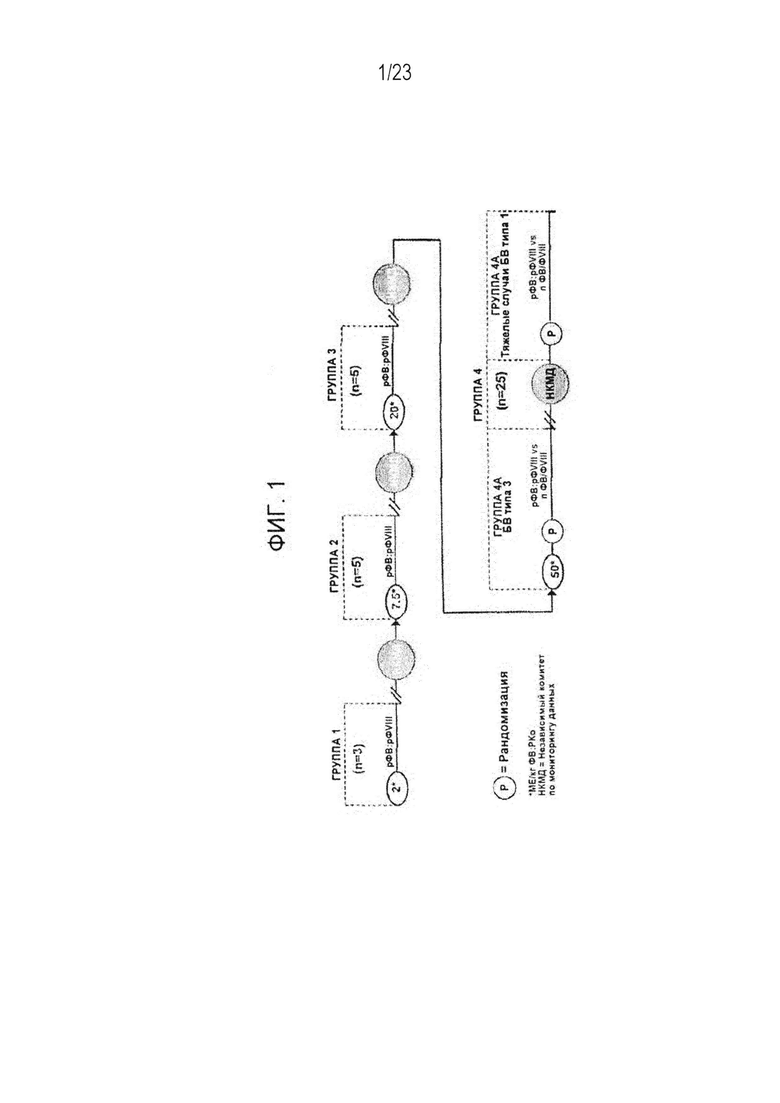
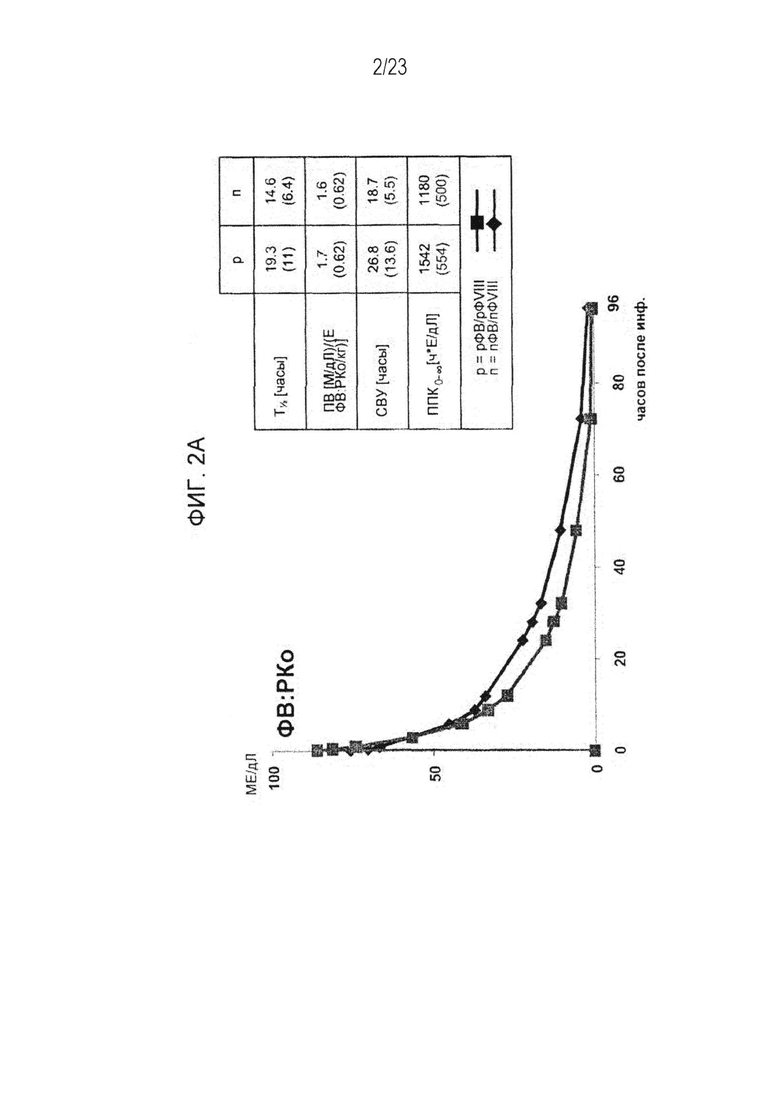

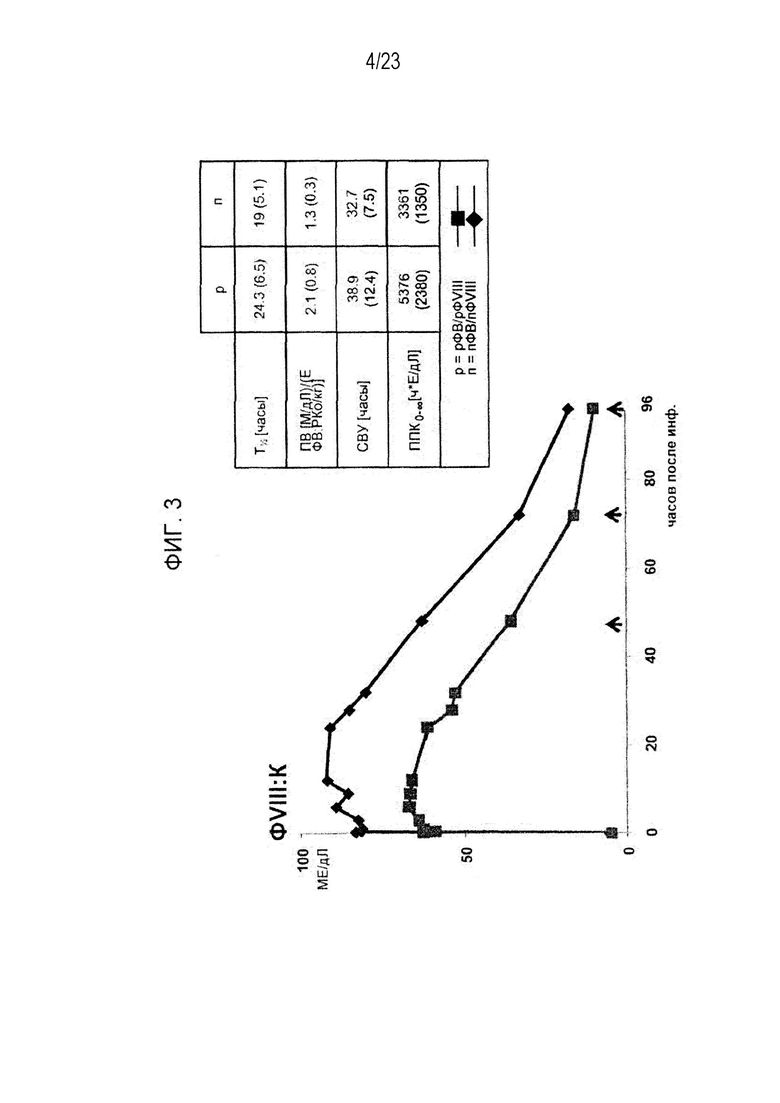
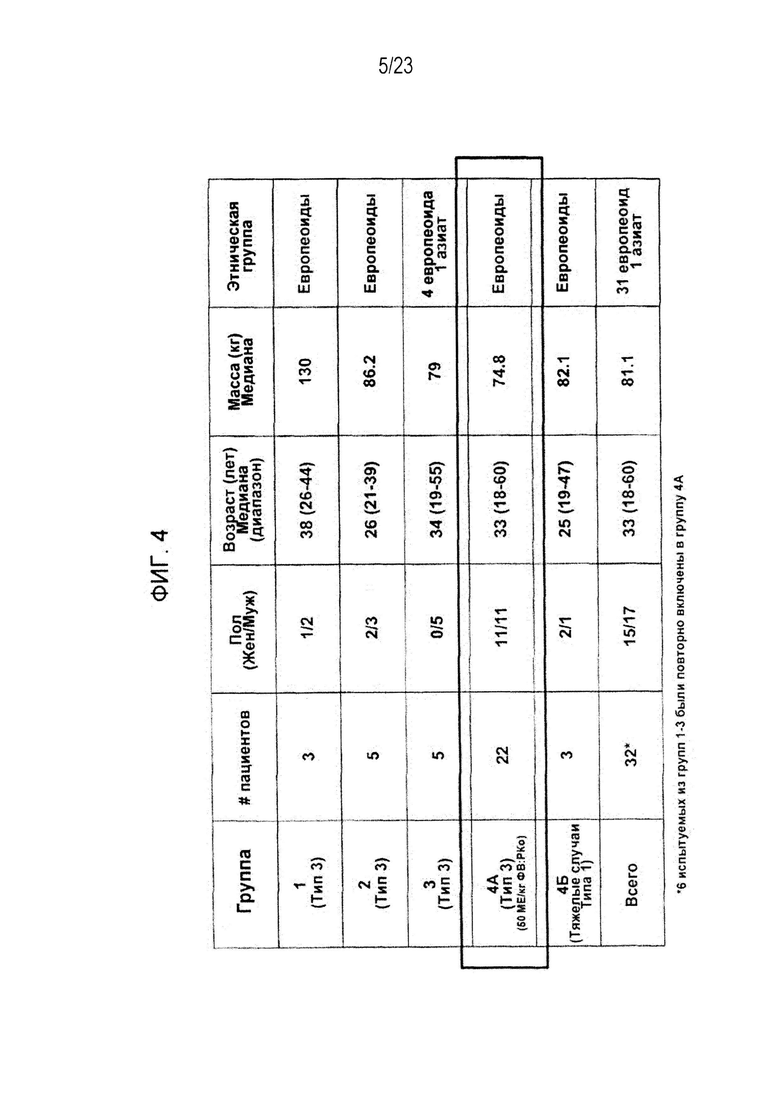
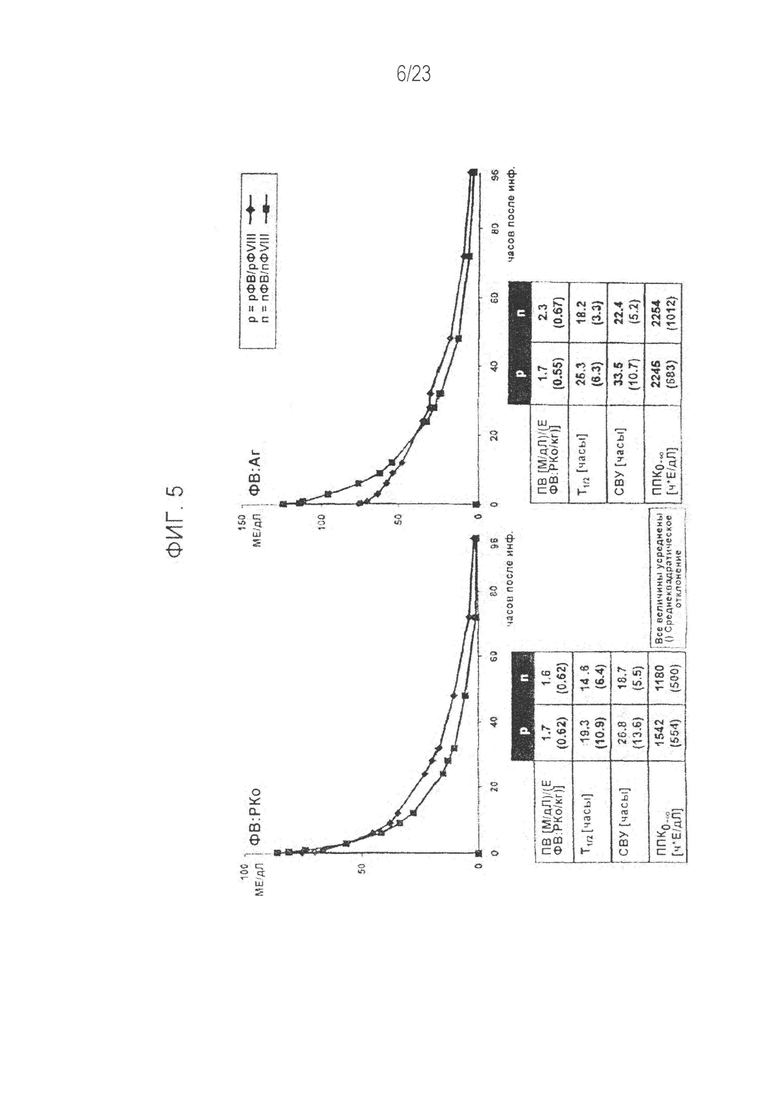
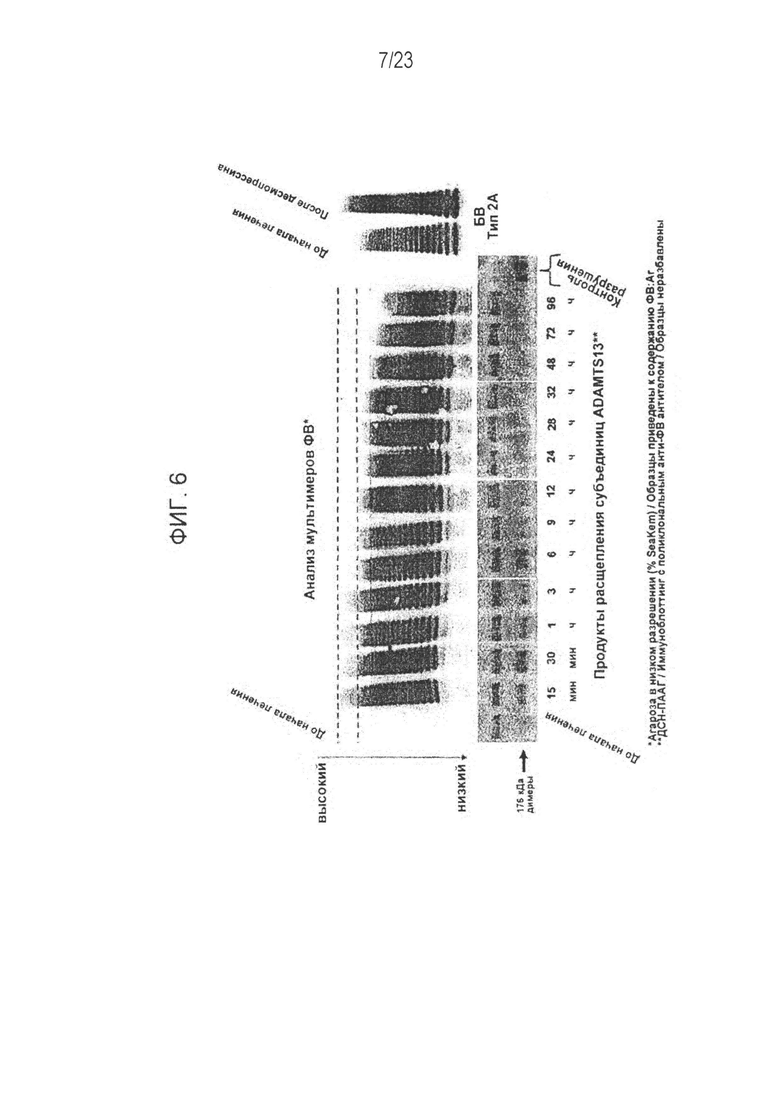
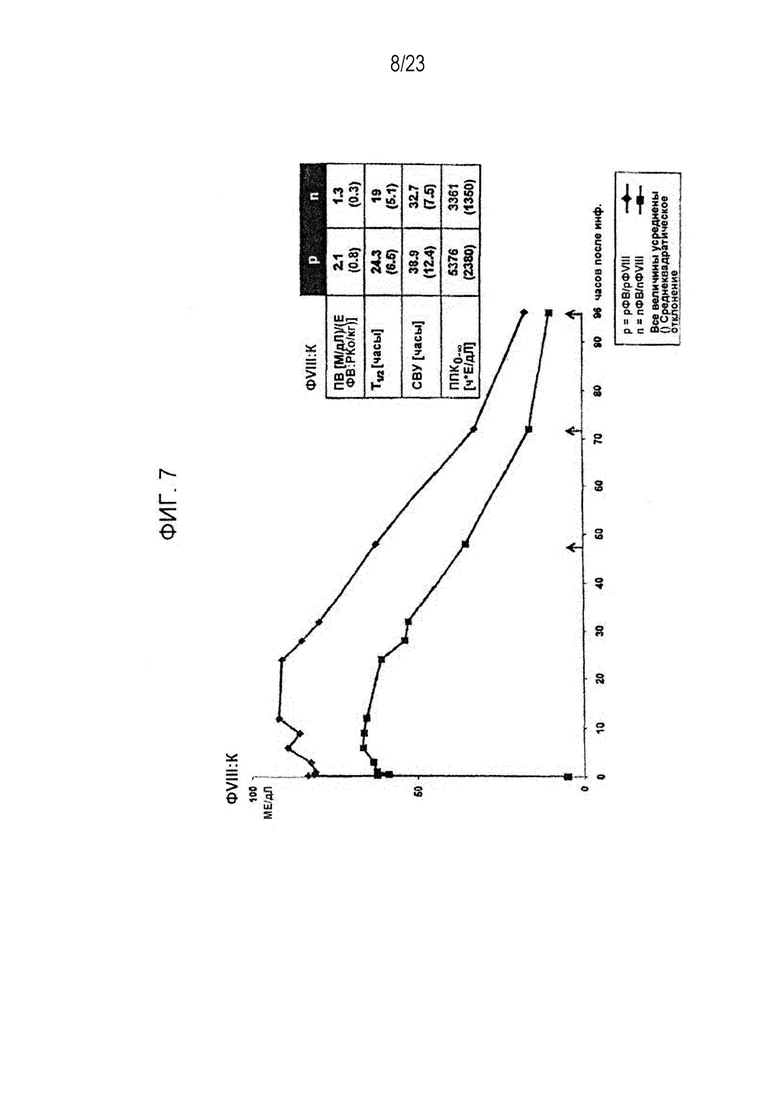

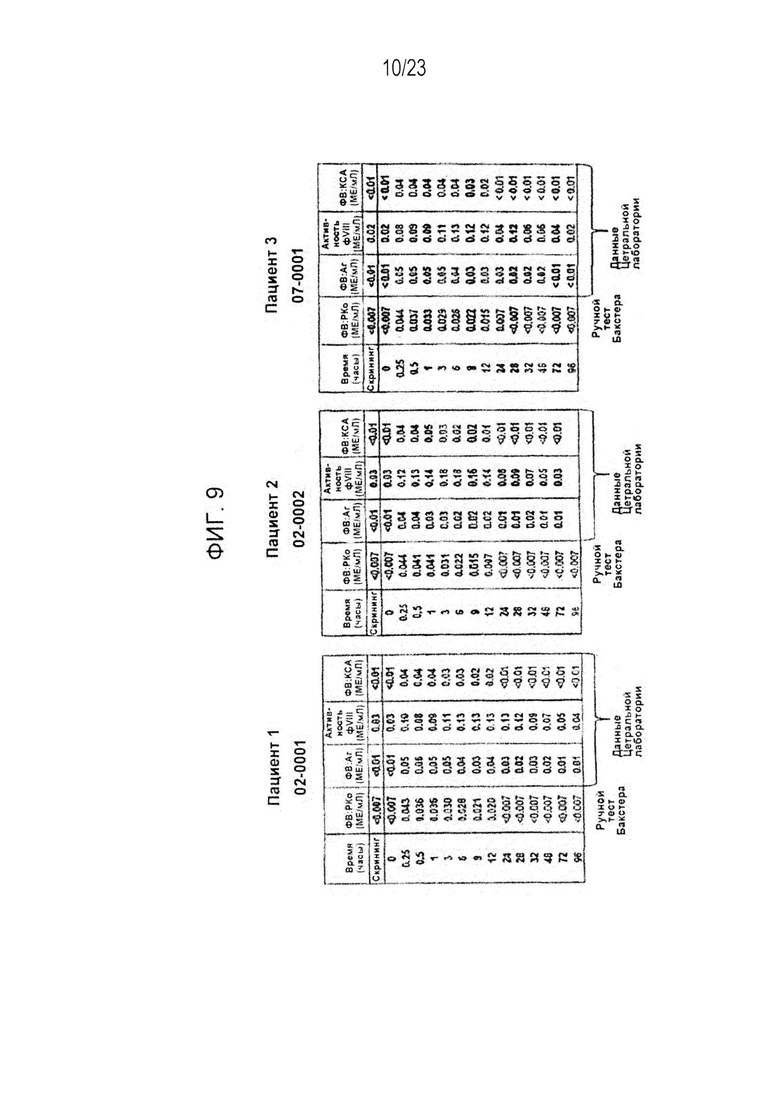
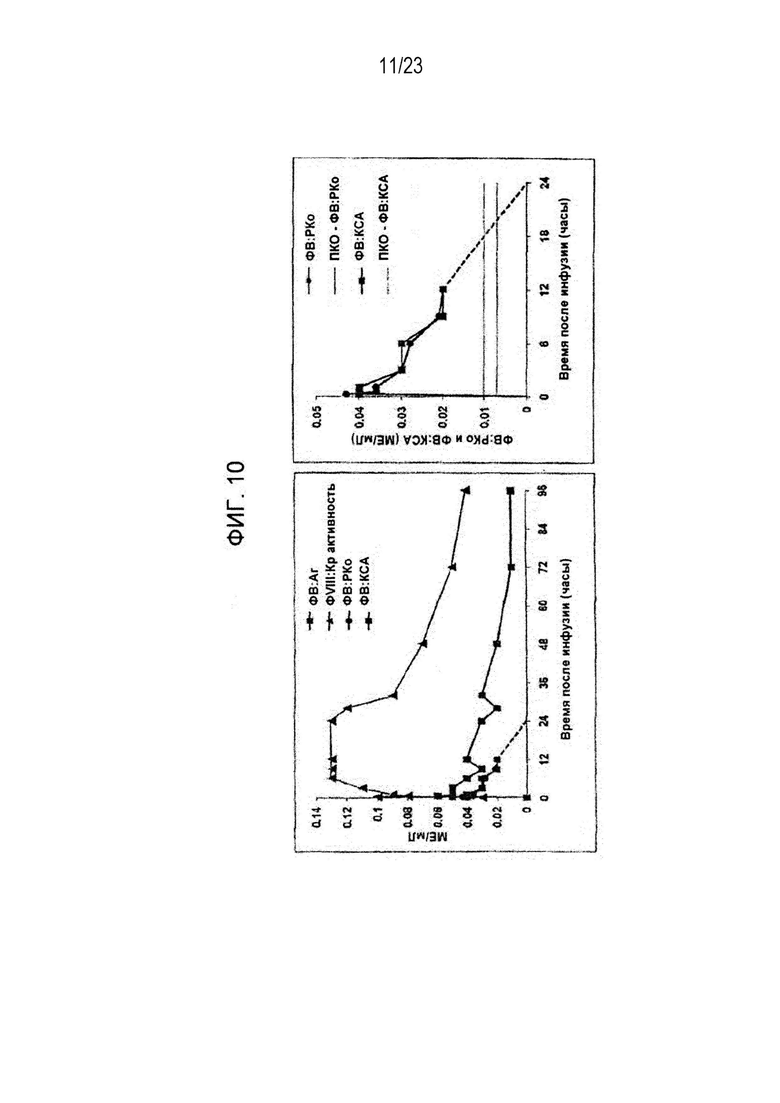
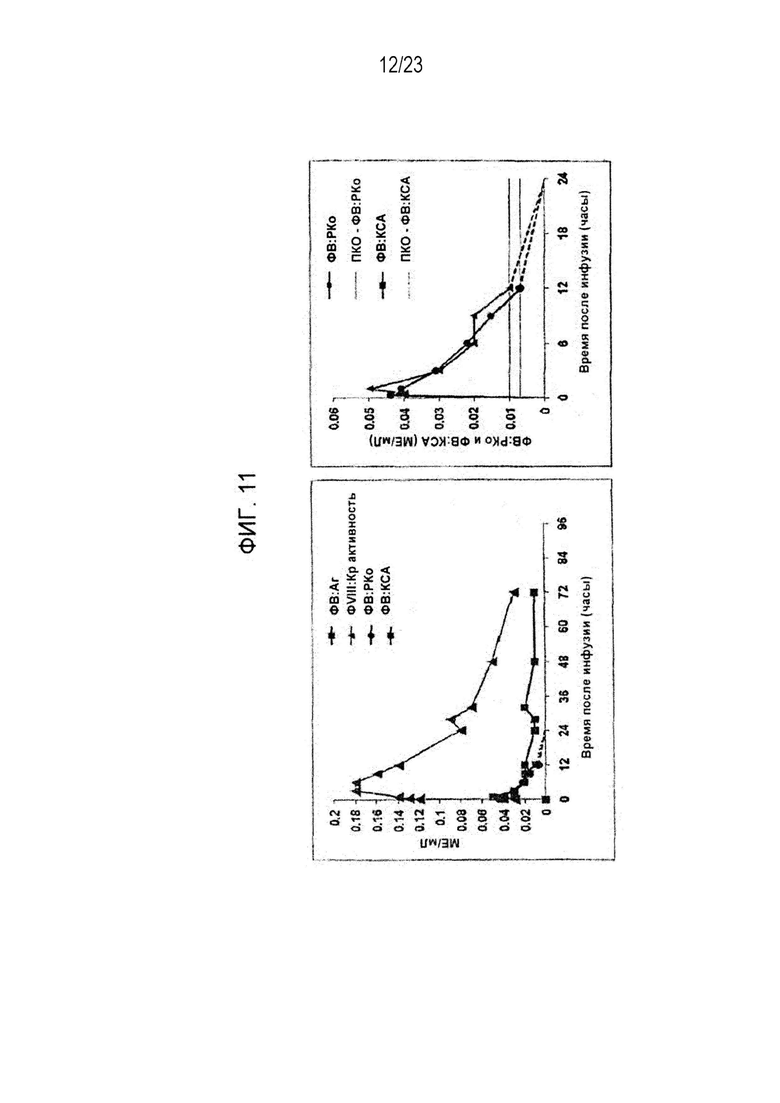
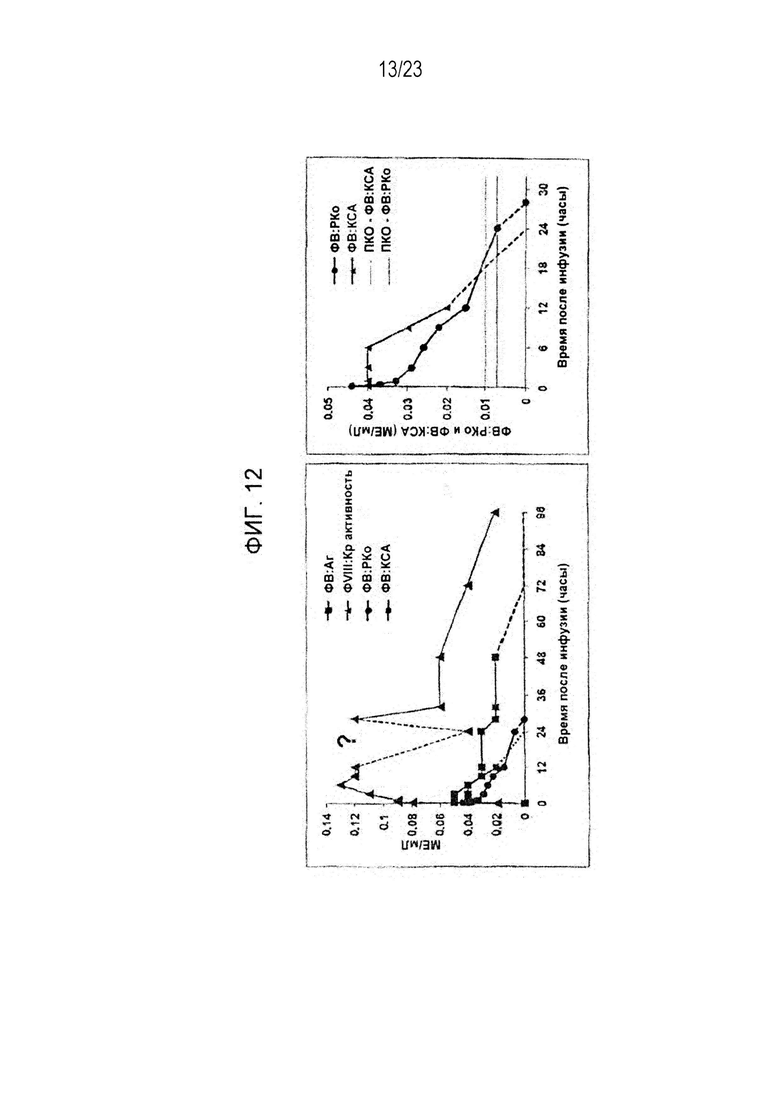
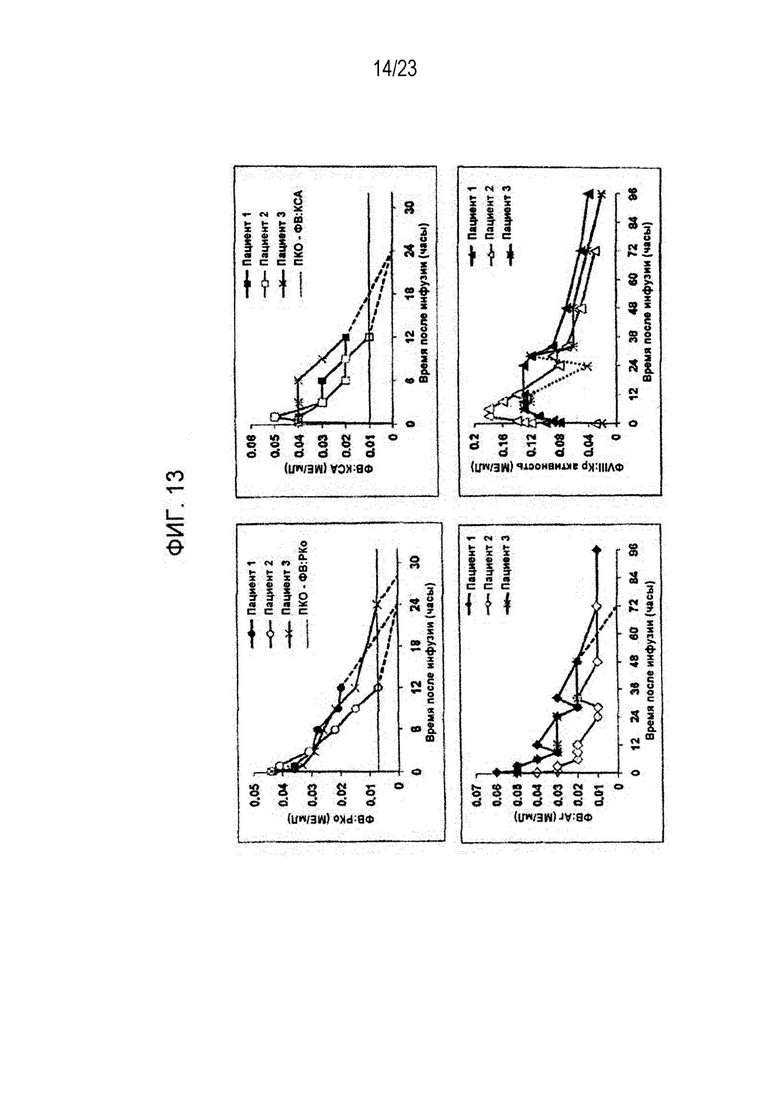
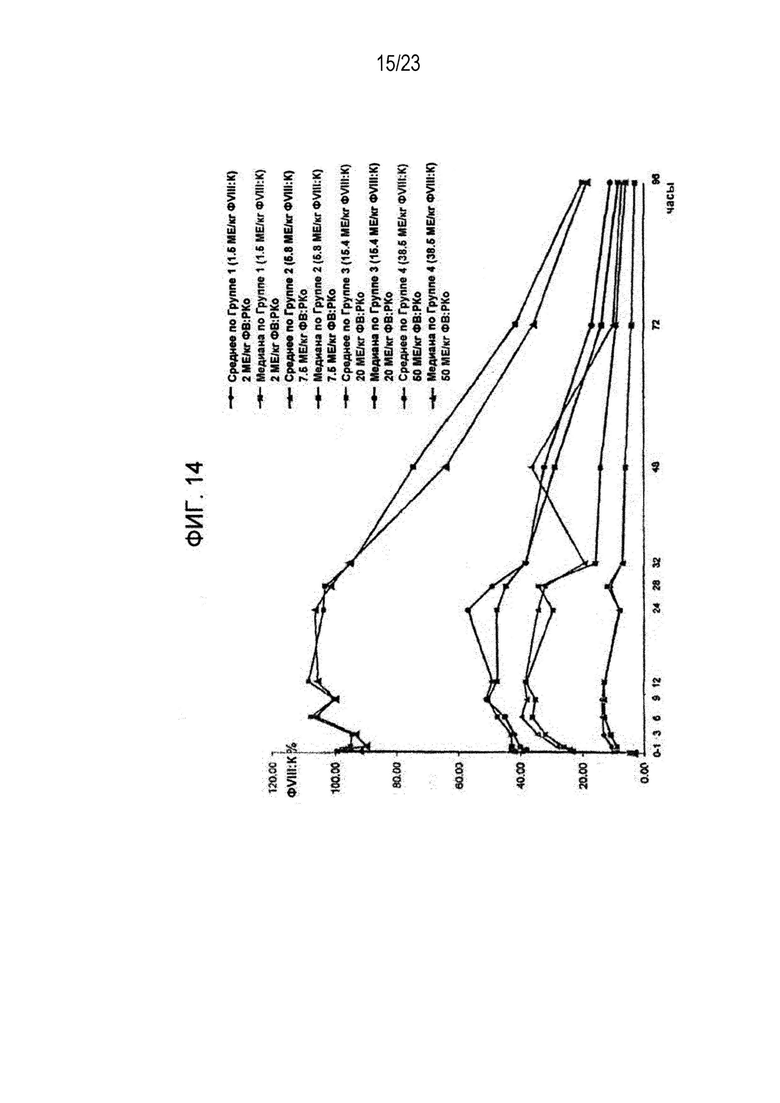
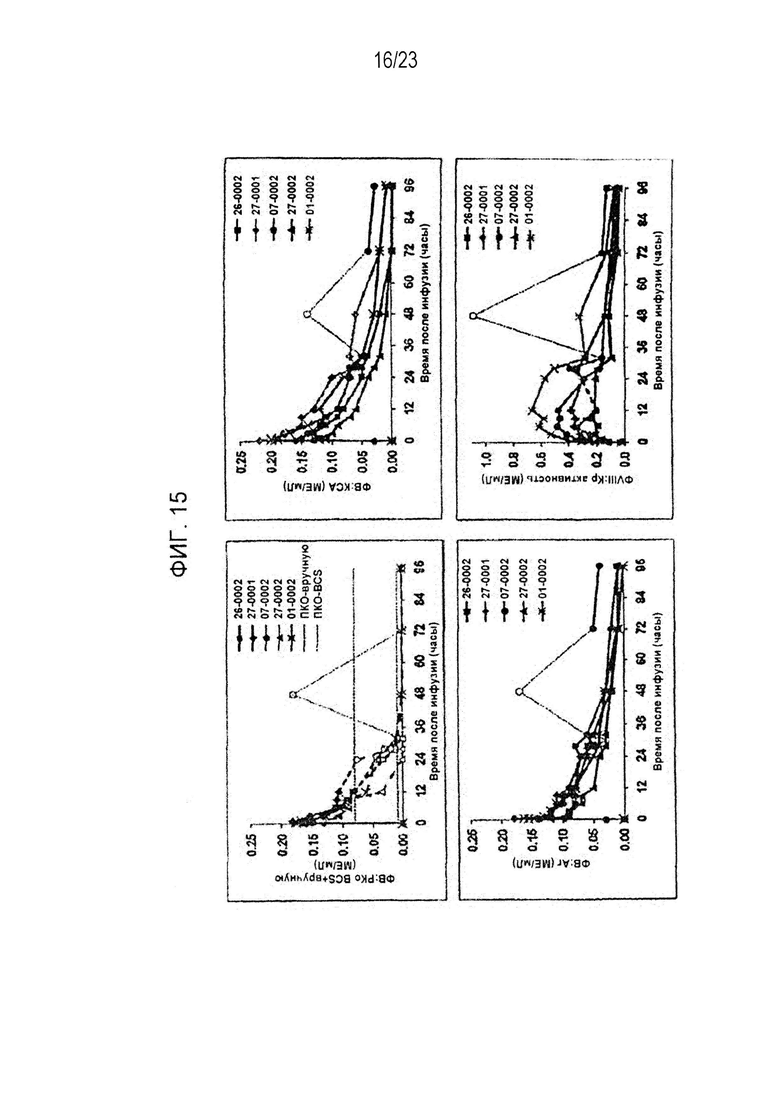
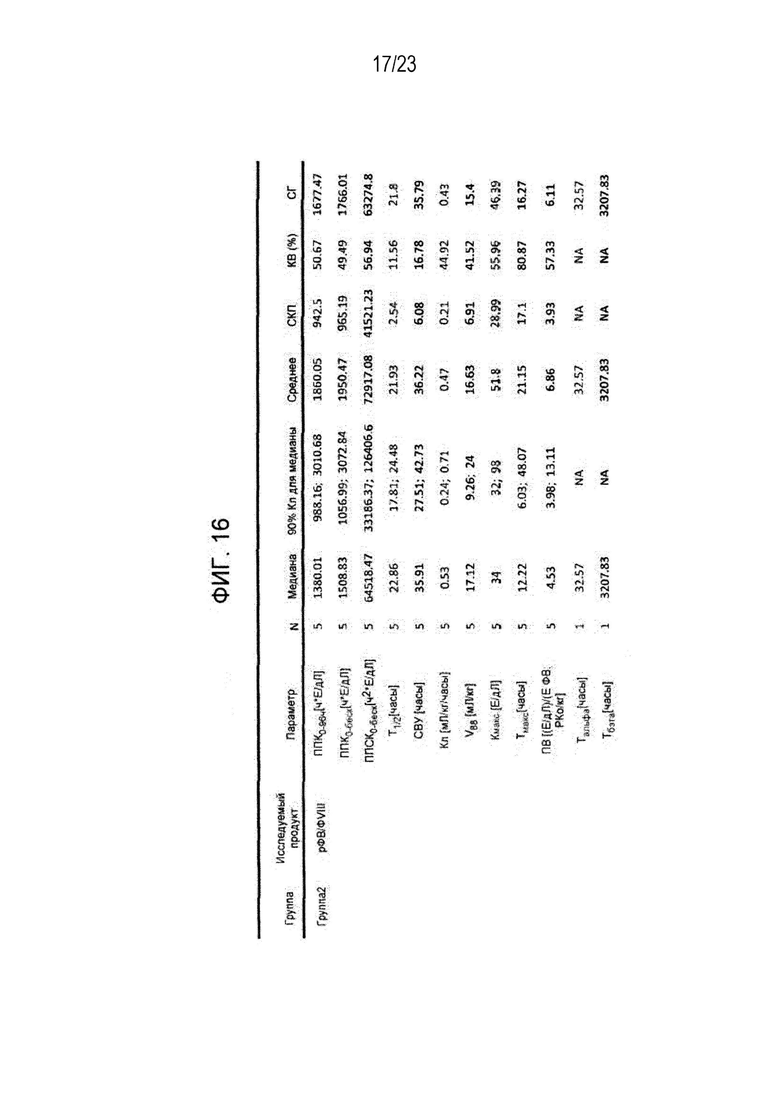
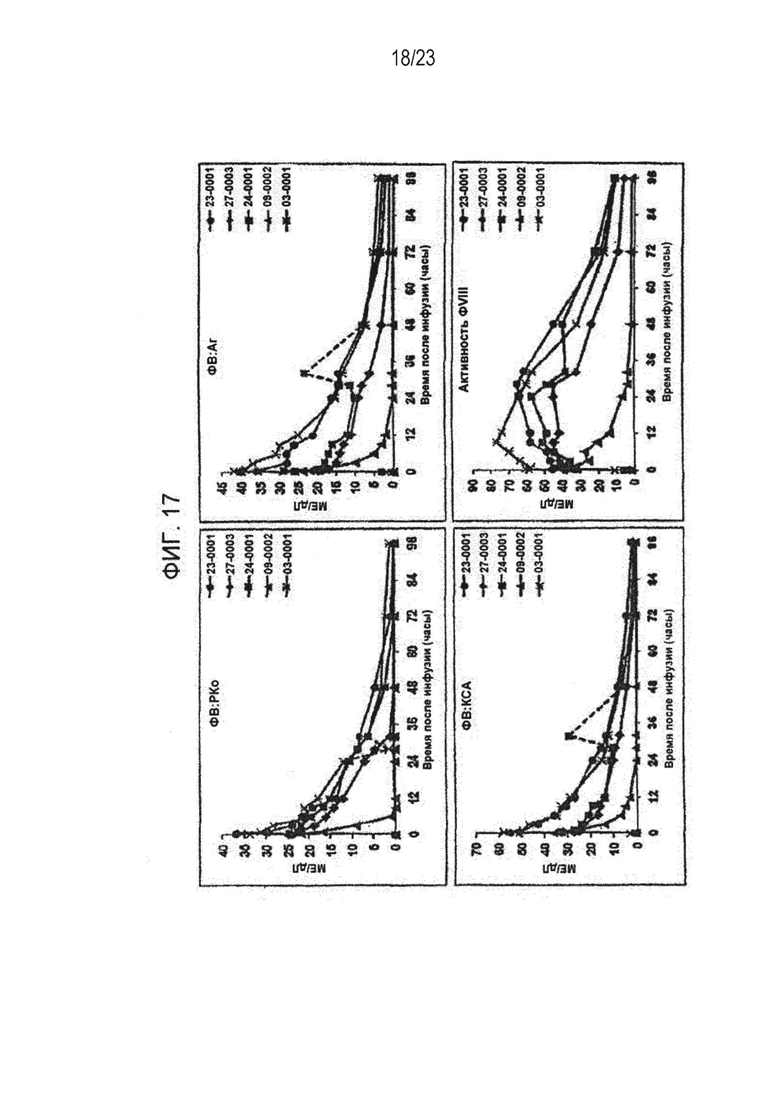
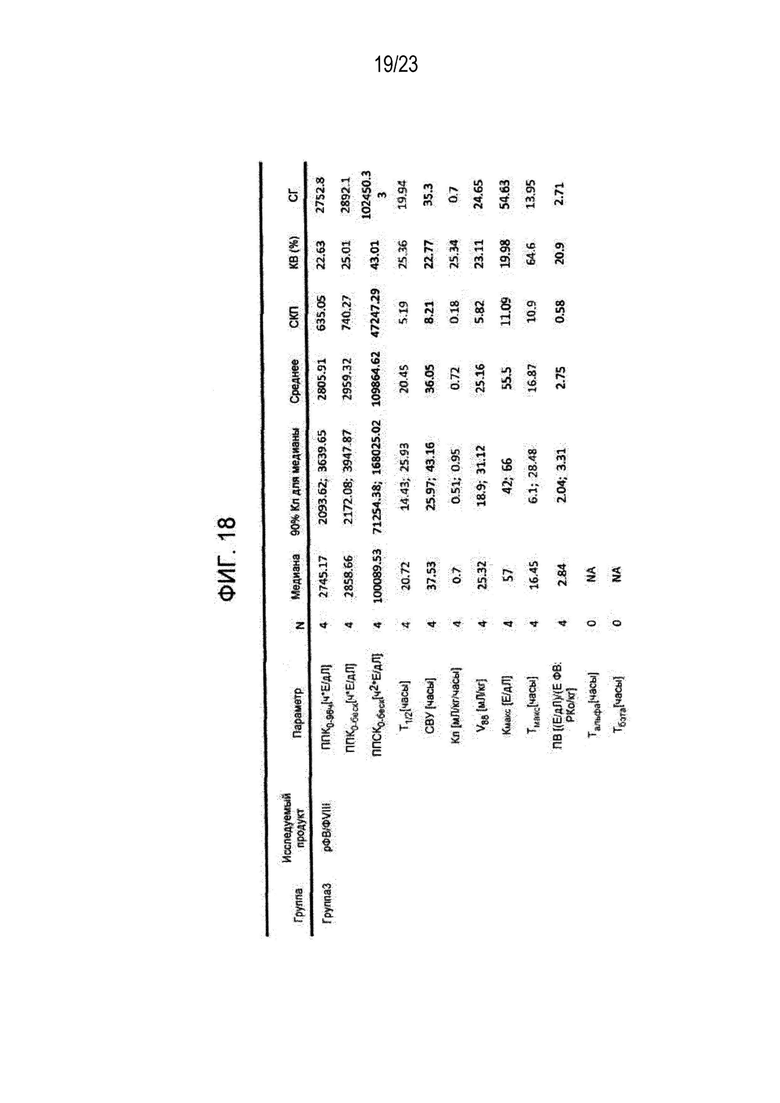
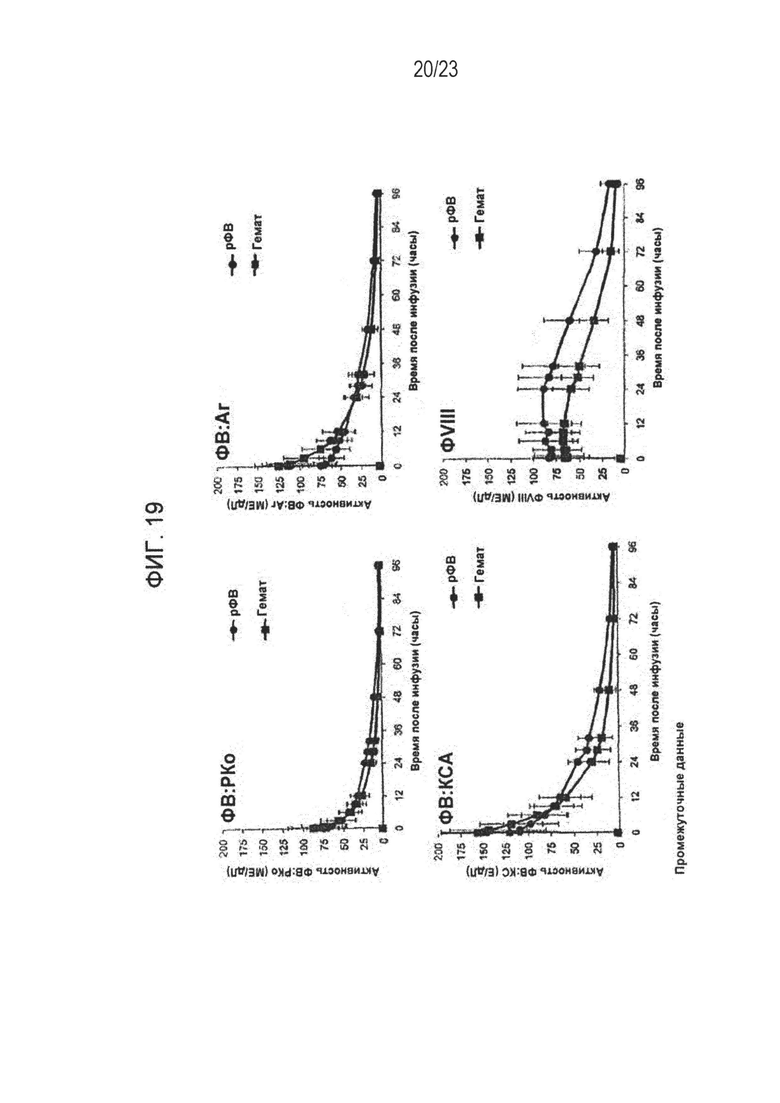
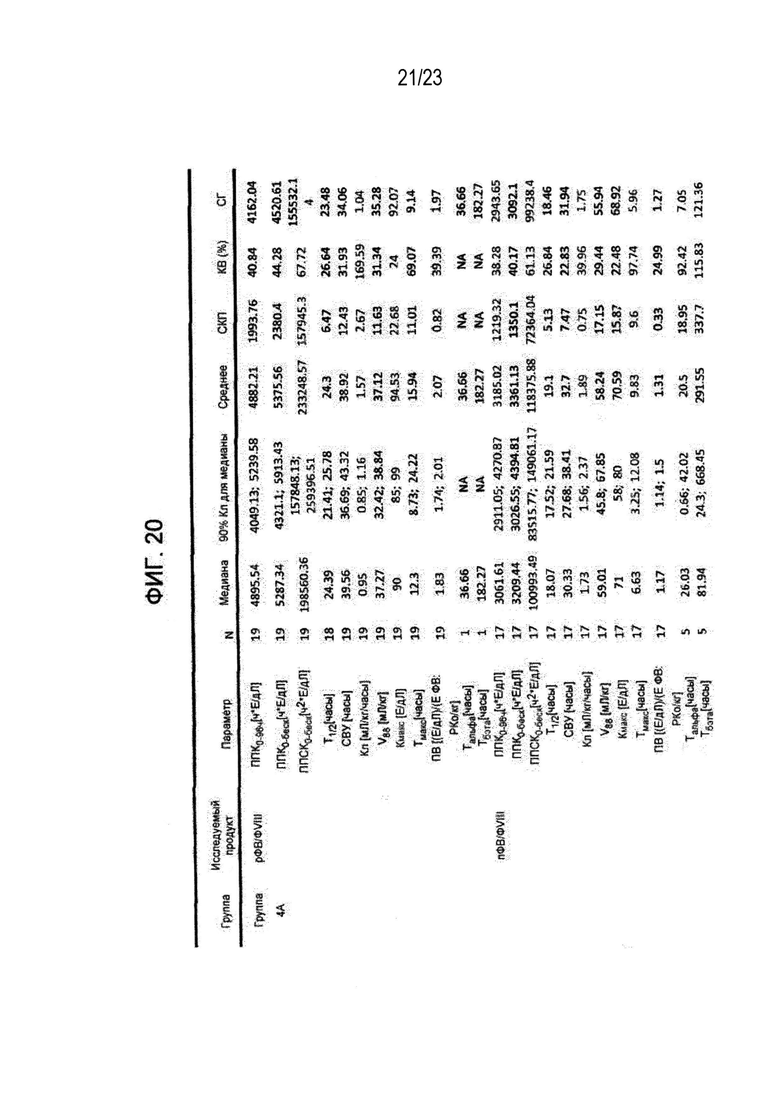
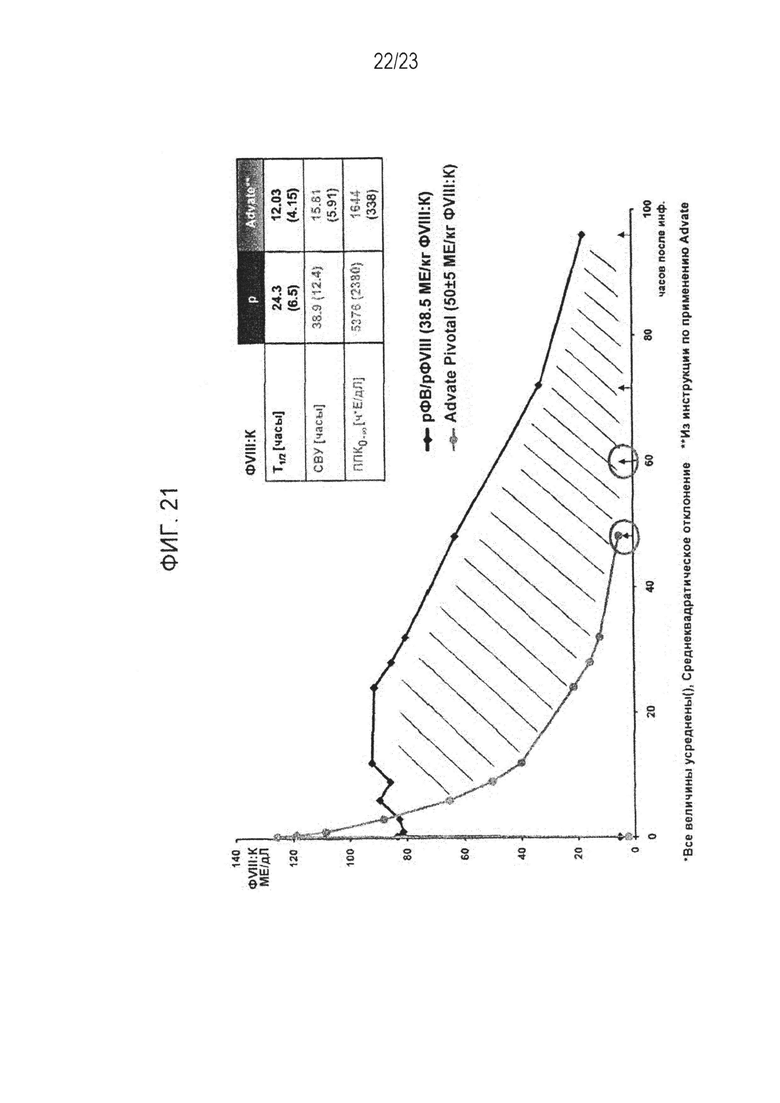
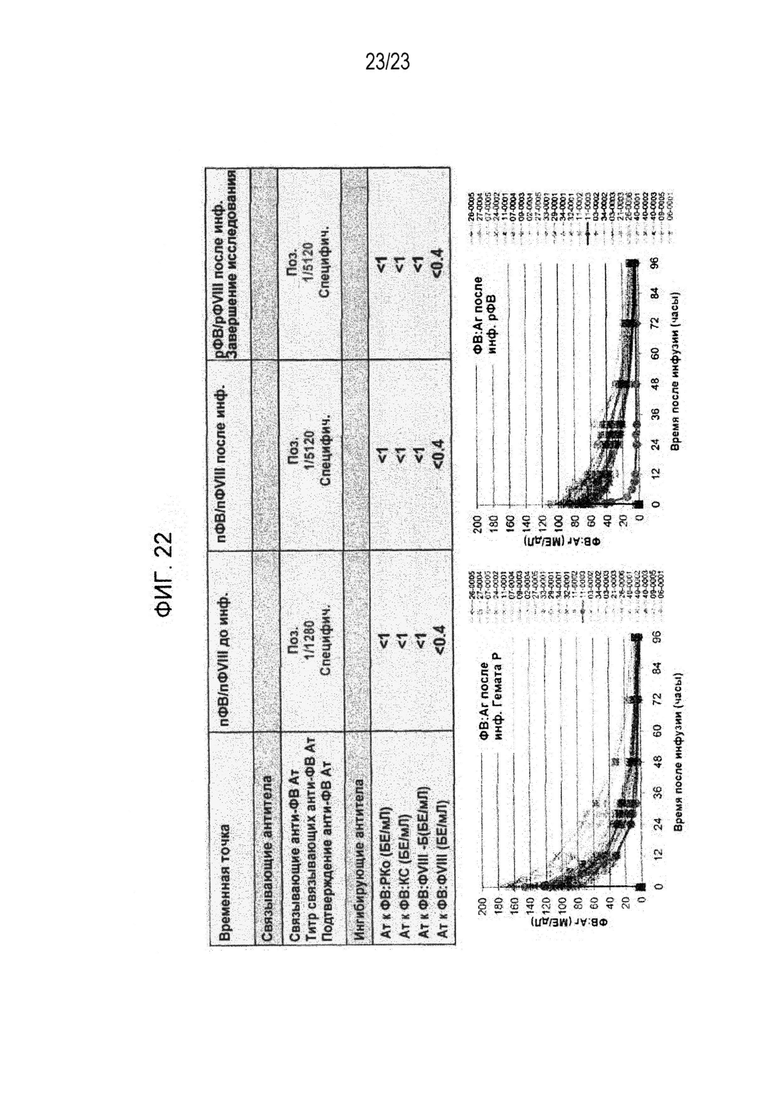
Группа изобретений относится к медицине и касается способа лечения болезни Виллебранда или гемофилии А у нуждающегося в лечении пациента, включающего введение пациенту рекомбинантного фактора Виллебранда (рФВ) таким образом, что время полужизни фактора VIII продлевается по сравнению с пациентом, которому вводили фактор Виллебранда, полученный из плазмы крови, где рФВ не модифицирован водным растворимым полимером, при этом рФВ является составом из высокомолекулярных мультимеров ФВ, содержащим как минимум 20% декамеров ФВ или мультимеров высших порядков, причем рФВ обладает более высокой специфической активностью, чем фактор Виллебранда, полученный из плазмы крови. Группа изобретений также касается способа лечения гемофилии А или болезни Виллебранда у нуждающегося в лечении пациента, который включает введение пациенту рекомбинантного фактора Виллебранда (рФВ), при этом время полужизни ФVIII как минимум в 1.5 раза выше по сравнению со временем полужизни ФVIII у пациента, которому вводили фактор Виллебранда, полученный из плазмы крови. Группа изобретений обеспечивает увеличение времени полужизни ФVIII при лечении болезни Виллебранда или гемофилии А у субъекта. 2 н. и 27 з.п. ф-лы, 5 пр., 22 ил., 34 табл.
1. Способ лечения болезни Виллебранда или гемофилии А у нуждающегося в лечении пациента, включающий:
введение пациенту рекомбинантного фактора Виллебранда (рФВ) таким образом, что время полужизни фактора VIII продлевается по сравнению с пациентом, которому вводили фактор Виллебранда, полученный из плазмы крови, где рФВ не модифицирован водным растворимым полимером, при этом рФВ является составом из высокомолекулярных мультимеров ФВ, содержащим как минимум 20% декамеров ФВ или мультимеров высших порядков, причем рФВ обладает более высокой специфической активностью, чем фактор Виллебранда, полученный из плазмы крови, и мультимеры рФВ высших порядков являются стабильными в течение по меньшей мере 3 часов после введения.
2. Способ по п. 1, в котором способ включает совместное введение пациенту рекомбинантного фактора Виллебранда (рФВ) и рекомбинантного фактора VIII (рФVIII).
3. Способ по п. 2, в котором рФВ и pФVIII вводят совместно в одном составе.
4. Способ по любому из пп. от 1 до 3, в котором пациенту вводят от 1.0 МЕ/кг ФВ : РКо до 150 МЕ/кг ФВ: РКо на дозу.
5. Способ по п. 4, в котором пациенту вводят от 2 МЕ/кг ФВ : РКо до 50 МЕ/кг ФВ : РКо на дозу.
6. Способ по п. 4, в котором пациенту вводят от 5 МЕ/кг ФВ : РКо до 40 МЕ/кг ФВ : РКо на дозу.
7. Способ по п. 4, в котором пациенту вводят от 10 МЕ/кг ФВ : РКо до 20 МЕ/кг ФВ : РКо на дозу.
8. Способ по любому из пп. 1-3, 5-7, в котором рФВ созревает in vitro при обработке фурином.
9. Способ по любому из пп. 1-3, 5-7, в котором рФВ получают путем экспрессии в яичниках китайского хомячка (клеточная культура СНО).
10. Способ по пп. 1-3, 5-7, в котором pФVIII и рФВ получают путем экспрессии в одной и той же клеточной культуре.
11. Способ по любому из пп. 1-3, 5-7, в котором пациенту вводят рФВ не чаще, чем раз в день.
12. Способ по п. 11, в котором пациенту вводят рФВ не чаще, чем дважды в неделю.
13. Способ по любому из пп. 1-3, 5-7, 12, в котором время полужизни фактора VIII продлевается как минимум на 5 часов.
14. Способ по п. 13, в котором время полужизни фактора VIII продлевается как минимум на 12 часов.
15. Способ по п. 13, в котором время полужизни фактора VIII продлевается как минимум на 24 часа.
16. Способ по п. 13, в котором время полужизни фактора VIII продлевается как минимум на 36 часов.
17. Способ по п. 13, в котором время полужизни фактора VIII продлевается как минимум на 48 или 72 часа.
18. Способ по пп. 2-3, 5-7, 12, 14-17, в котором отношение прокоагулирующей активности ФVIII (ME ФVIII : К) к ристоцетин-кофакторной активности рФВ (ME рФВ : РКо), который вводят пациенту, составляет от 2:1 до 1:4.
19. Способ по п. 18, в котором отношение прокоагулирующей активности ФVIII (ME ФVIII : К) к ристоцетин-кофакторной активности рФВ (ME рФВ : РКо), который вводят пациенту, составляет от 3:2 до 1:3.
20. Способ по п. 18, в котором отношение прокоагулирующей активности ФVIII (ME ФVIII : К) к ристоцетин-кофакторной активности рФВ (ME рФВ : РКо), который вводят пациенту, составляет от 1:1 до 1:2.
21. Способ по п. 18, в котором отношение прокоагулирующей активности ФVIII (ME ФVIII : К) к ристоцетин-кофакторной активности рФВ (ME рФВ : РКо), который вводят пациенту, составляет приблизительно 3:4.
22. Способ по пп. 1-3, 5-7, 12, 14-17, 19-21, в котором рФВ обладает специфической активностью приблизительно в 20-150 мЕ/мкг.
23. Способ по пп. 1-3, 5-7, 12, 14-17, 19-21, в котором состав из высокомолекулярных мультимеров ФВ содержит как минимум 30% декамеров ФВ или мультимеров высших порядков.
24. Способ по пп. 1-3, 5-7, 12, 14-17, 19-21, в котором состав из высокомолекулярных мультимеров ФВ содержит как минимум 40% декамеров ФВ или мультимеров высших порядков.
25. Способ по пп. 1-3, 5-7, 12, 14-17, 19-21, в котором состав из высокомолекулярных мультимеров ФВ содержит как минимум 50% декамеров ФВ или мультимеров высших порядков.
26. Способ по пп. 1-3, 5-7, 12, 14-17, 19-21, в котором состав из высокомолекулярных мультимеров ФВ содержит как минимум 60% декамеров ФВ или мультимеров высших порядков.
27. Способ по пп. 1-3, 5-7, 12, 14-17, 19-21, в котором состав из высокомолекулярных мультимеров ФВ содержит как минимум 70% декамеров ФВ или мультимеров высших порядков.
28. Способ лечения гемофилии А или болезни Виллебранда у нуждающегося в лечении пациента, который включает:
введение пациенту рекомбинантного фактора Виллебранда (рФВ) таким образом, что время полужизни фактора VIII продлевается по сравнению с пациентом, которому вводили фактор Виллебранда, полученный из плазмы крови, при этом:
(а) рФВ является составом из высокомолекулярных мультимеров ФВ, содержащим как минимум 20% декамеров ФВ или мультимеров высших порядков;
(б) рФВ обладает более высокой специфической активностью, чем фактор Виллебранда, полученный из плазмы крови, а значение специфической активности рФВ составляет приблизительно 20-150 мЕ/мкг; и
(в) время полужизни ФVIII как минимум в 1.5 раза выше по сравнению со временем полужизни ФVIII у пациента, которому вводили фактор Виллебранда, полученный из плазмы крови.
29. Способ по пп. 1-3, 5-7, 12, 14-17, 19-21 или 28, при котором этот способ является способом лечения болезни Виллебранда типа 3.
| Кипятильник для воды | 1921 |
|
SU5A1 |
| FISCHER BE., Recombinant von Willebrand factor: potential therapeutic use.J Thromb Thrombolysis | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
| MEULIEN P., et al., Processing and characterization of recombinant von Willebrand factor expressed in different cell types using a vaccinia virus vector.Thromb Haemost | |||
| Пуговица для прикрепления ее к материи без пришивки | 1921 |
|
SU1992A1 |
| FISCHER BE., et al., Structural analysis of recombinant von Willebrand factor produced at industrial scale fermentation of transformed CHO cells co-expressing recombinant furin.FEBS Lett | |||
| Топка с качающимися колосниковыми элементами | 1921 |
|
SU1995A1 |
| TURECEK PL., et al., Structure and function of a recombinant von Willebrand factor drug candidate.Semin Thromb Hemost | |||
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Приспособление для суммирования отрезков прямых линий | 1923 |
|
SU2010A1 |
| RODEGHIERO F., et al., Treatment of von Willebrand disease.Semin Hematol | |||
| Способ обработки целлюлозных материалов, с целью тонкого измельчения или переведения в коллоидальный раствор | 1923 |
|
SU2005A1 |
Авторы
Даты
2017-08-18—Публикация
2012-06-11—Подача